2-піридилзаміщені імідазоли як терапевтичні інгібітори alk5 і/або alk4
Номер патенту: 106136
Опубліковано: 25.07.2014
Автори: Среєну Домалапаллі, Кім Дає Кеє, Парк Чул-Іонг, Крішнаях Маддебойна, Дзин Ченг Хуа, Рао Кота Судхакар, Субрахманям Вура Бала, Шеєн Іхун Іхонг
Формула / Реферат
1. Сполука формули (І):
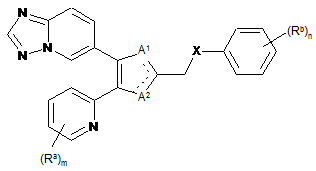 , (І)
, (І)
де
кожний Ra незалежно являє собою Н, галоген, С1-6-алкіл, С1-6-галогеналкіл, С3-6-циклоалкіл, ОН, -О-С1-6-алкіл, -О-С1-6-галогеналкіл, -О-С3-6-циклоалкіл, NH2, -NH-С1-6-алкіл, -NH-С1-6-галогеналкіл, -NH-С3-6-циклоалкіл, -S-С1-6-алкіл, -S-C1-6-галогеналкіл, -S-С3-6-циклоалкіл, CN або NO2;
m дорівнює 0, 1, 2, 3 або 4;
один з А1 і А2 являє собою N, і інший являє собою NR1, де R1 являє собою Н, ОН, С1-6-алкіл, С1-6-галогеналкіл або С3-6-циклоалкіл;
X являє собою зв'язок, -(СН2)p-, -NR2-, -О- або -S-, де p дорівнює 0 або 1, і R2 являє собою Η або С1-3-алкіл;
кожний Rb незалежно являє собою Н, галоген, С1-6-алкіл, С1-6-галогеналкіл, С3-6-циклоалкіл, С2-6-алкеніл, С2-6-алкініл, -(CH2)q-OR3, -(CH2)q-NR3R4, -(CH2)q-SR3, -(CH2)q-NO2, -(CH2)q-CONHOH, -(CH2)q-CN, -(CH2)q-COR3, -(CH2)q-CO2R3, -(CH2)q-CONR3R4, -(СН2)q-тетразол, -(CH2)q-CH=CH-CN, -(CH2)q-CH=CH-CO2R3, -(CH2)q-CH=CH-CONR3R4, -(СН2)q-СН=СН-тетразол, -(CH2)q-NHCOR3, -(CH2)q-NHCO2R3, -(CH2)q-CONHSO2R3, -(CH2)q-NHSO2R3, -(CH2)q-C≡C-CN, -(CH2)q-C≡C-CO2R3, -(CH2)q-C≡C-CONR3R4, -(СН2)q-С≡С-тетразол, -(CH2)q-SOR5, -(CH2)q-SO2R5 або -(CH2)r-(OR3)2, де R3 і R4 незалежно являють собою Η, С1-6-алкіл, С1-6-галогеналкіл або С3-6-циклоалкіл; або взяті разом з атомом азоту, до якого вони приєднані, утворюють моноциклічне кільце, таке як імідазол, піролідин, піперидин, морфолін, піперазин і гомопіперазин; R5 являє собою С1-6-алкіл, С1-6-галогеналкіл або С3-6-циклоалкіл; q дорівнює 0, 1, 2, 3 або 4; і r дорівнює 1, 2, 3 або 4;
n дорівнює 0, 1, 2, 3, 4 або 5;
або її фармацевтично прийнятна сіль або гідрат.
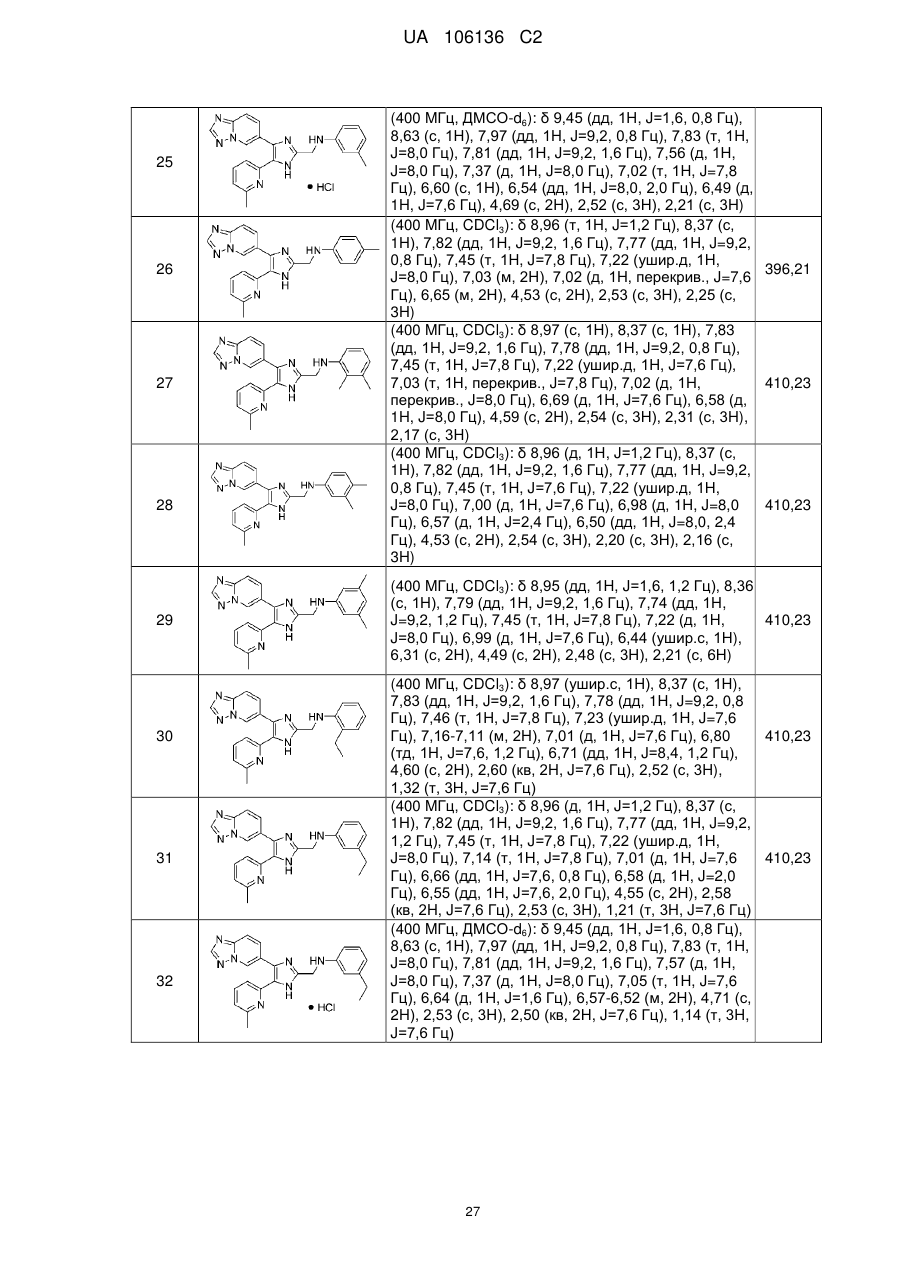
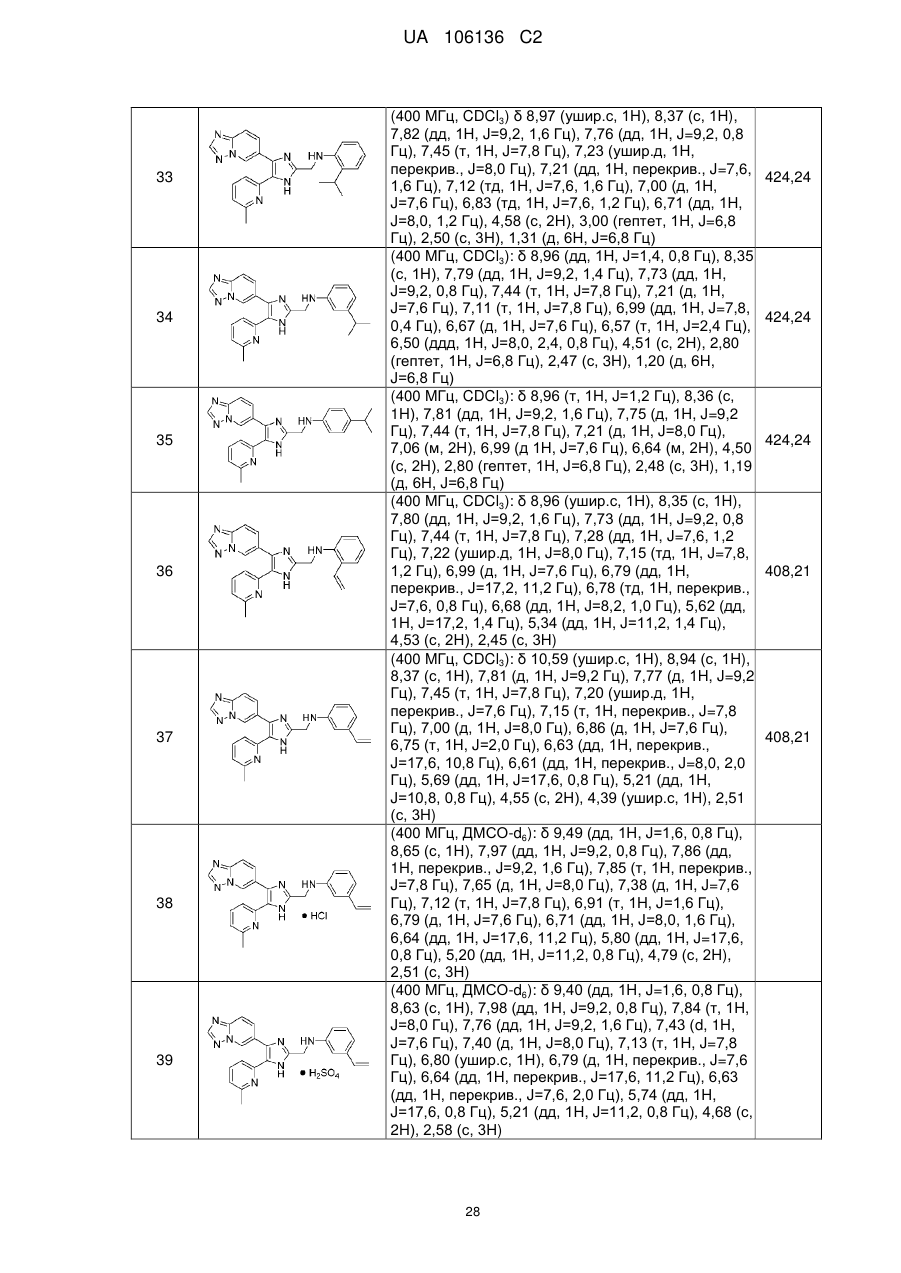
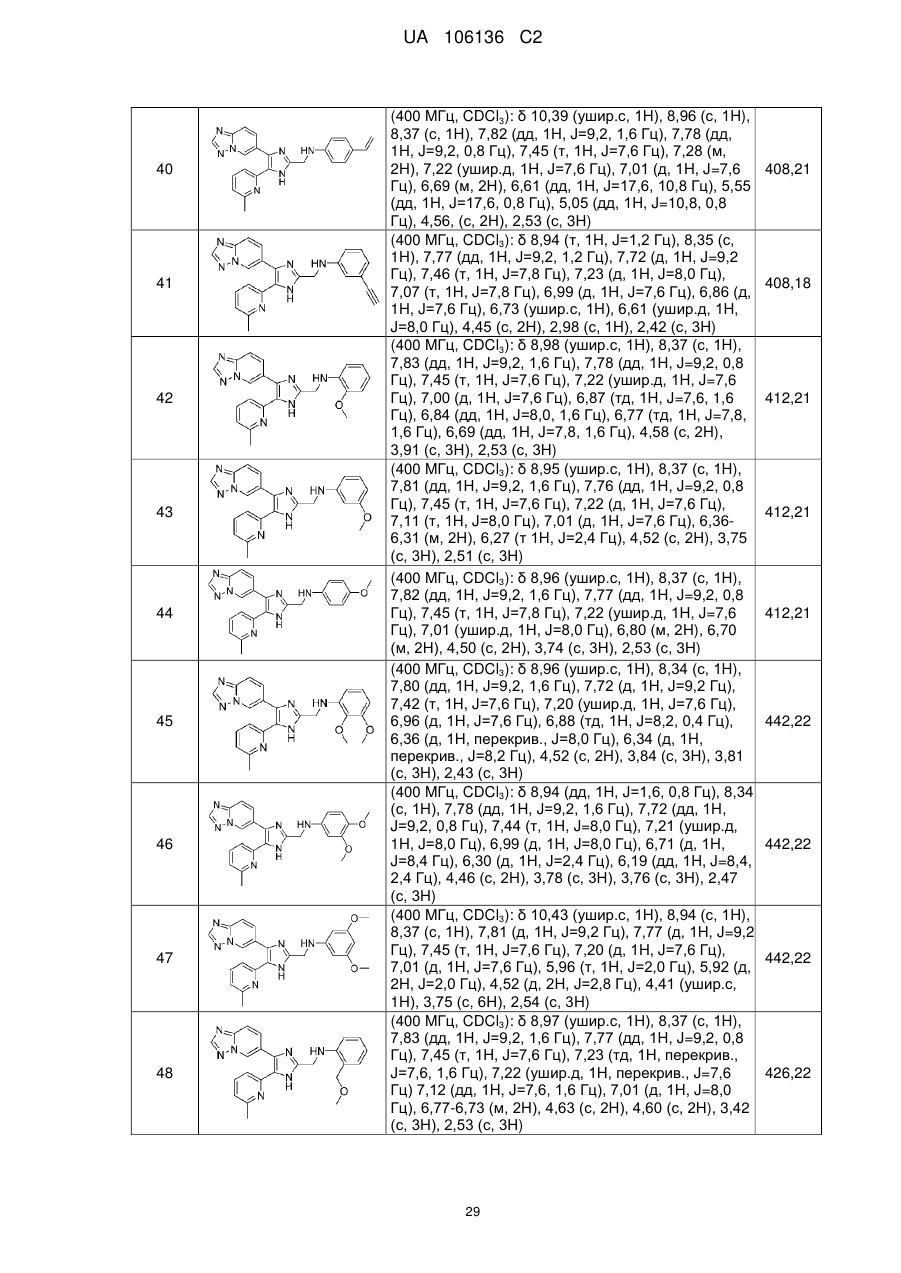
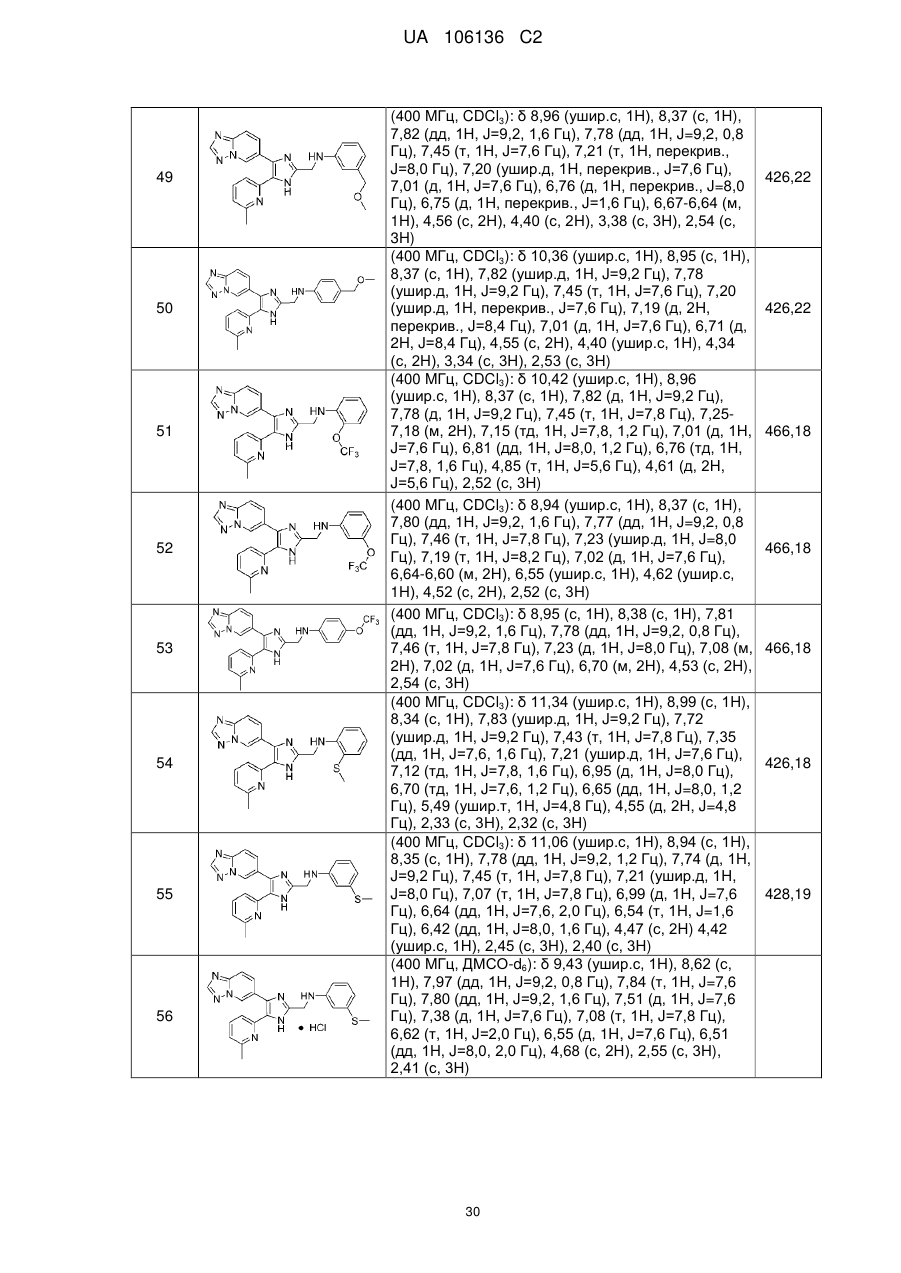
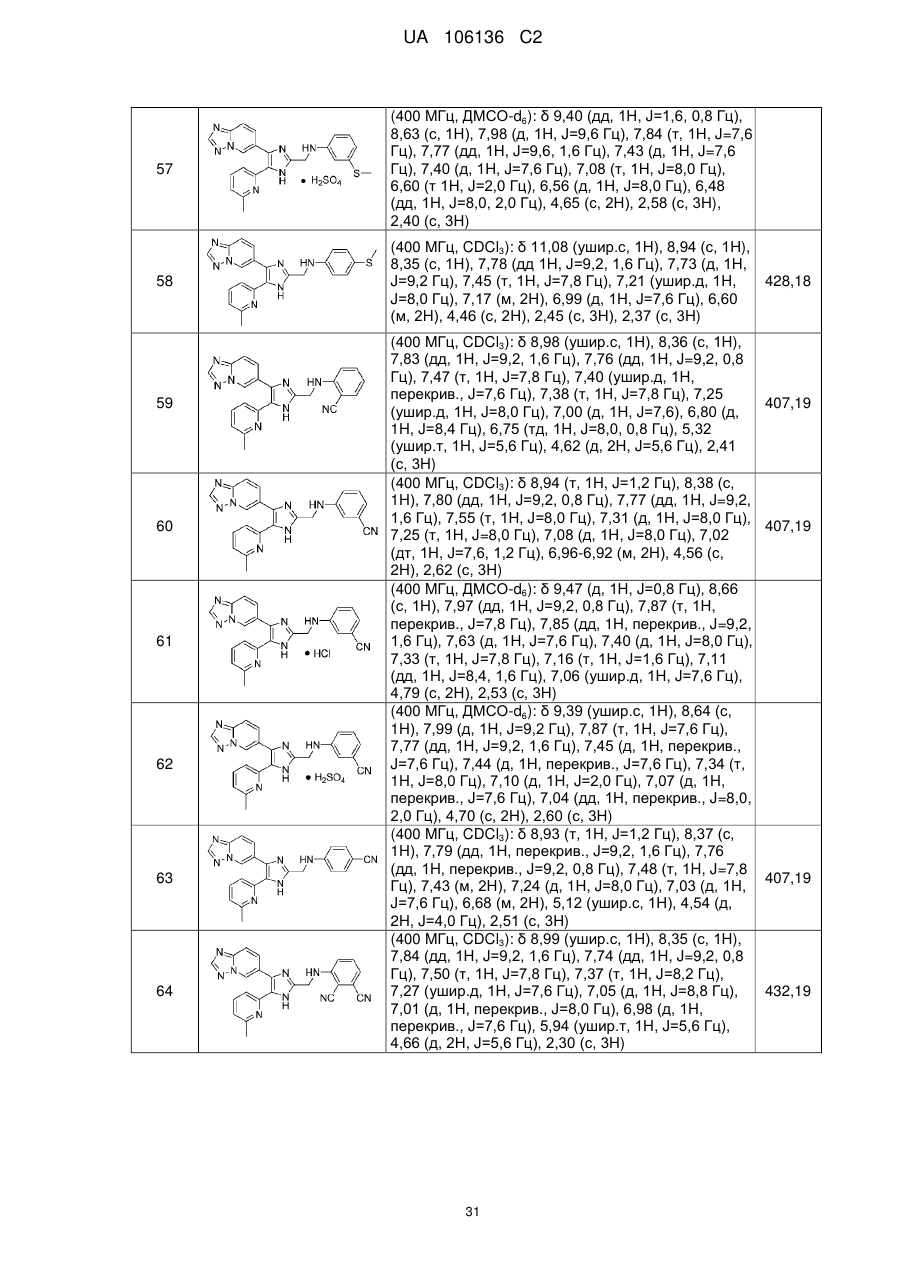
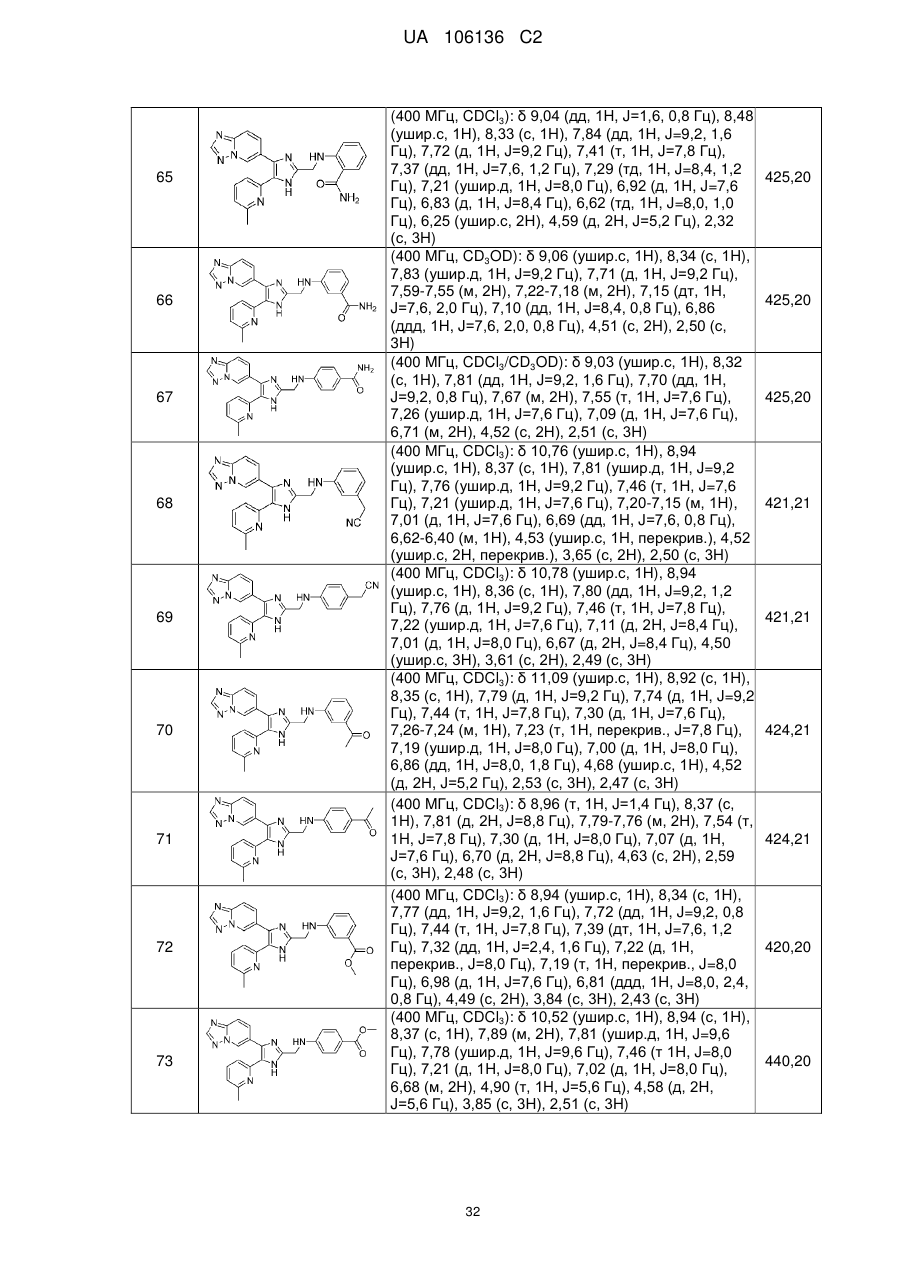
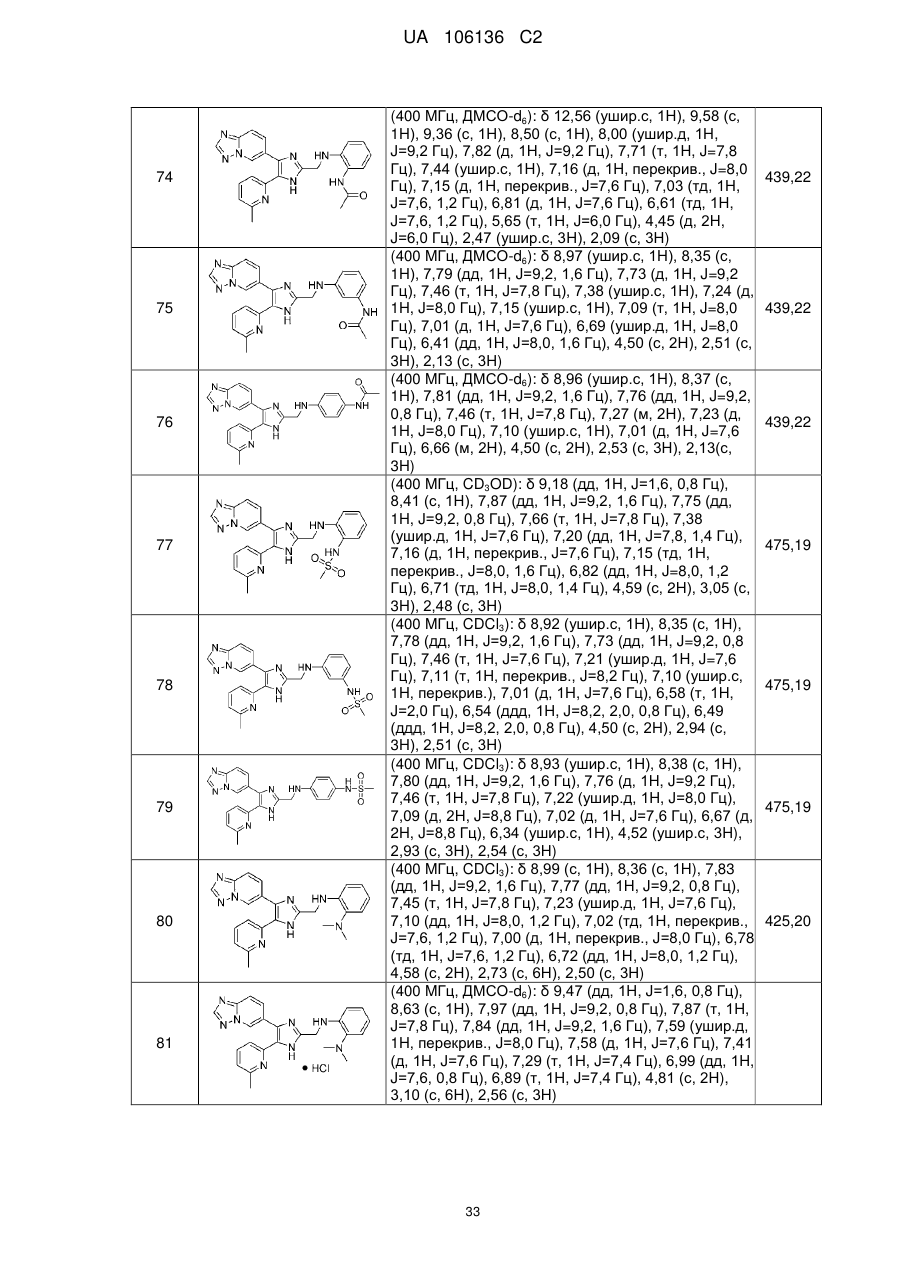
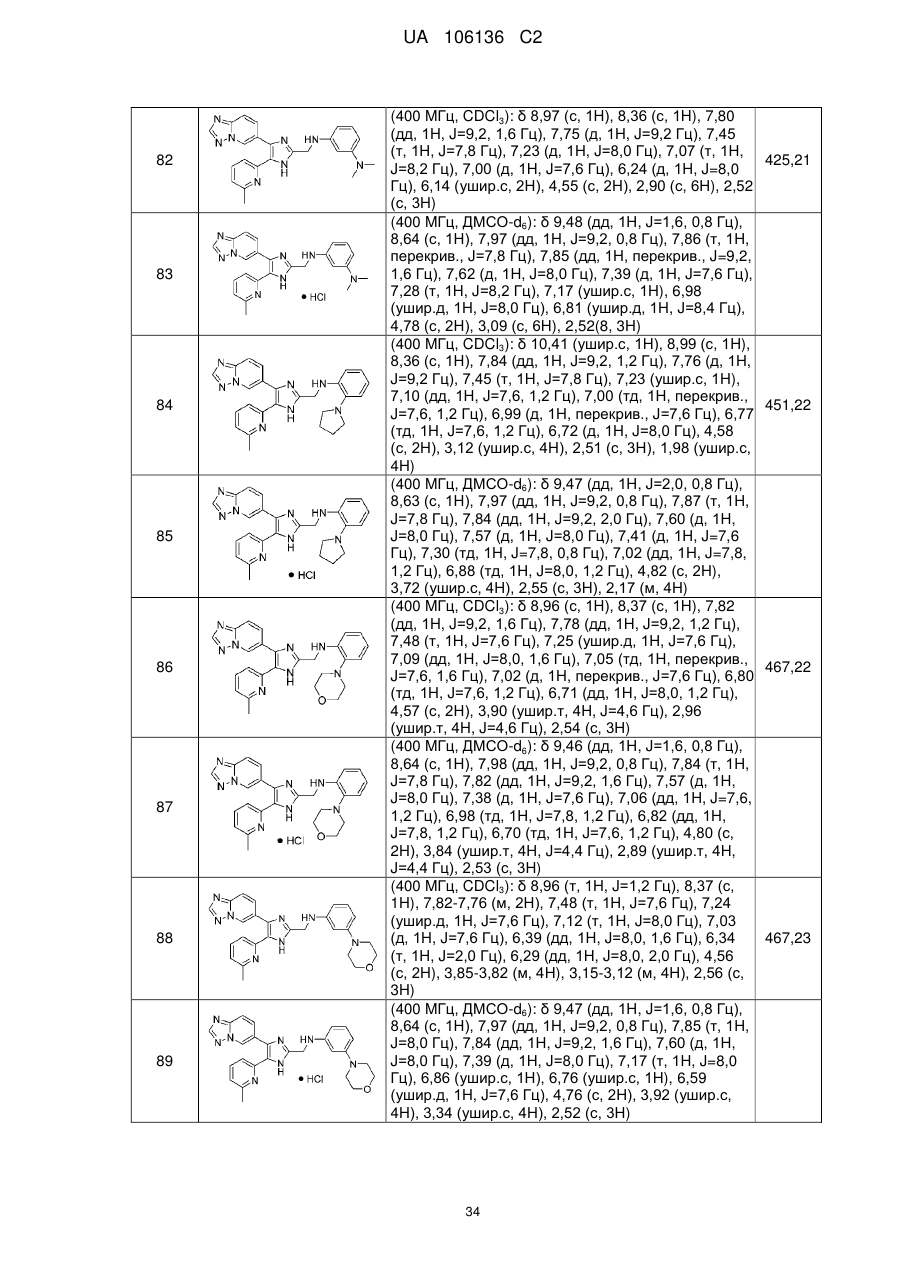
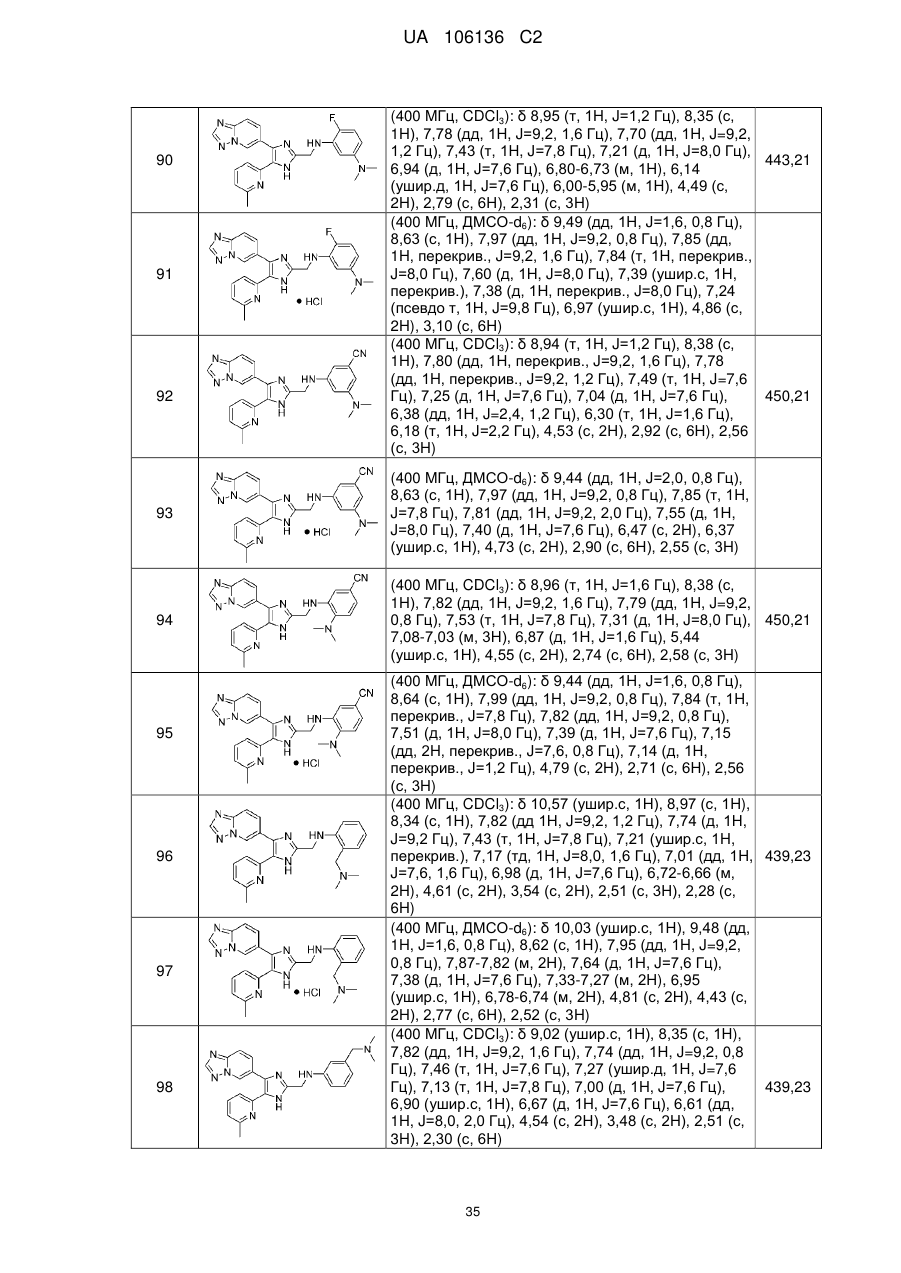
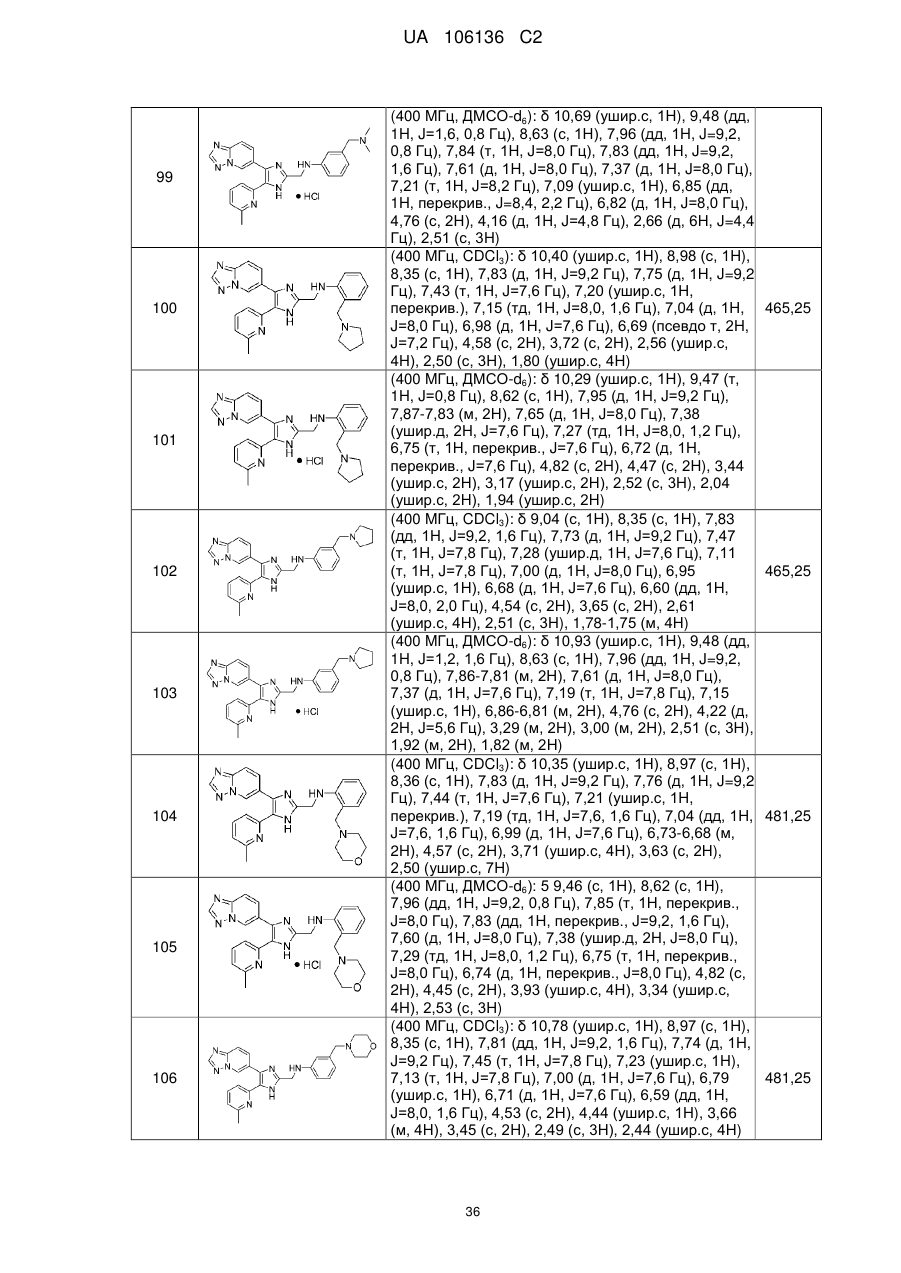
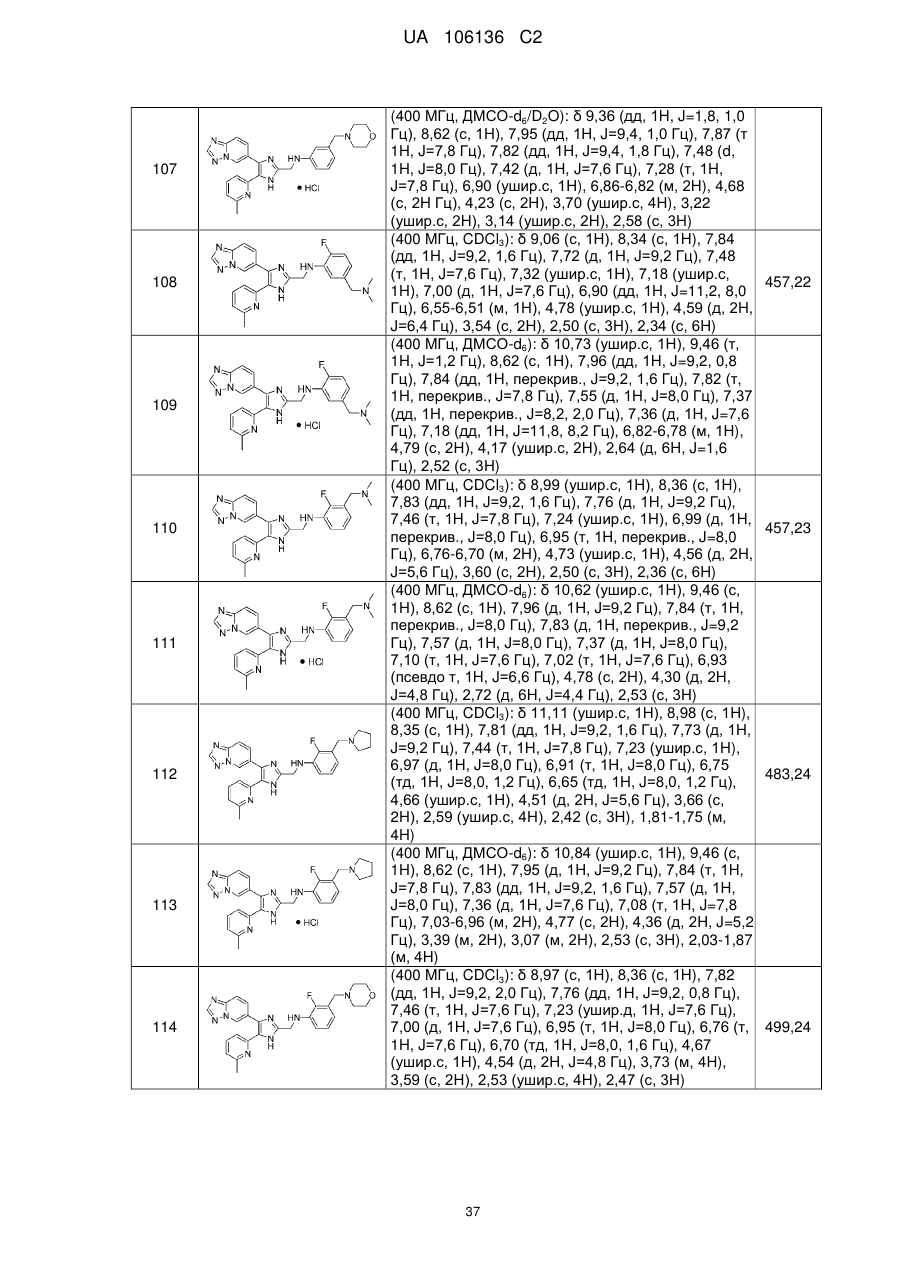
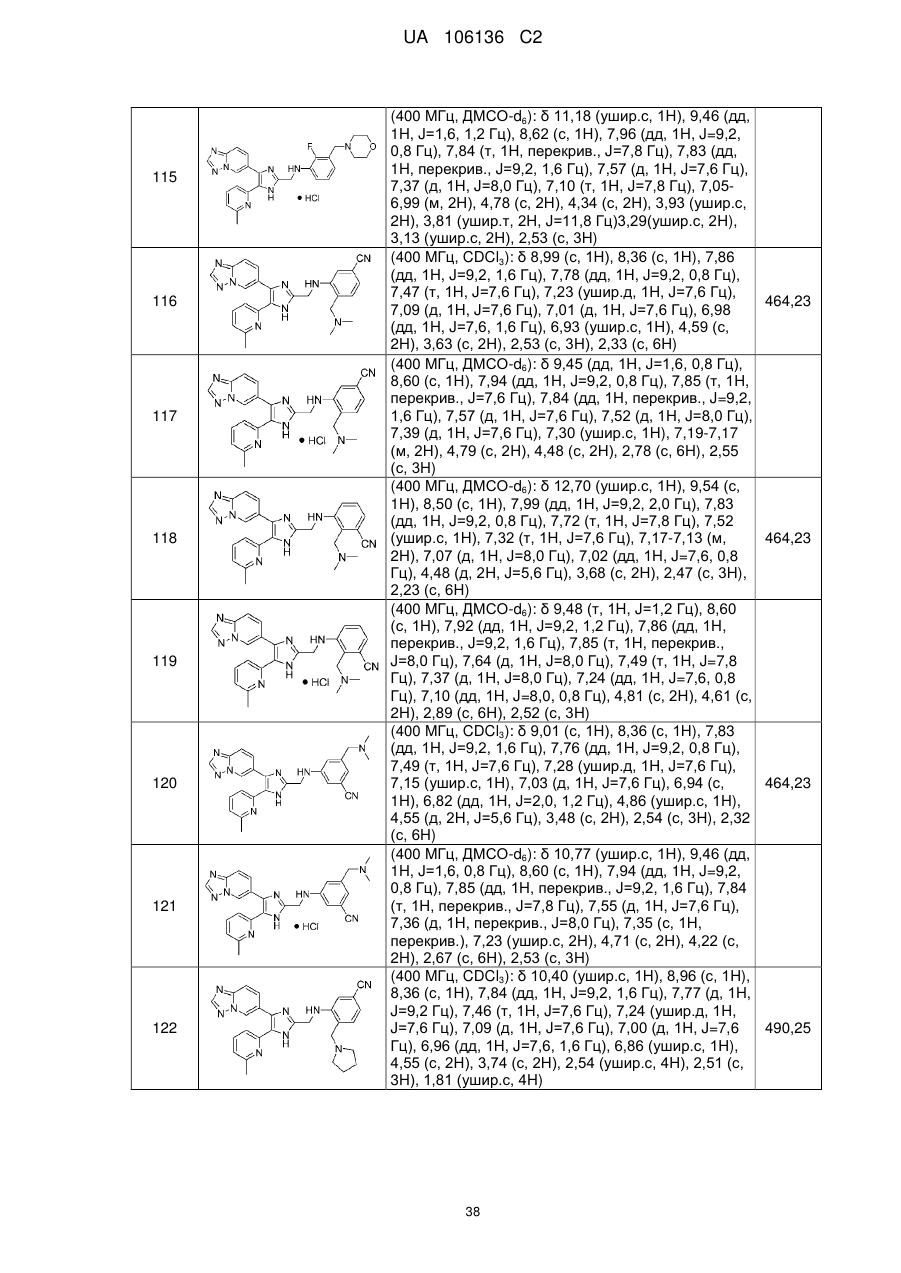
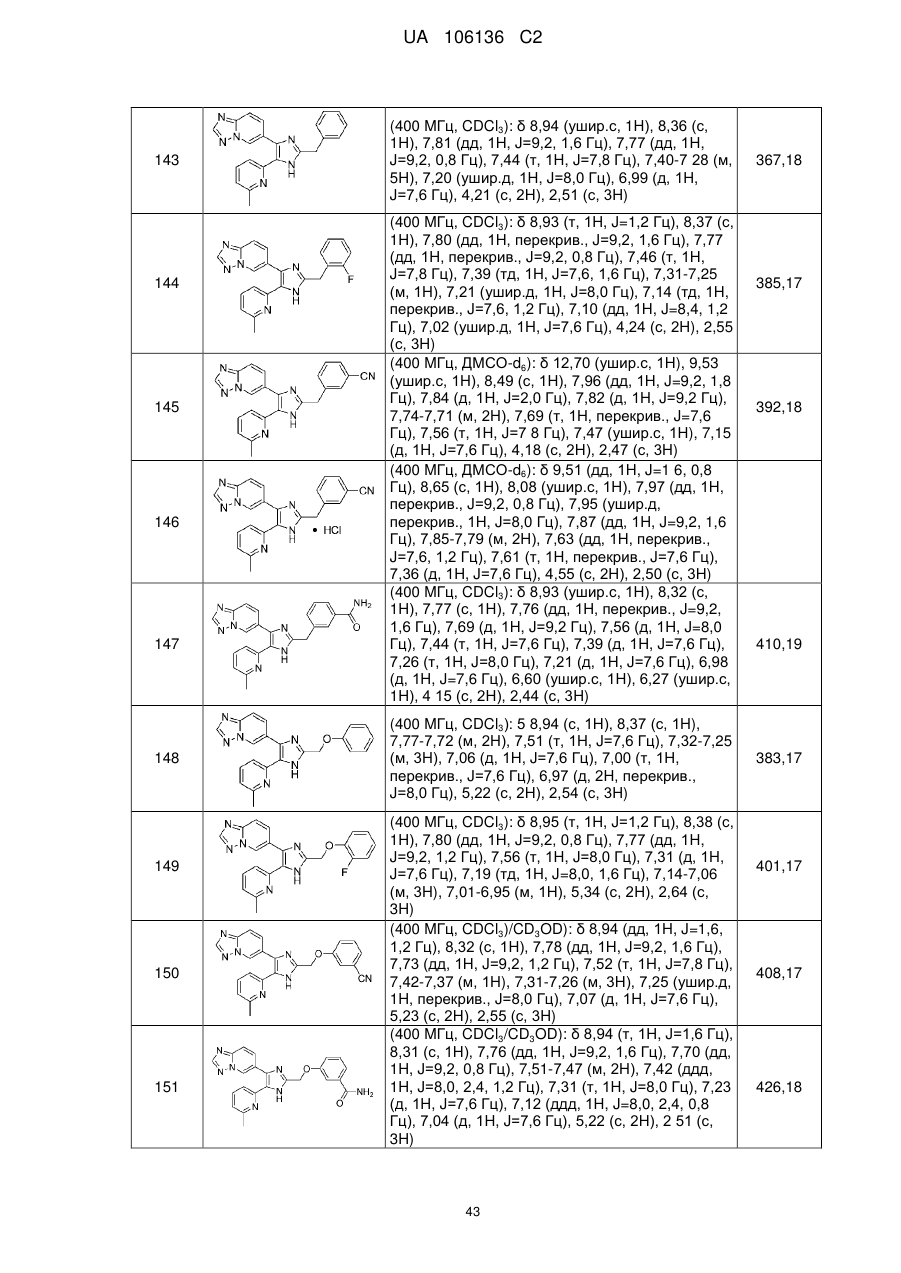
2. Сполука за п. 1, яку вибирають з групи, що складається з:
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)мeтил)-2-фтораніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-фтораніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-4-фтораніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2,3-дифтораніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3,4-дифтораніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3,5-дифтораніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-хлораніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-хлораніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-4-хлораніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2,3-дихлораніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3,4-дихлораніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3,5-дихлораніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-броманіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-броманіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-4-броманіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-метиланіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-метиланіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-4-метиланіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2,3-диметиланіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3,4-диметиланіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3,5-диметиланіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-етиланіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-етиланіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-ізопропіланіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-ізопропіланіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-4-ізопропіланіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-вініланіліну;
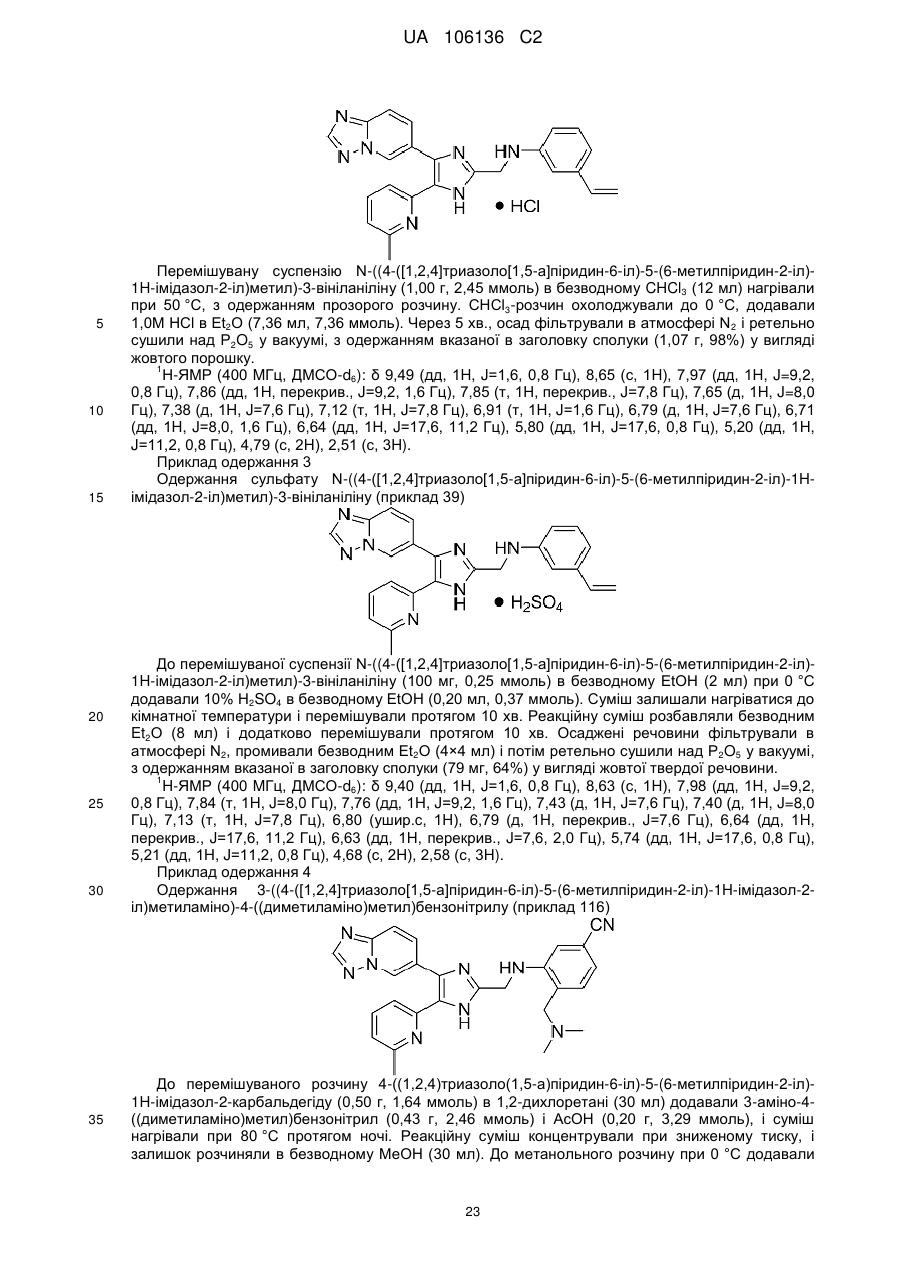
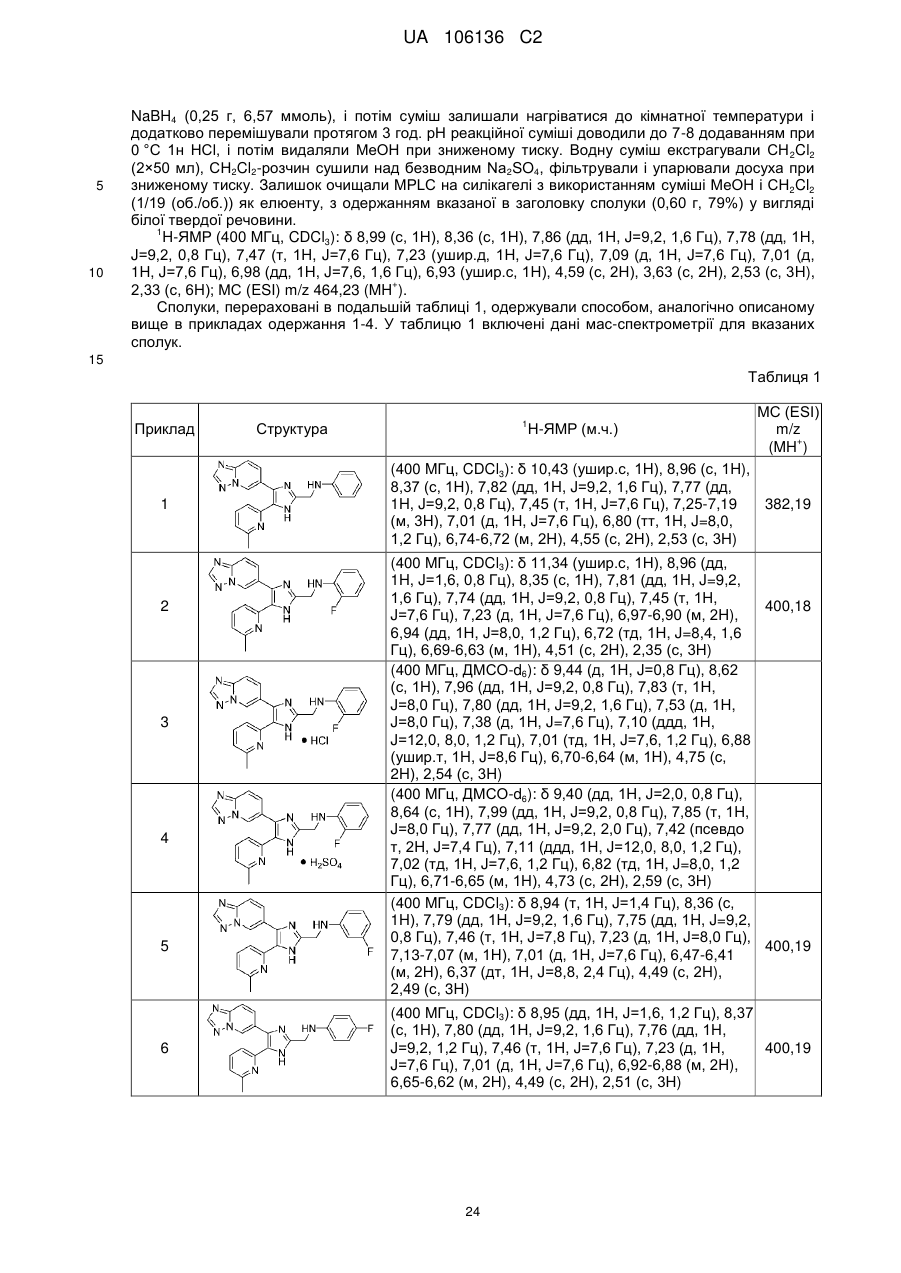
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-вініланіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-4-вініланіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-етиніланіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-метоксіаніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-метоксіаніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-4-метоксіаніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2,3-диметоксіаніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3,4-диметоксіаніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3,5-диметоксіаніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-(метоксиметил)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-(метоксиметил)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-4-(метоксиметил)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-(трифторметоксі)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-(трифторметоксі)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-4-(трифторметоксі)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-(метилтіо)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-(метилтіо)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридии-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-4-(метилтіо)аніліну;
2-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метиламіно)бензонітрилу;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)бензонітрилу;
4-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метиламіно)бензонітрилу;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)фталонітрилу;
2-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)бензаміду;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метиламіно)бензаміду;
4-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метиламіно)бензаміду;
2-(3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)феніл)ацетонітрилу;
2-(4-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)феніл)ацетонітрилу;
1-(3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метиламіно)феніл)етанону;
1-(4-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)феніл)етанону;
метил-3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)бензоату;
метил-4-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метиламіно)бензоату;
N-(2-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)феніл)ацетаміду;
N-(3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)феніл)ацетаміду;
N-(4-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)феніл)ацетаміду;
N-(2-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)феніл)метансульфонаміду;
N-(3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)феніл)метансульфонаміду;
N-(4-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)феніл)метансульфонаміду;
N1-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-N2,N2-диметилбензол-1,2-діаміну;
N1-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-N3,N3-диметилбензол-1,3-діаміну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-(піролідин-1-іл)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-морфоліноаніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-морфоліноаніліну;
N3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-4-фтор-N1,N1-диметилбензол-1,3-діаміну;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)-5-(диметиламіно)бензонітрилу;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)-4-(диметиламіно)бензонітрилу;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-((диметиламіно)метил)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-((диметиламіно)метил)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-(піролідин-1-ілметил)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-(піролідин-1-ілметил)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-(морфолінометил)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3-(морфолінометил)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-5-((диметиламіно)метил)-2-фтораніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-((диметиламіно)метил)-2-фтораніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-фтор-3-(піролідин-1-ілметил)аніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-фтор-3-(морфолінометил)аніліну;
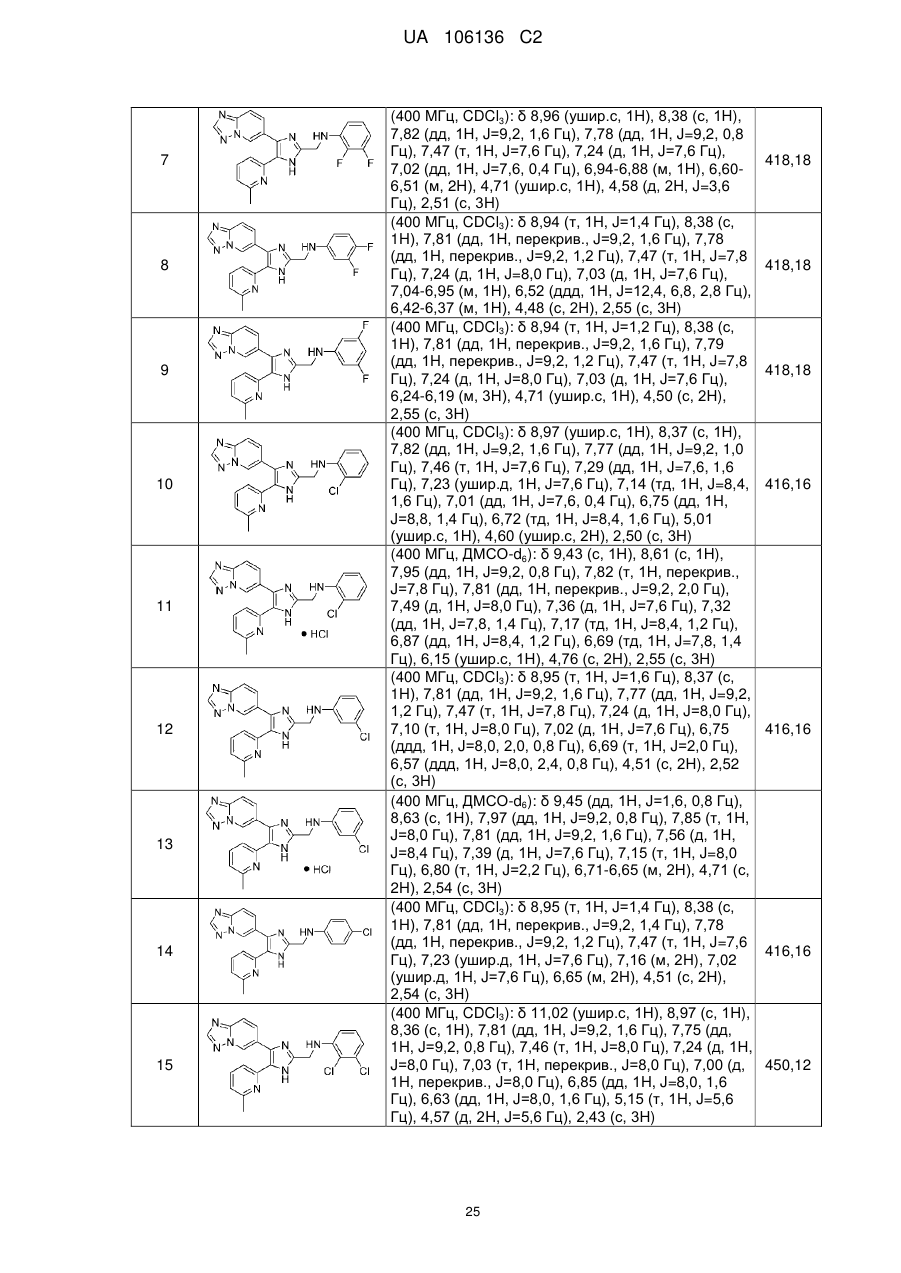
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)-4-((диметиламіно)метил)бензонітрилу;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)-2-((диметиламіно)метил)бензонітрилу;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)-5-((диметиламіно)метил)бензонітрилу;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)-4-(піролідин-1-ілметил)бензонітрилу;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)-2-(піролідин-1-ілметил)бензонітрилу;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)-5-(піролідин-1-ілметил)бензонітрилу;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)-4-(морфолінометил)бензонітрилу;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)-2-(морфолінометил)бензонітрилу;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метиламіно)-5-(морфолінометил)бензонітрилу;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-(2-(диметиламіно))етиланіліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-3-(2-(диметиламіно))етиланіліну;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-етилпіридин-2-іл)-1Н-імідазол-2-іл)метиламіно)бензонітрилу;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-етилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-фтораніліну;
N-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)-2-фтор-N-метиланіліну;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)(метиламіно)бензонітрилу;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)(метиламіно)бензаміду;
6-(2-бензил-5-(6-метилпіридин-2-іл)-1Н-імідазол-4-іл)-[1,2,4]триазоло[1,5-а]піридину;
6-(2-(2-фторбензил)-5-(6-метилпіридин-2-іл)-1Н-імідазол-4-іл)-[1,2,4]триазоло[1,5-а]піридину;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)бензонітрилу;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метил)бензаміду;
6-(5-(6-метилпіридин-2-іл)-2-(феноксиметил)-1Н-імідазол-4-іл)-[1,2,4]триазоло[1,5-а]піридину;
6-(2-((2-фторфенокси)метил)-5-(6-метилпіридин-2-іл)-1Н-імідазол-4-іл)-[1,2,4]триазоло[1,5-а]піридину;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метокси)бензонітрилу;
3-((4-([1,2,4]триазоло[1,5-а]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Н-імідазол-2-іл)метокси)бензаміду;
6-(5-(6-метилпіридин-2-іл)-2-(фенілтіометил)-1Н-імідазол-4-іл)-[1,2,4]триазоло[1,5-а]піридину;
6-(2-((2-фторфенілтіо)метил)-5-(6-метилпіридин-2-іл)-1Н-імідазол-4-іл)-[1,2,4]триазоло[1,5-а]піридину
і їх фармацевтично прийнятних солей і гідратів.
3. Фармацевтична композиція, яка містить одну або більше сполук за п. 1 або їх фармацевтично прийнятну сіль або гідрат і фармацевтично прийнятний розріджувач або носій.
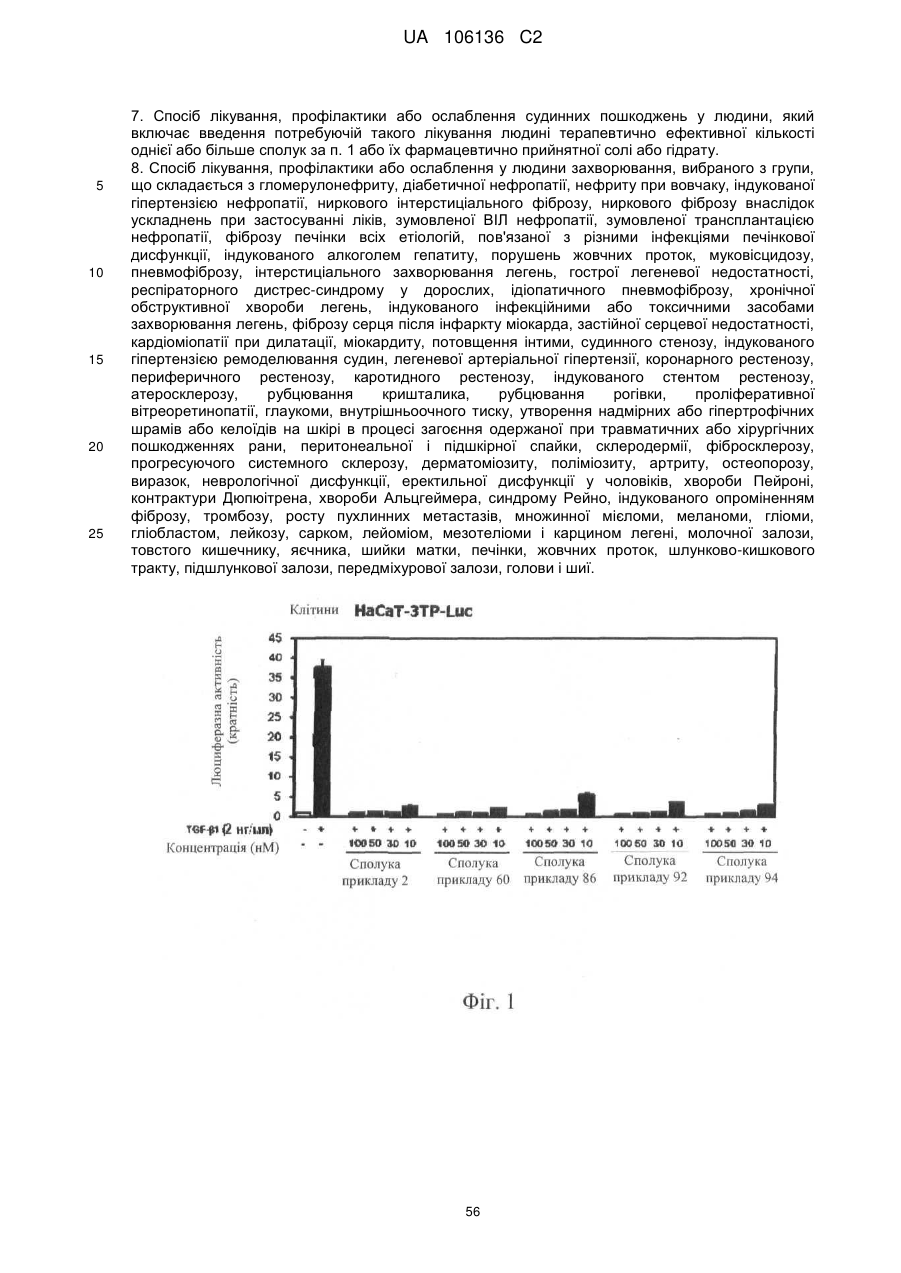
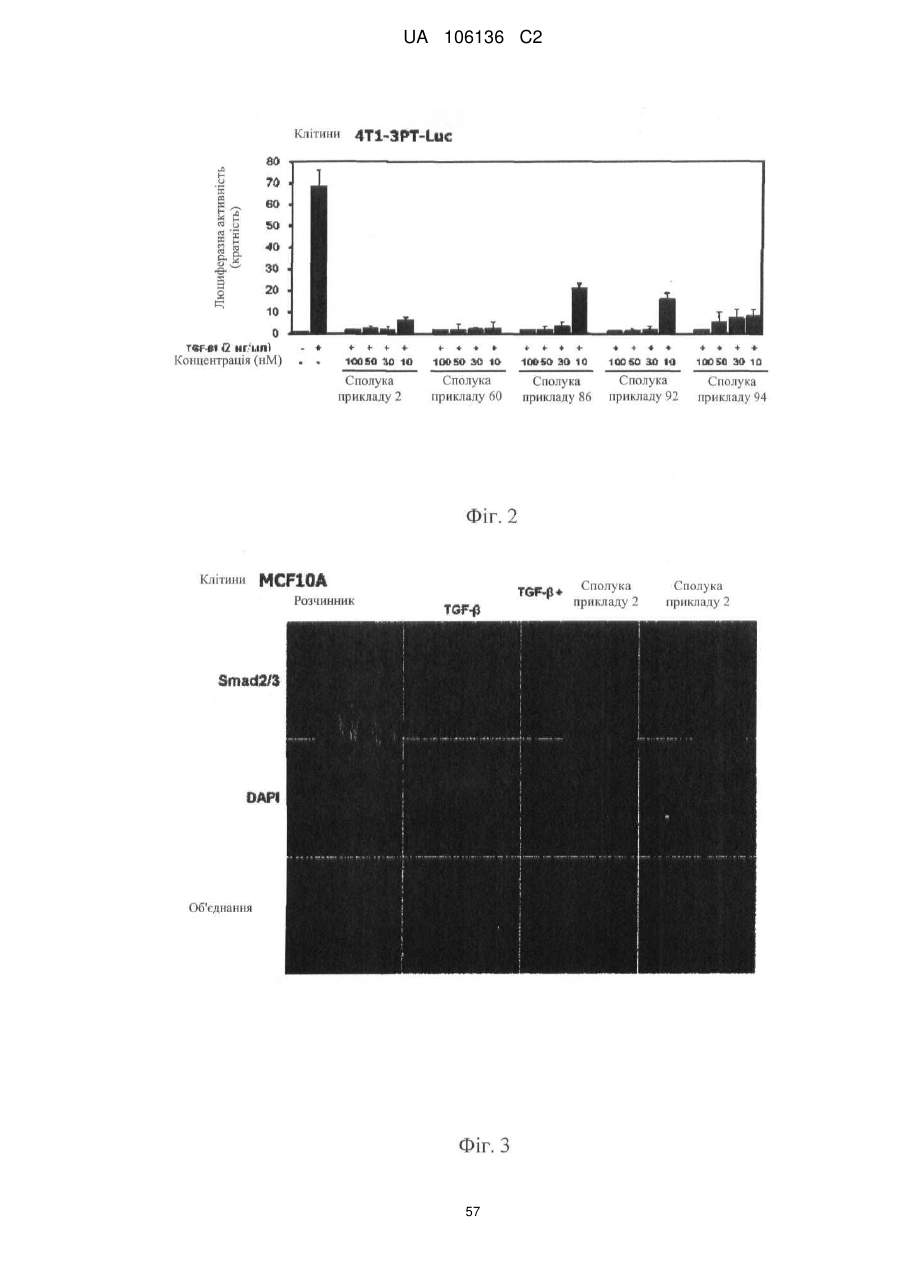
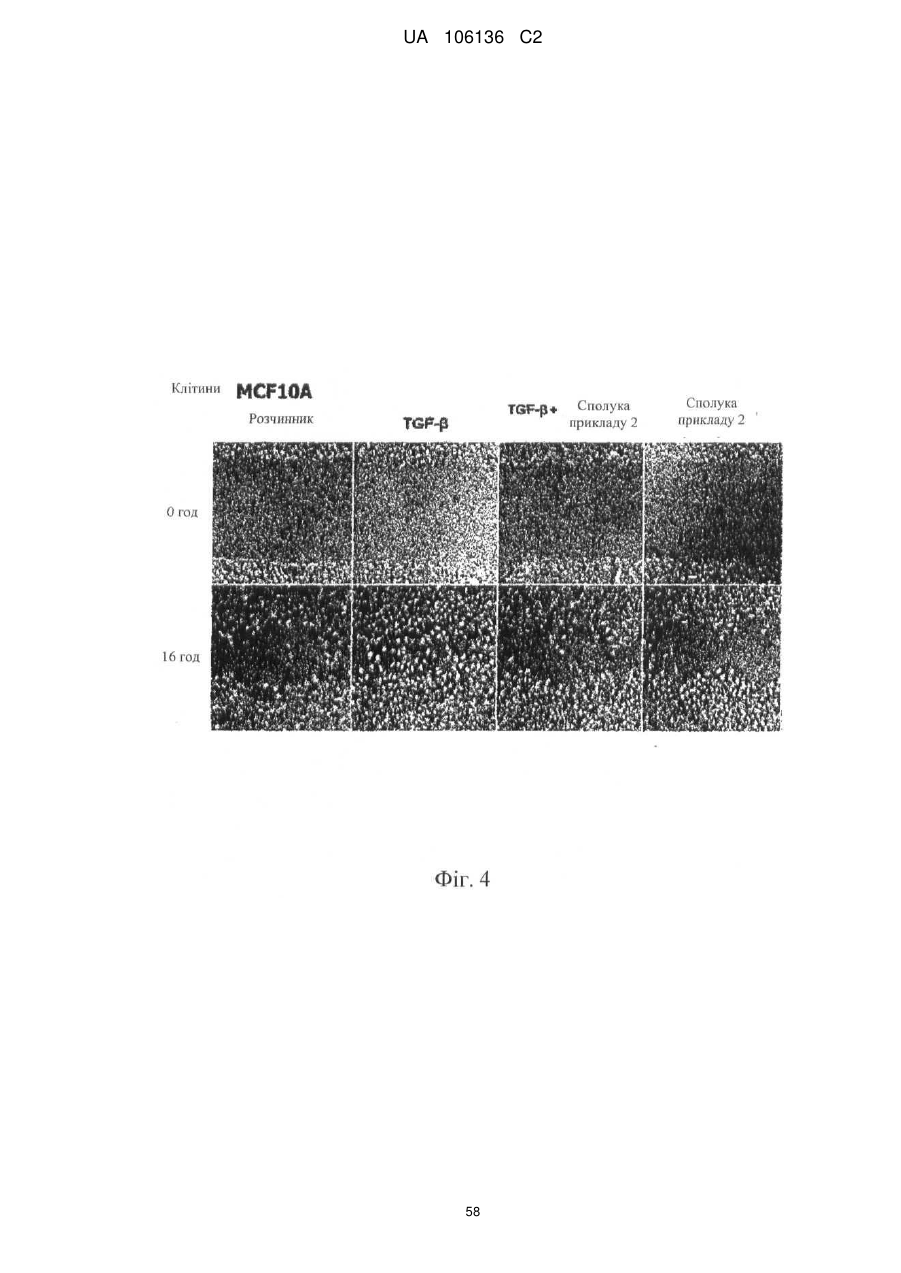
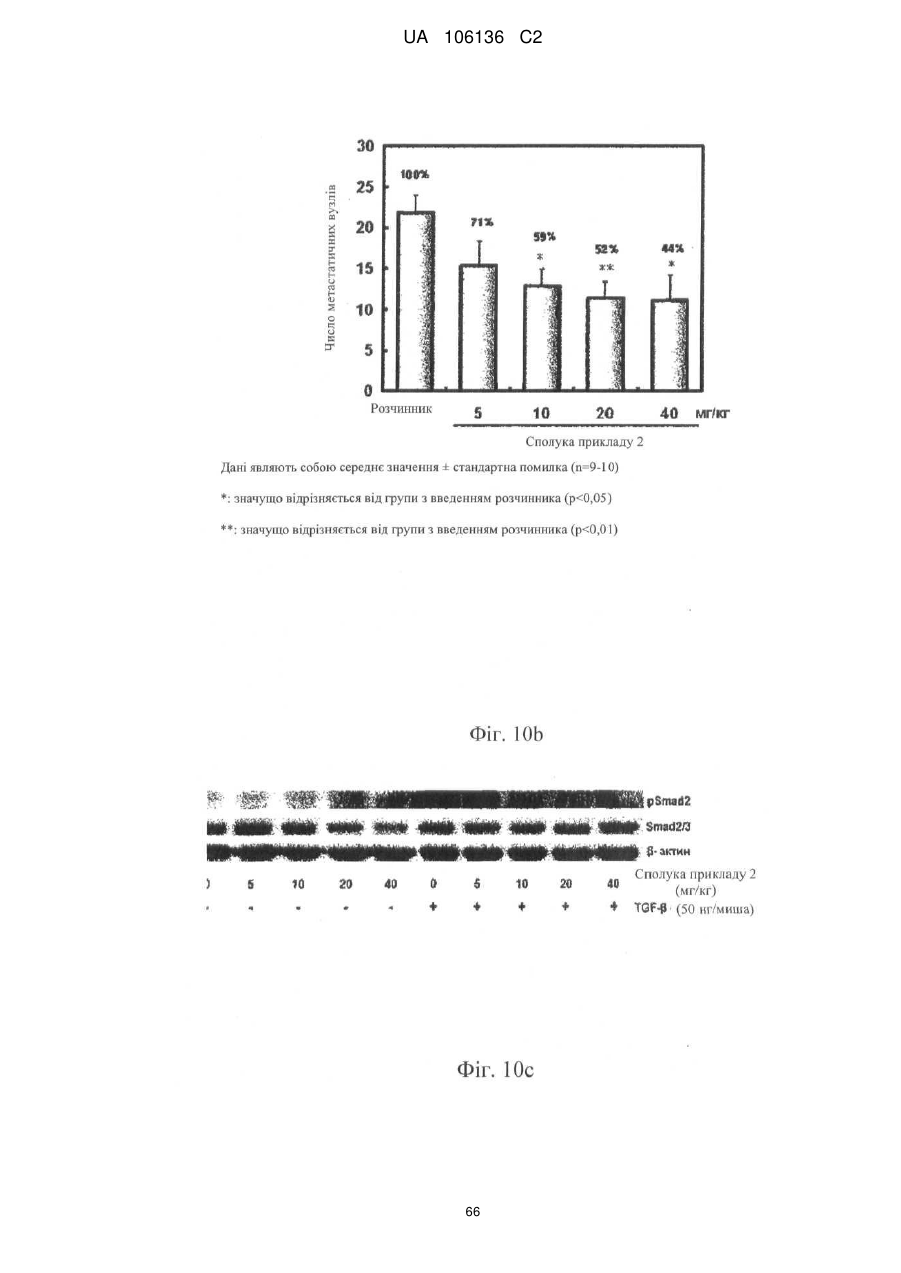
4. Спосіб інгібування шляхів передачі сигналу TGF-β або активіну або обох у людини, який включає введення потребуючій такого лікування людині терапевтично ефективної кількості однієї або більше сполук за п. 1 або їх фармацевтично прийнятної солі або гідрату.
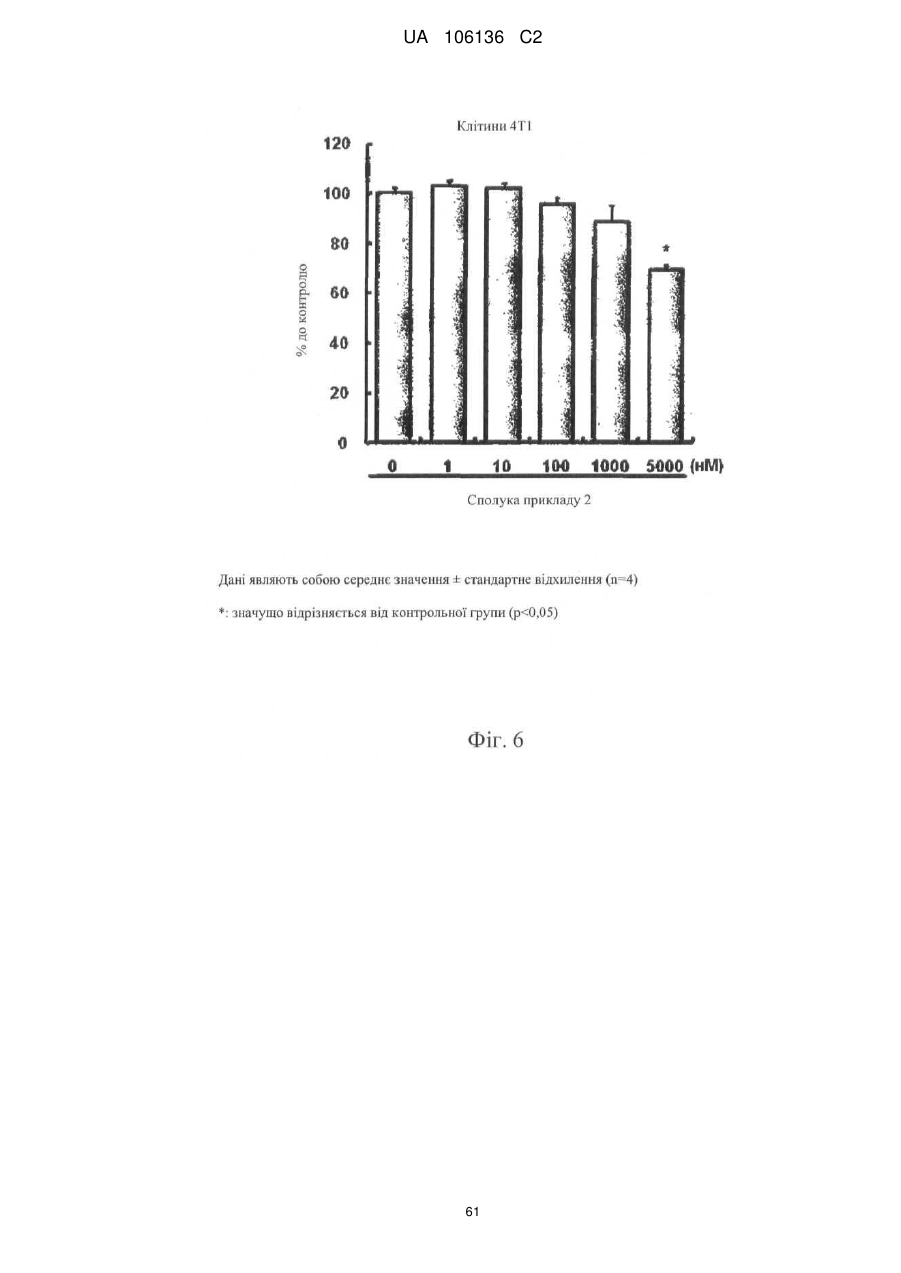
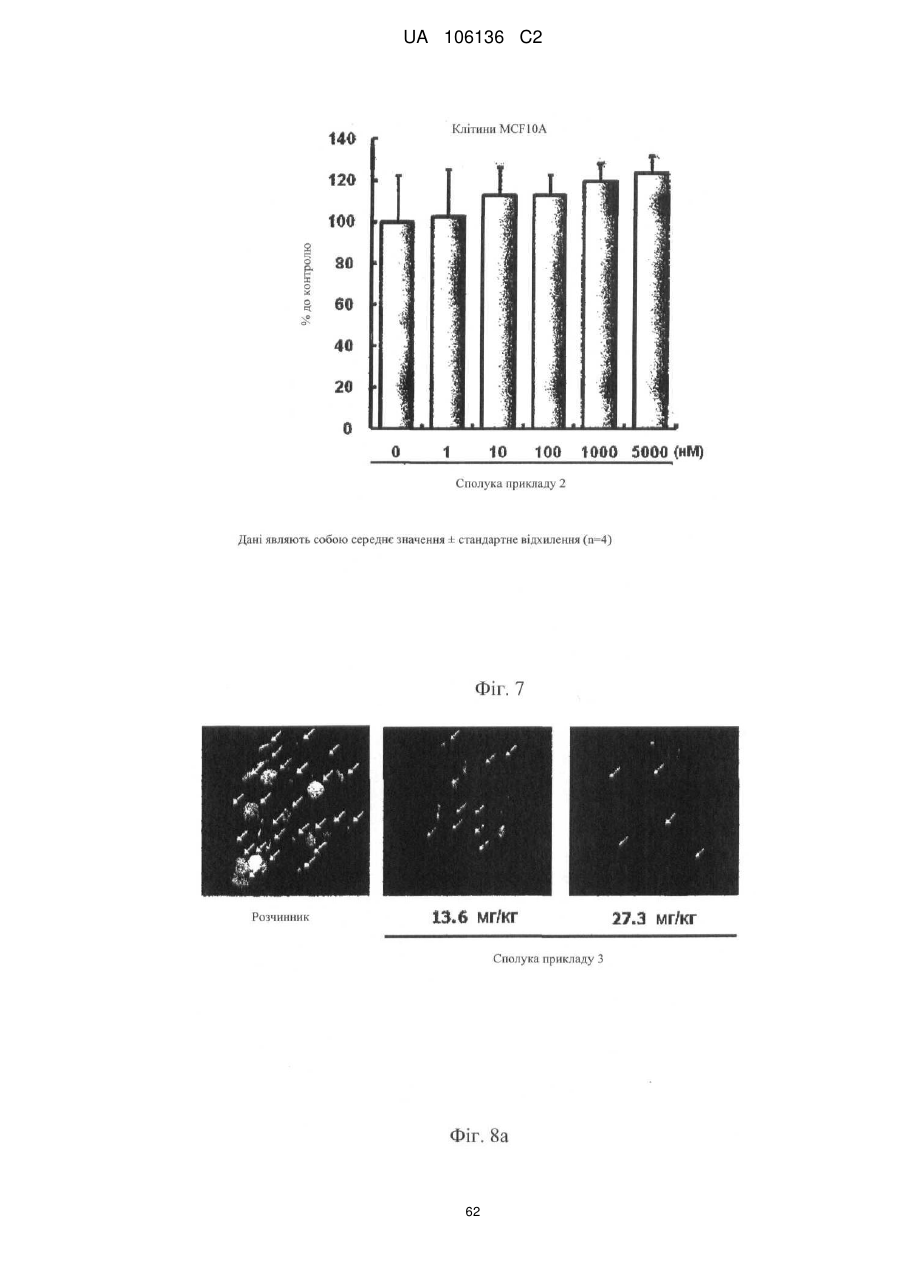
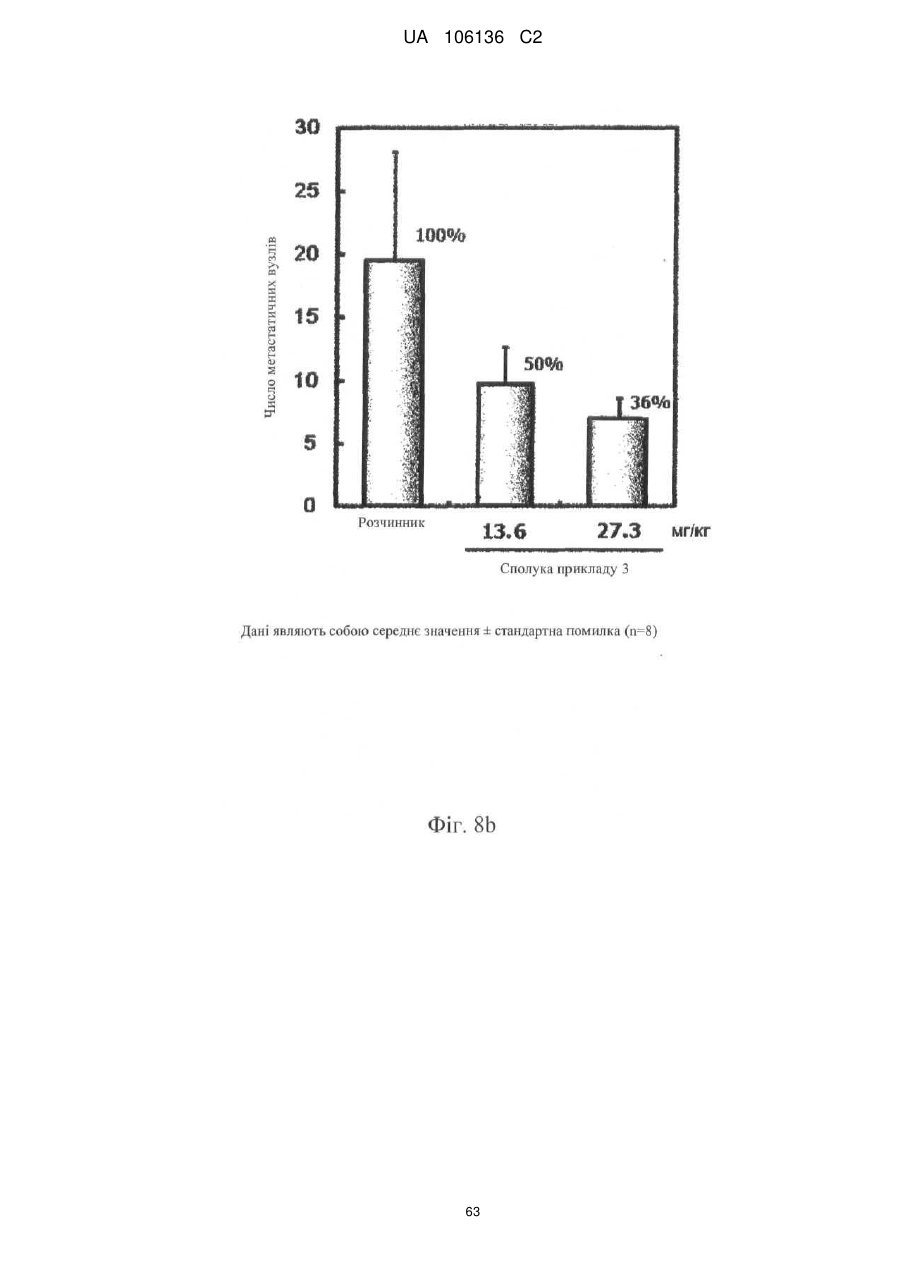
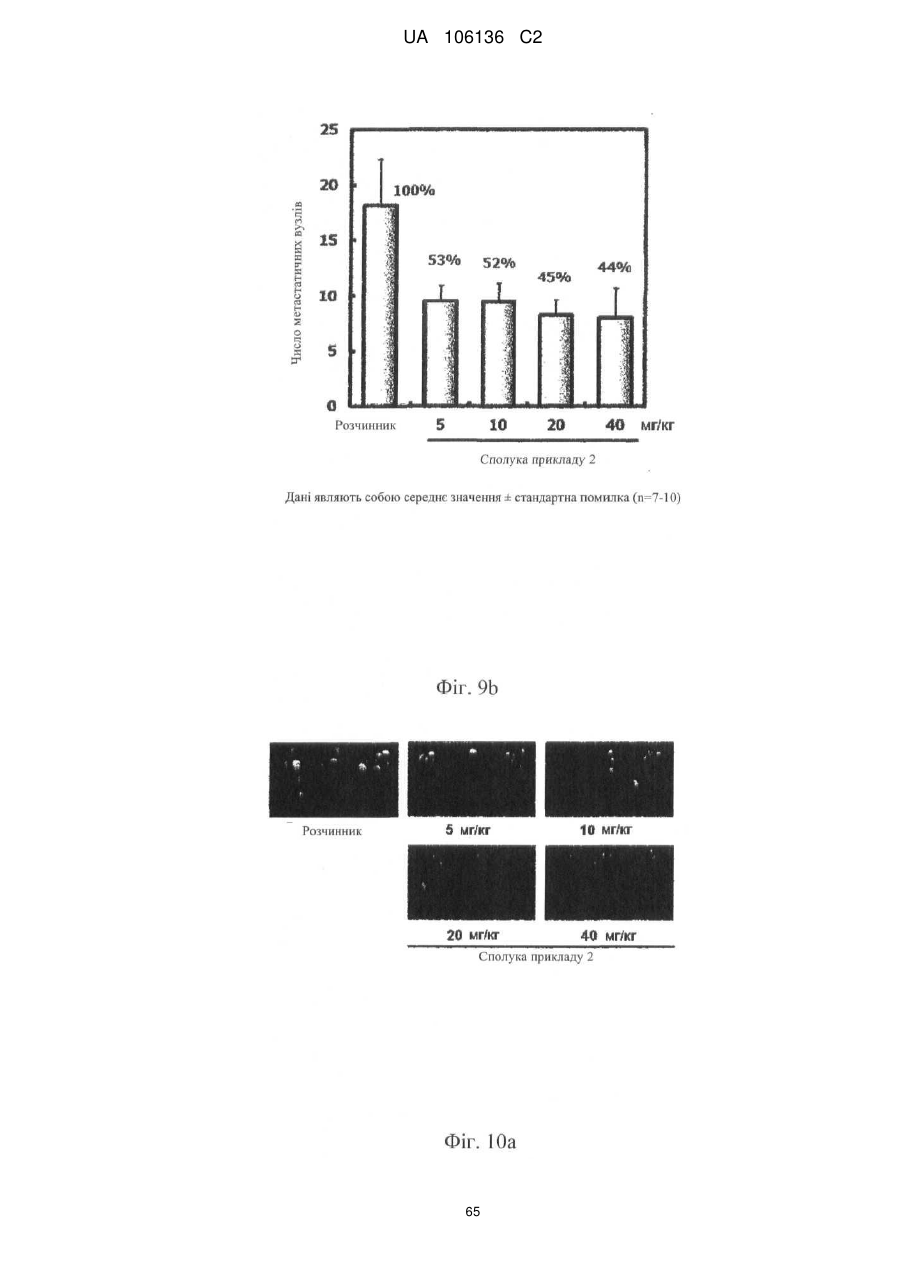
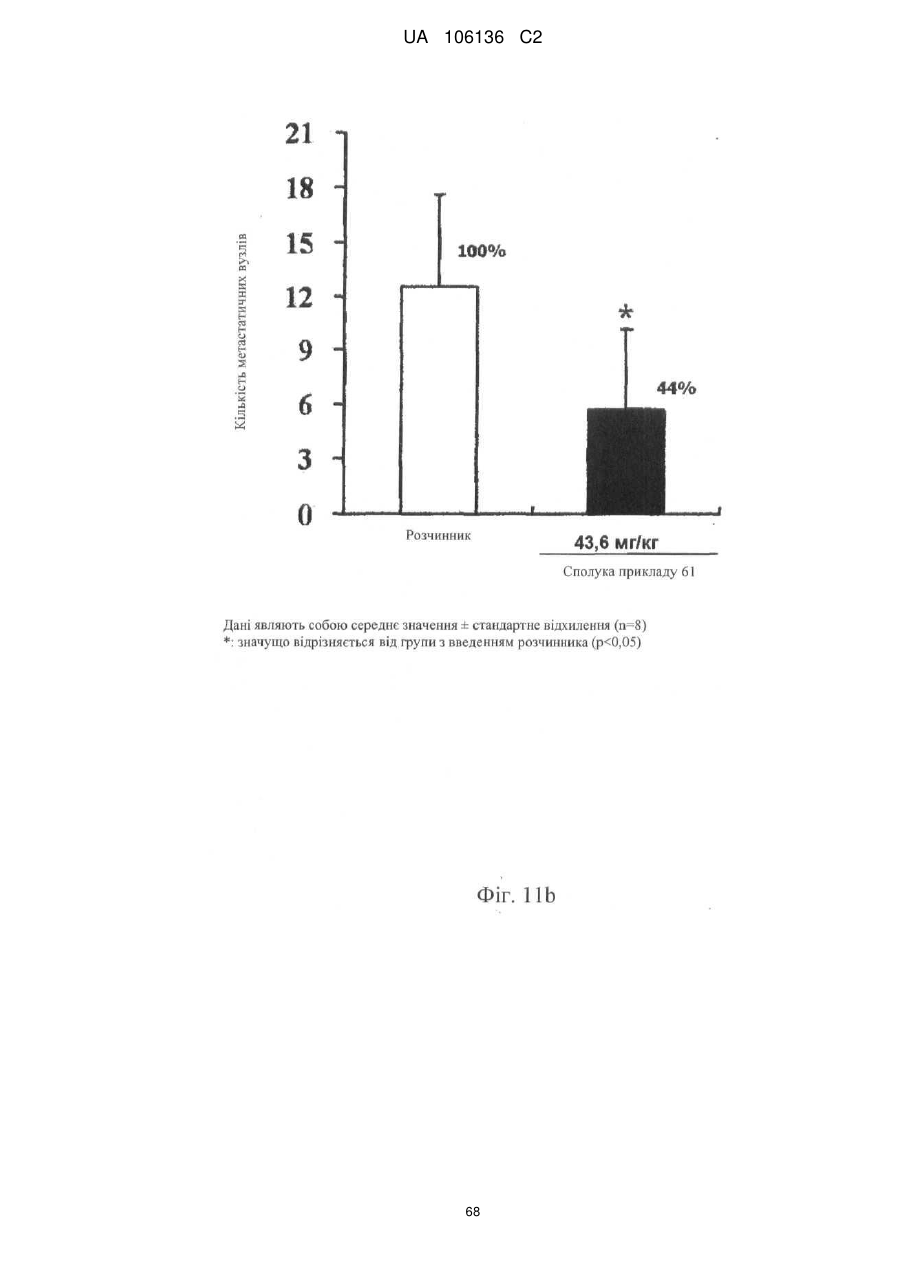
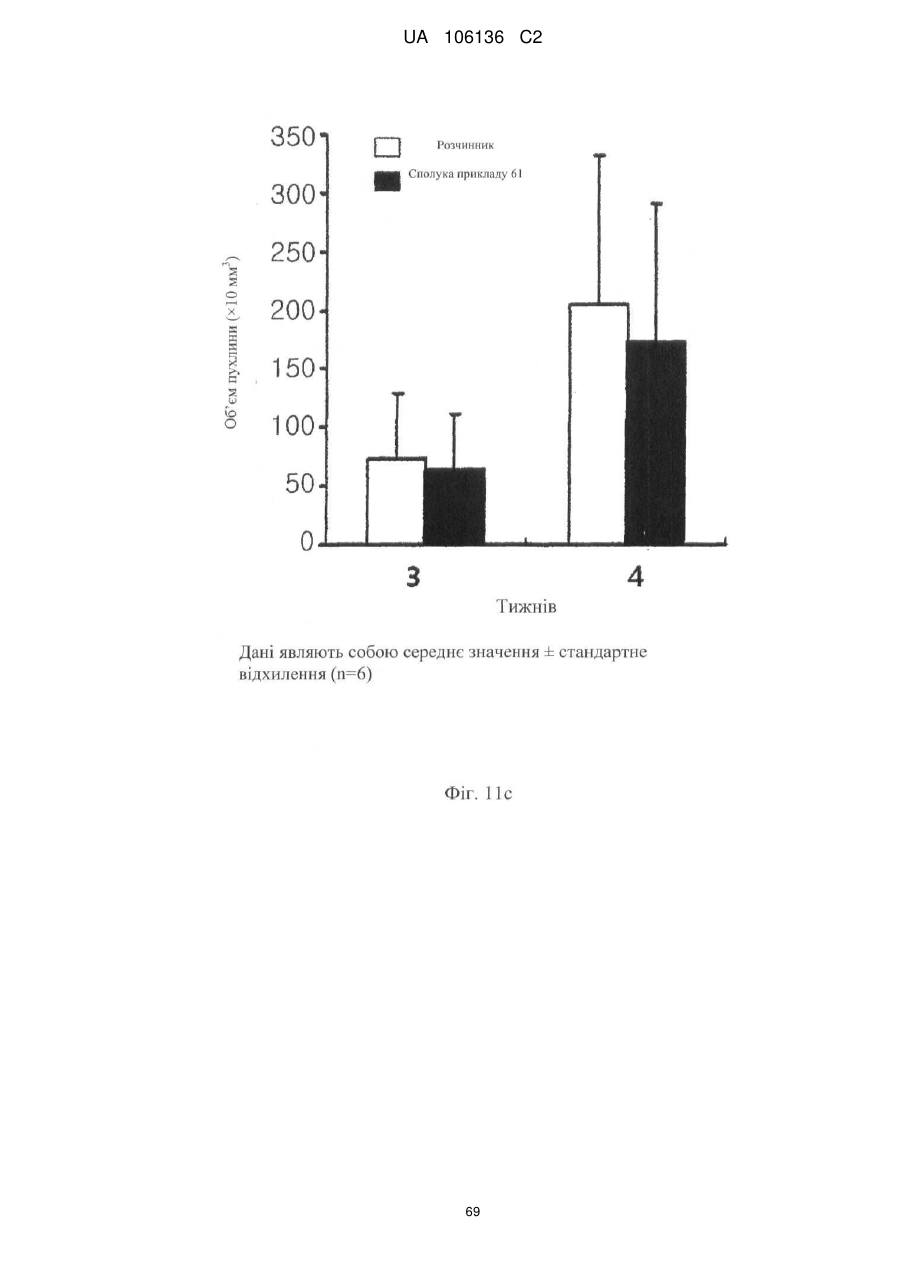
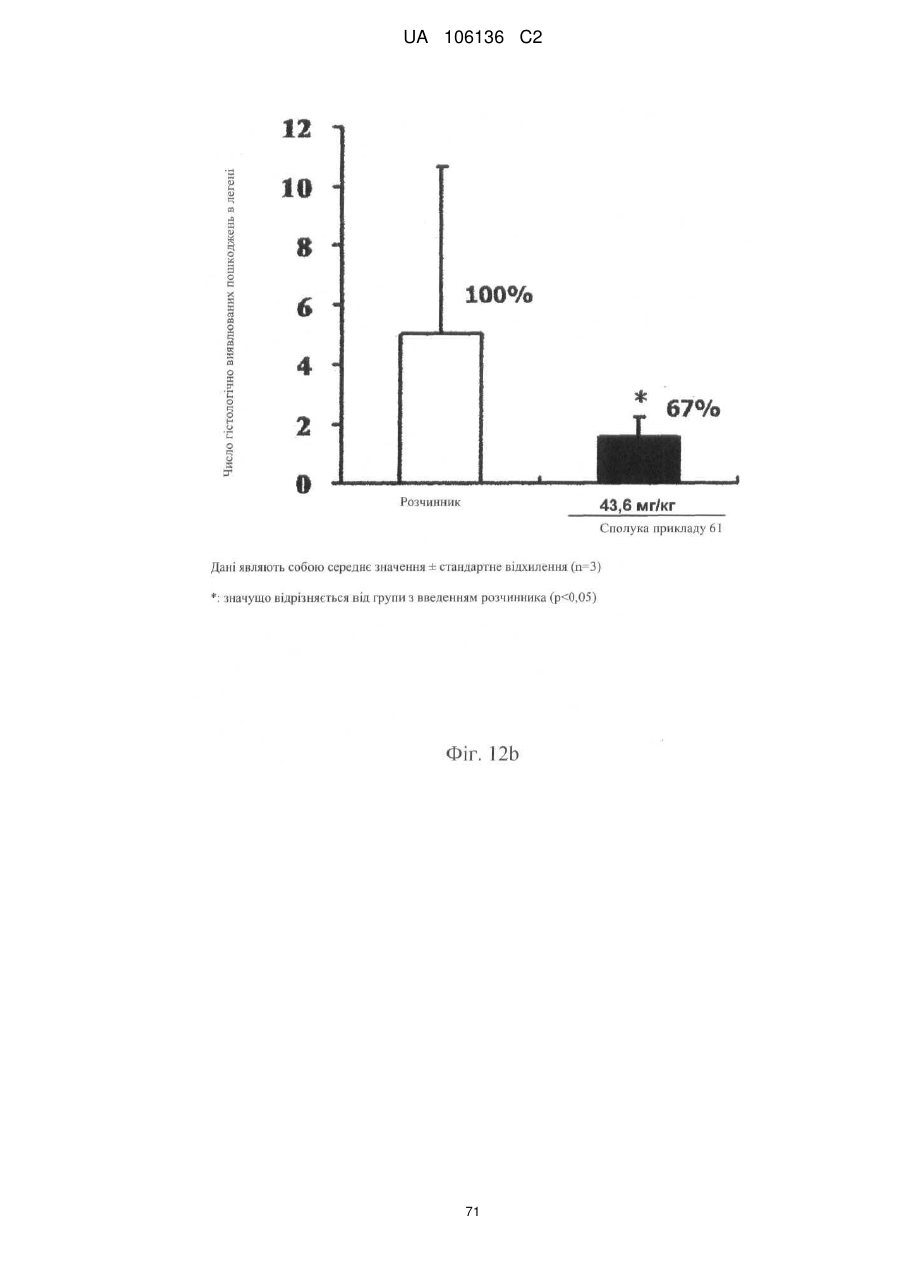
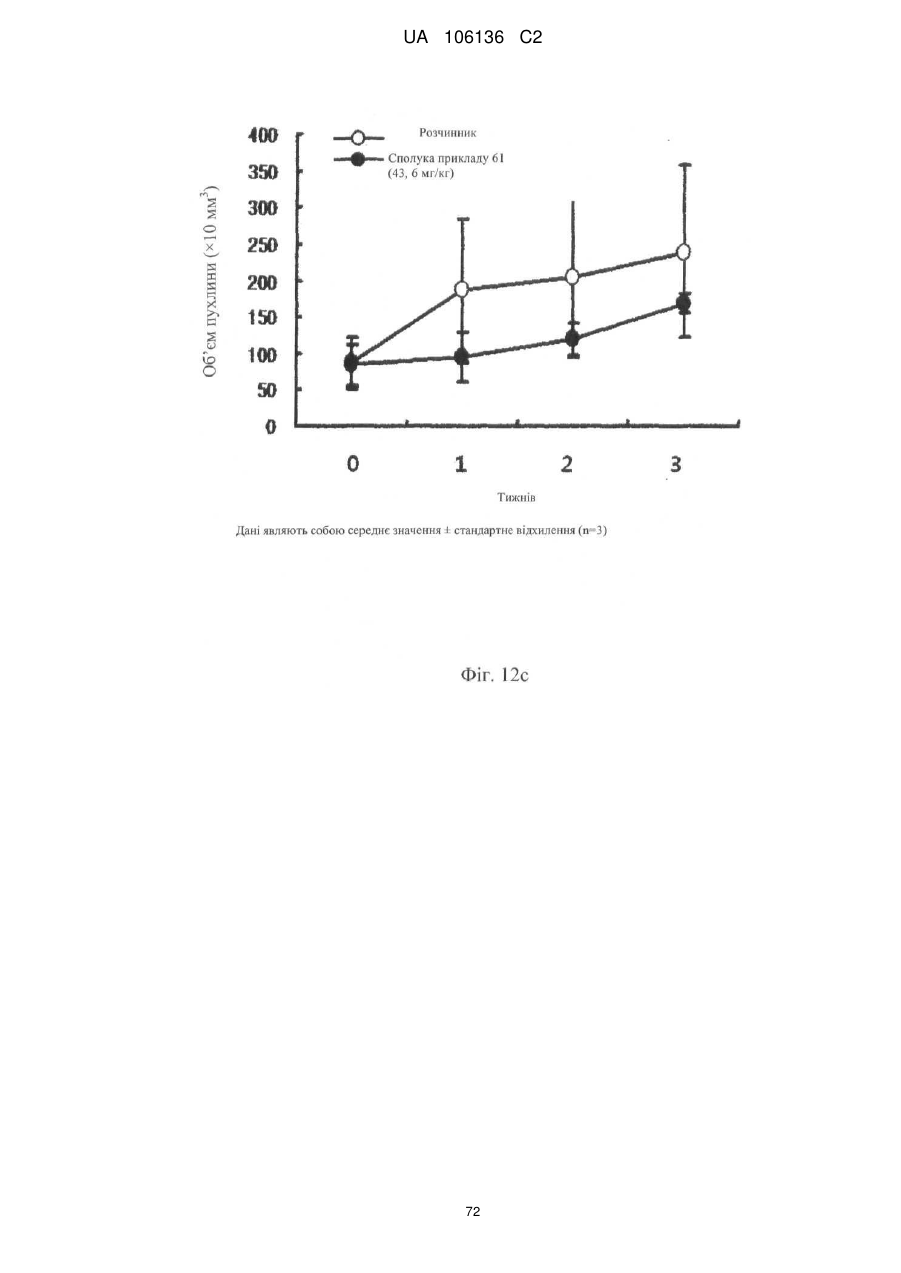
5. Спосіб лікування, профілактики або ослаблення метастазування пухлинних клітин у людини, який включає введення потребуючій такого лікування людині терапевтично ефективної кількості однієї або більше сполук за п. 1 або їх фармацевтично прийнятної солі або гідрату.
6. Спосіб лікування, профілактики або ослаблення карцином, опосередкованих надмірною експресією TGF-β, шляхом інгібування шляху передачі сигналу TGF-β у людини, який включає введення потребуючій такого лікування людині терапевтично ефективної кількості однієї або більше сполук за п. 1 або їх фармацевтично прийнятної солі або гідрату.
7. Спосіб лікування, профілактики або ослаблення судинних пошкоджень у людини, який включає введення потребуючій такого лікування людині терапевтично ефективної кількості однієї або більше сполук за п. 1 або їх фармацевтично прийнятної солі або гідрату.
8. Спосіб лікування, профілактики або ослаблення у людини захворювання, вибраного з групи, що складається з гломерулонефриту, діабетичної нефропатії, нефриту при вовчаку, індукованої гіпертензією нефропатії, ниркового інтерстиціального фіброзу, ниркового фіброзу внаслідок ускладнень при застосуванні ліків, зумовленої ВІЛ нефропатії, зумовленої трансплантацією нефропатії, фіброзу печінки всіх етіологій, пов'язаної з різними інфекціями печінкової дисфункції, індукованого алкоголем гепатиту, порушень жовчних проток, муковісцидозу, пневмофіброзу, інтерстиціального захворювання легень, гострої легеневої недостатності, респіраторного дистрес-синдрому у дорослих, ідіопатичного пневмофіброзу, хронічної обструктивної хвороби легень, індукованого інфекційними або токсичними засобами захворювання легень, фіброзу серця після інфаркту міокарда, застійної серцевої недостатності, кардіоміопатії при дилатації, міокардиту, потовщення інтими, судинного стенозу, індукованого гіпертензією ремоделювання судин, легеневої артеріальної гіпертензії, коронарного рестенозу, периферичного рестенозу, каротидного рестенозу, індукованого стентом рестенозу, атеросклерозу, рубцювання кришталика, рубцювання рогівки, проліферативної вітреоретинопатії, глаукоми, внутрішньоочного тиску, утворення надмірних або гіпертрофічних шрамів або келоїдів на шкірі в процесі загоєння одержаної при травматичних або хірургічних пошкодженнях рани, перитонеальної і підшкірної спайки, склеродермії, фібросклерозу, прогресуючого системного склерозу, дерматоміозиту, поліміозиту, артриту, остеопорозу, виразок, неврологічної дисфункції, еректильної дисфункції у чоловіків, хвороби Пейроні, контрактури Дюпюітрена, хвороби Альцгеймера, синдрому Рейно, індукованого опроміненням фіброзу, тромбозу, росту пухлинних метастазів, множинної мієломи, меланоми, гліоми, гліобластом, лейкозу, сарком, лейоміом, мезотеліоми і карцином легені, молочної залози, товстого кишечнику, яєчника, шийки матки, печінки, жовчних проток, шлунково-кишкового тракту, підшлункової залози, передміхурової залози, голови і шиї.
Текст
Реферат: UA 106136 C2 (12) UA 106136 C2 Даний винахід стосується 2-піридилзаміщених імідазолів, які є інгібіторами рецептора І типу трансформуючого фактора росту-β (TGF-β) (ALK5) і/або рецептора І типу активіну (ALK4), способів їх одержання і їх застосування в медицині, зокрема при лікуванні і профілактиці хворобливого стану, опосередкованого вказаними рецепторами. UA 106136 C2 5 10 15 20 25 30 35 40 45 50 55 60 Галузь техніки, до якої належить винахід Даний винахід стосується 2-піридилзаміщених імідазолів, які є інгібіторами рецептора I типу трансформуючого фактора росту-β (TGF-β) (ALK5) і/або рецептора I типу активіну (ALK4), способів їх одержання і їх застосування в медицині, особливо при лікуванні і профілактиці хворобливого стану, опосередкованого вказаними рецепторами. Рівень техніки TGF-β означає сімейство білків, TGF-β1, TGF-β2 і TGF-β3, які є плейотропними модуляторами клітинної проліферації і диференціювання, процесу загоєння рани, продукції позаклітинного матриксу і пригнічення імунної відповіді. Інші представники цього надсімейства включають активіни, інгібіни, морфогенетичні білки кісток, фактори росту і диференціювання і інгібувальну речовину Мюллера. TGF-β1 передає сигнали через дві висококонсервативні одиночні трансмембранні серин/треонінкінази, рецептори TGF-β I типу (ALK5) і II типу. Після опосередкованої лігандом олігомеризації рецептор II типу гіперфосфорилує серинові/треонінові залишки в області GS ALK5, що приводить до активації ALK5 шляхом створення зв'язуючого сайта для білків Smad. Активований ALK5, в свою чергу, фосфорилує білки Smad2 і Smad3 на С-кінцевому SSXSмотиві, викликаючи, тим самим, їх дисоціацію від рецептора і утворення гетеромерного комплексу з Smad4. Комплекси Smad транслокуються в ядро, асоціюються зі специфічними ДНК-зв'язуючими кофакторами і комодуляторами, зрештою, активуючи транскрипцію компонентів позаклітинного матриксу і інгібіторів руйнуючих матрикс протеаз. Активіни передають сигнали таким же чином, як і TGF-β. Активіни зв'язуються з серин/треонінкіназою, рецептором II типу активіну (ActRIIB), і активований рецептор II типу гіперфосфорилує серин/треонінові залишки в області GS ALK4. Активований ALK4, в свою чергу, фосфорилує Smad2 і Smad3. Подальше утворення гетеро-Smad комплексу з Smad4 приводить до індукованої активіном регуляції транскрипції генів. Численні дослідження на експериментальних тваринах показали взаємозв'язок між гломерулярною експресією TGF-β і фіброзом, включаючи Thy-1 модель проліферативного гломерулонефриту на щурах, анти-GBM гломерулонефрит на кроликах і модель 5/6 нефректомії осередкового сегментарного гломерулосклерозу на щурах, як повідомлялося нещодавно (наприклад, Bitzer M. et al., Kidney Blood Press. Res. 21:1-12 (1998)). Нейтралізація антитіла до TGF-β поліпшує гістологію клубочкової зони на Thy-1 моделі нефриту (наприклад, Border W.A. et al., Nature, 346:371-374 (1990)). Гіперглікемічні умови збільшують синтез мРНК TGF-β і білка як в клітинах проксимальних канальців нирки миші, так і в мезангіальних клітинах людини (наприклад, Wahab N.A. et al., Biochem. J. 316:985-992 (1996); Rocco M.V. et al., Kidney Int. 41:107-114 (1992)). У хворих діабетом з початковим захворюванням нирок виявляється підвищене накопичення мРНК TGF-β і білка в клубочках (наприклад, Yoshioka K. et al., Lab. Invest. 68:154-163 (1993)). В нирках з хронічним нирковим інтерстиціальним фіброзом характерними ознаками є потовщення базальних мембран канальців і збільшений інтерстиціальний компартмент з інтерстиціальним фіброзом, що характеризується збільшенням вмісту колагенів I, III, V, VII і фібронектину (наприклад, Eddy A.A., J. Am. Soc. Nephrol. 7:2495-2508 (1996)). Експресія гена TGF-β і продукція білка збільшуються в різних тваринних моделях пневмофіброзу, включаючи блеоміцинову, кремнеземну, азбестову і радіаційну моделі (наприклад, Phan S.H. and Kunkel S.L., Exp. Lung Res. 18:29-43 (1992); Williams A.O. et al., Am. J. Pathol. 142:1831-1840 (1993); Rube C.E. et al., Int. J. Radiat. Oncol. Biol. Phys. 47:1033-1042 (2000)). Супутнє збільшення вмісту білка TGF-β1 і експресії гена колагену в зрізах прилеглої тканини з ідіопатичного пневмофіброзу спостерігалося при легеневому фіброзному захворюванні людини (наприклад, Broekelmann T.J. et al., Proc. Natl. Acad. Sci. USA 88:66426646 (1991)). Підвищена продукція TGF-β описана у хворих саркоїдозом, пневмоконіозом, азбестозом і індукованим опроміненням фіброзом (наприклад, Khalil N. et al., Am. J. Respir. Cell. Mol. Biol. 14:131-138 (1996); Jagirdar J. et al., Environ. Health Perspect. 105:1197-1203 (1997)). Антитіла до TGF-β і TGF-β-розчинні рецептори могли частково інгібувати фіброз на моделях індукованого блеоміцином легеневого фіброзу у гризунів (наприклад, Giri S.N. et al., Thorax 48:959-966 (1993); Wang Q. et al., Thorax 54:805-812 (1999)). Вважають, що тютюновий дим є одним з найбільш важливих факторів, які можуть спричиняти захворюваннядрібних дихальних шляхів з подальшим розвитком хронічної обструктивної хвороби легень (COPD) (наприклад, Wright J.M. et al., Am. Rev. Respir. Dis. 146:240-262 (1992)). COPD є повільно прогресуючим і необоротним захворюванням, яке характеризується функціональним відхиленням обструкції дихальних шляхів. Була висунена гіпотеза про те, що TGF-β залучений в ремоделювання дихальних шляхів, виявлене при хронічних запальних порушеннях дихальних шляхів, таких як 1 UA 106136 C2 5 10 15 20 25 30 35 40 45 50 55 60 COPD (наприклад, Takizawa H. Int. J. Mol. Med. 1:367-378 (1998); Ning W. et al., Proc. Natl. Acad. Sci. USA 101:14895-14900 (2004)). Зірчасті клітини печінки (HSC) є основним джерелом білків позаклітинного матриксу при фіброзі печінки. Продукція позаклітинного матриксу активованими зірчастими клітинами печінки суттєво збільшується при дії TGF-β1 (наприклад, Friedman S.L., Prog. Liver Dis. 14:101-130 (1996); Pietrangelo А., Semin. Liver Dis. 16:13-30 (1996)). У трансгенних мишей, які надмірно експресують TGF-β1 в печінці, розвивається фіброз печінки, нарівні з такими позапечінковими патологіями як нирковий фіброз (наприклад, Sanderson N. et al., Proc. Natl. Acad. Sci. USA 92:2572-2576 (1995)). TGF-β1 і його рецептори надмірно експресуються в травмованих кровоносних судинах і в фібропроліферативних судинних пошкодженнях, приводячи до надмірної продукції позаклітинного матриксу (наприклад, Saltis J. et al., Clin. Exp. Pharmacol. Physiol. 23:193-200 (1996); McCaffrey T.A. et al., J. Clin. Invest. 96:2667-2675 (1995)). Антитіла до TGF-β знижують утворення рубців і поліпшують цитоархітектуру нових шарів шкіри у щурів (наприклад, Shah M., J. Cell. Sci. 108:985-1002 (1995)), поліпшують загоєння ран рогівки у кроликів (наприклад, Moller-Pedersen Т., Curr. Eye Res. 17:736-747 (1998)) і посилюють загоєння ран шлункових виразок у щурів (наприклад, Ernst Н., Gut 39:172-175 (1996)). Радіаційний фіброз є частим слідством терапевтичного або випадкового надмірного впливу опромінення на нормальні тканини людини. Як повідомлялося нещодавно, TGF-β1 грає центральну роль в ініціації, розвитку і стійкості радіаційного фіброзу (наприклад, Martin M. et al., Int. J. Radiat. Oncol. Biol. Phys. 47:277-290 (2000)). Трансплантація органів ускладняється в багатьох випадках хронічним відторгненням і, для деяких органів, таких як нирка, це являє собою основну форму загибелі пересадженого органа. У пацієнтів-людей хронічне відторгнення трансплантатів легені і нирки пов'язане з підвищеною експресією TGF-β в тканини (наприклад, El-Gamel А. et al., Eur. J. Cardiothorac. Surg. 13:424-430 (1998); Shihab F.S. et al., J. Am. Soc. Nephrol. 6:286-294 (1995)). TGF-β бере участь в утворенні перитонеальних спайок (наприклад, Saed G.M. et al., Wound Repair Regen. 7:504-510 (1999)). Утворення очеревинних і підшкірних фіброзних спайок може бути відвернене інгібіторами ALK5 і/або ALK4. Рівні TGF-β2 у водянистій волозі очей збільшуються майже в половині випадків первинної відкритокутової глаукоми (POAG) і в більшості випадків ювенільної глаукоми (наприклад, Picht G. et al., Graefes Arch. Clin. Exp. Ophthalmol. 239:199-207 (2001)). Повідомлялося, що як TGF-β1, так і TGF-β2 ізоформи підвищують продукцію позаклітинного матриксу в культивованих фібробластах тенонової капсули людини, одержаних від хворих псевдоексфоліативною глаукомою і POAG (наприклад, Kottler U.B. et al., Exp. Eye Res. 80:121-134 (2005)). В патентній заявці США 2007/0142376 A1 розкрите лікування глаукоми і регулювання внутрішньоочного тиску з використанням модулюючих засобів ALK5, і інгібітор ALK5 знижує рівень фібронектину в оброблених TGF-β2 перфузованих передніх відрізках ока людини і рівні фібронектину, інгібітору активатора плазміногена-1 (PAI-1) і С-пептиду проколагену I типу в оброблених TGF-β2 клітинних культурах трабекулярної мережі. Пухлинні клітини і стромальні клітини в пухлинах на останніх стадіях різних злоякісних пухлин, як правило, надмірно експресують TGF-β. Це приводить до стимуляції ангіогенезу і клітинної рухливості, пригнічення імунної системи і збільшеної взаємодії пухлинних клітин з позаклітинним матриксом (наприклад, Hojo M. et al., Nature 397:530-534 (1999)). Внаслідок цього, пухлинні клітини стають більш інвазивними і метастазують до віддалених органів (наприклад, Maehara Y. et al., J. Clin. Oncol. 17:607-614 (1999); Picon А. et al., Cancer Epidemiol. Biomarkers Prev. 7:497-504 (1998)). PAI-1 являє собою основний фізіологічний інгібітор як активатора плазміногена тканинного типу, так і активатора плазміногена урокіназного типу. Підвищені рівні PAI-1 пов'язані з тромбоутворенням і судинним захворюванням, дозволяючи передбачити, що високий рівень PAI-1 в плазмі може спричиняти стан гіперкоагуляції шляхом порушення природного балансу між фібринолізом і коагуляцією (наприклад, Vaughan D.E., J. Invest. Med. 46:370-376 (1998)). Відомо, що TGF-β стимулює експресію PAI-1 (наприклад, Dennler S. et al., EMBO J. 17:3091-3100 (1998)). Відповідно, інгібування продукції PAI-1 за допомогою інгібітору шляху передачі сигналу TGF-β може дати в результаті нову фібринолітичну терапію. Передача сигналу активіну і надмірна експресія активіну пов'язані з патологічними порушеннями, які включають накопичення позаклітинного матриксу і фіброз (наприклад, Matsuse Т. et al., Am. J. Respir. Cell Mol. Biol. 13:17-24 (1995); Inoue S. et al., Biochem. Biophys. Res. Comm. 205:441-448 (1994); Matsuse Т. et al., Am. J. Pathol. 148:707-713 (1996); De Bleser et al., Hepatology 26:905-912 (1997); Pawlowski J.E., et al., J. Clin. Invest. 100:639-648 (1997); 2 UA 106136 C2 5 10 15 20 25 30 35 40 45 50 55 60 Sugiyama M. et al., Gastroenterology, 114:550-558 (1998); Munz В. et al., EMBO J. 18:5205-5215 (1999)), запальні відповіді (наприклад, Rosendahl А. et al., Am. J. Respir. Cell Mol. Biol. 25:60-68 (2001), кахексію або виснаження (Matzuk M.M. et al., Proc. Natl. Acd. Sci. USA, 91:8817-8821 (1994); Coerver K.A. et al., Mol. Endocrinol. 10:534-543 (1996); Cipriano S.C. et al., Endocrinology 141:2319-2327 (2000)), захворювання або патологічні відповіді центральної нервової системи (наприклад, Logan А. et al., Eur. J. Neurosci. 11:2367-2374 (1999); Logan А. et al., Exp. Neurol. 159:504-510 (1999); Masliah Е. et al., Neurochem. Int. 39:393-400 (2001); De Groot C.J.A. et al., J. Neuropathol. Exp. Neurol. 58:174-187 (1999); John G.R. et al., Nat. Med. 8:1115-1121 (2002)) і гіпертензію (наприклад, Dahly A.J. et al., Am. J. Physiol. Regul. Integr. Comp. Physiol. 283:R757767 (2002)). Дослідження показали, що TGF-β і активін можуть діяти синергічно, викликаючи продукцію позаклітинного матриксу (наприклад, Sugiyama M. et al., Gastroenterology, 114:550558 (1998)). Отже, стає очевидним, що інгібування пов'язаного з ALK5 і/або ALK4 фосфорилування Smad2 і Smad3 за допомогою переважних сполук згідно з даним винаходом може забезпечувати лікування і профілактику порушень, що залучають ці шляхи передачі сигналу. У міжнародній патентній публікації WO 00/61576 і патентній заявці США 2003/0149277 A1 розкриті похідні триарилімідазолу і їх застосування як інгібіторів ALK5. У міжнародній патентній публікації WO 01/62756 A1 розкриті похідні піридинілімідазолу і їх застосування як інгібіторів ALK5. У міжнародній патентній публікації WO 02/055077 A1 розкрите застосування імідазолільних похідних циклічного ацеталю як інгібіторів ALK5. У міжнародній патентній публікації WO 03/087304 A2 розкриті тризаміщені гетероарили і їх застосування як інгібіторів ALK5 і/або ALK4. У міжнародній патентній публікації WO 2005/103028 A1 і патенті США 7407958 B2 розкриті 2-піридилзаміщені імідазоли як інгібітори ALK5 і/або ALK4. Особливо, продемонстроване застосування однієї з типових сполук, заявлених в міжнародній патентній публікації WO 2005/103028 A1 і патенті США 7407958 B2, IN-1130, на різних тваринних моделях як інгібітору ALK5 і/або ALK4. IN-1130 ефективно пригнічує нирковий фіброз, індукований одностороннім закупорюванням сечоводу (UUO) у щурів (Moon J.-A. et al., Kidney Int. 70:12341243 (2006)), поліпшує експериментальний аутоімунний енцефаломієліт (EAE) у SBE-luc і GFAP-luc мишей, імунізованих MOG35-55 (Luo J. et al., J. Clin. Invest. 117:3306-3315 (2007)), ослабляє фіброз білкової оболонки і коректує пенільний вигин у щурів (Ryu J.-K. et al., J. Sex. Med. 6:1284-1296 (2009)), і суттєво знижує об'єм пухлини з посиленою імунною відповіддю у мишей, оброблених клітинною лінією раку передміхурової залози мишей Tramp C2 (Lee G.T. et al., J. Urol. 180:2660-2667 (2008)). А також в патентній заявці США 2008/0319012 A1 розкриті 2піридилзаміщені імідазоли як інгібітори ALK5 і/або ALK4. Зокрема, продемонстроване застосування однієї з типових сполук, заявлених в US 2008/0319012 A1, IN-1233, на різних тваринних моделях як інгібітору ALK5 і/або ALK4. IN-1233 ефективно запобігає розвитку і прогресуванню легеневої артеріальної гіпертензії на монокроталіновій моделі у щурів за допомогою інгібування передачі сигналу TGF-β (Long L. et al., Circulation 119:566-576 (2009)), а також запобігає утворенню грануляційної тканини після поміщення непокритого металевого стента в уретральній моделі у щурів (Kim J.H. et al., Radiology 255:75-82 (2010)). Короткий опис суті винаходу Технічне рішення Несподівано було виявлено, що сполуки класу 2-піридилзаміщених імідазолів функціонують як сильні і селективні інгібітори ALK5 і/або ALK4 і, отже, вони застосовні при лікуванні, профілактиці і ослабленні різних опосередкованих ALK5 і/або ALK4 хворобливих станів, таких як гломерулонефрит, діабетична нефропатія, вовчаковий нефрит, індукована гіпертензією нефропатія, нирковий інтерстиціальний фіброз, нирковий фіброз внаслідок ускладнень при застосуванні лікарських засобів, зумовлена ВІЛ нефропатія, зумовлена трансплантацією нефропатія, фіброз печінки всіх етіологій, пов'язана з різними інфекціями печінкова дисфункція, індукований алкоголем гепатит, порушення жовчних проток, муковісцидоз, пневмофіброз, інтерстиціальне захворювання легень, гостра легенева недостатність, респіраторний дистрессиндром у дорослих, ідіопатичний пневмофіброз, хронічна обструктивна хвороба легень, індуковане інфекційними або токсичними засобами захворювання легень, фіброз серця після інфаркту міокарда, застійна серцева недостатність, кардіоміопатія при дилатації, міокардит, потовщення інтими, судинний стеноз, індуковане гіпертензією ремоделювання судин, легенева артеріальна гіпертензія, коронарний рестеноз, периферичний рестеноз, каротидний рестеноз, індукований стентом рестеноз, атеросклероз, рубцювання кришталика, рубцювання рогівки, проліферативна вітреоретинопатія, глаукома, внутрішньоочний тиск, утворення надмірних або гіпертрофічних шрамів або келоїдів на шкірі в процесі загоєння одержаної при травматичних або хірургічних пошкодженнях рани, перитонеальна і підшкірна спайка, склеродермія, 3 UA 106136 C2 5 10 15 20 25 30 35 40 45 50 55 60 фібросклероз, прогресуючий системний склероз, дерматоміозит, поліміозит, артрит, остеопороз, виразки, неврологічна дисфункція, еректильна дисфункція у чоловіків, хвороба Пейроні, контрактура Дюпюітрена, хвороба Альцгеймера, синдром Рейно, індукований опроміненням фіброз, тромбоз, ріст пухлинних метастазів, множинна мієлома, меланома, гліома, гліобластоми, лейкоз, саркоми, лейоміоми, мезотеліома і карциноми легені, молочної залози, товстого кишечнику, яєчника, шийки матки, печінки, жовчних проток, шлунковокишкового тракту, підшлункової залози, передміхурової залози, голови і шиї. Опис креслень Вищезгадані аспекти і інші ознаки даного винаходу будуть пояснюватися в подальшому описі у взаємозв'язку з супровідними кресленнями, де: на фіг. 1 показаний ефект сполук прикладів 2, 60, 86, 92 і 94 на індуковану TGF-β1 активність репортера 3TP-Luc в клітинах HaCaT-3TP-Luc; на фіг. 2 показаний ефект сполук прикладів 2, 60, 86, 92 і 94 на індуковану TGF-β1 активність репортера 3TP-Luc в клітинах 4T1-3TP-Luc; на фіг. 3 показаний ефект сполуки прикладу 2 на індуковану TGF-β1 Smad2/3 ядерну транслокацію в клітинах MCF10A; на фіг. 4 показаний ефект сполуки прикладу 2 на індуковану TGF-β1 клітинну міграцію в клітинах MCF10A; на фіг. 5a і 5b показаний ефект сполуки прикладу 2 на індуковану TGF-β1 клітинну інвазію в клітинах 4T1; (5a) забарвлені DAPI клітини, що залишилися на нижній поверхні; (5b) середнє число клітин на поле спостереження, поліковане від 5 випадкових полів; на фіг. 6 показаний ефект сполуки прикладу 2 на клітинний ріст клітин 4T1; на фіг. 7 показаний ефект сполуки прикладу 2 на клітинний ріст клітин MCF10A; на фіг. 8a і 8b показаний ефект сполуки прикладу 3 на метастазування пухлини молочної залози в легеню у мишей BALB/c з ксенотрансплантатом клітин 4T1; сполуку прикладу 3 (13,6 або 27,3 мг/кг), розчинену у воді (носії), давали мишам перорально BID п'ять днів поспіль на тиждень протягом чотирьох тижнів; (8a) білі плями на поверхні легені вказують на метастатичні вузли (білі стрілки); (8b) число метастатичних вузлів на всій поверхні легені; на фіг. 9a і 9b показаний ефект сполуки прикладу 2 на метастазування пухлини молочної залози в легеню у мишей BALB/c з ксенотрансплантатом клітин 4T1; сполуку прикладу 2 (5, 10, 20 або 40 мг/кг), розчинену в складі штучного шлункового соку (носії), давали мишам перорально п'ять днів поспіль на тиждень протягом трьох тижнів; (9a) білі плями на поверхні легені вказують на метастатичні вузли; (9b) число метастатичних вузлів на поверхні лівої частки легені; на фіг. 10a, 10b і 10c показаний ефект сполуки прикладу 2 на метастазування пухлини молочної залози в легеню у мишей BALB/c з ксенотрансплантатом клітин 4T1; сполуку прикладу 2 (5, 10, 20 або 40 мг/кг), розчинену в складі штучного шлункового соку (носії), давали мишам перорально через день (три рази на тиждень) протягом 24 днів; (10a) білі плями на поверхні легені вказують на метастатичні вузли; (10b) число метастатичних вузлів на поверхні лівої частки легені; (10c) ефект на індуковане TGF-β1 фосфорилування Smad2 в пухлинній тканині; на фіг. 11a, 11b і 11c показаний ефект сполуки прикладу 61 на метастазування пухлини молочної залози в легеню у мишей BALB/c з ксенотрансплантатом клітин 4T1; сполуку прикладу 61 (43,6 мг/кг), розчинену в сольовому розчині (носії), давали мишам інтраперитонеально через день (три рази на тиждень) протягом 2,5 тижня; (11a) білі плями на поверхні легені вказують на метастатичні вузли; (11b) число метастатичних вузлів на поверхні лівої частки легені; (11c) об'єм первинної пухлини; на фіг. 12a, 12b, 12c і 12d показаний ефект сполуки прикладу 61 на метастазування пухлини молочної залози в легеню у MMTV/c-Neu мишей; миші, що є носіями пухлини MMTV/c-Neu, одержували інтраперитонеально лікування сполукою прикладу 61 (43,6 мг/кг) через день протягом трьох тижнів; (12a) забарвлення пухлини молочної залози і тканин легені гематоксиліном і еозином (Н&Е); (12b) число гістологічно метастатичних уражень, що виявляються в легені; (12c) об'єм пухлини молочної залози; (12d) рівень мРНК β-казеїну; на фіг. 13a і 13b показаний ефект сполуки прикладу 3 на метастазування пухлини молочної залози в легеню у MMTV/c-Neu мишей; миші, що є носіями пухлини MMTV/c-Neu, одержували інтраперитонеально лікування сполукою прикладу 3 (43,6 мг/кг) через день протягом десяти тижнів; (13a) рівень мРНК β-казеїну; (13b) активність MMP-9 і MMP-2 в первинній пухлині молочної залози; на фіг. 14a, 14b, 14c і 14d показаний ефект сполуки прикладу 3 на фіброз печінки з перев'язкою жовчної протоки у щурів; сполуку прикладу 3 (21,8 або 43,6 мг/кг), розчинену в сольовому розчині (носії), давали щурам перорально три рази на тиждень протягом чотирьох 4 UA 106136 C2 5 10 15 20 25 30 35 40 45 50 тижнів, починаючи після операції BDL (перев'язка жовчних проток); (14a) активність сироваткової аланінамінотрансферази (ALT) і аспартатамінотрансферази (AST); (14b) рівень білка pSmad3 в печінці. (14c); рівень білків α-SMA, фібронектину і віментину в печінці; (14d) забарвлення тканин печінки гематоксиліном і еозином (Н&Е); на фіг. 15a, 15b і 15c показаний ефект сполуки прикладу 2 на фіброз печінки з перев'язкою жовчної протоки у щурів; сполуку прикладу 2 (5, 10 або 20 мг/кг), розчинену в складі штучного шлункового соку (носій), давали щурам перорально три рази на тиждень протягом чотирьох тижнів, починаючи після операції BDL; (15a) активність ALT і AST; (15b) рівень білків α-SMA і фібронектину в печінці; (15c) забарвлення тканин печінки гематоксиліном і еозином (Н&Е); на фіг. 16a і 16b показаний ефект сполуки прикладу 2 на індукований блеоміцином фіброз легені у мишей; сполуку прикладу 2 (5, 10 або 20 мг/кг), розчинену в складі штучного шлункового соку (носії), давали мишам перорально п'ять разів на тиждень протягом двох тижнів, починаючи з дня 7; (16a) рівень білків α-SMA і фібронектину в легені; (16b) забарвлення тканин легені гематоксиліном і еозином (Н&Е). 1 У таблиці 1 показані структури і спектральні дані H-ЯМР і мас-спектрів сполук прикладів 1139; 1 в таблиці 2 показані структури і дані H-ЯМР і мас-спектрів сполук прикладів 140-153; в таблиці 3 показані значення IC50 сполук вибраних прикладів для фосфорилування кінази ALK5; в таблиці 4 показано або значення IC50, або інгібування фосфорилування різних кіназ (в %) сполукою прикладу 2; в таблиці 5 показаний вплив сполуки прикладу 3 на зміну маси тіла і органів у щурів з BDL; і в таблиці 6 показаний вплив сполуки прикладу 2 на зміну маси тіла і органів у щурів з BDL. Найкращий спосіб здійснення У одному варіанті здійснення даний винахід стосується сполуки формули (I) або її фармацевтично прийнятної солі: , a де кожний R незалежно являє собою Н, галоген, C1-6-алкіл, C1-6-галогеналкіл, C3-6циклоалкіл, OH, -O-C1-6-алкіл, -O-C1-6-галогеналкіл, -O-C3-6-циклоалкіл, NH2, -NH-C1-6-алкіл, -NHC1-6-галогеналкіл, -NH-C3-6-циклоалкіл, -S-C1-6-алкіл, -S-C1-6-галогеналкіл, -S-C3-6-циклоалкіл, CN або NO2; m дорівнює 0, 1, 2, 3 або 4; 1 2 1 1 один з A і A являє собою N, і інший являє собою NR , де R являє собою Н, OH, C1-6-алкіл, C1-6-галогеналкіл або C3-6-циклоалкіл; 2 2 X являє собою зв'язок, -(CH2)p-, -NR -, -O - або -S-, де р дорівнює 0 або 1, і R являє собою Н або C1-3-алкіл; b кожний R незалежно являє собою Н, галоген, C1-6-алкіл, C1-6-галогеналкіл, C3-6-циклоалкіл, 3 3 4 3 C2-6-алкеніл, C2-6-алкініл, -(CH2)q-OR , -(CH2)q-NR R , -(CH2)q-SR , -(CH2)q-NO2, -(CH2)q-CONHOH, 3 3 3 4 (CH2)q-CN, -(CH2)q-COR , -(CH2)q-CO2R , -(CH2)q-CONR R , -(CH2)q-тетразол, -(CH2)q-CH=CH-CN, 3 3 4 3 (CH2)q-CH=CH-CO2R , -(CH2)q-CH=CH-CONR R , -(CH2)q-CH=CH-тетразол, -(CH2)q-NHCOR , 3 3 3 3 (CH2)q-NHCO2R , -(CH2)q-CONHSO2R , -(CH2)q-NHSO2R , -(CH2)q-C≡C-CN, -(CH2)q-C≡C-CO2R , 3 4 5 5 3 (CH2)q-C≡C-CONR R , -(CH2)q-C≡C-тетразол, -(CH2)q-SOR , -(CH2)q-SO2R або -(CH2)r-(OR )2, де 3 4 R і R незалежно являють собою Н, C1-6-алкіл, C1-6-галогеналкіл або C3-6-циклоалкіл; або взяті разом з атомом азоту, до якого вони приєднані, утворюють моноциклічне кільце, таке як 5 імідазол, піролідин, піперидин, морфолін, піперазин і гомопіперазин; R являє собою C1-6-алкіл, C1-6-галогеналкіл або C3-6-циклоалкіл; q дорівнює 0, 1, 2, 3 або 4; і r дорівнює 1, 2, 3 або 4; n дорівнює 0, 1, 2, 3, 4 або 5. Використовуваний в даному описі подвійний зв'язок, позначений в формулі (I) пунктирними лініями, являє собою можливі таутомерні циклічні форми сполук, які входять в обсяг даного винаходу, причому подвійний зв'язок утворений з незаміщеним азотом. a Переважно, R являє собою C1-3-алкіл або галоген. 5 UA 106136 C2 5 10 15 20 25 30 35 40 45 50 55 Переважно, m дорівнює 1 або 2. 1 2 1 1 Переважно, один з A і A являє собою N, і інший являє собою NR , де R являє собою Н. 2 2 Переважно, X являє собою -(CH2)р- або -NR -, де р дорівнює 0, і R являє собою Н. b Переважно, R являє собою галоген, C1-3-алкіл, C1-3-галогеналкіл, C3-4-циклоалкіл, C2-43 3 4 3 3 алкеніл, C2-4-алкініл, -(CH2)q-OR , -(CH2)q-NR R , -(CH2)q-SR , -(CH2)q-CN, -(CH2)q-COR , -(CH2)q3 3 4 3 3 5 5 CO2R , -(CH2)q-CONR R , -(CH2)q-NHCOR , -(CH2)q-NHSO2R , -(CH2)q-SOR або -(CH2)q-SO2R , де 3 4 R і R незалежно являють собою Н, C1-3-алкіл, C1-3-галогеналкіл або C3-4-циклоалкіл; або взяті разом з атомом азоту, до якого вони приєднані, утворюють моноциклічне кільце, таке як 5 імідазол, піролідин, піперидин, морфолін, піперазин і гомопіперазин; R являє собою метил; і q дорівнює 0, 1 або 2. Переважно, n дорівнює 1, 2 або 3. Конкретні сполуки за даним винаходом, які можуть бути наведені, включають наступні сполуки і їх фармацевтично прийнятні солі: N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метил)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2фторанілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3фторанілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-4фторанілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2,3дифторанілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3,4дифторанілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3,5дифторанілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2хлоранілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3хлоранілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-4хлоранілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2,3дихлоранілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3,4дихлоранілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3,5дихлоранілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2броманілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3броманілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-4броманілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2метиланілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3метиланілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-4метиланілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2,3диметиланілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3,4диметиланілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3,5диметиланілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2етиланілін; 6 UA 106136 C2 5 10 15 20 25 30 35 40 45 50 55 60 N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3етиланілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2ізопропіланілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3ізопропіланілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-4ізопропіланілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2вініланілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3вініланілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-4вініланілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3етиніланілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2метоксіанілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3метоксіанілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-4метоксіанілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2,3диметоксіанілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3,4диметоксіанілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3,5диметоксіанілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2(метоксиметил)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3(метоксиметил)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-4(метоксиметил)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2(трифторметоксі)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3(трифторметоксі)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-4(трифторметоксі)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2(метилтіо)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3(метилтіо)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-4(метилтіо)анілін; 2-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)бензонітрил; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)бензонітрил; 4-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)бензонітрил; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)фталонітрил; 2-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)бензамід; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)бензамід; 4-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)бензамід; 7 UA 106136 C2 5 10 15 20 25 30 35 40 45 50 55 60 2-(3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)феніл)ацетонітрил; 2-(4-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)феніл)ацетонітрил; 1-(3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)феніл)етанон; 1-(4-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)феніл)етанон; метил-3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)бензоат; метил-4-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)бензоат; N-(2-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)феніл)ацетамід; N-(3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)феніл)ацетамід; N-(4-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)феніл)ацетамід; N-(2-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)феніл)метансульфонамід; N-(3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)феніл)метансульфонамід; N-(4-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)феніл)метансульфонамід; 1 N -((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)2 2 N ,N -диметилбензол-1,2-діамін; 1 N -((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)3 3 N ,N -диметилбензол-1,3-діамін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2(піролідин-1-іл)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2морфоліноанілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3морфоліноанілін; 3 N -((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-41 1 фтор-N ,N -диметилбензол-1,3-діамін; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)-5-(диметиламіно)бензонітрил; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)-4-(диметиламіно)бензонітрил; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2((диметиламіно)метил)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3((диметиламіно)метил)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2(піролідин-1-ілметил)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3(піролідин-1-ілметил)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2(морфолінометил)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3(морфолінометил)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-5((диметиламіно)метил)-2-фторанілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3((диметиламіно)метил)-2-фторанілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2фтор-3-(піролідин-1-ілметил)анілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2фтор-3-(морфолінометил)анілін; 8 UA 106136 C2 5 10 15 20 25 30 35 40 45 50 55 60 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)-4-((диметиламіно)метил)бензонітрил; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)-2-((диметиламіно)метил)бензонітрил; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)-5-((диметиламіно)метил)бензонітрил; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)-4-(піролідин-1-ілметил)бензонітрил; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)-2-(піролідин-1-ілметил)бензонітрил; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)-5-(піролідин-1-ілметил)бензонітрил; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)-4-(морфолінометил)бензонітрил; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)-2-(морфолінометил)бензонітрил; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)-5-(морфолінометил)бензонітрил; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2(2-(диметиламіно))етиланілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-3(2-(диметиламіно))етиланілін; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-етилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)бензонітрил; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-етилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2фторанілін; N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2-іл)метил)-2фтор-N-метиланілін; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метил)(метиламіно)бензонітрил; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метил)(метиламіно)бензамід; 6-(2-бензил-5-(6-метилпіридин-2-іл)-1H-імідазол-4-іл)-[1,2,4]триазоло[1,5-a]піридин; 6-(2-(2-фторбензил)-5-(6-метилпіридин-2-іл)-1H-імідазол-4-іл)-[1,2,4]триазоло[1,5-a]піридин; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метил)бензонітрил; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метил)бензамід; 6-(5-(6-метилпіридин-2-іл)-2-(феноксиметил)-1H-імідазол-4-іл)-[1,2,4]триазоло[1,5-a]піридин; 6-(2-((2-фторфенокси)метил)-5-(6-метилпіридин-2-іл)-1H-імідазол-4-іл)-[1,2,4]триазоло[1,5a]піридин; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метокси)бензонітрил; 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метокси)бензамід; 6-(5-(6-метилпіридин-2-іл)-2-(фенілтіометил)-1H-імідазол-4-іл)-[1,2,4]триазоло[1,5-a]піридин; 6-(2-((2-фторфенілтіо)метил)-5-(6-метилпіридин-2-іл)-1H-імідазол-4-іл)-[1,2,4]триазоло[1,5a]піридин. Сполуки даного винаходу звичайно являють собою малі органічні молекули (непептидні малі молекули), як правило, розміром приблизно менше 1000 дальтон. Переважні непептидні малі молекули характеризуються молекулярною масою приблизно менше 750 дальтон, більш переважно приблизно менше 500 дальтон. Сполуки формули (I) також можуть бути надані в формі "проліків", які розроблені для вивільнення сполуки формули (I) при введенні суб'єкту. Розроблені форми проліків добре відомі в даній галузі техніки і залежать від замісників, що містяться в сполуці формули (I). Наприклад, гідроксилвмісний замісник може бути сполучений з носієм, який робить сполуку біологічно неактивною доти, поки він не буде видалений під дією ендогенних ферментів або, наприклад, під дією ферментів, націлених на конкретний рецептор або конкретну локалізацію у суб'єкта. Сполука формули (I), яка є кислою за природою (яка, наприклад, містить карбоксильну або фенольну гідроксильну групу), може утворювати фармацевтично прийнятну сіль, наприклад 9 UA 106136 C2 5 10 15 20 25 30 35 40 45 50 55 сіль натрію, калію, кальцію або золота. В обсяг винаходу входять також солі, утворені з такими фармацевтично прийнятними амінами, як аміак, алкіламіни, гідроксіалкіламіни і Nметилглюкамін. Сполука формули (I) може бути оброблена кислотою з утворенням кислотноадитивних солей. Приклади таких кислот включають хлористоводневу кислоту, бромистоводневу кислоту, йодистоводневу кислоту, сірчану кислоту, метансульфонову кислоту, фосфорну кислоту, пара-бромфенілсульфонову кислоту, вугільну кислоту, янтарну кислоту, лимонну кислоту, бензойну кислоту, щавлеву кислоту, малонову кислоту, саліцилову кислоту, яблучну кислоту, фумарову кислоту, аскорбінову кислоту, малеїнову кислоту, оцтову кислоту і інші неорганічні і органічні кислоти, добре відомі фахівцям в даній галузі техніки. Кислотноадитивні солі можуть бути одержані шляхом обробки сполуки формули (I) в її вільній основній формі достатньою кількістю кислоти (наприклад, хлористоводневої кислоти), з одержанням кислотно-адитивної солі (наприклад, гідрохлориду). Кислотно-адитивна сіль може бути перетворена зворотно в свою вільну основну форму шляхом обробки солі придатним розбавленим водним розчином основи (наприклад, гідроксидом натрію, бікарбонатом натрію, карбонатом калію або аміаком). Деякі сполуки даного винаходу можуть бути кристалізовані або перекристалізовані з розчинників, таких як водні і органічні розчинники. У таких випадках, можуть утворюватися сольвати. У обсяг даного винаходу входять стехіометричні сольвати, включаючи гідрати, а також сполуки, що містять змінну кількість води, які можуть бути одержані способами, такими як ліофілізація. Сполуки формули (I) можуть містити один або більше центрів асиметрії і тому можуть існувати у вигляді енантіомерів або діастереомерів. Потрібно розуміти, що даний винахід включає як суміші, так і окремі конкретні ізомери сполук формули (I). Крім того, певні сполуки формули (I), які містять алкенільні групи, можуть існувати у вигляді цис- або транс-ізомерів. У кожному випадку, винахід включає як суміші, так і окремі конкретні ізомери. Сполуки формули (I) також можуть існувати в таутомерних формах, і даний винахід включає як суміші, так і окремі конкретні таутомери. У даний винахід також включені мічені радіоактивним ізотопом похідні сполук формули (I), які придатні для біологічних досліджень. Використовуваний в даному описі термін "алкільна" група стосується насиченої аліфатичної вуглеводневої групи, що містить 1-6 атомів вуглецю. Алкільна група може бути нерозгалуженою або розгалуженою. Приклади алкільної групи включають, але без обмеження, метил, етил, пропіл, ізопропіл, бутил, ізобутил, втор-бутил, трет-бутил, н-пентил і н-гексил. Алкільна група може бути необов'язково заміщена одним або більше замісниками, такими як алкокси, циклоалкокси, аміно, нітро, карбокси, ціано, галоген, гідроксил, сульфо або меркаптогрупа. Використовуваний в даному описі термін "циклоалкільна" група стосується аліфатичного карбоциклічного кільця, що складається з 3-6 атомів вуглецю. Приклади циклоалкільних груп включають циклопропіл, циклобутил, циклопентил і циклогексил. Використовуваний в даному описі термін "галогеналкільна" група стосується алкільної групи, що містить один або більше атомів галогену. Приклади галогеналкільних груп включають фторметил, хлорметил, бромметил і трифторметил. Використовуваний в даному описі термін "галогенова" група стосується фтору, хлору, брому або йоду. Використовуваний в даному описі термін "алкенільна" група стосується аліфатичної вуглецевої групи, що містить 2-6 атомів вуглецю і щонайменше один подвійний зв'язок. Подібно алкільній групі алкенільна група може бути нерозгалуженою або розгалуженою. Приклади алкенільної групи включають, але без обмеження, вініл, аліл, ізопреніл, 2-бутеніл і 2-гексеніл. Алкенільна група може бути необов'язково заміщена одним або більше замісниками, такими як алкокси, циклоалкокси, аміно, нітро, карбокси, ціано, галоген, гідроксил, сульфо або меркаптогрупа. Використовуваний в даному описі термін "алкінільна" група стосується аліфатичної вуглецевої групи, що містить 2-6 атомів вуглецю і щонайменше один потрійний зв'язок. Алкінільна група може бути нерозгалуженою або розгалуженою. Приклади алкінільної групи включають, але без обмеження, етиніл, пропаргіл і бутиніл. Алкінільна група може бути необов'язково заміщена одним або більше замісниками, такими як алкокси, циклоалкокси, аміно, нітро, карбокси, ціано, галоген, гідроксил, сульфо або меркаптогрупа. Використовуваний в даному описі термін "інгібітор ALK5 і/або ALK4" стосується сполуки, відмінної від інгібіторних Smad, наприклад Smad6 і Smad7, яка селективно інгібує переважно рецептори ALK5 і/або ALK4 в порівнянні з рецепторами p38 або рецепторами II типу. 10 UA 106136 C2 5 10 15 20 25 30 Використовуваний в даному описі термін "опосередкований ALK5 і/або ALK4 хворобливий стан" стосується будь-якого хворобливого стану, який опосередковується (або модулюється) ALK5 і/або ALK4, наприклад захворювання, яке модулюється шляхом інгібування фосфорилування Smad2 і Smad3 в шляхах передачі сигналу TGF-β і/або активіну. Використовуваний в даному описі термін "виразки" застосовують для включення, але без обмеження, діабетичних виразок, хронічних виразок, виразок шлунка і виразок дванадцятипалої кишки. Сполуки формули (I) можуть бути одержані рядом відомих способів з комерційно доступних або відомих вихідних речовин. Якщо вихідні речовини не доступні з комерційного джерела, то вони можуть бути одержані способами, відомими в даній галузі техніки. Схема 1 1 2 1 2 Згідно з одним способом, сполуки формули (I), де A являє собою N, і A являє собою NH, 1 2 або A являє собою NH, і A являє собою N, і X являє собою -NH-, одержують, як представлено a на схемі 1. Зокрема, R -заміщений піридин-2-карбальдегід (II) піддають взаємодії з аніліном і дифенілфосфітом, з одержанням N,Р-ацеталю (III), який може бути потім підданий сполученню з [1,2,4]триазоло[1,5-a]піридин-6-карбальдегідом, з подальшим гідролізом в кислих умовах, з одержанням монокетону (IV). Монокетон (IV) може бути окислений до дикетону (V) за допомогою HBr в ДМСО. Одержаний дикетон (V) може бути конденсований з 2,2диметоксіацетальдегідом в присутності ацетату амонію, з одержанням ацетальзахищеного імідазолу (VI), який може бути гідролізований в кислих умовах, з одержанням імідазол-2b карбальдегіду (VII). Імідазол-2-карбальдегід (VII) може бути підданий сполученню з R заміщеним аніліном (VIII) в присутності кислоти, такої як оцтова кислота, з одержанням іміну, який може бути потім відновлений відновником, наприклад боргідридом натрію або a b триацетоксиборгідридом натрію, з одержанням сполуки формули (I). Значення R , R , m і n є такими, як визначено вище. Схема 2 Згідно з іншим способом, сполуки формули (I), де A являє собою N, і A являє собою NH, 1 2 2 або A являє собою NH, і A являє собою N, і X являє собою -(CH2)p-, -NR -, -O- або -S-, де р 11 UA 106136 C2 2 дорівнює 0 або 1, і R являє собою C1-3-алкіл, одержують, як представлено на схемі 2. Дикетон b (V) може бути конденсований з відповідним R -заміщеним альдегідом (IX) в присутності ацетату a b амонію, з одержанням сполуки формули (I). Значення R , R , m і n є такими, як визначено вище. Схема 3 5 b 10 15 20 25 30 35 Альтернативно, якщо в сполуках формули (I) R являє собою -(CH2)q-CN, -(CH2)q-CH=CH-CN або -(CH2)q-C≡C-CN, то він може бути потім функціоналізований з утворенням сполуки формули a 3 4 (I), як представлено на схемі 3. Значення R , R , R , X, m і q є такими, як визначено вище. Одержані сполуки даного винаходу, представлені формулами (I)-(IX), можуть бути розділені і очищені придатними традиційними способами, такими як колонкова хроматографія і перекристалізація. Сполуки даного винаходу можуть бути введені будь-яким придатним шляхом, наприклад, з використанням перорального, букального, сублінгвального, ректального, вагінального, назального, місцевого або парентерального (включаючи внутрішньовенне, внутрішньом'язове, підшкірне і інтракоронарне) введення. Місцеві склади за даним винаходом можуть бути представлені, наприклад, у вигляді мазей, кремів або лосьйонів, очних мазей і очних або вушних крапель, просочених пов'язок і аерозолів і можуть містити прийнятні загальноприйняті добавки, такі як консерванти, розчинники для сприяння проникненню лікарського засобу і пом’якшувачі для мазей і кремів. Склади також можуть містити сумісні загальноприйняті носії, такі як основи для мазей і кремів і етанол або олеїловий спирт для лосьйонів. Такі носії можуть бути присутніми в кількості приблизно від 1% приблизно до 98% складу. Частіше за все вони будуть складати приблизно до 80% складу. Для введення людині при терапевтичному або профілактичному лікуванні наведених вище порушень пероральні, букальні або сублінгвальні дозування сполуки формули (I), як правило, будуть знаходитися в діапазоні 50-5000 мг на добу для середнього дорослого пацієнта (70 кг). Таким чином, для звичайного дорослого пацієнта окремі таблетки або капсули містять 25-500 мг активної сполуки, у придатному фармацевтично прийнятному розчиннику або носії, для введення у вигляді однократної або множинних доз, один або декілька разів на добу. Дозування для парентерального введення, як правило, буде знаходитися в діапазоні 25-250 мг на одну дозу, за потреби. На практиці лікуючий спеціаліст буде визначати конкретну схему дозування, яка буде найбільш придатною для окремого пацієнта, і вона буде змінюватися залежно від віку, маси і реакцій конкретного пацієнта. Вищеперелічені дозування є ілюстративними для середнього випадку, але можуть мати місце окремі випадки, в яких можуть бути використані 12 UA 106136 C2 5 10 15 20 25 30 35 40 45 50 55 більш високі або більш низькі діапазони дозування, і такі діапазони входять в обсяг даного винаходу. Для застосування людині сполука формули (I) може бути введена окремо, але, як правило, буде вводитися в суміші з фармацевтичним носієм, вибраним з урахуванням заданого шляху введення і стандартної фармацевтичної практики. Наприклад, сполука може бути введена перорально, букально або сублінгвально у формі таблеток, що містять такі ексципієнти, як крохмаль або лактоза, або у формі капсул або супозиторіїв, або окремо, або в суміші з ексципієнтами, або у формі еліксирів або суспензій, що містять ароматизатори або барвники. Такі рідкі препарати можуть бути приготовані з такими фармацевтично прийнятними добавками, як суспендуючий засіб (наприклад, метилцелюлоза, напівсинтетичний гліцерид, такий як вітепсол, або суміш гліцеридів, така як суміш масла абрикосових кісточок і складних ефірів PEG-6 або суміш PEG-8 і каприлових/капринових гліцеридів). Сполука також може бути введена шляхом парентеральної ін'єкції, наприклад, внутрішньовенно, внутрішньом'язово, підшкірно або інтракоронарно. Для парентерального введення сполуку краще усього використовувати у формі стерильного водного розчину, який може містити інші речовини, наприклад соліабо моносахариди, такі як маніт або глюкоза, щоб зробити розчин ізотонічним по відношенню до крові. Таким чином, в наступному аспекті даний винахід стосується фармацевтичної композиції, яка містить сполуку формули (I) або її фармацевтично прийнятну сіль або сольват, разом з фармацевтично прийнятним розріджувачем або носієм. Даний винахід також стосується сполуки формули (I) або її фармацевтично прийнятної солі або сольвату, або фармацевтичної композиції за даним винаходом, що їх містить, для застосування в терапії. Даний винахід додатково стосується застосування сполуки формули (I) або її фармацевтично прийнятної солі або сольвату, або фармацевтичної композиції за даним винаходом, що їх містить, для виробництва лікарського засобу для лікування захворювання, опосередкованого рецепторами ALK5 і/або ALK4, у ссавців. Опосередковані ALK5 і/або ALK4 хворобливі стани включають, але без обмеження, гломерулонефрит, діабетичну нефропатію, нефрит при вовчаку, індуковану гіпертензією нефропатію, нирковий інтерстиціальний фіброз, нирковий фіброз внаслідок ускладнень при застосуванні лікарських засобів, зумовлену ВІЛ нефропатію, зумовлену трансплантацією нефропатію, фіброз печінки всіх етіологій, пов'язану з різними інфекціями печінкову дисфункцію, індукований алкоголем гепатит, порушення жовчних проток, муковісцидоз, пневмофіброз, інтерстиціальне захворювання легень, гостру легеневу недостатність, респіраторний дистрессиндром у дорослих, ідіопатичний пневмофіброз, хронічну обструктивну хворобу легень, індуковане інфекційними або токсичними засобами захворювання легень, фіброз серця після інфаркту міокарда, застійну серцеву недостатність, кардіоміопатію при дилатації, міокардит, потовщення інтими, судинний стеноз, індуковане гіпертензією ремоделювання судин, легеневу артеріальну гіпертензію, коронарний рестеноз, периферичний рестеноз, каротидний рестеноз, індукований стентом рестеноз, атеросклероз, рубцювання кришталика, рубцювання рогівки, проліферативну вітреоретинопатію, глаукому, внутрішньоочний тиск, утворення надмірних або гіпертрофічних шрамів або келоїдів на шкірі в процесі загоєння одержаної при травматичних або хірургічних пошкодженнях рани, перитонеальну і підшкірну спайку, склеродермію, фібросклероз, прогресуючий системний склероз, дерматоміозит, поліміозит, артрит, остеопороз, виразки, неврологічну дисфункцію, еректильну дисфункцію у чоловіків, хворобу Пейроні, контрактуру Дюпюітрена, хворобу Альцгеймера, синдром Рейно, індукований опроміненням фіброз, тромбоз, ріст пухлинних метастазів, множинну мієлому, меланому, гліому, гліобластоми, лейкоз, саркоми, лейоміоми, мезотеліому і карциноми легені, молочної залози, товстого кишечнику, яєчника, шийки матки, печінки, жовчних проток, шлунковокишкового тракту, підшлункової залози, передміхурової залози, голови і шиї. Даний винахід додатково стосується способу інгібування шляхів передачі сигналу TGF-β і/або активіну у людини, наприклад інгібування фосфорилування Smad2 або Smad3 ALK5 і/або ALK4. Даний винахід додатково стосується способу ослаблення накопичення надмірного позаклітинного матриксу у людини шляхом інгібування шляхів передачі сигналу TGF-β і/або активіну, наприклад інгібування фосфорилування Smad2 або Smad3 ALK5 і/або ALK4. Даний винахід додатково стосується способу лікування, профілактики або ослаблення метастазування пухлинних клітин у людини шляхом інгібування TGF-β шляху передачі сигналу. 13 UA 106136 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід додатково стосується способу лікування, профілактики або ослаблення карцином, опосередкованих надмірною експресією TGF-β, у людини шляхом інгібування шляху передачі сигналу TGF-β. Даний винахід додатково стосується способу лікування, профілактики або ослаблення судинних пошкоджень у людини шляхом інгібування шляху передачі сигналу TGF-β. Даний винахід додатково проілюстрований в подальших прикладах, які не повинні прийматися як такі, що обмежують обсяг даного винаходу, розкритий в формулі винаходу. У прикладах мас-спектри з іонізацією електророзпиленням (ESI-МС) одержували на Q-TOF2 масспектрометрі (Micromass, Manchester, UK). ПРИКЛАДИ Препаративний приклад 1 Одержання дифеніл(6-метилпіридин-2-іл)(феніламіно)метилфосфонату (сполука формули a (III), де R =CH3) Суміш 6-метилпіридин-2-карбоксальдегіду (2,12 г, 17,50 ммоль), аніліну (1,63 г, 17,50 ммоль), дифенілфосфіту (4,92 г, 21,00 ммоль) і октагідрату цирконілхлориду (0,56 г, 1,75 ммоль) перемішували при кімнатній температурі протягом 1 год. Реакційну суміш екстрагували CH 2Cl2 (350 мл), і CH2Cl2-розчин промивали водою (220 мл), сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням вказаної в заголовку сполуки (6,96 г, 92%) у вигляді білої твердої речовини. 1 Н-ЯМР (400 MГц, CDCl3): δ 7,51 (т, 1H, J=7,8 Гц), 7,38 (дд, 1H, J=7,6, 2,0 Гц), 7,27-7,22 (м, 4H), 7,19-7,15 (м, 2H), 7,14-7,07 (м, 4H), 7,05-7,02 (м, 3H), 6,80-6,74 (м, 3H), 5,53 (псевдо т, 1H, J=7,4 Гц), 5,36 (дд, 1H, J=21,0, 8,2 Гц), 2,54 (с, 3H). Препаративний приклад 2 Одержання дифеніл(6-етилпіридин-2-іл)(феніламіно)метилфосфонату (сполука формули a (III), де R =CH2CH3) Вказану в заголовку сполуку одержували, як описано в препаративному прикладі 1, при використанні 6-етилпіридин-2-карбоксальдегіду замість 6-метилпіридин-2-карбоксальдегіду. Вихід: 81%. 1 Н-ЯМР (400 MГц, CDCl3): δ 7,55 (т, 1H, J=7,6 Гц), 7,38 (дд, 1H, J=7,6, 2,0 Гц), 7,26-7,09 (м, 8H), 7,07-7,00 (м, 5H), 5,59 (псевдо т, 1H, J=7,0 Гц), 5,34 (дд, 1H, J=20,8, 8,0 Гц), 2,82 (кв, 2H, J=7,6 Гц), 1,28 (т, 3H, J=7,6 Гц). Препаративний приклад 3 Одержання 2-([1,2,4]триазоло[1,5-a]піридин-6-іл)-1-(6-метилпіридин-2-іл)етанону (сполука a формули (IV), де R =CH3) До перемішуваного розчину [1,2,4]триазоло[1,5-a]піридин-6-карбальдегіду (2,50 г, 17,01 ммоль) (одержаного згідно зі способом, описаним в WO 03/087304 A2) і дифеніл(6метилпіридин-2-іл)(феніламіно)метилфосфонату (7,32 г, 17,01 ммоль) в суміші ТГФ (40 мл) і ізоPrOH (10 мл) додавали Cs2CO3 (7,20 г, 22,11 ммоль) і перемішували суміш при кімнатній температурі протягом ночі. У реакційну суміш по краплях додавали розчин 3н HCl (25 мл) і перемішували суміш протягом 1 год. Потім суміш розбавляли трет-бутилметиловим ефіром (40 мл) і екстрагували 1н HCl (2×35 мл). Водні екстракти нейтралізували додаванням 50% KOH до досягнення pH 7-8. Осаджені речовини збирали фільтруванням, промивали водою і сушили над P2O5 у вакуумі, з одержанням вказаної в заголовку сполуки (3,41 г, 80%) у вигляді не зовсім білої твердої речовини. 1 Н-ЯМР (400 MГц, CDCl3): δ 8,61 (д, 1H, J=0,8 Гц), 8,31 (с, 1H), 7,88 (дд, 1H, J=7,6, 1,6 Гц), 7,73 (т, 1H, перекрив., J=7,6 Гц), 7,71 (дд, 1H, перекрив., J=9,2, 0,8 Гц), 7,54 (дд, 1H, J=9,2, 1,6 Гц), 7,37 (дд, 1H, J=7,6, 1,6 Гц), 4,62 (с, 2H), 2,67 (с, 3H). Препаративний приклад 4 Одержання 2-([1,2,4]триазоло[1,5-a]піридин-6-іл)-1-(6-етилпіридин-2-іл)етанону (сполука a формули (IV), де R =CH2CH3) Вказану в заголовку сполуку одержували, як описано в препаративному прикладі 3, при використанні дифеніл(6-етилпіридин-2-іл)(феніламіно)-метилфосфонату замість дифеніл(6метилпіридин-2-іл)(феніламіно)-метилфосфонату. Вихід: 78%. 1 Н-ЯМР (400 MГц, CDCl3): δ 8,61 (дд, 1H, J=1,6, 0,8 Гц), 8,29 (с, 1H), 7,88 (ушир.д, 1H, J=7,6 Гц), 7,74 (т, 1H, J=7,6 Гц), 7,70 (дд, 1H, J=9,2, 0,8 Гц), 7,54 (дд, 1H, J=9,2, 1,6 Гц), 7,37 (дд, 1H, J=7,6, 0,8 Гц), 4,62 (с, 2H), 2,93 (кв, 2H, J=7,6 Гц), 1,39 (т, 3H, J=7,6 Гц). Препаративний приклад 5 Одержання 1-([1,2,4]триазоло[1,5-a]піридин-6-іл)-2-(6-метилпіридин-2-іл)етан-1,2-діону a (сполука формули (V), де R =CH3) 14 UA 106136 C2 5 10 15 20 25 30 35 40 45 50 55 60 До перемішуваної суспензії 2-([1,2,4]триазоло[1,5-a]піридин-6-іл)-1-(6-метилпіридин-2іл)етанону (6,20 г, 24,57 ммоль) в ДМСО (48 мл) по краплях при 0 °C додавали HBr (48% мас. у воді, 5,96 г, 12,4 мл) і нагрівали суміш при 60-70 °C. Через 2 год., реакційну суміш охолоджували до 0 °C, вливали у воду з льодом (20 мл) і підлуговували до pH 10 додаванням твердого K 2CO3. Суміш екстрагували CHCl3 (2×250 мл), органічну фазу промивали водою (2×100 мл), сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші MeOH і CH 2Cl2 як елюенту, з одержанням вказаної в заголовку сполуки (6,02 г, 92%) у вигляді ясно-жовтої твердої речовини. 1 Н-ЯМР (400 MГц, CDCl3): δ 9,11 (дд, 1H, J=1,6, 1,2 Гц), 8,47 (с, 1H), 8,14 (дд, 1Н, J=9,2, 1,6 Гц), 8,04 (ушир.д, 1H, J=7,6 Гц), 7,88 (дд, 1Н, J=9,2, 1,2 Гц), 7,84 (т, 1H, J=7,8 Гц), 7,42 (ушир.д, 1H, J=8,0 Гц), 2,49 (с, 3H). Препаративний приклад 6 Одержання 1-([1,2,4]триазоло[1,5-a]піридин-6-іл)-2-(6-етилпіридин-2-іл)етан-1,2-діону a (сполука формули (V), де R =CH2CH3) Вказану в заголовку сполуку одержували, як описано в препаративному прикладі 5, при використанні 2-([1,2,4]триазоло[1,5-a]піридин-6-іл)-1-(6-етилпіридин-2-іл)етанону замість 2([1,2,4]триазоло[1,5-a]піридин-6-іл)-1-(6-метилпіридин-2-іл)етанону. Вихід: 79%. 1 Н-ЯМР (400 MГц, CDCl3): δ 9,11 (дд, 1H, J=1,6, 0,8 Гц), 8,42 (с, 1H), 8,08 (дд, 1H, J=9,2, 1,6 Гц), 7,98 (ушир.д, 1H, J=7,6 Гц), 7,83 (дд, 1H, перекрив., J=9,2, 0,8 Гц), 7,82 (т, 1H, перекрив., J=7,6 Гц), 7,38 (ушир.д, 1H, J=7,6 Гц), 2,71 (кв, 2H, J=7,6 Гц), 1,08 (т, 3H, J=7,6 Гц). Препаративний приклад 7 Одержання 6-(2-(диметоксиметил)-5-(6-метилпіридин-2-іл)-1H-імідазол-4-іл)a [1,2,4]триазоло[1,5-a]піридину (сполука формули (VI), де R =CH3) Перемішуваний розчин 1-([1,2,4]триазоло[1,5-a]піридин-6-іл)-2-(6-метилпіридин-2-іл)етан1,2-діону (6,00 г, 22,49 ммоль) в трет-бутилметиловому ефірі (120 мл) обробляли диметилацетальгліоксалем (60% мас. розчин у воді, 7,8 мл, 44,98 ммоль). Додавали NH 4OAc (4,33 г, 56,2 ммоль) в MeOH (60 мл) і перемішували одержану суміш при кімнатній температурі протягом 3 год. pH реакційної суміші доводили до 8 додаванням насиченого водного розчину NaHCO3. Реакційну суміш екстрагували CHCl3 (2×150 мл), CHCl3-розчин промивали водою (100 мл), сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші MeOH і CH 2Cl2 як елюенту, з одержанням вказаної в заголовку сполуки (6,13 г, 78%) у вигляді ясно-жовтої піни. 1 Н-ЯМР (400 MГц, CDCl3): δ 10,54 (ушир.с, 1H), 8,96 (с, 1H), 8,36 (с, 1H), 7,82 (дд, 1H, J=9,2, 1,6 Гц), 7,77 (дд, 1H, J=9,2, 0,8 Гц), 7,47 (т, 1H, J=7,8 Гц), 7,23 (д, 1H, J=7,6 Гц), 7,04 (д, 1H, J=8,0 Гц), 5,57 (с, 1H), 3,48 (с, 6H), 2,58 (с, 3H). Препаративний приклад 8 Одержання 6-(2-(диметоксиметил)-5-(6-етилпіридин-2-іл)-1H-імідазол-4-іл)a [1,2,4]триазоло[1,5-a]піридину (сполука формули (VI), де R =CH2CH3) Вказану в заголовку сполуку одержували, як описано в препаративному прикладі 7, при використанні 1-([1,2,4]триазоло[1,5-a]піридин-6-іл)-2-(6-етилпіридин-2-іл)етан-1,2-діону замість 1-([1,2,4]триазоло[1,5-a]піридин-6-іл)-2-(6-метилпіридин-2-іл)етан-1,2-діону. Вихід: 68%. 1 Н-ЯМР (400 MГц, CDCl3): δ 10,67 (ушир.с, 1H), 8,97 (ушир.с, 1H), 8,35 (с, 1H), 7,83 (дд, 1H, J=9,2, 1,6 Гц), 7,76 (дд, 1H, J=9,2, 0,8 Гц), 7,50 (т, 1H, J=7,8 Гц), 7,25 (ушир.д, 1H, J=7,6 Гц), 7,05 (д, 1H, J=8,0 Гц), 5,56 (с, 1H), 3,46 (с, 6H), 2,83 (кв, 2H, J=7,6 Гц), 1,31 (т, 3H,J=7,6 Гц). Препаративний приклад 9 Одержання 4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2a карбальдегіду (сполука формули (VII), де R =CH3) 6-(2-(Диметоксиметил)-5-(6-метилпіридин-2-іл)-1H-імідазол-4-іл)-[1,2,4]триазоло[1,5a]піридин (6,00 г, 17,12 ммоль) розчиняли в 1н HCl (120 мл) і нагрівали суміш при 70 °C протягом 3 год. Реакційну суміш залишали охолоджуватися до 0 °C і потім нейтралізували додаванням насиченого водного розчину NaHCO 3. Суміш екстрагували 10% MeOH в CHCl 3 (3×200 мл), органічну фазу сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску, з одержанням вказаної в заголовку сполуки (4,69 г, 90%) у вигляді ясно-жовтої твердої речовини. 1 Н-ЯМР (400 MГц, CDCl3): δ 9,82 (с, 1H), 9,01 (ушир.с, 1H), 8,41 (с, 1H), 7,85 (дд, 1H, J=9,2, 0,8 Гц), 7,82 (дд, 1Н, J=9,2, 1,6 Гц), 7,55 (т, 1H, J=7,8 Гц), 7,33 (ушир.с, 1H), 7,16 (д, 1H, J=8,0 Гц), 2,60 (с, 3H). Препаративний приклад 10 Одержання 4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-етилпіридин-2-іл)-1H-імідазол-2a карбальдегіду (сполука формули (VII), де R =CH2CH3) 15 UA 106136 C2 5 10 15 20 25 30 35 40 45 50 55 60 Вказану в заголовку сполуку одержували, як описано в препаративному прикладі 9, при використанні 6-(2-(диметоксиметил)-5-(6-етилпіридин-2-іл)-1H-імідазол-4-іл)-[1,2,4]триазоло[1,5a]піридину замість 6-(2-(диметоксиметил)-5-(6-метилпіридин-2-іл)-1H-імідазол-4-іл)[1,2,4]триазоло[1,5-a]піридину. Вихід: 99%. 1 H-ЯМР (400 MГц, ДМСО-d6): δ 9,86 (т, 1H, J=1,2 Гц), 9,59 (с, 1H), 8,43 (с, 1H), 8,21 (дд, 1H, J=9,2, 1,6 Гц), 7,82 (ушир.д, 1H, J=8,0 Гц), 7,73 (дд, 1H, J=9,2, 0,8 Гц), 7,69 (т, 1H, J=7,8 Гц), 7,08 (ушир.д, 1H, J=7,6 Гц), 2,71 (кв, 2H, J=7,6 Гц), 1,16 (т, 3H, J=7,6 Гц). Препаративний приклад 11 b Одержання 3-аміно-5-(диметиламіно)бензонітрилу (сполука формули (VIII), де R =3-ціано-5диметиламіно) Вказану сполуку одержували в 2 послідовні стадії, як описано нижче. 3-Бром-N,N-диметил-5-нітроанілін (1,73 г, 7,06 ммоль) (одержаний згідно зі способом, описаним в J. Org. Chem. 60:5091-5103 (2003)), піридин (24 мл) і CuCN (1,26 г, 2,14 ммоль) додавали в суху герметичну пробірку. Суміш нагрівали при 220 °C при перемішуванні протягом 3,5 год. Реакційну суміш залишали охолоджуватися до 100 °C, вливали в колбу, що містить суміш водного аміаку (100 мл) і води (100 мл), і екстрагували EtOAc (2×100 мл). EtOAc-розчин послідовно промивали розбавленим розчином аміаку (100 мл), водою (100 мл) і насиченим розчином солі (100 мл), сушили над безводним Na 2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням 3-(диметиламіно)-5-нітробензонітрилу (0,44 г, 33%) у вигляді оранжевої твердої речовини. 1 H-ЯМР (400 MГц, CDCl3): δ 7,74 (дд, 1H, J=2,0, 1,2 Гц), 7,65 (т, 1H, J=2,2 Гц), 7,11 (дд, 1H, J=2,4, 1,2 Гц), 3,10 (с, 6H). Одержаний вище 3-(диметиламіно)-5-нітробензонітрил (0,42 г, 2,22 ммоль) в метанолі (80 мл) гідрували в присутності 10% Pd/С (0,04 г) в атмосфері водню протягом ночі. Реакційну суміш фільтрували через шар целіту і упарювали фільтрат досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням вказаної в заголовку сполуки (0,29 г, 80%) у вигляді коричневої в'язкої рідини. 1 H-ЯМР (400 MГц, CDCl3): δ 6,35 (дд, 1H, J=2,4, 1,6 Гц), 6,28 (дд, 1H, J=2,0, 1,6 Гц), 6,14 (т, 1H, J=2,2 Гц), 3,76 (ушир.с, 2H), 2,92 (с, 6H). Препаративний приклад 12 b Одержання 3-((диметиламіно)метил)-2-фтораніліну (сполука формули (VIII), де R =3(диметиламіно)метил-2-фтор) Вказану сполуку одержували в 3 послідовні стадії, як описано нижче, використовуючи як вихідну речовину комерційно доступний 2-фтор-1-метил-3-нітробензол. Перемішуваний розчин 2-фтор-1-метил-3-нітробензолу (15,80 г, 101,94 ммоль) і Nбромсукциніміду (18,14 г, 101,94 ммоль) в CCl4 (400 мл) обробляли бензоїлпероксидом (0,37 г, 1,52 ммоль). Суміш нагрівали при температурі кипіння із зворотним холодильником протягом ночі і потім охолоджували до кімнатної температури. Реакційну суміш фільтрували і упарювали фільтрат досуха при зниженому тиску. Залишок розчиняли в CH 2Cl2 (100 мл) і знов упарювали. Фільтрат упарювали досуха при зниженому тиску, і очищали залишок MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням 1-(бромметил)-2-фтор-3нітробензолу (8,11 г, 34%) у вигляді не зовсім білої твердої речовини. 1 Н-ЯМР (400 MГц, CDCl3): δ 8,02 (м, 1H), 7,71 (м, 1H), 7,30 (тд, 1H, J=8,4, 1,6 Гц), 4,55 (д, 2H, J=1,6 Гц). До перемішуваної суміші 1-(бромметил)-2-фтор-3-нітробензолу (0,70 г, 2,99 ммоль) і гідрохлориду диметиламіну (0,48 г, 5,98 ммоль) в CH 2Cl2 (10 мл) по краплях додавали триетиламін (0,91 г, 8,97 ммоль). Суміш перемішували при кімнатній температурі протягом 3 год. і упарювали досуха при зниженому тиску. Залишок розбавляли водою (10 мл) і екстрагували EtOAc (2×25 мл). EtOAc-розчин промивали водою (20 мл), сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням 1-(2-фтор-3нітрофеніл)-N,N-диметилметанаміну (0,45 г, 76%) у вигляді жовтої в'язкої рідини. 1 Н-ЯМР (400 MГц, CD3OD): δ 8,04-7,99 (м, 1H), 7,78-7,73 (м, 1H), 7,37 (тд, 1H, J=8,0, 1,0 Гц), 3,64 (д, 2H, J=2,0 Гц), 2,29 (д, 6H, J=0,8 Гц). Суміш одержаного вище 1-(2-фтор-3-нітрофеніл)-N,N-диметилметанаміну (0,45 г, 1,93 ммоль), залізного порошку (1,35 г, 2,41 ммоль), 2н HCl (1 мл) і етанолу (5 мл) нагрівали при температурі кипіння із зворотним холодильником при перемішуванні протягом 2 год. Після охолоджування до кімнатної температури, суміш фільтрували через шар целіту. Фільтрат упарювали досуха при зниженому тиску, залишок розбавляли водою (10 мл) і підлуговували до 16 UA 106136 C2 5 10 15 20 25 30 35 40 45 50 55 pH 10 додаванням твердого K2CO3. Водну суміш екстрагували EtOAc (2×25 мл), EtOAc-розчин сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням вказаної в заголовку сполуки (0,35 г, 91%) у вигляді білої твердої речовини. 1 H-ЯМР (400 MГц, CDCl3): δ 6,88 (тд, 1H, J=7,8, 1,0 Гц), 6,72-6,67 (м, 2H), 3,71 (ушир.с, 2H), 3,47 (д, 2H, J=1,6 Гц), 2,27 (с, 6H). Препаративний приклад 13 b Одержання 2-фтор-3-(піролідин-1-ілметил)аніліну (сполука формули (VIII), де R =2-фтор-3(піролідин-1-ілметил)) До перемішуваного розчину 1-(бромметил)-2-фтор-3-нітробензолу (2,00 г, 8,54 ммоль) і піролідину (0,91 г, 12,82 ммоль) в CH2Cl2 (15 мл) по краплях при 0 °C додавали триетиламін (1,72 г, 17,08 ммоль). Суміш перемішували при кімнатній температурі протягом ночі і потім упарювали досуха при зниженому тиску. Залишок розбавляли водою (15 мл) і екстрагували EtOAc (2×30 мл). EtOAc-розчин промивали насиченим розчином солі (20 мл), сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням 1-(2фтор-3-нітробензил)піролідину (1,20 г, 63%) у вигляді в'язкого масла. 1 H-ЯМР (400 MГц, CD3OD): δ 8,02-7,97 (м, 1H), 7,81-7,76 (м, 1H), 7,36 (тд, 1H, J=8,0, 1,2 Гц), 3,81 (д, 1H, J=2,0 Гц), 2,62-2,58 (м, 4H), 1,84-1,80 (м, 4H). Вказану в заголовку сполуку одержували, як описано в препаративному прикладі 12, при використанні 1-(2-фтор-3-нітробензил)піролідину замість 1-(2-фтор-3-нітрофеніл)-N,Nдиметилметанаміну. Вихід: 80%. 1 H-ЯМР (400 MГц, CD3OD): δ 6,87 (тд, 1H, J=8,0, 0,8 Гц), 6,77 (тд, 1H, J=8,0, 2,0 Гц), 6,68-6,64 (м, 1H), 3,67 (д, 2H, J=1,6 Гц), 2,60-2,57 (м, 4H), 1,82-1,78 (м, 4H). Препаративний приклад 14 b Одержання 2-фтор-3-(морфолінометил)аніліну (сполука формули (VIII), де R =2-фтор-3(морфолінометил)) Перемішуваний розчин 1-(бромметил)-2-фтор-3-нітробензолу (2,50 г, 10,6 ммоль) і морфоліну (2,78 г, 32,0 ммоль) в толуолі (24 мл) нагрівали при температурі кипіння із зворотним холодильником протягом 2,5 год. Реакційну суміш залишали охолоджуватися до кімнатної температури і потім промивали 1н NaOH (2×20 мл). Водний шар екстрагували EtOAc (2×25 мл), об'єднаний розчин в толуолі і EtOAc-екстракти сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням 4-(2-фтор-3-нітробензил)морфоліну (1,95 г, 89%) у вигляді ясно-жовтої твердої речовини. 1 Н-ЯМР (400 MГц, CD3OD): δ 8,02-7,97 (м, 1H), 7,83-7,78 (м, 1H), 7,36 (тд, 1H, J=8,0, 1,0 Гц), 3,70-3,67 (м, 6H), 2,51 (ушир.т, 4H, J=4,6 Гц). Вказану в заголовку сполуку одержували, як описано в препаративному прикладі 12, при використанні 4-(2-фтор-3-нітробензил)морфоліну замість 1-(2-фтор-3-нітрофеніл)-N,Nдиметилметанаміну. Вихід: 90%. 1 H-ЯМР (400 MГц, CD3OD): δ 6,87 (тд, 1H, J=8,0, 0,8 Гц), 6,77 (тд, 1H, J=8,0, 2,0 Гц), 6,68-6,64 (м, 1H), 3,68 (ушир.т, 4H, J=4,8 Гц), 3,55 (д, 2H, J=1,6 Гц), 2,49 (ушир.т, 4H, J=4,8 Гц). Препаративний приклад 15 b Одержання 3-аміно-4-((диметиламіно)метил)бензонітрилу (сполука формули (VIII), де R =5ціано-2-(диметиламіно)метил) До перемішуваної суміші 4-(бромметил)-3-нітробензонітрилу (5,00 г, 20,74 ммоль) (одержаного згідно зі способом, описаним в WO 07/024945 A1) і гідрохлориду диметиламіну (2,03 г, 24,89 ммоль) в CH2Cl2 (70 мл) по краплях при 0 °C додавали триетиламін (6,30 г, 62,23 ммоль) і перемішували суміш при кімнатній температурі протягом ночі. Реакційну суміш упарювали досуха при зниженому тиску, залишок розбавляли водою (20 мл) і екстрагували CH2Cl2 (3×100 мл). CH2Cl2-розчин сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням 4-((диметиламіно)метил)-3-нітробензолу (3,58 г, 84%) у вигляді оранжевої твердої речовини. 1 H-ЯМР (400 MГц, CDCl3): δ 8,15 (ушир.с, 1H), 7,92 (ушир.с, 1H), 7,85 (ушир.д, 1H, J=7,2 Гц), 3,80 (с, 2H), 2,27 (с, 6H). Вказану в заголовку сполуку одержували, як описано в препаративному прикладі 11, при використанні 4-((диметиламіно)метил)-3-нітробензонітрилу замість 3-(диметиламіно)-5нітробензонітрилу. Вихід: 91%. 17 UA 106136 C2 1 5 10 15 20 25 30 35 40 45 50 55 H ЯМР (400 MГц, CDCl3): δ 7,02 (дд, 1Н, J=7,6, 0,4 Гц), 6,91 (дд, 1Н, J=7,6, 1,6 Гц), 6,84 (д, 1H, J=1,6 Гц), 5,05 (ушир.с, 2H), 3,43 (с, 2H), 2,18 (с, 6H). Препаративний приклад 16 b Одержання 3-аміно-2-((диметиламіно)метил)бензонітрилу (сполука формули (VIII), де R =3ціано-2-(диметиламіно)метил) До перемішуваної суміші 2-(бромметил)-3-нітробензонітрилу (1,10 г, 4,56 ммоль) (одержаного згідно зі способом, описаним в Tetrahedron, 40:1863-1868 (1984)) і гідрохлориду диметиламіну (0,74 г, 9,13 ммоль) в CH2Cl2 (15 мл) по краплях при 0 °C додавали триетиламін (1,85 г, 18,25 ммоль). Одержану суміш перемішували при кімнатній температурі протягом 2 год. і упарювали досуха при зниженому тиску. Залишок розбавляли водою (10 мл) і екстрагували EtOAc (3×50 мл). EtOAc-розчин сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням 2-((диметиламіно)метил)-3-нітробензонітрилу (0,75 г, 80%) у вигляді жовтого масла. 1 H-ЯМР (400 MГц, CDCl3): δ 7,93 (ушир.д, 1H, J=8,0 Гц), 7,85 (дд, 1H, J=8,0, 1,4 Гц), 7,55 (т, 1H, J=8,0 Гц), 3,94 (с, 2H), 2,24 (с, 6H). Вказану в заголовку сполуку одержували, як описано в препаративному прикладі 11, при використанні 2-((диметиламіно)метил)-3-нітробензонітрилу замість 3-(диметиламіно)-5нітробензонітрилу. Вихід: 93%. 1 Н-ЯМР (400 MГц, CDCl3): δ 7,15 (т, 1H, J=7,6 Гц), 7,00 (дд, 1H, J=7,6, 0,8 Гц), 6,83 (д, 1H, J=7,6 Гц), 5,06 (ушир.с, 2H), 3,73 (с, 2H), 2,29 (с, 6H). Препаративний приклад 17 b Одержання 3-аміно-5-((диметиламіно)метил)бензонітрилу (сполука формули (VIII), де R =3ціано-5-(диметиламіно)метил) До перемішуваної суміші 3-(бромметил)-5-нітробензонітрилу (1,50 г, 6,22 ммоль) (одержаного згідно зі способом, описаним в J. Org. Chem. 55:1040-1043 (1990)) і гідрохлориду диметиламіну (1,01 г, 12,44 ммоль) в CH2Cl2 (15 мл) по краплях при 0 °C додавали триетиламін (1,88 г, 18,66 ммоль). Одержану суміш перемішували при кімнатній температурі протягом 3 год. і упарювали досуха при зниженому тиску. Залишок розбавляли водою (15 мл) і екстрагували EtOAc (3×50 мл). EtOAc-розчин сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням 3-((диметиламіно)метил)-5-нітробензонітрилу (1,10 г, 87%) у вигляді в'язкої рідини. 1 H-ЯМР (400 MГц, CDCl3): δ 8,45 (с, 1H), 8,40 (д, 1H, J=1,6 Гц), 8,01 (с, 1H), 3,59 (с, 2H), 2,30 (с, 6H). Вказану в заголовку сполуку одержували, як описано в препаративному прикладі 11, при використанні 3-((диметиламіно)метил)-5-нітробензонітрилу замість 3-(диметиламіно)-5нітробензонітрилу. Вихід: 98%. 1 H-ЯМР (400 MГц, CDCl3): δ 6,96 (м, 1H), 6,88 (ушир.д, 1H, J=0,8 Гц), 6,80 (дд, 1Н, J=2,4, 1,6 Гц), 3,86 (ушир.с, 2H), 3,34 (с, 2H), 2,24 (с, 6H). Препаративний приклад 18 b Одержання 3-аміно-4-(піролідин-1-ілметил)бензонітрилу (сполука формули (VIII), де R =5ціано-2-(піролідин-1-ілметил)) До перемішуваного розчину 4-(бромметил)-3-нітробензонітрилу (5,12 г, 21,57 ммоль) і піролідину (1,84 г, 25,88 ммоль) в CH2Cl2 (72 мл) по краплях при 0 °C додавали триетиламін (6,54 г, 64,71 ммоль). Суміш перемішували при кімнатній температурі протягом 1,5 год. і упарювали досуха при зниженому тиску. Залишок розбавляли водою (30 мл) і екстрагували CH2Cl2 (3×100 мл). CH2Cl2-розчин сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням 3-нітро-4-(піролідин-1-ілметил)бензонітрилу (2,24 г, 45%) у вигляді жовтої твердої речовини. 1 Н-ЯМР (400 MГц, CDCl3): δ 8,16 (д, 1H, J=1,6 Гц), 7,94 (ушир.д, 1H, J=8,0 Гц), 7,83 (дд, 1H, J=8,0, 1,6 Гц), 3,99 (с, 2H), 2,54 (ушир.с, 4H), 1,79 (м, 4H). Вказану в заголовку сполуку одержували, як описано в препаративному прикладі 11, при використанні 3-нітро-4-(піролідин-1-ілметил)бензонітрилу замість 3-(диметиламіно)-5нітробензонітрилу. Вихід: 91%. 1 Н-ЯМР (400 MГц, CDCl3): δ 7,06 (д, 1H, J=7,6 Гц), 6,91 (дд, 1H, J=7,6, 1,6 Гц), 6,84 (д, 1H, J=1,6 Гц), 5,08 (ушир.с, 2H), 3,64 (с, 2H), 2,47 (ушир.с, 4H), 1,78 (ушир.с, 4H). Препаративний приклад 19 18 UA 106136 C2 b 5 10 15 20 25 30 35 40 45 50 55 60 Одержання 3-аміно-2-(піролідин-1-ілметил)бензонітрилу (сполука формули (VIII), де R =3ціано-2-(піролідин-1-ілметил)) До перемішуваного розчину 2-(бромметил)-3-нітробензонітрилу (1,10 г, 4,56 ммоль) і піролідину (0,65 г, 9,13 ммоль) в CH2Cl2 (15 мл) по краплях при 0 °C додавали триетиламін (1,85 г, 18,25 ммоль). Суміш перемішували при кімнатній температурі протягом 2 год. і упарювали досуха при зниженому тиску. Залишок розбавляли водою (10 мл) і екстрагували CH 2Cl2 (3×50 мл). CH2Cl2-розчин сушили над безводним Na 2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням 3-нітро-2-(піролідин-1-ілметил)бензонітрилу (0,96 г, 91%) у вигляді жовтої твердої речовини. 1 Н-ЯМР (400 MГц, CDCl3): δ 7,90 (д, 1H, J=7,6 Гц), 7,83 (дд, 1H, J=7,6, 0,8 Гц), 7,52 (т, 1H, J=7,6 Гц), 4,14 (с, 2H), 2,52 (ушир.с, 4H), 1,72 (ушир.с, 4H). Вказану в заголовку сполуку одержували, як описано в препаративному прикладі 11, при використанні 3-нітро-2-(піролідин-1-ілметил)бензонітрилу замість 3-(диметиламіно)-5нітробензонітрилу. Вихід: 93%. 1 Н-ЯМР (400 MГц, CDCl3): δ 7,13 (т, 1H, J=7,8 Гц), 6,99 (дд, 1H, J=7,8, 1,2 Гц), 6,82 (д, 1H, J=8,0 Гц), 5,11 (ушир.с, 2H), 3,91 (с, 2H), 2,58 (ушир.с, 4H), 1,81 (ушир.с, 4H). Препаративний приклад 20 b Одержання 3-аміно-5-(піролідин-1-ілметил)бензонітрилу (сполука формули (VIII), де R =3ціано-5-(піролідин-1-ілметил)) До перемішуваного розчину 3-(бромметил)-5-нітробензонітрилу (1,50 г, 6,22 ммоль) і піролідину (0,53 г, 7,46 ммоль) в CH2Cl2 (15 мл) по краплях при 0 °C додавали триетиламін (1,88 г, 18,68 ммоль) і перемішували суміш при кімнатній температурі протягом ночі. Реакційну суміш упарювали досуха при зниженому тиску, залишок розбавляли водою (15 мл) і екстрагували EtOAc (3×50 мл). EtOAc-розчин сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням 3-нітро-5-(піролідин-1-ілметил)бензонітрилу (1,30 г, 90%) у вигляді жовтої твердої речовини. 1 H-ЯМР (400 MГц, CDCl3): δ 8,45 (ушир.с, 1H), 8,39 (ушир.т, 1H, J=1,6 Гц), 8,02 (ушир.с, 1H), 3,78 (с, 2H), 2,56 (ушир.с, 4H), 1,84 (ушир.с, 4H). Вказану в заголовку сполуку одержували, як описано в препаративному прикладі 11, при використанні 3-нітро-5-(піролідин-1-ілметил)бензонітрилу замість 3-(диметиламіно)-5нітробензонітрилу. Вихід: 85%. 1 Н-ЯМР (400 MГц, CDCl3): δ 6,99 (псевдо т, 1H, J=1,6 Гц), 6,94 (псевдо т, 1H, J=1,6 Гц), 6,79 (дд, 1H, J=2,4, 1,6 Гц), 3,87 (ушир.с, 2H), 3,56 (с, 2H), 2,54 (м, 4H), 1,81 (м, 4H). Препаративний приклад 21 b Одержання 3-аміно-4-(морфолінометил)бензонітрилу (сполука формули (VIII), де R =5ціано-2-(морфолінометил)) До перемішуваного розчину 4-(бромметил)-3-нітробензонітрилу (7,12 г, 29,55 ммоль) і морфоліну (3,09 г, 35,45 ммоль) в CH2Cl2 (98 мл) по краплях при 0 °C додавали триетиламін (8,97 г, 88,64 ммоль). Суміш перемішували при кімнатній температурі протягом 1,5 год. і упарювали досуха при зниженому тиску. Залишок розбавляли водою (40 мл) і екстрагували CH2Cl2 (3×100 мл). CH2Cl2-розчин промивали водою (50 мл), сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням 4-(морфолінометил)-3нітробензонітрилу (5,84 г, 80%) у вигляді жовтої твердої речовини. 1 H-ЯМР(400 MГц, CDCl3): δ 8,12 (с, 1H), 7,83 (ушир.с, 2H), 3,84 (с, 2H), 3,67 (т, 4H, J=4,6 Гц), 2,45 (т, 4H, J=4,6 Гц). Вказану в заголовку сполуку одержували, як описано в препаративному прикладі 11, при використанні 4-(морфолінометил)-3-нітробензонітрилу замість 3-(диметиламіно)-5нітробензонітрилу. Вихід: 78%. 1 Н-ЯМР (400 MГц, CDCl3): δ 7,05 (д, 1H, J=8,0 Гц), 6,92 (дд, 1H, J=8,0, 1,6 Гц), 6,86 (д, 1H, J=1,6 Гц), 5,02 (ушир.с, 2H), 3,68 (ушир.т, 4H, J=4,0 Гц), 3,53 (с, 2H), 2,41 (ушир.с, 4H). Препаративний приклад 22 b Одержання 3-аміно-2-(морфолінометил)бензонітрилу (сполука формули (VIII), де R =3ціано-2-(морфолінометил)) До перемішуваного розчину 2-(бромметил)-3-нітробензонітрилу (1,10 г, 4,56 ммоль) і морфоліну (0,80 г, 9,13 ммоль) в CH2Cl2 (15 мл) по краплях при 0 °C додавали триетиламін (1,85 г, 18,25 ммоль). Суміш перемішували при кімнатній температурі протягом 1,5 год. і упарювали досуха при зниженому тиску. Залишок розбавляли водою (10 мл) і екстрагували CH 2Cl2 (3×50 19 UA 106136 C2 5 10 15 20 25 30 35 40 45 50 55 мл). CH2Cl2-розчин сушили над безводним Na 2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням 2-(морфолінометил)-3-нітробензонітрилу (1,02 г, 90%) у вигляді жовтої твердої речовини. 1 Н-ЯМР (400 MГц, CDCl3): δ 7,90 (ушир.д, 1H, J=8,0 Гц), 7,84 (дд, 1H, J=8,0, 1,2 Гц), 7,56 (т, 1H, J=8,0 Гц), 3,99 (с, 2H), 3,60 (ушир.т, 4H, J=4,4 Гц), 2,46 (ушир.с, 4H). Вказану в заголовку сполуку одержували, як описано в препаративному прикладі 11, при використанні 2-(морфолінометил)-3-нітробензонітрилу замість 3-(диметиламіно)-5нітробензонітрилу. Вихід: 82%. 1 Н-ЯМР (400 MГц, CDCl3): δ 7,15 (т, 1H, J=7,6 Гц), 7,01 (д, 1H, J=7,6 Гц), 6,83 (д, 1H, J=7,6 Гц), 5,00 (ушир.с, 2H), 3,78 (с, 2H), 3,69 (ушир.с, 4H), 2,50 (ушир.с, 4H). Препаративний приклад 23 b Одержання 3-аміно-5-(морфолінометил)бензонітрилу (сполука формули (VIII), де R =3ціано-5-(морфолінометил)) До перемішуваного розчину 3-(бромметил)-5-нітробензонітрилу (1,50 г, 6,22 ммоль) і морфоліну (0,65 г, 7,46 ммоль) в CH2Cl2 (15 мл) по краплях при 0 °C додавали триетиламін (1,88 г, 18,66 ммоль). Суміш перемішували при кімнатній температурі протягом ночі і потім упарювали досуха при зниженому тиску. Залишок розбавляли водою (15 мл) і екстрагували EtOAc (3×50 мл). EtOAc-розчин сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням 3-(морфолінометил)-5-нітробензонітрилу (0,87 г, 85%) у вигляді не зовсім білої твердої речовини. 1 Н-ЯМР (400 MГц, CDCl3): δ 8,45 (ушир.с, 1H), 8,41 (ушир.с, 1H), 8,01 (ушир.с, 1H), 3,74 (ушир.т, 4H, J=4,4 Гц), 3,64 (с, 2H), 2,48 (ушир.т, 4H, J=4,4 Гц). Вказану в заголовку сполуку одержували, як описано в препаративному прикладі 11, при використанні 3-(морфолінометил)-5-нітробензонітрилу замість 3-(диметиламіно)-5нітробензонітрилу. Вихід: 85%. 1 H-ЯМР (400 MГц, CDCl3): δ 7,00 (ушир.т, 1Н, J=1,6 Гц), 6,93 (ушир.с, 1H), 6,81 (дд, 1Н, J=2,4, 1,6 Гц), 3,88 (ушир.с, 2H), 3,74 (ушир.т, 4H, J=4,6 Гц), 3,44 (с, 2H), 2,47 (ушир.с, 4H). Препаративний приклад 24 b Одержання 2-(2-фторфеноксі)ацетальдегіду (сполука формули (IX), де R =2-фтор, X=О). Вказану сполуку одержували в 2 послідовні стадії. Перемішувану суміш 2-фторфенолу (1,00 г, 8,92 ммоль), 2-бром-1,1-діетоксіетану (1,75 г, 8,92 ммоль) і K2CO3 (1,47 г, 10,7 ммоль) в безводному ДМФА (10 мл) нагрівали при 110 °C протягом ночі. Реакційну суміш вливали в льодяну воду (15 мл) і екстрагували EtOAc (2×100 мл). EtOAc-розчин промивали водою (25 мл) і насиченим розчином солі (25 мл), сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням 1-(2,2діетоксіетокси)-2-фторбензолу (1,65 г, 81%) у вигляді в'язкої рідини. 1 Н-ЯМР (400 MГц, CDCl3): δ 7,09-6,96 (м, 3H), 6,93-6,87 (м, 1H), 4,85 (т, 1H, J=5,2 Гц), 4,07 (д, 2H, J=5,2 Гц), 3,82-3,74 (м, 2H), 3,69-3,61 (м, 2H), 1,24 (т, 6H, J=7,0 Гц). До перемішуваного розчину 1-(2,2-діетоксіетокси)-2-фторбензолу (1,65 г, 7,23 ммоль) в суміші 1,4-діоксану (50 мл) і води (40 мл) при 0 °C додавали конц. HCl (17,6 мл) і перемішували суміш при кімнатній температурі протягом ночі. Реакційну суміш охолоджували до 0 °C, нейтралізували додаванням насиченого розчину NaHCO 3 і екстрагували EtOAc (2×200 мл). EtOAc-розчин сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням вказаної в заголовку сполуки (0,78 г, 71%) у вигляді в'язкої рідини. 1 Н-ЯМР (400 MГц, CDCl3): δ 9,87 (с, 1H), 7,12 (ддд, 1H, J=11,4, 8,2, 1,6 Гц), 7,08-7,04 (м, 1H), 7,01-6,95 (м, 1H), 6,91 (тд, 1H, J=8,2, 1,6 Гц), 4,63 (с, 2H). Препаративний приклад 25 b Одержання 2-(2-фторфенілтіо)ацетальдегіду (сполука формули (IX), де R =2-фтор, X=S) Вказану сполуку одержували в 2 послідовні стадії. Суміш 2-фтортіофенолу (1,00 г, 7,80 ммоль), діетилацеталю бромацетальдегіду (1,41 мл, 9,36 ммоль) і Cs2CO3 (3,05 г, 9,36 ммоль) в безводному ДМФА (20 мл) перемішували в атмосфері N2 при кімнатній температурі протягом ночі. Реакційну суміш фільтрували через металокерамічну лійку і розбавляли фільтрат водою (20 мл). Водну суміш екстрагували Et2O (3×100 мл), органічну фазу сушили над безводним MgSO 4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану 20 UA 106136 C2 5 10 15 20 25 30 35 40 45 50 55 60 як елюенту, з одержанням (2,2-діетоксіетил)(2-фторфеніл)сульфану (1,81 г, 95%) у вигляді в'язкої рідини. 1 Н-ЯМР (400 MГц, CDCl3): 6 7,46-7,41 (м, 1H), 7,24-7,18 (м, 1H), 7,09-7,02 (м, 1H), 4,64 (т, 1H, J=5,6 Гц), 3,69-3,61 (м, 2H), 3,56-3,49 (м, 2H), 3,10 (д, 2H, J=5,6 Гц), 1,17 (т, 6H, J=7,2 Гц). До перемішуваного розчину (2,2-діетоксіетил)(2-фторфеніл)сульфану (1,00 г, 4,09 ммоль) в суміші 1,4-діоксану (30 мл) і води (25 мл) при 0 °C додавали конц. HCl (9 мл) і перемішували суміш при кімнатній температурі протягом 2 год. Реакційну суміш охолоджували до 0 °C, нейтралізували додаванням насиченого розчину NaHCO 3 і екстрагували CH2Cl2 (3×50 мл). Органічну фазу промивали водою (50 мл), сушили над безводним Na 2SO4, фільтрували і упарювали досуха при зниженому тиску, з одержанням вказаної в заголовку сполуки (0,59 г, 85%) у вигляді в'язкої рідини, яку відразу використовували на наступній стадії без додаткового очищення. 1 H-ЯМР (400 MГц, CDCl3): δ 9,56 (тд, 1H, J=3,2, 1,2 Гц), 7,42-7,38 (м, 1H), 7,31-7,25 (м, 1H), 7,12-7,06 (м, 2H), 3,58 (д, 2H, J=3,2 Гц). Препаративний приклад 26 b Одержання 3-(метил(2-оксоетил)аміно)бензонітрилу (сполука формули (IX), де R =3-ціано, X=NMe) Вказану сполуку одержували в 3 стадії, використовуючи як вихідну речовину комерційно доступний 3-амінобензонітрил. До перемішуваного розчину 3-амінобензонітрилу (2,50 г, 21,10 ммоль) в безводному ДМСО (30 мл) при 0 °C порціями додавали NaH (0,61 г, 25,39 ммоль), перемішували суміш при кімнатній температурі протягом 20 хв. і потім обробляли діетилацетальбромацетальдегідом (4,20 г, 21,10 ммоль). Через 2 год., при 0 °C повільно додавали насичений водний NH4Cl (20 мл) і екстрагували реакційну суміш EtOAc (2×50 мл). EtOAc-розчин сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням EtOAc і гексану як елюенту, з одержанням 3-(2,2-діетоксіетиламіно)бензонітрилу (0,86 г, 17%) у вигляді ясно-оранжевого масла. 1 H-ЯМР (400 MГц, CDCl3): δ 7,22 (тд, 1H, J=7,8, 0,6 Гц), 6,97 (м, 1H), 6,84-6,81 (м, 2H), 4,67 (т, 1H, J=5,4 Гц), 3,77-3,69 (м, 2H), 3,61-3,53 (м, 2H), 3,24 (д, 2H, J=5,6 Гц), 1,24 (т, 6H, J=7,0 Гц). До премішуваного розчину 3-(2,2-діетоксіетиламіно)бензонітрилу (0,84 г, 3,59 ммоль) в безводному ДМФА (5 мл) при 0 °C порціями додавали NaH (0,10 г, 4,30 ммоль). Через 20 хв., додавали MeI (0,61 г, 4,30 ммоль) і перемішували суміш при кімнатній температурі протягом 6 год. Реакційну суміш охолоджували до 0 °C і по краплях додавали водний розчин NH4Cl (10 мл). Водну суміш екстрагували CHCl3 (2×30 мл), органічну фазу сушили над безводним Na 2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші EtOAc і гексану як елюенту, з одержанням 3-((2,2діетоксіетил)(метил)аміно)бензонітрилу (0,65 г, 73%) у вигляді в'язкої рідини. 1 H-ЯМР (400 MГц, CDCl3): δ 7,28-7,24 (м, 1H), 6,96-6,93 (м, 3H), 4,60 (т, 1H, J=5,2 Гц), 3,763,69 (м, 2H), 3,55-3,47 (м, 2H), 3,46 (д, 2H, J=5,2 Гц), 3,02 (с, 3H), 1,20 (т, 6H, J=7,0 Гц). До перемішуваного розчину 3-((2,2-діетоксіетил)(метил)аміно)бензонітрилу (0,65 г, 2,61 ммоль) в безводному діоксані (6 мл) при 0 °C по краплях додавали 1н HCl (4,30 ммоль) і перемішували суміш при кімнатній температурі протягом 1 год. Реакційну суміш охолоджували до 0 °C, нейтралізували додаванням водного розчину NaHCO 3 і екстрагували CHCl3 (2×30 мл). CHCl3-розчин сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску, з одержанням вказаної в заголовку сполуки (0,24 г, 52%) у вигляді в'язкої рідини, яку використовували на наступній стадії без додаткового очищення. 1 Н-ЯМР (400 MГц, CDCl3): δ 9,74 (т, 1H, J=0,8 Гц), 7,29 (ддд, 1H, J=8,8, 7,4, 0,8 Гц), 7,02 (ддд, 1H, J=7,4, 0,8, 1,2 Гц), 6,86 (дд, 1H, J=2,4, 1,2 Гц), 6,82 (ддд, 1H, J=8,8, 2,4, 1,2 Гц) 4,14 (д, 2H, J=0,8 Гц), 3,10 (с, 3H). Препаративний приклад 27 b Одержання 2-((2-фторфеніл)(метил)аміно)ацетальдегіду (сполука формули (IX), де R =2фтор, X=NMe) Вказану сполуку одержували в 3 стадії, використовуючи як вихідну речовину комерційно доступний 2-фторанілін. Перемішувану суміш 2-фтораніліну (2,00 г, 17,90 ммоль), диметилацетальбромацетальдегіду (3,25 мл, 21,40 ммоль) і Cs 2CO3 (11,70 г, 35,80 ммоль) в безводному ДМФА (10 мл) нагрівали до 120 °C протягом ночі. Реакційну суміш упарювали досуха при зниженому тиску і екстрагували залишок Et2O (2×150 мл). Et2O-розчин промивали водою (4×50 мл) і насиченим розчином солі (2×50 мл), сушили над безводним MgSO 4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з 21 UA 106136 C2 5 10 15 20 25 30 35 40 45 використанням суміші EtOAc і гексану як елюенту, з одержанням N-(2,2-діетоксіетил)-2фтораніліну (2,00 г, 49%) у вигляді безбарвного масла. 1 Н-ЯМР (400MГц, CDCl3): δ 7,03-6,95 (м, 2H), 6,82-6,77 (м, 1H), 6,71-6,65 (м, 1H), 4,72 (т, 1H, J=5,6 Гц), 3,78-3,71 (м, 2H), 3,62-3,54 (м, 2H), 3,29 (д, 2H, J=5,6 Гц), 1,26-1,22 (м, 6H). До перемішуваного розчину N-(2,2-діетоксіетил)-2-фтораніліну (1,00 г, 4,40 ммоль) в безводному ДМФА (10 мл) при 0 °C порціями додавали NaH (0,16 г, 6,60 ммоль). Через 30 хв., додавали MeI (0,5 мл, 8,80 ммоль) і перемішували суміш при кімнатній температурі протягом ночі. Реакційну суміш екстрагували EtOAc (2×100 мл), EtOAc-розчин промивали водою (50 мл) і насиченим розчином солі (50 мл), сушили над безводним Na 2SO4, фільтрували і упарювали досуха при зниженому тиску, з одержанням N-(2,2-діетоксіетил)-2-фтор-N-метиланіліну (0,41 г, 38%) у вигляді безбарвного масла. 1 Н-ЯМР (400 MГц, CDCl3): δ 7,05-6,96 (м, 3H), 6,83-6,81 (м, 1H), 4,69 (т, 1H, J=5,2 Гц), 3,723,64 (м, 2H), 3,55-3,49 (м, 2H), 3,33 (дд, 2H, J=5,2, 1,2 Гц), 2,97 (с, 3H), 1,19-1,53 (м, 6H). До перемішуваного розчину N-(2,2-діетоксіетил)-2-фтор-N-метиланіліну (0,40 г, 1,60 ммоль) в 1,4-діоксані (5 мл) при 0 °C по краплях додавали 2,5н HCl (5 мл) і перемішували суміш при кімнатній температурі протягом ночі. Реакційну суміш охолоджували до 0 °C, нейтралізували додаванням насиченого розчину NaHCO3 і екстрагували CHCl3 (2×50 мл). CHCl3-розчин промивали водою (20 мл) і насиченим розчином солі (20 мл), сушили над Na 2SO4, фільтрували і упарювали досуха при зниженому тиску, з одержанням вказаної в заголовку сполуки (0,27 г, 98%) у вигляді безбарвного масла, яке використовували на наступній стадії без додаткового очищення. 1 Н-ЯМР (400 MГц, CDCl3): δ 9,80 (дд, 1H, J=2,4, 1,2 Гц), 7,07-6,89 (м, 4H), 3,91 (дд, 2H, J=1,8, 0,8 Гц), 2,97 (с, 3H). Приклад одержання 1 Одержання N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метил)-3-вініланіліну (приклад 37) До перемішуваного розчину 4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)1H-імідазол-2-карбальдегіду (4,00 г, 13,14 ммоль) в 1,2-дихлоретані (240 мл) додавали 3вініланілін (2,36 г, 19,71 ммоль) і AcOH (0,79 г, 13,14 ммоль), і нагрівали суміш при 80 °C протягом 2 год. Реакційну суміш охолоджували до 0 °C, і додавали NaBH(OAc)3 (5,56 г, 26,20 ммоль). Суміш перемішували при 40 °C протягом ночі, і потім доводили pH реакційної суміші до 7-8 додаванням при 0 °C 10% розчину K2CO3. Реакційну суміш екстрагували 5% MeOH в CHCl 3 (2×200 мл), органічну фазу сушили над безводним Na 2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші MeOH і CH 2Cl2 (1/19 (об./об.)) як елюенту, з одержанням вказаної в заголовку сполуки (2,89 г, 63%) у вигляді твердої речовини. 1 H-ЯМР (400 MГц, CDCl3): δ 10,59 (ушир.с, 1H), 8,94 (с, 1H), 8,37 (с, 1H), 7,81 (д, 1H, J=9,2 Гц), 7,77 (д, 1H, J=9,2 Гц), 7,45 (т, 1H, J=7,8 Гц), 7,20 (ушир.д, 1H, перекрив., J=7,6 Гц), 7,15 (т, 1H, перекрив., J=7,8 Гц), 7,00 (д, 1H, J=8,0 Гц), 6,86 (д, 1H, J=7,6 Гц), 6,75 (т, 1H, J=2,0 Гц), 6,63 (дд, 1H, перекрив., J=17,6, 10,8 Гц), 6,61 (дд, 1H, перекрив., J=8,0, 2,0 Гц), 5,69 (дд, 1H, J=17,6, 0,8 Гц), 5,21 (дд, 1H, J=10,8, 0,8 Гц), 4,55 (с, 2H), 4,39 (ушир.с, 1H), 2,51 (с, 3H); МС (ESI) m/z 408,21. Приклад одержання 2 Одержання гідрохлориду N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)1H-імідазол-2-іл)метил)-3-вініланіліну (приклад 38) 22 UA 106136 C2 5 10 15 20 25 30 35 Перемішувану суспензію N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)1H-імідазол-2-іл)метил)-3-вініланіліну (1,00 г, 2,45 ммоль) в безводному CHCl3 (12 мл) нагрівали при 50 °C, з одержанням прозорого розчину. CHCl3-розчин охолоджували до 0 °C, додавали 1,0M HCl в Et2O (7,36 мл, 7,36 ммоль). Через 5 хв., осад фільтрували в атмосфері N 2 і ретельно сушили над P2O5 у вакуумі, з одержанням вказаної в заголовку сполуки (1,07 г, 98%) у вигляді жовтого порошку. 1 Н-ЯМР (400 MГц, ДМСО-d6): δ 9,49 (дд, 1H, J=1,6, 0,8 Гц), 8,65 (с, 1H), 7,97 (дд, 1H, J=9,2, 0,8 Гц), 7,86 (дд, 1H, перекрив., J=9,2, 1,6 Гц), 7,85 (т, 1H, перекрив., J=7,8 Гц), 7,65 (д, 1H, J=8,0 Гц), 7,38 (д, 1H, J=7,6 Гц), 7,12 (т, 1H, J=7,8 Гц), 6,91 (т, 1H, J=1,6 Гц), 6,79 (д, 1H, J=7,6 Гц), 6,71 (дд, 1H, J=8,0, 1,6 Гц), 6,64 (дд, 1Н, J=17,6, 11,2 Гц), 5,80 (дд, 1Н, J=17,6, 0,8 Гц), 5,20 (дд, 1H, J=11,2, 0,8 Гц), 4,79 (с, 2H), 2,51 (с, 3H). Приклад одержання 3 Одержання сульфату N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1Hімідазол-2-іл)метил)-3-вініланіліну (приклад 39) До перемішуваної суспензії N-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)1H-імідазол-2-іл)метил)-3-вініланіліну (100 мг, 0,25 ммоль) в безводному EtOH (2 мл) при 0 °C додавали 10% H2SO4 в безводному EtOH (0,20 мл, 0,37 ммоль). Суміш залишали нагріватися до кімнатної температури і перемішували протягом 10 хв. Реакційну суміш розбавляли безводним Et2O (8 мл) і додатково перемішували протягом 10 хв. Осаджені речовини фільтрували в атмосфері N2, промивали безводним Et2O (4×4 мл) і потім ретельно сушили над P2O5 у вакуумі, з одержанням вказаної в заголовку сполуки (79 мг, 64%) у вигляді жовтої твердої речовини. 1 H-ЯМР (400 MГц, ДМСО-d6): δ 9,40 (дд, 1H, J=1,6, 0,8 Гц), 8,63 (с, 1H), 7,98 (дд, 1H, J=9,2, 0,8 Гц), 7,84 (т, 1H, J=8,0 Гц), 7,76 (дд, 1H, J=9,2, 1,6 Гц), 7,43 (д, 1H, J=7,6 Гц), 7,40 (д, 1H, J=8,0 Гц), 7,13 (т, 1H, J=7,8 Гц), 6,80 (ушир.с, 1H), 6,79 (д, 1H, перекрив., J=7,6 Гц), 6,64 (дд, 1H, перекрив., J=17,6, 11,2 Гц), 6,63 (дд, 1H, перекрив., J=7,6, 2,0 Гц), 5,74 (дд, 1H, J=17,6, 0,8 Гц), 5,21 (дд, 1H, J=11,2, 0,8 Гц), 4,68 (с, 2H), 2,58 (с, 3H). Приклад одержання 4 Одержання 3-((4-([1,2,4]триазоло[1,5-a]піридин-6-іл)-5-(6-метилпіридин-2-іл)-1H-імідазол-2іл)метиламіно)-4-((диметиламіно)метил)бензонітрилу (приклад 116) До перемішуваного розчину 4-((1,2,4)триазоло(1,5-a)піридин-6-іл)-5-(6-метилпіридин-2-іл)1H-імідазол-2-карбальдегіду (0,50 г, 1,64 ммоль) в 1,2-дихлоретані (30 мл) додавали 3-аміно-4((диметиламіно)метил)бензонітрил (0,43 г, 2,46 ммоль) і AcOH (0,20 г, 3,29 ммоль), і суміш нагрівали при 80 °C протягом ночі. Реакційну суміш концентрували при зниженому тиску, і залишок розчиняли в безводному MeOH (30 мл). До метанольного розчину при 0 °C додавали 23 UA 106136 C2 5 10 NaBH4 (0,25 г, 6,57 ммоль), і потім суміш залишали нагріватися до кімнатної температури і додатково перемішували протягом 3 год. pH реакційної суміші доводили до 7-8 додаванням при 0 °C 1н HCl, і потім видаляли MeOH при зниженому тиску. Водну суміш екстрагували CH 2Cl2 (2×50 мл), CH2Cl2-розчин сушили над безводним Na2SO4, фільтрували і упарювали досуха при зниженому тиску. Залишок очищали MPLC на силікагелі з використанням суміші MeOH і CH2Cl2 (1/19 (об./об.)) як елюенту, з одержанням вказаної в заголовку сполуки (0,60 г, 79%) у вигляді білої твердої речовини. 1 H-ЯМР (400 MГц, CDCl3): δ 8,99 (с, 1H), 8,36 (с, 1H), 7,86 (дд, 1H, J=9,2, 1,6 Гц), 7,78 (дд, 1H, J=9,2, 0,8 Гц), 7,47 (т, 1H, J=7,6 Гц), 7,23 (ушир.д, 1H, J=7,6 Гц), 7,09 (д, 1H, J=7,6 Гц), 7,01 (д, 1H, J=7,6 Гц), 6,98 (дд, 1H, J=7,6, 1,6 Гц), 6,93 (ушир.с, 1H), 4,59 (с, 2H), 3,63 (с, 2H), 2,53 (с, 3H), + 2,33 (с, 6H); МС (ESI) m/z 464,23 (MH ). Сполуки, перераховані в подальшій таблиці 1, одержували способом, аналогічно описаному вище в прикладах одержання 1-4. У таблицю 1 включені дані мас-спектрометрії для вказаних сполук. 15 Таблиця 1 Приклад 1 2 3 4 5 6 1 Структура Н-ЯМР (м.ч.) МС (ESI) m/z + (MH ) (400 MГц, CDCl3): δ 10,43 (ушир.с, 1H), 8,96 (с, 1H), 8,37 (с, 1H), 7,82 (дд, 1H, J=9,2, 1,6 Гц), 7,77 (дд, 1H, J=9,2, 0,8 Гц), 7,45 (т, 1H, J=7,6 Гц), 7,25-7,19 382,19 (м, 3H), 7,01 (д, 1H, J=7,6 Гц), 6,80 (тт, 1H, J=8,0, 1,2 Гц), 6,74-6,72 (м, 2H), 4,55 (с, 2H), 2,53 (с, 3H) (400 MГц, CDCl3): δ 11,34 (ушир.с, 1H), 8,96 (дд, 1H, J=1,6, 0,8 Гц), 8,35 (с, 1H), 7,81 (дд, 1H, J=9,2, 1,6 Гц), 7,74 (дд, 1H, J=9,2, 0,8 Гц), 7,45 (т, 1H, 400,18 J=7,6 Гц), 7,23 (д, 1H, J=7,6 Гц), 6,97-6,90 (м, 2H), 6,94 (дд, 1H, J=8,0, 1,2 Гц), 6,72 (тд, 1H, J=8,4, 1,6 Гц), 6,69-6,63 (м, 1H), 4,51 (с, 2H), 2,35 (с, 3H) (400 MГц, ДМСО-d6): δ 9,44 (д, 1H, J=0,8 Гц), 8,62 (с, 1H), 7,96 (дд, 1H, J=9,2, 0,8 Гц), 7,83 (т, 1H, J=8,0 Гц), 7,80 (дд, 1H, J=9,2, 1,6 Гц), 7,53 (д, 1H, J=8,0 Гц), 7,38 (д, 1H, J=7,6 Гц), 7,10 (ддд, 1H, J=12,0, 8,0, 1,2 Гц), 7,01 (тд, 1H, J=7,6, 1,2 Гц), 6,88 (ушир.т, 1H, J=8,6 Гц), 6,70-6,64 (м, 1H), 4,75 (с, 2H), 2,54 (с, 3H) (400 MГц, ДМСО-d6): δ 9,40 (дд, 1H, J=2,0, 0,8 Гц), 8,64 (с, 1H), 7,99 (дд, 1H, J=9,2, 0,8 Гц), 7,85 (т, 1H, J=8,0 Гц), 7,77 (дд, 1H, J=9,2, 2,0 Гц), 7,42 (псевдо т, 2H, J=7,4 Гц), 7,11 (ддд, 1H, J=12,0, 8,0, 1,2 Гц), 7,02 (тд, 1H, J=7,6, 1,2 Гц), 6,82 (тд, 1H, J=8,0, 1,2 Гц), 6,71-6,65 (м, 1H), 4,73 (с, 2H), 2,59 (с, 3H) (400 MГц, CDCl3): δ 8,94 (т, 1H, J=1,4 Гц), 8,36 (с, 1H), 7,79 (дд, 1H, J=9,2, 1,6 Гц), 7,75 (дд, 1H, J=9,2, 0,8 Гц), 7,46 (т, 1H, J=7,8 Гц), 7,23 (д, 1H, J=8,0 Гц), 400,19 7,13-7,07 (м, 1H), 7,01 (д, 1H, J=7,6 Гц), 6,47-6,41 (м, 2H), 6,37 (дт, 1H, J=8,8, 2,4 Гц), 4,49 (с, 2H), 2,49 (с, 3H) (400 MГц, CDCl3): δ 8,95 (дд, 1H, J=1,6, 1,2 Гц), 8,37 (с, 1H), 7,80 (дд, 1H, J=9,2, 1,6 Гц), 7,76 (дд, 1H, J=9,2, 1,2 Гц), 7,46 (т, 1H, J=7,6 Гц), 7,23 (д, 1H, 400,19 J=7,6 Гц), 7,01 (д, 1H, J=7,6 Гц), 6,92-6,88 (м, 2H), 6,65-6,62 (м, 2H), 4,49 (с, 2H), 2,51 (с, 3H) 24 UA 106136 C2 7 8 9 10 11 12 13 14 15 (400 MГц, CDCl3): δ 8,96 (ушир.с, 1H), 8,38 (с, 1H), 7,82 (дд, 1H, J=9,2, 1,6 Гц), 7,78 (дд, 1H, J=9,2, 0,8 Гц), 7,47 (т, 1H, J=7,6 Гц), 7,24 (д, 1H, J=7,6 Гц), 7,02 (дд, 1H, J=7,6, 0,4 Гц), 6,94-6,88 (м, 1H), 6,606,51 (м, 2H), 4,71 (ушир.с, 1H), 4,58 (д, 2H, J=3,6 Гц), 2,51 (с, 3H) (400 MГц, CDCl3): δ 8,94 (т, 1H, J=1,4 Гц), 8,38 (с, 1H), 7,81 (дд, 1H, перекрив., J=9,2, 1,6 Гц), 7,78 (дд, 1H, перекрив., J=9,2, 1,2 Гц), 7,47 (т, 1H, J=7,8 Гц), 7,24 (д, 1H, J=8,0 Гц), 7,03 (д, 1H, J=7,6 Гц), 7,04-6,95 (м, 1H), 6,52 (ддд, 1H, J=12,4, 6,8, 2,8 Гц), 6,42-6,37 (м, 1H), 4,48 (с, 2H), 2,55 (с, 3H) (400 MГц, CDCl3): δ 8,94 (т, 1H, J=1,2 Гц), 8,38 (с, 1H), 7,81 (дд, 1H, перекрив., J=9,2, 1,6 Гц), 7,79 (дд, 1H, перекрив., J=9,2, 1,2 Гц), 7,47 (т, 1H, J=7,8 Гц), 7,24 (д, 1H, J=8,0 Гц), 7,03 (д, 1H, J=7,6 Гц), 6,24-6,19 (м, 3H), 4,71 (ушир.с, 1H), 4,50 (с, 2H), 2,55 (с, 3H) (400 MГц, CDCl3): δ 8,97 (ушир.с, 1H), 8,37 (с, 1H), 7,82 (дд, 1H, J=9,2, 1,6 Гц), 7,77 (дд, 1H, J=9,2, 1,0 Гц), 7,46 (т, 1H, J=7,6 Гц), 7,29 (дд, 1H, J=7,6, 1,6 Гц), 7,23 (ушир.д, 1H, J=7,6 Гц), 7,14 (тд, 1H, J=8,4, 1,6 Гц), 7,01 (дд, 1H, J=7,6, 0,4 Гц), 6,75 (дд, 1H, J=8,8, 1,4 Гц), 6,72 (тд, 1H, J=8,4, 1,6 Гц), 5,01 (ушир.с, 1H), 4,60 (ушир.с, 2H), 2,50 (с, 3H) (400 MГц, ДМСО-d6): δ 9,43 (с, 1H), 8,61 (с, 1H), 7,95 (дд, 1H, J=9,2, 0,8 Гц), 7,82 (т, 1H, перекрив., J=7,8 Гц), 7,81 (дд, 1H, перекрив., J=9,2, 2,0 Гц), 7,49 (д, 1H, J=8,0 Гц), 7,36 (д, 1H, J=7,6 Гц), 7,32 (дд, 1H, J=7,8, 1,4 Гц), 7,17 (тд, 1H, J=8,4, 1,2 Гц), 6,87 (дд, 1H, J=8,4, 1,2 Гц), 6,69 (тд, 1H, J=7,8, 1,4 Гц), 6,15 (ушир.с, 1H), 4,76 (с, 2H), 2,55 (с, 3H) (400 MГц, CDCl3): δ 8,95 (т, 1H, J=1,6 Гц), 8,37 (с, 1H), 7,81 (дд, 1H, J=9,2, 1,6 Гц), 7,77 (дд, 1H, J=9,2, 1,2 Гц), 7,47 (т, 1H, J=7,8 Гц), 7,24 (д, 1H, J=8,0 Гц), 7,10 (т, 1H, J=8,0 Гц), 7,02 (д, 1H, J=7,6 Гц), 6,75 (ддд, 1H, J=8,0, 2,0, 0,8 Гц), 6,69 (т, 1H, J=2,0 Гц), 6,57 (ддд, 1H, J=8,0, 2,4, 0,8 Гц), 4,51 (с, 2H), 2,52 (с, 3H) (400 MГц, ДМСО-d6): δ 9,45 (дд, 1H, J=1,6, 0,8 Гц), 8,63 (с, 1H), 7,97 (дд, 1H, J=9,2, 0,8 Гц), 7,85 (т, 1H, J=8,0 Гц), 7,81 (дд, 1H, J=9,2, 1,6 Гц), 7,56 (д, 1H, J=8,4 Гц), 7,39 (д, 1H, J=7,6 Гц), 7,15 (т, 1H, J=8,0 Гц), 6,80 (т, 1H, J=2,2 Гц), 6,71-6,65 (м, 2H), 4,71 (с, 2H), 2,54 (с, 3H) (400 MГц, CDCl3): δ 8,95 (т, 1H, J=1,4 Гц), 8,38 (с, 1H), 7,81 (дд, 1H, перекрив., J=9,2, 1,4 Гц), 7,78 (дд, 1H, перекрив., J=9,2, 1,2 Гц), 7,47 (т, 1H, J=7,6 Гц), 7,23 (ушир.д, 1H, J=7,6 Гц), 7,16 (м, 2H), 7,02 (ушир.д, 1H, J=7,6 Гц), 6,65 (м, 2H), 4,51 (с, 2H), 2,54 (с, 3H) (400 MГц, CDCl3): δ 11,02 (ушир.с, 1H), 8,97 (с, 1H), 8,36 (с, 1H), 7,81 (дд, 1H, J=9,2, 1,6 Гц), 7,75 (дд, 1H, J=9,2, 0,8 Гц), 7,46 (т, 1H, J=8,0 Гц), 7,24 (д, 1H, J=8,0 Гц), 7,03 (т, 1H, перекрив., J=8,0 Гц), 7,00 (д, 1H, перекрив., J=8,0 Гц), 6,85 (дд, 1H, J=8,0, 1,6 Гц), 6,63 (дд, 1H, J=8,0, 1,6 Гц), 5,15 (т, 1H, J=5,6 Гц), 4,57 (д, 2H, J=5,6 Гц), 2,43 (с, 3H) 25 418,18 418,18 418,18 416,16 416,16 416,16 450,12 UA 106136 C2 16 (400 MГц, CDCl3): δ 8,94 (т, 1H, J=1,2 Гц), 8,37 (с, 1H), 7,80 (дд, 1H, перекрив., J=9,2, 1,6 Гц), 7,77 (дд, 1H, перекрив., J=9,2, 1,2 Гц), 7,47 (т, 1H, J=8,0 450,12 Гц), 7,24 (ушир.д, 1H, J=8,0 Гц), 7,20 (д, 1H, J=8,8 Гц), 7,03 (д, 1H, J=8,0 Гц), 6,77 (д, 1H, J=2,8 Гц), 6,53 (дд, 1H, J=8,8, 2,8 Гц), 4,47 (с, 2H), 2,51 (с, 3H) 17 (400 MГц, CDCl3/CD3OD): δ 8,90 (с, 1H), 8,24 (с, 1H), 7,71 (дд, 1H, J=9,2, 1,6 Гц), 7,64 (дд, 1H, J=9,2, 0,8 Гц), 7,45 (т, 1H, J=7,6 Гц), 7,16 (ушир.д, 1H, 450,12 J=7,6 Гц), 6,99 (д, 1H, J=7,6 Гц), 6,57 (т, 1H, J=1,6 Гц), 6,51 (д, 2H, J=1,6 Гц), 4,36 (с, 2H), 2,45 (с, 3H) 18 19 20 21 22 23 24 (400 MГц, CDCl3): δ 10,94 (ушир.с, 1H), 8,97 (ушир.с, 1H), 8,36 (с, 1H), 7,82 (д, 1H, J=9,2 Гц), 7,75 (д, 1H, J=9,2 Гц), 7,45 (т, 1H, перекрив., J=7,8 Гц), 7,43 (дд, 1H, J=8,0, 1,6 Гц), 7,21 (д, 1H, J=8,0 Гц), 7,16 (тд, 1H, J=8,4, 1,2 Гц), 6,99 (д, 1H, J=7,6 Гц), 6,71 (дд, 1H, J=8,4, 1,2 Гц), 6,63 (тд, 1H, J=8,0, 1,6 Гц), 4,99 (т, 1H, J=5,6 Гц), 4,57 (д, 2H, J=5,6 Гц), 2,44 (с, 3H) (400 MГц, ДМСО-d6): δ 9,43 (дд, 1H, J=1,6, 0,8 Гц), 8,62 (с, 1H), 7,96 (дд, 1H, J=9,2, 0,8 Гц), 7,83 (т, 1H, J=7,6 Гц), 7,80 (дд, 1H, J=9,2, 1,6 Гц), 7,50 (д, 1H, J=7,6 Гц), 7,48 (дд, 1H, J=8,0, 1,6 Гц), 7,37 (д, 1H, J=7,6 Гц), 7,21 (тд, 1H, J=7,6, 1,6 Гц), 6,87 (дд, 1H, J=8,0, 1,2 Гц), 6,63 (тд, 1H, J=7,6, 1,2 Гц), 6,04 (ушир.с 1H), 4,78 (с, 2H), 2,55 (с, 3H) (400 MГц, CDCl3): δ 8,89 (ушир.с, 1H), 8,30 (с, 1H), 7,75 (дд, 1H, J=9,2, 1,6 Гц), 7,69 (д, 1H, J=9,2 Гц), 7,44 (ушир.т, 1H, J=7,6 Гц), 7,12 (ушир.д, 1H, J=7,6 Гц), 7,00 (д, 1H, J=8,0 Гц), 6,97 (т, 1H, перекрив., J=8,0 Гц), 6,82-6,78 (м, 2H), 6,58 (ддд, 1H, J=8,2, 2,4, 0,8 Гц), 4,41 (с, 2H), 2,49 (с, 3H) (400 MГц, ДМСО-d6): δ 9,44 (д, 1H, J=0,8 Гц), 8,61 (с, 1H), 7,95 (дд, 1H, J=9,2, 0,8 Гц), 7,83 (т, 1H, J=7,8 Гц), 7,82 (дд, 1H, J=9,2, 1,6 Гц), 7,50 (д, 1H, J=8,0 Гц), 7,37 (д, 1H, J=7,6 Гц), 7,08 (т, 1H, J=8,0 Гц), 6,94(т, 1H, J=2,0 Гц), 6,79 (ддд, 1H, J=7,6, 2,0, 0,8 Гц), 6,71 (ддд, 1H, J=8,4, 2,0, 0,8 Гц), 4,63 (с, 2H), 2,55 (с, 3H) (400 MГц, CDCl3): δ 8,94 (ушир.с, 1H), 8,38 (с, 1H), 7,82-7,77 (м, 2H), 7,46 (т, 1H, J=7,6 Гц), 7,29 (м, 2H), 7,21 (д, 1H, J=7,6 Гц), 7,02 (д 1H, J=7,6 Гц), 6,61 (м, 2H), 4,51 (с, 2H), 4,44 (ушир.с, 1H), 2,54 (с, 3H) (400 MГц, CDCl3): δ 8,97 (с, 1H), 8,37 (с, 1H), 7,83 (дд, 1H, J=9,2, 1,6 Гц), 7,78 (дд, 1H, J=9,2, 0,8 Гц), 7,46 (т, 1H, J=7,8 Гц), 7,23 (ушир.д, 1H, J=7,6 Гц), 7,14 (т, 1H, перекрив., J=8,0 Гц), 7,12 (д, 1H, перекрив., J=7,6 Гц), 7,01 (д, 1H, J=8,0 Гц), 6,76 (тд, 1H, J=7,6, 0,8 Гц), 6,69 (д, 1H, J=7,6 Гц), 4,61 (с, 2H), 2,54 (с, 3H), 2,26 (с, 3H) (400 MГц, CDCl3): δ 8,96 (дд, 1H, J=1,6, 1,2 Гц), 8,37 (с, 1H), 7,82 (дд, 1H, J=9,2, 1,6 Гц), 7,78 (дд, 1H, J=9,2, 1,2 Гц), 7,46 (т, 1H, J=7,8 Гц), 7,22 (ушир.д, 1H, J=8,0 Гц), 7,11 (т 1H, J=7,8 Гц), 7,01 (д, 1H, J=7,6 Гц), 6,63 (дт, 1H, J=7,6, 0,8 Гц), 6,57-6,53 (м, 2H), 4,55 (с, 2H), 2,54 (с, 3H), 2,29 (с, 3H) 26 460,11 460,11 460,11 396,21 396,21 UA 106136 C2 25 26 27 28 29 30 31 32 (400 MГц, ДМСО-d6): δ 9,45 (дд, 1H, J=1,6, 0,8 Гц), 8,63 (с, 1H), 7,97 (дд, 1H, J=9,2, 0,8 Гц), 7,83 (т, 1H, J=8,0 Гц), 7,81 (дд, 1H, J=9,2, 1,6 Гц), 7,56 (д, 1H, J=8,0 Гц), 7,37 (д, 1H, J=8,0 Гц), 7,02 (т, 1H, J=7,8 Гц), 6,60 (с, 1H), 6,54 (дд, 1H, J=8,0, 2,0 Гц), 6,49 (д, 1H, J=7,6 Гц), 4,69 (с, 2H), 2,52 (с, 3H), 2,21 (с, 3H) (400 MГц, CDCl3): δ 8,96 (т, 1H, J=1,2 Гц), 8,37 (с, 1H), 7,82 (дд, 1H, J=9,2, 1,6 Гц), 7,77 (дд, 1H, J=9,2, 0,8 Гц), 7,45 (т, 1H, J=7,8 Гц), 7,22 (ушир.д, 1H, 396,21 J=8,0 Гц), 7,03 (м, 2H), 7,02 (д, 1H, перекрив., J=7,6 Гц), 6,65 (м, 2H), 4,53 (с, 2H), 2,53 (с, 3H), 2,25 (с, 3H) (400 MГц, CDCl3): δ 8,97 (с, 1H), 8,37 (с, 1H), 7,83 (дд, 1H, J=9,2, 1,6 Гц), 7,78 (дд, 1H, J=9,2, 0,8 Гц), 7,45 (т, 1H, J=7,8 Гц), 7,22 (ушир.д, 1H, J=7,6 Гц), 7,03 (т, 1H, перекрив., J=7,8 Гц), 7,02 (д, 1H, 410,23 перекрив., J=8,0 Гц), 6,69 (д, 1H, J=7,6 Гц), 6,58 (д, 1H, J=8,0 Гц), 4,59 (с, 2H), 2,54 (с, 3H), 2,31 (с, 3H), 2,17 (с, 3H) (400 MГц, CDCl3): δ 8,96 (д, 1H, J=1,2 Гц), 8,37 (с, 1H), 7,82 (дд, 1H, J=9,2, 1,6 Гц), 7,77 (дд, 1H, J=9,2, 0,8 Гц), 7,45 (т, 1H, J=7,6 Гц), 7,22 (ушир.д, 1H, J=8,0 Гц), 7,00 (д, 1H, J=7,6 Гц), 6,98 (д, 1H, J=8,0 410,23 Гц), 6,57 (д, 1H, J=2,4 Гц), 6,50 (дд, 1H, J=8,0, 2,4 Гц), 4,53 (с, 2H), 2,54 (с, 3H), 2,20 (с, 3H), 2,16 (с, 3H) (400 MГц, CDCl3): δ 8,95 (дд, 1H, J=1,6, 1,2 Гц), 8,36 (с, 1H), 7,79 (дд, 1H, J=9,2, 1,6 Гц), 7,74 (дд, 1H, J=9,2, 1,2 Гц), 7,45 (т, 1H, J=7,8 Гц), 7,22 (д, 1H, 410,23 J=8,0 Гц), 6,99 (д, 1H, J=7,6 Гц), 6,44 (ушир.с, 1H), 6,31 (с, 2H), 4,49 (с, 2H), 2,48 (с, 3H), 2,21 (с, 6H) (400 MГц, CDCl3): δ 8,97 (ушир.с, 1H), 8,37 (с, 1H), 7,83 (дд, 1H, J=9,2, 1,6 Гц), 7,78 (дд, 1H, J=9,2, 0,8 Гц), 7,46 (т, 1H, J=7,8 Гц), 7,23 (ушир.д, 1H, J=7,6 Гц), 7,16-7,11 (м, 2H), 7,01 (д, 1H, J=7,6 Гц), 6,80 410,23 (тд, 1H, J=7,6, 1,2 Гц), 6,71 (дд, 1H, J=8,4, 1,2 Гц), 4,60 (с, 2H), 2,60 (кв, 2H, J=7,6 Гц), 2,52 (с, 3H), 1,32 (т, 3H, J=7,6 Гц) (400 MГц, CDCl3): δ 8,96 (д, 1H, J=1,2 Гц), 8,37 (с, 1H), 7,82 (дд, 1H, J=9,2, 1,6 Гц), 7,77 (дд, 1H, J=9,2, 1,2 Гц), 7,45 (т, 1H, J=7,8 Гц), 7,22 (ушир.д, 1H, J=8,0 Гц), 7,14 (т, 1H, J=7,8 Гц), 7,01 (д, 1H, J=7,6 410,23 Гц), 6,66 (дд, 1H, J=7,6, 0,8 Гц), 6,58 (д, 1H, J=2,0 Гц), 6,55 (дд, 1H, J=7,6, 2,0 Гц), 4,55 (с, 2H), 2,58 (кв, 2H, J=7,6 Гц), 2,53 (с, 3H), 1,21 (т, 3H, J=7,6 Гц) (400 MГц, ДМСО-d6): δ 9,45 (дд, 1H, J=1,6, 0,8 Гц), 8,63 (с, 1H), 7,97 (дд, 1H, J=9,2, 0,8 Гц), 7,83 (т, 1H, J=8,0 Гц), 7,81 (дд, 1H, J=9,2, 1,6 Гц), 7,57 (д, 1H, J=8,0 Гц), 7,37 (д, 1H, J=8,0 Гц), 7,05 (т, 1H, J=7,6 Гц), 6,64 (д, 1H, J=1,6 Гц), 6,57-6,52 (м, 2H), 4,71 (с, 2H), 2,53 (с, 3H), 2,50 (кв, 2H, J=7,6 Гц), 1,14 (т, 3H, J=7,6 Гц) 27 UA 106136 C2 33 34 35 36 37 38 39 (400 MГц, CDCl3) δ 8,97 (ушир.с, 1H), 8,37 (с, 1H), 7,82 (дд, 1H, J=9,2, 1,6 Гц), 7,76 (дд, 1H, J=9,2, 0,8 Гц), 7,45 (т, 1H, J=7,8 Гц), 7,23 (ушир.д, 1H, перекрив., J=8,0 Гц), 7,21 (дд, 1H, перекрив., J=7,6, 1,6 Гц), 7,12 (тд, 1H, J=7,6, 1,6 Гц), 7,00 (д, 1H, J=7,6 Гц), 6,83 (тд, 1H, J=7,6, 1,2 Гц), 6,71 (дд, 1H, J=8,0, 1,2 Гц), 4,58 (с, 2H), 3,00 (гептет, 1H, J=6,8 Гц), 2,50 (с, 3H), 1,31 (д, 6H, J=6,8 Гц) (400 MГц, CDCl3): δ 8,96 (дд, 1H, J=1,4, 0,8 Гц), 8,35 (с, 1H), 7,79 (дд, 1H, J=9,2, 1,4 Гц), 7,73 (дд, 1H, J=9,2, 0,8 Гц), 7,44 (т, 1H, J=7,8 Гц), 7,21 (д, 1H, J=7,6 Гц), 7,11 (т, 1H, J=7,8 Гц), 6,99 (дд, 1H, J=7,8, 0,4 Гц), 6,67 (д, 1H, J=7,6 Гц), 6,57 (т, 1H, J=2,4 Гц), 6,50 (ддд, 1H, J=8,0, 2,4, 0,8 Гц), 4,51 (с, 2H), 2,80 (гептет, 1H, J=6,8 Гц), 2,47 (с, 3H), 1,20 (д, 6H, J=6,8 Гц) (400 MГц, CDCl3): δ 8,96 (т, 1H, J=1,2 Гц), 8,36 (с, 1H), 7,81 (дд, 1H, J=9,2, 1,6 Гц), 7,75 (д, 1H, J=9,2 Гц), 7,44 (т, 1H, J=7,8 Гц), 7,21 (д, 1H, J=8,0 Гц), 7,06 (м, 2H), 6,99 (д 1H, J=7,6 Гц), 6,64 (м, 2H), 4,50 (с, 2H), 2,80 (гептет, 1H, J=6,8 Гц), 2,48 (с, 3H), 1,19 (д, 6H, J=6,8 Гц) (400 MГц, CDCl3): δ 8,96 (ушир.с, 1H), 8,35 (с, 1H), 7,80 (дд, 1H, J=9,2, 1,6 Гц), 7,73 (дд, 1H, J=9,2, 0,8 Гц), 7,44 (т, 1H, J=7,8 Гц), 7,28 (дд, 1H, J=7,6, 1,2 Гц), 7,22 (ушир.д, 1H, J=8,0 Гц), 7,15 (тд, 1H, J=7,8, 1,2 Гц), 6,99 (д, 1H, J=7,6 Гц), 6,79 (дд, 1H, перекрив., J=17,2, 11,2 Гц), 6,78 (тд, 1H, перекрив., J=7,6, 0,8 Гц), 6,68 (дд, 1H, J=8,2, 1,0 Гц), 5,62 (дд, 1H, J=17,2, 1,4 Гц), 5,34 (дд, 1H, J=11,2, 1,4 Гц), 4,53 (с, 2H), 2,45 (с, 3H) (400 MГц, CDCl3): δ 10,59 (ушир.с, 1H), 8,94 (с, 1H), 8,37 (с, 1H), 7,81 (д, 1H, J=9,2 Гц), 7,77 (д, 1H, J=9,2 Гц), 7,45 (т, 1H, J=7,8 Гц), 7,20 (ушир.д, 1H, перекрив., J=7,6 Гц), 7,15 (т, 1H, перекрив., J=7,8 Гц), 7,00 (д, 1H, J=8,0 Гц), 6,86 (д, 1H, J=7,6 Гц), 6,75 (т, 1H, J=2,0 Гц), 6,63 (дд, 1H, перекрив., J=17,6, 10,8 Гц), 6,61 (дд, 1H, перекрив., J=8,0, 2,0 Гц), 5,69 (дд, 1H, J=17,6, 0,8 Гц), 5,21 (дд, 1H, J=10,8, 0,8 Гц), 4,55 (с, 2H), 4,39 (ушир.с, 1H), 2,51 (с, 3H) (400 MГц, ДМСО-d6): δ 9,49 (дд, 1H, J=1,6, 0,8 Гц), 8,65 (с, 1H), 7,97 (дд, 1H, J=9,2, 0,8 Гц), 7,86 (дд, 1H, перекрив., J=9,2, 1,6 Гц), 7,85 (т, 1H, перекрив., J=7,8 Гц), 7,65 (д, 1H, J=8,0 Гц), 7,38 (д, 1H, J=7,6 Гц), 7,12 (т, 1H, J=7,8 Гц), 6,91 (т, 1H, J=1,6 Гц), 6,79 (д, 1H, J=7,6 Гц), 6,71 (дд, 1H, J=8,0, 1,6 Гц), 6,64 (дд, 1H, J=17,6, 11,2 Гц), 5,80 (дд, 1H, J=17,6, 0,8 Гц), 5,20 (дд, 1H, J=11,2, 0,8 Гц), 4,79 (с, 2H), 2,51 (с, 3H) (400 MГц, ДМСО-d6): δ 9,40 (дд, 1H, J=1,6, 0,8 Гц), 8,63 (с, 1H), 7,98 (дд, 1H, J=9,2, 0,8 Гц), 7,84 (т, 1H, J=8,0 Гц), 7,76 (дд, 1H, J=9,2, 1,6 Гц), 7,43 (d, 1H, J=7,6 Гц), 7,40 (д, 1H, J=8,0 Гц), 7,13 (т, 1H, J=7,8 Гц), 6,80 (ушир.с, 1H), 6,79 (д, 1H, перекрив., J=7,6 Гц), 6,64 (дд, 1H, перекрив., J=17,6, 11,2 Гц), 6,63 (дд, 1H, перекрив., J=7,6, 2,0 Гц), 5,74 (дд, 1H, J=17,6, 0,8 Гц), 5,21 (дд, 1H, J=11,2, 0,8 Гц), 4,68 (с, 2H), 2,58 (с, 3H) 28 424,24 424,24 424,24 408,21 408,21
ДивитисяДодаткова інформація
Назва патенту англійською2-pyridyl substituted imidazoles as therapeutic alk5 and/or alk4 inhibitors
Автори англійськоюKim, Dae Kee, Sheen, Yhun Yhong, Jin, Cheng Hua, Park, Chul-Yong, Sreenu, Domalapally, Rao, Kota Sudhakar, Krishnaiah, Maddeboina, Subrahmanyam, Vura Bala
Автори російськоюКим Дае Кее, Шеен Ихун Ихонг, Дзин Ченг Хуа, Парк Чул-Ионг, Среену Домалапалли, Рао Кота Судхакар, Кришнаях Маддебойна, Субрахманям Вура Бала
МПК / Мітки
МПК: A61P 13/12, A61K 31/437, A61P 11/00, C07D 471/04, C07D 413/14, A61P 19/10, C07D 401/14, A61P 25/28
Мітки: 2-піридилзаміщені, інгібітори, терапевтичні, імідазоли
Код посилання
<a href="https://ua.patents.su/85-106136-2-piridilzamishheni-imidazoli-yak-terapevtichni-ingibitori-alk5-i-abo-alk4.html" target="_blank" rel="follow" title="База патентів України">2-піридилзаміщені імідазоли як терапевтичні інгібітори alk5 і/або alk4</a>
Попередній патент: Спосіб одержання сипкого комплексного бактеріального препарату для рослинництва
Наступний патент: Різально-метальний робочий орган
Випадковий патент: Паливна суміш для двигунів внутрішнього згоряння