Спосіб одержання акрилових ефірів гліколів
Номер патенту: 32883
Опубліковано: 15.02.2001
Автори: Оглашенний Юрій Іванович, Семенюк Ігор Васильович, Маршалок Галина Олексіївна, Ятчишин Йосип Йосипович
Текст
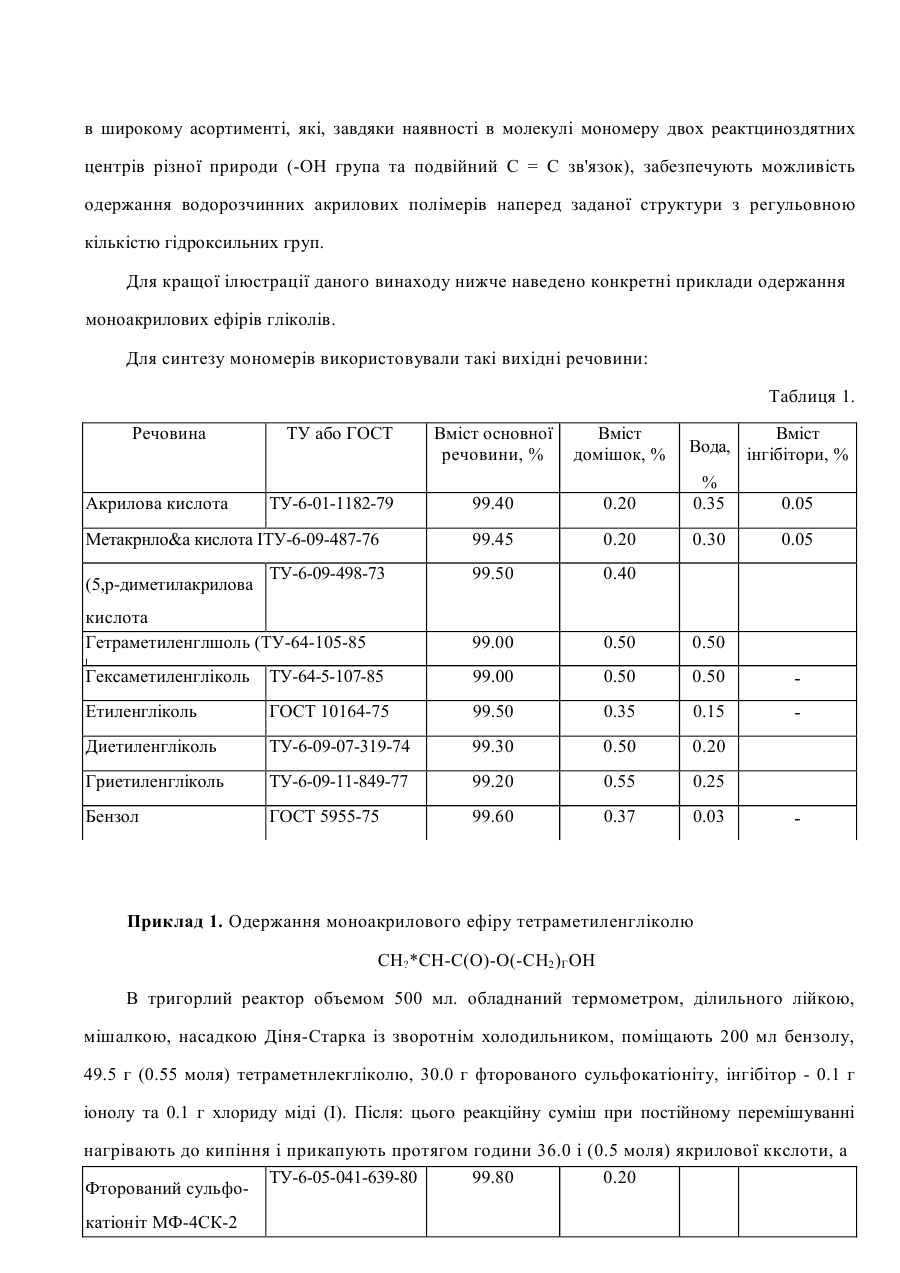
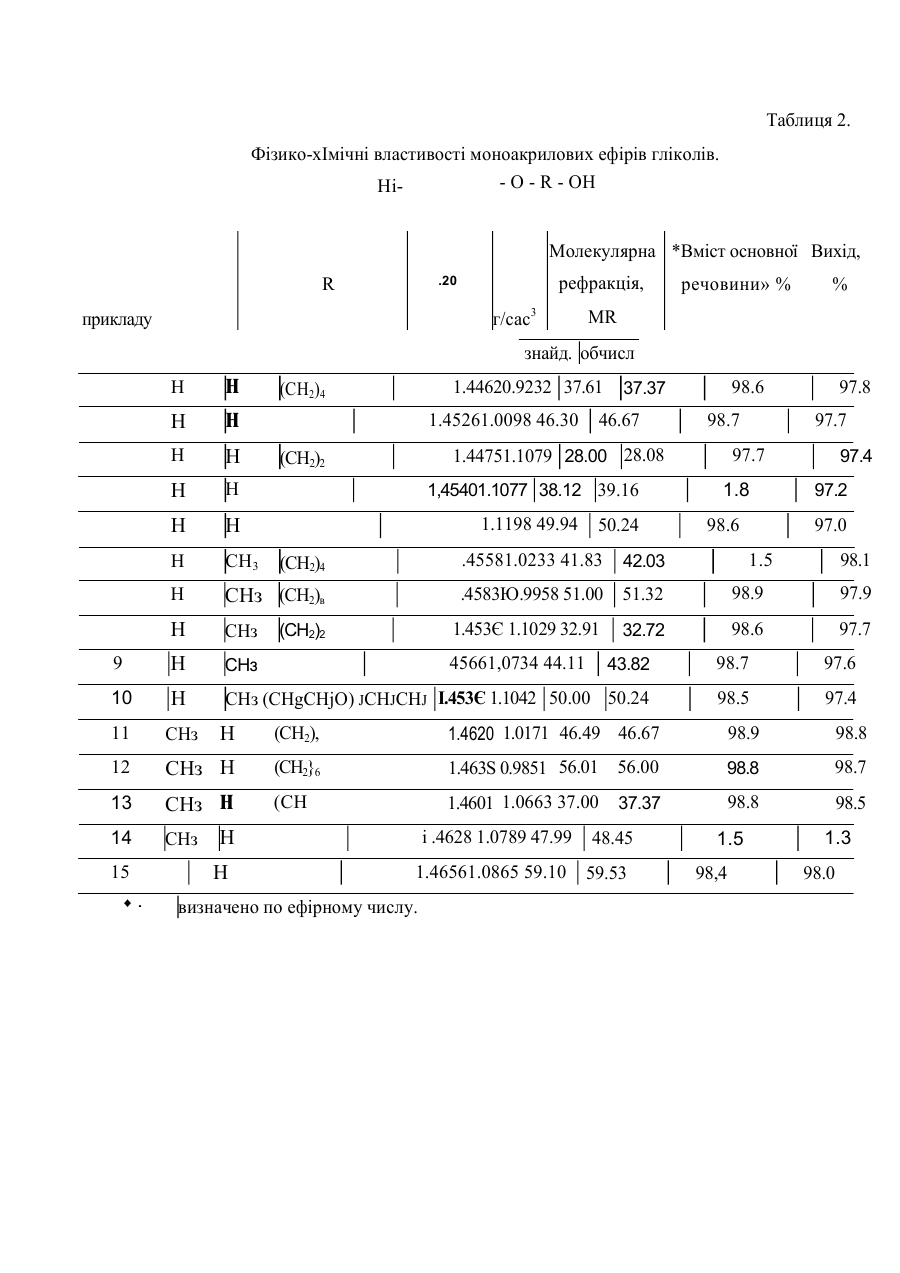
C МПК« С 07 С СПОСІБ ОДЕРЖАННЯ АКРИЛОВИХ ЕФІРІВ ГЛІКОЛІВ Винахід відкоситься до хімії мономерів, зокрема до одержання акрилових ефірів гліколів, які € поліфункцджяльними акриловими мономерами. Ці мономери можуть бути використані для одержання водорозчинних гідроксилвшених акрилових полімерів у вигляді водних дисперсій, що, в свою чергу, дозволить одержувати полімерні покриття та плівки тривимірної структури з високою міцністю, адгезією, еластичністю, світло- водо- та атмосферостійкісію І застосовувати їх для нанесення на різноманітні матеріали, зокрема на натуральну І штучну шкіру, дереко, метал. Відомий спосіб одержання акр^гловттх ефтрів шляхом етерифікації спиртів КИСЛОТАМИ З азеотропною відгонкою реакційної вода в присутності гомогенного кислотного каталізатора H2SO4l HC1 (Пат США № 4187383, С 07 С 69/54, С 07 С 69/06, опубл. 5.02.1980. Пяі СРР №79862, С 07 С 69/54, опубл. 30.09.1982). Однак, внаслідок протікання побічних реакцій сульфування, пдрохлорування та гідратації по подвійному зв'язку в присутності вказаних каталізаторів, спосіб не дозволяє одержувати чисті цільові продукіи з високим виходом. Відомий спосіб одержання акрилових ефірів гліколів шляхом етерифікації спиртів кислотами з азеотропною відгонкою реакційної води в присутності гетерогенного кислотного каталізатора - сульфокатіонітів КУ-1. КУ-2. КУ-2/8 (А.с. № 1206271, СРСР, С 07 С 67/08; опубл. в Бюл. 1986, № 3). Однак, через низьку механічну стійкість цих каталізаторів, їх здатність до набухання І часткову розчинність в реакційній суміші, спосіб не дозволяє одержати високочисті мономери з високим виходом внаслідок забруднення продуктів розчинними компонентами сульфокатіоніту. Найбільш близьким за технічною суітю до пропонованого винаходу є спосіб одержання акрилових ефірів гліколів (А.с. № 1097607. СРСР, С 07 С 69/54. С 07 С 67/08. опубл. 15.06.1984, Бюл. 1984, № 22) шляхом етерифікації гліколів ненасиченою кислотою в середовищі язеотроіїоутвоиюючої о розчинники в присутності гетерогенної о кя гал штора та їнгібітора з азеотропною відгонкою реакційної води. Але цей спосіб двостадійний - з виходом 60-70% на першій і 95-97% на другій стадії. Крім того, сульфоадтіоніший каталізатор неможливо багаторазово використоиувати: без регенерації і, внаслідок його низької термічної стійкості і невисокої каталітичної активності неможливо одержувати з високим виходом чисті цільові продукти В основу винаходу поставлено задачу вдосконалити спосіб одержання акрилових ефірів гліколів, в якому за рахунок використання нового каталізатора досягалася б практична можливість спростити процес і одержувати в одну стадію з високим виходом (>97%) широкий асоріименч виоокочистих моноакрилових ефірів гліколш. Поставлена задача вирішується тим, шо в способі одержання акрилових ефірів гліколів шляхом етерифікації гліколів ненасиченою кислотою в середовищі органічного розчинника в присутності гетерогенного каталізатора та їнгібітора з азеотропною відгонкою реакційної води, згідно з винаходом, як ненасичену кислілу викориепщуюіь або акрилову, або метакрилову, або р,р-диметилакрилову, а як гетерогенний каталізатор фторований сульфокяаонїі загальної формули' І - CF2 - CF2 - CF - CF2 -]n О CF2 - CF2 - О - CF2 - CF2 - SO3H, де п відповідає середній молекулярній масі 70000 Використання такого фторованого сульфокатіоніту як каталізатора для етерифікації вказаних -кекасичеяих кислот дозволяє з високим виходом в одну стадію одержувати моноакрилові ефіри гліколіз загальної формули: Rt-C-C-C-0-R-OH Rt (CH 2 ln - , - (СНЭ - СНо - О)т - СН« - СН2 п=4 або 6; т= 0. І або 2; 2) R t - Н, R 2 3) Ri = СНз, R 2 « Н; t Ко О де R= в широкому асортименті, які, завдяки наявності в молекулі мономеру двох реактциноздятних центрів різної природи (-ОН група та подвійний С = С зв'язок), забезпечують можливість одержання водорозчинних акрилових полімерів наперед заданої структури з регульовною кількістю гідроксильних груп. Для кращої ілюстрації даного винаходу нижче наведено конкретні приклади одержання моноакрилових ефірів гліколів. Для синтезу мономерів використовували такі вихідні речовини: Таблиця 1. Речовина Акрилова кислота ТУ або ГОСТ ТУ-6-09-498-73 кислота Гетраметиленглшоль (ТУ-64-105-85 І Вміст домішок, % Вміст Вода, інгібітори, % 99.40 0.20 % 0.35 99.45 0.20 0.30 99.50 0.40 99.00 ТУ-6-01-1182-79 Метакрнло&а кислота ІТУ-6-09-487-76 (5,р-диметилакрилова Вміст основної речовини, % 0.50 0.50 0.05 0.05 Гексаметиленгліколь ТУ-64-5-107-85 99.00 0.50 0.50 Етиленгліколь ГОСТ 10164-75 99.50 0.35 0.15 Диетиленгліколь ТУ-6-09-07-319-74 99.30 0.50 0.20 Гриетиленгліколь ТУ-6-09-11-849-77 99.20 0.55 0.25 Бензол ГОСТ 5955-75 99.60 0.37 0.03 Приклад 1. Одержання моноакрилового ефіру тетраметиленгліколю СН?*СН-С(О)-О(-СН2 )ГОН В тригорлий реактор объемом 500 мл. обладнаний термометром, ділильного лійкою, мішалкою, насадкою Діня-Старка із зворотнім холодильником, поміщають 200 мл бензолу, 49.5 г (0.55 моля) тетраметнлекгліколю, 30.0 г фторованого сульфокатіоніту, інгібітор - 0.1 г іонолу та 0.1 г хлориду міді (І). Після: цього реакційну суміш при постійному перемішуванні нагрівають до кипіння і прикапують протягом години 36.0 і (0.5 моля) якрилової ккслоти, а ТУ-6-05-041-639-80 99.80 0.20 Фторований сульфокатіоніт МФ-4СК-2 далі витримують в такому ж режимі до припинення виділення води в насадці Діна-Старкя П ІСЛЯ охолодженим реакційної суміші ди кімнгііної іемператури її промиваюча 50 мл 20%ного розчияу хлориду натрію, нейтралізують 50 мл 20%-ного розчину гідрокарбонату натрію І знову 50 мл 20%-пого розчину хлориду натрію Відгонку розчншіика проводить при 60-65 °С у вакуумі водосіруминкого каеогу, а ефіру - при 1-2 мм рі от. Одержують 70 4 г моноакрилового ефіру тетраметиленгліколю з виходом 97 8%, його фізико-хімічш властивості наведені в табл. 2, Приклад 2 Одержання \*о*ш&крилони>о ефіру гекеамеінленглііш..'ю СНЙ=СН-С(О)-О(-СН2)6-ОН. проводять в умовах, ідентичних прикладу і, при наступному співвідношенні реагентів Бензол - 200 мл; Гексаметиленгліколь - 64 9 г (0 55 моля): Акрилова кислота - 36,0 г (0,5 моля). Сульфокатіоиіт МФ-4СК-2 - 30.0 г. Іонол - 0,1 г, Хлорид міді (І) • 0 і г Одержують 83.9 г моноаіфіглового ефіру гексаметиленгліколю з виходом 97 7% Іїрш^іад 3 Одержання моноакрісловиго ефіру етиленгліколю СН2 =СН-С(ОЮ-СгІ2-СН2-ОН проводять в умовах, ідентичних прикладу І, при наступному співвідношенні реагентівБензол - 200 мл> Етиленгліколь - 34 1 г (0 55 МОЛЙІ: Акрилова кислота - 36.0 г (0.5 моля)» Сульфилягіоніт МФ4СК-2 30 0 г; їочол - 0 1г; Хлоріід міді (І) -0 1 г Одержують 56,5 г мокоакршювого ефіру етиленгліколю з виходом 97 4%, Приклад 4 Одержання моноакрилавого ефіру диетиленгліколю СН2=СН-С(О)-О(-СН2-СгІ2-ОЬ-ОН проводять в умовах, їдентичнкх прикладу 1, при наступному співвідношенні реагентів 4 Бензол - 200 мл; Диетиленгліколь - 58.3 г (0.55 моля); Акрилова кислота - 36.0 г (0 5 моля]; Сульфокатіоніт МФ-4СК-2 - 30.0 г; Іонол - 0.1 г; Хлорид міді (I) -0 1 г. Одержують 77.8 г моноакрилового ефіру диетиленгліколю з виходом 97.2%. Приклад 5. Одержання мопоакрилового ефіру триетиленгліколю СН2=СН-С(О)-О(-СН2-СН2-О)3-Н проводять в умовах, ідентичних прикладу 1, при нас.іупному співвідношенні реагентів Бензол - 200 мл; Триетиленгліколь - 82.5 г (0.55 моля); Акрилова кислота - 36.0 г (0.5 моля); Сульфокатпжіт МФ-4СК-2 - 30.0 гг Іонол - 0.1г, Хлорид міді (І) -0.1 г. Одержують 98.9 г моноакрилового ефіру триетиленгліколю з виходом 97.0%. Приклад 6 Одержання мономет акрилового ефіру тетраметиленгліколю СН2=С(СНз)-С(О)-О(-СН2)4-ОН проводять в умовах, ідентичних прикладу 1, при наступному співвідношенні реагентів: Бензол - 200 мл, Тетраметиленгліколь -49.5 г (0.55 моля); Метакрилова кислої а - 43.0 і (0.5 моля); Сулырокатюшт МФ-4СК-2 - ЗО 0 г; Іонол - 0,1г, Хлорид міді (І) -0.1 г. Одержують 77,5 г мономегакрнлового ефіру теграметилеишколю з виходом 98.1 о/ /о Приклад 7. Одержання монометакрилового ефіру гексаметиленгліколю СН2*=С(СН3)-С(О)-О(-СН2)6-ОН проводять в умовах, ідентичних прикладу 1, при наступному співвідношенні реагентів. Бензол - 200 мл; Гексаметшгенгліколь - 64.9 г (0.55 моля); 5 Метакрилова кислота - 43.0 г (0.5 моля); Сульфокатіоьгіт МФ-4СК-2 - 30.0 г; Іонол - О Л г; Хлорид міді (І) -0.1 г. Одержують 90.9 г монометакрилового ефіру гексаметиленгліколю з виходом 97.9%. Приклад 8. Одержання монометакрилового ефіру етиленгліколю СН2~С(СН3)-С(О)-О(-СН2)2-ОН проводять в умовах, ідентичних прикладу 1, при наступному співвідношенні реагентів: Бензол - 200 мл; Етиленгліколь - 34.1 г (0.55 моля); Метакрилова кислота - 43.0 г (0,5 моля); Сульфокатіокіт МФ-4СК-2 - 30.0 г; Іонол - 0.1г; Хлорид міді (І) -0.1 г. Одержують 63.5 г монометакрилового ефіру етиленгліколю з виходом 97.7%. Приклад 9. Одержячня монометакрилового ефіру диетиленгліколю проводять в умовах, Ідентичних прикладу і, при наступному співвідношенні реагентівБензол - 200 мл. Диетиленгліколь - 58.3 г (0.55 моля); Метакрилова кислота - 43.0 г (0.5 моля); Сульфокатіоніт МФ-4СК-2 - 30.0 г; Іонол - 0.1г, Хлорид міді (1) -0.1 г. Одержують 84.9 г монометакрилового ефіру диетиленгліколю з виходом 97.6%. Приклад 10. Одержання мономегакрилового ефіру гри«тиленгліколю проводять в умовах, ідентичних прикладу 1, при наступному співвідношенні реагентів* Бензол - 200 мл; Триетиленгліколь - 82.5 г (0.55 моля); Метакрилова кислота - 43.0 г (0.5 моля); Сульфокятіоніт МФ-4СК-2 - 300 г; Іонол - 0.1г; Хлорид міді (П -0.1 г. Одержують І06,) г монометагфилового ефіру тркетшгенглїколю з виходом 97 4%, Приклад Ц. Одержаний моноф,(3-д#мег;ідакрїш>8ого ефіру тетрамеіиленглїкш.ю СН3-С(СН^)=С(О)-О(-СН2.)4-ОН проводять в умовах, ідентичних прикладу І, при наступному співвідношенні реагентів: Бензол - 200 мл; Тетраметилекгліколь - 49 5 г (0.55 моля); І3,р-Дііметїілакріілова кислота - 50,0 г (0.5 молн); Сульфокагіояїт МФ-4СК-2 - 30.0 г, Іонол - 0,1г; Хлорид міді (І) -0.І г Одержують 84 9 г мочо-рі|Н-днм*1тнлак.рнлового ефіру тетраметяленглїколт з виходом 98.8% Приклад 12. Одержання моноф.р-дкметилакрилового ефїр\ гексаметилекгліколю СЦг-С(СНз)=С(О)-О(-СН2)н-ОН проводять в умовах, ідентичних прикладу 1, при наступному співвідношенні реагентів: Бензол - 200 мл, Гексаметиленгдіколь 64.9 г (0.55 моляї; |ї,р-Дішешлшфшгова кислота - 50,0 г (0,5 моля), Сульфоьагіоніт МФ-4СЮ2 • 30.0 г, Іонол - 0,1г; Хлорид міді (ї) '0.1 г. Одержують 98 7 г моно-р.р-^щметїтлякридпвого ефіру гексамстилешліколк> з виходпм 98.7%, Приклад 13. Одержання моно-р,р-диметилаи.рилового ефіру етиленгліколю СН5-С(СНз)=С(О)-О-СН2-СНй-ОН проводять в умовах, ідентичних прикладу 1, при наступному илівзідношсйш pt-ягентш. Бензол - 200 мл; Етиленгліколь - 34.1 г (0.55 МОЛИ): (5$-Диметилакрнлов£ кислота - 50,0 г (0 5 моля); Сульфокдтіоніт МФ-4СК-2 - 30.0 г. Іонол - 0,1г; Хлорид міді (І) -0.1 г. 7 Одержують 70.9 г моно-р-р-диметилакріглового ефіру етиленгліколю з виходом 96.5% Приклад 14. Одержання моно-р,р-диметнлакрклового ефіру диетиленгліколю СН3-С(СН3)=С(О)-О(-СНгСНп-0)о-Н проводять в умовах, ідентичних прикладу 1, при наступному співвідношенні реагентів: Бензол - 200 мл, Диетиленгліколь - 58.3 г (0.55 моля); р,р-Диметил акри лова кислота - 50.0 г (0.5 моля); Сульфокатіоніт МФ-4СК-2 - 30.0 г; Іонол - 0.1г; Хлорид міді (І) -0.1 г. Одержують 92.4 г моно-р,р-дігметшгакршювого ефіру диетиленгліколю з виходом 98.3%. Приклад 15. Одержання моно-р,р-диметилакрилового ефіру триетиленгліколю СНГС(СН3)=С(О)-О(-СНГСН2-О)3-Н проводять в умовах, Ідентичних прикладу І, при наступному співвідношенні реагентів. Бензол - 200 мл; Триетиленглїколь - 82.5 г (0.55 МОЛИ); р,р-Диметилакрилова кислота - 50.0 г (0.5 моля); Сульфокатіоніт МФ-4СК-2 - 30.0 г; Іонол - 0.1г; Хлорид міді 0) -0.1 г. Одержують 113.7 г моно-р,р-диметилакрилового ефіру триетиленгліколю з виходом 98.0%. 8 Таблиця 2. Фізико-хІмічні властивості моноакрилових ефірів гліколів. - О - R - ОН НіМолекулярна *Вміст основної Вихід, рефракція, .20 R г/сас3 прикладу речовини» % % MR знайд. обчисл Н н н Н Н Н Н 1,45401.1077 38.12 39.16 Н Н 1.1198 49.94 50.24 Н СН3 Н СНз (СН2)в Н СНз 9 Н СНз 43.82 98.7 97.6 10 Н СНз (CHgCHjO) JCHJCHJ І.453Є 1.1042 50.00 50.24 98.5 97.4 11 СНз Н (СН2), 1.4620 1.0171 46.49 46.67 98.9 98.8 12 СНз Н (СН2}6 1.463S 0.9851 56.01 56.00 98.8 98.7 13 СНз н (СН 1.4601 1.0663 37.00 37.37 98.8 98.5 14 СНз Н Н 15 ♦ . Н 1.44620.9232 37.61 (СН2)4 1.45261.0098 46.30 98.6 37.37 46.67 98.7 .45581.0233 41.83 (СН2)4 1.8 1.453Є 1.1029 32.91 45661,0734 44.11 і .4628 1.0789 47.99 визначено по ефірному числу. 98.1 98.9 97.9 98.6 32.72 1.46561.0865 59.10 59.53 97.2 1.5 42.03 48.45 97.4 97.0 98.6 .4583Ю.9958 51.00 51.32 (СН2)2 97.7 97.7 1.44751.1079 28.00 28.08 (СН2)2 97.8 97.7 1.5 98,4 1.3 98.0
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for preparation of acrylic glycol ethers
Автори англійськоюSemeniuk Ihor Vasyliovych, Marshalok Halyna Olelsiivna, Ohlashennyi Yurii Ivanovych, Yatchyshyn Yosyp Yosypovych
Назва патенту російськоюСпособ получения акриловых эфиров гликолей
Автори російськоюСеменюк Игорь Васильевич, Маршалок Галина Алексеевна, Оглашенный Юрий Иванович, Ятчишин Иосиф Иосифович
МПК / Мітки
МПК: C07C 67/08, B01J 31/06, C07C 69/54
Мітки: ефірів, акрилових, гліколів, одержання, спосіб
Код посилання
<a href="https://ua.patents.su/9-32883-sposib-oderzhannya-akrilovikh-efiriv-glikoliv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання акрилових ефірів гліколів</a>
Попередній патент: Термоелектричний датчик температури
Наступний патент: Спосіб передачі сповіщень в комплексній інтегрованій системі централізованної охорони “дунай”
Випадковий патент: Протез міжхребцевого диска