Спосіб одержання похідних 8-метокси-3-хінолонкарбонової кислоти
Номер патенту: 56286
Опубліковано: 15.05.2003
Автори: Герінг Райнхольд, Хайльманн Вернер, Діль Херберт, Морс Клаус
Формула / Реферат
1. Спосіб одержання похідних 8-метокси-3-хінолонкарбонової кислоти загальної формули (І):
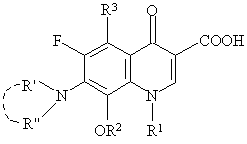 , (І)
, (І)
в якій
R' і R" разом з атомом азоту, із яким вони зв'язані, утворюють моно- або біциклічний гетероцикл, який може бути заміщеним у всіх положеннях кільця і може містити інші гетероатоми азоту, кисню або сірки,
R1 - алкіл з 1-3 атомами вуглецю, фторетил, циклопропіл, незаміщений або заміщений від одного до трьох разів галогенами феніл і циклопропіл,
R2 - метил,
R3 - водень, галоген, аміно, метил,
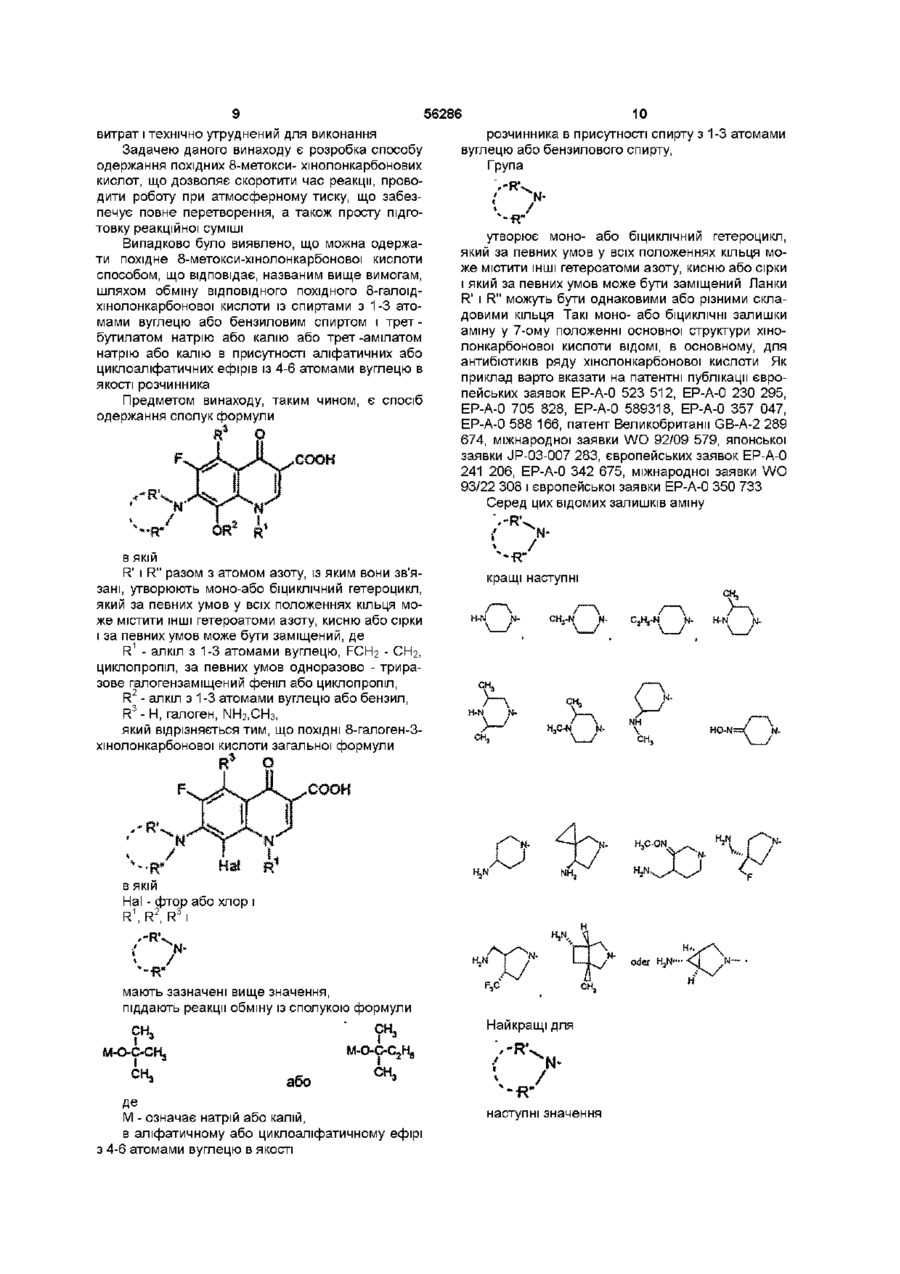
який відрізняється тим, що похідні 8-галоген-3-хінолонкарбонової кислоти загальної формули (II):
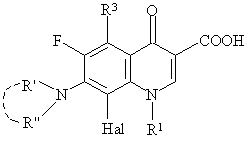 , (ІІ)
, (ІІ)
в якій Hal - фтор або хлор, і
R1, R3 і 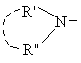 мають наведені вище значення,
мають наведені вище значення,
вводять у взаємодію з метанолом в середовищі розчинника, аліфатичного або циклоаліфатичного етеру з 4-6 атомами вуглецю, і в присутності алкоголяту формули (III):
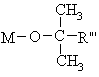 , (ІІІ)
, (ІІІ)
де
R'" означає метил або етил,
М - натрій або калій.
2. Спосіб згідно з п. 1, який відрізняється тим, що як розчинник використовують сполуку, яку вибирають з групи, що містить диметоксіетан, діоксан і тетрагідрофуран.
3. Спосіб згідно з п. 2, який відрізняється тим, що як розчинник використовують тетрагідрофуран.
4. Спосіб згідно з одним із пп. 1-3, який відрізняється тим, що використовують сполуку формули (II), в якій Hal означає фтор.
5. Спосіб згідно з одним із пп. 1-4, який відрізняється тим, що використовують сполуку формули (III), в якій М означає калій.
6. Спосіб згідно з одним із пп. 1-5, який відрізняється тим, що на 1 еквівалент сполуки формули (II) використовують від 1 до 3, найкраще від 1,1 до 1,3, еквівалента метанолу і від 2 до 3, краще від 2,1 до 2,3, еквівалента сполуки формули (III).
7. Спосіб згідно з одним із пп. 1-6, який відрізняється тим, що реакцію проводять при температурі від 20°С до температури кипіння розчинника при атмосферному тиску.
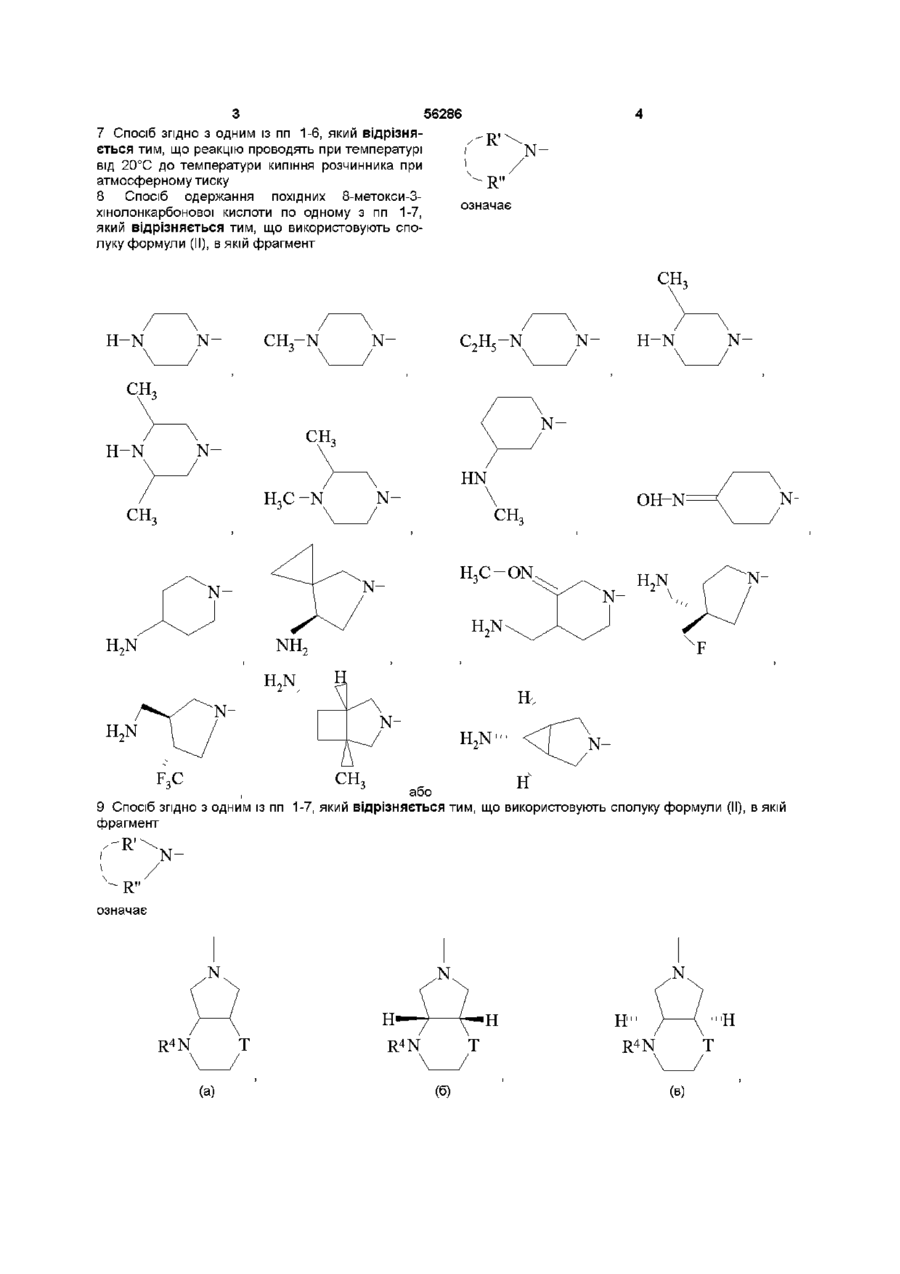
8. Спосіб одержання похідних 8-метокси-3-хінолонкарбонової кислоти по одному з пп. 1-7, який відрізняється тим, що використовують сполуку формули (II), в якій фрагмент
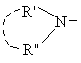
означає
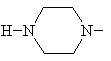 ,
,
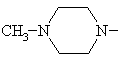 ,
,
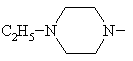 ,
,
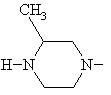 ,
,
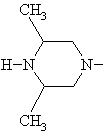 ,
,
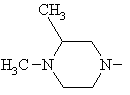 ,
,
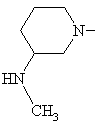 ,
,
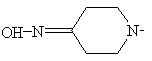 ,
,
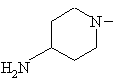 ,
,
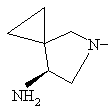 ,
,
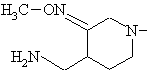 ,
,
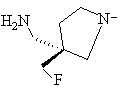 ,
,
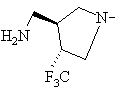 ,
,
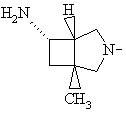 або
або
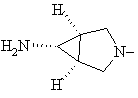 .
.
9. Спосіб згідно з одним із пп. 1-7, який відрізняється тим, що використовують сполуку формули (II), в якій фрагмент
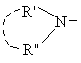
означає
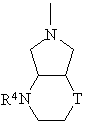 ,
,
(а)
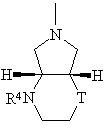 ,
,
(б)
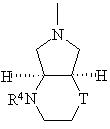 ,
,
(в)
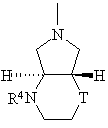 або
або
(г)
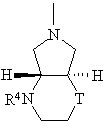 ,
,
(д)
де
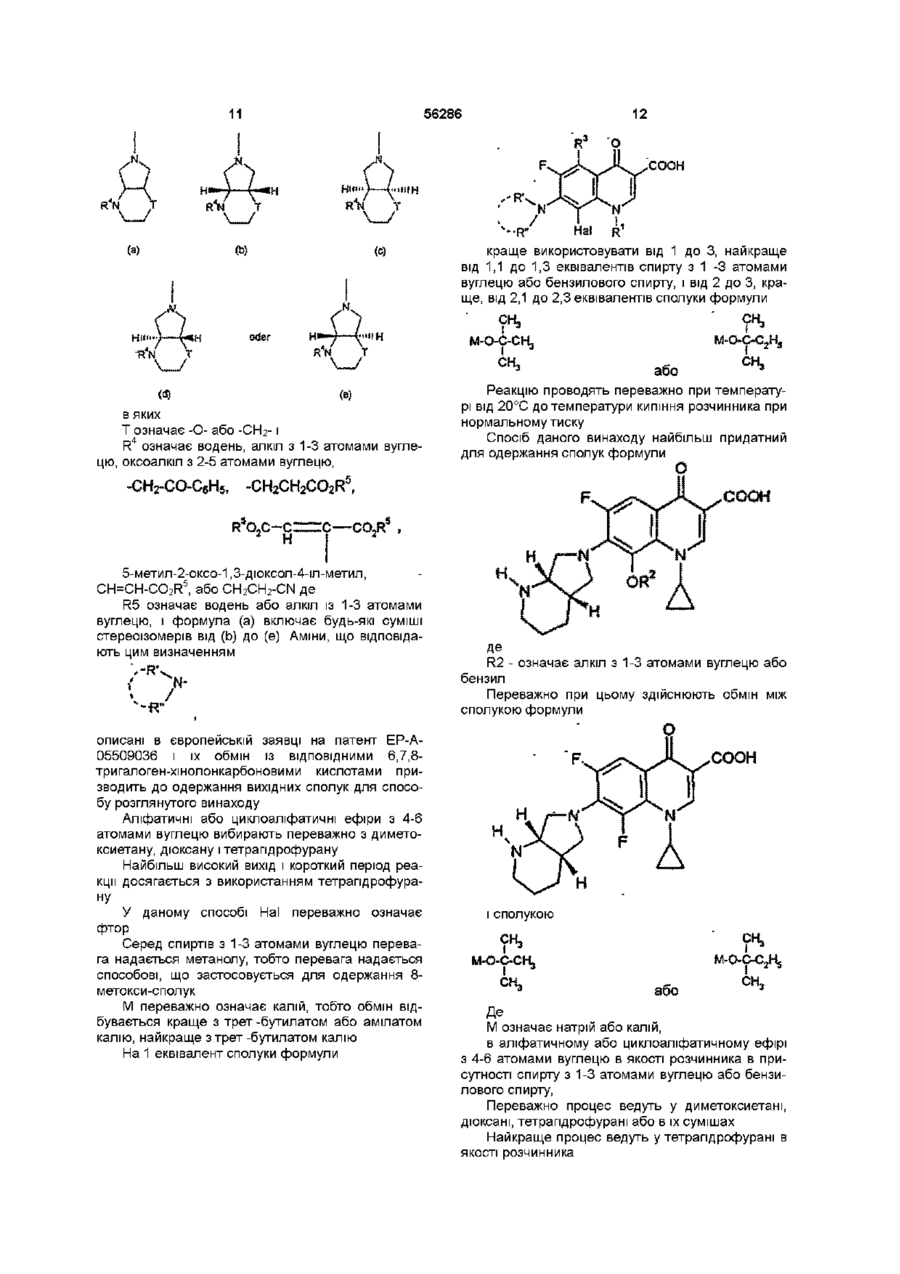
Т означає -О- або -CH2-, і
R4 означає водень, алкіл з 1-3 атомами вуглецю, оксоалкіл з 2-5 атомами вуглецю,
-CH2-CO-C6H5, -CH2CH2CO2R5, ![]() ,
,
5-метил-2-оксо-1,3-діоксол-4-іл-метил, -CH=CH-CO2R5 або CH2CH2-CN,
де
R5 означає водень або алкіл з 1-3 атомами вуглецю, і формула (а) включає будь-які суміші стереоізомерів (б)-(д).
10. Спосіб згідно з п. 1, який відрізняється тим, що використовують сполуку формули (II), в якій фрагмент
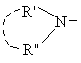
означає групу формули
 , (б)
, (б)
де
Т означає -СН2-,
R4 означає водень,
R1 означає циклопропіл,
Hal означає фтор,
R3 означає водень.
11. Спосіб згідно з п. 10, який відрізняється тим, що як розчинник використовують тетрагідрофуран.
12. Спосіб згідно з п. 10, який відрізняється тим, що використовують сполуку формули (III), в якій М означає калій.
13. Спосіб згідно з п. 10, який відрізняється тим, що на 1 еквівалент сполуки формули (II) використовують від 1 до 3, найкраще від 1,1 до 1,3, еквівалента метанолу і від 2 до 3, краще від 2,1 до 2,3, еквівалента сполуки формули (III).
14. Спосіб згідно з п. 10, який відрізняється тим, що реакцію проводять при температурі від 20°С до температури кипіння розчинника при атмосферному тиску.
15. Спосіб згідно з п. 1, який відрізняється тим, що використовують сполуку формули (II), в якій фрагмент
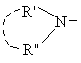
означає групу формули
 , (б)
, (б)
де
Т означає -CH2-,
R4 означає водень,
R1 означає циклопропіл,
Hal означає фтор,
R3 означає водень,
яку вводять у взаємодію з метанолом і трет.-бутилатом калію в середовищі тетрагідрофурану як розчинника.
16. Спосіб згідно з п. 15, який відрізняється тим, що на 1 еквівалент сполуки формули (II) використовують від 1 до 3, краще від 1,1 до 1,3, еквівалента метанолу і від 2 до 3, краще від 2,1 до 2,3, еквівалента трет.-бутилату калію.
17. Спосіб згідно з одним із пп. 15 або 16, який відрізняється тим, що реакцію проводять при температурі від 20°С до температури кипіння розчинника при атмосферному тиску.
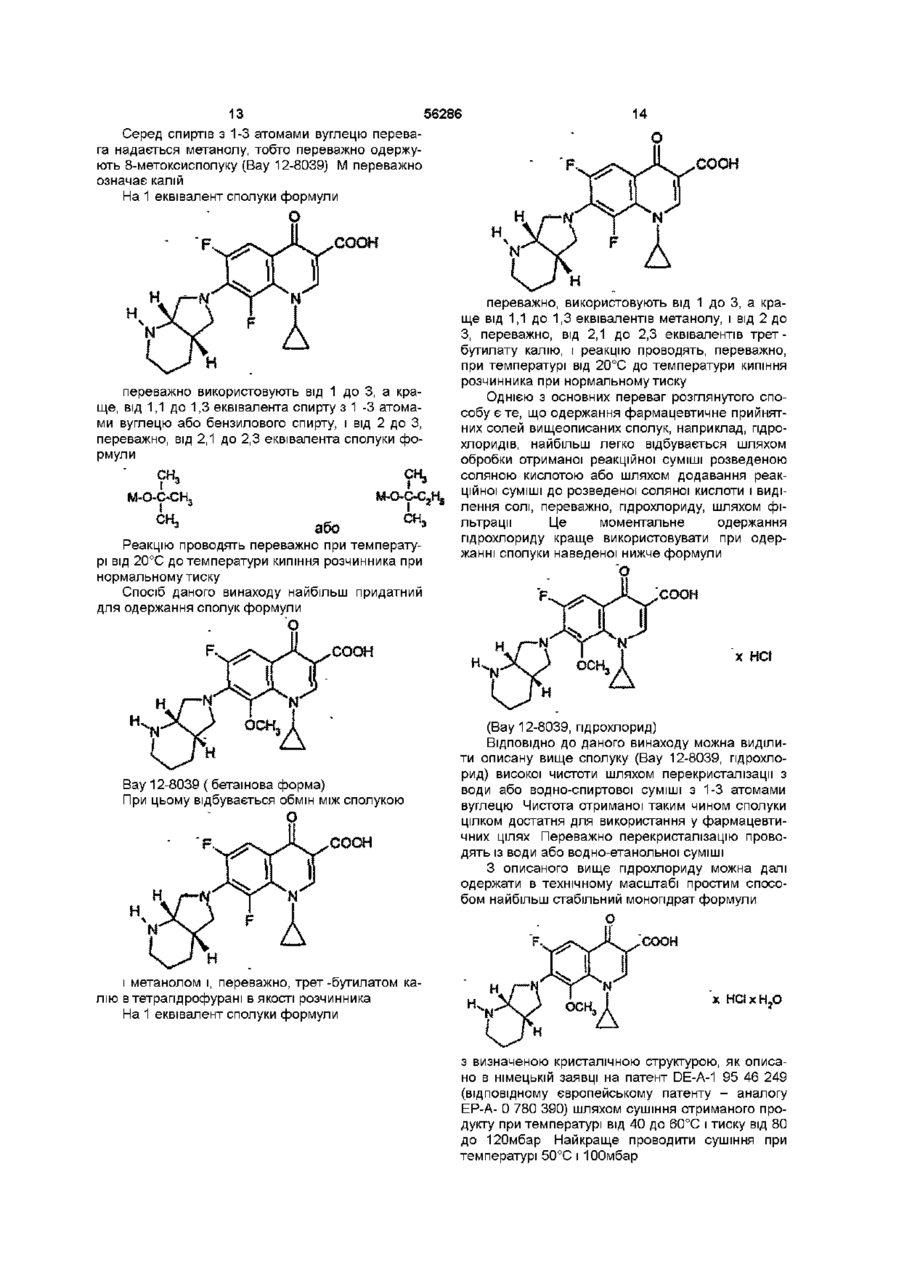
18. Спосіб згідно з одним із пп. 15-17, який відрізняється тим, що після завершення реакції реакційну суміш обробляють розведеною соляною кислотою або реакційну суміш додають до розведеної соляної кислоти і гідрохлорид, що випав в осад, відокремлюють за допомогою фільтрування.
19. Спосіб згідно з одним з пп. 1-18, який відрізняється тим, що цільовий продукт піддають перекристалізації з води або водно-спиртової суміші, де спирт містить від 1 до 3 атомів вуглецю.
20. Спосіб згідно з п. 19, який відрізняється тим, що перекристалізацію проводять з води або водно-етанольної суміші.
21. Спосіб згідно з пп. 19 або 20, який відрізняється тим, що одержаний продукт висушують при температурі від 40 до 60°С і тиску від 80 до 120 мбар з одержанням гідрату гідрохлориду.
22. Спосіб згідно з п. 21, який відрізняється тим, що висушування проводять при температурі близько 50°С і тиску близько 100 мбар.
Текст
1 Спосіб одержання похідних 8-метокси-Зхінолонкарбонової кислоти загальної формули (І) R3 СООН \ / R Hal Б в якій Hal - фтор або хлор, і 3 R" R1, R і мають наведені вище значення, вводять у взаємодію з метанолом в середовищі розчинника, аліфатичного або циклоаліфатичного етеру з 4-6 атомами вуглецю, і в присутності алкоголяту формули (III) II соон M - O - C - R " СН, , (НІ) Де OR2 в якій R' і R" разом з атомом азоту, із яким вони зв'язані, утворюють моно- або біциклічний гетероцикл, який може бути заміщеним у всіх положеннях кільця і може містити ІНШІ гетероатоми азоту, кисню або сірки, R - алкіл з 1-3 атомами вуглецю, фторетил, циклопропіл, незаміщений або заміщений від одного до трьох разів галогенами феніл і циклопропіл, R2 - метил, R3 - водень, галоген, аміно, метил, який відрізняється тим, що ПОХІДНІ 8-галоген-Зхінолонкарбонової кислоти загальної формули (II) О R'" означає метил або етил, М - натрій або калій 2 Спосіб згідно з п 1, який відрізняється тим, що як розчинник використовують сполуку, яку вибирають з групи, що містить диметоксіетан, діоксан і тетрапдрофуран 3 Спосіб згідно з п 2, який відрізняється тим, що як розчинник використовують тетрапдрофуран 4 Спосіб згідно з одним із пп 1-3, який відрізняється тим, що використовують сполуку формули (II), в якій Hal означає фтор 5 Спосіб згідно з одним із пп 1-4, який відрізняється тим, що використовують сполуку формули (III), в якій М означає калій 6 Спосіб згідно з одним із пп 1-5, який відрізняється тим, що на 1 еквівалент сполуки формули (II) використовують від 1 до 3, найкраще від 1,1 до 1,3, еквівалента метанолу і від 2 до 3, краще від 2,1 до 2,3, еквівалента сполуки формули (III) (О 00 (О ю З 56286 7 Спосіб згідно з одним із пп 1-6, який відрізня•R' ється тим, що реакцію проводять при температурі від 20°С до температури кипіння розчинника при атмосферному тиску R" 8 Спосіб одержання похідних 8-метокси-Зозначає хінолонкарбонової кислоти по одному з пп 1-7, який відрізняється тим, що використовують сполуку формули (II), в якій фрагмент CH CH.-N N C?H,-N H~N N N CH H-N N HN CH, CH, OH-N H3C-ON N H2N NH2 H2N Б-, N H2N CH, або 9 Спосіб згідно з одним із пп 1-7, який відрізняється тим, що використовують сполуку формули (II), в якій фрагмент і N означає 4 RN н«4 RN Т (б) 56286 або (г) Де Т означає -О- або -СН2-, і 4 R означає водень, алкіл з 1-3 атомами вуглецю, оксоалкіл з 2-5 атомами вуглецю, -CH2-CO-C6П5, RH - HC 9 OR C 9 HC 9 с= с CO2R н 5-метил-2-оксо-1,3-дюксол-4-іл-метил, 5 R5O2C 5 15 Спосіб згідно з п 1, який відрізняється тим, що використовують сполуку формули (II), в якій фрагмент -СН=СН N означає групу формули CO2R або CH2CH2-CN, Д ! R означає водень або алкіл з 1-3 атомами вуглецю, і формула (а) включає будь-які суміші стереоізомерів (б)-(д) 10 Спосіб згідно з п 1, який відрізняється тим, що використовують сполуку формули (II), в якій фрагмент Nозначає групу формули Н« R4N Де Т Т означає -СН2-, R4 означає водень, R1 означає циклопропіл, Hal означає фтор, R3 означає водень 11 Спосіб згідно з п 10, який відрізняється тим, що як розчинник використовують тетрапдрофуран 12 Спосіб згідно з п 10, який відрізняється тим, що використовують сполуку формули (III), в якій М означає калій 13 Спосіб згідно з п 10, який відрізняється тим, що на 1 еквівалент сполуки формули (II) використовують від 1 до 3, найкраще від 1,1 до 1,3, еквівалента метанолу і від 2 до 3, краще від 2,1 до 2,3, еквівалента сполуки формули (III) 14 Спосіб згідно з п 10, який відрізняється тим, що реакцію проводять при температурі від 20°С до температури кипіння розчинника при атмосферному тиску Н« R4N Де Т Т означає -СН2-, R4 означає водень, R1 означає циклопропіл, Hal означає фтор, R3 означає водень, яку вводять у взаємодію з метанолом і третбутилатом калію в середовищі тетрапдрофурану як розчинника 16 Спосіб згідно з п 15, який відрізняється тим, що на 1 еквівалент сполуки формули (II) використовують від 1 до 3, краще від 1,1 до 1,3, еквівалента метанолу і від 2 до 3, краще від 2,1 до 2,3, еквівалента трет -бутилату калію 17 Спосіб згідно з одним із пп 15 або 16, який відрізняється тим, що реакцію проводять при температурі від 20°С до температури кипіння розчинника при атмосферному тиску 18 Спосіб згідно з одним із пп 15-17, який відрізняється тим, що після завершення реакції реакційну суміш обробляють розведеною соляною кислотою або реакційну суміш додають до розведеної соляної кислоти і пдрохлорид, що випав в осад, відокремлюють за допомогою фільтрування 19 Спосіб згідно з одним з пп 1-18, який відрізняється тим, що цільовий продукт піддають перекристалізації з води або водно-спиртової суміші, де спирт містить від 1 до 3 атомів вуглецю 20 Спосіб згідно з п 19, який відрізняється тим, що перекристалізацію проводять з води або водно-етанольної суміші 21 Спосіб згідно з пп 19 або 20, який відрізняється тим, що одержаний продукт висушують при температурі від 40 до 60°С і тиску від 80 до 120 мбар з одержанням гідрату пдрохлориду 7 56286 8 22 Спосіб згідно з п 21, який відрізняється тим, зько 50°С і тиску близько 100 мбар що висушування проводять при температурі бли Винахід стосується способу одержання 8метокси-хшолон карбонових кислот 8-метокси-хшолонкарбонові кислоти являють собою антибіотики з високою бактеріальною дією проти грам-негативних і грам-позитивних бактерій В антибютиках-1-циклопропіл-б-фтор-1,4-дипдро8-метокси-7-(3-метил-1-піперазиніл)-4-оксо-3хінолшкарбонової кислоті (INN, Гатіфлоксацин, європейська заявка на патент ЕР-А-230 295) і моногідраті пдрохлориду 1-L|Hmonpomn-7-[S,S]-2,8діазабіцикло[4 3 0]нон-8-іл)-6-фтор-1,4-дипдро-8метокси-4-оксо-З-хшолон-карбоновій кислоті (Bay 12-8039, європейська заявка на патент ЕР-А- 0 350 733) метокси-група знаходиться у 8-ому положенні Наведені вище хінолонкарбонові кислоти з високою антибактеріальною дією містять, як правило, залишок гетеромоноциклічного або гетеропоЛІЦИКЛІЧНОГО аміну у 7-ому положенні хінолонкарбонової кислоти Цей циклічний залишок аміну одержують, як правило, шляхом нуклеофільного заміщення відповідної 7-галогенхінолонкарбонової кислоти ВІДПОВІДНИМ аміном Введення у 8-е положення алкоксигрупи в принципі можливе до введення залишку циклічного аміну в 7-е положення або після цього Так, в європейській заявці на патент ЕР-А-0 350 733 описано одержання рацемату бетаїну вищезгаданого Bay 128039, виходячи з відповідної 8-метоксисполуки, одержання якої описано в європейській заявці на патент ЕР-А-0 241 206 (препарат 6), шляхом нуклеофільного заміщення ВІДПОВІДНИМ рацемічним аміном Аналогічно описується одержання бетаїну Bay 12-8039, що не містить енантюмерів, виходячи з 8-метоксисполуки шляхом нуклеофільного заміщення аміном, що не містить енантюмерів, у європейській заявці на патент ЕР-А-0 550 903 (приклад 19) Проте описаний спосіб одержання вимагає стадій, що дорого коштують, виділення і очищення з використанням колонкової хроматографії, що не бажана для використання в промисловому масштабі Останній спосіб описаний також у європейській заявці на патент ЕР-А-0 591 808 (приклад Z 19) Інший спосіб введення 8-алкокси-замісника в 7-амшозаміщені хінолонкарбонові кислоти полягає у введенні 8-алкокси-замісника після введення замісника - циклічного аміну - у 7-е положення відповідної 7,8-дигалоген-заміщеноі вихідної сполуки Так у європейській заявці на патент ЕР-А-0 106 489 описаний спосіб одержання 8-метоксизаміщеного похідного після введення гетероциклічного замісника в 7-е положення шляхом проведення перетворення відповідної 8-фторсполуки у метанолі в присутності трет -бутилату калію Проте, наведена там реакція з 7-[ 2-[Метиламшо)метил]-4-тіазолом] вимагає 24 годин нагрівання із зворотним холодильником і тому не придатна для проведення в технічному масштабі Крім цього ясно, що деякі хінолонкарбонові кислоти, як наприклад, описану вище Bay 12-8039, не можна одержати таким способом, тому що за 24 години нагрівання із зворотним холодильником неможливо здійснити реакцію обміну або заміщення Спосіб одержання 8-алкоксизаміщених сполук із похідних 8-галощ-7-моноциклоамшу у метанолі в присутності алкоголятів лужних металів описаний також у європейській заявці на патент ЕР-А-02 ЗО 295 Описане в прикладах зазначеного патенту перетворення в присутності метилату натрію вимагає дуже високих температур - від 140 до 150°С і дуже тривалого часу реакції в закритих ємностях під тиском Крім того, описаний спосіб не можна широко використовувати для одержання 8метокси-хшолонкарбонових кислот Так, застосування цього способу для одержання вищеописаного Bay 12-8039 за умови використання в якості розчинника метанолу не призводить до одержання кінцевого продукту навіть після закінчення 70 годин У випадку проведення реакції ВІДПОВІДНОГО 8фторпохідного з метилатом натрію у тетрапдрофурані для повного перетворення потрібно більше 24 годин і надлишок метилату Аналогічним способом відбувається одержання 8-алкоксипохідного ВІДПОВІДНО ДО європейської заявки на патент ЕР-А-0 235 762 шляхом обміну 8галоід-7-моноциклоамшопохідного з алкоголятами лужних металів Описано також одержання 8метокси-хшолонкарбонових кислот шляхом реакції обміну з алкоголятами лужних металів у таких розчинниках, як диметилізофталат (DMI) (міжнародна заявка WO 93/22308, Chugai), з метилатом натрію в диметилформа-міді (DMF) або диметилсульфоксиді (DMSO) (європейська заявка на патент ЕР-А-0 342 675, Chugai), з системою гідрид натрію / бензиловий спирт (Research Disclosure No 291 097, 1988), із метилатом натрію в диметилформаміді (DMF) при температурі 80°С протягом 9 годин (японська заявка на патент JP 03007283 Yoshitomi), із метанолом і основою (міжнародна заявка WO 90/06305 Daimppon), із гідрид натрію^рифторетанолом у диметилформаміді (DMF) (міжнародна заявка WO 92/09579), із метилатом натрію в метанолі (японська заявка на патент JP62 252722), із системою метилат натрію/ диметилізофталат (DMI) при температурі 80°С (японська заявка на патент JP- 05117 238, Chugai), а також перетворення під дією метилату натрію в метанолі (J Med Chem 30,2163-2169) Хоча заміщення 8-гало]д похід ного під дією алкоголятів лужних металів у випадку, якщо алкоголят лужного металу беруть у надлишку, у полярних, апротонних розчинниках, як наприклад, диметилформаміді (DMF), призводить загалом практично до повного перетворення, процес виділення солей 8-алкокси-хшолонкарбонових кислот із таких розчинників трудомісткий, вимагає великих 56286 витрат і технічно утруднений для виконання Задачею даного винаходу є розробка способу одержання похідних 8-метокси- хінолонкарбонових кислот, що дозволяє скоротити час реакції, проводити роботу при атмосферному тиску, що забезпечує повне перетворення, а також просту підготовку реакційної суміші Випадково було виявлено, що можна одержати похідне 8-метокси-хшолонкарбоновоі кислоти способом, що відповідає, названим вище вимогам, шляхом обміну ВІДПОВІДНОГО похідного 8-галоідхінолонкарбонової кислоти із спиртами з 1-3 атомами вуглецю або бензиловим спиртом і третбутилатом натрію або калію або трет-амілатом натрію або калію в присутності аліфатичних або циклоаліфатичних ефірів із 4-6 атомами вуглецю в якості розчинника Предметом винаходу, таким чином, є спосіб одержання сполук формули в якій R' і R" разом з атомом азоту, із яким вони зв'язані, утворюють моно-або біциклічний гетероцикл, який за певних умов у всіх положеннях кільця може містити ІНШІ гетероатоми азоту, кисню або сірки і за певних умов може бути заміщений, де R1 - алкіл з 1-3 атомами вуглецю, FCbb - СН2, циклопропіл, за певних умов одноразово - триразове галогензаміщений феніл або циклопропіл, R2 - алкіл з 1-3 атомами вуглецю або бензил, R 3 -H, галоген, NH2,CH3, який відрізняється тим, що ПОХІДНІ 8-галоген-Зхінолонкарбонової кислоти загальної формули 10 розчинника в присутності спирту з 1-3 атомами вуглецю або бензилового спирту, Група і > -Я" утворює моно- або біциклічний гетероцикл, який за певних умов у всіх положеннях кільця може містити ІНШІ гетероатоми азоту, кисню або сірки і який за певних умов може бути заміщений Ланки R' і R" можуть бути однаковими або різними складовими кільця Такі моно- або біциклічні залишки аміну у 7-ому положенні основної структури хінолонкарбонової кислоти ВІДОМІ, в основному, для антибіотиків ряду хінолонкарбонової кислоти Як приклад варто вказати на патентні публікації європейських заявок ЕР-А-0 523 512, ЕР-А-0 230 295, ЕР-А-0 705 828, ЕР-А-0 589318, ЕР-А-0 357 047, ЕР-А-0 588 166, патент Великобританії GB-A-2 289 674, міжнародної заявки WO 92/09 579, японської заявки JP-03-007 283, європейських заявок ЕР-А-0 241 206, ЕР-А-0 342 675, міжнародної заявки WO 93/22 308 і європейської заявки ЕР-А-0 350 733 Серед цих відомих залишків аміну кращі наступні мають зазначені вище значення, піддають реакції обміну із сполукою формули GH3-N ^N CH, HCN 3 N HN , в якій Hal - фтор або хлор і R1, R , R і ,-R% 4 N Н^ NH, Ы HN N о? FC , СН, Найкращі для СН, ! м-о-с-с,нч М-0-C-CHj І або 2 сн, s Де М - означає натрій або калій, в аліфатичному або циклоаліфатичному ефірі з 4-6 атомами вуглецю в якості Cfy-Ы наступні значення сн. Н 11 56286 12 соон R * N R'N T R T * N (c) краще використовувати від 1 до 3, найкраще від 1,1 до 1,3 еквівалентів спирту з 1 -3 атомами вуглецю або бензилового спирту, і від 2 до 3, краще, від 2,1 до 2,3 еквівалентів сполуки формули -о-с-сн '2"s Oder И»' і ^ (є) (Ф В ЯКИХ Т означає -О- або -СН2-1 R4 означає водень, алкіл з 1-3 атомами вуглецю, оксоалкіл з 2-5 атомами вуглецю, або Реакцію проводять переважно при температурі від 20°С до температури кипіння розчинника при нормальному тиску Спосіб даного винаходу найбільш придатний для одержання сполук формули -CH2CH2CO2R5, R о,с-с: 2 н •ссу*3 5-метил-2-оксо-1,3-дюксол-4-іл-метил, CH=CH-CO2R5, або CH2CH2-CN де R5 означає водень або алкіл із 1-3 атомами вуглецю, і формула (а) включає будь-які суміші стереоізомерів від (Ь) до (є) Аміни, ЩО відповідають цим визначенням описані в європейській заявці на патент ЕР-А05509036 і їх обмін із ВІДПОВІДНИМИ 6,7,8тригалоген-хшолонкарбоновими кислотами призводить до одержання вихідних сполук для способу розглянутого винаходу Аліфатичні або циклоаліфатичні ефіри з 4-6 атомами вуглецю вибирають переважно з диметоксиетану, діоксану і тетрапдрофурану Найбільш високий вихід і короткий період реакції досягається з використанням тетрапдрофурану У даному способі Hal переважно означає фтор Серед спиртів з 1-3 атомами вуглецю перевага надається метанолу, тобто перевага надається способові, що застосовується для одержання 8метокси-сполук М переважно означає калій, тобто обмін відбувається краще з трет-бутилатом або амілатом калію, найкраще з трет -бутилатом калію На 1 еквівалент сполуки формули R2 - означає алкіл з 1-3 атомами вуглецю або бензил Переважно при цьому здійснюють обмін між сполукою формули СООН і сполукою М-0-C-CHj або сн, Де М означає натрій або калій, в аліфатичному або циклоаліфатичному ефірі з 4-6 атомами вуглецю в якості розчинника в присутності спирту з 1-3 атомами вуглецю або бензилового спирту, Переважно процес ведуть у диметоксиетані, діоксані, тетрагідрофурані або в їх сумішах Найкраще процес ведуть у тетрагідрофурані в якості розчинника 13 56286 Серед спиртів з 1-3 атомами вуглецю перевага надається метанолу, тобто переважно одержують 8-метоксисполуку (Bay 12-8039) М переважно означає калій На 1 еквівалент сполуки формули 14 СООН 'F, соон переважно використовують від 1 до 3, а краще, від 1,1 до 1,3 еквівалента спирту з 1 -3 атомами вуглецю або бензилового спирту, і від 2 до З, переважно, від 2,1 до 2,3 еквівалента сполуки формули M-O-C-CR сн * або Ін > Реакцію проводять переважно при температурі від 20°С до температури кипіння розчинника при нормальному тиску Спосіб даного винаходу найбільш придатний для одержання сполук формули F, переважно, використовують від 1 до 3, а краще від 1,1 до 1,3 еквівалентів метанолу, і від 2 до З, переважно, від 2,1 до 2,3 еквівалентів третбутилату калію, і реакцію проводять, переважно, при температурі від 20°С до температури кипіння розчинника при нормальному тиску Однією З ОСНОВНИХ переваг розглянутого способу є те, що одержання фармацевтичне прийнятних солей вищеописаних сполук, наприклад, пдрохлоридів, найбільш легко відбувається шляхом обробки отриманої реакційної суміші розведеною соляною кислотою або шляхом додавання реакційної суміші до розведеної соляної кислоти і виділення солі, переважно, пдрохлориду, шляхом фільтрації Це моментальне одержання пдрохлориду краще використовувати при одержанні сполуки наведеної нижче формули О СООН СООН х HCt / X Bay 12-8039 ( беташова форма) При цьому відбувається обмін між сполукою СООН (Bay 12-8039, пдрохлорид) ВІДПОВІДНО ДО даного винаходу можна виділити описану вище сполуку (Bay 12-8039, пдрохлорид) високої чистоти шляхом перекристалізації з води або водно-спиртової суміші з 1-3 атомами вуглецю Чистота отриманої таким чином сполуки цілком достатня для використання у фармацевтичних цілях Переважно перекристалізацію проводять із води або водно-етанольної суміші З описаного вище пдрохлориду можна далі одержати в технічному масштабі простим способом найбільш стабільний моногідрат формули СООН і метанолом і, переважно, трет-бутилатом калію втетрапдрофурані в якості розчинника На 1 еквівалент сполуки формули х НС!хНгО з визначеною кристалічною структурою, як описано в німецькій заявці на патент DE-A-1 95 46 249 (відповідному європейському патенту - аналогу ЕР-А- 0 780 390) шляхом сушіння отриманого продукту при температурі від 40 до 60°С і тиску від 80 до 120мбар Найкраще проводити сушіння при температурі 50°С і ЮОмбар 16 15 56286 Алкіл з 1-3 атомами вуглецю або алкільні запереходять у розчин Перемішування продовжулишки у вищенаведених визначеннях означають, ють ще протягом однієї години при температурі від як правило, метил, етил, пропіл, ізопропіл 20 до 22°С, фільтрують і промивають 3 х 15мл етанолу Сушіння при температурі 50°С і тиску Переважно, алкіл з 1-3 атомами вуглецю і алЮОмбар призводить до одержання моногідрату кільний залишок з 1-3 атомами вуглецю у ВІДПОВІBay 12-8039-пдрохлориду ДНИХ аліфатичних залишках означає метил Приклад 1 Одержують 31,9г кристалізату жовтого кольоОдержання пдрохлориду 1-циклопропіл-7ру, який має достатню для використання у фарма([8,8]-2,8-діазабіцикло[4 3 0]нон-8-іл)-6-фтор-1,4кологи чистоту дипдро-8-метокси-4-оксо-3-хшолонкарбоновоі кисПриклад 2 лоти з використанням трет -бутилату калію ВикоОдержання пдрохлориду 1-циклопропт-7ристовувані КІЛЬКОСТІ ([8,8]-2,8-діазабіцикло[4 3 0]нон-8-іл)-6-фтор-1,4дипдро-8-метокси-4-оксо-3-хшолонкарбоновоі кис50,0г (0,129моль)1-циклопропіл-7-([8,8]-2,8лоти з використанням трет -амілату калію Викоридіазабіцикло[4 3 0] нон-8-іл)-6,8-дифтор-1,4стовувані КІЛЬКОСТІ дипдрокси-4-оксо-З-хшолонкарбоновоі кислоти (Bay z 7906) (отримано ВІДПОВІДНО ДО приклада 1 10,0г (25,7ммоль) Bay z 7906, Pt 501781 ЕР-А-0 550 903) 54 мл ТГФ 270,0мл ТГФ 1,24мл 6,2мл (0,155 (30,8ммоль) метанол 35,6г (56,5 розчин трет -амілату калію ммоль) метанол 159,1г (0,284 розчин трет -бутилату каммоль) (20%-ний у ТГФ) ммоль) лію ( 20%-ний у ТГФ) 26,6мл вода 128мл вода 7,6мл соляна кислота, концентр 38мл соляна кислота, концентр 6,0мл вода ЗОмл вода 12,0мл етанол 60мл етанол Метод роботи 110мл етанол 10r Bay z 7906 поміщають у 54мл ТГФ і 1,24мл ЗЗмл вода метанолу Вміст підігрівають і, починаючи приблизно з 60°С, приблизно за 5 хвилин подають 17мл З х 15мл етанол розчину трет-амілату калію (20%-ного в ТГФ), що Метод роботи відповідає 1 еквіваленту Перемішують протягом У ЮООмл тригорлову колбу з мішалкою і терЗО хвилин, нагріваючи із зворотним холодильнимометром поміщають в атмосфері азоту 50,0г Bay ком У цих умовах за п'ять хвилин подають залиz 7906 у 270мл ТГФ і 6,2мл метанолу Вміст підішок розчину трет -амілату калію Перемішують грівають і починаючи приблизно з 60°С приблизно протягом 2,5 годин, нагріваючи із зворотним холоза 5 хвилин подають 80мл розчину трет-бутилату дильником, а потім охолоджують до кімнатної темкалію (20%-ного в ТГФ), що відповідає 1 еквівалеператури Для осадження пдрохлориду необхідно нту Утворюється суспензія жовтого кольору, яка мати 26,6мл води і 7,6мл концентрованої соляної поступово густішає, набуваючи білого кольору кислоти При 500 оборотах у хвилину і охолодженПеремішують протягом 15 хвилин, нагріваючи із ні за 2 години при температурі від 20 до 22°С по зворотним холодильником При цьому суспензія краплях подають реакційний розчин Після подачі не змінюється У цих умовах протягом 5 хвилин порядку 9мл вносять затравку кристалізації у виподають залишок трет-бутилату калію Перемігляді Bay 12-8039 Після повної подачі реакційного шують протягом 2,5 годин, нагріваючи із зворотрозчину проводять протягом приблизно ЗО хвилин ним холодильником, а потім охолоджують до кімперемішування при температурі 8°С Утворюється натної температури Для осадження пдрохлориду суспензія, її відфільтровують, промивають бмл необхідно мати 128мл води і 38мл концентрованої води, а потім 12мл етанолу і сушать у вакуумі при соляної кислоти в ДВОСТІННІЙ колбі (подвійний котемпературі 50°С Одержують 8,6г продукту жух) з мішалкою, лічильник числа оборотів і термостат При 500 оборотах у хвилину при охолоОтриманий продукт за аналогією з прикладом дженні протягом 2 годин при температурі від 20 до 1 може бути очищений і переведений у моногід22°С по краплях подають отриманий вище реакрат ційний розчин Після подачі порядку 50мл вносять Порівняльний приклад затравку кристалізації у вигляді 12,5мг Bay 12(обмін Bay z 7906 у ТГФ із метилатом натрію) 8039 Перемішують протягом приблизно ЗО хвилин Використовувані КІЛЬКОСТІ при температурі 8°С Утворюється суспензія, її 50,0г відфільтровують і промивають ЗОмл води, а потім (0,129моль) Bayz7906 60мл етанолу Отриманий кінцевий продукт легко 1040мл ТГФ фільтрують і сушать у вакуумі при температурі 116,1г РОЗЧИН метилату натрію ( 50°С Одержують 47,1г продукту (0,645моль) 30%-ний у метанолі) Очищення і утворення моногідрату 49мл соляна кислота, концентр Для очищення розчиняють 46,6г отриманого 7мл ТГФ продукту в 110мл етанолу/ЗЗОмл води, нагріваючи 38мл вода із зворотним холодильником, і охолоджують про385мл вода тягом 2 годин до температури 20-22°С При тем2х38мл вода пературі приблизно 50°С проводять затравлюван297мл метанол ня кристалізації з 12,5мг Bay 12-8039 Кристали не 2x1 Омл метанол 18 17 56286 68мл етанол при температурі 20-25°С, відсмоктують і ДВІЧІ промивають 38мл води (погане відсмоктування) 34мл вода 2х10мл етанол Тверду речовину (40,4г) після сушіння у вакуМетод роботи умі при температурі 50°С розчиняють у 297мл метанолу при нагріванні із зворотним холодильниУ 2000мл тригорлову колбу з мішалкою і терком Після охолодження до температури 10°С мометром поміщають в атмосфері азоту 50,0г Bay кристали, що випали в осад, відсмоктують і ДВІЧІ z 7906 у 1040мл ТГФ і 116,1 г розчину метил ату промивають Юмл метанолу натрію (30%-ного в метанолі) Вміст нагрівають при перемішуванні із зворотним холодильником і Тверду речовину (21,1г) після сушіння у вакухід реакції контролюють за допомогою рідинної умі при температурі 50°С розчиняють у 68мл етахроматографії високого тиску (HPLC) нолу і 34мл води при нагріванні із зворотним хоВміст ( Bay z 7906 [ вихідний малодильником Після охолодження до температури теріал] після 6 годин RF (нагрі20-25°С продовжують перемішування кристали, вання із зворотним холодильнищо випали в осад, відсмоктують і ДВІЧІ промивають ком) = 56,5 % Юмл етанолу Після сушіння у вакуумі при темпепісля ЗО годин RF =11,7% ратурі 50°С одержують 16,2г кристалізату жовтопісля 70 годин RF = 1,4%) гарячого кольору Після 70 годин перемішування із зворотним Порівняння прикладів розглянутого винаходу і холодильником охолоджують до температури 10порівняльного прикладу показує, що навіть після 15°С і концентрованою соляною кислотою встано70 годин реакції з метилатом натрію в ТГФ утвовлюють величину рН 6,8-7,0 (витрати концентрорюється незначний вихід ваної соляної кислоти 48 мл) Осад відсмоктують і Таким чином спосіб розглянутого винаходу дає промивають спочатку 77мл ТГФ, а потім 38мл вовеликі переваги в промисловому масштабі з точки ди зору виходу цільового продукту, умов проведення реакції і попередньої підготовки Вологу тверду речовину (108,2г) суспендують у 385мл води, перемішують протягом ЗО хвилин Підписано до друку 05 06 2003 р Тираж 39 прим ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)236-47-24
ДивитисяДодаткова інформація
Назва патенту англійськоюA method for producing 8-methoxy-quinoline carboxylic acids
Автори англійськоюGehring Reinhold, Mohrs Klaus, Heilmann Werner
Назва патенту російськоюСпособ получения 8-метокси-хинолонкарбоновых кислот
Автори російськоюГеринг Райнхольд, Морс Клаус, Хайльманн Вернер
МПК / Мітки
МПК: C07D 471/04, A61P 31/04, A61K 31/47, A61K 31/4709, A61K 31/496, C07D 215/56, C07D 401/04
Мітки: кислоти, похідних, одержання, спосіб, 8-метокси-3-хінолонкарбонової
Код посилання
<a href="https://ua.patents.su/9-56286-sposib-oderzhannya-pokhidnikh-8-metoksi-3-khinolonkarbonovo-kisloti.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання похідних 8-метокси-3-хінолонкарбонової кислоти</a>
Попередній патент: Біорозкладний фільтр для сигарет
Наступний патент: Пристрій для відділення головного аеродинамічного обтічника космічної ракети
Випадковий патент: Турбінний перетворювач витрати