Застосування похідних азаіндазолу або діазаіндазолу для лікування болю
Формула / Реферат
1. Застосування сполуки наступної загальної формули (I)
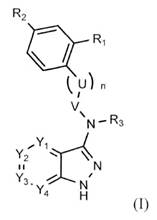
або її фармацевтично прийнятної солі,
де:
- Y1 означає групу CH,
- Y4 означає атом азоту,
- Y2 означає групу C-X-Ar,
- Y3 означає групу C-W,
- Ar означає фенільну групу, необов'язково заміщену одним або більше атомами галогену,
- X означає двовалентну групу, вибрану з О, S, S(О), S(О)2, -S(О)2NH, NHS(О)2, CH2 та CH2CH2,
- W означає групу H або NH2,
- V означає C(O) або C(S),
- n означає 0,
- R1 означає  ,
,
- R2  та
та
- R3 означає атом водню,
для лікування або попередження болю.
2. Застосування за п. 1, яке відрізняється тим, що біль являє собою ноцицептивний біль, запальний біль, невропатичний біль, ідіопатичний біль або психогенний біль.
3. Застосування за п. 2, яке відрізняється тим, що біль являє собою запальний біль або невропатичний біль.
4. Застосування за будь-яким з пп. 1-3, де біль є наслідком раку, пошкодження нервів або ревматичних захворювань.
5. Застосування за будь-яким з пп. 1-4, яке відрізняється тим, що X означає двовалентну групу, вибрану з S, S(O), S(O)2, СН2, NHS(O)2, S(O)2NH і СH2CH2, де перший атом цих груп зв'язаний з атомом С ланцюга С-Х-Аr.
6. Застосування за п. 5, яке відрізняється тим, що X означає двовалентну групу, вибрану з S, S(O), S(O)2, СН2, S(O)2NH і СH2CH2, де перший атом цих груп зв'язаний з атомом С ланцюга С-Х-Аr.
7. Застосування за п. 5, яке відрізняється тим, що X означає двовалентну групу, вибрану з S, S(O)2, СН2, S(O)2NH і СH2CH2, де перший атом цих груп зв'язаний з атомом С ланцюга С-Х-Аr.
8. Застосування за будь-яким з пп. 1-7, яке відрізняється тим, що Аr означає групу, вибрану з наступних груп:
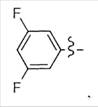
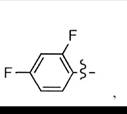
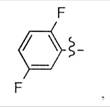
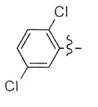 та
та 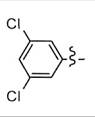 .
.
9. Застосування за будь-яким з пп. 1-8, яке відрізняється тим, що W означає атом водню.
10. Застосування за будь-яким з пп. 1-9, яке відрізняється тим, що сполука вибрана з наступних сполук:
14-10
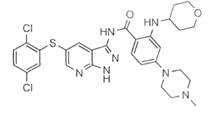
14-11
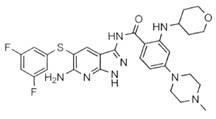
27-1

30
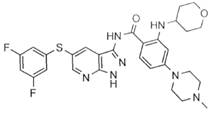
30-8
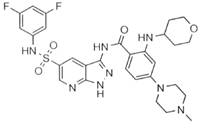
30-9
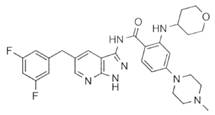
30-72
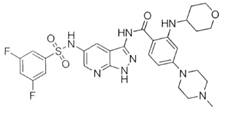
11. Застосування фармацевтичної композиції, яка містить щонайменше один фармацевтично прийнятний ексципієнт і одну сполуку, зазначену у будь-якому з пп. 1 та 5-9, як активної речовини при лікуванні або попередженні болю.
Текст
Реферат: Даний винахід стосується сполуки наступної формули (І) UA 116107 C2 (12) UA 116107 C2 або її фармацевтично прийнятних солей або сольватів, її таутомера або її стереоізомера або суміші стереоізомерів в будь-яких співвідношеннях, такої як суміш енантіомерів, зокрема рацемічна суміш; де дану сполуку застосовують при лікуванні болю. R2 R1 U n V N Y2 Y3 R3 Y1 N Y4 N H (I) UA 116107 C2 5 10 15 20 25 30 35 40 45 50 55 Даний винахід відноситься до конденсованих біциклічних похідних азаіндазолу і діазаіндазолу, вживаних при лікуванні або попередженні болю, зокрема, болю, що асоціюється щонайменше з одним білком Trk. Біль є терміном, використовуваним для опису аномального і хворобливого відчуття, що відчувається живим організмом і сприймається головним мозком. Цим відчуттям є несприятливий сенсорний і емоційний досвід, що асоціюється з пошкодженням тканини, або описуваний в даний момент або потенційно відносно такого пошкодження. Біль може бути гострим або хронічним, і обумовлений різними патологіями. Описано декілька механізмів походження болю: - Ноцицептивний біль: цей біль є сигналом тривоги у відповідь на агресію проти організму, наприклад, біль, викликаний опіками, травмою, контузією, оперізувальним лишаєм, хірургічною операцією або видаленням зуба. У головний мозок посилається сигнал, щоб оповістити його про атаку. - Запальний біль обумовлений гострим або хронічним запаленням, оскільки він може виявлятися при інфекціях, артриті або хворобі Крону. - Невропатичний біль: є болем внаслідок пошкодження нервів. Це пошкодження викликає порушення функції периферичної або центральної нервової системи. Невропатичний біль може мати центральне походження, наприклад, внаслідок пошкодження або інфаркту головного мозку, або бути периферичним невропатичним болем, таким як ішіалгія внаслідок хребетної грижі. - Ідіопатичний біль: є больовим синдромом, причини якого слабо пояснені. Тести є нормальними, але біль присутній. Такий біль присутній у пацієнтів, що проявляють, наприклад, функціональні синдроми, такі як фіброміалгія або синдром подразненої кишки. - Психогенний біль: є болем психологічного походження (симптомокомплекс, викликаний втратою близької людини, депресією, травмою і т. д.). Зокрема, він є хронічним болем, обумовленим депресією. Біль іноді має змішане походження: ноцицептивне і запальне, як, наприклад, при раках. Анальгетиками або болезаспокійливими засобами є лікарські засоби, вживані для полегшення болю. Всесвітньою Організацією Охорони Здоров'я (ВОЗ) вони можуть бути класифіковані на три рівні: - Рівень 1 складається з неопіоїдних анальгетиків (парацетамолу, протизапальних лікарських засобів). Їх застосовують для слабкого або помірного болю; - Рівень 2 включає слабкі опіоїди (наприклад, кодеїн). Їх застосовують при болі від помірного до важкого ступеня або в тих випадках, коли болезаспокійливі засоби рівня 1 були неефективні для купірування болю; - Рівень 3 складається з сильних опіоїдів (наприклад, морфіну). Ці лікарські засоби застосовують для гострого болю або в тих випадках, коли анальгетики рівня 2 були неефективні для купірування болю. Для лікування певного болю також застосовують інші класи лікарських засобів, такі як нейролептики або антидепресанти для невропатичного болю або триптани для головних болів за типом мігрені. Необхідність в пошуку нових терапевтичних засобів для лікування болю неминуча з урахуванням обмеженої ефективності або побічних ефектів сучасних терапевтичних засобів, незалежно від рівня анальгетика ВОЗ, типу або походження болю. Наприклад, анальгетики рівня I згідно ВОЗ, що включають серед іншого парацетамол, аспірин, нестероїдні протизапальні лікарські препарати (НСПЗЛ) та інгібітори циклооксигенази, як правило, неефективні проти інтенсивного болю, але добре переносяться, хоча можуть зустрічатися несприятливі шлункові ефекти. Проте, селективні інгібітори циклооксигенази типу 2, такі як рофекоксиб (Vioxx®), показали серйозні серцево-судинні ризики. Опіати, такі як морфін та його похідні, ефективні відносно певних гострих болів або важкого хронічного болю, але можуть викликати сонливість, нудоту і блювоту на початку лікування, а потім констипацію або пригноблення дихання при передозуванні. Повторне або хронічне застосування опіатів може привести до толерантності до анальгезуючого ефекту, при якій потрібні вищі дози, близькі до токсичних доз, залежності і синдрому відміни при перерві в лікуванні. Опіати та їх похідні не дуже ефективні відносно невропатичного болю і хронічного болю від низької до помірної інтенсивності. Протеїнкінази є ферментами, що відіграють ключову роль в перетворенні клітинного сигналу. Вони залучені, наприклад, в такі фізіологічні процеси, як проліферація, мітоз, диференціювання, клітинна інвазія, рухливість і апоптоз клітин. 1 UA 116107 C2 5 10 15 20 25 30 35 40 45 50 55 Порушення регуляції фізіологічних механізмів, контрольованих протеїнкіназами, є центральним фактором для виникнення і розвитку багатьох патологій, зокрема, що включають раки і біль. Особливий інтерес в контексті винаходу представляють рецепторні тирозинкінази з тропоміозин-споріднених кіназ (Trk; від англ. "tropomyosine-related kinases"), асоційовані з гострим або хронічним болем. Trk є рецепторними тирозинкіназами, які залучені в розвиток нервової системи. Сімейство рецепторів Trk складається з трьох членів TrkA, TrkB і TrkC, що активуються специфічними лігандами, званими нейротрофінами. Описано, що білки Trk і асоційовані з ними ліганди відіграють роль при розвитку болю (Sah et al. 2003 Nat Rev Drug Discovery. 2:460-472). Наприклад, мутації в гені рецептора TrkA описані у пацієнтів з природженою нечутливістю до болю (Indo et al., 1996, Nat Genet. 13: 485-488; Indo et al., 2001, Hum Mutations, 18: 308-318). TrkA експресується в ноцицептивних нейронах, тобто в нейронах, які передають больові сигнали, і впливає на електрофізіологічні властивості натрієвих каналів, залучених в передачу больових сигналів (Fang et al., J. Neurosci. 25: 4868-4878). В декількох оглядових статтях висвітлена роль TrkA та його ліганда, що є фактором росту нервів (NGF; від англ. "Nerve growth Factor"), при ініціації болю на рівні ноцицептивних нейронів, зокрема, при запальних больових станах, наприклад, при ревматичних захворюваннях, таких як остеоартрит, біль в нижній частині спини, люмбальна хребетна грижа і здавлення нервових корінців (Hefti et al., 2006; Trends Pharmacol Sci. 27:85-91; Pezet and Mcmahon, 2006, Ann Rev Neurosci. 29:507-538; Cheng and Ji, 2008, Neurochem Res. 33:1970-1978; Seidel et al. 2010, Semin Arthritis Rheum. 40:109-126). TrkB або його ліганд, що є нейротрофічним фактором головного мозку (BDNF; від англ. "Brain-derived Neurotrophic factor"), також залучений в хронічний біль. BDNF синтезується в первинних сенсорних нейронах і антероградно транспортується в центральні закінчення первинних аферентів в спинному мозку (Obata et al., 2006, Neurosci Res. 55: 1-10). BDNF, що синтезується мікроглією в спинному мозку, викликає зсув в нейрональному аніонному градієнті, що приводить до розгальмування передачі болю після пошкодження нервів (Coull et al., 2005, Nature, 438: 1017-1021). Цей результат вказує на те, що блокування біохімічного шляху BDNF/TrkB корисно для лікування невропатичного болю. Супраспінальний BDNF також відіграє роль при знятті болю (Guo et al., 2006, J Neurosci. 26: 126-137). Підвищена сироваткова концентрація BDNF також описана при фіброміалгії (Laske et al., 2006, J Psychiatric Res, 41: 600605). Зроблений огляд ролі передачі сигналу BDNF/TrkB при модуляції болю (Merighi et al., 2008 85: 297-317). Блокування біохімічного шляху TrkA або TrkB може бути досягнуте за рахунок розчинних рецепторів Trk або нейтралізуючих антитіл. Такі стратегії оцінені для біохімічного шляху NGF/TrkA у тварин, де вони зменшували біль, обумовлений раком кістки (Sevcik et al., 2005, Pain 115: 128-141), або незапальний біль в суглобах (Mcnamee et al., 2010 Pain 149:386-392). Танезумаб, що є рекомбінантним гуманізованим моноклональним антитілом проти NGF, в даний час випробовують як терапевтичний засіб у людей для лікування гострого і хронічного болю, обумовленого декількома станами (Cattaneo, 2010, Curr Opin Mol Ther 12: 94-106). Проте, такий терапевтичний засіб необхідно вводити за допомогою повторних внутрішньовенних інфузій. Дуже бажані інші форми лікування, такі як низькомолекулярні інгібіторні молекули Trk з пероральною біодоступністю. Число інгібіторів Trk, описаних в літературі, обмежене, і до цих пір їх ще не застосовують як лікарський засіб проти болю, хоча для інгібіторів Trk вже продемонстрована анальгезуюча ефективність в експериментальних доклінічних моделях, зокрема, в моделях болю при раку кістки (Ghilardi et al. 2010, Mol Pain 6: 87) і хронічного запального болю (Winckler et al. 2009, 8th International Association for the Study of Pain Research Symposium, Poster # 348). Таким чином, існує необхідність в сполуках, здібних до інгібування Trk. Стаття Wang et al. (Expert Opin. Ther. Patents 2009, 19(3), 305-319) є оглядом заявок на патенти з 2002 року, що відносяться до інгібіторів Trk та до їх застосування при лікуванні раку і болю. Жодна з розкритих сполук не відповідає сполуці азаіндазолу або діазаіндазолу. У WO 2008/112695 розкриті сполуки типу 5-азаіндазолу або 5,7-діазаіндазолу, заміщеного в положенні 6, як інгібітори протеїнкіназ, таких як Trk. Проте, в даній заявці відсутній біологічний результат, що доводить інгібування яких-небудь протеїнкіназ і, зокрема, протеїнкінази Trk. Крім того, в даній заявці ніде не вказано, що ці сполуки можуть лікувати або попереджувати біль. У WO 2004/113303 розкриті, зокрема, сполуки типу 5-азаіндазолу, заміщеного в положенні 6, як інгібітори протеїнкінази JNK. Ніде не згадано, що такі сполуки могли б також інгібувати протеїнкіназу Trk. 2 UA 116107 C2 5 10 15 У WO 2007/023110 розкриті, зокрема, сполуки типу азаіндазолу або діазаіндазолу як інгібітори протеїнкінази p38. Ніде не згадано, що такі сполуки могли б також інгібувати протеїнкіназу Trk. У WO 2008/089307 розкриті сполуки типу азаіндазолу або діазаіндазолу як інгібітори активності ∆5-десатурази. Ніде не згадано, що такі сполуки могли б також інгібувати протеїнкіназу Trk. Сполуки за даним винаходом мають властивість інгібування або модуляції ферментативної активності білків Trk. Отже, ці сполуки можна застосовувати як лікарські засоби при лікуванні або попередженні болю, зокрема, болю, що асоціюється щонайменше з одним білком Trk. Крім того, сполуки згідно винаходу представляють особливий інтерес, якщо автори винаходу зуміли показати, що вони інгібують або модулюють активність більше ніж одного білка Trk. Таким чином, вони дають можливість лікувати одночасно болі декількох етіологій (наприклад, поєднання запальних і ноцицептивних болів, що спостерігають у разі раку). Таким чином, конкретніше об'єктом даного винаходу є сполука наступної загальної формули (I): R2 R1 U n V N Y2 Y3 20 25 30 35 40 45 R3 Y1 N Y4 N H (I) або її фармацевтично прийнятна сіль або сольват, її таутомер, її стереоізомер або суміш стереоізомерів в будь-яких співвідношеннях, така як суміш енантіомерів, зокрема, рацемічна суміш, де: - Y1 і Y4 кожен позначає, незалежно один від одного, групу CH або атом азоту, - Y2 позначає атом азоту, або групу CH або C-X-Ar, - Y3 позначає атом азоту, або групу C-X-Ar або C-W, за умови, що: щонайменше одна і максимум дві групи Y1, Y2, Y3 і Y4 позначають атом азоту, Y2 і Y4 не можуть позначати атом азоту одночасно, коли Y2=C-X-Ar, Y3 позначає атом азоту або групу C-W, і коли Y2=CH або N, Y3 позначає групу C-X-Ar, - Ar позначає арильну або гетероарильну групу, необов'язково заміщену однією або більше груп, вибраних з атома галогену, (C1-C6)алкілу, (C1-C6)галогеналкілу, (C1-C6) галогеналкокси, (C1-C6)галогентіоалкокси, CN, NO2, OR11, SR12, NR13R14, CO2R15, CONR16R17, SO2R18, SO2NR19R20, COR21, NR22COR23, NR24SO2R25 и R26NR27R28, та/або що необов'язково конденсовану з гетероциклом, - X позначає двовалентну групу, вибрану з O, S, S(O), S(O)2, NR4, S(NR4), S(O)(NR4), S(O)2(NR4), NR4S, NR4S(O), NR4S(O)2, CH2, CH2S, CH2S(O), CH2S(O)2, SCH2, S(O)CH2, S(O)2CH2, CH2CH2, CH=CH, CC, CH2O, OCH2, NR4CH2 і CH2NR4, - W позначає групу R5, SR5, OR5 або NR5R6, - U позначає групу CH2 або NH, один або більше атомів водню якої можуть бути заміщені (C1-C6)алкільною групою, - V позначає C(O), C(S) або CH2, - n дорівнює 0 або 1, - R1 позначає атом водню, або групу OR7 або NR7R8, - R2 позначає атом водню, необов'язково заміщений гетероцикл, NO2, OR9 або NR9R10, - R3, R4, R11-R25 і R27-R28 кожен позначає, незалежно один від одного, атом водню або (C1C6)алкільну групу, - R5 і R6 кожен позначає, незалежно один від одного, атом водню або (C1-C6)алкіл, необов'язково заміщену арильну або необов'язково заміщену бензильну групу, 3 UA 116107 C2 5 10 - R7, R8, R9 і R10 кожен позначає, незалежно один від одного, атом водню або необов'язково заміщену (C1-C6)алкільну або (C3-C12)циклоалкільну групу або необов'язково заміщений гетероцикл, і - R26 позначає (C1-C6)алкіл, вживана при лікуванні або попередженні болю, зокрема, болю, що асоціюється щонайменше з одним білком Trk. У наведених вище визначеннях всі комбінації заступників або змінних можливі, якщо вони приводять до стабільних сполук. Крім того, слід зазначити, що щонайменше один, але тільки один з Y2 і Y3 позначає групу CX-Ar. У переважному втіленні винаходу об'єктом даного винаходу є сполука наступної загальної формули (I): R2 R1 U n V N Y2 Y3 15 20 25 30 35 40 45 R3 Y1 N Y4 N H (I) або її фармацевтично прийнятна сіль або сольват, її таутомер, її стереоізомер або суміш стереоізомерів в будь-яких співвідношеннях, така як суміш енантіомерів, зокрема, рацемічна суміш, де: - Y1 і Y4 кожен позначає, незалежно один від одного, групу CH або атом азоту за умови, що щонайменше один з Y1 і Y4 позначає атом азоту, - Y2 позначає групу C-X-Ar, - Y3 позначає групу C-W, - Ar позначає арильну або гетероарильну групу, необов'язково заміщену однією або більше груп, вибраних з атома галогену, (C1-C6)алкілу, (C1-C6)галогеналкілу, (C1-C6) галогеналкокси, (C1-C6)галогентіоалкокси, CN, NO2, OR11, SR12, NR13R14, CO2R15, CONR16R17, SO2R18, SO2NR19R20, COR21, NR22COR23, NR24SO2R25 і R26NR27R28, та/або необов'язково конденсовану з гетероциклом, - X позначає двовалентну групу, вибрану з O, S, S(O), S(O)2, NR4, S(NR4), S(O)(NR4), S(O)2(NR4), NR4S, NR4S(O), NR4S(O)2, CH2, CH2S, CH2S(O), CH2S(O)2, SCH2, S(O)CH2, S(O)2CH2, CH2CH2, CH=CH, CC, CH2O, OCH2, NR4CH2 і CH2NR4, - W позначає групу R5, SR5, OR5 або NR5R6, - U позначає групу CH2 або NH, один або більше атомів водню якої можуть бути заміщені (C1-C6)алкільною групою, - V позначає C(O), C(S) або CH2, - n дорівнює 0 або 1, - R1 позначає атом водню, або групу OR7 або NR7R8, - R2 позначає атом водню, необов'язково заміщений гетероцикл, NO2, OR9 або NR9R10, - R3, R4, R11-R25 і R27-R28 кожен позначає, незалежно один від одного, атом водню або (C1C6)алкільну групу, - R5 і R6 кожен позначає, незалежно один від одного, атом водню або (C1-C6)алкіл, необов'язково заміщену арильну або необов'язково заміщену бензильну групу, - R7, R8, R9 і R10 кожен позначає, незалежно один від одного, атом водню або необов'язково заміщену (C1-C6)алкільну або (C3-C12)циклоалкільну групу, або необов'язково заміщений гетероцикл, і - R26 позначає (C1-C6)алкільну групу, вживана при лікуванні або попередженні болю. Термін "атом галогену" відноситься до атома фтору, хлору, брому або йоду. Термін "(C1-C6)алкіл" відноситься до насичених нормальних або розгалужених вуглеводневих ланцюгів, що містять від 1 до 6 атомів вуглецю. Він може бути метильною, 4 UA 116107 C2 5 10 15 20 25 30 35 40 45 50 55 60 етильною, пропільною, ізопропільною, бутильную, ізобутильною, втор-бутильною, третбутильною, пентильною або гексильною групою. Термін "(C1-C6)алкокси" відноситься до (C1-C6)алкільного ланцюга, пов'язаного з іншою частиною молекули через атом кисню. Як приклад можна згадати метокси, етокси, пропокси, ізопропокси, бутокси або трет-бутоксигрупи. Термін "(C1-C6)тіоалкокси" відноситься до (C1-C6)алкільного ланцюга, пов'язаного з іншою частиною молекули через атом сірки. Як приклад можна згадати тіометокси, тіоетокси, тіопропокси, тіоізопропокси, тіобутокси або тіо-трет-бутоксигрупи. Термін "(C1-C6)галогеналкіл" відноситься до (C1-C6)алкільного ланцюга, як визначено вище, де один або більше атомів водню заміщено атомом галогену, як визначено вище. Він може бути, зокрема, тіофторметильною групою. Термін "(C1-C6)галогеналкокси" відноситься до ланцюга (C1-C6)алкокси, як визначено вище, де один або більше атомів водню заміщено атомом галогену, як визначено вище. Він може бути, зокрема, тіофторметоксигрупою. Термін "(C1-C6)галогентіоалкокси" відноситься до ланцюга (C1-C6)тіоалкокси, як визначено вище, де один або більше атомів водню заміщено атомом галогену, як визначено вище. Він може бути, зокрема, тіофтортіометокси групою. Термін "(C3-C12)циклоалкіл" відноситься до циклічних вуглеводневих систем, що містять від 3 до 12 атомів вуглецю і що містить одне або більше кілець, зокрема, конденсованих кілець. Як приклад можна згадати адамантильну або циклогексильну групу. Термін "арил" відноситься до ароматичної вуглеводневої групи, що переважно містить від 6 до 14 атомів вуглецю і що містить одне або більше конденсованих кілець, таку як, наприклад, фенільна або нафтильна група. Переважно він є фенільною групою. Термін "гетероарил" відноситься до циклічної ароматичної групи, що містить від 5 до 7 атомів, включених в кільце, або до біциклічної ароматичної групи, що містить від 8 до 11 атомів, включених в кільця, де від 1 до 4 атомів, включених в кільця, є гетероатомом, незалежно вибраним з атомів сірки, азоту і кисню, і де інші атоми, включені в кільця, є атомами вуглецю. Приклади гетероарильних груп включають фурильні, тієнільні, піридинільні і бензотієнільні групи. Термін "гетероцикл" відноситься або до стабільного моноциклу, що містить від 4 до 7 циклічних атомів, або до стабільного біциклу, що містить від 8 до 11 циклічних атомів, який може бути або насиченим, або ненасиченим, де від 1 до 4 циклічних атомів є гетероатомом, незалежно вибраним з атомів сірки, азоту та кисню, і де іншими циклічними атомами є атоми вуглецю. Як приклад можна згадати фуран, пірол, тіофен, тіазол, ізотіазол, оксадіазол, імідазол, оксазол, ізоксазол, піридин, піперидин, піразин, піперазин, тетрагідропіран, піримідин, хіназолін, хінолін, хіноксалін, бензофуран, бензотіофен, індолін, індолізин, бензотіазол, бензотієніл, бензопіран, бензоксазол, бензо[1,3]діоксол, бензізоксазол, бензімідазол, хроман, хромен, дигідробензофуран, дигідробензотієніл, дигідроізоксазол, ізохінолін, дигідробензо[1,4]діоксан, імідазо[1,2-a]піридин, фуро[2,3-c]піридин, 2.3-дигідро-1H-інден, [1,3]діоксоло[4,5-c]піридин, піроло[1,2-c]піримідин, піроло[1,2-a]піримідин, тетрагідронафталін, бензо[b][1,4]оксазин. У контексті даного винаходу "необов'язково заміщений" означає, що обговорювана група необов'язково заміщена одним або більше заступниками, які можуть бути вибрані, зокрема, з атома галогену, (C1-C6)алкілу, (C1-C6)галогеналкілу, (C1-C6)галогеналкокси, (C1-C6) галогентіоалкокси, CN, NO2, OR11, SR12, NR13R14, CO2R15, CONR16R17, SO2R18, SO2NR19R20, COR21, NR22COR23, NR24SO2R25 і R26NR27R28, де R11-R28 є такими, як визначено вище. У даному винаході "фармацевтично прийнятний" відноситься до того, що корисно при одержанні фармацевтичної композиції, що є в цілому безпечною, нетоксичною та ні біологічно, ні інакше небажаною, а також прийнятною для ветеринарного і медичного фармацевтичного застосування. "Фармацевтично прийнятна сіль або сольват" сполуки відноситься до солей і сольватів, що є фармацевтично прийнятними, як визначено в даному описі, і що має бажану фармацевтичну активність початкової сполуки. Прийнятні солі для терапевтичного застосування сполук за даним винаходом включають традиційні нетоксичні солі сполук за винаходом, таких як солі, утворені з фармацевтично прийнятних органічних або неорганічних кислот або з фармацевтично прийнятних органічних або неорганічних основ. Як приклад можна згадати солі, утворені з неорганічних кислот, таких як соляна кислота, бромисто-воднева кислота, фосфорна кислота і сірчана кислота, і солі, утворені з органічних кислот, таких як оцтова кислота, трифтороцтова кислота, пропіонова кислота, янтарна кислота, фумарова кислота, яблучна кислота, винна кислота, лимонна кислота, аскорбінова кислота, малеїнова кислота, глутамінова кислота, бензойна кислота, 5 UA 116107 C2 5 10 15 20 25 30 35 40 45 50 55 60 саліцилова кислота, толуолсульфонова кислота, метансульфонова кислота, стеаринова кислота і молочна кислота. Як приклад можна згадати солі, утворені з неорганічних основ, таких як сода, поташ або гідроксид кальцію, і солі, утворені з органічних основ, таких як лізин або аргінін. Ці солі можна синтезувати із сполук за винаходом, що містять основну або кислотну частину, і відповідних кислот або основ відповідно до традиційних хімічних способів, добре відомих фахівцям в даній області техніки. Прийнятні сольвати для терапевтичного застосування сполук за даним винаходом включають традиційні сольвати, такі як сольвати, утворені на останній стадії одержання сполук за винаходом за рахунок присутності розчинників. Як приклад можна згадати сольвати, утворені за рахунок присутності води або етанолу. У контексті даного винаходу "стереоізомер" відноситься до геометричного ізомеру або до оптичного ізомеру. Геометричні ізомери утворюються в результаті різного положення заступників на подвійному зв'язку і можуть, таким чином, мати Z або E конфігурацію. Оптичні ізомери утворюються, зокрема, в результаті різного положення в просторі заступників на атомі вуглецю, що містить чотири різних заступника. Цей атом вуглецю складає, таким чином, хіральний або асиметричний центр. Оптичні ізомери включають діастереоізомери і енантіомери. Оптичні ізомери, що є дзеркальними відображеннями один одного, але що не накладаються один на одного, є енантіомери. Оптичні ізомери, що не є дзеркальними відображеннями один одного, є діастереоізомерами. У контексті даного винаходу "таутомер" відноситься до структурного ізомеру сполуки, одержаної в результаті прототропії, тобто в результаті міграції атома водню і зміни положення подвійного зв'язку. Різні таутомери сполуки, як правило, взаємно перетворювані і знаходяться в рівновазі в розчині в співвідношеннях, які можуть варіювати відповідно до використовуваного розчинника, температури або pH. Згідно першому втіленню винаходу Y4=n. Переважно Y2=C-X-Ar, і Y3 переважно позначає групу C-W. Зокрема: - Y1=CH або N, і переважно CH, - Y2=C-X-Ar, - Y3=C-W, і - Y4=N. Згідно другому втіленню винаходу Y1 та/або Y4 позначає атом азоту. В даному випадку Y2 і Y3 переважно позначає не атом азоту. Зокрема: - Y1 та/або Y4=N, - Y2=CH або C-X-Ar, і - Y3=C-W або C-X-Ar. Зокрема: - Y1 позначає групу CH, - Y4 позначає атом азоту, - Y2 позначає групу CH або C-X-Ar, і - Y3 позначає групу C-X-Ar або C-W, за умови, що: коли Y2=C-X-Ar, Y3 позначає групу C-W, і коли Y2=CH, Y2 позначає групу C-X-Ar. Переважно X позначає двовалентну групу, вибрану з O, S, S(O), S(O)2, NR4, CH2, CH2S, CH2S(O), CH2S(O)2, NHS(O)2, SCH2, S(O)CH2, S(O)2CH2, S(O)2NH, CH2CH2, CH=CH, CC, CH2O, OCH2, NR4CH2 і CH2NR4. Зокрема, X позначає двовалентну групу, вибрану з S, S(O), S(O)2, NR4, CH2, CH2S, CH2S(O), CH2S(O)2, NHS(O)2, SCH2, S(O)CH2, S(O)2CH2, S(O)2NH, CH2CH2, CC, CH2O, OCH2, NR4CH2 і CH2NR4. Більш конкретно X може бути вибраний з S, S(O), S(O)2, CH2, CH2S, CH2S(O), CH2S(O)2, NHS(O)2, SCH2, S(O)CH2, S(O)2CH2, S(O)2NH, CH2CH2, CH=CH і CC. Зокрема, X може бути вибраний з S, S(O)2, CH2, SCH2, S(O)2CH2, S(O)2NH, CH2S, CH2S(O)2, NHS(O)2, CH2CH2 і CC. X може бути, зокрема, выбраний з S, S(O), S(O)2, NR4, CH2, SCH2, S(O)CH2, S(O)2CH2, S(O)2NH, CH2CH2, CC, OCH2 и NR4CH2; зокрема, з S, S(O)2, CH2, SCH2, S(O)2CH2, S(O)2NH, CH2CH2 і CC, де перший атом цих груп з'вязаний з атомом C ланцюга C-X-Ar. 6 UA 116107 C2 5 10 15 X може позначати, зокрема, S, S(O)2, SCH2, S(O)2CH2, S(O)2NH, CH2S, CH2S(O)2 або NHS(O)2, і, зокрема, S, S(O)2, SCH2, S(O)2CH2 або S(O)2NH, де перший атом цих груп з'вязаний з атомом C ланцюга C-X-Ar. Переважно Ar позначає гетероарильну групу, таку як піридин, або арильну групу, таку як феніл, необов'язково заміщену однією або більше груп, вибраних з атома галогену (C1C6)алкілу, (C1-C6)галогеналкілу, (C1-C6)галогеналкокси, (C1-C6)галогентиоалкокси, CN, NO2, OR11, SR12, NR13R14, CO2R15, CONR16R17, SO2R18, SO2NR19R20, COR21, NR22COR23 і NR24SO2R25; та/або необов'язково конденсовану з гетероциклом. Конкретніше Ar може бути арильною групою, такою як феніл, необов'язково заміщеною однією або більше груп, вибраних з атома галогену, (C1-C6)алкілу, (C1-C6)галогеналкілу, (C1C6)галогеналкокси, (C1-C6)галогентиоалкокси, CN, NO2, OR11, SR12, NR13R14, CO2R15, CONR16R17, SO2R18, SO2NR19R20, COR21, NR22COR23 і NR24SO2R25. Ar може, зокрема, бути арильною групою, такою як феніл, необов'язково заміщений однією або більше груп, вибраних з атома галогену, (C1-C6)алкілу, (C1-C6)галогеналкілу і CONR16R17, і, зокрема, з атома галогену, такого як атом фтору, (C1-C6)алкілу, такого як метил, і CONR16R17, такого як CONH2. Ar може також бути піридиновою групою. Ar може бути, зокрема, вибраний з наступних груп: Cl F F , , , , , Cl H 2N O 20 Cl , зокрема, з наступних груп: CF3 , Cl і , Cl F N , Cl H 2N O F , , Cl CF3 , Cl , N , зокрема, з наступних груп: Cl F H 2N O 25 Cl F , , Ar може переважно бути групою: і . . 7 , і UA 116107 C2 5 10 15 20 25 W може переважно позначати групу R5, SR5, OR5 або NR5R6, і переважно R5, OR5 або NR5R6, де R5 і R6 позначають, незалежно один від одного, атом водню або (C1-C6)алкільну групу. W може позначати, зокрема, H, OMe, Me, OH або NH2, і, зокрема, H. Переважно R3 позначає атом водню. U може позначати більш конкретно групу CH2 або NH. Переважно n може дорівнювати 0. V може позначати більш конкретно групу C(O) або C(S), і переважно групу C(O). Згідно конкретному втіленню винаходу: - R3=H, - U=CH2 або NH, - V=C(O) або C(S), і, зокрема, C(O), і - n=0 або 1, і, зокрема, 0. Згідно іншому конкретному втіленню винаходу: - V=C(O) або C(S), і, зокрема, C(O), і - n=0. Згідно іншому конкретному втіленню винаходу: - R3=H, - V=C(O) або C(S), і, зокрема, C(O), і - n=0. R1 може позначати більш конкретно атом водню або групу NR7R8, де R7, зокрема, позначає атом водню, а R8, зокрема, позначає необов'язково заміщену (C3-C12)циклоалкільну групу або необов'язково заміщений гетероцикл. (C3-C12)циклоалкільна група може бути, зокрема, циклогексилом. Вона може бути заміщена одним або більше атомів галогену. Ця група може, зокрема, бути групою: . Гетероциклічна група може бути, зокрема, тетрагідропіраном, зокрема, незаміщеним. Таким чином, вона може бути наступною групою: . R1 може, таким чином, бути більш конкретно однією з наступних груп: 30 35 H, і ; і, зокрема, H і ; і переважно . R2 може позначати більш конкретно необов'язково заміщений гетероцикл (зокрема, заміщений (C1-C6)алкілом або NH2), NO2 або NR9R10, де, зокрема, R9=R10=H або інакше R9 і R10 кожний позначає H або необов'язково заміщений (C1-C6)алкіл. R2 може позначати, зокрема, необов'язково заміщений гетероцикл, зокрема, заміщений (C1C6)алкілом або NH2. Гетероцикл може бутити, зокрема, гетероциклом з 5 або 6 членами, що включають щонайменше один атом азоту, і, зокрема, один або два. Гетероцикл може бути, таким чином, вибраний з піперазину, піперидину і піролідину. R2 може, зокрема, позначати одну з наступних груп: 8 UA 116107 C2 NH2, NH(CH2)3NMe2, NMe(CH2)3NMe2, NO2, , і ; і, зокрема, NH2, NO2, , і ; і, зокрема, 5 і ; і більш конкретно . Сполуки за даним винаходом можуть бути вибрані із сполук, перелічених в наступній таблиці: 14-2 14-10 14-11 15 26-4 26-8 27 27-1 28 29 9 UA 116107 C2 29-a 30 30-1 30-3 O O HN HN 30-4 30-5 F S N MeO F F F O 30-8 O HN S O HN O HN 30-9 N N N H N N 30-10 30-11 30-12 30-a 31 32 10 N N H N N UA 116107 C2 32-1 33 35 26-12 30-69 27-2 27-3 27-4 30-73 14біс 30-70 30-71 30-72 27-5 11 UA 116107 C2 30-13 30-14 30-15 30-16 30-17 30-18 30-19 30-20 30-21 30-22 30-23 30-24 30-25 30-26 12 UA 116107 C2 30-27 30-28 30-29 30-30 30-31 30-32 30-33 30-34 30-35 30-36 30-37 30-38 30-39 30-40 13 UA 116107 C2 30-41 30-42 30-43 30-44 30-45 30-46 30-47 30-48 30-49 30-50 30-51 30-52 14 UA 116107 C2 30-53 30-54 30-55 30-56 30-57 30-58 30-59 30-60 30-61 30-62 30-63 30-64 30-65 30-66 15 UA 116107 C2 30-67 30-68 31-1 5 10 15 20 25 30 35 40 Даний винахід також відноситься до застосування сполуки формули (I), як визначено вище, для одержання лікарського засобу, зокрема, призначеного для лікування або попередження болю, зокрема, болю, що асоціюється щонайменше з одним білком Trk. Даний винахід також відноситься до способу лікування або попередження болю, зокрема, болю, що асоціюється щонайменше з одним білком Trk, що включає введення людині, що потребує цього, ефективної дози сполуки формули (I), як визначено вище. Даний винахід також відноситься до фармацевтичної композиції, що містить щонайменше одну сполуку формули (I), як визначено вище, і щонайменше один фармацевтично прийнятний ексципієнт, вживану при лікуванні або попередженні болю, зокрема, болю, що асоціюється щонайменше з одним білком Trk. Фармацевтичні композиції, вживані при лікуванні або попередженні болю, зокрема, болю, що асоціюється щонайменше з одним білком Trk, згідно винаходу можна включати в препарати, зокрема, для перорального введення або для ін'єкції, де дані композиції призначені для ссавців, включаючи людей. Активний інгредієнт можна вводити в стандартних дозованих формах введення в суміші із стандартними фармацевтичними носіями, тваринам або людям. Сполуки за винаходом як активні інгредієнти можна застосовувати в дозах, що знаходяться в діапазоні від 0,01 мг до 1000 мг на добу, що даються в одноразовій дозі один раз на добу або що вводиться в декількох дозах протягом доби, наприклад, двічі на добу в рівних дозах. Доза, що вводиться на добу, переважно складає від 5 мг до 500 мг, ще переважніше від 10 мг до 200 мг. Може бути необхідним введення доз, що знаходяться поза цими діапазонами, як визначено фахівцями в даній області техніки. Фармацевтичні композиції, вживані при лікуванні або попередженні болю, зокрема, болю, що асоціюється щонайменше з одним білком Trk, згідно винаходу можуть додатково містити щонайменше один інший активний інгредієнт, такий як, наприклад, протираковий засіб. Об'єктом даного винаходу також є фармацевтична композиція, вживана при лікуванні або попередженні болю, зокрема, болю, що асоціюється щонайменше з одним білком Trk, що містить: a) щонайменше одну сполуки формули (I), як визначено вище, і b) щонайменше один інший активний інгредієнт, такий як протираковий засіб, у вигляді комбінованого препарату для одночасного, окремого або послідовного застосування. У контексті винаходу термін "лікування" означає усунення або полегшення болю. Термін "біль" згідно винаходу означає будь-який вид болю, зокрема, ноцицептивний біль, запальний біль, невропатичний біль, ідіопатичний біль або психогенний біль, переважно запальний або невропатичний біль. Біль згідно винаходу може бути комбінацією двох або більше цих видів болю, наприклад, комбінацію між запальним і ноцицептивним болем. Біль відповідно до винаходу може мати будь-яке походження. У втіленні винаходу біль відповідно до винаходу є наслідком раку, наприклад, раку кістки. В іншому втіленні винаходу біль відповідно до винаходу є наслідком пошкодження нервів, яке зустрічається, наприклад, при невропатичному болі. В іншому втіленні винаходу біль відповідно до винаходу є наслідком запального стану, який зустрічається, наприклад, при ревматичних захворюваннях, таких як остеоартрит, біль в нижній частині спини, люмбальна хребетна грижа і здавлення нервових 16 UA 116107 C2 5 10 15 20 25 корінців. В іншому втіленні винаходу біль відповідно до винаходу обумовлений функціональними розладами, такими як, наприклад, фіброміалгія. Згідно винаходу "білок Trk" означає будь-який член сімейства Trk, наприклад, TrkA (зокрема, описаний в GenBank під номером AB019488), TrkB (зокрема, описаний в GenBank під номером AAB33109.1) і TrkC (зокрема, описаний в GenBank під номером CAA12029.1), переважно TrkA. Білок Trk відповідно до винаходу може знаходитися в його нативній формі або в модифікованій формі. Під "модифікованою формою" мають на увазі мутовану форму білка дикого типу. Мутація може бути точковою мутацією, а також може бути делецією або інсерцією однієї або більше амінокислот в послідовності білка Trk. Альтернативно модифікований білок Trk відповідно до винаходу може бути злитим білком, наприклад, одержаним після хромосомної перебудови. Модифікований білок Trk може бути також результатом альтернативного сплайсингу. Відповідно до винаходу мають на увазі, що вираз "асоційований щонайменше з одним білком Trk" означає, що біль, який підлягає лікуванню, ретранслюється біохімічними шляхами передачі сигналу, які йдуть через один або більше білків Trk. Зокрема, біль вважають асоційованим з білком Trk, коли він є запальним або невропатичним болем. Біохімічні шляхи передачі сигналу Trk добре відомі фахівцям в даній області техніки. Сполуки згідно винаходу мають властивість інгібування або модуляції ферментативної активності одного або більше білків Trk, переважно більше одного білка Trk. Мають на увазі, що інгібування або модуляція активності одного або більше білків Trk згідно винаходу означає, що сполука згідно винаходу здатна модулювати активацію щонайменше одного білка Trk, що призводить в результаті до зниження, можливо, до інактівації біохімічного шляху передачі сигналу Trk, яка, у свою чергу, приводить в результаті до зменшення відчуття болю. Сполуки згідно винаходу дають можливість, наприклад, зниження активності білка Trk приблизно на 5% або більше, зокрема, приблизно на 10% або більше, зокрема, приблизно на 50% або більше. Сполуки формули (I) згідно даному винаходу можуть бути одержані різними способами, зокрема, стисло викладеними на схемах 1a і 1b нижче. 30 17 UA 116107 C2 5 10 15 20 25 30 35 Спосіб A: Згідно способу A сполуки формули (I) одержують шляхом попереднього синтезу сполук формули (V), що характеризуються галогенованим гетеробіциклічним кільцем, що має екзоциклічний первинний амін. Ці сполуки одержують за допомогою синтезу проміжних сполук загальної формули (II) або (III). Спосіб A1: Спосіб A1, представлений на схемі 2 (йодовані сполуки) або 3 (бромовані сполуки) нижче, описує загальний спосіб одержання сполук загальної формули (V), де W визначений, як в описі загальної формули (I), і, зокрема, як H, (C1-C6)алкіл або арил, і Rj=H або N-захисна група. Схема 2 У контексті схеми 2 необов'язково заміщений 2-хлор-5-йоднікотинонітрил (IIa) одержують з відповідного гідроксинікотинонітрилу шляхом послідовного використання агента йодування, такого як N-йодсукцинімід (NIS), або молекулярного йоду з неорганічною основою, такою як, наприклад, K2CO3 або Na2CO3, зокрема, в полярному розчиннику, такому як гарячий N,Nдиметилформамід (ДМФ), з подальшою обробкою оксихлоридом фосфору, чистим або розведеним в неполярному розчиннику з високою температурою кипіння, або будь-яким іншим еквівалентним агентом хлорування, добре відомим фахівцям в даній області техніки. Температури реакції складають від -20 °C до 200 °C. Потім одержану таким шляхом сполуку (IIa) перетворюють в необов'язково заміщений 5-йод-піразоло[3,4-b]піридин-3-амін (Va) шляхом його взаємодії, переважно при нагріванні, у присутності гідразину, що необов'язково несе N-захисну групу, таку як тритил, трет-бутил або ВОС. Бромовані аналоги загальної формули (V), як описано на схемі 1a, можуть бути одержані шляхом використання способу, описаного в наступних посиланнях: Witherington et al., Bioorg. Med. Chem. Lett., 2003, 13, 1577-1580 і Lijuan Chen et al., Bioorg. Med. Chem. Lett., 2010, 20, 4273-4278. Для зручності ці молекули були одержані шляхом використання послідовності реакцій, представлених на наступній схемі 3. Схема 3 Необов'язково функціоналізований 2-метокси-нікотинонітрил одержують, наприклад, шляхом взаємодії метаноляту натрію в метанолі при температурі від -20 °C до температури кипіння суміші. Альтернативно ця сполука може бути одержана шляхом метилування 2гідроксинікотинонітрилу або іншими способами, описаними вище. Бромування 2-метоксинікотинонітрилу в характерному випадку проводять дибромом в оцтовій кислоті при температурі, що змінюється від 20 °C до 110 °C. Утворення піразолу в характерному випадку 18 UA 116107 C2 5 10 15 20 25 30 35 проводять шляхом взаємодії надлишку гідразину, що несе або не несе функціональну групу, при температурі, що змінюється від 20 °C до 100 °C, у присутності полярного розчинника, такого як вода, етанол, тетрагідрофуран (ТГФ) або будь-який інший розчинник з порівнянними властивостями. Альтернативно також можливе використання гідразину у фізіологічному розчині або в гідратованій формі без розчинника. Спосіб A2: Спосіб A2 відноситься до синтезу функціоналізованих піразолопіразинів, представленому на схемі 4 нижче, де Rj=H або N-захисна група, Hal = атом галогену, і, зокрема, W=H, (C1-C6) алкіл або арил. Схема 4 Необов'язково функціоналізовані 3-аміно-6-йодпіразин-2-карбоксаміди в характерному випадку одержують в дві стадії з відповідних метил-3-амінопіразин-2-карбоксилатів шляхом йодування у присутності N-йодсукциніміду або молекулярного йоду, необов'язково у присутності кофактора, такого як KIO3, AgCO2CF3, Ag2SO4, AlCl3, CuCl2 або HgO, з подальшою реакцією перетворення функціональної групи метилового ефіру в карбоксамід, зокрема, шляхом використання аміаку в полярному розчиннику, такому як вода, метанол або ТГФ, при температурах, що змінюються від 0 °C до 100 °C. Потім карбоксамідну функціональну групу необов'язково функціоналізованого 3-аміно-6-йодпіразин-2-карбоксаміду перетворюють в нітрил шляхом використання агентів дегідратації, таких як, зокрема, CCl4/PPh3, SOCl2, PhSO2Cl, P2O5, TsCl, COCl2, DCC/py (N,N'-дициклогексилкарбодіімід/піридин) або (COCl)2, використовуваних залежно від обставин, можливо, у присутності органічної основи, такої як піридин. Переважний спосіб включає використання оксихлориду фосфору в диметилформаміді (ДМФ). Видалення захисту функціональної групи диметилформімідаміду проводять шляхом обробки кислотою, такою як водна соляна кислота, або іншим реагентом з еквівалентними властивостями. Утворення піразольного кільця здійснюють шляхом реакції Зандмейера, добре відомої фахівцям в даній області техніки, з подальшою взаємодією у присутності гідразину, що несе або не несе функціональну групу, в умовах, описаних в приведених вище способах. Альтернативно діазонієву сіль, що є проміжною сполукою реакції Зандмейера, можна відновлювати шляхом використання, наприклад, хлориду олова в кислому середовищі або іншого еквівалентного агента, з метою утворення функціональної групи гідразину, яка може зазнавати внутрішньомолекулярну циклізацію під дією нагрівання. Спосіб A3: Спосіб A3 націлений на одержання похідних загальної формули (V), що відрізняються змінною функціональною групою в положенні 6 піразолопіридинового біцикла. Це детально описано на схемі 5 нижче. 19 UA 116107 C2 5 10 15 20 25 30 Взаємодія ціанотіоацетаміду з етил-3-етоксиакрилатами, різно заміщеними, згідно способам, описаним, зокрема, Litrivnor et al. у Russ. Chem. Bull., 1999, 48(1), 195-196 і Tsann-long Su et al. у J. Med. Chem., 1988, 31, 1209-1215 дає можливість одержати в дві стадії етил-5-ціано6-(метилтіо)нікотинати, що несуть змінну функціональну групу в положенні 2. Ці синтези в характерному випадку проводять для першої стадії в безводному полярному розчиннику, такому як, наприклад, етанол, при температурі в діапазоні від 0 °C до 70 °C у присутності органічної основи, такої як метилморфолін, триетиламін, DIPEA (N,N-діізопропілетиламін) або DBU (1,8-діазабіцикло[5,4,0]уедец-7-ен). Другу стадію внутрішньомолекулярної циклізації і алкілування в характерному випадку проводять шляхом нагрівання до температури в діапазоні від 20 °C до 100 °C розчину проміжного тіоамідату в полярному розчиннику, наприклад, в етанолі, у присутності відповідного алкілуючого агента, такого як алкілгалогенід або діалкілсульфат. 5-Ціано-6-(метилтіо)нікотинові кислоти, заміщені в положенні 2, в характерному випадку одержують шляхом обмилення відповідних етилових ефірів згідно способам, добре відомим фахівцям в даній області техніки, зокрема, шляхом використання гарячого гідроксиду літію. Декарбоксилювання цих сполук здійснюють шляхом обробки нагріванням в розчиннику з високою температурою кипіння, такому як дифеніловий ефір, при температурі в діапазоні від 150 °C до 250 °C. Реакції галогенування, в основному, націлені на одержання йодованих, бромованих або хлорованих похідних, більш конкретно йодованих похідних. Останні в характерному випадку одержують шляхом обробки молекулярним йодом у присутності солі срібла, такої як, наприклад, Ag2SO4, в полярному розчиннику, такому як етанол, при температурі в діапазоні від 0 °C до 70 °C. Розглянуті також альтернативні способи, зокрема, способи, засновані на інших солях, таких як KIO3, AgCO2CF3, AlCl3, CuCl2 або HgO, або інших йодуючих агентах, таких як Nйодсукцинімід. Можливі способи бромування в характерному випадку засновані на агентах, таких як N-бромсукцинімід або дибром, згідно способам, добре відомим фахівцям в даній області техніки. У випадку, в якому W=OH (у характерному випадку в результаті використання діетил-2(етоксиметилен)малонату), відповідні сполуки захищають за допомогою реакції алкілування. Цю реакцію, зокрема, проводять шляхом використання метилйодиду або бромметану і карбонату срібла в діоксані, ТГФ, ацетонітрилі або ацетоні, або будь-якого еквівалентного агента, такого як диметилсульфат. Одержані 5-галоген-2-(метилтіо)нікотинонітрили піддають окисленню їх функціональної групи тіометокси, в характерному випадку шляхом використання m-CPBA (m 20 UA 116107 C2 5 10 15 20 25 30 35 хлорпербензойної кислоти), оксону або будь-якого іншого еквівалентного агента, що приводить до утворення відповідного сульфоксиду. Ці сполуки, які можуть містити різні кількості відповідного сульфону, вступають в реакцію у присутності необов'язково заміщеного гідразину з утворенням відповідного 5-галоген-піразоло[3,4-b]піридин-3-аміну, що несе змінну функціональну групу в положенні 6. Спосіб A4: Спосіб A4 націлений на одержання похідних загальної формули (V) із сполук загальної формули (III) за допомогою утворення проміжної сполуки для сполуки формули (IV). Ці сполуки в характерному випадку одержують шляхом, представленим на схемі 6. Використовуваний спосіб проілюстрований наступними посиланнями: Gueiffier et al. Heterocycles, 1999, 51(7), 16611667; Gui-dong Zhu et al. Bioorg. Med. Chem., 2007, 15, 2441-2452. Сполуки загальної формули (IIIa), попередньо ацетильовані одним або іншим із способів, добре відомих фахівцям в даній області техніки, піддають дії ізоамілнітриту, нітриту натрію або будь-якого іншого еквівалентного органічного або неорганічного нітриту у воді або в оцтовій кислоті протягом періодів, які в характерному випадку варіюють від 1 до 3 діб, при температурах, що змінюються від 0 °C до 40 °C. Захист одержаних таким шляхом сполук загальної формули (IVa) видаляють в кислих умовах, наприклад, шляхом використання соляної кислоти, після чого піддають дії агентів нітрації, таких як концентрована азотна кислота або нітрат калію, в сірчаній кислоті при температурах, що змінюються від 0 °C до 25 °C. Слід зазначити, що пряме перетворення сполук формули (IIIa) в сполуки (IVb) з видаленим захистом в цілому можливо. Одержані таким шляхом нітропіразоли в характерному випадку відновлюють до амінопіразолів загальної формули (Ve) шляхом використання SnCl2 в соляній кислоті. Альтернативні способи включають використання заліза, цинку або олова в кислих умовах, і способи каталітичної гідрогенізації у присутності комплексів платини, нікелю або Pd/C в атмосфері водню або у присутності еквівалентних агентів, таких як циклогексадієн, циклогексен, боргідрид натрію або гідразин. Спосіб B: Згідно способу B сполуки формули (I) одержують шляхом попереднього синтезу сполук формули (VI), що характеризуються функціоналізованим гетеробіциклічним кільцем, що несе екзоциклічний амін. Ці сполуки одержують за допомогою синтезу проміжних сполук загальної формули (VI). Спосіб B1: Спосіб B1 представлений на схемі 7 нижче, де W, зокрема, позначає H, (C1-C6)алкіл, арил або бензил. 21 UA 116107 C2 5 10 15 20 25 30 35 40 Похідні 3-нітро-6-тіоксо-1,6-дигідропіридин-2-карбонітрилу і 3-нітро-6-тіоксо-1,6дигідропіразин-2-карбонітрилу, необов'язково функціоналізовані в положенні 5, в характерному випадку одержують з відповідних 2,6-дихлор-3-нітропіридинів або 2,6-дихлор-3-нітропіразинів шляхом послідовних взаємодій солі ціаніду, такої як ціанід міді, в полярному розчиннику з високою температурою кипіння, такому як N-метилпіролідон, при температурах в діапазоні від 100 °C до 200 °C; з подальшою взаємодією з водним гідросульфітом натрію в полярному розчиннику. Потім ці сполуки алкілують, наприклад, шляхом використання заміщеного бензилброміду, в основному середовищі згідно способам, добре відомим фахівцям в даній області техніки. Переважний протокол включає використання апротонного і безводного полярного розчинника, такого як ацетон, при його температурі кипіння і органічної основи, такої як піридин, триетиламін або DIPEA, або неорганічної основи, такої як карбонат натрію, калію або кальцію. Реакції відновлення функціональної нітрогрупи в аміні переважно проводять шляхом використання SnCl2 в соляній кислоті. Альтернативні способи включають використання заліза, цинку або олова в кислих умовах і способи каталітичної гідрогенізації у присутності комплексів паладію, нікелю або Pd/C в атмосфері водню або у присутності еквівалентних агентів, таких як циклогексадієн, циклогексен, боргідрид натрію або гідразин. В деяких випадках продукт реакції відновлення на додаток до первинної амінної має карбоксамідну функціональну групу, що утворюється в результаті гідролізу нітрильної функціональної групи. В цьому випадку виділення відповідних 3-амінопіколінонітрилів або 3амінопіразин-2-карбонітрилів може бути виконане шляхом дегідратації карбоксаміду до нітрилу шляхом використання оксихлориду фосфору у присутності ДМФ або будь-якого іншого способу, добре відомого фахівцям в даній області техніки. Нарешті, утворення амінопіразольного кільця проводять переважно шляхом утворення діазонію, одержаного шляхом послідовної взаємодії при низькій температурі ізоамілнітриту, нітриту натрію або іншого еквівалентного органічного або неорганічного нітриту у воді, соляній кислоті, оцтовій кислоті або сірчаній кислоті при температурах, що змінюються від 0 °C до 20 °C, з його подальшим відновленням до гідразину і внутрішньомолекулярною циклізацією, що активується нагріванням реакційної суміші. Реакцію відновлення переважно проводять з хлоридом олова в кислих умовах, але його можна також проводити шляхом каталітичної гідрогенізації або будь-яким іншим способом, добре відомим фахівцям в даній області техніки. В якості альтернативи цієї останньої стадії можливо, щоб проміжний діазоній зазнавав реакцію Зандмейера, в процесі якого ця функціональна група заміщається атомом галогену, таким як атом йоду, шляхом взаємодії адекватної солі, такої як NaI. Якщо даний варіант переважний, утворення амінопіразольного кільця проводять шляхом використання гідразину, що несе або не несе функціональну групу, в полярному розчиннику, такому як етанол, при температурах, що змінюються від 25 °C до 150 °C. Спосіб B2: Альтернативно можливо використовувати перевагу реакції ароматичного нуклеофільного заміщення для функціоналізації піридинового або піразинового кілець в положенні 6. В цьому випадку використовуваними нуклеофілами є феноли, тіофеноли, бензилові спирти або тіобензилові спирти, а також аніліни або бензиламін, що несе або не несе функціональну групу. Загальна схема реакції 8a представлена нижче, зокрема, де W=H, (C1-C6)алкіл, арил або бензил. 22 UA 116107 C2 5 10 15 20 25 30 У випадку, в якому X=O або S, 6-хлор-3-нітропіколінонітрили і 6-хлор-3-нітропіразин-2карбонітрили, необов'язково заміщені в положенні 5, піддають взаємодії у присутності відповідного нуклеофілу, спирту або тіолу, в полярному розчиннику, такому як ацетонітрил, у присутності неорганічної основи, такої як карбонат калію або натрію. Можуть бути також розглянуті розчинники, такі як ДМСО (диметилсульфоксид), ДМФ (диметилформамід), ацетон, ТГФ (тетрагідрофуран) або піридин. При необхідності ці реакції можна каталізувати під дією міді, а також можна проводити без розчинника. У характерному випадку переважний протокол включає температури в діапазоні від 20 °C до 150 °C. Альтернативно також можливе використання основ, таких як піридин, DIPEA, діізопропіламін, триетиламін, DBU, трет-бутилат калію, NEt3 або NaH. У випадку, в якому X=N, толуол є переважним розчинником, а основою вибору є триетиламін (NEt3). Наступні стадії аж до сполук загальної формули (VIIb) ідентичні стадіям, що документуються в способі B1 вище. Спосіб B3: Спосіб B3, представлений на схемі 8b нижче, є варіантом способу B2, який відрізняється першою стадією, що є результатом реакції каталітичного поєднання між бензилборонатом в кислотній або складноефірній формі і похідної 6-хлор-3-нітропіколінонітрилу або 6-хлор-3нітропіразин-2-карбонітрилу. Фахівцям в даній області техніки також добре відомо, що можливі також реакції каталітичного поєднання з використанням альтернативних каталізаторів і бензильних похідних. Серед іншого може бути розглянута реакція Стілла, заснована на комплексах олова, або реакції, засновані на цинкорганічних сполуках. Необов'язково заміщений 2-бензил-4,4,5,5-тетраметил-1,3,2-діоксаборолан одержують попередньо, наприклад, з відповідного бензилхлориду і октаметил-бі-діоксаборолану в діоксані у присутності ацетату калію і Pt(dppf)Cl2 (dppf=1,1'-біс(дифенілфосфіно)фероцен). Цю сполуку об'єднують з 6-хлор-3-нітропіколінонітрилом, 6-хлор-3-нітропіразин-2-карбонітрилом, необов'язково заміщеним в положенні 5 або 5-хлор-2-нітронікотинонітрилом, необов'язково заміщеним в положенні 6, і паладієвим каталізатором, таким як Pd(dppf)Cl2 або Pd(PPh3)4, з органічною основою, такою як триетиламін або алкоголят, або з неорганічною основою, такою як карбонат натрію, калію або цезію, в розчиннику, такому як толуол, бензол, ТГФ або діоксан. Переважні температури цієї реакції складають від 20 °C до 100 °C. Продукти цих реакцій 23 UA 116107 C2 5 10 15 20 25 30 35 відповідають заміщеним похідним 6-бензил-3-нітропіколінонітрилу, 6-бензил-3-нітропіразин-2карбонітрилу або 5-бензил-2-нітронікотинонітрилу, для яких наступні стадії перетворення відтворюють з описаного вище способу B1. Спосіб B4: Спосіб B4, представлений на схемі 9 нижче, дає можливість одержати піразолопіридинові і піразолопіразинові біцикли, які характеризуються необов'язково функціоналізованими арилсульфонамідними функціональними групами, де Rl=(C1-C6)алкіл і, зокрема, W = H, (C1C6)алкіл, арил або бензил. Похідні етил-2-хлор-5-(хлорсульфоніл)нікотинату, необхідні для даної послідовності реакцій, можуть бути одержані згідно способам, описаним Levett P.c. et al., Org. Proc. Res. Dev., 2002, 6(6), 767-772; WO 01/98284 і WO 2008/010964. Утворення сульфонамідів в характерному випадку проводять шляхом змішування, що представляє інтерес, 2-хлор-5-(хлорсульфоніл)нікотинату з первинним або вторинним аніліном, необов'язково функціоналізованим, в апротонному розчиннику, такому як дихлорметан, ТГФ, ацетон або ацетонітрил, у присутності органічної основи, такої як триетиламін (NEt3), піридин або DIPEA. Може бути також розглянуте використання неорганічної основи, такої як карбонат натрію або калію. Оптимальні температури реакції складають від 0 °C до 70 °C. Реакція обмилення одержаного таким шляхом продукту, зокрема, шляхом використання гідроксиду літію в суміші ТГФ/вода, дає можливість одержати 2-хлор-5-(N-фенілсульфамоїл) нікотинові кислоти. Відповідні хлорангідриди одержують шляхом обробки тіонілхлоридом в толуолі із зворотним холодильником або будь-яким іншим способом дегідрохлорування, добре відомим фахівцям в даній області техніки. Взаємодія цих проміжних сполук з водним аміаком дає можливість утворити необов'язково функціоналізовані 2-хлор-5-(N-фенілсульфамоїл) нікотинаміди, які потім вступають в реакцію дегідратації, зокрема, шляхом використання POCl3 при температурі в діапазоні від 75 °C до 150 °C. Може бути також розглянуте альтернативне використання агентів, таких як P2O5 або трифтороцтовий ангідрид і піридин. Нарешті, ці похідні загальної формули (VIh) піддають взаємодії у присутності гідразину, що несе або не несе функціональну групу, в полярному розчиннику, такому як етанол, при температурах, що змінюються від 25 °C до 150 °C, з утворенням відповідних похідних загальної формули (VIId). Спосіб B5: Спосіб B5, представлений на схемі 10 нижче, дає можливість одержати піразолопіридинові біцикли, які характеризуються необов'язково функціоналізованими бензилефірними функціональними групами, зокрема, де W=H, (C1-C6)алкіл, арил або бензил. 24 UA 116107 C2 5 10 15 20 25 30 35 40 Спосіб, описаний нижче, заснований на роботі J. Baldwin et al., J. Heterocyclic. Chem., 1980, 17(3), 445-448. Похідні 5-гідроксинікотинонітрилу, необов'язково функціоналізовані в положенні 6, алкілують, в характерному випадку шляхом використання необов'язково функціоналізованого бензилгалогеніду у присутності основи. Для переважного способу потрібне використання апротонного полярного розчинника, такого як ДМФ, і основи, такої як NaH. Оптимальні температури реакції складають від 20 °C до 100 °C. Альтернативно розчинники, які можна використовувати, включають, наприклад, ТГФ, ДМСО, діоксан, ацетонітрил, дихлорметан або t ацетон, і основи, такі як BuOK, DIPEA, піридин, триетиламін, DBU або карбонат натрію, калію або цезію. Окислення піридинового кільця до піридин-N-оксиду в характерному випадку проводять шляхом використання m-CPBA в дихлорметані при кімнатній температурі. Проте, можливо багато альтернативних способів, зокрема, заснованих на використанні перкарбонату натрію у присутності ренієвого каталізатора, перборату натрію у присутності оцтової кислоти або комплекс сечовини з пероксидом водню. Обробка цих похідних піридин-N-оксиду оксихлоридом фосфору приводить до утворення відповідних 2-хлорнікотинонітрилів (VI). Взаємодія цих сполук при нагріванні з гідразином, що несе або не несе функціональну групу, в полярному розчиннику, такому як ізопропанол або етанол, приводить до утворення потрібних піразолопіридинових біциклів (VIIe). Спосіб B6: Спосіб B6, представлений на схемі 10a нижче, дає можливість одержати необов'язково функціоналізовані піразолопіридинові і піразолопіразинові біцикли, що характеризуються оборотними сульфонамідними функціональними групами, зокрема, де W=H,(C1-C6)алкіл, арил або бензил. Спосіб, описаний нижче, полягає в утворенні сульфонамідної функціональної групи з ароматичного аміну і арилсульфонілгалогеніду або будь-якого іншого еквівалентного реагенту у присутності основи, яку можна необов'язково вводити як розчинник або співрозчинник. Альтернативно арилсульфонілгалогенід або його еквівалент може бути утворений in situ. Ця реакція при нагріванні з гідразином, що несе або не несе функціональну групу, в полярному розчиннику, такому як ізопропанол або етанол, приводить до утворення бажаних піразолопіридинових і піразолопіразинових біциклів (VIIf). Спосіб C: Спосіб C націлений на одержання сполук формули (XI), як описано на схемі 1. Спосіб C1: Спосіб C1, представлений на схемі 11 нижче, призначений для одержання піразолопіридинів і піразолопіразинів, функціоналізованих в положенні 6, де Rn=атом галогену, мезилат, тозилат або трифлат X=O, S, NH, N-(C1-C6)алкіл і необов'язково CH2 для (Xc) і (Xd), і Rj=H або N-захисна група. Даний спосіб можна також використовувати для виконання синтезу молекул, що містять двоатомну групу X, відповідну, зокрема, групі ArX, що позначає: -ArCH2NH-, -ArCH2N(R4)-, ArCH2O-, -ArCH2S-, -ArCH2CH2-, -ArCHCH- або -ArCC-. 25 UA 116107 C2 5 10 15 20 25 30 35 40 6-Гідрокси-2-(метилтіо)нікотинонітрили або 5-гідрокси-3-(метилтіо)піразин-2-карбонітрили піддають реакції дегідрохлорування, в характерному випадку у присутності оксихлориду фосфору, з розчинником або без розчинника, при температурах, що змінюються від 70 °C до 180 °C. При використанні розчинника переважний неполярний розчинник з високою температурою кипіння, такий як толуол або ксилол. Альтернативно можливо активувати 6гідрокси-2-(метилтіо)нікотинонітрили і 5-гідрокси-3-(метилтіо)піразин-2-карбонітрили шляхом їх перетворення в сульфонові ефіри за допомогою утворення відповідних тозилатів, мезилатів або трифлатів. Якщо даний варіант переважний, використання тозил-, мезил- або трифлілхлоридів в розчиннику, такому як толуол, дихлорметан, ТГФ, ацетонітрил, ацетон або діоксан, у присутності органічної або неорганічної основи надає можливість одержання цих похідних. Потім відповідно одержані 6-хлор-2(метилтіо)нікотинонітрили і 5-хлор-3-(метилтіо) піразин-2карбонітрили або їх сульфоефірні аналоги, якщо даний варіант переважний, піддають взаємодії з нуклеофілом, таким як фенол, анілін або тіофенол, в контексті ароматичного нуклеофільного заміщення. В даному випадку реакцію проводять в полярному розчиннику, такому як ДМСО, ДМФ, ацетон, ТГФ або ацетонітрил, у присутності основи, такої як трет-бутилат натрію або NaH. При необхідності ці реакції можна каталізувати під дією міді, і можна також проводити без розчинника. У характерному випадку переважний протокол включає температури в діапазоні від 20 °C до 150 °C. Альтернативно також можливе використання органічних основ, таких як піридин, діізопропіламін, триетиламін або DBU, або неорганічних основ, таких як карбонат натрію або калію. Альтернативно сполуки формули (IXb) можуть вступати в каталітичну реакцію сполучення, таку як реакція Сузуки. В даному випадку ці сполуки об'єднують з необов'язково заміщеним 2бензил-4,4,5,5-тетраметил-1,3,2-діоксабороланом, вже описаним в попередньому способі B3, паладієвим каталізатором, таким як Pd(dppf)Cl2 або Pd(PPh3)4, органічною основою, такою як триетиламін або алкоголят, або неорганічною основою, такою як карбонат натрію, калію або цезію, в розчиннику, такому як толуол, бензол, ТГФ або діоксан. Переважні температури реакції складають від 20 °C до 100 °C. Потім похідні, одержані одним або іншим з цих способів, окисляють, в характерному випадку шляхом використання m-CPBA або оксону з утворенням відповідних метилсульфоксидів або метилсульфонів. Ці сполуки, іноді одержані у вигляді сумішей, використовують як такі в реакції утворення амінопіразольного кільця, шляхом використання необов'язково заміщеного гідразину в полярному розчиннику, такому як етанол, при температурах, що змінюються від 25 °C до 150 °C. Альтернативно можливо модифікувати послідовність реакцій, зокрема, шляхом зворотного порядку стадій синтезу. Спосіб C2: Спосіб C2, представлений на схемі 12 нижче, призначений для одержання піразолопіридинів і піразолопіридазинів, функціоналізованих в положенні 6, де X=O, S, NH, N(C1-C6)алкіл або CH2, і Rj=H або N-захисна група. 26 UA 116107 C2 5 10 15 20 25 30 35 Похідні 6-гідрокси-4-(метилтіо)нікотинонітрилу або 6-гідрокси-4-(метилтіо)піридазин-3карбонітрилу окисляють, в характерному випадку шляхом використання m-CPBA або оксону, з утворенням відповідних метилсульфоксидів або метилсульфонів. Ці сполуки, іноді одержані у вигляді сумішей, використовують як такі в реакції утворення амінопіразольного кільця, шляхом використання необов'язково заміщеного гідразину в полярному розчиннику, такому як етанол, при температурах, що змінюються від 25 °C до 150 °C. Одержані таким шляхом піразолопіридини і піразолопіридазини піддають реакції дегідрохлорування, в характерному випадку у присутності оксихлориду фосфору, з розчинником або без розчинника, при температурах, що змінюються від 70 °C до 180 °C. При використанні розчинника переважний неполярний розчинник з високою температурою кипіння, такий як толуол або ксилол. Потім відповідно одержаний необов'язково заміщений 6-хлор-піразоло[4,3c]піридин-3-амін і 6-хлор-піразоло[4,3-c]піридазин-3-амін піддають взаємодії з нуклеофілом, таким як фенол, анілін або тіофенол, в контексті ароматичного нуклеофільного заміщення. В даному випадку реакцію проводять в полярному розчиннику, такому як ДМСО, ДМФ, ацетон, ТГФ або ацетонітрил, у присутності основи, такої як трет-бутилат калію або NaH. При необхідності ці реакції можна каталізувати під дією міді, і можна проводити без розчинника. У характерному випадку переважний протокол включає температури в діапазоні від 20 °C до 150 °C. Альтернативно можливе використання органічних основ, таких як піридин, діізопропіламін, триетиламін або DBU, або неорганічних основ, таких як карбонат натрію або калію. Альтернативно сполуки формули (XIVa) можуть вступати в каталітичну реакцію сполучення, таку як реакція Сузуки. В цьому випадку ці сполуки об'єднують з необов'язково заміщеним 2бензил-4,4,5,5-тетраметил-1,3,2-діоксабороланом, описаним вище в попередньому способі B3, паладієвим каталізатором, таким як Pd(dppf)Cl2 или Pd(PPh3)4, органічною основою, такою як триетиламін або алкоголят, або неорганічною основою, такою як карбонат натрію, калію або цезію, в розчиннику, такому як толуол, бензол, ТГФ або діоксан. Переважні температури реакції складають від 20 °C до 100 °C. Спосіб C3: Спосіб C3, представлений на схемі 12a нижче, є варіантом способу C1, заснованим на регіоселективній функціоналзації 2,6-дихлорнікотинонітрилу або аніонним нуклеофілом, таким як фенат або тіофенат, або металоорганічною сполукою, такою як хлорид бензилцинку. В останньому випадку реакцію каталізують, наприклад, комплексомпаладію(II). Перетворення одержаного таким шляхом хлорнікотинонітрилу у відповідний піразолопіридин, у випадку, де Y1=CH, виконують, як описано вище в способі A1. Спосіб D: Об'єктом цих способів є синтез сполук формули (I) або (VII) шляхом використання різних способів каталітичного сполучення. 27 UA 116107 C2 Спосіб D1: У способі D1, представленому на схемі 13 нижче, використовують каталітичну реакцію сполучення, як описано в J.A.C.S., 1984, 106, 158, між цинкорганічною сполукою, одержаною in situ, і арилбромідом, що каталізується паладієвими комплексами. 5 10 15 20 Необов'язково заміщені 3-аміно-діазаіндазоли і 3-аміно-азаіндазоли об'єднують з необов'язково заміщеним хлоридом бензилцинку в апротонному полярному розчиннику, такому як ТГФ або діоксан, у присутності каталітичної кількості паладієвого комплексу, такого як (dppf)2PdCl2·CH2Cl2. Реакцію сполучення проводять при температурах в діапазоні від 25 °C до 100 °C. Спосіб D2: У способі D2, представленому на схемі 14 нижче, використовують реакцію сполучення, як описано в Gueiffier A. et al., Tetrahedron, 2006, 62, 6042-6049, між тіолом, зокрема, тіофенолом або бензилтіолом, і арилйодидом, що каталізується комплексами міді. Цю реакцію в характерному випадку проводять в полярному розчиннику з високою температурою кипіння, такому як 2-пропанол, у присутності каталітичної кількості поліетиленгліколю, солі металу, такої як йодид міді (CUI), і надлишку неорганічної основи, такої як карбонат калію, карбонат кальцію або карбонат натрію. Температури реакції в характерному випадку змінюються від 50 °C до 100 °C. Спосіб D3: У способі D3, представленому на схемі 15 нижче, використовують реакцію сполучення, як описано в Sonogashira, K. et al. у Tetrahedron Lett., 1975, 16, 4467-4470, між похідним ацетилену і арилгалогенідом, що каталізується комплексами міді і паладію. 28
ДивитисяДодаткова інформація
Назва патенту англійськоюDerivatives of azaindazole or diazaindazole type for treating pain
Автори англійськоюSokoloff, Pierre, Cachoux, Frederic
Автори російськоюСоколофф Пьер, Кашу Фрэдэрик
МПК / Мітки
МПК: A61K 31/5025, A61K 31/519, A61K 31/437, A61K 31/4985
Мітки: азаіндазолу, болю, діазаіндазолу, похідних, лікування, застосування
Код посилання
<a href="https://ua.patents.su/104-116107-zastosuvannya-pokhidnikh-azaindazolu-abo-diazaindazolu-dlya-likuvannya-bolyu.html" target="_blank" rel="follow" title="База патентів України">Застосування похідних азаіндазолу або діазаіндазолу для лікування болю</a>
Попередній патент: Будівельний модуль та спосіб монтажу будівельних модулів
Наступний патент: Паперова обгортка мундштука
Випадковий патент: Спосіб поліпшення здоров'я і продуктивності сільськогосподарських тварин та птиці в т.ч. в умовах стресового навантаження