Похідні хінуклідину та їх застосування
Номер патенту: 78812
Опубліковано: 25.04.2007
Автори: Йерґенсен Тіно Дюрінґ, Нільсен Ельсебет Естерґор, Арінґ Філіп К., Петерс Дан, Ольсен Гуннар М.
Формула / Реферат
1. Хінуклідинове похідне формули
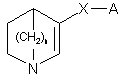 , (І)
, (І)
його енантіомер, суміш його енантіомерів, його фармацевтичнo прийнятна адитивна сіль, або його онієва сіль, де,
----------- зображує можливий подвійний зв'язок;
n=1, 2 або 3;
X - лінкер з групи: -O-, -O-СН2-, -O-CH2-CH2-, -S-, -SO-, -SO2-, -CH2-, -S-CH2-CH2-, -СH2, -C(=CH2)-,-NH-, -N(алкіл)-, -С(=O)-, -C(=S)-,
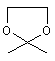 ,
, 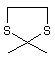 ,
,
А –
мoноциклічна або поліциклічна карбоциклічна група, як-то:
інданіл;
інденіл;
нафтил;
5,6,7,8-тетрагідронафтил;
азуленіл та
антраценіл; або
моноциклічна гетероциклічна група, як-то: піридазиніл та тіазоліл; або
поліциклічна гетероциклічна група, як-то:
індоліл;
ізоіндоліл;
хінолініл;
хіноксалініл;
бензоксазоліл;
бензтіазоліл;
бензизотіазоліл;
бензтриазоліл та імідазо[1,2-b]піридазиніл;
ці моно або поліциклічні, карбоциклічні або гетероциклічні групи, як варіант, заміщені одним або більше із замісників: алкіл, циклоалкіл, циклоалкілалкіл, алкоксил, гідроксіалкоксил, алкоксіалкіл, алкоксіалкоксил, циклоалкоксил, циклоалкоксіалкіл, циклоалкоксіалкоксил, галоген, CF3, CN, NO2, NH2, карбоксил, карбамоїл, амідо, сульфамоїл та феніл, або іншою моноциклічною або поліциклічною, карбоциклічною або гетероциклічною групою, ця додаткова моноциклічна або поліциклічна, карбоциклічна або гетероциклічна група може, як варіант, бути заміщена одним або більше із замісників: алкіл, циклоалкіл, циклоалкілалкіл, алкоксил, гідроксіалкоксил, алкоксіалкіл, алкоксіалкоксил, циклоалкоксил, циклоалкоксіалкіл, циклоалкоксіалкоксил, галоген, CF3, CN, NO2, NH2, карбоксил, карбамоїл, амідо, сульфамоїл та феніл.
2. Хінуклідинове похідне за п. 1, де ----------- зображує одинарний (ковалентний) зв'язок.
3. Хінуклідинове похідне за будь-яким з пп. 1-2, де n=1, 2 або 3.
4. Хінуклідинове похідне за п. 3, де n=2.
5. Хінуклідинове похідне за будь-яким з пп. 1-4, де Х - лінкер з групи: -O-, -O-CH2-, -O-CH2-CH2-, -S- та –СН2-.
6. Хінуклідинове похідне за п. 5, де Х - -O-, -О-СН2- або -O-СН2-СН2-.
7. Хінуклідинове похідне за п. 5, де Х - -O-.
8. Хінуклідинове похідне за будь-яким з пп. 1-7, де А - моноциклічна або поліциклічна карбоциклічна група, як-то:
інданіл;
інденіл;
нафтил;
5,6,7,8-тетрагідронафтил;
азуленіл та антраценіл;
ця карбоциклічна група, як варіант, заміщена одним або двома із замісників: алкіл, циклоалкіл, циклоалкілалкіл, алкоксил, гідроксіалкоксил, алкоксіалкіл, алкоксіалкоксил, циклоалкоксил, циклоалкоксіалкіл, циклоалкоксіалкоксил, галоген, CF3, CN, NO2, NH2, карбоксил, карбамоїл, амідо, сульфамоїл та феніл.
9. Хінуклідинове похідне за п. 8, де А - моноциклічна або поліциклічна карбоциклічна група, як-то:
4-інданіл та 5-інданіл;
1-інденіл, 2- інденіл та 3-інденіл;
1-нафтил та 2-нафтил;
5,6,7,8-тетрагідро-1-нафтил та 5,6,7,8-тетрагідро-2-нафтил;
1-азуленіл, 2-азуленіл та 3-азуленіл; та 1-антраценіл та 2-антраценіл;
ця карбоциклічна група, як варіант, заміщена одним або двома із замісників: алкіл, циклоалкіл, циклоалкілалкіл, алкоксил, гідроксіалкоксил, алкоксіалкіл, алкоксіалкоксил, циклоалкоксил, циклоалкоксіалкіл, циклоалкоксіалкоксил, галоген, CF3, CN, NO2, NH2, карбоксил, карбамоїл, амідо, сульфамоїл та феніл.
10. Хінуклідинове похідне за п. 9, яким є (±)-3-(нафт-2-илоксі)-1-азадицикло[2.2.2]октан; (±)-3-(5,6,7,8-тетрагідро-2-нафтилоксі)-1-аза-дицикло[2.2.2]октан
або (±)-3-(5-інданілоксі)-1-азадицикло[2.2.2]октан;
або його енантіомер, його фармацевтично прийнятна адитивна сіль, або його онієва сіль.
11. Хінуклідинове похідне за будь-яким з пп. 1-7, де А - моноциклічна або поліциклічна гетероциклічна група, як-то:
піридазиніл;
тіазоліл;
хінолініл;
хіноксалініл;
бензоксазоліл;
бензтіазоліл;
ця моноциклічна або поліциклічна гетероциклічна група, як варіант, заміщена одним або більше із замісників: алкіл, циклоалкіл, циклоалкілалкіл, алкоксил, гідроксіалкоксил, алкоксіалкіл, алкоксіалкоксил, циклоалкоксил, циклоалкоксіалкіл, циклоалкоксіалкоксил, галоген, CF3, CN, NO2, NH2, карбоксил, карбамоїл, амідо, сульфамоїл та феніл, або іншою моноциклічною або поліциклічною, карбоциклічною або гетероциклічною групою, ця додаткова моноциклічна або поліциклічна, карбоциклічна або гетероциклічна група може, як варіант, бути заміщена одним або більше із замісників: алкіл, циклоалкіл, циклоалкілалкіл, алкоксил, гідроксіалкоксил, алкоксіалкіл, алкоксіалкоксил, циклоалкоксил, циклоалкоксіалкіл, циклоалкоксіалкоксил, галоген, CF3, CN, NO2, NH2, карбоксил, карбамоїл, амідо, сульфамоїл та феніл.
12. Хінуклідинове похідне за п. 11, де А - моноциклічна або поліциклічна гетероциклічна група, як-то:
піридазин-3-іл та піридазин-4-іл;
тіазол-2-іл, тіазол-4-іл та тіазол-5-іл;
хінолін-2-іл, хінолін-3-іл, хінолін-4-іл, хінолін-5-іл та хінолін-6-іл;
хіноксалін-2-іл та хіноксалін-3-іл;
бензоксазол-2-іл та бензтіазол-2-іл;
ця моноциклічна або поліциклічна гетероциклічна група, як варіант, заміщена одним або більше із замісників: алкіл, циклоалкіл, циклоалкілалкіл, алкоксил, гідроксіалкоксил, алкоксіалкіл, алкоксіалкоксил, циклоалкоксил, циклоалкоксіалкіл, циклоалкоксіалкоксил, галоген, CF3, CN, NO2, NH2, карбоксил, карбамоїл, амідо, сульфамоїл та феніл, або іншою моноциклічною або поліциклічною, карбоциклічною або гетероциклічною групою, ця додаткова моноциклічна або поліциклічна, карбоциклічна або гетероциклічна група може, як варіант, бути заміщена одним або більше із замісників: алкіл, циклоалкіл, циклоалкілалкіл, алкоксил, гідроксіалкоксил, алкоксіалкіл, алкоксіалкоксил, циклоалкоксил, циклоалкоксіалкіл, циклоалкоксіалкоксил, галоген, CF3, CN, NO2, NH2, карбоксил, карбамоїл, амідо, сульфамоїл та феніл.
13. Хінуклідинове похідне за п. 11, де А - піридазин-3-іл або піридазин-4-іл;
що як варіант, заміщено одним або більше із замісників: алкіл, циклоалкіл, циклоалкілалкіл, алкоксил, гідроксіалкоксил, алкоксіалкіл, алкоксіалкоксил, циклоалкоксил, циклоалкоксіалкіл, циклоалкоксіалкоксил, галоген, CF3, CN, NO2, NH2, карбоксил, карбамоїл, амідо, сульфамоїл та феніл, або іншою моноциклічною або поліциклічною, карбоциклічною або гетероциклічною групою, ця додаткова моноциклічна або поліциклічна, карбоциклічна або гетероциклічна група може, як варіант, бути заміщеною одним або більше із замісників: алкіл, циклоалкіл, циклоалкілалкіл, алкоксил, гідроксіалкоксил, алкоксіалкіл, алкоксіалкоксил, циклоалкоксил, циклоалкоксіалкіл, циклоалкоксіалкоксил, галоген, CF3, CN, NO2, NH2, карбоксил, карбамоїл, амідо, сульфамоїл та феніл.
14. Хінуклідинове похідне за п. 13, де А -
піридазин-3-іл або піридазин-4-іл;
як варіант, заміщені поліциклічною гетероциклічною групою.
15. Хінуклідинове похідне за п. 14, де А –
піридазин-3-іл або піридазин-4-іл;
як варіант, заміщені індолілом;
ізоіндолілом;
хінолінілом;
хіноксалінілом;
бензоксазолілом; бензтіазолілом;
бензизотіазолілом;
бензтриазолілом або
імідазо[1,2-b]піридазинілом.
16. Хінуклідинове похідне за п. 15, де А - піридазин-3-іл або піридазин-4-іл;
як варіант, заміщені індолілом.
17. Хінуклідинове похідне за п. 16, де А -
піридазин-3-іл, заміщений індолілом.
18. Хінуклідинове похідне за будь-яким з пп. 1-7, де А - моноциклічна гетероциклічна група, як-то:
піридазиніл та тіазоліл;
ця моноциклічна гетероциклічна група, як варіант, заміщена одним або більше із замісників алкіл, циклоалкіл, алкоксил, циклоалкоксил, галоген, CF3, CN, NO2, NH2, феніл, 2-тієніл, 3-тієніл, 2-фураніл, 3-фураніл та 3-піридиніл, ці феніл, 2-тієніл, 3-тієніл, 2-фураніл, 3-фураніл та 3-піридиніл можуть, як варіант, бути заміщеними одним або двома із замісників: алкіл, циклоалкіл, алкоксил, галоген, CF3, CN, NO2, NH2 та феніл.
19. Хінуклідинове похідне за будь-яким з пп. 1-7, де А - моноциклічна гетероциклічна група, як-то:
піридазин-3-іл та піридазин-4-іл; та
тіазол-2-іл тіазол-4-іл та тіазол-5-іл;
ця моноциклічна гетероциклічна група, як варіант, заміщена одним або більше із замісників: алкіл, циклоалкіл, алкоксил, циклоалкоксил, галоген, CF3, CN, NO2, NH2, феніл, 2-тієніл, 3-тієніл, 2-фураніл, 3-фураніл та 3-піридиніл, ці феніл, 2-тієніл, 3-тієніл, 2-фураніл, 3-фураніл та 3-піридиніл можуть, як варіант, бути заміщеними одним або двома із замісників: алкіл, циклоалкіл, алкоксил, галоген, CF3, CN, NO2, NH2 та феніл.
20. Хінуклідинове похідне за будь-яким з пп. 1-7, де А - моноциклічна гетероциклічна група, як-то:
піридазин-3-іл та піридазин-4-іл; та тіазол-2-іл, тіазол-4-іл та тіазол-5-іл;
ця моноциклічна гетероциклічна група, як варіант, заміщена одним або більше із замісників: галоген, феніл, 2-тієніл, 3-тієніл, 2-фураніл, 3-фураніл та 3-піридиніл, ці феніл, 2-тієніл, 3-тієніл, 2-фураніл, 3-фураніл та 3-піридиніл можуть, як варіант, бути заміщеними одним або двома галогенами.
21. Хінуклідинове похідне за п. 18, котрим є:
(±)-3-(5-бромтіазол-2-ілоксі)-1-азадицикло[2.2.2]октан;
(±)-3-(5-фенілтіазол-2-ілоксі)-1-азадицикло[2.2.2]октан;
(±)-3-[5-(2,4-дифлуорфеніл)-тіазол-2-ілоксі]-1-азадицикло[2.2.2]октан;
(±)-3-[5-(3-тієніл)-тіазол-2-ілоксі]-1-азадицикло[2.2.2]октан;
(±)-3-[5-(2-тієніл)-тіазол-2-ілоксі]-1-азадицикло[2.2.2]октан;
(±)-3-[5-(3-фураніл)-тіазол-2-ілоксі]-1-азадицикло[2.2.2]октан;
(±)-3-[5-(3-піридил)-тіазол-2-ілоксі]-1-азадицикло[2,2.2]октан;
(±)-3-(6-хлорпіридазин-3-ілоксі)-1-азадицикло[2.2.2]октан;
(±)-3-(6-бромпіридазин-3-ілоксі)-1-азадицикло[2.2.2]октан;
(±)-3-(6-фенілпіридазин-3-ілоксі)-1-азадицикло[2.2.2]октан;
(±)-3-[6-(3-тієніл)-піридазин-3-ілоксі]-1-азадицикло[2.2.2]октан;
(±)-3-[6-(2-тієніл)-піридазин-3-ілоксі]-1-азадицикло[2.2.2]октан;
(±)-3-[6-(2-фураніл)-піридазин-3-ілоксі]-1-азадицикло[2.2.2]октан;
(±)-3-[6-(3-фураніл)-піридазин-3-ілоксі]-1-азадицикло[2.2.2]октан або
(±)-3-[6-(3-піридил)-піридазин-3-ілоксі]-1-азадицикло[2.2.2]октан;
або його енантіомер, його фармацевтичнo прийнятна адитивна сіль, або його онієва сіль.
22. Хінуклідинове похідне за будь-яким з пп. 1-7, де А - поліциклічна гетероциклічна група, як-то:
індоліл;
ізoіндоліл;
хінолініл;
хіноксалініл;
бензоксазоліл;
бензтіазоліл;
бензизотіазоліл;
бензтриазоліл та імідазо[1,2-b]піридазиніл;
ця моноциклічна або поліциклічна гетероциклічна група, як варіант, заміщена одним або більше із замісників: алкіл, циклоалкіл, алкоксил, циклоалкоксил, галоген, CF3, CN, NO2, NH2 та феніл, цей феніл може, як варіант, бути заміщеним одним або більше із замісників: алкіл, циклоалкіл, алкоксил, галоген; CF3, CN, NO2, NH2 та феніл.
23. Хінуклідинове похідне за п. 22, де А - поліциклічна гетероциклічна група, як-то:
індол-2-іл та індол-3-іл;
ізоіндол-2-іл;
хінолін-2-іл, хінолін-3-іл, хінолін-4-іл, хінолін-5-іл та хінолін-6-іл;
хіноксалін-2-іл та хіноксалін-3-іл;
бензоксазол-2-іл;
бензтіазол-2-іл;
бензизотіазол-3-іл;
1,2,3-бензтриазол-1-іл та імідазо[1,2-b]піридазин-6-іл;
ця моноциклічна або поліциклічна гетероциклічна група, як варіант, заміщена одним або більше із замісників: алкіл, циклоалкіл, алкоксил, циклоалкоксил, галоген, CF3, CN, NO2, NH2 та феніл, цей феніл може, як варіант, бути заміщеним одним або більше із замісників: алкіл, циклоалкіл, алкоксил, галоген, CF3, CN, NO2, NH2 та феніл.
24. Хінуклідинове похідне за п. 23, де А - поліциклічна гетероциклічна група, як-то:
ізоіндол-2-іл;
хінолін-2-іл, хінолін-3-іл, хінолін-4-іл, хінолін-5-іл та хінолін-6-іл;
хіноксалін-2-іл та хіноксалін-3-іл;
бензоксазол-2-іл;
бензтіазол-2-іл;
бензизотіазол-3-іл;
1,2,3-бензтриазол-1-іл та імідазо[1,2-b]піридазин-6-іл;
ця моноциклічна або поліциклічна гетероциклічна група, як варіант,заміщена одним або більше із замісників: алкіл, алкоксил та галоген.
25. Хінуклідинове похідне за п. 24, котрим є:
(±)-3-[(1,3-діон)-2-ізоіндолілметоксі]-1-азадицикло[2.2.2]октан;
(±)-3-[(1,3-діон)-2-ізоіндолілетоксі]-1-азадицикло[2.2.2]октан;
(±)-3-(2-хінолінілоксі)-1-азадицикло[2 2.2]октан;
(±)-3-(2-хінолінілоксі)-1-азадицикло[2.2.2]октан метилій йодид;
(±)-3-(6-хінолінілоксі)-1-азадицикло[2.2.2]октан;
(±)-3-(2-хіноксалінілоксі)-1-азадицикло[2.2.2]октан;
(±)-3-(2-хіноксалінілоксі)-1-азадицикло[2.2.2]октан метилій йодид;
(±)-3-(3-хлор-2-хіноксалінілоксі)-1-азадицикло[2.2.2]октан;
(±)-3-(3-метокси-2-хіноксалінілоксі)-1-азадицикло[2.2.2]октан;
(±)-3-(бензоксазол-2-ілоксі)-1-азадицикло[2.2.2]октан;
(±)-3-(бензтіазол-2-ілоксі)-1-азадицикло[2,2.2]октан;
(±)-3-(6-хлор-бензтіазол-2-ілоксі)-1-азадицикло[2.2.2]октан;
(±)-3-(1,2-бензизотіазол-3-ілоксі)-1-азадицикло[2.2.2]октан;
(±)-3-(1,2-бензизотіазол-3-ілоксі)-1-азадицикло[2.2.2]октан;
(±)-3-(бензтриазол-1-ілоксі)-1-азадицикло[2.2.2]октан або
(±)-3-(2-фенілімідазо[1,2-b]піридазин-6-ілоксі)-1-азадицикло[2.2.2]октан;
або його енантіомер, його фармацевтичнo прийнятна адитивна сіль, або його оніева сіль.
26. Фармацевтична композиція, яка містить терапевтичнo ефективну кількість хінуклідинового похідного за будь-яким з пп. 1-25 або його фармацевтичнo прийнятної адитивної солі.
27. Застосування хінуклідинового похідного за будь-яким з пп. 1-25 або його фармацевтичнo прийнятної адитивної солі для виробництва фармацевтичної композиції/медикаменту для лікування, попередження або пом'якшення хвороби, розладу або стану ссавця, включаючи людину, причому хвороба, розлад або стан є чутливими до модуляції холінергічних рецепторів та/або рецепторів моноамінів.
28. Застосування за п. 27, де хвороба, розлад або стан стосуються центральної нервової системи.
29. Застосування за п. 28, де хворобою, розладом або станом є тривожність, когнітивні розлади, недостатня здатність до навчання, дефіцит та дисфункція пам'яті, хвороба Альцгеймера, дефіцит уваги, гіперактивний розлад з дефіцитом уваги (ADHD), хвороба Паркінсона, хвороба Гентингтона, бічний аміотрофний склероз, синдром Жіль де ла Туретта, психоз, депресія, манія, маніакальна депресія, шизофренія, обесивно-компульсивні розлади (OCD), панічні розлади, розлади харчування, як-то нервово-психічна анорексія, булімія та ожиріння, нарколепсія, ноцицепція, СНІД-деменція, сенільна деменція, периферійна невропатія, аутизм, дислексія, пізня дискінезія, гіперкінезія, епілепсія, булімія, посттравматичний синдром, соціальна фобія, розлади сну, псевдодеменція, синдром Гансера, передменструальний синдром, синдром пізньої лютеальної фази, синдром хронічної втоми, мутизм, трихотиломанія та порушення добового ритму організму.
30. Застосування за п. 27, де хвороба, розлад або стан асоційовані зі скороченням гладких м'язів, охоплюючи конвульсивні розлади, стенокардія, передчасні пологи, конвульсії, діарея, астма, епілепсія, пізня дискінезія, гіперкінезія, передчасна еякуляція та труднощі ерекції.
31. Застосування за п. 27, де хвороба, розлад або стан стосуються ендокринної системи, як-то тиреотоксикоз, феохромоцитома, гіпертензія та аритмії.
32. Застосування за п. 27, де хворобою, розладом або станом є нейродегенеративні розлади, охоплюючи тимчасову аноксію та індуковану нейродегенерацію.
33. Застосування за п. 27, де хворобою, розладом або станом є запальний розлад, охоплюючи запальні розлади шкіри, як-то вугри та рожеві вугри, хвороба Крона, запальна хвороба кишечнику, виразковий коліт та діарея.
34. Застосування за п. 27, де хворобою, розладом або станом є слабкий, помірний і навіть суворий біль гострого, хронічного або рецидивного характеру, біль, викликаний мігренню, постопераційний біль, біль фантомних кінцівок, невропатичний біль, хронічний головний біль, центральний біль, біль при діабетичній невропатії, післятерапевтичній невралгії, або при пошкодженні периферійних нервів.
35. Застосування за п. 27, де хвороба, розлад або стан асоційовані з сиптомами відторгнення, викликаними завершенням застосування речовин, що викликають звичку, охоплюючи продукти з нікотином, як-то тютюн, опіоїди, як-то героїн, кокаїн та морфін, бензодіазепіни і бензодіазепіноподібні ліки, та алкоголь.
Текст
Цей винахід стосується нових хінуклідинових похідних та їх застосування як фармацевтичних препаратів. Завдяки їх фармакологічному профілю сполуки винаходу можуть бути корисними для лікування різноманітних хвороб або розладів, які стосуються холінергічної системи, центральної нервової системи (ЦНС), периферичної нервової системи (ПНС), хвороб або розладів, що стосуються контрактури гладеньких м'язів, ендокринних хвороб або розладів, хвороб або розладів, що стосуються нейродегенерації, хвороб або розладів, що стосуються запалення, болю та симптомів абстиненції, обумовлених припиненням зловживання хімічними речовинами. Ендогенний холінергічний нейротрансмітер, ацетилхолін, реалізує свою біологічну дію через два типи холінергічних рецепторів, мускаринові ацетилхолінові рецептори (мАХР) та нікотинові ацетилхолінові рецептори (нАХР). Добре відомо, що мускаринові ацетилхолінові рецептори важливі для пам'яті та здатності до пізнання, і багато досліджень, спрямованих на удосконалення засобів лікування розладів пам'яті, зосереджені на синтезі модуляторів мускаринових ацетилхолі-нових рецепторів. Дійсно, декілька розладів ЦНС можуть бути віднесені до холінергічної недостатності, допамінергічної недостатності, адренергічної недостатності або серотонінергічної недостатності. Браун та ін. [Brown et al.: Quinuclidine Inhibitors of 2,3-Oxidosqualene Cyclase-Lanostero! Syntase: Optimization from Lipid Profiles; J. Med. Chem. 1999 42 1306-1311] описує синтез три-заміщених похідних хінуклідину, корисних, як інгібітори біосинтезу холестерину. Повідомлення про дію на нікотинові та/або моноамінові рецептори відсутні. Представлений винахід стосується одержання нових похідних хінуклідину -модуляторів нікотинових та/або моноамінових рецепторів, які корисні для лікування хвороб або розладів, що стосуються холінергічних рецепторів, та, зокрема, нікотинового ацетилхолінового рецептору, моноамінових рецепторів, зокрема, серотонінового рецептору (5-HTR), допамінового рецептору (ДАР) та норадренолінового рецептору (НАР), та транспортерів біогенного аміну до серотоніну (5-НТ), допаміну (ДА) та норадреналіну (НА). Завдяки їх фармакологічному профілю сполуки винаходу можуть бути корисними для лікування різноманітних хвороб або розладів, які стосуються холінергічної системи, центральної нервової системи (ЦНС), периферичної нервової системи (ПНС), хвороб або розладів, що стосуються контрактури гладеньких м'язів, ендокринних хвороб або розладів, хвороб або розладів, що стосуються нейродегенерації, хвороб або розладів, що стосуються запалення, болю, та симптомів абстиненції, обумовлених припиненням зловживання хімічними речовинами. Сполуки винаходу можуть також бути корисними, як діагностичні інструменти або засоби моніторингу у різних способах діагностики, і, зокрема, для відображення in vivo (нейровідображення) рецептору, та їх можна застосовувати у міченій або неміченій формі. Згідно першого аспекту винахід стосується хінуклідинових похідних, представлених Формулою І їх енантіомеру, або суміші їх енантіомерів, або їх фармацевтично прийнятної, адитивної солі, або їх онієвої солі, де,. представляє, як варіант, подвійний зв'язок; n дорівнює 1, 2 або 3; X вибрано з груп: -О-, -О-СН2-, -О-СН2-СН2-, -S-, -SO-, -SO2) -CH2-, -S-CH2-CH2-, -СН2-, -С(=СН2)-, -NH-, ІМ(алкіл)-, -С(=О)-, -C(=S)-, А представляє моноциклічну або поліциклічну, карбоциклічну або гетероциклічну груп у, як варіант, заміщену одним або більше замісниками, вибраними із груп: алкіл, ци-клоалкіл, циклоалкілалкіл, алкокси, гідроксіалкокси, алкоксіалкіл, алкоксіалкокси, циклоалкокси, циклоалкоксіалкіл, циклоалкоксіалкокси, галоген, CF3, CN, NH2, NH2, карбокси, карбамоїл, амід, сульфамоїл, та феніл, або іншою моноциклічною або поліциклічною, карбоциклічною або гетероциклічною групою, де додаткова моноциклічна або поліциклічна, карбоциклічна або гетероциклічна група може, як варіант, бути заміщеною одним або більше замісниками, вибраними з груп: алкіл, циклоалкіл, циклоалкілалкіл, алкокси, гідроксіалкокси, алкоксіалкіл, алкоксіалкокси, циклоалкокси, циклоалкоксіалкіл, циклоалкоксіалкокси, галоген, CF3, CN, NO2, NH2, карбокси, карбамоїл, амід, сульфамоїл, та феніл; за умови, однак, якщо X представляє О або S; тоді А не є фенілом або фенілом, заміщеним якою-небудь відмінною від фенільної групою (тобто, дифенільною групою). В другому аспекті винахід стосується фармацевтичної композиції, що містить терапевтично ефективну кількість хінуклідинового похідного винаходу. У третьому аспекті винахід стосується застосування хінуклідинового похідного винаходу, або його фармацевтично-прийнятної адитивної солі, для виробництва фармацевтичної композиції/медикаменту для лікування, попередження або полегшення хвороби або розладу або стану ссавця, охоплюючи людину, хвороба, розлад або стан, котрої чутливі до дії модулятора нікотинового ацетилхолінового рецептору. У подальшому аспекті винахід стосується способу лікування або полегшення хвороби або розладу організму тварини, охоплюючи людину, хвороба або розлад котрої, чутли ві до дії модулятора нікотинового ацетилхолінового рецептору, цей спосіб залучає етап застосування до такого організму тварини, охоплюючи людину, у разі потреби, терапевтично ефективної кількості хінуклідинового похідного винаходу. Інші об'єкти винаходу будуть очевидними для спеціалістів із наступного детального опису та прикладів. Хінуклідинові похідні У першому аспекті, представлений винахід стосується нових хін уклідинових похідних, представлених Формулою І їх енантіомеру, або суміші їх енантіомерів, або їх фармацевтично-прийнятної адитивної солі, або їх онієвої солі, де представляє, як варіант, подвійний зв'язок; n дорівнює 1, 2 або 3; X вибрано з груп: -О-, -О-СН2-, -О-СН2-СН2-, -S-, -SO-, -SO2, -CH2-, -S-CH2-CH2-, -СН2-, -С(=СН2)-, -NH-, М(алкіл)-, -С(=О)-, -C(=S)-, А представляє моноциклічну або поліциклічну, карбоциклічну або гетероциклічну груп у, як варіант, заміщену одним або більше замісниками, вибраними із груп: алкіл, ци-клоалкіл, циклоалкілалкіл, алкокси, гідроксіалкокси, алкоксіалкіл, алкоксіалкокси, циклоалкокси, циклоалкоксіалкіл, циклоалкоксіалкокси, галоген, CF3, CN, NO2 , NH2, карбокси, карбамоїл, амід, сульфамоїл, та феніл, або іншою моноциклічною або поліциклічною, карбоциклічною або гетероциклічною групою, де додаткова . моноциклічна або поліциклічна, карбоциклічна або гетероциклічна група може як варіант, бути заміщеною одним або більше замісниками, вибраними з груп: алкіл, або більше замісниками, вибраними з груп: алкіл, циклоалкіл, циклоалкілалкіл, алкокси, гідроксіалкокси, алкоксіалкіл, алкоксіалкокси, циклоалкокси, циклоалкоксіалкіл, циклоал-коксіалкокси, галоген, CF3, CN, NO 2, NH2, карбокси, карбамоїл, амід, сульфамоїл, та феніл; за умови, однак, якщо X представляє О або S; тоді А не є фенілом або фенілом, заміщеним якою-небудь відмінною від фенільної групою (тобто якщо X представляє О або S, а А представляє фенільну груп у, тоді ця фенільна група повинна бути тільки дифенільною групою). У переважному втіленні хінуклідинове похідне винаходу є сполукою формули І, де представляє одиничний (ковалентний) зв'язок. В іншому переважному втіленні хінуклідинове похідне винаходу є сполукою формули І, де п дорівнює 1, 2 або 3. У третьому переважному втіленні хінуклідинове похідне винаходу є сполукою формули І, де X вибрано з груп: -О-, -О-СН2-, -О-СН2-СН2-, -S-, та -СН2-. У більш переважному втіленні X вибрано з груп: -О-, -О-СН2-, та О-СН2-СН2-. У четвертому переважному втіленні хінуклідинове похідне винаходу є сполукою формули І, де А представляє моноциклічну або поліциклічну карбоциклічну групу, вибрану з груп: феніл; інданіл, зокрема, 4інданіл та 5-інданіл; інденіл, зокрема, 1-інденіл, 2-інденіл та 3-інденіл; нафтил, зокрема, 1-нафтил та 2нафтил; 5,6,7,8-те трагідронафтил, зокрема, 5,6,7,8-тетрагідро-1-нафтил та 5,6,7,8-тетрагідро-2нафтил;.азуленіл, зокрема, 1-азуленіл, 2-азуленіл та 3-азуленіл; та флуореніл, зокрема, 1-флуореніл, 2флуореніл, 3-флуореніл та 4-флуореніл; та антраценіл, зокрема, 1-антраценіл та 2-антраценіл; де карбоциклічна група, як варіант, заміщена одним або двома замісниками, вибраними з груп: алкіл, циклоалкіл, циклоалкілалкіл, алкокси, гідроксіалкокси, алкоксіалкіл, алкоксіалкокси, циклоалкокси, циклоалкоксіалкіл, циклоалкоксіалкокси, галоген, CF3, CN, NO2, NH2, карбокси, карбамоїл, амід, сульфамоїл та феніл. У п'ятому переважному втіленні хінуклідинове похідне винаходу є сполукою формули І, де А представляє ароматичну моноциклічну або поліциклічну карбоциклічну групу, вибрану з гр уп: феніл; інденіл, зокрема, 1інденіл, 2-інденіл та 3-інденіл; нафтил, зокрема, 1-нафтил та 2-нафтил; азуленіл, зокрема, 1-азуленіл, 2азуленіл та 3-азуленіл; та антраценіл, зокрема, 1-антраценіл та 2-антраценіл; де ароматична карбоциклічна група, як варіант, заміщена один або два рази замісниками, вибраними з груп: алкіл, циклоалкіл, циклоалкілалкіл, алкокси, гідроксіалкокси, алкоксіалкіл, алкоксіалкокси, циклоалкокси, циклоалкоксіалкіл, циклоалкоксіалкокси, галоген, CF3, CN, NO2, NH2, карбокси, карбамоїл, амід, сульфамоїл та феніл. У найбільш переважному втіленні хінуклідинове похідне винаходу формули І представляє (±)-3-{2-Фенілфенілокси)-1-азадицикло[2.2.2]октан; (±)-3-(3-Фенілфенілокси)-1-азадицикло[2.2.2]октан; (±)-3-(4-Фенілфенілокси)-1-азадицикло[2.2.2]октан; (±)-3-(4-Фенілфенілметокси)-1-азадицикло[2.2.2]октан; (±)-3-(Нафталін-2-ілокси)-1-азадицикло[2.2.2]октан; (±)-3-(5,6,7,8-Тетрагідро-2-нафтилокси)-1-азадицикло[2.2.2]октан; або (±)-3-(5-інданілокси)-1-азадицикло[2.2.2]октан; або його енантіомер, або його фармацевтично прийнятну адитивну сіль, або його онієву сіль. У шостому переважному втіленні хінуклідинове похідне винаходу є сполукою формули І, де А представляє моноциклічну або поліциклічну гетероциклічну групу, вибрану з груп: піридил, зокрема, пірид-2-іл, пірид-3-іл та пірид-4-іл; тієніл, зокрема, тієн-2-іл та тієн-3-іл; фураніл, зокрема, фуран-2-іл та фуран-3-іл; піридазиніл, зокрема, піридазин-3-іл та піридазин-4-іл; тіазоліл, зокрема, тіазол-2-іл, тіазол-4-іл та тіазол-5-іл; тіадіазоліл, зокрема, 1,3,4-тіадіазол-2-іл, 1,3,4-тіадіазол-5-іл, 1,2,4-тіадіазол-З-іл та 1,2,4-тіадіазол-5-іл; хінолініл, зокрема, хінолін-2-іл, хінолін-3-іл, хінолін-4-іл, хінолін-5-іл та хінолін-6-іл; хіноксалініл, зокрема, хіноксалін-2-іл та хіноксалін-3-іл; бензімідазоліл, зокрема, бензі-мідазол-2-іл; бензоксазоліл, зокрема, бензоксазол-2-іл; бензтіазоліл, зокрема, бензтіа-зол-2-іл; де моноциклічна. або поліциклічна гетероциклічна група, як варіант, заміщена одним або більше замісниками, вибраними із груп: алкіл, циклоалкіл, циклоалкілалкіл, алкокси, гідроксіалкокси, алкоксіалкіл, алкоксіалкокси, циклоалкокси, циклоалкоксіалкіл, циклоалкоксіалкокси, галоген, CF3, CN, NO2 , NH2, карбокси, карбамоїл, амід, сульфамоїл, та феніл, або іншою моноциклічною або поліциклічною, карбоциклічною або гетероциклічною групою, де додаткова моноциклічна або поліциклічна, карбоциклі-чна або гетероциклічна група, як варіант, заміщена одним або більше замісниками, вибраними з груп: алкіл, циклоалкіл, циклоалкілалкіл, алкокси, гідроксіалкокси, алкоксіалкіл, алкоксіалкокси, циклоалкокси, циклоалкоксіалкіл, циклоалкоксіалкокси, галоген, CF3, CN, NO2, NH2, карбокси, карбамоїл, амід, сульфамоїл, та феніл. У сьомому переважному втіленні хінуклідинове похідне винаходу є сполукою формули І, де А представляє моноциклічну групу, вибрану з груп: піридил, зокрема, пірид-2-іл, пірид-3-іл та пірид-4-іл; тієніл, зокрема, тієн2-іл та тієн-3-іл; фураніл, зокрема, фуран-2-іл та фуран-3-іл; піридазиніл, зокрема, піридазин-3-іл та піридазин4-іл; тіазоліл, зокрема, тіазол-2-іл, тіазол-4-іл та тіазол-5-іл; тіадіазоліл, зокрема, 1,3,4-тіадіазол-2-іл, 1,3,4тіадіазол-5-іл, 1,2,4-тіадіазол-З-іл та 1,2,4-тіадіазол-5-іл; де моноциклічна гетероциклічна група, як варіант, заміщена одним або більше циклічна група, як варіант, заміщена одним або більше замісниками, вибраними з груп: алкіл, циклоалкіл, алкокси, циклоалкокси, галоген, CF3, CN, NO2, NH2, феніл, 2-тіеніл, 3-тієніл, 2-фураніл, 3-фураніл, та 3-піридиніл, феніл, в яких групи 2-тієніл, 3-тієніл, 2-фураніл, 3-фураніл, та 3-піридиніл можуть, як варіант, бути заміщеними заміщена одним або двома замісниками, вибраними з груп: алкіл, циклоалкіл, алкокси, галоген, CF3, CN, NO2, NH2, та феніл. У найбільш переважному втіленні хінуклідинове похідне винаходу формули І представляє (±)-3-(3,4,5-Трихлортієн-2-ілокси)-1-азадицикло[2.2.2]октан; (±)-3-(5-Бромтіазол-2-ілокси)-1-азадицикло[2.2.2]октан; (±)-3-(5-Фенілтіазол-2-ілокси)-1-азадицикло[2.2.2]октан; (±)-3-[5-(2,4-Дифлуорфеніл)-тіазол-2-ілокси]-1-азадицикло[2.2.2]октан; (±)-3-[5-{3-Тіеніл)-тіазол-2-ілокси]-1-азадицикло[2.2.2]октан; (±)-3-[5-{2-Тієніл)-тіазол-2-ілокси]-1-азадицикло[2.2.2]октан; (±)-3-[5-(3-Фураніл)-тіазол-2-ілокси]-1-азадицикло[2.2.2]октан; (±)-3-[5-(3-Піридил)-тіазол-2-ілокси]-1-азадицикло[2.2.2]октан; (±)-3-(6-Хлорпіридазин-3-ілокси)-1-азадицикло[2.2.2]октан; (±)-3-(6-Бромпіридазин-3-ілокси}-1-азадицикло[2.2.2]октан; (±}-3-(6-Фенілпіридазин-3-ілокси)-1-азадицикло[2.2.2]октан; (±)-3-[6-(3-Тієніл)-піридазин-3-ілокси]-1-азадицикло[2.2.2]октан; (±)-3-[6-(2-Тієніл)-піридазин-3-ілокси]-1-азадицикло[2.2.2]октан; (±)-3-[6-(2-Фураніл)-піридазин-3-ілокси]-1-азадицикло[2.2.2]октан; (±)-3-[6-{3-Фураніл)-піридазин-3-ілокси]-1-азадицикло[2.2.2]октан; (±)-3-[6-(3-Піридил)-піридазин-3-ілокси]-1-азадицикло[2.2.2]октан; (±)-3-(5-Феніл-1,3,4-тіадіазол-2-ілокси)-1-азадицикло[2.2.2]октан; (±)-3-(5-Феніл-1,2,4-тіадіазол-3-ілокси)-1-азадицикло[2.2.2]октан; або (±)-3-[5-(2-Тієніл)-1,3,4-тіадіазол-2-ілокси]-1-азадицикло[2.2.2]октан; або його енантіомер, або його фармацевтично прийнятну адитивну сіль, або його онієву сіль. У восьмому переважному втіленні хінуклідинове похідне винаходу є сполукою формули І, де А представляє поліциклічну гетероциклічну гр упу, вибрану з гр уп: індоліл, зокрема, індол-2-іл та індол-3-іл; ізоіндоліл, зокрема, ізоіндол-2-іл; хінолініл, зокрема, хінолін-2-іл, хінолін-3-іл, хінолін-4-іл, хінолін-5-іл та хінолін-6-іл; хіноксалініл, зокрема, хіноксалін-2-іл та хіноксалін-3-іл; бензімідазоліл, зокрема, бензімідазол-2-іл; бензокса-золіл, зокрема, бензоксазол-2-іл; бензтіазоліл, зокрема, бензтіазол-2-іл; бен-зизотіазоліл, зокрема, бензизотіазол-3-іл; бензтриазоліл, зокрема, 1,2,3-бензтриазол-1-іл; [1,2-b]піридазиніл, зокрема, імідазо[1,2Ь]піридазин-6-іл: дібензофураніл, зокрема, дібензофуран-2-іл; де моноциклічна або поліциклічна гетероциклічна група, як варіант, заміщена одним або більше замісниками, вибраними з груп: алкіл, циклоалкіл, алкокси, циклоалкокси, галоген, CF3, CN, NO2, NH2, та феніл, фенільна група котрої може, як варіант, бути заміщеною одним або більше замісниками, вибраними з груп: алкіл, циклоалкіл, алкокси, галоген, CF3, CN, NO 2, NH2, та феніл. У найбільш переважному втіленні хінуклідинове похідне винаходу формули І представляє (±)-3-[(1,3-Діон)-2-ізоіндолілметокси]-1-азадицикло[2.2.2]октан; (±)-3-[(1,3-Діон)-2-ізоіндолілетокси]-1-азадицикло[2.2.2]октан; (±)-3-{2-Хінолінілокси)-1-азадицикло[2.2.2]октан; (±)-3-(2-Хінолінілокси)-1-азадицикло[2.2.2]октан метиліум йодид; (±)-3-(6-Хінолінілокси)-1-азадицикло[2.2.2]октан; (±)-3-(2-Хіноксалінілокси}-1-азадицикло[2.2.2]октан; (±)-3-{2-Хіноксалінілокси)-1 -азадицикло[2.2.2]октан метиліум йодид; (±)-3-(3-Хлор-2-хіноксалінілокси)-1-азадицикло[2.2.2]октан; (±)-3-(3-Метокси-2-хіноксалінілокси)-1-азадицикло[2.2.2]октан; (±)-3-(Бензоксазол-2-ілокси)-1-азадицикло[2.2.2]октан; (±)-3-(Бензотіазол-2-ілокси)-1-азадицикло[2.2.2]октан; (±)-3-(6-Хлор-бензотіазол-2-ілокси)-1-азадицикло[2.2.2]октан; (±)-3-(1,2-Бензоізотіазол-3-ілокси)-1-азадицикло[2.2.2]октан; (±)-3-(1,2-Бензоізотіазол-3-ілокси)-1 -азадицикло[2.2.2]октан; (±)-3-(1 -Метилбензоімідазолі-2-ілокси)-1 -азадицикло[2.2.2]октан; або (±)-3-(Бензотриазол-1-ілокси)-1-азадицикло[2.2.2]октан; або його енантіомер, або його фармацевтично прийнятну адитивну сіль, або його онієву сіль. В іншому переважному втіленні хінуклідинове похідне винаходу є сполукою формули II n дорівнює 1,2 або 3, X вибрано з груп: -О-, -О-СН2-, -О-СН2-СН2-, -S-, -SO-, -SO2, -CH2-, -S-CH2-CH2-, -СН2-, -С(=СН2)-, -NH-, ІЧ(алкіл)-, -С(=О)-, -C(=S)-, Y представляє О, S, SO2 , або NR', де R' представляє гідроген або алкіл. У більш переважному втіленні цього аспекту хінуклідинове похідне винаходу є сполукою формули II, де ......представляє одиничний (ковалентний) зв'язок. В іншому переважному втіленні цього аспекту хінуклідинове похідне винаходу є сполукою формули II, де п дорівнює 1, 2 або 3. У третьому переважному втіленні цього аспекту хінуклідинове похідне винаходу є сполукою формули II, де X вибрано з груп: -О-, -О-СН 2-, -О-СНа-СНг, -S-, та -СН2-. У четвертому переважному втіленні цього аспекту хінуклідинове похідне винаходу є сполукою формули II, де Y представляє О, S, SO2 , або NR', де R' представляє гідроген або алкіл. У найбільш переважному втіленні хінуклідинове похідне винаходу формули II представляє (±)-3-(Дібензофуран-2-ілокси)-1-азадицикло[2.2.2]октан; або його енантіомер, або його фармацевтично прийнятну адитивну сіль, або його онієву сіль. У ще іншому переважному втіленні хінуклідинове похідне винаходу є сполукою формули III X вибрано з груп: -О-, -О-СН2-, -О-СН2-СН2, -S-, -SO-, -SO2 , -CH2-, -S-CH2-CH2-, -СН2-, -С(=СН2)-, -NH-, М(алкіл)-, -С(=О)-, -C(=S)-, В представляє моноциклічну або поліциклічну, карбоциклічну або гетероциклічну групу, як варіант, заміщену одним або більше замісниками, вибраними із груп: алкіл, ци-клоалкіл, циклоалкілалкіл, алкокси, гідроксіалкокси, алкоксіалкіл, алкоксіалкокси, циклоалкокси, циклоалкоксіалкіл, циклоалкоксіалкокси, галоген, CF3, CN, NO2 , NH2, карбокси, карбамоїл, амід, сульфамоїл, та феніл, або іншою моноциклічною або поліциклічною, карбоциклічною або гетероциклічною групою, де додаткова моноциклічна або поліциклічна, карбоциклічна або гетероциклічна група може, як варіант, бути заміщеною одним або більше замісниками, вибраними з груп: алкіл, циклоалкіл, циклоалкілалкіл, алкокси, гідроксіалкокси, алкоксіалкіл, алкоксіалкокси, циклоалкокси, циклоалкоксіалкіл, циклоалкоксіалкокси, галоген, CF3, CN, NO2, NH2, карбокси, карбамоїл, амід, сульфамоїл та феніл; У більш переважному втіленні цього аспекту хінуклідинове похідне винаходу є сполукою формули III, де представляє одиничний (ковалентний) зв'язок. В іншому переважному втіленні цього аспекту хінуклідинове похідне винаходу є сполукою формули III, де п дорівнює 1, 2 або 3. У третьому переважному втіленні цього аспекту хінуклідинове похідне винаходу є сполукою формули III, де X вибрано з груп: -О-, -О-СН 2-, -О-СН 2-СН2, -S-, та -СН2-. У четвертому переважному втіленні цього аспекту хінуклідинове похідне винаходу є сполукою формули III, де В представляє моноциклічну або поліциклічну, карбоциклічну або гетероциклічну групу, як варіант, заміщену одним або більше замісниками, вибраними із груп: алкіл, циклоалкіл, циклоалкілалкіл, алкокси, гідроксіалкокси, алкоксіалкіл, алкоксіалкокси, циклоалкокси, циклоалкоксіалкіл, циклоалкоксіалкокси, галоген, CF3, CN, NO2 , NH2, карбокси, карбамоїл, амід, сульфамоїл, та феніл, або іншою моноциклічною або поліциклічною, карбоциклічною або гетероциклічною групою, де додаткова моноциклічна або поліциклічна, карбоциклічна або гетероциклічна група може як варіант, бути заміщеною одним або більше замісниками, вибраними з груп: алкіл, циклоалкіл, циклоалкілалкіл, алкокси, гідроксіалкокси, алкоксіалкіл, алкоксіалкокси, циклоалкокси, циклоалкоксіалкіл, циклоалкоксіалкокси, галоген, CF3, CN, NO2, NH2, карбокси, карбамоїл, амід, сульфамоїл, та феніл; У п'ятому переважному втіленні цього аспекту хінуклідинове похідне винаходу є сполукою формули III, де В представляє фенільну груп у, де феніл, як варіант, заміщено одним або двома замісниками, вибраними з груп: алкіл, циклоалкіл, алкокси, циклоалкокси, галоген, CF3, CN, NO2, NH2, та феніл. У найбільш переважному втіленні хінуклідинове похідне винаходу формули II! представляє. (±)-3-(2-Фенілімідазо[1,2-b]піридазин-6-ілокси)-1-азадицикло[2.2.2]октан; або його енантіомер, або його фармацевтично прийнятну адитивну сіль, або його онієву сіль. Будь-яка комбінація двох або більше описаних тут утілень, розглядається у рамках представленого винаходу. Визначення замісників У контексті цього винаходу галоген представляє флуор, хлор, бром або йод. Відповідно тригалогенметильну груп у представляє, наприклад, трифлуорметил, трихлор-метил, та, подібно, тригалогензаміщені метильні групи. У контексті цього винаходу алкільна група означає одновалентний насичений, лінійний або розгалужений вуглеводневий ланцюг. Вуглеводневий ланцюг переважно містить від одного до вісімнадцятьох атомів карбону (С1-18-алкіл), ще краще - від одного до 6 атомів карбону (С1-6-алкіл; нижчий алкіл), охоплюючи пентил, ізопентил, неопентил, третинний пентил, гексил та ізогексил. У переважному втіленні алкіл представляє С 14алкільну групу, охоплюючи бутил, ізобутил, вторинний бутил та третинний бутил. В іншому переважному втіленні цього винаходу алкіл представляє С 1-3-алкіл, котрий може, зокрема, бути метилом, етилом, пропілом або ізопропілом. У контексті цього винаходу циклоалкільна група означає циклічну алкільну груп у, яка переважно містить від трьох до семи атомів карбону (С3-7-циклоалкіл), охоплюючи циклопропіл, циклобутил, циклопентил, циклогексил та циклогептил. У контексті цього винаходу циклоалкілалкільна група означає циклоалкільну гр упу, яка визначена вище, де циклоалкільна група заміщена на алкільній групі, яка також визначена вище. Приклади переважних циклоалкілалкільних гр уп винаходу о хоплюють циклопропілметил та циклопропілетил. У контексті цього винаходу алкоксигрупа означає "алкіл-О" груп у, де алкіл визначено вище. Приклади переважних алкоксигруп винаходу о хоплюють метоксил та еток-сил. У контексті цього винаходу гідроксіалкоксильна група означає алкоксигрупу, яка визначена вище, де алкоксигрупа заміщена одною або більше гідроксигрупами. Переважні гідроксіалкоксигрупи винаходу охоплюють 2-гідроксіетоксил, 3-гідроксипропоксил, 4-гідроксибутоксил, 5-гідроксипентоксил та 6-гідроксил. У контексті цього винаходу циклоалкоксигрупа означає "циклоалкіл-О-"-груп у, де циклоалкіл визначено вище. У контексті цього винаходу алкоксіалкілгрупа означає "алкіл-О-алкіл-"-групу, де алкіл визначено вище. Приклади переважних алкоксіалкілгруп винаходу охоплюють мето-ксиметил, метоксіетил, етоксиметил, та етоксіетил. У контексті цього винаходу алкоксіалкоксигрупа означає "алкіл-О-алкіл-О-"-групу, де алкіл визначено вище. Приклади переважних алкоксіалкоксигруп винаходу охоплюють метоксиметоксил, метоксіетоксил, етоксиметоксил, та етоксіетоксил. У контексті цього винаходу циклоалкоксіалкілгрупа означає "циклоалкіл-О-алкіл"-групу, де циклоалкіл та алкіл визначено вище. У контексті цього винаходу циклоалкоксіалкоксигрупа означає "циклоалкіл-О-алкіл-О-"-групу, де циклоалкіл та алкіл визначено вище. У контексті цього винаходу моно- або поліциклічна карбоциклічна група є моно-або поліциклічною карбоциклічною групою, що містить карбон тільки як атом кільця. Структура кільця може, зокрема, бути ароматичною (тобто арилгрупою), або насиченою, або частково насиченою. Переважні моно- або поліциклічні карбоциклічні групи винаходу охоплюють феніл; інданіл, зокрема, 4інданіл та 5-інданіл; інденіл, зокрема, 1-інденіл, 2-інденіл та 3-інденіл; нафтил, зокрема, 1-нафтил та 2нафтил; 5,6,7,8-тетрагідронафтил, зокрема, 5,6,7,8-тетрагідро-1-нафтил та 5,6,7,8-тетрагідро-2-нафтил; азуленіл, зокрема, 1-азуленіл, 2-азуленіл та 3-азуленіл; флуореніл, зокрема, 1-флуореніл, 2-флуореніл, 3флуореніл та 4-флуореніл; та антраценіл, зокрема, 1-антраценіл та 2-антраценіл. Моно- або поліциклічна карбоциклічна група може, зокрема, бути ароматичною групою (арил). Переважні арильні групи винаходу охоплюють феніл; інденіл, зокрема, 1-інденіл, 2-інденіл та 3-інденіл; нафтил, зокрема, 1-нафтил та 2-нафтил; азуленіл, зокрема, 1-азуленіл, 2-азуленіл та 3-азуленіл; та антраценіл, зокрема, 1антраценіл та 2-антраценіл. У контексті цього винаходу моно- або поліциклічна гетероциклічна група представляє моно- або поліциклічну сполуку, котра містить один або більше гетероатомів у структурі її кільця. Термін полігетероциклічні групи охоплює бензо-конденсоване, п'яти-та 6-членне гетероциклічне кільце, що містить один або більше гетероатомів. Переважні гетероатоми охоплюють нітроген (N), оксиген (О), та сульфур (S). Одна або більше структур кільця можуть, зокрема, бути ароматичними (тобто гетероариловими). Переважні моноциклічні гетероциклічні групи винаходу о хоплюють піридил, зокрема, пірид-2-іл, пірид-3-іл та пірид-4-іл; тієніл, зокрема, тієн-2-іл та тієн-3-іл; фураніл, зокрема, фуран-2-іл та фуран-3-іл; піридазиніл, зокрема, піридазин-3-іл та піридазин-4-іл; тіазоліл, зокрема, тіазол-2-іл, тіазол-4-іл та тіазол-5-іл; та тіадіазоліл, зокрема, 1,3,4-тіадіазол-2-іл, 1,3,4-тіадіазол-5-іл, 1,2,4-тіадіазол-З-іл та 1,2,4-тіадіазол-5-іл. Переважні поліциклічні гетероциклічні групи винаходу охоплюють індоліл, зокрема, індол-2-іл та індол-3-іл; ізоіндоліл, зокрема, ізоіндол-2-іл; хінолініл, зокрема, хінолін-2-іл, хінолін-3-іл, хінолін-4-іл, хінолін-5-іл та хінолін-6-іл; хіноксалініл, зокрема, хіноксалін-2-іл та хіноксалін-3-іл; бензімідазоліл, зокрема, бензімідазол-2-іл; бензоксазоліл, зокрема, бензоксазол-2-іл; бензтіазоліл, зокрема, бензтіазол-2-іл; бензизотіазоліл, зокрема, бен-зизотіазол-3-іл; бензтриазоліл, зокрема, 1,2,3-бензтриазол-1-іл; імідазо[1,2-Ь]піридазиніл, зокрема, імідазо[1,2-Ь]піридазин-6-іл; та дібензофураніл, зокрема, ді-бензофуран-2-іл. Фармацевтично прийнятні солі. Хінуклідинове похідне винаходу можна пропонувати у будь-якій формі, придатній для призначеного застосування. Придатні форми охоплюють фармацевтично (тобто фізіологічно) прийнятні солі, та до- або пролікарняні форми хінуклідинового похідного винаходу. Приклади фармацевтично прийнятних адитивних солей охоплюють, без обмеження, нетоксичні адитивні солі неорганічних та органічних кислот, як-то гідрохлорид, похідний від хлоридної кислоти, гідробромід, похідний від бромідної кислоти, нітрат, похідний від нітратної кислоти, перхлорат, похідний від хлорної кислоти, фосфат, похідний від фосфа тної кислоти, сульфат, похідний від сульфатної кислоти, форміат, похідний від мурашиної кислоти, ацетат, похідний від оцтової кислоти, аконат, похідний від аконітової кислоти, аскорбат, похідний від аскорбінової кислоти, бензосульфонат, похідний від бензолсульфокислоти, бензоат, похідний від бензойної кислоти, р-фенілакрилат, похідний від коричної кислоти, цитрат, похідний від лимонної кислоти, ембонат, похідний від ембонової кислоти, енантат, похідний від енантової кислоти, фумарат, похідний від фумарової кислоти, глутамат, похідний від глутамінової кислоти, гліколят, похідний від глі-колевої кислоти, лактат, похідний від молочної кислоти, малеат, похідний від малеїнової кислоти, малонат, похідний від малонової кислоти, манделат, похідний від мигдалевої кислоти, метансульфонат, похідний від метансульфокислоти, нафталін-2-сульфонат, похідний від нафталін-2-сульфокислоти, фталат, по хідний від фталевої кислоти, саліцилат, похідний від саліцилової кислоти, сорбат, похідний від сорбінової кислоти, стеарат, похідний від стеаринової кислоти, сукцинат, похідний від бурштинової кислоти, тар-трат, похідний від винної кислоти, толуол-п-сульфонат, похідний від п-толуолсульфокислоти, та подібне. Такі солі можна отримати способами, добре відомими у галузі. Інші кислоти, як-то щавлева кислота, які не вважаються фармацевтично прийнятними, можуть бути корисними у отриманні солей, корисних як інтермедіати у одержанні хімічних сполук винаходу та їх фармацевтично прийнятної кислотно-адитивної солі. Приклади фармацевтично прийнятних катіонних солей хімічної сполуки винаходу містять, без обмежень, сіль натрію, калію, кальцію, магнію, цинку, алюмінію, літію, холіну, лізину, та амонію тощо, хімічних сполук винаходу, що містять аніонну групу. Солі таких катіонів можна отримати способами, добре відомими у галузі. У контексті цього винаходу "онієві солі" N-вмісних сполук також розглядають, як фармацевтично прийнятні солі (аза-онієві солі). Переважно аза-онієві солі містять алкіл-онієві солі, особливо метил- та етил-оніеві солі; циклоалкіл-онієві солі, особливо цикло-пропіл-онієві солі; та циклоалкілалкіл-онієві солі, особливо циклопропілметил-онієві солі. Стереоізомери Хінуклідинові похідні представленого винаходу можуть існувати у (+) та (-) формах, а також у рацемічних формах (±). Рацемати цих ізомерів та самі індивідуальні ізомери находяться у рамках представленого винаходу. Рацемічні форми можна розділяти на оптичні антиподи відомими способами та технічними засобами. Один спосіб розділення діастереоізомерних солей представляє застосування оптично активних кислот, та виділення оптично активних амінових сполук обробкою основою. Інший спосіб розділення рацематів на оптичні антиподи базується на хроматографії на оптично активній матриці. Рацемічні сполуки представленого винаходу можна відповідно розділяти на їх оптичні антиподи, наприклад, фракційною кристалізацією d- або І(тартратів, манделатів, або камфорсульфонатів). Хінуклідинові похідні представленого винаходу можна також розділяти утворенням діастереоізомерних амідів реакцією хімічної сполуки представленого винаходу з оптично активною активованою карбоновою кислотою, як-то похідних (+) або (-) фенілаланіну, (+) або {-) фенілгліцину, (+) або (-) камфанової кислоти або утворенням діастереоізомерних карбаматів реакцією хімічних сполук представленого винаходу з оптично активним хлорформіатом або подібно. Додаткові способи розділення оптичних ізомерів відомі у галузі. Такі способи охоплюють описані в [Jaques J, Collet A, & Wilen S у "Enantiomers, Racemates, та Resolutions", John Wiley та Sons, New York (1981)]. Оптично активні сполуки також можна отримувати з оптично активних вихідних матеріалів. Способи отримання Хінуклідинові похідні винаходу можна отримувати відповідними способами хімічних синтезів, наприклад, описаних у робочих прикладах. Вихідні матеріали для способів, описаних у представленій заявці; відомі або їх можна легко отримувати відповідними способами з наявних у продажу реактивів. Також одну сполуку винаходу можна перетворювати в іншу сполуку винаходу, застосовуючи відповідні способи. Кінцеві продукти реакцій, описані тут, можна виділяти відповідними способами, наприклад, екстракцією, кристалізацією, дистиляцією, хроматографією, т.д. Біологічна активність Представлений винахід стосується нових хінуклідинових похідних, котрі, як знайдено, представляють холінергічні ліганди на нікотинових ацетилхолінових рецепторах (нАХР), та модулятори моноамінових рецепторів, зокрема, транспортерів біогенного аміну, як-то серотонінового рецептору (5-HTR), допамінового рецептору (ДАР) та нора-дренолінового рецептору (НАР), та транспортерів біогенного аміну до серотоніну (5НТ), допаміну (ДА) та норадреналіну (Н А). Також переважні хінуклідинові похідні винаходу показують селективну ос7-активність, як показано у робочих прикладах. Сполуки представленого винаходу, зокрема, можуть бути а гоністами, частковими агоністами, антагоністами та алостеричними модуляторами рецептору. Завдяки їх фармакологічному профілю сполуки винаходу можуть бути корисними для лікування різноманітних хвороб або розладів, які стосуються хвороб ЦНС, хвороб ПНС, хвороб або розладів, що стосуються контрактури гладеньких м'язів, ендокринних хвороб або розладів, хвороб або розладів, що стосуються нейродегенерації, хвороб або розладів, що стосуються запалення, болю, та симптомів абстиненції, обумовлених припиненням зловживання хімічними речовинами. У переважному втіленні хінуклідинові похідні винаходу застосовують для лікування хвороб, розладів, або станів, що стосуються центральної нервової системи. Такі хвороби або розлади охоплюють тривожність, порушення пізнавальної здатності, нестачу здатності до навчання, нестачу та дисфункцію пам'яті, хворобу Альцгеймера, нестачу уваги, розлад з нестачею уваги при гіперактивності (РНУГ), хворобу Паркінсона, хворобу Гентингтона, бічний аміотрофічний склероз, синдром Жилль де ла Туретта, психози, депресію, манію, маніакальну депресію, шизофренію, нав'язливо-невротичні розлади (ННР), панічні розлади, розлади харчування, як-то нервова анорексія, підвищене відчуття голоду та ожиріння, нарколепсію, ноцицепцію, СПІДдеменцію, старече слабоумство, периферичну невропатію, аутизм, дислексію, пізню дискінезію, гіперкінезію, епілепсію, булімію, пост-травматичний синдром, соціальну фобію, порушення сну, псевдодемен-цію, синдром Ганзера, предменструальний синдром, синдром пізньої лютеальної фази, синдром хронічної втоми, мутизм, трихотиломанію, та порушення добового ритму організму. У переважному втіленні хвороби, розлади, або стани, що стосуються центральної нервової системи, для яких застосовують хінуклідинові похідні винаходу, представляють розлади пізнавальної здатності, психози, шизофренію та/або депресію. В іншому переважному втіленні хінуклідинові похідні винаходу можуть бути корисними для лікування хвороб, розладів, або станів, що стосуються контрактури гладеньких м'язів, охоплюючи конвульсивні розлади, стенокардію, передчасні пологи, конвульсії, пронос, астму, епілепсію, пізню, дискінезію, гіперкінезію, передчасну еякуляцію та еректильну утр удненість. У ще одному іншому переважному втіленні хінуклідинові похідні винаходу можуть бути корисними для лікування ендокринних розладів, як-то тиреотоксикозу, феохрома-цитоми, гіпертензії та аритмій. Крім того, в іншому переважному втіленні хінуклідинові похідні винаходу можуть бути корисними для лікування нейродегенеративних розладів, охоплюючи нетривале кисневе голодування та індуковану нейродегенерацію. Ще в одному іншому переважному втіленні хінуклідинові похідні винаходу можуть бути корисними для лікування запальних хвороб, розладів, або станів, охоплюючи запальні розлади шкіри, як-то акне та червоні вугри, хвороба Крона, запалення кишок, виразковий коліт та пронос. Крім того, в іншому переважному втіленні хінуклідинові похідні винаходу можуть бути корисними для лікування слабкого, помірного або навіть важкого болю, гострого, хронічного або рецидивного, а також болю, обумовленого мігренню, післяопераційного болю, та болю фантомних кінцівок. Зокрема, біль може бути невропатичним болем, хронічним головним болем, центральним болем, болем, спорідненим з діабетичною невропатією, пост-терапевтичною невралгією, або травмою периферійного нерва. Нарешті, хін уклідинові похідні винаходу можуть бути корисними для лікування симптомів абстиненції, обумовлених припиненням зловживання речовинами, що викликають звикання. Така речовина, що викликає звикання, охоплює продукти, які містять нікотин, як-то тютюн, опіоїди як-то героїн, кокаїн та морфін, бензодіазепіни та бензодіа-зепіноподібні ліки та алкоголь. Абстиненція від речовини, що викликає звикання, у загальному травматичному досвіді характеризується тривожністю та безнадією, гнівом, тривожністю, труднощами концентрації, дисфорією, зниженням серцевого ритму та зменшенням апетиту та приросту ваги.. У цьому контексті "лікування" охоплює лікування, попередження, профілактику та полегшення симптомів абстиненції та абстиненцію, а також лікування, яке призводить до добровільного зниження зловживання речовинами, що викликають звикання. В іншому аспекті, хінуклідинові похідні винаходу застосовують як діагностичні засоби, наприклад, для ідентифікації та локалізації нікотинових рецепторів у різних тканинах. Фармацевтичні композиції В іншому аспекті винахід стосується нових фармацевтичних композицій, що містять терапевтично ефективну кількість хінуклідинових похідних винаходу. Хоча хімічна сполука винаходу для застосування у терапії може бути застосована у вигляді необроблених хімічних сполук, краще вводити активний інгредієнт, як варіант, у вигляді фізіологічно прийнятної солі у фармацевтичній композиції разом з одним або більше ад'ювантами, наповнювачами, носіями, буферами, розріджувачами, та/або іншими звичайними фармацевтичними допоміжними засобами. У переважному втіленні, винахід стосується фармацевтичної композиції, що містить хінуклідинове похідне разом з одним або більше фармацевтично прийнятними носіями, та, як варіант, з іншими терапевтичними та/або профілактичними інгредієнтами, відомими та застосованими у галузі. Носій(ї) повинен бути "прийнятним" у сенсі сумісності з іншими інгредієнтами композиції та нешкідливості для реципієнта. Фармацевтична композиція винаходу може бути застосована будь-яким зручним способом, котрий відповідає потрібній терапії. Переважні способи застосування охоплюють пероральне застосування, зокрема, у таблетках, капсула х, драже, порошку, або рідинній формі, та парентеральне застосування, зокрема, шкірну, підшкірну, внутрішньом'язову або внутрішньовенну ін'єкцію. Фармацевтична композиція винаходу може бути одержана спеціалістами галузі застосуванням стандартних способів та відповідних способів, доцільних для виготовлення потрібної композиції. Коли потрібно, можна уживати композиції, адаптовані до подовженого виділення активного інгредієнту, Подальші деталі способів формулювання та застосування можна знайти у останньому виданні Remington's Pharmaceutical Sciences (Maack Publishing Co., Easton, PA). Фактичне дозування залежить від природи та суворості хвороби, яку лікують, та є на розсуді лікаря, і може бути змінено титруванням дозування до конкретних обставин цього винаходу для отримання потрібного терапевтичного ефекту. Однак, зараз передбачають, що фармацевтичні композиції, які містять приблизно від 0,1 до 500мг активного інгредієнту у індивідуальній дозі, переважно приблизно від 1 до 100мг, найкраще приблизно від 1 до 10 мг, є придатними для терапевтичного лікування. Активний інгредієнт може бути застосованим по одній або кілька доз на день. Відповідний результат у деяких випадках можна отримати при дозуванні нижче 0,1мкг/кг внутрішньовенно (в.в.) та 1мкг/кг перорально (п.о.). Зараз вважають верхньою межею дозування приблизно 10мг/кг в.в. та 100мг/кг п.о.. Переважні рівні складають приблизно від 0,1мкг/кг до 10мг/кг/день в.в., та приблизно від 1мкг/кг до 100мг/кг/день п.о. Способи терапії Завдяки їх фармакологічному профілю сполуки винаходу можуть бути корисними для лікування різноманітних хвороб або розладів, які стосуються хвороб ЦНС, хвороб (ПНС), хвороб або розладів, що стосуються контрактури гладеньких м'язів, ендокринних . хвороб або розладів, хвороб або розладів, що стосуються нейродегенерації, хвороб або розладів, що стосуються запалення, болю, та симптомів абстиненції, обумовлених припиненням зловживання хімічними речовинами. У іншому аспекті винахід стосується способу лікування або полегшення хвороби або розладу організму тварини, охоплюючи людину, хвороба або розлад котрої, чутливі до дії модулятора моноамінового рецептору, спосіб залучає етап застосування до такого організму тварини, охоплюючи людину, у разі потреби, терапевтично ефективної кількості хінуклідинового похідного винаходу. У контексті цього винаходу термін "лікування" охоплює лікування, попередження, профілактики та полегшення, та термін "хвороба" охоплює нездужання, хвороби, розлади та стани, що стосуються даних хвороб. Зараз розглядається, що придатне дозування знаходиться у діапазоні приблизно від 0,1 до 500 мг активної речовини щоденно, ще краще приблизно від 10 до 70 мг активної речовини щоденно, застосованої один або два рази на день, звичайно, залежно від точності режиму застосування, форми застосування, показання, назустріч котрому спрямоване застосування, суб'єкта втручання, ваги тіла суб'єкта втручання, та подалі від переваги та досвіду відповідального лікаря або ветеринара. Приклади Винахід далі ілюстровано наступними прикладами, які не призначені обмежити рамки заявленого винаходу. Загальні зауваження: Усі реакції, які містять чутливі до повітря реагенти або ін-термедіати, проводять під азотом та у неводних розчинниках. У залучених методиках як сушильний засіб застосовують магній сульфат, і розчинники випаровують під зниженим тиском. Спосіб А (±)-3-(Нафталін-2-ілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука А1) До суміші 2-нафтолу (5,0г, 34,5ммол), (±)-3-хінуклідинолу (2,94г, 23,1ммол), трифенілфосфіну (9,0г, 34,5 у) та тетрагідрофурану (100мл) додають: діетилазодикар-боксилат (5,4мл, 34,5ммол) при кімнатній температурі протягом 30 хвилин. Реакційну суміш перемішують протягом 20 годин при 50°С. Додають водний натрій гідроксид (100мл, 1М). Суміш екстрагують дихлорметаном (3 х 100мл). Хроматографія на силікагелі дихлорметаном, метанолом та конц. аміаком (89:10:1) дає названу сполуку Відповідну сіль отримують додаванням суміші діетилового етеру та метанолу (9:1), насиченої фумаровою кислотою. Вихід 3,7 г (43%). Т.пл. 140,9-141,6°С. (±)-3-(4-Фенілфенілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука А2) Отримують способом А із 4-фенілфенолу. Т.пл. 173,5-185,1 °С. (±)-3-(3-Фенілфенілокси)-1-азадицикло[2.2.2]октан, вільна основа (Сполука A3) Отримують способом А із 3-фенілфенолу. Продукт виділяють у вигляді масла. (±)-3-(2-Фенілфенілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука А4) Отримують способом А із 2-фенілфенолу. Т.пл. 125,4°С. (±)-3-(6-Хінолінокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука А5) Отримують способом А із 6-гідроксихіноліну. Т.пл. 146,0-147,0°С. (±)-3-(5-Інданілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука А6) Отримують способом А із 5-інданолу. Т.пл. 149,3-150,5°С. (±)-3-(5,6,7,8-Тетрагідро-2-нафтилокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука А7) і Отримують способом А із 5,6,7,8-тетрагідро-2-нафтолу. Т.пл. 109,7-111,3°С. Спосіб В (±)-2-(1-Азадицикло[2.2.2]окт-3-ілокси)-хінолін, сіль фумарової кислоти (Сполука В1) Суміш (±)-3-хінуклідинолу (2,0г, 15,7ммол), 2-хлорхіноліну (2,6г, 15,7ммол) та ДМФ (30 мл) перемішують при кімнатній температурі. Додають малими порціями натрій гідрид (0,94 г, 23,6 ммол, 60% у маслі). Реакційну суміш перемішують 1,5 годин при 50°С. додають водний натрій гідроксид (50мл, 1М), подалі екстрагують діетиловим етером (3 х 50мл). Комбіновані ефірні фази промивають водним натрій гідроксидом (2 х 50мл, 1М). Відповідну сіль отримують додаванням діетилового етеру та суміші метанолу (9:1), насиченого фумаровою кислотою. Вихід 4,62г (79%). Т.пл. 160,0-160,5°С. (±)-3-(6-Хлорбензотіазол-2-ілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука В2) Отримують способом В із 2,6-дихлорбензотіазолу. Т.пл. 203-205°С. (+)-3-(Бензотіазол-2-ілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука ВЗ) Отримують способом В із 2-хлорбензотіазолу. Т.пл. 173,7-174,2°С. (±)-2-(1-Азадицикло[2.2.2]окт-3-ілокси)-3-хлорхіноксалін, сіль фумарової кислоти (Сполука В4) Отримують способом В із 2,3-дихлорхіноксаліну. Т.пл. 120,8-122,1°С. (±)-3-(1 -Метилбензоімідазол-2-ілокси)-1 -азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука В5) Отримують способом В із 2-хлор-1-метилбензоімідазолу Т.пл. 184,9-185,9°С. (±)-3-(Бензоксазол-2-ілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука В6) Отримують способом В із 2-хлорбензоксазолу Т.пл. 187,2-188,8°С. (±)-2-(1-Азадицикло[2.2.2]окт-3-ілокси)-хіноксалін, сіль фумарової кислоти (Сполука В7) Отримують способом В із 2-хлорхіноксаліну. Т.пл. 127,7-128,5°С. (±)-3-(6-Фенілпіридазин-3-ілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука В8) Отримують способом В із З-хлор-6-фенілпіридазину. Т.пл. 168,5-172,0°С. (±)-3:{5-Феніл-1,3,4-тіадіазол-2-ілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука В9) Отримують способом В із 2-хлор-5-феніл-1,3,4-тіадіазолу. Т.пл. 168,5-172,0°С. (+)-3-(5-Бромтіазол-2-ілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука В10) Отримують способом В із 2,5-дібромтіазолу, застосовуючи 0°С як температуру реакції. Т.пл. 157,8162,1°С. (±)-3-(1,2-Бензоізотіазол-3-ілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука В11) Отримують способом В із 3-хлор-1,2-бензоізотіазолу. Т.пл. 172,3-173,6°С. (±)-3-(5-Феніл-1,2,4-тіадіазол-3-ілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука В12) Отримують способом В із 3-хлор-5-феніл-1,2,4-тіадіазолу. Т.пл. 155,0-159,3°С. (±)-3-(6-Бромпіридазин-3-ілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука В13) Отримують способом В із 3,6-дібромпіридазину. Т.пл. 152,8°С. (±)-3-(6-Хлорпіридазин-3-ілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука В14) Отримують способом В із 3,6-дихлорпіридазину. Т.пл. 164-164,5°С. (±)-3-(3,4,5-Трихлор-2-ілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука В15) Отримують способом В в умовах: калій трет-бутоксид, краун-етер (18:6), із тетрах-лортіофену. Т.пл. 188189,4°С. (±)-3-(3-Метокси-2-хіноксалінілокси)-1 -азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука В16) Суміш (±)-2-(1-Азадицикло[2.2.2]окт-3-ілокси)-3-хлорхіноксаліну {Сполука В4; 1,38г, 4,76ммол), цезій карбонату (1,55г, 4,76ммол) та метанолу (15мл) перемішують протягом 3 годин при 45°С. Додають водний натрій гідроксид (50мл, 1М), подалі екстрагують діетиловим етером (3 х 50мл). Відповідну сіль отримують додаванням суміші діетилового етеру та метанолу (9:1), насиченої фумаровою кислотою. Вихід 0,51г, 27%, Т.пл. 168,5-170,0°С. (±)-3-[5-(3-Тієніл)-1,3,4-тіадіазол-2-ілокси]-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука В17) Отримують способом В із 2-хлор-5-(3-тіеніл)-1,3,4-тіадіазолу. Т.пл., 186-188°С. (±)-3-[(1,3-Діон)-2-ізоіндолілметокси]-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука В18) Отримують способом В із М-(2-бромметил)-фталіміду. Т.пл.212-213°С. (±)-3-[(1,3-Діон)-2-ізоіндолілетоксил-1-азадицикло[2.2.2]октан-вільна основа (Сполука В19) Отримують способом В із ІЧ-(2-брометил)-фталіміду. Виділена як вільна основа, масло. (±)-3-(Бензотриазол-1-ілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука В20) Отримують способом В із 1-(хлорметил)-1Н-бензотриазолу Т.пл. 163,3-164,5°С. Спосіб С (+)-2-(1 -Азадицикло[2.2.2]окт-3-ілокси)-хіноксалін метиліум, йодид (Сполука С1) У суміш (±)-3-(хіноксалін-2-ілокси)-1-азадицикло[2.2.2]октану (1,27г, 5,0ммол) ди-хлорметану (10мл) додають при -70°С: метилйодид (0,31г, 5,0ммол), розчинений у ди-хлорметані (1,5мл), додають через 10 хвилин. Реакційну суміш перемішують при -70°С протягом 40 хвилин. Реакційну суміш перемішують при кімнатній температурі протягом 3 годин. Осад виділяють фільтрацією. Т.пл. 229-230°С. (+)-2-(1-Азадицикло[2.2.2]окт-3-ілокси)-хінолін метиліум йодид (Сполука С2) Отримують способом С із (±)-2-(1-Азадицикло[2.2.2]окт-3-ілокси)-хіноліну. Т.пл. 156,6-175,2°С. (+)-3-(1,2-Бензоізотіазол-3-ілокси)-1 -азадицикло[2.2.2]октан метиліум йодид (Сполука СЗ) Отримують способом С із (±)-3-(1,2-бензоізотіазол-3-ілокси)-1-азадицикло[2.2.2]октану. Т.пл. 180,1186,4°С. Спосіб D (±)-3-(5-Фенілтіазол-2-ілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука D1) Суміш (±)-3-(5-Бромтіазол-2-ілокси)-1-азадицикло[2.2.2]октану (1,25г, 4,32ммол), фенілборонової кислоти (0,791г, 6,48ммол), Pd(PPh3)4 (0,150г, 0,13ммол), водного калій карбонату (6,5мл, 2М), 1,3-пропандіолу (0,97мл, 13,0ммол) та,1,2-диметоксіетану (30мл) перемішують під зворотнім холодильником протягом 15 годин. Додають водний натрій гідроксид (50 мл, 1 М), суміш екстрагують етилацетатом (3 х 50мл). Хроматографія на силікагелі дихлорметаном, метанолом та конц. аміаком (89:10:1) дає названу сполуку Вихід 3,7г (43%). Відповідну сіль отримують додаванням суміші діетилового етеру та метанолу (9:1), насиченої фумаровою кислотою. Т.пл. 170,9-172,2°С. (+)-3-[5-(2,4-Дифлуор-феніл)-тіазол-2-ілокси]-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука D2) Отримують способом D. Т.пл. 84,3-86,3°С. (+)-3-[5-(3-Тієніл)-тіазол-2-ілокси]-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука D3) Отримують способом D. Т.пл. 68,5-74,3°С. (±)-3-[5-(2-Тієніл)-тіазол-2-ілокси]-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука D4) Отримують способом D. Т.пл. 152,6-154,9°С. (±)-3-[5-(3-Фуранілтіазол-2-ілокси]-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука D5) Отримують способом D. Т.пл. 127,6-136,2°С. (±)-3-[5-(3-Піридил)-тіазол-2-ілокси]-1 -азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука D6) Отримують способом D. Т.пл. 82,7-86,0°С. (±)-3-[6-(3-Тієніл)-піридазин-3-ілокси]-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука D7) Отримують способом D із (±)-3-{6-бромпіридазин-3-ілокси)-1азадицикло[2.2.2]октану. Т.пл. 197,9°С. (±)-3-[6-(2-Тієніл)-піридазин-3-ілокси]-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука D8) Отримують способом D із (±)-3-(6-бромпіридазин-3-ілокси)-1-азадицикло[2.2.2]октану. Т.пл.. 180,3-191,1°С, (±)-3-[6-(2-Фураніл)-піридазин-3-ілокси]-1 -азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука D9) Отримують способом D із (±)-3-(6-бромпіридазин-3-ілокси)-1азадицикло[2.2.2]октану. Т.пл. 175,8-178,2°С. (±)-3-[6-(3-Фураніл)-піридазин-3-ілокси]-1 -азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука D10) Отримують способом D із (±)-3-(6-бромпіридазин-3-ілокси)-1-азадицикло[2.2.2]октану. Т.пл. 224,8-225,4°С. (±)-3-[6-(3-Піридил)-піридазин-3-ілокси]-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука D11) Отримують способом D із (±)-3-(6-бромпіридазин-3-ілокси)-1-азадицикло[2.2.2]октану. Т.пл. 137,2-143,2°С. Спосіб Е (+)-3-(4-Фенілфенілметокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука ED) Суміш (±)-3-хіноклідинолу (2,0г, 15,7ммол), 4-фенілбензилхлориду (3,2г, 15,7ммол), натрій гідриду, 60% у маслі (1,26г, 31,4ммол), та ДМФ (30мл) тримають при 50°С протягом 4,5 годин. Додають водний натрій гідроксид (100мл, 1М). Суміш екстрагують діетиловим етером (3 х 50мл). Хроматографія на силікагелі дихлорметаном, метанолом та конц. аміаком (89:10:1) дає названу сполуку. Ви хід 2,0г (29%). Відповідну сіль отримують додаванням суміші діетилового етеру та метанолу (9:1), насиченої фумаровою кислотою. Т.пл. 159,8-160,4°С. Сполуку також можна назвати (±)-3-(дифеніл-4-ілметокси)-хінуклідином. Спосіб F (±)-3-(2-Фенілімідазо[1,2-b]піридазин-6-ілокси)-1 -азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука F1) До суміші 6-хлор-2-фенілімідазо[1,2-b]піридазину (отримано відповідно J. Heterocycl. CHem. 39, 737, 2002) (3,6 г, 15,7ммол), (±)-3-хінуклідинолу 2,0 г, 15,7ммол) у ДМФ (30мл): через 20 хвилин додають при кімнатній температурі натрій гідрид (1,26 г, • 31,4ммол), подалі перемішують при 50°С протягом 4 годин. Додають водний натрій гідроксид (100 мл, 1 М). Суміш екстрагують діетиловим етером (3 х 100 мл). Хроматографія на силікагелі дихлорметаном, метанолом та конц. аміаком (89:10:1) дає названу сполуку. Ви хід 2,9г (57%). Відповідну сіль отримують додаванням суміші діетилового етеру та метанолу (9:1), насиченої фумаровою кислотою. Т.пл. 211-216°С. Спосіб Г (±)-3-(Дибензофуран-2-ілокси)-1-азадицикло[2.2.2]октан, сіль фумарової кислоти (Сполука G1) До суміші (±)-3-хіноклідинолу (3,0г, 23,6ммол), 2-гідроксидибензофурану (4,3г, 23,6ммол), трифенілфосфіну (9,29г, 35,4ммол) та ТГФ через 40 хвилин при кімнатній температурі додають: діетилазодикарбоксилат (6,3мл, 35,4ммол). Суміш перемішують при 50°С 7 днів. Додають водний натрій гідроксид (100мл, 1М). Суміш екстрагують ди-хлорметаном (3 х 100мл). Хроматографія на силікагелі дихлорметаном, метанолом та конц. аміаком (89:10:1) дає названу сполуку. Ви хід 2,0г (29%). Відповідну сіль фумарової кислоти отримують додаванням суміші діетилового етеру та метанолу (9:1), насиченої фумаровою кислотою. Т.пл. 131,3-133,8°С. Сполуку також можна назвати (±)-3-(Дібензофуран-2-ілокси)-хінуклідином. Біологічна активність Інгібування зв'язування 3Н-a-бунгаротоксину in vitro у мозку щура. У цьому прикладі визначають здатність сполук винаходу зв'язувати ос7-підтип нікотинових рецепторів. сс-Бунгаротоксин є пептидом, виділеним з отрути змії роду Elapidae виду Bungarus multicinctus. Він має високу афінність до нейронального та нервом'язового нікотиновоих рецепторів і діє, як потенціальний антагоніст. 3 Н-ос-Бунгаротоксин мітить нікотинові ацетилхолінові рецептори, утворені ос7-субодиничною ізоформою, знайденою у мозку, та осгізоформою - у нервом'язовому сполученні. Отримання тканини Отримання здійснюють при 0-4°С. Кору головного мозку від самців щурів Wistar (150-250г) гомогенізують протягом 10 секунд у 15мл 20ммол Гепес-буфері, який містить 118ммол NaCI, 4,8ммол КСІ, 1,2ммол MgSO4 та 2,5ммол СаСІ2 (рН 7,5), застосовуючи гомогенізатор Uitra-Turrax. Суспензію тканин центрифугують при 27000 х g протягом 10 хвилин. Надосадкову рідину відкидають та гранулят двічі промивають центрифугуванням при 27000 х g протягом 10 хвилин у 20мл свіжого буферу, та кінцевий гранулят потім ресуспендують у свіжому буфері, котрий містить 0,01% альбуміну бичачої сироватки (35мл на г вихідної тканини) та застосовують для аналізу зв'язування. Аналіз Аліквоти по 500 мкл гомогенату додають до 25 мкл тестового розчину та 25 мкл 3Н-а-бунгаротоксину (2 нМ, кінцева концентрація), перемішують та інкубують протягом 2 годин при 37°С. Неспецифічне зв'язування визначають, застосовуючи (-)-нікотин (1ммол, кінцева концентрація). Після інкубації до зразків додають 5 мл охолодженого льодом Гепес-буферу, який містить 0,05% поліетиленіміну, та заливають на фільтр із скловолокна Whatman GF/C (просочений 0,1% поліетиленіміном принаймні 6 годин) під висмоктуванням, та негайно промивають 2 х 5мл охолодженого льодом буферу. Кількість радіоактивності на фільтрах визначають відповідним лічильником сцинтиляції у рідині. Специфічне зв'язування дорівнює загальному зв'язуванню мінус неспецифічне зв'язування. Експериментальне значення надане, як ІК50 (концентрація тестової речовини, котра інгібує специфічне зв'язування 3Н-a-бунгаротоксину на 50%). Результати цих експериментів представлено нижче у Таблиці 1. Таблиця 1 Інгібування зв'язування 3Н-ос-бунгаротоксину Сполука №, А2 В2 ВЗ В17 D1 D3 D4 D5 D6 D7 D8 ІК50 (мкМ) 0,16 0,18 0,17 0,15 0,052 0,11 0,020 0,048 0,18 0,13 0,053
ДивитисяДодаткова інформація
Назва патенту англійськоюQuinuclidine derivatives and their use
Автори англійськоюPeters, Dan, Olsen, Gunnar, M., Nielsen Elsebet Oestergaard, JORGENSEN TINO DYHRING
Назва патенту російськоюПроизводные хинуклидина и их применение
Автори російськоюПетерс Дан, Ольсен Гуннар М., Нильсен Эльсебет Эстергор, Йергенсен Тино Дюринг
МПК / Мітки
МПК: A61P 11/06, A61K 31/4709, A61P 25/18, A61P 5/24, A61P 9/10, A61P 21/00, A61P 3/04, A61P 15/06, A61P 25/00, C07D 453/00, A61K 31/444, A61P 25/08, A61P 25/02, A61P 25/24, A61P 9/06, A61K 31/501, A61K 31/498, A61P 1/14, A61P 15/10, A61P 5/14, A61K 31/439, A61P 25/22, A61P 9/12, A61P 25/28, A61P 25/16, A61P 25/14, A61P 17/00, A61P 3/00, A61P 21/04, A61P 15/08
Мітки: похідні, хінуклідину, застосування
Код посилання
<a href="https://ua.patents.su/11-78812-pokhidni-khinuklidinu-ta-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Похідні хінуклідину та їх застосування</a>
Попередній патент: Силовий гібридний фільтр
Наступний патент: Замкове кріплення для фіксації знімних покривних протезів у ротовій порожнині
Випадковий патент: Спосіб відновлення та плавлення металовмісної сполуки та пристрій для його здійснення















