Похідні фенілнафталіну, спосіб їх одержання і фармацевтична композиція (варіанти), яка їх містить
Номер патенту: 80580
Опубліковано: 10.10.2007
Автори: Ренар Пьєр, Лезьє Даніель, Пуассоньє-Дюрьє Софі, Беннежан Каролін, Ію Саід, Делягранж Філіп
Формула / Реферат
1. Сполуки формули (І)
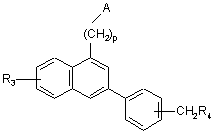 , (I)
, (I)
в якій:
А являє собою групу
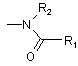 ,
,
в якій R1 являє собою лінійну або розгалужену (С1-С6)алкільну групу або (С3-С8)циклоалкільну групу, і R2 являє собою атом водню,
можливим є, додатково, для R1 і R2 разом утворювати лінійний або розгалужений алкіленовий ланцюг, який містить від 3 до 6 атомів вуглецю,
R3 являє собою лінійну або розгалужену (С1-С6)алкоксигрупу,
R4 являє собою атом галогену, гідроксигрупу, лінійну або розгалужену (С1-С6)алкоксигрупу або аміногрупу, необов'язково заміщену однією або двома лінійними або розгалуженими (С1-С6)алкільними групами,
р дорівнює 1, 2 або 3,
їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою.
2. Сполуки формули (І) за п. 1, де А являє собою групу 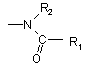 , їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою.
, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою.
3. Сполуки формули (І) за п. 1, де R1 являє собою лінійну або розгалужену (С1-С6)алкільну групу, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою.
4. Сполуки формули (І) за п. 1, де R1 являє собою лінійну або розгалужену (С3-С8)циклоалкільну групу, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою.
5. Сполуки формули (І) за п. 1, де R2 являє собою атом водню, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою.
6. Сполуки формули (І) за п. 1, де р дорівнює 2, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою.
7. Сполуки формули (І) за п. 1, де R3 являє собою метоксигрупу, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою.
8. Сполуки формули (І) за п. 1, де R4 являє собою ОН групу, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою.
9. Сполуки формули (І) за п. 1, де R4 являє собою групу ОМе, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою.
10. Сполуки формули (І) за п. 1, де R4 являє собою NH2 групу, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою.
11. Сполуки формули (І) за п. 1, де R4 являє собою атом галогену, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою.
12. Сполуки формули (І) за п. 1, де група -CH2R4 знаходиться в положенні 3 (мета) на фенільній групі, і їх адитивні солі з фармацевтично прийнятною кислотою або основою.
13. Сполука формули (І) за п. 1, яка являє собою N-(2-{3-[3-(гідроксиметил)феніл]-7-метокси-1-нафтил}етил)ацетамід, і її адитивні солі з фармацевтично прийнятною кислотою або основою.
14. Сполука формули (І) за п. 1, яка являє собою N-(2-{3-[3-(амінометил)феніл]-7-метокси-1-нафтил}етил)ацетамід, і її адитивні солі з фармацевтично прийнятною кислотою або основою.
15. Спосіб одержання сполук формули (І), який відрізняється тим, що як вихідний матеріал використовують сполуку формули (II):
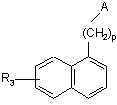 , (II)
, (II)
де А, р і R3 є такими ж, як визначено для формули (І), яку піддають дії брому, з тим, щоб одержати сполуку формули (III):
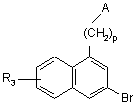 , (III)
, (III)
де А, р і R3 є такими ж, як визначено вище, яку конденсують, у присутності паладій ацетату або тетракис(трифенілфосфін)паладію, зі сполукою формули (IV):
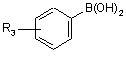 , (IV)
, (IV)
де R5 являє собою лінійну або розгалужену (С1-С6)алкоксикарбонільну групу, групу формілу або ціаногрупу, з тим, щоб одержати сполуку формули (V):
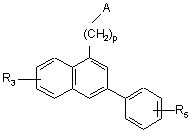 , (V)
, (V)
де А, р, R3 і R5 є такими ж, як визначено вище,
сполуку формули (V),
коли R5 являє собою групу CN, піддають дії нікелю Ренея, щоб одержати сполуку формули (І/а), конкретний випадок сполук формули (І):
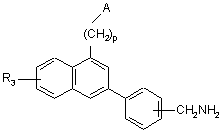 , (I/a)
, (I/a)
де А, р і R3 є таким ж, як визначено вище,
сполуку формули (І/а) піддають дії одного або більше алкілуючих агентів, з тим, щоб одержати сполуку формули (І/b), конкретний випадок сполук формули (І):
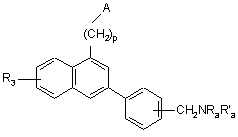 , (I/b)
, (I/b)
де А, р і R3 є такими ж, як визначено вище, Ra являє собою алкільну групу і R'a являє собою атом водню або алкільну групу,
коли R5 являє собою групу формілу, піддають дії NaBH4 або триетилсилану і, коли R5 являє собою алкоксикарбонільну групу, піддають дії LiAlH4, з тим, щоб одержати сполуку формули (I/с), конкретний випадок сполук формули (І):
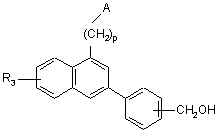 , (I/c)
, (I/c)
де А, р і R3 є таким ж, як визначено вище,
сполуку формули (І/с) піддають дії гідрогалогенової кислоти, з тим, щоб одержати сполуку формули (I/d), конкретний випадок сполук формули (І):
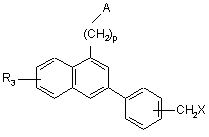 , (I/d)
, (I/d)
де А, р і R3 є таким ж, як визначено вище, і X являє собою атом галогену, або сполуку формули (І/с) піддають дії алкоголяту, з тим, щоб одержати сполуку формули (І/е), конкретний випадок сполук формули (І):
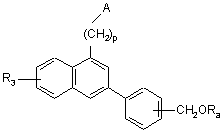 , (I/e)
, (I/e)
де А, р, R3 і Ra є такими ж, як визначено вище,
сполуки (І/а) - (І/е) складають сукупність сполук формули (І), сполуки якої можуть бути очищені відповідно до звичайної техніки очищення, перетворені, якщо бажано, в адитивні солі з фармацевтично прийнятною кислотою або основою, і необов'язково розділені на їх ізомери відповідно до звичайної техніки розділення.
16. Сполуки формули (V’):
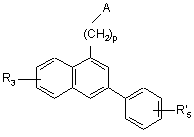 , (V’)
, (V’)
де
А являє собою групу
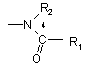 ,
, 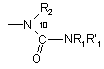 або
або 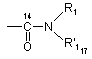
(де R1 і R'1, які можуть бути однаковими або відрізнятись, кожний являє собою лінійну або розгалужену (С1-С6)алкільну групу, лінійну або розгалужену (С2-С6)алкенільну групу, лінійну або розгалужену (С2-С6)алкінільну групу, (С3-С8)циклоалкільну групу, (С3-С8)циклоалкіл-(С1-С6)алкільну групу, в якій алкільна частина може бути лінійною або розгалуженою, арильну групу, арил-(С1-С6)алкільну групу, в якій алкільна частина може бути лінійною або розгалуженою, гетероарильну групу або гетероарил-(С1-С6)алкільну групу, в якій алкільна частина може бути лінійною або розгалуженою,
і R2 являє собою атом водню або лінійну або розгалужену (С1-С6)алкільну групу,
можливим є, додатково, для R1 і R2 разом утворювати лінійний або розгалужений алкіленовий ланцюг, який містить від 3 до 6 атомів вуглецю),
R3 являє собою лінійну або розгалужену (С1-С6)алкоксигрупу,
R’5 являє собою лінійну або розгалужену (С1-С6)алкоксикарбонільну групу або групу формілу,
їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою для застосування як проміжних сполук синтезу для одержання сполук формули (І), але також як лігандів мелатонінергічного рецептора.
17. Фармацевтична композиція, яка містить сполуку формули (І) за будь-яким з пп. 1-14 або сполуку формули (V’) за п. 16, або одну з їх адитивних солей з фармацевтично прийнятною кислотою або основою, в поєднанні з одним або більше фармацевтично прийнятними ексципієнтами.
18. Фармацевтична композиція за п. 17 для застосування в одержанні ліків для лікування розладів мелатонінергічної системи.
19. Фармацевтична композиція за п. 17 для застосування в одержанні ліків для лікування розладів сну, стресу, тривоги, сезонних емоційних розладів або суворої депресії, серцево-судинних патологій, патологій травного тракту, безсоння і втоми через порушення добового режиму організму, шизофренії, нападів паніки, меланхолії, розладів апетиту, ожиріння, безсоння, психотичних розладів, епілепсії, діабетів, хвороби Паркінсона, сенільної деменції, різних розладів, асоційованих з нормальним або патологічним старінням, мігрені, втрати пам'яті, хвороби Альцгеймера і розладів мозкового кровообігу, а також сексуальних дисфункцій, як інгібітор овуляції, імуномодулятор і для лікування різних типів раку.
Текст
1. Сполуки формули (І) A C2 2 (19) 1 3 4. Сполуки формули (І) за п. 1, де R1 являє собою лінійну або розгалужену (С3-С8)циклоалкільну групу, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою. 5. Сполуки формули (І) за п. 1, де R2 являє собою атом водню, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою. 6. Сполуки формули (І) за п. 1, де р дорівнює 2, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою. 7. Сполуки формули (І) за п. 1, де R3 являє собою метоксигрупу, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою. 8. Сполуки формули (І) за п. 1, де R4 являє собою ОН групу, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою. 9. Сполуки формули (І) за п. 1, де R4 являє собою групу ОМе, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою. 10. Сполуки формули (І) за п. 1, де R4 являє собою NH2 групу, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою. 11. Сполуки формули (І) за п. 1, де R4 являє собою атом галогену, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою. 12. Сполуки формули (І) за п. 1, де група -CH2R4 знаходиться в положенні 3 (мета) на фенільній групі, і їх адитивні солі з фармацевтично прийнятною кислотою або основою. 13. Сполука формули (І) за п. 1, яка являє собою N-(2-{3-[3-(гідроксиметил)феніл]-7-метокси-1нафтил}етил)ацетамід, і її адитивні солі з фармацевтично прийнятною кислотою або основою. 14. Сполука формули (І) за п. 1, яка являє собою N-(2-{3-[3-(амінометил)феніл]-7-метокси-1нафтил}етил)ацетамід, і її адитивні солі з фармацевтично прийнятною кислотою або основою. 15. Спосіб одержання сполук формули (І), який відрізняється тим, що як вихідний матеріал використовують сполуку формули (II): A 80580 4 A (CH2)p R3 Br , (III) де А, р і R3 є такими ж, як визначено вище, яку конденсують, у присутності паладій ацетату або тетракис(трифенілфосфін)паладію, зі сполукою формули (IV): B(OH)2 R3 , (IV) де R5 являє собою лінійну або розгалужену (С1С6)алкоксикарбонільну групу, групу формілу або ціаногрупу, з тим, щоб одержати сполуку формули (V): A (CH2)p R3 R5 , (V) де А, р, R3 і R5 є такими ж, як визначено вище, сполуку формули (V), коли R5 являє собою групу CN, піддають дії нікелю Ренея, щоб одержати сполуку формули (І/а), конкретний випадок сполук формули (І): A (CH2)p R3 CH2NH2 , (I/a) де А, р і R3 є таким ж, як визначено вище, сполуку формули (І/а) піддають дії одного або більше алкілуючих агентів, з тим, щоб одержати сполуку формули (І/b), конкретний випадок сполук формули (І): A (CH2)p R3 , (II) де А, р і R3 є такими ж, як визначено для формули (І), яку піддають дії брому, з тим, щоб одержати сполуку формули (III): (CH2)p R3 CH2NRa R'a , (I/b) де А, р і R3 є такими ж, як визначено вище, Ra являє собою алкільну групу і R'a являє собою атом водню або алкільну групу, 5 80580 коли R5 являє собою групу формілу, піддають дії NaBH4 або триетилсилану і, коли R5 являє собою алкоксикарбонільну групу, піддають дії LiAlH4, з тим, щоб одержати сполуку формули (I/с), конкретний випадок сполук формули (І): A 6 А являє собою групу R2 N 4 С R1 O , 14 С O NR1R'1 або С N R3 CH2OH , (I/c) де А, р і R3 є таким ж, як визначено вище, сполуку формули (І/с) піддають дії гідрогалогенової кислоти, з тим, щоб одержати сполуку формули (I/d), конкретний випадок сполук формули (І): A (CH2)p R3 CH2X , (I/d) де А, р і R3 є таким ж, як визначено вище, і X являє собою атом галогену, або сполуку формули (І/с) піддають дії алкоголяту, з тим, щоб одержати сполуку формули (І/е), конкретний випадок сполук формули (І): A (CH2)p R3 CH2ORa , (I/e) де А, р, R3 і Ra є такими ж, як визначено вище, сполуки (І/а) - (І/е) складають сукупність сполук формули (І), сполуки якої можуть бути очищені відповідно до звичайної техніки очищення, перетворені, якщо бажано, в адитивні солі з фармацевтично прийнятною кислотою або основою, і необов'язково розділені на їх ізомери відповідно до звичайної техніки розділення. 16. Сполуки формули (V’): A (CH2)p R3 R'5 , (V’) де R'1 N R1 O (CH2)p R2 10 17 (де R1 і R'1, які можуть бути однаковими або відрізнятись, кожний являє собою лінійну або розгалужену (С1-С6)алкільну групу, лінійну або розгалужену (С2-С6)алкенільну групу, лінійну або розгалужену (С2-С6)алкінільну групу, (С3С8)циклоалкільну групу, (С3-С8)циклоалкіл-(С1С6)алкільну групу, в якій алкільна частина може бути лінійною або розгалуженою, арильну групу, арил-(С1-С6)алкільну групу, в якій алкільна частина може бути лінійною або розгалуженою, гетероарильну групуабо гетероарил-(С1С6)алкільну групу, в якій алкільна частина може бути лінійною або розгалуженою, і R2 являє собою атом водню або лінійну або розгалужену (С1-С6)алкільну групу, можливим є, додатково, для R1 і R2 разом утворювати лінійний або розгалужений алкіленовий ланцюг, який містить від 3 до 6 атомів вуглецю), R3 являє собою лінійну або розгалужену (С1С6)алкоксигрупу, R’5 являє собою лінійну або розгалужену (С1С6)алкоксикарбонільну групу або групу формілу, їх енантіомери і діастереоізомери, і адитивні солі з фармацевтично прийнятною кислотою або основою для застосування як проміжних сполук синтезу для одержання сполук формули (І), але також як лігандів мелатонінергічного рецептора. 17. Фармацевтична композиція, яка містить сполуку формули (І) за будь-яким з пп. 1-14 або сполуку формули (V’) за п. 16, або одну з їх адитивних солей з фармацевтично прийнятною кислотою або основою, в поєднанні з одним або більше фармацевтично прийнятними ексципієнтами. 18. Фармацевтична композиція за п. 17 для застосування в одержанні ліків для лікування розладів мелатонінергічної системи. 19. Фармацевтична композиція за п. 17 для застосування в одержанні ліків для лікування розладів сну, стресу, тривоги, сезонних емоційних розладів або суворої депресії, серцево-судинних патологій, патологій травного тракту, безсоння і втоми через порушення добового режиму організму, шизофренії, нападів паніки, меланхолії, розладів апетиту, ожиріння, безсоння, психотичних розладів, епілепсії, діабетів, хвороби Паркінсона, сенільної деменції, різних розладів, асоційованих з нормальним або патологічним старінням, мігрені, втрати пам'яті, хвороби Альцгеймера і розладів мозкового кровообігу, а також сексуальних дисфункцій, як інгібітор овуляції, імуномодулятор і для лікування різних типів раку. Даний винахід відноситься до нових сполук фенілнафталіну, до способу їх одержання і до фармацевтичних композицій, які їх містять. Сполуки за даним винаходом є новими і володіють фармакологічними властивостями, які представляють великий інтерес відносно мелатонінергічних рецепторів. За останні десять років, численні дослідження продемонстрували значну роль, яку відіграє мелатонін (N-ацетил-5-метокситриптамін) у великій кількості фізіопатологічних явищ і у регулюванні циркадного ритму, але мелатонін має досить короткий період напівжиття внаслідок факту, що він швидко метаболізується. Великий інтерес таким чином полягає у можливості створення доступних для клініциста аналогів мелатоніну, які метаболічно є більш стійкими і мають агоністичний або антагоністичний характер і терапевтичний вплив від яких очікується переважним у порівнянні з впливом самого гормону. На додаток до їх переважної дії відносно розладів циркадного ритму [J. Neurosurg. 1985, 63, pp.321-341] і розладів сну [Psychopharmacology, 1990, 100, pp.222-226], ліганди мелатонінергічної системи володіють цінними фармакологічними властивостями щодо центральної нервової системи, особливо анксіолігичними і антипсихотичними властивостями [Neuropharmacology of Pineal Secretions, 1990, 8 (34), pp.264-272) і анальгетичними властивостями (Pharmacopsychiat., 1987, 20. pp.222-223], а також для лікування хвороби Паркінсона [J. Neurosurg. 1985, 63, рр.321-341] і хвороби Альцгеймера [Brain Research, 1990, 528, pp.170-174]. Сполуки також демонстрували активність відносно конкретних типів раку [Melatonin - Clinical Perspectives, Oxford University Press, 1988, pp.164-165], овуляції [Science 1987, 227, pp.714-720], діабетів [Clinical Endocrinology, 1986, 24. pp.359-364] і у лікуванні ожиріння [International Journal of Eating Disorders, 1996,20 (4), pp.443-446]. Такі різні впливи діють через посередник конкретних рецепторів мелатоніну. Молекулярні біологічні дослідження продемонстрували існування ряду підтипів рецепторів, що здатні до зв'язування цього гормону [Pharmacol. Sci., 1995.16, p.50; WO 97.04094]. Для деяких з таких рецепторів можливим було бути розміщеними і характеризованими для різних видів, включаючи ссавців. Для того, щоб зрозуміти фізіологічні функції рецепторів краще, великою перевагою є наявність доступних селективних лігандів. Крім того такі сполуки, за допомогою взаємодії селективно з тим або іншим з цих рецепторів, можуть бути відмінними ліками для клініциста у лікуванні патологій, пов'язаних з мелатонінергічною системою, деякі з яких були згадані вище. На додаток до того, що вони є новими, сполуки за даним винаходом виявляють дуже сильну афінність для рецепторів мелатоніну і/або селективність для одного або іншого мелатонінергічного сайту зв'язування. Даний винахід відноситься, більш конкретно, до сполук формули (І): (І) де: А являє собою групи (де R1 і R'1, які можуть бути однаковими або відрізнятись, кожний являєсобою лінійну або розгалужену (С1-С6)алкільну групу, лінійну або розгалужену (С2-С6)алкенільну групу, лінійну або розгалужену (С2-С6)алкінільну групу, (С3С8)циклоалкільну групу, (С3-С8)циклоалкіл(С1С6)алкільну групу, в якій алкільна частина може бути лінійною або розгалуженою, арильну групу, арил-(С1-С6)алкільну групу, в якій алкільна частина може бути лінійною або розгалуженою, гетероарильну групу або гетероарил-(С1С6)алкільну групу, в якій алкільна частина може бути лінійною або розгалуженою, і R2 являє собою атом водню або лінійну або розгалужену (С1-С6)алкільну групу, можливим є, додатково, для R1 і R2 разом утворювати лінійний або розгалужений алкіленовий ланцюг, який містить від 3 до 6 атомів вуглецю), R3 являє собою лінійну або розгалужену (С1С6)алкокси групу, R4 являє собою атом галогену, гідрокси групу, лінійну або розгалужену (С1-С6)алкокси групу або аміно групу, необов'язково заміщену однією а(іо двома лінійними або розгалуженими (С1С6)алкільними групами, р дорівнює 1, 2 або 3, повинно бути зрозумілим, що: - "арил" означає фенільну, нафтильну або біфенільну групу, - "гетероарил" означає будь-яку моно- або біциклічну ароматичну групу, яка містить від 1 до 3 гетероатомів, вибраних з кисню, сірки і азоту, де арильна і гетероарильна група, визначені таким чином, можуть заміщуватись за допомогою від 1 до 3 груп, вибраних з лінійного або розгалуженого (С1-С6)алкілу, лінійного або розгалуженого (С1-С6)алкокси, гідрокси, карбокси, формілу, нітро, ціано, лінійного або розгалуженого полігало(С1-С6)алкілу, алкоксикарбонілу і атомів галогену, 9 80580 до їх енантіомерів і діастереоізомерів, і до адитивних солей з фармацевтично прийнятною кислотою або основою. Серед фармацевтично прийнятних кислот можуть бути згадані, без будь-якого обмеження, хлористоводнева кислота, бромистоводнева кислота, сірчана кислота, фосфонова кислота, оцтова кислота, трифтороцтова кислота, молочна кислота, піровиноградна кислота, малонова кислота, янтарна кислота, глутарова кислота, фумарова кислота, винна кислота, малеїнова кислота, лимонна кислота, аскорбінова кислота, оксалінова кислота, метансульфонова кислота, камфорна кислота і т.д. Серед фармацевтично прийнятних основ можуть бути згадані, без будь-якого обмеження, гідроксид натрію, гідроксид калію, триетиламін, трет-бутиламін і т.д. Переважні сполуки за даним винаходом являють собою сполуки формули (І), де А являє собою групу Переважно, R1 являє собою лінійну або розгалужену (С1-С6)алкільну групу, таку як, наприклад, метальну, етильну, n-пропільну або nбутильну групу, або лінійну або розгалужену (С3С8)циклоалкільну групу, таку як, наприклад, циклопропільну або циклобутильну групу. R2 переважно являє собою атом водню. Переважне значення ρ складає 2. Переважна R3 група являє собою метокси групу. R4 переважно являє собою ОН, метокси або групу NH2, або атом галогену, такий як бром або йод. Переважним положенням на фенільному ядрі для групи -CH2R4 є 3 положення (або мета). Навіть більш конкретно, винахід відноситься до наступних сполук формули (І): N-(2-{3-[3(гідроксиметил)феніл]-7-метокси-1нафтил}етил)ацетамід і N-(2-{3-[3(амінометил)феніл]-7-метокси-1нафтил}етил)ацетамід. Енантіомери, діастереоізомери, а також адитивні солі з фармацевтично прийнятною кислотою або основою переважних сполук даного винаходу утворюють невід'ємну частину винаходу. Даний винахід відноситься також до способу одержання сполук формули (І), який відрізняється тим, що як вихідний матеріал використовують сполуку формули (II): (ІІ) де А, р і R3 є такими ж, як визначено для формули (І), яку піддають дії брому, з тим, щоб одержати сполуку формули (III): 10 (ІІІ) де А, р і R3 є такими ж, як визначено вище, яку конденсують, у присутності паладій ацетату або тетракіс(трифенілфосфін)паладію, зі сполукою формули (IV): (ІV) де R5 являє собою лінійну або розгалужену (С1-С6)алкоксикарбонільну групу, групу формілу або ціано групу, з тим, щоб одержати сполуку формули (V): (V) де А, р, R3 і R5 є такими ж, як визначено вище, сполуку формули (V), коли R5 являє собою групу CN, піддають дії нікелю Ренею, щоб одержати сполуку формули (І/а), конкретний випадок сполук формули (І): (І/a) де А, р і R3 є таким ж, як визначено вище, сполука формули (І/а) може бути піддана дії одного або більше алкілуючих агентів, з тим, щоб одержати сполуку формули (І/b), конкретний випадок сполук формули (І): (І/b) де А, р і R3 є такими ж, як визначено вище, Ra являє собою алкільну групу і R'a являє собою атом водню або алкільну групу, коли R5 являє собою групу формілу, піддають дії NaBH4 або триети. їсилану і, коли R5 являє собою алкоксикарбонільну групу, піддають дії LiAlH4, з тим, щоб одержати сполуку формули (І/с), конкретний випадок сполук формули (І): 11 80580 (І/c) де А, р і R3 є таким ж, як визначено вище, сполуку формули (І/с) піддають дії гідрогалогенової кислоти, з тим, щоб одержати сполуку формули (I/d), конкретний випадок сполук формули (І): (І/d) де А, р і R3 є таким ж, як визначено вище, і X являє собою атом галогену, або, сполуку формули (І/с) піддають дії алкоголяту, з тим, щоб одержати сполуку формули (І/е), конкретний випадок сполук формули (І): (І/e) де А, р, R3 і Ra є такими ж, як визначено вище, сполуки (І/а) - (І/е) складають сукупність сполук формули (І), сполуки якої можуть бути очищені відповідно до звичайної техніки очищення, перетворені, якщо бажано, в адитивні солі з фармацевтично прийнятною кислотою або основою, і необов'язково розділені на їх ізомери відповідно до звичайної техніки розділення. Сполуки формули (II) є або комерційно доступними або одержуються кваліфікованим в даній галузі фахівцем за допомогою звичайних хімічних реакцій, які описуються в літературі. Зокрема, одержання сполук формули (II) розкрите, наприклад, в списах до [патентних заявок ЕР 0 447 285 і ЕР 0 745 584]. Винахід відноситься також до сполук формули (V'): (V') де А, р і R3 є такими ж, як визначено для формули (І), і R'5 являє собою лінійну або розгалужену (С1-С6)алкоксикарбонільну групу або групу формілу, до їх енантіомерів і діастереоізомерів, і до адитивних солей з фармацевтично прийнятною кислотою або основою, для застосування як проміжних сполук синтезу для одержання сполук 12 формули (І), але також як лігандів мелатонінергічного рецептору. Фармакологічне дослідження сполук за даним винаходом фактично продемонструвало, що вони є нетоксичними, мають дуже високу селективну афінність до рецепторів мелатоніну і мають суттєву активність щодо центральної нервової системи і, зокрема, виявили, що вони володіють терапевтичними властивостями щодо розладів сну, анксіолітичними, антипсихотичними і анальгетичними властивостями і властивостями щодо мікроциркуляції, що дає можливість встановити, що сполуки за даним винаходом корисні у лікуванні стресу, розладів сну, тривоги, сезонних емоційних розладів або суворої депресії, серцево-судинних патологій, патологій травного тракту, безсоння і втоми завдяки порушенню добового режиму організму, шизофренії, нападів паніки, меланхолії, розладів апетиту, ожиріння, безсоння, психотичних розладів, епілепсії, діабетів, хвороби Паркінсона, сенільної деменції, різних розладів, асоційованих з нормальним або патологічним старінням мігрені, втрати пам'яті, хвороби Альцгеймера, і розладів мозкового кровообігу. В іншому полі активності виявляється, що сполуки даного винаходу можуть бути використані у лікуванні сексуальних дисфункцій, що вони володіють інгібуючими овуляцію та імуномодуляторними властивостями і здатні бути використаними у лікуванні різних типів раку. Сполуки переважно використовувати у лікуванні сезонних емоційних розладів, суворої депресії, розладів сну, серцево-судинних патологій, патологій травного тракту, безсоння і втоми завдяки порушенню добового режиму організму, розладів апетиту і ожиріння. Наприклад, сполуки будуть використані у лікуванні сезонних емоційних розладів, суворої депресії і розладів сну. Даний винахід відноситься також до фармацевтичних композицій, які включають щонайменше одну сполуку формули (І) або одну сполуку формули (V'), одну або в поєднанні з одним або більше фармацевтично прийнятними ексципієнтами. Серед фармацевтичних композицій відповідно до даного винаходу мої суть бути згадані більш конкретно ті, які придатні для орального, парентерального, незального, підабо черезшкірного, ректального, під'язикового, очного або респіраторного введення, особливо таблетки або драже, під'язикові таблетки, саше, желатинові капсули, коржики, супозиторії, креми, мазі, шкірні гелі і придатні для пиття або ін'єктовані ампули. Дозування змінюється відповідно до статі, віку і ваги пацієнта, шляху зведення, природи терапевтичних показань або будь-якого пов'язаного лікування, і знаходиться в діапазоні від 0,01мг до 1г за 24 години за одне або більше введень. Наступні Приклади ілюструють винахід, але не обмежують його жодним чином. Наступні Приготування закінчуються синтезом проміжних сполук для застосування в одержанні сполук за даним винаходом. 13 Приготування 1: N-[2-(3-Бром-7-метокси-1нафтил)етил]ацетамід N-[2-(7-метокси-1-нафтил)етил]ацетамід (29ммол) розчиняють в 160мл оцтової кислоти. Суміш нагрівають до 70°С і бром (35ммол) додають краплями у розчин в 20мл оцтової кислоти. Після перемішування протягом 6 годин при цій температурі, реакційну суміш охолоджують і потім виливають в заморожену воду. Після сильного перемішування протягом 30 хвилин, суміш екстрагують етилацетатом. Етилацетатну фазу сушать над сульфатом магнію і потім випаровують під зменшеним тиском. Залишок, який одержують, перекристалізовують з толуолу, з тим, щоб одержати вказаний у заголовку продукт у формі твердої речовини бежевого кольору. Точка плавлення: 103-105°С Приготування 2: N-[2-(3-Бром-7-метокси-1нафтил)етил]пропанамід Методика є такою ж, як і у Приготуванні 1, із заміною N-[2-(7-метокси-1-нафтил)етил]ацетаміду на N-[2-(7-метокси-1-нафтил)етил]пропанамід. Вказаний у заголовку продукт перекристалізовують з 95° етанолу і виділяють у формі твердої речовини білого кольору. Точка плавлення: 146-148°С Приготування 3: N-[2-(3-Бром-7-метокси-1нафтил)етил]бутанамід Методика є такою ж, як і у Приготуванні 1, із заміною N-[2-(7-метокси-1-нафтил)етил]ацетаміду на N-[2-(7-метокси-1-нафтил)етил]бутанамід. Вказаний у заголовку продукт перекристалізовують з 95°С етанолу і виділяють у формі твердої речовини білого кольору. Точка плавлення: 86-88°С Приготування 4: N-[2-(3-Бром-7-метокси-1нафтил)етил]циклобутанкарбоксамід Методика є такою ж, як і у Приготуванні 1, із заміною N-[2-(7метокси-1-нафтил)етил]ацетаміду на N-[2-(7метокси-1-нафтил)етил]циклобутанкарбоксамід. Вказаний у заголовку продукт перекристалізовують з 95° етанолу і виділяють у формі твердої речовини білого кольору. Точка плавлення: 154-155°С Приготування 5: 1-[2-(3-Бром-7-метокси-1нафтил)етил]-2-піролідинон Методика є такою ж, як і у Приготуванні 1, із заміною N-[2-(7-метокси-1-нафтил)етил]ацетаміду на N-[2-(7-метокси-1-нафтил)етил]-2-піролідинон. Вказаний у заголовку продукт перекристалізовують з 95° етанолу і виділяють у формі твердої речовини білого кольору. Точка плавлення: 137-139°С Приклад 1: N-(2-{3-[2-Гідроксиметил)феніл]-7метокси-1-нафтил}етил)ацетамід Стадія А: N-{2-[3-(2-Формілфеніл)-7-метокси-1нафтил]етил}ацетамід Сполуку, одержану у Приготуванні 1 (6,2ммол), розчиняють в 30мл толуолу і розчин вміщують під потік азоту протягом 10 хвилин. Тетракіс(трифенілфосфін)паладій (0,25ммол) додають до розчину і суміш знову залишають під потоком азоту протягом 10 хвилин. Карбонат натрію (27ммол), розчинений заздалегідь в 10мл води, і 2-формілфенілборонову кислоту (6,8ммол), 80580 14 розчинену заздалегідь в 6мл етанолу, додають до суміші. Реакційну суміш нагрівають зі зворотним холодильником протягом 12 годин і потім охолоджують до температури навколишнього середовища, фільтрують і додають в 50мл води і 50мл етилацетату. Дві фази розділяють і органічну фазу сушать над сульфатом магнію і випаровують під зменшеним тиском. Залишок, який одержують, очищують флеш-хроматографією на силікагелі (ацетон/циклогексан: 2/8), щоб одержати вказаний у заголовку продукт у формі блідо-жовтої олії. Стадія В: N-(2-{3-[2-(Гідроксиметил)феніл]-7метокси-1-нафтил}етил)ацетамід Сполуку, одержану на Стадії А (2,9ммол), розчиняють у 40мл метанолу. Боргідрид натрію (5,8ммол) потім додають невеликими порціями і розчин перемішують при температурі навколишнього середовища протягом 10 хвилин. Метанол випаровують і залишок, який одержують, додають у водний 1N розчин хлористоводневої кислоти і потім екстрагують етилацетатом. Органічну фазу сушать над сульфатом магнію і потім випаровують під зменшеним тиском. Залишок перекристалізовують з циклогексану, щоб одержати вказаний у заголовку продукт у формі твердої речовини блідо-жовтого кольору. Точка плавлення: 57-59°С Приклад 2: N-(2-{3-[3-(Гідроксиметил)феніл]-7метокси-1-нафтил}етил)-ацетамід Стадія А: N-{2-[3-(3-Формілфеніл)-7-метокси-1нафтил]етил}ацетамід Методика є такою ж, як і на Стадії А Прикладу 1, із заміною 2-формілфеніл-боронової кислоти на 3-формілфенілборонову кислоту. Вказаний у заголовку продукт одержують після очищення хроматографією на силікагелі (ацетон/циклогексан: 3/7), у формі твердої речовини білого кольору, яку перекристалізовують з 95° етанолу. Точка плавлення: 123-125° Елементний мікроаналіз: Підраховано Знайдено %С 76,06 75,76 %Н 6,09 6,10 %N 4,03 4,01 Стадія В: N-(2-{3-[3-(Гідроксиметил)феніл]-7метокси-1-нафтил}етил)ацетамід Методика є такою ж, як і на Стадії В Прикладу 1, починаючи зі сполуки, одержаної на Стадії А. Після очищення хроматографією на силікагелі (ацетон/циклогексан: 3/7), вказаний у заголовку продукт одержують у формі твердої речовини білого кольору, яку перекристалізовують з 95° етанолу. Точка плавлення: 153-155°С Елементний мікроаналіз: Підраховано Знайдено %С 75,62 75,33 %Н 6,63 6,61 %N 4,01 4,22 15 80580 Приклад 3: N-(2-{3-[4-Гідроксиметил)феніл]-7метокси-1-нафтил}етил)ацетамід Стадія А: Метил 4-{4-[2-(ацетиламіно)етил]-6метокси-2-нафтил}бензоат Сполуку, одержану у Приготуванні 1 (25ммол), 4-(метоксикарбоніл)фенілборонову кислоту (27ммол), паладій ацетат (0,05ммол), гідрокарбонат натрію (49ммол) і тетрабутиламоній бромід (0,3ммол) розчиняють в суміші діоксан/вода (60мл/40мл). Суміш нагрівають зі зворотним холодильником протягом 4 годин і потім охолоджують до температури навколишнього середовища. Додають 150мл етилацетату і дві фази розділяють. Органічну фазу сушать над сульфатом магнію і випаровують під зменшеним тиском. Залишок, який одержують, очищають хроматографією на силікагелі (ацетон/циклогексан: 3/7), щоб здержати вказаний у заголовку продукт у формі твердої речовини білого кольору, яку перекристалізовують з 95° етанолу. Точка плавлення: 147-149°С Стадія В: N-(2-{3-[4-(Гідроксиметил)феніл]-7метокси-1-нафтил}етил)ацетамід Сполуку, одержану на Стадії А (5,5ммол), розчиняють в 30мл ефіру і 10мл ТГФ. Розчин охолоджують до 0°С і потім літій алюміній гідрид (16,5ммол) додають невеликими порціями. Суміш перемішують при температурі навколишнього середовища протягом 6 годин і потім літій алюміній гідрид гідролізують декількома краплями водного 20% розчину гідроксиду натрію, доки не одержують білий осад. Після фільтрування ефір і ТГФ випаровують під зменшеним тиском і залишок очищують хроматографією на силікагелі (ацетон/циклогексан: 3/7), щоб одержати вказаний у заголовку продукт у формі твердої речовини білого кольору, яку перекристалізовують з 95° етанолу. Точка плавлення: 164-166°С Приклад 4: N-(2-{3-[3-(Бром метил)феніл]-7метокси-1-нафтил)етил)ацетамід Сполуку, одержану у Прикладі (0,6г; 1,7ммол), розчиняють в 10мл льодяної оцтової кислоти і 3,1мл (17ммол) 45% розчину бромистоводневої кислоти в оцтовій кислоті. Суміш перемішують при температурі навколишнього середовища протягом 24 годин і потім виливають в 30мл замороженої води. Утворений осад відфільтровують, відсмоктують і потім перекристалізовують з 95° етанолу, щоб одержати вказаний у заголовку продукт у формі твердої речовини блідо-жовтого кольору. Елементний мікроаналіз: Підраховано Знайдено %С 64,09 63,92 %Н 5,38 5,37 %N 3,40 3,42 Приклад 5: N-(2-{3-[3-(Йодметил)феніл]-7метокси-1-нафтил}етил)ацетамід Сполуку, одержану у Прикладі 4 (0,35г; 0,85ммол), розчиняють в 20мл ацетону і потім до розчину додають 0,14г (0,94ммол) йодиду натрію. 16 Суміш нагрівають зі зворотним холодильником з енергійним перемішуванням протягом двох годин. Після охолодження реакційну суміш фільтрують і потім випаровують ацетон під зниженим тиском. Залишок додають у воду і потім екстрагують ефіром. Органічну фазу сушать над сульфатом магнію, фільтрують і випаровують під зниженим тиском. Одержаний залишок перекристалізовують з толуолу з тим, щоб одержати вказаний у заголовку продукт у формі твердої речовини блідо-жовтого кольору. Точка плавлення: 155-157°С Елементний мікроаналіз: Підраховано Знайдено %С 57,53 57,53 %Н 4,83 4,83 %N 3,05 3,06 Приклад 6: N-(2-{7-Метокси-3-[3(метоксиметил)феніл]-1-нафтил}етил)ацетамід Сполуку, одержану у Прикладі 4 (0,1г; 0,24ммол), розчинену заздалегідь у 2мл метанолу, краплями додають до 10мл свіжоприготованого розчину метанолату натрію (0,012г; 0,48ммол). Суміш нагрівають при кипінні протягом 4 годин. Після охолодження метанол випаровують під зменшеним тиском і залишок додають у воду і екстрагують ефіром. Органічну фазу сушать над сульфатом магнію, фільтрують і потім випаровують під зменшеним тиском. Одержаний залишок перекристалізовують з 95° етанолу, щоб одержати вказаний у заголовку продукт у формі твердої речовини білого кольору. Точка плавлення: 86-87°С Елементний мікроаналіз: Елементний мікроаналіз: Підраховано Знайдено %С 76,01 75,37 %Н 6,93 6,92 %N 3,85 3,82 Приклад 7: N-(2-{3-[3-(Амінометил)феніл]-7метокси-1-нафтил}етил)ацетамід гідрохлорид Стадія А: N-{2-[3-(3-Ціанофеніл)-7-метокси-1нафтил]етил}ацетамід Методика є такою ж, як і на Стадії А Прикладу 1, із заміною 2-формілфенілборонової кислоти на 2-ціанофенілборонову кислоту. Вказану у заголовку сполуку очищують хроматографією на силікагелі (ацетон/гексан: 4/6) і одержують у формі твердої речовини білого кольору після перекристалізації з 95° етанолу. Точка плавлення: 141-143°С Стадія В: N-(2-{3-[3-(Амінометил)феніл]-7метокси-1-нафтил}етил)ацетамід гідрохлорид Сполуку, одержану на Стадії А (1,2г; 3,5ммол), розчиняють в 100мл метанолу. Розчин виливають в автоклав, і потім додають 0,5г нікелю Ренея і розчин насичують газоподібним аміаком. Подають водень доти, доки не досягають тиску в 50 бар, і реакційну суміш перемішують протягом 12 годин при 60°С. Автоклав охолоджують до температури навколишнього середовища, нікель Ренея 17 80580 відфільтровують і метанол випаровують під зменшеним тиском. Залишок додають в етиловий ефір і розчин етилового ефіру, насичений газом НСl, додають краплями доти, доки не одержують осад. Осад потім відфільтровують відсмоктуванням і перекристалізовують з ізопропанолу. Точка плавлення: 239-241°С Приклад 8: N-(2-{3-[3-(Гідроксиметил)феніл]-7метокси-1-нафтил}етил)-пропанамід Стадія А: Метил 3-{6-метокси-4-[2(пропіоніламіно)етил]-2-нафтил}бензоат Методика є такою ж, як і на Стадії Прикладу 3, починаючи зі сполуки, одержаної у Приготуванні 2, і 3-(метоксикарбоніл)фенілборонової кислоти. Вказану у заголовку сполуку одержують у формі твердої речовини білого кольору після перекристалізації з 95° етанолу. Точка плавлення: 113-115°С %С 73,64 73,70 %Н 6,44 6,44 %N 3,58 3,58 Стаді В: N-(2-{3-[3-(Гідроксиметил)феніл]-7метокси-1-нафтил}етил)-пропанамід Методика є такою ж, як і на Стадії В Прикладу 3, починаючи зі сполуки, одержаної на Стадії А. Вказану у заголовку сполуку одержують у формі твердої речовини білого кольору після перекристалізації з 95° етанолу. Точка плавлення: 135-137°С Приклад 9: N-(2-{3-[3-(Гідроксиметил)феніл]-7метокси-1-нафтил}етил)-бутанамід Стадія А: Метил 3-{4-[2-(бутириламіно)етил]-6метокси-2-нафтил}бензоат Методика є такою ж, як і на Стадії А Прикладу 1, починаючи зі сполуки, одержаної у Приготуванні 3 і із заміною 2-формілфенілборонової кислоти на (3-метоксикарбоніл)фенілборонову кислоту. Вказану у заголовку сполуку одержують у формі твердої речовини білого кольору після перекристалізації з 95° етанолу. Точка плавлення: 86-88°С Елементний мікроаналіз: Підраховано Знайдено Підраховано Знайдено %С 74,05 73,93 %Н 6,71 6,77 %N 3,45 3,64 Стадія В: N-(2-{3-[3-(Гідроксиметил)феніл]-7метокси-1-нафтил}етил)бутанамід Методика є такою ж, як і на Стадії В Прикладу 3, починаючи зі сполуки, одержаної на Стадії А. Вказану у заголовку сполуку одержують у формі твердої речовини білого кольору після перекристалізації з 95° етанолу. Точка плавлення: 113-115°С Елементний мікроаналіз: %С %Н %N 76,36 76,21 7,21 7,15 3,71 3,72 Приклад 10: N-(2-{3-[3-(Гідроксиметил)феніл]7-метокси-1-нафтил}етил)-циклобутанкарбоксамід Стадія А: Метил 3-(4-{2[(циклобутилкарбоніл)аміно]етил}-6-метокси-2нафтил)бензоат Методика є такою ж, як і на Стадії А Прикладу 3, починаючи зі сполуки, одержаної у Приготуванні 4. Вказану у заголовку сполуку одержують у φοριν і твердої речовини білого кольору після очищення хроматографією на силікагелі (ацетон/циклогексан:3/7) з наступною перекристалізацією з 95° етанолу. Точка плавлення: 128-130°С Елементний мікроаналіз: Підраховано Знайдено Елементний мікроаналіз: Підраховано Знайдено 18 %С 74,80 74,55 %Н 6,52 6,48 %N 3,35 3,32 Стадія В: N-(2-{3-[3-(Гідроксиметил)феніл]-7метокси-1-нафтил}етил)-циклобутанкарбоксамід Методика є такою ж, як і на Стадії В Прикладу 3, починаючи зі сполуки, одержаної на Стадії А. Вказану у заголовку сполуку одержують у форм: твердої речовини білого кольору після перекристалізації з 95° етанолу. Точка плавлення: 131-133°С Елементний мікроаналіз: Підраховано Знайдено %С 77,09 76,98 %Н 6,99 7,05 %N 3,60 3,53 Приклад 11: 1-(2-{3-[3-(Гідроксиметил)феніл]7-метокси-1-нафтил}етил)-2-піролідинон Стадія А: Метил 3-{6-метокси-4-[2-(2-оксо-1піролідиніл)етил]-2-нафтил}бензоат Методика є такою ж, як і на Стадії А Прикладу 3, починаючи зі сполуки, одержаної у Приготуванні 5. Вказану у заголовку сполуку одержують у формі твердої речовини білого кольору після очищення хроматографією на силікагелі (ацетон/циклогексан:3/7) з наступною перекристалізацією з 95° етанолу. Точка плавлення: 110-112°С Елементний мікроаналіз: Підраховано Знайдено %С 74,42 74,09 %Н 6,25 6,29 %N 3,47 3,63 Стадія В: 1-(2-{3-[3-(Гідроксиметил)феніл]-7метокси-1-нафтил}етил)-2-піролідинон Методика є такою ж, як і а Стадії В Прикладу 3, починаючи зі сполуки, одержаної на Стадії А. Вказану у заголовку сполуку одержують у формі твердої речовини білого кольору після перекристалізації з 95° етанолу. Точка плавлення: 129-131°С 19 Фармакологічні дослідження Приклад А: Дослідження гострої токсичності Гостру токсичність оцінювали після орального введення групам, кожна з яких містить 8 мишей (26±2 грамів). Тварин спостерігали з регулярними проміжками часу протягом першого дня, і щодня протягом наступних двох тижнів лікування. Оцінювали LD50 (доза, яка викликає смерть 50% тварин), і вона демонструвала низьку токсичність сполук даного винаходу. Приклад В: Дослідження на зв'язування рецептора мелатоніну на клітинах вівці Pars tuberalis Дослідження сполук даного винаходу на зв'язування рецептора мелатоніну було проведене відповідно до звичайної техніки на клітинах вівці Pars tuberalis. Pars tuberalis аденогіпофізу фактично характеризується у ссавців високою щільністю рецепторів мелатоніну [Journal of Neuroendocrinology, 1, pp.1-4, 1989]. Протокол 1) Мембрани Pars tuberalis вівці готують і використовують як цільову тканину в експериментах насичення, щоб визначити зв'язувальні можливості і афінностй для 2[125І]йодмелатоніну. 2) Мембрани Pars tuberalis вівці використовують як цільову тканину у порівняльних експериментах на зв'язування, використовуючи різні тест-сполуки у порівнянні з мелатоніном. Кожний експеримент проводять тричі і для кожної сполуки досліджують діапазон різних концентрацій. Результати, після статистичної обробки, дають можливість визначити афінності зв'язування досліджуваної сполуки. Результати Виявляється, що сполуки за даним винаходом мають сильну афінність до рецепторів мелатоніну. Приклад С: 1. Дослідження на зв'язування до рецепторів мелатоніну MT1 і МТ2 Експерименти на зв'язування рецепторів МТ1 або МТ2 проводять, використовуючи 2-[125І]йодмелатонін як посилальний радіоліганд. Радіоактивність, яка підтримується, визначають, використовуючи рідинний сцинтиляційний лічильник. Порівняльні експерименти на зв'язування потім проводять тричі, використовуючи різні тест-сполуки. Для кожної сполуки досліджують діапазон різних концентрацій. Результати дають можливість визначити афінності зв'язування досліджуваних сполук (Kі). 2. Дослідження на зв'язування до сайту мелатоніну МТ3 Експерименти на зв'язування до МТ3 сайтів проводять на мембранах мозку хом'яка, використовуючи 2-[125І]-йодмелатонін як радіоліганд. Мембрани інкубують протягом 30 хвилин з 2-[125І]-йодмелатоніном при температурі 4°С і при різних концентраціях досліджуваних сполук. Після інкубації мембрани швидко фільтрують і потім промивають холодним буфером, використовуючи фільтраційну систему. Радіоактивність, яка підтримується, вимірюють 80580 20 сцинтиляційним лічильником. Значення ІС50 (концентрація, яка інгібує специфічне зв'язування на 50%) підраховують з порівняльних кривих відповідно до моделі нелінійної регресії. Таким чином, Kі значення, знайдені для сполук даного винаходу, показують зв'язування для того або іншого сайту мелатонінергічного зв'язування, і складають £10μΜ. З метою прикладу, сполука Прикладу 2 має K2, що дорівнює 0,36мкМ відносно сайту МТ2, і сполука Прикладу 7 має Ki, що дорівнює 3,40мкМ відносно сайту МТ2. Крім того, сполука, одержана на Стадії А Прикладу 2, має Ki, що дорівнює 0,42мкМ відносно сайту МТ2. Приклад D: Дія сполук даного винаходу на циркадні ритми рухової активності щура Залучення мелатоніну у вплив на більшість фізіологічних, біохімічних і поведінкових циркадних ритмів чергуванням день/ніч зробило можливим встановити фармакологічну модель для дослідження мелатонінергічних лігандів. Впливи сполук досліджують відносно численних параметрів і, зокрема, відносно циркадних ритмів рухової активності, які є надійним індикатором активності ендогенного циркадного годинника. У цьому дослідженні оцінювали впливи таких сполук на конкретній експериментальній моделі, а саме щурі, тимчасово ізольованому (постійна темрява). Експериментальний протокол Одномісячних самців щурів піддавали, як тільки вони доставлялись до лабораторії, світловому циклу: 12 годин світла за 24 години (LD 12:12). Після 2-3 тижневого звикання їх вміщують в клітки, обладнані колесом, приєднаним до реєструючої системи для того, щоб виявити фази рухової активності і таким чином контролювати добовий (LD) або циркадний (DD) ритми. Як тільки ритми, які реєструються, демонструють стійкий характер у світловому циклі LD 12:12, щурів вміщують в постійну темряву (DD). Через два - три тижні, коли вільний хід (ритм, який відображає ритм ендогенного годинника) очевидно встановлений, щурам дають денне введення сполуки, яку досліджують. Спостереження здійснюють за допомогою візуалізації ритмів активності: - вплив світлового ритму на ритми активності, - зникнення впливу на ритми в постійній темряві, - вплив щоденним введенням сполуки; скороминущий або тривалий вплив. Система програмного забезпечення робить можливим: - виміряти тривалість та інтенсивність активності, період ритму тварин протягом вільного ходу і протягом лікування, - демонструвати спектральним аналізом існування циркадного і нециркадного (наприклад ультрадіан) компонентів, де присутні. Результати 21 Очевидно виявляється, що сполуки даного винаходу можуть сильно діяти на циркадні ритмі через мелатонінергічну систему. Приклад Е: Тестування у світлих/темних клітках Сполуки винаходу досліджують на поведінковій моделі, тестування у світлих/темних клітках, яке дає можливість виявити анксиолітичну активність сполук. Обладнання включає дві полівінілові коробки, покриті плексигласом. Одна з коробок знаходиться у темряві. Світильник розміщують над іншою коробкою, даючи інтенсивність світла приблизно 4000 люкс в центрі коробки. Непрозорий пластичний тунель відокремлює світлу коробку від темної коробки. Тварин досліджують індивідуально протягом сеансу у 5 хвилин. Підлогу кожної коробки очищують перед кожним сеансом. На початку кожного дослідження мишу вміщують в тунель, головою до темної коробки. Час, який витрачається мишею в освітленій коробці, і кількість проходжень через тунель записують після першого входу в темну коробку. Після введення сполук за 30 хвилин до початку дослідження, сполуки даного винаходу суттєво збільшують час, який витрачається в освітленій клітці, і кількість проходжень через тунель, що демонструє анксиолітичну активність сполук за даним винаходом. Приклад F: Активність сполук даного винаходу на хвостовій артерії щура Сполуки винаходу досліджували in vitro на хвостовій артерії щура. Мелатонінергічні рецептори присутні в цих судинах, таким чином забезпечуючи відповідну фармакологічну модель для дослідження меалтонінергічної лігандної активності. Стимулювання рецепторів може індукувати або вазоконстрикцію або вазодилатацію, в залежності від артеріального сегмента, який досліджується. Протокол її Одномісячних щурів привчають до циклу світло/темрява 12год./12год. протягом періоду у 23 тижні. Після умертвлення хвостову артерію виділяють і підтримують у високо окисленому середовищі. Артерії потім канулюють на обох кінцях, суспендують вертикально в камері для органу у придатному середовищі і перфузують керез їх проксимальний кінець. Зміни тиску в потоці перфузії роблять можливою оцінку вазоконстрикторного або вазодилаторного впливу сполук. Активність сполук оцінюють на сегментах, які були попередньо скорочені фенілефрином (1мкМ). Криву концентрація/відповідь визначають некумулятивно додаванням концентрації тестсполуки до попередньо скороченого сегмента. Коли ефект, що спостерігається, досягає рівноваги, середовище змінюють і приготування залишають на 20 хвилин перед додаванням тієї ж концентрації фенілефрину і наступної концентрації тест-сполуки. Результати 80580 22 Сполуки винаходу суттєво змінюють діаметр хвостових артерій, які попередньо скорочуються фенілефрином. Приклад G: Фармацевтична композиція: таблетки 1000 таблеток, кожна з яких містить дозу 5мг N-[(2-{3-[3-(гідроксиметил)феніл]-7-метокси-1нафтил}етил)ацетаміду (Приклад 2) 5г пшеничний крохмаль 20г маїсовий крохмаль 20г лактоза 30г стеарат магнію 2г кремнезем 1г гідроксипропілцелюлоза 2г.
ДивитисяДодаткова інформація
Назва патенту англійськоюPhenylnaphtaline derivatives, method of their obtaining and pharmaceutical composition that comprises them
Автори англійськоюPoissonnier Durieux Sophie, Yous Said, Lesieur Daniel, Bennejean Caroline, Delagrange Philippe, Renard Pierre
Назва патенту російськоюПроизводные фенилнафталина, способ их получения и фармацевтическая композиция (варианты), которая их содержит
Автори російськоюПуассонье-Дюрье Софи, Ию Саид, Лезье Даниэль, Беннежан Каролин, Делягранж Филлип, Ренар Пьер
МПК / Мітки
МПК: A61P 9/10, A61P 15/18, A61P 1/00, A61P 37/02, A61P 3/10, A61P 3/04, C07C 233/18, C07D 207/27, A61P 25/00, A61P 3/00, C07C 233/36, A61P 35/00, C07C 233/60
Мітки: спосіб, фенілнафталіну, композиція, похідні, фармацевтична, одержання, варіанти, яка, містить
Код посилання
<a href="https://ua.patents.su/11-80580-pokhidni-fenilnaftalinu-sposib-kh-oderzhannya-i-farmacevtichna-kompoziciya-varianti-yaka-kh-mistit.html" target="_blank" rel="follow" title="База патентів України">Похідні фенілнафталіну, спосіб їх одержання і фармацевтична композиція (варіанти), яка їх містить</a>
Попередній патент: Сполуки піридопіримідинону, спосіб їх одержання і фармацевтична композиція, яка їх містить
Наступний патент: Спосіб визначення фізичних характеристик середовищ
Випадковий патент: Взуття з електрообігрівом















