Дифенілазетидинони, лікарський засіб (варіанти), що містить ці сполуки, і їх застосування
Номер патенту: 80754
Опубліковано: 25.10.2007
Автори: Лінденшмідт Андреас, Флор Штефані, Галіа Ерік, Гломбік Хайнер, Фрік Венделін, Крамер Вернер, ШЕФЕР Ханс-Людвіг, Хойєр Хуберт, Йєне Герхард
Формула / Реферат
1. Cполука формули (І):
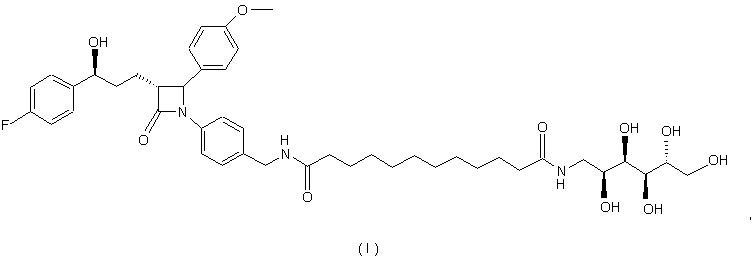
а також її фармацевтично прийнятні солі.
2. Лікарський засіб, що містить сполуку за п.1.
3. Лікарський засіб, що містить сполуку за п.1 і щонайменше одну іншу біологічно активну речовину.
4. Лікарський засіб за п. 3, який відрізняється тим, що як іншу біологічно активну речовину він містить одну або декілька сполук, які нормалізують ліпідний обмін.
5. Лікарський засіб за п. 3 або 4, який відрізняється тим, що як іншу біологічно активну речовину він містить один або декілька антидіабетичних засобів, гіпоглікемічних біологічно активних речовин, засобів проти ожиріння, засобів, що пригнічують апетит, інгібіторів HMGCoA-редуктази, інгібіторів резорбції холестерину, агоністів PPAR-гамма, агоністів PPAR-альфа, агоністів PPAR-альфа/гамма, фібратів, інгібіторів МТР, інгібіторів резорбції жовчної кислоти, інгібіторів СЕТР, полімерних адсорберів жовчної кислоти, активаторів рецептора LDL, інгібіторів АСАТ, антиоксидантів, інгібіторів ліпопротеїн-ліпази, інгібіторів АТФ-цитрат-ліази, інгібіторів скваленсинтетази, антагоністів ліпопротеїну(ів), інгібіторів ліпази, інсулінів, сульфонілсечовин, бігуанідів, меглітинідів, тіазолідиндіонів, інгібіторів ![]() -глюкозидази; біологічно активних речовин, що впливають на АТФ-залежний калієвий канал бета-клітин; агоністів CART, агоністів NPY, антагоністів канабіноїдного рецептора 1, антагоністів рецептора МСН, агоністів МС4, агоністів орексину, агоністів Н3, агоністів фактора некрозу пухлини, агоністів CRF, антагоністів CRF ВР, похідних GLP-1, агоністів урокортину, агоністів
-глюкозидази; біологічно активних речовин, що впливають на АТФ-залежний калієвий канал бета-клітин; агоністів CART, агоністів NPY, антагоністів канабіноїдного рецептора 1, антагоністів рецептора МСН, агоністів МС4, агоністів орексину, агоністів Н3, агоністів фактора некрозу пухлини, агоністів CRF, антагоністів CRF ВР, похідних GLP-1, агоністів урокортину, агоністів ![]() , агоністів MSH (меланоцитстимулюючий гормон), агоністів ССК-А, інгібіторів повторного поглинання серотоніну, змішаних серотонін- і норадренергічних сполук, агоністів 5НТ, агоністів бомбезину, антагоністів галаніну, гормонів росту, сполук, що вивільняють гормон росту, агоністів ТRH, 2- або 3-модуляторів розриваючих зв'язки протеїнів, агоністів лептину, агоністів DA (бромкриптин, допрексин), інгібіторів ліпази/амілази, інгібіторів 11
, агоністів MSH (меланоцитстимулюючий гормон), агоністів ССК-А, інгібіторів повторного поглинання серотоніну, змішаних серотонін- і норадренергічних сполук, агоністів 5НТ, агоністів бомбезину, антагоністів галаніну, гормонів росту, сполук, що вивільняють гормон росту, агоністів ТRH, 2- або 3-модуляторів розриваючих зв'язки протеїнів, агоністів лептину, агоністів DA (бромкриптин, допрексин), інгібіторів ліпази/амілази, інгібіторів 11![]() -HSD1, інгібіторів АСС, інгібіторів DPP-IV, модуляторів PPAR, модуляторів RXR або агоністів TR-
-HSD1, інгібіторів АСС, інгібіторів DPP-IV, модуляторів PPAR, модуляторів RXR або агоністів TR-![]() або амфетамінів.
або амфетамінів.
6. Сполука за п.1 для використання як лікарського засобу для лікування порушень ліпідного обміну.
7. Спосіб отримання лікарського засобу, що містить сполуку за п.1, який відрізняється тим, що діючу речовину змішують з фармацевтично прийнятним носієм і цю суміш переводять в придатну для введення форму.
8. Застосування сполуки за п.1 для отримання лікарського засобу для лікування гіперліпідемії.
9. Застосування сполуки за п.1 для отримання лікарського засобу для зниження рівня холестерину в сироватці.
10. Застосування сполуки за п.1 для отримання лікарського засобу для лікування артеріосклеротичних явищ.
11. Застосування сполуки за п.1 для отримання лікарського засобу для лікування резистентності до інсуліну.
12. Проміжний продукт формули (III):
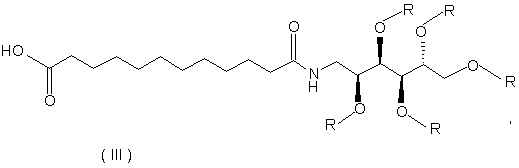
де R означає ацетил, бензоїл, арил, (С1-С12)-алкіларил, (С1-С12)-алкіл.
13. Проміжний продукт формули (IV):
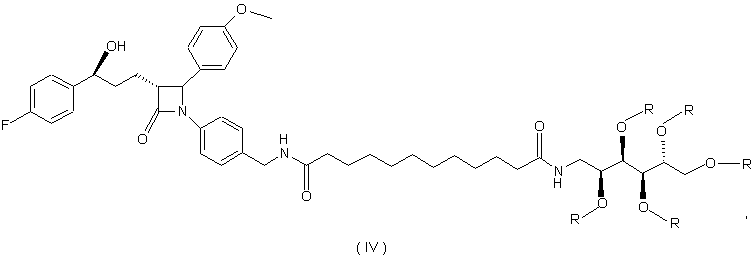
де R означає ацетил, бензоїл, арил, (С1-С12)-алкіларил, (С1-С12)-алкіл.
14. Проміжний продукт формули (VIII):
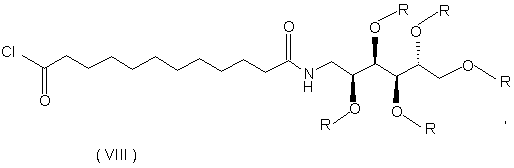
де R означає ацетил, бензоїл, арил, (С1-С12)-алкіларил, (С1-С12)-алкіл.
Текст
1. Cполука формули (І): C2 2 (19) 1 3 80754 4 O 10. Застосування сполуки за п.1 для отримання лікарського засобу для лікування артеріосклеротичних явищ. 11. Застосування сполуки за п.1 для отримання лікарського засобу для лікування резистентності до інсуліну. 12. Проміжний продукт формули (III): R O O R N H R O O O H N O R R O O N H O O R O R R , ( IV ) де R означає ацетил, бензоїл, арил, (С1-С12)алкіларил, (С1-С12)-алкіл. R O O R N F 14. Проміжний продукт формули (VIII): O HO O OH O R , 13. Проміжний продукт формули (IV): Винахід відноситься до заміщеного дифенілазетидінону, його фізіологічно прийнятних солей, а також фізіологічно функціональних похідних. Вже описані дифенілазетидінони, а також їх застосування для лікування гіперліпідемії, як і артеріосклерозу і гіперхолестеринемії [Міжнародна заявка WO-02/50027]. В основу винаходу покладена задача отримання сполуки, яка, в протилежність описаним [в Міжнародній заявці WO-02/50027] сполукам, має виразно підвищену розчинність у верхньому відділі тонкого кишечнику в стані до, відповідно, після вживання їжі. За рахунок підвищеної розчинності сполуки забезпечується більш висока доступність розчиненої речовини в місці дії і разом з тим поліпшена дія. Для тестування цієї підвищеної розчинності використовують середовища FaSSIF (Fasted State Simulating Intestinal Fluid) і FeSSIF (Fed State Simulating Intestinal Fluid), які відображають умови значення рН/солюбілізація у верхній тонкій кишці в стані до, відповідно, після вживання їжі. В основу винаходу, далі, покладена задача отримання сполуки, яка, в протилежність описаним [в Міжнародній заявці WO-02/50027] сполукам, має підвищену стабільність як в кислій області (шлунок), так і також в слаболужній області (тонкий кишечник). Ця властивість приводить до меншої кількості побічних сполук/продуктів розщеплення, які, зі свого боку, можуть чинити небажані побічні дії. Підвищена стабільність в кислій області значень рН, однак, також має велику перевагу при отриманні лікарської форми, оскільки не потрібно кислотостійкої капсули/таблетки. Винахід, отже, відноситься до сполук формули (І):2 R O Cl O N H O ( III ) де R означає ацетил, бензоїл, арил, (С1-С12)алкіларил, (С1-С12)-алкіл. O R O O R R , ( VIII ) де R означає ацетил, бензоїл, арил, (С1-С12)алкіларил, (С1-С12)-алкіл. а також до їх фармацевтично прийнятних солей. Фармацевтично прийнятні солі завдяки своїй високій розчинності у воді, в порівнянні з вихідними, відповідно, основними сполуками, особливо придатні для використань в медицині. Ці солі повинні містити фармацевтично прийнятний аніон або катіон. Придатними фармацевтично прийнятними адитивними солями з кислотами сполуки, що пропонується згідно з винаходом, є солі з неорганічними кислотами, такими як соляна кислота, бромоводнева кислота, фосфорна кислота, метафосфорна кислота, азотна кислота і сірчана кислота, а також з органічними кислотами, такими як, наприклад, оцтова кислота, бензолсульфокислота, бензойна кислота, лимонна кислота, етансульфокислота, фумарова кислота, глюконова кислота, гліколева кислота, ізетіонова кислота,молочна кислота, лактобіонова кислота, малеїнова кислота, яблучна кислота, метансульфокислота, янтарна кислота, птолуолсульфокислота і винна кислота. Придатними фармацевтично прийнятними основними солями є солі амонію, солі лужних металів (як солі натрію і калію), солі лужноземельних металів (як солі магнію і кальцію), трометамолу (2-аміно-2-гідроксиметил-1,3пропандіол), діетаноламіну, лізину або етилендіаміну. Солі з фармацевтично неприйнятним аніоном, такі як, наприклад, трифторацетат, також входять в рамки винаходу як корисні проміжні продукти для отримання або очищення фармацевтично 5 прийнятних солей і/або для використання у разі не терапевтичних, наприклад, in vitro, застосувань. Використовуване в даному контексті поняття "фізіологічно функціональне похідне" означає будь-яке фізіологічно прийнятне похідне сполуки формули (І), що пропонується згідно з винаходом, наприклад, складний ефір, яке при введенні ссавцеві, як, наприклад, людині, здатне (прямо або опосередковано) утворювати сполуку формули (І) або її активний метаболіт. До фізіологічно функціональних похідних відносяться також пролікарські форми сполуки, що пропонується згідно з винаходом, як, [наприклад, описується Н. Okada і інш., Chem. Pharm. Bull., 42, 57-61 (1994)]. Такі пролікарські форми можуть метаболізуватися in vivo до сполуки, що пропонується згідно з винаходом. Ці пролікарські форми самі можуть бути активними або ні. Запропонована згідно з винаходом сполука може бути також в різних поліморфних формах, наприклад, в аморфній або кристалічній поліморфній формі. Всі поліморфні форми сполуки, що пропонується згідно з винаходом, входять в рамки винаходу і складають подальший аспект винаходу. Надалі всі вказівки на "сполуку (сполуки) формули (І)" відносяться до сполуки формули (І), як вона описана вище, а також до її солей, сольватів і фізіологічно функціональних похідних, як ті, що описуються в даному контексті. Під арильним залишком розуміють фенільний, нафтильний, біфенільний, тетрагідронафтильний, альфа- або бета-тетралоновий, інданільний або індан-1-онільний залишок. Сполуку (сполуки) формули (І) можна вводити також в комбінації з іншими біологічно активними речовинами. Кількість сполуки формули (І), яка є необхідною для досягнення бажаного біологічного ефекту, залежить від ряду чинників, наприклад, вибраної конкретної сполуки, передбачуваного застосування, способу введення і клінічного стану пацієнта. Загалом, добова доза складає величину в межах від 0,01мг до 100мг (більш типово, від 0,05мг до 50мг) на добу на кілограм маси тіла, наприклад, 0,1-10мг/кг/добу. Перорально лікарські форми, що вводяться у вигляді разової дози, як, наприклад, таблетки або капсули, можуть містити, наприклад, від 1,0мг до 1000мг, більш типово, від 10мг до 600мг, біологічно активної речовини. Для лікування вищезгаданих станів сполуки формули (І) можна використати індивідуально у вигляді сполуки, переважно, однак, вони знаходяться разом з прийнятним носієм в формі фармацевтичної композиції. Носій, природно, повинен бути прийнятний в тому значенні, що він сумісний з іншими компонентами композиції і не загрожує здоров'ю пацієнта. Носій може являти собою тверду речовину або рідину або і те, й інше, і переважно використовується разом із сполукою для отримання лікарської форми у вигляді разової дози, наприклад, у вигляді таблетки, яка може містити від 0,05мас.% до 95мас.% біологічно активної речовини. Також можуть бути присутніми 80754 6 інші фармацевтично активні речовини, включаючи інші сполуки формули (І). Фармацевтичні композиції, що пропонуються згідно з винаходом, можна отримувати будь-яким з відомих фармацевтичних способів, які по суті полягають в тому, що компоненти змішують з фармакологічно прийнятними носіями і/або допоміжними речовинами. Фармацевтичними композиціями, що пропонуються згідно з винаходом, є такі, які придатні для орального або перорального (наприклад, під'язичного) введення, хоч найприйнятніший шлях введення в кожному окремому випадку залежить від роду і тяжкості стану, що підлягає лікуванню, і від роду сполуки формули (І), що використовується у кожному випадку. У рамки винаходу також входять дражовані готові лікарські форми і дражовані готові лікарські форми пролонгованої дії. Переважні резистентні до кислоти і шлункового соку готові лікарські форми. Придатні, резистентні до шлункового соку покриття включають ацетатфталат целюлози, полівінілацетатфталат, гідроксипропілметилцелюлозофталат і аніонні полімери метакрилової кислоти і метилового ефіру метакрилової кислоти. Придатні фармацевтичні сполуки для перорального введення можуть бути у вигляді окремих разових форм, як, наприклад, капсули, оболонки облаток, таблетки для смоктання або таблетки, які, відповідно, містять певну кількість сполуки формули (І); у вигляді порошків або гранулятів; у вигляді розчину або суспензії у водній або неводній рідині; або у вигляді емульсії масло-в-воді або вода-в-маслі. Ці композиції, як вже згадувалося, можна отримувати будь-яким придатним фармацевтичним способом, що включає стадію, на якій біологічно активну речовину і носій (який може складатися з одного або декількох додаткових компонентів) вводять в контакт. Загалом, композиції готують шляхом рівномірного і гомогенного змішування біологічно активної речовини з рідким і/або високодисперсним твердим носієм, після чого продукт, якщо необхідно, формують. Так, наприклад, таблетки можна отримувати тим, що порошок або гранулят сполуки пресують або формують, у разі необхідності, разом з одним або декількома додатковими компонентами. Пресовані таблетки можна отримувати шляхом таблетування в придатній машині сполуки у вільно текучій формі, як, наприклад, в формі порошку або грануляту, у разі необхідності, змішаного зі зв'язувальною речовиною, що додає ковзкості (таблеткам), інертним розріджувачем і/або однією (декількома) поверхнево-активною речовиною і/або диспергатором. Формовані таблетки можна отримувати шляхом формування в придатній машині порошкоподібної, змоченої інертним рідким розріджувачем сполуки. Фармацевтичні композиції, які придатні для перорального (під'язичного) введення, включають таблетки для смоктання, які містять сполуку формули (І) разом із смаковою речовиною, звичайно сахарозою і гуміарабіком або трагантом, 7 і пастилки, які включають сполуку в інертній основі, такій як желатин і гліцерин або сахароза і гуміарабік. Як інші біологічно активні речовини для комбінованих препаратів придатні: Всі антидіабетичні засоби, які вказуються в Червоному списку 2003, розділ 12. Їх можна комбінувати із сполуками формули (І), що пропонуються згідно з винаходом, особливо для синергічного підвищення дії. Введення комбінації біологічно активних речовин можна здійснювати або шляхом роздільного введення пацієнту біологічно активних речовин, або у вигляді комбінованих препаратів, де декілька біологічно активних речовин знаходяться в одній фармацевтичній композиції. Більшість нижчевказаних біологічно активних речовин вказуються в фармакопейному довіднику США по USAN і міжнародним назвам лікарських засобів, Фармакопеї США, Роквілл, 2001. Антидіабетичні засоби включають інсулін і похідні інсуліну, як, наприклад, Lantus® (див. www.lantus.com) або HMR 1964, інсуліни швидкої дії [див. патент США 6221633], похідні GLP-1, як, наприклад, такі, які описуються [в Міжнародній заявці WO-98/08871 на ім'я фірми Novo Nordisk A/S, в Міжнародній заявці WO-01/04156 на ім'я фірми Zealand або в Міжнародній заявці WO00/34331 на ім'я фірми Beautofour-Ipsen], а також ефективні при пероральному прийомі гіпоглікемічні біологічно активні речовини. Ефективні при пероральному прийомі гіпоглікемічні біологічно активні речовини переважно включають сульфонілсечовини, бігуанідини, меглітиніди, оксадіазолідиндіони, тіазолідиндіони, інгібітори глюкозидази, інгібітори глікогенфосфорилази, антагоністи глюкагону, агоністи GLP-1, відкривачі калієвих каналів, як, наприклад, такі, які описуються [в Міжнародних заявках WO-97/26265 і WO-99/03861 на ім'я Novo Nordisk A/S], сенсибілізатори інсуліну; інгібітори ферментів печінки, які беруть участь в стимуляції глюконеогенезу і/або глікогенолізу; модулятори поглинання глюкози, транспорту глюкози і зворотної резорбції глюкози; сполуки, що змінюють жировий обмін, як антигіперліпідемічні біологічно активні речовини і антиліпідемічні біологічно активні речовини; сполуки, які сприяють зменшенню потреби в продуктах харчування; агоністи PPAR і PXR і біологічно активні речовини, які впливають на АТФ-залежний калієвий канал бета-клітин. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з інгібітором HMGCoA-редуктази, такими як симвастатин, флувастатин, правастатин, ловастатин, аторвастатин, церивастатин, розувастатин. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з інгібітором резорбції холестерину, такими як, наприклад, езетиміб, тиквесид, памаквесид. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з 80754 8 агоністом PPAR-гамма, таким як, наприклад, розиглітазон, піоглітазон, JTT-501,GI 262570. Згідно з варіантом здійснення винаходу, сподуки формули (І) вводять в комбінації з агоністом PPAR-альфа, таким як, наприклад, GW 9578, GW 7647. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з агоністами змішаного PPAR-альфа/гамма, такими як, наприклад, GW 1536, AVE 8042, AVE 8134, AVE 0847, або як описується [в PCT/US 11833, PCT/US 11490, патенті ФРН 10142734.4]. Згідно з варіантом здійснення винаходу, сподуки формули (І) вводять в комбінації з фібратом, таким як, наприклад, фенофібрат, клофібрат, безафібрат. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з інгібітором МТР, таким як, наприклад, імплітапід, BMS-201038, R-103757. Згідно з варіантом здійснення винаходу, сподуки формули (І) вводять в комбінації з інгібітором резорбції жовчної кислоти [див., наприклад, патенти США 6245744 або 6221897], такими як, наприклад, HMR 1741. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з інгібітором СЕТР, таким як, наприклад, JTT-705. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з полімерним адсорбером жовчної кислоти, таким як, наприклад, холестирамін, колесевелам. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з активатором рецептора LDL [див. патент США 6342512], таким як, наприклад, HMR 1171, HMR 1586. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з інгібітором AC AT, таким як, наприклад, авасиміб. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з антиоксидантом, таким як, наприклад, ОРС-14117. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з інгібітором ліпопротеїн-ліпази, таким як, наприклад, NO-1886. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з інгібітором АТФ-цитрат-ліази, таким як, наприклад, SB-204990. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з інгібітором скваленсинтетази, таким як, наприклад, BMS-188494. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з антагоністом ліпопротеїну(а), таким як, наприклад, СІ-1027 або нікотинова кислота. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з інгібітором ліпази, таким як, наприклад, орлістат. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з інсуліном. 9 Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з сульфоніл сечовиною, такою як, наприклад, толбутамід, глібенкламід, гліпізид або глімепірид. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з бігуанідом, таким як, наприклад, метформін. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з меглітинідом, таким як, наприклад, репаглінід. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з тіазолідиндіоном, таким як, наприклад, троглітазон, циглітазон, піоглітазон, розіглітазон, або описаними [в Міжнародній заявці WO97/41097, Dr. Reddy's, Research Foundation], сполуками, особливо, 5-[4-[(3,4-дигідро-3-метил-4оксо-2-хіназолінілметокси)феніл]метил]-2,4тіазолідиндіоном. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з інгібітором α-глюкозидази, таким як, наприклад, міглітол або акарбоза. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з біологічно активною речовиною, яка впливає на АТФ-залежний калієвий канал бета-клітин, такою як, наприклад, толбутамід, глібенкламід, гліпізид, глімепірид або репаглінід. Згідно з варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з більш, ніж однією з вищезгаданих сполук, наприклад, в комбінації з сульфонілсечовиною і метформіном, сульфонілсечовиною і акарбозою, репаглінідом і метформіном, інсуліном і сульфонілсечовиною, інсуліном і метформіном, інсуліном і троглітазоном, інсуліном і ловастатином і т.д. Згідно з іншим варіантом здійснення винаходу, сполуки формули (І) вводять в комбінації з модуляторами CART [див. "Cocaine-amphetamineregulated transcript influences energy metabolism, anxiety and gastric emptying in mice", Asakawa А. та інш., М.: Hormone and Metabolic Research, 33 (9), 554-558 (2001)]; антагоністами NPY, такими як, наприклад, {4-[(4-аміно-хіназолін-2-іламіно)метил] циклогексилметил}амідгідрохлорид нафталін-1сульфокислоти [CGP 71683А]; антагоністами каннабіноїдного рецептора 1 [див., наприклад, Європейський патент 0656354, Міжнародні заявки WO-00/15609 або WO-02/076949]; агоністами МС4 (такими як, наприклад, [2-(3а-бензил-2-метил-3оксо-2,3,3а,4,6,7-гексагідропіразоло[4,3-с]піридин5-іл)-1-(4-хлорфеніл)-2-оксоетил]амід 1-аміно1,2,3,4-тетрагідронафталін-2-карбонової кислоти; [WO-01/91752]; антагоністами орексину (такими як, наприклад, гідрохлорид 1-(2-метилбензоксазол-6іл)-3-[1,5]нафтиридин-4-іл-сечовини [SB-334867-A]; агоністами Н3 (такими як сіль щавлевої кислоти 3циклогексил-1-(4,4-диметил-1,4,6,7тетрагідроімідазо-[4,5-с]піридин-5-іл)пропан-1-ону [WO-00/63208]; агоністами фактора некрозу пухлини; антагоністами CRF (такими як, наприклад, [2-метил-9-(2,4,6-триметилфеніл)-9Н1,3,9-триазафлуорен-4-іл]-дипропіламін [WO00/66585]); антагоністами CRF BP (такими як, 80754 10 наприклад, урокортин); агоністами урокортину; агоністами β3 (такими як, наприклад, 1-(4-хлор-3метансульфонілметилфеніл)-2-[2-(2,3-диметил1H-індол-6-ілокси)етиламіно]етанолгідрохлорид [WO-01/83451]); агоністами MSH (меланоцитстимулюючий гормон); антагоністами рецептора МСН (меланінконцентруючий гормон) [див., наприклад, Міжнародну заявку WO03/15769]; агоністами ССК-А (такими як, наприклад, трифторацетат {2-[4-(4-хлор-2,5диметоксифеніл)-5-(2-циклогексилетил)тіазол-2ілкарбамоїл]-5,7-диметиліндол-1-іл}оцтовоі кислоти [WO-99/15525] або SR-146131 [WO0244150] або SSR-125180); інгібіторами повторного поглинання серотоніну (такими як, наприклад, дексфенфлурамін); змішаними серотонін- і норадренергічними сполуками [див., наприклад, WO-00/71549]; агоністами 5НТ, такими як, наприклад, сіль щавлевої кислоти 1-(3етилбензофуран-7-іл)піперазину [WO-01/09111]; агоністами бомбезину; антагоністами галаніну; гормонами росту (такими як, наприклад, гормон росту людини); сполуками, що вивільняють гормон росту (такими як трет-бутиловий ефір 6бензилокси-1-(2-діізопропіламіноетилкарбамоїл)3,4-дигідро-1Н-ізохінолін-2-карбонової кислоти [WO-01/85695]); агоністами TRH [див., наприклад, Європейський патент 0462884]; 2і 3модуляторами розриваючих зв'язок протеїнів; агоністами лептину [див., наприклад, Lee Daniel W.; Leinung Matthev С; Rozhavskaya-Arena Marina; "Grasso Patricia Leptin agonists as a potential approach to the treatment of obesity", Drugs of the Future, 26 (9), 873-881 (2001)]; агоністами DA (бромкриптин, допрексин); інгібіторами ліпази/амілази [див., наприклад, WO-00/40569]; модуляторами PPAR [див., наприклад, WO00/78312]; інгібіторами 11β-HSDl (11-бетагідроксистероїддегідрогеназа тину 1) [див., наприклад, WO-01/90094 або Т. Barf і інш., J. Med. Chem., 45, 3813-3815 (2002)]; інгібіторами ацетилСоА-карбоксилази [АСС; див., наприклад, WO99/46262]; інгібіторами дипептидпептидази IV [DPP-IV; див., наприклад, Європейський патент 1259246]; модуляторами RXR або агоністами TRβ. Згідно з варіантом здійснення винаходу, іншою біологічно активною речовиною є лептин: [див., наприклад, "Perspectives in the therapeutic use of leptin", Salvador Javier; Gomez-Ambrosi Javier; Fruhbeck Gema; Exspert Opinion on Pharmacotherapy, 2 (10), 1615-1622 (2001)]. Згідно з варіантом здійснення винаходу, іншою біологічно активною речовиною є дексамфетамін або амфетамін. Згідно з варіантом здійснення винаходу, іншою біологічно активною речовиною є фенфлурамін або дексфенфлурамін. Згідно з ще одним варіантом здійснення винаходу, іншою біологічно активною речовиною є сибутрамін. Згідно з варіантом здійснення винаходу, іншою біологічно активною речовиною є орлістат. 11 80754 Згідно з варіантом здійснення винаходу, іншою біологічно активною речовиною є мазіндол або фентермін. Згідно з варіантом здійснення, сполуки формули (І) вводять в комбінації з баластними речовинами, переважно, з нерозчинними баластними речовинами [див., наприклад, Carob/Caromax® (Zunft H.J. та інш., "Carob pulp preperation for treatment of hypercholesterolemia", ADVANCES IN THERAPY, 18 (5), 230-236 (2001, вересень-жовтень)]. Каромакс являє собою продукт, що містить кароб, фірми Nutrinova, Nutrition and Food Ingredients GmbH, Industriepark Hochst, 65926, Франкфурт-на-Майні). Комбінацію з Caromax можна здійснювати у вигляді композиції або шляхом роздільного введення сполук формули (І) і Caromax. При цьому Caromax можна вводити також в формі харчових продуктів, наприклад, в формі хлібобулочних виробів або батончиків мюслі. Само собою зрозуміло, що будь-яка придатна комбінація сполук, що пропонуються згідно з винаходом з одним або декількома вищезгаданими сполуками і, на вибір, з одним або декількома іншими фармакологічно активними речовинами розглядається як така, що підпадає під об'єм охорони даного винаходу. Винахід відноситься, далі, отримання сполуки формули (І). до способів 12 Спосіб А отримання сполуки формули (І) відрізняється тим, що амін формули (II) [див. WO02/50027], вводять у взаємодію з моноглюкамідом 1,12-додекандикарбонової кислоти (формула (III), причому гідроксильні групи глюкамінової частини можуть бути захищені, наприклад, ацильними групами, такими як, наприклад, ацетильні групи, або простими ефірними групами, такими як, наприклад, групи простого бензилового ефіру, з отриманням внаслідок реакції зв'язування пептидів сполуки формули (IV). У разі цієї взаємодії можна працювати, наприклад, при використанні Nгідроксибензтриазолу (HOBt) і N-етил-N'-(3диметиламінопропіл)карбодііміду (EDC) при кімнатній температурі, наприклад, в диметилформаміді (ДМФА) як розчиннику. Також можна використовувати інші реагенти реакції зв'язування пептидів і розчинники або суміші розчинників [див., наприклад, A. Speicher та інш., Journal fur Praktische Chemie/Chemiker-Zeitung, 340, 581-583 (1998); Y.S. Klausner M. Bodansky, Synthesis, 453 і подальші (1972); K. Ishihara та інш., J. Org. Chem., 61, 4196 (1996); Μ. Kunishima. та інш., Tetrahedron, 55, 13159-13170 (1999); або також R.C. Larock "Comprehensive Organic Transformations", VCH, Нью-Йорк, 1969, с.981 і подальші]. 13 80754 14 взаємодію з галогенангідридом, наприклад, хлорангідридом, 11-((4R,6R)-4,5,6-тpигiдpoкcи-3(R)-гiдpoкcи-2-(S)гiдpoкcигeкcилкapбaмoїл)yндeкaнoвoї кислоти формули (VIII), наприклад, в піридині або в дихлорметані, з додаванням первинного аміну або без нього, при кімнатній температурі. Гідроксильні групи глюкамінної частини при цьому переважно забезпечені вищезгаданими захисними групами і після реакції зв'язування їх можна відщеплювати з отриманням аміду формули (Іа). Далі, винахід відноситься до проміжних продуктів формул (III), (IV) і (VIII), де R означає ацил, наприклад, ацетил або бензоїл, або де R означає аралкіл, алкіл або арил, наприклад, бензил. Приклад 1 Спосіб ΑΙ: 1.) Монометиловий ефір додекандикарбонової кислоти Інший спосіб (В), що пропонується згідно з винаходом, включає введення у взаємодію аміну формули (II) з 1,12-додекандикарбоновою кислотою формули (V) в умовах реакції зв'язування пептидів і подальшу взаємодію продукту формули (VI) з глюкаміном формули (VII), гідроксильні групи якого можуть бути забезпечені захисними групами (такими як, наприклад, ацетильні захисні групи або бензильні захисні групи), знову в умовах реакції зв'язування пептидів, з отриманням сполуки формули (І) або відповідно забезпеченої захисними групами сполуки формули (Іа). На наступній стадії захисні групи можна відщеплювати або в слаболужних умовах, наприклад, в розбавленому водному розчині аміаку, або гідролітично (у разі використання захисних груп простого бензилового ефіру) для отримання сполуки формули (І). Згідно з іншим запропонованим у винаході способом С, амін формули (II) вводять у 4,6г (20ммоль) Додекандикарбонової кислоти при нагріванні розчиняють в 40мл безводного тетрагідрофурану, повільно змішують з 0,73мл (10ммоль) тіонілхлориду і перемішують протягом 30 хвилин при кімнатній температурі. Потім повільно додають 0,8мл (20ммоль) безводного метанолу і перемішують протягом 4 годин при кімнатній температурі; суміш потім витримують протягом 4 днів при кімнатній температурі. Після цього тонкошарова хроматографія не показує ніякого подальшого перетворення; реакційну суміш концентрують у вакуумі, залишок перемішують з водою (ультразвукова баня). Осад відфільтровують під вакуумом, промивають водою і знову відфільтровують під вакуумом. Вологий залишок перемішують з дихлорметаном (ультразвукова баня), відфільтровують через складчастий фільтр, промивають дихлорметаном і фільтрат концентрують у вакуумі. Отримують монометиловий ефір додекандикарбонової кислоти (3,09г) з виходом 63%.молекулярна маса: 244,34; МС (мас-спектрометрія): 245,4 (М+Н+). 2.) Синтез метилового ефіру 11-((4R,6R)-4,5,6тригідрокси-3-(R)-гідрокси-2-(S)гідроксигексилкарбамоїл)ундеканової кислоти 3.07г (12,6ммоль) Монометилового ефіру додекандикарбонової кислоти при кімнатній температурі розчиняють в 30мл безводного диметилформаміду, змішують з 2,2г (12,1ммоль) глюкаміну, 1,9г (12,4ммоль) Nгідроксибензтриазолу (HOBt) і 2,4г (12,5ммоль) Nетилi-N'-(3-диметиламінопропіл)карбодііміду (EDC) і перемішують протягом 6 годин при кімнатній температурі. Витримують протягом ночі при кімнатній температурі. На наступний день тонкошарова хроматографія показує повне перетворення. Реакційну суміш концентрують у вакуумі і висушують у високому вакуумі. Залишок перемішують у воді (ультразвукова баня), відфільтровують під вакуумом, промивають водою 15 80754 16 і відфільтровують під вакуумом. Вологий сирий продукт перемішують в дихлорметані, відфільтровують під вакуумом, промивають дихлорметаном і висушують. Отримують метиловий ефір 11-((4R,6R)-4,5,6-тpигiдpoкcи-3(R)-гiдpoкcи-2-(S)-гiдpoкcигeкcилкapбaмoїл)yндeкaнoвoї кислоти; 4,45г (вихід: 90%).молекулярна маса: 407,51; МС: 408,20 (М+Н+). 3.) Синтез 11-((4R,6R)(-4,5,6-тригідрокси-3-(R)гідрокси-2-(S)гідроксигексилкарбамоїл)ундеканової кислоти (формула (III); R=Н); під вакуумом. Сирий продукт перекристалізують з ізопропанолу. Кристалізат ще раз перемішують з водою, відфільтровують під вакуумом і висушують. Отримують 0,38г (32%) 4-[(2S,3R)-3-[(S)-3-(4фторфеніл)-3-гідроксипропіл]-2-(4-метоксифеніл)4-оксоазетидин-1-іл]бензиламід-((2S,3R,4R,5R)2,3,4,5,6-пентагідроксигексил)аміду додекандикарбонової кислоти (І). Молекулярна маса: 809,97; МС: 810,49 (М+Н+). Спосіб А2: 1.) 11-((2S,3R,4R,5R)-2,3,4,5,6Пентаацетоксигексилкарбамоїл) ундеканова кислота (формула (III); R=ацетил): 4,45г (10,9ммоль) Метилового ефіру 11((4R,6R)-4,5,6-тригідрокси-3-(R)-гідрокси-2-(S)гідроксигексилкарбамоїл)-ундеканової кислоти при кімнатній температурі суспендують в 75мл безводного етанолу, змішують з 25мл води і 2,2г КОН (85%-ний розчин) (33ммоль). Після перемішування протягом 2 годин при температурі 80°С тонкошарова хроматографія показує повне перетворення. Реакційну суміш концентрують у вакуумі; залишок розчиняють у воді і підкисляють концентрованою соляною кислотою. Сирий продукт, що випав в осад, відфільтровують під вакуумом, промивають водою і відфільтровують під вакуумом. Вологий сирий продукт перекристалізують з приблизно 100мл етаноду, відфільтровують в гарячому стані і осаджують на бані з льодом. Осад відфільтровують під вакуумом, промивають його етанолом і висушують його. Отримують 2,2г (51%) 11-((4R,6R)-4,5,6тригідрокси-3-(R) -гідрокси-2-(S)гідроксигексилкарбамоїл)-ундеканової кислоти. Молекулярна маса: 393,48; МС: 394,28 (М+Н+). 4.) Синтез 4-[(2S,3R)-3-[(S)-3-(4-фторфеніл)-3гідроксипропіл]-2-(4-мeтoкcифeнiл)-4oкcoaзeтидин-1-iл]бeнзилaмiд-((2S,3R,4R/5R)2,3,4,5,6-пентагідроксигексил)амід додекандикарбонової кислоти (формула (І)): 0,4г 11-((4R,6R)-4,5,6-тригідрокси-3-(R)гідрокси-2-(S)гідроксигексилкарбамоїл)ундеканової кислоти (формула (III); R=H) при кімнатній температурі змішують з 3мл безводного піридину і 3мл ангідриду оцтової кислоти і перемішують протягом 4 годин при кімнатній температурі. По закінченні реакції реакційну суміш змішують з водою і концентрують у вакуумі. Залишок перемішують з невеликою кількістю води і відфільтровують. Залишок на фільтрі промивають водою і потім висушують у вакуумі. Отримують 0,56г 11((2S,3R,4R,5R)-2,3,4,5,6пeнтaaцeтoкcигeкcилкapбaмoїл)yндeкaнoвoї кислоти. Молекулярна маса: 603,66; МС: 604,22 (М+Н+). 2) (2R,3R,4R,5S)-2,3,4,5-тетрагыдрокси-6-(11{4-[(2S,3R)-3-[(S)-3-(4-фторфеніл)-3гідроксипропіл]-2-(4-метоксифеніл)-4оксоазетидин-1іл]бензилкарбамоїл}ундеканоїламіно)гексиловий ефір оцтової кислоти (формула (IV); R=ацетил): 0,63г (1,45ммоль) Бензиламіну формули (II) [отримання див. патент ФРН 10064398] і 0,65г (1,65ммоль) моноаміду дикарбонової кислоти (див. вище) злегка при нагріванні розчиняють в 15мл безводного диметилформаміду, змішують з 0,25г (1,63ммоль) HOBt і 0,31г (1,67ммоль) EDC і перемішують протягом 4 годин при кімнатній температурі. Реакційну суміш витримують протягом ночі при кімнатній температурі. На наступний ранок тонкошарова хроматографія показує повне перетворення. Реакційну суміш концентрують у вакуумі і висушують у високому вакуумі. Залишок перемішують у воді (ультразвукова баня), відфільтровують під вакуумом, промивають водою і відфільтровують 87мг Аміну формули (II) при кімнатній температурі розчиняють в 3мл безводного диметилформаміду і змішують з 120мг вищезгаданої карбонової кислоти, 31мг Nгідроксибензтриазолу і 39мг N-етил-N'-(3диметиламінопропіл)карбодііміду. Реакційну суміш перемішують протягом ночі при кімнатній температурі і потім концентрують у вакуумі. Залишок обробляють етилацетатом, органічну фазу промивають водою і сушать над сульфатом магнію. Після цього фільтрують і фільтрат концентрують у вакуумі. Отримують 90мг (2R,3R,4R,5S)-2,3,4,5-тетраацетокси-6-(11-{4[(2S,3R)-3-[(S)-3-(4-фторфеніл)-3-гідроксипропіл] 17 2-(4-метоксифеніл)-4-оксоазетидин-1іл]бензилкарбамоїл}ундеканоїламіно)гексилового ефіру оцтової кислоти. Молекулярна маса: 1020,16. 3.) 4-[(2S,3R)-3-[(S)-3-(4-Фтopфeнiл)-3гiдpoкcипpoпiл]-2-(4-мeтoкcифeнiл)-4оксоазетидин-1-іл]бензиламід(2R,3R,4R,5R2,3,4,5,6-пентагідроксигексил)амід додекандикарбонової кислоти (формула (І)): 90мг Вищезгаданої сполуки обробляють з допомогою гуанідину в суміші з метанолу і дихлорметану. Отримують похідне глюкаміну формули (І) з молекулярною масою 809,97. Спосіб В: 1.) 11-{4-[(2S,3R)-3-[(3)-3-(4-Фторфеніл)-3гідроксипропіл1-2-(4-метоксифеніл)-4оксоазетидин-1-іл]бензилкарбамоїл}-ундеканова кислота (формула (VI)): До розчину з 371мг додекандикарбонової кислоти, 63мкл діізопропілкарбодііміду, 55мг гідроксибензтриазолу в 2мл диметилформаміду додають розчин з 70мг аміну формули (І), 23мкл триетиламіну в 1мл диметилформаміду і перемішують протягом 12 годин при кімнатній температурі. Реакційний розчин концентрують і розділяють шляхом високоефективної рідинної хроматографії (ВЕРХ) (Knauer Eurosper-100-10C18, вода (0,1% трифтороцтової кислоти)/ацетонітрил (0,1% трифтороцтової кислоти) =80/20→10/90). Отримують продукт змолекулярною масою 646,81 (C38H47FiN2O6); MC (іонізація електронним розпиленням (ESI)): 647,35 (М+Н+). 2.) 4-[(2S,3R)-3-[(S)-3-(4-Фторфеніл)-3гідроксипропіл]-2-(4-метоксифеніл)-4oкcoaзeтидин-1-iл]бeнзилaмiд-((2S,3R,4R,5R)2,3,4,5,6-пeнтaгiдpoкcигeкcил)aмiд додекандикарбонової кислоти (формула (І)): 80754 18 Як описується у випадку других реакцій зв'язування, взаємодія кислоти формули (VI) з глюкаміном (формула (VII); R=H) і HOBt/EDC в диметилформаміді приводить до отримання сполуки формули (І) (R=H). Якщо замість глюкаміну використовують захищене похідне глюкаміну, наприклад, формули (VII) (R=ацетил), то отримують сполуку формули (Іа) з R=ацетил. Спосіб С: 1) (2R,3R,4R,5S)-2,3,4,5-Тетраацетокси-6-(11хлоркарбонілундеканоїламіно)гексиловий ефір оцтової кислоти (формула (VIII); R=ацетил): Сполуку формули (III) R=ацетил) розчиняють в тетрагідрофурані і повільно змішують з тіонілхлоридом; перемішують протягом 1 години при кімнатній температурі. Після цього реакційний розчин концентрують у вакуумі і сирий продукт використовують на найближчій стадії. 2.) (2R,3R,4R,5S)-2,3,4,5-Тетраацетокси-6-(11{4-[(2S,3R)-3-[(S)-3-(4-фторфеніл)-3гідроксипропіл]-2-(4-метоксифеніл)-4оксоазетидин-1-іл]бензилкарбамоїл}ундеканоїламіно)гексиловий ефір оцтової кислоти (формула (IV); R=ацетил): Вищезгаданий хлорангідрид кислоти в суміші з піридину і дихлорметану при кімнатній температурі змішують з аміном і перемішують протягом ночі при кімнатній температурі. Обробка приводить до аміду формули (IV) з R=ацетил. Сполуку формули (І), що пропонується згідно з винаходом, тестували на його дію за допомогою нижчеописаного способу: Вплив абсорбції холестерину + виділення 3Нтаурохолевої кислоти на основі виділення фекалій миші, щура або хом'яка Мишей лінії NMRI, щурів лінії Wistar або золотистих сірійських хом'ячків (в групах з n=4-6) утримують на стандартній дієті (альтромін; положення (губа)) в респіраційних камерах. У другій половині дня перед введенням радіоактивного індикатора (14С-холестерин) тварин витримують голодними і адаптують до запобіжних грат. Додатково, за 24 години до перорального введення пробного сніданку (С-холестерин в Intralipid®20, Pharmacia-Upjohn) тварин підшкірно 19 80754 мітять за допомогою 3Н-таурохолевої кислоти (3НТСА) (наприклад, від 1мкКі/миша до 5мкКі/щур). Тест на абсорбцію холестерину: 0,25мл/миша Intralipid®20 (Pharmacia-Upjohn) (максимально з 0,25мкКі 14С-холестерину в 0,1мг холестерину) вводять перорально за допомогою шлункового зонда. Речовини, що тестуються, розводять роздільно в 0,5% метил-целюлоза (Sigma)/5% солутол (BASF, Людвігсхафен) або в придатному ексципієнті. Об'єм, що вводиться, речовини, яка тестується, становить 0,5мл/миша. Речовину, що тестується, вводять безпосередньо перед пробним сніданком (інтраліпід з міткою у вигляді 14 С-холестерину) (тест на абсорбцію холестерину). Фекалії збирають протягом 24 годин: фекальне елімінування 14С-холестерину і 3Нтаурохолевої кислоти (ТСА) визначають через 24 години. Витягують печінку, гомогенізують і аліквоти спалюють в оксиматі (модель 307, Packard) для визначення поглиненої/резорбованої кількості 14Схолестерину. Оцінка Зразки фекалій: Визначають загальну масу, доливають водою до певного об'єму, потім гомогенізують, аліквоту висушують і спалюють в оксиматі (модель 307, Packard, для спалення радіоактивно мічених зразків): кількість радіоактивних 3Н-Н2О і 14С-СО2 3 екстраполюють на виділену кількість Нтаурохолевої кислоти, відповідно, 14С-холестерину (технологія бінарних ізотопів). Значення ED200 інтерполюють у вигляді дози з кривої доза-дія як ті дози, які подвоюють виділення ТСА, відповідно, холестерину, в перерахунку на одночасно піддану обробці контрольну групу. Зразки печінки: Поглинену кількість 14С-холестерину в печінці співвідносять до введеної дози. Значення ED50 інтерполюють з кривої доза-дія як ту дозу, яка зменшує вдвічі поглинання 14С-холестерину в печінці (50%), в перерахунку на контрольну групу. Наступне значення ED50 підтверджує активність сполуки формули, що пропонується згідно з винаходом (І): Приклад № 1 ED50 (печінка) [мг/миша] 0,005 З таблиці можна бачити, що сполука формули (І) має дуже хорошу дію по зниженню вмісту холестерину. Розчинність сполуки, а також порівняльної сполуки формули (VI) тестували наступним чином: Як порівняльну сполуку було вибрано структурно подібну сполуку, описану [в Міжнародній заявці WO-02/50027]: 20 0,5мг сполуки, що тестується, точно зважують в пробірці Еппендорфа і змішують з 0,5мл відповідного розчинника (водний буфер). Пробірку Еппендорфа потім вміщують в термоміксер і струшують при температурі 25°С протягом 4 годин з швидкістю 1400 обертів на хвилину. Потім пробірку Еппендорфа вміщують в центрифугу. Після центрифугування аліквоту супернатанта використовують для визначення розчиненої кількості шляхом ВЕРХ/УФ-аналізу. У наступній таблиці представлені досягнуті при цьому результати: умови рН Вода (рН) РН1,2 рН4,5 рН6,8 рН8,0 FaSSIF FeSSIF Приклад Розчинність в мкг/мл Розчинність в мкг/мл 3 (6,8)
ДивитисяДодаткова інформація
Назва патенту англійськоюDiphenyl azetidinones, medicaments containing said compound and use of the latter
Автори англійськоюJaehne Gerhard, Frick Wendelin, Frick, Wendelin, Lindenschmidt Andreas, Flohr Stefanie, Heuer, Hubert, CHAEFER HANS-LUDWIG, Schaefer, Hans-Ludwig, Kramer, Werner, Galia Eric, Glombik Heiner, Glombik, Heiner
Назва патенту російськоюДифенилазетидиноны, лекарственное средство (варианты), которое содержит эти соединения, и их применение
Автори російськоюЙэне Герхард, Фрик Венделин, Линденшмидт Андреас, Флор Штефани, Хойер Хуберт, Шефер Ханс-Людвиг, Крамер Вернер, Галиа Эрик, Гломбик Хайнер
МПК / Мітки
МПК: A61P 3/06, C07D 205/00, A61K 31/397
Мітки: засіб, сполуки, дифенілазетидинони, містить, лікарський, варіанти, застосування
Код посилання
<a href="https://ua.patents.su/11-80754-difenilazetidinoni-likarskijj-zasib-varianti-shho-mistit-ci-spoluki-i-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Дифенілазетидинони, лікарський засіб (варіанти), що містить ці сполуки, і їх застосування</a>
Попередній патент: Спосіб транспортування і очистки коренебульбоплодів та пристрій для його здійснення
Наступний патент: Вихрострумовий метод і система безконтактного визначення опору
Випадковий патент: Вітамінно-мінеральний комплекс












