Похідні аміду гетероциклічної карбонової кислоти
Номер патенту: 88643
Опубліковано: 10.11.2009
Автори: Галгоци Корнель, Шаги Каталін, Борза Іштван, Колок Шандор, Фаркаш Шандор, Надь Йожеф, Хорват Чілла, Дьєртьян Іштван
Формула / Реферат
1. Похідні аміду гетероциклічної карбонової кислоти формули (І):
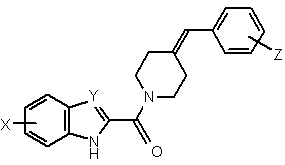 , (I)
, (I)
в якій значення
X відповідає водню або атому галогену, гідрокси, ціано, С1-С4алкілсульфонамідо, факультативно заміщеній атомом галогену або атомами галогену, С1-С4алканоїламідо, факультативно заміщеній атомом галогену або атомами галогену, арилсульфонамідогрупі,
Y відповідає -СН= групі або атому -N=,
Z відповідає атому водню або атому галогену, С1-С4алкільній, С1-С4алкокси, ціано, трифторметильній, трифторметоксигрупі,
а також їхні солі.
2. Сполука за п. 1, вибрана з наведеної нижче групи
(4-бензиліденпіперидин-1-іл)-(6-гідрокси-1Н-бензоімідазол-2-іл)-метанон,
(6-гідрокси-1Н-бензоімідазол-2-іл)-[4-(4-метилбензиліден)-піперидин-1-іл]-метанон,
[4-(4-фторбензиліден)-піперидин-1-іл]-(6-гідрокси-1Н-бензоімідазол-2-іл)-метанон,
[4-(4-хлорбензиліден)-піперидин-1-іл]-(6-гідрокси-1Н-бензоімідазол-2-іл)-метанон,
(4-бензиліденпіперидин-1-іл)-(6-гідрокси-1Н-індол-2-іл)-метанон
та їхні солі.
3. Фармацевтична композиція, яка містить ефективну кількість похідних аміду гетероциклічної карбонової кислоти формули (І), де значення X, Y, Z визначені у п. 1, або їхніх солей як активні речовини та допоміжні речовини, які широко застосовують у фармацевтичній практиці, такі як носії, наповнювачі, розріджувачі, стабілізатори, змочувальні або емульгувальні агенти, речовини, що впливають на рН та осмотичний тиск, духмяні або ароматизувальні речовини, а також добавки, що активують або доставляють композицію.
4. Спосіб одержання похідних аміду гетероциклічної карбонової кислоти формули (І), в якій значення X, Y, Z визначені в п. 1, який відрізняється тим, що проводять реакцію вторинного аміну формули (II)
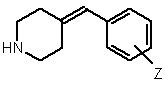 , (II)
, (II)
де Z має те саме значення, що визначене для формули (І),
з хімічно активною похідною карбонової кислоти формули (III)
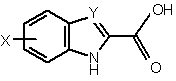 , (III)
, (III)
в якій значення X і Y відповідають тим значенням, які були визначені для формули (І),
у придатному розчиннику,
з подальшою необов’язковою трансформацією одержаних таким чином похідних аміду гетероциклічної карбонової кислоти формули (І), де значення, X, Y, і Z відповідають тим значенням, які наведені в п. 1, на інші сполуки, що відповідають формулі (І), шляхом введення нових замісників та/або модифікації або видалення наявних замісників, та/або шляхом формування солі і/або вивільнення сполуки, що відповідає формулі (І), зі складу солей із застосуванням відомих методів.
5. Спосіб за п. 4, який відрізняється тим, що здійснюють реакцію активної похідної карбонової кислоти формули (III), в якій значення X і Y відповідають тим значенням, які наведені у п. 1, з вторинним аміном формули (II), де значення Z відповідають значенням, які наведені у п. 1, краще у присутності основи.
6. Спосіб за п. 4, який відрізняється тим, що здійснюють реакцію активної похідної карбонової кислоти формули (III), де значення X і Y відповідають значенням, які наведені у п. 1, з вторинним аміном формули (II), де значення Z відповідають тим значенням, які наведені у п. 1, у присутності триетиламіну і о-бензотриазол-1-іл-N,N,N’,N’-тетраметилуроніумгексафторфосфату (HBTU) в диметилформаміді.
7. Спосіб одержання фармацевтичної композиції, що має ефект NR2B-селективного антагоніста рецептора NMDA, який відрізняється тим, що проводять змішування похідної аміду гетероциклічної карбонової кислоти формули (І), в якій значення X, Y, Z відповідають тим значенням, які наведені у п. 1, або його фармацевтично прийнятних солей як активних речовин і допоміжних речовин, які широко застосовують у фармацевтичній практиці, таких як носії, наповнювачі, розріджувачі, стабілізатори, змочувальні або емульгувальні агенти, речовини, що впливають на рН та осмотичний тиск, духмяні або ароматизувальні речовини, а також добавки, що активують або доставляють композицію.
8. Спосіб лікування та полегшення симптомів таких захворювань ссавців, у тому числі людини, як травматичне пошкодження головного або спинного мозку, пошкодження нервових клітин, пов’язаних з наявністю вірусу імунодефіциту людини (ВІЛ), бічного аміотрофічного склерозу (хвороби Шарко), толерантності та/або залежності при лікуванні болю із застосуванням синтетичних наркотичних препаратів (опіоїдів), синдромів відміни, наприклад, алкоголю, опіоїдів або кокаїну, ішемічних розладах ЦНС, хронічних нейродегенеративних захворювань, таких як хвороба Альцгеймера, хвороба Паркінсона, хвороба Хантингтона, болю та хронічних больових станів, таких як невропатичний біль або біль, пов’язаний з раковим захворюванням, епілепсії, тривожності, депресії, мігрені, психозу, м’язового спазму, слабоумства різного походження, гіпоглікемії, дегенеративних розладів сітківки, глаукоми, астми, дзвону у вухах, втрати слуху, індукованої антибіотиком-аміноглікозидом, який відрізняється тим, що ссавцеві, що потребує лікування, вводять ефективну кількість похідної аміду гетероциклічної карбонової кислоти формули (І), в якій значення X, Y, Z відповідають тим значенням, які наведені у п. 1, або його фармацевтично прийнятних солей як самих по собі, так і у комбінації з носіями, наповнювачами і тому подібним, що традиційно застосовують у фармацевтичній практиці.
9. Застосування похідної аміду гетероциклічної карбонової кислоти формули (І), де значення X, Y, Z відповідають тим значенням, які наведені у п. 1, і/або його оптичних ізомерів, рацемічних сполук і/або фармацевтично прийнятних солей для виробництва фармацевтичних препаратів для лікування та полегшення симптомів таких захворювань ссавців, у тому числі людини, як травматичного пошкодження головного або спинного мозку, пошкодження нервових клітин, пов’язаних з наявністю вірусу імунодефіциту людини (ВІЛ), бічного аміотрофічного склерозу (хвороба Шарко), толерантності та/або залежності при лікуванні болю із застосуванням синтетичних наркотичних препаратів (опіоїдів), синдромів відміни, наприклад, алкоголю, опіоїдів або кокаїну, ішемічних розладів ЦНС, хронічних нейродегенеративних розладів, таких як хвороба Альцгеймера, хвороба Паркінсона, хвороба Хантингтона, болю та хронічних больових станів, таких як невропатичний біль або біль, пов’язаний з раковим захворюванням, епілепсії, тривожності, депресії, мігрені, психозу, м’язового спазму, слабоумства різного походження, гіпоглікемії, дегенеративних розладів сітківки, глаукоми, астми, дзвону у вухах, втрати слуху, викликаної застосуванням антибіотика-аміноглікозиду.
Текст
1. Похідні аміду гетероциклічної карбонової кислоти формули (І): C2 2 (19) 1 3 OH 88643 4 дини (ВІЛ), бічного аміотрофічного склерозу (хвоY роби Шарко), толерантності та/або залежності при X лікуванні болю із застосуванням синтетичних нарN котичних препаратів (опіоїдів), синдромів відміни, O H , (III) наприклад, алкоголю, опіоїдів або кокаїну, ішемічв якій значення X і Y відповідають тим значенням, них розладах ЦНС, хронічних нейродегенеративякі були визначені для формули (І), них захворювань, таких як хвороба Альцгеймера, у придатному розчиннику, хвороба Паркінсона, хвороба Хантингтона, болю з подальшою необов’язковою трансформацією та хронічних больових станів, таких як невропатиодержаних таким чином похідних аміду гетероцикчний біль або біль, пов’язаний з раковим захворюлічної карбонової кислоти формули (І), де значенванням, епілепсії, тривожності, депресії, мігрені, ня, X, Y, і Z відповідають тим значенням, які навепсихозу, м’язового спазму, слабоумства різного дені в п. 1, на інші сполуки, що відповідають походження, гіпоглікемії, дегенеративних розладів формулі (І), шляхом введення нових замісників сітківки, глаукоми, астми, дзвону у вухах, втрати та/або модифікації або видалення наявних замісслуху, індукованої антибіотиком-аміноглікозидом, ників, та/або шляхом формування солі і/або вивіякий відрізняється тим, що ссавцеві, що потребує льнення сполуки, що відповідає формулі (І), зі лікування, вводять ефективну кількість похідної складу солей із застосуванням відомих методів. аміду гетероциклічної карбонової кислоти форму5. Спосіб за п. 4, який відрізняється тим, що здійли (І), в якій значення X, Y, Z відповідають тим снюють реакцію активної похідної карбонової кисзначенням, які наведені у п. 1, або його фармацелоти формули (III), в якій значення X і Y відповідавтично прийнятних солей як самих по собі, так і у ють тим значенням, які наведені у п. 1, з комбінації з носіями, наповнювачами і тому подібвторинним аміном формули (II), де значення Z ним, що традиційно застосовують у фармацевтичвідповідають значенням, які наведені у п. 1, краще ній практиці. у присутності основи. 9. Застосування похідної аміду гетероциклічної 6. Спосіб за п. 4, який відрізняється тим, що здійкарбонової кислоти формули (І), де значення X, Y, снюють реакцію активної похідної карбонової кисZ відповідають тим значенням, які наведені у п. 1, лоти формули (III), де значення X і Y відповідають і/або його оптичних ізомерів, рацемічних сполук значенням, які наведені у п. 1, з вторинним аміном і/або фармацевтично прийнятних солей для вироформули (II), де значення Z відповідають тим знабництва фармацевтичних препаратів для лікуванченням, які наведені у п. 1, у присутності триетиня та полегшення симптомів таких захворювань ламіну і о-бензотриазол-1-іл-N,N,N’,N’ссавців, у тому числі людини, як травматичного тетраметилуроніумгексафторфосфату (HBTU) в пошкодження головного або спинного мозку, подиметилформаміді. шкодження нервових клітин, пов’язаних з наявніс7. Спосіб одержання фармацевтичної композиції, тю вірусу імунодефіциту людини (ВІЛ), бічного що має ефект NR2B-селективного антагоніста реаміотрофічного склерозу (хвороба Шарко), толецептора NMDA, який відрізняється тим, що прорантності та/або залежності при лікуванні болю із водять змішування похідної аміду гетероциклічної застосуванням синтетичних наркотичних препаракарбонової кислоти формули (І), в якій значення X, тів (опіоїдів), синдромів відміни, наприклад, алкоY, Z відповідають тим значенням, які наведені у п. голю, опіоїдів або кокаїну, ішемічних розладів 1, або його фармацевтично прийнятних солей як ЦНС, хронічних нейродегенеративних розладів, активних речовин і допоміжних речовин, які широтаких як хвороба Альцгеймера, хвороба Паркінсоко застосовують у фармацевтичній практиці, таких на, хвороба Хантингтона, болю та хронічних бояк носії, наповнювачі, розріджувачі, стабілізатори, льових станів, таких як невропатичний біль або змочувальні або емульгувальні агенти, речовини, біль, пов’язаний з раковим захворюванням, епілещо впливають на рН та осмотичний тиск, духмяні псії, тривожності, депресії, мігрені, психозу, або ароматизувальні речовини, а також добавки, м’язового спазму, слабоумства різного походженщо активують або доставляють композицію. ня, гіпоглікемії, дегенеративних розладів сітківки, 8. Спосіб лікування та полегшення симптомів таглаукоми, астми, дзвону у вухах, втрати слуху, ких захворювань ссавців, у тому числі людини, як викликаної застосуванням антибіотикатравматичне пошкодження головного абоспинноаміноглікозиду. го мозку, пошкодження нервових клітин, пов’язаних з наявністю вірусу імунодефіциту лю Цей винахід стосується нових похідних аміду гетероциклічної карбонової кислоти, що є антагоністами NMDA рецептора або являють собою проміжні продукти для їх одержання. Рецептори N-метил-D-аспарагінової кислоти (NMDA) являють собою катіонні канали, керовані лігандами, які широко представлені у центральній нервовій системі. Рецептори NMDA залучені до росту, розвитку та адаптаційних змін нейронів. Надактивація рецепторів NMDA глутаміновою кислотою, їхнім природним лігандом, може призводити до кальцієвого перевантаження клітин. Це запускає каскад внутрішньоклітинних процесів, які змінюють функціонування клітин і, у кінцевому рахунку, можуть призвести до загибелі нейронів. Антагоністи рецепторів NMDA можуть бути вико 5 88643 6 ристані для лікування безлічі розладів, що супровелика потреба у нових антагоністах NR2B, що воджуються надлишковим вивільненням глутамімають незначну важкість побічних ефектів (мають нової кислоти, або надактивацією рецепторів високий терапевтичний індекс), гарну ефективNMDA з будь-якої іншої причини [Curr Opin Investig ність у разі перорального прийняття (біодоступнісDrugs. 2003 4: 826-32]. тю) і які мають гарну перспективу для удосконаРецептори NMDA являють собою гетеромірні лення у терапевтичних цілях, особливо з метою комплекси, що складаються з принаймні однієї перорального застосування. субодиниці NR1 та однієї або більше з чотирьох Близькі структурні аналоги похідних 4субодиниць NR2 (NR2A - D). Як просторовий розбензиліден-піперидину, що відповідають формулі поділ у центральній нервовій системі (ЦНС), так і (І), з літературі не відомі. Насичені аналоги сполук, фармакологічна чутливість рецепторів NMDA, що що є предметом цього винаходу, описані у патенті мають у своєму складі різні NR2 субодиниці, є різNo. WO 200234718 як селективні антагоністи NR2B ними. Особливо цікавою є NR2B субодиниція у підтипу NMDA. зв'язку з її обмеженим розподілом (найвищі щільБуло виявлено, що нові похідні аміду гетероності у передньому мозку та драглистій речовині циклічної карбонової кислоти, що відповідають спинного мозку) [Neuropharmacology, 38, 611-623 формулі (І), які є предметом цього винаходу, яв(1999)]. Сполуки, селективні для цього підтипу, є ляють собою функціонально активні антагоністи доступними, і їх ефективність була показана на NMDA, селективні для рецепторів, які містять субтваринних моделях інсульту [Stroke, 28, 2244-2251 одиницю NR2B. Ми також виявили, що нові похідні (1997)], при травматичних пошкодженнях мозку аміду гетероциклічної карбонової кислоти мають [Brain Res., 792, 291-298 (1998)], хворобі Паркінсоанальгетичні властивості in vivo, подібні до тих, що на [Ехр. Neural., 163, 239-243 (2000)], невропатичїх мають їхні насичені бензил-піперидинові аналоному та запальному болю [Neuropharmacology, 38, ги. Дивним є таке: в той час як останні молекули 611-623 (1999)]. викликають підвищення рухової активності при Крім того, селективні антагоністи NR2B підтипу рівні, що відповідає їхній ефективній анальгетичній рецепторів NMDA можуть забезпечувати терапевдозі, сполуки, що є предметом цього винаходу, не тичну перевагу порівняно з неселективними антамають ефекту підвищення рухової активності до гоністами рецепторів NMDA. Неселективні антагодосягнення рівня, який принаймні 6-кратно переністи рецепторів NMDA, що діють за типом вищує їх анальгетичну дозу. Ця властивість може блокатора каналу, фенциклідин і кетамін, індукузабезпечити терапевтичну перевагу перед NR2B ють психодислептичні ефекти, галюцинації, дисселективними антагоністами NMDA, що мають форію, кататонію та амнезію у людини. Ці серйозні більш низький терапевтичний індекс. несприятливі ефекти ускладнюють їх клінічне виТаким чином, цей винахід стосується, у першу користання як потенційно можливого препарату. чергу, нових похідних аміду гетероциклічної карСполуки, що належать до цього класу, також обубонової кислоти формули (І) мовлюють аномальну поведінку у тварин, наприклад, збуджують рухову активність, індукують амнезію та погіршують координацію рухів. Наявність цих серйозних ефектів у тварин розглядають як передумову для прояву несприятливих клінічних побічних ефектів. Очікують, що селективні антагоністи NR2B підтипу позбавлені більшої частини цих побічних ефектів. За підсумками експериментів із вивчення поведінки тварин повідомляли про те, що деякі МР2В-селективні сполуки [Ro 63-1908 - в якій значення в J. Pharmacol. Exp. Then, 302 (2002) 940-948 і Ro X відповідає водню або атому галогену, гідро25-6981 в Behav. Pharmacol., 14 (2003) 477-487] кси, ціано, С1-С4 алкілсульфонамідо, не обов'язкозбільшують рухову активність, в той час як такий во заміщеній атомом галогену або атомами галоефект не спостерігають у разі СР-101,606, іншого гену, С1-С4 алканоїламідо, не обов'язково NR2B-селективного антагоніста, і Ro 256981 - за заміщеній атомом галогену або атомами галогену, результатами інших дослідників арилсульфонамідо групі, [Neuropharmacology, 38, 611-623 (1999)]. ВідсутΥ відповідає -СН= групі або атому -Ν= ність ефекту стимулювання рухової активності у Ζ відповідає одному або більше атому водну разі СР-101,606 аж до рівня 56мг/кг підшкірно і або атому галогену, С1-С4 алкільній, С1-С4 алкокси, 100мг/кг внутрішньочеревинно була також підтвеціано, трифторметильній, трифторметокси групі, рджена іншими даними [Soc.Neurosc.Abstr. 21, а також їхніх солей. 439.9 1995]. Таким чином, наскільки нам відомо, Крім того, об'єктами цього винаходу є фармаСР-101,606 є єдиним NR2B-селективним антагоніцевтичні композиції, які мають у своєму складі як стом, який, згідно із повідомленнями, не має ефекактивні компоненти нові похідні аміду гетероцикліту стимулювання рухової активності. Оскільки СРчної карбонової кислоти формули (І) або їхні опти101,606 має невисоку ефективність при пероральчні ізомери, рацемічні сполуки чи солі. ному прийнятті і, згідно з опублікованими даними, Наступними об'єктами цього винаходу є спобув досліджений лише за допомогою внутрішньособи виробництва нових похідних аміду гетероцивенного способу введення людині, крім того, він клічної карбонової кислоти формули (І) та фармаметаболізується поліморфом CYP2D6 [Drug цевтичного виготовлення медикаментів, що мають Metabolism and Disposition 31: 76-87], зберігається у своєму складі ці сполуки, рівно як і способи ліку 7 88643 8 вання із застосуванням цих сполук, що означає матографії із використанням силікагелю Kieselgel введення в організм ссавця, у тому числі людини, 60 (Merck) як адсорбенту та відповідного елюенту. що потребує лікування, ефективної кількості нових Підходящі фракції концентрують, після чого, з мепохідних аміду гетероциклічної карбонової кислоти тою одержання чистого продукту, відбувається формули (І), що є об'єктом цього винаходу, як сарекристалізація з підходящого розчинника. Струкмих по собі, так і у складі медикаменту. туру продуктів визначають методом інфрачервоної Нові похідні аміду гетероциклічної карбонової спектроскопії (ІЧ), ядерного магнітного резонансу кислоти формули (І), що є об'єктом цього винахо(ЯМР) і мас-спектрометрії. ду, є високо ефективними та селективними антаСпособи синтезу 4-бензиліден-піперидинів гоністами рецептора NMDA, і, більше того, більша формули (II) і карбонових кислот формули (III) частина цих сполук є селективними антагоністами описані у розділі прикладів. NR2B підтипу рецепторів NMDA. Протоколи експериментів Згідно з цим винаходом похідні аміду карбоноЕкспресія рекомбінантних рецепторів NMDA вої кислоти формули (І) можуть бути синтезовані Аби довести селективність наших сполук відза допомогою реакції вторинного аміну формули носно NR2B, що означає дослідження їхньої дії на (II) рецептори NMDAB, які містять субодиницю NR2A, ми випробували найефективніші з них на клітинних лініях, які стійко експресують рекомбінантні рецептори NMDA із субодиничним складом NR1/NR2A. кДНК субодиниць NR1 і NR2A людини, субклоновані в індуцибельні експресійні вектори ссавців, були інтродуковані у НЕК 293 клітини, які - де Ζ має те саме значення, що визначене у не містять рецепторів NMDA, із використанням разі формули (І), - з хімічно активною похідною опосередкованого позитивно зарядженими ліпідакарбонової кислоти формули (III) ми методу трансфекції [Biotechniques, 22,, 982-987 (1997); Neurochemistry International, 43, 19-29 (2003)]. Стійкість до неоміцину і гігроміцину використовували для відбирання клонів, що містять обидва вектори, і моноклональні клітинні лінії були одержані на основі тих клонів, які забезпечували - де значення X і Υ є тими самими, що визнанайбільшу відповідь на взаємодію з NMDA. Сполучені раніше для формули (І), після чого одержані ки випробували на їхню інгібіторну активність відпохідні аміду гетероциклічної карбонової кислоти носно викликаного NMDA збільшення рівня внутформули (І), де значення Χ, Υ, Ζ відповідають тим рішньоклітинного кальцію, який реєстрували при значенням, що були визначені у разі формули (І), у флуоресцентних вимірюваннях вмісту кальцію. цьому разі трансформуються на інші сполуки фоДослідження проводили через 48-72 годин після рмули (І), шляхом введення нових замісних груп, додавання індукувального агента. Кетамін та/або модифікації, або видалення груп, присутніх (500мкМ) також був присутній у перебігу індукції з спочатку, та/або шляхом утворення солі, та/або метою запобігання цитотоксичності. виділення сполуки зі складу солей із застосуванВизначення активності антагоніста NMDA in ням відомих методів. vitro шляхом вимірювання внутрішньоклітинної Реакцію карбонової кислоти формули (III) і 4концентрації кальцію із використанням скандувабензиліден-піперидину формули (II), тобто формульного Флуориметра для читання планшетів у вання амідного зв'язку, краще здійснюють шляхом культурі коркових клітин пацюка утворення активної похідної з карбонової кислоти Вимірювання внутрішньоклітинної концентраформули (III), яка і реагує зі вторинним аміном ції кальцію були здійснені із використанням кульформули (II), краще у присутності основи. тур первинних клітин нової кори головного мозку, Перетворення карбонової кислоти на хімічно одержаних з 17-денних ембріонів пацюків лінії активну похідну краще відбувається in situ у проCharles River (докладний опис одержання культури цесі формування амідного зв'язку у розчиннику клітин нової кори головного мозку дивись у (наприклад, диметилформаміді, ацетонітрилі, хлоJohnson, Μ.І.; Bunge, R.P. (1992): Культури клітин рованих вуглеводнях або вуглеводнях). Хімічно первинних периферійних і центральних нейронів активні похідні можуть являти собою хлориди киста нейроглії. В: Protocols for Neural Cell Culture, лот (одержані, наприклад, з карбонової кислоти і eds: Fedoroff, S.; Richardson Α., The Humana Press тіонілхлориду), змішані ангідриди (одержані, наInc., 51-75). Після виділення клітини розсіювали на приклад, з карбонової кислоти та ізобутилхлоростандартні 96-лункові мікропланшети, після цього формату у присутності основи, наприклад, тріетикультури інкубували в атмосфері 95% повітря, 5% ламіну), хімічно активні складні ефіри (одержані, СО2 при 37°С до проведення вимірювань концентнаприклад, з карбонової кислоти і гідроксибензтрірації кальцію. азолу і дициклогексилкарбодііміду або оКультури клітин використовували для вимірюбензотріазол-1-іл-Ν,Ν,Ν',Ν'вання внутрішньоклітинної концентрації кальцію in тетраметилуроніумгексафторфосфату (HBTU) у vitro через 3-7 днів. Вважають, що на цій стадії присутності основи, наприклад, тріетиламіну). Хіклітини in vitro експресують переважно NR2Bмічно активні похідні утворюються у діапазоні темвмісні рецептори NMDA [Mol. Pharmacol. 45, 846ператур від кімнатної температури до 0°С. Необ853 (1994)]. Перед вимірюваннями у клітини ввохідний час реакції складає 6-20 годин. Реакційну дили флуоресцентний Са2+-чутливий барвник суміш очищують із застосуванням колонкової хро 9 88643 10 Fluo-4/AM (2мкМ). Для зупинення введення барвконцентрації кальцію у присутності різних концентника у клітини їх двічі промивали розчином, який рацій випробуваних сполук. використовували під час вимірювань (140мМ NaCI, Криві залежності доза - ефект і значення ІС50 визначали, використовуючи дані, одержані при5мМ KCl, 2мМ СаСІ2, 5мМ HEPES, 5мМ HEPESнаймні в трьох незалежних експериментах. ІнгібіNa, 20мМ глюкози, 10мкМ гліцину, рН=7,4). Після торну активність сполуки в одній концентраційній промивання до культур клітин додавали випробуточці виражали як процент інгібування (ослабленвані сполуки, розчинені у вказаному вище розчині ня) відповіді на NMDA. За експериментальними (90мкл/лунка). Вимірювання внутрішньоклітинної точками були побудовані сигмоїдальні криві конконцентрації кальцію проводили із використанням центрація-інгібування, і значення ІС50 були визнасканувального флуориметра для читання планшечені як концентрація, що забезпечує напівмакситів: збільшення флуоресценції Fluo-4, що відповімальне інгібування при використанні сполуки. дало збільшенню внутрішньоклітинної концентраВ таблиці 1 наведені активності як антагоністів ції кальцію, індукували шляхом введення 40мкМ NR2B більшості ефективних сполук, що є предмеNMDA. Інгібіторну активність випробуваних сполук том цього винаходу, які були визначені у цьому визначали шляхом вимірювання зниження росту експерименті. Таблиця 1 Активність сполук як антагоністів NMDA, виміряна флуориметричним методом із використанням клітин кори головного мозку (NR2B активність) або із використанням трансформованих клітин НЕК293 (NR2A активність) Сполука з прикладу Приклад 1 Приклад 2 Приклад 3 Приклад 4 Приклад 5 Приклад 6 Клітини кори головного мозку пацюка (NR2B) Приблизне значення ІС50 +++ +++ +++ +++ +++ ++ Клітини НЕК293 (NR2A) Інгібування при концентрації 15мкМ 33% 34% Н.Е. Н.Е. 52% Н.Е. ++: ІС50 - між 50 і 500нМ +++: ІС50 менше 50нМ -: Не визначали Н.Е.: не ефективно, тобто інгібування менше 30%. В таблиці 2 наведені результати для декількох NR2B-селективних антагоністів і неселектив ного антагоніста рецептора NMDA MK-801, який використовували як сполука порівняння. Таблиця 2 Активність сполук як антагоністів NMDA, використаних для порівняння, виміряна флуориметричним методом із використанням клітин кори головного мозку (NR2B активність) або із використанням трансформованих клітин НЕК293 (NR2A активність) Кодова назва сполуки порівняння СІ-1041 Со-101244 EMD 95885 СР-101,606 Ro 25.6981 Еритро-іфенпродил МK-801 Клітини кори головного мозку пацюка ІС50[нМ] n 6,6 4 23 3 35 1 41 3 159 4 483 5 37 3 Сполуками для порівняння є такі: СІ-1041: 6-{2-[4-(4-фтор-бензил)-піперидин-1іл]-етансульфініл}-3H-бензооксазол-2-он Со-101244:1-[2-(4-гідроксифенокси)етил]-4гідрокси-4-(4-метилбензил)піперидин EMD 95885: 6-[3-(4-фторбензил)піперидин-1іл]пропіоніл]-2,3-дигідро-бензоксазол-2-он СР-101,606: (1S,2S)-1-(4-гідроксифеніл)-2-(4гідрокси-4-фенілпіперидин-1-іл)-1-пропанол NR1-3/NR2A % інгібування при 10мкМ 21,0 -8,7 0,1 2,5 1,0 -2,7 ІС50=386нМ N 1 1 1 1 1 1 2 Ro 256981: R-(R*,S*)-1-(4-гідроксифеніл)-2метил-3-[4-(фенілметил) піперидин-1-іл]-1пропанол Іфенпродил: еритро-2-(4-бензилпіперидино)-1(4-гідроксифеніл)-1-пропанол МK-801: (+)-5-Метил-10,11-дигідро-5Ндибензо[а,d]циклогептен-5,10-імін Мишаче Формалінове випробування для вимірювання ефективності in vivo 11 88643 12 Відомо, що ін'єкція розведеного формаліну у день, якій давали лише розчинник. Величини ED50 (тобто дози, що викликають зменшення на 50%) задню лапу пацюка або миші обумовлює появу та були розраховані із застосуванням методу побурозвиток двофазової поведінки, пов'язаної з бодови сигмоїдальної кривої за Больцманом лем, інтенсивність якої вимірюють як час, витраче(Boltzman's). ний на зализування/кусання пораненої лапи. Другу Вимірювання мимовільної рухової активності у фазу, як правило, визначають як пов'язані з болем мишей події, детектовані у 15-60 хвилинному інтервалі В експериментах використовували самців мипісля ін'єкції формаліну з піком активності близько шей лінії NMRI вагою 20-22г. 30хв. Відомо, що рецептори NMDA залучені до Мимовільну рухову активність вимірювали із другої фази відповіді на ін'єкцію формаліну, і ця використанням чотириканального контролера акповедінкова відповідь є чутливою до блокування тивності. Установка складалася з чотирьох акрирецепторів NMDA [Dickenson, A. and Besson J.-M. (Editors): Chapter 1, pp. 6-7: Animal models of лових клітин (43см´43см´32см), обладнаних 2´16 Analgesia; and Chapter 8, pp. 180-183: Mechanism парами фотоелементів вздовж усієї нижньої осі of Central Hypersensitivity: Excitatory Amino Acid клітини. Додатковий набір фотоелементів (16 пар) Mechanisms and Their Control - In Pharmacology of клали вздовж двох протилежних боків клітки на Pain. Springer-Verlag (Berlin) 1997]. Таким чином, висоті 10см з метою фіксування відповіді у вигляді ми використовували другу фазу формалінового піднімання на задні лапи. випробування для визначення ефективності споЕкспериментальні групи складалися з 10 твалук in vivo. Вважають, що інгібування другої фази рин. Через тридцять хвилин після перорального відповіді вказує на анальгетичний ефект проти прийняття випробуваної сполуки або розчинника тривалого хімічно-індукованого болю [Hunker, S., (tween-80) тварин клали індивідуально в одну з et al.: Formalin Test in Mice, a Useful Technique for чотирьох кліток на одну годину. Горизонтальні та Evaluating Mild Analgesics, Journal of Neuroscience вертикальні пересування визначали як число пеMethods, 14 (1985) 69-76]. реривань променя впродовж однієї години з 15 Використовували самців альбіносів мишей ліхвилинними інтервалами. нії Charles River NMRI (20-25г). Тварини не одерДля кожної групи розраховували середні знажували будь-якої твердої їжі впродовж приблизно чення±стандартна помилка горизонтальної рухо16 годин перед експериментом, але мали вільний вої активності, після чого визначали відхилення від доступ до 20% розчину глюкози. Далі тварини контрольної (що одержувала розчинник) групи, одержували 1-годинний період акліматизації у виражені у процентах. Вважали, що сполука вискляному циліндрі (приблизно 15см у діаметрі), кликає стимуляцію рухової активності, коли її потім їх клали у такий самий циліндр із розташоефект призводить до більш ніж 50%-ого збільшенваним позаду дзеркалом для полегшення спостеня кількості переривань променя. Відповідно, дози, реження. Випробувані сполуки суспендували у 5% визначені як такі, що не мають стимулювальної дії tween-80 (10мл на кг маси тіла), і вводили перора(LMAfree), викликали менш ніж 50% збільшення. льно шляхом годування за 15 хвилин до ін'єкції У таблиці 3 наведені результати, одержані для формаліну (20мкл 1% формаліну у 0,9% розчині деяких вибраних сполук, що є предметом цього хлориду натрію у воді (фізіологічному розчині) винаходу, і для їхніх близьких бензилвводили підшкірно у вигляді ін'єкцій у дорзальну піперидинових аналогів під час анальгетичного поверхню правої задньої лапи). Час, витрачений випробування і випробування на рухову активна зализування та кусання пораненої лапи при ність. Таким чином, пари приклад 1 - «А» і приклад проведенні вимірювань, складав від 20 до 25 хви6 - «В» структурно відрізняються лише наявністю лин після ін'єкції формаліну. Для визначення веподвійного зв'язку замість одинарного. [«В»=(4личини ED50 різні дози (принаймні п'ять різних доз) бензил-піперидин-1-іл)-(6-гідрокси-1Н-індол-2-іл)випробуваних сполук давали групам по 5 мишей, і метанон і «А»=(4-бензил-піперидин-1-іл)-(6результати виражали як процент зменшення часу, гідрокси-1Н-бензоімідазол-2-іл)-метанон]. витраченого на зализування, порівняно до контрольної групи, за якою спостерігали у той самий 13 88643 14 Таблиця 3 Характеристика двох типів антагоністів NR2B під час формалінового випробування і випробування на рухову активність (випробування LMA). Обчислення терапевтичних індексів (ТІ) Сполука з Прикладу Формалін ED50 мг/кг Приклад 1 2,6 Приклад 6 0,43 Формалін Сполука порівняння ED50 мг/кг "А" 1,6 "В" 1,7 Бензиліден-піперидини LMA Доза мг/кг % збільшення 15 27 30 63 3,75 0 7,5 55 15 69 Бензил-піперидини LMA Доза мг/кг % збільшення 1,875 80 1,875 90 В таблиці 4 наведені дані анальгетичного випробування і випробування на рухову активність для неселективного антагоніста рецептора NMDA ТІ LMAfree/ED50 5,8 8,7 ТІ LMAfree/ED50 20* LMA %збільшення 114 217 137 ТІ LMAfree/ED50
ДивитисяДодаткова інформація
Назва патенту англійськоюHeterocyclic carboxylic acid amide derivatives
Автори англійськоюBorza Istvan, Horvath Csilla, Farkas Sandor, Gyertyan Istvan, Nagy Jozsef, Kolok Sandor, Galgoczy Kornel, Saghy Katalin
Назва патенту російськоюПроизводные амида гетероциклической карбоновой кислоты
Автори російськоюБорза Иштван, Хорват Чилла, Фаркаш Шандор, Дьертьян Иштван, Надь Йожеф, Колок Шандор, Галгоци Корнель, Шаги Каталин
МПК / Мітки
МПК: C07D 401/06, A61K 31/445, A61P 25/28
Мітки: похідні, гетеро)циклічно, карбонової, аміду, кислоти
Код посилання
<a href="https://ua.patents.su/11-88643-pokhidni-amidu-geterociklichno-karbonovo-kisloti.html" target="_blank" rel="follow" title="База патентів України">Похідні аміду гетероциклічної карбонової кислоти</a>
Попередній патент: Панель для підлоги і покриття підлоги, складене з таких панелей
Наступний патент: Спосіб електрокаталітичної активації вуглеводнів палива перед спалюванням в двигуні внутрішнього згорання
Випадковий патент: Переносний верстат, наприклад, свердлильний












