Одно- та двовалентні солі n-(5-гідроксинікотиноїл)-l-глутамінової кислоти, що мають психотропну (антидепресивну та анксіолітичну), нейропротекторну, геропротекторну і протиінсультну дію
Номер патенту: 93269
Опубліковано: 25.01.2011
Автори: Якімук Павєл Васільєвіч, Стовбун Сєргєй Вітальєвіч, Літвін Алєксандр Анатольєвіч
Формула / Реферат
Сіль N-(5-гідроксинікотиноїл)-L-глутамінової кислоти, вибрана з її одно- або двовалентних солей загальної формули
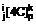 ,
,
де
х = СаОН, у = Н, (І)
x = y = Na, (II)
х = у = K, (III)
що має антидепресивну, анксіолітичну, нейропротекторну, протиінсультну, геропротекторну, ноотропну, протигіпоксичну активність, а також психотропний антидепресивний та анксіолітичний ефект та нейропротекторну дію.
Текст
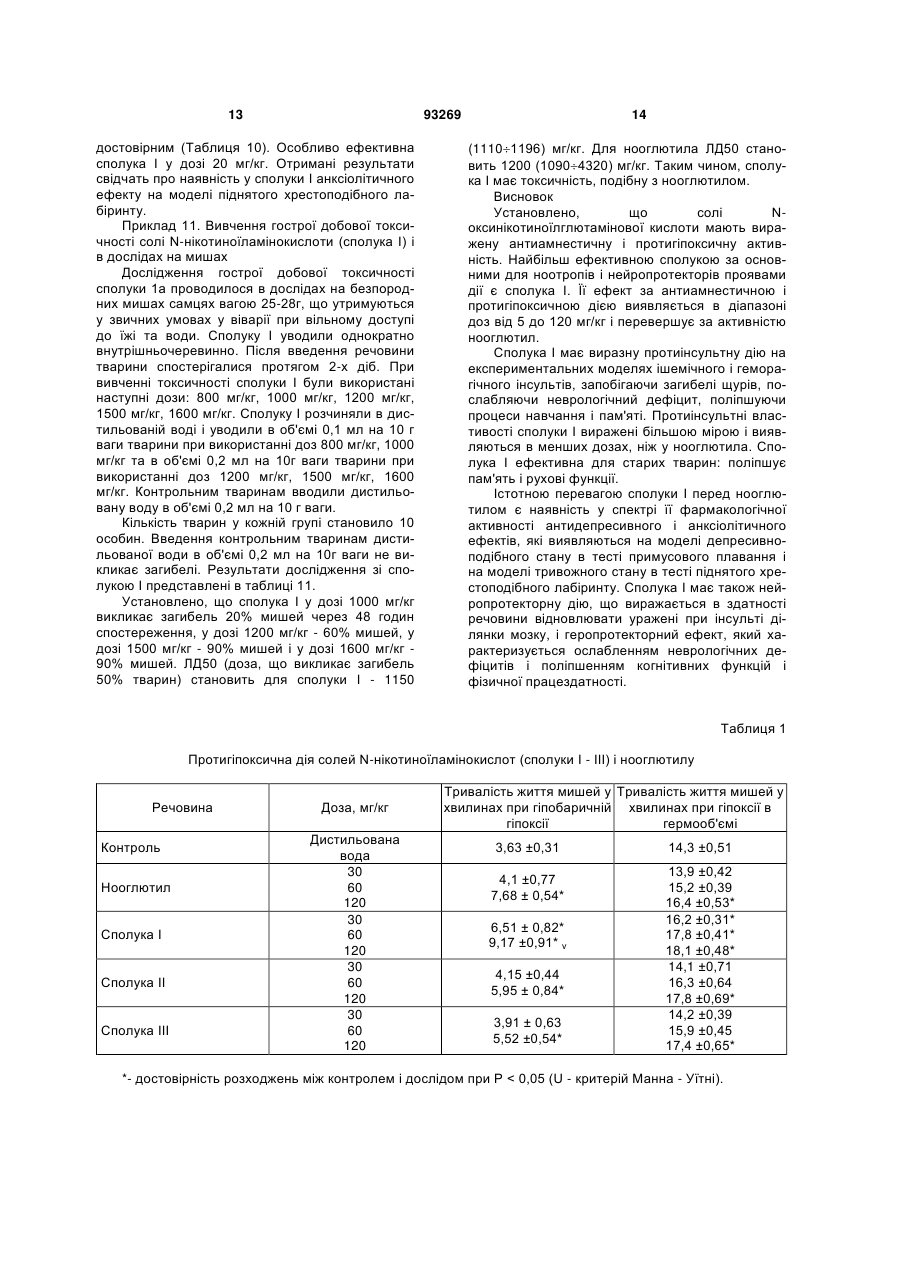
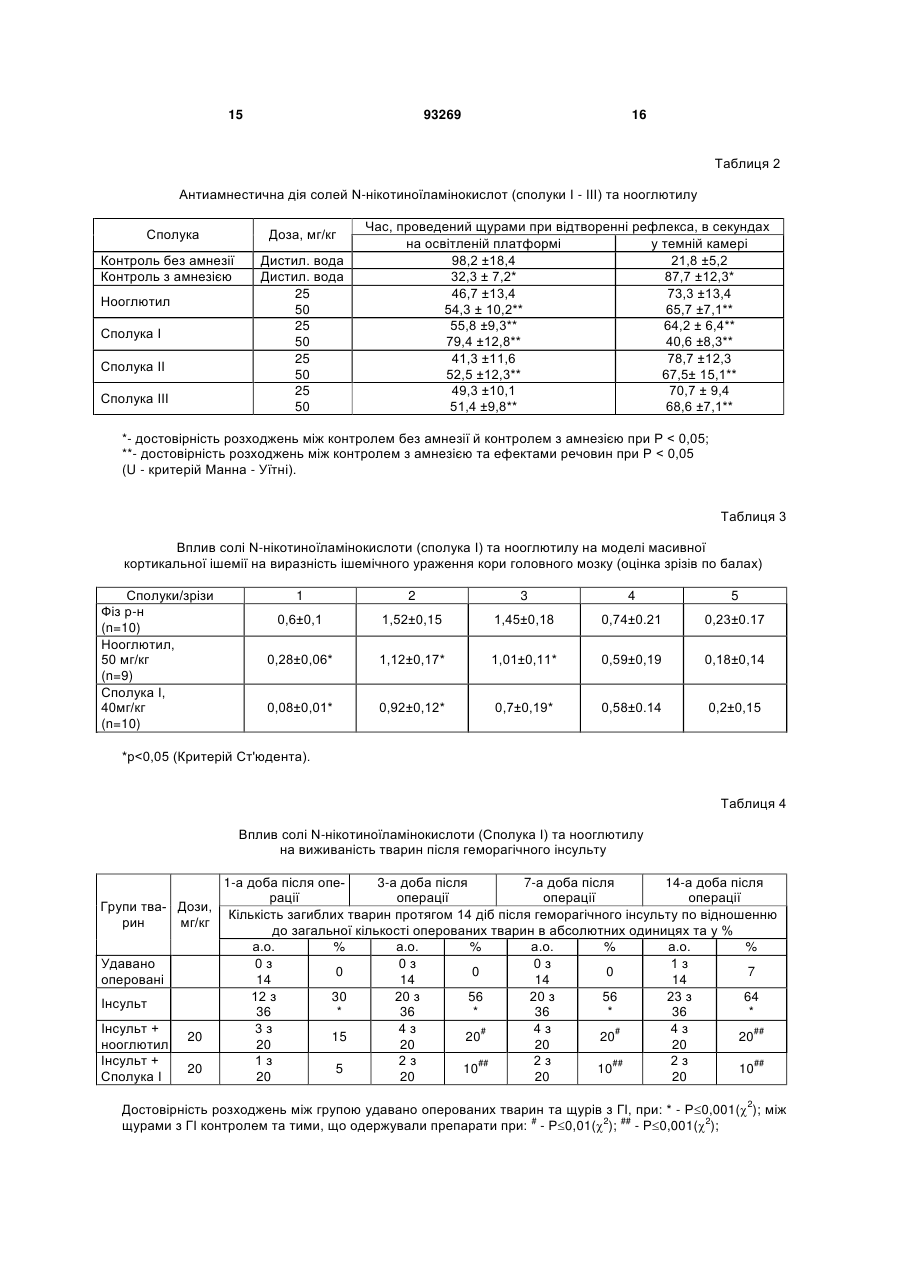
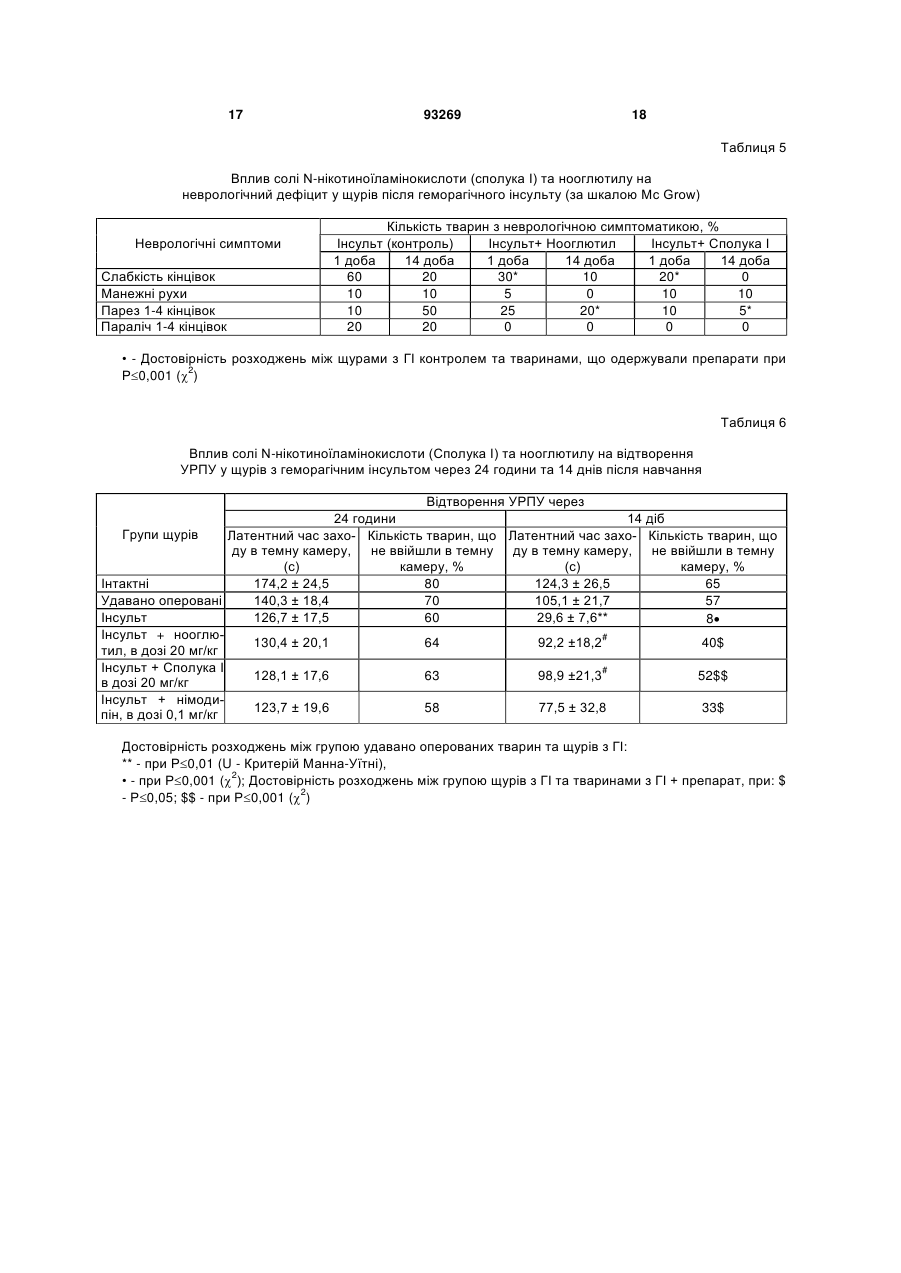
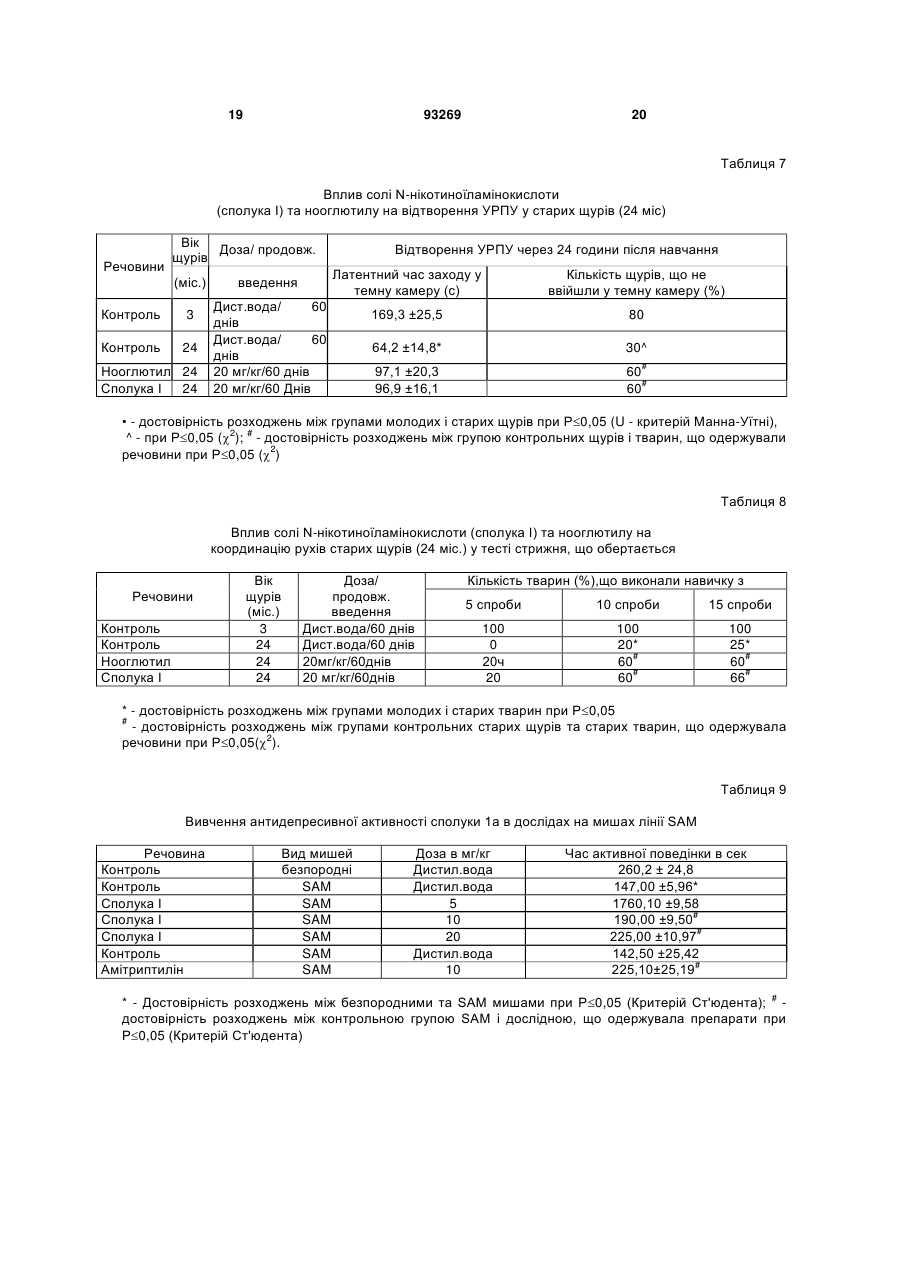
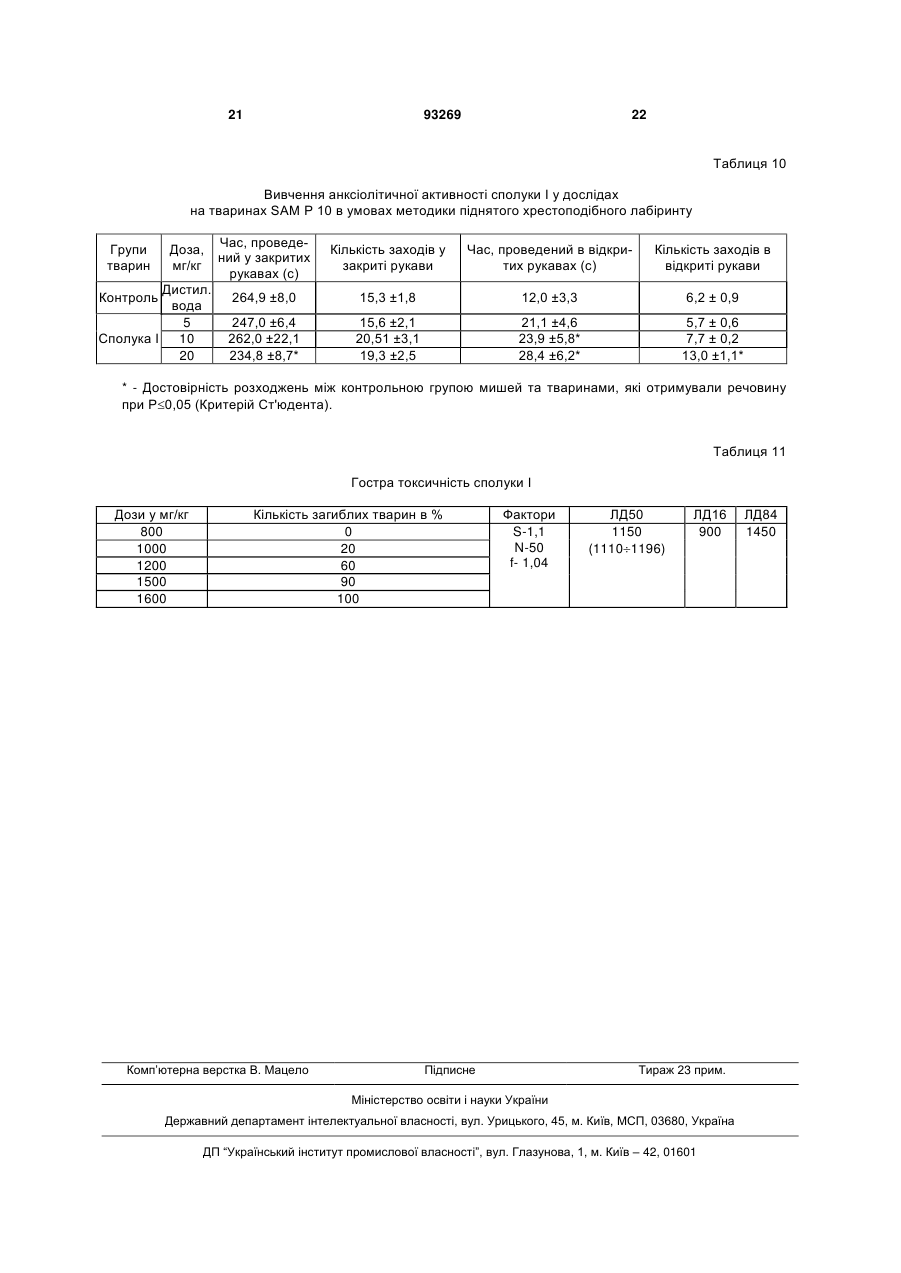
Сіль N-(5-гідроксинікотиноїл)-L-глутамінової кислоти, вибрана з її одно- або двовалентних солей загальної формули CH2 COOY HO CONH CH CH2 Винахід відноситься до медицини, а саме до нових біологічно активних сполук, конкретно до одно та двовалентних солей N-(5гідроксинікотиноїл)-L-глутамінової кислоти, які мають психотропну (антидепресивну та анксіолітичну), нейропротекторну та протиінсультну дію, котрі можуть застосовуватися для лікування депресії, тривоги, ішемічних і геморагічних інсультів, порушень при старінні та інших захворювань, що супроводжуються тривогою, депресією, зниженням когнітивних функцій та нейродегенерацією. Депресія та тривога є в наш час найпоширенішими психічними захворюваннями та часто супроводжують інші стани, зокрема, старіння, інсульти, онкологічні захворювання, хвороби Альцгеймера та Паркінсона та ін. Інсульт (судинне ураження мозку) серед причин смертності посідає друге місце в Росії та третє місце у світі. При цьому частота розвитку ішемічних інсультів (недостатність кровопостачання мозку) становить 70-80%, а геморагічних (крово вилив у мозок) - 20-30%. Ці дві форми інсультів різні за патогенезом та вимагають різних підходів до їхнього лікування, однак при всіх формах інсульту спостерігаються нейродегенеративні процеси. Диференційна діагностика цих двох форм інсульту на ранніх етапах хвороби утруднена, а в більш ніж 25% і неможлива. У зв'язку із цим, доцільне створення препаратів, які були б ефективні при обох формах інсультів. Нині при інсультах застосовуються антагоністи кальцієвих каналів, але вони мають істотні побічні ефекти та недоліки, одним із яких є наявність серцево-судинних ефектів, що призводять до "обкрадання" мозку. Порушення когнітивних функцій і гіпоксичні стани спостерігаються при багатьох захворюваннях, як у дітей, так і при природному старінні, стресах, захворюваннях, що протікають із, нейродегенерацією. Препарати, що мають протигіпоксичну і ноотропну дію, можуть застосовуватися для лікування хворих, що страждають зниженням розумових здібностей при старінні, при хворобі Альцгеймера після мозкової травми, пренаталь COOX (19) UA (11) 93269 (13) , де х = СаОН, у = Н, (І) x = y = Na, (II) х = у = K, (III) що має антидепресивну, анксіолітичну, нейропротекторну, протиінсультну, геропротекторну, ноотропну, протигіпоксичну активність, а також психотропний антидепресивний та анксіолітичний ефект та нейропротекторну дію. C2 N 3 ній гіпоксії, при алкоголізмі, вегетосудинній дистонії та інших захворюваннях. Застосований для лікування цих станів препарат пірацетам має слабку активність. За хімічною структурою найбільш близьким до нових пропонованих сполук є нооглютил (основа N-(5-гідроксинікотиноїл) -L-глутамінової кислоти). Однак нооглютил не має психотропних ефектів (антидепресивного та анксіолітичного) та нейропротекторної дії (патент РФ №1368314, опублікований у БИ №3, 1988р., а також "Nнікотиноїламінокислоти, що мають протигіпоксичну та антиамнестичну активність"; Вороніна Т.А. та співавт. Нова речовина з ноотропною активністю N-(5-оксинікотиноїл)-L-глутамінова кислота. Фармакол. та токсикол., 1990, т.53, №4, с.13-16). Задачею даного винаходу є створення нових високоефективних і малотоксичних сполук, що поєднують психотропні (анксіолітичний, антидепресивний) ефекти з нейропротекторною, протиінсультною, геропротекторною, протигіпоксичною, поліпшуючою навчання та пам'ять дією, та які мають, таким чином переваги перед відомими засобами. Ця задача вирішена шляхом створення нових сполук, а саме, одно- та двовалентних солей N(5-гідроксинікотиноїл)-L-глутамінової кислоти (сполуки І, II, III) загальної формули: , де х=СаОН, у=Н (І), або x=y=Na (II), або х=у=К (III), що мають антидепресивну, анксіолітичну, нейропротекторну, протиінсультну, геропротекторну, ноотропну, протигіпоксичну активність. Заявлені сполуки принципово відрізняються від нооглютила наявністю в спектрі фармакологічної активності психотропних ефектів (антидепресивного та анксіолітичного) та нейропротекторної дії, а також характеризуються більш високою активністю відносно психотропних ефектів. Заявлені сполуки являють собою білі кристалічні речовини, нерозчинні в метиловому, етиловому та ізопропіловому спиртах, практично нерозчинні в бензолі, хлороформі, етилацетаті та інших органічних розчинниках. Речовини розчинні у воді, розбавлених, розчинах кислот та лугів. Заявлені у даному патенті сполуки є новими і у літературі не описані. Приклади здійснення винаходу Приклад 1 Суспензію 2,68 г (0,01 моля) N-(5гідроксинікотиноїл)-L-глутамінової кислоти в 50 мл води нагрівають до 60-70° і до неї невеликими порціями додають 0,68 г (0,012 моля) окису кальцію. Осад поступово розчиняється. Нагрівають до повного розчинення. Водяний розчин упарюють до 20 мл. Отриманий розчин при перемішуванні додають по краплях до 200 мл етилового спирту. Осад, що утворився, перемішують 0,5 години та залишають на 12 годин при кімнатній температурі. Осад відфільтровують, промивають спиртом і 93269 4 висушують при 100° до постійної ваги (3 години). Одержують Са-сіль N-(5-гідроксинікотиноїл) -Lглутамінової кислоти (І), вихід 2,7г (83%), [ά]D20 + 11,0° (с 1, вода). Знайдено, %: С 40,80; Н 3,64; N 8,80. C11H12CaN2O7 або (C11H10CaN2O6.1H2O для хелата. Уточнити по ПМР) Обчислено, %: С 40,76; Н 3,70; N 8,64 ІЧ-спектр (у КВr), см-1 УФ-спектр (у воді): max Спектр ПМР (в D2O), внутрішній стандарт (ГМДС): Приклад 2 Суспензію 0,27 г (0,001 моля) N- (5гідроксинікотиноїл)-L-глутамінової кислоти в 5 мл води нагрівають до 50-60° і до неї обережно додають порціями 0,2 г (0,0024 моля) бікарбонату натрію, нагрівають до повного розчинення та упарюють у вакуумі досуха. У залишок додають етиловий спирт і знову упарюють у вакуумі. Залишок розтирають із сухим ефіром та відфільтровують осад. Потім його висушують при 60°/1мм та одержують ди-Na-cіль N(5гідроксинікотиноїл)-L-глутамінової кислоти (II), вихід 0,25 г (80,6%). [ά]D20=+13,7°(с1, вода) Знайдено, %: С 42,51; Н 3,46; N 9,15. C11H10Na2N2O6 Обчислено, %: С 42,31; Н 3,23; N 8,97 ІЧ-спектр (у КВr), см-1 УФ-спектр (у воді): max Спектр ПМР (в D2O), внутрішній стандарт (ГМДС): Приклад 3 Суспензію 0,27 г (0,001 моля) N- (5гідроксинікотиноїл)-L-глутамінової кислоти в 5 мл води нагрівають до 50-60° і до неї обережно додають порціями 0,24 г (0,0024 моля) бікарбонату калію. Нагрівають до повного розчинення та упарюють у вакуумі досуха. У залишок додають етиловий спирт і знову упарюють у вакуумі. Залишок розтирають із сухим ефіром та відфільтровують осад, промивають сухим ефіром і висушують при 60°/1мм. Одержують ди- К -сіль N- (5гідроксинікотиноїл)-L-глутамінової кислоти (III), гігр., вихід 0,27 г (79,4%). [ά]D20 =+10,5°(с1, вода) Знайдено, %: С 38,64; Н 3,15; N 8,35. C11H10K2N2O6 Обчислено, %: С 38,36; Н 2,93; N 8,14 ІЧ-спектр (у КВr), см-1 УФ-спектр (у воді): max Спектр ПМР (в D2O), внутрішній стандарт (ГМДС): Далі наводяться приклади, що ілюструють ефективність солей N-нікотиноїламінокислот, які мають протиінсультну, протигіпоксичну, антидепресивну, анксіолітичну, поліпшуючу навчання та пам'ять дію. Приклад 4. Вивчення протигіпоксичної активності солей N-нікотиноїламінокислот. Протигіпоксичний ефект досліджувався в умовах 2-х методик: гіпобаричної гіпоксії та гіпоксії з гіперкапнією в гермооб'ємі (Вороніна Т.А. та 5 співавт. Посібник з експериментального, (доклінічного) вивчення нових фармакологічних речовин. М. Медицина. 2005, с.308-320). Досліди проводили на білих безпородних мишах-самцях масою 22-28 г. Кожну дозу речовини вивчали на 10 тваринах. Контрольним групам тварин вводилася дистильована вода в еквівалентному об'ємі. Як препарат для порівняння використали нооглютил. Речовини вводили внутрішньочеревинно за 40 хвилин до досліду. Гостру гіпобаричну гіпоксію моделювали в проточно-витяжній барокамері. Тиск реєстрували висотометром, швидкість підйому -варіометром. Тварин "піднімали" зі швидкістю 20 м/с до площадки "висотою" 11000м. Експозиція становила 10 хвилин. Потім протягом 5 хвилин тварин "спускали" до вихідних умов. Гіпоксію з гіперкапнією у гермооб'ємі створювали шляхом поміщення тварини в герметично закупорену скляну ємність об'ємом 200 мл. Реєстрували тривалість життя тварин в умовах гіпоксії. У кожній групі використали 10 тварин. Установлено, що в умовах гіпобаричної гіпоксії після 10-ти хвилинної експозиції в контролі гинули всі тварини; середня тривалість життя становила 3,6 хвилини. Всі вивчені "речовини 1а1в мають здатність збільшувати тривалість життя мишей в умовах гострої кисневої недостатності в барокамері, а найбільшу активність має сполука І. Ефект сполуки І реалізується в менших дозах, ніж у нооглютила. При використанні однакових доз 30 та, 60мг/кг сполука І має більш виражений ефект, ніж нооглютил (Таблиця 1). В умовах гіпоксії з гіперкапнією у гермооб'ємі середня тривалість життя контрольних тварин становила 14,3 хвилини. Всі вивчені речовини І-IIІ мають здатність збільшувати тривалість життя мишей в умовах гіпоксії з гіперкапнією у гермооб'ємі, а найбільшу активність має сполука І. Ефект сполуки І реалізується в менших дозах, ніж у нооглютила. При використанні однакових доз 60 та 120 мг/кг сполука І має більш виражений ефект, ніж нооглютил (Таблиця 1). Приклад 5. Вивчення антиамнестичної активності солей N-нікотиноїламінокислот. Дослідження проводили на білих безпородних щурах самцях масою 250-280 г. Кожну дозу речовини вивчали на 10 тваринах. Контрольним групам тварин уводилася дистильована вода в еквівалентному об'ємі. Як препарат для порівняння використали нооглютил. Речовини вводили внутрішньочеревинно за 40 хвилин до досліду. Дослідження проводили на стандартній автоматизованій установці умовного рефлексу пасивного уникання (УРПУ) (Passive Avoidance) фірми Lafayette Instrument Co (США) (Ader R. et al. Retention of a passive avoidance response as a function of the intensity and duration of electric shock. Psychon. Sci. 1972, v. 26, p. 125-128; Вороніна Т.А. та співавт. Посібник з експериментального (доклінічного) вивчення нових фармакологічних речовин. М. Медицина. 2005, с. 253-263 та 308-320). Конструктивно установка складається з маленької платформи, розташованої на відстані 1 м від підлоги, освітленої, спеціальною лампою 93269 6 та сполученої з нею темної камери з електродною підлогою. Щура поміщали на освітлену платформу перед входом у темну камеру установки хвостом до вхідного отвору, і тварина, віддаючи перевагу темній камері, швидко переходить у неї. З метою навчання щур у темній камері одержував однократне больове подразнення електрострумом (0,45 мА) через електродну підлогу, і тварина запам'ятовувала, що в темну камеру заходити небезпечно. Тривалість подразнення визначалася вибіганням тварини з темного відсіку. Для одержання амнезії використовували максимальний електрошок (50 гц, 0,2сек), що проводили через корнеальні електроди безпосередньо після навчання. Електрошок викликає стирання пам'ятного сліду. Тест на відтворення УРПУ (на збереження пам'ятного сліду), здійснювали через 24 години після навчання і електрошоку. Тварину знову поміщали на освітлену платформу і протягом 2-х хвилин реєстрували час знаходження тварини на освітленій платформі та у небезпечному темному відсіку (струм на підлогу при відтворенні УРПУ не подається). Контрольні навчені тварини при відтворенні УРПУ без дії електрошоку воліють перебувати на світлій платформі. Стирання навчання за допомогою електрошоку викликає у тварин амнезію, у результаті чого тварини з коротким латентним періодом заходять у темну камеру й залишаються там значно більшу частину часу, ніж тварини без амнезії (Таблиця 2). Всі вивчені сполуки мають виражену антиамнестичну активність, що виражається у тому, що час знаходження тварин на безпечній освітленій платформі значно збільшується в порівнянні з контрольними тваринами з амнезією. Найбільшу антиамнестичну активність має сполука І, що перевершує по ефективності нооглютил (Таблиця 2). Статистично достовірний ефект нооглютила проявляється в дозі 50мг/кг, а аналогічний по вираженості ефект сполуки 1-у дозі 25мг/кг, що свідчить про більш високу активність сполуки І у порівнянні з нооглютилом. Приклад 6. Вивчення ефективності солі Nнікотиноїламінокислоти (сполука І) і нооглютила на моделі масивної кортикальної ішемії. Експерименти виконані на білих безпородних самцях щурів вагою 350-450 г, наркотизованих хлоралгідратом (400 мг/кг, в/б). Тваринам проводили перев'язку лівої сонної артерії, а потім під мікроскопом (збільшення 14.0 х 3.3) проводили оклюзію середньої мозкової артерії (ОСМА) проксимальніше місця її біфуркації на фронтальну й париетальну гілки (S.T.Chen et al., Stroke, 1986, v. 17, № 4, 738-743). Після завершення операції тварин випадковим чином ділили на 3 групи. Тваринам дослідних груп уводили сполуку 1а або нооглютил внутрішньочеревинно через 30 хвилин, потім через 2, 24 та 48 годин після операції. Тваринам контрольної групи в ті ж строки вводили фізіологічний розчин (0.9% хлористий натрій). Через 72 години після ОСМА тварин декапітували. Із замороженого при -20 С готовили 5 фронтальних зрізів товщиною 2,5 мм, які забарвлювали розчином 2,3,5 7 трифенілтетразолій хлориду (ТФТХ). За допомогою морфометричної програми Auc 1 проводили планіметрію, визначали обсяг зони ураження й відсоток обсягу зони ураження щодо обсягу іпсилатеральної півкулі. У результаті операції створюється обширне ішемічне ураження кори головного мозку, що локалізується в межах фронтопариетальної і дорсо-латеральної зон. Для порівняння вираженості змін у різних зрізах використалася умовна шкала, у якій ураження 75% півкулі оцінювалися як 2,5 бала, 60% - 2 бали, 45% 1,5 бала, 20% - 1 бал, 5% - 0,5 бала, 0% - 0 балів. У контрольних тварин, лікованих фізіологічним розчином, загальний обсяг ураження становить 20,17± 3,12%. Максимальне ішемічне ушкодження має місце на рівні 2-го й 3-го зрізів. (Таблиця 3). Сполука І у дозі 40 мг/кг, застосована після ішемізуючого впливу, викликає достовірне зменшення обсягу ушкодження на рівні трьох перших зрізів (Таблиця 3). Загальна площа ураження після використання сполуки І знижувалася до 10,54 ± 1,84% (контроль 20,17 ± 3,12%) і, отже, речовина зменшує загальний обсяг ураження на 47,3 % (р< 0,05). Нооглютил створює ефект у більш високій дозі 50 мг/кг і викликає менш виражені зміни (Таблиця 3). Загальна площа ураження після введення нооглютила знижувалася до 14,31± 2,14%. Таким чином, сполука І уведена після здійснення ішемізуючого впливу, достовірно послаблює вираженість морфологічних змін кори головного мозку, обумовлених перев'язкою іпсилатеральної сонної артерії. Ці результати свідчать про нейропротекторну дію сполуки І. В окремій серії експериментів тварини навчалися в тесті умовного рефлексу пасивного уникання (УРПУ), що виробляється в апараті "Lafayette Instrument Co", USA, який складається з яскраво освітленої висячої платформи, приєднаної до темної камери з електрифікованою підлогою. У силу вродженого кіркового рефлексу щур при навчанні заходив у темну камеру, де одержував електробольове подразнення. Оцінку пам'яті проводили через 24 години після навчання, реєструючи кількість тварин, що не зайшли в темну камеру протягом 180 сек, а для тих, що зайшли - латентний час заходу. Як показано раніше в численних контрольних експериментах на інтактних щурах вони звичайно не заходять у небезпечну камеру або заходять у самому кінці тестування (середній латентний період становить 145±10,1 сек). В ішемізованих тварин (контроль) латентний час заходу в темну камеру знижується й становить 31,2± 8,3 сек (більшість тварин не пам'ятає про нанесене напередодні подразнення й швидко заходять у небезпечну камеру). Ішемізовані тварини, ліковані нооглютилом або сполукою І, показували поліпшення пам'яті, що виражалося в збільшенні латентного періоду заходу в темну небезпечну камеру: під впливом нооглютила до 56,2±8,3 сек і під впливом сполуки І -до 62,3±7,2 сек. Ці ефекти нооглютила та сполуки 1а достовірні в порівнянні з контролем при р< 0,05. 93269 8 Приклад 7. Вивчення ефективності солі Nнікотиноїламінокислоти (сполука І) і нооглютилу на моделі інтрацеребральної посттравматичної гематоми (геморагічного інсульту) Експерименти проводилися на безпородних, білих щурах самцях вагою 200-250 г, які утримувалися у віварії при вільному доступі до їжі (стандартний брикетований корм) і воді, при природній зміні дня й ночі. Моделювання ГІ - локального крововиливу в головному мозку проводилося відповідно до методики А.Н. Макаренко та співавторів (Метод моделювання локального крововиливу в різних структурах головного мозку в експериментальних тварин. Ж. высш. нервн. деят.,2002, т. 52, № 6, стор. 765-768). Щурам, наркотизованим нембуталом (40мг/ кг, в/м) за допомогою спеціального пристрою (мандрен-ніж) і стереотаксиса здійснювали деструкцію мозкової тканини в області capsule interna, з наступним (через 2-3 хвилини) введенням, у місце ушкодження, крові, узятої з-під язика щура (0,02- 0,03 мл). Удавано оперованим тваринам проводили скальпування та трепанацію черепа. Тварини були розділені на 5 груп: інтактні щури, удавано оперовані, група тварин з ГІ, тварини з ГІ, які одержували нооглютил у дозі 20 мг/кг, щури з ГІ, які одержували сполуку 1 у дозі 20 мг/кг. Реєстрацію ефектів речовин проводили через 24 години і 14 діб після операції. Навчання і пам'ять щурів досліджували на моделі умовного рефлексу пасивного уникання (УРПУ, Passive avoidance фірми Lafayette Instrument Co США). Неврологічний дефіцит у тварин визначали за шкалою Stroke-index McGrow у модифікації І.В. Ганнушкіної (Функціональна ангіоархітектоніка головного мозку, Москва, Медицина, 1977, 224 стор.). Тяжкість стану визначалася за сумою відповідних балів. Відзначалася кількість щурів з легкою симптоматикою до 2,5 балів за шкалою Stroke-index (млявість рухів, слабкість кінцівок, односторонній полуптоз, тремор, манежні рухи) і важкими проявами неврологічних порушень (від 3 до 10 балів) - парези кінцівок, параліч нижніх кінцівок, бічне положення. Нооглютил і сполуку І в однакових дозах 20 мг/кг уводили тваринам внутрішньочеревинно однократно через 3-3,5 години після операції. Контрольним групам тварин уводили фізіологічний розчин. Кожна група на початку експерименту складалася з 15 - 20 тварин. Реєстрацію загибелі щурів проводили протягом усього часу спостереження (14 днів). Статистичну обробку даних проводили за допомогою програми "Біостат" з використанням параметричних і непараметричних методів. Як еталон використовувався німодипін (у дозі 0,1 мг/кг) за описаною вище схемою. При реєстрації загибелі тварин показано, що в групі удавано оперованих щурів до 14-го дня спостерігалася загибель лише 7% тварин, а в групі з геморагічним інсультом цей показник склав 64%, при цьому в перші три доби загинуло більше 56% тварин (Таблиця 4). Нооглютил мав сильну протективну дію. Так, у дозі 20 мг/кг препарат майже повністю запобігав загибелі тварин протягом усього часу спостереження: загинуло 9 20% (4 з 20) тварин. У групі щурів, які одержували сполуку І протягом усього часу спостереження (14 діб) загинуло лише 10% тварин (2 з 20). Під впливом сполуки І відзначалося статистично достовірне зменшення загибелі щурів уже в першу добу після інсульту, чого не викликав нооглютил. Отримані результати свідчать про високу протективну активність сполуки 1а у тварин після геморагічного інсульту. Дослідження неврологічного статусу тварин, які вижили, з використанням шкали Stroke-index McGrow показало, що в групі тварин з ГІ в перший день спостереження важка симптоматика відзначалася в 20%, а вже до 7-го дня цей показник становив 50% (Таблиця 5). Нооглютил і сполука І істотно послаблювали у тварин неврологічний дефіцит. Особливо яскраво ефект речовин проявлявся на 14-у добу, коли в контрольній групі щурів з ГІ спостерігалося 60% тварин з важкими неврологічними симптомами. Під впливом нооглютила цей показник знижувався до 25%, а в щурів, які одержували сполуку І - до 15%. Таким чином, сполука 1а справляла виражений позитивний ефект відносно динаміки розвитку неврологічного дефіциту в щурів після ГІ і цей ефект речовини був виражений більшою мірою, ніж у нооглютила. Дослідження процесів навчання й пам'яті у тварин на моделі УРПУ показало, що при відтворенні рефлексу через 24 години після навчання, поведінка удавано оперованих щурів істотно не відрізнялася від поведінки як інтактних тварин, так і щурів з ГІ, що одержували і не одержували нооглютил або сполуку І (Таблиця 6). 70 - 80 % тварин пам'ятали про удар струмом у темній камері й не заходили туди. Інші закономірності відзначалися при відтворенні УРПУ на 14 добу. Так, якщо в 65% інтактних й в 57% удавано оперованих тварин відзначалося збереження пам'ятного сліду, то в групі з ГІ про удар струмом пам'ятали лише 8% щурів. Нооглютил, у дозі 20 мг/кг, збільшував цей показник у щурів з ГІ в 5 разів, а сполука І, в дозі 20 мг/кг, - в 6,5 рази, тобто сприяло більш тривалому збереженню пам'ятного сліду (Таблиця 6). Обидва препарати статистично достовірно скорочували латентний час заходу в темну небезпечну камеру. Німодипін справляв більш слабкий ефект на цій моделі. Таким чином, у результаті проведених досліджень установлено, що в щурів з ГІ спостерігався виражений неврологічний дефіцит, ослаблення процесів навчання і пам'яті, загибель тварин. При цьому відзначалося поглиблення патологічної симптоматики до 14-го дня спостереження. Динаміка погіршення стану й загибелі щурів з ГІ може свідчити про приховану недостатність компенсаторних реакцій організму, які наростають у певні критичні дні (3, 7, 14 . доба) післяопераційного періоду й розвитку супутніх ускладнень (набряк, набрякання тканин, порушення інтрацеребральної гемодинаміки, підвищеного внутрішньочерепного тиску, ішемії мозку). Сполука І при введенні тваринам однократно через 3-3,5 години після створення геморагічного інсульту має виражену протиінсультну дію, запо 93269 10 бігаючи загибелі щурів й істотно послабляючи порушення неврологічного статусу, поліпшуючи пам'ять тварин з посттравматичною гематомою геморагічним інсультом. За протиінсультною активністю сполука І перевершує нооглютил. Приклад 8. Вивчення ефективності солі Nнікотиноїламіно-кислоти (сполука І) і нооглютила на порушення пам'яті та неврологічний дефіцит у старих щурів (24 міс.) У роботі використали білих безпородних щурів-самців лінії Вистар у статевозрілому віці 3 міс. масою 250-300 г та старому віці 24 міс. масою 350-450 г. Нооглютил у дозі 20 мг/кг і сполуку І уводили старим щурам внутрішньочеревинно протягом 2-х місяців, а потім оцінювали вплив речовини на порушені старінням навчання й пам'ять та неврологічний дефіцит. Статистичну обробку результатів проводили з використанням методу варіаційної статистики за Ст'юдентом, методу долей варіант, U-тесту. Вплив сполуки І на порушення пам'яті в старих тварин. Вироблення умовного рефлексу пасивного уникання (УРПУ) у щурів проводиться в установці Passive avoidance фірми Lafauette Instrument Co (США) (Ader R. et al., Retention of a passive avoidance response as a function of the intensity and duration of electric shock., Psychon.Sci.1972,v.26,p. 125-128; Вороніна Т.А. та співавт. Посібник з експериментального (доклінічного) вивчення нових фармакологічних речовин. М.Медицина.2005, с.308-320). Установка складається з маленької платформи, розташованої на відстані 1 метра від підлоги, освітленої спеціальною лампою та темної камери з електродною підлогою. Тварину поміщають на освітлену платформу перед входом у темну камеру установки хвостом до вхідного отвору й протягом трьох хвилин реєструють латентний час рефлексу, час перебування щура у світлому відсіку й кількість тварин, що не зайшли в темний відсік. Тварини, що віддають перевагу світлому відсіку, в досліді не використовуються. Потім у темній камері щур одержує однократне больове подразнення (0,45 мА), тривалість подразнення визначається вибіганням тварини з темного відсіку. Тест на відтворення УРПУ здійснюють через 24 години після навчання й проводять при повторному поміщенні тварин в установку з реєстрацією протягом 3 хвилин латентного періоду першого заходу щура в темну експериментальну камеру і кількості тварин, які не зайшли до неї. Показано, що контрольні щури 3-й місячного віку при відтворенні рефлексу через 24 години після навчання в 80% випадків не заходили в темну камеру або заходили з більшим латентним часом рефлексу (Таблиця 7). У групі старих 24-х місячних щурів умовний рефлекс відтворювали тільки 30% тварин, інші щури заходили в темну небезпечну камеру з коротким латентним часом рефлексу, що свідчить про порушення в щурів пам'яті. Старі щури, що одержували сполуку І а в дозі 20 мг/кг при відтворенні здійснювали рефлекс в 60% випадків. Такий же виразний ефект мав нооглютил, значно поліпшуючи в 60% щурів 11 процес відтворення пам'ятного сліду. Сполука І і нооглютил також статистично достовірно збільшували латентний час заходу в темну небезпечну камеру. Для оцінки в старих тварин неврологічного дефіциту (порушення координації рухів і здатності навчатися руховим реакціям) тварин поміщали на стрижень, що обертався. Реєструвалася кількість спроб необхідних для навчання навичці утримання на стрижні, що обертався, протягом 2х хвилин. Показано, що 100% молодих тварин з перших п'яти посадок навчалися утримуватися на стрижні, що обертався (0,5 про/хв), протягом 2-х хвилин (Таблиця 8). У цих умовах тільки 25% старих щурів навчалися цій навичці та й то починаючи з 11-ї по 14-у спробу. Це свідчить про порушення неврологічного статусу в старих щурів і ослабленні їхньої здатності навчатися руховим реакціям. Старі щури, що одержували протягом 2-х місяців нооглютил до 10 спроби навчилися навичці в 60% випадків, а ті, що одержували сполуку І - в 66% випадків. Аналіз кількості спроб, необхідних для навчання 50% тварин, показав, що зрілі щури досягали цього критерію з першої спроби, старі з 17-ї, старі тварини, що одержували нооглютил - з 7-ї, старі щури, що одержували сполуку 1а - з 6-ї. Таким чином, нооглютил і сполука І мають виражену геропротекторну дію в дослідах на старих 24-х місячних щурах, поліпшуючи процеси навчання й пам'яті і послаблюючи неврологічний дефіцит. Приклад 9. Вивчення антидепресивної активності солі N-нікотиноїламінокислоти (сполука І) і в дослідах на мишах лінії SAM У дослідженні були використані безпородні миші й миші лінії SAM P 10 (Takeda T. et al. Senescence-Accelerated Mouse(SAM): A novel murine model of accelerated senescence. J. Amer. Geriatr. Soc. 1991, v. 39, p. 911-919) вагою 26-31 г с прискореним старінням у віці 11 місяців. У тварин цієї лінії генетично детерміновані депресія і порушення навчання й пам'яті, симптоматика, що активно наростає, починаючи з 6 місячного віку (прискорене-старіння) (Miyamoto M. Characteristics of age-related behavioral changes in Senescence-Accelerated Mouse SAMP8 and SAMP 10. Exp. Gerontol. 1997, v.32, p.139-148; Shimada A. et al. Age-related deterioration in conditional avoidance task in the SAM-P/10 mouse, an animal model of spontaneous brain atrophy. Brain Res., 1993, v. 608, p. 266-272). Для оцінки депресивного стану була використана методика примусового плавання (Porsolt R.D et al. Behavioral despaire in rats: a new model sensitive to antidepressant treatment. Europ.J.Pharmacol., 1978, V. 47, p. 370391). Мишей поміщали в циліндр діаметром 10см, висотою -25см. Циліндр наповнювали на 1/3 водою (27° С). Після невдалих спроб вибратися з води тварини приймають характерну нерухому позу, що розцінюють як прояв пригніченості, "розпачу". Фіксують час всіх активних спроб тварин вибратися з води протягом перших 6 хвилин після занурення у воду. Під впливом антидепресантів, незалежно від механізму їхньої дії, актив 93269 12 ність тварин зростає й час нерухомості (іммобілізації) зменшується. Показано, що миші лінії SAM значно менш активні, ніж безпородні тварини, тобто тривалість активного плавання цих тварин статистично достовірно менше (Таблиця 9). Відповідно до використовуваного методу це свідчить про більш виражений депресивноподібний стан мишей лінії SAM. Сполука І у всіх використовуваних дозах 5,10 і 20 мг/кг збільшувало час активної поведінки мишей. Найбільш яскраво цей ефект виявлявся в речовини в дозі 20 мг/кг (Р 0,03). Отримані результати свідчать про наявність антидепресивної активності у сполуки І. Ефект сполуки 1а порівняємо з дією амітриптиліна. Приклад 10. Вивчення анксіолітичної активності сполуки І у дослідах на мишах лінії SAM P10 У дослідженні були використані безпородні миші і миші лінії SAM P 10 (Scenecent accelerated mause) вагою 26-31 г з прискореним старінням (Takeda T. et al. Senescence-Accelerated Mouse(SAM): A novel murine model of accelerated senescence. J. Amer. Geriatr. Soc. 1991, v. 39, p. 911-919) у віці 11 місяців. У тварин цієї лінії генетично детерміновані депресія і порушення навчання й пам'яті, симптоматика, що активно наростає починаючи з 6 місячного віку (прискорене старіння) (Miyamoto M. Characteristics of agerelated behavioral changes in SenescenceAccelerated Mouse SAMP8 and SAMP 10. Exp. Gerontol. 1997, v. 32, p. 139-148; Shimada A. et al. Age-related deterioration in conditional avoidance task in the SAM-P/10 mouse, an animal model of spontaneous brain atrophy. Brain Res., 1993, v. 608, p. 266-272). Оцінка рівня тривожності мишей проводилася в умовах методики піднятого хрестоподібного лабіринту (ПХЛ) (Pellow S., et al. Validation of open: closed arm entries in elevated plus-maze as a nuasure of anxiety in the rat. Neurosci Meth J. 1985, № 14, p. 149-167; Вороніна Т.А.та співавт. Посібник з експериментального (до клінічного) вивчення нових фармакологічних речовин. М. Медицина. 2005, с. 253-263). Лабіринт являє собою перехрещені смужки розміром 5x45 см, два протилежних відсіки мають вертикальні стінки висотою 30 см (закриті, темні рукави), а два інших - відкриті, світлі рукави. Лабіринт піднятий від підлоги на 30 см. У місці перехрестя площин перебуває центральна платформа 50x50 см. Мишей поміщали на центральну площадку хвостом до світлого рукава. Реєструвався час, проведений тваринами у відкритих і закритих рукавах, число заходів у світлі й темні рукави. Загальний час спостереження для кожної тварини становив 5 хв. Як критерій анксіолітичного ефекту використовували показник часу, проведеного у відкритих рукавах установки. Установлено, що контрольні тварини більшу частину 5-ти хвилинного часу спостереження проводили в закритих рукавах лабіринту. Сполука І у всіх використовуваних дозах, а саме - 5,10 і 20 мг/кг збільшувала основний показник поведінки мишей - час, проведений у відкритих, незахищених рукавах лабіринту. При цьому й ефект речовини в дозах 10 і 20 мг/кг був статистично 13 93269 достовірним (Таблиця 10). Особливо ефективна сполука І у дозі 20 мг/кг. Отримані результати свідчать про наявність у сполуки І анксіолітичного ефекту на моделі піднятого хрестоподібного лабіринту. Приклад 11. Вивчення гострої добової токсичності солі N-нікотиноїламінокислоти (сполука І) і в дослідах на мишах Дослідження гострої добової токсичності сполуки 1а проводилося в дослідах на безпородних мишах самцях вагою 25-28г, що утримуються у звичних умовах у віварії при вільному доступі до їжі та води. Сполуку І уводили однократно внутрішньочеревинно. Після введення речовини тварини спостерігалися протягом 2-х діб. При вивченні токсичності сполуки І були використані наступні дози: 800 мг/кг, 1000 мг/кг, 1200 мг/кг, 1500 мг/кг, 1600 мг/кг. Сполуку І розчиняли в дистильованій воді і уводили в об'ємі 0,1 мл на 10 г ваги тварини при використанні доз 800 мг/кг, 1000 мг/кг та в об'ємі 0,2 мл на 10г ваги тварини при використанні доз 1200 мг/кг, 1500 мг/кг, 1600 мг/кг. Контрольним тваринам вводили дистильовану воду в об'ємі 0,2 мл на 10 г ваги. Кількість тварин у кожній групі становило 10 особин. Введення контрольним тваринам дистильованої води в об'ємі 0,2 мл на 10г ваги не викликає загибелі. Результати дослідження зі сполукою І представлені в таблиці 11. Установлено, що сполука І у дозі 1000 мг/кг викликає загибель 20% мишей через 48 годин спостереження, у дозі 1200 мг/кг - 60% мишей, у дозі 1500 мг/кг - 90% мишей і у дозі 1600 мг/кг 90% мишей. ЛД50 (доза, що викликає загибель 50% тварин) становить для сполуки І - 1150 14 (11101196) мг/кг. Для нооглютила ЛД50 становить 1200 (10904320) мг/кг. Таким чином, сполука І має токсичність, подібну з нооглютилом. Висновок Установлено, що солі Nоксинікотиноїлглютамінової кислоти мають виражену антиамнестичну і протигіпоксичну активність. Найбільш ефективною сполукою за основними для ноотропів і нейропротекторів проявами дії є сполука І. Її ефект за антиамнестичною і протигіпоксичною дією виявляється в діапазоні доз від 5 до 120 мг/кг і перевершує за активністю нооглютил. Сполука І має виразну протиінсультну дію на експериментальних моделях ішемічного і геморагічного інсультів, запобігаючи загибелі щурів, послабляючи неврологічний дефіцит, поліпшуючи процеси навчання і пам'яті. Протиінсультні властивості сполуки І виражені більшою мірою і виявляються в менших дозах, ніж у нооглютила. Сполука І ефективна для старих тварин: поліпшує пам'ять і рухові функції. Істотною перевагою сполуки І перед нооглютилом є наявність у спектрі її фармакологічної активності антидепресивного і анксіолітичного ефектів, які виявляються на моделі депресивноподібного стану в тесті примусового плавання і на моделі тривожного стану в тесті піднятого хрестоподібного лабіринту. Сполука І має також нейропротекторну дію, що виражається в здатності речовини відновлювати уражені при інсульті ділянки мозку, і геропротекторний ефект, який характеризується ослабленням неврологічних дефіцитів і поліпшенням когнітивних функцій і фізичної працездатності. Таблиця 1 Протигіпоксична дія солей N-нікотиноїламінокислот (сполуки І - III) і нооглютилу Речовина Контроль Нооглютил Сполука І Сполука II Сполука III Доза, мг/кг Дистильована вода 30 60 120 30 60 120 30 60 120 30 60 120 Тривалість життя мишей у Тривалість життя мишей у хвилинах при гіпобаричній хвилинах при гіпоксії в гіпоксії гермооб'ємі 3,63 ±0,31 4,1 ±0,77 7,68 ± 0,54* 6,51 ± 0,82* 9,17 ±0,91* v 4,15 ±0,44 5,95 ± 0,84* 3,91 ± 0,63 5,52 ±0,54* 14,3 ±0,51 13,9 ±0,42 15,2 ±0,39 16,4 ±0,53* 16,2 ±0,31* 17,8 ±0,41* 18,1 ±0,48* 14,1 ±0,71 16,3 ±0,64 17,8 ±0,69* 14,2 ±0,39 15,9 ±0,45 17,4 ±0,65* *- достовірність розходжень між контролем і дослідом при Р < 0,05 (U - критерій Манна - Уїтні). 15 93269 16 Таблиця 2 Антиамнестична дія солей N-нікотиноїламінокислот (сполуки І - III) та нооглютилу Сполука Контроль без амнезії Контроль з амнезією Нооглютил Сполука І Сполука II Сполука III Доза, мг/кг Дистил. вода Дистил. вода 25 50 25 50 25 50 25 50 Час, проведений щурами при відтворенні рефлекса, в секундах на освітленій платформі у темній камері 98,2 ±18,4 21,8 ±5,2 32,3 ± 7,2* 87,7 ±12,3* 46,7 ±13,4 73,3 ±13,4 54,3 ± 10,2** 65,7 ±7,1** 55,8 ±9,3** 64,2 ± 6,4** 79,4 ±12,8** 40,6 ±8,3** 41,3 ±11,6 78,7 ±12,3 52,5 ±12,3** 67,5± 15,1** 49,3 ±10,1 70,7 ± 9,4 51,4 ±9,8** 68,6 ±7,1** *- достовірність розходжень між контролем без амнезії й контролем з амнезією при Р < 0,05; **- достовірність розходжень між контролем з амнезією та ефектами речовин при Р < 0,05 (U - критерій Манна - Уїтні). Таблиця 3 Вплив солі N-нікотиноїламінокислоти (сполука І) та нооглютилу на моделі масивної кортикальної ішемії на виразність ішемічного ураження кори головного мозку (оцінка зрізів по балах) Сполуки/зрізи Фіз р-н (n=10) Нооглютил, 50 мг/кг (n=9) Сполука І, 40мг/кг (n=10) 1 2 3 4 5 0,6±0,1 1,52±0,15 1,45±0,18 0,74±0.21 0,23±0.17 0,28±0,06* 1,12±0,17* 1,01±0,11* 0,59±0,19 0,18±0,14 0,08±0,01* 0,92±0,12* 0,7±0,19* 0,58±0.14 0,2±0,15 *р
ДивитисяДодаткова інформація
Назва патенту англійськоюMono-and divalent salts of n-(5-hydroxynicotinoil)-l-glutaminic acid exhibiting psychotropic (antidepressant, anxyolytic), neuroprotective, heroprotective and cerebroprotective action
Автори англійськоюYakimuk Pavel Vasilievich, Stovbun Serhei Vitalievich, Litvin Aleksandr Anatolievich
Назва патенту російськоюОдно- и двухвалентные соли n-(5-гидроксиникотиноил)-l-глутаминовой кислоты, которые имеют психотропное (антидепрессивное и анксиолитическое), нейропротекторное, геропротекторное и противоинсультное действие
Автори російськоюЯкимук Павел Васильевич, Стовбун Сергей Витальевич, Литвин Александр Анатольевич
МПК / Мітки
МПК: A61K 31/195, C07D 213/04, A61P 25/00, A61K 31/435
Мітки: кислоти, протиінсультну, психотропну, геропротекторну, солі, анксіолітичну, мають, антидепресивну, нейропротекторну, одної, двовалентні, n-(5-гідроксинікотиноїл)-l-глутамінової, дію
Код посилання
<a href="https://ua.patents.su/11-93269-odno-ta-dvovalentni-soli-n-5-gidroksinikotinol-l-glutaminovo-kisloti-shho-mayut-psikhotropnu-antidepresivnu-ta-anksiolitichnu-nejjroprotektornu-geroprotektornu-i-protiinsultnu-diyu.html" target="_blank" rel="follow" title="База патентів України">Одно- та двовалентні солі n-(5-гідроксинікотиноїл)-l-глутамінової кислоти, що мають психотропну (антидепресивну та анксіолітичну), нейропротекторну, геропротекторну і протиінсультну дію</a>
Попередній патент: Система та спосіб вирощування рослин
Наступний патент: Спосіб прокатування-розділяння
Випадковий патент: Пристрій керування положенням виконавчого механізму з використанням сервоклапана із заморожуванням при відмові