Фармацевтична композиція з інгібіторами dpp iv
Формула / Реферат
1. Фармацевтична композиція, яка містить як діючу речовину сполуку-інгібітор DPP IV з аміногрупою або її сіль, перший розріджувач, другий розріджувач, сполучне, розпушувач і змащувальну речовину, де інгібітор DPP IV присутній у кількості від 0,5 мг до 10 мг, зокрема 0,5 мг, 1 мг, 2,5 мг, 5 мг або 10 мг, де розріджувачі вибирають з порошкової целюлози, безводного дикальційфосфату, дигідрату дикальційфосфату, еритриту, гідроксипропілцелюлози з низьким ступенем заміщення, маніту, попередньо желатинізованого крохмалю та ксиліту.
2. Фармацевтична композиція за п. 1, яка містить додатковий розпушувач.
3. Фармацевтична композиція за п. 1 або 2, яка містить додаткову ковзну речовину.
4. Фармацевтична композиція за п. 1, у якій перший розріджувач являє собою маніт, а другий розріджувач являє собою попередньо желатинізований крохмаль.
5. Фармацевтична композиція за п. 1, у якій змащувальна речовина являє собою тальк, поліетиленгліколь, бегенат кальцію, стеарат кальцію, гідрогенізовану рицинову олію або стеарат магнію.
6. Фармацевтична композиція за п. 1, у якій сполучне являє собою коповідон (співполімери вінілпіролідону з іншими похідними вінілу), гідроксипропілметилцелюлозу, гідроксипропілцелюлозу або полівінілпіролідон (повідон).
7. Фармацевтична композиція за п. 1, у якій розпушувач являє собою кукурудзяний крохмаль.
8. Фармацевтична композиція за п. 2, у якій додатковий розпушувач являє собою кросповідон.
9. Фармацевтична композиція за п. 3, у якій необов'язкова ковзна речовина являє собою колоїдний діоксид кремнію.
10. Фармацевтична композиція за п. 1, у якій перший розріджувач являє собою маніт, другий розріджувач являє собою попередньо желатинізований крохмаль, сполучне являє собою коповідон, розпушувач являє собою кукурудзяний крохмаль, а змащувальна речовина являє собою стеарат магнію.
11. Фармацевтична композиція за п. 1, яка містить діючу речовину в кількості від 0,5 до 20 %, розріджувач 1 у кількості від 40 до 88 %, розріджувач 2 у кількості від 3 до 40 %, сполучне у кількості від 1 до 5 %, розпушувач у кількості від 5 до 15 % і змащувальну речовину у кількості від 0,1 до 4 %.
12. Фармацевтична композиція за п. 1, яка містить діючу речовину в кількості від 0,5 до 7 %, розріджувач 1 у кількості від 50 до 75 %, розріджувач 2 у кількості від 5 до 15 %, сполучне у кількості від 2 до 4 %, розпушувач у кількості від 8 до 12% і змащувальну речовину у кількості від 0,5 до 2 %.
13. Фармацевтична композиція за п. 1, представлена в лікарській формі у вигляді капсули, таблетки або таблетки із плівковим покриттям.
14. Фармацевтична композиція за п. 13, у якій на частку плівкового покриття припадає від 2 до 4 %.
15. Фармацевтична композиція за п. 14, у якій плівкове покриття містить плівкоутворювач, пластифікатор, ковзну речовину і необов'язково один або декілька пігментів.
16. Фармацевтична композиція за п. 15, у якій плівкове покриття містить гідроксипропілметилцелюлозу, поліетиленгліколь, тальк, діоксид титану й оксид заліза.
17. Спосіб приготування фармацевтичної композиції за п. 1, який полягає в тому, що
а) сполучне розчиняють у розчиннику з одержанням рідини для гранулювання
б) інгібітор DPP IV змішують із розріджувачем і розпушувачем з одержанням преміксу,
в) премікс зволожують рідиною для гранулювання й потім зволожений премікс гранулюють,
г) гранульований премікс при необхідності просіюють через сито з розміром комірок принаймні 1,0 мм,
д) гранулят сушать при температурі приблизно від 40 до 75 °С до зменшення маси висушуваного матеріалу на 1-5 %,
є) висушений гранулят просіюють через сито з розміром комірок принаймні 0,6 мм і
ж) до грануляту додають змащувальну речовину для остаточного змішування.
18. Спосіб за п. 17, при здійсненні якого додатково
з) з залишкової суміші пресують серцевини таблеток,
ж) готують суспензію для нанесення покриття й
к) на серцевини таблеток наносять покриття із суспензії для нанесення покриття до збільшення їх маси на приблизно 2-4 % з одержанням таблеток із плівковим покриттям.
19. Спосіб за п. 17, при здійсненні якого частину допоміжних речовин додають після процесу гранулювання, перед остаточним змішуванням на стадії ж).
20. Спосіб за п. 17, при здійсненні якого гранулят на стадіях а)-д) одержують методом гранулювання в одному багатофункціональному апараті для гранулювання зі створенням високого зсувного зусилля й потім сушать у ньому отриманий гранулят.
21. Фармацевтична композиція за п. 1, яка містить як діючу речовину сполуку-інгібітор DPP IV з аміногрупою, вибрану із
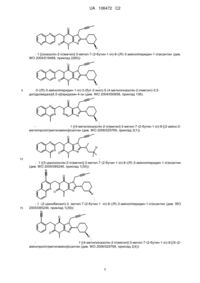
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-аміпопінеридин-1-іл)ксантину,
1-[([1,5]нафтиридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(хіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
2-((R)-3-амінопіперидин-1-іл)-3-(бут-2-иніл)-5-(4-метилхіназолін-2-ілметил)-3,5-дигідроімідазо[4,5-d]піридазин-4-ону,
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(2-аміно-2-метилпропіл)метиламіно]ксантину,
1-[(3-ціанохінолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
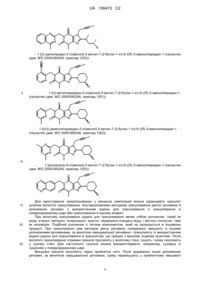
1-(2-ціанобензил)-3-метил-7-(2-бутин-1-іл)-8-((R)-3-аміноніперидин-1-іл)ксантину,
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(S)-(2-амінопропіл)метиламіно]ксантину,
1-[(3-ціанопіридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(4-метилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(4,6-диметилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину та
1-[(хіноксалін-6-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
або її сіль, перший розріджувач, другий розріджувач, сполучне, розпушувач і змащувальну речовину; де розріджувачі вибирають з еритриту, гідроксипропілцелюлози з низьким ступенем заміщення, маніту, попередньо желатинізованого крохмалю та ксиліту.
22. Фармацевтична композиція за п. 1, де сполучне вибирають з коповідону (співполімеру вінілпіролідону з іншими похідними вінілу), гідроксипропілметилцелюлози, гідроксипропілцелюлози, полівінілпіролідону (повідону), попередньо желатинізованого крохмалю та гідроксипропілцелюлози з низьким ступенем заміщення; розпушувач вибирають з кукурудзяного крохмалю, кросповідону, гідроксипропілцелюлози з низьким ступенем заміщення та попередньо желатинізованого крохмалю; та змащувальну речовину вибирають з тальку, поліетиленгліколю, бегенату кальцію, стеарату кальцію, гідрогенізованої рицинової олії та стеарату магнію.
23. Спосіб за п. 17, де сполучне вибирають з коповідону (співполімеру вінілпіролідону з іншими похідними вінілу), гідроксипропілметилцелюлози, гідроксипропілцелюлози, полівінілпіролідону (повідону), попередньо желатинізованого крохмалю та гідроксипропілцелюлози з низьким ступенем заміщення; розпушувач вибирають з кукурудзяного крохмалю, кросповідону, гідроксипропілцелюлози з низьким ступенем заміщення та попередньо желатинізованого крохмалю; та змащувальну речовину вибирають з тальку, поліетиленгліколю, бегенату кальцію, стеарату кальцію, гідрогенізованої рицинової олії та стеарату магнію.
Текст
Реферат: У заявці описані фармацевтичні композиції на основі інгібіторів DPP IV з аміногрупою, їх приготування і їх застосування при лікуванні цукрового діабету. UA 106472 C2 (12) UA 106472 C2 UA 106472 C2 5 10 15 20 25 30 35 40 45 50 55 Даний винахід стосується фармацевтичних композицій на основі вибраних інгібіторів DPP IV, їх приготування й їх застосування в медицині для лікування певних станів. Фермент DPPIV (дипептидилпептидаза IV), відомий також за назвою CD26, являє собою серинпротеазу, що сприяє відщепленню дипептидів у білків із проліновим або аланіновим залишком на N-кінці. Тим самим інгібітори DPP IV впливають на рівень біоактивних пептидів, включаючи пептид GLP-1, у плазмі крові й вважаються багатообіцяючими лікарськими речовинами при лікуванні цукрового діабету. При спробах приготування фармацевтичних композицій на основі вибраних інгібіторів DPPIV виявлялося, що інгібітори DPPIV з первинною або вторинною аміногрупою виявляються несумісні із багатьма традиційними допоміжними речовинами, такими як мікрокристалічна целюлоза, натрійкрохмальгліколят, натрієва сіль кроскармелози, винна кислота, лимонна кислота, глюкоза, фруктоза, сахароза, лактоза й мальтодекстрини, проявляють схильність до розкладання або створюють проблеми з екстракцією при контакті з такими допоміжними речовинами. Хоча такі сполуки й мають винятково високу власну стабільність, однак вони реагують із більшістю використовуваних у твердих лікарських формах допоміжних речовин і з домішками, які містяться в них, насамперед при тісному контакті з ними, наприклад, у таблетках і при високому співвідношенні між допоміжними речовинами й лікарською (діючою) речовиною. Вважають, що при цьому аміногрупа вступає в реакцію із цукрами, які мають відновну дію, і з іншими реакційноздатними карбонільними групами, а також з функціональними карбоксигрупами, які утворюються, наприклад, на поверхні мікрокристалічної целюлози в результаті окислення. З подібними непередбаченими труднощами доводиться зіштовхуватися головним чином при застосуванні вибраних інгібіторів у низьких дозах, у яких їх потрібно використовувати у зв'язку з їх винятково високою активністю або ефективністю. Виходячи з вищевикладеного, існує потреба у фармацевтичних композиціях, які дозволили б усунути вказані технічні проблеми, пов'язані зі несподівано високою активністю вибраних сполукінгібіторів DPP IV. Для вирішення цієї задачі у винаході пропонується фармацевтична композиція, призначена для регуляції рівня глюкози в крові (глікемічного контролю) у пацієнта із цукровим діабетом типу 1 або типу 2 і яка містить як діючу речовину інгібітор DPP IV з аміногрупою, насамперед з вільною або первинною аміногрупою, перший і другий розріджувачі, сполучне, розпушувач і змащувальну речовину. Запропонована у винаході фармацевтична композиція може також містити додатковий розпушувач і додаткову ковзну речовину. Запропоновані у винаході фармацевтичні композиції можуть використовуватися також для лікування ревматоїдного артриту, ожиріння й остеопорозу, а також для підтримуючої терапії після алотрансплантації. Для застосування як розріджувачі в запропонованій у винаході фармацевтичній композиції придатні порошкова целюлоза, безводний дикальційфосфат, дигідрат дикальційфосфату, еритрит, гідроксипропілцелюлоза з низьким ступенем заміщення, маніт, попередньо желатинізований крохмаль (ПЖК) і ксиліт. Серед цих розріджувачів переважний маніт і попередньо желатинізований крохмаль. До числа розріджувачів, які переважно використовувати як другий розріджувач, належать вказані вище розріджувачі - попередньо желатинізований крохмаль і гідроксипропілцелюлоза з низьким ступенем заміщення (НЗ-ГПЦ), які додатково мають властивості сполучних. Для застосування як змащувальні речовини в запропонованій у винаході фармацевтичній композиції придатні тальк, поліетиленгліколь, бегенат кальцію, стеарат кальцію, гідрогенізована рицинова олія й стеарат магнію. Переважною змащувальною речовиною є стеарат магнію. Для застосування як сполучні у запропонованій у винаході фармацевтичній композиції придатні коповідон (співполімери вінілпіролідону з іншими похідними вініла), гідроксипропілметилцелюлоза (ГПМЦ), гідроксипропілцелюлоза (ГПЦ), полівінілпіролідон (повідон), попередньо желатинізований крохмаль і гідроксипропілцелюлоза з низьким ступенем заміщення (НЗ-ГПЦ), серед яких переважні коповідон і попередньо желатинізований крохмаль. Вказані вище сполучні - попередньо желатинізований крохмаль і НЗ-ГПЦ - додатково мають властивості розріджувачів і розпушувачів і тому можуть використовуватися як другий розріджувач або розпушувач. Для застосування як розпушувачі в запропонованій у винаході фармацевтичній композиції придатні кукурудзяний крохмаль, кросповідон, гідроксипропілцелюлоза з низьким ступенем заміщення (НЗ-ГПЦ) і попередньо желатинізований крохмаль, серед яких переважний кукурудзяний крохмаль. У запропонованій у винаході фармацевтичній композиції можна як додаткову ковзну речовину використовувати колоїдний діоксид кремнію. 1 UA 106472 C2 5 10 15 20 25 В одному з варіантів запропонована у винаході фармацевтична композиція містить, наприклад, маніт як розріджувач, попередньо желатинізований крохмаль як розріджувач, який додатково має властивості сполучного, коповідон як сполучне, кукурудзяний крохмаль як розпушувач і стеарат магнію як змащувальну речовину. Дозовані лікарські форми, які готують на основі запропонованих у винаході фармацевтичних композицій, містять діючі речовини в дозі від 0,1 до 100 мг. Переважні дозовані лікарські форми, що містять діючі речовини в дозі 0,5 мг, 1 мг, 2,5 мг, 5 мг і 10 мг. Типові фармацевтичні композиції містять (у мас. %) діючу речовину в кількості від 0,5 до 20 %, розріджувач 1 у кількості від 40 до 88 %, розріджувач 2 у кількості від 3 до 40 %, сполучне у кількості від 1 до 5 %, розпушувач у кількості від 5 до 15 % і змащувальну речовину у кількості від 0,1 до 4 %. Переважні фармацевтичні композиції містять (у мас. %) діючу речовину в кількості від 0,5 до 7 %, розріджувач 1 у кількості від 50 до 75 %, розріджувач 2 у кількості від 5 до 15 %, сполучне у кількості від 2 до 4 %, розпушувач у кількості від 8 до 12 % і змащувальну речовину у кількості від 0,5 до 2 %. Запропоновані у винаході фармацевтичні композиції призначені для перорального застосування (прийому всередину) і можуть бути представлені в дозованій лікарській формі у вигляді капсули, таблетки або таблетки із плівковим покриттям (філм-таблетки). Звичайно на частку плівкового покриття припадає від 2 до 4 %, переважно 3 %, від всієї композиції, і воно містить плівкоутворювач, пластифікатор, ковзну речовину й необов'язково один або декілька пігментів. Композиція для нанесення плівкового покриття може містити, наприклад, гідроксипропілметилцелюлозу (ГПМЦ), поліетиленгліколь (ПЕГ), тальк, діоксид титану й необов'язково оксид заліза. Переважними згідно із даним винаходом діючими речовинами є інгібітори DPPIV з первинною аміногрупою і їх солі, наприклад, будь-який інгібітор DPP IV і його сіль формули (І) O R1 N N O R2 N N (І), або формули (II) O R1 N N R2 N 30 35 N (ІІ), де R1 означає ([1,5]нафтиридин-2-іл)метил, (хіназолін-2-іл)метил], (хіноксалін-6-іл)метил, (4метилхіназолін-2-іл)метил, 2-ціанобензил, (3-ціанохінолін-2-іл)метил, (3-ціанопіридин-2іл)метил, (4-метилпіримідин-2-іл)метил або (4,6-диметилпіримідин-2-іл)метил, a R2 означає 3(R)-амінопіперидин-1-іл, (2-аміно-2-метилпропіл)метиламіногрупу або (2-(S)амінопропіл)метиламіногрупу. До переважних інгібіторів DPP IV належать наступні сполуки і їх солі: 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1іл)ксантин (див. WO 2004/018468, приклад 2(142): O N N N N O N N N N ; 1-[([1,5]нафтиридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1іл)ксантин (див. WO 2004/018468, приклад 2(252)): 2 UA 106472 C2 O N N N N O N N N N ; - 1-[(хіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантин (див. WO 2004/018468, приклад 2(80)): O N N N N O N N N N 5 ; -2-((R)-3-амінопіперидин-1-іл)-3-(бут-2-иніл)-5-(4-метилхіназолін-2-ілметил)-3,5дигідроімідазо[4,5-е]піридазин-4-он (див. WO 2004/050658, приклад 136): O N N N N N N N N ; 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(2-аміно-2метилпропіл)метиламіно]ксантин (див. WO 2006/029769, приклад 2(1)): O N N 10 N N O N N N N ; - 1-[(3-ціанохінолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантин (див. WO 2005/085246, приклад 1(30)): N O N N N 15 O N N N N ; - 1 -(2-ціанобензил)-3 -метил-7-(2-бутин-1 -іл)-8-((R)-3-амінопіперидин-1-іл)ксантин (див. WO 2005/085246, приклад 1(39)): N O N N O N N N N ; 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(S-(2амінопропіл)метиламіно]ксантин (див. WO 2006/029769, приклад 2(4)): 3 UA 106472 C2 O N N N N O N N N N ; - 1-[(3-ціанопіридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантин (див. WO 2005/085246, приклад 1(52)): N O N N N O N N N N 5 ; 1-[(4-метилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1іл)ксантин (див. WO 2005/085246, приклад 1(81)): O N N N N O N N N N ; - 1-[(4,6-диметилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1 іл)ксантин (див. WO 2005/085246, приклад 1(82)): O N N 10 N N O N N N N ; 1-[(хіноксалін-6-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантин (див. WO 2005/085246, приклад 1(83)): O N N NN O N N N N 15 20 25 . Для приготування запропонованих у винаході композицій можна одержувати гранулят шляхом вологого гранулювання. Альтернативними методами гранулювання діючої речовини й допоміжних речовин з використанням рідини для гранулювання є гранулювання в псевдозрідженому шарі або гранулювання в одному апараті. При вологому гранулюванні рідина для гранулювання являє собою розчинник, такий як вода, етанол, метанол, ізопропанол, ацетон, переважно очищену воду, і містить сполучне, таке як коповідон. Подібний розчинник є летким компонентом, який не залишається в кінцевому продукті. При гранулюванні цим методом діючу речовину попередньо змішують із іншими допоміжними речовинами, за винятком змащувальної речовини і гранулюють із використанням водної рідини для гранулювання в грануляторі, що працює з високим зсувним зусиллям. Після вологого гранулювання отримані гранули просіюють у вологому стані, сушать і знову просіюють у сухому стані. Для наступного сушіння можна використовувати, наприклад, сушарку із сушінням у псевдозрідженому шарі. Висушені гранули просіюють через прийнятне сито. Після додавання інших допоміжних речовин, за винятком змащувальної речовини, суміш перемішують у прийнятному змішувачі 4 UA 106472 C2 5 10 15 20 25 30 35 40 45 звичайного типу, наприклад, у гравітаційному змішувачі, після чого додають змащувальну речовину наприклад, стеарат магнію, і остаточно перемішують у змішувачі. Таким чином, спосіб приготування запропонованої у винаході фармацевтичної композиції методом вологого гранулювання полягає, наприклад, у тому, що а) сполучне, наприклад коповідон, при навколишній температурі розчиняють у розчиннику, наприклад очищеній воді, з одержанням рідини для гранулювання, б) інгібітор DPP IV змішують у прийнятному змішувачі з розріджувачем і розпушувачем з одержанням преміксу (попередньо приготовленої суміші), в) премікс зволожують рідиною для гранулювання й потім зволожений премікс гранулюють, наприклад, у змішувачі, що працює з високим зсувним зусиллям, г) гранульований премікс при необхідності просіюють через сито з розміром комірок принаймні 1,0 мм, переважно 1,6 мм, д) гранулят сушать при вхідній температурі сушильного повітря приблизно від 40 до 75 °C, переважно від 55 до 65 °C, наприклад, у сушарці із сушінням у псевдозрідженому шарі до зменшення маси висушуваного матеріалу на 1-5 %, є) висушений гранулят деагломерують, наприклад, шляхом просіювання через сито з розміром комірок від 0,6 до 1,6 мм, переважно 1,0 мм, і ж) до грануляту додають, переважно просіяну, змащувальну речовину для остаточного змішання, наприклад, у змішувачі з кубічним барабаном. В іншому варіанті частину допоміжних речовин або частину їх кількості, зокрема частину розпушувача (наприклад, кукурудзяного крохмалю) або розріджувача (наприклад, попередньо желатинізованого крохмалю), або додатковий розпушувач (кросповідон) можна додавати, після процесу гранулювання, перед остаточним змішуванням на стадії ж). У ще одному варіанті гранулят на стадіях а)-д) одержують методом гранулювання в одному - багатофункціональному - апараті для гранулювання зі створенням високого зсувного зусилля й потім сушать у ньому отриманий гранулят. Для одержання капсул остаточну суміш надалі розфасовують у капсули. Для виготовлення таблеток або їх серцевин з остаточної суміші надалі на прийнятному таблетувальному пресі пресують таблетки або їх серцевини з необхідною масою, з необхідними розмірами й з необхідною міцністю на роздавлювання. Для виготовлення таблеток із плівковим покриттям готують суспензію для нанесення покриття, з якої потім на отримані пресуванням серцевини таблеток у стандартній машині для нанесення плівкового покриття наносять покриття до збільшення їх маси приблизно на 2-4 %, переважно на 3 %. Використовуваний у складі подібної суспензії для нанесення плівкового покриття розчинник є летким компонентом, який не залишається в кінцевому продукті. Для зменшення необхідної кількості змащувальної речовини у таблетках можна використовувати зовнішню змащувальну систему. Приклади Приклад 1: Композиція для прямого пресування Діючу речовину - інгібітор DPP IV з первинною аміногрупою - змішують у змішувачі, що працює з високим зсувним зусиллям, з усіма іншими допоміжними речовинами, за винятком стеарату магнію. Отриманий таким шляхом премікс просіюють через сито з розміром комірок 1 мм. Після додавання стеарату магнію премікс перемішують у гравітаційному змішувачі з одержанням остаточної суміші. Із цієї остаточної суміші наприйнятному таблетувальному пресі потім пресують таблетки. Таким способом можна виготовляти таблетки наступного складу: Компонент Діюча речовина Маніт ПЖК Стеарат магнію Усього мг/таблетку 1,000 43,250 5,000 0,750 50,000 %/таблетку 2,000 86,500 10,000 1,500 100,000 мг/таблетку 2,500 108,125 12,500 1,875 125,000 %/таблетку 2,000 86,500 10,000 1,500 100,000 Компонент Діюча речовина Маніт ПЖК Стеарат магнію Усього мг/таблетку 5,000 216,250 25,000 3,750 250,000 %/таблетку 2,000 86,500 10,000 1,500 100,000 мг/таблетку 10,000 432,500 50,000 7,500 500,000 %/таблетку 2,000 86,500 10,000 1,500 100,000 5 UA 106472 C2 5 Приклад 2: Альтернативна композиція для прямого пресування Діючу речовину - інгібітор DPP IV з первинною аміногрупою - змішують у змішувачі, що працює з високим зсувним зусиллям, з усіма іншими допоміжними речовинами, за винятком стеарату магнію. Отриманий таким шляхом премікс просіюють через сито з розміром комірок 1 мм. Після додавання стеарату магнію премікс перемішують у гравітаційному змішувачі з одержанням остаточної суміші. Із цієї остаточної суміші на прийнятному таблетувальному пресі потім пресують таблетки. Таким способом можна виготовляти таблетки наступного складу: Компонент Діюча речовина Дикальційфосфат, безводний НЗ-ГПЦ Стеарат магнію Усього мг/таблетку 1,000 46,400 12,000 0,600 60,000 %/таблетку 1,667 77,333 20,000 1,000 100,000 мг/таблетку 0,500 46,900 12,000 0,600 60,000 %/таблетку 0,833 78,177 20,000 1,000 100,000 Компонент Діюча речовина Дикальційфосфат, безводний НЗ-ГПЦ Стеарат магнію Усього мг/таблетку 10,000 464,000 120,000 6,000 600,000 %/таблетку 1,667 77,333 20,000 1,000 100,000 мг/таблетку 10,000 344,000 90,000 6,000 450,000 %/таблетку 2,222 76,788 20,000 1,000 100,000 10 15 20 Приклад 3: Таблетки Коповідон розчиняють при навколишній температурі в очищеній воді з одержанням рідини для гранулювання. Окремо в прийнятному змішувачі діючу речовину - інгібітор DPP IV з первинною аміногрупою - змішують із манітом і частиною попередньо желатинізованого крохмалю з одержанням преміксу. Цей премікс зволожують рідиною для гранулювання й потім гранулюють. Після цього вологий гранулят просіюють через сито з розміром комірок 1,6 мм. Далі гранулят сушать при 55 °C у прийнятній сушарці до залишкового вмісту вологи, що відповідає зменшенню маси висушуваного матеріалу на 2-5 %. Висушений гранулят потім просіюють через сито з розміром комірок 1,0 мм. Після цього гранулят змішують у прийнятному змішувачі з іншою частиною попередньо желатинізованого крохмалю. До цієї суміші після деагломерації пропусканням через сито з розміром комірок 1 мм додають стеарат магнію. Потім шляхом остаточного перемішування в прийнятному змішувачі одержують остаточну суміш, з якої пресують таблетки. Таким способом можна виготовляти таблетки наступного складу: Компонент Діюча речовина Попередньо желатинізований крохмаль Маніт Коповідон Усього (гранулят) Попередньо желатинізований крохмаль Стеарат магнію Усього мг/таблетку 10,000 210,000 236,000 18,000 474,000 120,000 6,000 600,000 %/таблетку 1,667 35,000 39,333 3,000 79,000 20,000 1,000 100,000 25 30 35 Приклад 4: Таблетки з покриттям Коповідон розчиняють при навколишній температурі в очищеній воді з одержанням рідини для гранулювання. Окремо в прийнятному змішувачі діючу речовину - інгібітор DPP IV з первинною аміногрупою - змішують із манітом, попередньо желатинізованим крохмалем і кукурудзяним крохмалем з одержанням преміксу. Цей премікс зволожують рідиною для гранулювання й потім гранулюють у змішувачі, що працює з високим зсувним зусиллям. Після цього вологий гранулят просіюють через сито з розміром комірок 1,6 мм. Потім гранулят сушать у сушарці із псевдозрідженим шаром при температурі приблизно 60 °C до зменшення маси висушуваного матеріалу на 2-4 %. З остаточної суміші потім пресують серцевини таблеток. В прийнятному змішувачі при навколишній температурі гідроксипропілметилцелюлозу (ГПМЦ), поліетиленгліколь (ПЕГ), тальк, діоксид титану й оксид заліза суспендують в очищеній воді, готуючи таким шляхом суспензію для нанесення покриття. Цією суспензією покривають 6 UA 106472 C2 серцевини таблеток до збільшення їх маси приблизно на 3 % з одержанням таблеток із плівковим покриттям. Таким способом можна виготовляти таблетки наступного складу: Компонент Діюча речовина Маніт Попередньо желатинізований крохмаль Кукурудзяний крохмаль Коповідон Стеарат магнію Загальна маса (серцевина таблетки) ГПМЦ ПЕГ Діоксид титану Тальк Оксид заліза, жовтий Загальна маса (таблетка з покриттям) 5 10 15 25 30 35 мг 1,000 66,950 9,000 9,000 2,700 1,350 90,000 1,500 0,150 0,750 0,525 0,075 93,000 мг 2,500 65,450 9,000 9,000 2,700 1,350 90,000 1,500 0,150 0,750 0,525 0,075 93,000 мг 5,000 130,900 18,000 18,000 5,400 2,700 180,000 2,500 0,250 1,250 0,875 0,125 185,000 мг 10,000 125,900 18,000 18,000 5,400 2,700 180,000 2,500 0,250 1,250 0,875 0,125 185,000 Приклад 5: Таблетки Коповідон розчиняють при навколишній температурі в очищеній воді з одержанням рідини для гранулювання. Окремо в прийнятному змішувачі діючу речовину - інгібітор DPP IV з первинною аміногрупою - змішують у прийнятному змішувачі з манітом і попередньо желатинізованим крохмалем (ПЖК) з одержанням преміксу. Цей премікс зволожують рідиною для гранулювання й потім гранулюють. Після цього вологий гранулят просіюють через прийнятне сито. Потім гранулят сушать у прийнятній сушарці при температурі приблизно 50 °C до зменшення маси висушуваного матеріалу на 3-5 %. Висушений гранулят потім просіюють через сито з розміром комірок 1,0 мм. Стеарат магнію пропускають через сито з розміром комірок 1,0 мм і додають до грануляту. Потім шляхом остаточного перемішування в прийнятному змішувачі одержують остаточну суміш, з якої пресують таблетки. Таким способом можна виготовляти таблетки наступного складу: Компонент Діюча речовина Маніт ПЖК Коповідон Стеарат магнію Загальна маса таблетки 20 мг 0,500 67,450 9,000 9,000 2,700 1,350 90,000 1,500 0,150 0,750 0,525 0,075 93,000 мг 0,500 27,500 20,000 1,500 0,500 50,000 мг 1,000 27,000 20,000 1,500 0,500 50,000 мг 2,500 67,500 50,000 3,750 1,250 125,000 мг 5,000 135,000 100,000 7,500 2,500 250,000 мг 10,000 130,000 100,000 7,500 2,500 250,000 Приклад 6: Варіанти таблеток Коповідон розчиняють при навколишній температурі в очищеній воді з одержанням рідини для гранулювання. Окремо в прийнятному змішувачі діючу речовину - інгібітор DPP IV з первинною аміногрупою - змішують із частиною маніту, попередньо желатинізованого крохмалю (ПЖК) і кукурудзяного крохмалю з одержанням преміксу. Цей премікс зволожують рідиною для гранулювання й потім гранулюють. Після цього вологий гранулят просіюють через прийнятне сито. Потім гранулят сушать у сушарці із псевдозрідженим шаром при вхідній температурі сушильного повітря приблизно 60 °C до зменшення маси висушуваного матеріалу на 1-4 %. Висушений гранулят потім просіюють через сито з розміром комірок 1,0 мм. Стеарат магнію деагломерують пропусканням через сито й додають до грануляту. На цій же стадії додають також іншу частину, відповідно іншу кількість допоміжних речовин, які не використовували при гранулюванні. Потім шляхом остаточного перемішування в прийнятному змішувачі одержують остаточну суміш, з якої пресують серцевини таблеток. У прийнятному змішувачі при навколишній температурі гідроксипропілметилцелюлозу (ГПМЦ), поліетиленгліколь, тальк, діоксид титану й оксид заліза суспендують в очищеній воді, готуючи таким шляхом суспензію для нанесення покриття. Цією суспензією покривають серцевини таблеток до збільшення їх маси приблизно на 3 % з одержанням таблеток із плівковим покриттям. Таким способом можна виготовляти таблетки наступного складу: Приклад 6.1: Таблетка з допоміжними речовинами, які додають після процесу гранулювання 7 UA 106472 C2 Компонент Діюча речовина Маніт ПЖК Кукурудзяний крохмаль Коповідон Усього (гранулят) Кукурудзяний крохмаль ПЖК Маніт Стеарат магнію Усього (серцевина таблетки) Композиція Д мг/таблетку %/таблетку 1,000 1,111 23,300 25,889 4,500 5,000 4,500 5,000 1,350 1,500 34,650 38,500 4,500 5,000 4,500 5,000 45,000 50,000 1,350 1,500 90,000 100,000 Композиція Е мг/таблетку %/таблетку 1,000 1,111 66,950 74,389 4,500 5,000 4,500 5,000 2,700 3,000 79,650 88,500 4,500 5,000 4,500 5,000 1,350 90,000 1,500 100,000 Приклад 6.2: Таблетка з додатковим розпушувачем, який додають після процесу гранулювання 5 Компонент Діюча речовина Маніт ПЖК Кукурудзяний крохмаль Коповідон Загальна маса (гранулят) Стеарат магнію Кросповідон Загальна маса (серцевина таблетки) ГРМЦ ПЕГ Діоксид титану Тальк Оксид заліза, жовтий Загальна маса (таблетка з покриттям) мг 0,500 67,450 9,000 9,000 2,700 88,650 1,350 2,000 92,000 1,500 0,150 0,750 0,525 0,075 95,000 мг 1,000 66,950 9,000 9,000 2,700 88,650 1,350 2,000 92,000 1,500 0,150 0,750 0,525 0,075 95,000 мг 2,500 65,450 9,000 9,000 2,700 88,650 1,350 2,000 92,000 1,500 0,150 0,750 0,525 0,075 95,000 мг 5,000 130,900 18,000 18,000 5,400 177,300 2,700 4,000 184,000 2,500 0,250 1,250 0,875 0,125 189,000 мг 10,000 125,900 18,000 18,000 5,400 177,300 2,700 4,000 184,000 2,500 0,250 1,250 0,875 0,125 189,000 Приклад 6.3: Таблетка з високим вмістом діючої речовини (композиція Г) Компонент Діюча речовина Маніт ПЖК Кукурудзяний крохмаль Коповідон Усього (гранулят) Кросповідон Стеарат магнію Усього (серцевина таблетки) ГПМЦ Поліетиленгліколь Діоксид титану Тальк Оксид заліза, жовтий Усього (таблетка з покриттям) мг/таблетку 25,000 40,700 9,000 9,000 2,700 86,400 2,700 0,900 90,000 %/таблетку 27,778 45,222 10,000 10,000 3,000 96,000 3,000 1,000 100,000 мг/таблетку 50,000 81,400 18,000 18,000 5,400 172,800 5,400 1,800 180,000 %/таблетку 27,778 45,222 10,000 10,000 3,000 96,000 3,000 1,000 100,000 1,500 0,150 0,750 0,525 0,075 93,000 1,667 0,167 0,833 0,583 0,083 103,333 2,500 0,250 1,250 0,875 0,125 185,000 1,389 0,139 0,694 0,486 0,069 102,778 8 UA 106472 C2 ФОРМУЛА ВИНАХОДУ 5 10 15 20 25 30 35 40 45 50 55 60 1. Фармацевтична композиція, яка містить як діючу речовину сполуку-інгібітор DPP IV з аміногрупою або її сіль, перший розріджувач, другий розріджувач, сполучне, розпушувач і змащувальну речовину, де інгібітор DPP IV присутній у кількості від 0,5 мг до 10 мг, зокрема 0,5 мг, 1 мг, 2,5 мг, 5 мг або 10 мг, де розріджувачі вибирають з порошкової целюлози, безводного дикальційфосфату, дигідрату дикальційфосфату, еритриту, гідроксипропілцелюлози з низьким ступенем заміщення, маніту, попередньо желатинізованого крохмалю та ксиліту. 2. Фармацевтична композиція за п. 1, яка містить додатковий розпушувач. 3. Фармацевтична композиція за п. 1 або 2, яка містить додаткову ковзну речовину. 4. Фармацевтична композиція за п. 1, у якій перший розріджувач являє собою маніт, а другий розріджувач являє собою попередньо желатинізований крохмаль. 5. Фармацевтична композиція за п. 1, у якій змащувальна речовина являє собою тальк, поліетиленгліколь, бегенат кальцію, стеарат кальцію, гідрогенізовану рицинову олію або стеарат магнію. 6. Фармацевтична композиція за п. 1, у якій сполучне являє собою коповідон (співполімери вінілпіролідону з іншими похідними вінілу), гідроксипропілметилцелюлозу, гідроксипропілцелюлозу або полівінілпіролідон (повідон). 7. Фармацевтична композиція за п. 1, у якій розпушувач являє собою кукурудзяний крохмаль. 8. Фармацевтична композиція за п. 2, у якій додатковий розпушувач являє собою кросповідон. 9. Фармацевтична композиція за п. 3, у якій необов'язкова ковзна речовина являє собою колоїдний діоксид кремнію. 10. Фармацевтична композиція за п. 1, у якій перший розріджувач являє собою маніт, другий розріджувач являє собою попередньо желатинізований крохмаль, сполучне являє собою коповідон, розпушувач являє собою кукурудзяний крохмаль, а змащувальна речовина являє собою стеарат магнію. 11. Фармацевтична композиція за п. 1, яка містить діючу речовину в кількості від 0,5 до 20 %, розріджувач 1 у кількості від 40 до 88 %, розріджувач 2 у кількості від 3 до 40 %, сполучне у кількості від 1 до 5 %, розпушувач у кількості від 5 до 15 % і змащувальну речовину у кількості від 0,1 до 4 %. 12. Фармацевтична композиція за п. 1, яка містить діючу речовину в кількості від 0,5 до 7 %, розріджувач 1 у кількості від 50 до 75 %, розріджувач 2 у кількості від 5 до 15 %, сполучне у кількості від 2 до 4 %, розпушувач у кількості від 8 до 12 % і змащувальну речовину у кількості від 0,5 до 2 %. 13. Фармацевтична композиція за п. 1, представлена в лікарській формі у вигляді капсули, таблетки або таблетки із плівковим покриттям. 14. Фармацевтична композиція за п. 13, у якій на частку плівкового покриття припадає від 2 до 4 %. 15. Фармацевтична композиція за п. 14, у якій плівкове покриття містить плівкоутворювач, пластифікатор, ковзну речовину і необов'язково один або декілька пігментів. 16. Фармацевтична композиція за п. 15, у якій плівкове покриття містить гідроксипропілметилцелюлозу, поліетиленгліколь, тальк, діоксид титану й оксид заліза. 17. Спосіб приготування фармацевтичної композиції за п. 1, який полягає в тому, що а) сполучне розчиняють у розчиннику з одержанням рідини для гранулювання б) інгібітор DPP IV змішують із розріджувачем і розпушувачем з одержанням преміксу, в) премікс зволожують рідиною для гранулювання й потім зволожений премікс гранулюють, г) гранульований премікс при необхідності просіюють через сито з розміром комірок принаймні 1,0 мм, д) гранулят сушать при температурі приблизно від 40 до 75 °С до зменшення маси висушуваного матеріалу на 1-5 %, є) висушений гранулят просіюють через сито з розміром комірок принаймні 0,6 мм і ж) до грануляту додають змащувальну речовину для остаточного змішування. 18. Спосіб за п. 17, при здійсненні якого додатково з) з залишкової суміші пресують серцевини таблеток, ж) готують суспензію для нанесення покриття й к) на серцевини таблеток наносять покриття із суспензії для нанесення покриття до збільшення їх маси на приблизно 2-4 % з одержанням таблеток із плівковим покриттям. 19. Спосіб за п. 17, при здійсненні якого частину допоміжних речовин додають після процесу гранулювання, перед остаточним змішуванням на стадії ж). 9 UA 106472 C2 5 10 15 20 25 30 35 20. Спосіб за п. 17, при здійсненні якого гранулят на стадіях а)-д) одержують методом гранулювання в одному багатофункціональному апараті для гранулювання зі створенням високого зсувного зусилля й потім сушать у ньому отриманий гранулят. 21. Фармацевтична композиція за п. 1, яка містить як діючу речовину сполуку-інгібітор DPP IV з аміногрупою, вибрану із 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-аміпопінеридин-1-іл)ксантину, 1-[([1,5]нафтиридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(хіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 2-((R)-3-амінопіперидин-1-іл)-3-(бут-2-иніл)-5-(4-метилхіназолін-2-ілметил)-3,5дигідроімідазо[4,5-d]піридазин-4-ону, 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(2-аміно-2метилпропіл)метиламіно]ксантину, 1-[(3-ціанохінолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-(2-ціанобензил)-3-метил-7-(2-бутин-1-іл)-8-((R)-3-аміноніперидин-1-іл)ксантину, 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(S)-(2амінопропіл)метиламіно]ксантину, 1-[(3-ціанопіридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4-метилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4,6-диметилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1іл)ксантину та 1-[(хіноксалін-6-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, або її сіль, перший розріджувач, другий розріджувач, сполучне, розпушувач і змащувальну речовину; де розріджувачі вибирають з еритриту, гідроксипропілцелюлози з низьким ступенем заміщення, маніту, попередньо желатинізованого крохмалю та ксиліту. 22. Фармацевтична композиція за п. 1, де сполучне вибирають з коповідону (співполімеру вінілпіролідону з іншими похідними вінілу), гідроксипропілметилцелюлози, гідроксипропілцелюлози, полівінілпіролідону (повідону), попередньо желатинізованого крохмалю та гідроксипропілцелюлози з низьким ступенем заміщення; розпушувач вибирають з кукурудзяного крохмалю, кросповідону, гідроксипропілцелюлози з низьким ступенем заміщення та попередньо желатинізованого крохмалю; та змащувальну речовину вибирають з тальку, поліетиленгліколю, бегенату кальцію, стеарату кальцію, гідрогенізованої рицинової олії та стеарату магнію. 23. Спосіб за п. 17, де сполучне вибирають з коповідону (співполімеру вінілпіролідону з іншими похідними вінілу), гідроксипропілметилцелюлози, гідроксипропілцелюлози, полівінілпіролідону (повідону), попередньо желатинізованого крохмалю та гідроксипропілцелюлози з низьким ступенем заміщення; розпушувач вибирають з кукурудзяного крохмалю, кросповідону, гідроксипропілцелюлози з низьким ступенем заміщення та попередньо желатинізованого крохмалю; та змащувальну речовину вибирають з тальку, поліетиленгліколю, бегенату кальцію, стеарату кальцію, гідрогенізованої рицинової олії та стеарату магнію. 40 Комп’ютерна верстка І. Скворцова Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 10
ДивитисяДодаткова інформація
Автори англійськоюKohlrausch Anja, Romer Patrick, Seiffert Gerd
Автори російськоюРомер Патрик, Зайфферт Герд
МПК / Мітки
МПК: A61K 9/32, A61K 45/08, A61P 3/10
Мітки: фармацевтична, композиція, інгібіторами
Код посилання
<a href="https://ua.patents.su/12-106472-farmacevtichna-kompoziciya-z-ingibitorami-dpp-iv.html" target="_blank" rel="follow" title="База патентів України">Фармацевтична композиція з інгібіторами dpp iv</a>
Попередній патент: Спосіб розрахунку електричних мереж з негармонійними струмом і напругою
Наступний патент: Спосіб спалювання низькоякісного палива
Випадковий патент: Пристрій для ректальних маніпуляцій "наручій"