Спосіб отримання 5-заміщених-8-алкокси[1,2,4]триазоло[1,5-c]піримідин-2-амінів
Формула / Реферат
1. Спосіб отримання 5-заміщених-8-алкокси-[1,2,4]триазоло[1,5-с]піримідин-2-амінів формули (І):
 , (І)
, (І)
де
X являє собою галоген або OR; і
R являє собою С1-С4алкіл;
в якому проводять:
і) взаємодію 2-заміщеного-4-аміно-5-алкоксипіримідину формули:
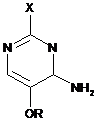 ,
,
де X і R є такими, як визначено вище,
з ізотіоціанатiдокарбонатом формули:
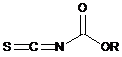 ,
,
де R є таким, як визначено вище,
в полярному апротонному розчиннику, з отриманням (піримідиніламіно)карбонотіоїлкарбамату формули:
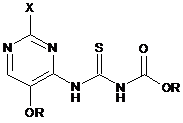 ,
,
де X і R є такими, як визначено вище;
іі) приведення в контакт (піримідиніламіно)карбонотіоїлкарбамату з гідроксиламіном в присутності основи, з отриманням ((піримідиніламіно)гідроксііміно)метилкарбамату формули:
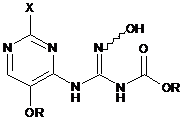 ,
,
де X і R є такими, як визначено вище; і
ііі) циклізацію ((піримідиніламіно)гідроксііміно)метилкарбамату нагріванням в інертному розчиннику, з отриманням 5-заміщеного-8-алкокси[1,2,4]триазоло[1,5-с]піримідин-2-аміну.
2. Спосіб за п. 1, в якому X являє собою ОСН3, і R являє собою СН3.
3. Спосіб за п. 1, в якому ((піримідиніламіно)гідроксііміно)метилкарбамат стадії іі) використовують без виділення для отримання 2-аміно-5-заміщеного-8-алкокси[1,2,4]триазоло[1,5-с]піримідин-2-аміну на стадії ііі).
4. Сполука формули:
 ,
,
де
X являє собою галоген або OR; і
R являє собою С1-С4алкіл.
5. Сполука формули:
 ,
,
де
X являє собою галоген або OR; і
R являє собою С1-С4алкіл.
6. Сполука формули:
 ,
,
де
X являє собою галоген; і
R являє собою С1-С4алкіл.
7. Спосіб за п. 1, в якому додатково проводять стадію перетворення 5-галоген-8-алкокси[1,2,4]триазоло[1,5-с]піримідин-2-аміну формули:
 ,
,
де
X являє собою галоген; і R являє собою С1-С4алкіл;
у відповідні 2-аміно-5,8-алкокси[1,2,4]триазоло[1,5-с]піримідини формули:
 ,
,
де
R являє собою С1-С4алкіл;
за допомогою алкоксиду лужного металу в спиртовому розчиннику.
Текст
Реферат: 5-Заміщені-8-алкокси[1,2,4]триазоло[1,5-с]піримідин-2-аміни отримують із 2-заміщених-4-аміно5-метоксипіримідинів способом, в якому виключається гідразин і ціангалогенід. UA 109440 C2 (12) UA 109440 C2 UA 109440 C2 5 10 15 20 Даний винахід стосується способу отримання 5-заміщених-8-алкокси[1,2,4]триазоло[1,5с]піримідин-2-амінів. У патенті США 6005108 описані деякі заміщені 5,8-дизаміщені-[1,2,4]триазоло[1,5с]піримідин-2-амінні сполуки і їх застосування як проміжних сполук для отримання сульфонамідних гербіцидів. 5,8-Диметокси[1,2,4]триазоло[1,5-с]піримідин-2-амін є корисною проміжною сполукою для отримання пеноксуламу. У Monatsh. Chem. 1983, 114, 789 описане отримання деяких (аміно)карбонотіоїлкарбаматів з подальшою їх взаємодією з гідроксиламіном і подальшою циклізацією в [1,2,4]триазоло[1,5-а]піримідин-2-аміни. У WO 2009/047514 A1 описане отримання деяких (аміно)карбонотіоїлкарбаматів з подальшою їх взаємодією з гідроксиламіном і подальшою циклізацією в [1,2,4]триазоло[1,5-а]піридинові і [1,2,4]триазоло[1,5-с]піримідинові сполуки. У US 6559101 В2 описане отримання деяких (аміно)карбонотіоїлкарбаматів з подальшою їх взаємодією з гідроксиламіном і подальшою циклізацією в піримідинзаміщені [1,2,4]триазоло[1,5-а] піримідин-2-аміни. 5,8-Диметокси[1,2,4]триазоло[1,5-с]піримідин-2-амін отримують з 2,4-дихлор-5метоксипіримідину в багатостадійному способі, який включає як гідразин, так і ціангалогенід. Гідразин представляє серйозну небезпеку вибуху і є токсичним при проковтуванні, вдиханні і адсорбції шкірою. Він класифікується як канцероген і має TLV 0,1 ч./млн. в повітрі. Ціангалогеніди є сильними подразниками і дуже отруйні. Було б вигідно отримувати 5-заміщені8-алкокси[1,2,4]триазоло[1,5-с]піримідин-2-аміни ефективно і з високим виходом у виробничому процесі, який дозволить уникнути використання гідразину і ціангалогеніду. Даний винахід стосується отримання 5-заміщених-8-алкокси[1,2,4]триазоло[1,5-с]піримідин2-амінів із 2-заміщених-4-аміно-5-метоксипіримідинів. Більш конкретно, даний винахід стосується способу отримання 5-заміщених-8-алкокси[1,2,4]триазоло[1,5-с]піримідин-2-амінів формули (I): 25 , 30 де X являє собою галоген або OR; і R являє собою C1-C4алкіл; який включає: i) взаємодію 2-заміщеного-4-аміно-5-алкоксипіримідину формули: , 35 де X і R є такими, як визначено вище, з ізотіоціанатидокарбонатом формули: , 40 де R є таким, як визначено вище, 1 UA 109440 C2 в полярному апротонному (піримідиніламіно)карбонотіоїлкарбамату формули: розчиннику, з отриманням , 5 де X і R є такими, як визначено вище; ii) приведення в контакт (піримідиніламіно)карбонотіоїлкарбамату з гідроксиламіном в присутності основи, з отриманням (піримідиніламіно)гідроксііміно)метилкарбамату формули: 10 15 , де X і R є такими, як визначено вище; і iii) циклізацію ((піримідиніламіно)гідроксііміно)метилкарбамату нагріванням в інертному розчиннику, з отриманням 5-заміщеного-8-алкокси[1,2,4]триазоло[1,5-с]піримідин-2-аміну. У іншому варіанті здійснення винаходу 5-галоген-8-алкокси[1,2,4]триазоло[1,5-с]піримідин-2аміни можуть бути перетворені у відповідні 5,8-диалкокси[1,2,4]триазоло[1,5-с]піримідин-2-аміни заміною галогену алкоксидом лужного металу в спиртовому розчиннику. Інший варіант здійснення винаходу включає (піримідиніламіно)карбонотіоїлкарбамат формули: , 20 25 де X являє собою галоген або OR; і R являє собою C1-C4алкіл. Ще один варіант здійснення (піримідиніламіно)гідроксііміно)метилкарбамат формули: винаходу включає , 30 35 де X являє собою галоген або OR; і R являє собою C1-C4алкіл. Дана речовина може існувати у вигляді пари геометричних ізомерів (Е і Z), а також в різних таутомерних формах. Додатковий варіант здійснення винаходу включає 5-галоген-8-алкокси[1,2,4]триазоло[1,5с]піримідин-2-аміни формули: 2 UA 109440 C2 , 5 10 15 20 25 30 35 40 де X являє собою галоген; і R являє собою C1-C4алкіл. Термін алкіл і похідні терміни, такі як алкокси, як використовується в даному описі, стосуються груп з нерозгалуженим або розгалуженим ланцюгом. Конкретні алкільні групи являють собою метил, етил, пропіл, 1-метилетил, бутил, 1,1-диметилетил і 1-метилпропіл. Метил і етил є звичайно переважними. Термін галоген, як використовується в даному описі, стосується фтору, хлору, брому і йоду. Група хлору є звичайно переважною. 2-Заміщені-4-аміно-5-алкоксипіримідинові і алкілізотіоціанатидокарбонатні вихідні речовини є відомими сполуками або можуть бути отримані способами, добре відомими фахівцям в даній галузі. Даний винахід стосується отримання 5-заміщених-8-алкокси[1,2,4]триазоло[1,5-с]піримідин2-амінів із 2-заміщених-4-аміно-5-метоксипіримідинів. Перша стадія (а) даного винаходу стосується перетворення 4-амінопіримідину, де X являє собою галоген або OR, і R являє собою С1-С4алкіл, в (піримідиніламіно)карбонотіоїлкарбамат. Це досягається за допомогою щонайменше одного еквівалента і, переважно, надлишку ізотіоціанатидокарбонату в полярному апротонному розчиннику, переважно ацетонітрилі або етилацетаті. Також можливо проводити реакцію в присутності додаткових розріджувачів, за умови, що ці розчинники не заважають протіканню бажаної реакції і хімічно інертні відносно реагентів. Ізотіоціанатидокарбонат додають при температурі від 0 °C до кімнатної температури; суміш, як правило, нагрівають до деякої температури в діапазоні від кімнатної температури до температури кипіння зі зворотним холодильником доданого розріджувача, переважно до температури кипіння зі зворотним холодильником. Продукт виділяють звичайними способами, такими як фільтрування осадженої або кристалізованої речовини. У конкретній реакції амінопіримідин розчиняють або суспендують в етилацетаті і потім обробляють відповідною кількістю ізотіоціанатидокарбонату. Після нагрівання до температури кипіння зі зворотним холодильником реакційну суміш охолоджують до температури, при якій цільова сполука осаджується, і відділяють фільтруванням і сушать. Необов'язково, деяка або більша частина розчинника може бути видалена перегонкою перед фільтруванням, для поліпшення фільтрування кристалів або зниження розчинності продукту в розчиннику і, тим самим, поліпшення виділення. Друга стадія (b) даного винаходу стосується перетворення (піримідиніламіно)карбонотіоїлкарбамату в його (піримідиніламіно)гідроксііміно)метилкарбаматний еквівалент. Це досягається використанням 3 UA 109440 C2 5 10 15 20 25 30 щонайменше еквівалента гідроксиламіну, переважно у вигляді солі, і основи, такої як карбонат натрію або калію, гідроксид натрію або калію або триалкіламін. Карбонат натрію або гідроксид натрію є переважними допоміжними основами. Звичайно використовують аж до 4 еквівалентів гідроксиламіну і основи в цій реакції. Реакційну суміш розбавляють водою і полярним розчинником, переважно етилацетатом або ацетонітрилом, і перемішують при температурі від 0 °C до 35 °C, переважно при кімнатній температурі. Також можливо провести реакцію в присутності додаткових розріджувачів, за умови, що ці розріджувачі не заважають протіканню бажаної реакції і хімічно інертні відносно реагентів. Продукт необов'язково охолоджують і виділяють звичайними способами, такими як виділення фільтруванням і сушіння, або флешхроматографією. Речовина може існувати у вигляді Е/Z ізомерної суміші і/або в різних таутомерних формах. Необов'язково, замість того щоб виділяти (піримідиніламіно)гідроксііміно)метилкарбамат, реакція може бути продовжена в реакційній суміші при нагріванні для здійснення циклізації в 5-заміщені-8-алкокси[1,2,4]триазоло[1,5с]піримідин-2-аміни і виділення відповідно до докладного опису нижче. У конкретній реакції (піримідиніламіно)карбонотіоїлкарбамат, гідроксиламін і основу розчиняють у воді і або в ацетонітрилі, або в етилацетаті. Реакційну суміш перемішують при кімнатній температурі і потім або нагрівають для перетворення в 5-заміщений-8алкокси[1,2,4]триазоло[1,5-с]піримідин-2-амін, або фільтрують і перекристалізовують з ацетонітрилу з виділенням (піримідиніламіно)гідроксііміно)метилкарбамату. Необов'язково, деяка або більша частина розчинника може бути видалена перегонкою перед фільтруванням, для поліпшення фільтрування кристалів або зниження розчинності продукту в розчиннику і, тим самим, поліпшення виділення. Третя стадія (с) даного винаходу стосується перетворення необов'язково виділеного (піримідиніламіно)гідроксііміно)метилкарбамату в 5-заміщений-8-алкокси[1,2,4]триазоло[1,5с]піримідин-2-амін при нагріванні і в інертному розчиннику. Часто переважно перетворювати (піримідиніламіно)гідроксііміно)метилкарбамат в 5-заміщений-8-алкокси[1,2,4]триазоло[1,5с]піримідин-2-амін без виділення. Це перетворення здійснюють нагріванням реакційної суміші. Продукт необов'язково охолоджують і виділяють звичайними методами, такими як виділення фільтруванням і сушіння. Інший варіант здійснення винаходу стосується перетворення (d) 5-галоген-8алкокси[1,2,4]триазоло[1,5-с]піримідин-2-аміну: , 35 40 45 50 55 де X являє собою галоген; і R являє собою C1-C4алкіл, в його алкокси аналог, 5,8-алкокси[1,2,4]триазоло[1,5-с]піримідин-2-амін, з використанням щонайменше одного еквівалента і переважно надлишку метоксиду натрію або калію в спиртовому розчиннику. Також можна проводити реакцію в присутності додаткових розріджувачів, за умови, що ці розріджувачі не заважають протіканню бажаної реакції і хімічно інертні відносно реагентів. Суміш перемішують при деякій температурі від 0 °C до 50 °C, переважно при кімнатній температурі. Продукт необов'язково охолоджують і виділяють звичайними методами, такими як виділення фільтруванням і сушіння. У конкретній реакції 5-хлор-8-алкокси[1,2,4]триазоло[1,5-с]піримідин-2-амін розчиняють в ацетонітрилі при кімнатній температурі і обробляють 25 % метоксидом натрію в метанолі. Отриману суспензію перемішують при кімнатній температурі декілька годин і потім фільтрують і сушать, з отриманням 5-метокси-8-алкокси[1,2,4]триазоло[1,5-с]піримідин-2-аміну. Необов'язково, деяка або більша частина розчинника може бути видалена перегонкою перед фільтруванням, для поліпшення фільтрування кристалів або зниження розчинності продукту в розчиннику і, тим самим, поліпшення виділення. Наступні приклади приведені для ілюстрації винаходу. ПРИКЛАДИ Всі описані реагенти були куплені і використовувалися без додаткового очищення. Аналіз ВЕРХ проводили на приладі Perkin Elmer Series 200 з діодно-матричним ультрафіолетовим 4 UA 109440 C2 5 детектором. Використовували колонку Zorbax RX-C8 з різними співвідношеннями ацетонітрилвода, модифіковану 0,1 % фосфорну кислоту як елюент при швидкості потоку 1 мл/хв. і ультрафіолетове детектування при 220 нм. Спектри ядерного магнітного резонансу отримували на спектрометрі Bruker AC 300 NMR (300 мГц). Мас-спектральні дані отримували з використанням точної мас-рідинної хроматографії з електророзпиленням-мас-спектрометрії (ESI/РХ/МС) в позитивно іонному (PI) режимі і точної мас-рідинної хроматографії з електророзпиленням-мас-спектрометрії-мас-спектрометрії- (ESI/РХ/МС/МС). Приклад 1. Отримання етил[(2-хлор-5-метоксипіримідин-4-іл)аміно]карбонотіоїлкарбамату (2) 10 15 20 2-Хлор-5-метоксипіримідин-4-амін (1) (6,4 г, 0,040 моль) суспендували в етилацетаті (100 мл) і нагрівали майже до температури кипіння зі зворотним холодильником. Додавали відразу весь етилізотіоціанатидокарбонат (8,9 г, 1,7 екв) і суміш кип'ятили зі зворотним холодильником протягом 10 годин. Отриману суспензію охолоджували до 15 °C, твердий продукт виділяли фільтруванням і промивали осад свіжим етилацетатом, з отриманням вказаної в заголовку сполуки декількома порціями у вигляді твердої речовини (7,8 г, 67 %): т.пл. 182 °C; 1 H ЯМР (ДМСО-d6): δ 11,97 (с, 1H), 11,72 (с, 1H), 8,50 (с, 1H), 4,22 (кв, 2H), 3,72 (с, 3H), 1,17 13 : (т, 3H); C ЯМР (ДМСО-d6) 177,82, 153,58, 150,00, 149,01, 144,26, 142,63, 62,76, 57,56, 14,44; мас-спектр (точна маса): обчислено для C9H11ClN4O3S: 290,024039; знайдено, 290,0241. Приклад 2. Отримання етил-(Z і Е)-[(2-хлор-5-метоксипіримідин-4іл)аміно](гідроксііміно)метилкарбамату (3) 25 30 35 40 Об'єднували гідрохлорид гідроксиламіну (280 мг, 4 екв) і бікарбонат натрію (335 мг, 4 екв) і розчиняли у воді (6 мл) при кімнатній температурі. До отриманого додавали суспензію етил[(2хлор-5-метоксипіримідин-4-іл)аміно]карбонотіоїлкарбамату (2; 290 мг, 1,0 ммоль) в ацетонітрилі (15 мл). Отриману суспензію перемішували при кімнатній температурі протягом 1 години, і тверді частинки відділяли фільтруванням. Перекристалізацією з ацетонітрилу отримували вказану в заголовку сполуку у вигляді світло-жовтої твердої речовини (170 мг, 59 %): т.пл. 183184 °C (розклад.); 1 H ЯМР (ДМСО-d6) (суміш ізомерів): δ 10,77 (с, 0,6 Н), 10,5 (с, 0,4 Н), 9,48 (с, 0,6 Н), 9,34 (с, 0,4 Н), 9,09 (с, 0,4 Н), 8,40 (с, 0,6 Н), 8,11 (с, 0,6 Н), 8,11 (с, 0,6 Н), 7,95 (с, 0,4 Н) 4,19-3,89 (м, 13 5H), 1,17-1,09 (м, 3H); C ЯМР (ДМСО-d6): δ 154,4, 154,0, 149,9, 140,2, 140,0, 139,1, 138,6, 138,0, 61,2, 60,9, 57,3, 56,5, 14,8, 14,5; Мас-спектр (точна маса): обчислено для C9H12ClN5O4 289,05778; знайдено, 289,0577. Приклад 3. Отримання 5-хлор-8-метокси[1,2,4]триазоло[1,5-с]піримідин-2-аміну (4) без виділення (3) 5 UA 109440 C2 5 10 15 20 25 Об'єднували етил[(2-хлор-5-метоксипіримідин-4-іл)аміно]карбонотіоїлкарбамат (2) (290 мг, 1,0 ммоль), гідрохлорид гідроксиламіну (143 мг, 2 екв) і бікарбонат натрію (170 мг, 2 екв). Додавали воду (5 мл) і ацетонітрил (5 мл) при кімнатній температурі. Отриману суспензію перемішували при кімнатній температурі протягом ночі, потім обробляли 20 краплями насиченого водного розчину карбонату натрію. Отриманий розчин продували азотом і охолоджували, отримуючи продукт у вигляді вапнякового осаду, який відділяли фільтруванням (в двох порціях), промивали водою і сушили, з отриманням вказаної в заголовку сполуки у вигляді твердої речовини (139 мг, 68 %): т. пл. 251 °C; 1 13 H ЯМР (ДМСО-d6): δ 7,73 (с, 1H), 3,98 (с, 3H); 6,63 (с, 2H); С ЯМР (ДМСО-d6): 166,30, 148,14, 128,91, 124,67, 57,51; Мас-спектр (точна маса): обчислено для C6H6ClN5O 199,026087; знайдено, 199,0256. Приклад 4. Отримання 5-хлор-8-метокси[1,2,4]триазоло[1,5-с]піримідин-2-аміну (4) без виділення (3) Гідрохлорид гідроксиламіну (280 мг, 4 екв) і бікарбонат натрію (210 мг, 2,5 екв) об'єднували у воді (5 мл) і перемішували протягом 5 хвилин. Додавали при кімнатній температурі етил[(2хлор-5-метоксипіримідин-4-іл)аміно]карбонотіоїлкарбамат (2) (290 мг, 1,0 ммоль), суспендований в трет-бутанолі (15 мл). Реакцію перемішували при кімнатній температурі протягом 5 годин і потім обробляли 10 краплями насиченого водного розчину карбонату натрію. Реакційну суспензію потім фільтрували і отримані тверді частинки промивали водою і сушили, з отриманням вказаної в заголовку сполуки у вигляді сірувато-білої твердої речовини (330 мг, 83 %), яка була ідентичною по ВЕРХ утримуванню описаному вище 5-хлор-8метокси[1,2,4]триазоло[1,5-с]піримідин-2-аміну (4). Приклад 5. Отримання 5,8-диметокси[1,2,4]триазоло[1,5-с] піримідин-2-аміну (5) 30 35 5-Хлор-8-метокси[1,2,4]триазоло[1,5-с]піримідин-2-амін (4; 100 мг, 0,50 ммоль) суспендували в ацетонітрилі (5 мл) при кімнатній температурі і обробляли 25 % метоксидом натрію в метанолі (200 мг, 2 екв.). Отриману суспензію перемішували при кімнатній температурі протягом 1,5 годин і потім фільтрували. Тверді частинки промивали водою і сушили, з отриманням вказаної в заголовку сполуки у вигляді речовини вапнякового кольору (87 мг, 88 %), яка була ідентичною 6 UA 109440 C2 по ВЕРХ утримуванню даного 5,8-диметокси[1,2,4]триазоло[1,5-с]піримідин-2-аміну (5): т.пл. 185-186 °C; 1 H ЯМР (ДМСО-d6) 7,48 (с, 1H), 6,38 (ушир. с, 2H), 4,04 (с, 3H), 3,88 (с, 3H); EIMS m/z 195. Приклад 6. Отримання етил[(2,5-диметоксипіримідин-4-іл)аміно]карбонотіоїлкарбамату 5 10 15 У 18 г етилацетату розчиняли 2,5-диметоксипіримідин-4-амін (6) (3 г, 0,0193 моль). Додавали етилізотіоціанатидокарбонат (2,77 г, 0,0208 моль) однією порцією. Розчин нагрівали до 78 °C і витримували при цій температурі протягом 11 год. Додавали додаткові 1,4 г етилізотіоціанатидокарбонату і суміш нагрівали протягом 2,5 год. Суміш охолоджували до 22 °C і фільтрували. Отриману тверду речовину промивали етилацетатом (20 мл) і сушили до постійної маси у витяжній шафі, з отриманням вказаної в заголовку сполуки у вигляді жовтої твердої речовини (4,81 г, 89 %): 13 C ЯМР (ДМСО-d6, 100 мГц): δ 177,5, 158,4, 153,3, 149,5, 142,3, 139,5, 62,6, 57,6, 55,2, 14,4; HRMS (ESI), обчислено для C10H14N4O4S, 286,0736; знайдено, 286,0727. Приклад 7. Додавання гідроксиламіну для отримання сполуки 8 і циклізація з утворенням 5,8-диметокси[1,2,4]триазоло[1,5-с]піримідин-2-аміну (5) 20 25 30 35 Етил[(2,5-диметоксипіримідин-4-іл)аміно]карбонотіоїлкарбамат (7; 4,30 г, 0,0154 моль) диспергували в 24 г етилацетату. Потім до перемішуваної суспензії додавали гідрохлорид гідроксиламіну (1,28 г, 0,0193 моль), воду (3,84 г) і 2М NaOH (12,61 г, 0,0252 моль). Після додавання NaOH температура всередині піднялася до 26 °C. Етил-(Е/Z)-[(2-хлор-5метоксипіримідин-4-іл)аміно](гідроксііміно)метилкарбамат (8) не виділяли, але нагрівали до 50 °C для циклізації. Суміш охолоджували до кімнатної температури і перемішували протягом ночі. Суспензію фільтрували при кімнатній температурі, осад промивали водою (3×8 г) і сушили до постійної маси у витяжній шафі, з отриманням вказаної в заголовку сполуки у вигляді рудуватої твердої речовини (3,16 г, 105 % вихід по масі). Основний компонент мав час витримування, ідентичний справжньому 5,8-диметокси[1,2,4]триазоло[1,5-с]піримідин-2-аміну (5). В окремому експерименті етил-(Е/Z)-[(2,5-диметоксипіримідин-4іл)аміно](гідроксііміно)метилкарбамат (8) виділяли хроматографією на силікагелі (хлороформ як елюент), з отриманням білої твердої речовини (0,4 г, 13 %), яка являло собою близько 77/23 суміш геометричних ізомерів: 1 H ЯМР (ДМСО-d6) (суміш ізомерів): δ 10,65 (с, 1H), 10,34 (с, 0,3 Н), 9,56 (с, 1H), 8,98 (с, 0,3 Н), 8,94 (с, 0,3 Н), 8,20 (с, 1H), 8,00 (с, 1H), 7,82 (с, 0,3 Н), 4,25-3,90 (м, 2,6 Н), 3,88 (с, 3H), 3,81 (с, 0,9 Н), 3,78 (с, 3H), 3,22 (с, 0,9 Н), 1,20-1,15 (м, 3H); Мас-спектр (точна маса): обчислено для C9H12ClN5O4 289,0578; знайдено, 289,0571. 40 ФОРМУЛА ВИНАХОДУ 1. Спосіб отримання 5-заміщених-8-алкокси-[1,2,4]триазоло[1,5-с]піримідин-2-амінів формули (І): 7 UA 109440 C2 X N N N NH2 N OR 5 , (І) де X являє собою галоген або OR; і R являє собою С1-С4алкіл; в якому проводять: і) взаємодію 2-заміщеного-4-аміно-5-алкоксипіримідину формули: X N N NH2 OR , де X і R є такими, як визначено вище, з ізотіоціанатiдокарбонатом формули: O 10 S C N OR , де R є таким, як визначено вище, в полярному апротонному розчиннику, з отриманням (піримідиніламіно)карбонотіоїлкарбамату формули: X N N S N H O N H OR OR 15 , де X і R є такими, як визначено вище; іі) приведення в контакт (піримідиніламіно)карбонотіоїлкарбамату з гідроксиламіном присутності основи, з отриманням ((піримідиніламіно)гідроксііміно)метилкарбамату формули: в X OH N N N N H O N H OR OR 20 25 , де X і R є такими, як визначено вище; і ііі) циклізацію ((піримідиніламіно)гідроксііміно)метилкарбамату нагріванням в інертному розчиннику, з отриманням 5-заміщеного-8-алкокси[1,2,4]триазоло[1,5-с]піримідин-2-аміну. 2. Спосіб за п. 1, в якому X являє собою ОСН3, і R являє собою СН3. 3. Спосіб за п. 1, в якому ((піримідиніламіно)гідроксііміно)метилкарбамат стадії іі) використовують без виділення для отримання 2-аміно-5-заміщеного-8алкокси[1,2,4]триазоло[1,5-с]піримідин-2-аміну на стадії ііі). 4. Сполука формули: 8 UA 109440 C2 X N N S N H O N H OR OR 5 , де X являє собою галоген або OR; і R являє собою С1-С4алкіл. 5. Сполука формули: X OH N N N N H O N H OR OR 10 , де X являє собою галоген або OR; і R являє собою С1-С4алкіл. 6. Сполука формули: X N N N NH2 N OR 15 , де X являє собою галоген; і R являє собою С1-С4алкіл. 7. Спосіб за п. 1, в якому додатково проводять стадію перетворення 5-галоген-8алкокси[1,2,4]триазоло[1,5-с]піримідин-2-аміну формули: X N N N NH2 N OR 20 , де X являє собою галоген; і R являє собою С1-С4алкіл; у відповідні 2-аміно-5,8-алкокси[1,2,4]триазоло[1,5-с]піримідини формули: OR N N N NH2 N OR , де R являє собою С1-С4алкіл; за допомогою алкоксиду лужного металу в спиртовому розчиннику. 9 UA 109440 C2 Комп’ютерна верстка Л. Ціхановська Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 10
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 5-substituted-8-alkoxy[1,2,4]triazolo[1,5-c]pyrimidin-2-amines
Автори англійськоюBott, Craig, Hamilton, Christopher, Roth, Gary
Автори російськоюБотт Крейг, Хэмилтон Кристофер, Рот Гари
МПК / Мітки
МПК: C07D 487/04
Мітки: 5-заміщених-8-алкокси[1,2,4]триазоло[1,5-c]піримідин-2-амінів, спосіб, отримання
Код посилання
<a href="https://ua.patents.su/12-109440-sposib-otrimannya-5-zamishhenikh-8-alkoksi124triazolo15-cpirimidin-2-aminiv.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання 5-заміщених-8-алкокси[1,2,4]триазоло[1,5-c]піримідин-2-амінів</a>
Попередній патент: Пачка для курильних виробів та заготівка для неї
Наступний патент: Система контролю і діагностики системи енергетичних машин для текучих середовищ, а також система енергетичних машин для текучих середовищ
Випадковий патент: Спосіб отримання солодкого супу "тропічна лагуна" із збереженням натурального аромату












