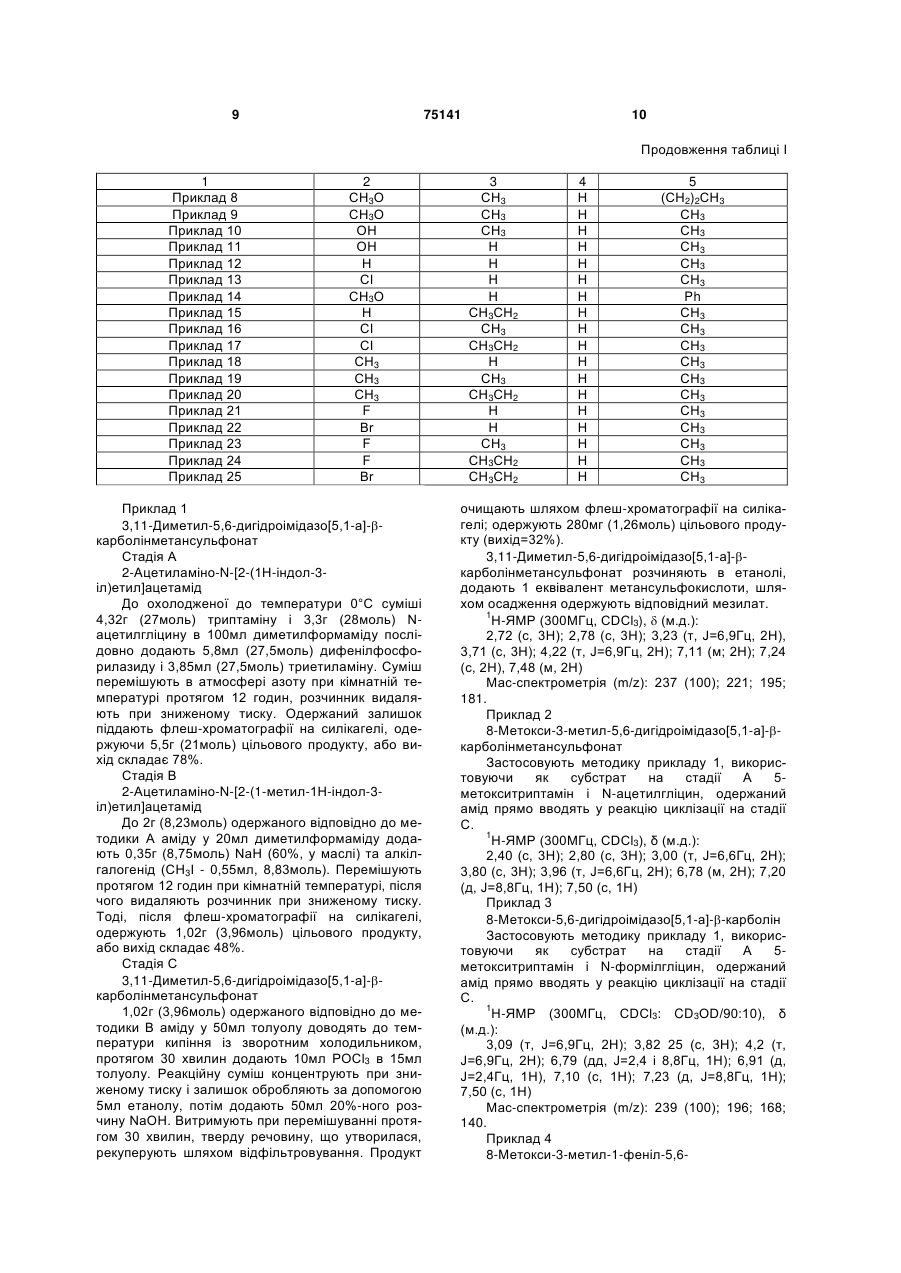
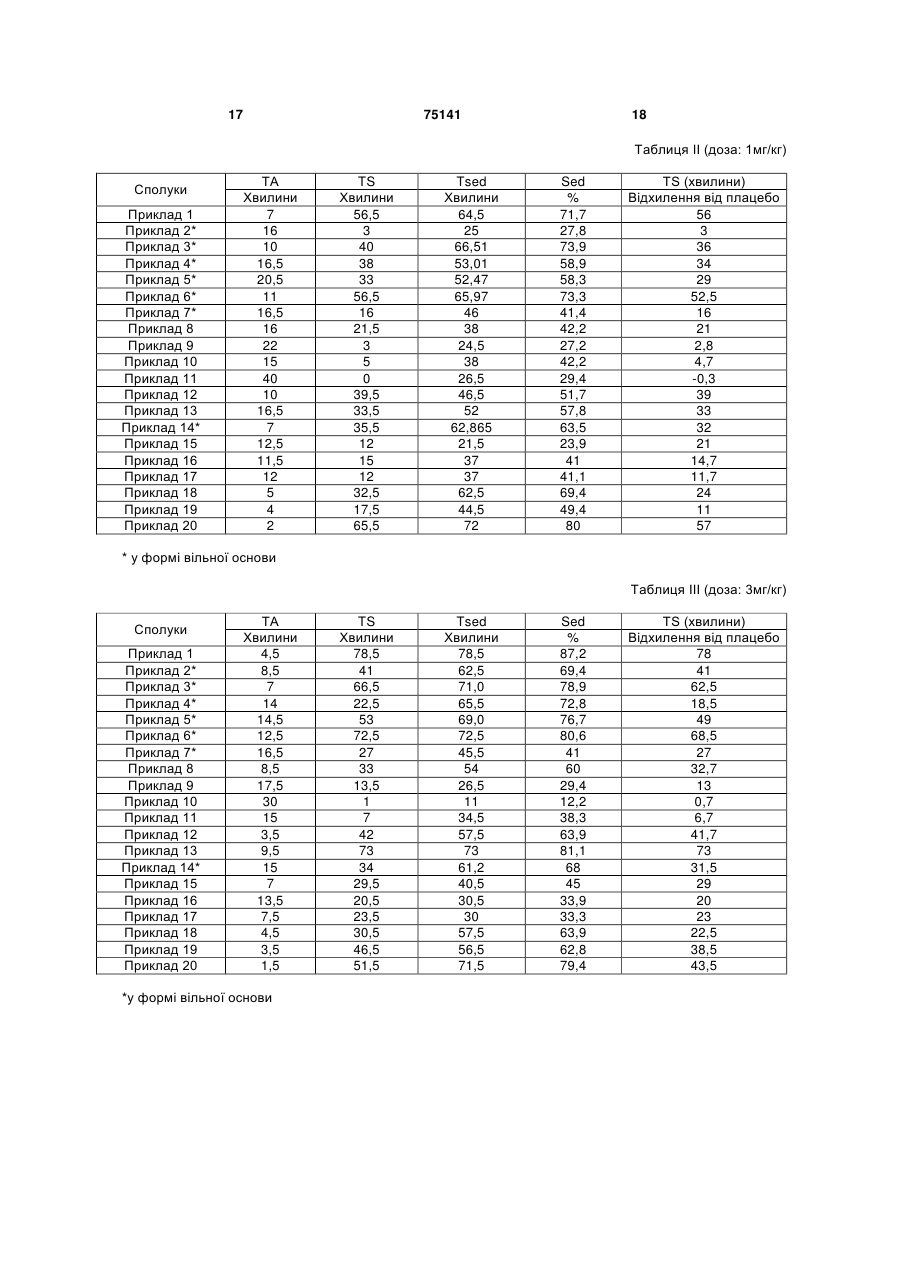
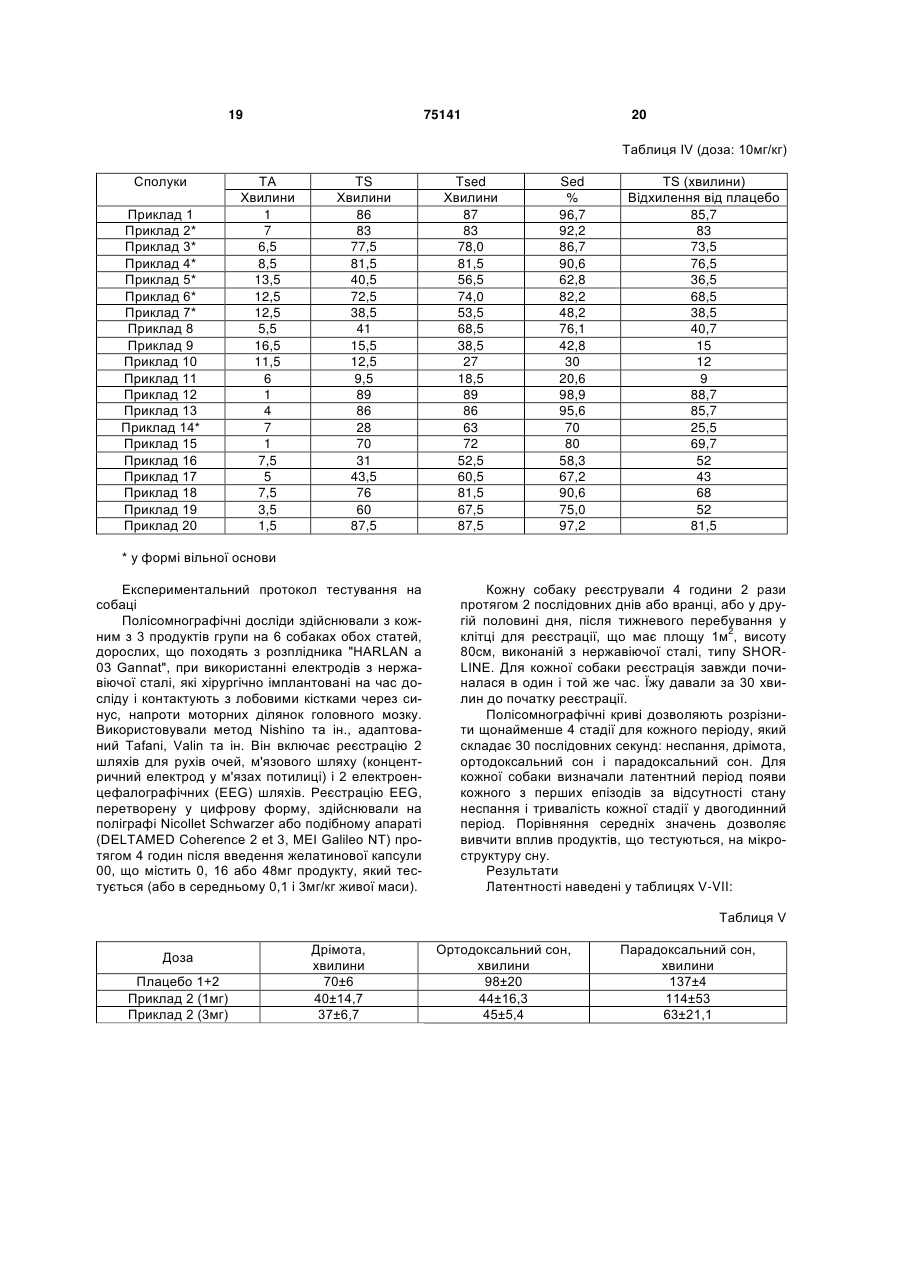
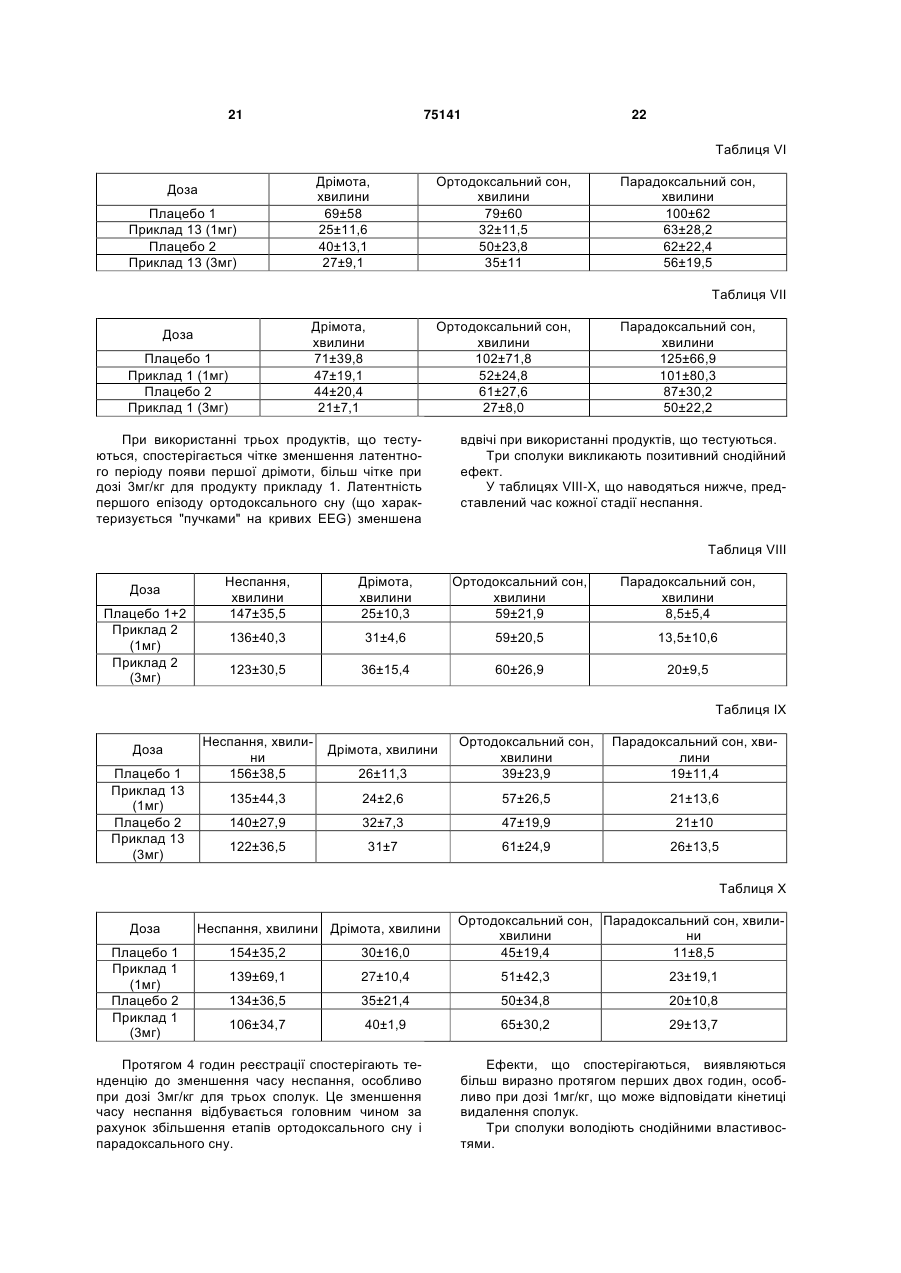
Похідні дигідроімідазо[5,1-a]-b-карболіну, спосіб їх одержання та фармацевтична композиція на їх основі
Номер патенту: 75141
Опубліковано: 15.03.2006
Автори: Карам Омар, Жакезі Жан-Клод, Зюніно Фабьєн, Фуртіллан Жан-Бернар, Тафані Жан-Пьєр, Фуртіллан Маріанн
Формула / Реферат
1. Похідні дигідроімідазо[5,1-а]-![]() -карболіну загальної формули (І):
-карболіну загальної формули (І):
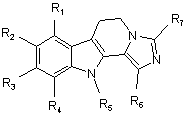 , (І)
, (І)
в якій:
R1, R2, R3 і R4, однакові або різні, незалежно один від одного, означають атом водню, атом галогену, лінійний або розгалужений (С1-С6)-алкіл, гідроксил, лінійний або розгалужений (С1-С6)-алкоксил, лінійний або розгалужений (С1-С6)-тригалогеналкіл, лінійний або розгалужений (С1-С6)-тригалогеналкоксил, нітрогрупу, ціаногрупу, аміногрупу, лінійну або розгалужену (С1-С6)-алкіламіногрупу, лінійну або розгалужену ді-[(С1-С6)-алкіл]аміногрупу, арил, лінійний або розгалужений арил-(С1-С6)-алкіл, карбоксил, лінійну або розгалужену (С1-С6)-алкілкарбонілоксигрупу, лінійний або розгалужений (С1-С6)-ацил, арилоксигрупу або лінійний або розгалужений арил-(С1-С6)-алкоксил;
R5 означає атом водню, лінійний або розгалужений (С1-С6)-алкіл або лінійний або розгалужений арил-(С1-С6)-алкіл;
R6 і R7, однакові або різні, незалежно один від одного, означають атом водню, атом галогену, лінійний або розгалужений (С1-С6)-алкіл, гідроксил, лінійний або розгалужений (С1-С6)-алкоксил, лінійний або розгалужений (С1-С6)-тригалогеналкіл, лінійний або розгалужений (С1-С6)-тригалогеналкоксил, ціаногрупу, аміногрупу, лінійну або розгалужену (С1-С6)-алкіламіногрупу, лінійну або розгалужену ді-[(С1-С6)-алкіл]аміногрупу, арил, лінійний або розгалужений арил-(С1-С6)-алкіл, карбоксил, лінійну або розгалужену (С1-C6)-алкілкарбонілоксигрупу, лінійний або розгалужений (С1-С6)-ацил, арилоксигрупу або лінійний або розгалужений арил-(С1-С6)-алкоксил;
за винятком сполук загальної формули (І), в якій R1-R6 означають атом водню і R7 означає групу СН3 або феніл;
їх ізомери, а також їх адитивні солі з фармацевтично прийнятною кислотою.
2. Сполуки за п. 1, які відрізняються тим, що:
R1, R3 і R4 означають атом водню;
R6 і R7, незалежно один від одного, означають атом водню, лінійний або розгалужений (С1-С6)-алкіл, арил, особливо феніл; і
R5 означає атом водню, лінійний або розгалужений (С1-С6)-алкіл.
3. Сполуки за будь-яким з пп. 1 і 2, які відрізняються тим, що:
R2 означає атом водню, атом галогену (атом фтору, хлору або брому), лінійний або розгалужений (С1-С6)-алкіл, гідроксил, лінійний або розгалужений (С1-С6)-алкоксил.
4. Сполуки за будь-яким з пп. 1-3, які відрізняються тим, що їх вибирають з наступних сполук:
3,11-диметил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
8-метокси-3-метил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
8-метокси-5,6-дигідроімідазо[5,1-а]-![]() -карболін;
-карболін;
8-метокси-3-метил-1-феніл-5,6-дигідроімідазо[5,1-а]-![]() -карболін;
-карболін;
1-етил-8-метокси-3-метил-5,6-дигідроімідазо[5,1-а]-![]() -карболін;
-карболін;
8-метокси-3-ізопропіл-5,6-дигідроімідазо[5,1-а]-![]() -карболін;
-карболін;
8-метокси-3-пропіл-5,6-дигідроімідазо[5,1-а]-![]() -карболін;
-карболін;
8-метокси-11-метил-3-пропіл-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
8-метокси-3,11-диметил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
8-гідрокси-3,11-диметил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
8-гідрокси-3-метил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
3-метил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
8-хлор-3-метил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
8-метокси-3-феніл-5,6-дигідроімідазо[5,1-а]-![]() -карболін;
-карболін;
11-етил-3-метил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
8-хлор-3,11-диметил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
8-хлор-3-метил-11-етил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
3,8-диметил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
3,8,11-триметил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
11-етил-3,8-диметил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
8-фтор-3-метил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
8-бром-3-метил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
8-фтор-3,11-диметил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
8-фтор-11-етил-3-метил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат;
-карболінметансульфонат;
8-бром-11-етил-3-метил-5,6-дигідроімідазо[5,1-а]-![]() -карболінметансульфонат.
-карболінметансульфонат.
5. Спосіб одержання сполук формули (І) за будь-яким з пп. 1-4, який відрізняється тим, що сполуку формули (II):
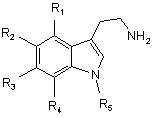 , (II)
, (II)
в якій R1, R2, R3, R4 і R5 мають такі ж значення, як у формулі (І), вводять у взаємодію, відповідно до умов синтезу типу пептидного сполучення, зі сполукою формули (III):
 , (III)
, (III)
в якій R6, і R7 є такими, як вказані у формулі (І), одержуючи сполуку формули (IV):
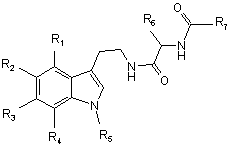 , (IV)
, (IV)
в якій R1, R2, R3, R4, R5, R6 і R7 мають згадані вище значення, яку обробляють у присутності оксихлориду фосфору у розчиннику, такому як толуол, одержуючи сполуки формули (І):
 ,(I)
,(I)
в якій R1, R2, R3, R4, R5, R6 і R7 мають згадані вище значення, причому сполуки загальної формули (І), за бажанням, перетворюють в їх адитивні солі з фармацевтично прийнятною кислотою.
6. Фармацевтична композиція, яка містить як діюче начало щонайменше одну сполуку формули (І) або одну з її адитивних солей з фармацевтично прийнятною кислотою, за будь-яким з пп. 1-4, у поєднанні з одним або декількома ексципієнтами або інертними нетоксичними фармацевтично прийнятними носіями.
7. Сполуки за будь-яким з пп. 1-4 як лікарські засоби.
8. Сполуки за будь-яким з пп. 1-4 як снодійні лікарські засоби.
Текст
1. Похідні дигідроімідазо[5,1-а]- -карболіну загальної формули (І): R1 R7 R2 N C2 2 (19) 1 3 75141 4 R1 8-метокси-5,6-дигідроімідазо[5,1-а]- -карболін; 8-метокси-3-метил-1-феніл-5,6-дигідроімідазо[5,1R2 NH2 а]- -карболін; (II) 1-етил-8-метокси-3-метил-5,6-дигідроімідазо[5,1N а]- -карболін; R3 8-метокси-3-ізопропіл-5,6-дигідроімідазо[5,1-а]- R5 R4 , карболін; в якій R1, R2, R3, R4 і R5 мають такі ж значення, як у 8-метокси-3-пропіл-5,6-дигідроімідазо[5,1-а]- формулі (І), вводять у взаємодію, відповідно до карболін; умов синтезу типу пептидного сполучення, зі спо8-метокси-11-метил-3-пропіл-5,6лукою формули (III): дигідроімідазо[5,1-а]- -карболінметансульфонат; R6 O 8-метокси-3,11-диметил-5,6-дигідроімідазо[5,1-а] -карболінметансульфонат; HO (III) N 8-гідрокси-3,11-диметил-5,6-дигідроімідазо[5,1-а]R7 H -карболінметансульфонат; O , 8-гідрокси-3-метил-5,6-дигідроімідазо[5,1-а]- в якій R6, і R7 є такими, як вказані у формулі (І), карболінметансульфонат; одержуючи сполуку формули (IV): O 3-метил-5,6-дигідроімідазо[5,1-а]- R6 R7 карболінметансульфонат; R1 8-хлор-3-метил-5,6-дигідроімідазо[5,1-а]- N H карболінметансульфонат; R2 N H (IV) 8-метокси-3-феніл-5,6-дигідроімідазо[5,1-а]- O карболін; N 11-етил-3-метил-5,6-дигідроімідазо[5,1-а]- R3 карболінметансульфонат; R5 R4 , 8-хлор-3,11-диметил-5,6-дигідроімідазо[5,1-а]- в якій R1, R2, R3, R4, R5, R6 і R7 мають згадані вище карболінметансульфонат; значення, яку обробляють у присутності оксихло8-хлор-3-метил-11-етил-5,6-дигідроімідазо[5,1-а]риду фосфору у розчиннику, такому як толуол, -карболінметансульфонат; одержуючи сполуки формули (І): 3,8-диметил-5,6-дигідроімідазо[5,1-а]- R1 R7 карболінметансульфонат; R2 N 3,8,11-триметил-5,6-дигідроімідазо[5,1-а]- карболінметансульфонат; N (I) 11-етил-3,8-диметил-5,6-дигідроімідазо[5,1-а]- N R3 карболінметансульфонат; R5 R6 8-фтор-3-метил-5,6-дигідроімідазо[5,1-а]- R4 , карболінметансульфонат; в якій R1, R2, R3, R4, R5, R6 і R7 мають згадані вище 8-бром-3-метил-5,6-дигідроімідазо[5,1-а]- значення, причому сполуки загальної формули (І), карболінметансульфонат; за бажанням, перетворюють в їх адитивні солі з 8-фтор-3,11-диметил-5,6-дигідроімідазо[5,1-а]- фармацевтично прийнятною кислотою. карболінметансульфонат; 6. Фармацевтична композиція, яка містить як діюче 8-фтор-11-етил-3-метил-5,6-дигідроімідазо[5,1-а]начало щонайменше одну сполуку формули (І) або одну з її адитивних солей з фармацевтично при -карболінметансульфонат; йнятною кислотою, за будь-яким з пп. 1-4, у поєд8-бром-11-етил-3-метил-5,6-дигідроімідазо[5,1-а]нанні з одним або декількома ексципієнтами або -карболінметансульфонат. інертними нетоксичними фармацевтично прийнят5. Спосіб одержання сполук формули (І) за будьними носіями. яким з пп. 1-4, який відрізняється тим, що сполу7. Сполуки за будь-яким з пп. 1-4 як лікарські засоку формули (II): би. 8. Сполуки за будь-яким з пп. 1-4 як снодійні лікарські засоби. Даний винахід відноситься до нових похідних дигідроімідазо[5,1-а]--карболіну загальної формули (І): в якій: R1, R2, R3 і R4, однакові або різні, незалежно один від одного, означають атом водню, атом галогену, лінійний або розгалужений (С1-С6)-алкіл, гідроксил, лінійний або розгалужений (С1-С6)алкоксил, лінійний або розгалужений (С1-С6)тригалогеналкіл, лінійний або розгалужений (С1С6)-тригалогеналкоксил, нітрогрупу, ціаногрупу, аміногрупу, лінійну або розгалужену (С1-С6)алкіламіногрупу, лінійну або розгалужену ді-[(С1С6)-алкіл]аміногрупу, арил, лінійний або розгалужений арил-(С1-С6)-алкіл, карбоксил, лінійну або розгалужену (С1-С6)-алкіл карбоні локсигрупу, лінійний або розгалужений (С1-С6)-ацил, арилоксигрупу або лінійний або розгалужений арил-(С1-С6)алкоксил; R5 означає атом водню, лінійний або розгалужений (С1-С6)-алкіл, або лінійний або розгалужений арил-(С1-С6)-алкіл; R6 і R7, однакові або різні, незалежно один від одного, означають атом водню, атом галогену, лінійний або розгалужений (С1-С6)-алкіл, гідроксил, лінійний або розгалужений (С1-С6)-алкоксил, лінійний або розгалужений (С1-С6)-тригалогеналкіл, лінійний або розгалужений (С1-С6)тригалогеналкоксил, ціаногрупу, аміногрупу, лінійну або розгалужену (С1-С6)-алкіламіногрупу, лінійну або розгалужену ді-[(С1-С6)-алкіл]аміногрупу, арил, лінійний або розгалужений арил-(С1-С6)алкіл, карбоксил, лінійну або розгалужену (С1-С6)алкілкарбонілоксигрупу, лінійний або розгалужений (С1-С6)-ацил, арилоксигрупу або лінійний або розгалужений арил-(С1-С6)-алкоксил; їх ізомерів, а також їх адитивних солей з фармацевтично прийнятною кислотою. Відповідно до даного опису, під арилом розуміють фенільну, нафтильну, тетрагідронафтильну, дигідронафтильну, інденільну або інданільну групу, причому кожна з цих груп може бути заміщена, однаковим або різним чином, одним абодекількома атомами галогену, гідроксилом, ціаногрупою, нітрогрупою, лінійним або розгалуженим (С1-С6)алкілом, лінійним або розгалуженим (С1-С6)алкоксилом, аміногрупою, лінійною або розгалуженою (С1-С6)-алкіламіногрупою, лінійною або розгалуженою ді[(С1-С6)-алкіл]аміногрупою, арилоксигрупою, лінійним або розгалуженим арил-(С1-С6)алкоксилом, лінійним або розгалуженим (С1-С6)тригалогеналкілом, лінійним або розгалуженим (С1-С6)-ацилом, лінійним або розгалуженим (С1С6)-алкоксикарбонілом, лінійним або розгалуженим (С1-С6)-алкіламінокарбонілом або оксогрупою. Відповідно до переважного варіанту, переважними сполуками, що пропонуються у винаході, є такі, в яких: R1, R3 і R4 означають атом водню; R6 і R7, незалежно один від одного, означають атом водню, лінійний або розгалужений (С1-С6) алкіл, арил; і R5 означає атом водню, лінійний або розгалужений (С1-С6)-алкіл. Переважними замісниками R2 відповідно до винаходу є атом водню, атом галогену (атом фтору, хлору або брому), лінійний або розгалужений (С1-С6)-алкіл, гідроксил, лінійний або розгалужений (С1-С6)-алкоксил. Переважними сполуками відповідно до винаходу є наступні: 3,11-диметил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат; 8-метокси-3-метил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат; 8-метокси-5,6-дигідроімідазо[5,1-а]--карболін; 8-метокси-3-метил-1-феніл-5,6дигідроімідазо[5,1-а]--карболін; 1-етил-8-метокси-3-метил-5,6дигідроімідазо[5,1-а]--карболін; 8-метокси-3-ізопропіл-5,6-дигідроімідазо[5,1-а]-карболін; 8-метокси-3-пропіл-5,6-дигідроімідазо[5,1-а]-карболін; 8-метокси-11-метил-3-пропіл-5,6дигідроімідазо[5,1-а]--карболінметансульфонат; 8-метокси-3,11-диметил-5,6-дигідроімідазо[5,1а]--карболінметансульфонат; 8-гідрокси-3,11-диметил-5,6-дигідроімідазо[5,1а]--карболінметансульфонат; 8-гідрокси-3-метил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат; 3-метил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат; 8-хлор-3-метил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат; 8-метокси-3-феніл-5,6-дигідроімідазо[5,1-а]-карболін; 11-етил-3-метил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат; 8-хлор-3,11-диметил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат; 8-хлор-3-метил-11-етил-5,6-дигідроімідазо[5,1а]--карболінметансульфонат; 3,8-диметил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат; 3,8,11-триметил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат; 11-етил-3,8-диметил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат; 8-фтор-3-метил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат; 8-бром-3-метил-5,6-дигідроімІдазо[5,1-а]-карболінметансульфонат; 8-фтор-3,11-диметил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат; 8-фтор-11-етил-3-метил-5,6дигідроімідазо[5,1-а]--карболінметансульфонат; 8-бром-11-етил-3-метил-5,6-дигідроімідазо[5,1а]--карболінметансульфонат. Винахід відноситься також до способу одержання сполук формули (І), який відрізняється тим, що як вихідну сполуку використовують сполуку формули (II): 7 75141 в якій R1, R2, R3, R4 і R5 мають таке ж значення, як у формулі (І), яку вводять у взаємодію, відповідно до умов синтезу типу пептидного сполучання, зі сполукою формули (III): в якій R6 і R7 є такими, як вказані у формулі (І), одержуючи сполуку формули (IV): в якій R1, R2, R3, R4, R5, R6 і R7 мають згадані вище значення, яку обробляють у присутності оксихлориду фосфору у розчиннику, такому, як толуол, з одержанням сполуки формули (І): 8 Об'єктом даного винаходу також є фармацевтичні композиції, що включають як діючий початок щонайменше одну сполуку формули (І), або її адитивні солі з фармацевтично прийнятною кислотою, індивідуально або у поєднанні з одним або декількома ексципієнтами або інертними, нетоксичними, фармацевтично прийнятними наповнювачами. З фармацевтичних композицій відповідно до винаходу особливо потрібно назвати такі, які придатні для перорального, парентерального (внутрішньовенного, внутрішньом'язового або підшкірного), черезшкірного, назального, ректального, під'язикового, очного або респіраторного введення, і, зокрема, у вигляді простих таблеток або таблеток у вигляді драже, під'язикових таблеток, пакетиків, желатинових капсул, коржів, свічок, кремів, мазей, гелів для лікування шкіри, препаратів для ін'єкцій або придатних для пиття препаратів, аерозолів, крапель для очей або крапель у ніс. Наступні приклади пояснюють винахід, але жодним чином не обмежують його обсягу охорони. Похідні дигідроімідазо[5,1-а]--карболіну описані у рівні техніки як проміжні сполуки синтезу: сполуки, в яких R1=R2=R3=R4=R5=R6=H і R7=CH3, описані Y.Kanaoke, E.Sato, O.Yonemitsu, Tetrahedron, 24, 2591-2594 (1968); сполуки, в яких R1=R2=R3=R4=R5=R6=H і R7=C6H5, описані Elliott, J.Chem., 3302-3305 (1962). Однак дані похідні описані тільки як проміжні продукти і їх терапевтична активність невідома. Вони складають частину даного винаходу тільки як лікарський засіб, зокрема, як снодійне. Вихідні продукти і/або використовувані реагенти являють собою відомі або одержувані за відомими методиками продукти. Структури сполук, описаних у прикладах і на стадіях синтезу, визначені звичайними спектрофотометричними методами (інфрачервона спектроскопія, ядерний магнітний резонанс, масспектрометрія). Для ілюстрації об'єкта даного винаходу нижче наводиться декілька прикладів похідних загальної формули (І), в яких R1=R3=R4=H: в якій R1, R2, R3, R4, R5, R6 і R7 мають згадані вище значення, одержані сполуки формули (І) відповідно до винаходу, за бажанням, перетворюють в їх адитивні солі з фармацевтично прийнятною кислотою. Сполуки формул (II) і (III) або є у продажу, або їх одержують способами, відомими в органічному синтезі. Таблиця І Приклад Приклад 1 Приклад 2 Приклад 3 Приклад 4 Приклад 5 Приклад 6 Приклад 7 R2 Η СН3О СН3О СН3о СН3О СН3О СН3О R5 СН3 Η Η Η Η Η Η R6 Η Η Η Ph CH3CH2 Η Η R7 СН3 СН3 Η СН3 СН3 СН(СН3)2 (СН2)2СН3 9 75141 10 Продовження таблиці І 1 Приклад 8 Приклад 9 Приклад 10 Приклад 11 Приклад 12 Приклад 13 Приклад 14 Приклад 15 Приклад 16 Приклад 17 Приклад 18 Приклад 19 Приклад 20 Приклад 21 Приклад 22 Приклад 23 Приклад 24 Приклад 25 2 СН3О СН3О ОН ОН Η СІ СН3О Η СІ СІ СН3 СН3 СН3 F Вr F F Вr Приклад 1 3,11-Диметил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат Стадія А 2-Ацетиламіно-N-[2-(1Н-індол-3іл)етил]ацетамід До охолодженої до температури 0°С суміші 4,32г (27моль) триптаміну і 3,3г (28моль) Nацетилгліцину в 100мл диметилформаміду послідовно додають 5,8мл (27,5моль) дифенілфосфорилазиду і 3,85мл (27,5моль) триетиламіну. Суміш перемішують в атмосфері азоту при кімнатній температурі протягом 12 годин, розчинник видаляють при зниженому тиску. Одержаний залишок піддають флеш-хроматографії на силікагелі, одержуючи 5,5г (21моль) цільового продукту, або вихід складає 78%. Стадія В 2-Ацетиламіно-N-[2-(1-метил-1Н-індол-3іл)етил]ацетамід До 2г (8,23моль) одержаного відповідно до методики А аміду у 20мл диметилформаміду додають 0,35г (8,75моль) NaH (60%, у маслі) та алкілгалогенід (СН3І - 0,55мл, 8,83моль). Перемішують протягом 12 годин при кімнатній температурі, після чого видаляють розчинник при зниженому тиску. Тоді, після флеш-хроматографії на силікагелі, одержують 1,02г (3,96моль) цільового продукту, або вихід складає 48%. Стадія С 3,11-Диметил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат 1,02г (3,96моль) одержаного відповідно до методики В аміду у 50мл толуолу доводять до температури кипіння із зворотним холодильником, протягом 30 хвилин додають 10мл РОСl3 в 15мл толуолу. Реакційну суміш концентрують при зниженому тиску і залишок обробляють за допомогою 5мл етанолу, потім додають 50мл 20%-ного розчину NaOH. Витримують при перемішуванні протягом 30 хвилин, тверду речовину, що утворилася, рекуперують шляхом відфільтровування. Продукт 3 СН3 СН3 СН3 Η Η Η Η СН3СН2 СН3 СН3СН2 Η СН3 СН3СН2 Η Η СН3 СН3СН2 СН3СН2 4 Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η 5 (СН2)2СН3 СН3 СН3 СН3 СН3 СН3 Ph СН3 СН3 СН3 СН3 СН3 СН3 СН3 СН3 СН3 СН3 СН3 очищають шляхом флеш-хроматографії на силікагелі; одержують 280мг (1,26моль) цільового продукту (вихід=32%). 3,11-Диметил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат розчиняють в етанолі, додають 1 еквівалент метансульфокислоти, шляхом осадження одержують відповідний мезилат. 1 Н-ЯМР (300МГц, CDCl3), (м.д.): 2,72 (с, 3Н); 2,78 (с, 3Н); 3,23 (т, J=6,9Гц, 2Н), 3,71 (с, 3Н); 4,22 (т, J=6,9Гц, 2Н); 7,11 (м; 2Н); 7,24 (с, 2Н), 7,48 (м, 2Н) Мас-спектрометрія (m/z): 237 (100); 221; 195; 181. Приклад 2 8-Метокси-3-метил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат Застосовують методику прикладу 1, використовуючи як субстрат на стадії А 5метокситриптамін і N-ацетилгліцин, одержаний амід прямо вводять у реакцію циклізації на стадії С. 1 Н-ЯМР (300МГц, CDCl3), δ (м.д.): 2,40 (с, 3Н); 2,80 (с, 3Н); 3,00 (т, J=6,6Гц, 2Н); 3,80 (с, 3Н); 3,96 (т, J=6,6Гц, 2Н); 6,78 (м, 2Н); 7,20 (д, J=8,8Гц, 1Н); 7,50 (с, 1Н) Приклад 3 8-Метокси-5,6-дигідроімідазо[5,1-а]--карболін Застосовують методику прикладу 1, використовуючи як субстрат на стадії А 5метокситриптамін і N-формілгліцин, одержаний амід прямо вводять у реакцію циклізації на стадії С. 1 Н-ЯМР (300МГц, CDCl3: CD3OD/90:10), δ (м.д.): 3,09 (т, J=6,9Гц, 2Η); 3,82 25 (с, 3Н); 4,2 (т, J=6,9Гц, 2Н); 6,79 (дд, J=2,4 і 8,8Гц, 1H); 6,91 (д, J=2,4Гц, 1Н), 7,10 (с, 1Н); 7,23 (д, J=8,8Гц, 1Н); 7,50 (с, 1Н) Мас-спектрометрія (m/z): 239 (100); 196; 168; 140. Приклад 4 8-Метокси-3-метил-1-феніл-5,6 11 75141 12 1 Н-ЯМР (300МГц, CDCl3:CD3OD/90:10), δ дигідроімідазо[5,1-а]--карболін (м.д.): Застосовують методику прикладу 1, викорис1,06 (т, 7,5Гц, 3Н); 1,83 (м, 2Н); 2,75 (т, 7,5Гц, товуючи як субстрат на стадії А 52Н); 3,08 (т, J=6,8Гц, 2Н); 3,8 (с, 3Н), 3,88 (с, 3Н), метокситриптамін і N-ацетил-2-фенілгліцин, одер4,06 (т, J=6,8Гц, 2Н); 6,86 (дд, J=2,4 і 8,7Гц, 1Н); жаний амід прямо вводять у реакцію циклізації на 6,96 (д, J=2,4Гц, 1Н); 7,15 (с, 1Н); 7,18 (д, J=8,7Гц, стадії С. 1 1Н). Н-ЯМР (300МГц, CDCl3), δ (м.д.): Мас-спектрометрія (m/z): 295 (100); 266; 223; 2,5 (с, 3Н); 3,15 (т, J=6,9Гц, 2Н); 3,85 (с, 3Н), 133. 4,08 (т, J=6,9Гц, 2Н); 6,8 (дд, J=2,4 і 8,8Гц, 1Н); Приклад 9 6,94 (д, J=2,4Гц, 1Н); 7,15 (д, J=8,8Гц, 1Н); 7,36 (м, 8-Метокси-3,11-диметил-5,61Н); 7,46 (м, 2Н); 7,74 (м, 2Н); 8,30 (с, 1Н). Мас-спектрометрія (m/z): 329 (100); 286; 165; дигідроімідазо[5,1-а]--карболінметансульфонат 143. Застосовують методику прикладу 1, викорисПриклад 5 товуючи як субстрат на стадії А 51-Етил-8-метокси-3-метил-5,6метокситриптамін і N-ацетилгліцин. 1 Н-ЯМР (300МГц, CDCl3:CD3OD/90:10), δ дигідроімідазо[5,1-а]--карболін (м.д.): Застосовують методику прикладу 1, викорис2,44 (с, 3Н); 3,05 (т, J=6,9Гц, 2H); 3,77 (с, 3Н), товуючи як субстрат на стадії А 53,85 (с, 3Н), 3,99 (т, J=6,9Гц, 2Н); 6,86 (дд, J=2,4 і метокситриптамін і N-ацетил-2-етилгліцин, одер8,7Гц, 1Н); 6,93 (д, J=2,4Гц, 1Н); 7,15 (д, J=8,7Гц, жаний амід прямо вводять у реакцію циклізації на 1Н). стадії С. 1 Mac-спектрометрія (m/z): 267 (100); 251; 235; Н-ЯМР (300МГц, CDCl3), δ (м.д.): 224. 1,30 (т, 7Гц, 3Н); 2,43 (с, 3Н); 2,80 (кв, 7Гц, 2Н); Приклад 10 3,11 (т, J=7Гц, 2Н); 3,88 (с, 3Н), 4,06 (т, J=7Гц, 2Н); 8-Гідрокси-3,11-диметил-5,66,83 (дд, J=2,4 і 8,7Гц, 1Н); 6,97 (д, J=2,4Гц, 1Н); 7,27 (д, J=8,7Гц, 1Н); 8,71 (уш. с, 1Н). дигідроімідазо[5,1-а]--карболінметансульфонат Мас-спектрометрія (m/z): 281 (100); 266; 250; 300мг (1моль) 8-Метокси-3,11-Диметил-5,6233. дигідроімідазо[5,1-а]--карболіну, одержаного відПриклад 6 повідно до прикладу 9, розчиняють у безводному 8-Метокси-3-ізопропіл-5,6-дигідроімідазо[5,1дихлорметані при температурі -78°С. Потім додаа]--карболін ють 8мл ВВr3 і витримують протягом 12 годин при Застосовують методику прикладу 1, викорисперемішуванні і в атмосфері азоту при підвищенні товуючи як субстрат на стадії А 5температури до кімнатної. Додають 15мл 2М розметокситриптамін і N-ізобутирилгліцин, одержаний чину NaHCO3, після декантації продукт осаджують амід прямо вводять у реакцію циклізації на стадії у дихлорметані, рекуперують 150мг (0,6моль) ціС. льового продукту (вихід=50%). 1 1 H-ЯМР (300МГц, CDCl3:CD3OD/90:10), 5 Н-ЯМР (300МГц, CDCl3:CD3OD/90:10), δ (м.д.): (м.д.): 1,33 (д, J=6,8Гц, 6Н); 3,04 (м, 4Н); 3,86 (с, 3Н); 2,45 (с, 3Н); 3,05 (т, J=6,7Гц, 2Н), 3,84 (с, 3Н), 4,04 (т, J=6,8Гц, 2H); 6,79 (д, J=8,76Гц, 1Н); 6,95 (с, 4,06 (т, J=6,7Гц, 2Н); 6,80 (д, J=8,7Гц, 1Н); 6,91 (с, 1Н); 6,98 (с, 1Н); 7,22 (д, J=8,76Гц, 1Н);·10,30 (с, 1Н)); 7,15 (д, J=8,7Гц, 1Н). 1Н) Mac-спектрометрія (m/z): 253 (100); 224; 211; Mac-спектрометрія (m/z): 281 (100); 266; 196; 126. 133. Приклад 11 Приклад 7 8-Гідрокси-3-метил-5,6-дигідроімідазо[5,1-а]-8-Метокси-3-пропіл-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат карболін 350мг (1,4моль) 8-Метокси-3-метил-5,6Застосовують методику прикладу 1, викорисдигідроімідазо-[5,1-а]--карболіну, одержаного товуючи як субстрат на стадії А 5відповідно до прикладу 2, розчиняють у безводнометокситриптамін і N-бутирилгліцин, одержаний му дихлорметані при температурі -78°С. Потім амід прямо вводять у реакцію циклізації на стадії додають 8мл ВВr3 і витримують протягом 12 годин С. при перемішуванні і в атмосфері азоту при підви1 Н-ЯМР (300МГц, CDCl3), δ (м.д.): щенні температури до кімнатної. Додають 15мл 1,00 (т, 7,5Гц, 3Н); 1,76 (м, 2Н); 2,70 (т, 7,5Гц, 2М розчину NaHCO3, після декантації продукт оса2Н); 3,08 (т, J=7,5Гц, 2Н); 3,87 (с, 3Н), 3,97 (т, джують у дихлорметані, рекуперують 200мг J=7,5Гц, 2Н); 6,81 (дд, J=2,7 і 8,7Гц, 1Н); 6,88 (д, (0,83моль) цільового продукту (вихід=59%). 1 J=2,7Гц, 1Н); 7,08 (с, 1Н); 7,28 (д, J=8,7Гц, 1Н), Н-ЯМР (300МГц, CDCl3:CD3OD/90:10), δ 10,38 (уш. с, 1Н). (м.д.): Мас-спектрометрія (m/z): 281 М+; 269; 252 2,67 (с, 3Н); 3,19 (т, J=7,2Гц, 2H); 4,21 (т, (100); 209. J=7,2Гц, 2H); 6,78 (дд, J=2,4 і 8,7Гц, 1Н); 6,88 (д, ПРИКЛАД 8 J=2,4Гц, 1Н); 7,23 (д, J=8,7Гц, 1Н). 8-Метокси-11-метил-3-пропіл-5,6Приклад 12 дигідроімідазо[5,1-а]--карболінметансульфонат 3-Метил-5,6-дигідроімідазо[5,1-а]-Застосовують методику прикладу 1, викорискарболінметансульфонат товуючи як субстрат на стадії А 5Застосовують методику прикладу 1, викорисметокситриптамін і N-бутирилгліцин. товуючи як субстрат на стадії А триптамін і N 13 75141 14 ацетилгліцин, одержаний амід прямо вводять у мід як алкілувальний агент на стадії В. 1 реакцію циклізації на стадії С. Н-ЯМР (300МГц, CDCl3), δ (м.д.): 1 Н-ЯМР (300МГц, CDCl3), δ (м.д.): 1,39 (т, J=4,8Гц, 3Н); 2,70 (с, 3Н); 2,85 (с, 3Н); 2,53 (с, 3Н); 3,08 (т, J=6,8Гц, 2H), 3,99 (т, 3,2 (т, J=7Гц, 2Н); 4,3 (м, 4Н); 7,2 (дд, J=2,4 і 8,8Гц, J=6,8Гц, 2Н); 7,04 (м, 2Н), 7,16 (м, 2Н), 7,36 (с, 1Н); 1Н); 7,35 (д, J=8,8Гц, 1Н); 7,53 (д, J=2,4Гц, 1Н); 7,6 7,44 (д, 1Н) (с, 1Н). Mac-спектрометрія (m/z): 223 (100); 208; 181; Мас-спектрометрія (m/z): 285 (100); 270; 249; 154. 180. Приклад 13 Приклад 18 8-Хлор-3-метил-5,6-дигідроімідазо[5,1-а]-3,8-Диметил-5,6-дигідроімідазо[5,1-а]-карболінметансульфонат карболінметансульфонат Застосовують методику прикладу 1, викорисЗастосовують методику прикладу 1, використовуючи як субстрат на стадії А 5-хлортриптамін і товуючи як субстрат на стадії А 5-метилтриптамін і N-ацетилгліцин, одержаний амід прямо вводять у N-ацетилгліцин, одержаний амід прямо вводять у реакцію циклізації на стадії С. реакцію циклізації на стадії С. 1 1 Η-ΗΜΡ (300МГц,CDCl3:CD3OD/90:10), δ Н-ЯМР (300МГц, CDCl3:CD3OD/90:10), δ (м.д.): (м.д.): 2,72 (с, 3Н); 2,81 (с, 3Н); 3,16 (т, J=6,9Гц, 2Н); 2,43 (с, 3Н); 2,61 (с, 3Н); 2,85 (с, 3Н); 3,14 (т, 4,13 (т, J=6,9Гц, 2Н); 7,12 (дд, J=2 і 8,7Гц, 1Н); 7,31 J=7Гц, 2H); 4,08 (т, J=7Гц, 2Н); 7,05 (д, 8,6Гц, 1Н); (д, J=8,7Гц, 1Н); 7,44 (д, J=2Гц, 1Н); 7,52 (с, 1Н) 7,28 (с, 1Н), 7,32 (д, J=8,6Гц, 1Н); 7,51 (с, 1Н). Mac-спектрометрія (m/z): 257 (100); 242; 221; Мас-спектрометрія (m/z): 237 (50); 129; 73; 55 215. (100). Приклад 14 Приклад 19 8-Метокси-3-феніл-5.6-дигідроімідазо[5,1-а]-3,8,11-Триметил-5,6-дигідроімідазо[5,1-а]-карболін карболінметансульфонат Застосовують методику прикладу 1, викорисЗастосовують методику прикладу 1, використовуючи як субстрат на стадії А 5товуючи як субстрат на стадії А 5-метилтриптамін і метокситриптамін і гіпурову кислоту, одержаний N-ацетилгліцин. 1 амід прямо вводять у реакцію циклізації на стадії Н-ЯМР (300МГц, CDCl3:CD3OD/90:10), δ С. (м.д.): 1 H-ЯМР (300МГц, CD3COCD3), δ (м.д.): 2,40 (с, 3Н); 2,70 (с, 3Н); 2,75 (с, 3Н); 3,2 (т, 2,87 (с, 3Н); 3,16 (т, J=6,8Гц, 2Н); 3,82 (с, 3Н), J=6,9Гц, 2Н); 3,75 (с, 3Н); 4,18 (т, J=6,9Гц, 2Н); 7,07 4,45 (т, J=6,8Гц, 2Н); 6,77 (дд, J=2,4 і 9,6Гц, 1Н); (д, J=8,5Гц, 1Н), 7,21 (д, J=8,5Гц, 1Н); 7,27 (с, 1Н); 7,05 (д, J=2,4Гц, 1Н); 7,30 (с, 1Н); 7,31 (д, J=9,6Гц, 7,50 (с, Н) 1Н); 7,52 (м, 3Н); 7,75 (м, 2Н); 8,02 (с, 1Н) Мас-спектрометрія (m/z): 251 (100); 235; 203. Mac-спектрометрія (m/z): 315 (100); 272; 211; Приклад 20 168. 11-Етил-3,8-диметил-5,6-дигідроімідазо[5,1-а]Приклад 15 -карболінметансульфонат 11-Етил-3-метил-5,6-дигідроімідазо[5,1-а]-Застосовують методику прикладу 1, викорискарболінметансульфонат Застосовують методику товуючи як субстрат на стадії А 5-метилтриптамін і прикладу 1, використовуючи як субстрат на стадії N-ацетилгліцин, а також використовуючи етилброА триптамін і N-ацетилгліцин, а також використомід як алкілувальний агент на стадії В. 1 вуючи етилбромід як алкілувальний агент на стадії Н-ЯМР (300МГц, COCl3:CD3OD/90:10), δ В. (м.д.): 1 1,32 (т, J=7,2Гц, 3Н); 2,40 (с, 3Н); 2,72 (с, 3Н); Н-ЯМР (300МГц, CD3OD), (м.д.): 2,78 (с, 3Н); 3,21 (т, J=6,9Гц, 2Н); 4,19 (м, 4Н); 7,08 1,33 (т, 7,1Гц, 3Н); 2,76 (с, 3Н); 2,78 (с, 3Н); (д, J=8,4Гц, 1Н); 7,20 (д, J=8,4Гц, 1Н); 7,29 (с, 1Н); 3,25 (т, J=6,9Гц, 2Н), 4,24 (м, 4Н); ,12 (т, 1Н); 7,3 7,45 (с, 1Н) (м, 2Н); 7,49 (д+1с, 2Н). Mac-спектрометрія (m/z): 265 (100); 250; 236; Приклад 16 223. 8-Хлор-3,11-диметил-5,6-дигідроімідазо[5,1-а]Приклад 21 -карболінметансульфонат 8-Фтор-3-метил-5,6-дигідроімідазо[5,1-а]-Застосовують методику прикладу 1, викорискарболінметансульфонат товуючи як субстрат на стадії А 5-хлортриптамін і Застосовують методику прикладу 1, викорисN-ацетилгліцин. 1 товуючи як субстрат на стадії А 5-фтортриптамін і Η-ΗΜΡ (300МГц, CDCl3), 5 (м.д.): N-ацетилгліцин, одержаний амід прямо вводять у 2,60 (с, 3Н); 2,70 (с, 3Н); 3,16 (т, J=6,8Гц, 2Н); реакцію циклізації на стадії С. 4,20 (т, 6,8Гц, 2Н); 7,12 (д, J=8,8Гц, 1Н); 7,25 (д, 1 H-ЯМР (300МГц, CDCl3:CD3OD/90:10), δ J=8,8Гц, 1Н); 7,50 (с, 1Н); 7,6 (с, 1Н). (м.д.): Мас-спектрометрія (m/z): 271 (100); 235; 193; 2,60 (с, 3Н); 2,75 (с, 3Н); 3,09 (т, J=7Гц, 2Н); 167. 4,10 (т, J=7Гц, 2H); 6,87 (дт, J=2,4 і 9Гц, 1Η), 7,02 Приклад 17 (дд, J=2,4 і 9Гц, 1Н); 7,26 (дд, J=3 і 9Гц, 1Н); 7,50 8-Хлор-3-метил-11-етил-5,6-дигідроімідазо[5,1(с, 1Н). а]--карболінметансульфонат Мас-спектрометрія (m/z): 241 (100); 226; 199; Застосовують методику прикладу 1, викорис172. товуючи як субстрат на стадії А 5-хлортриптамін і Приклад 22 N-ацетилгліцин, а також використовуючи етилбро 15 75141 16 ного дослідження щонайменше протягом 4 годин. 8-Бром-3-метил-5,6-дигідроімідазо[5,1-а]-Експериментальний протокол тестування на карболінметансульфонат курчаті Застосовують методику прикладу 1, викорисКурчат виду JA 657, які походять з Couvoir товуючи як субстрат на стадії А 5-бромтриптамін і Gauguet, 44 Le Pin, утримували щонайменше проN-ацетилгліцин, одержаний амід прямо вводять у тягом 6 днів по програмі освітлення, що чергуєтьреакцію циклізації на стадії С. 1 ся: 12 годин у денний час і 12 годин у нічний час, Η-ΗΜΡ (300МГц, CDCl3:CD3OD/90:10), δ при температурі, регульованій при 25°С±2°С. їх (м.д.): годували за бажанням і піддавали випробуванню у 2,68 (с, 3Н); 2,86 (с, 3Н); 3,19 (т, J=7,2Гц, 2Н); віварії групами по З індивідууми з середньою ма4,20 (т, J=7,2Гц, 2Н); 7,28 (м, 2Н); 7,34 (с, 1Н); 7,58 сою 100±10г у день досліду. У цьому віці у даного (с, 1Н), 7,61 (с, 1Н) виду не існує ефективного менінгеального (гематоМас-спектрометрія (m/z): 301/302 (100); 286; мозкового) бар'єра. Продукти, що тестуються, 259; 234. вводили шляхом ін'єкції у трьох дозах (1, 3 і Приклад 23 10мг/кг) внутрішньом'язово у вигляді водного роз8-Фтор-3,1-диметил-5,6-дигідроімідазо[5,1-а]чину або у вигляді водної суспензії (1 крапля твіну -карболінметансульфонат 80 на мл) кожній з двох груп по 3 курчати, за якими Застосовують методику прикладу 1, викорисспостерігали протягом 90 хвилин. Для кожної серії товуючи як субстрат на стадії А 5-фтортриптамін і тесту (18 віваріїв) існує щонайменше одна група N-ацетилгліцин. 1 контрольних "негативних" курчат, яка одержує таН-ЯМР (300МГц, CDCl3:CD3OD/90:10), (м.д.): кий же об'єм (0,2мл внутрішньом'язово) води для 2,78 (с, 3Н); 2,83 (с, 3Н); 3,25 (т, J=6,9Гц, 2Н); препаратів, що ін'єктуються. 4,31 (т, J=6,9Гц, 2H); 7,07 (д, J=2,4 і 9Гц, 1Н), 7,22 Протягом періоду спостереження, що складає (дд, J=2,4 і 9ГЦ, 1Н); 7,32 (дд, J=3 і 9Гц, 1Н), 7,66 90 хвилин, всіх курчат інтенсивно стимулювали (с, 1Н). кожні 15 хвилин шляхом надання повної годівниці і Mac-спектрометрія (m/z): 255 (100); 213; 185; у кожний період, що складає 5 хвилин, присвою128. вали оцінку, яка відповідає стану неспання на пеПриклад 24 ріод, що розглядається, вибраному з наступних 5 8-Фтор-11-етил-3-метил-5,6-дигідроімідазо[5,1станів: мобільний; лежачий під час неспання; стан а]--карболінметансульфонат дрімоти; сонливий; сон стоячи (подібний до сну Застосовують методику прикладу 1, викорисстан). Параметрами, що досліджуються, є термін товуючи як субстрат на стадії А 5-фтортриптамін і настання дрімотного стану (ТА), що протікає між N-ацетилгліцин, а також використовуючи етил ін'єкцією і першим етапом сну, тривалість першого бромід як алкілу вальний агент на стадії В. 1 сну (TS) і загальний час заспокоєного стану за Н-ЯМР (300МГц, CDCl3:CD3OD/90:10), δ період спостереження (Tsed), виражений у хвили(м.д.): нах і у % від періоду спостереження (Sed). 1,32 (т, J=7,2Гц, 3Н); 2,70 (с, 3Н); 2,80 (с, 3Н); Для порівняння результатів дослідів, реалізо3,16 (т, J=6,9Гц, 2Н); 4,2 (м, 4Н); 6,97 (дт, J=2,4 і ваних у різні дати, визначали подовження трива9Гц, 1Н), 7,13 (дд, J=2,4 і 9Гц, 1Н); 7,23 (дд, J=4 і лості першого сну (TS) у порівнянні з контрольни9Гц, 1Н); 7,65 (с, 1Н). ми піддослідними групами. Мас-спектрометрія (m/z): 269 (100); 254; 227; Результати 199. У курчат цього віку поза дослідом тривалість Приклад 25 циклу неспання-сон складає 20-30 хвилин протя8-Бром-11-етил-3-метил-5,6гом дня. Отже, починаючи з дози 1мг, виявилося, дигідроімідазо[5,1-а]--карболінметансульфонат що принаймні 11 сполук (з 20) викликають дуже Застосовують методику прикладу 1, викориссильне зменшення рухової активності, судячи з товуючи як субстрат на стадії А 5-бромтриптамін і тривалості першого сну (TS), коли дана тривалість N-ацетилгліцин, а також використовуючи етил перевищує 20 хвилин. бромід як алкілувальний агент на стадії В. 1 При більш високих дозах 3мг/кг і 10мг/кг число H-ЯМР (300МГц, CDCl3:CD3OD/90:10), 5 продуктів, що тестуються, з таким же ефектом (м.д.): складає 18 з 20 і 20 з 20. 1,32 (т, J=7Гц, 3Н); 2,70 (с, 3Н); 2,75 (с, 3Н); Існує чітка позитивна залежність доза-ефект 3,18 (т, J=7Гц, 2Н); 3,59 (с, 3Н); 4,20 (м, 4Н); 7,19 для більшості тестованих сполук, що полягає у (д, J=8,7Гц, 1Н), 7,30 (дд, J=1,8 і 8,7Гц, 1Н); 7,53 (с, зменшенні терміну настання дрімотного стану, 1Н); 7,63 (д, J=1,8Гц, 1Н). якщо доза підвищується. Мас-спектрометрія (m/z): 329/330 (100); 316; За 90 хвилин спостереження відхилення між 300; 273. часом у заспокоєному стані і тим же часом, що Похідні дигідроімідазо[5,1-а]--карболіну відспостерігається при введенні плацебо, перевищує повідно до винаходу, особливо у формі (розчинній) 52 хвилини для двох сполук, починаючи з дози метилсульфонатів, були піддані тестуванню на 1мг/кг, для 4 сполук при дозі 3мг/кг і для 12 сполук курчаті і деякі, активні у випадку курчати сполуки при дозі 10мг/кг. вводили у разових дозах 6 собакам породи коротконогих гончих обох статей для полісомнографіч 17 75141 18 Таблиця II (доза: 1мг/кг) Сполуки Приклад 1 Приклад 2* Приклад 3* Приклад 4* Приклад 5* Приклад 6* Приклад 7* Приклад 8 Приклад 9 Приклад 10 Приклад 11 Приклад 12 Приклад 13 Приклад 14* Приклад 15 Приклад 16 Приклад 17 Приклад 18 Приклад 19 Приклад 20 ТА Хвилини 7 16 10 16,5 20,5 11 16,5 16 22 15 40 10 16,5 7 12,5 11,5 12 5 4 2 TS Хвилини 56,5 3 40 38 33 56,5 16 21,5 3 5 0 39,5 33,5 35,5 12 15 12 32,5 17,5 65,5 Tsed Хвилини 64,5 25 66,51 53,01 52,47 65,97 46 38 24,5 38 26,5 46,5 52 62,865 21,5 37 37 62,5 44,5 72 Sed % 71,7 27,8 73,9 58,9 58,3 73,3 41,4 42,2 27,2 42,2 29,4 51,7 57,8 63,5 23,9 41 41,1 69,4 49,4 80 TS (хвилини) Відхилення від плацебо 56 3 36 34 29 52,5 16 21 2,8 4,7 -0,3 39 33 32 21 14,7 11,7 24 11 57 * у формі вільної основи Таблиця III (доза: 3мг/кг) Сполуки Приклад 1 Приклад 2* Приклад 3* Приклад 4* Приклад 5* Приклад 6* Приклад 7* Приклад 8 Приклад 9 Приклад 10 Приклад 11 Приклад 12 Приклад 13 Приклад 14* Приклад 15 Приклад 16 Приклад 17 Приклад 18 Приклад 19 Приклад 20 ТА Хвилини 4,5 8,5 7 14 14,5 12,5 16,5 8,5 17,5 30 15 3,5 9,5 15 7 13,5 7,5 4,5 3,5 1,5 *у формі вільної основи TS Хвилини 78,5 41 66,5 22,5 53 72,5 27 33 13,5 1 7 42 73 34 29,5 20,5 23,5 30,5 46,5 51,5 Tsed Хвилини 78,5 62,5 71,0 65,5 69,0 72,5 45,5 54 26,5 11 34,5 57,5 73 61,2 40,5 30,5 30 57,5 56,5 71,5 Sed % 87,2 69,4 78,9 72,8 76,7 80,6 41 60 29,4 12,2 38,3 63,9 81,1 68 45 33,9 33,3 63,9 62,8 79,4 TS (хвилини) Відхилення від плацебо 78 41 62,5 18,5 49 68,5 27 32,7 13 0,7 6,7 41,7 73 31,5 29 20 23 22,5 38,5 43,5 19 75141 20 Таблиця IV (доза: 10мг/кг) Сполуки Приклад 1 Приклад 2* Приклад 3* Приклад 4* Приклад 5* Приклад 6* Приклад 7* Приклад 8 Приклад 9 Приклад 10 Приклад 11 Приклад 12 Приклад 13 Приклад 14* Приклад 15 Приклад 16 Приклад 17 Приклад 18 Приклад 19 Приклад 20 ТА Хвилини 1 7 6,5 8,5 13,5 12,5 12,5 5,5 16,5 11,5 6 1 4 7 1 7,5 5 7,5 3,5 1,5 TS Хвилини 86 83 77,5 81,5 40,5 72,5 38,5 41 15,5 12,5 9,5 89 86 28 70 31 43,5 76 60 87,5 Tsed Хвилини 87 83 78,0 81,5 56,5 74,0 53,5 68,5 38,5 27 18,5 89 86 63 72 52,5 60,5 81,5 67,5 87,5 Sed % 96,7 92,2 86,7 90,6 62,8 82,2 48,2 76,1 42,8 30 20,6 98,9 95,6 70 80 58,3 67,2 90,6 75,0 97,2 TS (хвилини) Відхилення від плацебо 85,7 83 73,5 76,5 36,5 68,5 38,5 40,7 1512 9 88,7 85,7 25,5 69,7 52 43 68 52 81,5 * у формі вільної основи Експериментальний протокол тестування на собаці Полісомнографічні досліди здійснювали з кожним з 3 продуктів групи на 6 собаках обох статей, дорослих, що походять з розплідника "HARLAN а 03 Gannat", при використанні електродів з нержавіючої сталі, які хірургічно імплантовані на час досліду і контактують з лобовими кістками через синус, напроти моторних ділянок головного мозку. Використовували метод Nishino та ін., адаптований Tafani, Valin та ін. Він включає реєстрацію 2 шляхів для рухів очей, м'язового шляху (концентричний електрод у м'язах потилиці) і 2 електроенцефалографічних (EEG) шляхів. Реєстрацію EEG, перетворену у цифрову форму, здійснювали на поліграфі Nicollet Schwarzer або подібному апараті (DELTAMED Coherence 2 et 3, МЕІ Galileo NT) протягом 4 годин після введення желатинової капсули 00, що містить 0, 16 або 48мг продукту, який тестується (або в середньому 0,1 і 3мг/кг живої маси). Кожну собаку реєстрували 4 години 2 рази протягом 2 послідовних днів або вранці, або у другій половині дня, після тижневого перебування у 2 клітці для реєстрації, що має площу 1м , висоту 80см, виконаній з нержавіючої сталі, типу SHORLINE. Для кожної собаки реєстрація завжди починалася в один і той же час. Їжу давали за 30 хвилин до початку реєстрації. Полісомнографічні криві дозволяють розрізнити щонайменше 4 стадії для кожного періоду, який складає 30 послідовних секунд: неспання, дрімота, ортодоксальний сон і парадоксальний сон. Для кожної собаки визначали латентний період появи кожного з перших епізодів за відсутності стану неспання і тривалість кожної стадії у двогодинний період. Порівняння середніх значень дозволяє вивчити вплив продуктів, що тестуються, на мікроструктуру сну. Результати Латентності наведені у таблицях V-VII: Таблиця V Доза Плацебо 1+2 Приклад 2 (1мг) Приклад 2 (3мг) Дрімота, хвилини 70±6 40±14,7 37±6,7 Ортодоксальний сон, хвилини 98±20 44±16,3 45±5,4 Парадоксальний сон, хвилини 137±4 114±53 63±21,1 21 75141 22 Таблиця VI Дрімота, хвилини 69±58 25±11,6 40±13,1 27±9,1 Доза Плацебо 1 Приклад 13 (1мг) Плацебо 2 Приклад 13 (3мг) Ортодоксальний сон, хвилини 79±60 32±11,5 50±23,8 35±11 Парадоксальний сон, хвилини 100±62 63±28,2 62±22,4 56±19,5 Таблиця VII Дрімота, хвилини 71±39,8 47±19,1 44±20,4 21±7,1 Доза Плацебо 1 Приклад 1 (1мг) Плацебо 2 Приклад 1 (3мг) Ортодоксальний сон, хвилини 102±71,8 52±24,8 61±27,6 27±8,0 При використанні трьох продуктів, що тестуються, спостерігається чітке зменшення латентного періоду появи першої дрімоти, більш чітке при дозі 3мг/кг для продукту прикладу 1. Латентність першого епізоду ортодоксального сну (що характеризується "пучками" на кривих EEG) зменшена Парадоксальний сон, хвилини 125±66,9 101±80,3 87±30,2 50±22,2 вдвічі при використанні продуктів, що тестуються. Три сполуки викликають позитивний снодійний ефект. У таблицях VIII-X, що наводяться нижче, представлений час кожної стадії неспання. Таблиця VIII Доза Плацебо 1+2 Приклад 2 (1мг) Приклад 2 (3мг) Неспання, хвилини 147±35,5 Дрімота, хвилини 25±10,3 Ортодоксальний сон, хвилини 59±21,9 Парадоксальний сон, хвилини 8,5±5,4 136±40,3 31±4,6 59±20,5 13,5±10,6 123±30,5 36±15,4 60±26,9 20±9,5 Таблиця IX Доза Плацебо 1 Приклад 13 (1мг) Плацебо 2 Приклад 13 (3мг) Неспання, хвилини 156±38,5 26±11,3 Ортодоксальний сон, хвилини 39±23,9 Парадоксальний сон, хвилини 19±11,4 135±44,3 24±2,6 57±26,5 21±13,6 140±27,9 32±7,3 47±19,9 21±10 122±36,5 31±7 61±24,9 26±13,5 Дрімота, хвилини Таблиця X Доза Плацебо 1 Приклад 1 (1мг) Плацебо 2 Приклад 1 (3мг) Неспання, хвилини Дрімота, хвилини Ортодоксальний сон, Парадоксальний сон, хвилихвилини ни 45±19,4 11±8,5 154±35,2 30±16,0 139±69,1 27±10,4 51±42,3 23±19,1 134±36,5 35±21,4 50±34,8 20±10,8 106±34,7 40±1,9 65±30,2 29±13,7 Протягом 4 годин реєстрації спостерігають тенденцію до зменшення часу неспання, особливо при дозі 3мг/кг для трьох сполук. Це зменшення часу неспання відбувається головним чином за рахунок збільшення етапів ортодоксального сну і парадоксального сну. Ефекти, що спостерігаються, виявляються більш виразно протягом перших двох годин, особливо при дозі 1мг/кг, що може відповідати кінетиці видалення сполук. Три сполуки володіють снодійними властивостями. 23 75141 24 На відміну від відомих сполук, немає змін у чанеспання, прискорюють настання сну (позитивний совому співвідношенні ні у стані дрімоти, ні параснодійний ефект). У курчати і у собаки відбуваєтьдоксального сну у період відсутності неспання. ся зменшення активності під час неспання. У цьоВсі імідазопіридоіндольні похідні відповідно до му останньому випадку не відбувається зміна ульвинаходу володіють фармакологічною активністю траструктури сну. Отже, сполуки відповідно до відносно центральної нервової системи щонаймевинаходу придатні як лікарські засоби, особливо, нше відносно двох видів тварин. Вони зменшують як снодійні. Комп’ютерна верстка Л. Купенко Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюDihydroimidazo[5,l-a]-0100090000039d00000002001c00000000000500000009020000000005000000020101000000050000000102ffffff00050000002e0118000000050000000b0200000000050000000c02a00100011200000026060f001a00ffffffff000010000000c0ffffffc1ffffffc0000000610100000b00000026060f000c004d61746854797065000040001c000000fb02e0fe0000000000009001000000020002001053796d626f6c007740000000a2090aac7da8f47786a8f4770100000000003000040000002d01000008000000320a20012e000100000062790a00000026060f000a00ffffffff0100000000001c000000fb021000070000000000bc02000000cc0102022253797374656d000000000a000000040000000000ffffffff0100000000003000040000002d01010004000000f0010000030000000000 -carboline derivatives, a method for the preparation thereof and a pharmaceutical composition based thereon
МПК / Мітки
МПК: C07D 471/14, A61K 31/437, A61P 25/20
Мітки: спосіб, одержання, основі, дигідроімідазо[5,1-a]-b-карболіну, композиція, фармацевтична, похідні
Код посилання
<a href="https://ua.patents.su/12-75141-pokhidni-digidroimidazo51-a-b-karbolinu-sposib-kh-oderzhannya-ta-farmacevtichna-kompoziciya-na-kh-osnovi.html" target="_blank" rel="follow" title="База патентів України">Похідні дигідроімідазо[5,1-a]-b-карболіну, спосіб їх одержання та фармацевтична композиція на їх основі</a>
Попередній патент: Спосіб одержання провідної фторованої полімерної композиції, що містить поліаналін
Наступний патент: Пристрій для ущільнення дверних отворів коксових печей
Випадковий патент: Гідравлічний привід телескопічної стріли