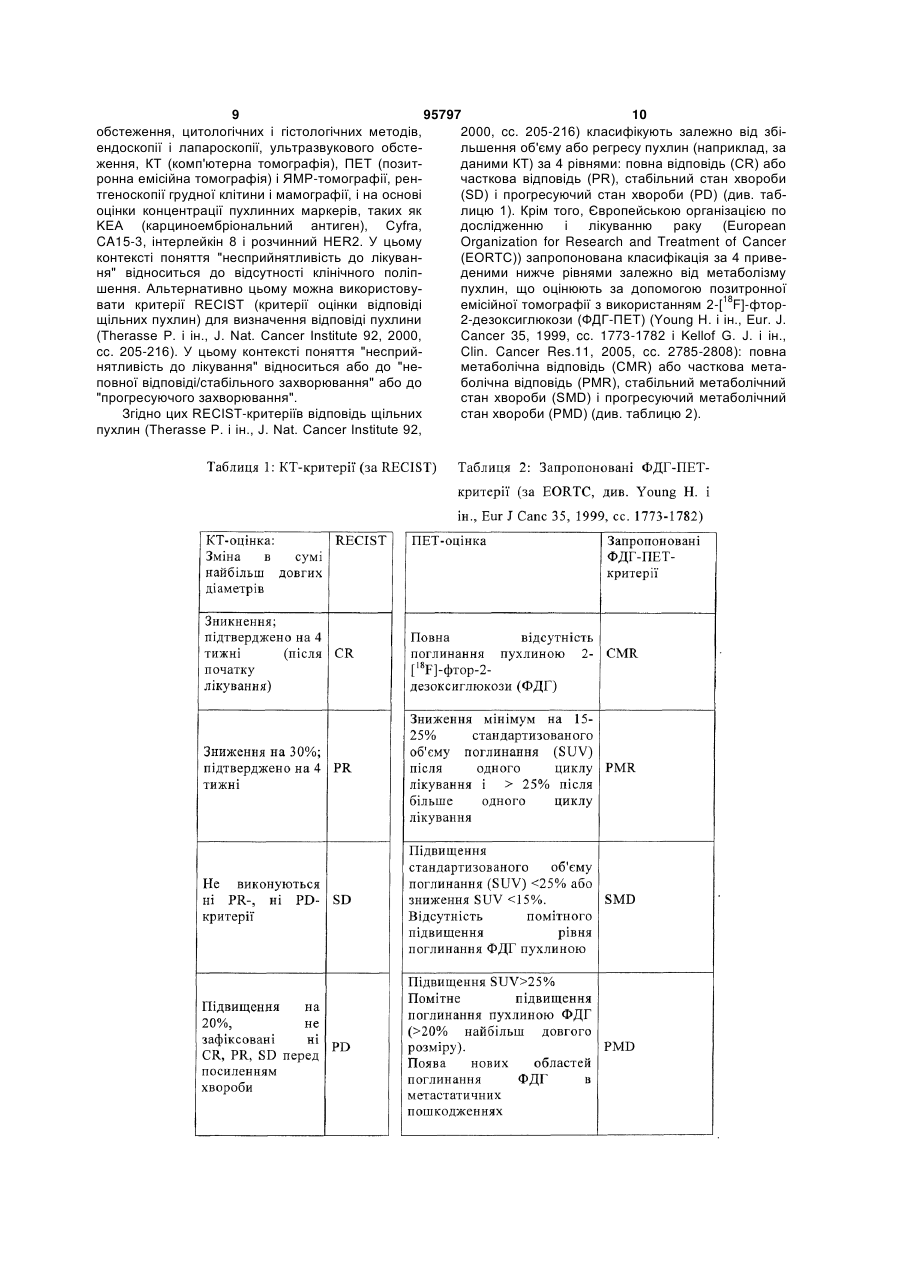
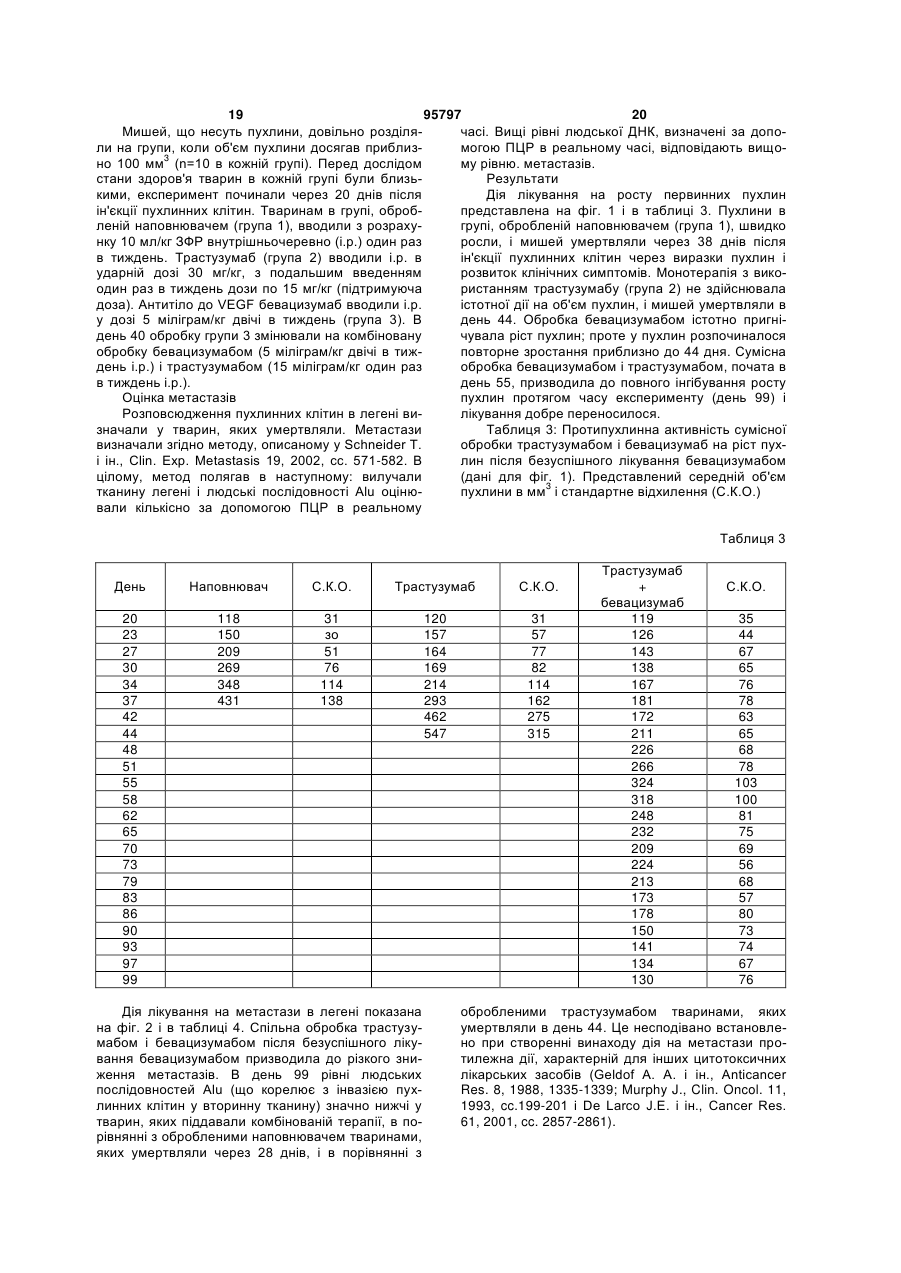
Терапія пухлин з використанням судинного ендотеліального фактора росту і антитіла до рецептора типу 2 людського епітеліального фактора росту
Формула / Реферат
1. Застосування антитіла до HER2 та антитіла до VEGF для приготування лікарського засобу для лікування раку молочної залози, який характеризується надекспресією білка рецептора НЕR2, у пацієнта, не сприйнятливого до попередньої терапії з використанням антитіла до VEGF, що полягає в тому, що пацієнтові вводять терапевтично ефективну кількість антитіла до HER2 і антитіла до VEGF.
2. Застосування за п. 1, в якому антитіло до VEGF є бевацизумабом.
3. Застосування за п. 1 або п. 2, в якому пацієнт є людиною.
4. Застосування за будь-яким з пп. 1-3, в якому антитіло до HER2 є трастузумабом.
5. Застосування за будь-яким з пп. 1-4, в якому лікарський засіб призначено для зменшення метастазів.
6. Застосування антитіла до HER2 в способі зменшення метастазів у пацієнта із раком молочної залози, що характеризується надекспресією білка рецептора HER2, не сприйнятливого до попередньої терапії з використанням антитіла до VEGF, що полягає в тому, що пацієнтові вводять терапевтично ефективну кількість антитіла до HER2 і антитіла до VEGF.
7. Застосування за п. 6, в якому антитіло до VEGF, призначене для введення, є бевацизумабом.
8. Застосування за п. 6 або п. 7, в якому пацієнт є людиною.
9. Застосування за будь-яким з пп. 6-8, в якому антитіло до HER2 є трастузумабом.
10. Застосування антитіла до VEGF в способі зменшення метастазів у пацієнта із раком молочної залози, що характеризується надекспресією білка рецептора HER2, не сприйнятливого до попередньої терапії з використанням антитіла до VEGF, що полягає в тому, що пацієнтові вводять терапевтично ефективну кількість антитіла до HER2 і антитіла до VEGF.
11. Застосування за п. 10, в якому антитіло до VEGF є бевацизумабом.
12. Застосування за п. 10 або п. 11, в якому пацієнт є людиною.
13. Застосування за будь-яким з пп. 10-12, в якому антитіло до HER2, призначене для введення, є трастузумабом.
Текст
1. Застосування антитіла до HER2 та антитіла до VEGF для приготування лікарського засобу для лікування раку молочної залози, який характери 2 (19) 1 3 Дійсний винахід відноситься до сумісної терапії з використанням антитіл до HER2 і до VEGF. Зокрема, винахід відноситься до застосування вказаних антитіл для лікування раку молочної залози у пацієнта, несприйнятливого до попередньої терапії з використанням антитіла до VEGF. Ангіогенез бере участь в патогенезі різних порушень, включаючи щільні пухлини, синдроми внутрішньоочної неоваскуляризації, такі як проліферативні ретинопатії або пов'язана з віком дегенерація жовтої плями (AMD), ревматоїдний артрит і псоріаз (Folkman J. і ін., J. Biol. Chem. 267, 1992, сс. 10931-10934; Klagsbrun Μ. і ін., Annu. Rev. Physiol. 53, 1991, сс. 217-239; і Garner Α., Vascular diseases, в: Pathobiology of ocular disease, A dynamic approach, під ред. Garner А. і Klintworth G.K., 2-е видавництво, вид-во Marcel Dekker, New York, 1994, cc.1625-1710). У разі щільних пухлин неоваскуляризація призводить до того, що пухлинні клітини набувають переваги з позицій зростання і автономії проліферації в порівнянні із здоровими клітинами. Так, виявлена кореляція між щільністю мікросудин в зрізах пухлини і виживанням пацієнта, що страждає раком молочної залози, а також у разі деяких інших пухлин (Weidner N. і ін., N. Engl. J. Med. 324, 1991, cc. 1-6; Horak E. R. і ін., Lancet 340, 1992 ,cc. 1120-1124 і Macchiarini P. і ін., Lancet 340, 1992, cc. 145-146). Судинний ендотеліальний фактор росту (VEGF) бере участь в регуляції нормального і аномального ангіогенезу і неоваскуляризації, що асоціюється з пухлинами і внутрішньоочними порушеннями (Ferrara N. і ін., Endocr. Rev. 18, 1997, cc.4-25; Berkman R. A. і ін., J. Clin. Invest. 91, 1993, cc. 153-159; Brown L. F. і ін., Human Pathol. 26, 1995, cc. 86-91; Brown L. F. і ін., Cancer Res. 53, 1993, cc. 4727-4735; Mattern J. і ін., Brit. J. Cancer 73, 1996, cc. 931-934; і Dvorak H. F. і ін., Am. J. Pathol. 146, 1995, cc. 1029-1039). Антитіла, які є нейтралізуючими до VEGF, пригнічують зростання різних людських ліній пухлинних клітин в мишах (Кіт К. J. і ін., Nature 362, 1993, cc. 841-844; Warren R. S. і ін., J. Clin. Invest. 95, 1995, cc. 1789-1797; Borgstrom P. і ін., Cancer Res. 56, 1996, cc. 40324039; і Melnyk О. і ін., Cancer Res. 56, 1996, cc. 921-924). У WO 94/10202, WO 98/45332, WO 2005/00900 і WO 00/35956 описані антитіла до VEGF. Гуманізованим моноклональним антитілом бевацизумаб (надходить у продаж під товарним знаком Avastin®) є антитіло до VEGF, яке застосовують для терапії пухлин і яке є єдиним антиангіогенним лікарським засобом, дозволеним для лікування раку (WO 98/45331). HER2 є представником сімейства рецепторів людського епідермального фактору росту і володіє тирозинкіназною активністю в домені цитоплазми. У пухлинних клітинах відбувається надекспресія HER2, і це корелює з несприятливим прогнозом і малим часом виживання. Таким чином, HER2 є важливою мішенню при лікуванні раку молочної залози. Антитіла до HER2 описані у Такаі N. і ін., Cancer 104, 2005, сс. 2701-2708; Yeon С. Η. і ін., 95797 4 Invest. New Drugs 23, 2005, сс. 391-409; Wong W. Μ. і ін., Cancer Pract.7, 1999, сс. 48-50; Albanell J. і ін., Drugs Today (Barc). 35, 1999, cc. 931-46. Трастузумаб (надходить у продаж під товарним знаком Herceptin®) є рекомбінантним гуманізованим моноклональним антитілом до HER2, яке застосовують для лікування метастатичного раку молочної залози, що характеризується надекспресією НЕR2/ампліфікацією гена HER2. Доклінічні дослідження продемонстрували, що антитіло володіє протипухлинною активністю in vivo і in vitro. Крім того, на мишачих моделях виявлена адитивна або підвищена в результаті синергізму протипухлинна активність трастузумабу при його застосуванні у поєднанні з різними протипухлинними агентами. У клінічних дослідженнях у пацієнтів, що страждають раком молочної залози, який характеризується надекспресією HER2, виявлено триваліше виживання. Згідно WO 98/45331 ефективність антитіла до VEGF відносно попередження або лікування захворювання можна підвищувати шляхом введення антитіла періодично або у поєднанні з іншим агентом, який володіє ефективністю відносно таких станів, наприклад, з антитілом, яке володіє здатністю зв'язуватися з рецептором HER2. У WO 2005/012531 описані антитіла, які можна об'єднувати з антитілом до VEGF (наприклад, Avastin®) і/або антитілами до ERBB (наприклад, Herceptin®), для лікування колоректального раку, метастатичного раку молочної залози і раку нирки. Згідно WO 2005/063816 антитіла до VEGF можна об'єднувати з антитілами до ERBB для лікування метастатичного раку молочної залози. У WO 2005/00090 і WO 2003/077841 описана також комбінація антитіл до VEGF і антитіл до ЕrbВ2 для лікування пухлин. Практикуючі онкологи сходяться на думці, що відсутність успіху в лікуванні раку не обов'язково пов'язана із зростанням первинної пухлини, з якою, як правило, можна боротися за допомогою хірургічного втручання, а швидше з метастатичним розповсюдженням в інші органи. Регрес первинних пухлин, що досягається за допомогою різних цитотоксичних лікарських засобів, не завжди є показником антиметастатичної активності per se. Навпаки, виявлений підвищений рівень метастазування у відповідь на застосування деяких протиракових лікарських засобів (Geldof А. А. і ін., Anticancer Res. 8, 1988, cc. 1335-1339; Murphy S. В., J. Clin. Oncol.11, 1993, cc. 199-201; і De Larco J. E. і ін., Cancer Res. 61, 2001, cc. 2857-2861). Очевидно, що існує потреба в розробці лікарських терапій, мішенню яких є не тільки первинна пухлина, але які володіють також властистивістю пригнічувати метастази. Дійсний винахід відноситься до застосування антитіла до HER2 і антитіл до VEGF для приготування лікарського засобу, призначеного для лікування раку молочної залози у пацієнта, несприйнятливого до попередньої терапії з використанням антитіла до VEGF, яке передбачає введення паці 5 95797 6 єнтові в терапевтично ефективній кількості антитінесприйнятливого до попередньої терапії з викола до HER2 і антитіл до VEGF. ристанням антитіла до VEGF, яка полягає в тому, Переважним варіантом здійснення винаходу є що пацієнтові вводять в ефективних кількостях застосування трастузумаба і бевацизумаба для антитіло до VEGF і антитіла до HER2, при цьому приготування лікарського засобу, призначеного сумісне введення антитіла до VEGF і антитіл до для лікування раку молочної залози, який характеHER2 призводить до статистично достовірного і ризується надекспресією білка рецептора HER2 у клінічно значущого поліпшення стану пацієнта, пацієнта, несприйнятливого до попередньої терапідданого лікуванню з позицій тривалості життя, пії з використанням антитіла до VEGF, такого як тривалості життя до прогресу захворювання, рівня бевацизумаб, яке передбачає введення пацієнтові відповіді або тривалості відповіді. в терапевтично ефективній кількості трастузумабу Дійсний винахід відноситься також до способу і бевацизумабу. зменшення метастазів у пацієнта, що страждає Винахід відноситься також до способу лікуванраком молочної залози, несприйнятливого до поня раку молочної залози у пацієнта, несприйнятпередньої терапії з використанням антитіла до ливого до попередньої терапії з використанням VEGF, яка полягає в тому, що пацієнтові вводять в антитіла до VEGF, що полягає в тому, що пацієнефективних кількостях антитіло до VEGF і антитіла тові вводять в терапевтично ефективній кількості до HER2, при цьому сумісне введення антитіла до антитіло до HER2, продовжуючи при цьому лікуVEGF і антитіл до HER2 ефективно зменшує мевання з використанням антитіла до VEGF. тастази. Винахід відноситься також до способу лікуванВинахід відноситься також до способу лікування раку молочної залози, . який характеризується ня групи пацієнтів, що страждають раком молочної надекспресією білка рецептора HER2, у пацієнта, залози і несприйнятливих до попередньої терапії з несприйнятливого до попередньої терапії з виковикористанням антитіла до VEGF, яка полягає в ристанням антитіла до VEGF, що полягає в тому, тому, що пацієнтам вводять в ефективних кількосщо пацієнтові вводять в терапевтично ефективній тях антитіло до VEGF і антитіла до HER2, при кількості трастузумаб, продовжуючи при цьому цьому сумісне введення антитіла до VEGF і антилікування з використанням бевацизумабу. тіл до HER2 ефективно зменшує метастази у групи Винахід відноситься також до способу подовпацієнтів. ження тривалості життя пацієнта, що страждає Винахід відноситься до виробу, що являє сораком молочної залози, несприйнятливого до побою контейнер, в який входить композиція, що передньої терапії з використанням антитіла до містить антитіло до VEGF, і листівка-вкладиш в VEGF, яка полягає в тому, що пацієнтові вводять в упаковці з інструкцією щодо застосування компоефективних кількостях антитіло до VEGF і антитіла зиції для введення пацієнтові, що страждає раком до HER2, при цьому сумісне введення антитіла до молочної залози, несприйнятливому до попередVEGF і антитіл до HER2 ефективно підвищує триньої терапії з використанням антитіла до VEGF, валість життя. антитіла до VEGF і антитіл до HER2. Винахід відноситься також до способу подовВинахід відноситься до виробу, що являє соження тривалості життя до прогресу захворювання бою контейнер, в який входить композиція, що у пацієнта, що страждає раком молочної залози, містить антитіло до HER2, і листівка-вкладиш в несприйнятливого до попередньої терапії з викоупаковці з інструкцією щодо застосування компористанням антитіла до VEGF, яка полягає в тому, зиції для введення пацієнтові, що страждає раком що пацієнтові вводять в ефективних кількостях молочної залози, несприйнятливому до попередантитіло до VEGF і антитіла до HER2, при цьому ньої терапії з використанням антитіла до VEGF, сумісне введення антитіла до VEGF і антитіл до антитіла до HER2 і антитіл до VEGF. HER2 ефективно підвищує тривалість життя до Винахід відноситься також до композиції, що прогресу захворювання. містить антитіло до HER2 і антитіло до VEGF, яку Винахід відноситься також до способу лікуванможна застосовувати для лікування раку молочної ня групи пацієнтів, що страждають раком молочної залози у пацієнта, несприйнятливого до попередзалози і несприйнятливих до попередньої терапії з ньої терапії з використанням антитіла до VEGF. використанням антитіла до VEGF, яка полягає в Переважно антитілом до HER2 є трастузумаб. тому, що пацієнтам вводять в ефективних кількосПереважно також антитілом до VEGF є бевацизутях антитіло до VEGF і антитіла до HER2, при маб. цьому сумісне введення антитіла до VEGF і антиНа кресленнях показано: тіл до HER2 ефективно підвищує рівень відповіді на фіг. 1 - протипухлинна активність сумісної (рівень чутливості) групи пацієнтів. обробки трастузумабом і бевацизумабом відносно Винахід відноситься також до способу підвизростання пухлини після того, як лікування беващення тривалості відповіді у пацієнта, що стражцизумабом не дало результату. На осі у представ3 дає раком молочної залози, несприйнятливого до лені середні значення об'єму пухлин (мм ); на осі x попередньої терапії з використанням антитіла до представлена кількість днів після ін'єкції пухлинних VEGF, яка полягає в тому, що пацієнтові вводять в клітин. Представлені дані, отримані при обробці ефективних кількостях антитіло до VEGF і антитіла наповнювачем (кола), трастузумабом в ударній до HER2, при цьому сумісне введення антитіла до дозі 30 мг/кг і підтримуючій дозі 15 мг/кг (квадрати), VEGF і антитіл до HER2 ефективно підвищує трибевацизумабом в дозі 5 мг/кг до дня 55, коли в валість відповіді. схему лікування був включений також трастузумаб Винахід відноситься також до способу лікуванв дозі 15 мг/кг (трикутники); ня пацієнта, що страждає раком молочної залози, 7 95797 8 на фіг. 2 - ефективність сумісної обробки трасздійснення винаходу антитіло до HER2 є трастутузумабом і бевацизумабом відносно метастазів зумабом. Трастузумаб і методи його отримання легені. Середні значення рівня людської послідовописані в ЕР 0590058. ності ДНК Alu (нг/мл), кількісно оцінені в тканині Мається на увазі, що поняття "надекспресія" легені за допомогою ПЦР в реальному часі і предбілка рецептора HER2 відноситься до аномальноставлені на осі у. го рівня експресії білка рецептора HER2 в клітині, . Поняття "VEGF" в контексті винаходу відноотриманій з пухлини конкретної тканини або оргаситься до фактора росту судинних ендотеліальних ну пацієнта, щодо рівня експресії в здоровій клітині клітин (Swiss-Prot № Ρ 15692), його отриманих в з цієї тканини або органу. Пацієнтів, які страждарезультаті альтернативного сплайсингу форм ють раком, що характеризується надекспресією (див., наприклад, Leung D.W. і ін., Science, 246, рецептора HER2, можна виявляти за допомогою 1989, сс. 1306-1309; і Houck К. А. і ін., Моl. стандартних аналізів, відомих в даній області. ПеEndocrin. 5, 1991, сс. 1806-1814) і активних фрагреважно надекспресію оцінюють у фіксованих кліментів, переважно N-кінцевих фрагментів. тинах заморожених або занурених в парафін зріПоняття "Антитіло до VEGF" в контексті дійсзах тканини за допомогою імуногістохімічного (ІГХ) ного винаходу відноситься до антитіла, яке спевиявлення. За допомогою гістологічного фарбуцифічно зв'язується з VEGF. Зв'язування перевавання можна виявляти локалізацію цільового білка жного гуманізованого антитіла до VEGF або і можна оцінювати рівень його експресії в пухлині варіанту антитіла до VEGF, пропонованого у винаяк якісно, так і напівкількісно. Такі ІГХ-аналізи віході, з людським VEGF характеризується значендомі в даній області і включають аналіз в клінічноням Kd, що складає не більше ніж приблизно 1 x му дослідженні (Clinical Trial Assay (СТА)), тест -8 10 Μ і переважно не більше ніж приблизно 5 x 10 фірми LabCorp 4D5, що надходить у продаж, і тест 9 М. Переважне антитіло до VEGF є моноклональфірми DAKO HercepTest®(DAKO, Карпінтерія, шт. ним антитілом, яке зв'язується з тим самим епітоКаліфорнію), що надходить у продаж. Останній пом, що і рекомбінантне гуманізоване моноклонааналіз заснований на оцінці ступеня специфічного льне антитіло до VEGF, створене згідно методу, фарбування клітин, що характеризується балами описаного у Presta L. G. і ін., Cancer Res. 57, 1997, від 0 до 3+ (0 означає нормальний рівень експресс. 4593-4599. Переважним антитілом є бевацизусії, 3+ позначає найбільш високу позитивну ексмаб. Антитіла до VEGF і методи їх отримання опипресію), для ідентифікації раку, що характеризусані, наприклад, в US 6054297, US 2003/0190317, ється надекспресією білка HER2 (див. повну US 6632926, US 6884879 і US 2005/0112126. надану інформацію про Herceptin® (трастузумаб), Бевацизумаб містить каркасні ділянки мутантів вересень 1998p., фірма Genentech Inc., Санлюдського IgG1 і антигензвязуючі гіперваріабельні Франциско, шт. Каліфорнія). Так, для пацієнтів, рак ділянки мишачого моноклонального антитіла до яких характеризується надекспресією білка HER2 hVEGF, яке блокує зв'язування людського VEGF з на рівні 1+, 2+ або 3+, переважно 2+ або 3+, перейого рецепторами. Приблизно 93 % амінокислотважніше 3+, повинно надавати сприятливу дію ної послідовності бевацизумабу, що включає везастосування способів лікування, пропонованих в лику частину каркасних ділянок, виведено з люддійсному винаході. ського IgG1, a приблизно 7 % послідовностей Поняття "хвороба, що являє собою рак молочвиведено з мишачого антитіла А4.6.1. Бевацизуної залози" ("рак молочної залози") відноситься до маб має молекулярну масу приблизно 149000 Да і неконтрольованого зростання аномальних клітин є глікозильованим. Бевацизумаб і метод його молочної залози. Воно включає карциному in situ, отримання описані в ЕР 1325932. що відноситься до протоки, інвазивну карциному in HER2 є рецептором фактору росту, що має situ, що відноситься до протоки, карциному частомолекулярну масу 185 кДа, який позначають також чок in situ, інвазивну карциному часточок, медуляяк neu і c-erbB-2 (Slamon D.J. і ін., рну карциному, хворобу Педжета (рак соска) і меScience235,1987, сс. 177-182; Swiss-Prot P04626), тастатичний рак молочної залози. функція якого пов'язана з неопластичною трансПоняття "несприйнятливість до попередньої формацією клітин раку молочної залози людини. терапії з використанням антитіла до VEGF" або Надекспресія цього білка виявлена у 20-30 % паці"несприйнятливість до лікування" в контексті дійсєнтів, що страждають раком молочної залози, що ного опису відноситься до пацієнтів, що страждакорелює з регіональним прогресом захворювання, ють раком, у яких відсутня реакція на попередню підвищеною імовірністю рецидиву пухлини і зментерапію з використанням антитіла до VEGF ("не шеною тривалістю життя пацієнтів. У 30-40 % пареспонденти") або які спочатку реагують на попецієнтів, що страждають раком шлунку, ендометрія, редню терапію, але у яких терапевтична відповідь слинних залоз, недрібноклітинним раком легені, не зберігається (позначені як "пацієнти на стадії раком підшлункової залози, яєчника, перитонеарецидиву"). Переважне поняття "несприйнятлильним раком, раком передміхурової залози або вість до попередньої терапії з використанням анколоректальним раком, також може мати місце титіла до VEGF" відноситься до пацієнтів на стадії надекспресія цього білка. Антитіла до HER2 і мерецидиву. Відсутність успіху лікування (відповідно тоди їх отримання описані, наприклад, в US відповідь (RE) і відсутність відповіді (NR)) оціню6054297,WO 89/06692,US6953842, US 6949245, ють на основі медичного висновку лікаря-куратора US 6399063, US 6165464, US 6054297, US за наслідками клінічних і лабораторних дослі5772997, WO 2003/087131, WO 01/00245, WO джень, які, як правило, застосовують в даній обла01/00238, WO 00/69460, WO 00/52054, WO сті для оцінки дії лікування на пацієнта. Такі дані 99/31140 і WO98/17797. У переважному варіанті можна отримувати, наприклад, на основі клінічного 9 95797 10 обстеження, цитологічних і гістологічних методів, 2000, cc. 205-216) класифікують залежно від збіендоскопії і лапароскопії, ультразвукового обстельшення об'єму або регресу пухлин (наприклад, за ження, КТ (комп'ютерна томографія), ПЕТ (позитданими КТ) за 4 рівнями: повна відповідь (CR) або ронна емісійна томографія) і ЯМР-томографії, ренчасткова відповідь (PR), стабільний стан хвороби тгеноскопії грудної клітини і мамографії, і на основі (SD) і прогресуючий стан хвороби (PD) (див. табоцінки концентрації пухлинних маркерів, таких як лицю 1). Крім того, Європейською організацією по ΚΕΑ (карциноембріональний антиген), Cyfra, дослідженню і лікуванню раку (European CA15-3, інтерлейкін 8 і розчинний HER2. У цьому Organization for Research and Treatment of Cancer контексті поняття "несприйнятливість до лікуван(EORTC)) запропонована класифікація за 4 привеня" відноситься до відсутності клінічного поліпденими нижче рівнями залежно від метаболізму шення. Альтернативно цьому можна використовупухлин, що оцінюють за допомогою позитронної 18 вати критерії RECIST (критерії оцінки відповіді емісійної томографії з використанням 2-[ F]-фторщільних пухлин) для визначення відповіді пухлини 2-дезоксиглюкози (ФДГ-ПЕТ) (Young Η. і ін., Eur. J. (Therasse P. і ін., J. Nat. Cancer Institute 92, 2000, Cancer 35, 1999, cc. 1773-1782 і Kellof G. J. і ін., cc. 205-216). У цьому контексті поняття "несприйClin. Cancer Res.11, 2005, cc. 2785-2808): повна нятливість до лікування" відноситься або до "неметаболічна відповідь (CMR) або часткова метаповної відповіді/стабільного захворювання" або до болічна відповідь (PMR), стабільний метаболічний "прогресуючого захворювання". стан хвороби (SMD) і прогресуючий метаболічний Згідно цих RECIST-критеріїв відповідь щільних стан хвороби (PMD) (див. таблицю 2). пухлин (Therasse P. і ін., J. Nat. Cancer Institute 92, 11 Таким чином, переважно "Відповідь (RE)» і "Відсутність відповіді (NR)» згідно дійсного винаходу визначають на основі даних, отриманих шляхом комбінації комп'ютерної томографії (КТ) і позитронної емісійної томографії з використанням 218 [ F]-фтор-2-дезоксиглюкози (ФДГ-ПЕТ) (Kellof G.J. і ін., Clin. Cancer Res.11, 2005, cc. 2785-2808 і Young Η. і ін., Eur. J. Cane. 35, 1999, cc. 17731782), з використанням описаних вище і RECIST-, і ФДГ-ПЕТ-критеріїв. Таким чином, наявність Відповіді (RE) і Відсутність відповіді (NR) згідно дійсного винаходу визначають переважно таким чином: Відповідь (RE): CR або PR визначають за допомогою KT-RECIST-критерія (таблиця 1) і одночасно визначають CMR або PMR за допомогою ФДГ-ПЕТ (таблиця 2). Таким чином, Відповідь (RE) означає відповідність одному з чотирьох варіантів об'єднаної КТ- або ПЕТ-оцінки: CR і CMR, PR і PMR, CR і PMR, і PR і CMR. Відсутність відповіді (NR): SD або PD визначають на основі KT-RECIST-критерія (таблиця 1) і одночасно визначають SMD або PMD за допомогою ФДГ-ПЕТ (таблиця 2). Таким чином, Відсутність відповіді (NR) означає відповідність одному з чотирьох варіантів об'єднаної КТ- або ПЕТ- оцінки: SD і SMD, SD і PMD, PD і SMD, і PD і PMD. Як правило, відповідь визначають приблизно через 3-8 тижнів, переважно приблизно через 6 тижнів, після початку лікування. Цю Відповідь визначають, "як правило" повторно, з інтервалами 48 тижнів, переважно 6-8 тижнів. Коли при першому визначенні ідентифікована виражена відповідь (RE), то рецидив (що означає Відсутність відповіді (RE) після першого визначення) може бути виявлений не раніше, чим при визначенні другої відповіді. У цьому контексті поняття "пацієнт, несприйнятливий до попередньої терапії з використанням антитіла до VEGF" відноситься до пацієнта, у якого або перша відповідь класифікована як відсутність відповіді (NR), що дозволяє віднести його до "не респондентів", або перша відповідь класифікована як "Відповідь" (RE), а друга або подальші відповіді класифіковані як "Відсутність відповіді" (NR), що дозволяє віднести його до "Пацієнта на стадії рецидиву". Поняття "метастаз" згідно дійсного винаходу відноситься до трансмісії ракових клітин від первинної пухлини ще в одну або декілька областей в організмі пацієнта, що призводить до утворення вторинних пухлин. Пухлину, що утворилася з клітин, що розповсюдилися, позначають як "метастатична пухлина" або "метастаз". Метастатична пухлина містить клітини, подібні до клітин початкової (первинної) пухлини. Методи визначення, чи є пухлина метастазуючою, відомі в даній області і включають тести з використанням маркерів пухлин, сканування кісткової тканини, рентгеноскопію грудної клітки, комп'ютерну томографію (КТ), комп'ютерну трансаксіальну томографію (CAT), ЯМРтомографію, позитронну емісійну томографію (ПЕТ), однофотонну емісійну комп'ютерну томографію (SPECT), флуоресцентну візуалізацію (FI) і біолюмінісцентну візуалізацію (ВLI) і оцінку марке 95797 12 рів пухлин (див., наприклад, Helms Μ. W. і ін., Contributions to microbiology 13, 2006, cc. 209-231 і Pantel K. і ін., J. Nat. Cancer Inst. 91, 1999, cc. 11131124). У контексті дійсного опису поняття "пацієнт" переважно відноситься до людини, що потребує лікування раку або передракового стану або пошкодження. Проте поняття "пацієнт" відноситься також серед іншого до тварин окрім людини, переважно ссавців, таких як собаки, кішки, коні, корови, свині, вівці і примати окрім людини, які потребують лікування. Поняття "група" відноситься до групи пацієнтів, а також до підгрупи пацієнтів. Поняття «листівка-вкладиш в упаковці" відноситься до інструкцій, які зазвичай входять в упаковки терапевтичних продуктів, що надходять у продаж, вони можуть включати інформацію про показання, застосування, дозу, шлях введення, протипоказання і/або запобіжні засоби, що стосуються застосування таких терапевтичних продуктів. Раком може бути, наприклад, рак легені, недрібноклітинний рак легені (NSCL), альвеолярноклітинний рак легені, рак кісткової тканини, рак підшлункової залози, рак шкіри, рак голови і шиї, шкірна або внутрішньоочна меланома, рак матки, рак яєчника, ректальний рак, рак анальної області, рак шлунку, гастральний рак, рак ободової кишки, рак молочної залози, карцинома маткових труб, карцинома ендометрія, карцинома шийки матки, карцинома піхви, карцинома вульви, хвороба Ходжкіна, рак стравоходу, рак тонкого кишечника, рак ендокринної системи, рак щитовидної залози, рак паращитовидної залози, рак наднирників, саркома м'яких тканин, рак сечовипускального каналу, рак пеніса, рак передміхурової залози, рак сечового міхура, рак нирки або сечовипускального каналу, печінковоклітинна карцинома, карцинома ниркової миски, мезотеліома, печінковоклітинний рак, рак жовчного міхура, хронічний або гострий лейкоз, лімфоцитарна лімфома, неоплазма центральної нервової системи (ЦНС), пухлини спинномозкових хребців, гліома стовбура головного мозку, мультиформна гліома, астроцитоми, невриноми, епендимоми, медулобластоми, менінгіоми, плоскоклітинні карциноми, аденоми гіпофіза, включаючи стійкі варіанти будь-якого з перерахованих вище видів раку або комбінацію одного або декількох вищеперерахованих видів раку. Передраковий стан або пошкодження включає, наприклад, групу таких станів або пошкоджень, як оральна лейкоплакія, старечий кератоз, сонячний кератоз), передракові поліпи ободової або прямої кишки, гастральну епітеліальну дисплазію, аденоматозну дисплазію, спадковий неполіпозний раковий синдром ободової кишки (HNPCC), виразку стравоходу Баррета, дисплазію сечового міхура і передракові стани шийки матки. У переважному варіанті здійснення винаходу рак, що підлягає лікуванню є рак молочної залози. Крім того, в переважному варіанті здійснення винаходу рак характеризується надекспресією білка рецептора HER2. Винахід відноситься також до способу лікування раку молочної залози у пацієнта, несприйнят 13 95797 14 ливого до попередньої терапії з використанням зотоцин, триетиленмеламін (ТЕМ), мітоміцин С і антитіла до VEGF, що полягає в тому, що пацієнт.п.; антиметаболіти, такі як метотрексат (МТХ), тові вводять в терапевтично ефективній кількості етопозид (VP16; наприклад, Vepesid®), 6антитіло до HER2, зберігаючи при цьому терапію з меркаптопурин (6МР), 6-тіогуанін (6TG), цитабін використанням антитіла до VEGF. (ARA-C), 5-фторурацил (5-FU), капецитабін (наПоняття "лікування" в контексті дійсного опису, приклад, Xeloda®), декарбазин (DTIC) і т.п.; антиякщо не вказане інше, означає реверсію, ослаббіотики, такі як актиноміцин D, доксорубіцин (DXR; лення, інгібування розвитку або попередження, наприклад, Adriamycin®), даунорубіцин (дауноміабо часткове, або повне, росту пухлин, метастазів цин), блеоміцин, мітраміцин і т.п.; алкалоїди, такі пухлин або інших клітин, що викликають рак або алкалоїди барвінку, такі як вінкрістин (VCR), вінбнеопластичних клітин у пацієнта. Поняття "лікуластин і т.п.; і інші протипухлинні агенти, такі як вання" в контексті дійсного опису, якщо не вказане паклітаксел (наприклад, Тахої®) і похідні паклітакінше, відноситься до акту лікування. села, цитостатичні агенти, глюкокортикоїди, такі як Поняття "спосіб лікування" або його еквівалендексаметазон (DEX; наприклад, Decadron®), корти, стосовно, наприклад, раку, відноситься до протикостероїди, такі як преднізон, інгібітори нуклеоцедури або послідовності дій, направлених на. зидних ферментів, такі як гідроксисечовина, ферзниження або елімінацію кількості ракових клітин в менти, що розщеплюють (виснажують) організмі пацієнта або полегшення симптомів раку. амінокислоти, такі як аспарагиназа, лейковорин і "Спосіб лікування" раку або іншого проліферативінші похідні фолієвої кислоти і аналогічні різноманого порушення не обов'язково означає, що ракові нітні протипухлинні агенти. Як додаткові агенти клітини або інше порушення повинні бути фактичможна використовувати також: арніфостин (наприно еліміновані, що кількість клітин або міра іншого клад, Ethyol®), дактиноміцин, мехлоретамін (гірчипорушення повинні бути фактично понижені, або чний газ), стрептозоцин, циклофосфамід, ломусщо симптоми раку або іншого порушення повинні тин (CCNU), доксорубіцин ліпо (наприклад, бути фактично ослаблені. Часто спосіб лікування Doxil®), гемцитабін (наприклад, Gemzar®), даунораку можна здійснювати навіть при невеликій йморубіцин ліпо (наприклад, Daunoxome®), прокарбавірності успіху, але, якщо при цьому з урахуванням зин, мітоміцин, доцетаксел (наприклад, історії хвороби або очікуваної тривалості життя Taxotere®), альдслеукин, карбоплатин, оксаліплапацієнта, однак, можна чекати сприятливої дії літин, кладрибін, камптотецин, СРТ 11 (іринотекан), кування. 10-гідрокси-7-етилкампотецин (SN38), флоксуріПоняття "терапевтично ефективна кількість" дин, флударабін, іфосфамід, ідарубіцин, месна, або "ефективна кількість" означає кількість пропоінтерферон бета, інтерферон альфа, мітоксантнованої у винаході сполуки або комбінації, яка порон, топотекан, леупролід, мегестрол, мелфалан, винна викликати біологічну або медичну відповідь меркаптопурин, плікаміцин, мітотан, пегаспаргаз, тканини, системи, тварини або людини, яка вибипентостатин, піпоброман, плікаміцин, томоксифен, рається дослідником, ветеринаром, доктором метеніпозид, тестолактон, тіогуанін, тіотепу, урацил дицини або іншим клініцистом. мустард, вінорелбін, хлорамбуцил. Винахід відноситься також до застосування У контексті дійсного опису у поєднанні з антиантитіла до HER2 і антитіл до VEGF для приготутілом до VEGF плюс антитілом до HER2 можна вання лікарського засобу, призначеного для лікузастосовувати антигормональний агент. У контексвання раку молочної залози у пацієнта, несприйті дійсного опису поняття "антигормональний нятливого до попередньої терапії з використанням агент" включає органічні або пептидні сполуки, що антитіла до VEGF, що передбачає введення пацізустрічаються в природних умовах або синтетичні, єнтові в терапевтично ефективній кількості антитіякі володіють здатністю регулювати або інгібувати ла до HER2, зберігаючи при цьому терапію з викогормональну дію на пухлини. До антигормональристанням антитіла до VEGF. Антитіла можна них агентів відносяться, наприклад: антагоністи вводити окремо або одночасно. стероїдного рецептора, антиестрогени, такі як таПоняття "спосіб приготування лікарського замоксифен, ралоксифен, 4(5) -імідазоли, що інгібусобу" відноситься до приготування лікарського ють ароматазу, інші інгібітори ароматази, 42засобу, призначеного для застосування при покагідрокситамоксифен, триоксифен, кеоксифен, LY заннях, вказаних в дійсному описі, і, зокрема, при117018, онапристон і тореміфен (наприклад, значеного для лікування пухлин, метастазів пухFareston®); антиандрогени, такі як флутамід, нілулин або раку в цілому. Поняття відноситься до тамід, бікалутамід, леупролід і госерелін; і фармаформату формули винаходу так званого "Швейцевтично прийнятні солі, кислоти або похідні будьцарського типу" відносно вказаних показань. якого з вищеперерахованих агентів; агоністи і/або У контексті дійсного винаходу у поєднанні з антагоністи глікопротеїнових гормонів, таких як антитілом до VEGF плюс антитілом до HER2 можфолікулостимулюючий гормон (ФСК), тіреотропний на застосовувати також інші цитотоксичні, хіміотегормон (ТГ) і лютеїнізуючий гормон (ЛГ) і ЛГРФ рапевтичні або протиракові агенти або сполуки, які (рилізинг-фактор лютеїнізуючого гормону); і агопідсилюють ефективність вказаних агентів. Такі ніст ЛГРФ госереліну ацетат, що надходить у проагенти є, наприклад: алкілуючими агентами або даж як Zoladex® (фірма AstraZeneca); і антагоніст агентами з алкілуючою дією, такі як циклофосфаЛГРФ D-аланінамін N-ацетил-3-(2-нафталеніл)-Dмід (СТХ; наприклад Cytoxan®), хлорамбуцил аланіл-4-хлор-D-фенілаланіл-3-(3-піридиніл)-D(CHL; наприклад, Leukeran®), цисплатин (CISP; аланіл-L-серіл-N6-(3-піридинілкарбоніл)-L-лізилнаприклад, Platinol®), бусульфан (наприклад, N6-(3-піридинілкарбоніл)-D-лізил-L-лейцил-N6-(1Myleran®), мелфалан, кармустин (BCNU), стрептометилетил)-L-лізил-L-проліна (наприклад, Antide®, 15 95797 16 фірма Ares-Serono); антагоніст ЛГРФ ганіреліксу в контексті дійсного винаходу, вибирають з групи, ацетат; стероїдні антиадрогени ципротерону ацеяка включає (але не обмежена тільки ними), радій, тат (СРА) і мегестролу ацетат, що надходить у цезій-137, іридій-192, америцій-241, золото-198, продаж як Megace® (фірма Bristol-Myers кобальт-57, мідь-67, технецій-99, йод-123, йод-131 Oncology); нестероїдний антиандроген флутамід і індій-111. Коли інгібітор кіназного EGFR, що про(2-метил-N-[4, 20-нітро-3-(трифторметил) фенілппонується в дійсному винаході, є антитілом, то ропанамід), що надходить у продаж як Eulexin® воно може бути також антитілом, що мітиться вка(фірма Schering Corp.); не стероїдний антиандрозаними радіоактивними ізотопами. ген нілутамід (5,5-диметил-3-[4-нітро-3Променева терапія є стандартним лікуванням, (трифторметил-4'-нітрофеніл)-4,4що застосовується для контролю нерезектабельдиметилімідазолідиндіон); і антагоністи інших нених або неоперабельних пухлин і/або пухлин, що обов'язкових рецепторів, наприклад, антагоністи метастазують. Були отримані покращені результаRAR (рецептор ретиноєвої кислоти), RXR (ретиоїти при сумісному застосуванні променевої терапії і дний Х-рецептор), TR (тиреоїдини рецептор), VDR хіміотерапії. Принципом, покладеним в основу (рецептор вітаміну-D) і тому подібне. променевої терапії, є те, що висока доза випроміЗастосування цитотоксичних і інших протиранювання, що досягає області-мішені, може призкових агентів, описаних вище, в хіміотерапевтичводити до загибелі репродуктивних клітин в пухних режимах, як правило, добре відомо в області лині і в здорових тканинах. Використовувану дозу терапії раку, і їх застосування передбачає викорилікування, як правило, позначають в поняттях растання таких самих умов моніторингу толерантнодіаційної поглиненої дози (Гр), часу і сті і ефективності і контролю шляхів введення і доз фракціонування, і її повинен ретельно підбиз певним регулюванням. Наприклад, фактичні дорати онколог. Доза випромінювання, яку отримує зи цитотоксичних агентів можуть варіюватися запацієнт, повинна залежати від різних концентралежно від реакції клітин пацієнта в культурі, яку цій, але двома більш важливими факторами є ловизначають в культурі за допомогою гістологічних калізація пухлини відносно інших структур або методів. Як правило, дозу можна знижувати в поорганів, що мають вирішальне значення для оргарівнянні з кількістю, вживаною у відсутності додатнізму, і ступінь розповсюдження пухлини. Звичайкових інших агентів. ний курс лікування пацієнта, що піддається промеТипові дози ефективного цитотоксичного агенневій терапії, повинен відповідати режиму та можуть знаходитися в діапазонах, рекомендолікування тривалістю в 1-6 тижнів, при цьому загаваних виробником, і, якщо це встановлено за відльна доза, що вводиться, при щоденній обробці повідями in vitro або за відповідями створених на складає від 10 до 80 Гр, 1,8-2,0 Гр в день, 5 днів в тваринах моделей, можуть містити понижені прибтиждень. У переважному варіанті здійснення винализно на порядок концентрацію або кількість. Так, ходу при обробці пухлин хворого комбінацією, фактична доза повинна залежати від рекомендапропонованою у винаході, у поєднанні з променецій лікаря-куратора стану пацієнта і ефективності вою терапією, виявлений синергізм. Іншими слотерапевтичного методу, оціненої in vitro на основі вами, інгібування росту пухлини за допомогою сприйнятливості первинних злоякісних клітин в агентів, що входять в комбінацію, пропоновану у культурі або зразку тканини, який культивують для винаході, посилюється при сумісному застосуванні гістологічних методів, або за відповідями, отримаз випромінюванням, необов'язково у поєднанні з ними на відповідних створених на тваринах модехіміотерапевтичними або протираковими лікарсьлях. кими засобами. Параметри допоміжних променеУ контексті дійсного винаходу додаткові антивих терапій описані, наприклад, в опублікованій проліферативні агенти можна застосовувати у міжнародній заявці на патент WO 99/60023. поєднанні з антитілом до VEGF плюс антитілом до Антитіла вводять пацієнтові за допомогою віHER2, такі, наприклад, як: інгібітори ферменту домих методів, шляхом внутрішньовенного ввефарнезилпротеїнтрансферази і інгібітори рецепдення у вигляді болюсної ін'єкції або шляхом безторної тирозинкінази PDGFR, включаючи сполуки, перервної інфузії протягом певного періоду часу, описані і заявлені в US 6080769; 6194438; внутрішньом'язево, внутрішньочеревно, в спинний 6258824; 6586447; 6071935; 6495564; 6150377; мозок, підшкірно, внутрішньосуставно, внутріш6596735 і 6479513 і в опублікованій міжнародній ньосиновіально або підоболонково. Переважним є заявці на патент WO 01/40217. внутрішньовенне або підшкірне введення антитіл. У контексті дійсного винаходу можна викорисКількість антитіла до VEGF і антитіл до HER2, товувати іонізуюче випромінювання в ефективній що вводиться, і режим введення повинні залежати дозі і/або застосовувати радіофармацевтичне лівід типу пацієнта, що піддається лікуванню (викування у поєднанні із застосуванням антитіла до гляд, стать, вік, вага і так далі) і його стану і серйоVEGF плюс антитіла до HER2. Джерело випромізності або стану захворювання, що піддається нювання може бути або зовнішнім, або внутрішнім лікуванню. по відношенню до пацієнта, що піддається лікуДози, в яких застосовують антитіла, запропованню. Коли джерело є зовнішнім по відношенню новані у винаході, складають приблизно від 1 до пацієнта, таку терапію відносять до зовнішньої мкг/кг до 50 мг/кг (наприклад, 0,1-20 мг/кг) антитіла дистанційної променевої терапії (EBRT). Коли в одне або декілька введень або їх вводять шляджерело випромінювання є внутрішнім по віднохом безперервної інфузії. Звичайна добова доза шенню до пацієнта, таке лікування відносять до може знаходитися в діапазоні від приблизно 1 близькофокусної променевої терапії (брахітерапія, мкг/кг до приблизно 100 мг/кг. У переважному ваВТ). Радіоактивні атоми, які можна застосовувати ріанті здійснення винаходу антитіла вводять кожні 17 95797 18 2-3 тижні в дозі, що складає від приблизно 1 мг/кг 79, 1999, 707-717), що характеризується надекспдо приблизно 15 мг/кг. Переважна доза бевацизуресією, Пухлинні клітини згідно загальноприйнямабу складає 5 мг/кг один раз кожні 14 днів у витому методу культивували в середовищі DMEM гляді внутрішньовенної (IV) інфузії до виявлення (фірма РАА Laboratories, Австрія), доповненому прогресу захворювання. Для трастузумабу пере10 % фетальною бичачою сироваткою (РАА) і 2мМ важною дозою є ударна доза 4 мг/кг, яку вводять L-глутаміном (фірма Gibco) при 37 °C в насиченій протягом 90-хвилинного періоду і подальші щотиводою атмосфері з 5 % СО2. Пасажі культури здійжневі інфузії по 2 мг/кг, які вводять протягом 30снювали двічі в тиждень з розщеплюванням трипхвилинного періоду. сином/ЕДТК 1 (РАА). Клітинний пасаж Р6 викорисДійсний винахід відноситься також до набору, товували для досліду in vivo. що містить антитіло до VEGF і листівку-вкладиш в Тварини упаковці з інструкцією по застосуванню композиції Миші з важким комбінованим імунодефіцитом для введення пацієнтові, що страждає раком мо(SCID) з вродженою відсутністю природних клітинлочної залози, несприйнятливому до попередньої кілерів (С.В.-17); вік 10-12 тижнів; вага тіла " 18-20 терапії з використанням антитіла до VEGF, антитіг (фірма Charles River, Сулзфельд, Німеччина) ла до VEGF і антитіл до HER2. У переважному утримували в специфічних безпатогенних умовах з варіанті здійснення винаходу контейнери, що входобовим циклом 12 год. світла/12 год. темряви дять до складу набору містять також фармацевтизгідно міжнародним вказівкам (GV-Solas; Felasa; чно прийнятний носій. У набір може входити також TIERSCHG). Після отримання тварин поміщали у стерильний розчинник, який переважно зберігають відсік для карантину віварію на один тиждень для в індивідуальному додатковому контейнері. У натого, щоб вони могли звикнути до нових умов, і бір може входити також листівка-вкладиш в упакодля обстеження. На регулярній основі здійснювали вці, що містить надруковані інструкції, що реглапостійний моніторинг стану здоров'я. Тварини маментують застосування сумісного лікування як ли вільний доступ до корму (Alltromin) і води (підметоду лікування раку молочної залози. кисленої до значення рН 2,5-3). Дійсний винахід відноситься також до фармаДосліди по інгібуванню зростання пухлини in цевтичної композиції, призначеної зокрема для vivo лікування раку молочної залози, несприйнятливого Збирали пухлинні клітини (трипсин-ЕДТК) з кудо попередньої терапії з використанням антитіла льтуральних колб (Greiner TriFlask) і переносили в до VEGF, яка містить антитіло до HER2 і антитіло 50 мл культурального середовища, одноразово до VEGF. Така композиція необов'язково містить промивали і ресуспендували в ЗФР. Після додатфармацевтично прийнятні носії і/або ексципієнти. кової стадії промивки ЗФР і фільтрації (клітинний У переважному варіанті здійснення винаходу анфільтр; Falcon, 100 мкм) кінцевий титр клітин дотитілом до VEGF є бевацизумаб, а антитілом до водили до 0,75108 /мл. Суспензію пухлинних кліHER2 є трастузумаб. тин обережно змішували за допомогою піпетки для Нижче представлені експериментальні дані, перенесення для того, щоб уникнути агрегації кліпризначені для кращого розуміння дійсного винатин. Здійснювали анестезію за допомогою приходу, дійсний об'єм якого визначається приведестрою для інгаляції дрібних тварин типу Stephens з ною нижче формулою винаходу. Слід розуміти, що камерою для попередньої інкубації (з плексиглаконкретні методи і обговорювані результати дані су), індивідуальною наркозною маскою, придатною тільки з метою ілюстрації винаходу і жодним чином для носа миші (з силікону), і ізофлураном (фірма не направлені на його обмеження. Pharmacia-Upjohn, Німеччина) в замкнутій циркуВведення ляційній системі. За два дні до ін'єкції у тварин У дійсному дослідженні оцінювали протипухзбривали шерсть. Для ін'єкції в жирове тіло мололинну активність комбінації бевацизумабу і трастучної залози (i.f.m.p.) клітини вводили ортотопічно в зумабу (після безуспішного лікування тільки беваоб'ємі 20 мкл в жирове тіло правої передостанньої цизумабом) на моделі з використанням людського пахової молочної залози кожної анестезованої ксенотрансплантату раку молочної залози. Додатмиші. Для ортотопічної імплантації клітинну суковими завданнями дослідження була оцінка ефеспензію ін'єктували через шкіру під соском. День ктивності лікування відносно метастазів. ін'єкції пухлини відповідав дню 1 експерименту. Агенти, що вивчаються Моніторинг Трастузумаб отримували у вигляді маточного Тварин піддавали щоденному контролю, вирозчину з концентрацією 25 мг/мл в гістидині-НСІ, значаючи клінічні симптоми побічних дій. Для моальфа-альфа трегалозі (60мМ), 0,01 % полісорба, ніторингу протягом всього експерименту реєструрН 6,0 (Herceptin®). Бевацизумаб отримували у вали вагу тіла тварин двічі в тиждень і визначали вигляді маточного розчину з концентрацією 25 об'єм пухлини за допомогою кронциркуля двічі в мг/мл в Na-фосфаті, альфа-альфа трегалозі тиждень. Первинний об'єм пухлини розраховували (60мМ), 0,01 % полісорба, рН 6,0 (Avastin®). Обидзгідно протоколу NCI (Національний онкологічний ва розчини розводили відповідним чином в ЗФР інститут) (TW=1/2аb2, де а і b є розмірами довгого і для ін'єкцій. короткого діаметру пухлини в мм, Teicher В., Клітинні лінії і умови культивування Anticancer drug development guide, вид-во Humana Людську лінію клітин раку молочної залози Press 5, 1997, с. 92). Розраховані величини реєстKPL-4 отримували із злоякісної плевральної кінціврували у вигляді середнього значення і стандартки пацієнта, що страждає раком молочної залози, ного відхилення. із запальними шкірними метастазами і сімейства Обробка тварин ЕrbВ-рецепторів (Kurebayashi J, і ін., Br. J. Cancer 19 95797 20 Мишей, що несуть пухлини, довільно розділячасі. Вищі рівні людської ДНК, визначені за дополи на групи, коли об'єм пухлини досягав приблизмогою ПЦР в реальному часі, відповідають вищо3 но 100 мм (n=10 в кожній групі). Перед дослідом му рівню. метастазів. стани здоров'я тварин в кожній групі були близьРезультати кими, експеримент починали через 20 днів після Дія лікування на росту первинних пухлин ін'єкції пухлинних клітин. Тваринам в групі, обробпредставлена на фіг. 1 і в таблиці 3. Пухлини в леній наповнювачем (група 1), вводили з розрахугрупі, обробленій наповнювачем (група 1), швидко нку 10 мл/кг ЗФР внутрішньочеревно (і.р.) один раз росли, і мишей умертвляли через 38 днів після в тиждень. Трастузумаб (група 2) вводили і.р. в ін'єкції пухлинних клітин через виразки пухлин і ударній дозі 30 мг/кг, з подальшим введенням розвиток клінічних симптомів. Монотерапія з викоодин раз в тиждень дози по 15 мг/кг (підтримуюча ристанням трастузумабу (група 2) не здійснювала доза). Антитіло до VEGF бевацизумаб вводили і.р. істотної дії на об'єм пухлин, і мишей умертвляли в у дозі 5 міліграм/кг двічі в тиждень (група 3). В день 44. Обробка бевацизумабом істотно пригнідень 40 обробку групи 3 змінювали на комбіновану чувала ріст пухлин; проте у пухлин розпочиналося обробку бевацизумабом (5 міліграм/кг двічі в тижповторне зростання приблизно до 44 дня. Сумісна день і.р.) і трастузумабом (15 міліграм/кг один раз обробка бевацизумабом і трастузумабом, почата в в тиждень і.р.). день 55, призводила до повного інгібування росту Оцінка метастазів пухлин протягом часу експерименту (день 99) і Розповсюдження пухлинних клітин в легені вилікування добре переносилося. значали у тварин, яких умертвляли. Метастази Таблиця 3: Протипухлинна активність сумісної визначали згідно методу, описаному у Schneider T. обробки трастузумабом і бевацизумаб на ріст пухі ін., Clin. Exp. Metastasis 19, 2002, сс. 571-582. В лин після безуспішного лікування бевацизумабом цілому, метод полягав в наступному: вилучали (дані для фіг. 1). Представлений середній об'єм 3 тканину легені і людські послідовності Alu оцінюпухлини в мм і стандартне відхилення (С.К.О.) вали кількісно за допомогою ПЦР в реальному Таблиця 3 День Наповнювач С.К.О. Трастузумаб С.К.О. 20 23 27 30 34 37 42 44 48 51 55 58 62 65 70 73 79 83 86 90 93 97 99 118 150 209 269 348 431 31 зо 51 76 114 138 120 157 164 169 214 293 462 547 31 57 77 82 114 162 275 315 Дія лікування на метастази в легені показана на фіг. 2 і в таблиці 4. Спільна обробка трастузумабом і бевацизумабом після безуспішного лікування бевацизумабом призводила до різкого зниження метастазів. В день 99 рівні людських послідовностей Alu (що корелює з інвазією пухлинних клітин у вторинну тканину) значно нижчі у тварин, яких піддавали комбінованій терапії, в порівнянні з обробленими наповнювачем тваринами, яких умертвляли через 28 днів, і в порівнянні з Трастузумаб + бевацизумаб 119 126 143 138 167 181 172 211 226 266 324 318 248 232 209 224 213 173 178 150 141 134 130 С.К.О. 35 44 67 65 76 78 63 65 68 78 103 100 81 75 69 56 68 57 80 73 74 67 76 обробленими трастузумабом тваринами, яких умертвляли в день 44. Це несподівано встановлено при створенні винаходу дія на метастази протилежна дії, характерній для інших цитотоксичних лікарських засобів (Geldof А. А. і ін., Anticancer Res. 8, 1988, 1335-1339; Murphy J., Clin. Oncol. 11, 1993, cc.199-201 і De Larco J.E. і ін., Cancer Res. 61, 2001, cc. 2857-2861). 21 95797 22 Таблиця 4: Дія лікування на метастази в легеню. ДНК Alu оцінювали кількісно за допомогою ПЦР в реальному часі, і результати представлені для кожної тварини Таблиця 4 Наповнювач Людська ДНК [нг/мл] Середнє Медіана Трастузумаб 0,224 0,225 0,148 0,011 0,037 0,058 0,084 0,099 0,048 0,279 0,1212* 0,0915 1,609 0,084 0,586 0,055 2,919 0,078 2,741 0,017 0,340 0,232 0,8661** 0,2861 Статистична достовірність сумісного лікування *р = 0,001; **р =
ДивитисяДодаткова інформація
Назва патенту англійськоюTumor therapy with an antibody for vascular endothelial growth factor and an antibody for human epithelial growth factor receptor type 2
Автори англійськоюFriess, Thomas, Hasmann, Max, Scheuer, Werner
Назва патенту російськоюТерапия опухолей с использованием сосудистого эндотелиального фактора роста и антитела к рецептору типа 2 человеческого эпителиального фактора роста
Автори російськоюФрисс Томас, Хасманн Макс, Шойер Вернер
МПК / Мітки
МПК: A61K 39/395, A61P 35/00
Мітки: використанням, людського, антитіла, пухлин, типу, терапія, росту, ендотеліального, фактора, судинного, рецептора, епітеліального
Код посилання
<a href="https://ua.patents.su/12-95797-terapiya-pukhlin-z-vikoristannyam-sudinnogo-endotelialnogo-faktora-rostu-i-antitila-do-receptora-tipu-2-lyudskogo-epitelialnogo-faktora-rostu.html" target="_blank" rel="follow" title="База патентів України">Терапія пухлин з використанням судинного ендотеліального фактора росту і антитіла до рецептора типу 2 людського епітеліального фактора росту</a>
Попередній патент: Похідні n-циклопропіл-бензиламіду, способи їх одержання, фунгіцидна композиція та спосіб боротьби із фітопатогенними грибами
Наступний патент: Похідні циклогексилпіразоллактаму як інгібітори 11-бета-гідроксистероїддегідрогенази 1
Випадковий патент: Спосіб передачі інформації з використанням носія даних, носій інформації і пристрій для відтворення інформації з такого носія