Застосування інгібіторів тирозинкінази брутона (втк)
Номер патенту: 107707
Опубліковано: 10.02.2015
Автори: Хедрік Ерік, Лоурі Девід Дж., Моді Тарак Д., Баггі Джозеф Дж., Файф Гвен, Еліас Лоренс
Формула / Реферат
1. Застосування сполуки, яка має структуру:
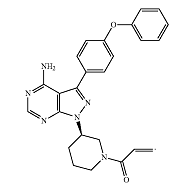 ,
,
у кількості від 420 мг/день до 840 мг/день включно для лікування рецидивної або рефрактерної неходжкінської лімфоми у індивіда.
2. Застосування за п. 1, в якому неходжкінська лімфома є рецидивним або рефрактерним хронічним лімфоцитарним лейкозом (ХЛЛ) або рецидивною, або рефрактерною дрібноклітинною лімфоцитарною лімфомою (ДЛЛ).
3. Застосування за п. 1, в якому неходжкінська лімфома є рецидивною або рефрактерною дифузною В-великоклітинною лімфомою (ДВКЛ), рецидивною або рефрактерною лімфомою з клітин мантійної зони, рецидивною або рефрактерною фолікулярною лімфомою або рецидивною або рефрактерною множинною мієломою.
4. Застосування за будь-яким із пунктів 1-3 для введення в дозі приблизно 420 мг/день, приблизно 560 мг/день або приблизно 840 мг/день.
5. Застосування за будь-яким із пунктів 1-4 для орального введення.
6. Застосування за будь-яким із пунктів 1-5 для введення з другою схемою лікування раку.
7. Застосування за п. 6, в якому друга схема лікування раку включає хіміотерапевтичний агент, стероїд, імунотерапевтичний агент, цільову терапію або їх комбінацію.
8. Застосування за п. 6, в якому інша друга лікування раку включає леналідомід, хлорамбуцил, іфосфамід, доксорубіцин, месалазин, талідомід, темсіролімус, еверолімус, флударабін, фостаматініб, паклітаксель, доцетаксель, офатумумаб, рітуксімаб, дексаметазон, преднізолон, CAL-101, ібрітумомаб, тосітумомаб, бортезоміб, пентостатин, ендостатин, бендамустин, циклофосфамід, ендостатіневеролімус, етопозид, гідроксидаунорубіцин, вінкристин або їх комбінацію.
9. Застосування за п. 6 для введення з анти-СD20 антитілом.
10. Застосування за п. 9, в якому анти-СD20 антитілом є ритуксимаб або офатумумаб.
11. Застосування за п. 6 для введення з ритуксимабом і бендамустином.
12. Застосування за п. 6 для введення з флударабіном і циклофосфамідом.
13. Застосування за п. 6 для введення з циклофосфамідом, вінкристином і преднізолоном.
14. Застосування за п. 6 для введення з циклофосфамідом, доксорубіцином; вінкристином і преднізолоном.
15. Застосування за будь-яким із пунктів 12-14 для введення з ритуксимабом.
16. Застосування за п. 7 для введення з дексаметазоном та леналідомідом.
17. Застосування за будь-яким з пунктів 1-16 для введення індивіду, який попередньо приймав щонайменше два протиракові агенти.
18. Застосування за п. 17, в якому щонайменше одним з щонайменше двох протиракових агентів є антитіло, нуклеозидний аналог або алкілуючий агент.
19. Застосування за п. 18, в якому антитілом є анти-СD20 або анти-СD52 антитіло.
20. Застосування за п. 19, в якому анти-СD20 антитілом є ритуксимаб або офатумумаб.
21. Застосування за п. 19, в якому анти-СD52 антитілом є алемтузумаб.
22. Застосування за п. 17, в якому щонайменше одним з протиракових агентів є бортезоміб.
23. Застосування за будь-яким з пунктів 1-22, в якому рецидивна або рефрактерна неходжкінська лімфома характеризується делецією нуклеїнової кислоти 17р13 в хромосомі 17 або делецією нуклеїнової кислоти 11q22 в хромосомі 11.
24. Лікарський засіб для лікування рецидивної або рефрактерної неходжкінської лімфоми, який містить сполуку, яка має структуру;
 ,
,
причому лікарський засіб призначений для введення у кількості від 420 мг/день до 840 мг/день включно.
25. Лікарський засіб за п. 24, в якому рецидивна або рефрактерна неходжкінська лімфома є рецидивним або рефрактерним хронічним лімфоцитарним лейкозом (ХЛЛ) або рецидивною, або рефрактерною дрібноклітинною лімфоцитарною лімфомою (ДЛЛ).
26. Лікарський засіб за п. 24, в якому рецидивна або рефрактерна неходжкінська лімфома є рецидивною або рефрактерною дифузною В-великоклітинною лімфомою (ДВКЛ), рецидивною або рефрактерною лімфомою з клітин мантійної зони, рецидивною або рефрактерною фолікулярною лімфомою або рецидивною, або рефрактерною множинною мієломою.
27. Лікарський засіб за п. 24, в якому рецидивна або рефрактерна неходжкінська лімфома являє собою високий ризик розвитку рецидивного або рефрактерного лімфоцитарного лейкозу.
28. Лікарський засіб за п. 24, в якому рецидивна або рефрактерна неходжкінська лімфома характеризується делецією нуклеїнової кислоти 17р13 в хромосомі 17 або делецією нуклеїнової кислоти 11q22 в хромосомі 11.
29. Лікарський засіб за будь-яким із пунктів 24-28 для орального введення.
Текст
Реферат: UA 107707 C2 (12) UA 107707 C2 Пропонується застосування сполуки, яка має структуру: , у кількості від 420 мг/день до 840 мг/день, включно, для лікування рецидивної або рефрактерної неходжкінської лімфоми у індивіда. UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 Споріднені заявки Ця заявка претендує на пріоритет попередньої заявки на патент США № 61/351,130, поданої 3 червня 2010 р.; попередньої заявки на патент США № 61/351,655, поданої 4 червня 2010 р.; попередньої заявки на патент США № 61/351,793, поданої 4 червня 2010 р.; попередньої заявки на патент США № 61/351,762, поданої 4 червня 2010 р.; попередньої заявки на патент США № 61/419,764, поданої 3 грудня 2010 р.; попередньої заявки на патент США № 61/472,138, поданої 5 квітня 2011 р.; всі з яких включені в даний документ за посиланням в їх повному об'ємі. Рівень техніки Тирозинкіназа Брутона (Btk), представник Tec-родини нерецепторних тирозинкіназ, є ключовим сигнальним ферментом, який експресується у всіх типах гематопоетичних клітин, крім Т-лімфоцитів і натуральних клітин-кілерів. Btk відіграє важливу роль в В-клітинному сигнальному шляху, зв'язуючи стимуляцію B-клітинного рецептора (BCR) поверхні клітини зі спадними внутрішньоклітинними відповідями. Btk є ключовим регулятором розвитку, активації, сигналізації і виживання B-клітин (Kurosaki, Curr Op Imm, 2000, 276-281; Schaeffer and Schwartzberg, Curr Op Imm 2000, 282-288). Крім того, Btk відіграє певну роль в ряді інших гематопоетичних клітинних сигнальних шляхах, наприклад в опосередкованій Толл-подібним рецептором (TLR) і цитокіновим рецептором продукції TNF-α в макрофагах, передачі сигналів IgE рецептора (FcepsilonRI) в тучних клітинах, інгібуванні сигналу апоптоза Fas/APO-1 в лімфоїдних клітинах B-лінії і стимульованій колагеном агрегації тромбоцитів. Дивись, наприклад, C. A. Jeffries, et al., (2003), Journal of Biological Chemistry 278:26258-26264; N. J. Horwood, et al., (2003), The Journal of Experimental Medicine 197:16031611; Iwaki et al. (2005), Journal of Biological Chemistry 280(48):40261-40270; Vassilev et al. (1999), Journal of Biological Chemistry 274(3):1646-1656 та Quek et al. (1998), Current Biology 8(20):11371140. Суть винаходу Описаним в даному документі, в конкретних варіантах здійснення, є спосіб лікування гемобластозу у індивіда, який того потребує, що включає: (а) введення цьому індивіду кількості необоротного інгібітору Btk, достатньої для мобілізації певної кількості злоякісних клітин; і (б) аналіз цієї мобілізованої кількості клітин. В певних варіантах здійснення кількість необоротного інгібітору Btk є достатньою для індукції лімфоцитозу певної кількості клітин із злоякісної пухлини. В певних варіантах здійснення гемобластозом є ХЛЛ (хронічний лімфолейкоз). В певних варіантах здійснення лікування гемобластозу включає тримання гемобластозу під контролем. В певних варіантах здійснення гемобластозом є B-клітинна злоякісна пухлина. В певних варіантах здійснення гемобластозом є лейкоз, лімфопроліферативний розлад або мієлоїдний лейкоз. В певних варіантах здійснення мобілізовані клітини є мієлоїдними клітинами або лімфоїдними клітинами. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення концентрації в периферичній крові мобілізованої кількості клітин. В певних варіантах здійснення спосіб додатково включає проведення другої схеми лікування раку після того, як концентрація в периферичній крові мобілізованої кількості клітин збільшується у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення проведення другої схеми лікування раку має місце після наступного зниження концентрації в периферичній крові мобілізованої кількості клітин. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості підвищення концентрації в периферичній крові мобілізованої кількості клітин у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає проведення другої схеми лікування раку після підвищення концентрації в периферичній крові мобілізованої кількості клітин впродовж попередньо визначеного періоду часу. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає підрахунок числа мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає проведення другої схеми лікування раку після підвищення числа мобілізованих клітин в периферичній крові у порівнянні з їх числом до введення інгібітору Btk. В певних варіантах здійснення проведення другої схеми лікування раку має місце після наступного зменшення числа мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості збільшення числа мобілізованих клітин в периферичній крові у порівнянні з їх числом до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає проведення другої схеми лікування раку після збільшення числа мобілізованих клітин в периферичній крові впродовж попередньо визначеного періоду часу. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає отримання профілю біомаркера для популяції клітин, виділених з певної кількості клітин, де цей профіль біомаркера показує експресію біомаркера, рівень експресії біомаркера, мутації в біомаркері або наявність 1 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 біомаркера. В певних варіантах здійснення біомаркер є будь-яким цитогенетичним, поверхневоклітинним молекулярним, або білковим маркером, або маркером експресії РНК. В певних варіантах здійснення біомаркером є: ZAP70; t(14,18); мікроглобулін β-2; мутаційний статус p53; мутаційний статус ATM; del(17)p; del(11)q; del(6)q; CD5; CD11c; CD19; CD20; CD22; CD25; CD38; CD103; CD138; експресія секретованого, поверхневого або цитоплазматичного імуноглобуліну; мутаційний статус VH або їх комбінація. В певних варіантах здійснення спосіб додатково включає забезпечення другої схеми лікування раку на основі профілю біомаркера. В певних варіантах здійснення спосіб додатково передбачає відмову від проведення на основі профілю біомаркера. В певних варіантах здійснення спосіб додатково включає прогнозування ефективності схеми лікування на основі профілю біомаркера. В певних варіантах здійснення гемобластоз є хронічним лімфоцитарним лейкозом (ХЛЛ), дрібноклітинною лімфоцитарною лімфомою (ДЛЛ), ХЛЛ з високим ризиком або неХЛЛ/ДЛЛ лімфомою. В певних варіантах здійснення гемобластоз є фолікулярною лімфомою, дифузною крупноклітинною В-клітинною лімфомою (ДККЛ), лімфомою з клітин мантійної зони, макроглобулінемією Вальденстрема, множинною мієломою, лімфомою маргінальної зони, лімфомою Беркітта, неберкіттівською Вклітинною лімфомою високого ступеня або В-клітинною лімфомою екстранодальної маргінальної зони. В певних варіантах здійснення гемобластоз є хронічним мієлогенним (або мієлоїдним) лейкозом або гострим лімфобластним лейкозом. В певних варіантах здійснення гемобластоз є рецидивною або рефрактерною дифузною крупноклітинною В-клітинною лімфомою (ДККЛ), рецидивною або рефрактерною лімфомою з клітин мантійної зони, рецидивною або рефрактерною фолікулярною лімфомою, рецидивним або рефрактерним ХЛЛ; рецидивною або рефрактерною ДЛЛ; рецидивною або рефрактерною множинною мієломою. В певних варіантах здійснення інгібітор Btk утворює ковалентний зв'язок з цистеїновим бічним ланцюгом тирозинкінази Брутона, гомолога тирозинкінази Брутона або цистеїнового гомолога тирозинкінази Btk. В певних варіантах здійснення необоротним інгібітором Btk є (R)-1-(3-(4аміно-3-(4-феноксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)піперидин-1-іл)проп-2-ен-1-он. В певних варіантах здійснення кількість необоротного інгібітору Btk становить від 300 мг/день аж до 1000 мг/день включно. В певних варіантах здійснення кількість необоротного інгібітору Btk становить від 420 мг/день до 840 мг/день включно. В певних варіантах здійснення кількість необоротного інгібітору Btk становить біля 420 мг/день, біля 560 мг/день або біля 840 мг/день. В певних варіантах здійснення кількість необоротного інгібітору Btk становить біля 420 мг/день. В певних варіантах здійснення AUC0-24 інгібітору Btk знаходиться між приблизно 150 і приблизно 3500 нг*год./мл. В певних варіантах здійснення AUC0-24 інгібітору Btk знаходиться між приблизно 500 і приблизно 1100 нг*год./мл. В певних варіантах здійснення інгібітор Btk вводять перорально. В певних варіантах здійснення інгібітор Btk вводять один раз на день, два рази на день або три рази на день. В певних варіантах здійснення інгібітор Btk вводять доки захворювання прогресує, до розвитку неприйнятної токсичності або за індивідуальним вибором. В певних варіантах здійснення інгібітор Btk вводять щоденно доки захворювання прогресує, до розвитку неприйнятної токсичності або за індивідуальним вибором. В певних варіантах здійснення інгібітор Btk вводять через день доки захворювання прогресує, до розвитку неприйнятної токсичності або за індивідуальним вибором. В певних варіантах здійснення інгібітор Btk є терапією першої лінії, терапією другої лінії, терапією третьої лінії, терапією четвертої лінії, терапією п'ятої лінії або терапією шостої лінії. В певних варіантах здійснення інгібітор Btk лікує рефрактерний гемобластоз. В певних варіантах здійснення цього винаходу інгібітор Btk є підтримуючою терапією. В певних варіантах здійснення друга схема лікування раку включає хіміотерапевтичний агент, стероїд, імунотерапевтичний агент, таргетну терапію або їх комбінацію. В певних варіантах здійснення друга схема лікування раку включає інгібітор провідного шляху B-клітинного рецептора. В певних варіантах здійснення інгібітором провідного шляху B-клітинного рецептора є інгібітор CD79A, інгібітор CD79B, інгібітор CD19, інгібітор Lyn, інгібітор Syk, інгібітор PI3K, інгібітор Blnk, інгібітор PLCγ, інгібітор PKCβ або їх комбінація. В певних варіантах здійснення друга схема лікування раку включає антитіло, інгібітор сигналізації B-клітинного рецептора, інгібітор PI3K, інгібітор IAP, інгібітор mTOR, радіоімунотерапевтичний агент, ДНК-пошкоджуючий агент, інгібітор протеосоми, інгібітор гістонодеацетилази, інгібітор протеїнкінази, хеджхог-інгібітор, інгібітор Hsp90, інгібітор теломерази, інгібітор Jak1/2, інгібітор протеази, інгібітор PKC, інгібітор PARP або їх комбінацію. В певних варіантах здійснення друга схема лікування раку включає хлорамбуцил, іфосфамід, доксорубіцин, месалазин, талідомід, леналідомід, темсіролімус, еверолімус, флударабін, фостаматиніб, паклітаксель, доцетаксель, офатумумаб, рітуксімаб, дексаметазон, преднізолон, CAL-101, ібритумомаб, тозітумомаб, бортезоміб, пентостатин, ендостатин або їх комбінацію. В певних варіантах здійснення друга схема лікування раку включає циклофосфамід, гідроксидаунорубіцин, вінкристин і преднізолон, 2 UA 107707 C2 5 10 а також необов'зково рітуксімаб. В певних варіантах здійснення друга схема лікування раку включає бендамустин і рітуксімаб. В певних варіантах здійснення друга схема лікування раку включає флударабін, циклофосфамід і рітуксімаб. В певних варіантах здійснення друга схема лікування раку включає циклофосфамід, вінкристин і преднізолон, а також необов'зково рітуксімаб. В певних варіантах здійснення друга схема лікування раку включає етопозид, доксорубіцин, вінкристин, циклофосфамід, преднізолон і необов'зково рітуксімаб. В певних варіантах здійснення друга схема лікування раку включає дексаметазон і леналідомід. В певних варіантах здійснення інгібітор тирозинкінази Брутона є оборотним інгібітором. В певних варіантах здійснення інгібітор тирозинкінази Брутона є необоротним інгібітором. В певних варіантах здійснення інгібітор тирозинкінази Брутона утворює ковалентний зв'язок з цистеїновим бічним ланцюгом тирозинкінази Брутона, гомолога тирозинкінази Брутона або цистеїнового гомолога тирозинкінази Btk. В певних варіантах здійснення інгібітор тирозинкінази Брутона має структуру Формули (D): La Ar NH2 N N N N Y Z R8 15 20 25 30 35 40 45 R6 R7 Формула (D) де: La являє собою CH2, O, NH або S; Ar являє собою заміщений або незаміщений арил або заміщений або незаміщений гетероарил; Y являє собою необов'зково заміщену групу, вибрану з алкілу, гетероалкілу, циклоалкілу, гетероциклоалкілу, арилу і гетероарилу; Z являє собою C(=O), °C(=O), NHC(=O), C(=S), S(=O)x, OS(=O)х, NHS(=O)х, де х являє собою 1 або 2; R7 і R8 незалежно являють собою H; чи R7 і R8, взяті разом, утворюють зв'язок; R6 являє собою Н; і фармацевтично активні метаболіти або фармацевтично прийнятні сольвати, фармацевтично прийнятні солі або фармацевтично прийнятні проліки. В певних варіантах здійснення інгібітор тирозинкінази Брутона являє собою (R)-1-(3-(4-аміно-3-(4феноксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)піперидин-1-іл)проп-2-ен-1-он. В певних варіантах здійснення La являє собою О. В певних варіантах здійснення Ar являє собою феніл. В певних варіантах здійснення Z являє собою C(=O), NHC(=O) або S(=O)2. В певних варіантах здійснення кожний з R7 і R8 являє собою H. В певних варіантах здійснення Y являє собою 4-, 5-, 6- або 7-членне циклоалкільне кільце; або Y являє собою 4-, 5-, 6- або 7-членне гетероциклоалкільне кільце. Описаним в даному документі, в конкретних варіантах здійснення, є спосіб лікування рецидивної або рефрактерної неходжкінської лімфоми у індивіда, що того потребує, який включає: введення цьому індивіду терапевтично ефективної кількості (R)-1-(3-(4-аміно-3-(4феноксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)піперидин-1-іл)проп-2-ен-1-ону. В певних варіантах здійснення неходжкінська лімфома є рецидивною або рефрактерною дифузною крупноклітинною В-клітинною лімфомою (ДККЛ), рецидивною або рефрактерною лімфомою з клітин мантійної зони або рецидивною або рефрактерною фолікулярною лімфомою. В певних варіантах здійснення кількість (R)-1-(3-(4-аміно-3-(4-феноксифеніл)-1H-піразоло[3,4-d]піримідин1-іл)піперидин-1-іл)проп-2-ен-1-ону становить від 300 мг/день до 1000 мг/день включно. В певних варіантах здійснення кількість (R)-1-(3-(4-аміно-3-(4-феноксифеніл)-1H-піразоло[3,4d]піримідин-1-іл)піперидин-1-іл)проп-2-ен-1-ону становить від 420 мг/день до 840 мг/день включно. В певних варіантах здійснення кількість (R)-1-(3-(4-аміно-3-(4-феноксифеніл)-1Hпіразоло[3,4-d]піримідин-1-іл)піперидин-1-іл)проп-2-ен-1-ону становить біля 420 мг/день, біля 3 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 560 мг/день або біля 840 мг/день. В певних варіантах здійснення кількість необоротного інгібітору Btk становить біля 420 мг/день. В певних варіантах здійснення AUC0-24 інгібітору Btk знаходиться між приблизно 150 і приблизно 3500 нг*год./мл. В певних варіантах здійснення AUC0-24 інгібітору Btk знаходиться між приблизно 500 і приблизно 1100 нг*год./мл. В певних варіантах здійснення (R)-1-(3-(4-аміно-3-(4-феноксифеніл)-1H-піразоло[3,4-d]піримідин-1іл)піперидин-1-іл)проп-2-ен-1-он вводять перорально. В певних варіантах здійснення (R)-1-(3-(4аміно-3-(4-феноксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)піперидин-1-іл)проп-2-ен-1-он вводять один раз на день, два рази на день або три рази на день. В певних варіантах здійснення (R)-1-(3-(4-аміно-3-(4-феноксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)піперидин-1іл)проп-2-ен-1-он вводять доки прогресує захворювання, до неприйнятної токсичності або за індивідуальним вибором. В певних варіантах здійснення (R)-1-(3-(4-аміно-3-(4-феноксифеніл)1H-піразоло[3,4-d]піримідин-1-іл)піперидин-1-іл)проп-2-ен-1-он вводять доки прогресує захворювання, до неприйнятної токсичності або за індивідуальним вибором. В певних варіантах здійснення (R)-1-(3-(4-аміно-3-(4-феноксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)піперидин-1іл)проп-2-ен-1-он вводять щоденно доки прогресує захворювання, до неприйнятної токсичності або за індивідуальним вибором. В певних варіантах здійснення (R)-1-(3-(4-аміно-3-(4феноксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)піперидин-1-іл)проп-2-ен-1-он вводять через день доки прогресує захворювання, до неприйнятної токсичності або за індивідуальним вибором. В певних варіантах здійснення (R)-1-(3-(4-аміно-3-(4-феноксифеніл)-1H-піразоло[3,4d]піримідин-1-іл)піперидин-1-іл)проп-2-ен-1-он є терапією другої лінії, терапією третьої лінії, терапією четвертої лінії, терапією п'ятої лінії або терапією шостої лінії. В певних варіантах здійснення інгібітор Btk є підтримуючою терапією. В певних варіантах здійснення спосіб додатково включає проведення другої схеми лікування раку. В певних варіантах здійснення друга схема лікування раку проводиться після мобілізації певної кількості лімфоїдних клітин з неходжкінської лімфоми. В певних варіантах здійснення друга схема лікування раку проводиться після лімфоцитозу певної кількості лімфоїдних клітин з неходжкінської лімфоми. В певних варіантах здійснення друга схема лікування раку включає хіміотерапевтичний агент, стероїд, імунотерапевтичний агент, таргетну терапію або їх комбінацію. В певних варіантах здійснення друга схема лікування раку включає інгібітор провідного шляху B-клітинного рецептора. В певних варіантах здійснення інгібітором провідного шляху B-клітинного рецептора є інгібітор CD79А, інгібітор CD79B, інгібітор CD19, інгібітор Lyn, інгібітор Syk, інгібітор PI3K, інгібітор Blnk, інгібітор PLCγ, інгібітор PKCβ або їх комбінація. В певних варіантах здійснення друга схема лікування раку включає антитіло, інгібітор сигналізації B-клітинного рецептора, інгібітор PI3K, інгібітор IAP, інгібітор mTOR, радіоімунотерапевтичний агент, ДНК-ушкоджуючий агент, інгібітор протеосоми, інгібітор гістондеацетилази, інгібітор протеїнкінази, хеджхогінгібітор, інгібітор Hsp90, інгібітор теломерази, інгібітор Jak1/2, інгібітор протеази, інгібітор PKC, інгібітор PARP або їх комбінацію. В певних варіантах здійснення друга схема лікування раку включає хлорамбуцил, іфосфамід, доксорубіцин, месалазин, талідомід, леналідомід, темсіролімус, еверолімус, флударабін, фостаматиніб, паклітаксель, доцетаксель, офатумумаб, рітуксімаб, дексаметазон, преднізолон, CAL-101, ібрітумомаб, тозітумомаб, бортезоміб, пентостатин, ендостатин або їх комбінацію. В певних варіантах здійснення друга схема лікування раку включає циклофосфамід, гідроксидаунорубіцин, вінкристин, преднізолон і необов'зково рітуксімаб. В певних варіантах здійснення друга схема лікування раку включає бендамустин і рітуксімаб. В певних варіантах здійснення друга схема лікування раку включає флударабін, циклофосфамід і рітуксімаб. В певних варіантах здійснення друга схема лікування раку включає циклофосфамід, вінкристин, преднизолон і необов'зково рітуксімаб. В певних варіантах здійснення друга схема лікування раку включає етопозид, доксорубіцин, вінкристин, циклофосфамід, преднізолон і необов'зково рітуксімаб. В певних варіантах здійснення друга схема лікування раку включає дексаметазон і леналідомід. Описаним тут, в конкретних варіантах здійснення, є спосіб лікування дифузної крупноклітинної В-клітинної лімфоми активованого, подібного до В-клітинного підтипу (AБКДККЛ) у індивіда, що того потребує, який включає введення цьому індивіду необоротного інгібітору Btk в кількості від 300 мг/день до 1000 мг/день включно. В певних варіантах здійснення цей спосіб додатково включає діагностику індивіда з дифузною крупноклітинною В-клітинною лімфомою активованого, подібного до В-клітинного підтипу (AБК-ДККЛ) шляхом визначення послідовності генів одного або більше біомаркерів в певній кількості лімфоїдних клітин, виділених з дифузної крупноклітинної В-клітинної лімфоми. В певних варіантах здійснення необоротним інгібітором Btk є (R)-1-(3-(4-аміно-3-(4-феноксифеніл)-1H-піразоло[3,4-d]піримідин1-іл)піперидин-1-іл)проп-2-ен-1-он. В певних варіантах здійснення AБК-ДККЛ характеризується мутацією CD79B. В певних варіантах здійснення мутація CD79B є мутацією сигнального модуля 4 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 імунорецепторного тирозинового активуючого мотиву (ITAM). В певних варіантах здійснення мутація CD79B є міс.-сенс мутацією першого імунорецепторного тирозинового активуючого мотиву (ITAM) тирозину. В певних варіантах здійснення мутація CD79B підвищує поверхневу експресію BCR і ослаблює активність кінази Lyn. В певних варіантах здійснення AБК-ДККЛ характеризується мутацією CD79A. В певних варіантах здійснення мутація CD79А є мутацією в сигнальному модулі активуючого мотиву на основі імунорецептору тирозину (ITAM). В певних варіантах здійснення мутація CD79А є мутацією сплайс-донорського-сайту сигнального модуля активуючого мотиву (ITAM) на основі імунорецептору тирозину. В певних варіантах здійснення мутація CD79А видаляє сигнальний модуль активуючого мотиву (ITAM) на основі імунорецептору тирозину. В певних варіантах здійснення AБК-ДККЛ характеризується мутацією в MyD88, A20 або їх комбінацією. В певних варіантах здійснення мутація MYD88 являє собою амінокислотне заміщення L265P в домені Toll/IL-1 рецептора (TIR) MYD88. В певних варіантах здійснення кількість необоротного інгібітору Btk становить від 420 мг/день до 840 мг/день включно. В певних варіантах здійснення кількість необоротного інгібітору Btk становить біля 420 мг/день, біля 560 мг/день або біля 840 мг/день. В певних варіантах здійснення кількість необоротного інгібітору Btk становить біля 420 мг/день. В певних варіантах здійснення AUC 0-24 інгібітору Btk знаходиться між приблизно 150 і приблизно 3500 нг*год./мл. В певних варіантах здійснення AUC0-24 інгібітору Btk знаходиться між приблизно 500 і приблизно 1100 нг*год./мл. В певних варіантах здійснення необоротний інгібітор Btk вводять перорально. В певних варіантах здійснення необоротний інгібітор Btk вводять щоденно доки захворювання прогресує, до неприйнятної токсичності або за індивідуальним вибором. В певних варіантах здійснення інгібітор Btk вводять через день доки захворювання прогресує, до неприйнятної токсичності або за індивідуальним вибором. В певних варіантах здійснення необоротний інгібітор Btk є терапією першої лінії, терапією другої лінії, терапією третьої лінії, терапією четвертої лінії, терапією п'ятої лінії або терапією шостої лінії. В певних варіантах здійснення необоротний інгібітор Btk лікує рефрактерний гемобластоз. В певних варіантах здійснення необоротний інгібітор Btk є підтримуючою терапією. В певних варіантах здійснення спосіб за цим винаходом додатково включає проведення щонайменше однієї додаткової схеми лікування раку. В певних варіантах здійснення ця додаткова схема лікування раку включає хіміотерапевтичний агент, імунотерапевтичний агент, стероїд, променеву терапію, таргетну терапію або їх комбінацію. В певних варіантах здійснення друга схема лікування раку включає антитіло, інгібітор сигналізації B-клітинного рецептора, інгібітор PI3K, інгібітор IAP, інгібітор mTOR, радіоімунотерапевтичний агент, ДНК-ушкоджуючий агент, інгібітор протеосоми, інгібітор гістондеацетилази, інгібітор протеїнкінази, хеджхог-інгібітор, інгібітор Hsp90, інгібітор теломерази, інгібітор Jak1/2, інгібітор протеази, інгібітор PKC, інгібітор PARP або їх комбінацію. Описаним в даному документі, в конкретних варіантах здійснення, є спосіб визначення схеми лікування раку для індивіда з гемобластозом, який включає: (а) введення цьому індивіду кількості необоротного інгібітору Btk, достатньої, щоб мобілізувати певну кількість клітин зі злоякісної пухлини; (б) аналіз мобілізованої кількості клітин; і (в) вибір схеми лікування раку. В певних варіантах здійснення схема лікування раку включає хіміотерапевтичний агент, імунотерапевтичний агент, стероїд, таргетну терапію або їх комбінацію. В певних варіантах здійснення друга схема лікування раку включає інгібітор провідного шляху B-клітинного рецептора. В певних варіантах здійснення інгібітором провідного шляху B-клітинного рецептора є інгібітор CD79А, інгібітор CD79B, інгібітор CD19, інгібітор Lyn, інгібітор Syk, інгібітор PI3K, інгібітор Blnk, інгібітор PLCγ, інгібітор PKCβ або їх комбінація. В певних варіантах здійснення схема лікування раку включає інгібітор провідного шляху B-клітинного рецептора. В певних варіантах здійснення схема лікування раку включає інгібітор CD79А, інгібітор CD79B, інгібітор CD19, інгібітор Lyn, інгібітор Syk, інгібітор PI3K, інгібітор Blnk, інгібітор PLCγ, інгібітор PKCβ або їх комбінацію. В певних варіантах здійснення схема лікування раку включає антитіло, інгібітор сигналізації B-клітинного рецептора, інгібітор PI3K, інгібітор IAP, інгібітор mTOR, радіоімунотерапевтичний агент, ДНК-ушкоджуючий агент, інгібітор протеосоми, інгібітор гістондеацетилази, інгібітор протеїнкінази, хеджхог-інгібітор, інгібітор Hsp90, інгібітор теломерази, інгібітор Jak1/2, інгібітор протеази, інгібітор PKC, інгібітор PARP або їх комбінацію. В певних варіантах здійснення схема лікування раку включає хлорамбуцил, іфосфамід, доксорубіцин, месалазин, талідомід, леналідомід, темсіролімус, еверолімус, флударабін, фостаматиніб, паклітаксель, доцетаксель, офатумумаб, рітуксімаб, дексаметазон, преднізолон, CAL-101, ібрітумомаб, тозітумомаб, бортезоміб, пентостатин, ендостатин або їх комбінацію. В певних варіантах здійснення схема лікування раку включає циклофосфамід, гідроксидаунорубіцин, вінкристин, преднізолон і необов'зково рітуксімаб. В певних варіантах здійснення схема лікування раку включає бендамустин і рітуксімаб. В певних варіантах 5 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 здійснення схема лікування раку включає флударабін, циклофосфамід і рітуксімаб. В певних варіантах здійснення схема лікування раку включає циклофосфамід, вінкристин, преднізолон і необов'зково рітуксімаб. В певних варіантах здійснення схема лікування раку включає етопозид, доксорубіцин, вінкристин, циклофосфамід, преднізолон і необов'зково рітуксімаб. В певних варіантах здійснення схема лікування раку включає дексаметазон і леналідомід. Короткий опис малюнків На Фіг. 1 показана роль активності Btk в ряді процесів в клітині ХЛЛ, які вносять внесок в патогенез захворювання. На Фіг. 2 є представленою абсолютна кількість лімфоцитів під час курсу лікування необоротним інгібітором Btk для індивіда з ХЛЛ. На Фіг. 3 є представленою зміна суми добутків діаметрів лімфатичного вузла (ЛВ) у пацієнтів з ХЛЛ і ДЛЛ, яких лічать необоротним інгібітором Btk. На Фіг. 4 показана відповідь ЛВ у пацієнта, який страждає від ХЛЛ. Ліве зображення показує ЛВ до лікування необоротним інгібітором Btk; праве зображення показує ЛВ після лікування необоротним інгібітором Btk. На Фіг. 5 показано вплив необоротного інгібітору Btk на тяжкість захворювання ЛВ і лімфоцитоз з часом у пацієнтів, які страждають від ХЛЛ та/або ДЛЛ. На Фіг. 6 показані побічні ефекти у пацієнтів, який лікували необоротним інгібітором Btk. Ступені 1-4 представляють серйозність ефектів, де 1 означає дуже помірний, а 4 означає крайнє дискомфортний. На Фіг. 7 показана абсолютна кількість лімфоцитів (АКЛ)/109 л проти Циклу і Дня після введення інгібітору Btk індивідам з фолікулярною лімфомою, які досягли повної або часткової відповіді (CR/PR). Вісь Y показує Абсолютну Кількість Лімфоцитів (АКЛ) в кожний момент часу по номеру циклу і дню по осі X. Всі пацієнти (за виключенням Pt 32009) отримали лікування по графіку 4 тижні лікування з наступним одним тижнем без лікування. Таким чином, день1 кожного циклу слідує за одним тижнем без препарату для цих пацієнтів. Зверніть увагу на підвищення АКЛ під час більшості циклів у більшості пацієнтів і падіння АКЛ на початку наступних циклів. Ця картина часто притуплюється на більш пізніх циклах, коли пацієнти реагували на лікування. Пацієнт 32009 отримував лікування без перерви і не показав такої циклічної картини, але дійсно показав збільшення в Циклі 1, день15, і поступові збільшення під час Циклів з 2 по 5. На Фіг. 8 показана абсолютна кількість лімфоцитів (АКЛ)/109 л проти Циклу і Дня після введення інгібітору Btk індивідам PD з фолікулярною лімфомою, які мали Стабільне Захворювання (SD) під час лікування. Вісь Y показує абсолютну кількість лімфоцитів (АКЛ) в кожний момент часу по номеру циклу і дню по осі X. Всі пацієнти отримували лікування по графіку 4 тижні лікування з наступним одним тижнем без лікування. Таким чином, день1 кожного циклу слідує за одним тижнем без препарату для цих пацієнтів. Зверніть увагу на поступове підвищення мобілізації АКЛ крові у пацієнта 32004, який спочатку був стабільним, але пізніше мав Прогресуюче Захворювання (PD). На Фіг. 9 показана абсолютна кількість лімфоцитів (АКЛ)/109 л проти Циклу і Дня після введення інгібітору Btk індивідам PD з фолікулярною лімфомою. Вісь Y показує абсолютну кількість лімфоцитів (АКЛ) в кожний момент часу по номеру циклу і дню по осі X. Всі пацієнти, за виключенням 38010, отримували лікування по графіку 4 тижні лікування з наступним одним тижнем без лікування. Таким чином, день 1 кожного циклу слідує за одним тижнем без препарату для цих пацієнтів. Зверніть увагу на відсутність мобілізації, особливо у пацієнтів 38010 і 32001. Пацієнт 323001 пройшов обмежене лікування перед тим, як був знятий з дослідження. Реакція лімфоцитів дозволяє припустити, що цей пацієнт міг би мати реакцію, якби була можливість залишатись на лікуванні довше. На Фіг. 10 показана абсолютна кількість лімфоцитів (АКЛ)/109 л проти Циклу і Дня після введення інгібітору Btk індивідам з PR і SD з ДККЛ. Вісь Y показує абсолютну кількість лімфоцитів (АКЛ) в кожний момент часу по номеру циклу і дню по осі X. Пацієнт 38011 отримав лікування по графіку 4 тижні лікування з наступним одним тижнем без лікування. Таким чином, день1 кожного циклу слідує за одним тижнем без препарату для цього пацієнта. Пацієнти 38008 і 324001 отримували лікування безперервними щоденними дозами. На Фіг. 11 показана абсолютна кількість лімфоцитів (АКЛ)/109 л проти Циклу і Дня після введення інгібітору Btk індивідам PD з ДККЛ. Вісь Y показує абсолютну кількість лімфоцитів (АКЛ) в кожний момент часу по номеру циклу і дню по осі X. Всі пацієнти отримували лікування по графіку 4 тижні лікування з наступним одним тижнем без лікування. Таким чином, день 1 кожного циклу слідує за одним тижнем без препарату для цих пацієнтів. Зверніть увагу на відсутність мобілізації у 3 з 4 пацієнтів. Пацієнт 32002 отримав тільки один цикл лікування. 6 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 На Фіг. 12 показана абсолютна кількість лімфоцитів (АКЛ)/109 л проти Циклу і Дня після введення інгібітору Btk індивідам з лімфомою клітин мантійної зони. Вісь Y показує абсолютну кількість лімфоцитів (АКЛ) в кожний момент часу по номеру циклу і дню по осі X. Пацієнти 32006, 38003, 38004 отримали лікування по графіку 4 тижні лікування з наступним одним тижнем без лікування. Таким чином, день 1 кожного циклу слідує за одним тижнем без препарату для цих пацієнтів. Інші пацієнти отримали лікування з безперервним щоденним введенням дози. Зверніть увагу на те, що пацієнт з початковою PD (32014) не показав мобілізації. На Фіг. 13 показана абсолютна кількість лімфоцитів (АКЛ)/109 л проти Циклу і Дня після введення інгібітору Btk індивідам з лімфомою клітин мантійної зони, показаним на Фіг. 12. Вісь було змінено порівняно з Фіг. 12, щоб продемонструвати низькі коливання амплітуди. Зверніть увагу на те, що всі пацієнти з реакцією на лікування показали певний ступінь мобілізації. На Фіг. 14 показано, що мобілізація лімфоцитів, зокрема B-клітинного типу, у порівнянні з клітинами лімфоми, зменшується, коли хвороба реагує на лікування. Пацієнт 32007, Когорта 4, мав фолікулярну лімфому 3 ступеня, яка поступово регресувала від SD до CR. Хоча зміни АКЛ в даному випадку не були драматичними, частка В-клітин перетерплює характерне циклічне збільшення у відповідь на лікування інгібітором Btk. Також зверніть увагу на зменшення від циклу до циклу величини перемін у відповідності з кумулятивним контролем захворювання. На Фіг. 15 демонструється збільшення мобілізації B-клітин с прогресуванням захворювання. Пацієнт 32004, Когорта 2, мав фолікулярну лімфому 1 ступеня, яка прогресувала від початкової SD до PD після Циклу 6. DIM На Фіг. 16 показана рання мобілізація і кінцеве зменшення субпопуляції CD45 B-клітин у пацієнта 200-005 з лімфомою клітин мантійної зони, яка реагувала на лікування. Ця DIM субпопуляція мала типовий імунофенотип MCL (CD45 ) і відрізняється від популяції нормальних лімфоцитів. + На Фіг. 17 показане аномально високе розсіювання світла клітин CD19 , які мобілізуються, в + потім регресують у Пацієнта 324001 з CR ДККЛ. Ці клітини CD45 з розсіюванням світла (SSC-H) на верхніх панелях були приховані і їх забарвлення CD3 проти CD19 є відображеним на нижніх панелях. Тут передбачувані злоякісні клітини були"сховані" у великому вікні MNC, яке нормально визначає моноцити. Послідовність мобілізації, за якою слідує відповідь, є подібною до інших прикладів. На Фіг. 18 представлені відповіді на лікування для клінічного дослідження з введенням інгібітору Btk пацієнтам похилого віку з ХЛЛ або ДЛЛ, які раніше не піддавались медикаментозному втручанню. Індивідам вводили 420 мг/день інгібітору Btk. На Фіг. 19 представлені відповіді на лікування для клінічного дослідження з введенням інгібітору Btk R/R пацієнтам з ХЛЛ або ДЛЛ. Індивідам вводили 420 мг/день інгібітору Btk. На Фіг. 20 представлені відповіді на лікування для клінічного дослідження з введенням інгібітору Btk індивідам з високим ризиком ХЛЛ. На Фіг. 21 представлена реакція з часом на лікування для клінічного дослідження з введенням інгібітору Btk індивідам з ХЛЛ або ДЛЛ. На Фіг. 22 представлені кращі відповіді на лікування для всіх пацієнтів в клінічному дослідженні з введенням інгібітору Btk індивідам з ХЛЛ або ДЛЛ. На Фіг. 23 представлені кращі відповіді на лікування для абстрактних пацієнтів в клінічному дослідженні з введенням інгібітору Btk індивідам з ХЛЛ або ДЛЛ. На Фіг. 24 представлена краща відповідь на лікування за прогностичним фактором у пацієнтів з ХЛЛ або ДЛЛ, які приймали участь в клінічному дослідженні з введенням інгібітору Btk. На Фіг. 25 представлена початкова (Цикл 2) оцінка відповіді на лікування і краща відповідь (Когорти 420 мг) пацієнтів з ХЛЛ або ДЛЛ, які приймали участь в клінічному дослідженні з введенням інгібітору Btk. На Фіг. 26 представлена початкова (Цикл 2) оцінка відповіді на лікування за дозою у пацієнтів с рецидивуючим/ рефрактерним ХЛЛ або ДЛЛ, які приймали участь в клінічному дослідженні з введенням інгібітору Btk. На Фіг. 27 представлені покращення гематологічних показників у пацієнтів з ХЛЛ або ДЛЛ, які приймали участь в клінічному дослідженні з введенням інгібітору Btk. На Фіг. 28 представлені дані, які ілюструють результати комбінування інгібітору Btk і Карбоплатину або Велкейду в клітинах DoHH2. На Фіг. 29 представлені дані, які ілюструють результати комбінування інгібітору Btk і Дексаметазону або Леналідоміду в клітинах DoHH2. 7 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 На Фіг. 30 представлені дані, які ілюструють результати комбінування інгібітору Btk і Темсиролімусу або R406 в клітинах DoHH2. На Фіг. 31 представлені дані, які ілюструють результати комбінування інгібітору Btk і Гемцитабіну або Доксорубіцину в клітинах DoHH2. На Фіг. 32 представлені дані, які ілюструють результати комбінування інгібітору Btk і Cal-101 в клітинах TMD8. На Фіг. 33 представлені дані, які ілюструють результати комбінування інгібітору Btk і R406 в клітинах TMD8. На Фіг. 34 представлені дані, які ілюструють результати комбінування інгібітору Btk і вінкристину в клітинах TMD8. На Фіг. 35 представлені дані, які ілюструють результати комбінування інгібітору Btk і доксорубіцину в клітинах TMD8. На Фіг. 36 представлені дані, які ілюструють результати комбінування інгібітору Btk і Ленолідоміду в клітинах TMD8. На Фіг. 37 представлені дані, які ілюструють результати комбінування інгібітору Btk і Велкейду в клітинах TMD8. На Фіг. 38 представлені дані, які ілюструють результати комбінування інгібітору Btk і Флударабіну в клітинах TMD8. На Фіг. 39 представлені дані, які ілюструють результати комбінування інгібітору Btk і таксолу в клітинах TMD8. Докладний опис винаходу В наш час існує потреба в способах лікування (включаючи діагностику) гемобластозів, в тому числі рецидивних і рефрактерних В-клітинних неоплазій, а також AБК-ДККЛ. Ця заявка базується, частково, на неочікуваному відкритті того, що інгібітори Btk індукують мобілізацію (або, в певних випадках, лімфоцитоз) лімфоїдних клітин в твердих гемобластозах. Мобілізація лімфоїдних клітин збільшує вплив на них додаткових схем лікування раку і їх доступність для біомаркерного скринінгу. Винахідники встановили також, що інгібітори Btk є корисними в лікуванні рецидивних і рефрактерних гематологічних злоякісних пухлин і AБК-ДККЛ. Описаним тут, в певних варіантах здійснення даного винаходу, є спосіб лікування гемобластозу у індивіда, що того потребує, який включає: (а) введення цьому індивіду кількості необоротного інгібітору Btk, достатньої, щоб мобілізувати певну кількість клітин зі злоякісної пухлини; і (б) аналіз мобілізованої кількості клітин. Описаним тут, в певних варіантах здійснення, є спосіб лікування дифузної крупноклітинної В-клітинної лімфоми активованого, подібного до Вклітинного підтипу (AБК-ДККЛ) у індивіда, що того потребує, який включає: введення цьому індивіду необоротного інгібітору Btk в кількості від 300 мг/день до 1000 мг/день включно. Також описаним тут, в певних варіантах здійснення, є спосіб лікування рецидивної або рефрактерної неходжкінськой лімфоми у індивіда, що того потребує, який включає: введення цьому індивіду терапевтично ефективної кількості (R)-1-(3-(4-аміно-3-(4-феноксифеніл)-1H-піразоло[3,4d]піримідин-1-іл)піперидин-1-іл) проп-2-ен-1-ону. Термінологія Коли не вказується інше, всі технічні і наукові терміни, використовувані в даному документі, мають те саме значення, яке звичайно розуміється спеціалістом в галузі техніки, до якої належить заявлений об'єкт. У випадку, коли є кілька визначень для використовуваних тут термінів, ті, що вказані в цьому розділі, превалюють. Там, де дається посилання на URL або інший такий ідентифікатор або адресу, слід розуміти, що такі ідентифікатори можуть змінюватись, и конкретна інформація в Інтернеті може з'являтись і щезати, але пошуком в Інтернеті може бути знайдена еквівалентна інформація. Посилання на неї свідчить про доступність і широке розповсюдження такої інформації. Слід розуміти, що наведений вище загальний опис і наступний докладний опис є тільки прикладами і поясненнями, які не обмежують будь-який заявлений тут об'єкт. В даному документі використання однини включає множину, коли спеціально не вказується інше. Слід зазначити, що використовувані в описі і формулі винаходу форми однини "a" (англ.), "an" (англ.) і "the" (англ.) включають множину, коли з контексту не слідує інше. В даному документі використання "або" означає "та/або", коли не вказується інше. Крім того, використання терміну "включаючи", а також інших форм, таких як "включає", "включають" і "включено", є не обмежуючим. Заголовки розділів, використані в даному документі, призначені тільки для організаційних цілей і не повинні розглядатись як обмежуючі описуваний об'єкт. Всі документи або частини документів, вказані в заявці, включаючи, без обмеження, патенти, патентні заявки, статті, книги, 8 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 довідники і монографії, вважаються прямо включеними за посиланням у всій їх повноті для будь-яких цілей. Визначення стандартних хімічних термінів можна знайти в довідниках, включаючи Carey and th Sundberg "ADVANCED ORGANIC CHEMISTRY 4 ED.» Vols. A (2000) і B (2001), Plenum Press, New York. Коли не вказується інше, застосовуються звичайні в цій галузі способи масспектроскопії, ЯМР, ВЕРХ, хімії білків, біохімії, технологій рекомбінантних ДНК і фармакології. Якщо не даються конкретні визначення, номенклатура, використовувана в зв'язку з аналітичною хімією, хімією органічного синтезу, медичною і фармацевтичною хімією, а також лабораторні процедури і методики, описані в даному документі, є відомою з рівня техніки. Стандартні методики можуть використовуватись для хімічного синтезу, хімічних аналізів, фармацевтичного приготування, складання рецептури і доставки, а також для лікування пацієнтів. Стандартні методики можуть використовуватись для рекомбінантної ДНК, синтезу олігонуклеотидів, тканинного культивування і трансформації (наприклад, електропорація, ліпофекція). Реакції і методики очистки можуть проводитись, наприклад, з використанням наборів за технічними умовами виробника, або вони проводяться як звичайно в даній галузі, або як описано тут. Вищевказані методики і процедури звичайно можуть проводитись звичайними способами, добре відомими в даній галузі, як описано в різних загальних і більш спеціальних посиланнях, які цитуються і обговорюються по всьому цьому опису. Слід розуміти, що способи і композиції, описані тут, не обмежуються конкретною методологією, протоколами, клітинними лініями, конструктами і реагентами, описаними в даному документі, і, як такі, можуть змінюватись. Слід також розуміти, що термінологія, використана в даному документі, призначена тільки для цілей опису конкретних варіантів здійснення цього винаходу і не призначалась для обмеження об'єму способів і композицій, описаних в даному документі, який буде обмежуватись тільки формулою винаходу, яка додається. Всі публікації і патенти, згадані в даному документі, включені сюди за посиланням у всій їх повноті для цілей опису і розкриття, наприклад, конструктів і методологій, описаних в публікаціях, які можуть бути використані стосовно способів, композицій і сполук, описаних в даному документі. Публікації, обговорювані в даному документі, наведені тільки для їх розкриття до дати подачі цієї заявки. Ніщо в даному документі не має розцінюватись як визнання того, що винахідники, вказані в заявці, не мають права датувати більш раннім числом таке розкриття на підставі попереднього винаходу або з будь-якої іншої причини. "Алкільна" група стосується аліфатичної вуглеводневої групи. Алкільний фрагмент може бути "насиченою алкільною" групою, а це означає, що вона не містить будь-яких алкенових або алкінових фрагментів. Алкільний фрагмент може бути також "ненасиченою алкільною" групою, а це означає, що вона містить щонайменше один алкеновий або алкіновий фрагмент. "Алкеновий" фрагмент стосується к групи, яка має щонайменше один подвійний зв'язок вуглецьвуглець, а "алкіновий" фрагмент стосується групи, яка має щонайменше один потрійний зв'язок вуглець-вуглець. Алкільний фрагмент, насичений або ненасичений, може бути розгалуженим, лінійним або циклічним. В залежності від структури алкільна група може бути монорадикальною або дирадикальною (тобто, алкіленовою групою). Алкільна група може також бути "нижчим алкілом", який має від 1 до 6 атомів вуглецю. Як використовується в даному документі, C 1-Cx включає C1-C2, C1-C3.. C1-Cx. "Алкільний" фрагмент може мати від 1 до 10 атомів вуглецю (коли б він не з'являвся в даному документі, числовий діапазон, такий як "від 1 до 10" стосується кожного цілого числа в цьому діапазоні, наприклад, "від 1 до 10 атомів вуглецю" означає, що алкільна група може мати 1 атом вуглецю, 2 атоми вуглецю, 3 атоми вуглецю і т.д. аж до і включаючи 10 атомів вуглецю, хоча дане визначення охоплює також застосування терміну "алкіл" без позначення числового діапазону). Алкільна група описаних тут сполук може бути позначена як "С 1-С4 алкіл" або подібним чином. Тільки в якості прикладу, "C1-C4 алкіл" показує, що в алкільному ланцюзі є присутніми від одного до чотирьох атомів вуглецю, тобто алкільний ланцюг вибирається з метилу, етилу, пропилу, ізопропилу, n-бутилу, ізобутилу, sec-бутилу і t-бутилу. Таким чином, С1С4 алкіл включає C1-C2 алкіл і С1-С3 алкіл. Алкільні групи можуть бути заміщеними або незаміщеними. Типові алкільні групи включають, жодним чином не обмежуючись ними, метил, етил, пропил, ізопропил, бутил, ізобутил, третинний бутил, пентил, гексил, етеніл, пропеніл, бутеніл, циклопропил, циклобутил, циклопентил, циклогексил і т.п. Термін "нециклічний алкіл", як він тут використовується, стосується алкілу, який не є циклічним (тобто, лінійний або розгалужений ланцюг містить щонайменше один атом вуглецю). Нециклічні алкіли можуть бути повністю насиченими або можуть містити нециклічні алкени та/або алкіни. Нециклічні алкіли можуть бути необов'зково заміщеними. 9 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 Термін "алкеніл" стосується того типу алкільної групи, в якому перші два атоми алкільної групи утворюють подвійний зв'язок, що не є частиною ароматичної групи. Тобто, алкенільна група починається з атомів -C(R)=C(R)-R, де R відноситься до решти частин алкенільної групи, які можуть бути такими самими або можуть відрізнятись. Алкенільний фрагмент можуть бути розгалуженим, лінійним або циклічним (в цьому випадку він відомий також як "циклоалкенільна" група). В залежності від структури, алкенільна група можуть бути монорадикальною або дирадикальною (тобто, алкеніленовою групою). Алкенільні групи можуть бути необов'зково заміщеними. Не обмежуючі приклади алкенільної групи включають -CH=CH2, -C(CH3)=CH2, CH=CHCH3, -C(CH3)=CHCH3. Алкеніленові групи включають, не обмежуючись ними, -CH=CH-, C(CH3)=CH-, -CH=CHCH2-, -CH=CHCH2CH2- і -C(CH3)=-CHCH2-. Алкенільні групи можуть мати від 2 до 10 вуглеців. Алкенільна група також можуть бути "нижчим алкенілом", який має від 2 до 6 атомів вуглецю. Термін "алкініл" стосується того типу алкільної групи, в якому перші два атоми алкільної групи утворюють потрійний зв'язок. Тобто, алкінільна група починається з атомів -C≡C-R, де R відноситься до решти частин алкінільної групи, які можуть бути такими самими або можуть відрізнятись. Частина "R" алкінільного фрагмента може бути розгалуженою, лінійною або циклічною. В залежності від структури, алкінільна група може бути монорадикальною або дирадикальною (тобто, алкініленовою групою). Алкінільні групи можуть бути необов'зково заміщеними. Не обмежуючі приклади алкінільної групи включають, не обмежуючись ними, C≡CH, -C≡CCH3, -C≡CCH2CH3, -C≡C- і -C≡CCH2-. Алкінільні групи можуть мати від 2 до 10 вуглеців. Алкінільна група також може бути "нижчим алкінілом", який має від 2 до 6 атомів вуглецю. "Алкоксильна" група відноситься до групи (алкіл)O-, де алкіл є таким, як тут визначено. "Гідроксиалкіл" відноситься до алкільного радикалу, як його тут визначено, заміщеного щонайменше однією гідроксильною групою. Не обмежуючі приклади гідроксиалкілу включають, не обмежуючись ними, гідроксиметил, 2-гідроксиетил, 2-гідроксипропил, 3-гідроксипропил, 1(гідроксиметил)-2-метилпропил, 2-гідроксибутил, 3-гідроксибутил, 4-гідроксибутил, 2,3дигідроксипропил, 1-(гідроксиметил)-2-гідроксиетил, 2,3-дигідроксибутил, 3,4-дигідроксибутил і 2-(гідроксиметил)-3-гідроксипропил. "Алкоксиалкіл" відноситься до алкільного радикалу, як його тут визначено, заміщеного алкоксильною групою, як її тут визначено. Група "алкенілокси" відноситься до групи (алкеніл)O-, де алкеніл є таким, як визначено тут. Термін "алкіламіно" відноситься до групи -N(алкіл)xHy, де х і у вибираються з х=1, у=1 і х=2, у=0. Коли х=2, алкільні групи, взяті разом з атомом N, до якого вони приєднані, можуть необов'зково утворювати циклічну кільцеву систему. "Алкіламіноалкіл" відноситься до алкільного радикалу, як його тут визначено, заміщеного алкіламіном, як його тут визначено. "Амід" є хімічною групою з формулою -C(O)NHR або NHC(O)R, де R вибирається з алкілу, циклоалкілу, арилу, гетероарилу (зв'язаного через кільцевий вуглець) і гетероаліциклу (зв'язаного через кільцевий вуглець). Амідна група може утворювати зв'язок між молекулою амінокислоти або пептиду і сполукою, описаною в даному документі, тим самим утворюючи варіант проліків. Будь-який амін або карбоксильний бічний ланцюг на описаних тут сполуках може бути амідованим. Методики і конкретні групи для отримання таких амідів відомі спеціалістам в цій галузі і можуть бути легко знайдені в довідниках, таких як Greene and Wuts, rd Protective Groups in Organic Synthesis, 3 Ed., John Wiley & Sons, New York, NY, 1999, який включено сюди за посиланням в повному об'ємі. Термін "складний ефір" стосується хімічного фрагменту з формулою -COOR, де R вибирається з алкілу, циклоалкілу, арилу, гетероарилу (зв'язаного через кільцевий вуглець) і гетероаліциклу (зв'язаного через кільцевий вуглець). Будь-яка гідроксильна група або карбоксильний бічний ланцюг на описаних тут сполуках можуть бути етерифікованими. Методики і конкретні групи для отримання таких складних ефірів відомі спеціалістам в цій галузі і можуть бути легко знайдені в довідниках, таких як Greene and Wuts, Protective Groups in rd Organic Synthesis, 3 Ed., John Wiley & Sons, New York, NY, 1999, який включено сюди за посиланням в повному об'ємі. Як він тут використовується, термін "кільце" стосується будь-якої ковалентно замкнутої структури. Кільця включають, наприклад, карбоцикли (наприклад, арили і циклоалкіли), гетероцикли (наприклад, гетероарили і неароматичні гетероцикли), ароматичні вуглеводні (наприклад, арили і гетероарили) і неароматичні сполуки (наприклад, циклоалкіли і неароматичні гетероцикли). Кільця можуть бути необов'зково заміщеними. Кільця можуть бути моноциклічними або поліциклічними. 10 UA 107707 C2 5 10 15 20 25 30 35 Термін "кільцева система", як він тут використовується, стосується одного или більше ніж одного кільця. Термін "членне кільце" може охоплювати будь-яку циклічну структуру. Термін "членний" призначений для позначення числа скелетних атомів, які утворюють кільце. Так, наприклад, циклогексил, піридин, піран і тіопіран являються 6-членними кільцями, а циклопентил, піррол, фуран і тіофен являються 5-членними кільцями. Термін "конденсований" стосується структур, в яких два або більше кілець поділяють один або більше зв'язків. Термін "карбоциклічний" або "карбоцикл" стосується кільця, де кожний з атомів, утворюючих кільце, являється атомом вуглецю. Карбоцикл включає арил і циклоалкіл. Отже, цей термін відрізняє карбоцикл від гетероциклу ("гетероциклічний"), в якого основа кільця містить щонайменше один атом, який відрізняється від вуглецю (тобто, гетероатом). Гетероцикл включає гетероарил і гетероциклоалкіл. Карбоцикли і гетероцикли можуть бути необов'зково заміщеними. Термін "ароматичний" стосується двохмірного кільця, що має делокалізовану π-електронну систему, яка містить 4n+2π електронів, де n є цілим числом. Ароматичні кільця можуть бути утвореними з п'яти, шести, семи, восьми, дев'яти або більше ніж дев'яти атомів. Ароматичні вуглеводні можуть бути необов'зково заміщеними. Термін "ароматичний" включає як карбоциклічні арильні (наприклад, феніл), так і гетероциклічні арильні (або "гетероарил", або "гетероароматичний") групи (наприклад, піридин). Цей термін включає моноциклічні або конденсовані поліциклічні кільцеві (тобто, кільця, які поділяють суміжні пари атомів вуглецю) групи. Термін "арил", як він тут використовується, стосується ароматичного кільця, де кожний з атомів, утворюючих кільце, являється атомом вуглецю. Арильні кільця можуть бути утворені з п'яти, шести, семи, восьми, дев'яти або більше ніж дев'яти атомів вуглецю. Арильні групи можуть бути необов'зково заміщеними. Приклади арильних груп включають, не обмежуючись ними, феніл, нафталеніл, фенантреніл, антраценіл, флуореніл і інденіл. В залежності від структури, арильна група може бути монорадикальною або дирадикальною (тобто, ариленовою групою). Група "арилокси" стосується групи (арил)O-, де арил є таким, як тут визначено. "Аралкіл" означає алкільний радикал, як його тут визначено, заміщений арильною групою. Не обмежуючі аралкільні групи включають бензил, фенетил і т.п. "Аралкеніл" означає алкенільний радикал, як його тут визначено, заміщений арильною групою, як її тут визначено. Термін "циклоалкіл" стосується моноциклічного або поліциклічного радикалу, який містить тільки вуглець і водень і може бути насиченим, частково ненасиченим або повністю ненасиченим. Циклоалкільні групи включають групи, що мають від 3 до 10 кільцевих атомів. Ілюстративні приклади циклоалкільних груп включають наступні фрагменти: , , , , , , , , , , 40 , , , , , 45 50 , , , і т.п. В залежності від структури циклоалкільна група може бути монорадикальною або дирадикальною (наприклад, циклоалкіленовою групой). Циклоалкільна група також може бути "нижчим циклоалкілом", що має від 3 до 8 атомів вуглецю. "Циклоалкілалкіл" означає алкільний радикал, як його тут визначено, заміщений циклоалкільною групою. Не обмежуючі циклоалкілалкільні групи включають циклопропилметил, циклобутилметил, циклопентилметил, циклогексилметил і т.п. Термін "гетероцикл" стосується гетероароматичних і гетероаліциклічних груп, що містять від одного до чотирьох гетероатомів, кожний з яких вибирається з O, S і N, де кожна гетероциклічна група має від 4 до 10 атомів в своїй кільцевій системі, і за умови, що кільце вказаної групи не 11 UA 107707 C2 5 10 15 20 25 30 35 40 містить двох суміжних атомів O або S. В даному документі, коли б не вказувалось число атомів вуглецю в гетероциклі (наприклад, С1-С6 гетероцикл), щонайменше один інший атом (гетероатом) має бути присутнім в кільці. Такі позначення, як "C 1-C6 гетероцикл", стосуються тільки числа атомів вуглецю в кільці і не стосуються загального числа атомів в кільці. Зрозуміло, що гетероциклічне кільце може мати додаткові гетероатоми в кільці. Такі позначення, як "4-6 членний гетероцикл", стосуються загального числа атомів, що містяться в кільці (тобто, чотирьох, п'яти або шестичленного кільця, в якому щонайменше один атом є атомом вуглецю, щонайменше один атом є гетероатомом, а решта від двох до чотирьох атомів є атомами вуглецю або гетероатомами). В гетероциклах, які мають два або більше гетероатоми, ці два або більше гетероатоми можуть бути однаковими або можуть відрізнятись один від одного. Гетероцикли можуть бути необов'зково заміщеними. Зв'язування з гетероциклом може здійснюватись на гетероатомі або через атом вуглецю. Неароматичні гетероциклічні групи включають групи, що мають тільки 4 атоми в своїй кільцевій системі, але ароматичні гетероциклічні групи повинні мати щонайменше 5 атомів в своїй кільцевій системі. Гетероциклічні групи включають бензо-конденсовані кільцеві системи. Прикладом 4-членної гетероциклічної групи являється азетидиніл (похідне азетидину). Прикладом 5-членної гетероциклічної групи являється тіазоліл. Прикладом 6-членної гетероциклічної групи являється піридил і прикладом 10-членної гетероциклічної групи - хінолініл. Прикладами неароматичних гетероциклічних груп є піролідиніл, тетрагідрофураніл, дигідрофураніл, тетрагідротієніл, тетрагідропіраніл, дигідропіраніл, тетрагідротіопіраніл, піперидино, морфоліно, тіоморфоліно, тіоксаніл, піперазиніл, азетидиніл, оксетаніл, тієтаніл, гомопіперидиніл, оксепаніл, тієпаніл, оксазепиніл, діазепиніл, тіазепиніл, 1,2,3,6-тетрагідропіридиніл, 2-піролініл, 3-піролініл, індолініл, 2H-піраніл, 4H-піраніл, діоксаніл, 1,3-діоксоланіл, піразолініл, дитіаніл, дитіоланіл, дигідропіранил, дигідротієніл, дигідрофураніл, піразолідиніл, імідазолініл, імідазолідиніл, 3азабіцикло[3.1.0]гексаніл, 3-азабіцикло[4.1.0]гептаніл, 3Н-індоліл і хінолізиніл. Прикладами ароматичних гетероциклічних груп є піридиніл, імідазоліл, піримідиніл, піразоліл, триазоліл, піразиніл, тетразоліл, фурил, тієніл, ізоксазоліл, тіазоліл, оксазоліл, ізотіазоліл, піроліл, хінолініл, ізохінолініл, індоліл, бензімідазоліл, бензофураніл, циннолініл, індазоліл, індолізиніл, фталазиніл, піридазиніл, триазиніл, ізоіндоліл, птеридиніл, пуриніл, оксадіазоліл, тіадіазоліл, фуразаніл, бензофуразаніл, бензотіофеніл, бензотіазоліл, бензоксазоліл, хіназолініл, хіноксалініл, нафтиридиніл і фуропіридиніл. Вищенаведені групи, як і похідні від вищенаведених груп, можуть бути С-приєднаними або N-приєднаними, де таке можливо. Наприклад, група, похідна від піролу, може бути пірол-1-іл (N-приєднаною) або пірол-3-іл (C-приєднаною). Крім того, група, похідна від імідазолу, може бути імідазол-1-іл або імідазол-3-іл (обидві N-приєднані) або імідазол-2-іл, імідазол-4-іл або імідазол-5-іл (всі C-приєднані). Гетероциклічні групи включають бензо-конденсовані кільцеві системи і кільцеві системи, заміщені одним або двома оксо (=O) фрагментами, такими як піролідин-2-он. В залежності від структури гетероциклічна група може бути монорадикальною або дирадикальною (наприклад, гетероцикленова група). Термін "гетероарил" або, альтернативно, "гетероароматичний" стосується арильної групи, яка включає один або більше кільцевих гетероатомів, вибраних з азоту, кисню і сірки. "Гетероароматичний" або "гетероарильний" фрагмент, який містить N, стосується ароматичної групи, в якій щонайменше один зі скелетних атомів кільця є атомом азоту. Ілюстративні приклади гетероарильних груп включають наступні фрагменти: NH N N N N N , , N S N N S , O , N O N S S N , 45 N , N O , , , N N N N , N , N , , N S , N N N , , N N , N N , N , N S 50 і т.п. В залежності від структури гетероарильна група може бути монорадикальною або дирадикальною (тобто, гетероариленовою групою). Терміни "неароматичний гетероцикл", "гетероциклоалкіл" або "гетероаліциклічний", як вони тут використовуються, стосуються неароматичного кільця, в якому один або більше атомів, 12 UA 107707 C2 5 10 15 утворюючих кільце, є гетероатомом. "Неароматичний гетероцикл" або "гетероциклоалкільна" група стосується циклоалкільної групи, яка включає щонайменше один гетероатом, вибраний з азоту, кисню і сірки. Радикали можуть бути конденсованими з арилом або гетероарилом. Гетероциклоалкільні кільця можуть бути утворені трьома, чотирма, п'ятьма, шістьма, сімома, вісьмома, дев'ятьма або більше ніж дев'ятьма атомами. Гетероциклоалкільні кільця можуть бути необов'зково заміщеними. В певних варіантах здійснення неароматичні гетероцикли містять одну або більше карбонільну або тіокарбонільну групи, такі як, наприклад, групи, що містять оксо- і тіо-частини. Приклади гетероциклоалкілів включають, не обмежуючись ними, лактами, лактони, циклічні іміди, циклічні тіоіміди, циклічні карбамати, тетрагідротіопіран, 4Hпіран, тетрагідропіран, піперидин, 1,3-діоксин, 1,3-діоксан, 1,4-діоксин, 1,4-діоксан, піперазин, 1,3-оксатіан, 1,4-оксатіїн, 1,4-оксатіан, тетрагідро-1,4-тіазин, 2Н-1,2-оксазин, малеімід, сукцинімід, барбітурову кислоту, тіобарбітурову кислоту, диоксопіперазин, гідантоїн, дигідроурацил, морфолін, триоксан, гексагідро-1,3,5-триазин, тетрагідротіофен, тетрагідрофуран, піролін, піролідин, піролідон, піролідіон, піразолін, піразолідин, імідазолін, імідазолідин, 1,3-диоксол, 1,3-диоксолан, 1,3-дитіол, 1,3-дитіолан, ізоксазолін, ізоксазолідин, оксазолін, оксазолідин, оксазолідинон, тіазолін, тіазолідин, і 1,3-оксатіолан. Ілюстративні приклади гетероциклоалкільних груп, які також відносяться до неароматичних гетероциклів, включають: O N S S N , O N O O N N , , N O O O O O O , , O N O , S , , O N O , , , , , H N N O 20 S , N H N H , N N N , , N N H , O O , , N H O N S O N , 25 30 35 40 45 N , O N , O і т.п. Термін гетероаліциклічний включає також всі кільцеві форми карбогідратів, включаючи, без обмеження ними, моносахариди, дисахариди і олігосахариди. В залежності від структури гетероциклоалкільна група може бути монорадикальною або дирадикальною (тобто, гетероциклоалкіленовою групою). Термін "гало" або, альтернативно, "галоген" або "галогенід" означає фторо, хлоро, бромо і йодо. Терміни "галоалкіл", "галоалкеніл", "галоалкініл" і "галоалкокси" включають алкіл, алкеніл, алкініл і алкокси структури, в яких щонайменше один атом водню є заміщеним на атом галогену. В певних варіантах здійснення, в яких два або більше атомів водню є заміщеними атомами галогену, всі атоми галогену є однаковими. В інших варіантах здійснення, в яких два або більше атомів водню є заміщеними атомами галогену, атоми галогену не всі є однаковими. Термін "фторалкіл", як він тут використовується, стосується алкільної групи, в якій щонайменше один атом водню є заміщеним на атом фтору. Приклади фторалкільних груп включають, не обмежуючись ними, -CF3, -CH2CF3, -CF2CF3, -CH2CH2CF3 і т.п. Як вони тут використовуються, терміни "гетероалкіл", "гетероалкеніл" і "гетероалкініл" включають необов'зково заміщені алкільні, алкенільні і алкінільні радикали, в яких один або більше атомів скелетного ланцюга є гетероатомом, наприклад киснем, азотом, сіркою, кремнієм, фосфором або їх комбінацією. Гетероатом(и) може знаходитись в будь-якій внутрішній позиції гетероалкільної групи або в тій позиції, в якій гетероалкільна група є приєднаною до іншої частини молекули. Приклади включають, не обмежуючись ними, -CH2-OCH3, -CH2-CH2-O-CH3, -CH2-NH-CH3, -CH2-CH2-NH-CH3, -CH2-N(CH3)-CH3, -CH2-CH2-NH-CH3, CH2-CH2-N(CH3)-CH3, -CH2-S-CH2-CH3, -CH2-CH2, -S(O)-CH3, -CH2-CH2-S(O)2-CH3, -CH=CH-OCH3, -Si(CH3)3, -CH2-CH=N-ОСН3 і -CH=CH-N(CH3)-CH3. Крім того, до двох гетероатомів можуть бути послідовними, такими як, в якості прикладу, -CH2-NH-ОСН3 і -CH2-O-Si(CH3)3. 13 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 Термін "гетероатом" стосується атому, який відрізняється від вуглецю або водню. Гетероатоми, як правило, незалежно вибираються з кисню, сірки, азоту, кремнію і фосфору, але не обмежуються цими атомами. В варіантах здійснення цього винаходу, в яких присутніми є два або більше гетероатомів, ці два або більше гетероатомів можуть бути однаковими або деякі або всі з цих двох або більше гетероатомів можуть кожний відрізнятись від інших. Термін "зв'язок" або "одинарний зв'язок" стосується хімічного зв'язку між двома атомами або двома фрагментами, коли ці атоми, з'єднані зв'язком, вважаються частиною більшої субструктури. Група "ізоціанато" стосується групи -NCO. Група "ізотіоціанато" стосується групи -NCS. Термін "фрагмент" стосується специфічного сегменту або функціональної групи молекули. Хімічні фрагменти часто визнаються хімічними структурними одиницями, які знаходяться в молекулі або приєднані до неї. "Сульфінільна" група стосується групи -S(=O)R. "Сульфонільна" група стосується групи -S(=O)2R. "Тіоалкокси" або "алкілтіо" група стосується -S-алкільної групи. "Алкілтіоалкільна" група стосується алкільної групи, заміщеної -S-алкільною групою. Як він тут використовується, термін "O-карбокси" або "ацилокси" стосується групи формули RC(=O)O-. "Карбокси" означає -C(O)OH радикал. Як він тут використовується, термін "ацетил" стосується групи формули -C(=O)CH3. "Ацил" стосується групи -C(O)R. Як він тут використовується, термін "тригалометансульфоніл" стосується групи формули X3CS(=O)2-, де X є галогеном. Як він тут використовується, термін "ціано" стосується групи формули -CN. "Ціаноалкіл" означає алкільний радикал, як його тут визначено, заміщений щонайменше однією ціано групою. Як він тут використовується, термін "N-сульфонамідо" або "сульфоніламіно" стосується групи формули RS(=O)2NH-. Як він тут використовується, термін "O-карбаміл" стосується групи формули -OC(=O)NR2. Як він тут використовується, термін "N-карбаміл" стосується групи формули ROC(=O)NH-. Як він тут використовується, термін "O-тіокарбаміл" стосується групи формули -OC(=S)NR2. Як він тут використовується, термін "N-тіокарбаміл" стосується групи формули ROC(=S)NH-. Як він тут використовується, термін "C-амідо" стосується групи формули -C(=O)NR2. "Амінокарбоніл" стосується радикалу -CONH2. Як він тут використовується, термін "N-амідо" стосується групи формули RC(=O)NH-. Як вона тут використовується, група заміщення "R", яка з'являється сама по собі і без числового позначення, стосується групи заміщення, вибраної з алкілу, циклоалкілу, арилу, гетероарилу (зв'язаного через кільцевий вуглець) і неароматичного гетероциклу (зв'язаного через кільцевий вуглець). Термін "необов'зково заміщений" або "заміщений" означає, що відповідна група може бути заміщеною однією або більше додатковою групою(ами), окремо і незалежно вибраними з алкілу, циклоалкілу, арилу, гетероарилу, гетероаліциклу, гідрокси, алкокси, арилокси, алкілтіо, арилтіо, алкілсульфоксиду, арилсульфоксиду, алкілсульфону, арилсульфону, ціано, галогену, ацилу, нітро, галогеналкілу, фторалкілу, амінокислоти, включаючи моно- і дизаміщені аміногрупи та їх захищені похідні. В якості прикладу необов'зковими групами заміщення можуть бути LsRs, де кожний Ls незалежно вибирається зі зв'язку, -O-, -C(=O)-, -S-, -S (=O)-, -S(=O)2-, NH-, -NHC(O)-, -C(O)NH-, S(=O)2NH-, -NHS(=O)2, -OC(O)NH-, -NHC(O)O-, -(заміщеного або незаміщеного C1-C6 алкілу) або -(заміщеного або незаміщеного С2-С6 алкенілу); і кожний Rs незалежно вибирається з H, (заміщеного або незаміщеного C1-C4 алкілу), (заміщеного або незаміщеного C3-C6 циклоалкілу), гетероарилу або гетероалкілу. Захисні групи, які можуть утворювати захисні похідні вищевказаних груп заміщення, відомі спеціалістам в цій галузі і можуть бути знайдені в посиланнях, таких як Greene and Wuts, вище. Термін "фрагмент акцептору Міхаеля" стосується функціональної групи, яка може брати участь в реакції Міхаеля, в якій утворюється новий ковалентний зв'язок між частиною фрагмента акцептору Міхаеля і донорського фрагмента. Фрагмент акцептору Міхаеля є електрофілом, а "донорський фрагмент" є нуклеофілом. Термін "нуклеофіл" або "нуклеофільний" стосується багатої електронами сполуки або їїфрагмента. Приклад нуклеофілу включає, жодним чином не обмежуючись ним, цистеїновий залишок молекули, такий як, наприклад, Cys 481 Btk. 14 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 Термін "електрофіл" або "електрофільний" стосується бідної електронами або електрондефіцитної молекули або її фрагмента. Приклади електрофілів включають, жодним чином не обмежуючись ними, фрагменти акцепторів Міхаеля. Термін "прийнятний" або "фармацевтично прийнятний" по відношенню до препарату, композиції або інгредієнту, як він тут використовується, означає, що вони не чинять стійкого негативного впливу на загальний стан здоров'я пацієнта, якого лічать, або не анулює біологічну активність або властивості сполуки і є відносно нетоксичним. "Біомаркери B-клітинних лімфопроліферативних захворювань (BCLD)», як цей термін тут використовується, стосується будь-якої біологічної молекули (яка знаходиться в крові, в інших рідинах організму або в тканинах) або будь-якої хромосомної аномалії, що є ознакою пов'язаного з BCLD стану або захворювання. "Пухлина", як цей термін тут використовується, стосується всякого росту і проліферації неопластичних клітин незалежно від того, або є вони злоякісними або доброякісними, і всіх передракових і ракових клітин і тканин. "Неопластичний", як цей термін тут використовується, стосується будь-якої форми розрегульованого або нерегульованого росту клітин незалежно від того, злоякісні вони або доброякісні, який призводить до аномального росту тканини. Таким чином, "неопластичні клітини" включають злоякісні і доброякісні клітини з розрегульованим або нерегульованим ростом. Терміни "рак" і "раковий" стосуються або описують фізіологічний стан у ссавців, який звичайно характеризується неконтрольованим ростом клітин. Приклади раку включають, не обмежуючись ними, B-клітинні лімфопроліферативні захворювання (BCLD), такі як лімфомі і лейкоз, і солідні пухлини. Під "раком, пов'язаним з В-клітинами" або "раком B-клітинної лінії" розуміють будь-який тип раку, в якому розрегульований або нерегульований ріст клітин є пов'язаним з В-клітинами. Під "рефрактерним" в контексті раку розуміють конкретний рак, що є стійким до терапії або не відповідає на терапію конкретним терапевтичним агентом. Рак може бути рефрактерним до терапії конкретним терапевтичним агентом або з початку лікування цим конкретним терапевтичним агентом (тобто, не реагує на початкову дію терапевтичного агента), або в результаті розвитку резистентності до терапевтичного агента, або впродовж першого періоду лікування терапевтичним агентом, або під час наступного періоду лікування терапевтичним агентом. Під "агоністичною активністю" розуміється, що дана речовина функціонує як агоніст. Агоніст приєднується до рецептора на клітині та ініціює реакцію або активність, яка подібна або така сама, що й ініційована натуральним лігандом цього рецептора. Під "антагоністичною активністю" розуміється, що дана речовина функціонує як антагоніст. Антагоніст Btk попереджує або зменшує індукцію будь-якої реакції, опосередкованої Btk. Під "суттєвою" агоністичною активністю розуміється активність, яка щонайменше на 30 %, 35 %, 40 %, 45 %, 50 %, 60 %, 70 %, 75 %, 80 %, 85 %, 90 %, 95 % або 100 % більша, ніж викликана нейтральною речовиною або негативним контролем агоністична активність, визначена в аналізі реакції В-клітин. Переважно, "суттєва" агоністична активність є активністю, яка щонайменше в 2 рази більша або щонайменше в 3 рази більша, ніж викликана нейтральною речовиною або негативним контролем агоністична активність, визначена в аналізі реакції Вклітин. Так, наприклад, коли реакцією B-клітин, що становить інтерес, є проліферація B-клітин, "суттєва" агоністична активність буде викликати рівень проліферації B-клітин, який щонайменше в 2 рази вищий або щонайменше в 3 рази вищий, ніж рівень проліферації B-клітин, викликаної нейтральною речовиною або негативним контролем. Речовина, "вільна від суттєвої агоністичної активності", буде проявляти агоністичну активність не більшу ніж на біля 25 % більшу, ніж агоністична активність, викликана нейтральною речовиною або негативним контролем, переважно не більше ніж на біля 20 % більшу, на біля 15 % більшу, на біля 10 % більшу, на біля 5 % більшу, на біля 1 % більшу, на біля 0,5 % більшу або навіть не більше ніж на біля 0,1 % більшу, ніж агоністична активність, викликана нейтральною речовиною або негативним контролем, визначена в аналізі реакції Вклітин. В певних варіантах здійснення цього винаходу терапевтичним агентом-інгібітором Btk є антагоністичне антитіло до Btk. Такі антитіла є вільними від суттєвої агоністичної активності, як зазначалось вище, коли зв'язуються з антигеном Btk в клітині людини. В одному варіанті здійснення цього винаходу антагоністичне антитіло до Btk є вільним від суттєвої агоністичної активності в одній клітинній відповіді. В іншому варіанті здійснення цього винаходу антагоністичне анти-Btk антитіло є вільним від суттєвої агоністичної активності в аналізах 15 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 більше ніж одній клітинній відповіді (наприклад, проліферації і диференціації, або проліферації, диференціації і, для В-клітин, утворення антитіл). Під "опосередкованою Btk сигналізацією" розуміються будь-які біологічні активності, які прямо або непрямо залежать від активності Btk. Прикладами опосередкованої Btk сигналізації є сигнали, які приводять до проліферації і виживання клітин, що експресують Btk, і стимуляції одного або більше Btk-сигнальних шляхів в клітинах, що експресують Btk. Терміни "сигнальний шлях" або "шлях передачі сигналів" Btk призначені для позначення щонайменше однієї біохімічної реакції або групи біохімічних реакцій, які є результатом активності Btk і які генерують такий сигнал, який, коли передається по сигнальному шляху, приводить до активації однієї або більше подальших молекул в сигнальному каскаді. Шляхи передачі сигналів включають низку молекул, що забезпечують передачу сигналу від поверхні клітини через плазматичну мембрану клітини і через одну або більше послідовних молекул, що передають сигнали, через цитоплазму клітини і, в певних випадках, в ядро клітини. Особливо цікавими для даного винаходу є шляхи передачі сигналів Btk, які в кінцевому рахунку регулюють (посилюють або пригнічують) активацію NF-kB через сигнальний шлях NF-kB. Способи за даним винаходом спрямовані на лікування раку і в певних варіантах здійснення використовують антитіла для визначення експресії або наявності певних біомаркерів BCLD в цих способах. Для таких антитіл застосовуються наступні терміни і визначення. "Антитіла" і "імуноглобуліни" (Ig) представляють собою глікопротеїни, що мають однакові структурні характеристики. Ці терміни використовуються як синоніми. В певних випадках антигенна специфічність імуноглобуліну може бути відомою. Термін "антитіло" використовується в широкому смислі і охоплює повністю зібрані антитіла, фрагменти антитіл, які можуть зв'язувати антиген (наприклад, Fab, F(ab') 2, Fv, одноланцюгові антитіла, діатіла, химери антитіл, гібридні антитіла, біспецифічні антитіла, гуманізовані антитіла і т.п.) і рекомбінантні пептиди, що містять згадане вище. Терміни "моноклональне антитіло" і "mAb", як вони тут використовуються, стосуються антитіла, отриманого з по суті гомогенної популяції антитіл, тобто індивідуальні антитіла, які складають популяцію, є ідентичними, за виключенням можливих природних мутацій, що можуть бути присутніми в незначних кількостях. "Нативні антитіла" і "нативні імуноглобуліни" представляють собою, як правило, гетеротетрамерні глікопротеїни близько 150000 дальтонів, що складаються з двох ідентичних легких (L) ланцюгів і двох ідентичних важких (H) ланцюгів. Кожний легкий ланцюг є зв'язаним з важким ланцюгом одним ковалентним дисульфідним зв'язком, тоді як число дисульфідних зв'язків не є постійним серед важких ланцюгів різних ізотипів імуноглобулінів. Кожний важкий і легкий ланцюг має також регулярно розміщені всередині ланцюгів дисульфідні містки. Кожний важкий ланцюг має на одному кінці варіабельний домен (V H), за яким слідує низка постійних доменів. Кожний легкий ланцюг має варіабельний домен на одному кінці (V L) і постійний домен на своєму іншому кінці; постійний домен легкого ланцюга знаходиться на одній лінії з першим постійним доменом важкого ланцюга, и варіабельний домен легкого ланцюга знаходиться на одній лінії з варіабельним доменом важкого ланцюга. Вважається, що конкретні амінокислотні залишки утворюють інтерфейс між варіабельними доменами легкого і важкого ланцюгів. Термін "варіабельний" стосується тієї обставини, що певні частини варіабельних доменів значно відрізняються за послідовністю серед антитіл. Варіабельні ділянки визначають специфічність щодо зв'язування з антигеном. Однак варіабельність є розподіленою нерівномірно по варіабельним доменам антитіл. Вона сконцентрована в трьох сегментах, які називають ділянками, які визначають комплементарність (CDR), або гіперваріабельними ділянками в варіабельних доменах як легкого ланцюга, так і важкого ланцюга. Більше збережені частини варіабельних доменів поміщені в каркасні (FR) ділянки. Варіабельні домени нативних важкого і легкого ланцюгів кожний містять чотири FR ділянки, які значною мірою приймають βскладчасту листову конфігурацію, з'єднані трьома CDR, які утворюють петлі, що з'єднують, а в певних випадках утворюють частину β-складчастої листової структури. CDR в кожному ланцюзі утримуються разом в безпосередній близькості FR ділянками і разом з CDR з другого ланцюга сприяють формуванню антигензв'язуючого сайту антитіл (дивись Kabat et al. (1991) NIH PubL. No. 91-3242, Vol. I, pages 647-669). Постійні домени не задіяні безпосередньо в зв'язуванні антитіла з антигеном, але проявляють різні ефекторні функції, такі як зв'язування з Fc рецептором (FcR), участь антитіла в антитіло-залежній клітинній токсичності, ініціювання комплемент-залежної цитотоксичності і дегрануляція тучних клітин. Термін "гіперваріабельна ділянка", як він тут використовується, стосується амінокислотних залишків антитіла, що є відповідальними за зв'язування антигену. Гіперваріабельна ділянка містить амінокислотні залишки з "ділянки, що визначає комплементарність" або "CDR" (тобто, 16 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 залишки 24-34 (L1), 50-56 (L2) і 89-97 (L3) в варіабельному домені легкого ланцюга і 31-35 (H1), 50-65 (Н2) і 95-102 (Н3) в варіабельному домені важкого ланцюга; Kabat et al. (1991) Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institute of Health, Bethesda, Md.), та/або залишки "гіперваріабельної петлі" (тобто, залишки 26-32 (L1), 50-52 (L2) і 91-96 (L3) в варіабельному домені легкого ланцюга і (H1), 53-55 (Н2) в варіабельному домені легкого ланцюга і 96-101 (13) в варіабельному домені важкого ланцюга; Clothia and Lesk, (1987) J. Mol. Biol., 196:901-917). "Каркасні" або "FR" залишки є залишками варіабельного домену, іншими ніж залишки гіперваріабельної ділянки, як тут вважається. "Фрагменти антитіла" являють собою частину інтактного антитіла, переважно антигензв'язуючої або варіабельної ділянки інтактного антитіла. Приклади фрагментів антитіл включають Fab, Fab, Fab, F(ab')2 і Fv фрагменти; діатіла; лінійні антитіла (Zapata et al. (1995) Protein Eng. 10:1057-1062); одноланцюгові молекули антитіл; і мультиспецифічні антитіла, утворені з фрагментів антитіл. Розщеплення папаїном антитіл дає два ідентичні антигензв'язуючі фрагменти, які називаються "Fab" фрагментами, кожний з одним антигензв'язуючий сайтом, і залишковий "Fc" фрагмент, назва якого відображає його здатність легко кристалізуватись. Обробка пепсином дає фрагмент F(ab')2, який має два антигеноб'єднуючих сайти і все ще є здатним до перехресного зшивання антигену. "Fv" являє собою мінімальний фрагмент антитіла, який містить повний сайт розпізнавання і зв'язування антигену. Ця ділянка складається з димера одного варіабельного домену важкого ланцюга і одного варіабельного домену легкого ланцюга в тісному нековалентному зв'язку. Саме в такій конфігурації три CDR кожного варіабельного домену взаємодіють, визначаючи антигензв'язуючий сайт на поверхні VH-VL димера. В сукупності шість CDR надають антитілу його антигензв'язуючу специфічність. Однак навіть єдиний варіабельний домен (або половина Fv, яка містить тільки три CDR, специфічних для антигену) володіє здатністю розпізнавати і зв'язувати антиген, хоча і з меншою афінністю, ніж повний сайт зв'язування. Фрагмент Fab містить також постійний домен легкого ланцюга і перший постійний домен (CH1) важкого ланцюга. Фрагменти Fab відрізняються від фрагментів Fab' додаванням кількох залишків на карбокси-кінці домену важкого ланцюга CH1, включаючи один або більше цистеїнів з шарнірної ділянки антитіла. Fab'-SH є позначенням в цьому документі для Fab', в якому цистеїнові залишки постійних доменів мають вільну тіолову групу. Фрагменти Fab' утворюються шляхом зменшення дисульфідного моста важкого ланцюга фрагмента F(аb')2. Відомі також інші хімічні сполучення фрагментів антитіл. "Легкі ланцюги" антитіл (імуноглобулінів) від будь-яких видів хребетних можуть бути віднесені до одного з двох чітко відмінних типів, які називаються каппа (k) і лямбда (λ), на основі амінокислотних послідовностей їх постійних доменів. В залежності від амінокислотної послідовності постійного домену їх важких ланцюгів імуноглобуліни можуть бути віднесені до різних класів. Існують п'ять основних класів імуноглобулінів людини: IgA, IgD, IgE, IgG і IgM, і певні з них можуть бути поділені далі на підкласи (ізотипи), наприклад IgG1, IgG2, IgG3, IgG4, IgA1 і IgA2. Постійні домени важкого ланцюга, які відповідають різним класам імуноглобулінів, називаються альфа, дельта, епсілон, гамма і мю, відповідно. Структури субодиниць і трьохмірні конфігурації різних класів імуноглобулінів є добре відомими. Різні ізотипи мають різні ефекторні функції. Наприклад, ізотипи IgG1 и IgG3 людини мають активність ADCC (антитіло-залежну, опосередковану клітинами цитотоксичність). Слово "мітка", коли використовується в даному документі, стосується сполуки або композиції, які піддаються виявленню і які сполучені прямо або непрямо з антитілом таким чином, щоб утворилось "мічене" антитіло. Мітка може виявлятись сама по собі (наприклад, радіоізотопні мітки або флуоресцентні мітки) або, у випадку ферментативної мітки, може каталізувати хімічну зміну субстрату (сполуки або композиції), що піддається виявленню. Термін "прийнятний" або "фармацевтично прийнятний" по відношенню до препарату, композиції або інгредієнту, як він тут використовується, означає такий, що не має стійкого негативного впливу на загальний стан здоров'я пацієнта, якого лікують, або не анулює біологічну активність або властивості сполуки і є відносно нетоксичним. Як він тут використовується, термін "агоніст" стосується сполуки, наявність якої має своїм результатом біологічну активність білка, що є такою ж, що й біологічна активність, обумовлена присутністю природного ліганду для цього білка, такого як, наприклад, Btk. Як він тут використовується, термін "частковий агоніст" стосується сполуки, наявність якої має своїм результатом біологічну активність білка, що є того самого типу, що й обумовлена присутністю природного ліганду для цього білка, але менша за величиною. 17 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 Як він тут використовується, термін "антагоніст" стосується сполуки, наявність якої має своїм результатом зменшення величини біологічної активності білка. В певних варіантах здійснення присутність антагоніста має своїм результатом повне пригнічення біологічної активності білка, такого як, наприклад, Btk. В певних варіантах здійснення антагоніст є інгібітором. Термін "тирозинкіназа Брутона (Btk)», як він тут використовується, стосується тирозинкінази Брутона від Homo sapiens, як описано, наприклад, в патенті США № 6326469 (GenBank Accession No. NP_000052). Термін "гомолог тирозинкінази Брутона", як він тут використовується, відноситься до ортологів тирозинкінази Брутона, наприклад до ортологів від миші (GenBank Accession No. AAB47246), собаки (GenBank Accession No. XP_549139.), щура (GenBank Accession No. NP_001007799), курки (GenBank Accession No. NP_989564) або полосатого даніо (GenBank Accession No. XP_698117), і до злитих білків будь-чого з попереднього, які показують активність кінази у відношенні одного або більше субстратів тирозинкінази Брутона (наприклад, пептидного субстрату, що має амінокислотну послідовність "AVLESEEELYSSARQ"). Терміни "спільне введення" або "комбінована терапія" і подібні, як вони тут використовуються, призначені для охоплення введення вибраних терапевтичних агентів одному пацієнту і включають схеми лікування, в яких агенти вводяться однаковим або різними шляхами введення або в один і той самий або різний час. Термін "ефективна кількість", як він тут використовується, стосується достатньої кількості агента-інгібітору Btk або сполуки-інгібітору Btk, яка будучи введеною, приводить до збільшення або появи у крові субпопуляції лімфоцитів (наприклад, фармацевтичної циторепродукції). Наприклад, "ефективна кількість" для діагностичних та/або прогностичних застосувань – це кількість композиції, що включає описану тут сполуку, необхідна для забезпечення клінічно значимого зниження підвищення або появи у крові субпопуляції лімфоцитів без надлишкових несприятливих побічних ефектів. Відповідна "ефективна кількість" в кожному індивідуальному випадку може бути визначена за допомогою методів, таких як дослідження з ескалацією дози. Термін "терапевтично ефективна кількість", як він тут використовується, стосується достатньої кількості агента або сполуки, яка будучи введеною, дозволяє ослабити певною мірою один або більше симптомів В-клітинного лімфопроліферативного розладу (BCLD). Результатом може бути зниження та/або полегшення ознак, симптомів або причин BCLD, або будь-яка інша бажана зміна біологічної системи. Термін "терапевтично ефективна кількість" включає, наприклад, профілактично ефективну кількість. "Ефективна кількість" описаної тут сполуки представляє собою кількість, ефективну для досягнення бажаного фармакологічного результату або терапевтичного покращення без надлишкових несприятливих побічних ефектів. Зрозуміло, що "ефективна кількість" або "терапевтично ефективна кількість" може коливатись від суб'єкта до суб'єкта через коливання в метаболізмі сполуки будь-якої з Формули (А), Формули (B), Формули (C) або Формули (D), в залежності від віку, маси тіла, загального стану суб'єкта, розладу, який лічать, тяжкості розладу, який лічать, і судження лікуючого лікаря. Тільки в якості прикладу, терапевтично ефективна кількість може бути визначена рутинним експериментальним шляхом, включаючи, але не обмежуючись ним, клінічне дослідження з ескалацією дози. Терміни "посилювати" або "посилення" означають збільшення або пролонгацію ефективності або тривалості бажаного ефекту. В якості прикладу, "посилення" ефекту терапевтичних агентів стосується здатності збільшити або пролонгувати активність або тривалість дії терапевтичних агентів під час лікування захворювання, розладу або стану. "Посилююча ефективна кількість", як цей вираз тут використовується, стосується кількості, достатньої для посилення ефекту терапевтичного агента в лікуванні захворювання, розладу або стану. При застосуванні в лікуванні пацієнта кількість, ефективна для цього, буде залежати від тяжкості і перебігу захворювання, розладу або стану, попередньої терапії, стану здоров'я пацієнта і реакції на ліки, а також від судження лікуючого лікаря. Термін "гомологічний цистеїн", як він тут використовується, стосується цистеїнового залишку, який може бути знайдений в позиції послідовності, що є гомологічною позиції цистеїну 481 з тирозинкінази Брутона, як тут визначено. Наприклад, цистеїн 482 є гомологічним цистеїну ортолога щура тирозинкінази Брутона; цистеїн 479 є гомологічним цистеїну ортолога курки; і цистеїн 481 є гомологічним цистеїну ортолога полосатого даніо. В іншому прикладі гомологічним цистеїну TXK, представнику родини Tec-кіназ, спорідненої з тирозинкіназою Брутона, є Cys 350. Дивись також зіставлення послідовностей тирозинкіназ (ТК), опубліковане у всесвітній комп'ютерній мережі на сайті kinase.com/human/kinome/phylogeny.html. 18 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 Термін "ідентичні", як він тут використовується, стосується двох або більше послідовностей або субпослідовностей, що є однаковими. Крім того, термін "суттєво ідентичні", як він тут використовується, стосується двох або більше послідовностей, які мають відсоток послідовних одиниць, що є однаковими при порівнянні і зіставленні для максимального збігу у вікні порівняння або на визначеній ділянці, при визначенні за допомогою алгоритмів порівняння або шляхом ручного зіставлення і візуального огляду. Тільки в якості прикладу, дві або більше послідовностей можуть бути "суттєво ідентичними", коли послідовні одиниці є приблизно на 60 % ідентичними, приблизно на 65 % ідентичними, приблизно на 70 % ідентичними, приблизно на 75 % ідентичними, приблизно на 80 % ідентичними, приблизно на 85 % ідентичними, приблизно на 90 % ідентичними або приблизно на 95 % ідентичними на визначеній ділянці. Такі відсотки описують як "відсоток ідентичності" двох або більше послідовностей. Ідентичність послідовності може існувати на ділянці довжиною щонайменше біля 75-100 послідовних одиниць, на ділянці довжиною щонайменше біля 50 послідовних одиниць, або, коли не уточнено, по всій послідовності. Це визначення стосується також комплементу тестової послідовності. Тільки в якості прикладу, дві або більше поліпептидних послідовностей є ідентичними, коли амінокислотні залишки є однаковими, тоді як дві або більше поліпептидних послідовностей є "суттєво ідентичними", коли амінокислотні залишки є ідентичними приблизно на 60 %, ідентичними приблизно на 65 %, ідентичними приблизно на 70 %, ідентичними приблизно на 75 %, ідентичними приблизно на 80 %, ідентичними приблизно на 85 %, ідентичними приблизно на 90 % або ідентичними приблизно на 95 % на визначеній ділянці. Ідентичність може існувати на ділянці довжиною щонайменше біля 75-100 амінокислот, на ділянці довжиною щонайменше біля 50 амінокислот, або, коли не уточнено, по всій довжині поліпептидної послідовності. Терміни "пригнічує", "пригнічення" або "інгібітор" кінази, як вони тут використовується, стосуються пригнічення ферментативної активності фосфотрансферази. Термін "необоротний інгібітор", як він тут використовується, стосується сполуки, яка при контакті з білком-мішенню (наприклад, кіназою) викликає утворення нового ковалентного зв'язку з білком або в білку, внаслідок чого одна або більше біологічних активностей білка-мішені (наприклад, активність фосфотрансферази) зменшується або пропадає незалежно від наступної присутності або відсутності необоротного інгібітору. Термін "необоротний інгібітор Btk", як він тут використовується, стосується інгібітору Btk, який може утворювати ковалентний зв'язок з амінокислотним залишком Btk. В одному варіанті здійснення цього винаходу необоротний інгібітор Btk може утворювати ковалентний зв'язок з Cys залишком Btk; в конкретних варіантах здійснення необоротний інгібітор може утворювати ковалентний зв'язок з Cys 481 залишком (чи його гомологом) Btk або цистеїновим остатком в гомологічно відповідній позиції іншої тирозинкінази. Термін "виділений", як він тут використовується, стосується відділення і видалення компонента, що становить інтерес, з нецільових компонентів. Виділені речовини можуть бути в сухому або в напівсухому стані або в розчині, включаючи, але не обмежуючись ним, водний розчин. Виділений компонент може бути в гомогенному стані або виділений компонент може бути частиною фармацевтичної композиції, яка включає додаткові, фармацевтично прийнятні носії та/або допоміжні речовини. Тільки в якості прикладу, нуклеїнові кислоти або білки є "виділеними", коли такі нуклеїнові кислоти або білки вільні від щонайменше деяких клітинних компонентів, з якими вони асоціюються в природному стані, або коли такі нуклеїнові кислоти або білки сконцентровані до рівня, вищого, ніж їх концентрація in vivo або продукція in vitro. Крім того, в якості прикладу, ген є виділеним, коли він відділений від відкритих рамок зчитування, які фланкують цей ген і кодують білок, інший ніж ген, що становить інтерес. "Метаболіт" описаної тут сполуки є похідним тієї сполуки, яка утворюється, коли ця сполука метаболізується. Термін "активний метаболіт" стосується біологічно активного похідного сполуки, яка утворюється, коли дана сполука метаболізується. Термін "метаболізований", як він тут використовується, стосується суми процесів (включаючи, але не обмежуючись ними, реакції гідролізу і реакції, каталізовані ферментами, такі як реакції окислення), в яких конкретна речовина змінюється організмом. Таким чином, ферменти можуть викликати специфічні структурні зміни в сполуці. Наприклад, цитохром Р450 каталізує низку окислювальних і відновлювальних реакцій, тоді як уридиндифосфат глюкуронілтрансферази каталізують перенесення активованої молекули глюкуронової кислоти в ароматичні спирти, аліфатичні спирти, карбонові кислоти, аміни і вільні сульфгідрильні групи. Додаткову інформація з метаболізму можна отримати з The Pharmacological Basis of Therapeutics, 9th Edition, McGrawHill (1996). Метаболіти описаних тут сполук можуть бути ідентифіковані шляхом введення сполук хазяїну і аналізу зразків тканини від хазяїна або шляхом інкубації сполук з клітинами 19 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 печінки in vitro і аналізу отриманих сполук. Обидва методи є добре відомими в даній галузі. В певних варіантах здійснення цього винаходу метаболіти сполуки утворюються в окислювальних процесах і відповідають відповідній сполуці, що містить групу гідрокси. В певних варіантах здійснення сполука метаболізується до фармакологічно активних метаболітів. Термін "модулювати", як він тут використовується, означає взаємодіяти з мішенню прямо або непрямо, з тим щоб змінити активність мішені, включаючи, тільки в якості прикладу, підвищення активності мішені, пригнічення активності мішені, обмеження активності мішені або розширення активності мішені. Як він тут використовується, термін "модулятор" стосується сполуки, яка змінює активність молекули. Наприклад, модулятор може викликати збільшення або зменшення величини певної активності молекули у порівнянні з величиною цієї активності за відсутності модулятора. В певних варіантах здійснення цього винаходу модулятор є інгібітором, який зменшує величину однієї або більше активностей молекули. В певних варіантах здійснення інгібітор повністю попереджає одну або більше активність молекули. В певних варіантах здійснення модулятор є активатором, який збільшує величину щонайменше однієї активності молекули. В певних варіантах здійснення присутність модулятора приводить до активності, яка не трапляється за відсутності модулятора. Як він тут використовується, термін "сполука вибіркового зв'язування" стосується сполуки, яка вибірково зв'язується з будь-якою частиною одного або більше білків-мішеней. Як він тут використовується, термін "вибірково зв'язується" стосується здатності сполуки вибіркового зв'язування зв'язуватись с білком-мішенню, таким як, наприклад, Btk, з більшою афінністю, ніж вона зв'язується з нецільовим білком. В певних варіантах здійснення специфічне зв'язування стосується зв'язування з мішенню з афінністю, яка щонайменше в 10, 50, 100, 250, 500, 1000 або більше разів вища, ніж афінність до нецільового білка. Як він тут використовується, термін "селективний модулятор" стосується сполуки, яка вибірково модулює цільову активність відносно нецільової активності. В певних варіантах здійснення специфічний модулятор стосується модуляції цільової активності щонайменше в 10, 50, 100, 250, 500, 1000 разів більше, ніж нецільової активності. Термін "суттєво очищений", як він тут використовується, стосується компоненту, що становить інтерес, який може бути суттєво або практично вільним від інших компонентів, які звичайно супроводжують або впливають на компонент, що становить інтерес, до очистки. Тільки в якості прикладу, компонент, що становить інтерес, може бути "суттєво очищеним", коли препарат компоненту, що становить інтерес, містить менше ніж біля 30 %, менше ніж біля 25 %, менше ніж біля 20 %, менше ніж біля 15 %, менше ніж біля 10 %, менше ніж біля 5 %, менше ніж біля 4 %, менше ніж біля 3 %, менше ніж біля 2 % або менше ніж біля 1 % (сухої ваги) компонентів, що є контамінантами. Таким чином, "суттєво очищений" компонент, що становить інтерес, може мати чистоту біля 70 %, біля 75 %, біля 80 %, біля 85 %, біля 90 %, біля 95 %, біля 96 %, біля 97 %, біля 98 %, біля 99 % або більше. Термін "суб'єкт", як він тут використовується, стосується тварини, яка є об'єктом лікування, спостереження або експерименту. Тільки в якості прикладу, об'єкт може являти собою, без обмеження, ссавця, включаючи, але не обмежуючись, людину. Як він тут використовується, термін "цільова активність" стосується біологічної активності, здатної бути модульованою селективним модулятором. Певні типові форми цільової активності включають, не обмежуючись ними, афінність до зв'язування, передачу сигналів, ферментативну активність, ріст пухлини, вплив на конкретні біомаркери, зв'язані з патологією В-клітинного лімфопроліферативного розладу. Як він тут використовується, термін "білок-мішень" стосується молекули або частини білка, здатної бути зв'язаною сполукою вибіркового зв'язування. В певних варіантах здійснення білком-мішенню є Btk. Терміни "лікувати", "здійснення лікування" або "лікування", як вони тут використовуються, включають полегшення, ослаблення або поліпшення захворювання або стану або їх симптомів; управління захворюванням або станом або їх симптомами; попередження додаткових симптомів; поліпшення або попередження основних метаболічних причин симптомів; пригнічення захворювання або стану, наприклад зупинка розвитку захворювання або стану; полегшення захворювання або стану; викликання регресу захворювання або стану, поліпшення стану, викликаного захворюванням або розладом; або припинення симптомів захворювання або стану. Терміни "лікувати", "здійснення лікування" або "лікування" включають, без обмеження, профілактичне та/або терапевтичне лікування. 20 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 Як тут використовується, IC50 стосується кількості, концентрації або дозування конкретної тестової сполуки, які забезпечують 50 % пригнічення максимальної реакції, такої як пригнічення Btk в аналізі, який вимірює таку реакцію. Як тут використовується, EC50 стосується дозування, концентрації або кількості конкретної тестової сполуки, які викликають дозо-залежну відповідь при 50 % максимального вираження конкретної відповіді, яка викликається, провокується або потенціюється конкретною тестовою сполукою. Гемобластози Описаним тут, в певних варіантах здійснення цього винаходу, є спосіб лікування гемобластозу у індивіда, що того потребує, який включає: (а) введення цьому індивіду кількості необоротного інгібітору Btk, достатньої, щоб мобілізувати певну кількість клітин з гематологічної злоякісної пухлини; і (б) аналіз мобілізованої кількості клітин. В певних варіантах здійснення кількість необоротного інгібітору Btk є достатньою, щоб індукувати лімфоцитоз певної кількості клітин з гематологічної злоякісної пухлини. В певних варіантах здійснення гемобластозом є ХЛЛ. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення концентрації мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після підвищення концентрації мобілізованих клітин в периферичній крові у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку здійснюється після наступного зниження концентрації мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості підвищення концентрації мобілізованих клітин в периферичній крові у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після того, як концентрація мобілізованих клітин в периферичній крові підвищилась впродовж попередньо визначеного періоду часу. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає підрахунок кількості мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку здійснюється після наступного зниження кількості мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості збільшення кількості мобілізованих клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові впродовж попередньо визначеного періоду часу. В певних варіантах здійснення гемобластозом є хронічний лімфоцитарний лейкоз (ХЛЛ), дрібноклітинна лімфоцитарна лімфома (ДЛЛ), ХЛЛ з високим ризиком або неХЛЛ/ДЛЛ лимфома. В певних варіантах здійснення гемобластозом є фолікулярна лімфома, дифузна крупноклітинна В-клітинна лімфома (ДККЛ), лімфома з клітин мантійної зони, макроглобулінемія Вальденстрема, множинна мієлома, лімфома маргінальної зони, лімфома Беркітта, неберкіттівська В-клітинна лімфома високого ступеня або В-клітинна лімфома екстранодальної маргінальної зони. В певних варіантах здійснення гемобластозом є гострий або хронічний мієлогенний (або мієлоїдний) лейкоз, мієлодиспластичний синдром або гострий лімфобластний лейкоз. В певних варіантах здійснення гемобластозом є рецидивна або рефрактерна дифузна крупноклітинна В-клітинна лімфома (ДККЛ), рецидивна або рефрактерна лімфома з клітин мантійної зони, рецидивна або рефрактерна фолікулярна лімфома, рецидивний або рефрактерний ХЛЛ; рецидивна або рефрактерна ДЛЛ; рецидивна або рефрактерна множинна мієлома. В певних варіантах здійснення гемобластозом є гемобластоз, який класифікують як такий з високим ризиком. В певних варіантах здійснення гемобластозом є ХЛЛ з високим ризиком або ДЛЛ з високим ризиком. B-клітинні лімфопроліферативні захворювання (BCLD) являють собою новоутворення крові і охоплюють inter alia неходжкінську лімфому, множинну мієлому і лейкоз. BCLD можуть виникати або в лімфатичних тканинах (як у випадку лімфоми), або в кістковому мозку (як у випадку лейкозу і мієломи), і всі вони пов'язані з неконтрольованим ростом лімфоцитів або білих кров'яних клітин. Існує багато підтипів BCLD, наприклад хронічний лімфоцитарний лейкоз (ХЛЛ) і неходжкінська лімфома (НХЛ). Перебіг хвороби і лікування BCLD залежать від підтипу BCLD; однак навіть в межах кожного підтипу клінічна картина, морфологічний вигляд і реакція на терапію не являються однорідними. Злоякісні лімфоми – це неопластичні зміни клітин, які розміщуються переважно всередині лімфоїдних тканин. Двома групами злоякісних лімфом є лімфома Ходжкіна і неходжкінська 21 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 лімфома (НХЛ). Обидва типи лімфом інфільтрують ретикулоендотеліальні тканини. Однак вони відрізняються походженням неопластичної клітини, місцезнаходженням захворювання, наявністю системних симптомів і реакцією на лікування (Freedman et al., "Non-Hodgkin's Lymphomas" Chapter 134, Cancer Medicine, (an approved publication of the American Cancer Society, B.C. Decker Inc., Hamilton, Ontario, 2003). Неходжкінські лімфоми Описаним тут, в певних варіантах здійснення цього винаходу, є спосіб лікування неходжкінської лімфоми у індивіда, що того потребує, який включає: (а) введення цьому індивіду кількості необоротного інгібітору Btk, достатньої щоб мобілізувати певну кількість клітин із злоякісної пухлини; і (б) аналіз мобілізованої кількості клітин. В певних варіантах здійснення цього винаходу кількість необоротного інгібітору Btk є достатньою, щоб індукувати лімфоцитоз певної кількості клітин із злоякісної пухлини. В певних варіантах здійснення гемобластозом є ХЛЛ. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення концентрації мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення концентрації мобілізованих клітин в периферичній крові у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку здійснюється після наступного зниження концентрації мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості підвищення концентрації мобілізованих клітин в периферичній крові у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після підвищення концентрації мобілізованих клітин в периферичній крові впродовж попередньо визначеного періоду часу. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає підрахунок кількості мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку здійснюється після наступного зниження кількості мобілізованих клітин в периферичній крови. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості підвищення кількості мобілізованих клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові впродовж попередньо визначеного періоду часу. Додатково описаним тут, в певних варіантах здійснення цього винаходу, є спосіб лікування рецидивної або рефрактерної неходжкінської лімфомі у індивіда, що того потребує, який включає: введення цьому індивіду терапевтично ефективної кількості (R)-1-(3-(4-аміно-3-(4феноксифеніл)-1Н-піразоло[3,4-d]піримидин-1-іл)піперидин-1-іл)проп-2-ен-1-ону. В певних варіантах здійснення неходжкінська лімфома є рецидивуною або рефрактерною дифузною крупноклітинною В-клітинною лімфомою (ДККЛ), рецидивною або рефрактерною лімфомою з клітин мантійної зони або рецидивною або рефрактерною фолікулярною лімфомою. Неходжкінські лімфоми (НХЛ) – це різні групи злоякісних пухлин, які переважно беруть своє походження з В-клітин. НХЛ може розвиватись в будь-яких органах, пов'язаних з лімфатичною системою, таких як селезінка, лімфатичні вузли або мигдалини, і може виникати у будь-якому віці. НХЛ часто характеризується збільшеними лімфатичними вузлами, лихоманкою і втратою маси тіла. НХЛ класифікується як В-клітинна або Т-клітинна НХЛ. Лімфоми, пов'язані з лімфопроліферативними розладами після трансплантації кісткового мозку або стовбурових клітин звичайно є В-клітинними НХЛ. В робочій класифікаційній схемі НХЛ поділяють на слабо-, середньо- або сильно виражені категорії в залежності від тяжкості перебігу (дивись "The NonHodgkin's Lymphoma Pathologic Classification Project" Cancer 49(1982):2112-2135). Слабовиражені лімфоми ростуть повільно і характеризуються середнім виживанням від 5 до 10 років (Horning and Rosenberg (1984) N. Engl. J. Med. 311:1471-1475). Хоча хіміотерапія може викликати ремісію при більшості лімфом, які ростуть повільно, виліковування настає рідко і у більшості пацієнтів в кінцевому рахунку відмічається рецидив, який вимагає подальшої терапії. Середньо- і сильно виражені лімфоми є найбільш агресивними пухлинами, але вони мають більший шанс на виліковування хіміотерапією. Однак у значної кількості таких пацієнтів буде наставати рецидив і потребується додаткове лікування. Не обмежуючий перелік В-клітинних НХЛ включає лімфому Беркітта (наприклад, ендемічну лімфому Беркітта і спорадичну лімфому Беркітта), шкірну В-клітинну лімфому, шкірну лімфому маргінальної зони (MZL), дифузну крупноклітинну лімфому (ДККЛ), дифузну змішану дрібно- і 22 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 крупноклітинну лімфому, дифузну дрібноклітинну лімфому з розщепленими ядрами, дифузну дрібноклітинну лімфоцитарну лімфому, В-клітинну екстранодальну лімфому маргінальної зони, фолікулярну лімфому, фолікулярну дрібноклітинну лімфому з розщепленими ядрами (Ступінь 1), фолікулярну змішану дрібноклітинну з розщепленими ядрами і крупноклітинну лімфому (Ступінь 2), фолікулярну крупноклітинну лімфому (Ступінь 3), внутрішньосудинну крупноклітинну В-клітинну лімфому, внутрішньосудинний лімфоматоз, крупноклітинну імунобластну лімфому, крупноклітинну лімфому (ККЛ), лімфобластну лімфому, лімфому типу MALT, лімфому з клітин мантійної зони (МКЛ), імунобластну крупноклітинну лімфому, попередник В-лімфобластної лімфоми, лімфа з клітин мантійної зони, хронічний лімфоцитарний лейкоз (ХЛЛ)/ дрібноклітинну лімфоцитарну лімфому (ДЛЛ), екстранодальну В-клітинну лімфому з клітин маргінальної зони, лімфому лімфоїдної тканини слизових оболонок (MALT), середостінну крупноклітинну Вклітинну лімфому, В-клітинну лімфому маргінальної зони лімфатичних вузлів, В-клітинну лімфому маргінальної зони селезінки, первинну середостінну В-клітинну лімфому, лімфоплазмоз, лейкоз волосистих клітин, макроглобулінемія Вальдернстрема та первинна лімфома центральної нервової системи (ЦНС). Додаткові Неходжкінські лімфоми передбачаються в межах даного винаходу та є очевидними для фахівця в даній галузі. ДККЛ Описаним тут, в певних варіантах здійснення цього винаходу, є спосіб лікування дифузну крупноклітинної лімфоми, у індивіда, що того потребує, який включаює: (а) введення індивіду кількості Btk достатьої, щоб мобілізувати певну кількість клітин із злоякісної пухлини; і (б) аналіз мобілізованої кількості клітин. В певних варіантах здійснення кількість необоротного інгібітору Btk є достатньої для індукування лімфоцитозу певної кількості клітин із злоякісної пухлини. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення в периферичній крові мобілізованої кількості клітин. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після підвищення концентрації мобілізованих клітин в периферичній крові у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку здійснюється після наступного зниження концентрації мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості підвищення концентрації мобілізованих клітин в периферичній крові у порівнянні з концентрацією до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після підвищення концентрації мобілізованих клітин в периферичній крові впродовж наперед визначеного періоду часу. В певних варіантах здійснення аналіз мобілізованих клітин включає підрахунок кількості мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові у порівнянні їх кількістю до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку має місце після наступного зниження кількості мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості підвищення мобілізованої кількості клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові впродовж наперед визначеного періоду часу. Як він тут використовується, термін "дифузна крупноклітинна В-клітинна лімфома (ДККЛ)» стосується неоплазми гермінального центру В-лімфоцитів з дифузною моделлю росту і індексом проліферації вище середнього. Частка ДККЛ становить близько 30 % серед всіх лімфом, і вона може зустрічатись в кількох морфологічних варіантах, включаючи центробластний, імунобластний, Т-клітинний/багатий на гістоцити, анапластичний і плазмобластний підтипи. Генетичні тести показали, що існують різні підтипи ДККЛ. Як гадається, ці підтипи мають різні перспективи (прогнози) і реакцію на лікування. ДККЛ може вражати будь-яку вікову групу, але в більшості випадків виникає у людей старшого віку (середній вік становить середину 60). Описаний тут, в певних варіантах здійснення цього винаходу, є спосіб лікування дифузної крупноклітинної В-клітинної лімфоми активованого, подібного до В-клітинного підтипу (АБКДККЛ) у індивіда, що того потребує, який включає введення цьому індивіду необоротного інгібітору Btk в кількості от 300 мг/день до 1000 мг/день включно. Підтип АБК дифузної крупноклітинної В-клітинної лімфоми (АБК-ДККЛ), як вважається, виникає з постгермінального центру В-клітин, які подавляються в ході плазматичної диференціації. Підтип АБК-ДККЛ (АБКДККЛ) зустрічається приблизно в 30 % всіхдіагнозів ДККЛ. Вважається, що у нього найменша виліковуваність з молекулярних підтипів ДККЛ, і в зв'язку з чим пацієнти з діагнозом АБК-ДККЛ 23 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 звичайно показують значно менше виживання у порівнянні з індивідами з іншими типами ДККЛ. АБК-ДККЛ частіше всього зв'язують з хромосомними транслокаціями, які розрегульовують головний регулятор BCL6 гермінального центру, і з мутаціями, які інактивують ген PRDM1, що кодує репресор транскрипції, потрібний для диференціації плазматичної клітини. Особливо важливим сигнальним шляхом в патогенезі АБК-ДККЛ є шлях, опосередкований ядерним фактором (NF)-kB комплексу транскрипції. Родина NF-kB включає 5 членів (p50, p52, p65, c-rel і RelB), які утворюють гомо- і гетеродимери і функціонують як транскрипційні фактори для опосередкування широкого кола функцій, таких як проліферація, апоптоз, запалення та імунні відповіді, і є вирішальними для нормального розвитку и виживання В-клітини. NF-kB широко використовується евкаріотичними клітинами як регулятор генів, який контролює проліферацію і виживання клітин. В зв'язку з цим багато різних типів пухлин людини мають нерегульований NF-kB: а це означає, що NF-kB є конститутивно активним. Активний NF-kB запускає експресію генів, які тримають клітину в проліферації і захищають клітину від умов, які інакше викликали б її смерть через апоптоз. Залежність АБК-ДККЛ від NF-kB залежить від сигнального шляху проти ходу транскрипції кінази IkB, складеного з CARD11, BCL10 і MALT1 (комплекс CBM). Інтерференція зі шляхом CBM гасить сигнал NF-kB в клітинах АБК-ДККЛ і викликає апоптоз. Молекулярна основа для конститутивної активності шляху NF-kB є предметом дослідження в наш час, але певні соматичні зміни в геномі АБК-ДККЛ достеменно викликають цей шлях. Наприклад, соматичні мутації в спіраль-спіральному домені CARD11 при ДККЛ передають цьому сигнальному каркасному білку здатність спонтанної ядерної білок-білкової взаємодії з MALT1 і BCL10, викликаючи активність IKK і активацію NF-kB. Конститутивна активність сигнального шляху Вклітинного рецептору потягла за собою активацію NF-kB в АБК-ДККЛ с диким типом CARD11, що пов'язано з мутаціями в цитоплазматичних кінцевих сегментах В-клітинних рецепторних субодиниць CD79A і CD79B. Онкогенні активаційні мутації в сигнальному адаптері MYD88 активують NF-kB і є синергічними з В-клітинним рецептором, сигналізуючим для підтримання виживання клітин АБК-ДККЛ. В доповнення до цього, інактивуючі мутації в негативному регуляторі шляху NF-kB, A20 мають місце практично виключно в АБК-ДККЛ. Дійсно, генетичні зміни, які впливають на численні компоненти сигнального шляху NF-kB, недавно були виявлені у більше ніж 50 % пацієнтів с АБК-ДККЛ, у яких ці пошкодження посилюють конститутивну активацію NF-kB, тим самим сприяючи росту лімфоми. Вони включають мутації CARD11 (~10 % випадків), лімфоцит-специфічний цитоплазматичний каркасний білок, який – разом з MALT1 і BCL10 – утворює сигналосому BCR, яка передає сигнали від рецепторів антигенів до медіаторів по ходу транскрипції активації NF-kB. Навіть більша частина випадків (~30 %) переносять біалельні генетичні пошкодження, які інактивують негативний регулятор NF-kB A20. Додатково, високі рівні експресії цільових генів NF-kB спостерігались в пухлинних зразках АБК-ДККЛ. Дивись, наприклад, U. Klein et al., (2008), Nature Reviews Immunology 8:22-23; R.E. Davis et al., (2001), Journal of Experimental Medicine 194:18611874; G. Lentz et al., (2008), Science 319:1676-1679; M. Compagno et al., (2009), Nature 459:712721; та L. Srinivasan et al., (2009), Cell 139:573-586). Клітини ДККЛ підтипу АБК, такі як OCI-Ly10, мають хронічно активну передачу сигналів BCR і є дуже чутливими до інгібіторів Btk, описаних в даному документі. Описані тут необоротні інгібітори Btk сильно і незворотно пригнічують ріст OCI-Ly10 (EC50 при постійній дії = 10 нМ, EC50 1-годинного викиду = 50 нМ). В доповнення до цього, в OCILy10 спостерігається індукція апоптозу, як показано активацією каспази, проточною цитометрією Анексину-V і збільшенням частки суб-G0. Як чутливі, так і резистентні клітини експресують Btk на схожих рівнях, і активний сайт Btk повністю займається інгібітором в обох, як показано з використанням флуоресцентноміченого афінного зонду. Клітини OCI-Ly10, як показано, мають хронічно активну передачу сигналу BCR до NF-kB, який дозо-залежно пригнічується інгібіторами Btk, описаними в даному документі. Активність інгібіторів Btk в клітинних лініях, вивчена тут, також характеризується шляхом порівняння профілів сигнальної трансдукції (Btk, PLCγ, ERK, NF-kB, AKT), профілів виділення цитокінів і профілів експресії мРНК, як зі стимулюванням BCR, так і без нього, і спостерігались значні відмінності в цих профілях, що приводить до клінічних біомаркерів, які ідентифікують найбільш чутливі до лікування інгібітором Btk групи пацієнтів. Дивись Патент США № 7,711,492 і Staudt et al., Nature, Vol. 463, Jan. 7, 2010, pp. 88-92, вміст яких у всій повноті включено сюди за посиланням. Фолікулярна лімфома Описаним тут, в певних варіантах здійснення цього винаходу, є спосіб лікування фолікулярної лімфоми у індивіда, що того потребує, який включає: (а) введення цьому індивіду кількості необоротного інгібітору Btk, достатньої, щоб мобілізувати певну кількість клітин зі 24 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 злоякісної пухлини; і (б) аналіз мобілізованої кількості клітин. В певних варіантах здійснення кількість необоротного інгібітору Btk є достатньою для індукції лімфоцитозу певної кількості клітин зі злоякісної пухлини. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення концентрації мобілізованої кількості клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після підвищення концентрації мобілізованих клітин в периферичній крові у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку призначається після зниження концентрації мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості підвищення мобілізованої кількості клітин в периферичній крові у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після того, як концентрація мобілізованих клітин в периферичній крові збільшилась впродовж попередньо визначеного періоду часу. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає підрахунок кількості мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після підвищення кількості мобілізованих клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку призначається після наступного зниження кількості мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості підвищення кількості мобілізованих клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові впродовж попередньо визначеного періоду часу. Як він тут використовується, термін "фолікулярна лімфома" стосується будь-якого з кількох типів неходжкінської лімфоми, при якому лімфоматозні клітини утворюють скупчення у вузлах або фолікулах. Термін фолікулярна використовується постільки, по скільки клітини мають тенденцію до росту в лімфатичних вузлах у вигляді головним чином кругових або вузлових утворень. Середній вік людей з такою лімфомою становить біля 60 років. ХЛЛ/ДЛЛ Розкритим тут, в певних варіантах здійснення, є спосіб лікування ХЛЛ або ДЛЛ у індивіда, що того потребує, який включає: (а) введення цьому індивіду кількості незворотного інгібітору Btk, достатньої, щоб мобілізувати певну кількість клітин зі злоякісної пухлини; і (б) аналіз мобілізованої кількості клітин. В певних варіантах здійснення ХЛЛ и ДЛЛ асоціюються з високим ризиком. В певних варіантах здійснення кількість незворотного інгібітору Btk є достатньою для стимулювання лімфоцитозу певної кількості клітин зі злоякісної пухлини. В певних варіантах здійснення аналіз мобілізованих клітин включає визначення концентрації мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після підвищення концентрації мобілізованих клітин в периферичній крові у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку передбачають після наступного зниження концентрації мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованих клітин включає визначення тривалості підвищення концентрації мобілізованих клітин в периферичній крові у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після того, як концентрація мобілізованих клітин в периферичній крові підвищилась впродовж попередньо визначеного періоду часу. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає підрахунок кількості мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку передбачається після наступного зниження кількості мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості підвищення кількості мобілізованих клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові впродовж попередньо визначеного періоду часу. Хронічний лімфоцитарний лейкоз і дрібноклітинна лімфоцитарна лімфома (ХЛЛ/ДЛЛ) звичайно вважаються одним захворюванням з незначними відмінностями в проявах. Місце накопичення злоякісних клітин визначає назву - або ХЛЛ, або ДЛЛ. Коли ракові клітини в первую 25 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 чергу виявляються в лімфатичних вузлах, у вигляді структур форми лімської квасолі в лімфатичній системі (яка має вигляд системи тонких судин в організмі), це називається ДЛЛ. На долю ДЛЛ приходиться приблизно від 5 % до 10 % всіх лімфом. Коли більшість ракових клітин знаходиться в потоці крові і кістковому мозку, це називається ХЛЛ. Як ХЛЛ, так і ДЛЛ є захворюваннями, що розвиваються повільно, хоча ХЛЛ, який є значно більше поширеним, має тенденцію до більш повільного розвитку. ХЛЛ і ДЛЛ лікуються однаково. Вони звичайно не вважаються виліковними стандартними методами, але в залежності від стадії і швидкості розвитку захворювання більшість пацієнтів проживають довше 10 років. Деколи з часом ці лімфоми повільного розвитку можуть трансформуватись в більш агресивний тип лімфоми. Хронічний лімфоїдний лейкоз (ХЛЛ) є найбільш типовим типом лейкозу. За оцінкою, 100760 людей в Сполучених Штатах живуть з ХЛЛ або мають ремісію. Більшість (>75 %) людей, у яких вперше діагностували ХЛЛ, мають вік понад 50 років. В теперішній час лікування ХЛЛ є спрямованим швидше на контролювання захворювання і його симптомів, ніж на повне виліковування. ХЛЛ лікується хіміотерапією, радіотерапією, біологічною терапією або трансплантацією кісткового мозку. Симптоми деколи лічать хірургічно (спленектомією – видаленням збільшеної селезінки) або радіотерапією ("циторедукцією" опухлих лімфатичних вузлів). Хоча ХЛЛ прогресує повільно в більшості випадків, його звичайно вважають невиліковним. Певні ХЛЛ класифікують як такі, що асоціюються з високим ризиком. Як цей термін тут використовується, "ХЛЛ з високим ризиком" означає ХЛЛ, який характеризується щонайменше одним з наступного: 1) 17p13-; 2) 11q22-; 3) немутованим IgVH разом з ZAP-70+ та/або CD38+; або 4) трисомією 12. Лікування ХЛЛ звичайно проводять, коли клінічні симптоми пацієнта або аналізи крові показують, що захворювання прогресувало до точки, в якій воно може впливати на якість життя пацієнта. Дрібноклітинна лімфоцитарна лімфома (ДЛЛ) є дуже подібною до вищеописаної ХЛЛ і теж являє собою рак B-клітин. При ДЛЛ аномальні лімфоцити головним чином вражають лімфатичні вузли. Однак при ХЛЛ аномальні клітини головним чином вражають кров і кістковий мозок. Селезінка може бути враженою при обох станах. Частка ДЛЛ становить біля 1 на 25 всіх випадків неходжкінської лімфоми. Вона може траплятись в будь-якому віці від юності до старості, але рідко до 50 років. ДЛЛ вважається лімфомою, що росте повільно. Це означає, що захворювання прогресує дуже повільно, і пацієнти звичайно живуть багато років після постановки діагнозу. Однак у більшості пацієнтів діагностують вже запущене захворювання, і хоча ДЛЛ добре реагує на різні хіміотерапевтичні препарати, як правило, вона вважається невиліковною. Хоча певні види раку мають тенденцію частіше виникати у представників однієї статі ніж у іншої, випадки захворювання і смерті у зв'язку з ДЛЛ є рівномірно розподіленими між чоловіками і жінками. Середній вік на момент постановки діагнозу становить 60 років. Хоча ДЛЛ росте повільно, вона постійно прогресує. Звичайною картиною цього захворювання є високий показник відповіді на радіотерапію та/або хіміотерапію з періодом ремісії захворювання. Далі, через місяці або роки невідворотно слідує рецидив. Повторне лікування знову приводить до відповіді, але захворювання знову буде рецидивувати. Це означає, що хоча короткостроковий прогноз ДЛЛ є доволі сприятливим, з часом у багатьох пацієнтів розвиваються смертельні ускладнення рецидивуючого захворювання. Враховуючи вік індивідів, у яких звичайно діагностують ХЛЛ і ДЛЛ, в даній галузі існує нагальна потреба в простому і ефективному лікуванні цього захворювання з мінімальними побічними ефектами, яке б не погіршувало якість життя пацієнта. Даний винахід задовольняє цю давно існуючу потребу. Лімфома з Клітин Мантійної Зони Описаним тут, в певних варіантах здійснення цього винаходу, є спосіб лікування лімфоми з клітин мантійної зони у індивіда, що потребує того, який включає: (а) введення цьому індивіду кількості незворотного інгібітору Btk, достатньої, щоб мобілізувати певну кількість клітин зі злоякісної пухлини; і (б) аналіз мобілізованої кількості клітин. В певних варіантах здійснення кількість незворотного інгібітору Btk є достатньою для стимулювання лімфоцитозу певної кількості клітин зі злоякісної пухлини. В певних варіантах здійснення аналіз мобілізованих клітин включає визначення концентрації мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після підвищення концентрації мобілізованих клітин в периферичній крові у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку передбачають після наступного зниження концентрації мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості підвищення кількості мобілізованих клітин в периферичній крові 26 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після підвищення концентрації мобілізованих клітин в периферичній крові впродовж попередньо визначеного періоду часу. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає підрахунок кількості мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після підвищення кількості мобілізованих клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку передбачають після наступного зниження кількості мобілізованих клітин в периферичній кров. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості підвищення кількості мобілізованих клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові впродовж попередньо визначеного періоду часу. Як він тут використовується, термін "лімфома з клітин мантійної зони" стосується підтипу Bклітинної лімфоми, пов'язаної з В-клітинним CD5-позитивним антиген-наївним прегермінальним центром в межах мантійної зони, яка оточує фолікули нормального гермінального центра. Клітини MCL звичайно надекспресують циклін D1 в зв'язку з хромосомною транслокацією t(11:14) в ДНК. Більш конкретно, транслокація знаходиться при t(11;14) (q13;q32). Тільки біля 5 % лімфом відносяться до цього типу. Клітини мають розмір від малого до середнього. Чоловіки страждають частіше. Середній вік пацієнтів становить трохи за 60. Лімфома звичайно вже є широко поширеною, коли її діагностують, включаючи лімфатичні вузли, кістковий мозок і дуже часто селезінку. Лімфома з клітин мантійної зони є не дуже швидкого росту, але важко піддається лікуванню. В-клітинна Лімфома Маргінальної Зони Описаним тут, в певних варіантах здійснення цього винаходу, є спосіб лікування В-клітинної лімфоми маргінальної зони у індивіда, що того потребує, який включає: (а) введення цьому індивіду кількості незворотного інгібітору Btk, достатньої, щоб мобілізувати певну кількість клітин зі злоякісної пухлини; і (б) аналіз мобілізованої кількості клітин. В певних варіантах здійснення кількість незворотного інгібітору Btk є достатньою для стимулювання лімфоцитозу певної кількості клітин зі злоякісної пухлини. В певних варіантах здійснення аналіз мобілізованих клітин включає визначення концентрації мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після підвищення концентрації мобілізованих клітин в периферичній крові у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку передбачають після наступного зниження концентрації мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості підвищення кількості мобілізованих клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після підвищення концентрації мобілізованих клітин в периферичній крові впродовж попередньо визначеного періоду часу. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає підрахунок кількості мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку передбачається після наступного зниження кількості мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості збільшення кількості мобілізованих клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові впродовж попередньо визначеного періоду часу. Як він тут використовується, термін "B-клітинна лімфома маргінальної зони" стосується групи зв'язаних з B-клітинами новоутворень, які вражають лімфоїдні тканини в маргінальній зоні, клаптевій ділянці за межами фолікулярної мантійної зони. Лімфоми маргінальної зони становлять приблизно від 5 % до 10 % всіх лімфом. Під мікроскопом клітини в цих лімфомах виглядять маленькими. Існують 3 основних типи лимфом маргінальної зони, включаючи Bклітинні екстранодальні лімфоми маргінальної зони, В-клітинну нодальну лімфому маргінальної зони і лімфому маргінальної зони селезінки. MALT (асоційована зі слизовою оболонкою лімфома лімфоїдної тканини) 27 UA 107707 C2 5 10 15 20 25 30 35 40 45 50 55 60 Описаним тут, в певних варіантах здійснення цього винаходу, є спосіб лікування MALT у індивіда, що того потребує, який включає: (а) введення цьому індивіду кількості незворотного інгібітору Btk, достатньої, щоб мобілізувати певну кількість клітин зі злоякісної пухлини; і (б) аналіз мобілізованої кількості клітин. В певних варіантах здійснення кількість незворотного інгібітору Btk є достатньою для стимулювання лімфоцитозу певної кількості клітин зі злоякісної пухлини. В певних варіантах здійснення аналіз мобілізованих клітин включає визначення концентрації мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після підвищення концентрації мобілізованих клітин в периферичній крові у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку передбачається після наступного зниження концентрації мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості підвищення концентрації мобілізованих клітин в периферичній крові у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові впродовж попередньо визначеного періоду часу. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає підрахунок кількості мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку передбачається після наступного зниження кількості мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості збільшення кількості мобілізованих клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові впродовж попередньо визначеного періоду часу. Термін "лімфома лімфоїдної тканини слизових оболонок (MALT)», як він тут використовується, стосується екстранодальних проявів лімфом маргінальної зони. Більшість лімфом MALT є лімфомами низького ступеня, хоча меншість або проявляє спочатку проміжний ступінь неходжкінської лімфоми (НХЛ), або розвивається з форми низького ступеня. Більшість лімфом MALT зустрічаються у шлунку, і приблизно 70 % шлункових лімфом MALT зв'язані з інфекцією Helicobacter pylori. Були виявлені певні цитогенетичні аномалії, причому найбільш поширеною є трисомія 3 або t(11;18). Багато які з цих інших лімфом MALT також пов'язувались з інфекціями бактеріями або вірусами. Середній вік пацієнтів з MALT лімфомою становить біля 60 років. В-клітинна Нодальна Лімфома Маргінальної Зони Описаним тут, в певних варіантах здійснення цього винаходу, є спосіб лікування В-клітинної нодальної лімфоми маргінальної зони у індивіда, що того потребує, який включає: (а) введення цьому індивіду кількості незворотного інгібітору Btk, достатньої, щоб мобілізувати певну кількість клітин зі злоякісної пухлини; і (б) аналіз мобілізованої кількості клітин. В певних варіантах здійснення кількість незворотного інгібітору Btk є достатньою для стимулювання лімфоцитозу певної кількості клітин зі злоякісної пухлини. В певних варіантах здійснення аналіз мобілізованих клітин включає визначення концентрації мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після підвищення концентрації мобілізованих клітин в периферичній крові у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку передбачається після наступного зниження концентрації мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення тривалості підвищення концентрації мобілізованих клітин в периферичній крові у порівнянні з їх концентрацією до введення інгібітору Btk. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові впродовж попередньо визначеного періоду часу. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає підрахунок кількості мобілізованих клітин в периферичній крові. В певних варіантах здійснення спосіб додатково включає введення другої схеми лікування раку після збільшення кількості мобілізованих клітин в периферичній крові у порівнянні з їх кількістю до введення інгібітору Btk. В певних варіантах здійснення введення другої схеми лікування раку передбачається після наступного зниження кількості мобілізованих клітин в периферичній крові. В певних варіантах здійснення аналіз мобілізованої кількості клітин включає визначення 28
ДивитисяДодаткова інформація
Назва патенту англійськоюThe use of inhibitors of bruton's tyrosine kinase (btk)
Автори англійськоюBuggy, Joseph, J., Elias, Laurence, Fyfe, Gwen, Hedrick, Eric, Loury, David, J., Mody, Tarak, D.
Автори російськоюБагги Джозеф Дж., Элиас Лоренс, Файф Гвэн, Хедрик Эрик, Лоури Дэвид Дж., Моди Тарак Д.
МПК / Мітки
МПК: A61K 31/519, A61K 31/505, A61P 35/02
Мітки: втк, брутона, інгібіторів, застосування, тирозинкінази
Код посилання
<a href="https://ua.patents.su/121-107707-zastosuvannya-ingibitoriv-tirozinkinazi-brutona-vtk.html" target="_blank" rel="follow" title="База патентів України">Застосування інгібіторів тирозинкінази брутона (втк)</a>
Попередній патент: Апоптоз-індукуючий засіб для лікування раку й імунних і аутоімунних захворювань
Наступний патент: Спосіб діагностики злоякісних пухлин передміхурової залози
Випадковий патент: Шахтна піч безкоксового одержання металу












