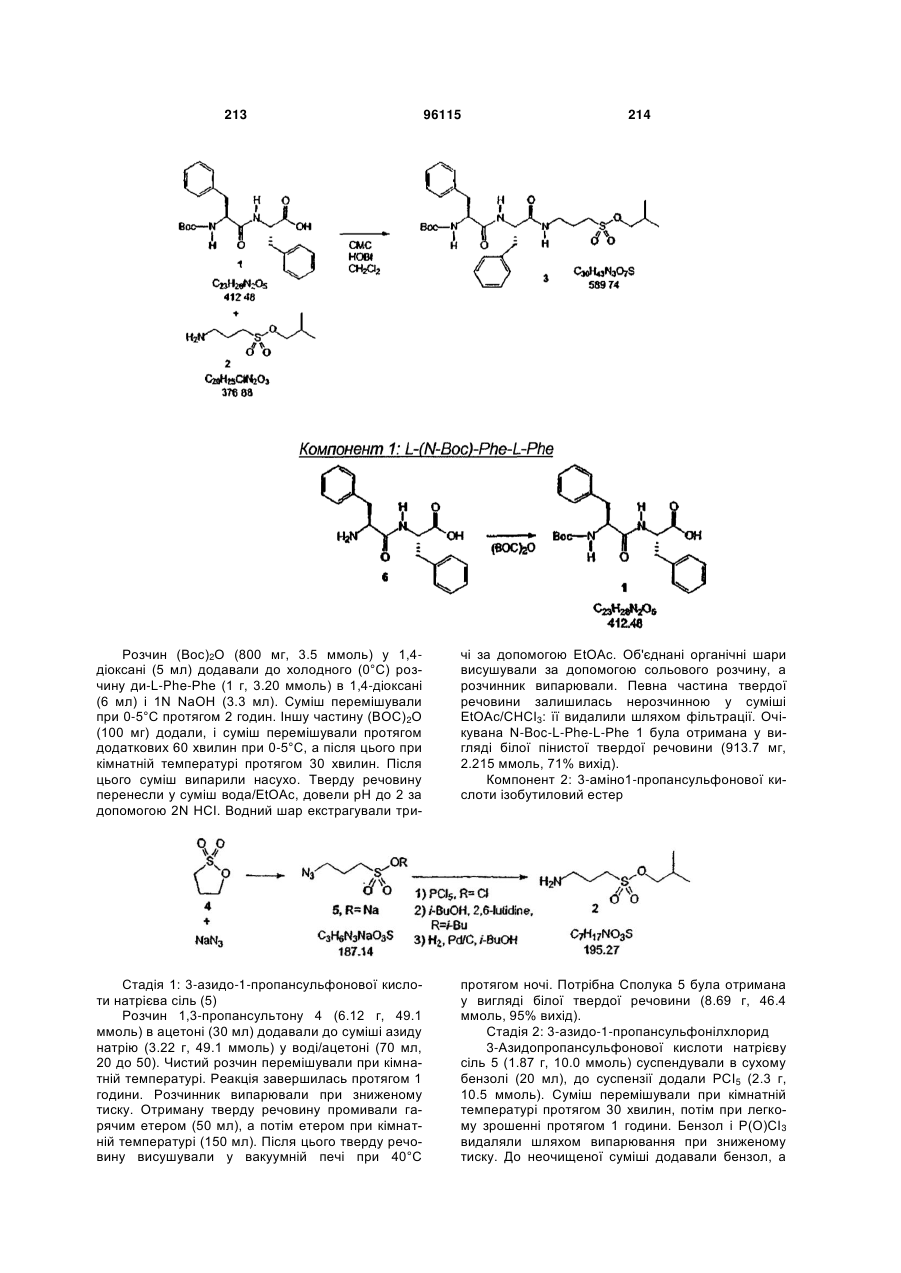
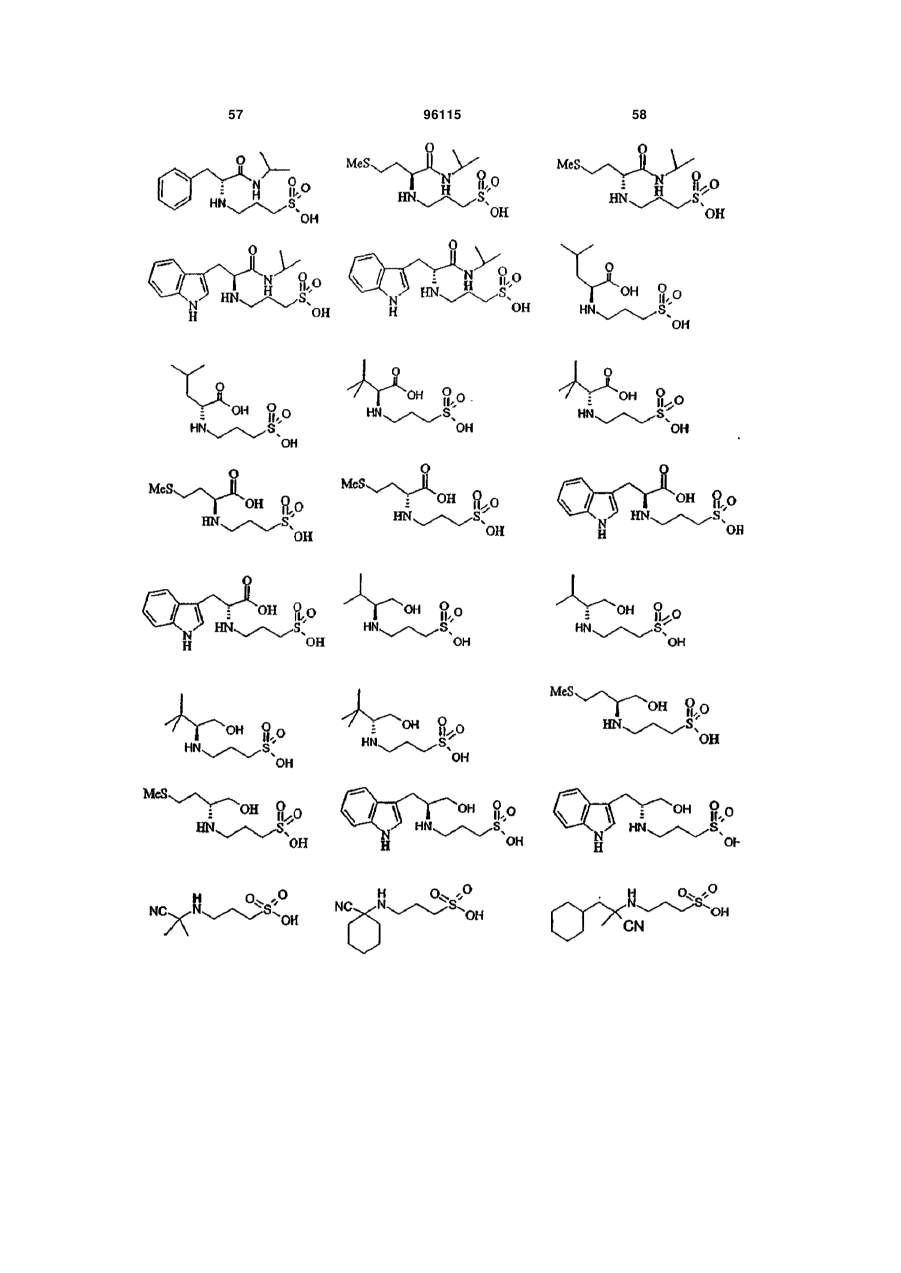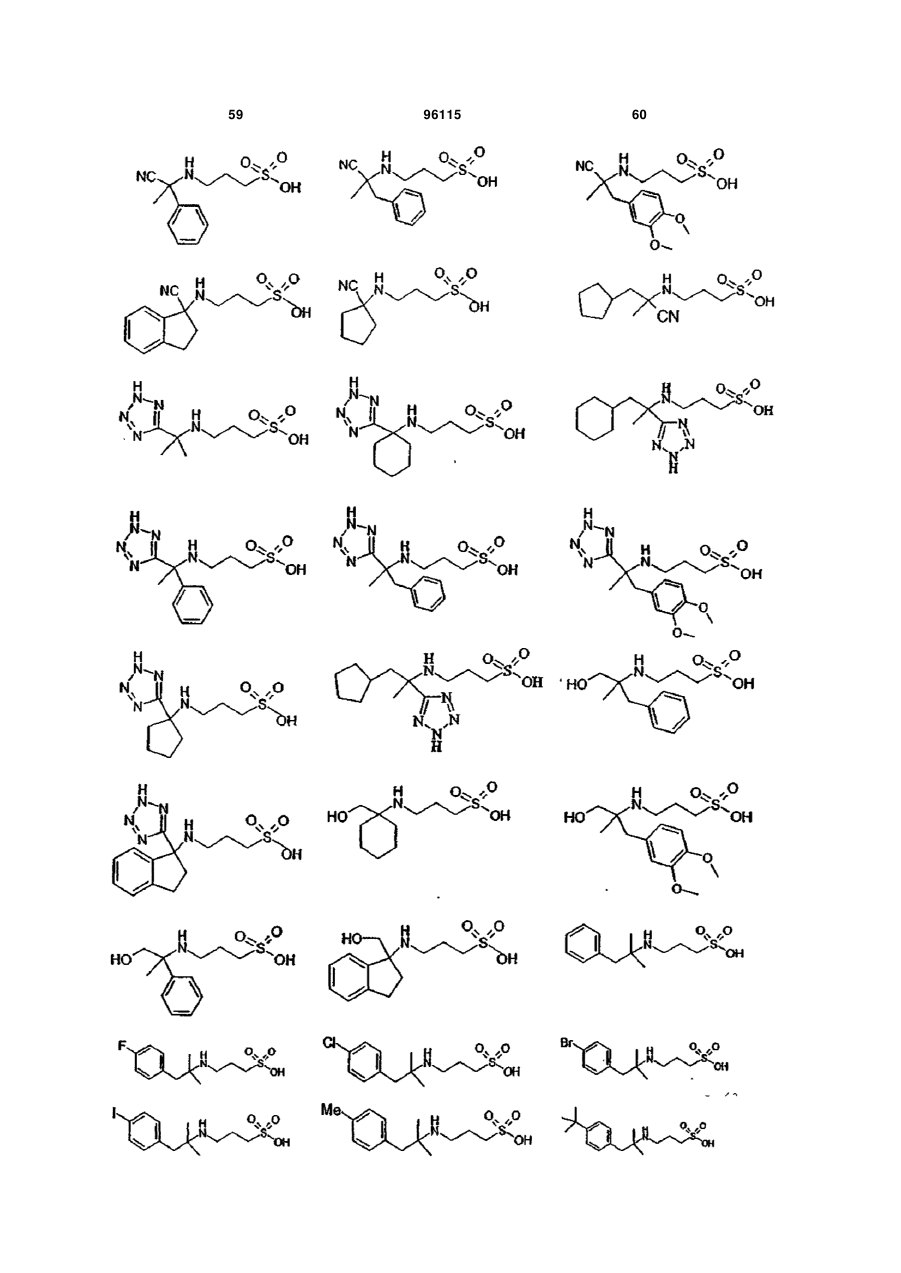Спосіб і композиція для лікування амілоїдогенних захворювань
Номер патенту: 96115
Опубліковано: 10.10.2011
Автори: Герваіс Франсін, Мігно Давід, Конг Ксянкві, Ву Ксінфу, Валаде Ізабелла
Формула / Реферат
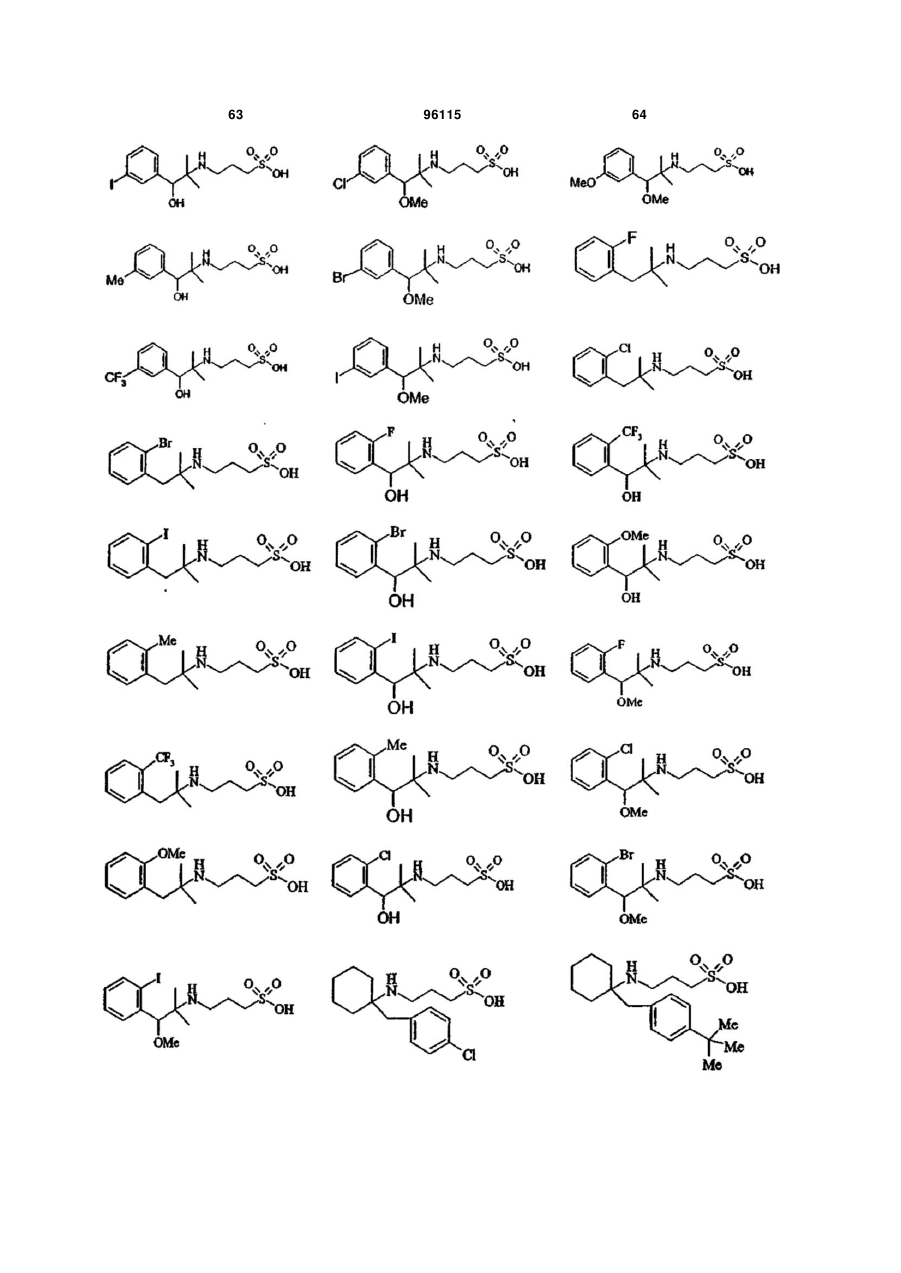
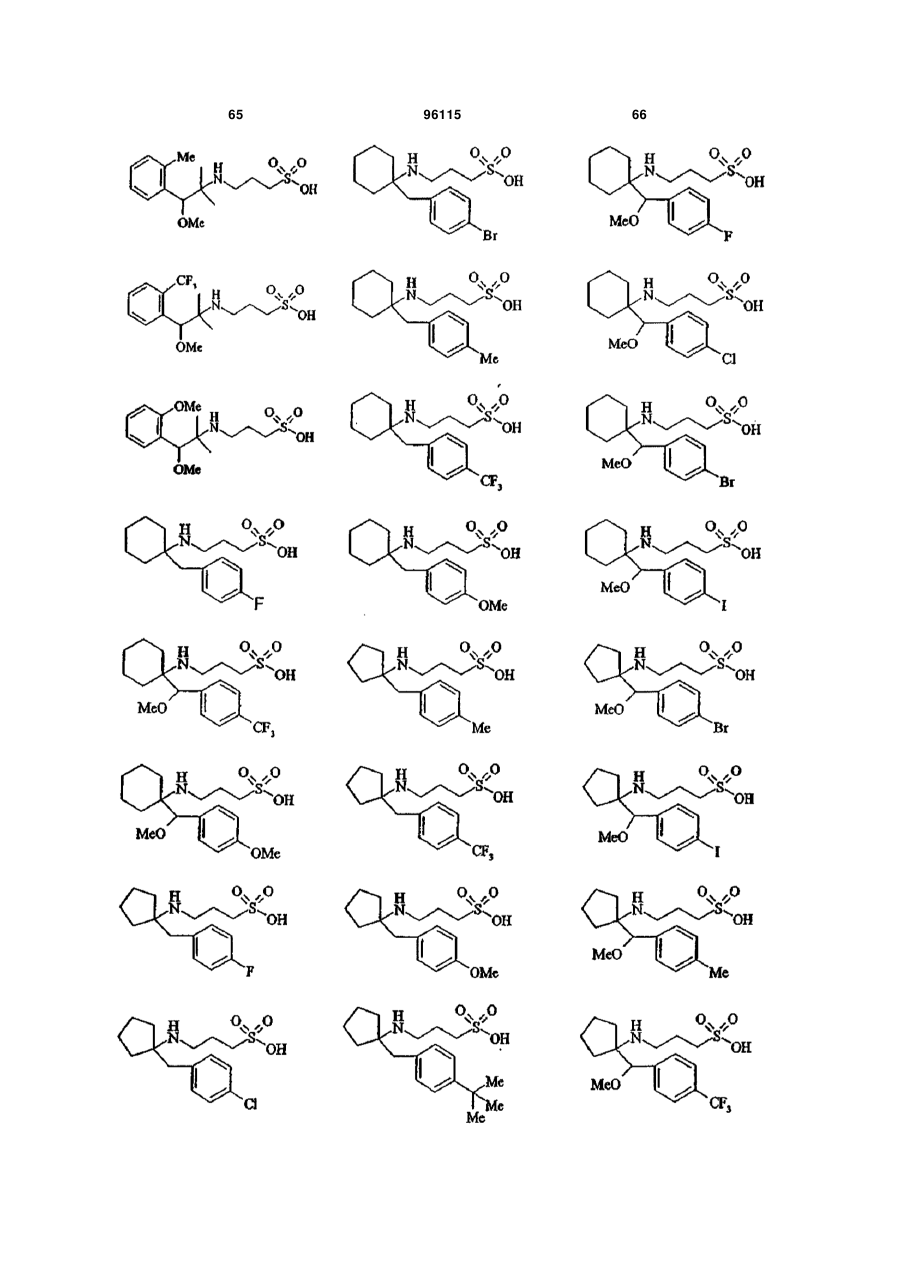
1. Сполука формули V:
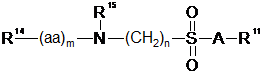 , (V)
, (V)
де:
А являє собою азот або кисень;
R11 - це водень, солеутворюючий катіон, естерна група, -(СН2)х-Q, або, коли А являє собою азот, А і R11, взяті разом, можуть бути залишком природної або неприродної амінокислоти, її сіллю або естером, де А і R11, взяті разом, не являють собою залишок лейцину;
Q - це водень, тіазоліл, триазоліл, імідазоліл, бензотіазоліл або бензоімідазоліл;
х являє собою 0, 1, 2, 3 або 4;
n являє собою 3;
аа - це природний або неприродний L-амінокислотний залишок;
m являє собою 1, 2 або 3;
R14 являє собою водень або захисну групу;
R15 являє собою водень, алкіл або арил;
і її фармацевтично прийнятні солі, естери або проліки;
в якій, коли А являє собою кисень, R11 являє собою водень або солеутворюючий катіон, n являє собою 3, m являє собою 2, і R14 і R15 обидва являють собою водень, тоді аа - це інший, ніж L-триптофан, D-фенілаланін або D-тирозин.
2. Сполука за п. 1, яка відрізняється тим, що m має значення 1 або 2.
3. Сполука за п. 2, яка відрізняється тим, що m має значення 1.
4. Сполука за п. 2, яка відрізняється тим, що m має значення 2.
5. Сполука за будь-яким з пп. 1-4, яка відрізняється тим, що A-R11 являє собою залишок природної амінокислоти або її сіль або естер.
6. Сполука за п. 5, яка відрізняється тим, що A-R11 являє собою залишок фенілаланіну.
7. Сполука за будь-яким з пп. 1-4, яка відрізняється тим, що А являє собою кисень і R11 являє собою водень або солеутворюючий катіон.
8. Сполука за будь-яким з пп. 1-7, яка відрізняється тим, що аа являє собою природний амінокислотний залишок.
9. Сполука за будь-яким з пп. 1-8, яка відрізняється тим, що (аа)m являє собою залишок фенілаланіну, гліцину або фенілаланін-фенілаланіну.
10. Сполука за будь-яким з пп. 1-9, яка відрізняється тим, що аа являє собою неприродний амінокислотний залишок.
11. Сполука за будь-яким з пп. 1-10, яка відрізняється тим, що R15 являє собою водень або заміщений алкіл.
12. Сполука за п. 11, яка відрізняється тим, що R15 являє собою арилалкіл.
13. Сполука за п. 11, яка відрізняється тим, що R15 являє собою водень.
14. Сполука за будь-яким з пп. 1-10, яка відрізняється тим, що R14 і R15 обидва являють собою водень.
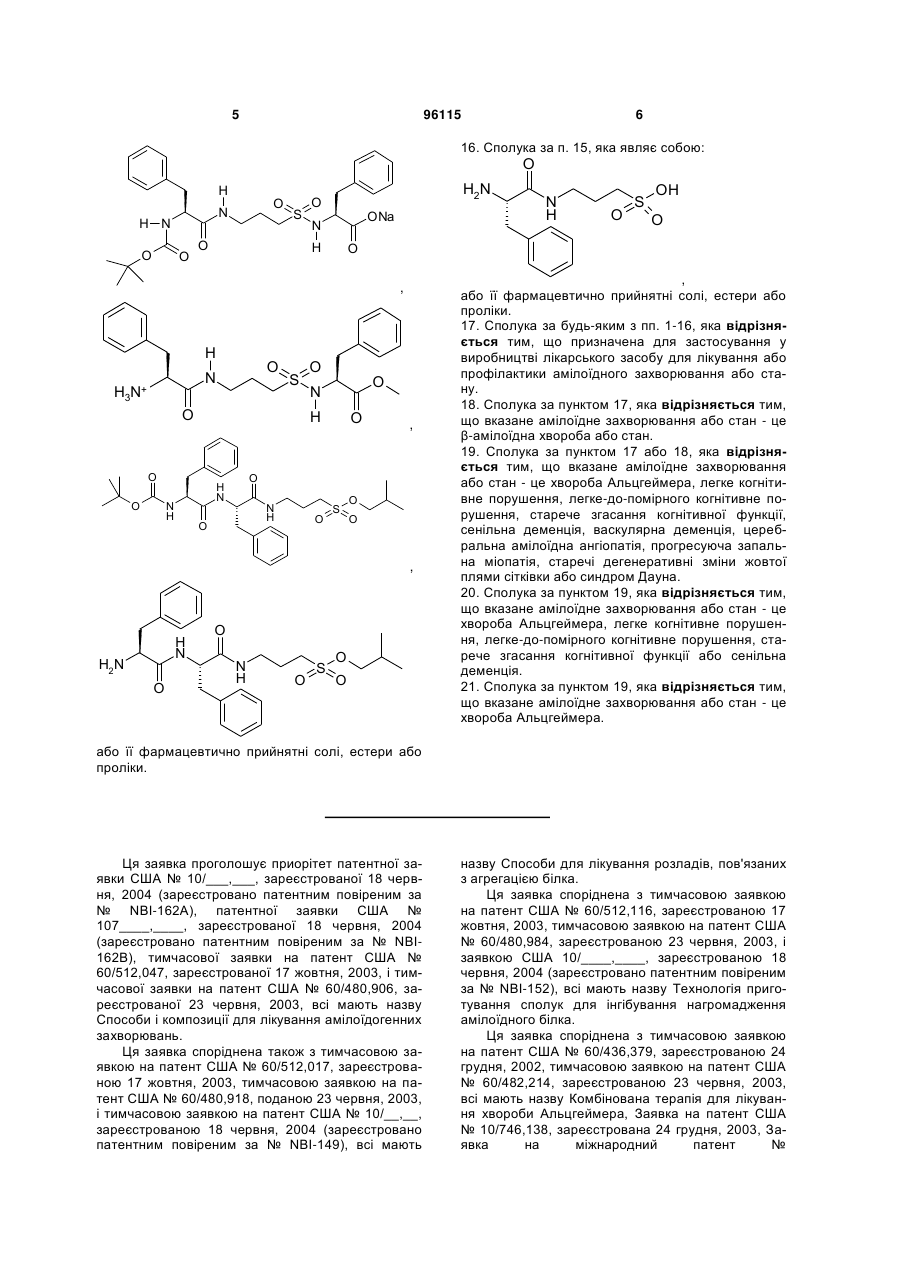
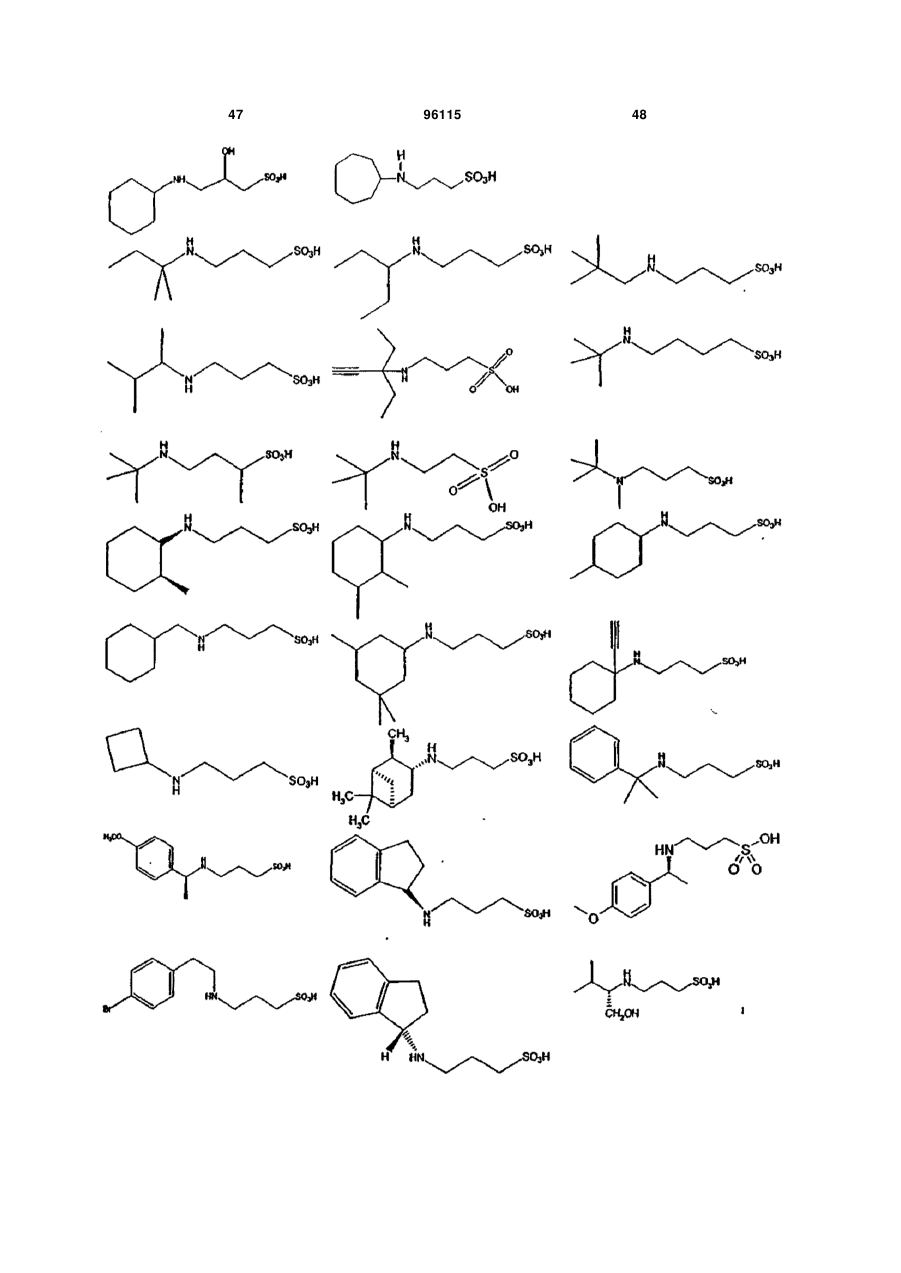
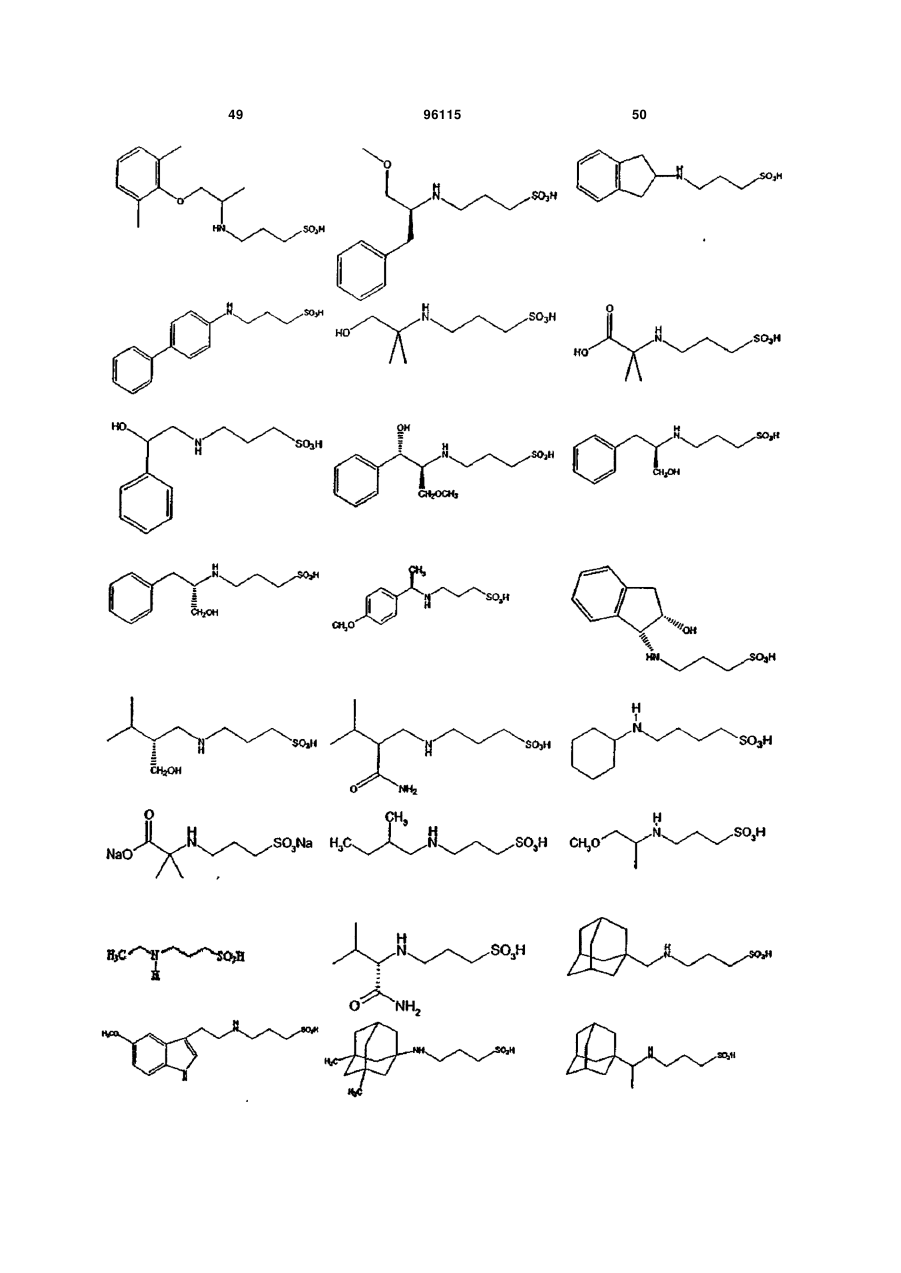
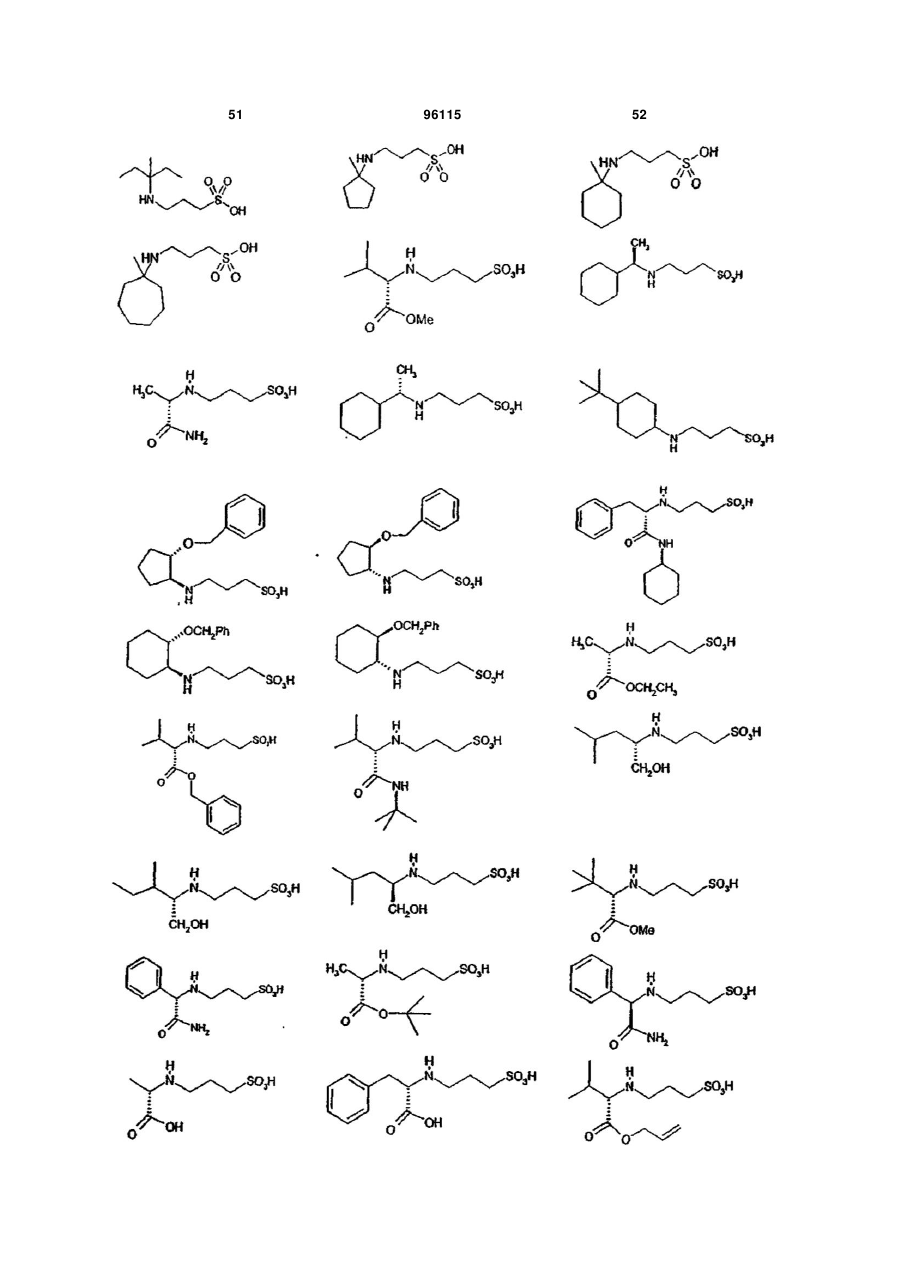
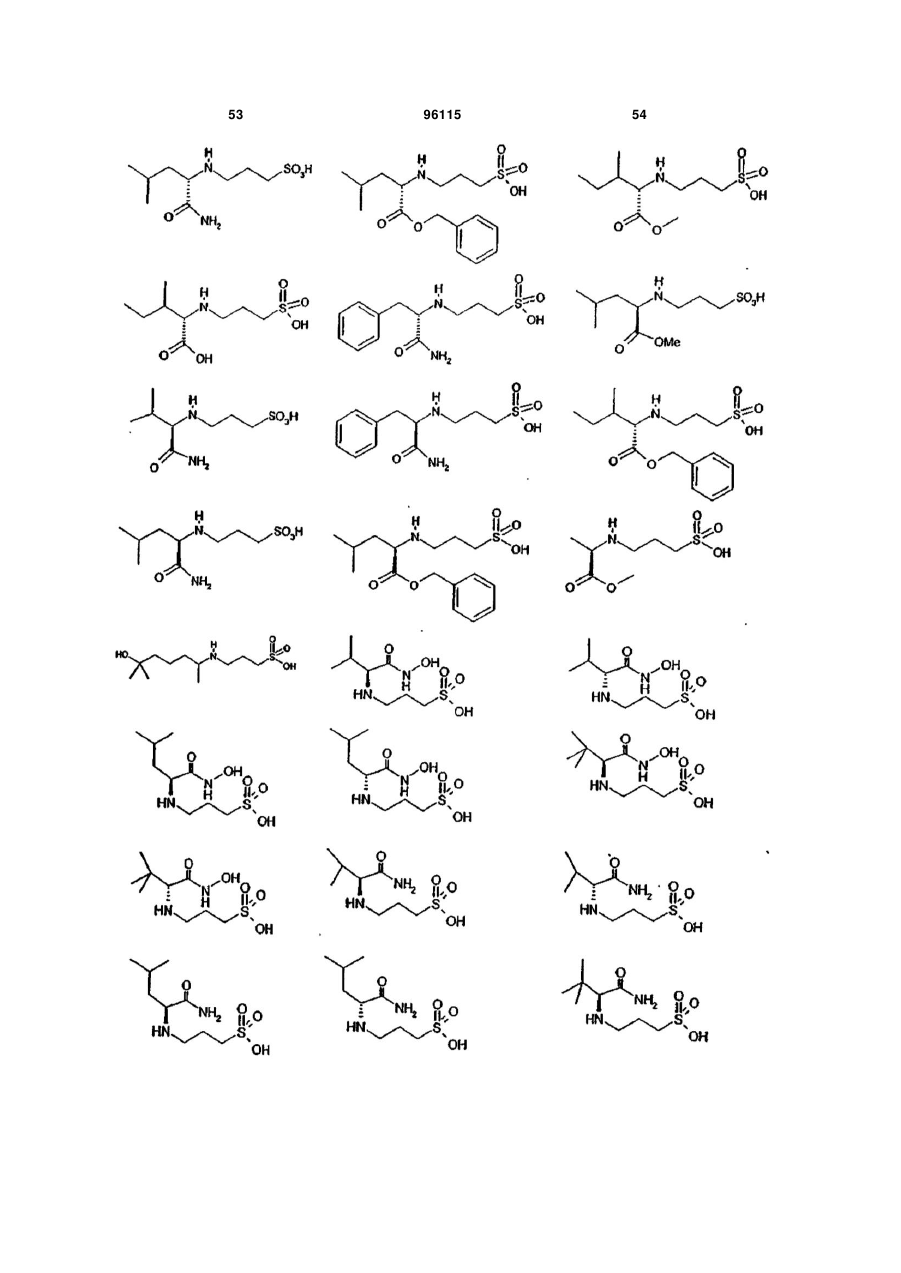
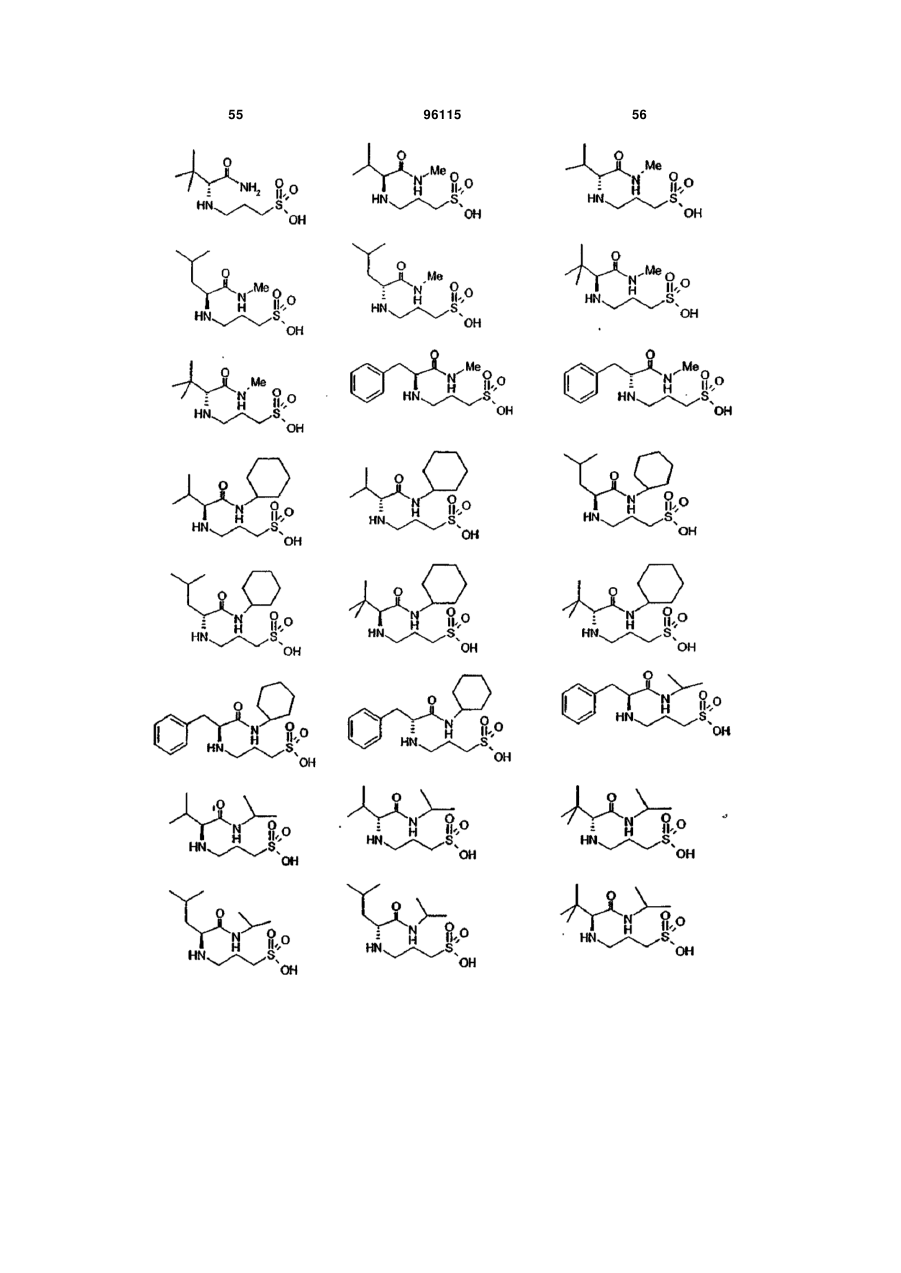
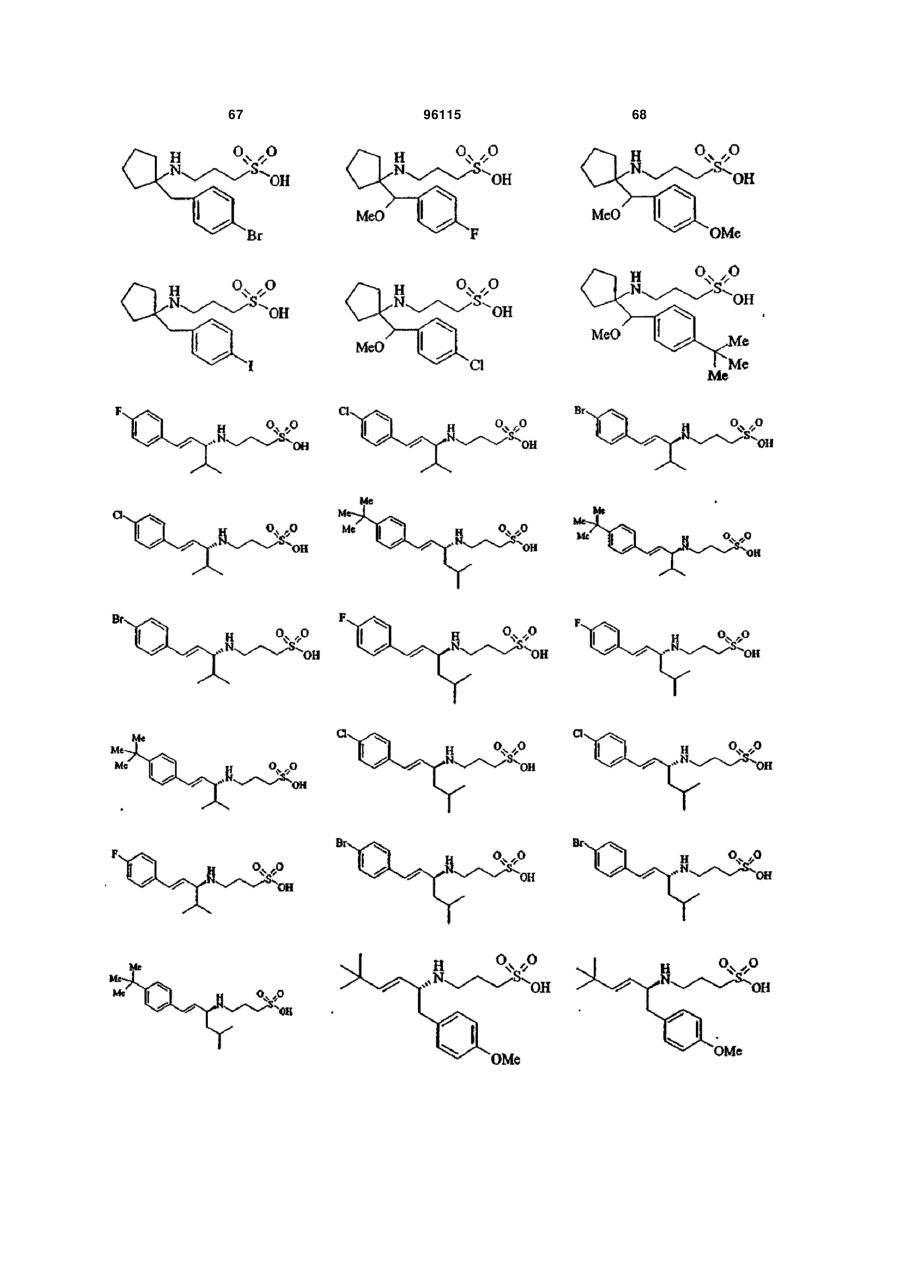
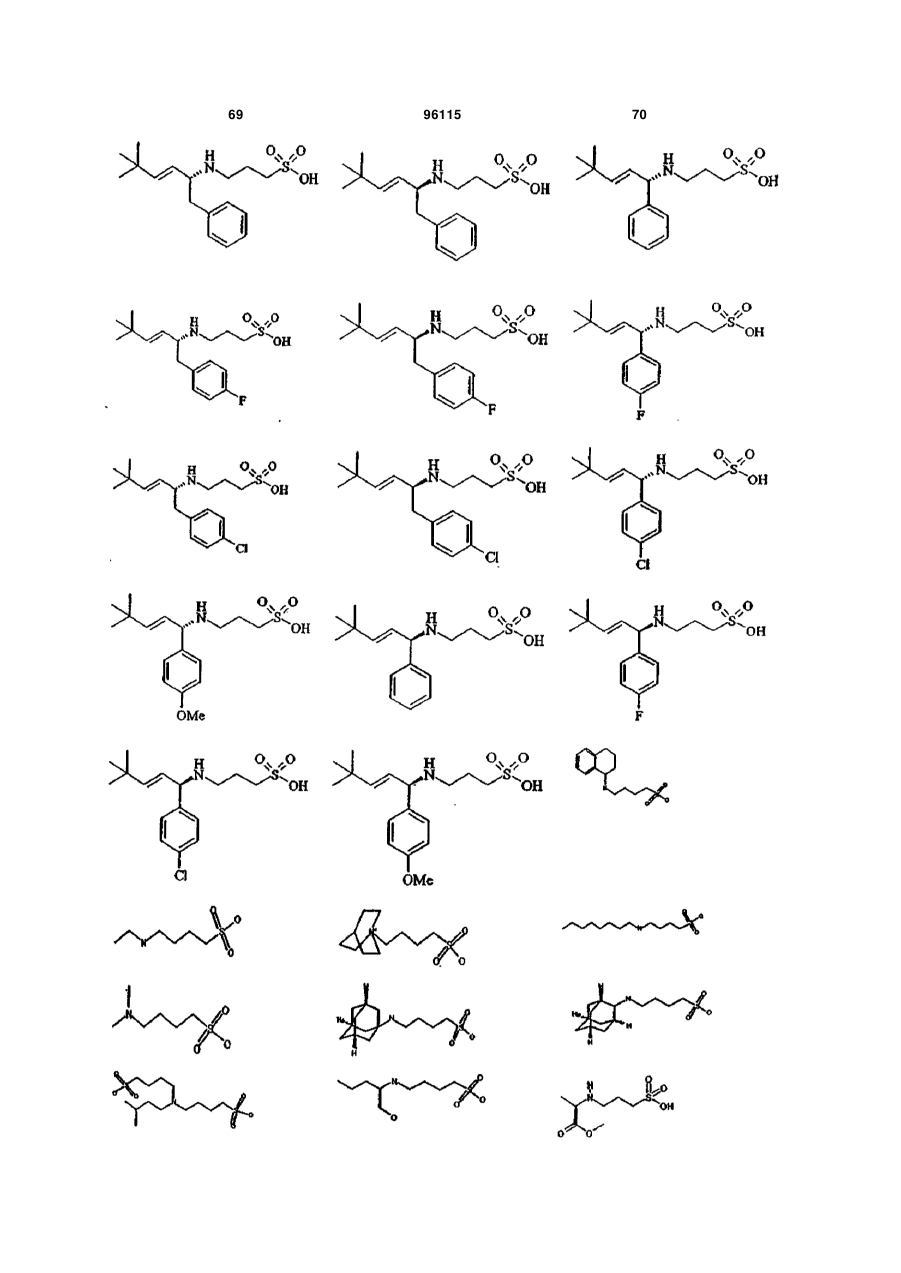
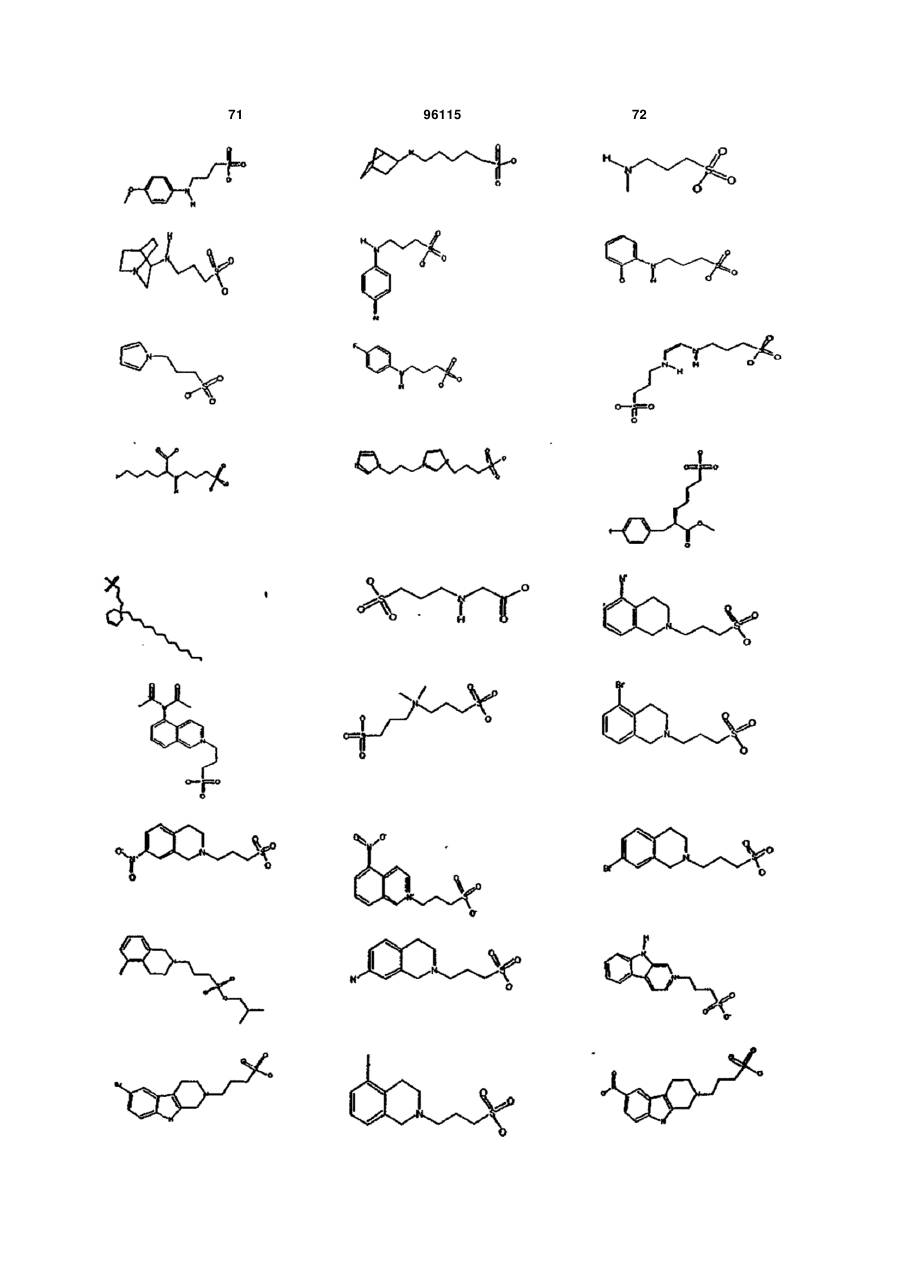
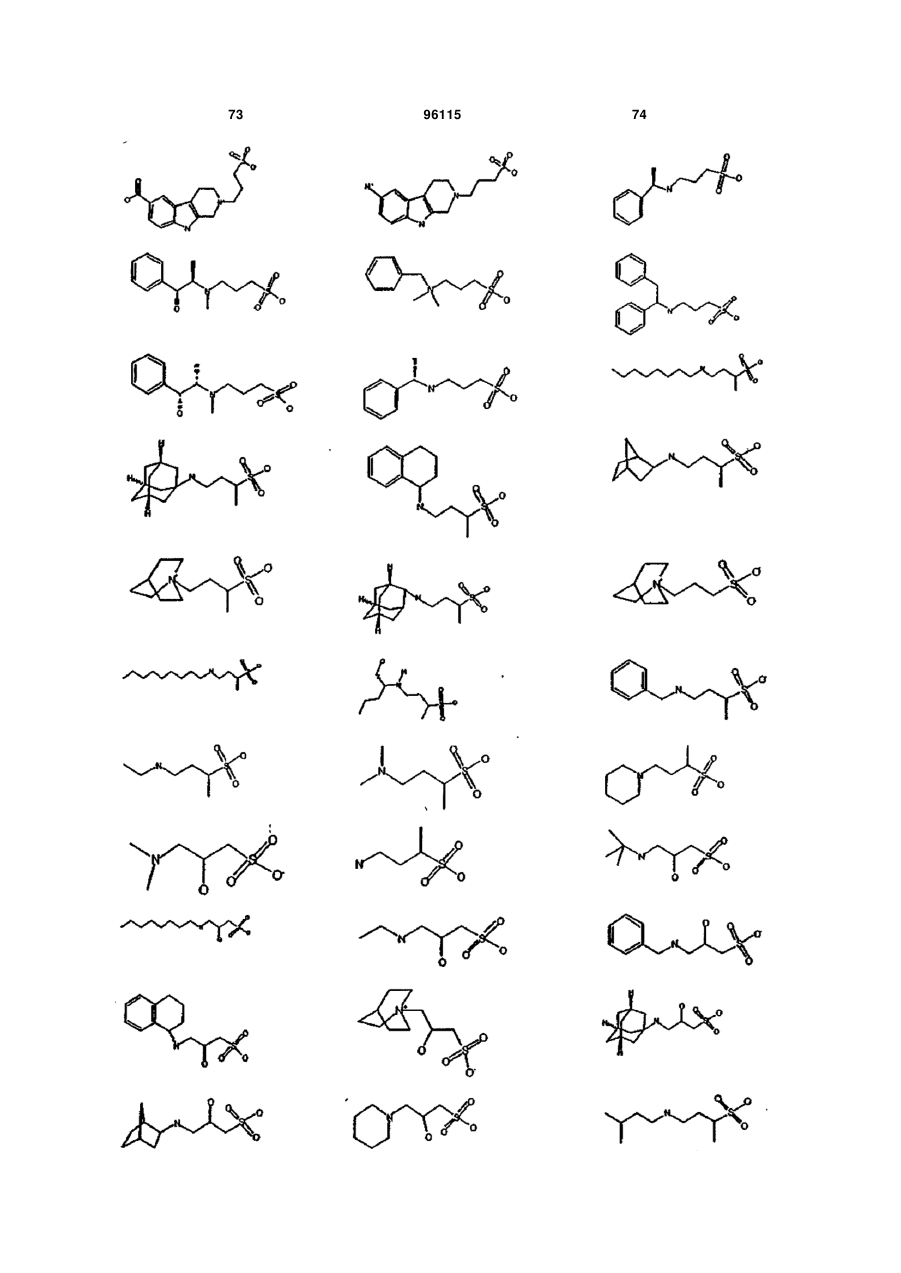
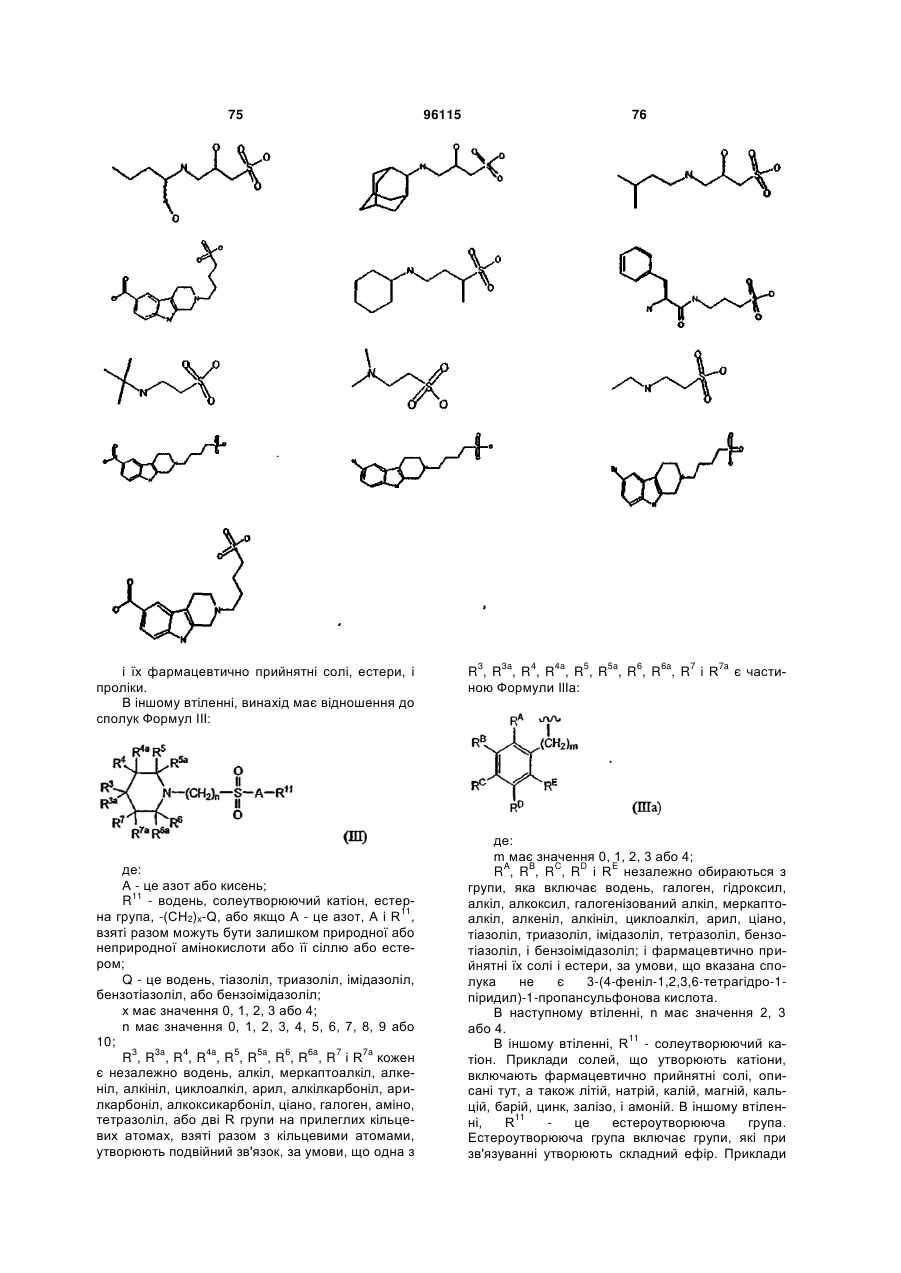
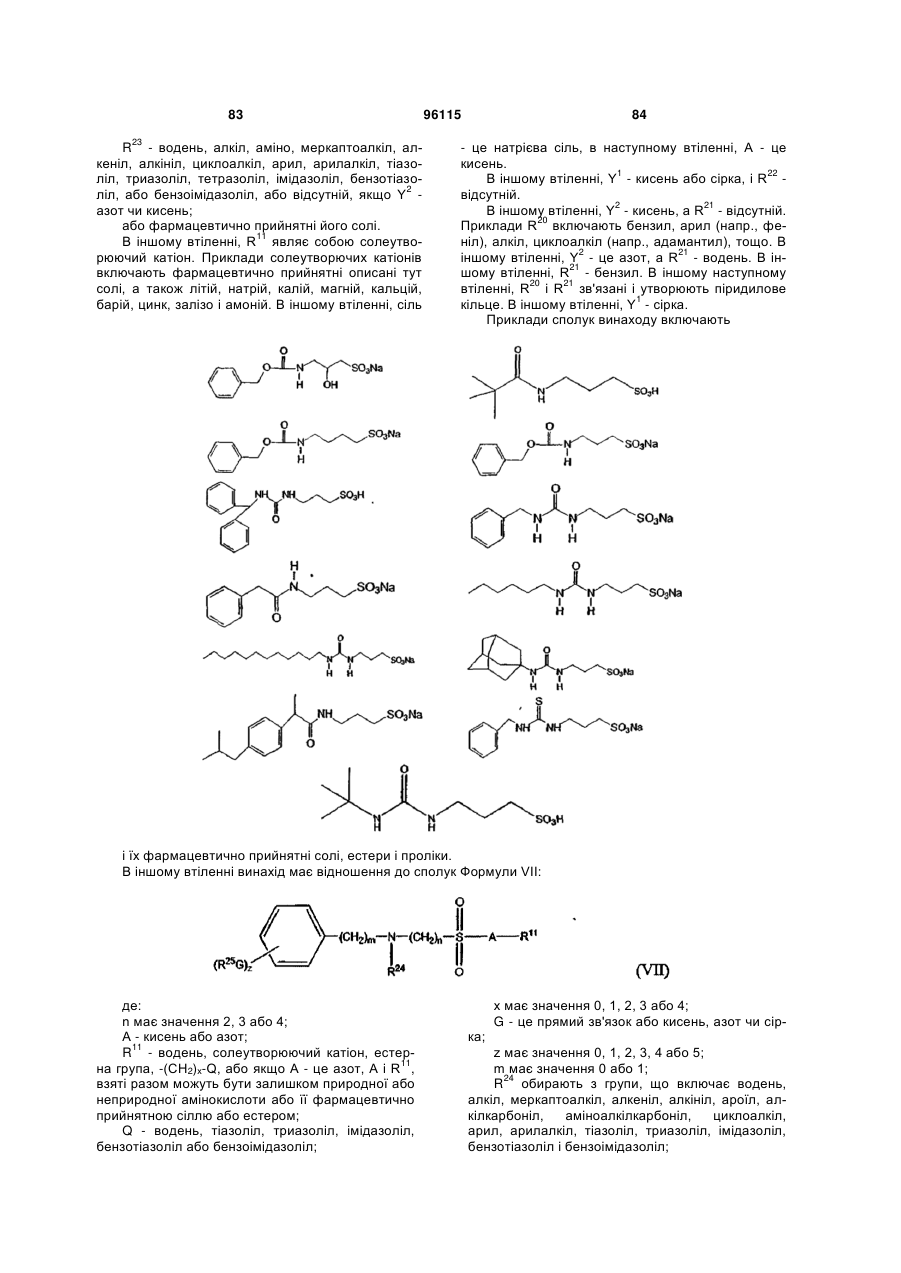
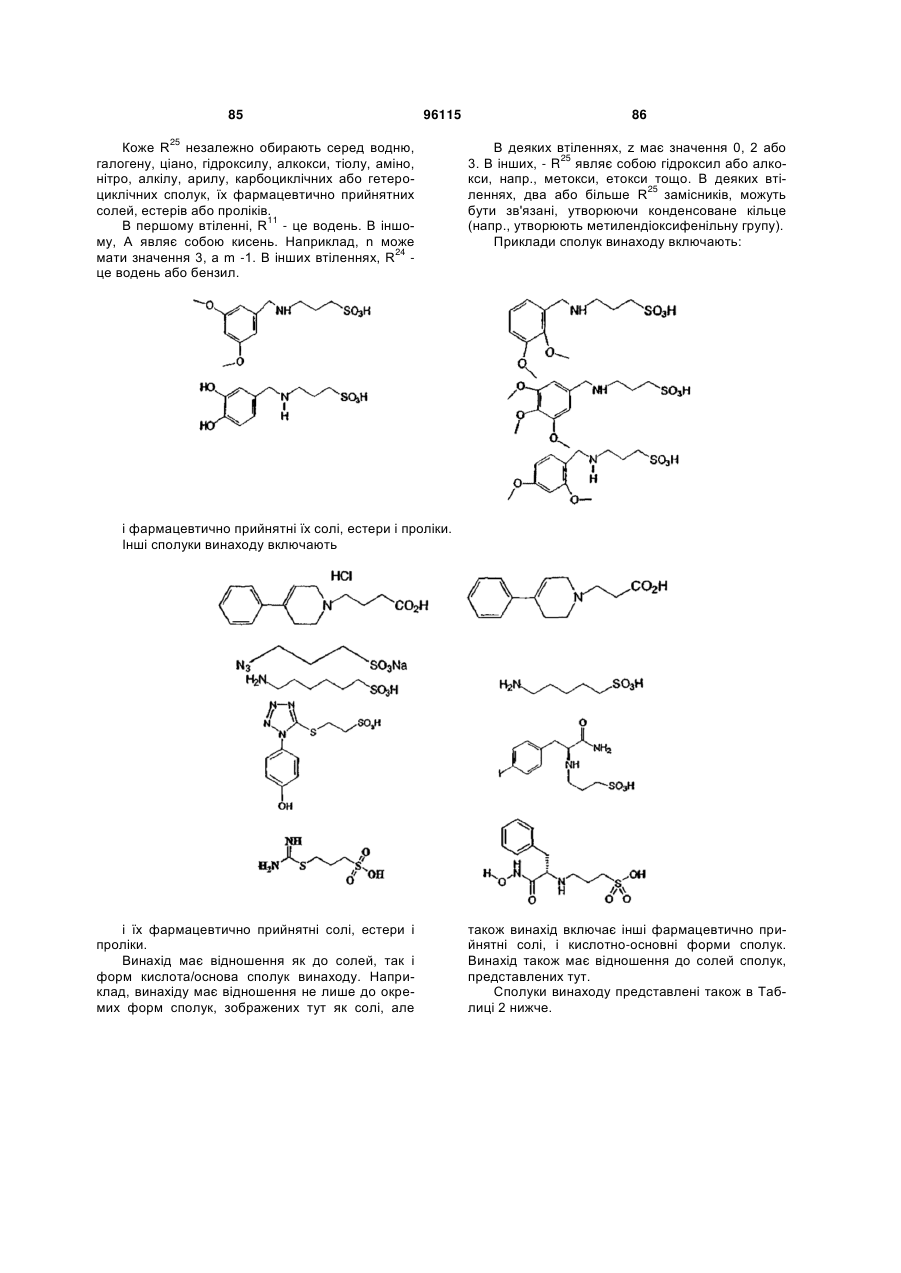
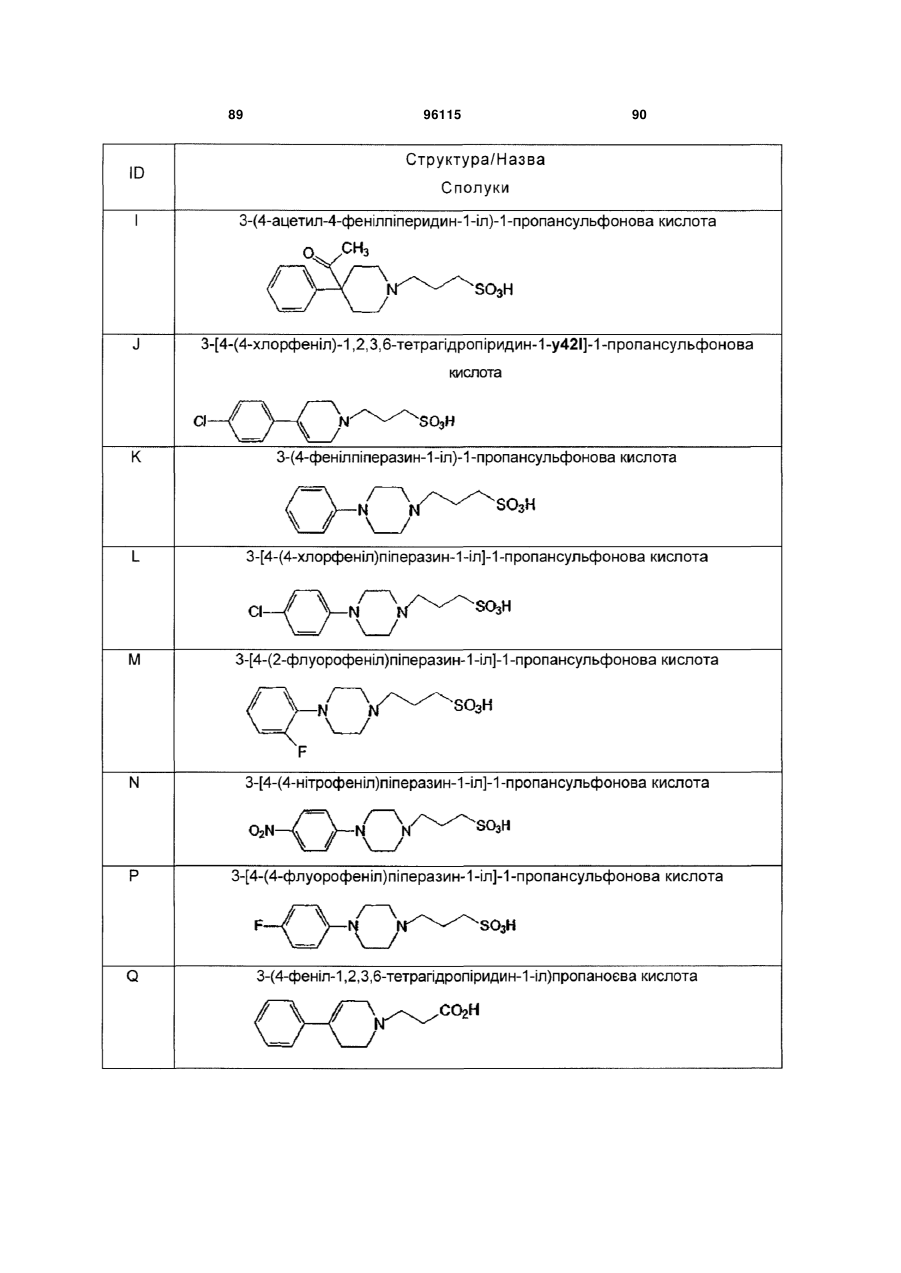
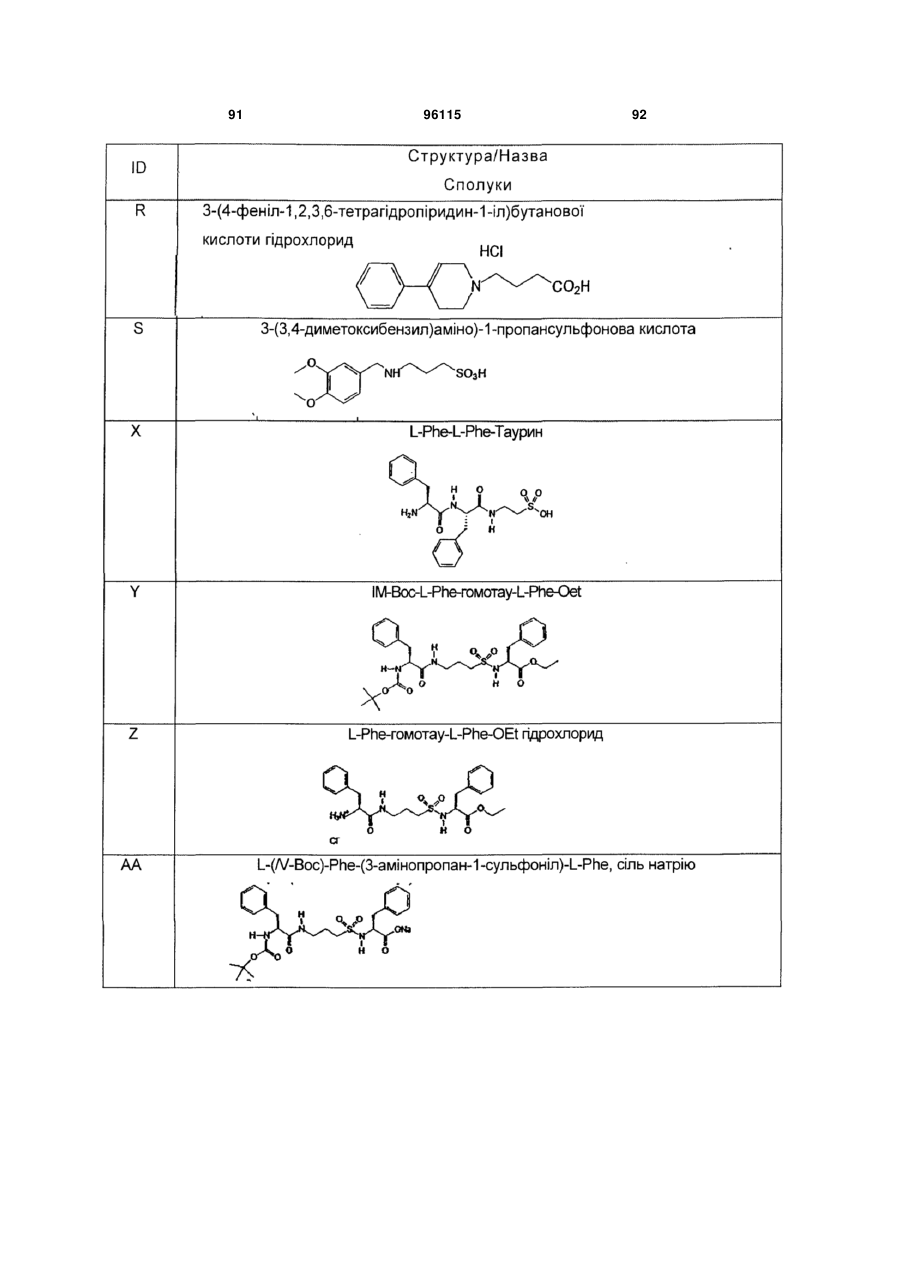
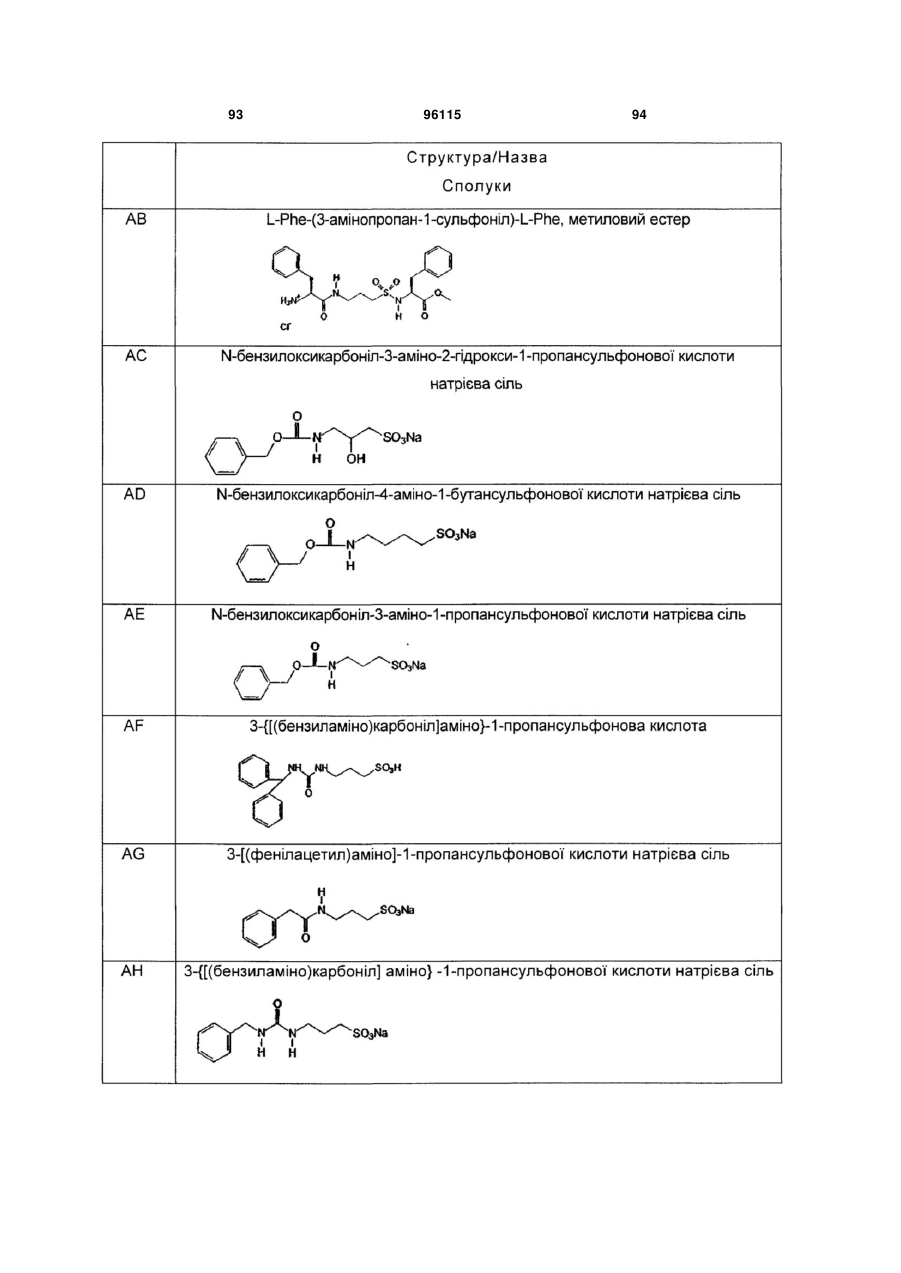
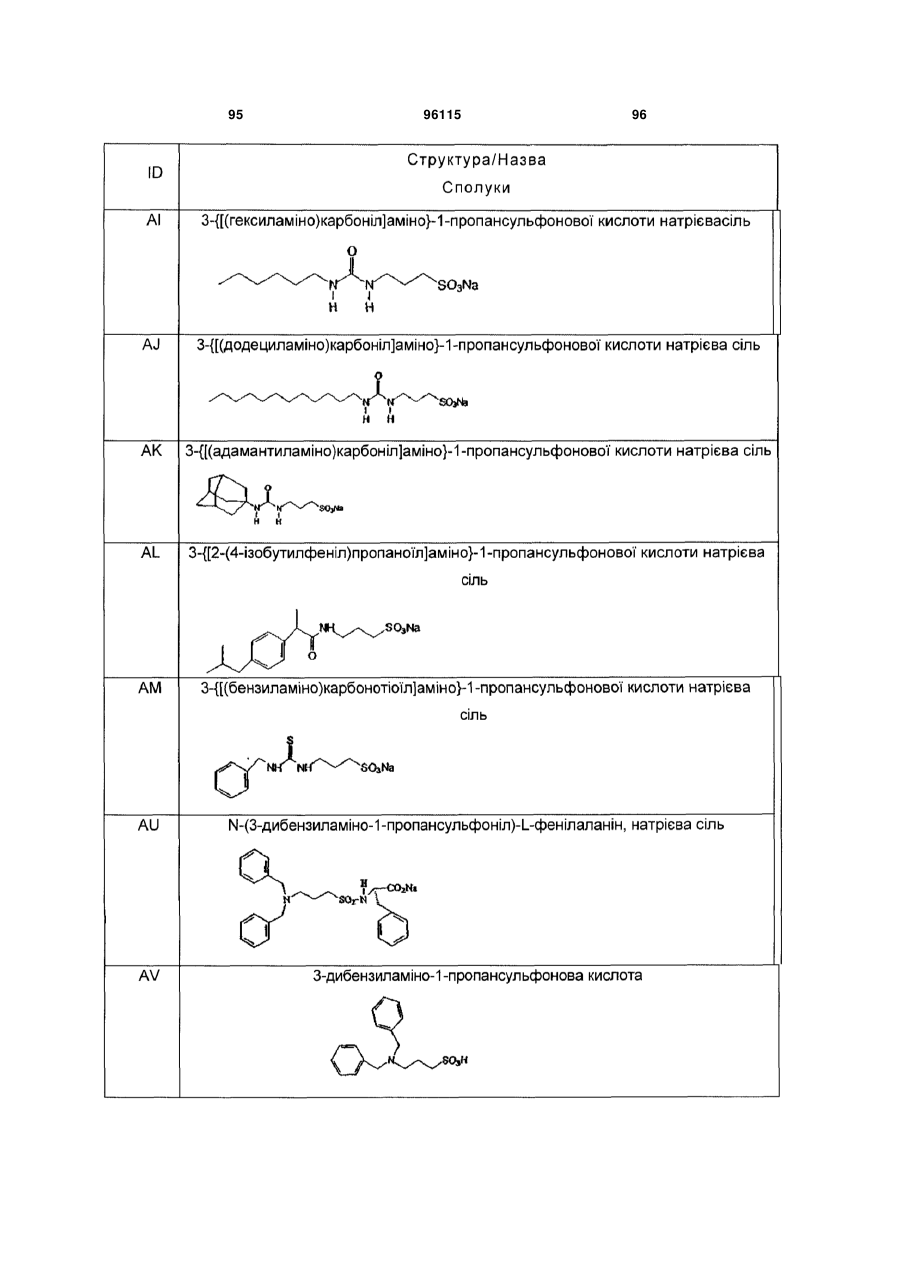
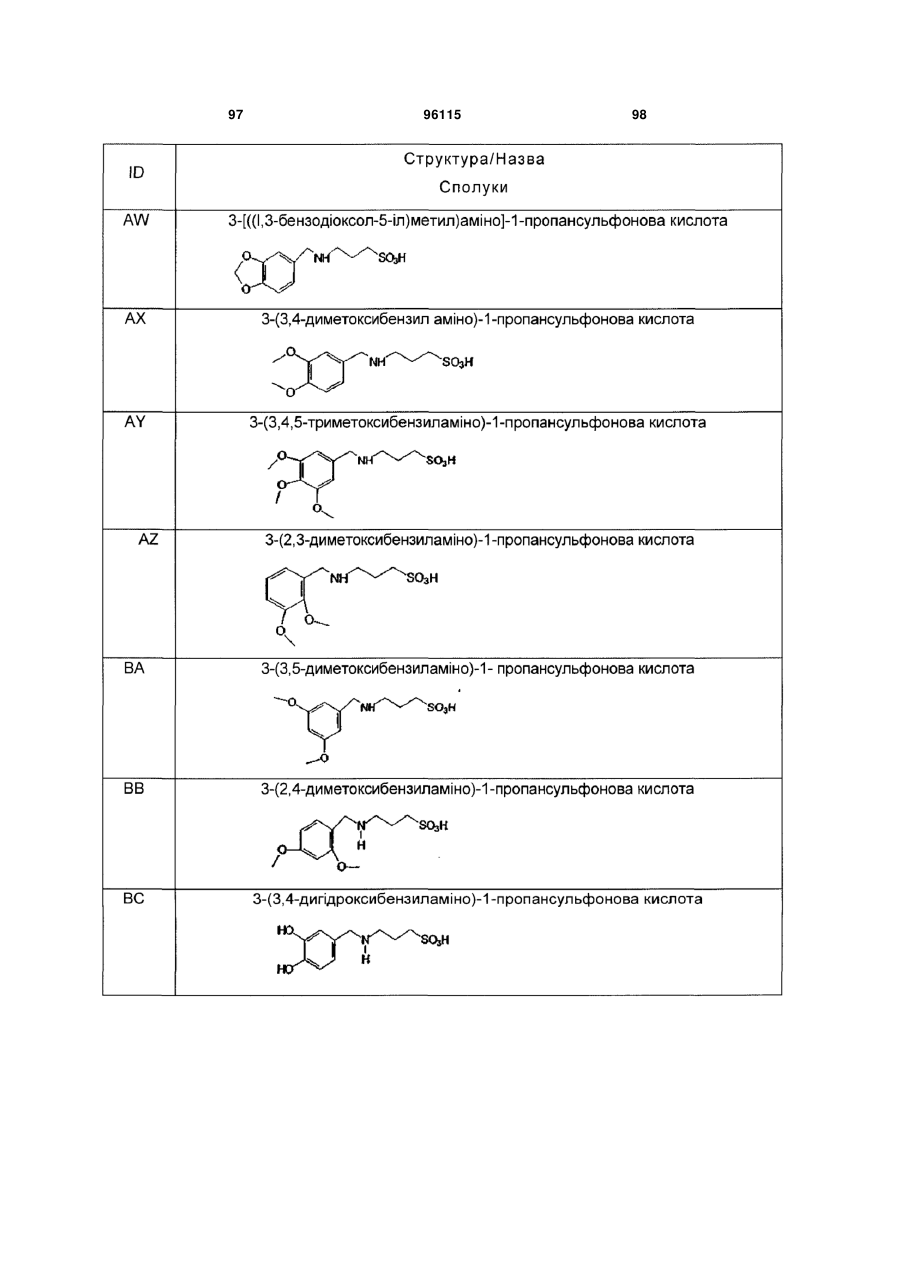
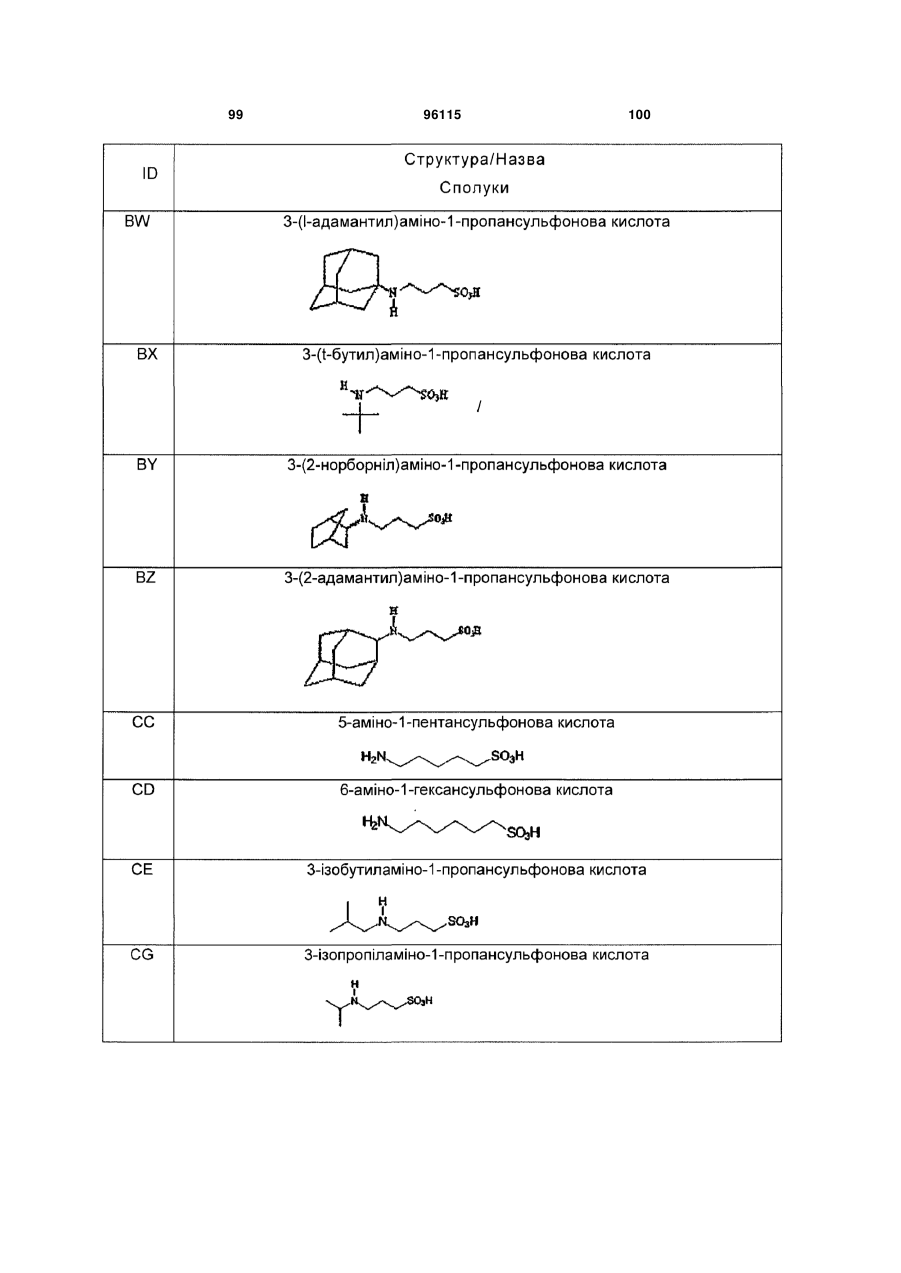
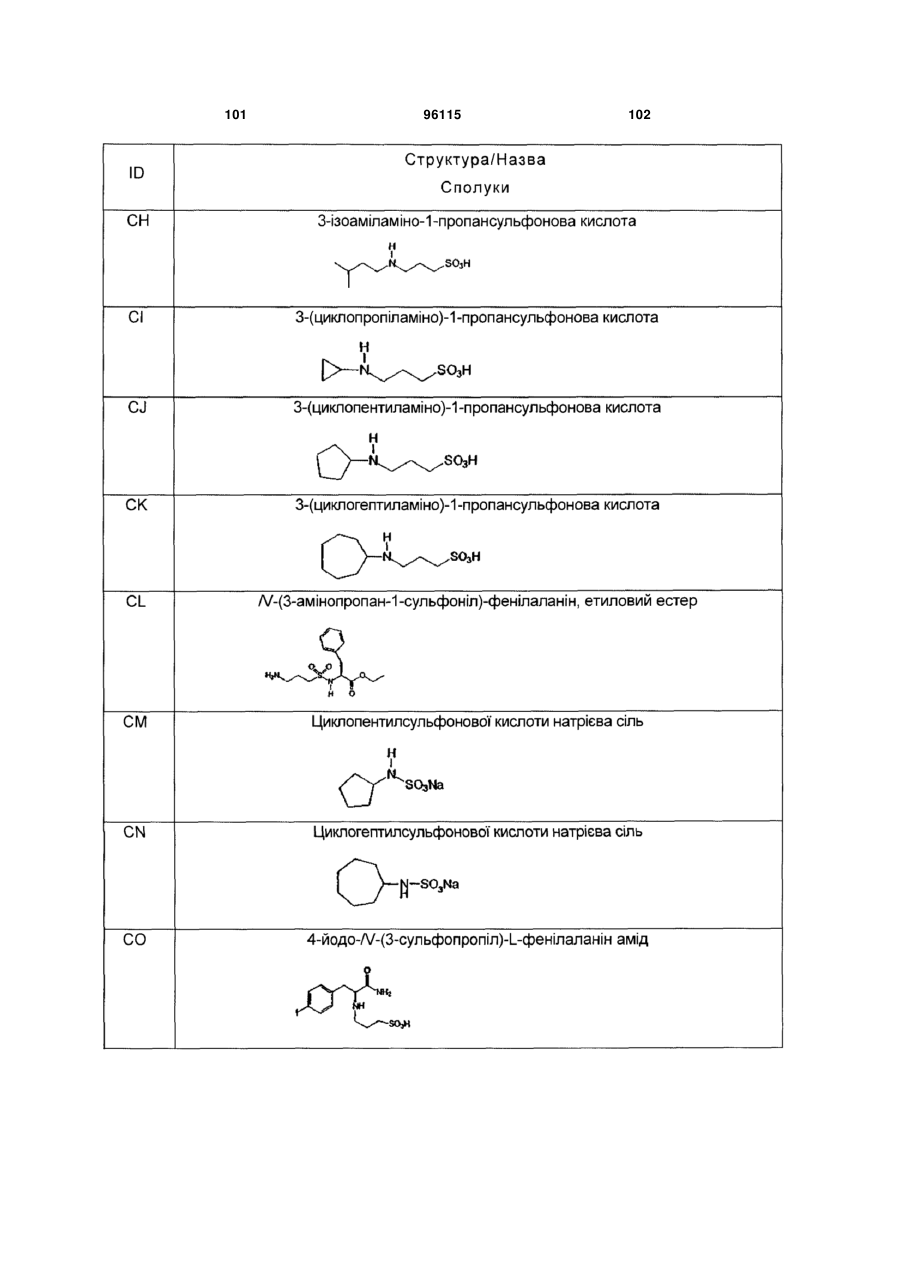
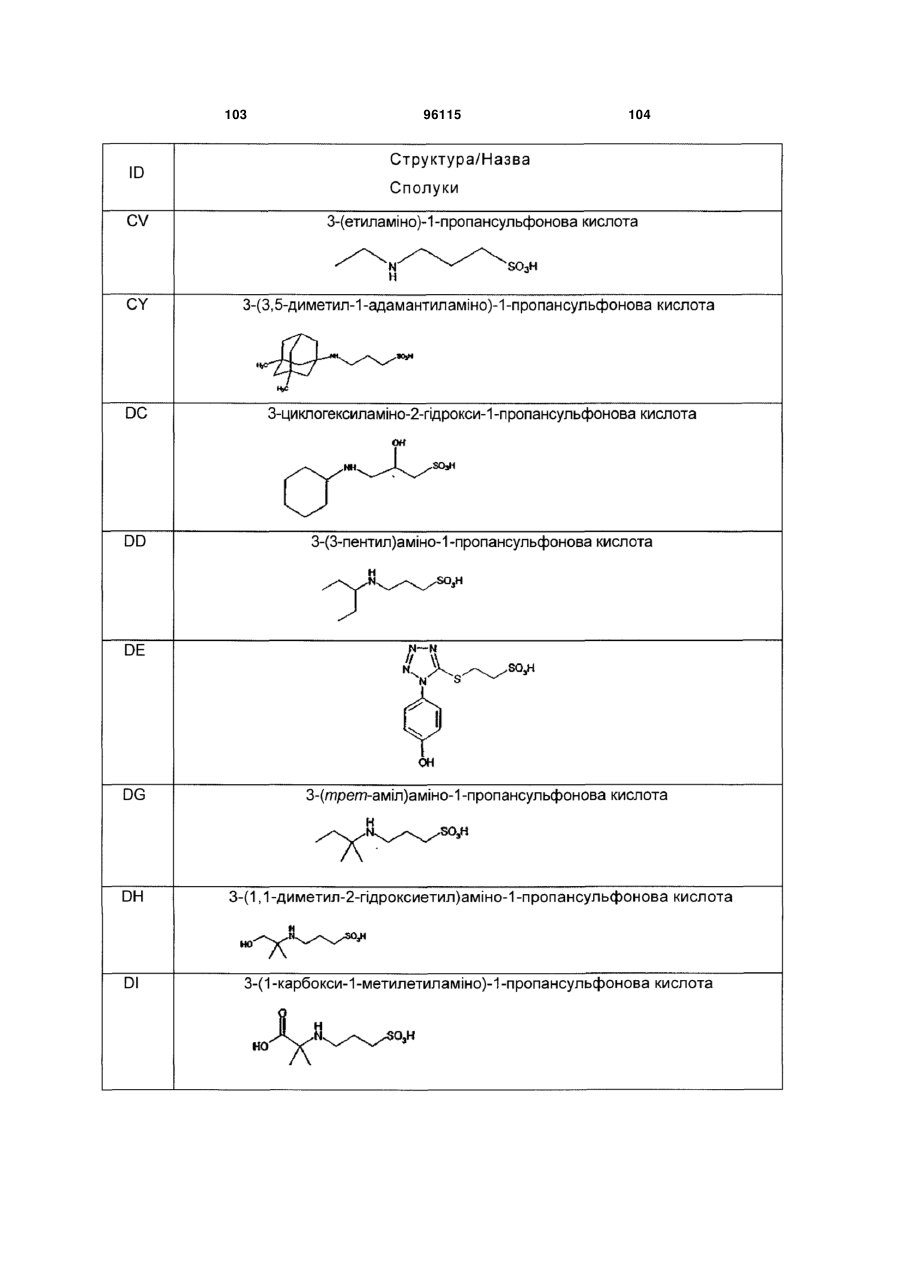
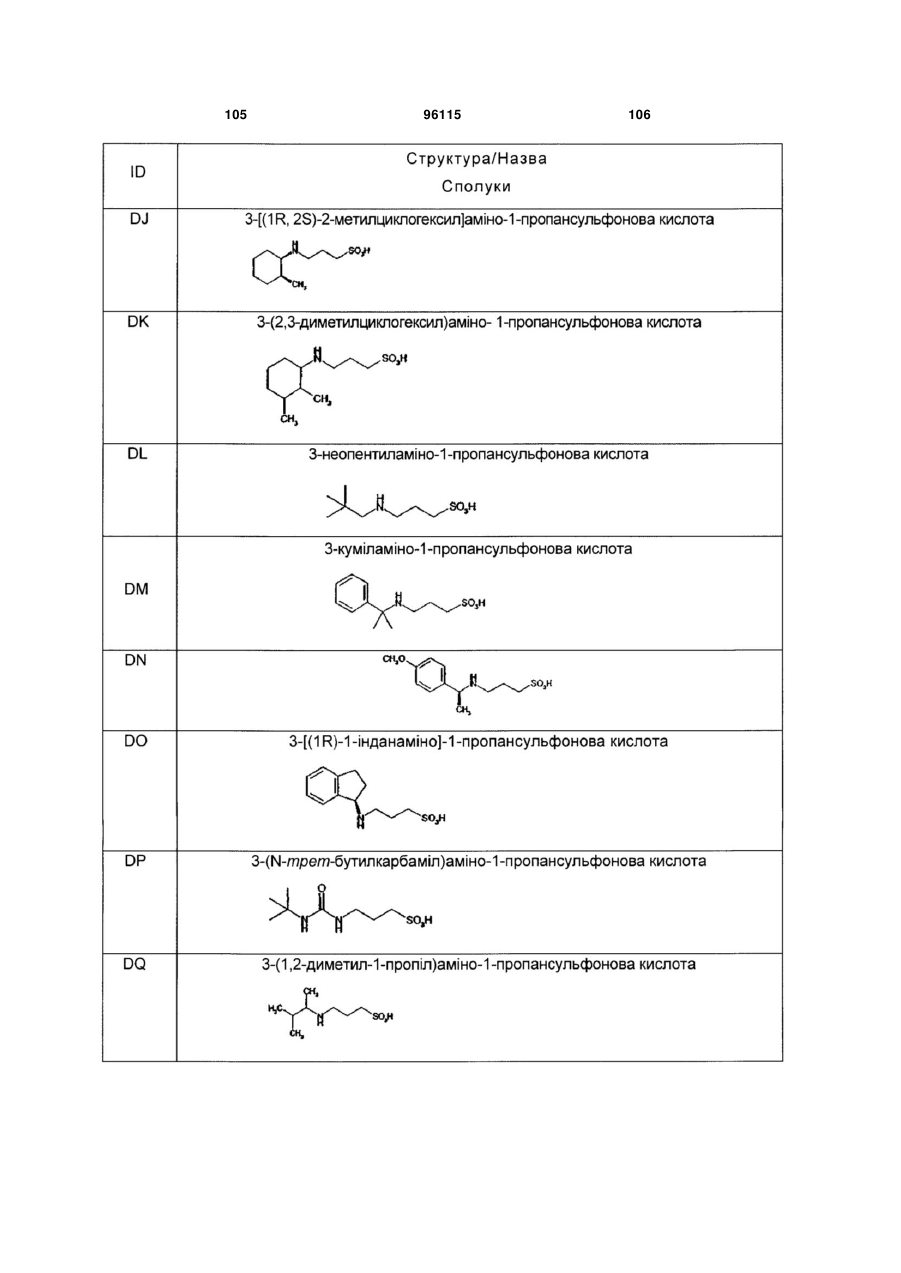
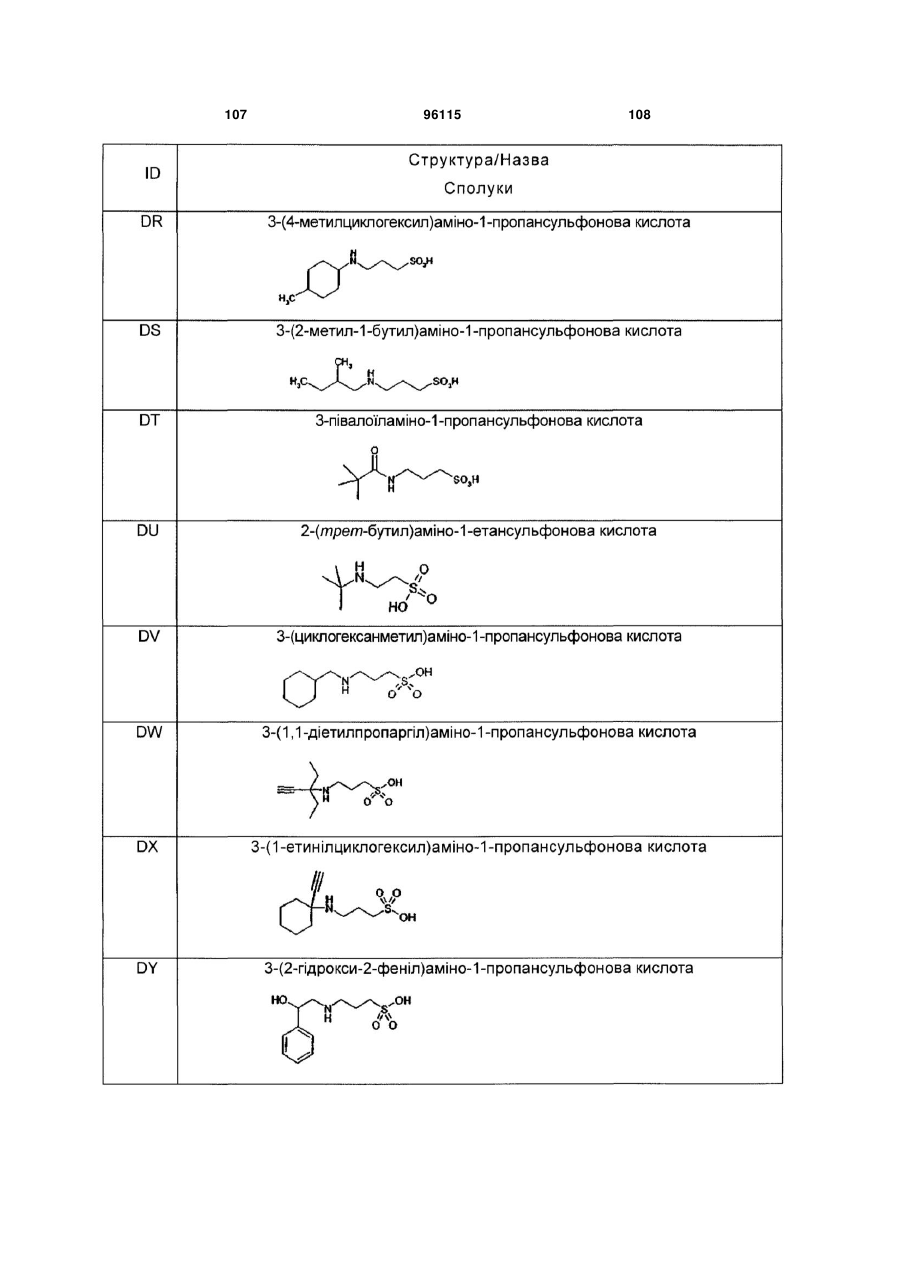
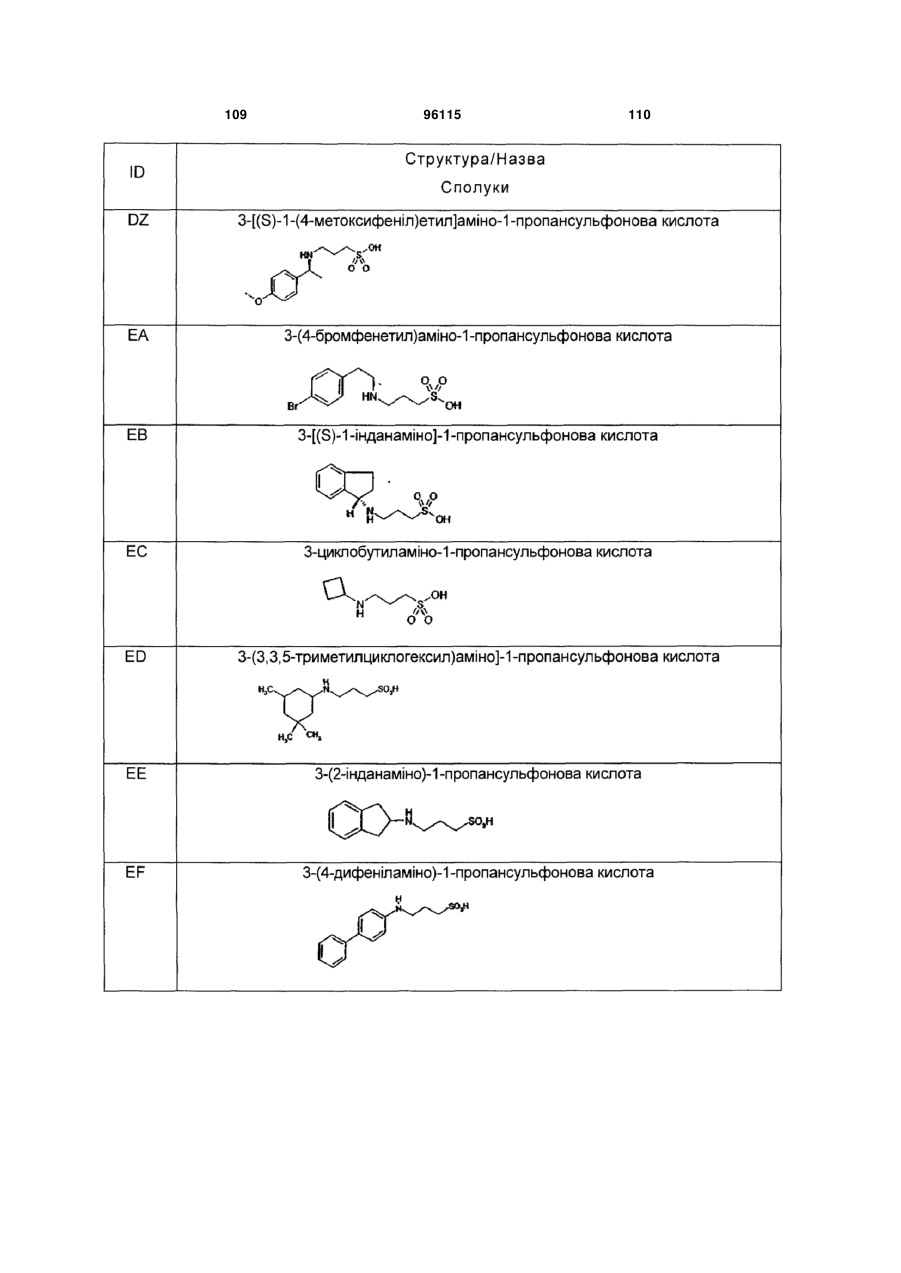
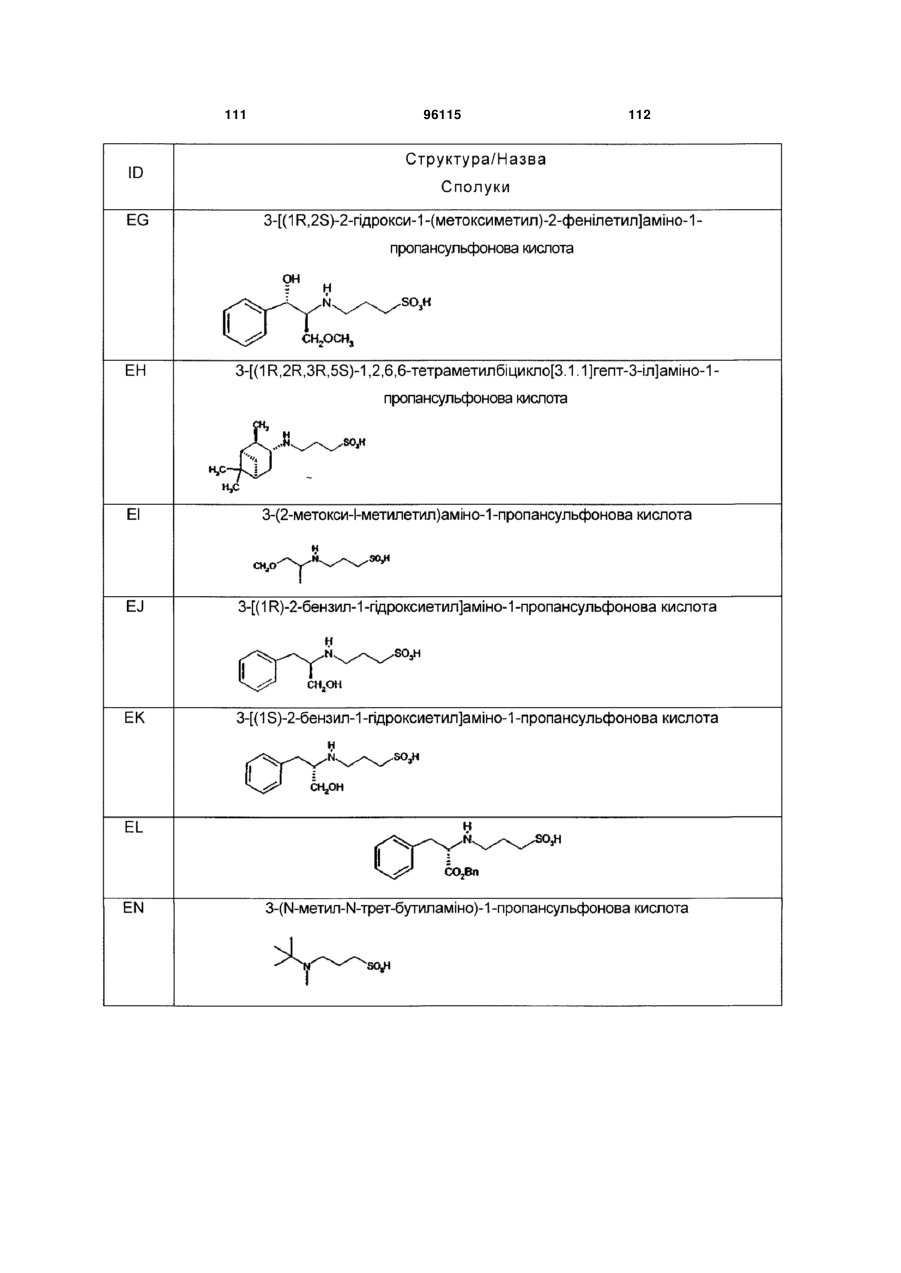
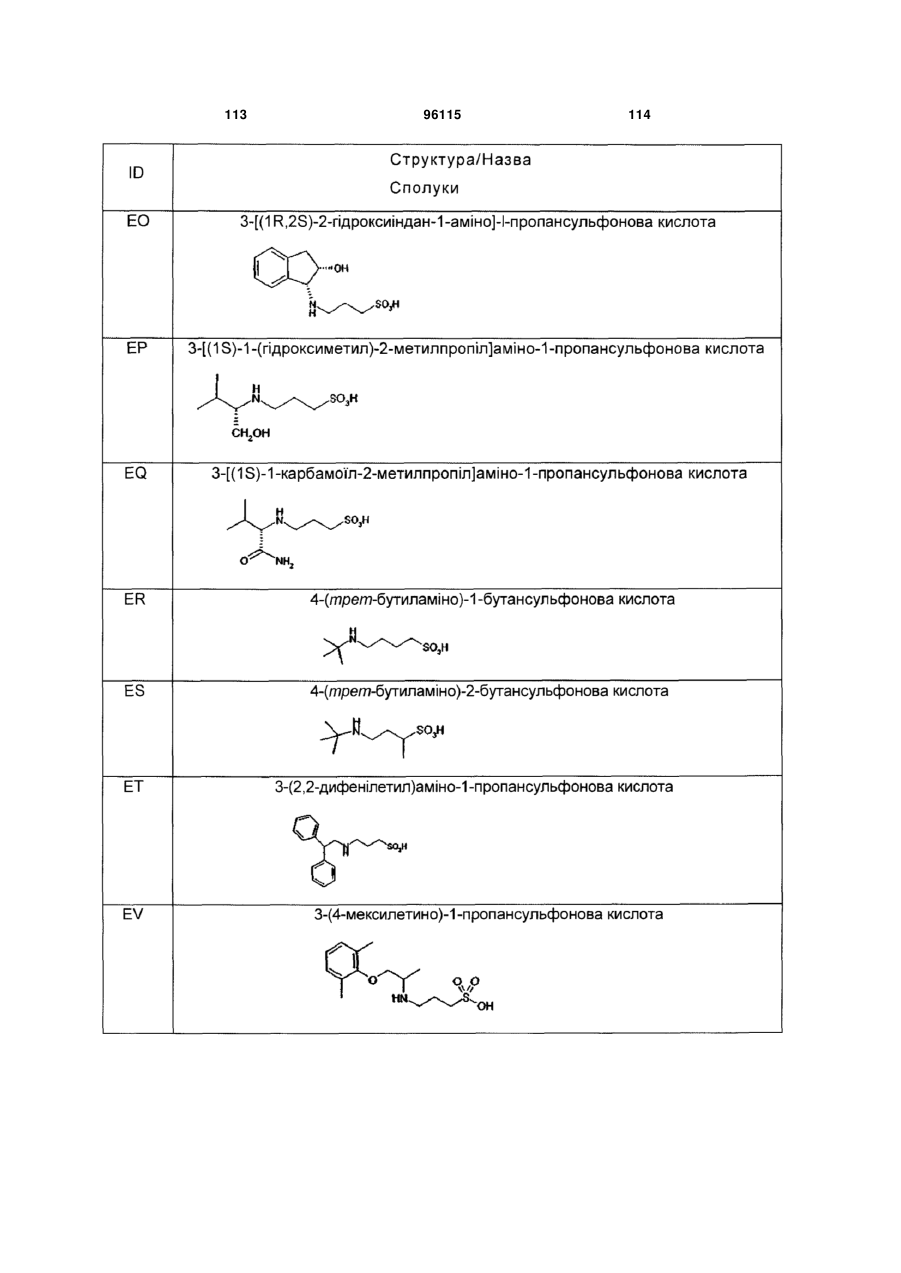
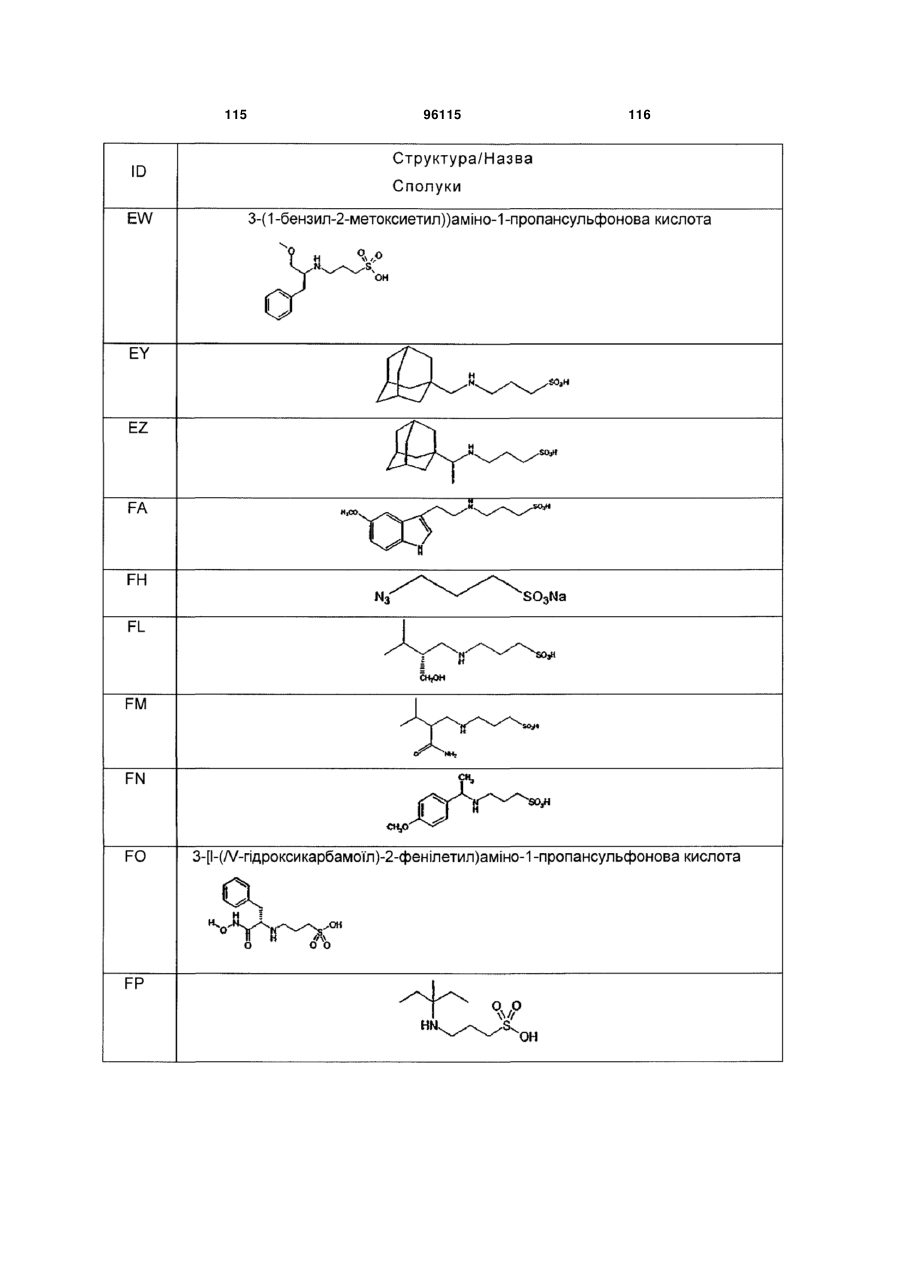
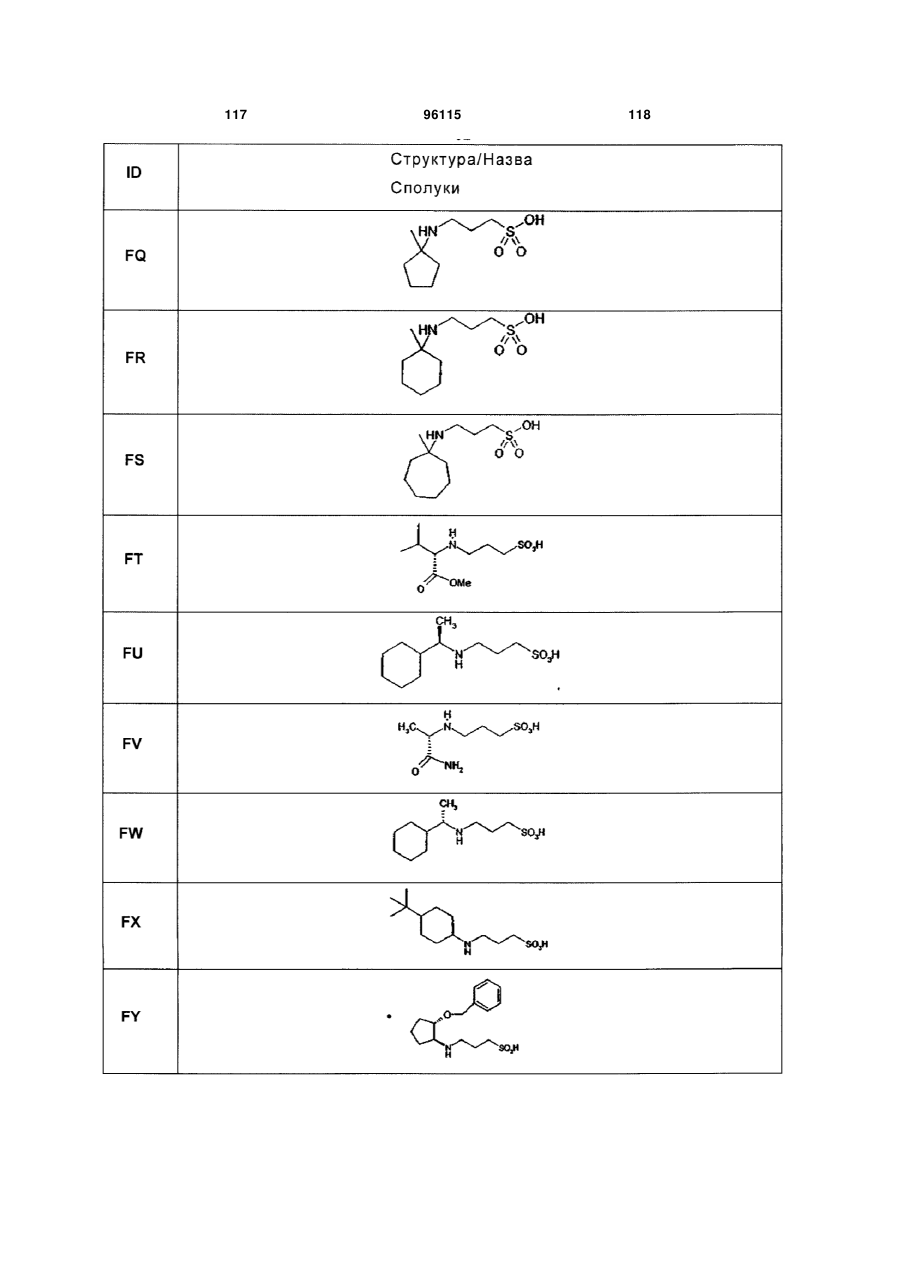
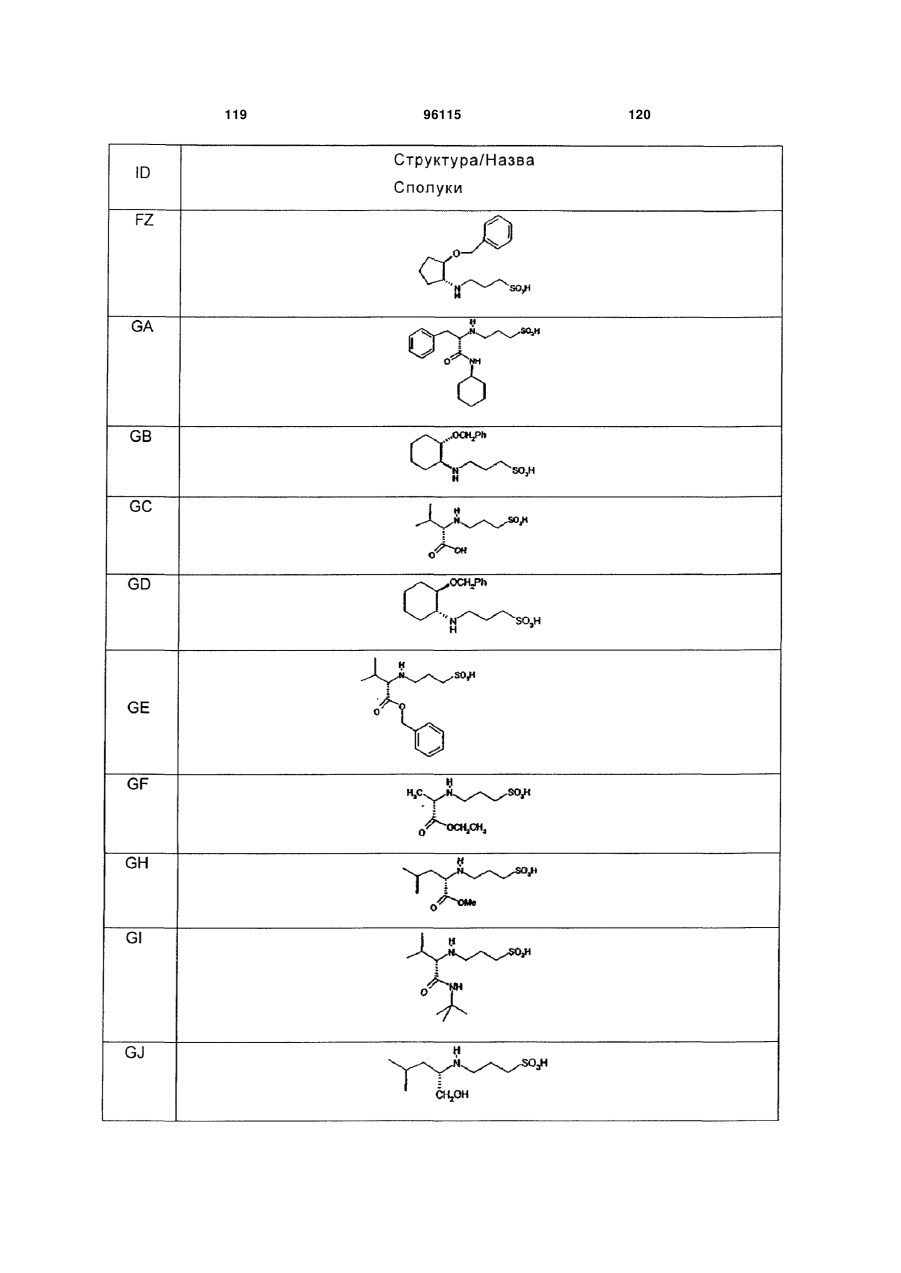
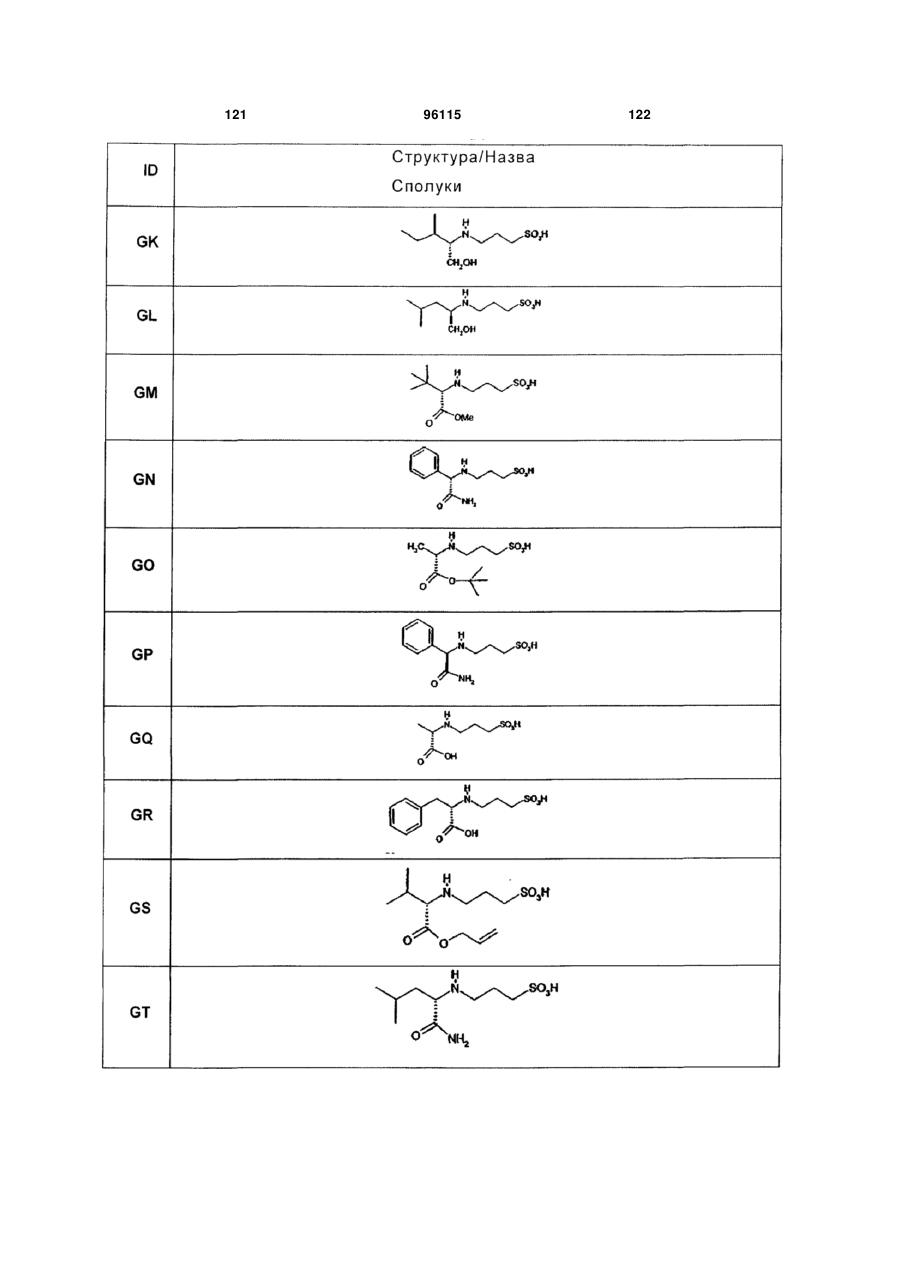
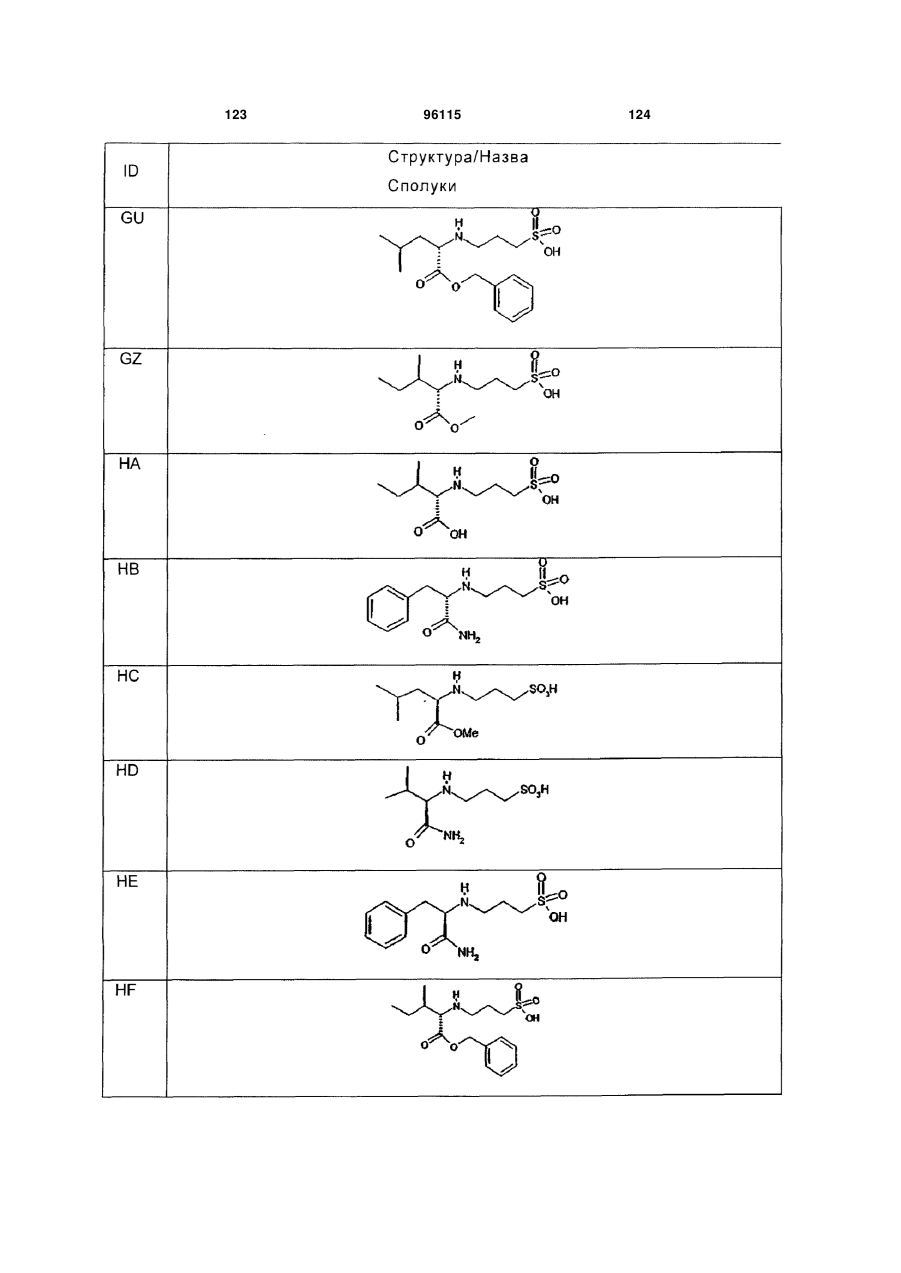
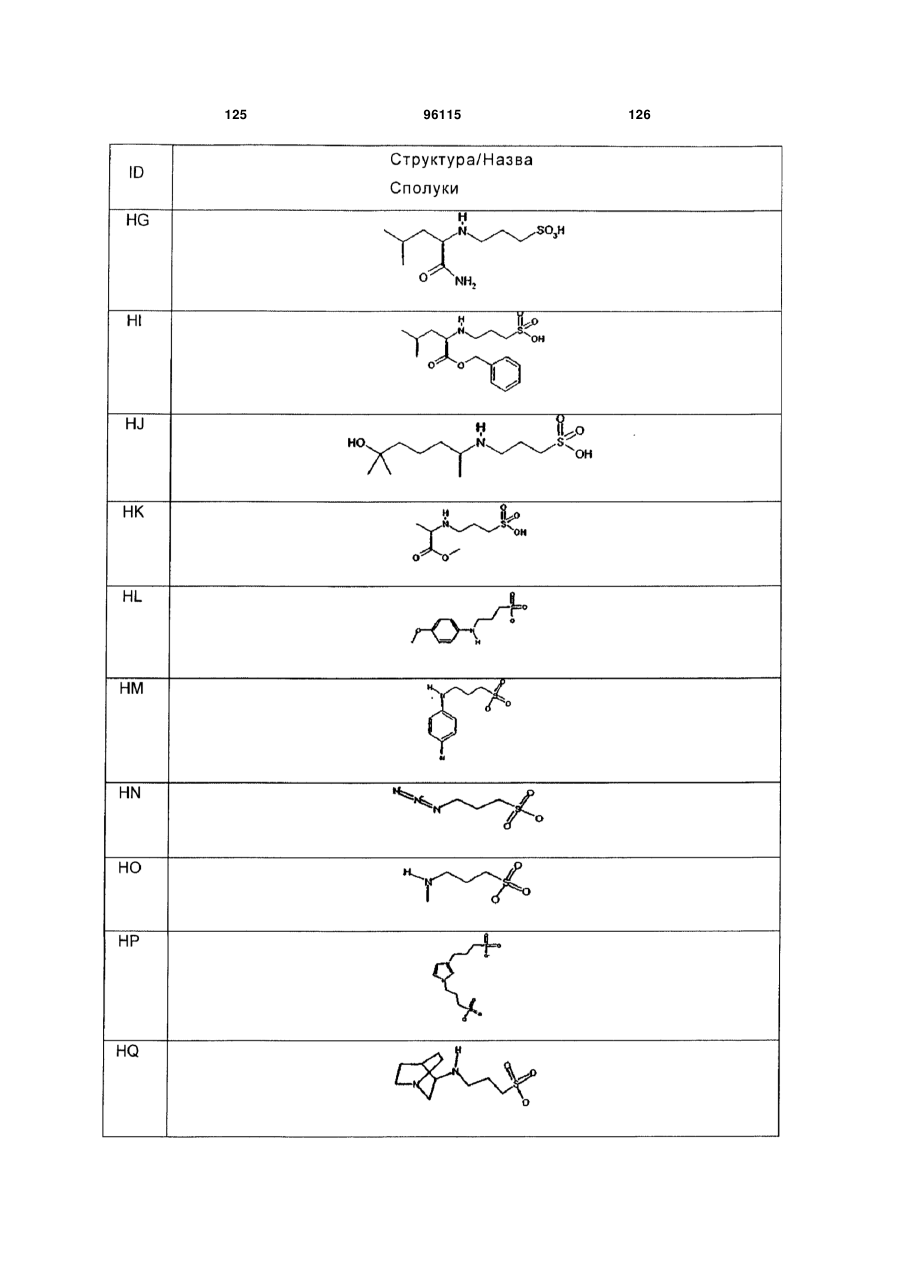
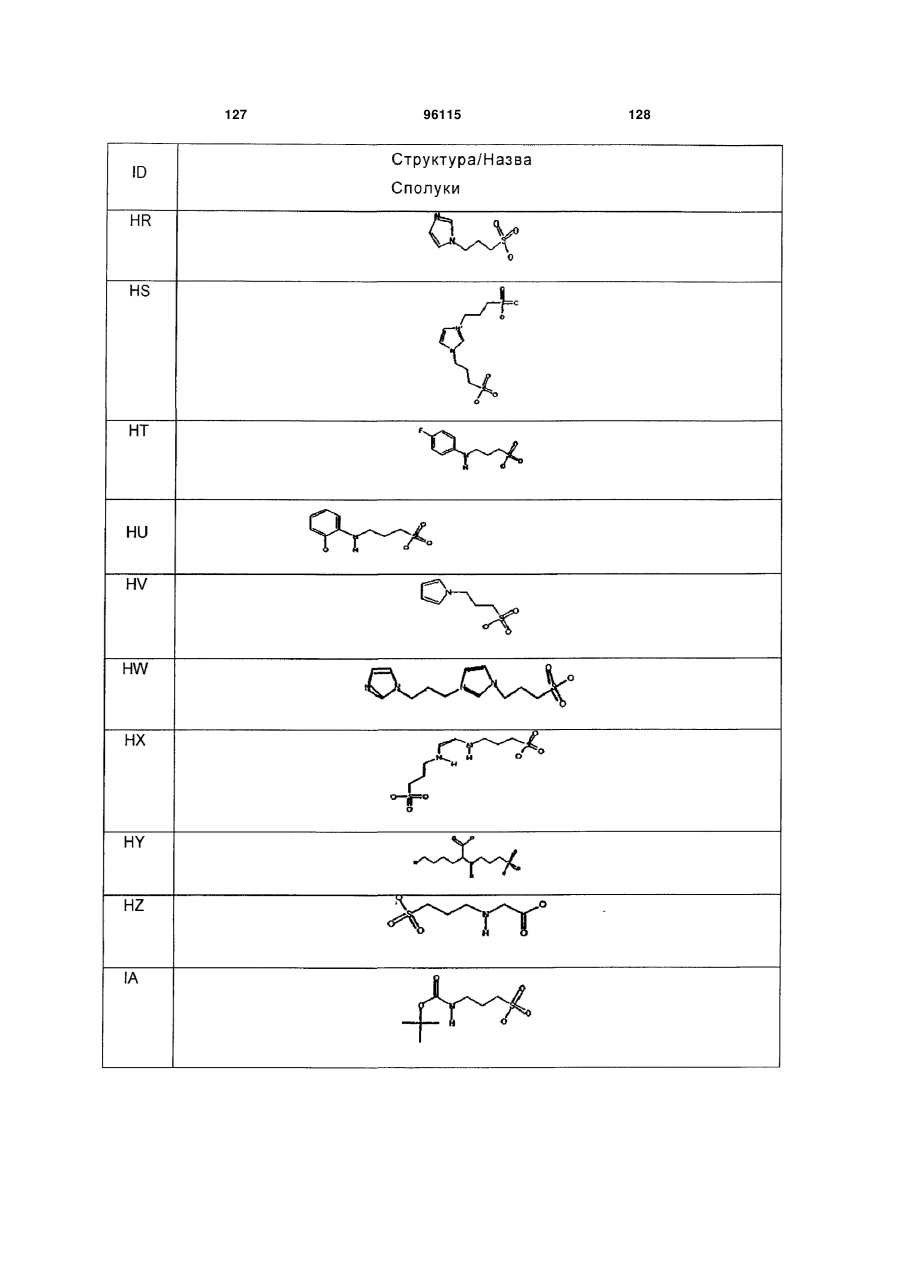
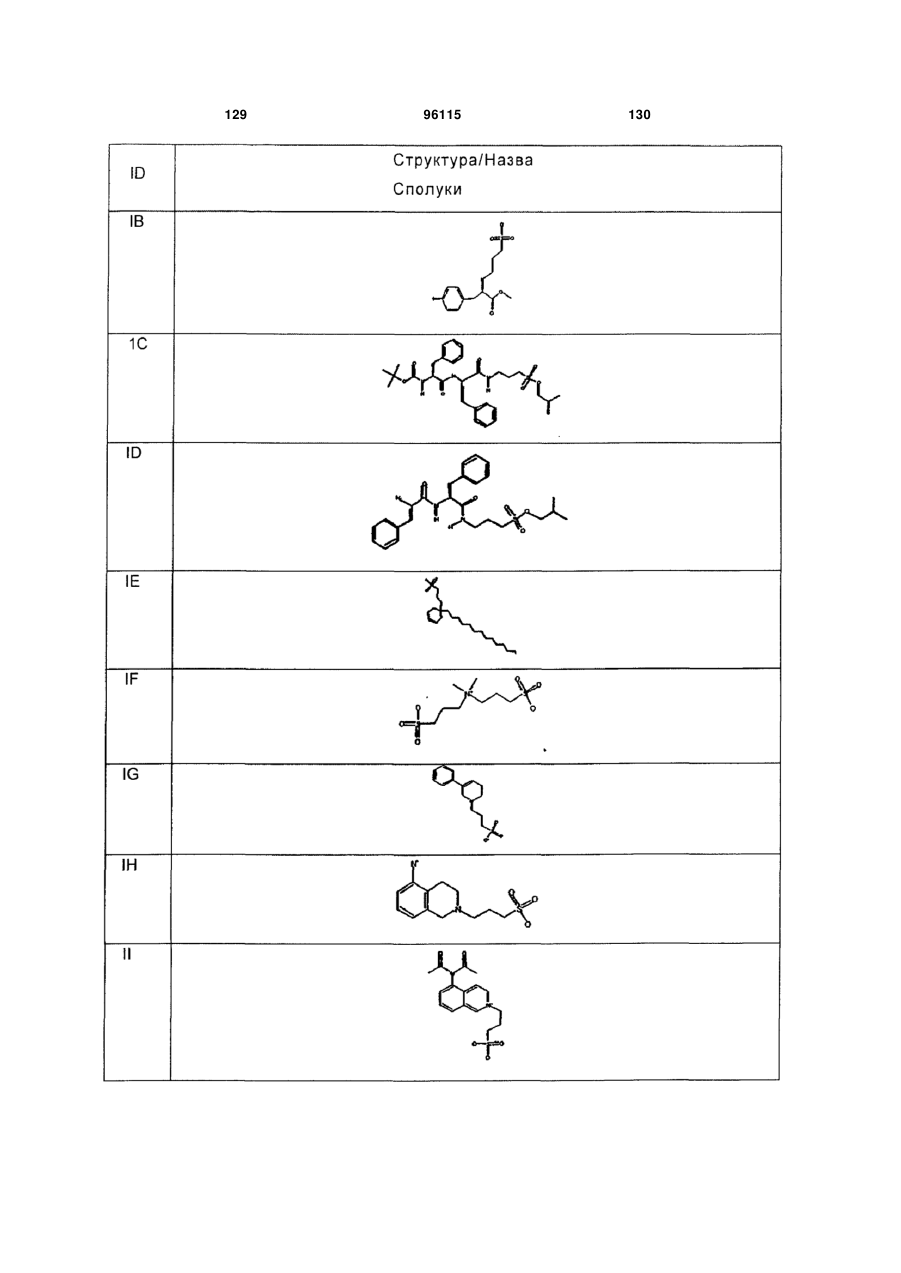
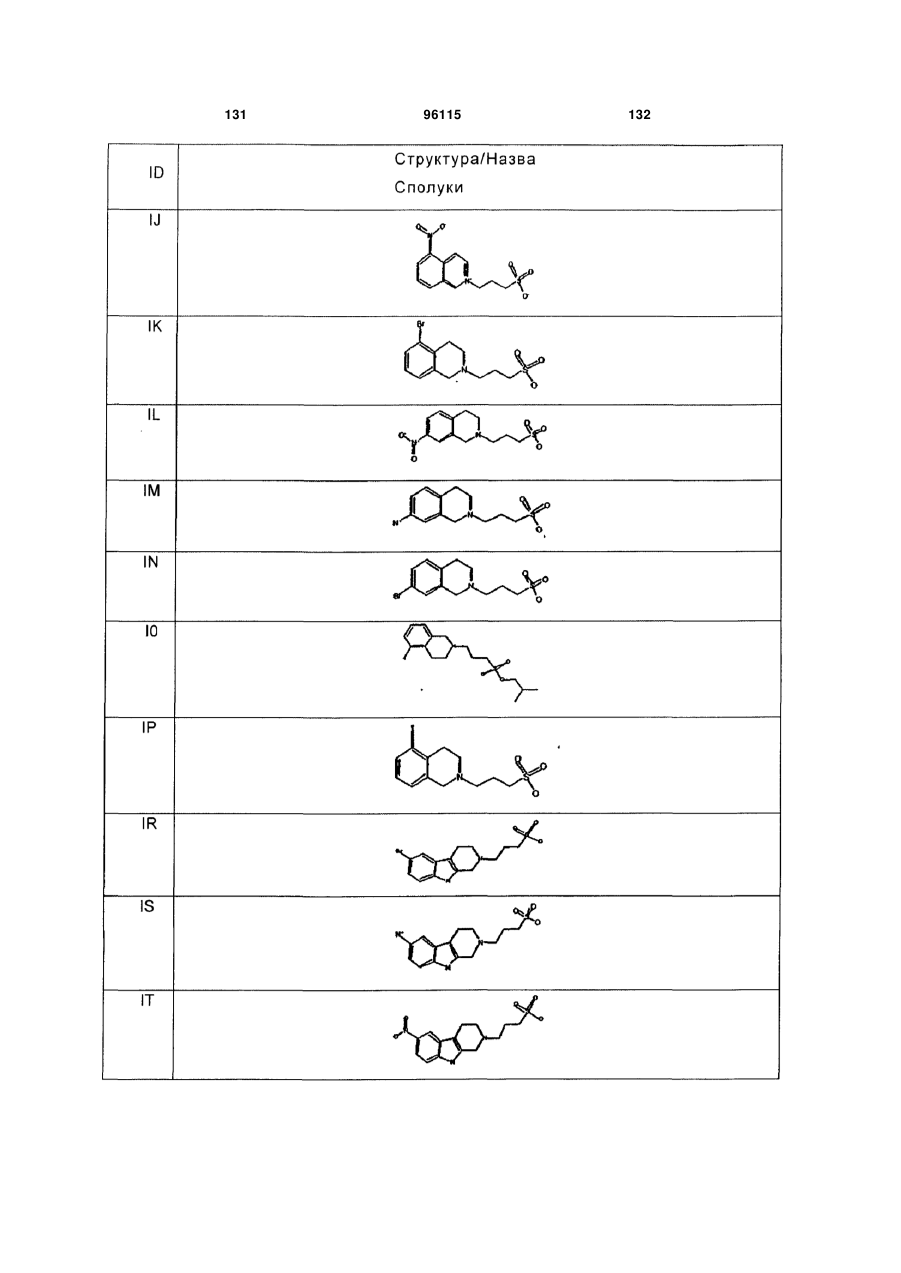
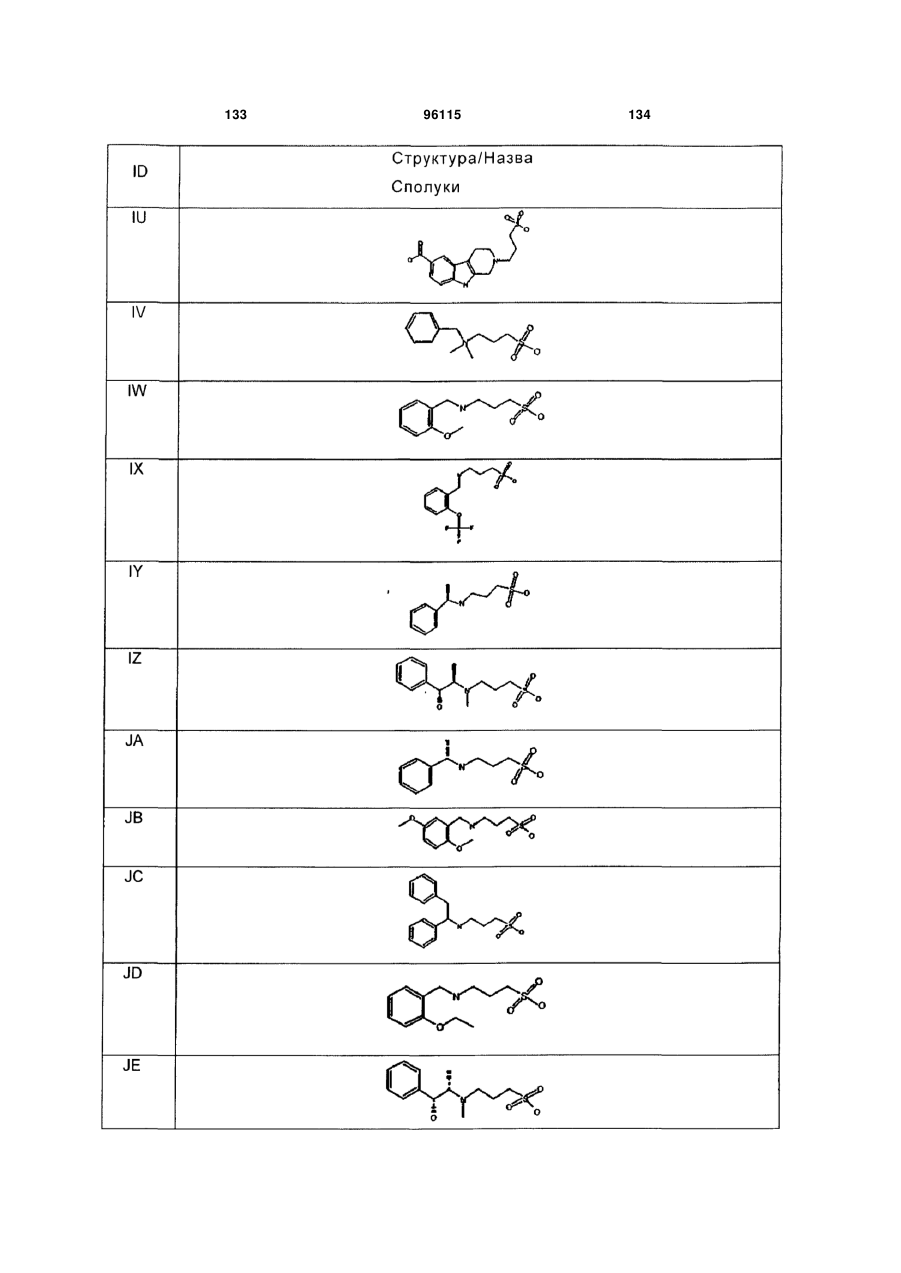
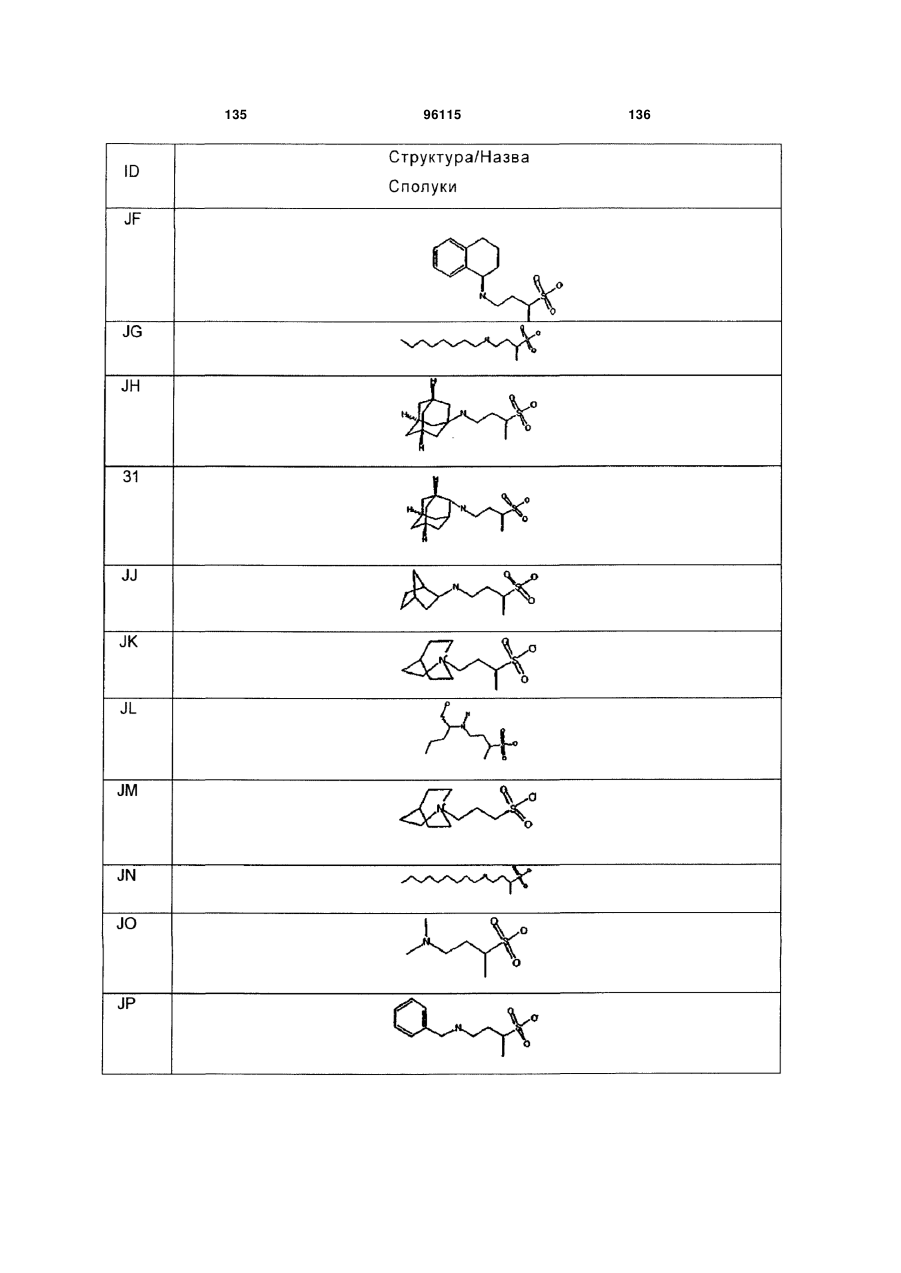
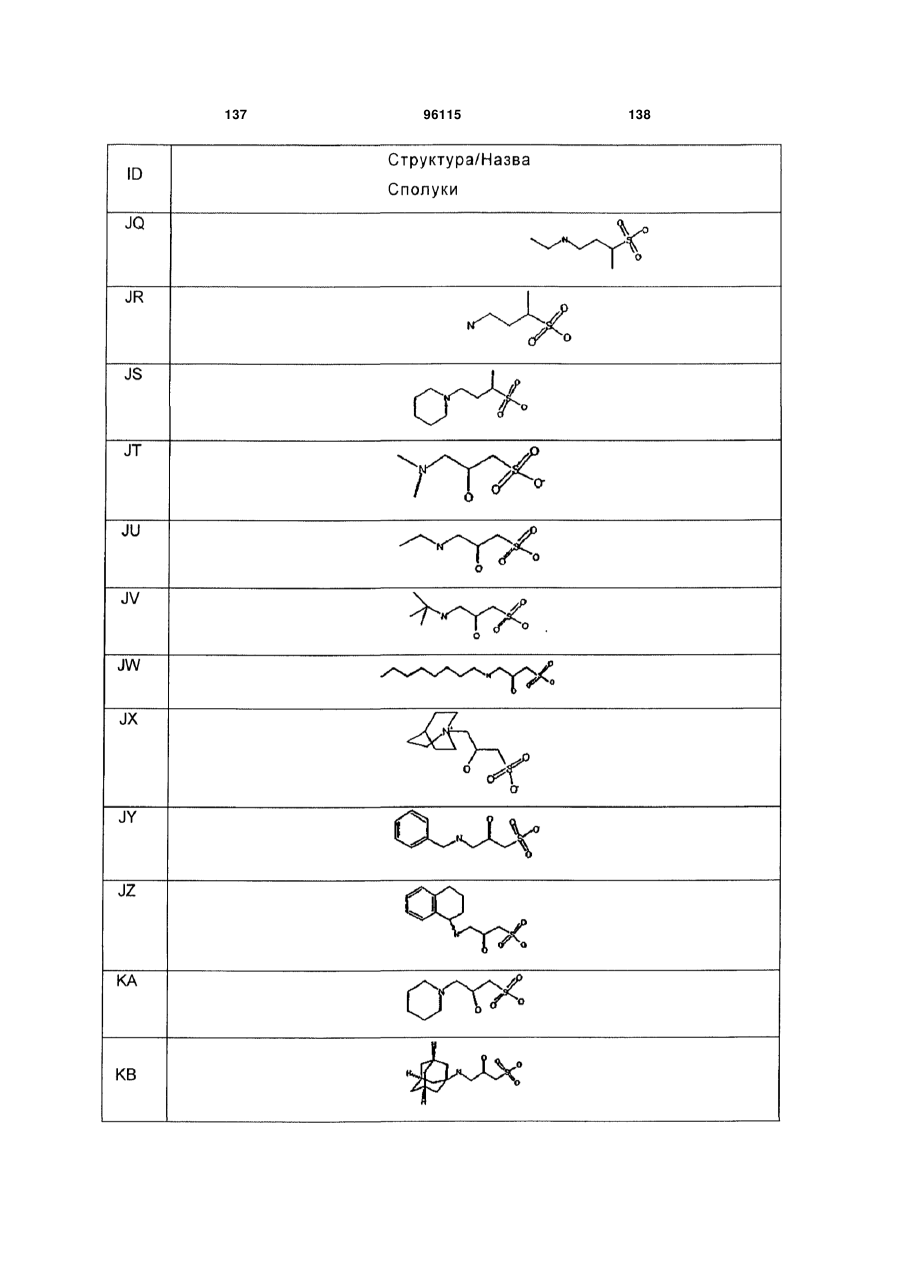
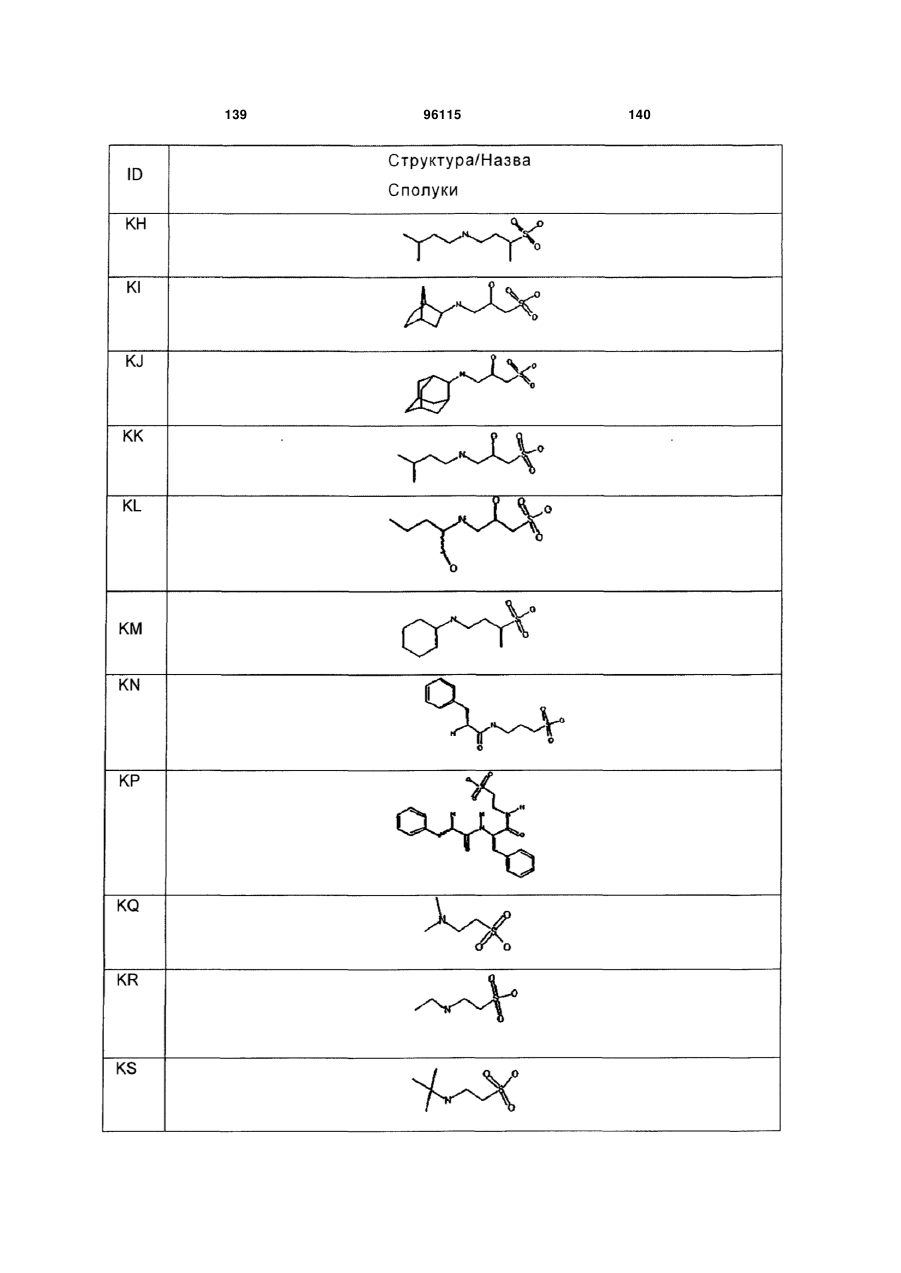
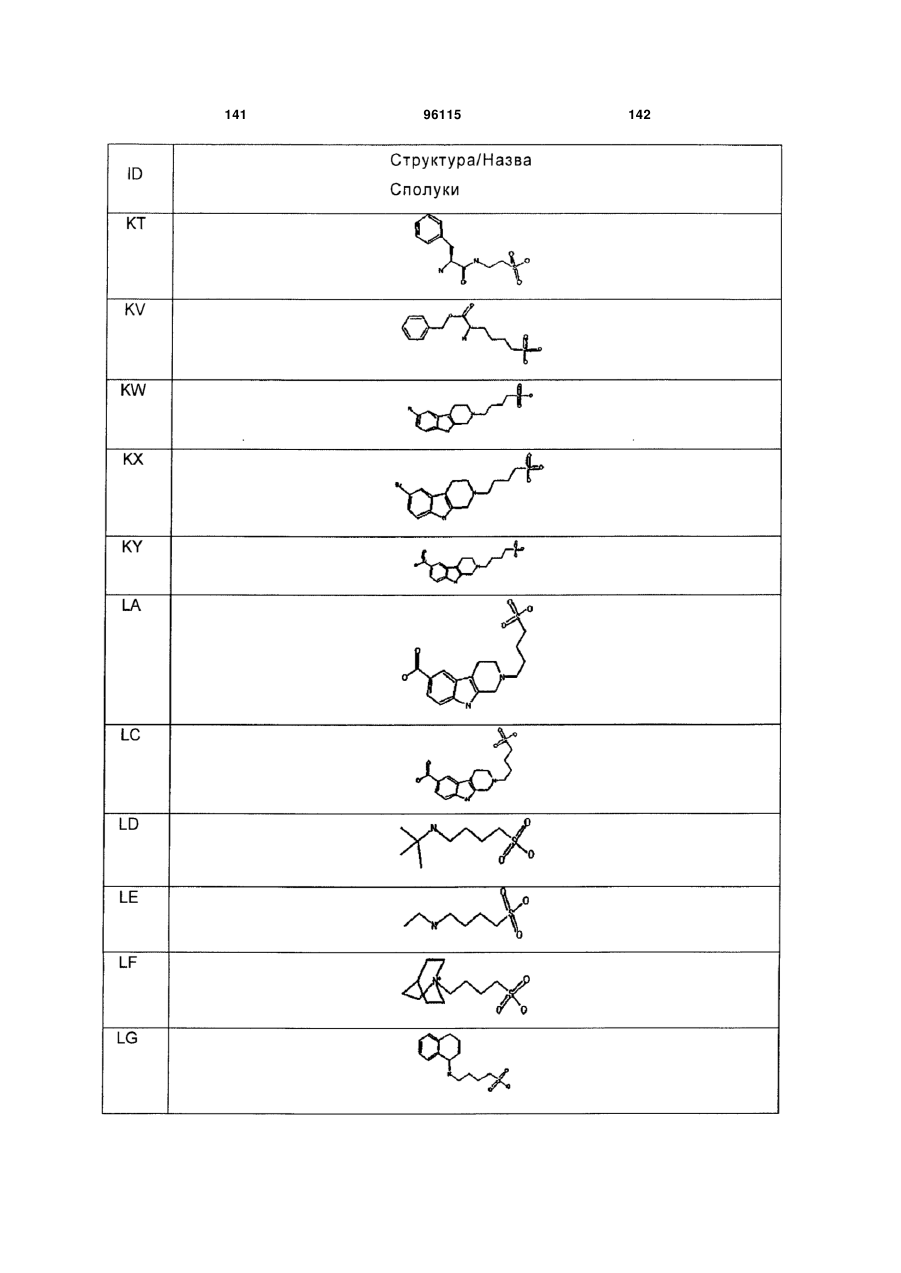
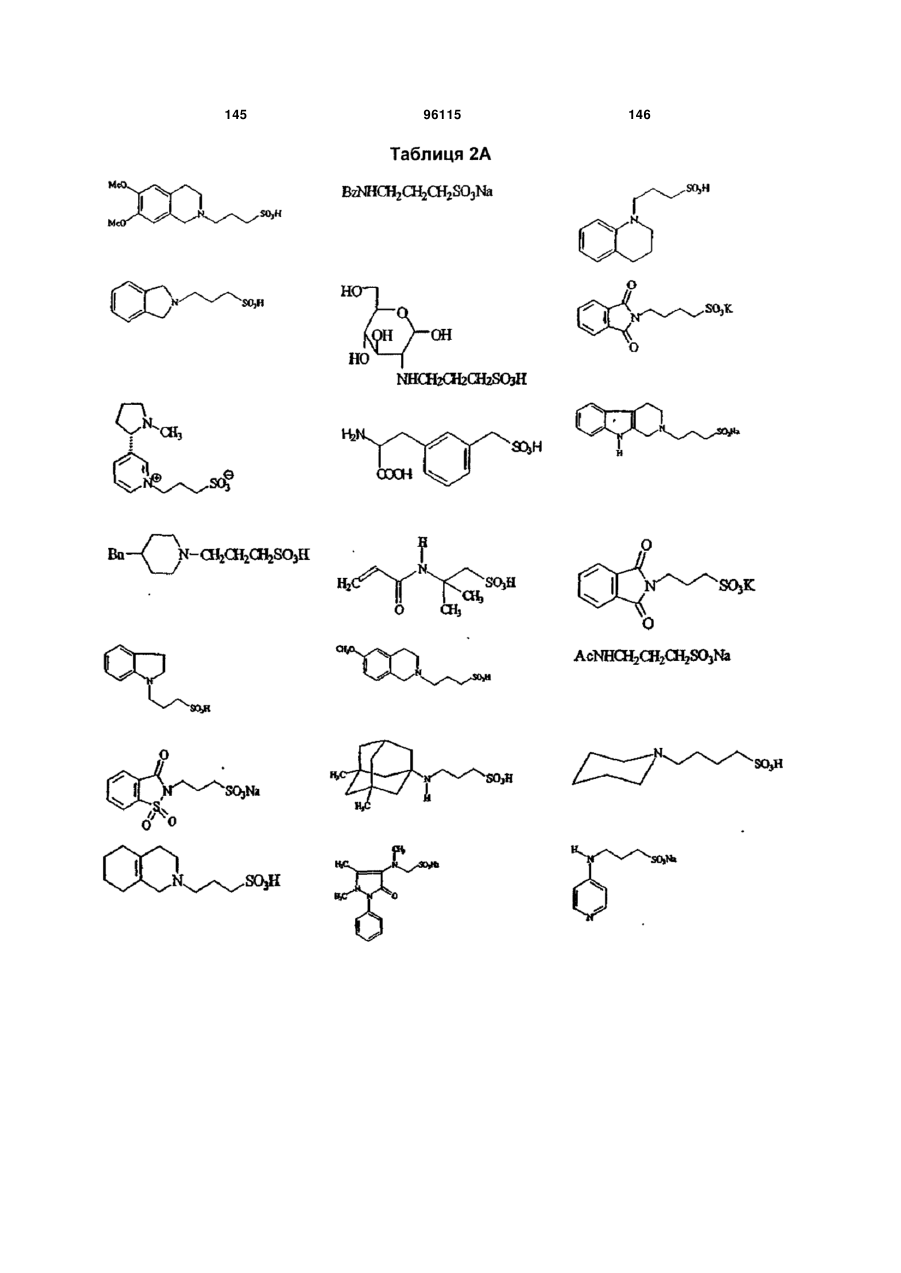
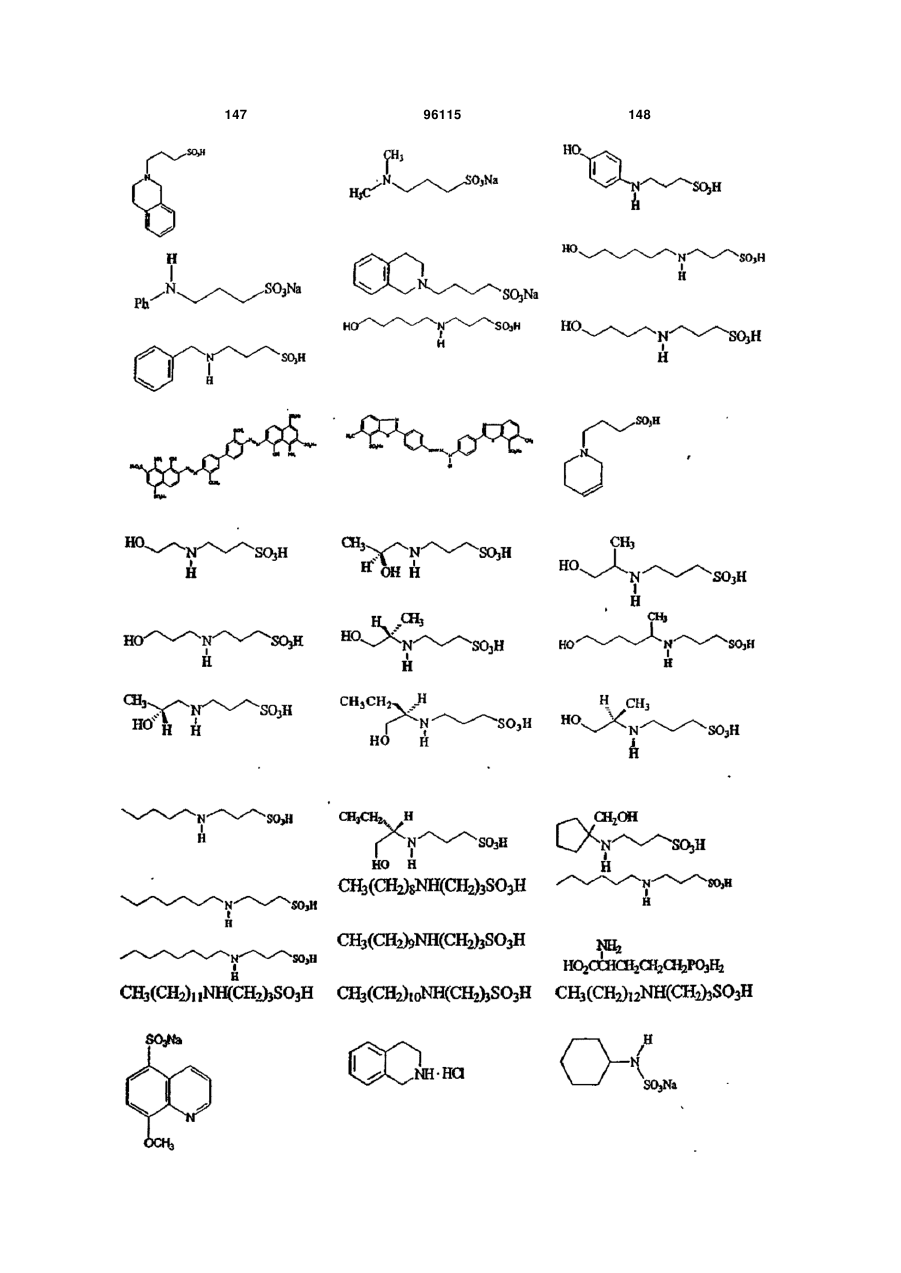
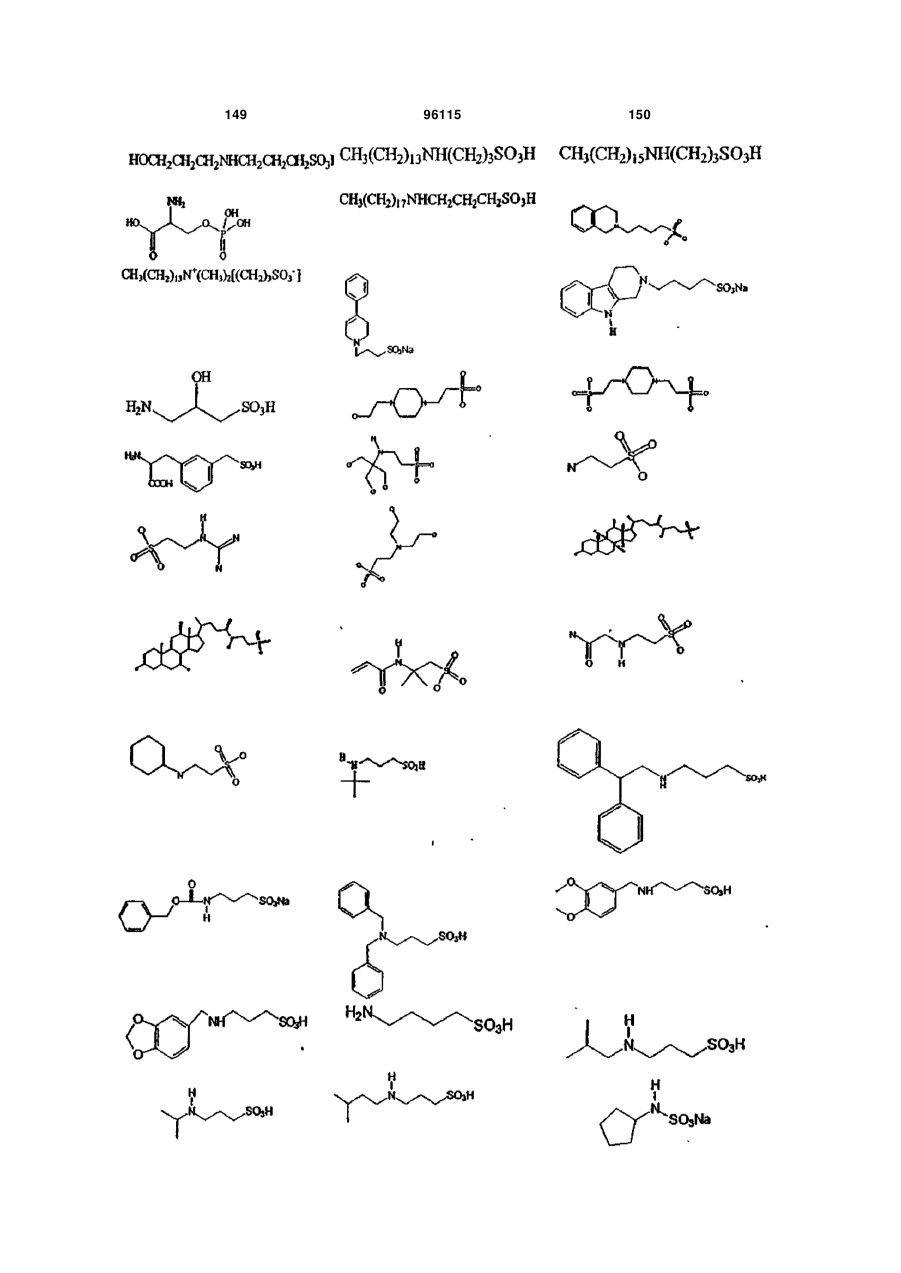
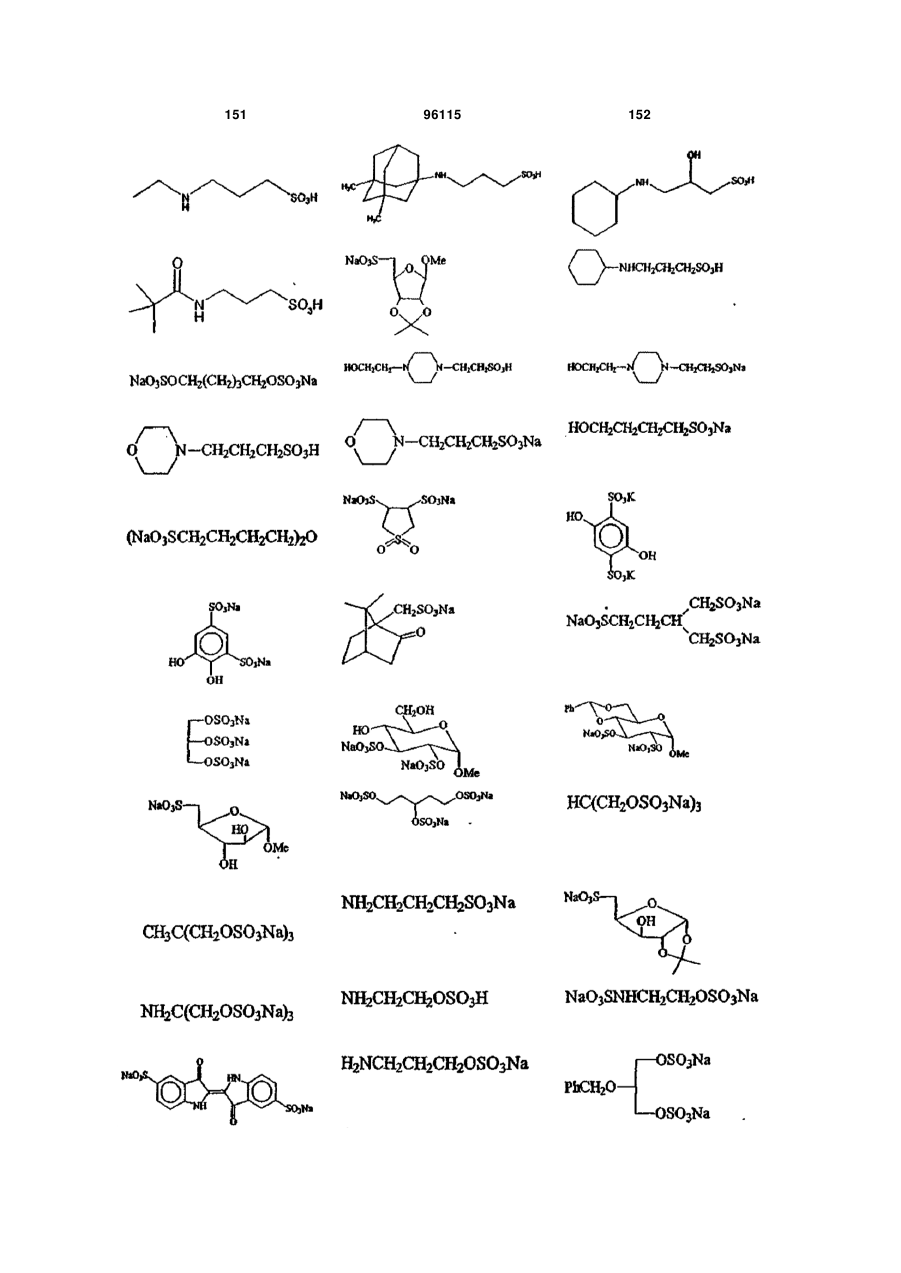
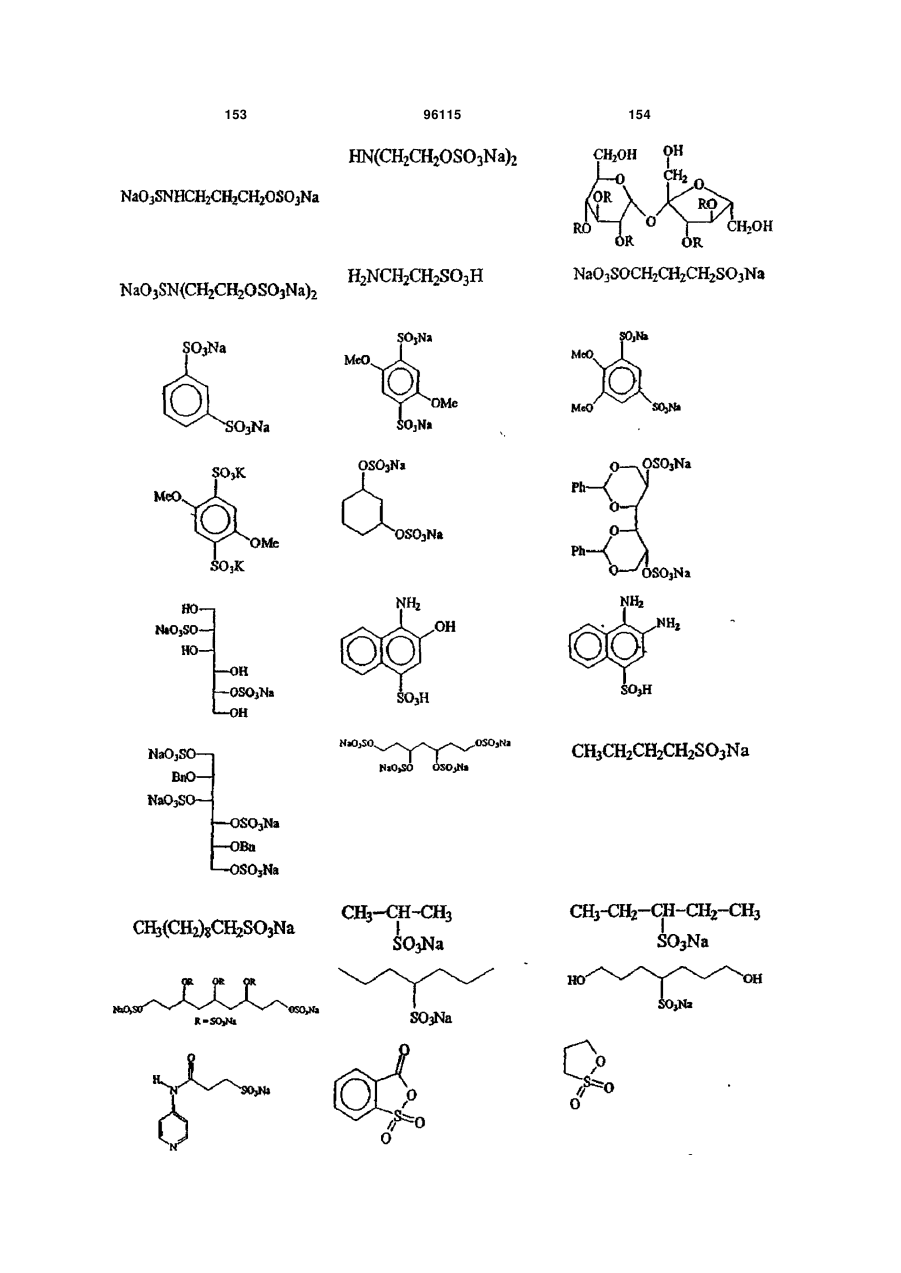
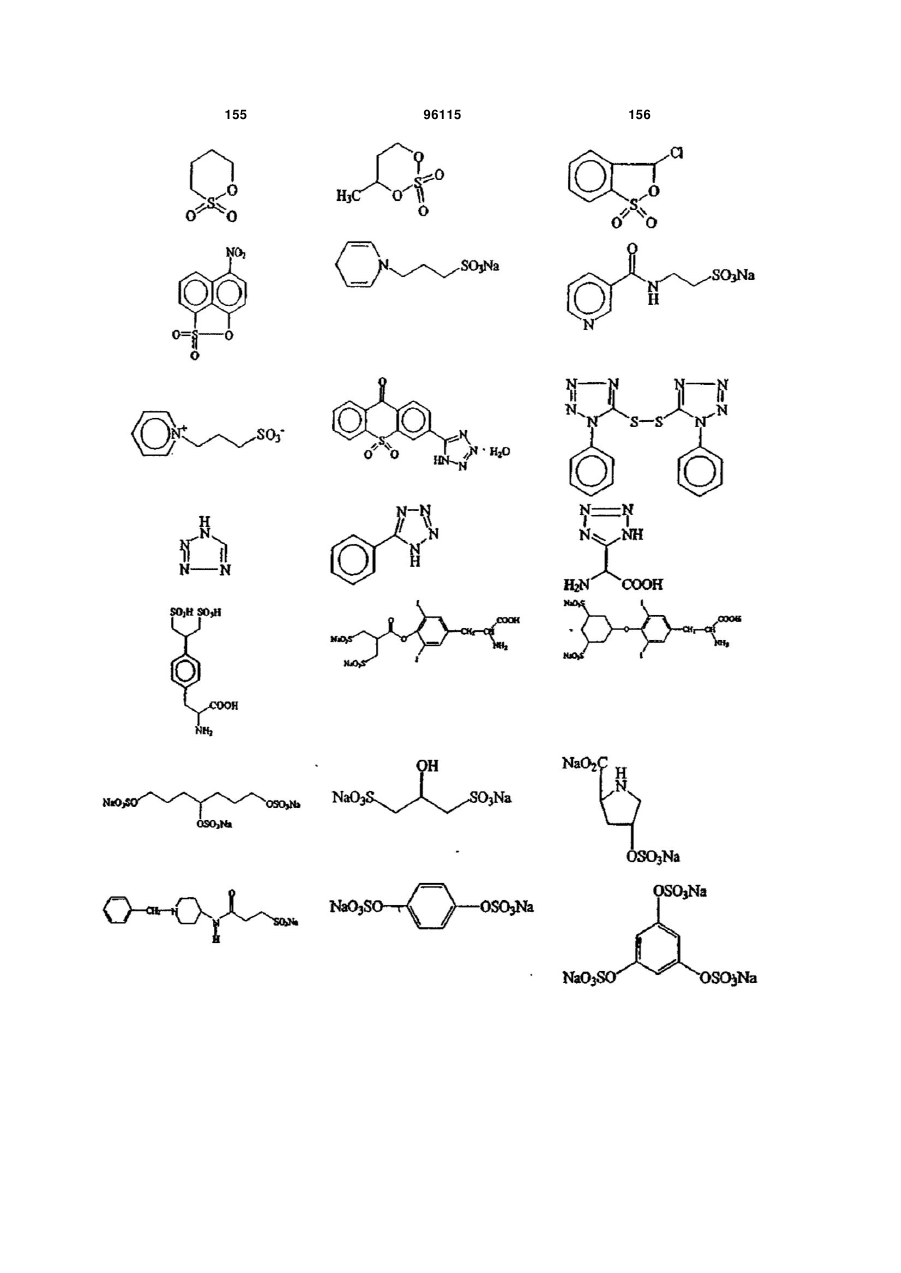
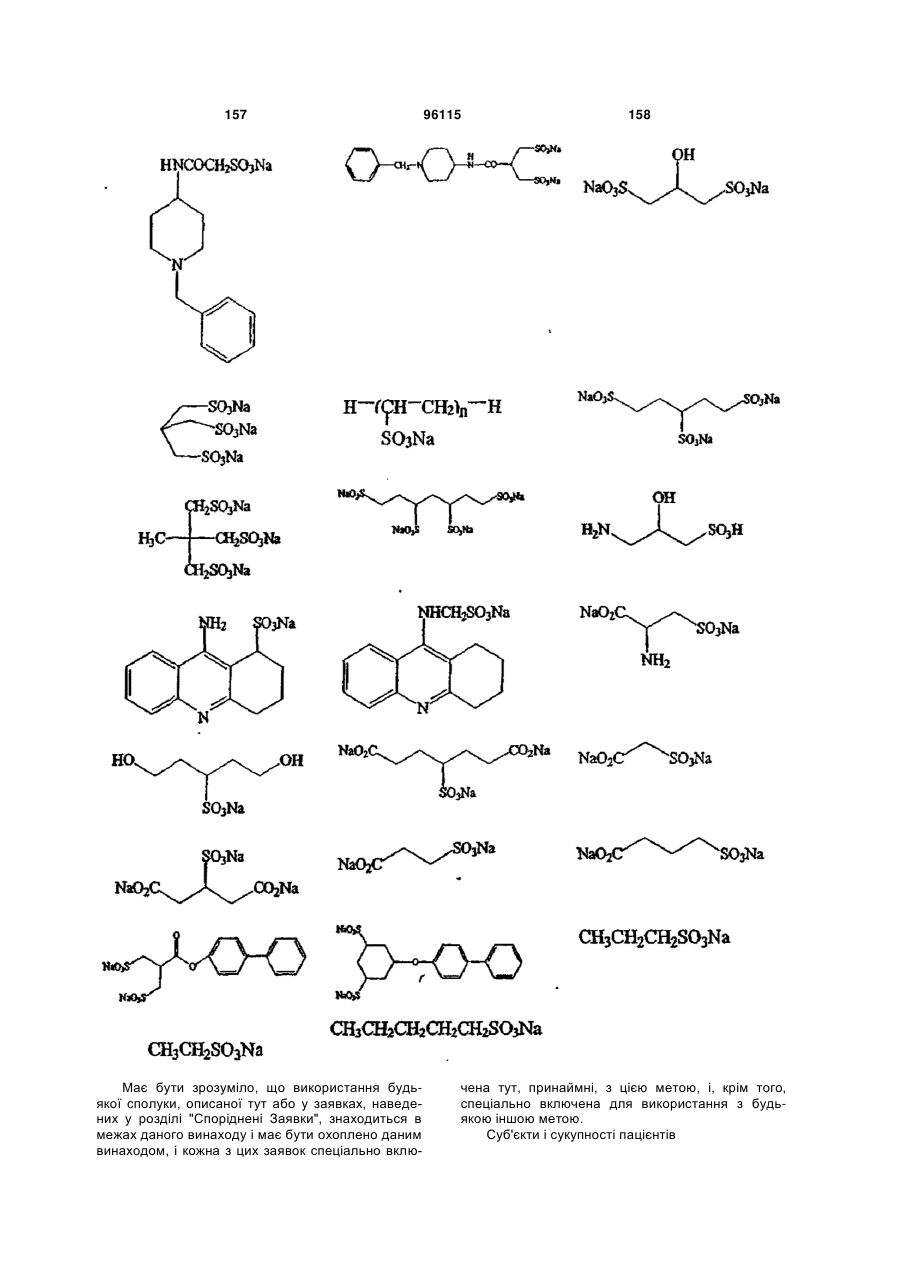
15. Сполука за п. 1, яка відрізняється тим, що вказану сполуку вибирають з групи, що складається з:
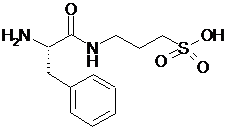 ,
,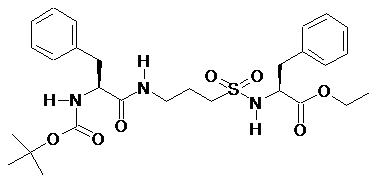 ,
, 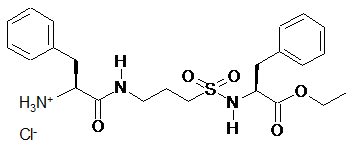 ,
, 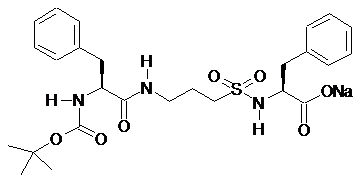 ,
, 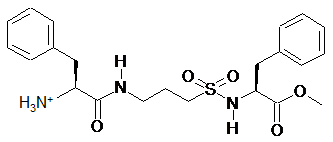 ,
, 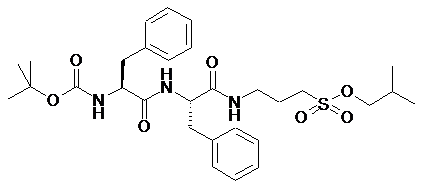 ,
, 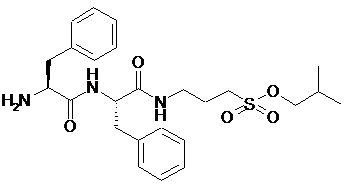
або її фармацевтично прийнятні солі, естери або проліки.
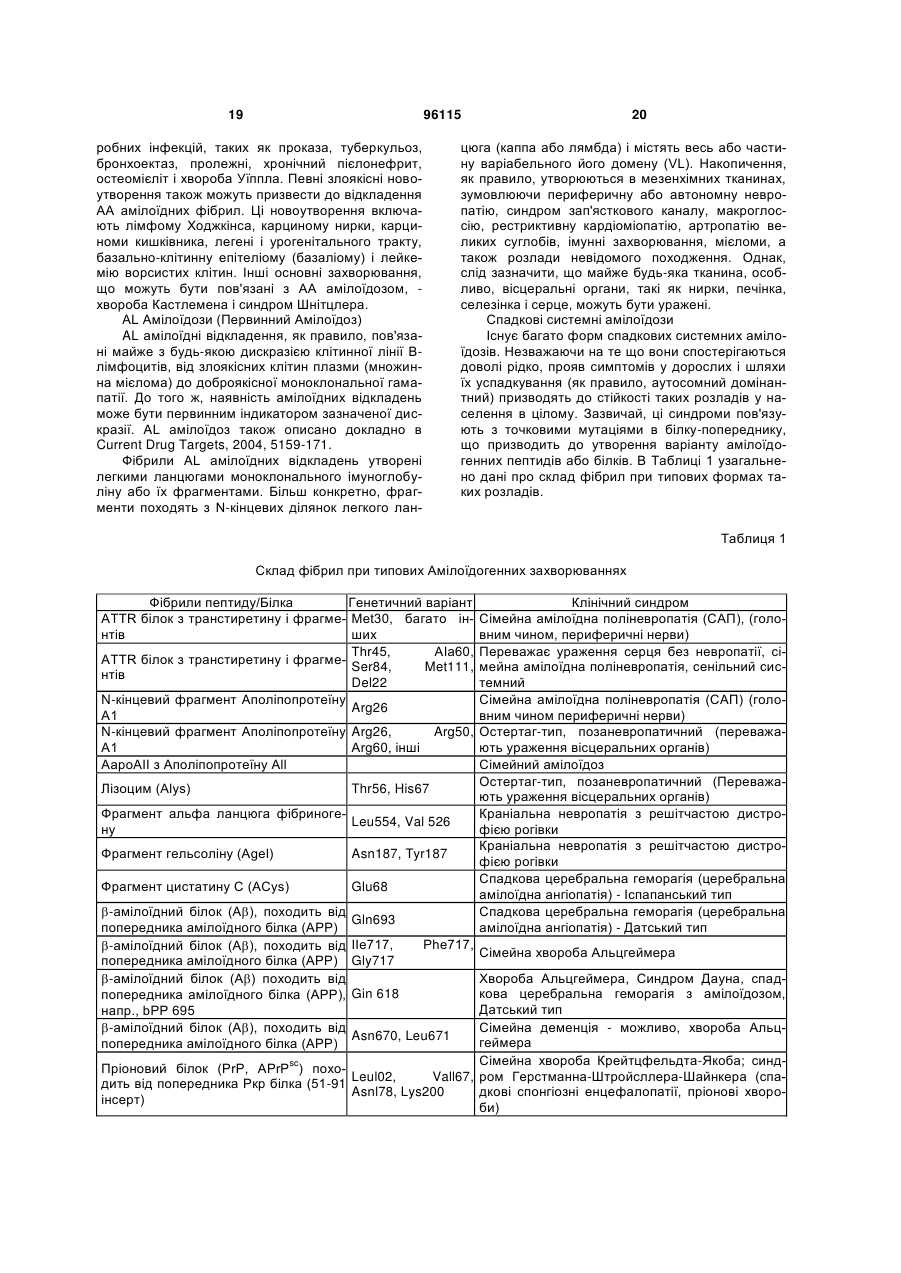
16. Сполука за п. 15, яка являє собою:
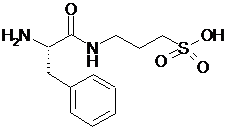 ,
,
або її фармацевтично прийнятні солі, естери або проліки.
17. Сполука за будь-яким з пп. 1-16, яка відрізняється тим, що призначена для застосування у виробництві лікарського засобу для лікування або профілактики амілоїдного захворювання або стану.
18. Сполука за пунктом 17, яка відрізняється тим, що вказане амілоїдне захворювання або стан - це β-амілоїдна хвороба або стан.
19. Сполука за пунктом 17 або 18, яка відрізняється тим, що вказане амілоїдне захворювання або стан - це хвороба Альцгеймера, легке когнітивне порушення, легке-до-помірного когнітивне порушення, старече згасання когнітивної функції, сенільна деменція, васкулярна деменція, церебральна амілоїдна ангіопатія, прогресуюча запальна міопатія, старечі дегенеративні зміни жовтої плями сітківки або синдром Дауна.
20. Сполука за пунктом 19, яка відрізняється тим, що вказане амілоїдне захворювання або стан - це хвороба Альцгеймера, легке когнітивне порушення, легке-до-помірного когнітивне порушення, старече згасання когнітивної функції або сенільна деменція.
21. Сполука за пунктом 19, яка відрізняється тим, що вказане амілоїдне захворювання або стан - це хвороба Альцгеймера.
Текст
1. Сполука формули V: R R 14 (aa)m N 15 O (CH2)n S A R 4 5. Сполука за будь-яким з пп. 1-4, яка відрізня11 ється тим, що A-R являє собою залишок природної амінокислоти або її сіль або естер. 6. Сполука за п. 5, яка відрізняється тим, що A11 R являє собою залишок фенілаланіну. 7. Сполука за будь-яким з пп. 1-4, яка відрізня11 ється тим, що А являє собою кисень і R являє собою водень або солеутворюючий катіон. 8. Сполука за будь-яким з пп. 1-7, яка відрізняється тим, що аа являє собою природний амінокислотний залишок. 9. Сполука за будь-яким з пп. 1-8, яка відрізняється тим, що (аа)m являє собою залишок фенілаланіну, гліцину або фенілаланін-фенілаланіну. 10. Сполука за будь-яким з пп. 1-9, яка відрізняється тим, що аа являє собою неприродний амінокислотний залишок. 11. Сполука за будь-яким з пп. 1-10, яка відрізня15 ється тим, що R являє собою водень або заміщений алкіл. 12. Сполука за п. 11, яка відрізняється тим, що 15 R являє собою арилалкіл. 13. Сполука за п. 11, яка відрізняється тим, що 15 R являє собою водень. 14. Сполука за будь-яким з пп. 1-10, яка відрізня14 15 ється тим, що R і R обидва являють собою водень. 15. Сполука за п. 1, яка відрізняється тим, що вказану сполуку вибирають з групи, що складається з: O 11 O , (V) де: А являє собою азот або кисень; 11 R - це водень, солеутворюючий катіон, естерна група, -(СН2)х-Q, або, коли А являє собою азот, А і 11 R , взяті разом, можуть бути залишком природної або неприродної амінокислоти, її сіллю або есте11 ром, де А і R , взяті разом, не являють собою залишок лейцину; Q - це водень, тіазоліл, триазоліл, імідазоліл, бензотіазоліл або бензоімідазоліл; х являє собою 0, 1, 2, 3 або 4; n являє собою 3; аа - це природний або неприродний Lамінокислотний залишок; m являє собою 1, 2 або 3; 14 R являє собою водень або захисну групу; 15 R являє собою водень, алкіл або арил; і її фармацевтично прийнятні солі, естери або проліки; 11 в якій, коли А являє собою кисень, R являє собою водень або солеутворюючий катіон, n являє 14 15 собою 3, m являє собою 2, і R і R обидва являють собою водень, тоді аа - це інший, ніж Lтриптофан, D-фенілаланін або D-тирозин. 2. Сполука за п. 1, яка відрізняється тим, що m має значення 1 або 2. 3. Сполука за п. 2, яка відрізняється тим, що m має значення 1. 4. Сполука за п. 2, яка відрізняється тим, що m має значення 2. H2N N H O OH S O , H N H N O O O S O O O N H O , H N H3N+ Cl O O S O O N H O , 5 96115 6 16. Сполука за п. 15, яка являє собою: O H N H N O O O S O H2N O ONa N H O N H3N+ S O O O N O , O H N N H O H O N H O O S O O , H N H2N O O N H O S O S OH O O , H N H O O , або її фармацевтично прийнятні солі, естери або проліки. 17. Сполука за будь-яким з пп. 1-16, яка відрізняється тим, що призначена для застосування у виробництві лікарського засобу для лікування або профілактики амілоїдного захворювання або стану. 18. Сполука за пунктом 17, яка відрізняється тим, що вказане амілоїдне захворювання або стан - це β-амілоїдна хвороба або стан. 19. Сполука за пунктом 17 або 18, яка відрізняється тим, що вказане амілоїдне захворювання або стан - це хвороба Альцгеймера, легке когнітивне порушення, легке-до-помірного когнітивне порушення, старече згасання когнітивної функції, сенільна деменція, васкулярна деменція, церебральна амілоїдна ангіопатія, прогресуюча запальна міопатія, старечі дегенеративні зміни жовтої плями сітківки або синдром Дауна. 20. Сполука за пунктом 19, яка відрізняється тим, що вказане амілоїдне захворювання або стан - це хвороба Альцгеймера, легке когнітивне порушення, легке-до-помірного когнітивне порушення, старече згасання когнітивної функції або сенільна деменція. 21. Сполука за пунктом 19, яка відрізняється тим, що вказане амілоїдне захворювання або стан - це хвороба Альцгеймера. або її фармацевтично прийнятні солі, естери або проліки. Ця заявка проголошує приорітет патентної заявки США № 10/___,___, зареєстрованої 18 червня, 2004 (зареєстровано патентним повіреним за № NBI-162A), патентної заявки США № 107____,____, зареєстрованої 18 червня, 2004 (зареєстровано патентним повіреним за № NBI162B), тимчасової заявки на патент США № 60/512,047, зареєстрованої 17 жовтня, 2003, і тимчасової заявки на патент США № 60/480,906, зареєстрованої 23 червня, 2003, всі мають назву Способи і композиції для лікування амілоїдогенних захворювань. Ця заявка споріднена також з тимчасовою заявкою на патент США № 60/512,017, зареєстрованою 17 жовтня, 2003, тимчасовою заявкою на патент США № 60/480,918, поданою 23 червня, 2003, і тимчасовою заявкою на патент США № 10/__,__, зареєстрованою 18 червня, 2004 (зареєстровано патентним повіреним за № NBI-149), всі мають назву Способи для лікування розладів, пов'язаних з агрегацією білка. Ця заявка споріднена з тимчасовою заявкою на патент США № 60/512,116, зареєстрованою 17 жовтня, 2003, тимчасовою заявкою на патент США № 60/480,984, зареєстрованою 23 червня, 2003, і заявкою США 10/____,____, зареєстрованою 18 червня, 2004 (зареєстровано патентним повіреним за № NBI-152), всі мають назву Технологія приготування сполук для інгібування нагромадження амілоїдного білка. Ця заявка споріднена з тимчасовою заявкою на патент США № 60/436,379, зареєстрованою 24 грудня, 2002, тимчасовою заявкою на патент США № 60/482,214, зареєстрованою 23 червня, 2003, всі мають назву Комбінована терапія для лікування хвороби Альцгеймера, Заявка на патент США № 10/746,138, зареєстрована 24 грудня, 2003, Заявка на міжнародний патент № 7 РСТ/СА2003/002011, і заявка на патент США №10/__,__, зареєстрована 18 червня, 2004 (зареєстровано за № NBI-154CP), що мають назву Терапевтичні композиції для лікування захворювань, пов'язаних з бета-амілоїдом. Ця заявка споріднена з тимчасовою заявкою на патент США № 60/512,135, зареєстрованою 17 жовтня, 2003, тимчасовою заявкою на патент США № 60/482,058, зареєстрованою 23 червня, 2003, обидві мають назву Процес синтезу для виготовлення сполук для лікування амілоїдозу, і Заявки на патент США № 10/___,____, зареєстрованої 18 червня, 2004 (зареєстровано патентним повіреним за № NBI-156), названої Покращені кандидати лікарських препаратів та способи їх виготовлення. Ця заявка споріднена з тимчасовою заявкою на патент США № 60/512,018, зареєстрованою 17 жовтня, 2003 і тимчасовою заявкою на патент США, серійний № 60/480,928, зареєстрованою 23 червня, 2003, і заявкою на патент США 10/___,___, зареєстрованою 18 червня, 2004 (зареєстровано патентним повіреним за № NBI-163), всі мають назву Способи і композиції для лікування амілоїдогенних захворювань та захворювань, пов'язаних з епілептогенезом. Ця заявка пов'язана також зі Способом лікування Амілоїдозу, Патентною заявкою США № 08/463,548, зараз Патент США № 5,972,328. Таким чином, повний зміст кожної з цих заявок на патент і кожного патенту спеціально включений тут у вигляді посилання, включаючи, без обмежень, докладний опис, формулу винаходу, реферат, а також будь-які їх фігури, таблиці або рисунки. Передумови винаходу Амілоїдоз - це патологічний стан, який характеризується наявністю амілоїдних фібрил. Амілоїд - це загальний термін, що охоплює групу різноманітних, але специфічних білкових відкладень (інтрацелюлярних або екстрацелюлярних), які спостерігаються при цілій низці різноманітних захворювань. Незважаючи на різноманітну локалізацію, всі амілоїдні відкладення мають спільні морфологічні особливості, забарвлюються специфічними барвниками (наприклад, Конго червоним), і мають характерний червоно-зелений двозаломний зовнішній вигляд у поляризованому світлі після забарвлювання. Вони також мають спільні ультраструктурні особливості, спільну дифракцію рентгенівських променів та інфрачервоні спектри. Амілоїдогенні захворювання можуть бути обмежені або одним органом, або поширюватись на кілька органів. У першому випадку йдеться про "локалізований амілоїдоз", тоді як в другому - про "системний амілоїдоз". Деякі амілоїдні захворювання можуть бути ідіопатичними, але більшість з цих захворювань виникають як ускладнення розладів, що вже раніше існували. Наприклад, первинний амілоїдоз (AL амілоїд) може з'являтись без будь-якої іншої патології або може розвиватись після дискразії клітинної плазми або множинної мієломи. Вторинний амілоїдоз, як правило, пов'язаний з хронічною інфекцією (такою як туберкульоз) або хронічним запаленням (таким як ревматоїдний 96115 8 артрит). Сімейна форма вторинного амілоїдозу також зустрічається серед інших типів сімейного амілоїдозу, наприклад, сімейна середземноморська гарячка (ССГ) - цей сімейний тип амілоїдозу генетично успадковується і виявляється в специфічних популяціях людей. Як при первинному, так і при вторинному амілоїдозі, відкладення виявляються в кількох органах, і, таким чином, вважаються системними амілоїдогенними захворюваннями. "Локалізовані амілоїдози" - це ті види амілоїдозу, які охоплюють одну систему органів. Різні амілоїдогенні захворювання відрізняються за типом білка, який входить до складу відкладень. Наприклад, нейродегенеративні хвороби, такі як скрепі, спонгіозний енцефаліт великої рогатої худоби, хвороба Крейтцфельда-Якоба, тощо характеризуються появою та накопиченням протеазорезистентної форми пріонового білка (названого як AScr або РrР-27) в центральній нервовій системі. Аналогічно, хвороба Альцгеймера, інший приклад нейродегенеративного розладу, характеризується наявністю невритичних бляшок і нейрофібрилярних клубків. В цьому випадку, амілоїдні бляшки, виявлені в паренхімі і кровоносних судинах, утворюються через відкладання фібрилярного Α амілоїдного білка. Інші хвороби, такі як доросла форма діабету (діабет II типу), характеризується локалізованим накопиченням амілоїдних фібрил у підшлунковій залозі. Якщо ці амілоїдні відкладення утворились, не існує відомої, широко розповсюдженої терапії або лікування, яке б істотно розчиняло амілоїдні відкладення in situ, попереджувало подальше нагромадження амілоїду або попереджувало ініціацію амілоїдних відкладень. Кожен амілоїдогенний білок має здатність зазнавати конформаційних змін і організовуватись в -складчасті структури і утворювати нерозчинні фібрили, які можуть відкладатись екстрацелюлярно або інтрацелюлярно. Кожен амілоїдогенний білок, незважаючи на відмінності у амінокислотній послідовності, має ту ж саму здатність утворювати фібрили і зв'язуватись з іншими елементами, такими як протеоглікан, амілоїд Ρ і компонент комплемента. Крім того, кожен амілоїдогенний білок має амінокислотну послідовність, яка, незважаючи на те, що є різною, виявляє спільні риси, такі як наявність ділянок, що мають здатність зв'язуватись з глікосаміноглікановою (ГАГ) частиною протеоглікану (названою як ГАГ-зв'язуючий центр), а також інших ділянок, які сприяють -складчастої структури. Протеоглікани - це макромолекули, що мають різні розміри та будову, які розповсюджені по всьому тілу. Їх можна виявити в інтрацелюлярному компартменті, на поверхнях клітин, і як частину екстрацелюляного матриксу. Основною структурою всіх протеогліканів є капсидний білок і, щонайменше, один, але часто більше, полісахаридних ланцюгів (ГАГ-ділянки), прикріплені до капсидного білка. Багато різних ГАГ було відкрито, включаючи хондроїтин сульфат, дерматан сульфат, кератан сульфат, гепарин і гіалуронан. В особливих випадках, амілоїдні фібили, якщо вже вони відклались, можуть ставати токсичними для оточуючих клітин. Наприклад, було показано, 9 що Α фібрили, які утворюють сенільні бляшки, зв'язані з мертвими нейронами, дистрофічними невритами, астроцитозом і мікрогліозом у пацієнтів з хворобою Альцгеймера. При дослідженні in vitro було показано, що олігомерний (розчинний), а також фібрилярний Α пептид здатні бути пусковим механізмом процесів активування мікрогліальних клітин (макрофагів мозку), що могло бути поясненням наявності мікрогліозу і запалення мозку, виявлених у хворих на хворобу Альцгеймера. Як олігомерний, так і фібрилярний Α пептид можуть також індукувати смерть нервових клітин in vitro. Див., наприк., МР Lambert, et al., Proc. Natl. Acad. Sci. USA 95,6448-53 (1998). При іншому типі амілоїдозу, що спостерігається у пацієнтів з діабетом II типу, було показано, що амілоїдогенний білок ІАРР, який присутній в олігомерній або фібрилярній формі, індукує токсичність клітин -острівців in vitro. Відповідно, поява ІАРР фібрил в підшлунковій залозі пацієнтів, що потерпають від діабету II типу, сприяє втраті -клітин острівців (Лангерганса) і дисфункції органу, що може призвести до інсулінемії. Інший тип амілоїдозу, який виявлено у хворих, що тривалий час перебувать на гемодіалізі, пов'язують з 2 мікроглобуліном. У пацієнтів, що підлягають гемодіалізу протягом тривалого часу, будуть розвиватись фібрили 2 мікроглобуліну в каналі зап'ястка і тканинах, багатих на колаген, у деяких суглобах. Це викликає серйозні болі, негнучкість та опухання суглобів. Амілоїдоз притаманний також для хвороби Альцгеймера. Хвороба Альцгеймера - це руйнівна хвороба мозку, що призводить до прогресуючої втрати пам'яті та розвитку деменції, інвалідності внаслідок соматичних порушень і відмирання протягом відносно тривалого проміжку часу. Зі старінням населення у розвинених країнах число пацієнтів, що потерпають від хвороби Альцгеймера, сягає розмірів епідемії. У осіб, які потерпають від хвороби Альцгеймера, розвивається прогресуюча деменція у дорослому віці, що супроводжується трьома основними структурними змінами в мозку: дифузною втратою нейронів у множинних частинах мозку; нагромадженням інтрацелюлярних білкових відкладень, які називаються нейрофібрилярними клубками; і нагромадженням екстрацелюлярних білкових відкладень, які називаються амілоїдними або сенільними бляшками, що оточені нервовими закінченнями, які мають неправильну форму (дистрофічні нейрити) і активізованими мікрогліальними клітинами (мікрогліоз і астроцитоз). Основним компонентом амілоїдних бляшок є -амілоїдний пептид (Α), утворений 39-43 амінокислотами білок, що утворюється внаслідок процесингу попередника -амілоїдного білка (АРР - amyloid precursor protein). Були виконані всебічні дослідження, для того щоб з'ясувати значення Α відкладень у розвитку хвороби Альцгеймера, див., наприклад, Selkoe, Trends in Cell Biology 8,447-453 (1998). Α природно виникає внаслідок метаболічного процесингу попередника амілоїдного білка ("АРР") в ендопла 96115 10 зматичному ретикулюмі ("ЕР"), апараті Гольджі, або ендосомально-лізосомальному шляху метаболізму, і , як правило, секретується у вигляді пептиду, утвореного 40 ("Α1-40") або 42 ("Α1-42") амінокислотами (Selkoe, Annu. Rev. Cell Biol. 10,373-403 (1994)). Значення Α як первинного чинника у виникненні хвороби Альцгеймера підтверджує наявність екстрацелюлярних відкладень Α в сенільних бляшках, що спостерігаються при хворобі Альцгеймера, зростання утворення Α в клітинах, що несуть мутантні гени, пов'язані з хворобою Альцгеймера, наприклад, попередника амілоїдного білка, пресенілін І і пресенілін II; і токсичність екстрацелюлярного розчинного (олігомерного) або фібрилярного Α щодо клітин в культурі. Див., наприклад, Gervais, Eur. Biophann. Review, 40-42 (Autumn 2001); May, DDT 6,459-62 (2001). Незважаючи на існування симптоматичного лікування хвороби Альцгеймера, наразі виникнення цієї хвороби не можна ні попередити, ні вилікувати її. Хвороба Альцгеймера характеризується дифузними і невритичними бляшками, церебральною ангіопатією і нейрофібрилярними клубками. Вважають, що амілоїд бляшок і кровоносних судин утворюється через нагромадження нерозчинного Α амілоїдного білка, який може бути описаний як дифузний або фібрилярний. Вважають, що як розчинний олігомерний Α, так і фібрилярний Α, є нейротоксичними і можуть викликати запалення. Іншим типом амілоїдозу є церебральна амілоїдна ангіопатія (ЦАА). ЦАА являє собою специфічне нагромадження -амілоїдних фібрил в стінках лептоменінгеальних або кортикальних артерій, артеріол і вен. Як правило, він пов'язаний з хворобою Альцгеймера, синдромом Дауна і звичайним старінням, а також з цілою низкою спадкових чинників, що обумовлюють раптовий напад або деменцію (див. Frangione e al., Amyloid: J. Protein Folding Disord. 8, Suppl. 1, 36-42 (2001)). Відомі на сьогодні способи лікування амілоїдогенних захворювань є цілковито симптоматичними, тобто вони забезпечують лише тимчасове або часткове покращення клінічних симптомів. Незважаючи на те що деякі фармацевтичні препарати були описані як такі, що приносять часткове симптоматичне покращення, наразі відсутня всебічна фармакологічна терапія для профілактики або лікування, наприклад, хвороби Альцгеймера. Короткий опис винаходу Цей винахід пов'язаний з використанням певних сполук для лікування амілоїдогенних захворювань. Зокрема, цей винахід пов'язаний зі способом лікування або попередження амілоїдогенного захворювання у суб'єкта, який полягає у введенні суб'єкту терапевтичної кількості сполуки винаходу. Цей винахід також стосується кожної нової сполуки винаходу, що тут описані. До сполук для використання у винаході належать сполуки за наступними Формулами, такі, що при введенні викликають зменшення або інгібування утворення амілоїдних фібрил, дисфункції певного органу (наприклад, нейродегенерацію) або клітинної токсичності. 11 В одному втіленні, винахід стосується, принаймні, частково, сполук за Формулою І: де: 1 R являє собою заміщене або незаміицене циклоалкільне, гетероциклічне, арильне, арилциклоалкільне, біциклічне або трициклічне кільце, біциклічну або трициклічну сконденсовану кільцеву групу, або заміщену чи незаміщену С2-С10 алкільну групу; 2 R обраний з групи, яка включає водень, алкіл, меркаптоалкіл, алкеніл, алкініл, цикпоалкіл, арил, арилалкіл, тіазоліл, триазоліл, імідазоліл, бензотіазоліл, і бензоімідазоліл; + + + Υ являє собою SO3X , OSO3X або SSO3X ; + Х - це водень, катіонна група або естерна група (тобто, якщо йдеться про проліки у будьякому іншому місці цього опису); і 1 2 кожен серед L і L є незалежно заміщена або незаміщена С1-С5 алкільна група, яка може бути відсутня, або фармацевтично прийнятна її сіль, за 1 1 умови, що, коли R являє собою алкіл, L відсутня. В іншому втіленні, винахід стосується, принаймні, частково сполук за Формулою II: де: 1 R являє собою заміщену або незаміщену циклічну, біциклічну, трициклічну, або бензогетероциклічну групу або заміщену чи незаміщену С2-С10 алкільну групу; 2 R являє собою водень, алкіл, меркаптоалкіл, алкеніл, алкініл, циклоалкіл, арил, арилалкіл, тіазоліл, триазоліл, імідазоліл, бензотіазоліл, бензоі1 мідазоліл, або зв'язаний з R і утворює гетероциклічну сполуку; + + + Υ являє собою SO3X , OSO3X або SSO3X ; + Х - це водень, катіонна група або частина молекули, що утворює естер; m має значення 0 або 1; n має значення 1,2, 3 або 4; L - заміщена або незаміщена С1-С3 алкільна група, що може бути відсутня, або фармацевтично де: А - це азот або кисень; 96115 12 1 прийнятна її сіль, за умови, що, коли R являє собою алкіл, L - відсутня. В іншому втіленні, винахід стосується, принаймні, частково сполук за Формулою III: де: А являє собою азот або кисень; 11 R являє собою водень, солеутворюючий катіон, естерну групу, -(СН2)х-Q, або якщо А являє 11 собою азот, А і R , взяті разом можуть бути залишком природної або неприродної амінокислоти або її сіллю чи естером; Q - це водень, тіазоліл, триазоліл, імідазоліл, бензотіазоліл або бензоімідазоліл; x являє собою 0, 1, 2, 3 або 4; n являє собою 0, 1, 2 ,3, 4, 5, 6, 7, 8, 9 або 10; 3 3a 4 4a 5 5a 6 6a 7 7a R , R , R , R , R , R , R , R , R і R є кожен незалежно водень, алкіл, меркаптоалкіл, алкеніл, алкініл, циклоалкіл, арил, алкілкарбоніл, арилкарбоніл, алкоксикарбоніл, ціано, галоген, аміно, тетразоліл або дві R групи на прилеглих кільцевих атомах, взяті разом з кільцевими атомами, утворюють подвійні зв'язки, за умови, що один з-поміж 3 3a 4 4a 5 5a 6 6a 7 7a R , R , R , R , R , R , R , R , R і R являє собою компонент Формули ІІІа: де: m являє собою 0, 1, 2, 3 або 4; A B C D E R , R , R , R , i R є незалежно обрані з групи, яка включає водень, галоген, гідроксил, алкіл, алкоксил, галогензаміщений алкіл, меркаптоалкіл, алкеніл, алкініл, циклоалкіл, арил, ціано, тіазоліл, триазоліл, імідазоліл, тетразоліл, бензотіазоліл, і бензоімідазоліл; і фармацевтично прийнятні його солі та естери, за умови, що вказані сполуки не є 3-(4-феніл-1,2,3,6-тетрагідро-1-піридил)-1пропансульфонова кислота. В ще одному втіленні, винахід стосується, принаймні, частково сполук за Формулою IV: 11 R являє собою водень, солеутворюючий катіон, естерну групу, -(СН2)х-Q, якщо А являє собою 13 11 96115 14 7 азот, А і R , взяті разом можуть бути залишком природної або неприродної амінокислоти, або її сіллю чи естером; Q - це водень, тіазоліл, триазоліл, імідазоліл, бензотіазоліл, або бензоімідазоліл; x являє собою 0, 1, 2, 3 або 4; n являє собою 0,1, 2 ,3, 4, 5, 6, 7, 8, 9 або 10; 4 4a 5 5a 6 6a 7 7a R , R , R , R , R , R , R , і R кожен незалежно є водень, алкіл, меркаптоалкіл, алкеніл, алкініл, циклоалкіл, арил, алкілкарбоніл, арилкарбоніл, алкоксикарбоніл, ціано, галоген, аміно, тетразоліл, 4 5 R і R , взяті разом з кільцевими атомами, до яких 6 вони приєднані, утворюють подвійні зв'язки, або R і R , взяті разом, з кільцевими атомами до яких вони прикріплені, утворюють подвійні зв'язки; m являє собою 0, 1, 2, 3 або 4; 8 9 10 11 12 R , R , R , R , і R незалежно обрані з групи, яка включає водень, галоген, гідроксил, алкіл, алкоксил, галогензаміщений алкіл, меркаптоалкіл, алкеніл, алкініл, циклоалкіл, арил, ціано, тіазоліл, триазоліл, імідазоліл, тетразоліл, бензотіазоліл, і бензоімідазоліл, і фармацевтично прийнятні його солі та естери. В іншому втіленні, винахід включає сполуки за Формулою V: де: А являє собою азот або кисень; 11 R - це водень, солеутворюючий катіон, естерна група, -(СН2)х-Q, або, коли А являє собою 11 азот, А і R , взяті разом можуть бути залишком природної або неприродної амінокислоти, її сіллю або естером; Q - це водень, тіазоліл, триазоліл, імідазоліл, бензотіазоліл, або бензоімідазоліл; x являє собою 0, 1, 2, 3 або 4; n являє собою 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 або 10; аа - це природний або неприродний амінокислотний залишок; m являє собою 0, 1, 2 або 3; 14 R являє собою водень або захисну групу; 15 R являє собою водень, алкіл або арил, і фармацевтично прийнятні їх солі або проліки. В іншому втіленні, винахід включає сполуки за Формулою VI: де: n - 1, 2, 3, 4, 5, 6, 7, 8, 9 або 10; А являє собою кисень або азот; 11 R - водень, солеутворюючий катіон, естерна група, -(СН2)х-Q, або якщо А являє собою азот, 11 А і R , взяті разом можуть бути залишком природної або неприродної амікослоти, її сіллю або естером; Q - це водень, тіазоліл, триазоліл, імідазоліл, бензотіазоліл, або бензоімідазоліл; x має значення 0, 1, 2, 3 або 4; 19 R - водень, алкіл або арил; 1 Y - кисень, сірка або азот; 2 Y - вуглець, азот або кисень; 20 R являє собою водень, алкіл, аміно, меркаптоалкіл, алкеніл, алкініл, циклоалкіл, арил, арилалкіл, тіазоліл, триазоліл, тетразоліл, імідазоліл, бензотіазоліл або бензоімідазоліл; 21 R являє собою водень, алкіл, меркаптоалкіл, алкеніл, алкініл, циклоалкіл, арил, арилалкіл, тіазоліл, триазоліл, тетразоліл, імідазоліл, бензо2 тіазоліл, бензоімідазоліл або відсутній, якщо Y являє собою кисень; 22 R являє собою водень, алкіл, меркаптоалкіл, алкеніл, алкініл, циклоалкіл, арил, арилалкіл, тіазоліл, триазоліл, тетразоліл, імідазоліл, бензо22 тіазоліл, бензоімідазоліл; або R являє собою 1 водень, гідроксил, алкокси або арилокси, якщо Y 22 1 являє собою азот; або R відсутній, якщо Y яв22 21 ляє собою кисень або сірку; або R і R можуть бути зв'язані і утворювати циклічну складову мо1 лекули, якщо Y - це азот; 23 R являє собою водень, алкіл, аміно, меркаптоалкіл, алкеніл, алкініл, циклоалкіл, арил, арилалкіл, тіазоліл, триазоліл, тетразоліл, імідазоліл, бензотіазоліл, або бензоімідазоліл, або відсутній, 2 якщо Y являє собою азот або кисень; або фармацевтично прийнятні їх солі. В іншому втіленні, винахід включає сполуки за Формулою VII 15 де: n - 2, 3 або 4; А - являє собою кисень або азот; 11 R - являє собою водень, солеутворюючий катіон, естерну групу, -(СН2)х-Q, або якщо А являє 11 собою азот, А і R , взяті разом можуть бути залишком природної або неприродної амікослоти, її сіллю або естером; Q - це водень, тіазоліл, триазоліл, імідазоліл, бензотіазоліл або бензоімідазоліл; X являє собою 0, 1, 2, 3 або 4; G означає прямий зв'язок або кисень, азот чи сірку; z являє собою 0, 1, 2, 3, 4 або 5; m має значення 0 або 1; 24 R обрано з групи, що включає водень, алкіл, меркаптоалкіл, алкеніл, алкініл, ароїл, алкілкарбоніл, аміноалкілкарбоніл, циклоалкіл, арил, арилалкіл, тіазоліл, триазоліл, імідазоліл, бензотіазоліл, і бензоімідазоліл; 25 кожен R є незалежно обраний з-поміж водню, галогену, ціано, гідроксилу, алкокси, тіолу, аміно, нітро, алкілу, арилу, карбоциклічних або гетероциклічних сполук і фармацевтично прийнятних їх солей. В одному втіленні, сполуки, розкриті тут, попереджують або інгібують агрегацію амілоїдного білка в нерозчинні фібрили, які in vivo нагромаджуються в різних органах, або сприяють очищенню відкладень, що утворились раніше, або уповільнють відкладення у пацієнтів, що вже мають такі відкладення. В іншому втіленні, сполука може також попереджувати зв'язування або адгезію амілоїдного білка, в його розчинній, олігомерній або його фібрилярній формі, з поверхнею клітин, що спричиняє ушкодження клітини або цитотоксичність. В ще іншому втіленні, сполука може блокувати клітинну токсичність, викликану амілоїдним білком, або активацію макрофагів. В іншому втіленні, сполука може блокувати нейротоксичність або активацію мікрогліальних клітин, обумовлену амілоїдним білком. В іншому втіленні, сполука захищає від цитотоксичності, обумовленої амілодним білком, клітини -острівців. В іншому втіленні, сполука може посилювати виведення амілоїдного білка з певного органу, наприклад, мозку або зменшення концентрації амілоїдного білка у такий спосіб, що відбувається попередження утворення амілоїдних фібрил в органі-мішені. Сполуки винаходу можуть бути застосовані терапевтично або профілактично, для того щоб лікувати захворювання, пов'язане з утворенням амілоїдних фібрил, їх агрегацією і нагромадженням. Сполуки винаходу можуть діяти, для того щоб покращувати протікання амілоїдогенного захворювання, завдяки будь-якому з наступних механізмів (цей перелік має на меті проілюструвати, а не об 96115 16 межувати): уповільнення швидкості утворення або нагромадження амілоїдних фібрил; зменшення ступеню нагромадження амілоїду; інгібування, зменшення або попередження утворення амілоїдних фібрил; інгібування нейродегенерації або клітинної токсичності, індукованої амілоїдом; інгібування запалення, індукованого амілоїдом; посилення очищення амілоїду; або сприяння розщепленню амілоїдного білка перед його організацією у фібрили. Сполуки винаходу можуть бути застосовані терапевтично або профілактично для лікування захворювань, пов'язаних з утворенням, агрегацією або нагромадженням -амілоїдних фібрил. Сполуки винаходу можуть діяти, для того щоб покращувати протікання захворювання, пов'язаного з утворенням -амілоїду завдяки будь-якому з наступних механізмів (цей перелік має на меті проілюструвати, а не обмежувати): уповільнення швидкості утворення або нагромадження -амілоїдних фібрил; зменшення ступеню нагромаження амілоїду; інгібування, зменшення, або попередження утворення -амілоїдних фібрил; інгібування нейродегенерації або клітинної токсичності, індукованої -амілоїдом; інгібування запалення, індукованого -амілоїдом; посилення очищення амілоїду з мозку; або сприяння розщепленню амілоїдного білка перед його організацією у фібрили. Терапевтичні сполуки винаходу можуть бути ефективними для контролю нагромадження амілоїду або після їх потрапляння до мозку (після проникнення через гематоенцефалічний бар'єр), або з периферії. Якщо дія відбувається з периферії, сполука може змінювати баланс Α між мозком і плазмою, для того щоб сприяти виведенню Α з мозку. Вони можуть також підвищувати катаболізм Α нейронів і змінювати швидкість виведення з мозку. Підвищення швидкості виведення Α з мозку призвело б до зниження концентрації Α в мозку і цереброспінальній рідині (ЦСР) і, таким чином, сприяло б зменшенню нагромадження Α. Крім того, сполуки, що проникають у мозок, могли б контролювати нагромадження шляхом безпосереднього впливу на Α мозку, наприклад, утримуючи його в нефібрилярній формі, сприяючи його виведенню з мозку, або уповільнюючи процесинг АРР. Ці сполуки могли б також перешкоджати взаємодії Α мозку з поверхнею клітин і, відповідно, запобігати нейротоксичності, нейродегенерації або запаленню. Вони також можуть зменшувати Α утворення активізованими мікрогліальними клітинами. Сполуки можуть також підвищувати деградацію макрофагами або нейронами. В одному втіленні, використовується спосіб для лікування хвороби Альцгеймера (наприклад, 17 спорадичної, сімейної або ранньої форми АХ). Цей спосіб може також бути використаний профілактично або терапевтично, для того щоб лікувати клінічні випадки накопичення -амілоїду, такі як у осіб з синдромом Дауна і у пацієнтів з церебральною амілоїдною ангіопатією ("ЦАА") або спадковою церебральною геморагією. В іншому втіленні, цей спосіб використовується для лікування легких когнітивних порушень. Легке Когнітивне Порушення ("ЛКП") - це стан, що характеризується легким але помітним порушенням навичок мислення, які необов'язково пов'язані з наявністю деменції. Часто ЛКП, але необов'язково, передує хворобі Альцгеймера. Крім того, було встановлено, що аномальне накопичення АРР і -амілоїдного білка в м'язових волокнах призводить до патології спорадичної прогресуючої запальної міопатії (ПЗМ) (Askanas, et al., Proc. Natl. Acad. Sci. USA 93, 1314-1319 (1996); Askanas, et al., Current Opinion in Rheumatology 7, 486-496 (1995)). Відповідно, сполуки винаходу можуть бути використані профілактично або терапевтично для лікуванні розладів, при яких бетаамілоїдний білок відкладається в місцях не пов'язаних з нервовою системою, таких як лікування ПЗМ шляхом доставки сполук до м'язових волокон. Крім того, було показано, що Α пов'язаний з аномальними екстрацелюлярними нагромадженнями, відомими як друзи, що акумулюються уздовж базальної поверхні пігментованого епітелію сітківки у осіб зі старечими дегенеративними змінами жовтої плями сітківки (ДЗЖПС). ДЗЖПС є чинником, що викликає незворотну втрату зору у осіб похилого віку. Вважають, що нагромадження Α може бути важливою складовою локальних запальних процесів, що призводять до атрофії пігментованого епітелію сітківки, біогенезу друз і патогенезу ДЗЖПС (Johnson, et al., Proc. Natl. Acad. Sci. USA 99(18), 11830-5(2002)). Таким чином, цей винахід пов'язаний з використанням сполук Формул І, II, III, IV, V, VI, VII, чи інших сполук, описаних тут, для профілактики або лікування амілоїдогенних захворювань, включаючи, inter alia, хворобу Альцгеймера, церебральну амілоїдну ангіопатію, легкі когнітивні порушення, прогресуючу запальну міопатію, синдром Дауна, дегенеративні зміни жовтої плями сітківки, а також інші типи амілоїдозу типу ІАРР-пов'язаного амілоїдозу (напр., діабет), первинний (AL) амілоїдоз, вторинний (АА) амілоїдоз і гемодіалізний амілоїдоз, пов'язаний з наявністю 2-мiкpoглoбyлiнy. Амілоїдоз, пов'язаний з діабетом Типу II (ІАРР), амілоїдогенний білок ІАРР індукує токсичність клітин -острівців, якщо об'єднується в олігомерні форми або у фібрили. Відповідно, поява ІАРР фібрил у підшлунковій залозі пацієнтів, які мають діабет Типу II, призводить до втрати клітин -острівців (Лангерганса) і дисфункції органу, що призводить до інсулінемії. Первинний амілоїдоз (AL амілоїдоз), як правило, пов'язаний з дискразією плазми клітин і множинною мієломою. Він також може бути виявлений як ідіопатичне захворювання. 96115 18 Вторинний (АА) амілоїдоз, як правило, спостерігається при хронічних інфекціях (таких як туберкульоз) або хронічне запалення (таке як ревматоїдний артрит). Сімейна форма вторинного амілоїдозу спостерігається також у випадку сімейної середземноморської гарячки (ССГ). 2-мікроглобулярний (гемодіалізний) амілоїдоз виявляють у пацієнтів, що тривалий час перебувають на гемодіалізі. У пацієнтів, які тривалий час перебувають на гемодіалізі, утворюються 2мікроглобулярні фібрили в каналах зап'ястка і багатих на колаген тканинах кількох суглобів. Це викликає сильні болі, негнучкість суглобів і опухання. Ці нагромадження відбуваються через нездатність підтримувати низькі рівні 2Μ в плазмі пацієнтів, що перебувають на діалізі. Зростання в плазмі концентрацій 2Μ білка може індукувати структурні зміни і призвести до нагромадження модифікованого 2Μ у вигляді нерозчинних фібрил у суглобах. Докладний опис винаходу Даний винахід пов'язаний з використанням сполук Формул І, II, III, IV, V, VI, VII, або інших сполук, описаних тут, для лікування амілоїдогенних захворювань. Для зручності, нижче наведено визначення деяких термінів, на які тут зроблено посилання. Амілоїдогенні захворювання АА (Реактивний) Амілоїдоз Як правило, АА амілоїдоз є проявом цілої низки захворювань, що провокують гострофазову відповідь. Такі захворювання включають хронічні запальні розлади, хронічні локальні або системні мікробні інфекції або злоякісні новоутворення. Найбільш відома форма реактивного або вторинного (АА) амілоїдозу проявляється як наслідок тривалого запального стану. Наприклад, у пацієнтів з ревматоїдним артритом або сімейною середземноморською гарячкою (яка ε спадковим захворюванням) може розвиватись АА амілоїдоз. Терміни "АА амілоїдоз" і "вторинний (АА) амілоїдоз" використовуються тут поперемінно. АА фібрили, як правило, складаються з фрагментів, що мають молекулярну масу 8,000 дальтонів (АА пептид або білок), які утворюються шляхом протеолітичного процесингу амілоїдного А білка сироватки (ApoSAA), і циркуляції аполіпопротеїну, який головним чином синтезується в гепатоцитах у відповідь на такі цитокіни, як IL-1, IL-6 і TNF. Після секреції, ApoSAA комплексується з ліпопротеїнами високої щільності (ЛВЩ). Відкладання АА фібрил може бути розповсюджено в межах всього тіла, однак при цьому переважно це відбувається в паренхіматозних органах. Зазвичай, місцем нагромадження є нирки, крім того, печінка і селезінка також можуть бути уражені. Нагромадження також спостерігаються в серці, кишково-шлунковому тракті та у шкірі. Основні захворювання, які можуть призводити до розвитку АА амілоїдозу, включають, але не обмежені ними, запальні хвороби, такі як ревматоїдний артрит, хронічний артрит у дітей, анкілозуючий спондиліт, псоріаз, псоріатичну артропатію, синдром Рейтера, хворобу Стілла у дорослих, синдром Бехчета і хворобу Крона. Нагромадження АА амілоїду також утворюються внаслідок хронічних мік 19 96115 робних інфекцій, таких як проказа, туберкульоз, бронхоектаз, пролежні, хронічний пієлонефрит, остеомієліт і хвороба Уїппла. Певні злоякісні новоутворення також можуть призвести до відкладення АА амілоїдних фібрил. Ці новоутворення включають лімфому Ходжкінса, карциному нирки, карциноми кишківника, легені і урогенітального тракту, базально-клітинну епітеліому (базаліому) і лейкемію ворсистих клітин. Інші основні захворювання, що можуть бути пов'язані з АА амілоїдозом, хвороба Кастлемена і синдром Шнітцлера. AL Амілоїдози (Первинний Амілоїдоз) AL амілоїдні відкладення, як правило, пов'язані майже з будь-якою дискразією клітинної лінії Влімфоцитів, від злоякісних клітин плазми (множинна мієлома) до доброякісної моноклональної гамапатії. До того ж, наявність амілоїдних відкладень може бути первинним індикатором зазначеної дискразії. AL амілоїдоз також описано докладно в Current Drug Targets, 2004, 5159-171. Фібрили AL амілоїдних відкладень утворені легкими ланцюгами моноклонального імуноглобуліну або їх фрагментами. Більш конкретно, фрагменти походять з N-кінцевих ділянок легкого лан 20 цюга (каппа або лямбда) і містять весь або частину варіабельного його домену (VL). Накопичення, як правило, утворюються в мезенхімних тканинах, зумовлюючи периферичну або автономну невропатію, синдром зап'ясткового каналу, макроглоссію, рестриктивну кардіоміопатію, артропатію великих суглобів, імунні захворювання, мієломи, а також розлади невідомого походження. Однак, слід зазначити, що майже будь-яка тканина, особливо, вісцеральні органи, такі як нирки, печінка, селезінка і серце, можуть бути уражені. Спадкові системні амілоїдози Існує багато форм спадкових системних амілоїдозів. Незважаючи на те що вони спостерігаються доволі рідко, прояв симптомів у дорослих і шляхи їх успадкування (як правило, аутосомний домінантний) призводять до стійкості таких розладів у населення в цілому. Зазвичай, ці синдроми пов'язують з точковими мутаціями в білку-попереднику, що призводить до утворення варіанту амілоїдогенних пептидів або білків. В Таблиці 1 узагальнено дані про склад фібрил при типових формах таких розладів. Таблиця 1 Склад фібрил при типових Амілоїдогенних захворюваннях Фібрили пептиду/Білка Генетичний варіант ATTR білок з транстиретину і фрагме- Met30, багато іннтів ших Thr45, АІа60, ATTR білок з транстиретину і фрагмеSer84, Met111, нтів Del22 N-кінцевий фрагмент Аполіпопротеїну Arg26 А1 N-кінцевий фрагмент Аполіпопротеїну Arg26, Arg50, А1 Arg60, інші АароАІІ з Аполіпопротеїну All Лізоцим (Alys) Thr56, His67 Фрагмент альфа ланцюга фібриногеLeu554, Val 526 ну Фрагмент гельсоліну (Agel) Asn187, Tyr187 Фрагмент цистатину С (ACys) Glu68 -амілоїдний білок (Α), походить від попередника амілоїдного білка (АPP) -амілоїдний білок (Α), походить від попередника амілоїдного білка (АPP) -амілоїдний білок (Α) походить від попередника амілоїдного білка (АРР), напр., bPP 695 -амілоїдний білок (Α), походить від попередника амілоїдного білка (АPP) Gln693 ІІе717, Gly717 Phe717, Клінічний синдром Сімейна амілоїдна поліневропатія (САП), (головним чином, периферичні нерви) Переважає ураження серця без невропатії, сімейна амілоїдна поліневропатія, сенільний системний Сімейна амілоїдна поліневропатія (САП) (головним чином периферичні нерви) Остертаг-тип, позаневропатичний (переважають ураження вісцеральних органів) Сімейний амілоїдоз Остертаг-тип, позаневропатичний (Переважають ураження вісцеральних органів) Краніальна невропатія з решітчастою дистрофією рогівки Краніальна невропатія з решітчастою дистрофією рогівки Спадкова церебральна геморагія (церебральна амілоїдна ангіопатія) - Іспапанський тип Спадкова церебральна геморагія (церебральна амілоїдна ангіопатія) - Датський тип Сімейна хвороба Альцгеймера Хвороба Альцгеймера, Синдром Дауна, спадкова церебральна геморагія з амілоїдозом, Датський тип Сімейна деменція - можливо, хвороба АльцAsn670, Leu671 геймера Сімейна хвороба Крейтцфельдта-Якоба; синдsc Пріоновий білок (PrP, APrP ) похоLeul02, Vall67, ром Герстманна-Штройсллера-Шайнкера (спадить від попередника Ркр білка (51-91 Asnl78, Lys200 дкові спонгіозні енцефалопатії, пріонові хвороінсерт) би) Gin 618 21 96115 22 Продовження таблиці 1 АА походить від амілоїдного А білка сироватки (ApoSAA) АА походить від амілоїдного А білка сироватки (ApoSAA) Сімейна середземноморська гарячка, переважно ураження нирок (аутосомна рецесивна) Синдром Макла-Веллса, невропатія, глухота, кропив'янка, болі в кінцівках Кардіоміопатія з постійною асистолією передсердь Шкірні відкладення (бульозні, папульозні, пустулодермальні) Невідомо Невідомо АН амілоїдний білок, походить від важкого ланцюга імуноглобуліну (гама ATI I) ACal амілоїдний білок від (Про)кальцитонін (про)кальцитоніну AANF амілоїдний білок з передсердного натрійуретичного фактора Арго з пролактину Abri/ADan з АBrі пептиду Амілоїдоз, пов'язаний з мієломою Медулярні карциноми щитовидної залози Амілоїд, ізольований з передсердя Пролактиноми Британська і Данська форми сімейної деменції Дані запозичено з Tan SY, Pepys MB. Amyloidosis. Histopathology, 25(5), 403-414 (Nov 1994), WHO/IUIS Nomenclature Subcommittee, Nomenclature of Amyloid and Amyloidosis. Bulletin of the World Health Organisation 1993; 71:10508; and Merlini et al., Clin Chem Lab Med 2001; 39(11): 1065-75. Дані, представлені в Таблиці 1, є типовими, і не мають на меті обмежити область застосування винаходу. Наприклад, описано понад 40 окремих точкових мутацій в гені транстиретину, всі з них призводять до розвитку клінічно подібних форм сімейної амілоїдної поліневропатії. Загалом, будь-який спадковий амілоїдний розлад може також проявлятись спорадично, і як при спадковій, так і при спорадичній формах, хвороба проявляється з тими ж самими характерними особливостями стосовно амілоїду. Наприклад, більшість поширених форм вторинного АА-амілоїдозу трапляються спорадично, напр., як наслідок наявного запалення, і не пов'язані з сімейною середземноморською гарячкою. Таким чином, загальне обговорення, що стосується спадкових амілоїдних розладів, наведене нижче, може також бути застосоване щодо спорадичних амілоїдозів. Транстиретин (ТТР) являє собою білок з молекулярною масою 14 кілодальтонів, який також інколи називають преальбуміном. Він виробляється печінкою і судинним сплетенням, а його функції полягають у транспортуванні тиреоїдних гормонів і вітаміну А. Щонайменше, 50 варіантних форм білок, кожна з яких відрізняється заміною єдиної амінокислоти, відповідають за різноманітні форми сімейної амілоїдної поліневропатії. Наприклад, заміна проліну на лейцин в 55 положенні призводить до особливо прогресуючої форми невропатії; заміна метионіну на лейцин у 111 положенні призводить до серйозної кардіопатії у данських пацієнтів. Амілоїдні відкладення, ізольовані із серцевої тканини пацієнтів, що потерпають від системного амілоїдозу, підтвердили, що ці відкладення утворені гетерогенною сумішшю ТТР і його фрагментів, яка разом називається як АТТР, непроцесовані послідовності яких були охарактеризовані. Компоненти ATTR-фібрил можуть бути екстраговані з таких бляшок, а їх структура і послідовність визначаються відповідно до методик, загальновідомих з рівня техніки (напр., Gustavsson, Α., et al., Laboratory Invest. 73: 703-708,1995; Kametani, F., et al., Biochem. Biophys. Res. Commun. 125: 622628,1984; Pras, M., et al.., PNAS 80: 539-42, 1983). Особи, що мають точкові мутації в молекулі аполіпопротеїну А1 (напр., GlyArg26; TrpArg50; LeuArg60), виявляють форму амілоїдозу ("Остертаг-тип"), який характеризується нагромадженнями аполіпопротеїнового білка А1 або його фрагментів (АароА1). Ці пацієнти мають низькі рівні ліпопротеїну високої щільності (ЛВЩ), що проявляється у периферичній невропатії або ураженні нирок. Мутація в альфа ланцюзі ферменту лізоциму (напр., llеThr56 або AspHis57) є основою для розвитку іншої форми Остертаг-типу позаневропатичного спадкового амілоїдозу, що відомий у британських родинах. У даному випадку, нагромаджуються фібрили мутантного білка лізоциму (Alys), і у пацієнтів, як правило, проявляється порушення функції нирок. Цей білок, на відміну від більшості білків, що утворюють фібрили, описаних тут, як правило, присутні у повній (нефрагментованій) формі (Benson, M.D., et al.. CIBAFdn. Symp. 199:104-131, 1996). Легкі лацюги імуноглобуліну мають тенденцію до агрегації у різні структури, що відрізняються морфологічно, включаючи фібрилярні (напр., AL амілоїдоз і АН амілоїдоз), гранулярні (напр., хвороба нагромадження легкого ланцюга (LCDD), хвороба нагромадження важкого ланцюга (HCDD), і хвороба нагромадження легкого-важкого ланцюгів (LHCDD)), кристалічні (напр., набутий синдром Фанконі), і мікротубулярний (напр., кріоглобулінемія). AL і АН амілоїдози ідентифікуються завдяки утворенню нерозчинних фібрил легких або важких ланцюгів імуноглобуліну, відповідно, і/або їх фраг 23 ментів. У AL фібрил, лямбда () ланцюги, такі як VI ланцюги (6 ланцюги), утворюються в більшій концентрації, ніж каппа () ланцюги. Концентрація ІІІ ланцюгів також дещо підвищена. Merlini et al., CLIN CHEM LAB MED 39(11): 1065-75 (2001). Амілоїдоз важких ланцюгів (АН), як правило, ідентифікується завдяки появі агрегатів гама-ланцюгів амілоїдних білків IgGI підкласу. Eulitz et al., PROC NATL ACAD Sci USA 87:6542-46 (1990). Порівняння амілоїдогенних і неамілоїдогенних легких ланцюгів підтвердило, що перший із вищезгаданих може включати заміщення або заміни, які призводять до дестабілізації тривимірної конформації білка і викликають агрегацію. AL і LCDD відрізняються від інших амілоїдогенних захворювань завдяки їх відносно малочисельній сукупності моноклональних легких ланцюгів, які утворюються новоутвореннями антитілоутворюючими Вклітинами. AL-агрегати у типовому випадку є правильно організовані фібрили лямбда ланцюгів. LCDD скупчення - це відносно аморфні конгломерати як каппа, так і лямбда ланцюгів, причому переважають каппа ланцюги, в деяких випадках IV. Bellotti et al., journal OF STRUCTURAL BIOLOGY 13:280-89 (2000). Порівняння амілоїдогенних і неамілоїдогенних важких ланцюгів у пацієнтів, що мають АН амілоїдоз, підтвердило втрату і/або заміну компонентів. Eulitz et al., PROC NATL ACADSci US A 87:6542-46 (1990) (патогенний важкий ланцюг характеризується значно нижчою молекулярною масою, ніж неамілоїдогенні важкі ланцюги); і Solomon et al. AM.J.HEMAT45(2) 1716(1994) (амілоїдогенний важкий ланцюг характеризується як такий, що утворений лише VH-D частиною неамілоїдогенного важкого ланцюга). Відповідно, потенційні способи виявлення і моніторингу лікування суб'єктів, що мають або щодо яких існує ризик AL, LCDD, АН, тощо включають але не обмежені ними, імунологічний аналіз плазми або сечі щодо наявності або зниженого накопичення амілоїдогенних легких або важких ланцюгів, напр., амілоїду , амілоїду , амілоїду IV, амілоїду , а амілоїду 1. Амілоїдоз мозку Амілоїд, що найчастіше утворюється в мозку, утворений головним чином фібрилами Α пептиду, що призводить до деменції, пов'язаної із спорадичною (неспадковою) хворобою Альцгеймера. Дійсно, кількість спорадичних випадків хвороби Альцгеймера значно перевищує кількість випадків хвороби, що є спадковою. Однак, фібрили пептидів, які утворюють бляшки, дуже подібні в обох випадках. Амілоїдоз мозку включає такі хвороби, стани, патології, та інші аномалії структури або функції мозку, включаючи його компоненти, при яких основним хвороботворним чинником є амілоїд. Ділянкою мозку, яка уражена амілоїдогенним захворюванням, може бути строма, включаючи судинну сітку або паренхіму, включаючи функціональні та анатомічні ділянки, або власне нейрони. Суб'єкт необов'язково повинен був отримати визначений діагноз конкретно визначеного амілоїдогенного захворювання. Термін "амілоїдогенне захворювання" включає амілоїдоз мозку. 96115 24 -амілоїдний пептид ("Α") являє собою пептид, утворений 39-43 амінокислотами, що утворюється внаслідок протеолітичного розщеплення більшого білка, відомого як попередник бета амілоїдного білка ("ΑΡΡ"). Мутації ΑΡΡ призводять до розвитку сімейних форм хвороби Альцгеймера, синдрому Дауна, церебральної амілоїдної ангіопатії і старечої деменції, що характеризуються нагромадженням в мозку бляшок, утворених Α фібрилами та іншими компонентами, які описуються далі детально. Відомі мутації в АРР, пов'язані з хворобою Альцгеймера, трапляються близько до сайтів розщеплення - або -секретази, або в межах Α. Наприклад, положення 717 є проксимальним до сайту гама-секретазного розщеплення АРР в його процесингу до Α, а положення 670/671 є проксимальними до сайту -секретазного розщеплення. Мутації за будь-яким з цих залишків можуть призводити до хвороби Альцгеймера, переважно, обумовлюючи зростання кількості 42/43 амінокислотної форми Α, що походить від АРР. Сімейна форма хвороби Альцгеймера становить лише 10% від загальної кількості випадків. Більшість випадків захворювання на хворобу Альцгеймера є спорадичними, де АРР і Α не несуть жодних мутацій. Структура та послідовність Α пептидів різної довжини є загальновідомими в галузі. Такі пептиди можуть бути отримані відповідно до методик, відомих в галузі, або можуть бути екстраговані з мозку відповідно до відомих методик (напр., Glenner and Wong, Biochem. Biophys. Res. Comm. 129, 885-90 (1984); Glenner and Wong, Biochem. Biophys. Res. Comm. 122,1131-35 (1984)). Крім того, різні форми пептидів є комерційно доступними. АРР експресується і конститутивно катаболізується в більшості клітин. Основним катаболічним шляхом метаболізму, очевидно, є розщеплення АРР в межах Α послідовності за допомогою фермента, який умовно називається -секретаза, що призводить до вивільнення розчинного фрагменту ектодомена, відомого як APPs. Це розщеплення перешкоджає утворенню Α пептиду. На противагу цьому неамілоїдогенному шляху метаболізму, АРР може також розщеплюватись ферментами, відомими як - і -секретаза в Ν- і С-кінцевих ділянках Α, відповідно, що супроводжується вивільненням Α в екстрацелюлярний простір. До теперішнього часу, ВАСЕ було ідентифіковано як -секретазу (Yasser, et al., Science 286:735-741,1999), і пресеніліни було пов'язано з -секретазною активністю (De Strooper, et al., Nature 391, 387-90 (1998)). Αпептид, утворений 39-43 амінокислотами, є продуктом послідовного протеолітичного процесингу попередника амілоїдного білка (АРР) і секретазними ферментами. Незважаючи на те, що Α40 є превалюючою формою, 5-7% від загального Α існує у формі Α42 (Сарраі et al., Int. J. Biochem. Cell Biol. 31. 885-89(1999)). Довжина Α-пептиду разюче змінює його біохімічні/біофізичні властивості. Особливо, дві додаткові амінокислоти на С-кінцевій ділянці Α42 є надзвичайно гідрофобними, і, очевидно, підвищують здатність Α42 до агрегації. Наприклад, 25 Jarrett, et al. показали, що Α42 агрегується дуже швидко in vitro у порівнянні з Α40, що дозволяє зробити припущення, що довші форми Α можуть бути важливими патологічними білками, які беруть участь в початковій десимінації невритичних бляшок при хворобі Альцгеймера (Jarrett, et al., Biochemistry 32, 4693-97 (1993); Jarrett, et al., Ann. N. Y. Acad. Sci. 695,144-48 (1993)). Пізніше ця гіпотеза була підтверджена за допомогою нещодавнього аналізу вкладу специфічних форм Α у випадках спадкових сімейних форм хвороби Альцгеймера ('САХ"). Наприклад, "Лондонська" мутантна форма АРР (APPV717I) пов'язана з САХ, селективно підвищуючи утворення Α 42/43 форми у порівнянні з Α40 (Suzuki, et al., Science 264,1336-40 (1994)), тоді як "Шведська" мутантна форма АРР (APPK670N/M671L) підвищує рівні як Α40, так і Α42/43 (Citron, et al., Nature 360, 672674 (1992); Cai, et al., Science 259, 514-16, (1993)). Крім того, спостерігали, що пов'язані з САХ мутації в Пресенілін -1 ("ПС1") або Пресенілін -2 ('ПС2") генах призводять до селективного зростання вироблення Α42/43, а не Α40 (Borchelt, et al., Neuron 17,1005-13 (1996)). Це відкриття було підтверджено на трансгенних мишачих моделях, що експресують мутантні ПС, які виявляють селективне зростання в мозку Α42 (Borchelt, op cit.; Duff, et al., Neurodegeneration 5(4), 293-98 (1996)). Таким чином, основна гіпотеза, що стосується етіології хвороби Альцгеймера, полягає в тому, що зростання концентрації Α42 в мозку у зв'язку із підвищенням вироблення і вивільнення Α42 або зниження його виведення (деградація або очищення мозку) є основним чинником у розвитку патології захворювання. Сайти множинних мутацій або в Α, або в АРР гені були ідентифіковані і клінічно пов'язані або з деменцією, або з церебральною геморагією. Типові ЦАА розлади включають, але не обмежені ними, спадкову церебральну геморагію з амілоїдозом Ісландського типу (HCHWA-I); Датський варіант HCHWA (HCHWA-D; мутація в Α); Фламандську мутацію Α; арктичну мутація Α; італійську мутацію Α; Айова мутацію Α; сімейну британську деменцію; і сімейну датську деменцію. ЦАА може також бути спорадичною. Як тут використовується, терміни "-амілоїд", "амілоїд-", тощо стосуються амілоїдних -білків або пептидів, попередників амілоїдних -білків або пептидів, проміжних речовин і їх модифікацій або фрагментів, якщо щось інше не було обумовлено. Зокрема, "Α" стосується будь-якого пептиду, утвореного шляхом протеолітичного процесингу продукту гена АРР, особливо пептидів, що пов'язані з амілоїдними патологіями, включаючи Α139, Α1-40, Α1-41, Α1-42, і Α1-43. Для того щоб чітко з'ясувати номенклатуру, "Α1-42" можуть тут називатись як "Α(1-42)" або просто як "Α42" або "Α42" (це ж стосується будь-якого іншого амілоїдного пептиду, що тут обговорюється). Як тут використовується, терміни "-амілоїд", "амілоїд-" і "Α" є синонімами. 96115 26 Якщо щось інше не було обумовлено, термін "амілоїд" стосується амілоїдогенних білків, пептидів або їх фрагментів, які можуть бути розчинними (наприклад, мономерними або олігомерними) або нерозчинними (наприклад, мають фібрилярну структуру або утворюють амілоїдні бляшки). Див., напр., МР Lambert, et al., Proc. Nat'lAcad. Sci. USA 95,6448-53 (1998). "Амілоїдоз" або "амілоїдна хвороба" або "амілоїдогенна хвороба" стосується патологічного стану, що характеризується наявністю амілоїдних волокон. "Амілоїд" - це є загальний термін, що стосується групи різноманітних, але специфічних білкових нагромаджень (інтрацелюлярних або екстрацелюлярних), які спостерігаються при цілій низці захворювань. Незважаючи на різноманітну локалізацію, всі амілоїдні відкладення мають спільні морфологічні особливості, забарвлюються специфічними барвниками (наприклад, конго червоним), і мають характерний червонозелений двозаломний зовнішній вигляд у поляризованому світлі після забарвлювання. Вони також мають спільні ультраструктурні особливості, спільну дифракцію рентгенівських променів та інфрачервоні спектри. Гельсолін є кальційзв'язуючий білок, який зв'язується з фрагментами і філаментами актину. Мутації в положенні 187 (напр., AspAsn; AspTyr) білка призводять до форми спадкового системного амілоїдозу, що, як правило, виявляється у пацієнтів з Фінляндії, а також у осіб, які мають данське або японське походження. У вражених осіб фібрили утворюються з фрагментів гельсоліну (Agel), що, як правило, утворені 173-243 амінокислотами (карбокситермінальний фрагмент з молекулярною масою 68 кДа), і нагромаджуються у кровоносних судинах і базальних мембранах, що призводить до дистрофії рогівки і краніальної невропатії, яка прогресує до периферичної невропатії, дистрофічних змін шкіри і відкладень в інших органах (Kangas, Η., et al. Human Mol. Genet. 5(9): 1237-1243, 1996). Інші мутантні білки, такі як мутантний альфа ланцюг фібриногену (AfibA) і мутантний цистатин (Acys) також утворюють фібрили і викликають характерний спадковий розлад. AfibA фібрили утворюють відкладення, які обумовлюють позаневропатичний спадковий амілоїдоз, що супроводжується хворобою нирок; накопичення призводять до спадкової церебральної амілоїдної ангіопатії, що була виявлена в Ісландії (Isselbacher, Harrison's Principles of Internal Medicine, McGraw-Hill, San Francisco, 1995; Benson, et al.). Було показано, принаймні, в деяких випадках, що пацієнти з церебральною амілоїдною ангіопатією (ЦАА) несуть амілоїдні фібрили, які утворені немутантною формою циста тину С у поєднанні з амілоїдним бета білком (Nagai, Α., et al. Molec. Chem. Neuropathol. 33:63-78,1998). Наразі вважають, що деякі форми пріонових захворювань є спадковими, їх частка становить до 15% від всіх випадків, раніше вважали, що вони переважно мають інфекційне походження (Baldwin, et al., in Research Advances in Alzheimer's Disease and Related Disorders, John Wiley and Sons, New York, 1995). При спадковій і спорадичній формах пріонових розладів, у пацієнтів відкладаються 27 бляшки, утворені аномальними ізоформами норSc мального пріонового білка (PrP ). Sc Превалююча мутантна ізоформа, PrP , яка ще називається також AScr, відрізняється від нормального целюлярного білка своєю резистентністю до дії протеази, нерозчинністю після екстракції детергентами, нагромадженням у вторинних лізосомах, посттрансляційним синтезом і високим вмістом -складчастих аркушів (у структурі білка). Зчеплення генів було встановлено, щонайменше, для п'яти мутацій, що призводять до хвороби Крейтцфельдта-Якоба (ХКЯ); синдрому Герстманна-Штройсллера-Шайнкера (ГШШ) і фатальної сімейної дисомнії (ФСД) (Baldwin, supra). Методики екстрагування фібрилярних пептидів із фібрил скрапі, визначення послідовностей і отримання таких пептидів відомі з рівня техніки (напр., Beekes, M., et al. J. Gen. Virol. 76: 2567-76, 1995). Наприклад, одна з форм ГШШ була пов'язана з РrР мутацією в кодоні 102, тоді як теленцефальну ГШШ виділяють за мутацією у кодоні 117. Мутації у кодонах 198 і 217 призводять до такої форми ГШШ, при якій невритичні бляшки, характерні для хвороби Альцгеймера, містять РrР замість Α пептиду. Певні форми сімейної хвороби Крейтцфельдта-Якоба (ХКЯ) були пов'язані з мутаціями 200 і 210 кодонів; мутації 129 і 178 кодонів були виявлені як при ХКЯ, так і при фатальній сімейній дисомнії (ФСД) (Baldwin, supra). Церебральний Амілоїдоз Локальні накопичення амілоїду є звичайними в мозку, особливо у осіб літнього віку. Найбільш розповсюджений тип амілоїду в мозку утворений переважно фібрилами Α пептиду, що призводить до деменції або спорадичної (неспадкової) хвороби Альцгеймера. Найчастіше зустрічаються спорадичні, а не спадкові випадки церебрального амілоїдозу. Наприклад, частка випадків спорадичної хвороби Альцгеймера і спорадичної церебральної амілоїдної ангіопатії (ЦАА) значно перевищує частку сімейної АХ і ЦАА. До того ж, спорадичні і сімейні форми хвороби не можна відрізнити одна від одної (вони відрізняються лише за наявністю або відсутністю спадкової генетичної мутації); наприклад, клінічні симптоми і амілоїдні бляшки, що утворюються як при спорадичній, так і при сімейній хворобі Альцгеймера є дуже подібними, якщо не ідентичними. Церебральна амілоїдна ангіопатія (ЦАА) належить до специфічного нагромадження амілоїдних фібрил в стінках лептоменінгеальних і кортикальних артерій, артеріол і вен. Вона, як правило, пов'язана з хворобою Альцгеймера, синдромом Дауна і звичайним старінням, а також з цілою низкою сімейних захворювань, пов'язаних з раптовим нападом або деменцією (див. Frangione et al., Amyloid: J. Protein Folding Disord. 8, Suppl. 1,36-42 (2001)). ЦАА може зустрічатись спорадично або успадковуватись. Сенільний системний амілоїдоз Амілоїдні нагромадження, системні або локальні, збільшуються з віком. Наприклад, фібрили природного типу транстиретину (TTR), зазвичай, виявляють у серцевій тканині осіб похилого віку. Ці відкладення можуть бути асимптоматичними, клі 96115 28 нічно "мовчазними", або можуть призводити до ураження серця. Асимптоматичні фібрилярні фокальні відкладення можуть також зустрічатись в мозку (Α), крохмальних тільцях передміхурової залози (2 мікроглобулін), суглобах і сім'яних пухирцях. Гемодіалізний Амілоїдоз (DRA) Бляшки, утворені фібрилами 2-мікроглобуліну (2Μ), як правило, розвиваються у пацієнтів, що тривалий час перебувають на гемодіалізі або перитонеальному діалізі, 2-мікроглобулін являє собою поліпептид з молекулярною масою 11.8 кілодальтонів і являє собою легкий ланцюг антигенів класу І МНС, які є у всіх клітинах, що містять ядро. За нормальних умов, 2Μ, як правило, знаходиться в екстрацелюлярному просторі, за умови, якщо не порушена функція нирок, в цьому випадку 2Μ транспортується в тканини, де він полімеризується і утворює амілоїдні фібрили. Недостатність виведення, що має місце у випадку порушення функції нирок, призводить до відкладання у зап'ястковому каналі та інших місцях (переважно в тканинах суглобів, які багаті на колаген). На відміну від інших фібрилярних білків, молекули 2Μ не утворюються шляхом розщеплення довшого білка попередника, і, як правило, присутні у нефрагментованому вигляді у фібрилах (Benson, supra). Було показано, що затримка і акумулювання цього попередника амілоїду є основним процесом, що визначає патогенез гемодіалізного амілоїдозу (ГДА). ГДА характеризується периферичною остеоартропатією суглобів (наприклад, негнучкість суглобів, болі, набряки тощо). Ізоформи 2Μ, глікозильований 2Μ, або полімери 2Μ в тканині є найбільш амілоїдогенною формою (на противагу природному 2Μ). На відміну від інших типів амілоїдозу, 2Μ притаманний головним чином для кісток і суглобів. Накопичення амілоїду у вісцеральних органах спостерігаються рідко. Зрідка, ці накопичення можуть уражати кровоносні судини та інші анатомічно важливі місця. Незважаючи на оптимізацію способів діалізу для видалення 2Μ, більшість пацієнтів мають концентрацію плазматичного 2Μ, що надзвичайно перевищує нормальні рівні. Ці підвищені концентрації 2Μ, як правило, призводять до гемодіалізного амілоїдозу (ГДА) і ускладнень, які сприяють смертності. Острівцевий амілоїдний поліпептид і діабет Паліноз острівців (відкладення амілоїду) вперше було описано понад століття тому як наявність фібринозних білкових агрегатів в підшлунковій залозі пацієнтів, що потерпали від сильної гіперглікемії (Opie, EL, J. Exp. Med. 5:397428,1901). Наразі, острівцевий амілоїд, утворений головним чином острівцевим амілоїдним поліпептидом (ІАРР), або аміліном, є основним гістопатологічним маркером у понад 90% випадків діабету Типу II (названий також як неінсулінозалежний діабет, або NIDDM). Ці фібрилярні накопичення є наслідком агрегації амілоїдного поліпептиду в острівцевих клітинах (ІАРР) або аміліну, який є пептидом, утвореним 37 амінокислотами, що походить 29 від більшого пептиду-попередника, що називається pro-ІАРР. ІАРР секретується разом з інсуліном у відповідь на секретогенні -клітини. Ця патологічна декомпенсація не пов'язана з інсулінзалежним діабетом (Тип І) і є спільною особливістю для гетерогенних клінічних фенотипів, діагностованих як NIDDM (діабет Типу II). Поздовжні дослідження у котів і імуноцитохімічні дослідження у мавп показали, що прогресуюче зростання амілоїду острівцевих клітин пов'язано із різким зниженням чисельності -клітин, що секретують інсулін, і зростанням серйозності хвороби. Нещодавно, трансгенні дослідження ще раз підтвердили взаємозв'язок між утворенням ІАРРбляшок та апоптозом і дисфункцією -клітин, що свідчить про те, що нагромадження амілоїду є принциповим фактором у зростанні серйозності діабету Типу II. Було також показано, що ІАРР індукує токсичність клітин -острівців in vitro, що свідчить про те, що поява ІАРР фібрил у підшлунковій залозі хворих на діабет Типу II і Типу І (післяострівцева трансплантація) може призводити до втрати клітин острівців (Лангерганса) і дисфункції органу. У пацієнтів з діабетом Типу II, накопичення панкреотичного ІАРР призводить до утворення олігомерного ІАРР, що веде до нагромадження ІАРР-амілоїду у вигляді нерозчинних волокнистих відкладень, які в кінцевому результаті руйнують -клітини остівців Лангерганса, що виробляють інсулін, що призводить до виснаження і відмови -клітин (Westermark, P., Grimelius, L, Ada Path. Microbiol. Scand, sect. A. 81: 291-300, 1973; de Koning, EJP., et al., Diabetologia 36: 378-384,1993; and Lorenzo, Α., et al., Nature 368: 756-760,1994). Акумулювання ІАРР у вигляді волокнистих накопичень може також значною мірою впливати на співвідношення про-ІАРР до ІАРР, яке у нормі виявлено в плазмі, шляхом зростання цього співвідношення завдяки "перехопленню" ІАРР відкладеннями. Зменшення кількості -клітин може проявлятись у формі геперглікемії та інсулінемії. Втрата сукупності -клітин може призвести до необхідності застосування інсулінової терапії. Хвороби, що виникли через дисфункцію певного типу або типів клітин, можна лікувати шляхом трансплантації пацієнтові здорових клітин відповідного типу. Такий підхід застосовувався щодо пацієнтів, які потерпають від діабету Типу І. Часто клітини панкреатичних острівців від донора культивуються in vitro перед трансплантацією, що дає змогу їм відновитись після методики ізоляції або щоб знизити їхню імуногенність. Однак, у багатьох відношеннях трансплантація клітин цих острівців не є успішною через загибель трансплантованих клітин. Однією з причин такого незначного успіху є ІАРР, який конгломерується в токсичні олігомери. Токсичні ефекти можуть виникати через інтрацелюлярне і екстрацелюлярне нагромадження фібрил олігомерів. ІАРР-олігомери можуть утворювати фібрили і ставати токсичними для клітин in vitro. Крім того, ІАРР-фібрили, ймовірно, продовжують рости після трансплантації клітин і викликають загибель або дисфункцію клітин. Це може відбува 96115 30 тись навіть тоді, якщо клітини походять від здорового донора, а пацієнт, що отримав транплантат, не має хвороби, що характеризується наявністю фібрил. Наприклад, сполуки даного винаходу можуть також бути використані при підготовці тканин або клітин для трансплантації відповідно до способів, описаних в Міжнародній Заявці на Патент (РСТ) № WO 01/003680. Сполуки винаходу можуть також стабілізувати співвідношення концентрацій pro-ІАРР/ІАРР, proІнсулін/Інсулін і рівні С-пептидів. Крім того, як біологічні маркери ефективності, результати різних тестів, таких як проби секреції аргініну-інсуліну, проби на толерантність до глюкози, проби на толерантність і чутливість до інсуліну, можуть бути використані як маркери зменшення кількості клітин і/або акумулювання амілоїдних нагромаджень. Такі класи ліків можуть бути використані разом з іншими ліками, що спрямовані на резистентність до інсуліну, виробництво глюкози печінкою і секрецію інсуліну. Такі сполуки можуть попередити застосування інсулінової терапії шляхом збереження функції -клітин і можуть знайти застосовування для збереження трансплантатів острівців. Гормональні Амілоїдози Ендокринні органи можуть нести нагромадження амілоїду, особливо у осіб похилого віку. Гормонсекретуючі пухлини можуть також включати амілоїдні бляшки, що мають гормональне походження, фібрили яких утворені гормонами поліпептидної природи, такими як кальцитонін (медулярна карцинома щитовидної залози), і передсердний натрійуретичний пептид (локальний передсердний амілоїдоз). Послідовності і структури цих білків є загальновідомими в галузі. Амілоїдози, що мають змішане походження Існує ціла низка інших форм амілоїдогенних захворювань, що, зазвичай, проявляються як локалізовані відкладення амілоїду. Загалом, ці хвороби, можливо, є результатом локалізованого продукування амілоїду або відсутності катаболізму специфічних попередників фібрил, або схильності певної тканини (такої як суглобова) до нагромадження фібрил. Приклади таких ідіопатичних нагромаджень включають вузликовий AL амілоїд, шкірний амілоїд, ендокринний амілоїд, пухлинний амілоїд. Інші амілоїдогенні захворювання включають ті, що описані в Таблиці 1, такі як сімейна амілоїдна поліневропатія (FAP), старечий системний амілоїдоз, тендосиновіт, сімейний амілоїдоз, Остертаг-тип позаневропатичного амілоїдозу, краніальна невропатія, спадкова церебральна геморагія, сімейна деменція, хронічний діаліз, сімейна хвороба Крейтцфельдта-Якоба; синдром Герстманна-Штройсллера-Шайнкера, спадкові спонгіозні енцефалопатії, пріонові хвороби, сімейна середземноморська гарячка, синдром Макла-Веллса, нефропатія, глухота, кропив'янка, болі у кінцівках, кардіоміопатія, шкірні відкладення, множинна мієлома, доброякісна моноклональна гамопатія, макоглобулінемія, мієломний амілоїдоз, медулярні карциноми щитовидної залози, локальний передсердний амілоїдоз і діабет. Сполуки винаходу можуть бути застосовані терапевтично або профілактично, для того щоб 31 лікувати захворювання, пов'язане з утворенням амілоїдних фібрил, їх агрегацією і нагромадженням, незалежно від клінічних проявів. Сполуки винаходу можуть діяти, для того щоб покращувати протікання амілоїдогенного захворювання, завдяки будь-якому з наступних механізмів, наприклад, таких як (але не обмежені ними), уповільнення швидкості утворення або нагромадження амілоїдних фібрил; зменшення ступеню нагромаження амілоїду; інгібування, зменшення, або попередження утворення амілоїдних фібрил; інгібування запалення, індукованого амілоїдом; посилення виведення амілоїду, наприклад, з мозку; або захист клітин від токсичності, індукованої амілоїдом (олігомерним або фібрилярним). В одному втіленні сполуки винаходу можуть бути застосовані терапевтично або профілактично для лікування захворювань, пов'язаних з утворенням, агрегацією або нагромадженням -амілоїдних фібрил. Сполуки винаходу можуть діяти, для того щоб покращувати протікання захворювання, пов'язаного з утворенням -амілоїду завдяки будьякому з наступних механізмів (цей перелік має на меті проілюструвати, а не обмежувати): уповільнення швидкості утворення або нагромадження амілоїдних фібрил; зменшення ступеню нагромаження -амілоїду; інгібування, зменшення або попередження утворення -амілоїдних фібрил; інгібування нейродегенерації або клітинної токсичності, індукованої -амілоїдом; інгібування запалення, індукованого -амілоїдом; посилення очищення -амілоїду з мозку; або сприяння розщепленню -амілоїдного білка. Сполуки винаходу можуть бути ефективними для контролю нагромадження -амілоїду або після їх проходження в мозок (після проникнення через гематоенцефалічний бар'єр), або з периферії. Якщо дія відбувається з периферії, сполука може змінювати баланс Α між мозком і плазмою, для того щоб сприяти виведенню Α з мозку. Підвищення швидкості виведення Α з мозку призвело б до зниження концентрації Α в мозку і цереброспінальній рідині (ЦСР) і, таким чином, сприяло б зменшенню нагромадження Α. Крім того, сполуки, що проникають в мозок, могли б контролювати нагромадження шляхом безпосереднього впливу на Α мозку, наприклад, утримуючи його в нефібрилярій формі, сприяючи його виведенню з мозку. Ці сполуки можуть уповільнювати процесинг АРР, можуть підвищувати деградацію фібрил Α фібрил макрофагами або нейронами; або можуть зменшувати утворення Α активізованими мікрогліальними клітинами. Ці сполуки можуть також перешкоджати взаємодії Α мозку з поверхнею клітин і, відповідно, запобігати нейротоксичності, нейродегенерації або запаленню. В кращому втіленні, спосіб використовується для лікування хвороби Альцгеймера (наприклад, спорадичної або сімейної АХ). Спосіб може також бути використаний профілактично або терапевтично, для того щоб лікувати інші клінічні прояви відкладення амілоїду-, такі як синдром Дауна у осіб і пацієнтів з церебральною амілоїдною ангіопатією ("ЦАА"), спадковою церебральною гемора 96115 32 гією або початковою стадією хвороби Альцгеймера. В іншому втіленні цей спосіб використовується для лікування легких когнітивних порушень. Легке Когнітивне Порушення ("ЛКП") - це стан, що характеризується легким але помітним порушенням навичок мислення, які необов'язково пов'язані з наявністю деменції. Часто ЛКП, але необов'язково, передує хворобі Альцгеймера. Крім того, було встановлено, що аномальне накопичення АРР і -амілоїдного білка у м'язових волокнах призводить до патології спорадичної прогресуючої запальної міопатії (ПЗМ) (Askanas, et al., Proc. Natl. Acad. Sci. USA 93, 1314-1319 (1996); Askanas, et al., Current Opinion in Rheumatology 7, 486-496 (1995)). Відповідно, сполуки винаходу можуть бути використані профілактично або терапевтично для лікування розладів, при яких бетаамілоїдний білок аномально відкладається в місцях, не пов'язаних з нервовою системою, таких як лікування ПЗМ шляхом доставки сполук до м'язових волокон. Крім того, було показано, що Α, пов'язаний з аномальними екстрацелюлярними нагромадженнями, відомими як друзи, що акумулюються уздовж базальної поверхні пігментованого епітелію сітківки у осіб з віковими дегенеративними змінами жовтої плями сітківки (ДЗЖПС). ДЗЖПС є чинником, що викликає незворотну втрату зору у осіб похилого віку. Вважають, що нагромадження Α може бути важливою складовою локальних запальних процесів, які призводять до атрофії пігментованого епітелію сітківки, біогенезу друз і патогенезу ДЗЖПС (Johnson, et al., Proc. Natl. Acad. Sci. USA 99(18), 11830-5(2002)). В іншому втіленні, винахід також пов'язаний зі способом лікування або попередження амілоїдогенного захворювання у суб'єкта (переважно - людини), що полягає у введенні суб'єкту терапевтичної кількості сполуки відповідно до наступних формул або інших сполук, тут описаних, завдяки чому зменшується або інгібується утворення амілоїдних фібрил, нейродегенерація або клітинна токсичність. І іншому втіленні, винахід пов'язаний зі способом лікування або попередження амілоїдогенного захворювання у суб'єкта (переважно - людини), що полягає у введенні суб'єкту терапевтичної кількості сполуки відповідно до наступних формул або інших сполук, тут описаних, внаслідок чого відбувається покращення або стабілізація когнітивної функції або попереджується, уповільнюється або зупиняється подальше погіршення когнітивної функції у пацієнтів з амілоїдозом мозку, наприклад, хворобою Альцгеймера, синдромом Дауна або церебральною амілоїдною ангіопатією. Ці сполуки можуть також покращувати якість повсякденного життя цих пацієнтів. Терапевтичні сполуки винаходу можуть лікувати амілоїдоз, пов'язаний з діабетом Типу II, наприклад, стабілізуючи глікемію, попереджаючи або зменшуючи втрату кількості -клітин, зменшуючи або попереджаючи геперглікемію через втрату кількості -клітин, і через модуляцію (наприклад, підвищення або стабілізацію) вироблення інсуліну. 33 Сполуки винаходу можуть також стабілізувати співвідношення концентрацій pro-ІАРР/ІАРР. Терапевтичні сполуки винаходу можуть лікувати АА (вторинний) амілоїдоз і/або AL (первинний) амілоїдоз шляхом стабілізації функції нирок, зниження протеїнурії, підвищення виведення креатиніну (наприклад, принаймні на 50% або більше, або принаймні, на 100% або більше), викликаючи ремісію хронічної діареї або збільшення ваги (наприклад, на 10% або більше), або знижуючи рівень креатиніну в сироватці. Вміст вісцерального амілоїду, як було визначено, наприклад, за допомогою SAP сцинтиграфії, може також бути зменшений. Сполуки Винаходу Даний винахід пов'язаний, принаймні, частково, з використанням певних хімічних сполук (або їх фармацевтичних композицій) для профілактики або лікування амілоїдогенних захворювань, включаючи, inter alia, хворобу Альцгеймера, церебральну амілоїдну ангіопатію, прогресуючу запальну міопатію, синдром Дауна, амілоїдоз, пов'язаний з діабетом, гемодіалізний амілоїдоз (2Μ), первинний амілоїдоз (напр., або ланцюговий), сімейну амілоїдну поліневропатію (САП), сенільний системний амілоїдоз, сімейний амілоїдоз, позаневропатичний амілоїдоз Остертаг-типу, краніальну невропатію, спадкову церебральну геморагію, сімейну деменцію, хронічний діаліз, сімейну хворобу Крейтцфельдта-Якоба; синдром ГерстманнаШтройсллера-Шайнкера, спадкові спонгіозні енцефалопатії, пріонові хвороби, сімейну середземноморську гарячку, синдром Макла-Веллса, нефропатію, глухоту, кропив'янку, болі у кінцівках, кардіоміопатію, шкірні відкладення, множинну мієлому, доброякісну моноклональну гамопатію, макоглобулінемію, мієломний амілоїдоз, медулярні карциноми щитовидної залози, локальний передсердний амілоїдоз. Хімічні структури зображені тут відповідно до традиційних стандартів, загальноприйнятних у галузі. Таким чином, у випадку, якщо зображується атом, такий як атом вуглецю, це означає, що є вільна валентність, крім того, робиться припущення, що вільна валентність насичується атомом водню, навіть якщо цей атом водню не є обов'язково зображений. Структури деяких сполук цьогу винаходу включають стереогенні атоми вуглецю. Слід мати на увазі, що ізомери, які виникають внаслідок такої асиметрії (наприклад, всі енантіомери і діастереомери), включені в межі цього винаходу, якщо не обумовлено щось інше. Тобто, якщо не обумовлено щось інше, центр будь-якого хірального атома вуглецю може перебувати або в (R)-, або в (S)-стереохімічному положенні. Такі ізомери можуть бути отримані в істотно чистому вигляді шляхом застосування класичних методик розділення і шляхом стереохімічно контрольованого синтезу. До того ж, алкени можуть включати або Е- або Zгеометрію, де це прийнятно. Крім того, сполуки даного винаходу можуть існувати у нерозчинних і розчинних формах з прийнятними розчинниками, такими як вода, THF, етанол тощо. Загалом, розчинні форми розглядаються як еквівалентні нерозчинним формам для досягнення мети даного винаходу. 96115 34 "Мала молекула" стосується сполуки, яка власне не є продуктом транскрипції або трансляції гена (наприклад, білок, РНК або ДНК) і, переважно, має низьку молекулярну вагу, напр., менше, ніж приблизно 2500 амо (атомна маса одиниці). Загалом, термін "нуклеофіл" є загальноприйнятим і означає хімічну групу, що має реактивну пару електронів, які реагують зі сполукою, шляхом заміщення відщеплюваної групи (як правило, іншого нуклеофілу), такого як те, що відбувається в хімії аліфатичних сполук як одномолекулярна (відоме як "SN1") або двохмолекулярна CSN2") реакції. Приклади нуклеофілів включають незаряджені сполуки, такі як аміни, меркаптани і спирти, і заряджені групи, такі як алкоксиди, тіоляти, карбаніони, і низку органічних і неорганічних аніонів. Ілюстративні аніонні нуклеофіли включають, inter alia, прості аніони, такі як азид, ціанід, тіоціанат, ацетат, формат або хлорформат і дисульфіт. Металоорганічні реагенти, такі як органокупрати, цинкорганічні, літійорганічні, реактиви Гріньяра, енолати, і ацетиленіди, можуть бути за відповідних умов реакції прийнятними нуклеофілами. Аналогічним чином, "електрофіл" означає атом, молекулу або іон, здатний прийняти електронну пару, особливо пару електронів від нуклеофілу, що типово відбувається протягом реакції електрофільного заміщення. В реакції електрофільного заміщення, електрофіл зв'язується з речовиною з виштовхуванням іншого електрофіла, наприклад, заміщенням протона іншим електрофілом, таким як іон нітронію на ароматичних речовинах (наприклад, бензол). Електрофіли включають циклічні сполуки, такі як епоксиди, азиридини, епісульфіди, циклічні сульфати, карбонати, лактони, і лактами; а нециклічні електрофіли включають сульфати, сульфонати (наприклад, тосилати), хлориди, броміди і йодиди. Загалом, електрофілом може бути насичений атом вуглецю (наприклад, метиленова група), зв'язаний з відщеплюваною групою; однак, електрофіл можуть бути також ненасиченою групою, такою як альдегід, кетон, естер, або спряжений (,-ненасичений) їх аналог, що при реакції з нуклеофілом утворює аддукт. Термін "відщеплювана група", як правило, стосується групи, яка легко витісняється і заміщується нуклеофілом (наприклад, аміном, тіолом, спиртом або ціанідом). Такі відщеплювані групи добре відомі і включають карбоксилати, Nгідроксисукцинімід ("NHS"), Nгідроксибензотриазол, галоген (фтор, хлор, бром, або йод), алкоксиди, і тіоалкоксиди. Низка сірковмісних відщеплюваних груп звичайно використовується в синтетичній хімії, включаючи алкансульфонілоксигрупи (наприклад, С1-С4 алкани, такі як метан сульфонілокси, етан сульфонілокси, пропан сульфонілокси, і бутан сульфонілокси групи) і галогензаміщені аналоги (наприклад, галогено(С1-С4 алкани) сульфонілокси групи, такі як трифторметан сульфонілокси (тобто, трифлат), 2,2,2трихлоретан сульфонілокси, 3,3,3-трибромпропан сульфонілокси, і 4,4,4-трифторбутан сульфонілокси групи), а також арилсульфонілокси групи (наприклад, С6-С10 арил, необов'язково заміщений від 35 1 до 3 С1-С4 алкільними групами, такими як бензол сульфонілокси, -нафтилсульфонілокси, нафтилсульфонілокси, -толуєнсульфонілокси (тобто, тосилати), 4-трет-бутилбензол сульфонілокси, мезитилен сульфонілокси, і 6-етил-нафтилсульфонілокси групи). "Активовані естери" можуть бути представлені формулою -COL, де L являє собою відщеплювану групу, типові приклади яких включають Nгідроксисульфосукцинімідил і Νгідроксисукцинімідил групи; арилокси групи, заміщені елекронакцепторними групами (наприклад, рнітро, пентафлуоро, пентахлоро, р-ціано, або ртрифлуорометил); і карбонові кислоти, активовані карбодиімідом, що дає ангідрид або суміш ангідa a b a b ридів, напр., -OCOR або -OCNR NHR , де R і R є незалежно С1-С6 алкіл, С5-С8 алкіл (напр., циклогексил), С1-С6 перфторалкіл, або С1-С6 алкокси групи. Активований естер може утворюватись in situ або може бути реагентом, що ізолюється. Сульфосукцинімідил естери, пентафлуоротіофенол естери, і сульфотетрафлуорофенол є кращими активованими естерами. Однак, естерна відщеплювана група може бути, наприклад, заміщеним або незаміщеним С1-С6 алкілом (таким як метил, етил, пропіл, ізопропіл, бутил, ізобутил, вторбутил, трет-бутил, пентил, або гексил), або заміщеною або незаміщеною С6-С14 арильною або гетероциклічною групою, такою як 2-фторетил, 2хлоретил, 2-брометил, 2,2-диброметил, 2,2,2трихлоретил, 3-фторпропіл, 4-хлорбутил, метоксиметил, 1,1-диметил-1-метоксиметил, етоксиметил, N-пропоксиметил, ізопропоксиметил, Nбутоксиметил, трет-бутоксиметил, 1-етоксиетил, 1метил-1-метоксиетил, 1-(ізопропокси)етил, 3метоксипропіл-4-метоксибутил, фторметоксиметил, 2,2,2-трихлоретоксиметил, біс(2хлоретокси)метил, 3-фторпропоксиметил, 4хлорбутоксиетил, дибромметоксиетил, 2хлоретоксипропіл, фторметоксибутил, 2метоксиетоксиметил, етоксиметоксиетил, метоксиетоксипропіл, метоксиетоксибутил, бензил, фенетил, 3-фенілпропіл, 4-фенілбутил, анафтилметил, β-нафтилметил, дифенілметил, трифенілметил, -нафтилдифеїлметил, 9антрилметил, 4-метилбензил, 2,4,6триметилбензил, 3,4,5-триметилбензил, 4метоксибензил, 4-метоксифенілдифенілметил, 2нітробензил, 4-нітробензил, 4-хлорбензил, 4бромбензил, 4-ціанобензил, 4ціанобензилдифенілметил, або біс(2нітрофеніл)метил групи. Термін "електроноакцепторна група" є загальноприйнятим в галузі і описує здатність замісника відтягувати валентні електрони (напр., піелектрони) від сусідніх атомів, напр., замісник є більш електронегативний, ніж сусідні атоми, або він притягує електрони до себе сильніше, ніж атом водню, якби він перебував у цьому положенні. Значення константи Гаммета сігма () є прийнятою мірою здатності груп віддавати електрони і відтягувати, особливо значення сігма пара (ρ). Див., напр., "Advanced Organic Chemistry" by J. th March, 5 Ed., John Wiley & Sons, Inc., New York, pp.368-75 (2001). Значення константи Гаммета є, 96115 36 як правило, негативним для груп, що віддають електрони (р=-0.66 для NH2), і позитивним для електроноакцепторних груп (p=0.78 для нітрогрупи), p є відображенням пара заміщення. Типові електронакцепторні групи включають нітро, ацил (кетон), форміл (альдегід), сульфоніл, трифлуорометил, галоген (напр., хлор і фтор), і ціано групи, серед інших. Навпаки, "електронодонорна група" означає замісник, який віддає електрони сильніше, ніж водень, якби він займав те ж саме положення в молекулі. Приклади включають аміно (включаючи алкіламіно і диалкіламіно), арил, алкокси (включаючи аралкокси), арилокси, меркапто і алкілтіо, і гідроксильні групи, серед інших. Як тут використовується, "алкільні" групи включають насичені вуглеводні, що мають один або більше атомів вуглецю, включаючи алкільні групи з прямими ланцюгами (наприклад, метил, етил, пропіл, бутил, пентил, гексил, гептил, октил, ноніл, децил, тощо), циклічні алкільні групи (або "циклоалкільні" або "аліциклічні" або "карбоциклічні" групи) (наприклад, циклопропіл, циклопентил, циклогексил, циклогептил, циклооктил, тощо), алкільні групи з розгалуженими ланцюгами (ізопропіл, трет-бутил, втор-бутил, ізобутил тощо), і алкілзаміщені алкільні групи (наприклад, алкілзаміщені циклоалкільні групи і циклоалкілзаміщені алкільні групи). Термін "аліфатична група" включає органічні сполуки, що характеризуються прямими або розгалуженими ланцюгами, і, як правило, мають від 1 до 22 атомів вуглецю. В складних структурах, ланцюги можуть бути розгалужені, з'єднані містками або зшиті. Аліфатичні групи включають алкільні групи, алкенільні групи і алкінільні групи. В деяких втіленнях, алкільні групи з прямими або розгалуженими ланцюгами можуть мати 30 або менше атомів вуглецю в їхньому скелеті, наприклад, С1-С30 для прямих ланцюгів або С3-С30 для розгалужених ланцюгів. В деяких втіленнях, алкільні групи з прямим або розгалуженим ланцюгом можуть мати 20 або менше атомів вуглецю в їхньому скелеті, наприклад, С1-С20 для прямого ланцюга або С3-С20 для розгалуженого ланцюга, і, найкраще, 18 або менше. Таким же чином, кращі циклоалкільні групи мають від 4-10 атомів вуглецю в їхній кільцевій структурі, і ще краще, мають 4-7 атомів вуглецю в їхній кільцевій структурі. Термін "нижчі алкіли" стосується алкільних груп, що мають від 1 до 6 атомів вуглецю в ланцюзі, циклоалкільних груп, що мають від 3 до 6 атомів вуглецю в кільцевій структурі. Якщо число атомів вуглецю не обумовлено у інший спосіб, "нижчий" як в терміні "нижчий аліфатичний", "нижчий алкіл", "нижчий алкеніл", тощо, як тут використовується, означає, що складова частина молекули має, щонайменше, один і менше, ніж, приблизно, 8 атомів вуглецю. В деяких втіленнях, нижчі алкільні групи з прямими або розгалуженими ланцюгами мають 6 або менше атомів вуглецю в їхньому скелеті (наприклад, С1-С6 для прямого ланцюга, С3-С6 для розгалуженого ланцюга), а краще 4 або менше. Аналогічно, кращі циклоалкільні групи мають від 3-8 атомів вуглецю в кільцевій структурі, а ще краще мають 5 або 6 37 атомів вуглецю в кільцевій структурі. Термін "С1С6" як в "С1-С6 алкіл" означає алкільні групи, що містять від 1 до 6 атомів вуглецю. Крім того, якщо не було обумовлено щось інше, термін алкіл включає як "незаміщені алкіли", так і "заміщені алкіли", останні із вищезгаданих стосуються алкільних груп, що мають замісники, які заміщують один або більше атомів водню на одному або більше атомах вуглецю вуглеводного скелету. Такі замісники можуть включати, наприклад, алкеніл, алкініл, галогено, гідроксил, алкілкарбонілокси, арилкарбонілокси, алкоксикарбонілокси, арилокси, арилоксикарбонілокси, карбоксилат, алкілкарбоніл, арилкарбоніл, алкоксикарбоніл, амінокарбоніл, алкіламінокарбоніл, диалкіламінокарбоніл, алкілтіокарбоніл, алкоксил, фосфат, фосфонато, фосфінато, ціано, аміно (включаючи алкіламіно, диалкіламіно, ариламіно, диариламіно, і алкілариламіно), ациламіно (включаючи алкілкарбоніламіно, арилкарбоніламіно, карбамоїл і уреїдо), іміно, сульфгідрил, алкілтіо, арилтіо, тіокарбоксилат, сульфати, алкілсульфініл, сульфонато, сульфамоїл, сульфонамідо, нітро, трифторметил, ціано, азидо, гетероциклічні, алкіларильні, або ароматичні (включаючи гетероароматичні) групи. "Арилалкільна" група являє собою алкільну групу, заміщену арильною групою (наприклад, фенілметил (тобто, бензил)). "Алкіларильна" група являє собою арильну групу, заміщену алкільною групою (наприклад, р-метилфеніл (тобто, р-толіл)). Термін "n-алкіл" означає незаміщену алкільну групу з прямим ланцюгом (тобто, нерозгалужену). "Алкіленова" група являє собою двохвалентний аналог відповідної алкільної групи. Терміни "алкеніл" і "алкініл" стосуються ненасичених аліфатичних груп, аналогічних алкілам, однак які включають, щонайменше, один подвійний або потрійний вуглець-вуглецевий зв'язок, відповідно. Прийнятні алкенільні і алкінільні групи включають групи, що мають від 2 до, приблизно, 12 атомів вуглецю, краще від 2 до, приблизно, 6 атомів вуглецю. Термін "ароматична група" або "арильна група" включає ненасичені і ароматичні циклічні вуглеводні, а також ненасичені і ароматичні гетероциклічні сполуки, що мають одне або більше кілець. Арильні групи можуть також бути конденсовані або з'єднані містками з аліциклічними або гетероциклічними кільцями, які не є ароматичними, утворюючи поліциклічні сполуки (наприклад, тетралін). "Ариленова" група являє собою двохвалентний аналог арильної групи. Арильні групи можуть також бути сконденсовані або з'єднані містками з аліциклічними або гетероциклічними кільцями, які не є ароматичними, утворюючи поліциклічні сполуки (наприклад, тетралін). Термін "гетероциклічна група" включає закриті кільцеві структури, аналогічні карбоциклічним групам, в яких один або більше атомів вуглецю в кільці є іншим елементом, ніж вуглець, наприклад, азот, сірка або кисень. Гетероциклічні групи можуть бути насичені або ненасичені. Крім того, гетероциклічні групи (такі як піроліл, піридил, ізохіноліл, хіноліл, піриніл і фурил) можуть мати ароматичний характер, у цьому випадку вони мо 96115 38 жуть називатись як "гетероарильні" або "гетероароматичні" групи. Якщо не обумовлено щось інше, арильні і гетероциклічні (включаючи гетероарильні) групи можуть також бути заміщені в одному або більше конститутивних атомах. Приклади гетероароматичних і гетероциклічних груп можуть мати від 1 до 3 окремих або конденсованих кілець з від 3 до, приблизно, 8 членами на кільці і з одним або більш гетероатомами Ν, Ο або S. Загалом, термін "гетероатом" включає атоми будь-якого елемента, іншого, ніж вуглець або водень, кращі приклади яких включають азот, кисень, сірку і фосфор. Гетероциклічні групи можуть бути насиченими або ненасиченими, або ароматичними. Приклади гетероциклічних сполук включають, але не обмежені ними, акридиніл; азоциніл; бензімідазоліл; бензофураніл; бензотіофураніл; бензотіофеніл; бензоксазоліл; бензтіазоліл; бензтриазоліл; бензтетразоліл; бензізоксазоліл; бензізотіазоліл; бензімідазоліл; карбазоліл; 4аНкарбазоліл; карболініл; хроманіл; хроменіл; циннолініл; декагідрохінолініл; 2Н,6Н-1,5,2-дитіазиніл; дигідрофуро[2,3-b]тетрагідрофуран; фураніл; фуразаніл; імідазолідиніл; імідазолініл; імідазоліл; 1Н-індазоліл; індоленіл; індолініл; індолізиніл; індоліл; 3H-індоліл; ізобензофураніл; ізохроманіл; ізоіндазоліл; ізоіндолініл; ізоіндоліл; ізохінолініл; ізотіазоліл; ізоксазоліл; метилендіоксифеніл; морфолініл; нафтиридиніл; октагідроізохінолініл; оксадіазоліл; 1,2,3-оксадіазоліл; 1,2,4-оксадіазоліл; 1,2,5-оксадіазоліл; 1,3,4-оксадіазоліл; оксазолідиніл; оксазоліл; оксазолідиніл; піримідиніл; фенантридиніл; фенантролініл; феназиніл; фенотіазиніл; феноксантиїніл; феноксазиніл; фталазиніл; піперазиніл; піперидиніл; піперидоніл; 4-піперидоніл; піпероніл; птеридиніл; пуриніл; піраніл; піразиніл; піразолідиніл; піразолініл; піразоліл; піридазиніл; піридооксазол; піридоімідазол; піридотіазол; піридиніл; піридил; піримідиніл; піролідиніл; піролініл; 2Н-піроліл; піроліл; хіназолініл; хінолініл; 4Нхінолізиніл; хіноксалініл; хінуклідиніл; тетрагідрофураніл; тетрагідроізохінолініл; тетрагідрохінолініл; тетразоліл; 6Н-1,2,5-тіадіазиніл; 1,2,3тіадіазоліл; 1,2,4-тіадіазоліл; 1,2,5-тіадіазоліл; 1,3,4-тіадіазоліл; тіантреніл; тіазоліл; тієніл; тієнотіазоліл; тієнооксазоліл; тієноімідазоліл; тіофеніл; триазиніл; 1,2,3-триазоліл; 1,2,4-триазоліл; 1,2,5триазоліл; 1,3,4-триазоліл; і ксантеніл. Кращі гетероциклічні сполуки включають, але не обмежені ними, піридиніл; фураніл; тієніл; піроліл; піразоліл; піролідиніл; імідазоліл; індоліл; бензімідазоліл; 1Ніндізоліл; оксазолідиніл; бензотриазоліл; бензізоксазоліл; оксіндоліл; бензоксазолініл; і ізатіноїл групи. Також включено сполуки, що мають конденсовані кільцеві і спіросполуки, наприклад, наведені вище гетероциклічні сполуки. Звичайна вуглеводнева арильна група - це фенільна група, яка має одне кільце. Двокільцеві вуглеводневі арильні групи включають нафтилову, інденілову, бензоциклооктенілову, бензоциклогептенілову, пенталенілову і азуленілову групи, а також частково їх гідрогенізовані аналоги, такі як інданіл і тетрагідронафтил. Типові трикільцеві вуглеводневі арильні групи включають ацефтилені 39 лову, флуоренілову, феналенілову, фенантренілову і антраценілову групи. Арильні групи також включають гетеромоноциклічні арильні групи, тобто, однокільцеві гетероарильні групи, такі як тієніл, фурил, піраніл, піроліл, імідазоліл, піразоліл, піридиніл, піразиніл, піримідиніл, і піридазиніл групи; і оксигенізовані їх аналоги, такі як піридоніл, оксазолоніл, піразолоніл, ізоксазолоніл і тіазолоніл групи. Відповідні гідрогенізовані (тобто, неароматичні) гетеромоноциклічні групи включають піролідиніл, піролініл, імідазолідиніл, імідазолініл, піразолідиніл, піразолініл, піперидил і піперидино, піперазиніл і морфоліно і морфолініл групи. Арильні групи також включають конденсовані двохкільцеві гетероарили, такі як індоліл, ізоіндоліл, індолізиніл, індизоліл, хінолініл, ізохінолініл, фталазиніл, хіноксалініл, хіназолініл, циннолініл, хроменіл, ізохроменіл, бензотієніл, бензімідазоліл, бензотіазоліл, пуриніл, хінолізиніл, ізохінолоніл, хінолоніл, нафтиридиніл і птеридиніл групи, а також частково гідрогенізовані аналоги, такі як хроманіл, ізохроманіл, індолініл, ізоіндолініл, і тетрагідроіндоліл групи. Арильні групи також включають конденсовані трикільцеві групи, такі як феноксантиніїлову, карбазолілову, фенантридинілову, акридинілову, перимідинілову, фенантролінілову, феназинілову, фенотіазинілову, феноксазинілову і дибензофуранілову групи. Деякі типові арильні групи включають заміщені або незаміщені 5- і 6-членні однокільцеві групи. В іншому аспекті, кожна Аr група може бути відібрана з групи, що складається із заміщених або незаміщених феніл, піроліл, фурил, тієніл, тіазоліл, ізотіаозоліл, імідазоліл, триазоліл, тетразоліл, піразоліл, оксазолілових, ізооксазоліл, піридиніл, піразиніл, піридазиніл і піримідиніл груп. Наступні приклади включають заміщені незаміщені феніл, 1-нафтил, 2-нафтил, дифеніл, 1-піроліл, 2-піроліл, 3-піроліл, 3-піразоліл, 2-імідазоліл, 4-імідазоліл, піразиніл, 2-оксазоліл, 4-оксазоліл, 5-оксазоліл, 3ізоксазоліл, 4-ізоксазоліл, 5-ізоксазоліл, 2-тіазоліл, 4-тіазоліл, 5-тіазоліл, 2-фурил, 3-фурил, 2-тієніл, 3-тієніл, 2-піридил, 3-піридил, 4-піридил, 2піримідил, 4-піримідил, 5-бензотіазоліл, пуриніл, 2бензімідазоліл, 5-індоліл, 1-ізохіноліл, 5-ізохіноліл, 2-хіноксалініл, 5-хіноксалініл, 3-хіноліл, і 6-хіноліл групи. Термін "амін" або "аміно", як тут використовується, стосується незаміщених або заміщених a b a b сполук Формул -NR R , в яких R і R кожен є незалежно водень, алкіл, арил, або гетероцикліл, a b або R і R , взяті разом з атомом азоту, до якого вони приєднані, утворюють циклічну сполуку, що має від 3 до 8 атомів у кільці. Таким чином, термін аміно включає циклічні аміносполуки, такі як піперидиніл або піролідиніл групи, якщо не обумовлено щось інше. Таким чином, термін "алкіламіно", як тут використовується, означає алкільну групу, що має аміногрупу, приєднану до неї. Прийнятні алкіламіно групи включають групи, що мають від 1 до, приблизно, 12 атомів вуглецю, переважно, від 1 до, приблизно, 6 атомів вуглецю. Термін аміно включає сполуки або складові частини молекули, в яких атом азоту ковалентно зв'язаний з, щонайме 96115 40 нше, одним атомом вуглецю або гетероатомом. Термін "диалкіламіно" включає групи, в яких атом азоту зв'язаний, щонайменше, з двома алкільними групами. Термін "ариламіно" і "диариламіно" включає групи, де азот зв'язаний, щонайменше, з однією або двома арильними групами, відповідно. Термін "алкілариламіно" стосується аміногрупи, яка зв'язана, щонайменше, з однією алкільною групою і, щонайменше, однією арильною групою. Термін "алкаміноалкіл" стосується алкільної, алкенільної або алкінільної груп, заміщених алкіламіно групою. Термін "амід" або "амінокарбоніл" включає сполуки або складові частини молекули, які містять атом азоту, який зв'язаний з вуглецем карбонільної або тіокарбонільної групи. Термін "алкілтіо" стосується алкільної групи, яка має сульфогідрильну групу, приєднану до неї. Прийнятні алкілтіогрупи включають групи, що мають від 1 до, приблизно, 12 атомів вуглецю, переважно, від 1 до, приблизно, 6 атомів вуглецю. Термін "алкілкарбоксил", як тут використовується, означає алкільну групу, що має карбоксильну групу, приєднану до неї. Термін "алкокси", як тут використовується, означає алкільну групу, що має атом кисню, прикріплений до неї. Репрезентативні алкокси групи включають групи, що мають від 1 до, приблизно, 12 атомів вуглецю, переважно, від 1 до, приблизно, 6 атомів вуглецю, наприклад, метокси, етокси, пропокси, трет-бутокси тощо. Приклади алкокси груп включають метокси, етокси, ізопропілокси, пропокси, бутокси і пентокси групи. Алкокси групи можуть бути заміщені групами, такими як алкеніл, алкініл, галоген, гідроксил, алкілкарбонілокси, арилкарбонілокси, алкоксикарбонілокси, арилоксикарбонілокси, карбоксилат, алкілкарбоніл, арилкарбоніл, алкоксикарбоніл, амінокарбоніл, алкіламінокарбоніл, диалкіламінокарбоніл, алкілтіокарбоніл, алкоксил, фосфат, фосфонато, фосфінато, ціано, аміно (включаючи алкіл аміно, диалкіламіно, ариламіно, диариламіно, і алкілариламіно), ациламіно (включаючи алкілкарбоніламіно, арилкарбоніламіно, карбамоїл і уреїдо), іміно, сульфгідрил, алкілтіо, арилтіо, тіокарбоксилат, сульфати, алкілсульфініл, сульфонато, сульфамоїл, сульфонамідо, нітро, трифлуорометил, ціано, азидо, гетероцикліл, алкіларил, або ароматичні чи гетероароматичні складові частини молекули. Приклади галогензаміщених алкоксигруп включають, але не обмежені ними, флуорометокси, дифлуорометокси, трифлуорометокси, хлорометокси, дихлорметокси, трихлорметокси, тощо, а також пергалогенізовані алкілокси групи. Термін "ациламіно" включає складові частини молекули, в яких аміногрупа зв'язана з ацильною групою. Наприклад, ациламіногрупи включають алкілкарбоніламіно, арилкарбоніламіно, карбамоїл і уреїдо групи. Терміни "алкоксиалкіл", "алкіламіноалкіл" і "тіоалкоксиалкіл" включають алкільні групи, як описано вище, що, крім того, включають атоми кисню, азоту або сірки, які заміщують один або більше атомів вуглецю у вуглеводневому скелеті. Термін "карбоніл" або "карбокси" включає сполуки і складові частини молекули, які містять вуг 41 лець, зв'язаний подвійним зв'язком з атомом кисню. Приклади складових частин молекули, які містять карбоніл, включають альдегіди, кетони, карбонові кислоти, аміди, естери, ангідриди тощо. Термін "етер" або "етеровий" включає сполуки або складові частини молекули, які містять кисень, зв'язаний з двома атомами вуглецю. Наприклад, етер або етерна група включає "алкоксиалкіл", який стосується алкільної, алкенільної або алкінільної груп, заміщених алкокси групою. "Сульфонатна" група являє собою -SO3H або + + SC3X групу, зв'язану з атомом вуглецю, де Х являє собою катіонну протилежно заряджену іонну групу. Аналогічно, сполука "сульфонова кислота" + має -SO3H або -SC3X групу, зв'язану з атомом + вуглецю, де Х являє собою катіонну групу. "Сульфат", як тут використовується, являє собою + OSO3H або -OSO3X групу, зв'язану з атомом вуглецю, а сполука "сірчана кислота" має -OSO3H або + + -OSO3X групу, з'єднану з атомом вуглецю, де Х являє собою катіонну групу. Відповідно до винаходу, прийнятним катіонними групами можуть бути атоми водню. В деяких випадках, катіонною групою може в дійності бути інша група на терапевтичній сполуці, що позитивно заряджена при фізіологічному рН, наприклад, аміногрупа. "Протилежно заряджений іон" потрібний, для того щоб підтримувати елекронейтральність. Приклади аніонних протилежно заряджених іонів включають галіди, трифлати, сульфати, нітрати, гідроксиди, карбонати, бікарбонати, ацетати, фосфати, оксалати, ціаніди, алкіл карбоксилати, Nгідроксисукциніміди, N-гідроксибензотриазоли, алкоксиди, тіоалкоксиди, алкан сульфонілокси, галогензаміщений алкан сульфонілокси, арилсульфонілокси, бісульфати, оксалати, валерати, олеати, пальмітати, стеарати, лаурати, борати, бензоати, лактати, цитрати, малеати, фумарати, сукцинати, тартрати, нафтилату мезилат, глюкогептонат або лактобіонат. Сполуки, що містять катіонну групу, ковалентно зв'язану з аніонною групою, можуть бути названі як "внутрішні солі". Термін "нітро" означає -NO2; термін "галоген" або "галогено" або "гало" позначає -F, -СІ, -Br або І; термін "тіол", "тіо", або "меркапто" означає SH; а термін "гідроксил" або "гідрокси" означає -ОН. Термін "ацил" стосується карбонільної групи, яка приєднана через її атом вуглецю до водню (тобто, форміл), аліфатичної групи (наприклад, ацетил), ароматичної групи (наприклад, бензоїл), тощо. Термін "заміщений ацил" включає ацильні групи, в яких один або більше атомів водню на одному або більше атомах вуглецю, заміщуються, наприклад, алкільною групою, алкінільною групою, галогеном, гідроксилом, алкілкарбонілокси, арилкарбонілокси, алкоксикарбонілокси, арилоксикарбонілокси, карбоксилатом, алкілкарбонілом, арилкарбонілом, алкоксикарбонілом, амінокарбонілом, алкіламінокарбонілом, диалкіламінокарбонілом, алкілтіокарбонілом, алкоксилом, фосфатом, фосфонато, фосфінато, ціано, аміно (включаючи алкіламіно, диалкіламіно, ариламіно, диариламіно, і алкілариламіно), ациламіно (включаючи алкілкарбоніламіно, арилкарбоніламіно, карбамоїл і уреїдо), іміно, сульфгідрилом, алкілтіо, арилтіо, тіока 96115 42 рбоксилатом, сульфатом, алкілсульфінілом, сульфонато, сульфамоїлом, сульфонамідо, нітро, трифлуорометилом, ціано, азидо, гетероциклілом, алкіларилом, або ароматичною або гетероароматичною складовою частиною молекули. Якщо не обумовлено щось інше, хімічні складові частини молекул сполук винаходу, включаючи ті групи, що обговорювались вище, можуть бути "заміщені або незаміщені". В деяких втіленнях термін "заміщені" означає, що складова частина молекули має замісники, розташовані на інших, ніж водень, групах (тобто, у більшості випадків, заміщуючі водень), які дозволяють молекулі виконувати задану функцію. Приклади замісників включають групи, обрані з-поміж прямого або розгалуженого алкілу (переважно С1-С5), циклоалкілу (переважно С3-С8), алкокси (переважно С1-С6), тіоалкілу (переважно С1-С6), алкенілу (переважно С2-С6), алкінілу (переважно С2-С6), гетероциклічних, карбоциклічних, арильних (наприклад, феніл), арилокси (наприклад, фенокси), аралкільних (наприклад, бензил), арилоксиалкільних (наприклад, фенілоксиалкільні), арилацетамідоїльних, алкіларильних, гетероаралкільних, алкілкарбонільних і арилкарбонільних чи інших таких ацильних груп, гетероарилкарбонільних і гетероарильних груп, а також (CR'R")0-3NR'R" (напр., -NH2), (CR'R")0-3CN (напр., -CN), -NO2, галоген (напр., -F, -СІ, -Br, або I), (CR'R")0-3C(галоген)3 (напр., -CF3), (CR'R")0(CR'R")0-3СН2(галоген), (CR'R")03CH(галоген)2, 3CONR'R", (CR'R")0-3(CNH)NR'R", (CR'R")0-3S(O)1(CR'R")0-3CHO, (CR'R")0-3O(CR'R")0-3H, 2NR'R", (CR'R")0-3S(O)0-3R' (напр., -SO3H), (CR'R")03O(CR'R")0-3H (напр., -CH2OCH3 і -OCH3), (CR'R")03S(CR'R")0-3H (напр., -SH і -SCH3), (CR'R")0-3OH (напр., -OH), (CR'R")0-3COR', (CR'R")0-3(заміщений або незаміщений феніл), (CR'R")0-3(C3-C8 циклоалкіл), (CR'R")0-3CO2R' (напр., -СО2Н), і (CR'R")0-3OR' 1 групи, де R і R" кожен є незалежно водень, С1-С5 алкіл, С2-С5 алкеніл, С2-С5 алкініл, або арильна група; або бічний ланцюг будь-якої амінокислоти, що зустрічається в природі. В іншому втіленні, замісник може бути обраний серед прямих або розгалужених алкілів (переважно С1-С5), циклоалкілів (переважно С3-С8), алкокси (переважно С1-С8), тіоалкілів (переважно С1С6), алкенілів (переважно С2-С6;), алкінілів (переважно С2-С6), гетероциклічних, карбоциклічних, арильних (напр., феніл), арилокси (напр., фенокси), аралкільних (напр., бензил), арилоксиалкільних (напр., фенілоксиалкіл), арилацетамідоїл, алкіларильних, гетероаралкільних, алкілкарбонільних і арилкарбонільних або інших таких ацильних груп, гетероарилкарбонільних або гетероарильних груп, (CR'R")0-10NR'R" (напр., NH2), (CR'R")0-10CN (напр., -CN), NO2, галоген (напр., F, СІ, Br, або I), (CR'R")0-10C(галоген)3 (напр., CF3), (CR'R")0-10CH(галоген)2, (CR'R")0(CR'R")0-10CONR'R", (CR'R")010CH2(галоген), (CR'R")0-10S(O)1-2NR'R", (CR'R")010(CNH)NR'R", 10CHO, (CR'R")0-10O(CR'R")0-10H, (CR'R")0-10S(O)0-3R' (напр., -SO3H), (CR'R")0-10O(CR'R")0-10H (напр., СН2ОСН3 і -OCH3), (CR'R")0-10S(CR'R")0-3H (напр., SH і -SCH3), (CR'R")0-10OH (напр., -ОН), (CR'R")010COR', (CR'R")0-10(заміщений або незаміщений 43 феніл), (CR'R")0-10(C3-C8 циклоалкіл), (CR'R")010CO2R' (напр., -СО2Н), або (CR'R")0-10OR' група, або бічний ланцюг будь-якої аміноксилоти, що зустрічається в природі; де R' і R" кожен незалежно є водень, С1-С5 алкіл, С2-С5 алкеніл, С2-С5 алкініл, або арильна група, або R' і R" взяті разом утворюють бензиліденову групу або -(СН2)2О(СН2)2- групу. Слід розуміти, що "заміщення" або "заміщені за допомогою" включають таке заміщення, яке відбувається відповідно до дозволеної валентності заміщеного атома і замісника, і що заміщення призводить до утворення стійкої сполуки, напр., такої, яка спостанно не буде зазнавати перетворень, таких як перегрупування, циклізація, елімінування тощо. Як тут використовується, термін "заміщені" має на меті включати всі прийнятні замісники органічних сполук. В широкому розумінні, прийнятні замісники включають ациклічні або циклічні, розгалужені і нерозгалужені, карбоциклічні і гетероциклічні, ароматичні і неароматичні замісники органічних сполук. Прийнятних замісників може бути один або більше. В деяких втіленнях, "замісник" може бути обраний з групи, що складається з, наприклад, галогено, трифторметильної, нітро, ціано, С1С6алкільної, С2-С6алкенільної, С2-С6алкінільної, С1-С6алкілкарбонілокси, арилкарбонілокси, С1С6алкоксикарбонілокси, арилоксикарбонілокси, С1С6алкілкарбонільної, С1-С6алкоксикарбонільної, С1-С6алкокси, С1-С6алкілтіо, арилтіо, гетероциклільної, аралкільної, і арильної (включаючи гетероарил)груп. В одному втіленні, винахід має відношення до сполук Формули І: де: 1 R являє собою заміщене або незаміщене циклоалкільне, гетероциклічне, арильне, арилциклоалкільне, біциклічне або трициклічне кільце, біциклічну або трициклічну конденсовану кільцеву групу, або заміщену або незаміщену С2-С10 алкільну групу; 2 R обирають з групи, яка включає водень, алкіл, меркаптоалкіл, алкеніл, алкініл, циклоалкіл, арил, арилалкіл, тіазоліл, триазоліл, імідазоліл, бензотіазоліл і бензоімідазоліл; + + + Υ являє собою SO3X , OSO3X або SSO3X ; + Х являє собою водень, катіонну групу або естерну групу; і 1 2 кожен з L і L є незалежно заміщена або незаміщена С1-С5 алкільна група або відсутні, або фармацевтично прийнятна її сіль, за умови, що, 1 коли R1 - алкіл, L відсутній. В наступному втіленні, винахід має відношення до сполук Формули II: 96115 44 де: 1 R являє собою заміщену або незаміщену циклічну, біциклічну, трициклічну, або бензогетероциклічну групу або заміщену або незаміщену С2С10 алкільну групу; 2 R - це водень, алкіл, меркаптоалкіл, алкеніл, алкініл, циклоалкіл, арил, арилалкіл, тіазоліл, триазоліл, імідазоліл, бензотіазоліл, бензоімідазоліл, 1 або зв'язаний з R , утворюючи гетероцикл; + + + Υ являє собою SO3X , OSO3X або SSO3X ; + Х являє собою водень, катіонну групу або естерну групу; m має значення 0 або 1; n має значення 1, 2, 3 або 4; L - заміщена або незаміщена С1-С3 алкільна група, або вона відсутня, або фармацевтично при1 йнятна її сіль, за умови, що коли R - алкіл, L - відсутня. 2 В наступному втіленні, R - це водень. В на1 ступному втіленні, R - це алкіл з прямим ланцюгом, наприклад, етил, n-пентил, n-гептил або n1 октил. В наступному втіленні, R - це t-бутил. В ще 1 одному альтернативному втіленні, R являє собою С7-С10 біциклоалкіл або трициклоалкіл, такий як, 3,7 наприклад, трицикло[3.3.1.0 ]децил (або адамантил), біцикло[2.1.2]гептил, або індоліл. В іншому 1 альтернативному втіленні, R -це тетрагідронафтил. 2 В одному втіленні, L являє собою -(СН2)3-. В 2 ще одному наступному втіленні, L являє собою (СН2)4- або -(СН2)5-. В ще одному іншому втіленні, 2 L являє собою -(СН2)2-· В ще одному іншому вті2 ленні, L являє собою заміщений алкіл, напр., СН2-(СНОН)-СН2-. 1 В іншому втіленні, L являє собою СН2СН2 або відсутня. 1 В наступному втіленні, R являє собою розгалужений алкіл, напр., t-бутил. В іншому втіленні, 1 1 R - адаманіл. В іншому втіленні втіленні, R - циклічний алкіл, напр., циклопропіл, циклогексил, циклогептил, цикло-октил, тощо. Циклоалкільні групи можуть надалі бути заміщені, напр., додатковими алкільними групами або іншими групами, які дозволяють молекулі набувати заданої функції. В 1 іншому втіленні, R - це алкіл, заміщений пропаргі1 ловою групою (напр., Н=С-). В іншому втіленні, R являє собою циклогексил, заміщений однією або більше метиловими або пропаргіловими групами. 1 В інших втіленнях, L являє собою С1-С2 алкільну лінкерну групу (напр., -СН(СН3)-або -(СН2)2-. 1 В іншому втіленні, R - це феніл. В деяких втілен1 нях, R заміщений метокси групою. В інших вті1 леннях, L являє собою С3, напр., -(СН2)3- або 1 С(СН3)2-. В деяких втіленнях, L заміщений, напр., алкокси, карбоксилат (-СООН), бензилом, амідо(С=О-NН-), або естерною(С=О-С-О) групою. В одному з втілень, естерна група - це метил, етил, пропіл, бутил, циклогексил, або бензил естер. В інших втіленнях, естерною групою може бути про1 пеніл. В інших втіленнях, L заміщена карбоксиль 45 96115 1 ною групою. В іншому втіленні, R заміщений заміщеною амідною групою, де амідна група заміщена алкільною, напр., метильною, етильною, пропільною, бутильною, пентильною або гексиль1 ною групою. В іншому втіленні, алкільна R група заміщена -C=O-NH-OH, C=O-NH2, або амідогрупою. В деяких втіленнях, амідогрупа заміщена алкільною (напр., метильною, етильною, пропільною, бутильною, пентильною, гексильною, циклогексильною тощо), бензильною або арильною групою. В іншому втіленні, амідогрупа заміщена 1 СН(СН2)2 групою. Власне R може бути заміщений фенілом або може бути алкілом з розгалуженим 1 або прямим ланцюгом. В деяких втіленнях, R може також бути заміщений тіоетерною групою. Приклади тіоетерів включають S-Me, S-Et, тощо. В 1 деяких втіленнях, алкільна R група може бути заміщена як арильною або тіоетерною групою, так 1 і амідогрупою. В інших втіленнях, алкільна R група може бути заміщена як тіоетерною, так і карбо1 ксилатною групами. В інших втіленнях, алкільні R 1 групи заміщені гідроксилом. R групи, напр., алкі1 льні R групи, можуть також бути заміщені як тіоетерною, так і гідроксильною групами. В інших вті1 1 леннях, R групи, напр., алкільні R групи заміщені 1 ціаногрупами. Приклади R груп включаючи -CN групи, включають -C(CH3)2CN, циклогексил, заміщений однією або більше ціаногрупами тощо. 1 В інших втіленнях, алкільні R групи заміщені арильними групами. Арильні групи можуть бути заміщені фенілом, наприклад. Заміщений феніл може бути заміщений одним або більше замісни 46 ками, такими як гідрокси, ціано і алкокси. В інших 1 втіленнях, алкільні R групи заміщені тетразолілом або заміщеним чи незаміщеним бензилом. 1 В іншому втіленні, L являє собою -С(СН3)21 (СН2)-. В іншому втіленні, L являє собою 1 (С(СН3)2-СНОН-. В ще іншому втіленні, L являє 1 собою -(С(СН3)2СН(ОМе)-. В іншому втіленні, R заміщений або незаміщений феніл. В наступному 1 втіленні, R являє собою пара-заміщений феніл. Приклади замісників включають, але не обмежені ними, фтор, хлор, бром, йод, метил, t-бутил, алко1 кси, метокси, тощо. В іншому втіленні, R заміщений в мета-положенні. Приклади замісників включають метокси, хлор, метил, t-бутил, фтор, алкіл, алкокси, йодо, трифторалкіл, метокси, тощо. В 1 іншому втіленні, R - це феніл, заміщений в орто положенні, подібними замісниками. В іншому вті1 ленні, L містить циклоалкільну групу, напр., цик1 лопентил. В іншому втіленні, L містить алкієнільну групу і, необов'язково, заміщену арильну групу, із замісниками, подібними до тих, що описані вище. 1 В певних втіленнях, R - циклопропіл або циклогексил. В деяких втіленнях, циклопропільна або циклогексильна група заміщується етерною групою або алкільною групою. В деяких наступних втіленнях, етерна група являє собою бензильну етерну групу. 1 В іншому втіленні, де R - алкіл, він заміщується групами, такими як фенільна або гідроксильна. В інших втіленнях, сполуку винаходу обирають з групи, що складається з: 47 96115 48 49 96115 50 51 96115 52 53 96115 54 55 96115 56 57 96115 58 59 96115 60
ДивитисяДодаткова інформація
Назва патенту англійськоюMethods and compositions for treating amyloid-related diseases
Автори англійськоюKong Xianqi, Migneault David, Valade Isabelle, Wu Xinfu, Gervais Francine
Назва патенту російськоюСпособ и композиция для лечения амилоидогенных заболеваний
Автори російськоюКонг Ксянкви, Мигно Давид, Валаде Изабелла, Ву Ксинфу, Герваис Франсин
МПК / Мітки
МПК: C07D 207/333, C07D 471/04, C07F 9/165, C07D 295/084, C07C 311/32, C07D 207/32, C07C 309/00, C07D 217/04, C07F 9/24
Мітки: лікування, захворювань, композиція, спосіб, амілоїдогенних
Код посилання
<a href="https://ua.patents.su/127-96115-sposib-i-kompoziciya-dlya-likuvannya-amilodogennikh-zakhvoryuvan.html" target="_blank" rel="follow" title="База патентів України">Спосіб і композиція для лікування амілоїдогенних захворювань</a>
Попередній патент: Подовжений електричний провідник, пристосований для електричного з’єднання з електричним контактом
Наступний патент: Вагонний залізничний візок та його елементи
Випадковий патент: Система подачі підземної води населенню із знезалізнюванням води