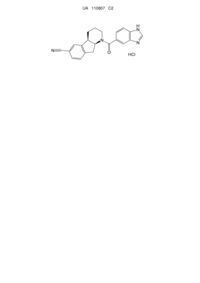
Кристалічні форми гідрохлориду (4a-r,9a-s)-1-(1н-бензоімідазол-5-карбоніл)-2,3,4,4а,9,9а-гексагідро-1н-індено[2,1-b]піридин-6-карбонітрилу та їх застосування як інгібіторів hsd 1
Номер патенту: 110807
Опубліковано: 25.02.2016
Автори: Зік Сандра, Екхардт Маттіас, Ян Бін-Шіу, Шюле Мартін, Мартін Ханс-Юрген
Формула / Реферат
1. Кристалічна Форма І сполуки, що представлена наступною структурною формулою:
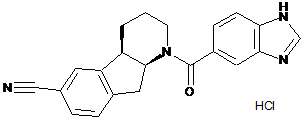
яка характеризується піками порошкової рентгенівської дифракції при кутах 2θ, вибраних з 12,5°, 12,9°, 14,8°, 20,0°, 22,2° та 26,1°.
2. Кристалічна Форма І за п. 1 для лікування або попередження хвороб або станів, на які можна впливати шляхом пригнічення ферменту 11β-гідроксистероїддегідрогеназа типу 1 (HSD).
3. Кристалічна Форма І за п. 2, де хвороба або стан, на який можна впливати шляхом пригнічення ферменту 11β-гідроксистероїддегідрогеназа типу 1 (HSD), являє собою метаболічний розлад.
4. Кристалічна Форма ІІ сполуки, що представлена наступною структурною формулою:
 ,
,
яка характеризується піками порошкової рентгенівської дифракції при кутах 2θ, вибраних з 13,7°, 17,6°, 21,3°, 21,9°, 23,3°, 25,6° та 26,5°.
5. Кристалічна Форма ІІ за п. 4 для лікування або попередження хвороб або станів, на які можна впливати шляхом пригнічення ферменту 11β-гідроксистероїддегідрогеназа типу 1 (HSD).
6. Кристалічна Форма ІІ за п. 5, де хвороба або стан, на який можна впливати шляхом пригнічення ферменту 11β-гідроксистероїддегідрогеназа типу 1 (HSD), являє собою метаболічний розлад.
7. Фармацевтична композиція, яка містить кристалічну Форму І за п. 1 та фармацевтично прийнятний носій або розріджувач.
8. Фармацевтична композиція, яка містить кристалічну Форму ІІ за п. 4 та фармацевтично прийнятний носій або розріджувач.
9. Спосіб одержання кристалічної Форми І за п. 1, в якому:
вільну основу сполуки, яка має наступну структуру
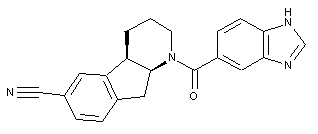 ,
,
розчиняють в етанолі при температурі нижче 30°С;
розчинену вільну основу протонують соляною кислотою; і
утворюють кристалічну Форму І шляхом охолодження розчиненої протонованої основи.
10. Спосіб одержання кристалічної Форми ІІ за п. 4, в якому:
сполуку, яка має наступну структуру
 ,
,
приводять в контакт з етанолом з утворенням суспензії, і
перемішують суспензію впродовж часу, достатнього для утворення кристалічної Форми ІІ.
11. Спосіб одержання кристалічної Форми ІІ за п. 4, в якому:
сполуку, яка має наступну структуру
 ,
,
розчиняють в етилацетаті при температурі вище 40°С; і
утворюють кристалічну Форму ІІ шляхом охолодження розчиненої сполуки.
12. Спосіб одержання кристалічної Форми ІІ за п. 4, в якому:
вільну основу сполуки, яка має наступну структуру
 ,
,
розчиняють в ізопропанолі при температурі вище 40°С;
вільну основу протонують соляною кислотою; і
утворюють кристалічну Форму ІІ шляхом охолодження розчиненої протонованої основи.
13. Спосіб одержання кристалічної Форми ІІ за п. 4, в якому:
вільну основу сполуки, яка має наступну структуру
 ,
,
розчиняють в етанолі при температурі вище 40°С;
розчинену вільну основу протонують соляною кислотою і підтримують розчинену протоновану основу при температурі вище 40°С впродовж принаймні двох годин; і
утворюють кристалічну Форму ІІ шляхом охолодження розчиненої протонованої основи.
Текст
Реферат: Даний винахід стосується кристалічних сполуки формули II H N N N N O HCl , які мають цінну фармакологічну активність. Зокрема, ці сполуки є інгібіторами 11гідроксистероїддегідрогенази типу 1 (HSD) і, відповідно, є придатними для лікування і попередження захворювань, на які можна впливати шляхом пригнічення цього ферменту, таких як метаболічні хвороби, зокрема діабет 2 типу, ожиріння і дисліпідемія. UA 110807 C2 (12) UA 110807 C2 UA 110807 C2 5 10 15 Споріднені заявки Дані заявки претендують на пріоритет попередньої заявки на патент США з серійним номером No. 61/484,995, поданої 11 травня 2011 року. Дані заявки також претендують на пріоритет міжнародної заявки з серійним номером No. PCT/US2010/055586, поданої 5 листопада 2010 року. Повний зміст цих двох заявок включено в даний опис за допомогою посилання. Галузь техніки Цей винахід стосується гексагідроінденопіридинів і октагідробензохінолінів та їх використання в якості інгібіторів 11β-гідроксистероїддегідрогенази типу 1 (HSD-1), а також фармацевтичних композицій, які містять вказані сполуки, і їх застосування для лікування метаболічних розладів, таких як метаболічний синдром, діабет, ожиріння і дизліпідемія. Крім того, даний винахід стосується процесів для приготування як фармацевтичної композиції, так і сполуки за цим винаходом. Рівень техніки Для лікування метаболічного синдрому, зокрема діабету 2 типу, ожиріння і дизліпідемії, в літературі пропонуються сполуки, які чинять інгібіторний вплив на фермент 11βгідроксистероїддегідрогеназа типу 1 (HSD-1). В Bulletin of the Chemical Society of Japan 1959, 32, p. 1005-7 і Journal of Organic Chemistry 1964, 29, p. 1419-24, описані сполуки наступної структури: 20 N N O O cis 25 trans . В Journal of Organic Chemistry 1984, 49, р. 2504-6, описаний хроматографічний метод розділення енантіомерів гетероциклічних амінів, в тому числі енантіомерів наступної рацемічної сполуки: N O O O trans . 30 В Journal of Medicinal Chemistry 1981, 24, p. 1432-7, наступна сполука описується як проміжний продукт для розділення cis- і trans-ізомерів: O N O O 35 40 . Суть винаходу Нами неочікувано було встановлено, що сполуки за цим винаходом не тільки чинять інгібіторний вплив на HSD 1 in vitro та/або in vivo, але й володіють високою метаболічною стабільністю, що робить їх придатними для застосування в якості лікарських препаратів. Відповідно, метою цього винаходу є запропонувати гексагідроінденопіридини і октагідробензохіноліни, які чинять інгібіторний вплив на HSD 1 in vitro та/або in vivo і володіють сприятливими фармакологічними і фармакокінетичними властивостями для їх застосування в якості лікарських препаратів. 1 UA 110807 C2 5 10 15 20 25 30 35 Інший аспект цього винаходу пропонує нові фармацевтичні композиції, які є придатними для попередження та/або лікування метаболічних розладів. Інший аспект цього винаходу стосується фізіологічно прийнятних солей сполук загальної формули І за цим винаходом з неорганічними або органічними кислотами або основами. Подальший аспект цього винаходу стосується фармацевтичних композицій, які містять принаймні одну сполуку загальної формули І або її фізіологічно прийнятну сіль за цим винаходом, необов'язково разом з одним або більше інертними носіями та/або розріджувачами. Подальший аспект цього винаходу стосується сполук загальної формули І або їх фізіологічно прийнятних солей для лікування або попередження захворювань або станів, на які може чинити вплив пригнічення ферменту 11β-гідроксистероїддегідрогеназа типу 1 (HSD-1), таких як метаболічні розлади. Подальший аспект цього винаходу стосується застосування принаймні однієї сполуки загальної формули І або її фізіологічно прийнятної солі для застосування фармацевтичної композиції, що є придатною для лікування або попередження захворювань або станів, на які може чинити вплив пригнічення ферменту 11β-гідроксистероїддегідрогеназа типу 1 (HSD-1), таких як метаболічні розлади. Інші цілі даного винаходу стануть очевидними для спеціаліста в цій галузі безпосередньо з попереднього і наступного опису. Короткий опис креслень Фіг. 1 представляє собою картину XRPD, одержану зі зразка Форми І сполуки формули (ІІ). 13 Фіг. 2 представляє собою спектр C SSNMR, одержаний зі зразка Форми І сполуки формули (ІІ). Фіг. 3 представляє собою графік термічного аналізу, одержаний зі зразка Форми І сполуки формули (ІІ), визначений шляхом вимірювань методом диференціальної скануючої калориметрії (DSC). Фіг. 4 представляє собою графік термічного аналізу, одержаний зі зразка Форми І сполуки формули (ІІ), визначений шляхом вимірювань методом термогравіметричного аналізу (TGA). Фіг. 5 представляє собою картину XRPD, одержану зі зразка Форми ІІ сполуки формули (ІІ). 13 Фіг. 6 представляє собою спектр C SSNMR, одержаний зі зразка Форми ІІ сполуки формули (ІІ). Фіг. 7 представляє собою графік термічного аналізу, одержаний зі зразка Форми ІІ сполуки формули (ІІ), визначений шляхом вимірювань методом DSC. Фіг. 8 представляє собою графік термічного аналізу, одержаний зі зразка Форми ІІ сполуки формули (ІІ), визначений шляхом вимірювань методом TGA. Докладний опис В першому аспекті даний винахід стосується сполук загальної формули І: 2 R 1 N R 3 R 4 R 40 45 50 55 ( )m I O , де: 1 1a R вибирається з групи R , що складається з фенілу, нафтилу, піролілу, фуранілу, тієнілу, піридилу, індолілу, бензофуранілу, бензотіофенілу, хінолінілу, ізохінолінілу, де в піроліловій, фураніловій, тієніловій і піридиновій групі 1 або 2 групи СН можуть бути необов'язково заміщеними на N і де в індоліловій, бензофураніловій, бензотіофенільній, хінолініловій або ізохінолініловій групі від 1 до 3 груп СН можуть бути необов'язково заміщеними на N, 2-оксо-1,2-дигідропіридинілу, 4-оксо-1,4-дигідропіридинілу, 3-оксо-2,3-дигідро-піридазинілу, 3,6-диоксо-1,2,3,6-тетрагідропіридазинілу, 2-оксо-1,2-дигідропіримідинілу, 4-оксо-3,4дигідропіримідинілу, 1,2,3,4-тетрагідро-2,4-диоксопіримідинілу, 2-оксо-1,2-дигідропіразинілу, 2,3диоксо-1,2,3,4-тетрагідропіразинілу, інданілу, 1-оксо-інданілу, 2,3-дигідро-індолілу, 2,3-дигідроізоіндолілу, 2-оксо-2,3-дигідро-індолілу, 1-оксо-2,3-дигідро-ізоіндолілу, 2,3дигідробензофуранілу, 2-оксо-2,3-дигідробензімідазолілу, 2-оксо-2,3-дигідробензоксазолілу, бензо[1,3]диоксолілу, 2-оксо-бензо[1,3]диоксолілу, 1,2,3,4-тетрагідронафтилу, 1,2,3,4тетрагідрохінолінілу, 2-оксо-1,2,3,4-тетрагідрохінолінілу, 2-оксо-1,2-дигідрохінолінілу, 4-оксо-1,4дигідрохінолінілу, 1,2,3,4-тетрагідро-ізохінолінілу, 1-оксо-1,2,3,4-тетрагідро-ізохинолінілу, 1-оксо 2 UA 110807 C2 5 10 15 20 25 30 35 40 45 50 55 1,2-дигідро-ізохінолінілу, 4-оксо-1,4-дигідро-ціннолінілу, 2-оксо-1,2-дигідрохіназолінілу, 4-оксо1,4-дигідрохіназолінілу, 2,4-диоксо-1,2,3,4-тетрагідрохіназолінілу, 2-оксо-1,2дигідрохіноксалінілу, 3-оксо-1,2,3,4-тетрагідро-хіноксалінілу, 2,3-диоксо-1,2,3,4тетрагідрохіноксалінілу, 1-оксо-1,2-дигідрофталазинілу, 1,4-диоксо-1,2,3,4тетрагідрофталазинілу, хроманілу, кумаринілу, 2,3-дигідро-бензо[1,4]диоксинілу, 3-оксо-3,4дигідробензо[1,4]оксазинілу, тетразолілу, 2-оксо-2,3-дигідробензотіазолілу і імідазо[1,2a]піридинілу, 1a де члени групи R є приєднаними до карбонільної групи у формулі I через атом ароматичного вуглецю, і 1a 5 де члени групи R можуть бути необов'язково заміщеними одним R , від одного до трьох 6 7 1 однакових та/або різних R , та/або одним R , за тієї умови, що у випадку, коли R є фенільною 5 6 7 групою, заміщення R , R та/або R не є приєднаними до атомів вуглецю, суміжними з тим атомом вуглецю, який приєднаний до карбонільної групи у формулі I; 2 2a R вибирається з групи R , що складається з водню, галогену, (гетеро)арилу, ціано, нітро, аміно, гідрокси, C1-6-алкілу, C3-6-циклоалкілу, C2-6-алкенілу і C2-6-алкінілу, де в кожній C1-6-алкіл-, C3-6-циклоалкіл-, C2-6-алкеніл- або C2-6-алкініл-групі одна група CH2 може бути необов'язково заміщеною на CO або SO2, одна група CH2 необов'язково може бути N заміщеною на O або NR і одна група CH може бути необов'язково заміщеною на N, і де кожна з цих груп може бути необов'язково моно- або поліфторованою і може бути необов'язково моноабо незалежно одна від одної дизаміщеною хлором, C1-3-алкілом, ціано, (гетеро)арилом, аміно, C1-3-алкіламіно, ди-(C1-3-алкіл)-аміно, гідрокси, C1-3-алкілокси, (гетеро)арилокси, C1-3-алкілсульфанілом, C1-3-алкілсульфінілом або C36-циклоалкілом, де одна або дві групи CH 2 C3-6-циклоалкільної групи можуть бути необов'язково N заміщеними незалежно одна від одної карбонільною групою, O або NR і одна група CH може бути необов'язково заміщеною на N, і яка може бути необов'язково моно- або незалежно заміщеною фтором або C1-3-алкілом; 3 4 3/4a R , R вибираються незалежно один від одного з групи R , яка складається з водню, галогену, C1-3-алкілу, трифторметилу, гідрокси, C1-3-алкілокси і ціано, або 3/4a 3 4 R означає R і R , які є зв'язаними з суміжними атомами вуглецю і об'єднаними з утворенням метилендиокси-, етилендиокси- або C3-5-алкіленової групи, кожна з яких може бути необов'язково заміщеною одною або двома групами, незалежно вибраними з фтору і метилу, або, разом з атомами вуглецю, до яких вони приєднані, утворюють бензольне, піридольне, піримідольне, піразинольне, піридазинольне, піризольне, імідазольне, триазольне, оксазольне, тіазольне, ізоксазольне або ізотіазольне кільце, кожне з яких може бути необов'язково заміщеним одним або двома заміщеннями, незалежно вибраними з галогену, C 1-3-алкілу, трифторметилу, аміно, C1-3-алкіламіно, ди-(C1-3-алкіл)аміно, гідрокси і C1-3-алкілокси; 5 5a R вибирається з групи R , яка складається з галогену, (гетеро)арилу, ціано, нітро, аміно, гідрокси, C1-6-алкілу, C3-6-циклоалкілу, C2-6-алкенілу і C2-6-алкінілу, де в кожній групі одна група CH2 може бути необов'язково заміщеною на CO або SO2, одна група CH2 необов'язково може N бути заміщеною на O або NR і одна група СН може бути необов'язково заміщеною на N, і де кожна група може бути необов'язково моно- або поліфторованою і необов'язково моно- або незалежно одна від одної дизаміщеною хлором, C1-3-алкілом, ціано, (гетеро)арилом, аміно, C1-3-алкіламіно, ди-(C1-3-алкіл)-аміно, гідрокси, C1-3-алкілокси, (гетеро)арилокси, C1-3-алкілсульфанілом, C1-3-алкілсульфінілом або C36-циклоалкілом, де одна або дві групи СН2 С3-6-циклоалкільної групи можуть бути необов'язково N заміщеними незалежно одна від одної на карбонільну групу, О або NR і одна група СН може бути необов'язково заміщеною на N, і яка необов'язково може бути моно- або незалежно дизаміщеною фтором або С1-3-алкілом; 6 7 6/7a R , R вибираються незалежно один від одного з групи R , яка складається з галогену, C13-алкілу, C2-3-алкінілу, трифторметилу, гідрокси, C 1-3-алкілокси і ціано, та/або 6/7a 6 7 R означає один R , об'єднаний з R , які приєднані до суміжних атомів вуглецю, що утворює метилендиокси-, дифторметилендиокси-, етилендиокси-, С3-5-алкіленову групу, або, разом з атомами вуглецю, до яких вони приєднані, утворюють піразольне, імідазольне, оксазольне, ізоксазольне, тіазольне або ізотіазольне кільце, кожне з яких може бути необов'язково моно- або дизаміщеним незалежно одне від одного С1-3-алкілом, трифторметилом, аміно, С1-3-алкіламіно, ди-(С1-3-алкіл)аміно, гідрокси, С1-3-алкілокси; N Na R вибирається незалежно один від одного з групи R , яка складається з водню, C1-6-алкілу, C3-6-циклоалкілу, C3-6-алкенілу, C3-6-алкінілу, (гетеро)арилу, C1-4-алкілкарбонілу, (гетеро)арилкарбонілу, C1-4-алкіламінокарбонілу, ди-(C1-3-алкіл)-амінокарбонілу, 3 UA 110807 C2 5 10 15 20 25 30 35 40 (гетеро)ариламінокарбонілу, C1-4-алкілоксикарбонілу, C1-4-алкілсульфонілу і (гетеро)арилсульфонілу, де кожна алкільна, алкенільна і алкінільна група може бути необов'язково моно- або полізаміщеною фтором і необов'язково монозаміщеною (гетеро)арилом, ціано, амінокарбонілом, С1-3-алкіламінокарбонілом, ди-(С1-3-алкіл)амінокарбонілом, карбокси, С1-4алкілоксикарбонілом, аміно, С1-4-алкіламіно, ди-(C1-3-алкіл)аміно, C1-4-алкілкарбоніламіно, гідрокси, C1-4-алкілокси, C1-4-алкілсульфанілом, C1-4-алкілсульфінілом або C1-4алкілсульфонілом; a (гетеро)арил вибирається незалежно один від одного з групи HA , яка складається з фенілу, нафтилу, піролілу, фуранілу, тієнілу, піридилу, індонілу, бензофуранілу, бензотіофенілу, хінолінілу, ізохінолінілу, де в піролільній, фуранільній, тієнільній і піридильній групі одна або дві групи СН можуть бути необов'язково заміщеними на N і де в індолільній, бензофуранільній, бензотіофенільній, хінолінільній і ізохінолінільній групі від однієї до трьох груп СН можуть бути необов'язково заміщеними на N, 2-оксо-1,2-дигідропіридинілу, 4-оксо-1,4-дигідропіридинілу, 3-оксо-2,3-дигідро-піридазинілу, 3,6-диоксо-1,2,3,6-тетрагідропіридазинілу, 2-оксо-1,2-дигідропіримідинілу, 4-оксо-3,4дигідропіримідинілу, 2,4-диоксо-1,2,3,4-тетрагідропіримідинілу, 2-оксо-1,2-дигідропіразинілу, 2,3диоксо-1,2,3,4-тетрагідропіразинілу, 2-оксо-2,3-дигидроіндолілу, 2,3-дигідробензофуранілу, 2оксо-2,3-дигідробензімідазолілу, 2-оксо-2,3-дигідро-бензоксазолілу, 2-оксо-1,2-дигідрохінолінілу, 4-оксо-1,4-дигідрохінолінілу, 1-оксо-1,2-дигідроізохінолінілу, 4-оксо-1,4-дигідроціннолінілу, 2оксо-1,2-дигідрохіназолінілу, 4-оксо-1,4-дигідрохіназолінілу, 2,4-диоксо-1,2,3,4тетрагідрохіназолінілу, 2-оксо-1,2-дигідро-хіноксалінілу, 3-оксо-1,2,3,4-тетрагідрохіноксалінілу, 2,3-диоксо-1,2,3,4-тетрагідро-хіноксалінілу, 1-оксо-1,2-дигідрофталазинілу, 1,4-диоксо-1,2,3,4тетрагідрофталазинілу, хроманілу, кумаринілу, 2,3-дигідробензо[1,4]диоксинілу, 3-оксо-3,4дигідро-бензо[1,4]оксазинілу і тетразолілу, і де вищевказані (гетеро)арильні групи можуть бути необов'язково заміщеними від одного до 10 трьох R , які можуть бути однаковими або різними; 10 10а R вибирається незалежно один від одного з групи R , яка складається з галогену, С1-3алкілу, дифторметилу, трифторметилу, ціано, амінокарбонілу, C 1-3-алкіламінокарбонілу, ди-(C1-3-алкіл)-амінокарбонілу, карбокси, C1-4-алкілокси-карбонілу, нітро, аміно, C1-3-алкіламіно, ди-(C1-3-алкіл)аміно, ацетиламіно, метилсульфоніламіно, гідрокси, C 1-3-алкілокси, дифторметокси, трифторметокси, метилсульфанілу, метилсульфінілу, метилсульфонілу, амуносульфонулу і фенілу, де фенільна група може бути необов'язково заміщеною одним або двома заміщеннями, вибраними незалежно один від одного з фтору, метилу, метокси, ціано і гідрокси; m означає 0 або 1; і де аліфатична частина трициклічної серцевинної структури загальної формули I є заміщеною однією або двома різними або ідентичними групами; 8 8a R вибирається незалежно один від одного з групи R , яка складається з водню, метилу і етилу; їх таутомерів, стереоізомерів, сумішей і солей, за виключенням наступних сполук: O N N N O O O O trans O O . 45 В іншому аспекті даний винахід стосується процесу для приготування сполук загальної формули I, який характеризується тим, що сполука загальної формули II: 4 UA 110807 C2 2 R NH 3 R 4 R 2 5 10 15 20 25 30 35 40 45 50 55 3 II ( )m , 4 в якій змінні R , R , R і m є такими, як визначено раніше або буде визначено далі, 1 вступає в реакцію зі сполукою загальної формули R -CO-Y, яку необов'язково готують in situ 1 з відповідної карбонової кислоти (Y=OH), де R є таким, як визначено раніше або буде визначено далі, і Y являє собою заміщувану групу і, зокрема, означає фтор, хлор, бром, ціано, C1-4-алкокси, C2-4-алкенілокси, C2-4-алкінілокси, C1-4-алкілсульфаніл, арилтриазолокси, гетероарилтриазолокси, гетероар-N-ил, сукциніл-N-окси, C1-4алкілкарбонілокси, ди-(C1-4-алкіл)-амінокарбонілокси, піролілкарбонілокси, піперидинілкарбонілокси, морфолінілкарбонілокси, [три-(С1-4-алкіл)-карбамімідоїл]окси, [ди-(С1-4+ алкіл)-аміно][ди-(C1-4-алкіл)-імініуміл]метокси{=[(C1-4-алкіл)2N]2C -O-}, (N, N’дициклогексилкарбамідоїл)окси, ди-(C1-4-алкілокси)-фосфорилокси, біс[ди-(C1-4-алкіл)-аміно]фосфорилокси, [біс(піролідин-1-іл)-фосфорил)окси, арилокси, арилсульфаніл, гетеросульфаніл або гетероарилокси, при цьому алкільна, алкенільна і алкінільна групи, згадані у визначенні вищевказаних заміщуваних груп, необов'язково можуть бути моно- або полізаміщеними фтором, хлором, С1-3алкілом або С1-3-алкокси, при цьому арильні групи, згадані у визначенні вищевказаних заміщуваних груп, окремо або як частина іншої групи, означають феніл або нафтил, а гетероарильні групи, згадані у визначенні вищевказаних груп, окремо або як частина іншої групи, означають піридиніл, піримідиніл, триазиніл, імідазоліл, піразоліл, триазоліл або тетразоліл, тоді як арильна і гетероарильна групи необов'язково можуть бути моно- або полізаміщеними незалежно одна від одної фтором, хлором, бромом, C1-3-алкілом, C1-3-алкілокси, нітро, ціано та/або ди-(С1-3алкіл)аміно, необов'язково в присутності основи, такої як третинний або ароматичний амін, наприклад етилдиізопропиламін, триетиламін, імідазол або піридин, або неорганічної солі, наприклад карбонату калію або оксиду кальцію, та/або іншої добавки, такої як 4-диметиламінопіридин або 1-гідроксибензотриазол, в розчинниках, переважно вибраних з тетрагідрофурану, 1,2диметоксиетану, ефіру, 1,4-діоксану, N, N-диметилформаміду, N, N-диметилацетаміду, Nметилпіролідинону, ацетонітрилу, етилацетату, дихлорметану, 1,2-дихлоретану, толуолу, бензолу і гексанів, при цьому для певних вищеперелічених комбінацій можна застосувати водні і спиртові розчини, переважно при температурі від -10 до 120 °C; і, коли це необхідно, будь-яка захисна група, використовувана в описаних вище реакціях, відщеплюється одночасно або послідовно; коли це бажано, сполука загальної формули I, одержана у такий спосіб, перетворюється на стереоізомери; коли це бажано, сполука загальної формули I, одержана у такий спосіб, перетворюється на свої солі, зокрема на фізіологічно прийнятні солі для фармацевтичного застосування. Докладний опис винаходу 1 2 3 4 5 6 7 Коли не вказується інше, всі групи, залишки і заміщення, зокрема R , R , R , R , R , R , R , 8 10 N R , R , R і m, є такими, як визначено раніше або буде визначено далі. Коли в якійсь сполуці залишки, заміщення або групи трапляються кілька разів, вони можуть мати однакові або різні значення. Певні кращі значення груп і заміщень в сполуках за цим винаходом будуть представлені далі. Кращі варіанти здійснення цього винаходу характеризуються наступними дефініціями: В одному варіанті здійснення даного винаходу 1 1b R вибирається з групи R , яка складається з фенілу, нафтилу, піролілу, фуранілу, тієнілу, піридилу, індолілу, бензофуранілу, бензотіофенілу, хінолінілу, ізохінолінілу, де в піролільній, фуранільній, тієнільній і піридильній групі одна група СН може бути необов'язково заміщена на N і де в індолільній, бензофуранільній, бензотіофенільній, хінолінільній і ізохінолінільній групах одна або дві групи СН можуть бути необов'язково заміщені на N, інданілу, 2,3-дигідро-індолілу, 2-оксо-2,3-дигідро-індолілу, 2,3-дигідробензо-фуранілу, 2оксо-2,3-дигідробензімідазолілу, 2-оксо-2,3-дигідробензотіазолілу, бензо[1,3]диоксолілу, 1,2,3,4 5 UA 110807 C2 5 10 15 20 25 30 35 40 45 50 55 60 тетрагідронафтилу, 1,2,3,4-тетрагідрохінолінілу, 1,2,3,4-тетрагідро-ізохінолінілу, 2-оксо-1,2дигідрохіноксалінілу, 3-оксо-1,2,3,4-тетрагідро-хіноксалінілу, хроманілу і імідазо[1,2-a]піридинілу, 1b при цьому члени групи R є приєднаними до карбонільної групи у формулі I через атом ароматичного вуглецю, і 1b 5 6 при цьому члени групи R можуть бути необов'язково заміщеними одним R , одним R 7 1 5 6 та/або одним R , за тієї умови, що у випадку, коли R є фенільною групою, заміщення R , R 7 та/або R не є приєднаними до атомів вуглецю, суміжних з тим атомом вуглецю, який приєднаний до карбонільної групи у формулі I. В другому варіанті здійснення даного винаходу 1 1с R вибирається з групи R , яка складається з фенілу, нафтилу, фуранілу, тієнілу, піразолілу, імідазолілу, оксазолілу, ізоксазолілу, тіазолілу, ізотіазолілу, піридилу, індолілу, бензофуранілу, бензотіофенілу, де в індолільній, бензофуранільній і бензотіофенільній групі одна або дві групи СН можуть бути необов'язково заміщеними на N, інданілу, 2,3-дигідро-індолілу, 2-оксо-2,3-дигідро-індолілу, 2,3-дигідробензо-фуранілу, 2оксо-2,3-дигідробензімідазолілу, 2-оксо-2,3-дигідробензотіазолілу, бензо[1,3]диоксолілу, 1,2,3,4тетрагідрохінолінілу, 2-оксо-1,2-дигідрохіноксалінілу, хроманілу і імідазо[1,2-a]піридинілу, 1с де члени групи R є приєднаними до карбонільної групи у формулі I через атом ароматичного вуглецю, і 1с 5 6 де члени групи R можуть бути необов'язково заміщеними одним R , одним R та/або одним 7 1 5 6 7 R , за тієї умови, що у випадку, коли R є фенільною групою, заміщення R , R та/або R не є приєднаними до атомів вуглецю, суміжних з тим атомом вуглецю, який приєднаний до карбонільної групи у формулі I. В іншому варіанті здійснення даного винаходу 1 1d R вибирається з групи R , яка складається з фенілу, індолілу, 2-оксо-2,3-дигідро-індолілу, бензімідазолілу, індазолілу, імідазол[1,2-а]піридинілу, 2-оксо-2,3-дигідро-бензоімідазолілу, 2оксо-2,3-дигідробензотіазолілу, імідазопіридинілу, бензотриазолілу, бензотіазолілу і 2-оксо-1,2дигідрохіноксалінілу, 1d де члени групи R є приєднаними до карбонільно групи у формулі I через атом ароматичного вуглецю, і 1d 5 6 де члени групи R можуть бути необов'язково заміщеними одним R , одним R та/або одним 7 1 5 6 7 R , за тієї умови, що у випадку, коли R є фенільною групою, заміщення R , R та/або R не є приєднаними до атомів вуглецю, суміжних з тим атомом вуглецю, який приєднаний до карбонільної групи у формулі I. В іншому варіанті здійснення даного винаходу 1 1d2 R вибирається з групи R , яка складається з 4-гідроксифенілу, 4-аміно-3-метоксифенілу, 3-фтор-4-гідроксифенілу, 4-аміно-3-хлорфенілу, 3-хлор-4-гідрокси-фенілу, індол-3-ілу, індол-5ілу, індол-6-ілу, 1-метил-індол-3-ілу, бензімідазол-5-ілу, 6-метил-бензімідазол-5-ілу, 7-метилбензімідазол-5-ілу, індазол-5-ілу і бензотіазол-6-ілу. В іншому варіанті здійснення даного винаходу 1 1е R вибирається з групи R , яка складається з 4-гідрокси-фенілу, 4-аміно-3-метокси-фенілу, 3-фтор-4-гідрокси-фенілу, 4-аміно-3-хлор-фенілу, 3-хлор-4-гідрокси-фенілу, індол-3-ілу, індол-5ілу, індол-6-ілу, 1-метил-індол-3-ілу, бензімідазол-5-ілу, індазол-5-ілу і бензотіазол-6-ілу. В іншому варіанті здійснення даного винаходу 1 1f R вибирається з групи R , яка складається з бензімідазол-5-ілу, 6-метил-бензімідазол-5-ілу і 7-метил-бензімідазол-5-ілу. В іншому варіанті здійснення даного винаходу 2 2b R вибирається з групи R , яка складається з водню, галогену, (гетеро)арилу, ціано, нітро, аміно, гідрокси, C2-6-алкінілу, C1-6-алкілу і C3-6-циклоалкілу, де в C1-6-алкільній і C3-6-циклоалкільній групі одна група СН2 може бути необов'язково N заміщеною на СО або SO 2, одна група CH2 може бути необов'язково заміщеною на O або NR і одна група СН може бути необов'язково заміщеною на N, при цьому обидві групи необов'язково можуть бути моно- або поліфторованими і необов'язково моно- або незалежно одна від одної заміщеними хлором, C1-3-алкілом, ціано, (гетеро)арилом, аміно, C1-3-алкіламіно, ди-(C1-3-алкіл)-аміно, гідрокси, C1-3-алкілокси, (гетеро)арилокси, C 1-3-алкілсульфанілом, C1-3-алкілсульфінілом та/або C3-6-циклоалкілом, при цьому в C3-6-циклоалкільній групі одна або дві групи СН2 можуть бути N необов'язково заміщеними незалежно одна від одної карбонілом, О або NR , і одна група CH може бути необов'язково заміщеною на N і необов'язково може бути моно- або незалежно заміщеною фтором або C1-3-алкілом. 6 UA 110807 C2 5 10 15 20 25 30 35 40 45 50 55 60 В іншому варіанті здійснення даного винаходу 2 2с R вибирається з групи R , яка складається з водню, фтору, хлору, брому, C1-3-алкілу, C3-6циклоалкілметилу, циклопропилу, (гетеро)арил-метилу, C2-4-алкінілу, (гетеро)арилу, ціано-C1-3алкілу, амінокарбоніл-C1-3-алкілу, C1-3-алкіл-амінокарбоніл-C1-3-алкілу, ди-(C1-3-алкіл)амінокарбоніл-C1-3-алкілу, піролідин-1-іл-карбоніл-C1-3-алкілу, піперидин-1-іл-карбоніл-C1-3алкілу, морфолін-4-іл-карбоніл-C1-3-алкілу, карбокси-C1-3-алкілу, C1-3-алкокси-карбоніл-C1-3алкілу, C1-3-алкілкарбоніл-аміно-C1-3-алкілу, N-(C1-3-алкіл)-C1-3-алкілкарбоніл-аміно-C1-3-алкілу, 2оксо-піролідин-1-іл-C1-3-алкілу, 2-оксо-піперидин-1-іл-C1-3-алкілу, 3-оксо-морфолін-4-іл-C1-3алкілу, гідрокси-C1-3-алкілу, C1-3-алкілокси-C1-3-алкілу, трифторметилу, дифторметилу, ціано, амінокарбонілу, C1-3-алкіл-амінокарбонілу, ди-(C1-3-алкіл)-амінокарбонілу, піролідин-1-ілкарбонілу, піперидин-1-іл-карбонілу, морфолін-4-іл-карбонілу, карбокси, C1-3-алкілоксикарбонілу, аміно, C1-3-алкіламіно, C1-3-алкіл-карбоніламіно, (гетеро)арил-карбоніламіно, N-(C1-3алкіл)-C1-3-алкіл-карбоніламіно, N-(C1-3-алкіл)-(гетеро)арил-карбоніламіно, 2-оксо-піролідин-1ілу, 2-оксо-піперидин-1-ілу, морфолін-4-ілу, 3-оксо-морфолін-4-ілу, C1-3-алкіл-сульфоніламіно, N(C1-3-алкіл)-C1-3-алкіл-сульфоніламіно, N-(C1-3-алкіл)-(гетеро)арил-сульфоніламіно, гідрокси, C1-4алкілокси, C3-6-циклоалкілокси, тетерагідрофуран-3-ілокси, тетрагідрофуран-3-ілокси, тетрагідропіран-4-ілокси, дифторметокси, трифторметокси, (гетеро)арилокси, ціано-C1-3алкілокси, амінокарбоніл-C1-3-алкілокси, C1-3-алкіл-амінокарбоніл-C1-3-алкілокси, ди-(C1-3-алкіл)амінокарбоніл-C1-3-алкілокси, піролідин-1-іл-карбоніл-C1-3-алкілокси, піперидин-1-іл-карбоніл-C1морфолін-4-іл-карбоніл-C1-3-алкіл-окси, карбокси-C1-3-алкілокси, C1-3-алкілокси3-алкілокси, карбоніл-C1-3-алкілокси, гідрокси-C1-3-алкілокси, C1-3-алкілокси-C1-3-алкілокси, тетрагідрофуранілC1-3-алкілокси, тетрагідропіраніл-C1-3-алкілокси, C1-4-алкілсульфонілу, C3-6циклоалкілсульфонілу, аміносульфонілу, C 1-3-алкіл-аміносульфонілу і ди-(C1-3-алкіл)аміносульфонілу, де вищезгаданий термін (гетеро)арил означає феніл, фураніл, тієніл, імідазоліл, піразоліл, оксазоліл, ізоксазоліл, тіазоліл, триазоліл, оксадиазоліл, піридиніл, піримідиніл, піразиніл або 10 піридазиніл, всі з яких необов'язково можуть бути моно- або дизаміщеними R . В іншому варіанті здійснення даного винаходу 2 2d R вибирається з групи R , яка складається з водню, фтору, хлору, брому, метилу, етинілу, циклопропилу, C3-6-циклоалкіл-метилу, фенілметилу, гідрокси-C1-3-алкілу, фенілу, ціано, амінокарбонілу, метиламінокарбонілу, диметиламінокарбонілу, піролідин-1-ілкарбонілу, морфолін-4-ілкарбонілу, карбокси, метоксикарбонілу, аміно, ацетиламіно, метилсульфоніламіно, гідрокси, С1-3-алкілокси, фенілокси і піридазинілокси, при цьому згадувані фенільна і піридазинільна групи необов'язково можуть бути монозаміщеними фтором, метилом, ціано або метокси. В іншому варіанті здійснення даного винаходу 2 2е R вибирається з групи R , яка складається з водню, фтору, хлору, брому, циклогексилметилу, фенілметилу, 4-метокси-фенілметилу, гідроксиметилу, 2-гідроксипроп-2-ілу, фенілу, ціано, амінокарбонілу, метиламінокарбонілу, диметиламінокарбонілу, піролідин-1ілкарбонілу, морфолін-4-ілкарбонілу, карбокси, метоксикарбонілу, аміно, гідрокси, метокси, 4метоксифенокси і 6-метил-піридазин-3-ілокси. 2 2f В іншому варіанті здійснення даного винаходу R вибирається з групи R , яка складається з водню і ціано. В іншому варіанті здійснення даного винаходу 3 4 3/4b R , R вибираються незалежно один від одного з групи R , яка складається з водню, фтору, хлору, С1-3-алкілу, трифторметилу, ціано, гідрокси і С 1-3-алкокси, або 3/4b 3 4 R означає R і R , які є приєднаними до суміжних атомів вуглецю і об'єднаними з утворенням метилендиокси- або етилендиокси-групи, або, разом з атомами вуглецю, до яких вони приєднані, утворюють імідазольне, оксазольне або тіазольне кільце, кожне з яких може бути необов'язково заміщеним одним або двома заміщеннями, незалежно вибраними з метилу, диметиламіно, гідрокси і метокси. В іншому варіанті здійснення даного винаходу 3 4 3/4с R , R вибираються незалежно один від одного з групи R , яка складається з водню, фтору, хлору, метилу, трифторметилу, ціано, гідрокси і метокси. В іншому варіанті здійснення даного винаходу 3 4 3/4с2 R , R вибираються незалежно один від одного з групи R , яка складається з водню, фтору і метилу. В іншому варіанті здійснення даного винаходу 3 4 3/4d R , R вибираються незалежно один від одного з групи R , яка складається з водню і фтору. 7 UA 110807 C2 5 10 15 20 25 30 35 40 45 50 55 60 В іншому варіанті здійснення даного винаходу 5 5b R вибирається з групи R , яка складається з фтору, хлору, брому, C1-4-алкілу, C3-6циклоалкіл-C1-3-алкілу, C3-6-циклоалкілу, (гетеро)арил-C1-3-алкілу, (гетеро)арилу, ціано-C1-3алкілу, амінокарбоніл-C1-3-алкілу, C1-3-алкіл-амінокарбоніл-C1-3-алкілу, ди-(C1-3-алкіл)амінокарбоніл-C1-3-алкілу, піролідин-1-іл-карбоніл-C1-3-алкілу, піперидин-1-іл-карбоніл-C1-3алкілу, піперазин-1-іл-карбоніл-C1-3-алкілу, 4-(C1-3-алкіл)-піперазин-1-іл-карбоніл-C1-3-алкілу, морфолін-4-іл-карбоніл-C1-3-алкілу, карбокси-C1-3-алкілу, C1-3-алкілокси-карбоніл-C1-3-алкілу, аміно-C1-3-алкілу, C1-3-алкіламіно-C1-3-алкілу, ди-(C1-3-алкіл)-аміно-C1-3-алкілу, піролідин-1-іл-C1-3алкілу, піперидин-1-іл-C1-3-алкілу, піперазин-1-іл-C1-3-алкілу, 4-(C1-3-алкіл)-піперазин-1-іл-C1-3алкілу, морфолін-4-іл-C1-3-алкілу, C1-3-алкілкарбоніламіно-C1-3-алкілу, (гетеро)арилкарбоніламіно-C1-3-алкілу, 2-оксо-піролідин-1-іл-C1-3-алкілу, 2-оксо-піперидин-1-ілC1-3-алкілу, 2-оксо-піперазин-1-іл-C1-3-алкілу, 3-оксо-піперазин-1-іл-C1-3-алкілу, 2-оксо-4-(C1-3алкіл)-піперазин-1-іл-C1-3-алкілу, 3-оксо-4-(C1-3-алкіл)-піперазин-1-іл-C1-3-алкілу, 3-оксоморфолін-4-іл-C1-3-алкілу, гідрокси-C1-3-алкілу, C1-3-алкілаокси-C1-3-алкілу, (гетеро)арилокси-C1-3алкілу, дифторметилу, трифторметилу, 2,2,2-трифтор-1-гідроксиетилу, 2,2,2-трифтор-1гідрокси-1-метилетилу, 2,2,2-трифтор-1-гідрокси-1-(трифторметил)етилу, ціано, амінокарбонілу, C1-3-алкіл-амінокарбонілу, ди-(C1-3-алкіл)-амінокарбонілу, (гетеро)арил-C1-3-алкіламінокарбонілу, N-(C1-3-алкіл)-(гетеро)арил-C1-3-алкіламінокарбонілу, (гетеро)ариламінокарбонілу, N-(C1-3-алкіл)(гетеро)арил-амінокарбонілу, піролідин-1-іл-карбонілу, піперидин-1-іл-карбонілу, піперазин-1-ілкарбонілу, 4-(C1-3-алкіл)-піперазин-1-іл-карбонілу, морфолін-4-іл-карбонілу, карбокси, C1-3алкокси-карбонілу, нітро, аміно, C1-3-алкіламіно, ди-(C1-3-алкіл)аміно, піролідин-1-ілу, піперидин1-ілу, піперазин-1-ілу, 4-(C1-3-алкіл)-піперазин-1-ілу, 4-(C1-3-алкілкарбоніл)-піперазин-1-ілу, 4-(C13-алкілоксикарбоніл)-піперазин-1-ілу, 4-(C1-3-алкілсульфоніл)-піперазин-1-ілу, морфолін-4-ілу, C13-алкіл-карбоніламіно, N-(C1-3-алкіл)-C1-3-алкіл-карбоніламіно, (гетеро)арилкарбоніламіно, N-(C1(гетеро)арил-C1-3-алкіл-карбоніламіно, N-(C1-3-алкіл)3-алкіл)-(гетеро)арилкарбоніламіно, (гетеро)арил-C1-3-алкіл-карбоніл аміно, 2-оксо-піролідин-1-ілу, 2-оксо-піперидин-1-ілу, 2-оксопіперазин-1-ілу, 2-оксо-4-(C1-3-алкіл)-піперазин-1-ілу, 3-оксо-піперазин-1-ілу, 3-оксо-4-(C1-3алкіл)-піперазин-1-ілу, 3-оксо-морфолін-4-ілу, амінокарбоніламіно, N-(амінокарбоніл)-C1-3алкіламіно, C1-3-алкіл-амінокарбоніламіно, N-(C1-3-алкіл-амінокарбоніл)-C1-3-алкіламіно, N-[ди(C1-3-алкіл)амінокарбоніл]-C1-3-алкіламіно, ди-(C1-3-алкіл)-амінокарбоніл-аміно, піролідин-1-ілкарбоніламіно, піперидин-1-іл-карбоніламіно, піперазин-1-іл-карбоніламіно, 4-(C1-3-алкіл)піперазин-1-іл-карбоніламіно, морфолін-4-іл-карбоніламіно, C1-3-алкілокси-карбоніл аміно, N-(C1C1-3-алкіл-сульфоніламіно, N-(C1-3-алкіл)-C1-3-алкіл3-алкіл)-C1-3-алкілокси-карбоніламіно, сульфоніламіно, (гетеро)арилсульфоніламіно, N-(C1-3-алкіл)-(гетеро)арилсульфоніламіно, оксоімідазолідин-1-іла, гідрокси, C1-4-алкілокси, C3-6-циклоалкіл-C1-3-алкілокси, (гетеро)арил-C1-3алкілокси, C3-6-циклоалкілокси, (гетеро)арил-окси, ціано-C1-3-алкілокси, амінокарбоніл-C1-3алкілокси, C1-3-алкіл-амінокарбоніл-C1-3-алкілокси, ди-(C1-3-алкіл)-амінокарбоніл-C1-3-алкілокси, піролідин-1-іл-карбоніл-C1-3-алкілокси, піперидин-1-іл-карбоніл-C1-3-алкілокси, піперазин-1-ілкарбоніл-C1-3-алкілокси, 4-(C1-3-алкіл)-піперазин-1-іл-карбоніл-C1-3-алкілокси, морфолін-4-ілкарбоніл-C1-3-алкіл-окси, карбокси-C1-3-алкілокси, C1-3-алкілокси-карбоніл-C1-3-алкілокси, аміноC1-3-алкілокси, C1-3-алкіламіно-C1-3-алкілокси, ди-(C1-3-алкіл)-аміно-C1-3-алкілокси, піролідин-1-ілC1-3-алкілокси, піперидин-1-іл-C1-3- алкілокси, піперазин-1-іл-C1-3-алкілокси, 4-(C1-3-алкіл)піперазин-1-іл-C1-3-алкілокси, морфолін-4-іл-C1-3-алкілокси, 2-оксо-піролідин-1-іл-C1-3- алкілокси, 2-оксо-піперидин-1-іл-C1-3-алкілокси, 2-oxo-піперазин-1-іл-C1-3-алкілокси, 3-оксо-піперазин-1-ілC1-3-алкілокси, 2-оксо-4-(C1-3-алкіл)-піперазин-1-іл-C1-3-алкілокси, 3-оксо-4-(C1-3-алкіл)-піперазин1-іл-C1-3-алкілокси, 3-оксо-морфолін-4-іл-C1-3-алкілокси, гідрокси-C1-3-алкілокси, C1-3-алкілоксиC1-3-алкілокси, тетрагідрофуран-3-іл-окси, тетрагидропиран-3-ил-окси, тетрагидропиран-4-илокси, тетрагидрофуранил-C1-3-алкілокси, тетрагідропіраніл-C1-3-алкілокси, дифторметокси, трифторметокси, C1-3-алкілсульфаніл-C1-3-алкілокси, C1-3-алкілсульфініл-C1-3-алкілокси, C1-3алкілсульфоніл-C1-3-алкілокси, C1-3-алкілсульфонілу, (гетеро)арилсульфонілу, аміносульфонілу, C1-3-алкіламіносульфонілу, ди-(C1-3-алкіл)-аміносульфонілу, піролідин-1-іл-сульфонілу, піперидин-1-іл-сульфонілу, морфолін-4-іл-сульфонілу, піперазин-1-іл-сульфонілу і 4-(C1-3-алкіл)піперазин-1-іл-сульфонілу, де вищезгаданий термін (гетеро)арил має таке значення, як визначено тут раніше або буде визначено далі. В іншому варіанті здійснення даного винаходу 5 5с R вибирається з групи R , яка складається з фтору, хлору, C1-4-алкілу, (гетеро)арил-C1-3алкілу, (гетеро)арилу, аміносульфонілу, аміно-C1-3-алкілу, C1-3-алкіламіно-C1-3-алкілу, ди-(C1-3алкіл)-аміно-C1-3-алкілу, піролідин-1-іл-C1-3-алкілу, морфолін-4-іл-C1-3-алкілу, C1-3алкілкарбоніламіно-C1-3алкілу, (гетеро)арилкарбоніламіно-C1-3-алкілу, 2-оксо-піролідин-1-іл-C1-3 8 UA 110807 C2 5 10 15 20 25 30 35 40 45 50 55 60 алкілу, 3-оксо-морфолін-4-іл-C1-3-алкілу, гідрокси-C1-3-алкілу, C1-3-алкілокси-C1-3-алкілу, 2,2,2трифтор-1-гідроксиетилу, 2,2,2-трифтор-1-гідрокси-1-метилетилу, 2,2,2-трифтор-1-гідрокси-1трифторметил-етилу, трифторметилу, ціано, амінокарбонілу, C1-3-алкіл-амінокарбонілу, ди-(C1-3алкіл)-амінокарбонілу, (гетеро)ариламінокарбонілу, піролидин-1-іл-карбонілу, піперидин-1-ілкарбонілу, піперазин-1-іл-карбонілу, морфолін-4-іл-карбонілу, 4-(C1-3-алкіл)-піперазин-1-ілкарбонілу, карбокси, C1-3-алкілокси-карбонілу, аміно, C1-3-алкіламіно, ди-(C1-3-алкіл)аміно, піролідин-1-ілу, піперидин-1-ілу, піперазин-1-ілу, морфолін-4-ілу, 2-оксо-піролидин-1-ілу, 2-оксопіперидин-1-ілу, 2-оксо-піперазин-1-ілу, 3-оксо-піперазин-1-ілу, 3-оксо-морфолін-4-ілу, C1-3-алкілкарбоніламіно, (гетеро)арилкарбоніламіно, амінокарбоніламіно, C1-3-алкіл-амінокарбоніламіно, ди-(C1-3-алкіл)амінокарбоніламіно, піролідин-1-іл-карбоніламіно, піперидин-1-іл-карбоніламіно, піперазин-1-іл-карбоніламіно, морфолін-4-іл-карбоніл-аміно, C1-3-алкілокси-карбоніламіно, гідрокси, C1-4-алкілокси, гідрокси-C1-3-алкілокси, C1-3-алкілокси-C1-3-алкілокси, дифторметокси, трифторметокси і (гетеро)арилокси, де вищезгаданий термін (гетеро)арил означає феніл, піроліл, піразоліл, імідазоліл, фураніл, оксазоліл, ізоксазоліл, тієніл, тіазоліл, триазоліл, оксадиазоліл, піридил, піридазиніл, піримідиніл 10 і піразиніл, кожний з яких необов'язково може бути заміщеним одним або двома R . В іншому варіанті здійснення даного винаходу 5 5d R вибирається з групи R , яка складається з фтору, хлору, C1-3-алкілу, гідрокси-C1-3-алкілу, амінокарбонілу, C1-3-алкіл-амінокарбонілу, аміно, C1-3-алкіламіно, C1-3-алкіл-карбоніламіно, гідрокси, C1-3-алкілокси, трифторметилу, дифторметокси, трифторметокси і аміносульфонілу. В іншому варіанті здійснення даного винаходу 5 5е R вибирається з групи R , яка складається з фтору, хлору, метилу, аміно, гідрокси і метокси. В іншому варіанті здійснення даного винаходу 6 7 6/7b R , R вибираються незалежно один від одного з групи R , яка складається з фтору, хлору, брому, C1-3-алкілу, C2-3-алкінілу, трифторметилу, гідрокси, C1-3-алкілокси і ціано, та/або 6/7b 6 7 R означає один R і один R , які є приєднаними до суміжних атомів вуглецю і об'єднаними з утворенням метилендиокси-, дифторметилендиокси-, етилендиокси- або С3-5-алкілен-групи. В іншому варіанті здійснення даного винаходу 6 7 6/7с R , R вибираються незалежно один від одного з групи R , яка складається з фтору, хлору, метилу, етилу, трифторметилу, гідрокси, метокси і етокси. В іншому варіанті здійснення даного винаходу 6 7 6/7d R , R вибираються незалежно один від одного з групи R , яка складається з фтору, хлору, метилу, гідрокси і метокси. В іншому варіанті здійснення даного винаходу 10 10b R вибирається незалежно один від одного з групи R , яка складається з фтору, хлору, брому, С1-3-алкілу, фенілу, дифторметилу, трифторметилу, ціано, амінокарбонілу, С 1-3алкіламінокарбонілу, ди-(C1-3-алкіл)амінокарбонілу, карбокси, C1-4-алкілокси-карбонілу, нітро, аміно, ацетиламіно, метилсульфоніламіно, гідрокси, C1-3-алкілокси, дифторметокси, трифторметокси, метилсульфанілу, метилсульфінілу, метилсульфонілу і аміносульфонілу. В іншому варіанті здійснення даного винаходу 10 10с R вибирається незалежно один від одного з групи R , яка складається з фтору, хлору, метилу, дифторметилу, трифторметилу, ціано, гідрокси, метокси, дифторметокси і трифторметокси. В іншому варіанті здійснення даного винаходу 10 10d R вибирається незалежно один від одного з групи R , яка складається з фтору, метилу, ціано і метокси. В іншому варіанті здійснення даного винаходу N Nb R вибирається незалежно один від одного з групи R , яка складається з водню, C1-6-алкілу, C3-6-циклоалкілу, C3-6-алкенілу, фенілу, C1-4-алкілкарбонилу, фенілкарбонілу, C1-3алкіламінокарбонілу, феніламінокарбонілу, C1-4-алкілоксикарбонілу, C1-4-алкіл-сульфонілу і фенілсульфонілу, де C1-6-алкільна група необов'язково може бути моно- або полізаміщеною фтором і необов'язково монозаміщеною фенілом, ціано, амінокарбонілом, C1-3-алкіламінокарбонілом, ди(C1-3-алкіл)амінокарбонілом, карбокси, C1-4-алкоксикарбонілом, C1-4-алкілкарбоніламіно, гідрокси або C1-4-алкокси. В іншому варіанті здійснення даного винаходу N Nс R вибирається незалежно один від одного з групи R , яка складається з водню, фенілу, C14-алкілкарбонільної, фенілкарбонільної, C 1-3-алкіламінокарбонільної, феніламінокарбонільної, C1-4-алкілоксикарбонільної, C1-4-алкілсульфонільної, фенілсульфонільної і C 1-4-алкільної групи, 9 UA 110807 C2 5 10 15 20 яка необов'язково може бути моно- або поліфторованою і необов'язково монозаміщеною гідрокси, C1-4-алкокси, ціано або фенілом. В іншому варіанті здійснення даного винаходу N Nd R вибирається незалежно один від одного з групи R , яка складається з водню, метилу, бензилу, фенілу, ацетилу, трет-бутоксикарбонілу і метилсульфонілу. В іншому варіанті здійснення даного винаходу 8 8b R вибирається незалежно один від одного з групи R , яка складається з водню і метилу. В іншому варіанті здійснення даного винаходу 8 8с R вибирається незалежно один від одного з групи R , яка складається з водню. В іншому варіанті даного винаходу m дорівнює 0. 1x 2x 3/4x 5x 6/7x Nx 8x 10x Кожний з R , R , R , R , R , R , R , R , m являє собою відмінний, індивідуальний варіант здійснення для відповідного заміщення, як описано вище. Таким чином, враховуючи вищенаведені визначення, кращі конкретні варіанти здійснення першого аспекту даного 1x 2x 3/4x 5x 6/7x Nx 8x 10x винаходу повністю характеризуються цим терміном (R , R , R , R , R , R , R , R , m), де кожному індексу х присвоєна конкретна цифра, яка доповнюється літерою від "а" і далі, по порядку. Індекси х і m можуть змінюватись незалежно один від одного. Всі окремі варіанти здійснення, описані терміном в дужках з повною комбінацією індексів х і m, у відношенні до наведених вище визначень, охоплюються даним винаходом. Наступна Таблиця 1 ілюструє в якості прикладу і в порядку збільшення преференції від першого рядка до останнього такі варіанти здійснення даного винаходу від Е-1 до Е-36, які вважаються кращими. Це означає, що варіант здійснення Е-36, представлений своїми даними в останньому рядку Таблиці 1, є найкращим варіантом. Таблиця 1: Кращі варіанти здійснення цього винаходу від Е-1 до Е-36 1 E-1 E-2 E-3 E-4 E-5 E-6 E-7 E-8 E-9 E-10 E-11 E-12 E-13 E-14 E-15 E-16 E-17 E-18 E-19 E-20 E-21 E-22 E-23 E-24 E-25 E-26 E-27 E-28 E-29 E-30 E-31 R 1b R 1c R 1b R 1b R 1b R 1c R 1c R 1b R 1c R 1c R 1c R 1b R 1c R 1c R 1c R 1c R 1d R 1d R 1d R 1d R 1d2 R 1e R 1e R 1e R 1d R 1e R 1e R 1e R 1d2 R 1d2 R 1d2 R 2 R 2b R 2c R 2b R 2b R 2b R 2b R 2b R 2c R 2b R 2c R 2c R 2c R 2b R 2c R 2c R 2c R 2c R 2c R 2d R 2e R 2e R 2e R 2e R 2e R 2f R 2f R 2f R 2f R 2c R 2d R 2e R 3 4 R /R 3/4b R 3/4c R 3/4d R 3/4d R 3/4d R 3/4b R 3/4b R 3/4c R 3/4c R 3/4c R 3/4c R 3/4c2 R 3/4c2 R 3/4c2 R 3/4c2 R 3/4d R 3/4d R 3/4d R 3/4d R 3/4d R 3/4d R 3/4d R 3/4d R 3/4d R 3/4d R 3/4d R 3/4d R 3/4d R 3/4d R 3/4d R 3/4d R 5 6 R 5b R 5c R 5c R 5d R 5e R 5c R 5d R 5c R 5c R 5c R 5d R 5c R 5c R 5c R 5d R 5d R 5d R 5e R 5e R 5e R -* -* -* -* R 7 R /R 6/7b R 6/7c R 6/7d R 6/7d R 6/7d R 6/7c R 6/7d R 6/7c R 6/7c R 6/7c R 6/7d R 6/7c R 6/7c R 6/7c R 6/7d R 6/7d R 6/7d R 6/7d R 6/7d R 6/7d R -* -* -* -* 6/7d R -* -* -* -* -* -* 5e -* -* -* -* -* -* 10 10 R 10b R 10c R 10d R 10d R 10d R 10d R 10d R 10d R 10d R 10d R 10d R 10d R 10d R 10d R 10d R 10d R 10d R 10d R -* -* -* -* -* -* -* -* -* -* 10d R -* -* 8 R 8a R 8a R 8a R 8b R 8b R 8b R 8b R 8b R 8b R 8b R 8b R 8b R 8b R 8b R 8b R 8b R 8b R 8b R 8b R 8b R 8b R 8b R 8c R 8c R 8b R 8b R 8c R 8c R 8b R 8b R 8b R N R Nb R m -* Nd R Nd R Nd R Nd R Nd R -* R Nd -* -* -* R Nd -* -* -* -* -* -* -* -* -* -* -* -* -* -* -* -* -* -* 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0,1 0 0,1 0,1 0,1 0 0,1 0,1 0,1 UA 110807 C2 Таблиця 1: Кращі варіанти здійснення цього винаходу від Е-1 до Е-36 E-32 E-33 E-34 E-35 E-36 1d2 2f R 1d2 R 1f R 1f R 1f R R 2f R 2f R 2f R 2f R 3/4d R 3/4d R 3/4d R 3/4d R 3/4d R -* -* -* -* -* -* -* -* -* -* -* -* -* -* -* 8b R 8b R 8b R 8c R 8c R -* -* -* -* -* 0,1 0 0,1 0,1 0 -* означає, що відповідної змінної не існує в даному варіанті здійснення їх таутомери, стереоізомери, суміші і солі, за виключенням наступних сполук: O N N N O O O O trans O O 5 10 15 20 25 30 35 40 45 Відповідно, Е-24 охоплює сполуки формули І, в яких: 1 1e R вибирається з групи R , яка складається з 4-гідрокси-фенілу, 4-аміно-3-метокси-фенілу, 3-фтор-4-гідрокси-фенілу, 4-аміно-3-хлор-фенілу, 3-хлор-4-гідрокси-фенілу, індол-3-ілу, індол-5ілу, індол-6-ілу, 1-метил-індол-3-ілу, бензімідазол-5-ілу, індазол-5-ілу і бензотіазол-6-ілу; 2 2е R вибирається з групи R , яка складається з водню, фтору, брому, циклогексилметилу, фенілметилу, 4-метокси-фенілметилу, гідроксиметилу, 2-гідроксипроп-2-ілу, фенілу, ціано, амінокарбонілу, метиламінокарбонілу, диметиламінокарбонілу, піролідин-1-ілкарбонілу, морфолін-4-ілкарбонілу, карбокси, метоксикарбонілу, аміно, гідрокси, метокси, 4метоксифенокси і 6-метил-піридазин-3-ілокси; 3 4 3/4d R , R вибираються незалежно один від одного з групи R , яка складається з водню і фтору; 8 8c R вибирається незалежно один від одного з групи R , яка складається з водню; і m=0, та їх таутомери, стереоізомери, суміші і солі. Відповідно, Е-28 охоплює сполуки формули І, в яких: 1 1e R вибирається з групи R , яка складається з 4-гідрокси-фенілу, 4-аміно-3-метокси-фенілу, 3-фтор-4-гідрокси-фенілу, 4-аміно-3-хлор-фенілу, 3-хлор-4-гідрокси-фенілу, індол-3-ілу, індол-5ілу, індол-6-ілу, 1-метил-індол-3-ілу, бензімідазол-5-ілу, індазол-5-ілу і бензотіазол-6-ілу; 2 2f R вибирається з групи R , яка складається з водню і ціано; 3 4 3/4d R , R вибираються незалежно один від одного з групи R , яка складається з водню і фтору; 8 8c R вибирається незалежно один від одного з групи R , яка складається з водню; і m=0, та їх таутомери, стереоізомери, суміші і солі. Відповідно, Е-33 охоплює сполуки формули І, в яких: 1 1d2 R вибирається з групи R , яка складається з 4-гідрокси-фенілу, 4-аміно-3-метокси-фенілу, 3-фтор-4-гідрокси-фенілу, 4-аміно-3-хлор-фенілу, 3-хлор-4-гідрокси-фенілу, індол-3-ілу, індол-5ілу, індол-6-ілу, 1-метил-індол-3-ілу, бензімідазол-5-ілу, 6-метил-бензімідазол-5-ілу, 7-метилбензімідазол-5-ілу, індазол-5-ілу і бензотіазол-6-ілу; 2 2f R вибирається з групи R , яка складається з водню і ціано; 3 4 3/4d R , R вибираються незалежно один від одного з групи R , яка складається з водню і фтору; 8 8b R вибирається незалежно один від одного з групи R , яка складається з водню і метилу; і m=0, та їх таутомери, стереоізомери, суміші і солі. Відповідно, Е-36 охоплює сполуки формули І, в яких: 1 1f R вибирається з групи R , яка складається з бензімідазол-5-ілу, 6-метил-бензімідазол-5-ілу і 7-метил-бензімідазол-5-ілу; 2 2f R вибирається з групи R , яка складається з водню і ціано; 11 UA 110807 C2 3 5 4 3/4d R , R вибираються незалежно один від одного з групи R , яка складається з водню і фтору; 8 8с R вибирається незалежно один від одного з групи R , яка складається з водню; і m=0, та їх таутомери, стереоізомери, суміші і солі. Інший кращий варіант здійснення цього винаходу описується формулою І.а 2 R H N H 3 R ( )m 4 R 10 1 R I.a O , де підструктура піперидину і підструктура тетраліну (m=1) або індану (m=0) утворюють 1 2 3 4 структуру трициклічного ядра в cis конфігурації, при цьому змінні R , R , R , R і m є такими, як було визначено раніше або буде визначено далі; відповідні сполуки охоплюються цим винаходом разом з їх таутомерами, стереоізомерами, сумішами і солями. Інший кращий варіант здійснення цього винаходу описується формулою І.b 15 2 R H N H 3 R ( )m 4 R 20 2 , H N H 3 R 4 30 35 40 I.b O де структура трициклічного ядра має R конфігурацію при C-10b (для m=1)/C-4a (для m=0) і S 1 2 3 4 конфігурацію при C-4a (для m=1)/C-9a (для m=0), при цьому змінні R , R , R , R і m є такими, як було визначено раніше або буде визначено далі; відповідні сполуки охоплюються цим винаходом разом з їх таутомерами, стереоізомерами, сумішами і солями. Відповідно, один варіант втілення кращих сполук за цим винаходом включає сполуки формули I.b R 25 1 R R ( )m 1 R I.b O , де: 1 1е R вибирається з групи R , яка складається з 4-гідрокси-фенілу, 4-аміно-3-метокси-фенілу, 3-фтор-4-гідрокси-фенілу, 4-аміно-3-хлор-фенілу, 3-хлор-4-гідрокси-фенілу, індол-3-ілу, індол-5ілу, індол-6-ілу, 1-метил-індол-3-ілу, бензімідазол-5-ілу, індазол-5-ілу і бензотіазол-6-ілу; 2 2е R вибирається з групи R , яка складається з водню, фтору, брому, циклогексилметилу, фенілметилу, 4-метокси-фенілметилу, гідроксиметилу, 2-гідроксипроп-2-ілу, фенілу, ціано, амінокарбонілу, метиламінокарбонілу, диметиламінокарбонілу, піролідин-1-ілкарбонілу, морфолін-4-ілкарбонілу, карбокси, метоксикарбонілу, аміно, гідрокси, метокси, 4метоксифенокси і 6-метил-піридазин-3-ілокси; 3 4 3/4d R , R вибираються незалежно один від одного з групи R , яка складається з водню і фтору; 8 8с R вибирається незалежно один від одного з групи R , яка складається з водню; і m=0, та їх таутомери, стереоізомери, суміші і солі. Іншим варіантом втілення кращих сполук за цим винаходом є сполуки формули I.b, де: 1 1е R вибирається з групи R , яка складається з 4-гідрокси-фенілу, 4-аміно-3-метокси-фенілу, 3-фтор-4-гідрокси-фенілу, 4-аміно-3-хлор-фенілу, 3-хлор-4-гідрокси-фенілу, індол-3-ілу, індол-5ілу, індол-6-ілу, 1-метил-індол-3-ілу, бензімідазол-5-ілу, індазол-5-ілу і бензотіазол-6-ілу; 12 UA 110807 C2 2 5 10 15 20 2f R вибирається з групи R , яка складається з водню і ціано; 3 4 3/4d R , R вибираються незалежно один від одного з групи R , яка складається з водню і фтору; 8 8с R вибирається незалежно один від одного з групи R , яка складається з водню; і m=0, та їх таутомери, стереоізомери, суміші і солі. Іншим варіантом втілення кращих сполук за цим винаходом є сполуки формули I.b, де: 1 1f R вибирається з групи R , яка складається з бензімідазол-5-ілу, 6-метил-бензімідазол-5-ілу і 7-метил-бензімідазол-5-ілу; 2 2f R вибирається з групи R , яка складається з водню і ціано; 3 4 3/4d R , R вибираються незалежно один від одного з групи R , яка складається з водню і фтору; 8 8с R вибирається незалежно один від одного з групи R , яка складається з водню; і m=0, та їх таутомери, стереоізомери, суміші і солі. Що стосується дефініцій гетероароматичних груп, що містять N, таких як (гетеро)арил, який має в своєму каркасі один або кілька атомів азоту, що несуть гідроксильну групу при атомі вуглецю, суміжному з азотом, або в іншій позиції кільця, що робить можливим мезомерну взаємодію з азотом, то ці групи можуть утворювати таутомерну амідну підструктуру, яка є частиною даного винаходу; таутомерний амід, одержаний в результаті об'єднання гідроксильної групи і гетероароматичної сполуки, що містить N, може нести заміщення, інші ніж водень, на амідному атомі азоту. Приклади таких підструктур гетероароматичних груп, де може утворюватись таутомерний амід, представлені наступною добіркою: N N N R N O N R N R N N O N O 25 O O R N O N N R N N R O S N N R N N R N O O O N R N O N O O N N R R N N N R N O N N R N R N N N R O O N N R N N R , N 30 де R є таким, як описано вище. Ці таутомерні структури можна віднести до гетероароматичних і ароматичних груп, наприклад таких, які утворюються (гетеро)арилом. В деяких варіантах даного винаходу пропонуються кристалічні сполуки наступної структурної формули (ІІ): (ІІ). 35 40 Термін "кристалічний", як він тут використовується, стосується твердої речовини, в якій молекули розподілені з періодично повторюваною у трьох вимірах структурою. Кристалічні сполуки формули (ІІ) можуть представляти собою індивідуальну кристалічну форму або суміш різних кристалічних форм. Індивідуальна кристалічна форма означає сполуку формули (ІІ) у вигляді індивідуального кристалу або великої кількості кристалів, при цьому кожний кристал має однакову кристалічну форму. В конкретному варіанті, принаймні, певний відсоток від маси сполуки формули (ІІ) представляє собою індивідуальну кристалічну форму. Певні масові відсотки включають 50 %, 52 %, 55 %, 57 %, 60 %, 62 %, 65 %, 67 %, 70 %, 72 %, 75 %, 77 %, 80 %, 82 %, 85 %, 86 %, 87 %, 13 UA 110807 C2 5 10 15 20 25 30 35 40 45 88 %, 89 %, 90 %, 91 %, 92 %, 93 %, 94 %, 95 %, 96 %, 97 %, 98 %, 99 %, 99,5 %, 99,9 % або відсоток в інтервалі між 50 % та 100 %. Якщо певний відсоток від маси сполуки формули (ІІ) визначений як кристалічна форма, то залишок сполуки формули (ІІ) представляє собою деяку комбінацію аморфних форм сполуки формули (ІІ). Якщо відсоток від маси сполуки формули (ІІ) визначений як індивідуальна кристалічна форма, то залишок сполуки формули (ІІ) представляє собою деяку комбінацію аморфних форм сполуки формули (ІІ) та/або одну або більше кристалічних форм сполуки формули (ІІ), відмінних від індивідуальної кристалічної форми. Приклади індивідуальних кристалічних форм включають форми І та ІІ сполуки формули (ІІ), а також індивідуальні кристалічні форми, що характеризуються одним або декількома властивостями, як тут описано. В подальшому описі конкретних кристалічних форм сполуки формули (ІІ) варіанти винаходу можуть бути описані по відношенню однієї конкретної кристалічної "Форми" сполуки формули (ІІ). Однак, конкретні кристалічні форми можуть також характеризуватись однією або більше властивостями кристалічних форм, як тут описано, відносно або незалежно від прив'язування до конкретної "Форми". Форма І В одному варіанті індивідуальна кристалічна форма сполуки формули (ІІ) характеризується як кристалічна Форма І. В іншому варіанті, принаймні, певний відсоток від маси сполуки формули (ІІ) представляє собою кристалічну Форму І. Певні масові відсотки включають 50 %, 52 %, 55 %, 57 %, 60 %, 62 %, 65 %, 67 %, 70 %, 72 %, 75 %, 77 %, 80 %, 82 %, 85 %, 86 %, 87 %, 88 %, 89 %, 90 %, 91 %, 92 %, 93 %, 94 %, 95 %, 96 %, 97 %, 98 %, 99 %, 99,5 %, 99,9 % або відсоток в інтервалі між 50 % та 100 %. В деяких варіантах кристалічна форма характеризується картиною порошкової рентгенівської дифракції (тут як "XPRD"), показаної на Фіг. 1, наприклад, з величинами кутів 2Θ, d-відстанями та відносними інтенсивностями, перерахованими в Таблиці 1, одержаними з застосуванням CuKα-випромінювання. В деяких варіантах кристалічна форма характеризується одним, двома, трьома, чотирма, п'ятьма або шістьма піками XPRD при кутах 2Θ, вибраних з 12,5°, 12,9°, 14,8°, 20,0°, 22,2° та 26,1°. В деяких варіантах кристалічна форма характеризується, принаймні, трьома піками XPRD при кутах 2Θ, вибраних з 12,5°, 12,9°, 14,8°, 20,0°, 22,2° та 26,1°. В деяких варіантах кристалічна форма характеризується, принаймні, чотирма піками XPRD при кутах 2Θ, вибраних з 12,5° 12,9°, 14,8°, 20,0°, 22,2° та 26,1°. В деяких варіантах кристалічна форма характеризується, принаймні, п'ятьма піками XPRD при кутах 2Θ, вибраних з 12,5°, 12,9°, 14,8°, 20,0°, 22,2° та 26,1°. В деяких варіантах кристалічна форма характеризується піками XPRD при кутах 2Θ, вибраних з 12,5°, 12,9°, 14,8°, 20,0°, 22,2° та 26,1°. В деяких варіантах кристалічна форма характеризується одним, двома, трьома або чотирма піками XPRD при кутах 2Θ, вибраних з 12,5°, 14,8°, 22,2° та 26,1°. В деяких варіантах кристалічна форма характеризується, принаймні, трьома піками XPRD при кутах 2Θ, вибраних з 12,5°, 14,8°, 22,2° та 26,1°. В деяких варіантах кристалічна форма характеризується піками XPRD при кутах 2Θ, вибраних з 12,5°, 14,8°, 22,2° та 26,1°. В деяких варіантах кристалічна форма характеризується одним, двома, трьома або чотирма основними піками XPRD при кутах 2Θ, вибраних з 12,5°, 14,8°, 22,2° та 26,1°. В деяких варіантах кристалічна форма характеризується основними піками XPRD при кутах 2Θ, вибраних з 12,5°, 14,8°, 22,2° та 26,1°. Слід розуміти, що вказаний кут 2Θ означає вказане значення ± 0.1°. "Основний пік XPRD", як він тут використовується, стосується піку XPRD з відносною інтенсивністю більшою, ніж 25 %. Відносна інтенсивність вираховується як відношення максимальної інтенсивності цікавого піка до максимальної інтенсивності найбільшого піка. Таблиця 1: Піки XPRD на Фіг. 1 2Θ [°] 5.77 5.93 6.47 9.81 11.55 11.94 12.54 Інтенсивність I/Io [%] 5 4 17 3 2 5 100 d-величина [Å] 15.30 14.88 13.65 9.01 7.66 7.40 7.05 14 UA 110807 C2 Таблиця 1: Піки XPRD на Фіг. 1 2Θ [°] 12.88 14.83 16.04 16.54 17.35 18.67 19.52 19.59 19.98 20.20 20.46 20.66 20.90 21.14 21.55 22.18 23.14 23.26 23.49 23.99 24.32 24.91 25.02 25.39 26.09 26.52 26.84 27.10 27.33 28.30 29.12 29.91 Інтенсивність I/Io [%] 23 31 12 4 5 2 5 5 21 7 5 4 3 5 4 49 8 11 10 3 4 9 14 4 60 12 2 1 2 14 3 4 d-величина [Å] 6.87 5.97 5.52 5.35 5.11 4.75 4.54 4.53 4.44 4.39 4.34 4.30 4.25 4.20 4.12 4.01 3.84 3.82 3.78 3.71 3.66 3.57 3.56 3.51 3.41 3.36 3.32 3.29 3.26 3.15 3.06 2.98 13 5 10 15 В деяких варіантах кристалічна форма характеризується спектром С ядерного магнітного резонансу твердого тіла (далі "SSNMR"), що показаний на Фіг. 2, наприклад, з хімічними зсувами, перерахованими в Таблиці 2, одержаними з застосуванням обертання під магічним кутом. В конкретному варіанті кристалічна форма характеризується 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 13 12, 13, 14, 15, 16, 17 або 18 піками С SSNMR при хімічних зсувах, вибраних з 170,3 чнм, 146,5 чнм, 142,8 чнм, 135,0 чнм, 130,6 чнм, 128,1 чнм, 122,1 чнм, 116,7 чнм, 115,6 чнм, 112,8 чнм, 109,8 чнм, 107,6 чнм, 44,6 чнм, 43,3 чнм, 41,4 чнм, 30,3 чнм, 26,3 чнм та 23,9 чнм. В одному 13 варіанті кристалічна форма характеризується, принаймні, десятьма піками С SSNMR при хімічних зсувах, вибраних з 170,3 чнм, 146,5 чнм, 142,8 чнм, 135,0 чнм, 130,6 чнм, 128,1 чнм, 122,1 чнм, 116,7 чнм, 115,6 чнм, 112,8 чнм, 109,8 чнм, 107,6 чнм, 44,6 чнм, 43,3 чнм, 41,4 чнм, 30,3 чнм, 26,3 чнм та 23,9 чнм. В одному варіанті кристалічна форма характеризується, 13 принаймні, п'ятнадцятьма піками С SSNMR при хімічних зсувах, вибраних з 170,3 чнм, 146,5 чнм, 142,8 чнм, 135,0 чнм, 130,6 чнм, 128,1 чнм, 122,1 чнм, 116,7 чнм, 115,6 чнм, 112,8 чнм, 109,8 чнм, 107,6 чнм, 44,6 чнм, 43,3 чнм, 41,4 чнм, 30,3 чнм, 26,3 чнм та 23,9 чнм. В одному 13 варіанті кристалічна форма характеризується піками С SSNMR при хімічних зсувах, вибраних з 170,3 чнм, 146,5 чнм, 142,8 чнм, 135,0 чнм, 130,6 чнм, 128,1 чнм, 122,1 чнм, 116,7 чнм, 115,6 чнм, 112,8 чнм, 109,8 чнм, 107,6 чнм, 44,6 чнм, 43,3 чнм, 41,4 чнм, 30,3 чнм, 26,3 чнм та 23,9 чнм. 20 15 UA 110807 C2 Таблиця 2 Хімічні зсуви 13 С ЯМР з Фіг.2 Пік 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 5 10 15 20 25 30 Хімічний зсув (чнм) 170.3 148.7 146.5 142.8 135.0 130.6 128.1 122.1 116.7 115.6 112.8 109.8 107.6 54.9 44.6 43.3 41.4 30.3 26.3 23.9 В деяких варіантах кристалічна форма характеризується ендотермічним переходом, що має початок приблизно при 231,7±0,5 °C на графіку диференційного сканування (далі "DSC"). В деяких варіантах кристалічна форма характеризується графіком DSC, показаним на Фіг. 3. Графік ілюструє тепловий потік як функцію температури зразка, що містить Форму І. DSC здійснювали на зразку з використанням швидкості сканування 10 °C/хвилину. Крім того, Форма І характеризується графіком термічного гравіметричного аналізу (далі "TGA"), показаним на Фіг. 4. Графік ілюструє відсоток втрати маси зразка як функцію температури при швидкості зміни температури 10 °C/хвилину. Графік ілюструє втрату маси приблизно 2,1 % при зміні температури зразка від кімнатної температури до 150 °C, що вказує на те, що Форма І є безводною. Форма ІІ В одному варіанті індивідуальна кристалічна форма сполуки формули (ІІ) характеризується як кристалічна Форма ІІ. В іншому варіанті, принаймні, певний відсоток від маси сполуки формули (ІІ) представляє собою кристалічну Форму ІІ. Певні масові відсотки включають 50 %, 52 %, 55 %, 57 %, 60 %, 62 %, 65 %, 67 %, 70 %, 72 %, 75 %, 77 % 80 %, 82 %, 85 %, 86 %, 87 %, 88 %, 89 %, 90 %, 91 %, 92 %, 93 %, 94 %, 95 %, 96 %, 97 %, 98 %, 99 %, 99,5 %, 99,9 % або відсоток в інтервалі між 50 % та 100 %. В деяких варіантах кристалічна форма характеризується картиною XRPD, показаною на Фіг. 5, наприклад з величинами кутів 2Θ, d-відстанями та відносними інтенсивностями, перерахованими в Таблиці 3, одержаними з застосуванням CuKα-випромінювання. В конкретному варіанті кристалічна форма характеризується одним, двома, трьома, чотирма, п'ятьма, шістьма або сімома, вісьма, дев'ятьма, десятьма, одинадцятьма або дванадцятьма піками XRPD при кутах 2Θ, вибраних з 13,3°, 13,7°,15,7°, 17,6°, 19,3°, 19,7°, 20,9°, 21,3°, 21,9°, 23,3°, 25,6° та 26,5°. В конкретному варіанті кристалічна форма характеризується, принаймні, сімома, вісьма, дев'ятьма, десятьма або одинадцятьма піками XRPD при кутах 2Θ, вибраних з 13,3°, 13,7°, 15,7°, 17,6°, 19,3°, 19,7°, 20,9°, 21,3°, 21,9°, 23,3°, 25,6° та 26,5°. В деяких варіантах кристалічна форма характеризується піками XRPD при кутах 2Θ 13,3°, 13,7°, 15,7°, 17,6°, 19,3°, 19,7°, 20,9°, 21,3°, 21,9°, 23,3°, 25,6° та 26,5°. В деяких варіантах кристалічна форма характеризується піками XRPD при кутах 2Θ 13,7°, 17,6°, 21,3°, 21,9°, 23,3°, 25,6° та 26,5°. В деяких варіантах кристалічна форма характеризується піками XRPD при кутах 2Θ 13,7°, 17,6°, 19,7°, 21,3°, 21,9°, 23,3°, 25,6° та 26,5°. В деяких варіантах кристалічна форма характеризується піками XRPD при кутах 2Θ 13,7°, 17,6°, 19,7°, 20,9°, 21,3°, 21,9°, 23,3°, 25,6° та 26,5°. В деяких варіантах кристалічна форма характеризується піками XRPD при кутах 2Θ 13,7°, 17,6°, 19,3°, 16 UA 110807 C2 5 19,7°, 20,9°, 21,3°, 21,9°, 23,3°, 25,6° та 26,5°. В деяких варіантах кристалічна форма характеризується піками XRPD при кутах 2Θ 13,3°, 13,7°, 17,6°, 19,3°, 19,7°, 20,9°, 21,3°, 21,9°, 23,3°, 25,6° та 26,5°. В деяких варіантах кристалічна форма характеризується піками XRPD при кутах 2Θ 13,3°, 13,7°,15,7°, 17,6°, 19,3°, 19,7°, 20,9°, 21,3°, 21,9°, 23,3°, 25,6° та 26,5°. В деяких варіантах кристалічна форма характеризується одним, двома, трьома, чотирма, п'ятьма, шістьма або сімома основними піками XRPD при кутах 2Θ, вибраних з 13,7°, 17,6°, 21,3°, 21,9°, 23,3°, 25,6° та 26,5°. В деяких варіантах кристалічна форма характеризується основними піками XRPD при кутах 2Θ 13,7°, 17,6°, 21,3°, 21,9°, 23,3°, 25,6° та 26,5°. Таблиця 3: Піки XRPD на Фіг. 5 2Θ [°] 9.79 10.73 12.54 13.31 13.70 14.83 15.71 16.68 17.58 18.41 19.07 19.27 19.66 20.88 21.32 21.56 21.91 22.99 23.29 23.61 24.27 24.89 25.37 25.55 26.05 26.50 26.79 27.68 d-величина [Å] 9.03 8.24 7.05 6.65 6.46 5.97 5.63 5.31 5.04 4.82 4.65 4.60 4.51 4.25 4.16 4.12 4.05 3.87 3.82 3.77 3.66 3.57 3.51 3.48 3.42 3.36 3.32 3.22 10 15 20 Інтенсивність I/Io [%] 19 18 3 26 100 2 20 19 40 7 10 33 39 38 48 8 50 10 56 8 19 9 15 40 5 41 10 19 13 В деяких варіантах кристалічна форма характеризується спектром C SSNMR, показаним на Фіг. 6, наприклад, з хімічними зсувами, перерахованими в Таблиці 4, одержаними з використанням обертання під магічним кутом. В конкретному варіанті кристалічна форма 13 характеризується 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 або 18 піками C SSNMR при хімічних зсувах, вибраних з 172,6 чнм, 147,1 чнм, 144,1 чнм, 132,9 чнм, 129,6 чнм, 125,9 чнм, 121,2 чнм, 119,5 чнм, 117,7 чнм, 114,6 чнм, 110,2 чнм, 45,1 чнм, 42,4 чнм, 32,6 чнм, 28,3 чнм та 24,4 чнм. В одному варіанті кристалічна форма характеризується, принаймні, десятьма 13 піками C SSNMR при хімічних зсувах, вибраних з 172,6 чнм, 147,1 чнм, 144,1 чнм, 132,9 чнм, 129,6 чнм, 125,9 чнм, 121,2 чнм, 119,5 чнм, 117,7 чнм, 114,6 чнм, 110,2 чнм, 45,1 чнм, 42,4 чнм, 32,6 чнм, 28,3 чнм та 24,4 чнм. В одному варіанті кристалічна форма характеризується, 13 принаймні, тринадцятьма піками C SSNMR при хімічних зсувах, вибраних з 172,6 чнм, 147,1 чнм, 144,1 чнм, 132,9 чнм, 129,6 чнм, 125,9 чнм, 121,2 чнм, 119,5 чнм, 117,7 чнм, 114,6 чнм, 110,2 чнм, 45,1 чнм, 42,4 чнм, 32,6 чнм, 28,3 чнм та 24,4 чнм. В одному варіанті кристалічна 13 форма характеризується піками C SSNMR при хімічних зсувах 172,6 чнм, 147,1 чнм, 144,1 чнм, 17 UA 110807 C2 132,9 чнм, 129,6 чнм, 125,9 чнм, 121,2 чнм, 119,5 чнм, 117,7 чнм, 114,6 чнм, 110,2 чнм, 45,1 чнм, 42,4 чнм, 32,6 чнм, 28,3 чнм та 24,4 чнм. Таблиця 4 Хімічні зсуви 13 С ЯМР на Фіг. 6 Пік 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 5 10 15 20 25 30 35 Хімічний зсув (чнм) 172.6 148.7 147.1 144.1 132.9 129.6 125.9 121.2 119.5 117.7 114.6 110.2 55.0 45.1 42.4 32.6 28.3 24.4 В деяких варіантах кристалічна форма характеризується ендотермічним переходом, що має початок приблизно при 235,5±0,5 °C на графіку DSC. В деяких варіантах кристалічна форма характеризується графіком DSC, показаним на Фіг. 7. Графік ілюструє тепловий потік як функцію температури зразка, що містить Форму ІІ. DSC здійснювали на зразку зі швидкістю сканування 10 °C/хвилину. В деяких варіантах кристалічна форма характеризується графіком термічного гравіметричного аналізу (далі "TGA"), показаним на Фіг. 8. Графік ілюструє відсоток втрати маси зразка як функцію температури зі швидкістю зміни температури 10 °C/хвилину. Графік ілюструє втрату маси приблизно 0,1 % при зміні температури зразка від кімнатної температури до 150 °C, що вказує, що Форма ІІ є безводною. Інші варіанти винаходу стосуються індивідуальної кристалічної форми сполуки формули (ІІ), яка характеризується комбінацією вищевказаних характеристик будь-якої з описаних тут індивідуальних кристалічних форм. Характеристикою може бути будь-яка комбінація однієї або декількох з XRPD, TGA, DSC та SSNMR, описаних для конкретної кристалічної форми. Наприклад, індивідуальна кристалічна форма сполука формули (ІІ) може бути охарактеризована будь-якою комбінацією 2Θ піків на рентгенограмі XRPD та/або будь-якою комбінацією піків хімічних зсувів на спектрі SSNMR, та/або будь-якою комбінацією інформації, одержаної з даних вимірів DSC, та/або змін маси зразка, одержаних методом TGA. Слід розуміти, що даний винахід включає будь-яку комбінацію аналітичних методів для характеристики кристалічної форми. Даний винахід також включає композиції, які містять будь-яку з описаних тут сполук. В деяких варіантах даний винахід забезпечує фармацевтичну композицію, яка містить будь-яку з описаних тут сполук та фармацевтично-прийнятний носій або розріджувач. В деяких варіантах даний винахід пропонує фармацевтичну композицію, що містить кристалічну сполуку Формули (ІІ) та фармацевтично-прийнятний носій або розріджувач. Деякі терміни, використовувані тут вище або нище для опису сполук за винаходом, будуть визначені тут більш детально. Терміни, не визначені тут окремо, мають ті значення, які надали б їм спеціалісти в даній галузі в світлі даного опису і контексту. Однак при використанні в описі, коли не вказується інше, наступні терміни мають вказані значення і дотримуються наступних правил. В групах, радикалах або фрагментах, визначених далі, число атомів вуглецю часто проставляється перед назвою групи, наприклад С 1-6-алкіл означає алкільну групу або радикал, що має від 1 до 6 атомів вуглецю. Загалом, для груп, що містять дві або більше підгруп, 18 UA 110807 C2 5 10 15 20 25 30 35 40 45 50 55 60 підгрупа, названа останньою, є місцем прикріплення радикала, наприклад заміщення "арил-С1-3алкіл-» означає арильну групу, зв'язану з С1-3-алкільною групою, яка є зв'язаною з ядром або групою, до якої приєднується заміщення. Загалом, місце приєднання даного залишку до іншої групи буде змінюватись, тобто будьякий доступний атом, який несе водні, що піддаються заміщенню, в межах цього залишку, може бути зв'язувальним місцем для групи, що приєднується, коли не вказується інше. Коли не вказується інше, у всьому описі і формулі винаходу, що додається, дана хімічна формула або назва будуть охоплювати всі можливі конституційні ізомери і стереоізомери, включаючи енантіомери, діастереомери, cis/trans ізомери, Е/Z ізомери і т.п., а також їх суміші, наприклад суміші 1:1 енантіомерів (які називають рацематами), суміші окремих енантіомерів в різних співвідношеннях, суміші діастереомерів або суміші будь-яких перелічених вище форм, де такі ізомери існують, а також їх солі, включаючи фармацевтично прийнятні солі, та їх сольвати, такі як гідрати, включаючи сольвати вільних сполук або сольвати якоїсь солі даної сполуки. Використовуваний тут вираз "фармацевтично прийнятний" стосується таких сполук, матеріалів, композицій та/або лікарських форм, які, в межах здорового медичного судження, є придатними для використання в контакті з тканинами людини і тварин без надмірної токсичності, подразнення, алергічної реакції або іншої проблеми або ускладнення і які відповідають розумному співвідношенню користі/ризику. Термін "заміщений", як він тут використовується, означає, що будь-який один або більше воднів на означеному атомі є заміщеним з вибором із вказаної групи, за тієї умови, що нормальна валентність означеного атому не перевищується і що це заміщення дає стабільну сполуку. Термін "частково ненасичений", як він тут використовується, означає, що в означеній групі або фрагменті є наявним один, два або більше, переважно один або два, подвійних зв'язків. Переважно, як він тут використовується, термін "частково ненасичений" не включає повністю ненасичених груп або фрагментів. Термін "галоген" означає атом, вибраний з групи, що включає F, Cl, Br і I. Термін "C1-n-алкіл", де n може приймати значення від 1 до 18, означає насичену, розгалужену або нерозгалужену вуглеводневу групу, що містить від 1 до n атомів С. Приклади таких груп включають метил, етил, n-пропил, ізопропил, бутил, ізобутил, втор-бутил, трет-бутил, n-пентил, ізопентил, неопентил, трет-пентил, n-гексил, ізогексил і т.д. Термін "C1-n-алкілен", де n є цілим числом від 1 до n, окремо або в комбінації з іншим радикалом, означає ациклічний двохвалентний алкільний радикал з прямим або розгалуженим ланцюгом, який містить від 1 до n атомів вуглецю. Наприклад, термін C1-4-алкілен включає (CH2)-, -(CH2-CH2)-, -(CH(CH3))-, -(CH2-CH2-CH2)-, -(C(CH3)2)-, -(CH(CH2CH3))-, -(CH(CH3)-CH2)-, (CH2-CH(CH3))-, -(CH2-CH2-CH2-CH2)-, -(CH2-CH2-CH(CH3))-, -(CH(CH3)-CH2-CH2)-, -(CH2-CH(CH3)CH2)-, -(CH2-C(CH3)2)-, -(C(CH3)2-CH2)-, -(CH(CH3)-CH(CH3))-, -(CH2-CH(CH2CH3))-, -(CH(CH2CH3)CH2)-, -(CH(CH2CH2CH3))-, -(CHCH(CH3)2)- і -C(CH3)(CH2CH3)-. Термін "C2-n-алкілен", де n приймає значення від 3 до 10, означає розгалужену або нерозгалужену вуглеводневу групу, що містить від 2 до n атомів С і подвійний зв'язок С=С. Приклади таких груп включають етеніл, 1-пропеніл, 2-пропеніл, 1-бутеніл, 2-бутеніл, 3-бутеніл, 1-пентеніл, 2-пентеніл, 3-пентеніл, 4-пентеніл, 1-гексеніл, 2-гексеніл, 3-гексеніл, 4-гексеніл, 5гексеніл і т.д. Термін "C2-n-алкініл", де n приймає значення від 3 до 10, означає розгалужену або нерозгалужену вуглеводневу групу, що містить від 2 до n атомів С і потрійний зв'язок С≡С. Приклади таких груп включають етиніл, 1-пропиніл, 2-пропиніл, 1-бутиніл, 2-бутиніл, 3-бутиніл, 1-пентиніл, 2-пентиніл, 3-пентиніл, 4-пентиніл, 1-гексиніл, 2-гексиніл, 3-гексиніл, 4-гексиніл, 5гексиніл і т.д. Коли не вказується інше, алкінільні групи з'єднуються з рештою молекули через атом С в позиції 1. Відповідно, такі терміни, як 1-пропиніл, 2-пропиніл, 1-бутиніл і т.д., є еквівалентними термінам 1-пропин-1-іл, 2-пропин-1-іл, 1-бутин-1-іл і т.д. Це аналогічним чином стосується також C2-n-алкенільних груп. Термін "C1-n-алкокси" означає групу C1-n-алкіл-O, в якій C1-n-алкіл є таким, як було визначено раніше. Приклади таких груп включають метокси, етокси, n-пропокси, ізопропокси, n-бутокси, ізобутокси, втор-бутокси, трет-бутокси, n-пентокси, ізопентокси, неопентокси, трет-пентокси, nгексокси, ізогексокси і т.д. Термін "C1-n-алкілкарбоніл" означає групу C1-n-алкіл-C(=O), в якій C1-n-алкіл є таким, як було визначено раніше. Приклади таких груп включають метилкарбоніл, етилкарбоніл, nпропилкарбоніл, ізопропилкарбоніл, n-бутилкарбоніл, ізобутилкарбоніл, втор-бутилкарбоніл, трет-бутилкарбоніл, n-пентилкарбоніл, ізопентилкарбоніл, неопентилкарбоніл, третпентилкарбоніл, n-гексилкарбоніл, ізогексилкарбоніл і т.д. 19 UA 110807 C2 5 10 15 20 25 30 35 40 45 50 55 60 Термін "C3-n-циклоалкіл" означає насичену моно-, бі-, три- або спірокарбоциклічну групу, що містить від 3 до n атомів С. Приклади таких груп включають циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклононіл, циклододецил, біцикло[3.2.1]октил, спіро[4.5]децил, норпиніл, норбоніл, норкарил, адамантил і т.д. Переважно, термін "C3-7-циклоалкіл" означає насичені моноциклічні групи. Термін "C5-n-циклоалкеніл" означає C5-n-циклоалкільну групу, як її було визначено раніше, і додатково має принаймні один подвійний зв'язок С=С. Термін "C3-n-циклоалкілкарбоніл" означає групу C3-n-циклоалкіл-C(=O), де C3-n-циклоалкіл є таким, як його було визначено раніше. Термін "C3-n-гетероциклоалкіл" означає насичену моно-, бі-, три- або спірокарбоциклічну групу, як її було визначено раніше, з від 3-m до n-m атомів С, де m атомів вуглецю є N заміщеними на m гетероатомів, незалежно вибраних з N, NR , O, S, SO і SO2. Приклади таких груп включають азирідиніл, оксираніл, азетидиніл, оксетаніл, піролідиніл, тетрагідрофураніл, тетрагідротіофеніл, піперидиніл, тетрагідропіраніл, тетрагідротіопіраніл, піперазиніл, морфолініл, 1,3-діоксаніл, 1,4-діоксаніл, тіоморфолініл, азепаніл, оксепаніл, тієпаніл, 1-азабіцикло[2.2.2]октан, 1,4-діаза-біцикло[2.2.2]октан і т.д. Переважно, термін "гетероциклоалкіл" означає насичені моноциклічні C5-6-циклоалкільні групи, в яких один або два атоми вуглецю є заміщеними на N та/або О. Термін "три-(C1-4-алкіл)силіл" означає силільні групи, які мають ідентичні або дві або три різні алкільні групи. Термін "ди-(C1-3-алкіл)аміно" означає аміногрупи з двома однаковими або різними алкільними групами. Коли групи або залишки є необов'язково заміщеними, це стосується будь-якої форми групи або залишку. Наприклад, коли алкільна група є необов'язково моно- або поліфторованою, це включає також алкільні залишки, що є частиною більших груп, наприклад алкілокси, алкілкарбоніл, алкоксиалкіл і т.д., або коли (гетеро)арильна група є необов'язково моно- або полізаміщеною певним заміщенням або набором заміщень, це також включає (гетеро)арильні групи, що є частиною більших груп, наприклад (гетеро)арил-C1-n-алкіл, (гетеро)арилокси, (гетеро)арилокси-C1-n-алкіл, (гетеро)арил-C1-n-алкілокси і т.д. 2 5 Відповідно, у випадках, коли, наприклад, R або R має значення, скажімо (гетеро)арилокси, тоді як (гетеро)арильні залишки є необов'язково моно- або поліфторованими, і (гетеро)арил означає, між іншим, феніл, значення моно-, ди-, три-, тетра- і пентафторфенокси також є включеними. Те ж саме стосується груп або залишків, в яких частина групи або залишку N заміщена іншою групою, наприклад група СН2 є необов'язково заміщеною на O, S, NR , CO або SO2. Наприклад, коли залишок має, зокрема, значення гідрокси-C1-3-алкіл, де група CH2 є необов'язково заміщеною на СО (=карбоніл), то це включає також карбокси, карбоксиметил, гідроксиметилкарбоніл, 1-гідрокси-2-оксо-етил, карбоксиетил, 2-карбоксиетил, 1-карбоксиетил, гідроксиметил-карбонілметил, 1-гідрокси-2-оксо-пропил, гідроксиетилкарбоніл, (2-гідроксиетил)карбоніл, гідрокси-3-оксо-пропил, 1-гідрокси-3-оксо-пропил, 2-гідрокси-3-оксо-пропил, (1гідроксиетил)-карбоніл, 2-гідрокси-1-оксо-проп-2-ил, гідрокси-2-оксо-проп-2-ил і 3-гідрокси-1оксо-проп-2-ил. Аналогічно, таке визначення, як C1-n-алкіл, де одна або більше груп СН2 є необов'язково заміщеними, наприклад карбонілом, і який є необов'язково заміщеним, наприклад гідрокси або аміно, включає також конкретні залишки, що не мають групи СН та/або СН2, наприклад карбокси і амінокарбоніл. Всі атоми/елементи, описані тут, включаючи атоми, які є частиною групи, включають всі стабільні ізотопні форми відповідного елемента. Наприклад, коли б не згадувався водень, окремо або як частина групи, такої як метил, це включає водень і дейтерій як стабільні ізотопні форми елемента водень. Сполуки за цим винаходом можуть бути одержані відомими методами синтезу. Переважно, такі сполуки одержуються методами за цим винаходом, які далі будуть описані більш докладно. На Схемі 1 показаний загальний спосіб одержання серцевинних структур сполук за цим винаходом з застосуванням трициклічного піридину в якості попередника для каркасу 2 3 4 трициклічного піридину; R , R , R і m мають значення, як їх було визначено раніше і буде визначено пізніше. Трициклічний піридин можна одержати з 2-інданонів (m=0) або 2-тетралонів (m=1) і пропаргіламіну або його похідного шляхом з'єднання цих двох вихідних сполук в присутності каталізатора, такого як солі або комплекси золота і міді, переважно NaAuCl4 і CuCl2 (дивись J. Org. Chem. 2003, 68, 6959-6966). Цю реакцію звичайно проводять в спиртах, таких як етанол, при температурі від 20 до 120ºС при звичайному нагріванні або нагріванні мікрохвильовим випромінюванням. Одержану структуру піридину перетворюють на похідне піперидину шляхом відновлення воднем в присутності каталізатора на основі перехідного 20 UA 110807 C2 5 10 15 20 25 30 35 40 45 металу, такого як PtO2, Pt/C, Pd/C, Rh/C, ренеєвський Ni або їх суміші. До числа розчинників, яким віддають перевагу, входять спирти, наприклад метанол і етанол, етилацетат, оцтова кислота, вода, ефір, тетрагідрофуран, 1,4-діоксан, N, N-диметилформамід, N, Nдиметилацетамід, N-метилпіролідинон, гексани, метилциклогексан або їх суміші, які необов'язково використовуються в комбінації з добавками, такими як кислота, наприклад трифтороцтова кислота, соляна кислота і сірчана кислота, при температурі від 10 до 150ºС, переважно від 20 до 80ºС, і тиску водню від 1 до 150 бар, переважно від 1 до 20 бар. Як варіант, відновлення можна здійснювати після перетворення піридину на іон піридинію шляхом Nалкілування, N-ацилування або N-сульфонілування з застосуванням обробки джерелом гідриду, таким як NaBH4 або LiAlH4. Останній реагент краще застосовувати у вуглеводнях, ефірі, тетрагідрофурані, 1,4-діоксані, бензолі або толуолі, тоді як перший краще застосовувати в спиртах, наприклад метанолі або етанолі, і воді, необов'язково в комбінації з ко-розчинником, таким як тетрагідрофуран, 1,4-діоксан або N-метилпіролідинон, а також з добавкою, такою як кислота, наприклад оцтова кислота, або основа, наприклад гідроксид натрію. Схема 1. Стратегія 1 створення трициклічного каркасу Другий реальний спосіб синтезу, альтернативний способу синтезу попередника 2 3 4 трициклічного піридину, описаному на Схемі 1, показано на Схемі 2; R , R , R і m є такими, як було тут визначено раніше і буде визначено пізніше. Зшивання металічного похідного фенілметилу (для m=0) або фенетилу (для m=1) в присутності каталізатора на основі перехідного металу з 2,3-дигалогенідом або псевдогалогенідом піридину забезпечує одержання необхідного проміжного продукту. Придатними металічними залишками в металічному похідному фенілметилу можуть бути, наприклад, MgCl, MgBr, B(OH) 2, B(OCMe2CMe2O), BF3K, ZnCl, ZnBr або ZnI, а придатним галогенідом або псевдогалогенідом при піридині переважно є Cl, Br, I, F3CSO3, p-TolSO3 і MeSO3. В залежності від партнерів по зшиванню можуть використовуватись різні каталізатори, головним чином на основі Pd, Ni, Cu або Fe. Pd(PPh 3)4, Pd[1,1’-біс(дифенілфосфіно)фероцен)]Cl2, Pd(PPh3)2Cl2, Ni(PPh3)2Cl2 або Pd на C, наночастки Pd або Fe, Pd(II), Ni(II), Fe(II) або солі Fe(III), такі як Pd(O 2CCH3)2, PdCl2, NiCl2 або FeCl3, необов'язково в комбінації з 2-(необов'язково заміщений феніл)феніл-дициклогексилом або дитрет-бутилфосфіном, трифенілфосфіном, тритолілфосфіном, трифурил-фосфіном, три-третбутил-фосфіном, трициклогексилфосфіном, при цьому сіль 1,3-диарил-імідазолідинію або сіль 1,3-диарил-дигідроімідазолідинію є деякими з найчастіше застосовуваних каталізаторів. Зшивання краще проводити в толуолі, тетрагідрофурані, 1,4-діоксані, 1,2-диметоксиетані, N, Nдиметилформаміді, N, N-диметилацетаміді, N-метилпіролідиноні або в їх сумішах, які в залежності від партнерів по зшиванню, необов'язково комбінуються зі спиртом, наприклад метанолом, водою, солями лужних металів, такими як LiCl, NaOH, Na 2CO3, K2CO3, Cs2CO3, NaO2CCH3 або K3PO4, солями амонію, наприклад Bu4NCl, або солями срібла, наприклад AgO3SCF3, при температурі від -10 до 150ºС. Наступну циклізацію бензил- або фенетилпіридину для одержання трициклічної структури піридину можна проводити з використанням іншої реакції в присутності каталізатора на основі перехідного металу, переважно Pd, наприклад на основі Pd(O2CC3)2 або Pd(O2CCMe3)2, і фосфінового ліганду, такого як, наприклад, ди-трет-бутилметил-фосфін, трициклогексилфосфін, трифеніл-фосфін, три(4-фторфеніл)фосфін або 2-(2диметиламінофеніл)феніл-дифеніл-фосфін. Найкраще проводити циклізацію в присутності солі калію, наприклад K2CO3 або KO2CCH3, необов'язково в комбінації з сіллю срібла, наприклад Ag2CO3 або AgO3SCF3, та/або півалевою кислотою в N, N-диметилацетаміді при температурі від 40 до 160 °C (дивись, наприклад, Tetrahedron 2008, 64, 6015-20 і наведені там посилання). Схема 2. Стратегія 2 створення трициклічного каркасу 50 21 UA 110807 C2 5 10 15 20 25 30 35 40 На Схемі 3 показана стратегія одержання попередника трициклічного піридину, 2 3 4 альтернативна описаній на Схемі 1; R , R , R і m є такими, як було тут визначено раніше і буде визначено пізніше. Зшивання металічного похідного фенілу, при цьому металом є, наприклад, MgCl, MgBr, B(OH)2, B(OCMe2CMe2O), BF3K, ZnCl, ZnBr або ZnI, в присутності каталізатора на основі перехідного металу, з похідним піридин-2-карбонової кислоти або похідним заміщеної 3галогенідом або псевдогалогенідом піридин-2-карбонової кислоти (m=0) або похідним пірид-2илоцтової кислоти (m=1), де похідним карбонової кислоти переважно є карбонова кислота, складний ефір карбонової кислоти або карбонітрил, забезпечує одержання першого проміжного продукту. В залежності від партнерів по зшиванню, можуть застосовуватись різні каталізатори, переважно на основі Pd, наприклад Pd(PPh3)4, Pd[1,1’-біс(дифенілфосфіно)фероцен]Cl2, Pd(PPh3)2Cl2, Pd на C, наночасток Pd, солей Pd(II), таких як Pd(O 2CCH3)2 або PdCl2, необов'язково в комбінації з 2-(необов'язково заміщений феніл)феніл-дициклогексилом або дитрет-бутил-фосфіном, трифенілфосфіном, тритолілфосфіном, трифурилфосфіном, три-третбутил-фосфіном, трициклогексилфосфіном, сіллю 1,3-диарил-імідазолідинію або сіллю 1,3диарил-дигідроімідазолідинію, необов'язково в присутності солей лужних металів, таких як LiCl, t t NaOH, NaO Bu, KO Bu, Na2CO3, K2CO3, Cs2CO3, NaO2CCH3 або K3PO4, солей амонію, наприклад Bu4NCl, та/або солей срібла, наприклад AgO3SCF3, переважно застосовуваних в толуолі, тетрагідрофурані, 1,4-діоксані, N, N-диметилформаміді, N, N-диметилацетаміді, Nметилпіролідиноні або їх сумішах, необов'язково в комбінації з водою, при температурі від -10 до 150 °C. Наступне внутрішньомолекулярне ацилування за Фріделем-Крафтсом забезпечує одержання трициклічного піридинового каркасу шляхом активації функціональності карбокси, наприклад карбонової кислоти, ангідриду, змішаного ангідриду або ефіру, карбонілхлориду або нітрилу, з кислотою Льюїса, в залежності від типу групи карбокси і електронної природи бензольної підструктури, наприклад бромисто-водневої кислоти, соляної кислоти, сірчаної кислоти, фосфорної кислоти, трифтороцтової кислоти, метансульфонової кислоти, толуолсульфонової кислоти, трифторметансульфонової кислоти, SnCl 4, FeCl3, AlBr3, AlCl3, SbCl5, BCl3, BF3, ZnCl2, монтморилонітів, POCl3 і PCl5, переважно в інертному розчиннику, наприклад ацетонітрилі, дихлорметані, 1,2-дихлорметані, 1,4-діоксані, 1,2-диметоксиетані, вуглеводнях, нітробензолі або хлорбензолі при температурі від 0 до 180 °C. Відновлення одержаної у такий спосіб кетогрупи краще здійснювати воднем в присутності каталізатора на основі перехідного металу, наприклад Pd/C, Pd(OH)2, PtO2, Pt/C або Rh/C, в спирті, наприклад метанолі, гліколі або етанолі, воді, оцтовій кислоті, етилацетаті, N-метилпіролідиноні, тетрагідрофурані, 1,4-діоксані, ефірі або їх сумішах, необов'язково в присутності кислоти, наприклад соляної кислоти, при температурі від 0 до 180 °C, переважно від 20 до 120 °C, і тиску водню від 1 до 100 бар, переважно від 1 до 10 бар. Як варіант, відновлення кетогрупи може здійснюватись за допомогою гідриду, наприклад триетилсилану, борану, борогідриду натрію або гідриду літію-алюмінію, необов'язково в присутності кислоти Льюїса, например BF 3, AlCl3, InCl3, SnCl4, FeCl3, ZnCl2, оцтової кислоти, трифтороцтової кислоти, соляної кислоти, метансульфонової кислоти або трифторметансульфонової кислоти при температурі від 0 до 140 °C. Схема 3. Стратегія 3 створення трициклічного каркасу 22 UA 110807 C2 5 10 15 20 25 На Схемі 4 показана стратегія, придатна для одержання каркасу сполук за цим винаходом, 2 3 4 де m дорівнює 0; R , R і R мають такі значення, які були визначені тут раніше і будуть визначені пізніше. Структура феніл-піридил збирається шляхом катализованого перехідним металом зшивання, як показано на Схемі 3. Для цієї мети було застосовано нуклеофільну фенільну групу, що несе М, і електрофільну піридинову групу, що несе Y, хоча можуть застосововуватись ароматичні будівельні блоки протилежної реактивності, тобто феніл несе Y, а піридин несе М, забезпечуючи такий самий продукт зшивання. Одержана сполука несе дві потенційні заміщувані групи, переважно фтор, хлор, бром, арилсульфонат, нітро або арилсульфоніл, по одній на кожному (гетеро)ароматичному кільці, суміжному зі зв'язком фенілпіридил. Дианіонний метиленовий синтон, наприклад малонова кислота, складний малоновий диефір, малодинітрил, ціанооцтова кислота або ціанооцтовий складний ефір, в комбінації з t i основою, наприклад Cs 2CO3, K2CO3, Na2CO3, KO Bu, NaOEt, NaOMe, NEt3, Pr2NEt, 1,8диазабіцикло[5.4.0]-ундек-7-ен, послідовно замінює обидві заміщувані групи ароматичними нуклеофільними заміщеннями з утворенням інденопіридинового каркасу. Кращими розчинниками для цього перетворення, яке переважно проводять при температурі від 0 до 180 ºС, серед інших, є N-метилпіролідинон, N, N-диметилацетамід, N, N-диметилформамід, спирт, наприклад етанол, ізопропанол або трет-бутанол, вода, диметилсульфоксид, 1,4-діоксан, тетрагідрофуран або їх суміші. Карбоксильні електроноакцепторні групи видаляють гідролізом з використанням основи, наприклад NaOH або KOH, або кислоти, наприклад HCl або H 2SO4, у водному або спиртовому розчині з утворенням групи карбокси, яка декарбоксилюється спонтанно або при нагріванні в кислому або основному середовищі. Така обробка особливо підходить для сполук, що несуть одну або більше електроноакцепторних груп на фенільному кільці. 23 UA 110807 C2 Схема 4. Стратегія 4 створення трициклічного каркасу 5 10 15 На Схемі 5 показане складання трициклічного каркасу за цим винаходом, починаючи з 2 3 4 відповідного піролідин енаміну 2-інданонів або 2-тетралонів і акриламіду; R , R , R і m мають такі значення, які були визначені тут раніше і будуть визначені пізніше. Бажану трициклічну структуру у вигляді дигідропіридинону було одержано шляхом нагрівання обох партнерів по реакції при температурі від 60 до 150ºС. Відновлення подвійного зв'язку воднем в присутності перехідного металу, такого як паладій на вуглеці, або з джерелом гідриду, таким як триалкілсилан, наприклад триетилсилан, борогідрид, наприклад NaBH4, NaBH(O2CCH3)3 або NaH3BCN, або аланат, наприклад LiAlH4, необов'язково в присутності добавки, такої як кислота Льюїса, наприклад оцтова кислота, трифтороцтова кислота, AlCl3 або BF3*OEt2, забезпечує одержання трициклічного піперидинону. Наступне відновлення аміду переважно досягається з використанням джерела гідриду, наприклад NaBH4, в комбінації з оцтовою кислотою в 1,4діоксані, LiAlH4 в тетрагідрофурані або ефірі, або дигідробіс(2-метоксиетокси)алюмінату натрію в етиленгліколевому диметиловому ефірі при температурі від 0 до 100ºС. Схема 5. Стратегія 5 створення трициклічного каркасу 20 25 30 35 Інший загальноприйнятний підхід до одержання основних структур сполук за цим винаходом 2 3 4 базується на реакції електрофільного ароматичного заміщення (Схема 6); R , R , R і m мають такі значення, які були визначені тут раніше і будуть визначені пізніше. При цьому ароматична частина молекули реагує з позитивно зарядженим атомом вуглецю піперидинового кільця з утворенням трициклічного каркасу. Реакційно здатний проміжний продукт, що несе позитивно заряджений атом вуглецю в азациклі, можна одержати шляхом додавання кислоти Льюїса до олефінового зв'язку або карбонільної групи або активацією відповідно позиціонованої заміщуваної групи, такої як Cl, Br, I, OH, O3SCF3, O3SMe або O3S-p-Tol. Для цієї класичної реакції описана велика кількість кислот Льюїса, які також можуть використовуватись. Кілька найбільш широко застосовуваних – це бромисто-воднева кислота, йодистоводнева кислота, соляна кислота, сірчана кислота, фосфорна кислота, P4O10, трифтороцтова кислота, метансульфонова кислота, толуолсульфонова кислота, трифторметансульфонова кислота, Sc(O3SCF3)3, InCl3, InBr3, SnCl4, FeCl3, AlBr3, AlCl3, SbCl5, BCl3, BF3, ZnCl2, монтморилоніти, POCl3 і PCl5. В залежності від нахилу заміщуваної групи і електронної природи ароматичного кільця, повинні використовуватись більш або менш сильні кислотні каталізатори. Крім згаданих кислотних каталізаторів, ефективними в таких реакціях можуть бути солі срібла, наприклад AgO3SCF3, при застосуванні галогенідів в якості заміщуваних груп. Кращими розчинниками є 24 UA 110807 C2 5 вуглеводні, такі як гексан або циклогексан, хлоровані вуглеводні, такі як дихлорметан або 1,2дихлорметан, перфторовані вуглеводні, нітробензол, ацетонітрил, хлоровані бензоли, гетероароматичні сполуки, такі як хінолін, 1,2-диметоксиетан, 1,4-діоксан, ефір, іонні ліпіди, вода, оцтова кислота або їх суміші, хоча не всі з цих розчинників можуть використовуватись з усіма переліченими вище кислотами Льюїса. Ці реакції здійснюються при температурі від -10 до 220ºС, переважно від 20ºС до 180ºС. Реакції можуть проводитись також під мікрохвильовим випромінюванням. Схема 6. Стратегія 6 створення трициклічного каркасу 10 15 20 25 30 35 40 45 Представлені способи синтезу ґрунтуються на використанні захисних груп. Придатні захисні групи для відповідних функцій та їх видалення є описаними тут далі і можуть використовуватись rd аналогічно (дивись також: Protecting Groups, Philip J. Kocienski, 3 edition, Georg Thieme Verlag, Stuttgart, 2004 і наведені там посилання). Далі субститутивно підсумовується одержання кількох можливих похідних сполук загальної формули I або їх попередників, описаних вище, що несуть певні функціональні групи для складання інших сполук загальної формули I або їх попередників. Ця добірка жодним чином не претендує на повноту, а лише пропонує деякі можливості в якості прикладу. Коли в процесі за цим винаходом одержується сполука загальної формули I або її попередник, які містять аміно-, алкіламіно- або іміногрупу, то шляхом ацилування або сульфонілування їх можна перетворити на відповідну ацильну або сульфонільну сполуку загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять групу гідрокси, то шляхом ацилування або сульфонілування їх можна перетворити на відповідну ацильну або сульфонільну сполуку загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять групу гідрокси, то шляхом алкілування їх можна перетворити на відповідний ефір загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять аміно-, алкіламіно- або іміногруппу, то шляхом алкілування або відновного алкілування їх можна перетворити на відповідну алкільну сполуку загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять нітрогрупу, то шляхом відновлення їх можна перетворити на відповідну аміносполуку. Коли одержується сполука загальної формули I або її попередник, які містять іміногрупу, то шляхом нітрозування і наступного відновлення їх можна перетворити на відповідну N-аміноіміносполуку. Коли одержується сполука загальної формули I або її попередник, які містять С 1-4алкілоксикарбонільну групу, то шляхом розщеплення ефіру їх можна перетворити на відповідну карбоксисполуку. Коли одержується сполука загальної формули I або її попередник, які містять групу карбокси, то шляхом етерифікації їх можна перетворити на відповідний складний ефір загальної формули I або його попередника. Коли одержується сполука загальної формули I або її попередник, які містять групу карбокси або складноефірну групу, то шляхом реакції з аміном їх можна перетворити на відповідний амід загальної формули I або його попередника. 25 UA 110807 C2 5 10 15 20 25 30 35 40 45 50 55 Коли одержується сполука загальної формули I або її попередник, які містять ароматичну підструктуру, то шляхом реакції електрофільного заміщення їх можна дериватизувати за допомогою атому хлору, брому або йоду, або групи нітро, сульфонової кислоти, хлорсульфонільної або ацильної групи у відповідну сполуку загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять аміногрупу, приєднану до ароматичної або гетероароматичної групи, то їх можна перетворити на відповідну ціано-, фтор-, хлор-, бром-, йод-, гідрокси-, меркапто- або азидо-дериватизовану сполуку загальної формули I або її попередника шляхом диазотування аміногрупи і наступного заміщення діазогрупи на ціанід, фторид, хлорид, бромід, йодид, гідроксид, алкіл або сірководень або азид відповідно. Коли одержується сполука загальної формули I або її попередник, які містять аміногрупу, приєднану до ароматичної або гетероароматичної групи, то їх можна перетворити на відповідну арил-дериватизовану ароматичну сполуку загальної формули I або її попередника шляхом диазотування аміногрупи і наступного заміщення одержаної діазогрупи на відповідний арильний нуклеофіл, опосередкованого придатним видом перехідного металу. Коли одержується сполука загальної формули I або її попередник, які містять атом хлору, брому або йоду або групу трифторметилсульфонілокси-, мезилокси- або тозилокси-, приєднану до ароматичної або гетероароматичної групи, то їх можна перетворити на відповідну арил-, алкеніл-, алкініл- або алкіл-дериватизовану сполуку загальної формули I або її попередника шляхом заміщення відповідної групи на арил, алкеніл, алкініл або алкіл з використанням процесу, опосередкованого придатним видом перехідного металу. Коли одержується сполука загальної формули I або її попередник, які містять атом хлору, брому або йоду або групу трифторметилсульфонілокси-, мезилокси- або тозилокси-, приєднану до ароматичної або гетероароматичної групи, то можна здійснити заміщення на ціано для одержання відповідної ароматичної сполуки загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять атом хлору, брому або йоду або групу трифторметилсульфонілокси-, мезилокси- або тозилокси-, приєднану до ароматичної або гетероароматичної групи, то можна здійснити заміщення на водень для одержання відповідної ароматичної сполуки загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять два гетероатоми біля суміжних атомів вуглецю, які являються аміно і гідрокси, аміно або меркапто, то ці гетероатоми можна зв'язати через атом вуглецю групи карбокси для утворення підструктури циклічного амідину, імінового ефіру або імінотіоефіру, яка може бути частиною ароматичного кільця. Коли одержується сполука загальної формули I або її попередник, які містять ціаногрупу, то їх шляхом відновлення можна перетворити на аміноалкіл-дериватизовану сполуку загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять ціаногрупу, то їх можна перетворити на N-гідроксикарбамімідоїльну групу шляхом обробки гідроксиламіном. Коли одержується сполука загальної формули I, яка містить N-гідроксикарбамімідоїльну групу, то її можна перетворити на оксадіазол-дериватизовану сполуку загальної формули I або її попередника шляхом обробки карбоксильною або спорідненою групою. Коли одержується сполука загальної формули I або її попередник, які містять амінокарбонільну групу, то їх можна перетворити шляхом дегідрування на відповідну ціаносполуку загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять кето- або альдегідну групу, то їх можна перетворити шляхом відновлення на відповідну сполуку гідрокси загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять карбонову кислоту або амінокарбонільну групу, то їх можна перетворити шляхом реакції перегрупування на відповідну аміно-дериватизовану сполуку загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять кето- або альдегідну групу, то їх можна перетворити на алкеніл-дериватизовану сполуку загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять олефіновий подвійний С=С або потрійний C≡C зв'язок, то їх можна відновити для одержання відповідної насиченої сполуки загальної формули I або її попередника. 26 UA 110807 C2 5 10 15 20 25 30 35 40 45 50 55 60 Коли одержується сполука загальної формули I або її попередник, які містять кето- або альдегідну групу, то їх можна перетворити на відповідну третинну або вторинну сполуку гідрокси загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять групу ефіру карбонової кислоти, то їх можна перетворити на третинний спирт шляхом додавання двох еквівалентів органометалічної сполуки. Коли одержується сполука загальної формули I або її попередник, які містять первинну або вторинну групу гідрокси, то їх можна перетворити шляхом окислення на відповідну карбонільну сполуку загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять олефіновий зв'язок, то їх можна перетворити на відповідну сполуку гідрокси загальної формули I або її попередника шляхом гідроборації з наступним окисленням. Коли одержується сполука загальної формули I або її попередник, які містять олефіновий зв'язок, то їх можна перетворити шляхом дигідроксилювання на відповідну сполуку 1,2дигідрокси загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять олефіновий зв'язок, то їх можна перетворити шляхом озонолізу на відповідну карбонільну сполуку загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять олефіновий зв'язок, то їх можна перетворити на відповідну сполуку гідрокси загальної формули I або її попередника шляхом епоксидування з наступним розкриттям оксиранового кільця за допомогою джерела гідриду. Коли одержується сполука загальної формули I або її попередник, які містять олефіновий зв'язок, то їх можна перетворити шляхом Вакер-окислення на відповідну карбонільну сполуку загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять олефіновий зв'язок, то їх можна перетворити шляхом гідроціанування на відповідну ціаносполуку загальної формули I або її попередника. Коли одержується сполука загальної формули I або її попередник, які містять ціаногрупу, то їх можна перетворити шляхом додавання води на відповідну амінокарбонільну сполуку загальної формули I або її попередника. Наступна етерифікація необов'язково здійснюється в розчиннику, такому як метиленхлорид, N, N-диметилформамід, бензол, толуол, хлорбензол, тетрагідрофуран, 1,4-діоксан, або їх суміші, або найкраще у відповідному спирті, необов'язково в присутності кислоти, наприклад соляної кислоти, або агента для дегідратації, наприклад ізобутилового ефіру хлормурашиної кислоти, тіонілхлориду, триметилхлорсилану, сірчаної кислоти, метансульфокислоти, ртолуолсульфонової кислоти, трихлориду фосфору, пентоксиду фосфору, N, N'карбонілдиімідазолу, N, N'-дициклогексилкарбодиіміду, трифенілфосфіну, комбінованого з чотирихлористим вуглецем, або їх комбінацій, необов'язково в присутності 4диметиламінопіридину та/або 1-гідроксибензотриазолу. Реакції проводять при температурі від 0 до 150ºС, переважно від 0 до 80ºС. Утворення складного ефіру також може здійснюватись шляхом проведення реакції між сполукою, що містить групу карбокси, і відповідним алкілгалогенідом в присутності основи. Наступне ацилуванння або сульфонілування необов'язково проводять в розчиннику, такому як метиленхлорид, N, N-диметилформамід, бензол, толуол, хлорбензол, тетрагідрофуран, 1,4діоксан або їх суміші, з застосуванням відповідного ацильного або сульфонільного електрофіла, необов'язково в присутності третинної органічної основи, неорганічної основи або агента для дегідратації. Як правило, застосовуваними агентами для дегідратації є, наприклад, ізобутил хлорформат, тіонілхлорид, триметилхлорсилан, сірчана кислота, метансульфонова кислота, ртолуолсульфонова кислота, трихлорид фосфору, пентоксид фосфору, N, N'-дициклогексилкарбодиімід, N, N'-карбонілдиімідазол, комбінований з чотирихлористим вуглецем трифенілфосфін або їх комбінації, які можуть використовуватись в присутності 4диметиламінопіридину та/або 1-гідроксибензотриазолу при температурі від 0 до 150ºС, переважно від 0 до 80ºС. Наступне алкілування необов'язково проводять в метиленхлориді, N, N-диметилформаміді, бензолі, толуолі, хлорбензолі, тетрагідрофурані, 1,4-діоксані або їх сумішах з застосуванням агента для алкілування, такого як відповідний галогенід або складний ефір сульфонової кислоти, наприклад з застосуванням метилйодиду, етилброміду, диметилсульфату або бензилхлориду, необов'язково в присутності третинної органічної основи або неорганічної основи при температурі від 0 до 150ºС, переважно від 0 до 100ºС. 27 UA 110807 C2 5 10 15 20 25 30 35 40 45 50 55 60 Наступне відновне алкілування здійснюється з застосуванням відповідної карбонільної сполуки, такої як формальдегід, ацетальдегід, пропіоновий альдегід, ацетон або бутиральдегід, в присутності комплексного гідриду металу, такого як борогідрид натрію, борогідрид літію, триацетоксиборогідрид натрію або ціаноборогідрид натрію, звичайно при значенні рН від 6 до 7 і при кімнатній температурі, або в присутності каталізатора гідрування, наприклад за допомогою водню в присутності каталізатора на основі перехідного металу, такого як паладій-на-вугіллі, при тиску водню від 1 до 5 бар. Метилування може також здійснюватись в присутності мурашиної кислоти в якості відновника при підвищеній температурі, наприклад від 60 до 120ºС. Наступне відновлення нітрогрупи проводять, наприклад, з застосуванням водню і каталізатора, такого як паладій-на-вугіллі, диоксид платини або ренеєвський нікель, або з застосуванням інших відновлювальних агентів, таких як хлорид олова(II), залізо або цинк, необов'язково в присутності кислоти, такої як оцтова кислота. Наступне нітрозування аміногрупи з подальшим відновленням для одержання N-аміноіміносполуки проводять, наприклад, з застосуванням алкілнітриту, такого як ізоамілнітрит, з утворенням N-нітрозо-іміносполуки, яку потім відновлюють до N-аміно-іміносполуки з застосуванням, наприклад, цинку в присутності кислоти, такої як оцтова кислота. Наступне відщеплення С1-4-алкілоксикарбонільної групи для одержання карбоксигрупи проводять, наприклад, шляхом гідролізу за допомогою кислоти, такої як соляна кислота або сірчана кислота, або гідроксиду лужного металу, такого як гідроксид літію, гідроксид натрію або гідроксид калію. Трет-бутильна група переважно видаляється шляхом обробки міцною кислотою, наприклад трифтороцтовою кислотою або соляною кислотою, в інертному розчиннику, такому як дихлорметан, 1,4-діоксан або етилацетат. Наступне утворення аміду здійснюється шляхом проведення реакції між відповідним реакційноздатним похідним карбонової кислоти і відповідним аміном в розчиннику, такому як метиленхлорид, N, N-диметилформамід, бензол, толуол, хлорбензол, тетрагідрофуран, 1,4діоксан або їх суміші, або без розчинника в надлишку аміну, необов'язково в присутності неорганічної або третинної органічної основи, 4-диметиламінопіридину та/або 1-гідроксибензотриазолу при температурі від 0 до 150ºС, переважно від 0 до 80ºС. Застосування карбонової кислоти може привести до утворення бажаного аміду шляхом in situ активації функції карбокси, наприклад за допомогою ізобутилового ефіру хлормурашиної кислоти, тіонілхлориду, оксалілхлориду, триметилхлорсилану, трихлориду фосфору, пентоксиду фосфору, N, N’-карбонілдиімідазолу, суміші трифенілфосфіну з тетрахлоридом вуглецю, 2-(1Нбензотриазол-1-іл)-1,1,3,3-тетраметилуронію тетрафторборату, N, N’дициклогексилкарбодиіміду або їх комбінації. Наступне введення атому хлору, брому або йоду в ароматичну підструктуру може проводитись з застосуванням реакції ароматичної сполуки з відповідним електрофілом відповідного атому галогену. Придатними електрофілами, що містять хлор або бром, можуть бути, наприклад, N-галосукцинімід, HOCl, HOBr, трет-BuOCl, трет-BuOBr, хлор, бром, дибромізоціанурова кислота, дихлорбромат піридинію, трибромід піридинію або хлористий сульфурил, які можуть використовуватись окремо або в комбінації з кислотою, наприклад соляною кислотою, бромисто-водневою кислотою, тетрафторборною кислотою, трифліковою кислотою, сірчаною кислотою або оцтовою кислотою, або кислотою Льюїса, наприклад галогенідом заліза(III), гідратом трифтористого бору, ефіратом трифтористого бору або галогенідом алюмінію. Іншими ефективними комбінаціями можуть бути LiBr і нітрат церію ® амонію, KCl або KBr з Oxone , або KBr і перборат натрію. Придатні електрофіли, що містять йод, можна одержати з йоду і окислювача, такого як азотна кислота, сірчаний ангідрид, двоокис ® марганцю, HIO3, перекис водню, перйодат натрію, пероксидисульфати і Oxone . Іншими придатними електрофілами, що містять йод, можуть бути, наприклад, хлорид йоду, дихлорйодати і N-йодосукцинімід. Ці електрофіли, що містять йод, необов'язково застосовуються без добавок або в присутності кислоти, такої як оцтова кислота, трифтороцтова кислота або сірчана кислота, або кислота Льюїса, така як гідрат трифториду бору або солі міді. Коли має вводитись нітрогрупа, відповідними джерелами електрофіла, що містить азот, можуть бути, наприклад, азотна кислота, ацетилнітрат, нітрат церію амонію, нітрат натрію, N2O5, алкілнітрат і тетрафторборат нітронію. Деякі з цих реагентів можуть застосовуватись без добавок, хоча певні з них краще застосовувати в комбінації з кислотою, наприклад сірчаною кислотою або трифліковою кислотою, оцтовим ангідридом, трифтороцтовим ангідридом, кислотою Льюїса, наприклад трифлатом ітербію або ацетатом заліза, P 2O5, або основою. Група SO3H може вводитись шляхом проведення реакції між ароматичною сполукою і, наприклад, концентрованою сірчаною кислотою, SO3, ClSO3H або ClSO2NMe2 в комбінації з трифлатом індію. Реакція ароматичної сполуки з ClSO3H дає можливість одержати відповідне 28
ДивитисяДодаткова інформація
Автори англійськоюEckhardt, Matthias, Martin, Hans-Juergen, Schuehle, Martin, Sick, Sandra, Yang, Bing-Shiou
Автори російськоюЭкхардт Маттиас, Мартин Ханс-Юрген, Шюле Мартин, Зик Сандра, Ян Бин-Шиу
МПК / Мітки
МПК: C07D 401/06, A61P 3/00, A61K 31/435
Мітки: 4a-r,9a-s)-1-(1н-бензоімідазол-5-карбоніл)-2,3,4,4а,9,9а-гексагідро-1н-індено[2,1-b]піридин-6-карбонітрилу, інгібіторів, форми, застосування, кристалічні, гідрохлориду
Код посилання
<a href="https://ua.patents.su/128-110807-kristalichni-formi-gidrokhloridu-4a-r9a-s-1-1n-benzoimidazol-5-karbonil-2344a99a-geksagidro-1n-indeno21-bpiridin-6-karbonitrilu-ta-kh-zastosuvannya-yak-ingibitoriv-hsd-1.html" target="_blank" rel="follow" title="База патентів України">Кристалічні форми гідрохлориду (4a-r,9a-s)-1-(1н-бензоімідазол-5-карбоніл)-2,3,4,4а,9,9а-гексагідро-1н-індено[2,1-b]піридин-6-карбонітрилу та їх застосування як інгібіторів hsd 1</a>
Попередній патент: Мікобактеріальна антигенна композиція
Наступний патент: Спосіб розташування робочих циліндрів на шліфувальній машині та машина для здійснення способу
Випадковий патент: Спосіб виготовлення виробів високої щільності