Похідні етинілу як модулятори активності рецептора mglur5
Номер патенту: 114529
Опубліковано: 26.06.2017
Автори: Річчі Антоніо, Рюхер Даніель, Ліндеманн Лотар, Віейра Ерік, Штадлєр Хайнц, Єшкє Гєорг
Формула / Реферат
1. Сполука формули І
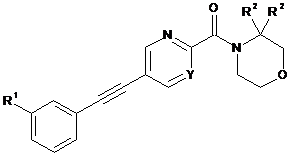 , І
, І
де
Υ позначає N або СН;
R1 позначає фтор- або хлор-;
R2 позначає водень або метил;
або її фармацевтично прийнятна кислотно-адитивна сіль.
2. Сполука формули І за п. 1, де Υ позначає N.
3. Сполука формули І за п. 2, яка є (3,3-диметилморфолін-4-іл)-[5-(3-хлорфенілетиніл)-піримідин-2-іл]-метаноном.
4. Сполука формули І за п. 1, де Υ позначає СН.
5. Сполука формули І за п. 4, яка є
(3,3-диметилморфолін-4-іл)-[5-(3-фторфенілетиніл)-піридин-2-іл]-метаноном [5-(3-хлорфенілетиніл)-піридин-2-іл]-морфолін-4-іл-метаноном або (3,3-диметилморфолін-4-іл)-[5-(3-хлорфенілетиніл)-піридин-2-іл]-метаноном.
6. Сполука за будь-яким з пп. 1-5 для застосування як терапевтично активної речовини.
7. Спосіб одержання сполуки формули І, як описано в п. 1, який включає варіант, за яким в реакцію вводять сполуку формули
 , 3
, 3
із сполукою формули
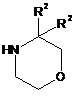 , 4
, 4
з утворенням сполуки формули
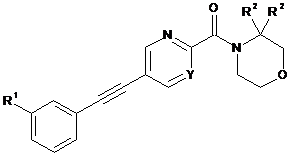 , І
, І
де замісники описані в п. 1.
8. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-5 і терапевтично активний носій.
9. Застосування сполуки за будь-яким з пп. 1-5 для лікування тривожності і болю, депресії, синдрому Мартіна-Белл, розладів аутичного спектра, хвороби Паркінсона і гастроезофагального рефлюксу (GERD).
10. Застосування сполуки за будь-яким з пп. 1-5 для виготовлення лікарського засобу для лікування тривожності і болю, депресії, синдрому Мартіна-Белл, розладів аутичного спектра, хвороби Паркінсона і гастроезофагального рефлюксу (GERD).
11. Сполука за будь-яким з пп. 1-5 для лікування тривожності і болю, депресії, синдрому Мартіна-Белл, розладів аутичного спектра, хвороби Паркінсона і гастроезофагального рефлюксу (GERD).
12. Спосіб лікування тривожності і болю, депресії, синдрому Мартіна-Белл, розладів аутичного спектра, хвороби Паркінсона і гастроезофагального рефлюксу (GERD), який включає введення ефективної кількості сполуки, як визначено за будь-яким з пп. 1-5.
Текст
Реферат: O N 2 R 2 N Y R R O 1 ,І 1 Даний винахід належить до похідних етинілу формули (І), де Υ позначає N або СН, R позначає 2 фтор- або хлор-, R позначає водень або метил, або до їх фармацевтично прийнятної кислотноадитивної солі. Тепер несподівано виявили, що сполуки загальної формули І є антагоністами метаботропного рецептора глутамату (негативні алостеричні модулятори) для застосування в UA 114529 C2 (12) UA 114529 C2 лікуванні тривожності і болю, депресії, синдрому Мартіна-Белл, розладів аутичного спектра, хвороби Паркінсона і гастроезофагального рефлюксу (GERD). UA 114529 C2 Даний винахід відноситься до похідних етинілу формули I: O R2 R2 N N Y O 1 R 5 10 15 20 25 30 35 40 45 50 I, де Y позначає N або СН; 1 R позначає фтор- або хлор-; 2 R позначає водень або метил; або до їх фармацевтично прийнятної кислотно-адитивної солі, до рацемічної суміші або до її відповідного енантіомера, та/або оптичного ізомеру, та/або стереоізомеру. Тепер несподівано виявили, що сполуки загальної формули I є антагоністами метаботропного рецептора глутамату (NAM - негативні алостеричні модулятори). Сполуки формули I відрізняються наявністю цінних терапевтичних властивостей. Їх можна використовувати в лікуванні або попередженні розладів, опосередкованих рецептором mGluR5 (метаботропний рецептор глутамату 5). У центральній нервовій системі (ЦНС) передача стимулів відбувається за допомогою взаємодії нейромедіатора, який випускається нейроном, з нейрорецептором. Глутамат є важливим збудливим нейромедіатором в мозку і відіграє унікальну роль в безлічі функцій центральної нервової системи (ЦНС). Рецептори стимулів, залежні від глутамату, ділять на дві головні групи. Перша головна група, а саме іонотропні рецептори, формує контрольовані лігандом іонні канали. Метаботропні рецептори глутамату (mGluR) належать до другої головної групи і, крім того, належать до сімейства рецепторів, пов'язаних з G-білком. В даний час відомо вісім різних членів даних mGluR, і деякі з них навіть мають підтипи. Згідно гомології їх послідовностей, механізмам трансдукції сигналу і селективності відносно агоністів ці вісім рецепторів можна підрозділяти на три підгрупи: mGluR1 і mGluR5 належать до групи I, mGluR2 і mGluR3 належать до групи II, і mGluR4, mGluR6, mGluR7 і mGluR8 належать до групи III. Негативні алостеричні модулятори метаботропних рецепторів глутамату, що належать до першої групи, можна використовувати для лікування або попередження гострих та/або хронічних неврологічних розладів, таких як хвороба Паркінсона, синдром Мартіна-Белл, аутистичні розлади, когнітивні розлади і порушення пам'яті, а також хронічного і гострого болю і гастроезофагального рефлюксу (GERD). Інші свідчення, що піддаються лікуванню, у зв'язку з цим є обмеженою функцією мозку, викликаною операціями шунтування або трансплантами, поганою подачею крові в мозок, травмами спинного мозку, травмами голови, гіпоксією, викликаною вагітністю, зупинкою серця і гіпоглікемією. Інші свідчення, що піддаються лікуванню, є ішемією, хореєю Гентінгтона, бічним аміотрофічним склерозом (ALS), деменцією, викликаною СНІД (синдром набутого імунодефіциту), травми ока, ретинопатію, ідіопатичний паркінсонізм або паркінсонізм, викликаний лікарськими засобами, а також стани, які приводять до функцій глутаматної недостатності, такі як, наприклад, м'язові спазми, конвульсії, мігрень, нетримання сечі, нікотинова залежність, опіатна залежність, тривожність, блювота, дискінезія і депресії. Розладами, повністю або частково опосередкованими mGluR5, є, наприклад, гострі, травматичні і хронічні дегенеративні процеси нервової системи, такі як хвороба Альцгеймера, старече недоумство, хвороба Паркінсона, хорея Гентінгтона, бічний аміотрофічний склероз і розсіяний склероз, психіатричні розлади, такі як шизофренія і тривожність, депресія, біль і залежність від лікарських засобів (Expert Opin. Ther. Patents (2002), 12 (12)). Селективні антагоністи mGluR5 є особливо корисними для лікування розладів, коли бажаним є зменшення активації рецептора mGluR5, таких як тривожність і біль, депресія, синдром Мартіна-Белл, розлади аутичного спектру, хвороба Паркінсона і гастроезофагальний рефлюкс (GERD). Цілями даного винаходу є сполуки формули I та їх фармацевтично прийнятні солі, вищезазначені сполуки як фармацевтично активні речовини та їх одержання. Іншими цілями даного винаходу є лікарські засоби на основі сполуки згідно винаходу та їх виготовлення, а також застосування даних сполук в контролі або попередженні розладів, опосередкованих 1 UA 114529 C2 5 10 15 20 25 30 35 40 45 50 55 60 рецептором mGluR5 (NAM), які є тривожністю і болем, депресією, синдромом Мартіна-Белл, розладами аутичного спектру, хворобою Паркінсона і гастроезофагальним рефлюксом (GERD), і, відповідно, одержанням відповідних лікарських засобів. Одним втіленням даного винаходу є сполуки формули I, де Y позначає N. Дані сполуки є: (3,3-диметил-морфолін-4-іл)-[5-(3-хлор-фенілетиніл)-піримідин-2-іл]-метанон. Одним іншим втіленням даного винаходу є сполуки формули I, де Y позначає СН. Дані сполуки є: (3,3-диметил-морфолін-4-іл)-[5-(3-фтор-фенілетиніл)-піридин-2-іл]-метанон [5-(3-хлор-фенілетиніл)-піридин-2-іл]-морфолін-4-іл-метанон або (3,3-диметил-морфолін-4-іл)-[5-(3-хлор-фенілетиніл)-піридин-2-іл]-метанон. Конкретне втілення даного винаходу складається з наступних сполук: (3,3-диметил-морфолін-4-іл)-[5-(3-хлор-фенілетиніл)-піримідин-2-іл]-метанон (3,3-диметил-морфолін-4-іл)-[5-(3-фтор-фенілетиніл)-піридин-2-іл]-метанон [5-(3-хлор-фенілетиніл)-піридин-2-іл]-морфолін-4-іл-метанон або (3,3-диметил-морфолін-4-іл)-[5-(3-хлор-фенілетиніл)-піридин-2-іл]-метанон. Сполуки, які є аналогічними сполукам за даним винаходом, загалом, були описані як позитивні алостеричні модулятори рецептора mGluR5. Несподівано виявили, що замість позитивних алостеричних модуляторів mGluR5 були одержані високоефективні антагоністи mGluR5, які мають повністю протилежну фармакологію в порівнянні з позитивними алостеричними модуляторами. Головна відмінність між позитивними і негативними алостеричними модуляторами можна побачити на Фіг. 1. Позитивний алостеричний модулятор mGluR5 (PAM) приводить до 2+ підвищеної активності рецептора (мобілізація Са ) у присутності фіксованої концентрації глутамату, тоді як алостеричний антагоніст (негативний алостеричний модулятор, NAM) приводить до зменшення активації рецептора. На Фіг. 1 показана загальна поведінка NAM і РАМ -7 за тих же самих умов. Афінність відносно рецептора на Фіг. 1 складає приблизно 10 М для -7 -8 РАМ і від 10 М до 10 М для NAM. Дані значення також можна вимірювати з використанням аналізу зв'язування з витісненням радіоактивного ліганда (МРЕР), див. опис аналізу. Фіг. 1: порівняння позитивного алостеричного модулятора (РАМ) mGluR5 і антагоніста mGluR5 (негативний алостеричний модулятор - NAM). Свідчення, на які можуть бути направлені дані сполуки, є не однаковими: NAM mGluR5 є корисними для свідчень, коли бажаним є зменшення надмірної активності рецептора, таких як тривожність і біль, депресія, синдром Мартіна-Белл, розлади аутичного спектру, хвороба Паркінсона і гастроезофагальний рефлюкс (GERD). РАМ mGluR5, з іншого боку, є корисними при свідченнях, коли бажаною є нормалізація зниженої активності рецептора, таких як психоз, епілепсія, шизофренія, хвороба Альцгеймера і асоційовані когнітивні розлади, а також склероз туберози. Дана відмінність може бути продемонстрована на практиці, наприклад, в тваринній моделі тривожності, як, наприклад, в «конфліктному тесті Фогеля пиття у щурів», коли сполуки за винаходом демонструють анксіолітичну активність, тоді як РАМ mGluR не демонструють активність в даній тваринній моделі. Біологічні аналізи і дані: 2+ Аналіз внутріклітинної мобілізації Са Була одержана моноклональна лінія клітин НЕК-293 (клітини ембріональної нирки людини), стабільно трансфікована кДНК, що кодує людський рецептор mGLu5; для роботи з позитивними алостеричними модуляторами (РАМ) mGLu5 була відібрана лінія клітин з низькими рівнями експресії рецептора і низькою конститутивною активністю рецептора для забезпечення розрізнення агоністичної активності в порівнянні з активністю РАМ. Клітини культивували згідно стандартним протоколам (Freshney, 2000) в середовищі Ігла, модифікованою за Дульбекко, з високою концентрацією глюкози, доповненої 1 мМ глутаміном, 10% (об./об.) інактивованою нагріванням сироваткою телят корів, пеніциліном/стрептоміцином, 50 мкг/мл гігроміцину і 15 мкг/мл бластицидину (всі реактиви для культури клітин і антибіотики - від Invitrogen, Базель, Швейцарія). Приблизно за 24 г до експерименту 5х104 клітин/лунку висівали на покриті полі-D-лізином 96-лункові планшети з чорним/прозорим дном. Клітини завантажували 2,5 мкМ Fluo-4AM в завантажувальному буфері (1хHBSS (збалансований сольовий розчин Хенкса), 20 мМ HEPES) протягом 1 г при 37°С і п'ять разів промивали завантажувальним буфером. Клітини переносили в Functional Drug Screening System 7000 (Hamamatsu, Париж, Франція) і додавали 11 напівлогарифмічних серійних розведень досвідченої сполуки при 37°С, і клітини інкубували 2 UA 114529 C2 5 10 15 20 25 протягом 10-30 хвилин із записом флуоресценції онлайн. Після даної стадії предінкубації до клітин додавали агоніст - L-глутамат в концентрації, відповідною ЕС20 (ефективна концентрація, що дає 20% від максимального ефекту) (типово близько 80 мкМ), із записом флуоресценції онлайн; для того, щоб врахувати варіації в чутливості клітин від доби до доби, ЕС 20 глутамату визначали негайно перед кожним експериментом шляхом запису всієї кривої відповіді на глутамат залежно від дози. Відповіді вимірювали як пікове збільшення флуоресценції мінус початковий рівень (тобто флуоресценція без додавання L-глутамату) при нормуванні за максимальним стимулюючим ефектом, одержаним з насичуючими концентраціями L-глутамату. Графіки будували з вказівкою % максимального стимулюючого ефекту, використовуючи XLift, програму для апроксимації кривих, яка ітераційно відкладає на графіці дані з використанням алгоритму ЛьовенбюргаМарквардта. Використовуваним рівнянням конкурентного аналізу в одному сайті було y = A + ((B-A)/(1+((x/C)D))), де у позначає % від максимального стимулюючого ефекту, А позначає мінімальний у, В позначає максимальний у, С позначає ЕС50, х позначає log10 концентрації конкуруючої сполуки, і D позначає нахил кривої (коефіцієнт Хілла). З даних кривих розраховували ЕС50 (концентрація, при якій досягається напівмаксимальна стимуляція), коефіцієнт Хілла, а також максимальна відповідь в % від максимальної стимулюючої відповіді, одержаної з насичуючими концентраціями L-глутамату. Позитивні сигнали, одержані під час предінкубації з досліджуваними сполуками, що є РАМ (тобто до застосування ЕС20 концентрації L-глутамату), указували на агоністичну активність, відсутність таких сигналів демонструвала недолік агоністичних актівностей. Падіння сигналу, спостережуване після додавання ЕС20 концентрації L-глутамату, указувало на інгібуючу активність досліджуваної сполуки. У наведеному нижче списку прикладів показані відповідні результати для сполук, які всі мають значення ЕС50, менші або рівні 100 нМ. PAM mGlu5 EC50 [нM] Приклад Ефективність [%] Еталонна сполука 1 O N 57 N O 46 F Еталонна сполука 2 O N 59 N 50 N Пр. 1 O N N O неактивна O неактивна F Пр. 2 O N N Cl 3 UA 114529 C2 Ефективність [%] PAM mGlu5 EC50 [нM] Приклад Пр. 3 O N N O неактивна O неактивна Cl Пр. 4 O N N N Cl 5 10 15 20 Аналіз зв’язування МРЕР: Для експериментів по зв’язуванню кДНК, що кодує людський рецептор mGLu 5a, тимчасово трансфікували в клітини EBNA з використанням методики, описаної Schlaeger і Christensen [Cytotechnology 15:1-13 (1998)]. Гомогенати клітинної мембрани зберігали при -80°С до доби аналізу, після чого їх відтавали, ресуспендували і політронізували в буфері для зв’язування, що містить 15 мМ Tris-HCl, 120 мМ NaCl, 100 мМ KCl, 25 мМ CaCl2, 25 мМ MgCl2, рН 7,4, до кінцевої концентрації в аналізі, що становить 20 мкг білка/лунку. Визначали ізотерми насичення шляхом додавання на дані мембрани дванадцяти 3 концентрацій [ H]MPEP (0,04-100 нМ) (у загальному об'ємі 200 мкл) на 1 г при 4°С. 3 Експерименти по конкуренції проводили з фіксованою концентрацією [ H]MPEP (2 нМ), і значення IC50 (напівмаксимальна інгібуюча концентрація) досліджуваних сполук оцінювали з використанням 11 концентрацій (0,3-10000 нМ). Інкубації проводили протягом 1 г при 4°С. В кінці інкубації мембрани фільтрували на Unifilter (96-лунковий білий мікропланшет із зв'язаним фільтром CF/C, предінкубованим 1 г в 0,1% PEI в промивальному буфері, Packard Bioscience, Meriden, CT) з колектором клітин Filtermate 96 (Packard Bioscience) і 3 рази промивали холодним 50 мM буфером Tris-HCl, pH 7,4. Неспецифічне зв’язування вимірювали у присутності 10 мкМ MPEP. Радіоактивність на фільтрі рахували (3 хв) на сцинтиляційному лічильнику для мікропланшетів Packard Top-count з поправкою гасіння після додавання 45 мкл Microscint 40 (Canberra Packard S.a., Цюріх, Швейцарія) і струшування протягом 20 хв. Порівняння сполук за винаходом з еталонними сполуками 1 і 2 Як можна бачити в наведеній нижче таблиці, сполуки за винаходом (NAM) демонструють профіль, що чітко відрізняється, в порівнянні із структурно схожими еталонними сполуками 1 і 2 (РАМ). 25 Пр. Аналіз PAM mGlu5 EC50 (нM) Зв’язуванняMPEP Ki (нM) Профіль активності 46 201 PAM 50 Структура 315 PAM O N Етал. 1 Пр. 35 N O F O N Етал. 1 Пр. 46 N N 4 UA 114529 C2 Аналіз PAM mGlu5 EC50 (нM) Зв’язуванняMPEP Ki (нM) Профіль активності O неактивна 72 NAM O неактивна 19 NAM O Пр. неактивна 23 NAM O неактивна 67 NAM Структура O N N 1 F O N N 2 Cl O N N 3 Cl O N N N 4 Cl 5 10 Сполуки формули I можна виготовляти наведеними нижче способами, способами, наведеними в прикладах, або аналогічними способами. Відповідні умови реакції для індивідуальних стадій реакції відомі фахівцю в даній області. Послідовність реакцій не обмежується послідовністю, показаною на схемах, проте, послідовність стадій реакції можна вільно змінювати, залежно від початкових речовин та їх відповідної реакційної здатності. Початкові речовини або є у продажу, або можуть бути одержані способами, аналогічними способами, приведеними нижче, способами, описаними в посиланнях, процитованих в описі або в прикладах, або способами, відомими в даній області. Дані сполуки формули I та їх фармацевтично прийнятні солі можна одержувати способами, відомими в даній області, наприклад, варіантами способу, описаними нижче, причому даний спосіб включає проведення взаємодії сполуки формули O N OH Y 1 R 3 15 із сполукою формули 2 R 2 R HN O 4 з утворенням сполуки формули I 20 5 UA 114529 C2 O R2 R2 N N Y O 1 R I, де заступники описані вище. Одержання сполук формули I надалі детальніше описано на схемі 1 і в прикладах 1-4. 5 10 15 20 25 30 35 Етиніл-піридинову або етиніл-піримідинову сполуки формули I можна одержувати, наприклад, поєднанням Соногашира метилового ефіру 5-бром-піридин-2-карбонової кислоти або метилового ефіру 5-бром-піримідин-2-карбонової кислоти 1 з відповідним чином заміщеним арилацетиленом 2, з подальшим омиленням з основою, такою як LiOH, з одержанням відповідної кислоти 3, або поєднанням Соногашира 5-бром-піридин-2-карбонової кислоти або 5бром-піримідин-2-карбонової кислоти 1 з відповідним чином заміщеним арилацетиленом 2 з прямим одержанням відповідної кислоти 3. Бажані етинільні сполуки загальної формули I (схема 1) одержують проведенням взаємодії відповідної кислоти 3 з відповідною морфоліновою похідною 4 у присутності основи, такої як основа Хуніга, і пептидного зв'язуючого реактиву, такого як TBTU, в розчиннику, такому як діоксан, або одержанням in situ відповідного хлорангідриду з оксалілхлоридом і DMF (кат.) в розчиннику, такому як дихлорметан, з подальшою реакцією з відповідним морфоліновою похідною 4 у присутності основи, такої як піридин. Фармацевтично прийнятні солі сполук формули I можуть бути легко виготовлені згідно способам, відомим як такі, і враховуючи природу сполуки, що підлягає перетворенню на сіль. Для утворення фармацевтично прийнятних солей основних сполук формули I підходять неорганічні або органічні кислоти, такі як, наприклад, соляна кислота, бромисто-воднева кислота, сірчана кислота, азотна кислота, фосфорна кислота або лимонна кислота, мурашина кислота, фумарова кислота, малеїнова кислота, оцтова кислота, янтарна кислота, винна кислота, метансульфонова кислота, п-толуолсульфонова кислота і тому подібні. Для утворення фармацевтично прийнятних солей кислотних сполук підходять сполуки, які містять лужні метали або лужноземельні метали, наприклад, натрій, калій, кальцій, магній або тому подібні, основні аміни або основні амінокислоти. Крім того, даний винахід також відноситься до лікарських засобів, що містять одну або більше ніж одну сполуку за даним винаходом і фармацевтично прийнятні ексципієнти, для лікування і попередження розладів, опосередкованих рецептором mGluR5, таких як тривожність і біль, депресія, синдром Мартіна-Белл, розлади аутичного спектру, хвороба Паркінсона і гастроезофагальний рефлюкс (GERD). Винахід також відноситься до застосування сполуки згідно даного винаходу, а також її фармацевтично прийнятної солі для виготовлення лікарських засобів для лікування і 6 UA 114529 C2 5 10 15 попередження розладів, опосередкованих рецептором mGluR5, як описано вище. Фармакологічна активність сполук була протестована з використанням наступного способу: кДНК, що кодує щурячий рецептор mGLu 5a, була тимчасово трансфікована в клітини EBNA з використанням методики, описаної E.-J. Schlaeger і K. Christensen (Cytotechnology 1998, 15, 12+ 13). Вимірювання [Ca ]внутр. проводили на клітинах EBNA, трансфікованих mGLu 5a, після інкубації клітин з Fluo 3-AM (доступним у FLUKA, кінцева концентрація 0,5 мкМ) протягом 1 години при 37°С, з подальшими 4 промивками буфером для аналізу (DMEM, доповнена солями 2+ Хенкса і 20 мМ HEPES). Вимірювання [Ca ]внутр. проводили з використанням планшет-рідера для флуориметричній візуалізації (FLIPR, Molecular Devices Corporation, La Jolla, CA, США). Коли сполуки були оцінені як антагоністи, їх тестували відносно 10 мкМ глутамату в якості агоніста. Криві інгібування (антагоністи) апроксимували з використанням чотирьохпараметричного логістичного рівняння, що дає IC50, і коефіцієнт Хілла, використовуючи програму ітераційної нелінійної апроксимації кривих Origin (Microcal Software Inc., Northampton, MA, США). Наведені значення Ki протестованих сполук. Значення Ki визначається за допомогою наступної формули: Ki IC 50 = 1+ [L] EC 50 20 25 30 35 40 45 50 55 в якій значення IC50 є тими концентраціями, протестованих сполук в мкМ, за допомогою яких виявляється 50%-на протидія ефекту сполук. [L] є концентрацією, і значення IC50 є концентрацією сполук в мкМ, яка здійснює 50%-ну стимуляцію. Сполуки за даним винаходом є антагоністами рецептора mGluR 5a. Активності сполук формули I, зміряні в описаному вище аналізі, знаходяться в інтервалі Ki менше 100 мкМ. Сполуки формули I та їх фармацевтично прийнятні солі можна використовувати як лікарські засоби, наприклад, у формі фармацевтичних препаратів. Фармацевтичні препарати можна вводити перорально, наприклад, у формі таблеток, покритих таблеток, драже, твердих і м'яких желатинових капсул, розчинів, емульсій або суспензій. Проте введення також може здійснюватися ректально, наприклад, у формі супозиторіїв, або парентерально, наприклад, у формі ін'єкційних розчинів. Сполуки формули I та їх фармацевтично прийнятні солі можна переробляти з фармацевтично інертними неорганічними або органічними носіями для одержання фармацевтичних препаратів. Як такі носії для таблеток, покритих таблеток, драже і твердих желатинових капсул можна використовувати, наприклад, лактозу, кукурудзяний крохмаль або його похідні, тальк, стеаринову кислоту або її солі і тому подібне. Відповідними носіями для м'яких желатинових капсул є, наприклад, рослинні олії, воски, жири, напівтверді і рідкі поліоли і тому подібне; проте, залежно від природи активної речовини, у разі м'яких желатинових капсул носії зазвичай не потрібні. Відповідними носіями для одержання розчинів і сиропів є, наприклад, вода, поліоли, сахароза, інвертований цукор, глюкоза і тому подібне. Для водних ін'єкційних розчинів водорозчинних солей сполук формули I можна використовувати ад'юванти, такі як спирти, поліоли, гліцерин, рослинні олії і тому подібне, але, як правило, вони не є необхідними. Відповідними носіями для супозиторіїв є, наприклад, природні або отверджені масла, воски, напіврідкі або рідкі поліоли і тому подібне. Крім того, фармацевтичні препарати можуть містити консерванти, солюбілізатори, стабілізатори, зволожувачі, емульгатори, підсолоджувачі, барвники, коригенти, солі для зміни осмотичного тиску, буфери, маскуючі агенти або антиоксиданти. Крім того, вони також можуть містити інші терапевтично корисні речовини. Як згадано раніше, метою даного винаходу також є лікарські засоби, що містять сполуку формули I або її фармацевтично прийнятні солі і терапевтично інертний ексципієнт, як і спосіб одержання таких лікарських засобів, який включає об'єднання одної або більше ніж одної сполуки формули I або її фармацевтично прийнятної солі і, якщо бажано, одної або більше ніж одної іншої терапевтично корисної речовини в лікарську форму спільно з одним або більше ніж одним терапевтично інертним носієм. Дозування може варіювати в широких межах і, природно, адаптується для індивідуальних вимог у кожному конкретному випадку. Загалом, ефективне дозування для перорального або парентерального введення складає 0,01-20 мг/кг/доба, причому дозування 0,1-10 мг/кг/доба є переважним для всіх описаних свідчень. Щодобове дозування для дорослої людини, що важить 70 кг, відповідно, складає 0,7-1400 мг на добу, переважно 7-700 мг на добу. 7 UA 114529 C2 Наступні приклади приведені для додаткового пояснення винаходу. Приклад 1 (3,3-Диметил-морфолін-4-іл)-[5-(3-фтор-фенілетиніл)-піридин-2-іл]-метанон O N N O F 5 Стадія 1: метиловий ефір 5-(3-фтор-фенілетиніл)-піридин-2-карбонової кислоти O N O F 10 15 Біс-(трифенілфосфін)-паладій(II) дихлорид (406 мг, 580 мкмоль, 0,05 екв.) розчиняли в 25 мл DMF (диметилформамід). При кімнатній температурі додавали метиловий ефір 5-бром-піридин2-карбонової кислоти (2,5 г, 11,6 ммоль) і 3-фторфенілацетилен (2,22 г, 18,5 ммоль, 1,6 екв.). Додавали триетиламін (3,5 г, 4,84 мл, 34,7 ммоль, 3 екв.), трифенілфосфін (91 мг, 347 мкмоль, 0,03 екв.) і йодид міді(I) (66 мг, 347 мкмоль, 0,03 екв.), і суміш перемішували протягом 20 годин при 80°С. Реакційну суміш охолоджували і упарювали насухо з використанням сорбенту Isolute®. Неочищений продукт очищали флеш-хроматографією на силікагелі (70 г), здійснюючи елюцію градієнтом етилацетат:гептан від 0:100 до 80:20. Бажаний метиловий ефір 5-(3-фторфенілетиніл)-піридин-2-карбонової кислоти (1,95 г, вихід 66%) одержували у вигляді світло+ жовтої твердої речовини, МС (мас-спектрометрія): m/e дорівнює 256,3 (М+Н ). Стадія 2: 5-(3-фтор-фенілетиніл)-піридин-2-карбонова кислота O N O F 20 25 Метиловий ефір 5-(3-фтор-фенілетиніл)-піридин-2-карбонової кислоти (1,9 г, 7,44 ммоль) (Приклад 1, стадія 1) розчиняли в THF (тетрагідрофуран) (30 мл) і воді (30 мл), і додавали при кімнатній температурі LiOH (357 мг, 24,9 ммоль, 2 екв.). Суміш перемішували протягом 16 годин при кімнатній температурі. Реакційну суміш підкисляли 4 н. HCl до рН 2,5, і випаровували THF з одержанням жовтої суспензії. Дану суспензію охолоджували до 0-5°С і фільтрували. Кристали промивали холодною водою і здійснювали упарювання насухо. Бажану 5-(3-фтор-фенілетиніл)піридин-2-карбонову кислоту (1,71 г, вихід 95%) одержували у вигляді світло-жовтої твердої + речовини. МС: m/e дорівнює 239,9 (М+Н ). Стадія 3: (3,3-диметил-морфолін-4-іл)-[5-(3-фтор-фенілетиніл)-піридин-2-іл]-метанон O N N O F 30 35 5-(3-Фтор-фенілетиніл)-піридин-2-карбонову кислоту (50 мг, 0,21 ммоль) (Приклад 1, стадія 2) розчиняли в DMF (0,5 мл) і додавали при кімнатній температурі основу Хуніга (44 мкл, 0,31 ммоль, 1,2 екв.), 3,3-диметилморфолін (36 мг, 0,25 ммоль, 1,5 екв.) і TBTU (73 мг, 0,23 ммоль, 1,1 екв.). Дану суміш перемішували протягом 16 годин при кімнатній температурі. Реакційну суміш упарювали і екстрагували насиченим розчином NaHCO 3 і двічі невеликим об'ємом дихлорметану. Неочищений продукт очищали флеш-хроматографією шляхом безпосереднього завантаження шарів дихлорметану на колонку з силікагелем і елюювання градієнтом етилацетат:гептан від 0:100 до 80:20. Бажаний (3,3-диметил-морфолін-4-іл)-[5-(3-фторфенілетиніл)-піридин-2-іл]-метанон (61 мг, вихід 87%) одержували у вигляді світло-жовтого + масла, МС: m/e дорівнює 339,2 (М+Н ). 8 UA 114529 C2 Приклад 2 [5-(3-Хлор-фенілетиніл)-піридин-2-іл]-морфолін-4-іл-метанон O N N O Cl Стадія 1: 5-(3-хлор-фенілетиніл)-піридин-2-карбонова кислота O N 5 O Cl Сполуку, зазначену в заголовку, одержували у вигляді білої твердої речовини, МС: m/e + дорівнює 258,4/260,4 (М+Н ), використовуючи хімію, аналогічну хімії, описаній в Прикладі 1, стадія 1, з 5-бром-піридин-2-карбонової кислоти і 3-хлорфенілацетилену. Стадія 2: [5-(3-хлор-фенілетиніл)-піридин-2-іл]-морфолін-4-іл-метанон O N N O Cl 10 15 Сполуку, зазначену в заголовку, одержували у вигляді білої твердої речовини, МС: m/e + дорівнює 327,5/329,5 (М+Н ), використовуючи хімію, аналогічну хімії, описаній в Прикладі 1, стадія 3, з 5-(3-хлор-фенілетиніл)-піридин-2-карбонової кислоти (Приклад 2, стадія 1) і морфоліну. Приклад 3 (3,3-Диметил-морфолін-4-іл)-[5-(3-хлор-фенілетиніл)-піридин-2-іл]-метанон O N N O Cl 20 Сполуку, зазначену в заголовку, одержували у вигляді білої твердої речовини, МС: m/e + дорівнює 355,5/357,5 (М+Н ), використовуючи хімію, аналогічну хімії, описаній в Прикладі 1, стадія 3, з 5-(3-хлор-фенілетиніл)-піридин-2-карбонової кислоти (Приклад 2, стадія 1) і 3,3диметилморфоліну. Приклад 4 (3,3-Диметил-морфолін-4-іл)-[5-(3-хлор-фенілетиніл)-піримідин-2-іл]-метанон O N N N O Cl 25 Стадія 1: 5-(3-хлор-фенілетиніл)-піримідин-2-карбонова кислота 9 UA 114529 C2 O N O N Cl 5 Сполуку, зазначену в заголовку, одержували у вигляді білої твердої речовини, МС: m/e + дорівнює 259,4/261,4 (М+Н ), використовуючи хімію, аналогічну хімії, описаній в Прикладі 1, стадія 1, з 5-бром-піримідин-2-карбонової кислоти і 3-хлорфенілацетилену. Стадія 2: (3,3-диметил-морфолін-4-іл)-[5-(3-хлор-фенілетиніл)-піримідин-2-іл]-метанон O N N O N Cl 10 15 5-(3-Хлор-фенілетиніл)-піримідин-2-карбонову кислоту (100 мг, 0,39 ммоль) (Приклад 4, стадія 1) суспендували в дихлорметані (1 мл) і DMF (10 мкл). Додавали по краплях оксалілхлорид (51 мкл, 0,59 ммоль, 1,5 екв.) при кімнатній температурі, і перемішували суміш протягом 1 години при температурі флегмоутворення. Потім реакційну суміш додавали до суміші діїзопропілетиламіну (235 мкл, 1,34 ммоль, 3,3 екв.) і 3,3-диметилморфоліну (46 мг, 0,40 ммоль, 1 екв.) в THF (2 мл). Дану суміш перемішували протягом 16 годин при кімнатній температурі і упарювали у присутності сорбента Isolute® насухо. Неочищений продукт очищали флеш-хроматографією на колонці з 20 г силікагелю, елююючи градієнтом гептан: етилацетат від 100:0 до 0:100. Бажаний (3,3-диметил-морфолін-4-іл)-[5-(3-хлор-фенілетиніл)-піримідин-2-іл]метанон (120 мг, вихід 94%) одержували у вигляді білої твердої речовини, МС: m/e дорівнює + 356,6/358,6 (М+Н ). ФОРМУЛА ВИНАХОДУ 20 1. Сполука формули І O N 25 30 35 2 R 2 N Y R R O 1 ,І де Υ позначає N або СН; 1 R позначає фтор- або хлор-; 2 R позначає водень або метил; або її фармацевтично прийнятна кислотно-адитивна сіль. 2. Сполука формули І за п. 1, де Υ позначає N. 3. Сполука формули І за п. 2, яка є (3,3-диметилморфолін-4-іл)-[5-(3-хлорфенілетиніл)піримідин-2-іл]-метаноном. 4. Сполука формули І за п. 1, де Υ позначає СН. 5. Сполука формули І за п. 4, яка є (3,3-диметилморфолін-4-іл)-[5-(3-фторфенілетиніл)-піридин-2-іл]-метаноном, [5-(3хлорфенілетиніл)-піридин-2-іл]-морфолін-4-ілметаноном або (3,3-диметилморфолін-4-іл)-[5-(3хлорфенілетиніл)-піридин-2-іл]-метаноном. 6. Сполука за будь-яким з пп. 1-5 для застосування як терапевтично активної речовини. 7. Спосіб одержання сполуки формули І, як описано в п. 1, який включає варіант, за яким в реакцію вводять сполуку формули 10 UA 114529 C2 O N OH Y R 1 ,3 із сполукою формули R 2 R 2 HN O ,4 з утворенням сполуки формули O N 5 10 15 20 2 R 2 N Y R R O 1 ,І де замісники описані в п. 1. 8. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-5 і терапевтично активний носій. 9. Застосування сполуки за будь-яким з пп. 1-5 для лікування тривожності і болю, депресії, синдрому Мартіна-Белл, розладів аутичного спектра, хвороби Паркінсона і гастроезофагального рефлюксу (GERD). 10. Застосування сполуки за будь-яким з пп. 1-5 для виготовлення лікарського засобу для лікування тривожності і болю, депресії, синдрому Мартіна-Белл, розладів аутичного спектра, хвороби Паркінсона і гастроезофагального рефлюксу (GERD). 11. Сполука за будь-яким з пп. 1-5 для лікування тривожності і болю, депресії, синдрому Мартіна-Белл, розладів аутичного спектра, хвороби Паркінсона і гастроезофагального рефлюксу (GERD). 12. Спосіб лікування тривожності і болю, депресії, синдрому Мартіна-Белл, розладів аутичного спектра, хвороби Паркінсона і гастроезофагального рефлюксу (GERD), який включає введення ефективної кількості сполуки, як визначено за будь-яким з пп. 1-5. 11 UA 114529 C2 Комп’ютерна верстка А. Крулевський Міністерство економічного розвитку і торгівлі України, вул. М. Грушевського, 12/2, м. Київ, 01008, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 12
ДивитисяДодаткова інформація
Назва патенту англійськоюEthynyl derivatives as modulators of mglur5 receptor activity
Автори англійськоюJaeschke, Georg, Lindemann, Lothar, Ricci, Antonio, Rueher, Daniel, Stadler, Heinz, Vieira, Eric
Автори російськоюЕшке Георг, Линдеманн Лотар, Риччи Антонио, Рюхер Даниель, Штадлер Хайнц, Виэйра Эрик
МПК / Мітки
МПК: C07D 413/06, C07D 213/81, A61K 31/4439
Мітки: похідні, рецептора, етинілу, активності, модулятори, mglur5
Код посилання
<a href="https://ua.patents.su/14-114529-pokhidni-etinilu-yak-modulyatori-aktivnosti-receptora-mglur5.html" target="_blank" rel="follow" title="База патентів України">Похідні етинілу як модулятори активності рецептора mglur5</a>
Попередній патент: Комбінації активних сполук, що містять карбоксамідні похідні та засіб біологічної боротьби
Наступний патент: Вдосконалений спосіб одержання металів
Випадковий патент: Плоскорізальна лапа












