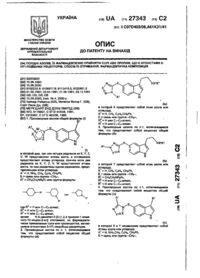
Похідні фосфоліпідів, спосіб отримання похідних фосфоліпідів, фармацевтична композиція та спосіб її отримання
Номер патенту: 40567
Опубліковано: 15.08.2001
Автори: КУТШЕР Берхард, ХІЛГАРД Петер, СТЕКАР Юрій, Енгел Юрген, ШУМАХЕР Вольфганг, НЬОСНЕР Герхард
Формула / Реферат
1. Производные фосфолипидов общей формулы (I)
в которой R обозначает алкильный радикал с неразветвленной или разветвленной цепью с 10-24 атомами углерода, которая может также содержать двойные или тройные связи, R1 и R2 независимо друг от друга обозначают водород или каждый неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 - 6 атомами углерода, который может также содержать Сl-, ОН- или NH2- группу и при этом два этих радикала могут быть соединены также в кольцо, А обозначает простую связь или одну из групп формул
причем группы (II) - (VI) ориентированы таким образом, что атом кислорода соединен с атомом фосфора соединения (I), X обозначает атом кислорода или серы, или NH, если А является простой связью, или обозначает атом кислорода или серы, если А является одной из групп (II) - (IV),
«Y» равен нулю или является натуральным числом от 1 до 3, тип независимо друг от друга равны 0 или являются натуральными числами при условии, что m + n составляет от 2 до 8,
используемые в качестве лекарственного средства.
2. Производное фосфолипидов по п. 1, общей формулы (I), отличающееся тем, что Х обозначает атом кислорода.
3. Производное фосфолипидов по любому из п. 1 или 2, общей формулы (I), отличающееся тем, что А обозначает простую связь.
4. Производное фосфолипидов по любому из п п. 1 - 3, общей формулы (I), отличающееся тем, что R1 и R2 являются соответственно метиловыми группами.
5. Производное фосфолипидов по любому из п.п. 1 - 4 общей формулы (I), отличающееся тем, что таким производньм является октадецил-(1,1-диметилпиперидино-4-ил)-фосфат, октадецил-( 1,1 -диметилгексагидроазефино-4-ил)-фосфат.
6. Способ получения производных фосфолипидов, отличающийся тем, что соединение общей формулы
R-X-A-H,(VII)
в которой R обозначает алкильный радикал с неразветвленной или разветвленной цепью с 10-24 атомами углерода, которая может также содержать двойные или тройные связи, Х обозначает атом кислорода или серы, или NH, если А является простой связью, или обозначает атом кислорода или серы, если А является одной из групп (II) - (IV), А обозначает простую связь или одну из групп формул
причем группы (II) - (VI) ориентированы таким образом, что атом кислорода соединен с атомом фосфора соединения (I), вводят в реакцию с фосфороксотрихлоридом в присутствии надлежащего вспомогательного основания с растворителем или без растворителя и затем с помощью соединения общей формулы
в которой R1 и R2 независимо друг от друга обозначают водород или каждый неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 - 6 атомами углерода, который может также содержать Сl -, ОН -или NH; - группу и при этом два этих радикала могут быть соединены также в кольцо, «Y» равен нулю или является натуральным числом от 1 до 3, тип независимо друг от друга равны 0 или являются натуральными числами при условии, что m + n составляет от 2 до 8,
а Y обозначает галогенид, мезилат или тозилат, преобразуют в соединения общей формулы (I), в случае необходимости могут преобразовываться в соединения общей формулы (IX)
(IX)
в которой R1 обозначают водород или неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 - 6 атомами углерода, который может также содержать Сl -, ОН - или NH2 - группу, «Y» равен нулю или является натуральным числом от 1 до 3, тип независимо друг от друга равны 0 или являются натуральными числами при условии, что m + n составляет от 2 до 8, причем соединения общей формулы (I), в которых R1 и/или R2 является водородом, преобразовываются известным способом с помощью алкилирующих средств R2-Y, в которых R2 обозначают водород или неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 - б атомами углерода, который может также содержать Сl -, ОН- или NH2;- группу, а Y одинаково является хлором, бромом, йодом, тозилом или мезилом.
7. Способ получения производных фосфолипидов по п. 6, отличающийся тем, что раствор соединений формулы (I) обрабатывают в органическом растворителе ионообменником, совместного Н-ОН-ионирования или смесью кислого и основного ионообменников, или кислым и затем основным ионообменником или наоборот.
8. Фармацевтическая композиция, обладающая противоопухолевым действием, содержащая в качестве активного начала производное фосфолипидов и целевые добавки, отличающаяся тем, что в качестве фосфолипидов она содержит эффективное количество одного или нескольких производных фосфолипидов общей формулы (I)
в которой R обозначает алкильный радикал с неразветвленной или разветвленной цепью с 10-24 атомами углерода, которая может также содержать двойные или тройные связи R1 и R2 независимо друг от друга обозначают водород или каждый неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 - 6 атомами углерода, который может также содержать Сl-, ОН - или NH2, - группу и при этом два этих радикала могут быть соединены также в кольцо, А обозначает простую связь или одну из групп формул
причем группы (II) - (VI) ориентированы таким образом, что атом кислорода соединен с атомом фосфора соединения (I), X обозначает атом кислорода или серы, или NH, если А является простой связью, или обозначает атом кислорода или серы, если А является одной из групп (II) - (IV);
«Y» равен нулю или является натуральным числом от 1 до 3, или независимо друг от друга равны 0 или являются натуральными числами при условии, что m + n составляет от 2 до 8, или их фармацевтически приемлемых солей.
9. Фармацевтическая композиция по п. 8, отличающаяся тем, что в качестве активного вещества она содержит октадецил-(1,1-диметилпиперидинио-4-ил)-фосфат, октадецил-(1,1 -диметилпергидроазефинио-4-ил)-фосфат, эруцил-(1,1 -диметилпиперидинио-4-ил)-фосфат, эруцил-(1,1-диметилпергидроазефинио-4-ил)-фосфат, причем количество активного вещества находится в пределах от 50 до 250 мг.
10. Фармацевтическая композиция по п. 8, отличающаяся тем, что в качестве активного вещества она содержит октадецил-(1,1-диметилпиперидинио-4-ил)-фосфат, причем количество активного вещества находится в пределах от 50 до 250 мг.
11. Способ получения фармацевтической композиции, обладающей противоопухолевым действием, включающий смешивание фосфолипидов с фармацевтически приемлемыми целевыми добавками, отличающийся тем, что в качестве фосфолипидов используют эффективное количество одного или нескольких производных фосфолипидов общей формулы (I)
в которой R обозначает алкильный радикал с неразветвленной или разветвленной цепью с 10-24 атомами углерода, которая может также содержать двойные или тройные связи, R1 и R2 независимо друг от друга обозначают водород или каждый неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 - 6 атомами углерода, который может также содержать Сl-, ОН - или NH2 - группу и при этом два этих радикала могут быть соединены также в кольцо, А обозначает простую связь или одну из групп формул
причем группы (II) - (VI) ориентированы таким образом, что атом кислорода соединен с атомом фосфора соединения (I), X обозначает атом кислорода или серы, или NH, если А является простой связью, или обозначает атом кислорода или серы, если А является одной из групп (II) - (IV);
«Y» равен нулю или является натуральным числом от 1 до 3, тип независимо друг от друга равны 0 или являются натуральными числами при условии, что m + n составляет от 2 до 8, или их фармацевтически приемлемых солей.
Текст
1. Производные фосфолипидов общей формулы (I) 40567 жать двойные или тройные связи, Х обозначает атом кислорода или серы, или NH, если А является простой связью, или обозначает атом кислоро да или серы, если А является одной из групп (II) (IV), А обозначает простую связь или одну из групп формул причем группы (II) - (VI) ориентированы таким образом, что атом кислорода соединен с атомом фосфора соединения (I), вводят в реакцию с фосфороксотрихлоридом в присутствии надлежащего вспомогательного основания с растворителем или без растворителя и затем с помощью соединения общей формулы ляет от 2 до 8, причем соединения общей формулы (I), в которых R1 и/или R2 является водородом, преобразовываются известным способом с помощью алкилирующих средств R2-Y, в которых R2 обозначают водород или неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 - 6 атомами углерода, который может также содержать Сl-, ОНили NH2-группу, а Y одинаково является хлором, бромом, йодом, тозилом или мезилом. 7. Способ получения производных фосфолипидов по п. 6, отличающийся тем, что раствор соединений формулы (I) обрабатывают в органическом растворителе ионообменником, совместного НОН-ионирования или смесью кислого и основного ионообменников, или кислым и затем основным ионообменником или наоборот. 8. Фармацевтическая композиция, обладающая противоопухолевым действием, содержащая в качестве активного начала производное фосфолипидов и целевые добавки, отличающаяся тем, что в качестве фосфолипидов она содержит эффективное количество одного или нескольких производных фосфолипидов общей формулы (I) (VIII) 1 2 в которой R и R независимо друг от друга обозначают водород или каждый неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 - 6 атомами углерода, который может также содержать Сl-, ОНили NH2-группу и при этом два этих радикала могут быть соединены также в кольцо, «Y» равен нулю или является натуральным числом от 1 до 3, m и n независимо друг от друга равны 0 или являются натуральными числами при условии, что m + n составляет от 2 до 8, а Y обозначает галогенид, мезилат или тозилат, преобразуют в соединения общей формулы (I), в случае необходимости могут преобразовываться в соединения общей формулы (IX) (I) в которой R обозначает алкильный радикал с неразветвленной или разветвленной цепью с 10-24 атомами углерода, которая может также содержать двойные или тройные связи, R1 и R2 независимо друг от друга обозначают водород или каждый неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 - 6 атомами углерода, который может также содержать Сl-, ОН- или NH2-группу и при этом два этих радикала могут быть соединены также в кольцо, А обозначает простую связь или одну из групп формул (ІХ) 1 в которой R обозначают водород или неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 - 6 атомами углерода, который может также содержать Сl-, ОН- или NH2-группу, «Y» равен нулю или является натуральным числом от 1 до 3, m и n независимо друг от друга равны 0 или являются натуральными числами при условии, что m + n состав 2 40567 причем группы (II) - (VI) ориентированы таким образом, что атом кислорода соединен с атомом фосфора соединения (I), X обозначает атом кислорода или серы, или NH, если А является простой связью, или обозначает атом кислорода или серы, если А является одной из групп (II) - (IV); «Y» равен нулю или является натуральным числом от 1 до 3, m и n независимо друг от друга равны 0 или являются натуральными числами при условии, что m + n составляет от 2 до 8, или их фармацевтически приемлемых солей. 9. Фармацевтическая композиция по п. 8, отличающаяся тем, что в качестве активного вещества она содержит октадецил-(1,1-диметилпиперидинио-4-ил)-фосфат, октадецил-(1,1-диметилпергидроазефинио-4-ил)-фосфат, эруцил-(1,1-диметилпиперидинио-4-ил)-фосфат, эруцил-(1,1-диметилпергидроазефинио-4-ил)-фосфат, причем количество активного вещества находится в пределах от 50 до 250 мг. 10. Фармацевтическая композиция по п. 8, отличающаяся тем, что в качестве активного вещества она содержит октадецил-(1,1-диметилпиперидинио4-ил)-фосфат, причем количество активного вещества находится в пределах от 50 до 250 мг. 11. Способ получения фармацевтической композиции, обладающей противоопухолевым действи ем, включающий смешивание фосфолипидов с фармацевтически приемлемыми целевыми добавками, отличающийся тем, что в качестве фосфолипидов используют эффективное количество одного или нескольких производных фосфолипидов общей формулы (I) причем группы (II) - (VI) ориентированы таким образом, что атом кислорода соединен с атомом фосфора соединения (I), X обозначает атом кислорода или серы, или NH, если А является простой связью, или обозначает атом кислорода или серы, если А является одной из групп (II) - (IV); «Y» равен нулю или является натуральным числом от 1 до 3, m и n независимо друг от друга равны 0 или являются натуральными числами при условии, что m + n составляет от 2 до 8, или их фармацевтически приемлемых солей. (I) в которой R обозначает алкильный радикал с неразветвленной или разветвленной цепью с 10-24 атомами углерода, которая может также содержать двойные или тройные связи, R1 и R2 независимо друг от друга обозначают водород или каждый неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 - 6 атомами углерода, который может также содержать Сl-, ОН- или NH2-группу и при этом два этих радикала могут быть соединены также в кольцо, А обозначает простую связь или одну из групп формул ______________________________ Настоящее изобретение относится к новым производным фосфолипидов, а именно к алкилфосфатам или алкенфосфатам, холиновый остаток которых является частью гетероциклического кольца, способу получения этих соединений, а также к лекарственным средствам и способу получения лекарственных средств, которые содержат эти соединения в качестве биологически активных веществ. Заявка на выдачу патента ЕПВ № 108565 касается соединений общей формулы и их фармацевтически приемлемых солей, в которых R1 является алифатическим остатком углеводородов с 8 - 30 атомами углерода, остатки R2, R3 и R4 одинаковы или различны и являются водородом или низкими алкильными радикалами, или в которой группа N R2 R3 R4 обозначает циклическую аммониевую группу, а n имеет значение 0 или 1. Для этих соединений указывается антиопухолевое действие, а также подавляющее грибки действие. В основу настоящего изобретения поставлена задача разработки эффективного лекарственного средства, обладающего противоопухолевым действием. Поставленная задача достигается тем, что получены новые производные фосфолипидов общей формулы 1 3 40567 работки способа получения и способа очистки новых производных фосфолипидов. Поставленная задача достигается тем, что соединение общей формулы R-X-A-H (VII) в которой R обозначает алкильный радикал с неразветвленной или разветвленной цепью с 10-24 атомами углерода, которая может также содержать двойные или тройные связи, Х обозначает атом кислорода или серы, или NH, если А является простой связью, или обозначает атом кислорода или серы, если А является одной из групп (II) - (IV), А обозначает простую связь или одну из групп формул в которой R обозначает алкильный радикал с неразветвленной или разветвленной цепью с 10-24 атомами углерода, которая может также содержать двойные или тройные связи, R1 и R2 независимо друг от друга обозначают водород или каждый неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 - 6 атомами углерода, который может также содержать CI-, ОН- или NH2-группу и при этом два этих радикала могут быть соединены также в кольцо, А обозначает простую связь или одну из групп формул (IV) (V) (IV) -(CH2)8-O (III) CH2-CH-O| CH3 (III) CH2-CH-O| CH3 -CH2-CH2-O (II) -CH2-CH2-O (II) -(CH2)8-O -СH2-CH2-CH2-O -СH2-CH2-CH2-O (V) -CH H2 C -CH CH-CH2-O H2 C O CH2 CH-CH2-OO CH2 (VI) причем группы (II) и -(VI) ориентированы таким образом, что атом кислорода соединен с атомом фосфора соединения (I), вводят в реакцию с фосфороксотрихлоридом в присутствии надлежащего вспомогательного основания с растворителем или без растворителя и затем с помощью соединения общей формулы (VI) причем группы (II) и -(VI) ориентированы таким образом, что атом кислорода соединен с атомом фосфора соединения (I), X обозначает атом кислорода или серы, или NH, если А является простой связью, или обозначает атом кислорода или серы, если А является одной из групп (II) - (IV), «Y» равен нулю или является натуральным числом от 1 до 3, m и n независимо друг от друга равны 0 или являются натуральными числами при условии, что m + n составляет от 2 до 8, которое можно использовать в качестве лекарственного средства. Кроме того, Х обозначает атом кислорода. Кроме того, А обозначает простую связь. Кроме того, R1 и R2 являются соответственно метиловыми группами. Кроме того, таким производным является октадецил - (1,1 - диметилпиперидино - 4 - ил) фосфат, октадецил - (1,1 - диметилгексагидроазефино - 4 - ил) - фосфат. Неожиданным образом было обнаружено, что соединения, согласно изобретению, обладают лучшим антиопухолевым действием, чем описанные в заявке на выдачу патента ЕПВ № 108565 производные с открытой цепью. В основу изобретения также поставлена задача раз в которой R1 и R2 независимо друг от друга обозначают водород или каждый неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 - 6 атомами углерода, который может также содержать CI-, ОНили NH2 - группу и при этом два этих радикала могут быть соединены также в кольцо, «Y» равен нулю или является натуральным числом от 1 до 3, m и n независимо друг от друга равны 0 или являются натуральными числами при условии, что m + n составляет от 2 до 8, а Y обозначает галогенид, мезилат или тозилат, преобразуют в соединения общей формулы І, в случае необходимости могут преобразовываться в соединения общей формулы 4 40567 в которой R обозначает алкильный радикал с неразветвленной или разветвленной цепью с 10-24 атомами углерода, которая может также содержать двойные или тройные связи. R1 и R2 независимо друг от друга обозначают водород или каждый неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 - 6 атомами углерода, который может также содержать CI-, ОН- или NH2-группу и при этом два этих радикала могут быть соединены также в кольцо, А обозначает простую связь или одну из групп формул (IX) в которой R1 обозначают водород или неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 - 6 атомами углерода, который может также содержать CI-, ОН- или NH2-группу, «Y» равен нулю или является натуральным числом от 1 до 3, m и n независимо друг от друга равны 0 или являются натуральными числами при условии, что m + n составляет от 2 до 8, причем соединения общей формулы І, в которых R1 и/или R2 является водородом, преобразовываются известным способом с помощью алкилирующих средств R2 - Y, в которых R2 обозначают водород или неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 - 6 атомами углерода, который может также содержать CI-, ОН- или NH2-группу, а Y одинаково является хлором, бромом, йодом, тозилом или мезилом. Кроме того, раствор соединений формулы 1 обрабатывают в органическом растворителе ионообменником, совместного Н-ОН-ионирования или смесью кислого и основного ионообменников, или кислым и затем основным ионообменником или наоборот. Объектом изобретения является также фармацевтическая композиция, обладающая противоопухолевым действием и способ ее получения. Наиболее близкой по сути и достигаемому результату является композиция, описанная в заявке на выдачу Европейского патента ЕПВ № 108565, кл. МПК А61К 31/665, опубл. 1983 г. Композиция включает производные фосфолипидов с открытой цепью и целевые добавки. Способ получения известной композиции, обладающей противоопухолевым действием включает смешивание производного фосфолипидов с фармацевтически приемлемыми целевыми добавками. В основу изобретения поставлена задача разработки фармацевтической композиции, обладающей лучшим противоопухолевым действием, а также способа ее получения. Поставленная задача по объекту "фармацевтическая композиция" достигается тем, что в фармацевтической композиции, обладающей противоопухолевым действием, содержащей в качестве активного начала производное фосфолипидов и целевые добавки, согласно изобретению, в качестве фосфолипидов она содержит эффективное количество одного или несколько производных фосфолипидов общей формулы I -СH2-CH2-CH2-O (II) -CH2-CH2-O (III) CH2-CH-O| CH3 (IV) -(CH2)8-O (V) -CH CH-CH2-O H2 C O CH2 (VI) причем группы (II) и - (VI) ориентированы таким образом, что атом кислорода соединен с атомом фосфора соединения (I), X обозначает атом кислорода или серы, или NH, если А является простой связью, или обозначает атом кислорода или серы, если А является одной из групп (II) - (IV), «Y» равен нулю или является натуральным числом от 1 до 3, m и n независимо друг от друга равны 0 или являются натуральными числами при условии, что m + n составляет от 2 до 8, или их фармацевтически приемлемые соли. Кроме того, в качестве активного вещества фармацевтическая композиция содержит октадецил - (1,1 - диметилпиперидинио - 4 - ил) - фосфат, октадецил - (1,1 - диметилпергидроазефинио-4 ил) -фосфат, эруцил - (1,1 - диметилпиперидинио - 4 ил) - фосфат, эруцил - (1,1 -диметилпергидроазефинио-4 ил) - фосфат, причем количество активного вещества находится в пределах от 50 до 250 мг. Кроме того, в качестве активного вещества фармацевтическая композиция, содержит октадецил - (1,1 - диметилпиперидинио - 4 - ил) - фосфат, причем количество активного вещества находится в пределах от 50 до 250 мг. Поставленная задача по объекту "способ получения фармацевтической композиции" достигается тем, что в способе получения фармацевтической композиции, обладающей противоопухолевым действием, включающем смешивание фосфолипидов с фармацевтически приемлемыми целевыми добавками, согласно изобретению, в качестве фосфолипидов используют эффективное 5 40567 ческих простых эфирах, насыщенных углеводородах с 1 - 5 атомами углерода, жидких ароматических углеводородах, которые также могут быть замещены галогеном (в частности, хлором), или в смесях из вышеупомянутых растворителей или без растворителей, в случае необходимости, в присутствии обычной для этого основной субстанции. В качестве галогенированных углеводородов во внимание принимаются, например, углеводороды с 1-6 атомами углерода, причем один, или несколько, или все атомы водорода заменены атомами хлора. Могут использоваться, например, хлористый метилен, хлороформ, хлористый этилен, хлорбензол, дихлорбензол. Если речь идет о замещенных галогенами ароматических углеводородах, то они предпочтительно замещены одним или двумя атомами галогена. В качестве простых насыщенных циклических эфиров могут использоваться, например, эфиры с размером кольца 5-6, которые состоят из атомов углерода и одного или двух атомов кислорода. Примерами этого являются тетрагидрофуран, диоксан. Ациклические простые эфиры состоят из 2-8 атомов углерода и являются жидкими. Во внимание принимаются, например, диэтиловый эфир, диизобутиловый эфир, третичный метилбутиловый эфир, диизопропиловый эфир. В качестве насыщенных углеводородов во внимание принимаются углеводороды с неразветвленной и разветвленной цепью, которые состоят из 5-10 атомов углерода и являются жидкими. Во внимание принимаются, например, пентан, гексан, гептан, циклогексан. В качестве ароматических углеводородов во внимание принимаются, например, бензол и замещенные алкилом бензолы, причем алкильные заместители состоят из 1-5 атомов углерода. В качестве основных субстанций как для реакции хлорокиси фосфора со спиртом с длинной цепью, так и для последующего преобразования в диэфир фосфорной кислоты во внимание принимаются амины, например, алифатические амины формулы NR1 R2 R3, причем R1, R2, R3 одинаковы или различны и обозначают водород или C1C6 - алкил, или также такие ароматические амины, как пиридин, пиколин, хинолин. При преобразовании до диэфира фосфорной кислоты в данном случае можно добавлять необходимую здесь основную субстанцию одновременно, или также перед аминоспиртом, или перед солью аммониевого спирта. В любом случае для этой реакции необходим растворитель: т.е. если первая стадия реакции происходит без специального растворителя, то теперь растворитель необходимо добавлять. Молярное отношение хлорокиси фосфора к спирту с длинной цепью находится, например, в пределах от 1,5 : 1 до 0,8 : 1. Аминоспирт или соль аммониевого спирта используют, например, в отношении к спирту с длинной цепью в избытке (примерно 1,1 -1,5 - молярного избытка). Если реакция хлорокиси фосфора со спиртом с длинной цепью происходит в присутствии количество одного или несколько производных фосфолипидов общей формулы I в которой R обозначает алкильный радикал с неразветвленной или разветвленной цепью с 10-24 атомами углерода, которая может также содержать двойные или тройные связи, R1 и R2 независимо друг от друга обозначают водород или каждый неразветвленный, разветвленный циклический насыщенный или ненасыщенный алкильный остаток с 1 – 6 атомами углерода, который может также содержать Сl-, ОН- или NH2-группу и при этом два этих радикала могут быть соединены также в кольцо, А обозначает простую связь или одну из групп формул -СH2-CH2-CH2-O (II) -CH2-CH2-O (III) CH2-CH-O| CH3 (IV) -(CH2)8-O (V) -CH CH-CH2-O H2 C O CH2 (VI) причем группы (II) и -(VI) ориентированы таким образом, что атом кислорода соединен с атомом фосфора соединения (I), Х обозначает атом кислорода или серы, или NH, если А является простой связью, или обозначает атом кислорода или серы, если А является одной из групп (II) - (IV), «Y» равен нулю или является натуральным числом от 1 до 3, m и n независимо друг от друга равны 0 или являются натуральными числами при условии, что m + n составляет от 2 до 8, или их фармацевтически приемлемые соли. Первая стадия способа получения производного фосфолипидов, согласно изобретению, заключается в реакции хлорокиси фосфора со спиртом с длинной цепью в галогенированных или ароматических углеводородах, насыщенных циклических простых эфирах или ациклических простых эфирах. Первая стадия способа А заключается в реакции оксихлорида фосфора со спиртом с длинной цепью в галогенированных углеводородах, насыщенных циклических простых эфирах, ацикли 6 40567 основной субстанции, то количество основной субстанции составляют, например, от 1 до 3 молей, отнесенных к 1 молю РОСІ3. Для последующего преобразования в диэфир фосфорной кислоты использованное количество основной субстанции составляет, например, от 1 до 5 молей, отнесенных к 1 молю. Температура реакции преобразования хлорокиси фосфора со спиртом с длинной цепью находится в пределах от -30°С до + 30°С, предпочтительно от -15°С до +5°С, в частности, от -10°С до -5°С. Время реакции этого преобразования составляет, например, 0,5-5 часов, предпочтительно 1-3 часа, в частности, 1,5 -2 часа. Если реакция происходит в присутствии основной субстанции, то она протекает в общем случае быстро (примерно в течение 30 минут). Затем порциями или сразу добавляют аминоспирт или соль аммониевого спирта. В качестве солей аммониевого спирта во внимание принимаются соли с минеральными кислотами, (как, например, серная кислота, соляная кислота), кроме того соли с органическими кислотами, как например, уксусная кислота, паратолуолсульфокислота и им подобные. Эту стадию реакции проводят в растворителе. В качестве растворителя здесь во внимание принимаются такие же, которые применяются для преобразования фосфора со спиртом с длинной цепью, если это преобразование происходит в среде растворителя. Затем основную субстанцию растворяют в одном из указанных растворителей или добавляют по каплям без растворителя. Предпочтительно в качестве растворителей для основных субстанций в данном случае применяются: галогенированные углеводороды, простые насыщенные циклические эфиры, простые ациклические эфиры, насыщенные углеводороды с 5-10 атомами углерода, жидкие ароматические углеводороды или смеси вышеупомянутых растворителей. В данном случае речь идет о тех же растворителях, которые могут использоваться для преобразования хлорокиси фосфора со спиртом с длинной цепью. Благодаря добавлению основной субстанции повышается температура. Необходимо позаботиться о том, чтобы температура поддерживалась в пределах от 0 до 40°С, предпочтительно от 10 до 30°С, в частности от 15 до 20°С. Затем реакционную смесь еще перемешивают при температуре от 5 до 30°С, предпочтительно от 15 до 25°С (например, в течение от 1 часа до 40 часов, предпочтительно от 3 до 15 часов). Гидролиз реакционной исходной смеси осуществляют путем добавления воды, причем температуру следует поддерживать в пределах от 10 до 30°С, предпочтительно от 15 до 30°С, в частности от 15 до 20°С. Упомянутые выше гидролизные жидкости могут содержать также основные субстанции. В качестве таковых основных субстанций во внимание принимаются карбонаты и гидрокарбонаты щелочных и щелочноземельных металлов. Затем для завершения гидролиза реакционную смесь еще перемешивают в течение 0,5 - 4 часов, предпочтительно 1-3 часов, в частности 1,5 - 2,5 часов, при температуре от 10 до 30°С, предпочтительно от 15 до 25°С, в частности от 18 до 22°С. Затем реакционный раствор промывают с помощью смеси, состоящей из воды и спиртов (предпочтительно алифатических насыщенных спиртов с 1 - 4 атомами углерода), которая при необходимости может содержать еще основную субстанцию. Отношение в смеси воды к спирту может составлять, например, 5 - 0,5, предпочтительно 1-3 (об./об.). В качестве основных субстанций для промывочной жидкости во внимание принимаются, например, карбонаты и гидрокарбонаты щелочных и щелочноземельных металлов, а также аммиак (например, водный аммиак). Особенно предпочтительным является 3-%-ный раствор карбоната натрия в воде. Затем при необходимости можно осуществлять промывку реакционного раствора кислым раствором. Предпочтительно промывку кислым раствором осуществлять для удаления еще непрореагированных основных фракций реакционного раствора, в частности, при использовании в качестве растворителя метиленхлорида. Промывочный раствор состоит из смеси воды и спирта. Предпочтительно во внимание принимаются смеси их алифатических насыщенных спиртов с 1 - 4 атомами углерода, причем при необходимости может присутствовать еще и кислая субстанция. Отношение в смеси воды к спирту может составлять, например, 5 - 0,5, предпочтительно 1-3 (об. /об.). В качестве кислых субстанций для промывочной жидкости во внимание принимаются, например, минеральные и органические кислоты, например, соляная кислота, серная кислота, винная или лимонная кислота. Особенно предпочтительным является 10-%-ный раствор соляной кислоты в воде. Затем реакционный раствор еще раз промывают с помощью смеси из воды и спиртов. Предпочтительно во внимание принимаются смеси из алифатических насыщенных спиртов с 1 - 4 атомами углерода, причем при необходимости может присутствовать еще и основная субстанция. Отношение в смеси воды к спирту может составлять, например, 5 - 0,5, предпочтительно 1-3 (об./об.). Затем промытые фазы объединяют и высушивают обычным образом, а затем растворитель (предпочтительно при пониженном давлении, например, от 5 до 100 мбар) удаляют, при необходимости после добавления 150-1000 мл, предпочтительно 300 - 700 мл, в частности 450 550 мл алифатического спирта (отнесенных к 1 молю весовой части сухого продукта). В качестве спиртов во внимание принимаются предпочтительно насыщенные алифатические спирты с длиной цепи 1 и 5 атомов углерода. При этом особенно предпочтительным в качестве спирта являются n-бутанол, изопропанол. Спирто 7 40567 вую обработку проводят для полного удаления остатков воды и предотвращения пенообразования. Дальнейшую очистку продукта можно осуществлять, например, тем, что исходный продукт в горячем виде растворяют в этаноле, осадок отфильтровывают, обрабатывают с помощью комбинированного ионообменника, например, амберлита МВЗ, в этаноловом растворе. Вместо комбинированного ионообменника можно также использовать одновременно или последовательно все имеющиеся в продаже кислые или основные ионообменники. Затем раствор перекристаллизовывают из кетонов, как, например, ацетон или метилэтиловый кетон, в некоторых случаях извлекают путем его многократного смешивания с вышеупомянутыми растворителями горячими. Целесообразной может быть очистка продуктов с помощью колоночной хроматографии или мгновенной хроматографии на силикагеле. В качестве растворителей используются, например, смеси из хлороформа, метиленхлорида, метанола и 25%-ного раствора аммиака. Вариант способа В заключается в дополнительном алкилировании продуктов, которые были получены по способу А при использовании аминоспиртов. В качестве алкилирующих агентов могут использоваться, например, сложные метиловые эфиры р-толуолсульфокислоты или диметилсульфат. В качестве растворителей во внимание принимаются вышеупомянутые растворители. В качестве основных субстанций используют, например, карбонаты щелочных металлов. Взаимодействие осуществляют при повышенной температуре, например, при температуре кипения растворителей. Нижеследующие примеры поясняют изобретение, не ограничивая его. вода/метанол (1:1). Органическую фазу концентрируют, осадок в горячем виде растворяют в 300 мл этанола и после охлаждения фильтруют. Фильтрат перемешивают с 80 г ионообменника амберлита МВЗ, отфильтровывают и концентрируют. Осадок перекристаллизовывают из 300 мл метилового кетона, фильтруют на Нутч-фильтре и высушивают в вакууме с помощью Р2O5. Выход: 4,71 г (10%) Элементарный анализ: С Н N рассчитано: 65,26% 11,63% 2,62% получено: 64,38% 11,61% 2,73% 65,04% 11,80% 2,78% Хроматограмма тонкослойной хроматографии : (хлороформ/метанол/ 1 М ацетата натрия в 25% аммиака 70:40:10), Rf = 0,17 (1 бутанол/ ледяная уксусная кислота/ вода 40 : 10 : 10), Rf = =0,12. Температура плавления: 270-271oС (разложение) Вариант получения В 20,1 мл (0,22 моля) хлорокиси фосфора помещают в 100 мл метиленхлорида, охлаждают до температуры 5-10°С и при перемешивании в течение 30 минут смешивают с раствором 54,1 г (0,20 моля) октадеканола в 400 мл метиленхлорида и 70,5 мл пиридина. После одного часа дополнительного перемешивания по каплям добавляют 29,9 г (0,26 моля) 4-гидрокси-1-метилпиперидина в 80 мл пиридина. После 3 часов перемешивания при температуре 10°С реакционный раствор гидролизуют при охлаждении льдом с помощью 30 мл воды и дополнительно перемешивают в течение одного часа. Органическую фазу промывают соответственно с помощью 200 мл раствора вода / метанол (1:1), 3%-ного раствора соляная кислота / метанол (1 : 1) и раствора вода / метанол (1). Высушенную с помощью Na2SO4 органическую фазу концентрируют до помутнения и смешивают с 1 л метилэтилового кетона. Кристаллизат перекристаллизовывают из 1 л метилэтилового кетона, фильтруют на Нутч-фильтре и высушивают с помощью P2O5 в вакууме. Выход: 54,1 г (60%) октадецил - (1 - метилпиперидинио - 4 -ил) -фосфата. 98,1 г (0, 22 моля) октадецил - (1 - метилпиперидинио - 4-ил) - фосфата суспензируют в 500 мл абсолютного этанола и нагревают до кипения. При флегме добавляют в восемь порций попеременно в целом 71,8 г (0,39 моля) метилового эфира р-толуолсульфокислоты и 26,5 г (0,19 моля) карбоната калия в течение 2 часов. После окончания добавления продолжают нагревание при флегме еще в течение одного часа. После охлаждения отфильтровывают, концентрируют фильтрат до половины и смешивают раствор со 150 г влажного ионообменника амберлита МВЗ. После двухчасового перемешивания осуществляют с помощью смеси кизельгур/активированный уголь отсасывание на Нутч-фильтре, фильтрат концентрируют и кристаллизовывают в присутствии ацетона. Кристаллический осадок перекристаллизовывают из метилэтилового кетона и высушивают с помощью P2O5 в вакууме. Выход: 46,1 г (46%) октадецил -(1,1 - диметилпиперидинио - 4 -ил) -фосфата. Примеры Пример 1. Наименование (номенклатура Международного союза по чистой и прикладной химии (ЮПАК). Внутренняя соль 4-(((октадецилокси) гидроксифосфенил) окси) - 1,1 - диметилпиперидингидроксида. Краткое наименование: Октадецил - (1,1 - диметилпиперидинио-4ил)-фосфат. C25H25NO4P (461.66) Х 1/2 Н2O Вариант получения А 10,3 мл (0,11 моля) хлорокиси фосфора помещают в 100 мл хлороформа и охлаждают до температуры 5-10°С. В течение 30 минут по каплям добавляют при перемешивании 27.0 (0,10 моля) - 1 - октадеканола, растворяют в 100 мл хлороформа и 35 мл пиридина. После 30 минут дополнительного перемешивания при температуре 5-10°С смешивают с 39,1 г (0,13 моля) 4-гидрокси 1,1 - метилпиридинтосилата в одной порции. После добавления 40 мл пиридина и 30 мл диметилформамида смесь перемешивают в течение 24 часов при комнатной температуре. Затем гидролизуют с помощью 15 мл воды, дополнительно перемешивают в течение 30 минут, а органическую фазу промывают соответственно с помощью растворов: 200 мл вода/метанол (1:1), 200 мл 3%-ного раствора Nа2СО3 / метанол (1:1) и затем 200 мл 8 40567 Элементарный анализ: С Н N рассчитано: 65,26% 11,63% 2,62% получено: 65,18% 11,62% 2,68% 65,07% 11,07% 2,70% Температура плавления : 271 - 272°С (разложение). Пример 2: гексадецил-пиперидинио - 4 - ил - фосфат C21H44NO4P (405,558) 7,1 мл (77 миллимолей) хлорокиси фосфора растворяют в 50 мл сухого тетрагидрофурана и после охлаждения до температуры 5-10°С при перемешивании по каплям с раствором из 17 г (70 миллимолей) гексадеканола и 48 мл триэтиламина в 150 мл тетрагидрофурана. После окончания добавления раствор дополнительно перемешивают в течение 30 минут в ледяной ванне и затем доводят температуру до комнатной 10,1 г (100 миллимолей) 4-пиперидинола растворяют в 100 мл тетрагидрофурана, смешивают с 17 мл триэтиламина и при перемешивании по каплям добавляют реакционный раствор, так чтобы температура не превышала 40°С. После окончания добавления раствор кипятят в течение часа при флегме. Еще горячий раствор отфильтровывают от хлорида триэтиламмония и после охлаждения при перемешивании вливают в смесь лед - 2М-соляная кислота. Выпадающий в осадок при охлаждении в холодильном шкафу продукт впитывается в метиленхлорид, высушивание осуществляют с помощью MgSО4 и после концентрирования хроматографируют на силикагеле с помощью смеси метиленхлорид (метанол /25-%-ный аммиак (70 : 30 - 5). Содержащие продукт фракции объединяют и концентрируют. После перекристаллизации из метанола осуществляют высушивание с помощью P2О5 в вакууме. Выход: 10,0 г (35%) Элементарный анализ: О Н N рассчитано: 62,19% 10,94% 3,45% получено: 65,15% 11,14% 3,54% 62,41% 11,19% 3,34% Хроматограмма тонкослойной хроматографии: хлороформ / метанол / 25-%-ный аммиак (70:20-10) Rf = 0,42; (1 - бутанол / ледяная уксусная кислота / вода 40:10:10) Rf=0,33. Пример 3: гексадецил - (1,1 - диметилпиперидинио-4-ил)-фосфат С23Н52NО4Р (461,64) х Н2О 5,7 г (14 миллимолей) гексадецил-пиперидинио-4-ил-фосфата растворяют в 100 мл метанола и смешивают с 11,6 г (84 миллимоля) карбоната калия. При хорошем перемешивании в течение 30 минут по каплям добавляют 4,0 мл (42 миллимоля) диметилсульфата. Смесь дополнительно перемешивают в течение 4 часов при температуре 40°С, после охлаждения фильтруют и концентрируют. Осадок извлекают из раствора путем его многократного смешивания с горячим растворителем и после отсасывания на Нутч-фильтре растворяют в 100 мл 96%-ного этанола. Добавляют 15 г ионообменника амберлита МВЗ, перемешивают в течение 3 часов. После отфильтровывания производят концентрирование и дважды перекристаллизовывают из метиленэтилового ке тона. Сушку осуществляют с помощью Р2О5 в вакууме. Выход: 3,70 г (61%) Элементарный анализ: С Н N рассчитано: 61,17% 11,16% 3,10% получено: 60,89% 11,14% 2,99% 60,92% 11,26% 3,00% Хроматограмма тонкослойной хроматографии: (хлороформ / метанол / 25-%-ный аммиак 70:20:10) Rf = 0,28; (1 - бутанол / ледяная уксусная кислота / вода 40:10:10), Rf=0,13. Температура плавления: 230°С (разложение). Пример 4: эруцил - (1,1 - диметилпиперидинио - 4 - ил) - фосфат C29H58NO4P (515,765) x Н2O 10,3 мл (0,11 моля) хлорокиси фосфора помещают в 50 мл хлороформа и по каплям при температуре 5-10°С смешивают с раствором из 32,5 г (0,10 моля) эруцилового спирта и 32 мл пиридина в 100 мл хлороформа. После дополнительного перемешивания в течение получаса добавляют порцией в 39,1 г (0,13 моля) 4-гидрокси-1,1-диметилпиперидинсульфата. После добавления по каплям 40 мл пиридина температуру раствора доводят до комнатной и перемешивают в течение 3 часов. Затем гидролизуют с помощью 15 мл воды, дополнительно перемешивают в течение получаса и промывают соответственно с помощью 100 мл раствора вода - метанол (1:1), 100 мл 3%-ного раствора карбоната натрия/метанол (1:1), 100 мл 3%-ного раствора лимонная кислота/метанол (1:1), 100 мл раствора вода/метанол (1:1). Полученный после концентрирования органической фазы остаток извлекают с помощью ацетона и затем растворяют в 150 мл 96%-ного этанола. Этот раствор перемешивают в течение 3 часов с 20 г ионообменника амберлита МВЗ и отфильтровывают до получения светлого раствора с помощью кизельгура. После концентрирования проводят хроматографию на силикагеле с помощью смеси хлороформ/метанол/25%-ный аммиак 70 : 40 : 10. Содержащие продукт фракции объединяются и концентрируются в вакууме до сухости. Выход: 4,4 г (9%) Элементарный анализ С Н N рассчитано: 65,26% 11,63% 2,62% получено: 64,38% 11,61% 2,73% 65,04% 11,80% 2,78% Хроматограмма тонкослойной хроматографии: (хлороформ / метанол /1 М ацетата натрия в 25%-ном аммиаке 70:20:10) Rf = 0,30. Пример 5: гексадецил - (1,1 - диметилпиперидинио - 3 - ил) - фосфат С23Н48NO4Р (433,616) Н2O 10,3 мл (0,11 моля) хлорокиси фосфора помещают в 50 мл хлороформа и охлаждают до температуры 0-10°С 24,2 г (0,10 моля n-гексадеканола растворяют в 100 мл хлороформа, смешивают с 32 мл пиридина и в течение часа при охлаждении льдом по каплям добавляют в раствор хлорокиси фосфора. После дополнительного получасового перемешивания добавляют порцией в 39,2 г (0,13 моля) 3 гидрокси-1,1-диметилпиперидинтосилата и при комнатной температуре в течение 15 минут 9 40567 по каплям добавляют 40 мл пиридина. После перемешивания в течение 16 часов при комнатной температуре раствор гидролизуют с помощью 15 мл воды, перемешивают в течение получаса и промывают соответственно с помощью 100 мл раствора вода/метанол (1:1), 100 мл 3%-ного раствора карбоната натрия/ метанол (1:1), 100 мл раствора лимонная кислота/ метанол (1:1) и 100 мл раствора вода/метанол (1:1). Органическую фазу после высушивания с помощью сульфата натрия концентрируют. Остаток растворяют в 150 мл 96%-ного этанола, фильтруют и фильтрат смешивают с ионообменником амберлитом МВЗ. После отфильтровывания ионообменника раствор концентрируют, остаток с помощью ацетона доводят до кристаллизации и после отсасывания на Нутч-фильтре высушивают с помощью P2O5 в вакууме. Выход: 13,5 г (31%) Элементарный анализ: С Н N рассчитано: 61,17% 11,1% 3,10% получено: 60,78% 11,41% 2,87% 60,85% 11,31% 2,86% Хроматограмма тонкослойной хроматографии: (хлороформ / метанол / 1 М ацетат натрия в 25%-ном аммиаке 70:40:10) Rf = 0,37 Пример 6: октадецил - (1,1 - диметилпиперидинио - 3 - ил) - фосфат C25H52NO4P (461,670) х 1/2 H2O Получение аналогично примеру 5 из 10,3 мл (0,11 моля) хлорокиси фосфора, 27,0 г (0,10 моля) октадеканола, 32+40 мл пиридина и 39,2 г (0,13 моля) - 3-гидрокси - 1,1-диметилпиперидинтозилата. Выход: 18,7 г (40%) Элементарный анализ: С Н N рассчитано: 63,80% 11,35% 2,98% получено: 63,38% 11,72% 2,63% 63,61% 11,98% 3,61% Хроматограмма тонкослойной хроматографии: (хлороформ / метанол / 1 М ацетата натрия в 25%-ном аммиаке 70 : 40 : 10) Rf = 0,35. Пример 7: гексадецил -(1,1 - диметилпиперидинио - 2 - ил) - метилфосфат C24H50NO4P (447,643) х 1/2 Н2О Получение аналогично примеру 5 из 10,3 мл (0,11 моля) хлорокиси фосфора, 24,2 г (0,10 моля) гексадеканола, 32 + 40 мл пиридина и 41,0 г (0,13 моля) 2 - гидроксиметил - 1,1-диметилпиперидинтозилата. Выход: 22,9 г (51%) Элементарный анализ: С Н N рассчитано: 63,13% 11,26% 3,07% получено: 63,69% 11,73% 3,04% 63,75% 11,71% 3,04% Хроматограмма тонкослойной хроматографии: (хлороформ / метанол / 1 М ацетат натрия в 25%-ном аммиаке 70 : 40 : 10) Rf = 0,47. Пример 8: октадецил - (1,1 - диметилпиперидинио - 2 - ил) метилфосфат С26Н54NO4Р (475,697) х 1/2 Н2О Получение аналогично примеру 5 из 10,3 мл (0,11 моля) хлорокиси фосфора, 27,0 г (0,10 моля) октадеканола, 32 + 40 мл пиридина и 41,0 г (0,13 моля) 2-гидроксиметил-1,1-диметилпиперидинтозилата. Выход : 23,9 г (50%) Элементарный анализ: С Н N рассчитано: 64,43% 11,44% 2,89% получено: 64,50% 11,61% 2,67% 64,11% 11,49% 2,77% Хроматограмма тонкослойной хроматографии : (хлороформ / метанол / 1 М ацетата натрия в 25%-ном аммиаке 70:40:10) Rf = 0,47. Пример 9: гексадецил - (1,1 - диметилпиперидинио - 3 - ил) -метилфосфат C24H50NО4P (447,643) х 1 Н2О Получение аналогично примеру 5 из 10,3 мл (0,11 моля) хлорокиси фосфора, 24,2 г (0,10 моля) гексадеканола, 32+40 мл пиридина и 41,0 г (0,13 моля) 3-гидроксиметил - 1,1-диметилпиперидинтозилата. Выход : 17,2 г (39%) Элементарный анализ: С Н N рассчитано: 61,91% 11,26% 3,01% получено: 62,32% 12,21% 2,86% 61,79% 11,96% 2,98% Хроматограмма тонкослойной хроматографии : (хлороформ / метанол / 1М ацетата натрия в 25%-ном аммиаке 70:40:10) Rf=0,29. Пример 10: октадецил - (1,1 - диметилпиперидинио - 3 - ил) - метилфосфат С26Н54NO4Р (475,697) х Н2O Получение аналогично примеру 5 из 10,3 мл (0,11 моля) хлорокиси фосфора, 27,0 г (0,10 моля) октадеканола, 32+40 мл пиридина и 41,0 г (0,13 моля) 3гидроксиметил -1,1 -диметилпиперидинтозилата. Выход: 16,7 г (35%) Элементарный анализ: С Н N рассчитано: 63,25% 11,43% 2,84% получено: 62,98% 12,21% 2,76% 63,67% 12,47% 2,80% Хроматограмма тонкослойной хроматографии: (хлороформ / метанол / 1 М ацетата натрия в 25%-ном аммиаке 70:40:10) Rf = 0,30. Пример 11: Тетрадецил- (1,1 - диметилгексагидроазефинио - 4 - ил) -фосфат С22Н46NO4Р(419,54)х Н2O Получение аналогично примеру 5 из 9,6 г (45 миллимолей) тетрадеканола, 4,6 мл (50 миллимолей) хлорокиси фосфора, 10+20 мл пиридина и 21,3 г (67,5 миллимоля) гидрокси-1,1-диметилгексагидроазепинтозилата. Очистку осуществляют с помощью мгновенной хроматографии на силикагеле с использованием смеси метиленхлорид/метанол/25%-ный аммиак 70 : 40 : 10. Выход: 2,70 г (15%) Элементарный анализ: С Н N рассчитано: 60,40% 11,05% 3,20% получено: 60,47% 11,29% 3,63% 60,78% 11,52% 3,68% Хроматограмма тонкостенной хроматографии : (хлороформ / метанол / 1 М ацетата натрия в 25%-ном аммиаке 70:40:10) Rf = 0,08 Пример 12: гексадецил - (1,1 - диметилгексагидроазефинио - 4 - ил) - фосфат 10 40567 C24H48NO4P (445,62) Получение аналогично примеру 5 из 10,8 г (45 миллимолей) гексадеканола, 4,6 мл (50 миллимолей) хлорокиси фосфора, 10+20 мл пиридина и 21,3 г (67,5 миллимолей) 4 - гидрокси - 1,1-диметилгексагидроазефинтозилата. Очистку осуществляют с помощью мгновенной хроматографии на силикагеле с использованием смеси метиленхлорид/метанол/25%-ный аммиак 70 : 30 : 10. Выход : 5,0 г (25%) Элементарный анализ: С Н N рассчитано: 64,69% 10,86% 3,14% получено: 63,90% 11,54% 3,22% 64,08% 11,59% 3,24% Хроматограмма тонкослойной хроматографии: (хлороформ / метанол / 25%-ный аммиак). Rf = 0,10; (1 - бутанол / ледяная уксусная кислота / вода 40:10:10), Rf = 0,10. Температура плавления : выше 250°С (разложение). Пример 13: октадецил - (1,1 - диметилгексагидроазефинио - 4 - ил) - фосфат С26Н54NO4Р (475,695) х 1/2 H2O Получение аналогично примеру 5 из 12,1 г (45 миллимолей) октадеканола, 4,6 мл (50 миллимолей) хлорокиси фосфора, 10+20 мл пиридина и 21,3 г (67,5 миллимолей) 4 - гидрокси - 1,1-диметилгексагидроазефинтозилата. Очистку осуществляют с помощью мгновенной хроматографии на силикагеле с использованием смеси метиленхлорид/метанол/25%-ный аммиак 70:30:10. Выход: 5,5 г (26%) Элементарный анализ: С Н N рассчитано: 64,43% 11,44% 2,89% получено: 64,54% 11,64% 2,82% 64,66% 11,58% 2,64% Хроматограмма тонкослойной хроматографии: (хлороформ / метанол / 1 М ацетата натрия в 25%-ном аммиаке 70:40:10) Rf = 0,22. Температура плавления: выше 250°С (разложение). Пример 14: цис -D9- октадецинил-(1,1-диметилгексагидроазефинио -4 - ил) - фосфат С26Н52NO4Р (473,679) х Н2O Получение аналогично примеру 5 из 12,1 г (45 миллимолей) цис -D9- октадеканола, 4,6 мл (50 миллимолей) хлорокиси фосфора, 10+20 мл пиридина и 21,3 г (67,5 миллимолей) 4 - гидрокси 1,1-диметилгексагидроксиазефинтозилата. Очистку осуществляют с помощью мгновенной хроматографии с использованием смеси метиленхлорид/метанол/25-%ный аммиак 70 : 30 : 10. Выход: 4,5 г (21%) Элементарный анализ: С Н N рассчитано: 63,51% 11,07% 2,85% получено: 64,05% 11,21% 3,10% 63,80% 11,06% 3,06% Хроматограмма тонкослойной хроматографии: (хлороформ / метанол / 25%-ный аммиак 70:40:10) Rf = 0,28; (1 - бутанол / ледяная уксусная кислота / вода 40 : 10 : 10), Rf=0,10. Пример 15: эйкозил- (1,1 - диметилгексагидроазефинио - 4 - ил) -фосфат С28Н58NО4Р (503,754) х H2O Получение аналогично примеру 5 из 13,4 г (45 миллимоля) эйкозанола, 4,6 мл (50 миллимоля) хлорокиси фосфора, 10+20 мл пиридина и 21,3 г (67,5 миллимоля) 4 - гидрокси -1,1 -диметилгексагидроазефинтозилата. Очистку осуществляют с помощью мгновенной хроматографии на силикагеле с использованием смеси метиленхлорид/метанол/25%-ный аммиак 70 : 30 : 10. Выход: 5,7 г (25%) Элементарный анализ: С Н N рассчитано: 64,46% 11,59% 2,68% получено: 63,51% 11,48% 2,95% 64,00% 11,79% 2,91% Хроматограмма тонкослойной хроматографии: (хлороформ / метанол / 25%-ный аммиак 70 : 40 : 10) Rf = 0,12. Пример 16: эруцил- (1,1 - диметилгексагидроазефинио - 4 - ил) -фосфат С30Н60NО4Р (529,789) х H2O Получение аналогично примеру 5 из 16,2 г (50 миллимолей) эруцилового спирта, 5,1 мл (55 миллимолей) хлорокиси фосфора, 18+30 мл пиридина и 20,5 г (65 миллимолей) 4 - гидрокси - 1,1диметилгексагидроазефинтозилата. Очистку осуществляют с помощью мгновенной хроматографии на силикагеле с использованием смеси метиленхлорид/метанол/25%-ный аммиак 70 : 30 : 10. Выход: 4,1 г (15%) Элементарный анализ: С Н N рассчитано: 65,78% 11,41% 2,56% получено: 65,76% 12,01% 2,97% 65,82% 11,63% 2,96% Хроматограмма тонкослойной хроматографии : (хлороформ / метанол / 1 М ацетата натрия в 25%-ном аммиаке 70 : 40 : 10) Rf = 0,30. Пример 17: октадецил - (1,1 - диметилпирролидинио - 3 - ил) -фосфат С24Н50NO4Р (447,643) х 1/2 Н2O Получение аналогично примеру 5 из 3,25 г (12 миллимолей) октадеканола, 1,21 мл (13 миллимолей) хлорокиси фосфора, 3,7+4,8 мл пиридина и 4,31 г (15 миллимолей) гидрокси - 1,1-диметилпирролидинтозилата. Очистка исходного продукта осуществлялась путем растворения в 96-%-ном этаноле и обработки с помощью ионообменника амберлита МВЗ. Выход: 1,31 г (25%) Элементарный анализ: С Н N рассчитано: 63,13% 11,26% 3,07% получено: 62,99% 11,28% 2,80% 62,74% 11,27% 2,89% Хроматограмма тонкослойной хроматографии: (хлороформ / метанол / 1 М ацетата натрия в 25%-ном аммиаке 70 : 40 : 10) Rf = 0,25. Пример 18: гексадецил -2- (1,1 - диметилпирролидинио - 2 - ил) -фосфат C24H50NO4P (447,643) х Н2O Получение аналогично примеру 5 из 9,21 г (38 миллимолей) гексадеканола, 3,9 мл (42 миллимоля) 11 40567 хлорокиси фосфора, 13 + 16 мл пиридина и 15,8 г (50 миллимолей) 2-(2-гидроксиэтил)-1,1-диметилпирролидинтозилата. Очистку осуществляли путем растворения в 90%-ном растворе этанола и обработки с помощью ионообменника амберлита МВЗ. Выход: 6,0 г (35%) Элементарный анализ: C Н N рассчитано: 61,91% 11,26% 3,01% получено: 61,82% 11,69% 3,21% 61,93% 11,86% 3,28% Хроматограмма тонкослойной хроматографии: (хлороформ/метанол/ 1 М ацетата натрия в 25%-ном аммиаке 70 : 40 : 10), Rf = 0,38. Пример 19: Октадецил-2- (1,1- диметилпирролидинио-2-ил) этил-фосфат C26H54NO4P (475,697) х 1/2 H2O Получено аналогично примеру 5 из 10,3 г (38 миллимолей) октадеканола, 3,9 мл (42 миллимоля) хпорокиси фосфора, 13 + 16 мл пиридина и 15,8 г (50 миллимолей) 2-(2-гидроксиэтил) -1,1 диметилпирролидинтозилата. Очистка осуществлялась путем растворения в 96%-ном этаноле и обработки с помощью ионообменника амберлита МВЗ. Выход: 7,8 г (43%) Элементарный анализ: C H N рассчитано: 64,43% 11,44% 2,89% получено: 64,69% 11,77% 2,64% 64,84% 11,88% 2,69% Хроматограмма тонкослойной хроматографии: хлороформ/метанол/1 М ацетата натрия в 25%-ном аммиаке 70 : 40 : 10), Rf = 0,35. Пример 20: гексадецил -(1,1 - диметилпирролидинио-2-ил) метилфосфат С23H48NO4Р (433,616) *S H2O Получение аналогично примеру 5 из 9,21 г (38 миллимолей) гексадеканола, 3,9 мл (42 миллимоля) хлорокиси фосфора, 13 + 16 мл пиридина и 15,1 г (50 миллимолей) 2 - гидроксиметил -1,1- диметилпирролидинтозилата. Очистку осуществляли путем растворения в 96%-ном этаноле и обработки с помощью ионообменника амберлита МВЗ. Выход: 8,3 г (51%) Элементарный анализ: С Н N рассчитано: 62,41% 11,16% 3,16% получено: 62,09% 11,48% 3,01% 62,25% 11,66% 3,09% Хроматограмма тонкослойной хроматографии : (хлороформ/метанол/1 М ацетата натрия в 25%-ном аммиаке 70 : 40 : 10) Rf = 0.33 Пример 21: октадецил -(1,1- диметилпирролидинио-2-ил) метилфосфат С25Н52NO4Р (461,67) * 1/2 H2O Получение аналогично примеру 5 из 10,3 г (38 миллимолей) октадеканола, 3,9 мл (42 миллимоля) хлорокиси фосфора, 13+16 мл пиридина и 15,1 г (50 миллимолей) 2-гидроксиметил - 1,1-диметилпирролидинтозилата. Очистку осуществляли путем растворения в 96%-ном этаноле и обработки с помощью ионообменника амберлита МВЗ. Выход: 9,0 г (52%) Элементарный анализ: С Н N рассчитано: 63,80% 11,35% 2,98% получено: 63,13% 11,57% 2,84% 63,55% 11,66% 2,82% Хроматограмма тонкослойной хроматографии: (хлороформ/метанол/ 1 М ацетата натрия в 25%-ном аммиаке 70:40:10) Rf = 0.35 Пример 22: Гексадецил - (1-хинуклидиниоЗ-ил)-фосфат С24Н48NO4Р (445,64) * 1,5 H2O 2,7 мл (30 миллимолей) хлорокиси фосфора растворяют в 25 мл хлороформа, охлаждают до 510oС и в течение одного часа по каплям смешивают с раствором из 6,4 г (26 миллимолей) гексадеканола и 10 мл пиридина в 50 мл хлороформа. После получасового дополнительного перемешивания при комнатной температуре добавляют раствор из 4,5 г (35 миллимолей) З-гидроксихинуклидина и 5 мл пиридина в 10 мл хлороформа. После перемешивания в течение 5 часов при комнатной температуре раствор гидролизуют с помощью 15 мл воды и дополнительно перемешивают в течение получаса. Затем дважды осуществляют промывание соответственно с помощью 100 мл раствора вода/метанол (1:1) и концентрируют органическую фазу после сушки с помощью сульфата магния до сухости. Остаток хроматографируют на силикагеле с использованием смеси метиленхлорид/ метанол 80:25 и затем метиленхлорид/метанол/25%-ный аммиак. Содержащие продукт фракции очищают, выпаривают до сухости и с целью кристаллизации смешивают с ацетоном. Сушку осуществляют в вакууме с помощью P2O5. Выход: 4,95 г (44%) гексадецил - (хинуклидинио -3 ил) - фосфат. 4,95 г (11,5 миллимолей) гексадецил - (хинуклидино-3-ил)-фосфата растворяют в 30 мл метанола, смешивают с 13,7 г (69 миллимолей) карбоната калия, 8,5 мл воды и по каплям при хорошем перемешивании с раствором из 3,3 мл (35 миллимолей) диметисульфата в 5 мл метанола. После перемешивания в течение 14 часов при комнатной температуре неорганические соли отфильтровывают, фильтрат концентрируют до сухости, а остаток растворяют в метиленхлориде. После фильтрования хроматографируют на силикагеле с использованием смеси метиленхлорид/метанол/25%ный аммиак 70 : 30 : 5. Содержащие продукт фракции объединяют, выпаривая до сухости, и для кристаллизации смешивают с ацетоном. Сушку осуществляют в вакууме с помощью Р2О5. Выход: 2,7 г (48%) Элементарный анализ: С Н N рассчитано: 60,99% 10,88% 2,96% получено: 61,38% 11,04% 3,29% 61,46% 11,22% 3,25% Хроматограмма тонкослойной хроматографии: (хлороформ/метанол/ 25%-ный аммиак 70 : 40 : 10) Rf = 0,44 Пример 23: Октадецил-(1-метилхинуклидинио-3-ил)-фосфат С26Н52NO4Р (473,68) * 2 H2O Получение аналогично примеру 5 из 18,3 г (67,5 миллимолей) октадеканола, 7,0 мл (75 миллимоля) хлорокиси фосфора, 18+20 мл пиридина 12 40567 и 28,3 г (90 миллимолей) З-гидрокси-1-метилхинуклидинтозилата. Очистку осуществляли путем растворения в 96%-ном этаноле и обработки с помощью ионообменника амберлита МВЗ. Выход: 18,4 г (57%) Элементарный анализ: С Н N рассчитано: 61,27% 11,07% 2,75% получено: 61,27% 10,91% 2,45% 61,95% 11,23% 2,51% Хроматограмма тонкослойной хроматографии: (хлороформ/метанол/ 1М ацетата натрия в 25%-ном аммиаке 70:40:10). Rf= 0,37 (1-бутанол/ледяная уксусная кислота/ вода 40:10:10), Rf = 0,13 Пример 24: гексадецил -(1,1 - диметилтропанио-4-ил)-фосфат C25H50NО4P (459,654) * Н2О Получение аналогично примеру 5 из 12,1 г (50 миллимолей) гексадеканола, 5,1 мл (55 миллимолей) хлорокиси фосфора, 17+40 мл пиридина и 21,3 г (65 миллимолей) 4-гидрокси - 1,1-тропантозилата. Очистку осуществляли путем растворения в 96%-ном этаноле и обработки с помощью ионообменника амберлита МВЗ и перекристаллизации из ацетона. Выход: 11,3 г (49%) Элементарный анализ: С Н N рассчитано: 62,86% 10,97% 2,93% получено: 62,45% 11,52% 2,82% 62,58% 11,52% 2,75% Хроматограмма тонкослойной хроматографии: (хлороформ/метанол/ 1М ацетата натрия в 25%-ном аммиаке 70:40:10). Rf= 0,28. Пример 25: октадецил - (1,1 - диметилтропанио-4-ил )-фосфат C27H54NО4P (487,708) Получение аналогично примеру 5 из 13,5 г (50 миллимолей) октадеканола, 5,1 мл (55 миллимолей) хлорокиси фосфора, 17 + 20 мл пиридина и 21,3 г (65 миллимолей) 4-гидрокси-1,1-диметилтропантозилата. Очистка осуществлялась путем растворения в 96%-ном этаноле и обработки с помощью ионообменника амберлита МВЗ. Выход: 10,7 г (44%) Элементарный анализ: С Н N рассчитано: 66,49% 11,16% 2,87% получено: 65,72% 11,48% 2,64% 66,27% 11,78% 2,65% Хроматограмма тонкослойной хроматографии: (хлороформ/метанол/ 1М ацетата натрия в 25%-ном аммиаке 70 : 40 : 10). Rf= 0,22 Пример 26: инъекционный раствор. Берут 500 г вещества по Примеру 1 на 40 литров 9% водного раствора хлористого натрия и размешивают при комнатной температуре до растворения вещества. Полученный таким образом раствор фильтруют и разливают в стеклянные ампулы. Наполненные и закупоренные ампулы стерилизуют паром при 121°С в течение 15 мин. Одна ампула содержит 50 мг вещества по Примеру 1. Пример 27: гель для местного противоподагрического применения. Берут 1,1 г траганта (вы сушенного астрагала) и растирают с 16,4 г глицерола. Растирку диспергируют в 80 г очищенной воды. К этой смеси добавляют 0,05 г хлоргексидиндиацетата, 0,07 г метил-4-гидроксибензоата, 0,03 г пропил-4-гидроксибензоата и 5 г вещества по Примеру 1, после чего смесь перемешивают. Непосредственно после этого доливают очищенную воду до 100 г. Полученную таким образом дисперсию оставляют на три часа при комнатной температуре. Образующийся при этом светлый гель содержит 5% весовых частиц вещества по Примеру 1. Пример 28: суппозитории. Берут 100 г твердого жира типа "Витепсоль" Н15, подогревают до температуры примерно 50°С растапливают. К полученному жиру добавляют 100 г твердого жира типа "Витепсоль" Е75 и эту смесь тщательно перемешивают. Непосредственно после этого к расплавленному жиру добавляют 10 г вещества по Примеру 1 и перемешивают при температуре 60°С. После этого еще теплый расплав заливают в подходящую неохлажденную суппозиторную форму. Как только залитая форма наполовину затвердеет, лишнюю массу соскабливают. После полного охлаждения форма может быть открыта, а готовые суппозитории извлечены из формы. Один суппозиторий весит 2,1 г и содержит 100 мг вещества по Примеру 1. Пример 29: таблетки. Берут 500 г вещества по Примеру 1, 500 г кукурузного крахмала и 40 г высокодисперсного оксида кремния, просеивают и после этого смешивают в течение 20 минут в подходящем смесителе. Смесь гранулируют с 220 г воды, пропускают через сито с отверстиями размером 2,5 мм и высушивают на решетке при 40°С в течение 65 минут. Полученный таким образом гранулят вместе с 620 г кальцийгидрогенфосфата и 10 г высокодисперсного оксида кремния просеивают и смешивают в течение 30 минут. После этого добавляют 10 г стеарата магния и все это еще 5 минут перемешивают. Изготовленную таким образом пресс-массу прессуют в таблетки весом до 250 г. Одна таблетка содержит 50 мг вещества по Примеру 1. Пример 30: пример изготовления фильмтаблеток, растворяющих желудочный сок. В 400 г нагретой воды вносят и растворяют путем размешивания 31,25 г полиэтиленгликоля 600 и 75 г гидроксипропилметилцеллюлозы. В подходящем сосуде гомогенизируют 93,2 г воды вместе с 0,63 г симетикона и 25 г диоксида титана. Обе жидкости после охлаждения до комнатной температуры смешивают одна с одной. Полученная суспензия дает в конечном итоге 2500 г зерен, которые получаются блестящими согласно Примеру 4. Изготовленные таким образом фильм-таблетки весят в среднем 256 мг и содержат в среднем 50 мг вещества по Примеру 1. Подобным образом можно обрабатывать также и другие действующие вещества, описанные здесь, для получения фармацевтических композиций. Само собой разумеется, что лекарственные средства могут также быть изготовлены и с другими действующими веществами, причем содержание действующего вещества предпочтительно находится в интервале 50 мг - 250 мг. 13 40567 Тираж 50 екз. Відкрите акціонерне товариство «Патент» Україна, 88000, м. Ужгород, вул. Гагаріна, 101 (03122) 3 – 72 – 89 (03122) 2 – 57 – 03 14
ДивитисяДодаткова інформація
Назва патенту англійськоюPhospholipides derivatives, method for producing phospholipides derivatives, pharmaceutical composition and method for producing thereof
Автори англійськоюNYOSNER Gerhard, KUTSCHER Berhard, Engel Jurgen, SHCHUMACHER Wolfgang, STEKAR Yurii, CHILGARD Peter
Назва патенту російськоюПроизводные фосфолипидов, способ получения производных фосфолипидов, фармацевтическая композиция и способ ее получения
Автори російськоюНЕСНЕР Герхард, КУТШЕР Берхард, Энгел Юрген, ШУМАХЕР Вольфганг, СТЕКАР Юрий, ХИЛГАРД Петер
МПК / Мітки
МПК: C07F 9/572, C07F 9/553, C07F 9/59, A61P 35/00, C07F 9/6561, A61K 31/685
Мітки: фармацевтична, композиція, похідні, фосфоліпідів, похідних, спосіб, отримання
Код посилання
<a href="https://ua.patents.su/14-40567-pokhidni-fosfolipidiv-sposib-otrimannya-pokhidnikh-fosfolipidiv-farmacevtichna-kompoziciya-ta-sposib-otrimannya.html" target="_blank" rel="follow" title="База патентів України">Похідні фосфоліпідів, спосіб отримання похідних фосфоліпідів, фармацевтична композиція та спосіб її отримання</a>