Конденсовані циклічні сполуки піридину
Номер патенту: 109550
Опубліковано: 10.09.2015
Автори: Сугано Юкіхіто, Нісігакі Фусако, Терасака Тадасі, Камеда Мінору, Хонда Суго, Мацусіма Юдзі, Терасава Такесі, Усуда Хіроюкі
Формула / Реферат
1. Сполука формули (І) або її сіль
 , (I)
, (I)
де
X і Y є СН, С-нижчим алкілом або N, де або X, або Y є N,
W є -NH-, -N(нижчим алкілом)-, -О-, -S-, -S(O)- або -S(O)2-,
R1 є циклоалкілом, який може бути заміщений одним або більше замісниками з групи D, арилом, який може бути заміщений одним або більше замісниками з групи D, ароматичним гетероциклом, який може бути заміщений одним або більше замісниками з групи D, неароматичним гетероциклом, який може бути заміщений одним або більше замісниками з групи D,
R2 є -Z-NR3R4 або Z-циклічним аміно, який може бути заміщений одним або більше замісниками з групи D, група D включає
(1) галоген,
(2) -ОН і -SH,
(3) ціано і нітро,
(4) циклоалкіл, -O-циклоалкіл і -С(О)-циклоалкіл, які можуть бути відповідно заміщені однією або більше групами, що включають нижчий алкіл, галоген, -ОН, -О-нижчий алкіл, -О-галогенонижчий алкіл та галогенонижчий алкіл,
(5) арил, -О-арил і -С(О)-арил, які можуть бути заміщені однією або більше групами, що включають нижчий алкіл, галоген, -ОН, -О-нижчий алкіл, -О-галогенонижчий алкіл і галогенонижчий алкіл,
(6) ароматичний гетероцикл, -О-ароматичний гетероцикл і -С(О)-ароматичний гетероцикл, які можуть бути заміщені однією або більше групами, що включають нижчий алкіл, галоген, -ОН, -О-нижчий алкіл, -О-галогенонижчий алкіл та галогенонижчий алкіл,
(7) неароматичний гетероцикл, -О-неароматичний гетероцикл і -С(О)-неароматичний гетероцикл, які можуть бути заміщені однією або більше групами, що включають нижчий алкіл, галоген, -ОН, -О-нижчий алкіл, -О-галогенонижчий алкіл та галогенонижчий алкіл,
(8) -С(О)-нижчий алкіл, -С(О)О-нижчий алкіл, -NH-С(О)-нижчий алкіл, -NH-нижчий алкіл, -N(нижчий алкіл)2, -С(О)-NH-нижчий алкіл і -С(О)-N(нижчий алкіл)2, де групи нижчого алкілу можуть бути відповідно заміщені однією або більше групами, що включають галоген, -ОН, -О-нижчий алкіл, -О-галогенонижчий алкіл,
(9) -NH2- і -C(O)-NH2,
(10) -S-нижчий алкіл, -S(О)-нижчий алкіл і -S(О)2-нижчий алкіл, де групи нижчого алкілу можуть бути відповідно заміщені однією або більше групами, що включають галоген, -ОН, -О-нижчий алкіл, -О-галогенонижчий алкіл, і
(11) нижчий алкіл і -О-нижчий алкіл, які можуть бути відповідно заміщені групами, що включають замісники, описані в (1)-(10) вище; частина А є групою, представленою формулою (II), (III) або (IV):
 ,
,
 ,
,
 ,
,
(II)
(III)
(IV)
R3 є Н або нижчим алкілом,
R4 є нижчим алкілом, заміщеним однією або більше групами, вибраними з групи, що включає -ОН-, -О-нижчий алкіл, галоген, циклоалкіл, ціано, -S-нижчий алкіл, -S(О)-нижчий алкіл, -S(О)2-нижчий алкіл і -О-галогенонижчий алкіл,
R5 є однаковими або різними і є нижчим алкілом або галогеном,
Z є однаковими або різними і є -С(О)-, -СН2- або -S(O)2-;
m є однаковими або різними і дорівнюють цілому числу від 0 до 10, і
n є однаковими або різними і дорівнюють цілому числу від 0 до 2.
2. Сполука за п. 1 або її сіль, де
R2 є групою, представленою формулою (V), (VI) або (VII), R6 однакові або різні є нижчим алкілом, який може бути заміщений однією або більше групами, вибраними з -ОН, -О-нижчого алкілу, галогену, циклоалкілу, ціано, -S-нижчого алкілу, -S(О)-нижчого алкілу, -S(О)2-нижчого алкілу і -О-галогенонижчого алкілу, -ОН, -О-нижчого алкілу, галогену, циклоалкілу, ціано, -О-нижчого алкілену-ОН, -S-нижчого алкілу, -S(О)-нижчого алкілу, -S(О)2-нижчого алкілу і -О-галогенонижчого алкілу,
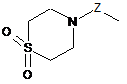 ,
,
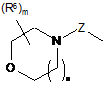 ,
,
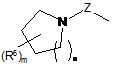 .
.
(V)
(VI)
(VII)
3. Сполука за п. 2 або її сіль,
де R2 є групою, представленою формулою (V) або (VI), Z є -С(О)-, W є -NH або О- і частина А є групою, представленою формулою (II) або (III).
4. Сполука за п. 3 або її сіль,
де X є СН, Y є N, R1 є і) циклоалкілом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген і -ОН, або іі) арилом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген, галогенонижчий алкіл, -О-нижчий алкіл і -О-галогенонижчий алкіл, ііі) неароматичним гетероциклом, який може бути заміщений однією або більше групами, вибраними із групи, що включає нижчий алкіл, галоген і -ОН, частина А є групою, представленою формулою (III), де n дорівнює 0 або 1, і m дорівнює 0, n в формулі (VI) дорівнює 1 або 2, і m в формулі (VI) дорівнює 0.
5. Сполука за п. 4 або її сіль,
де R1 є фенілом, який може бути заміщений однією або більше групами, вибраними з групи, що включає галоген, -О-галогенонижчий алкіл і галогенонижчий алкіл, R2 є групою, представленою формулою (V), і W є -NH-.
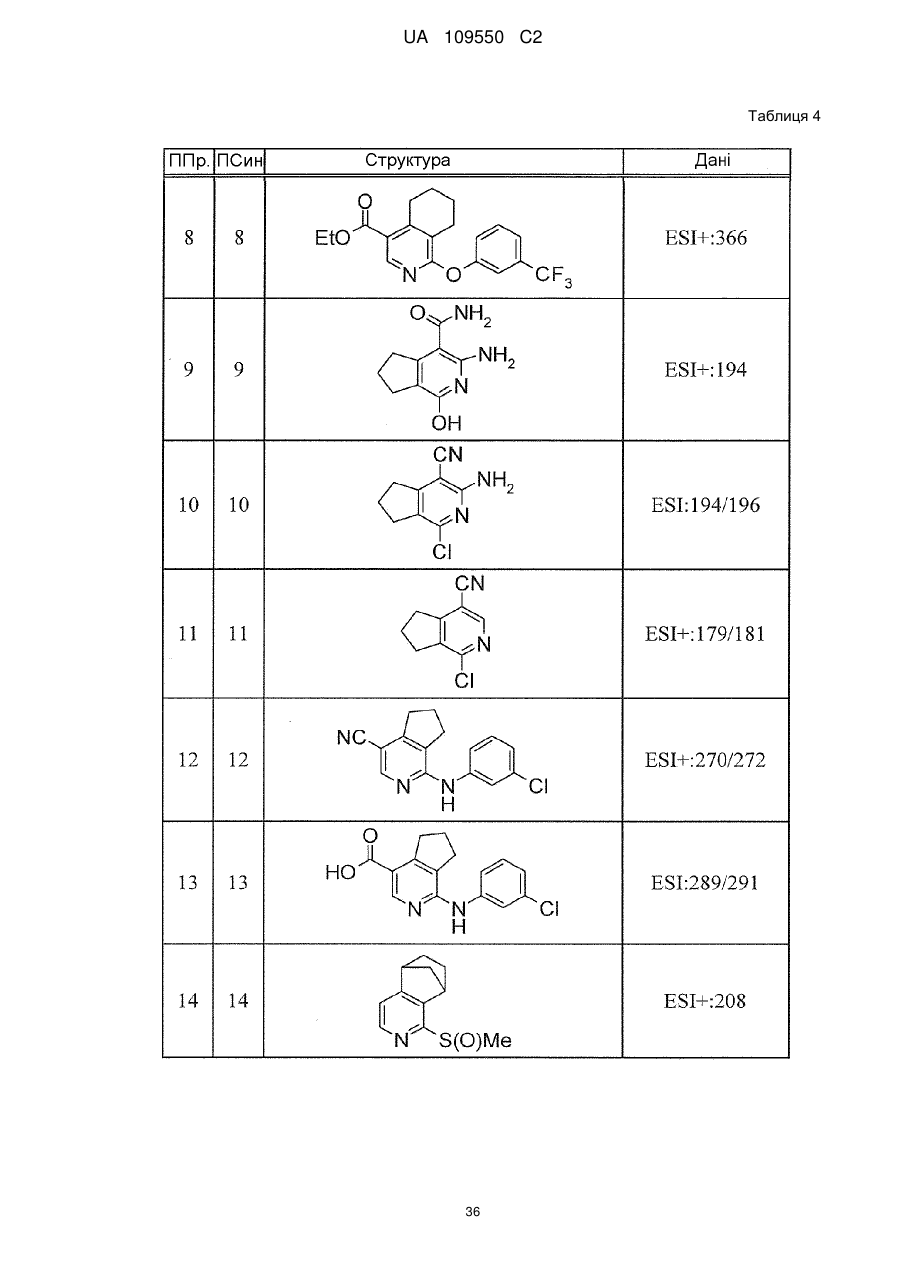
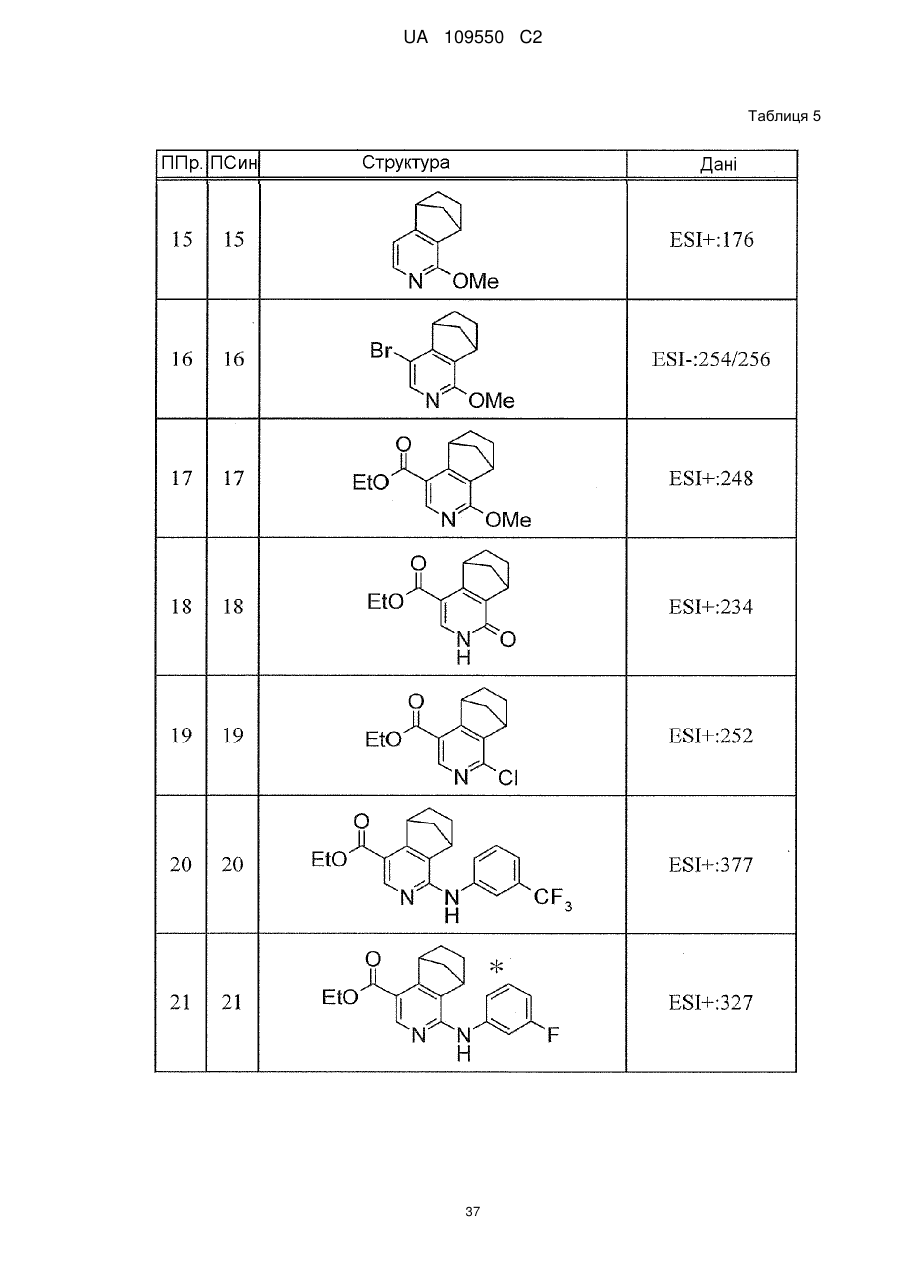
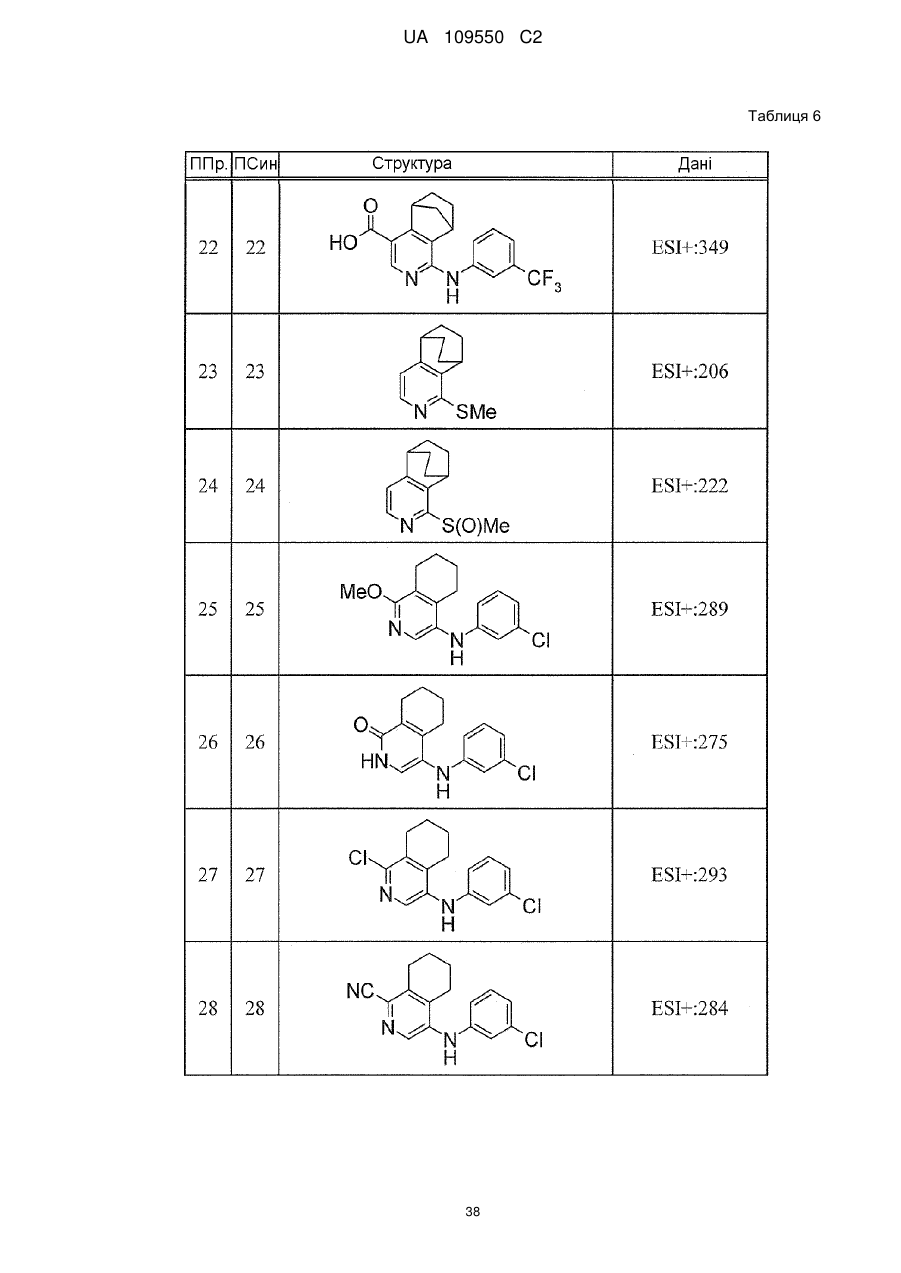
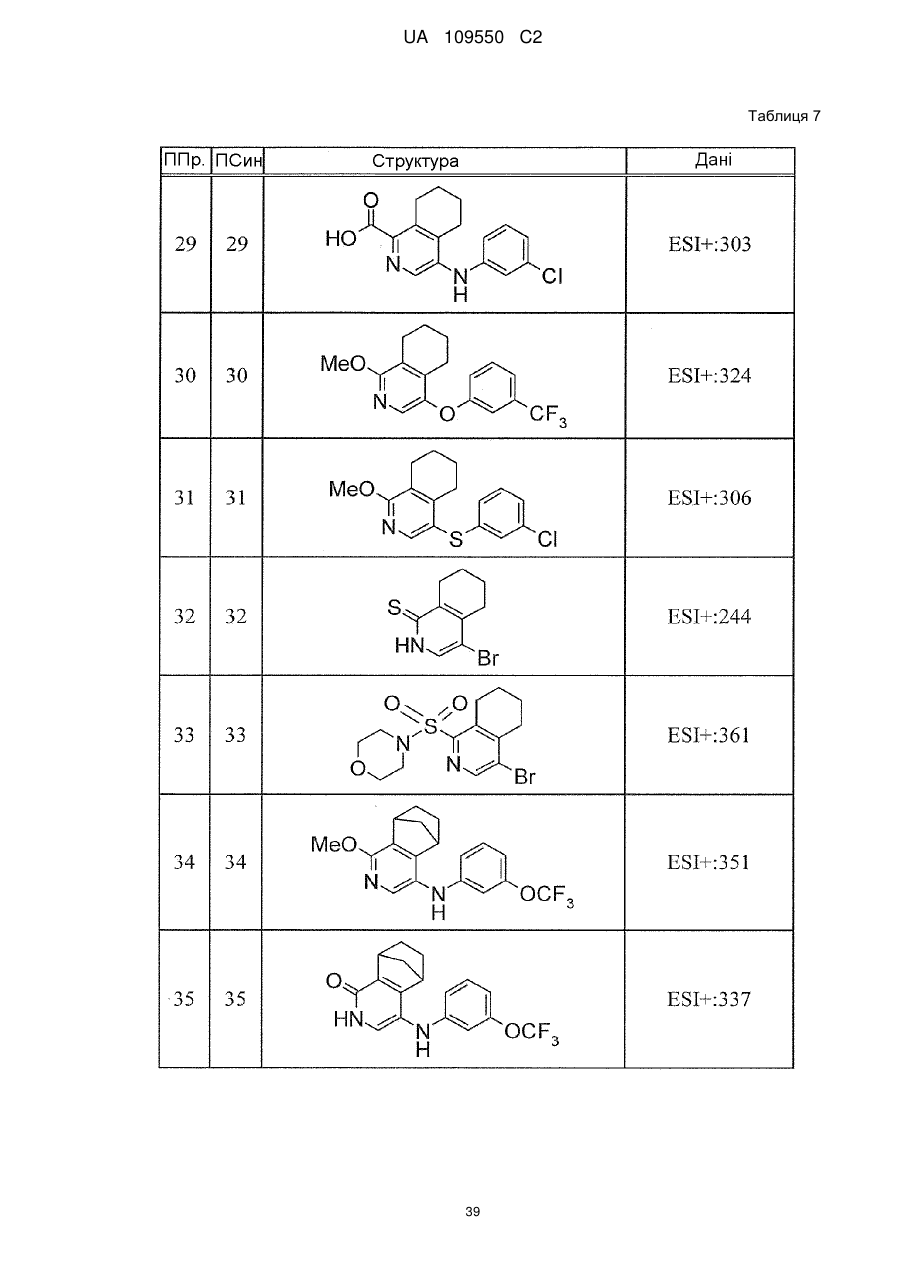
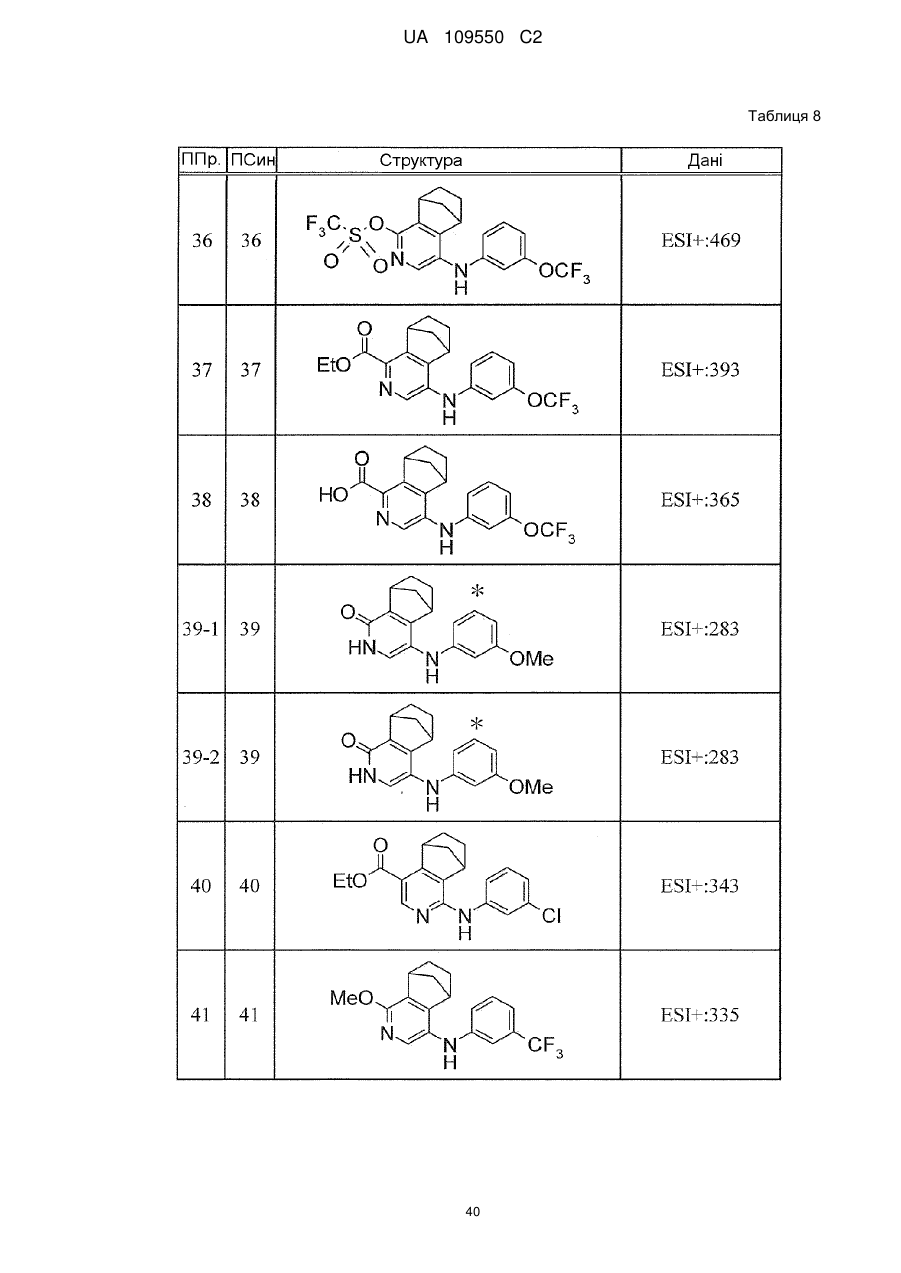
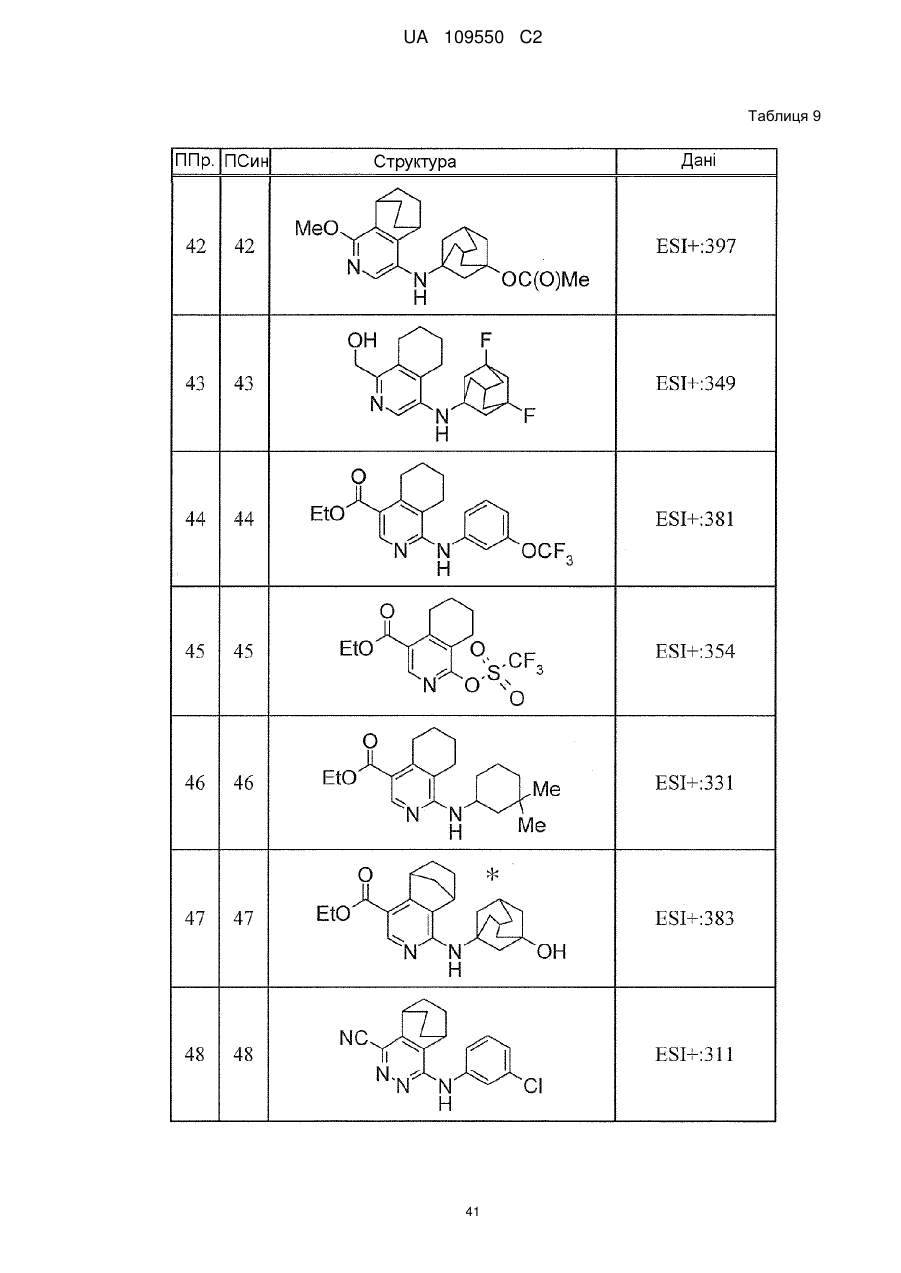
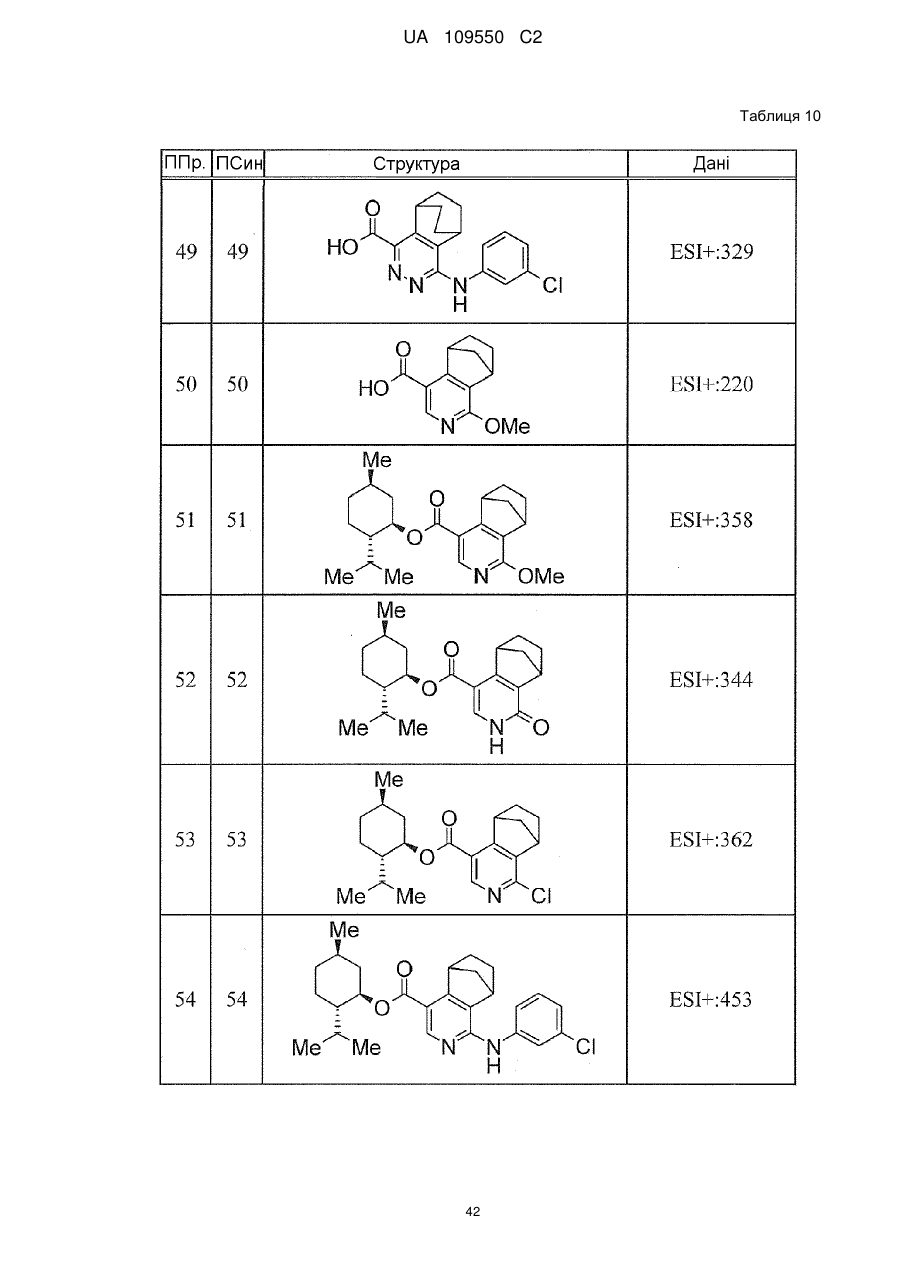
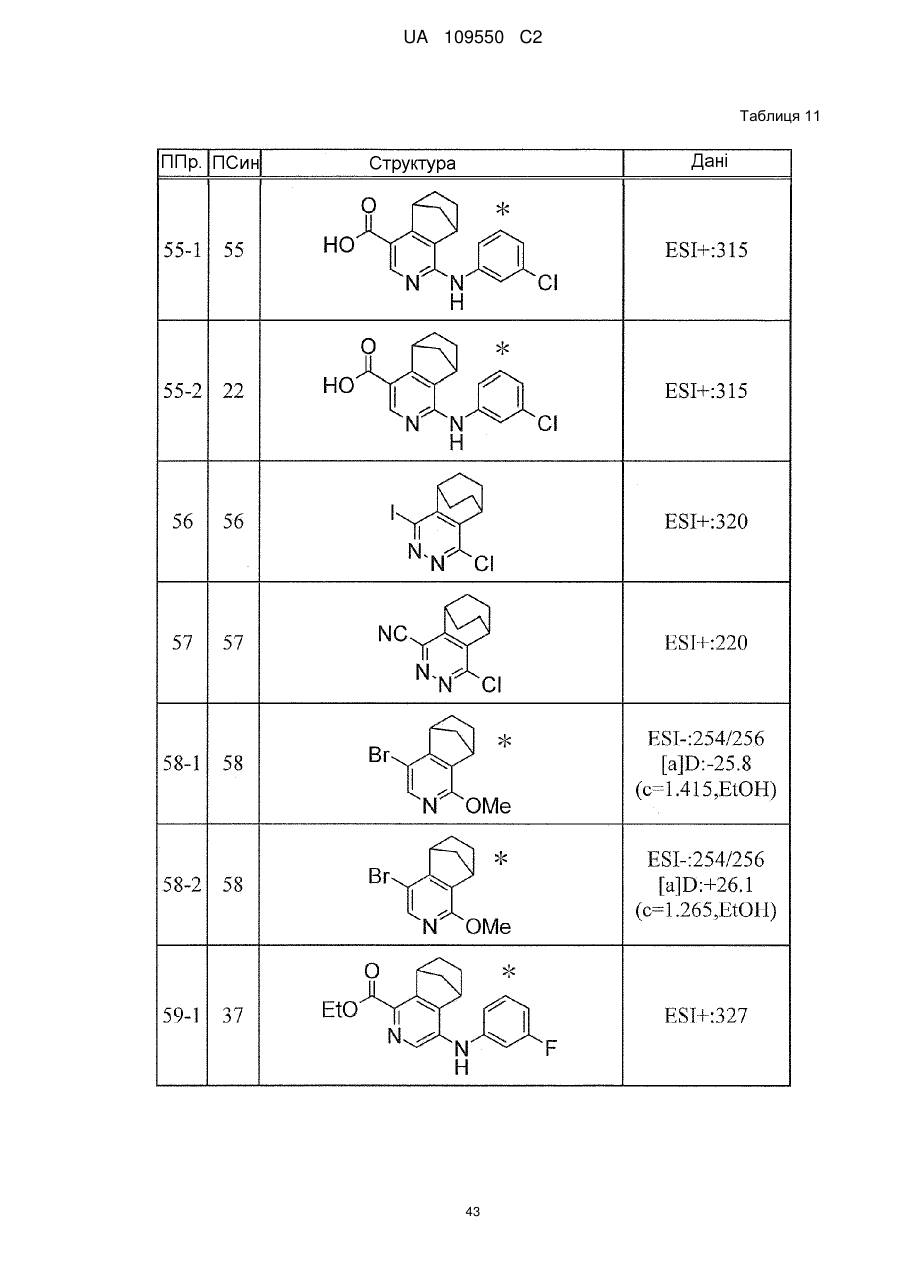
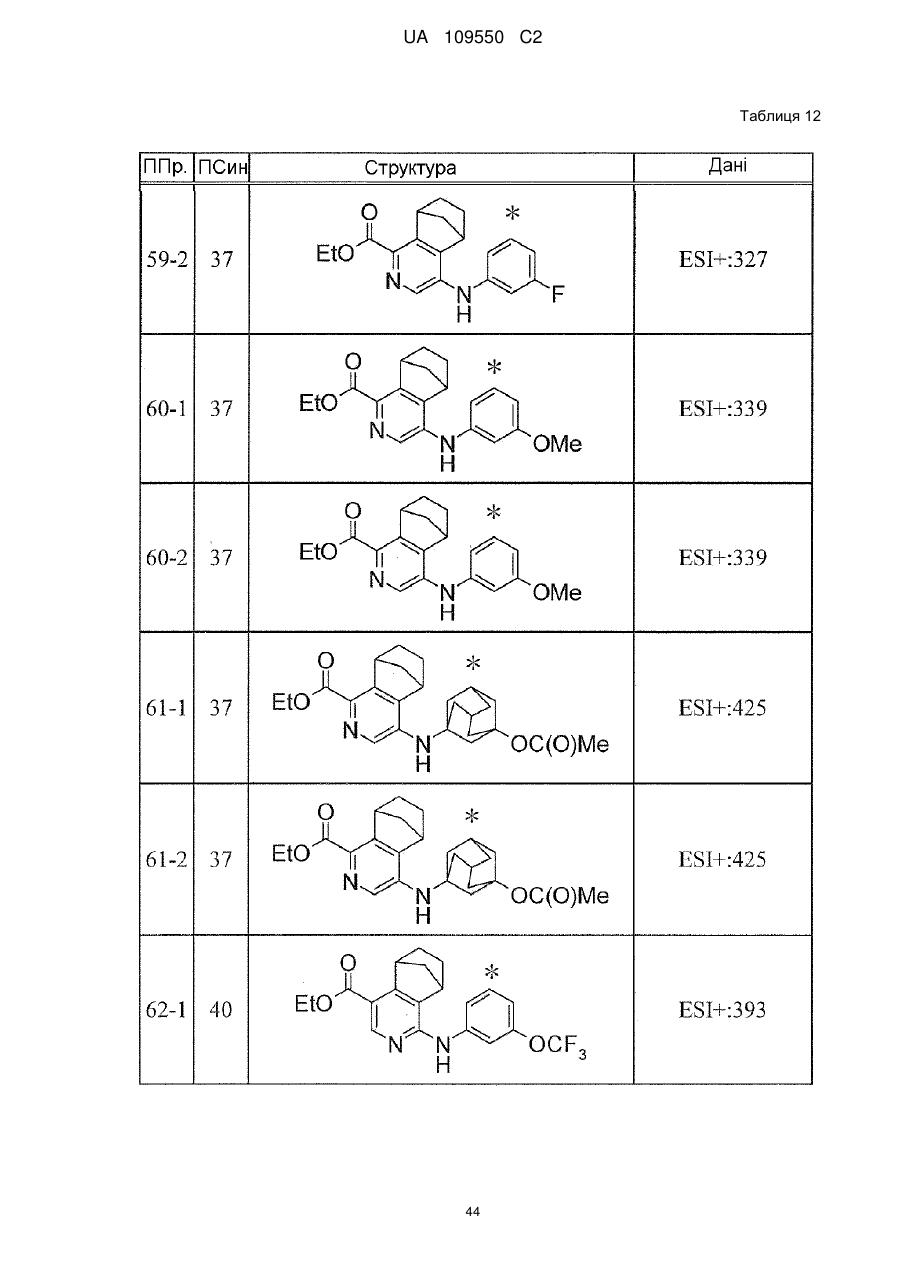
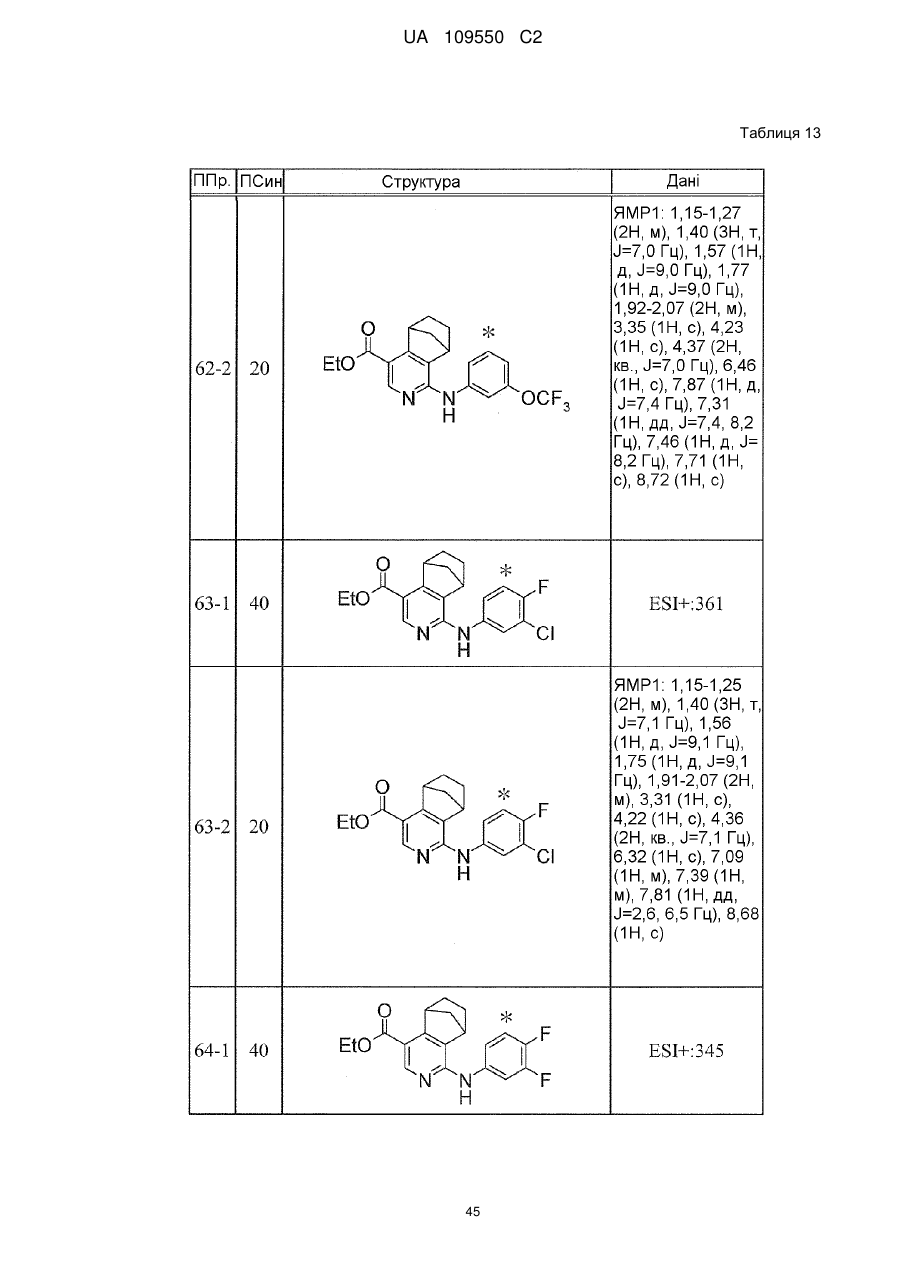
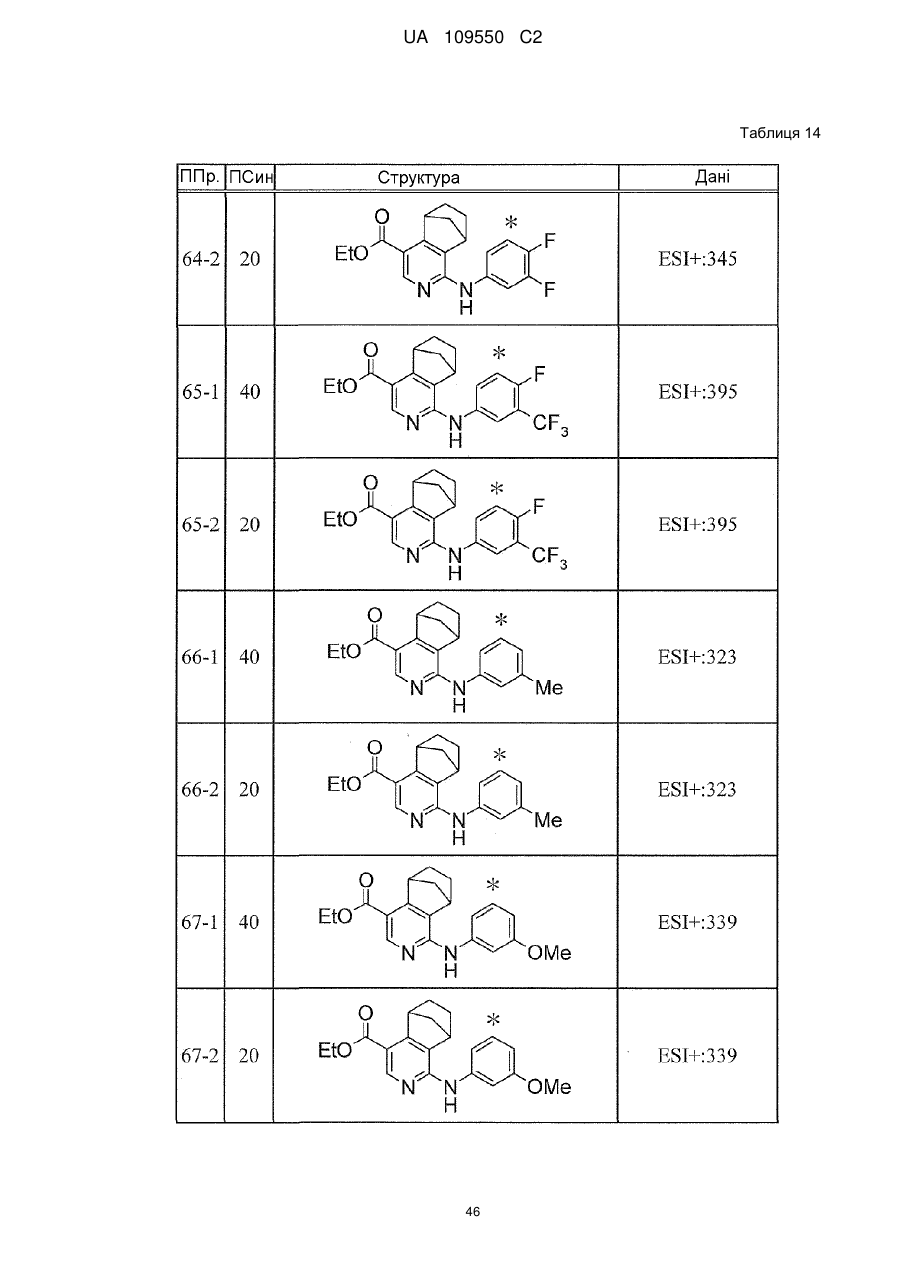
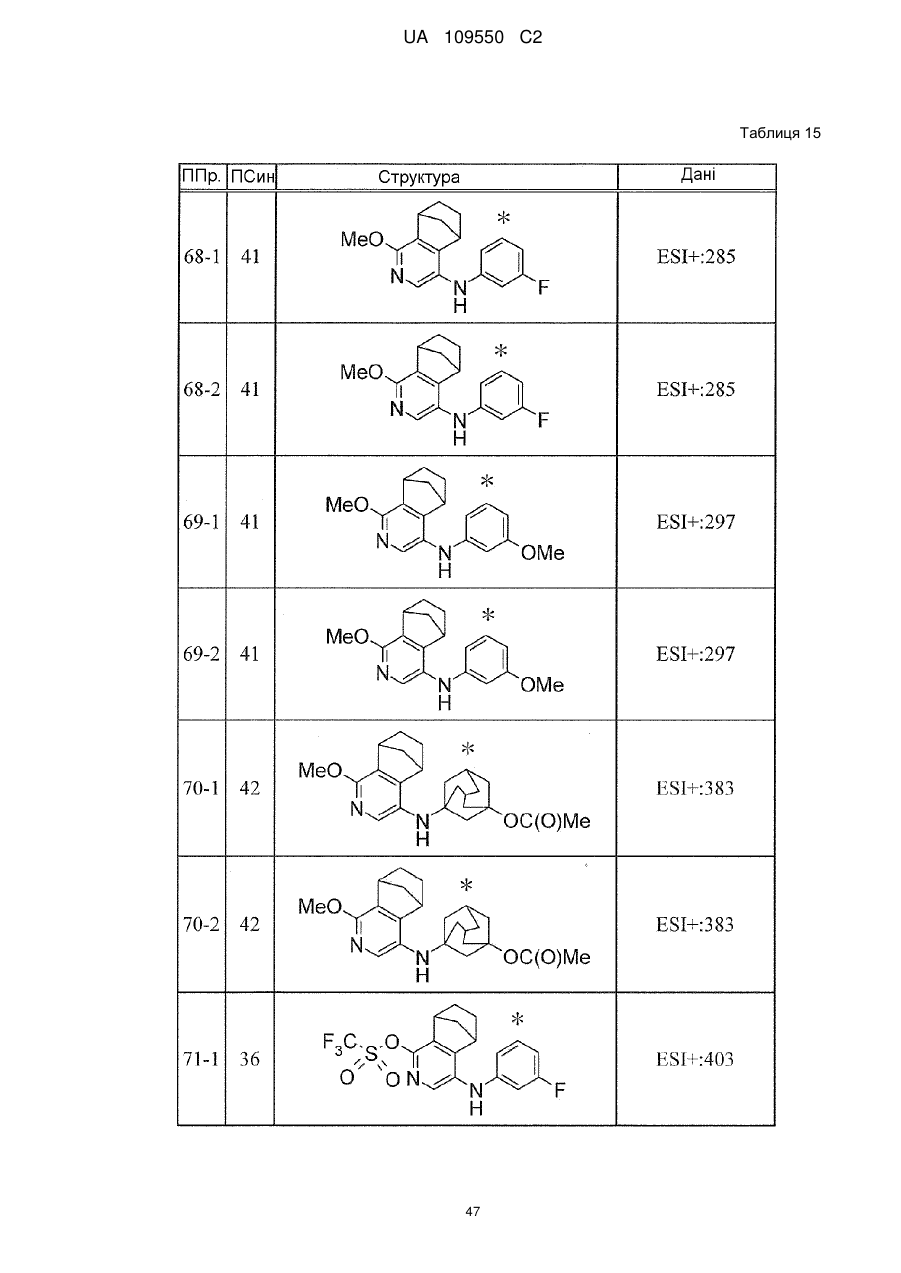
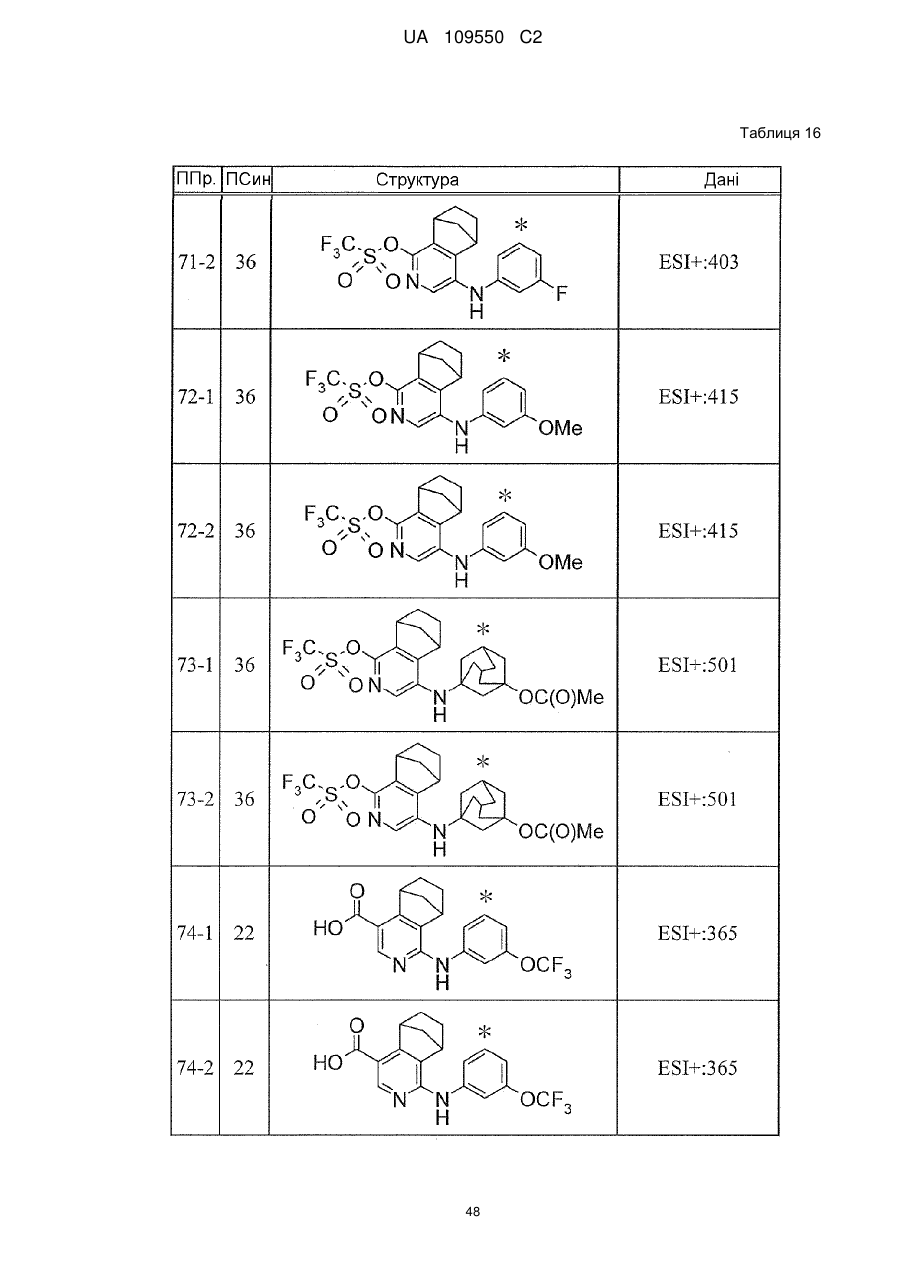
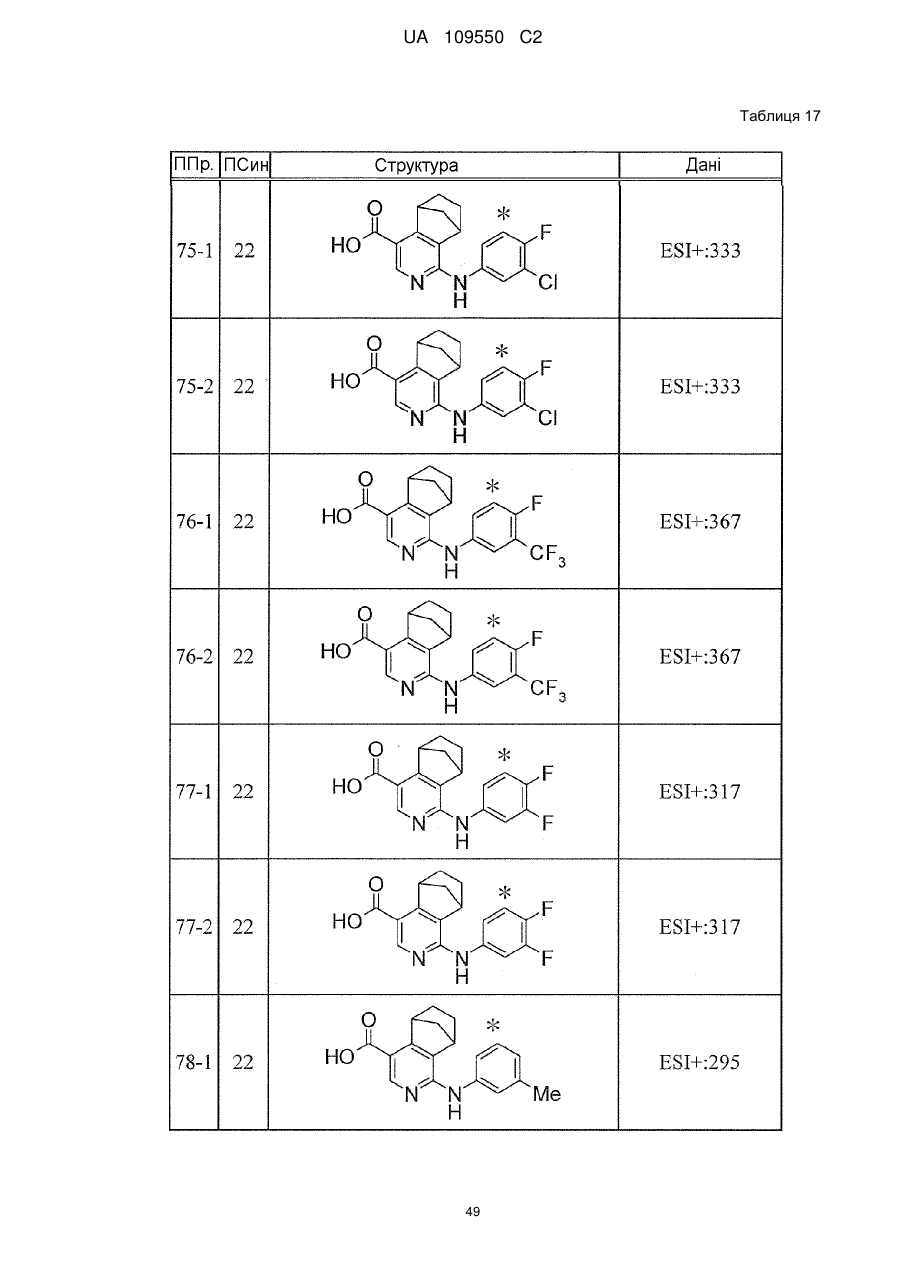
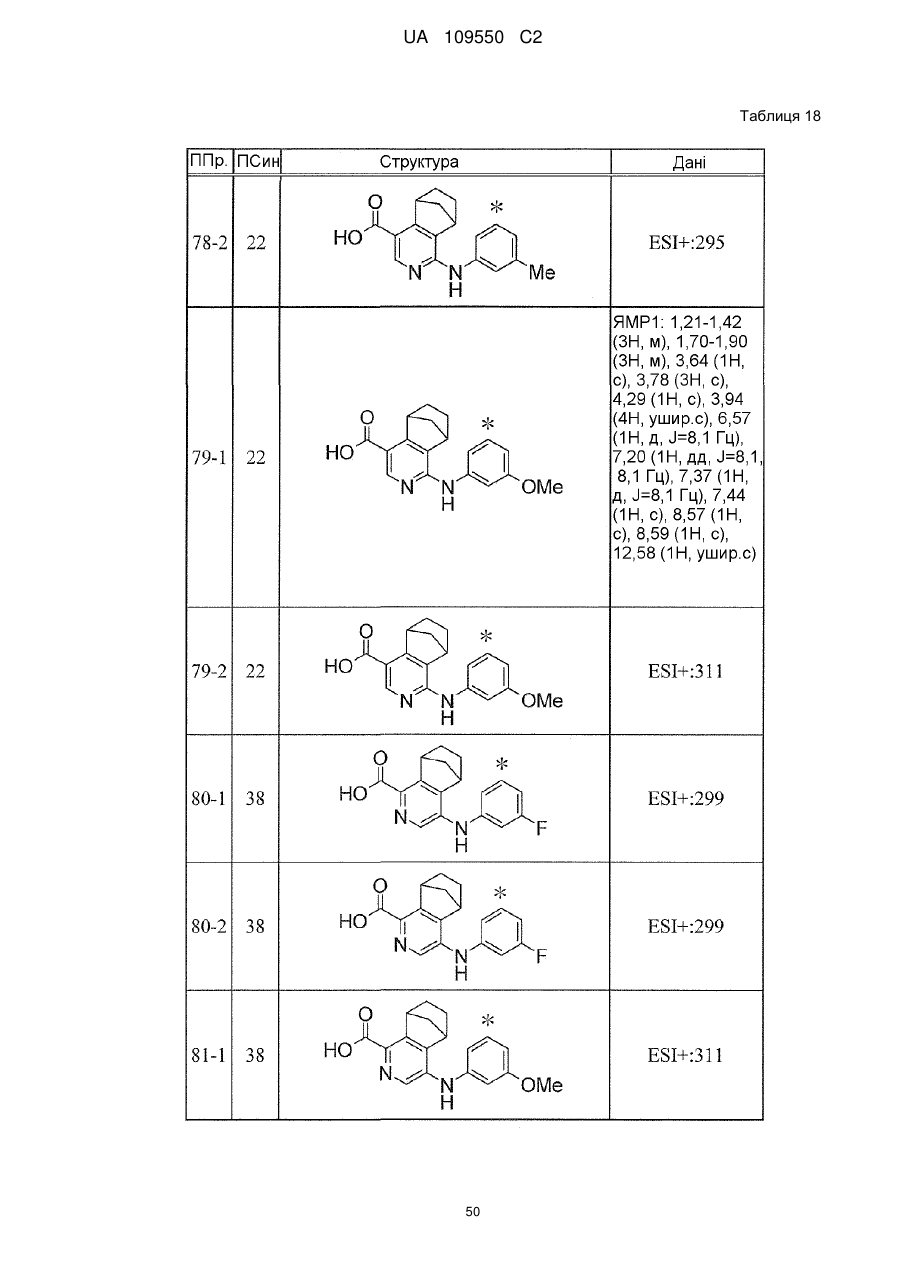
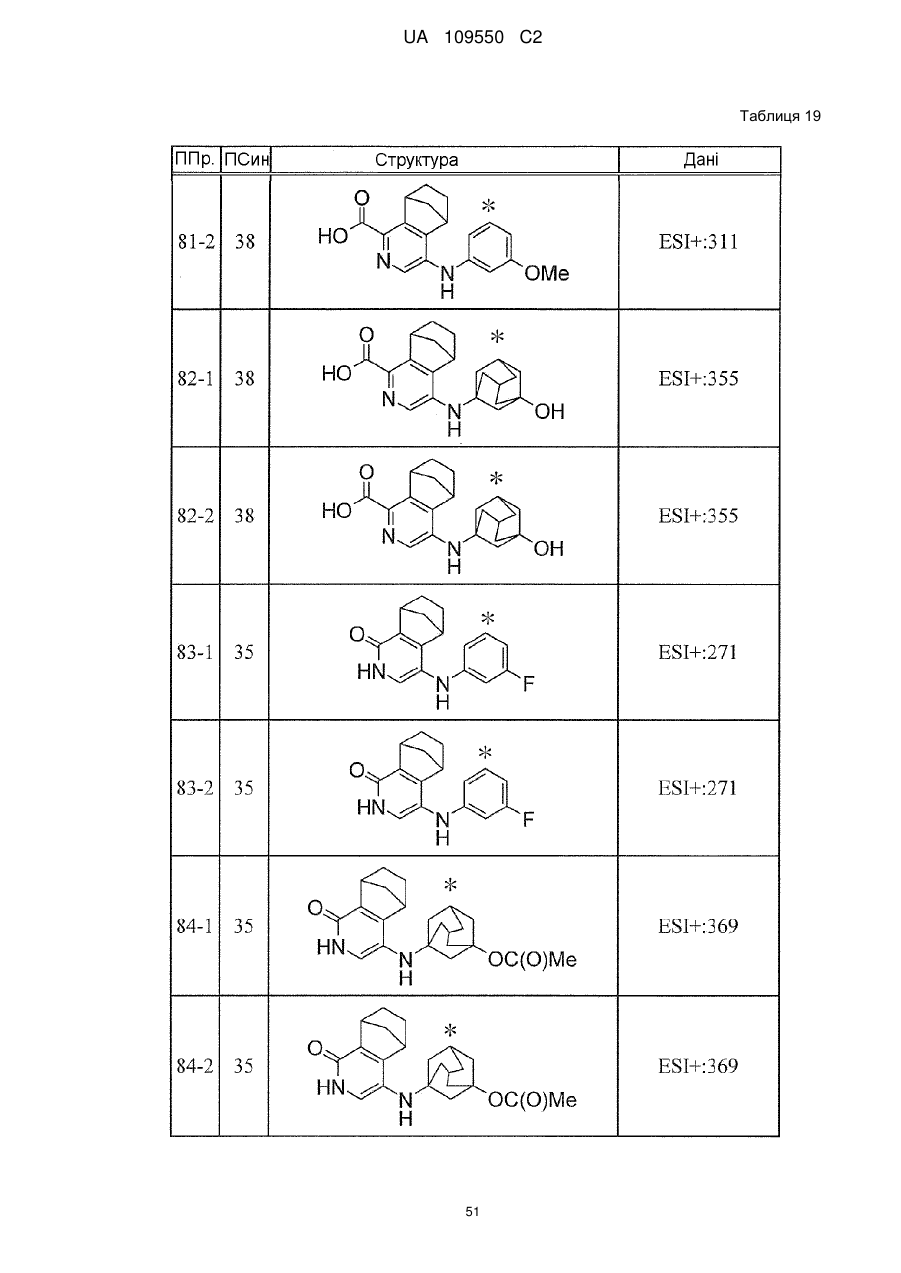
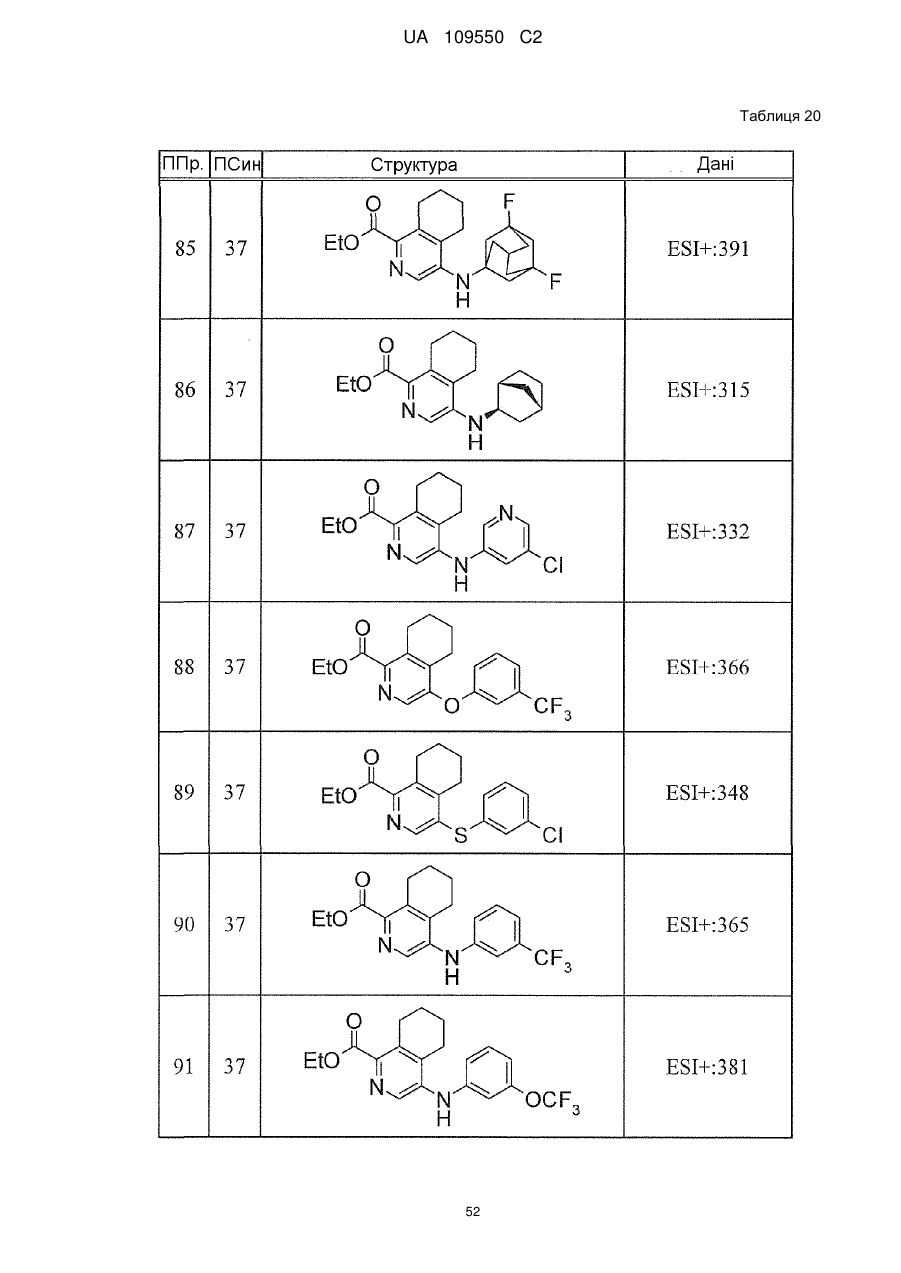
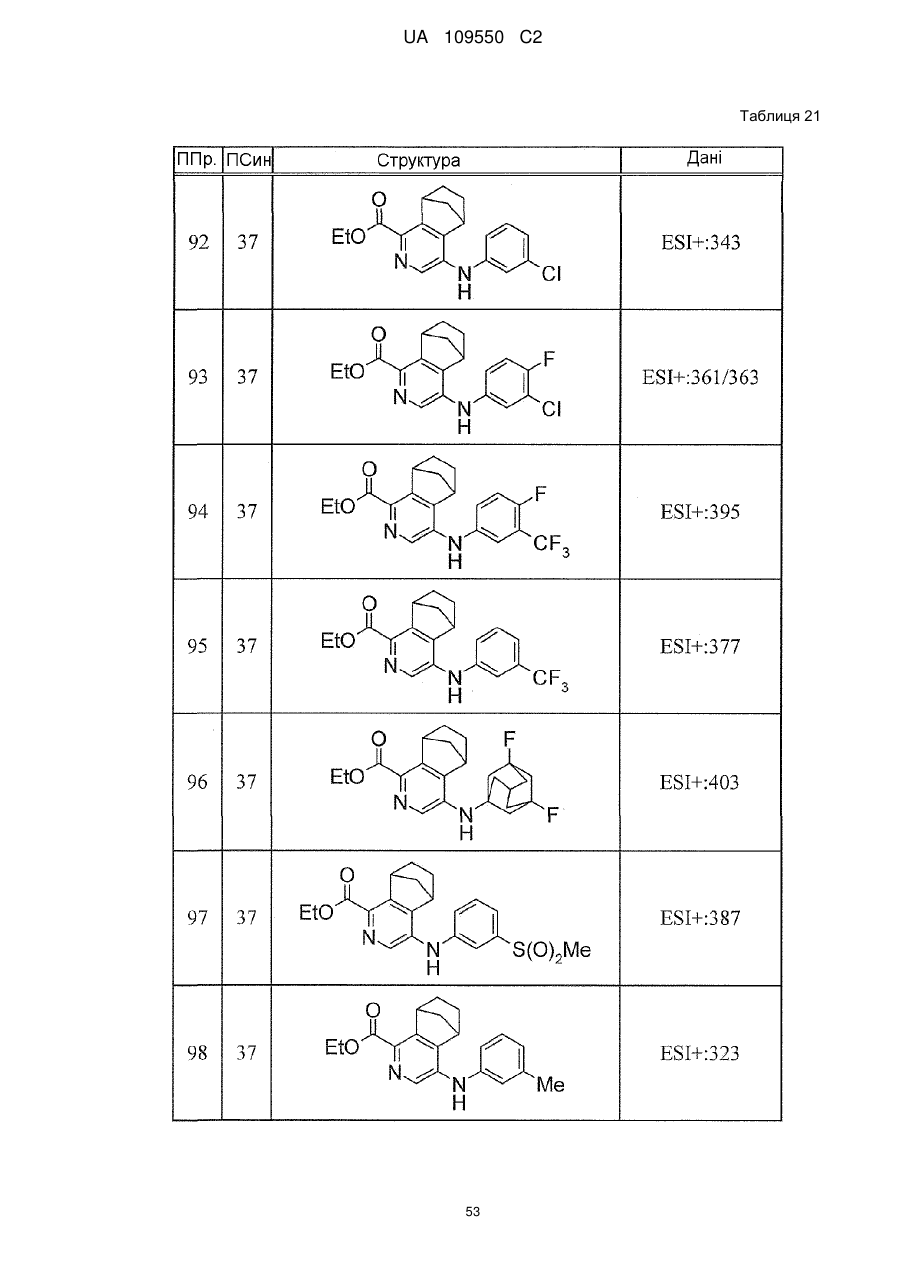
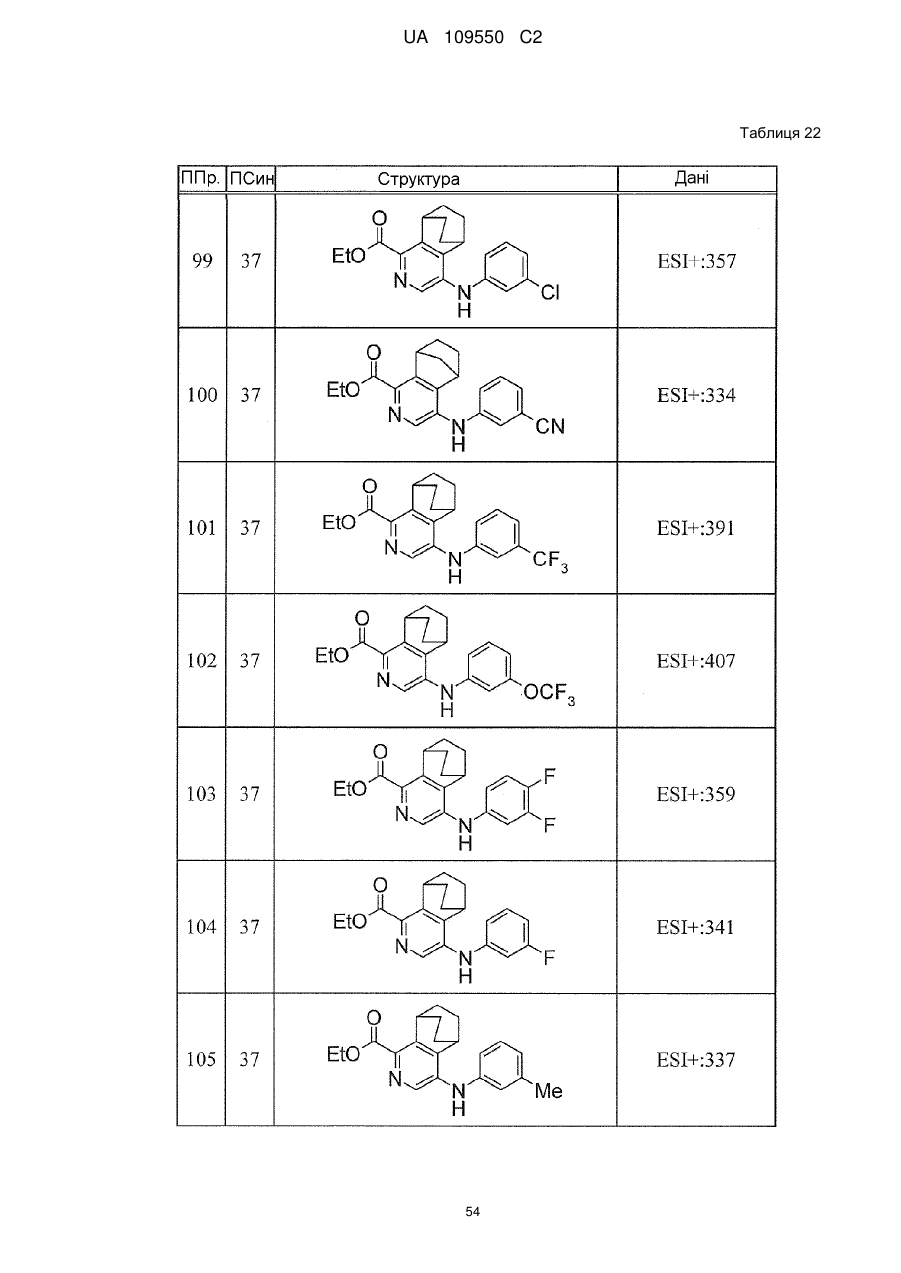
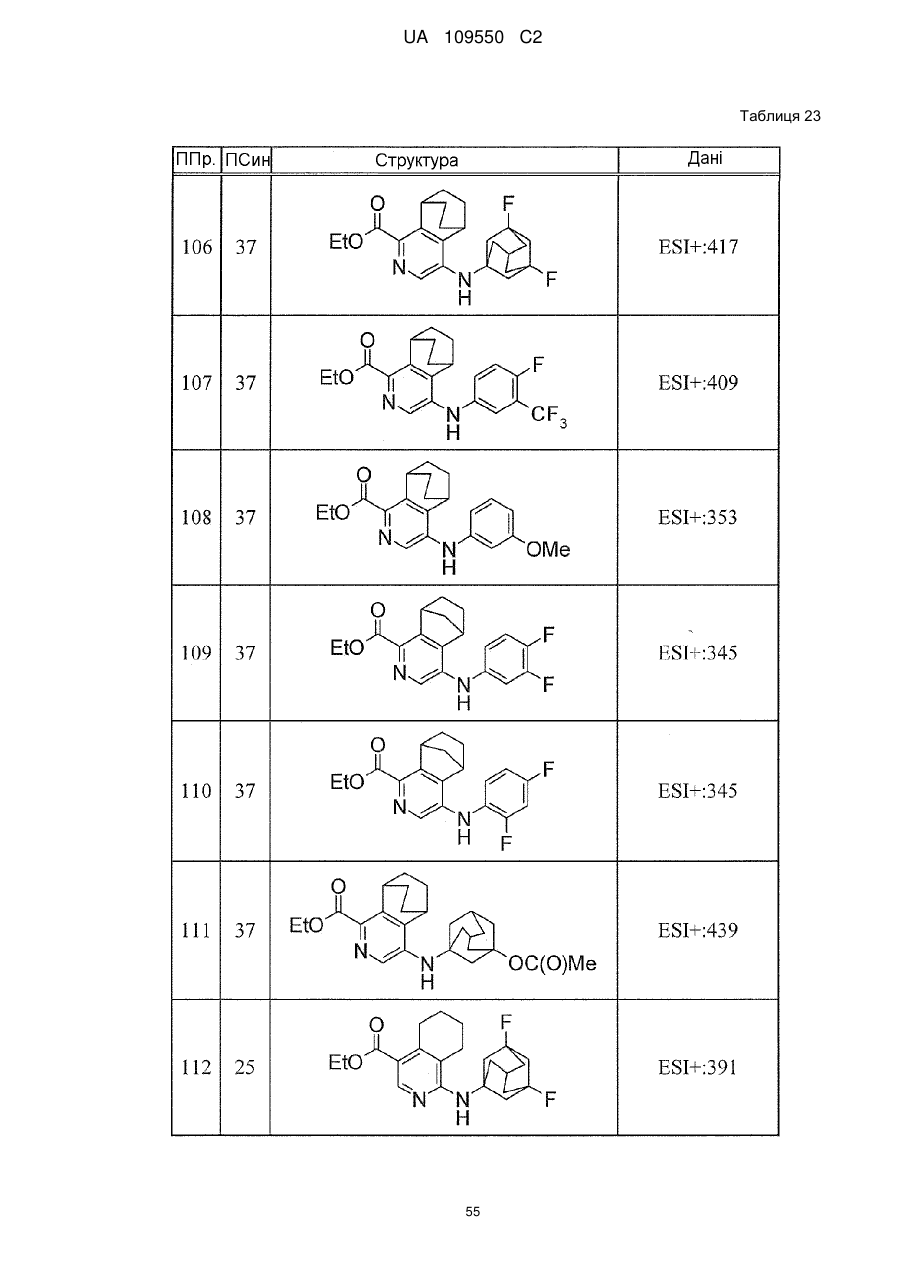
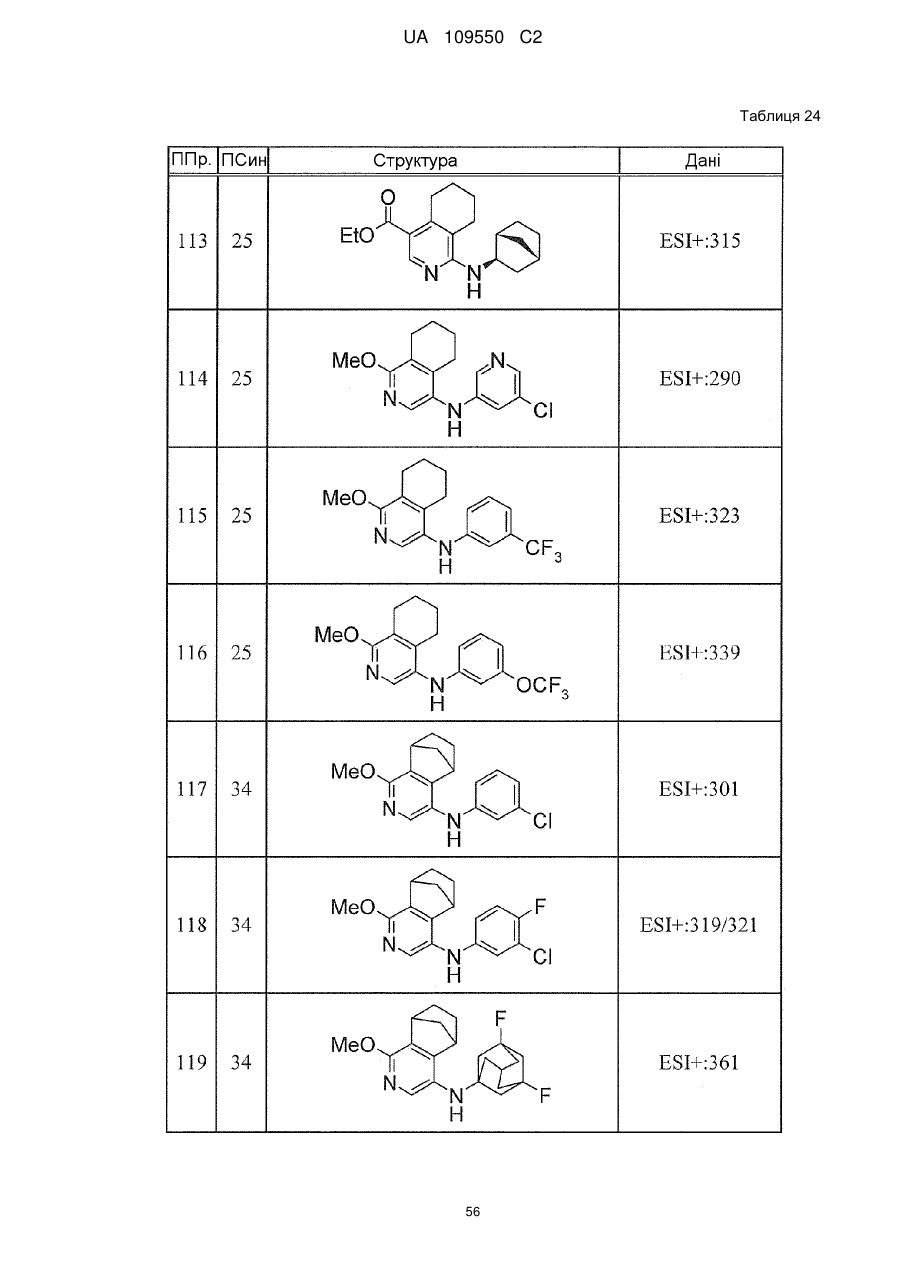
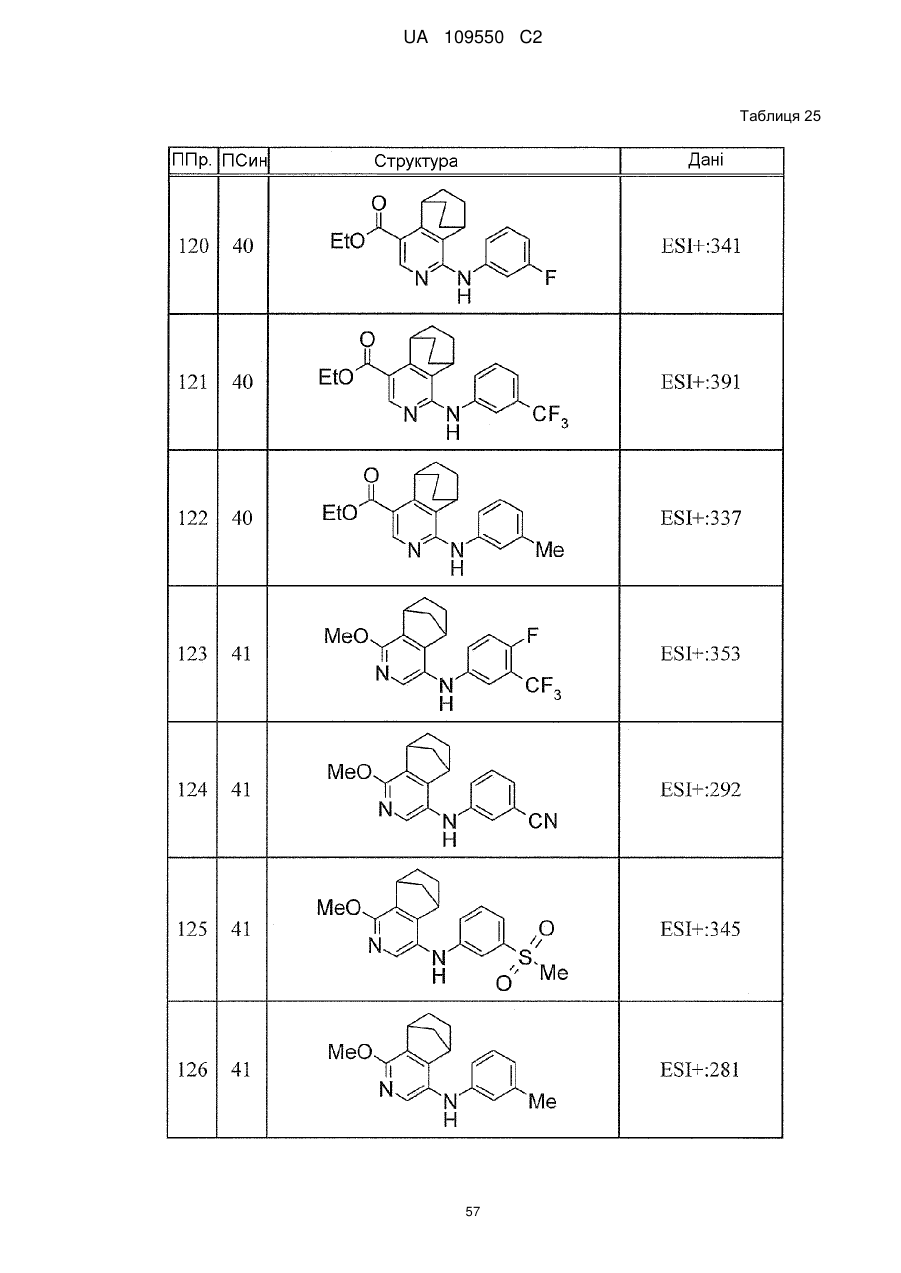
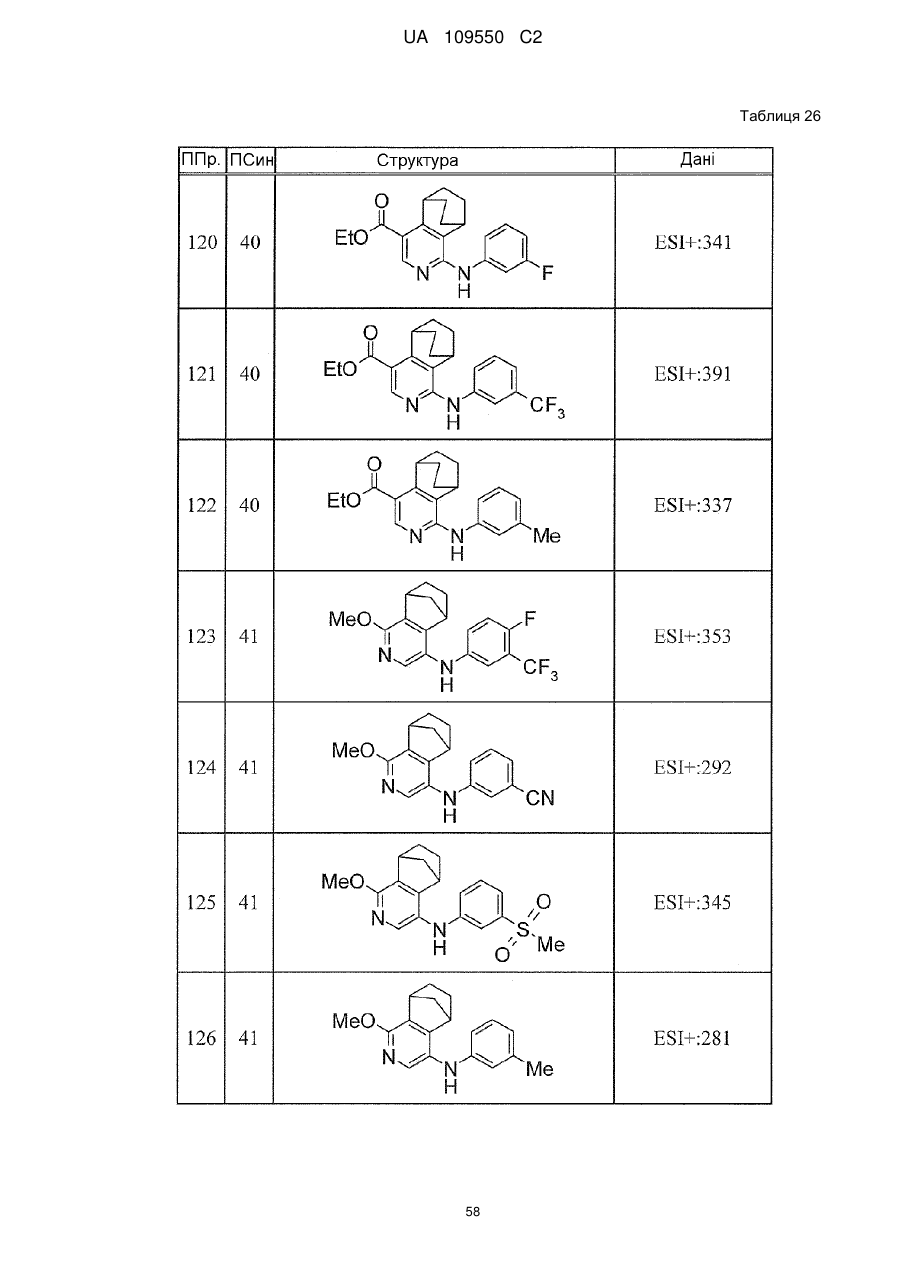
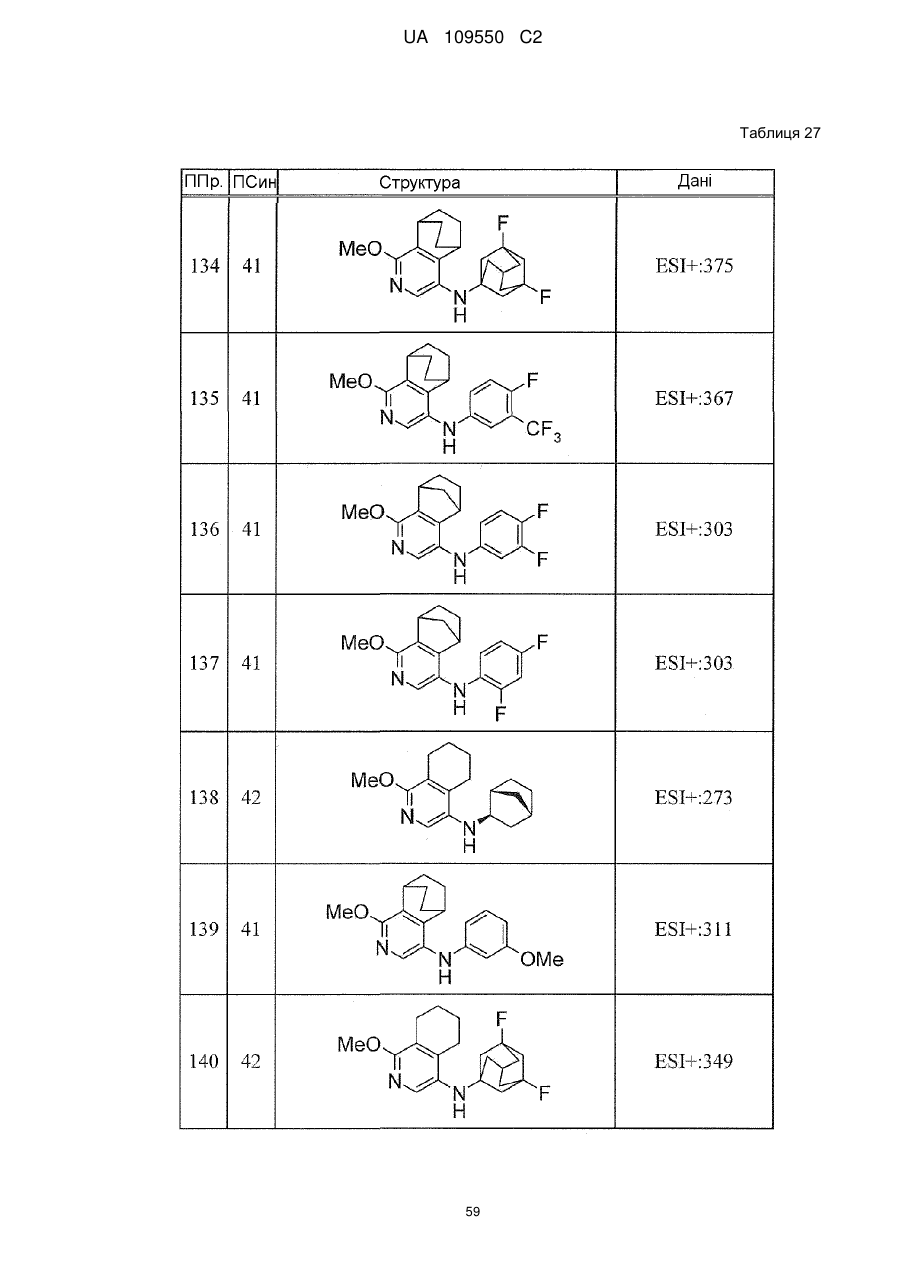
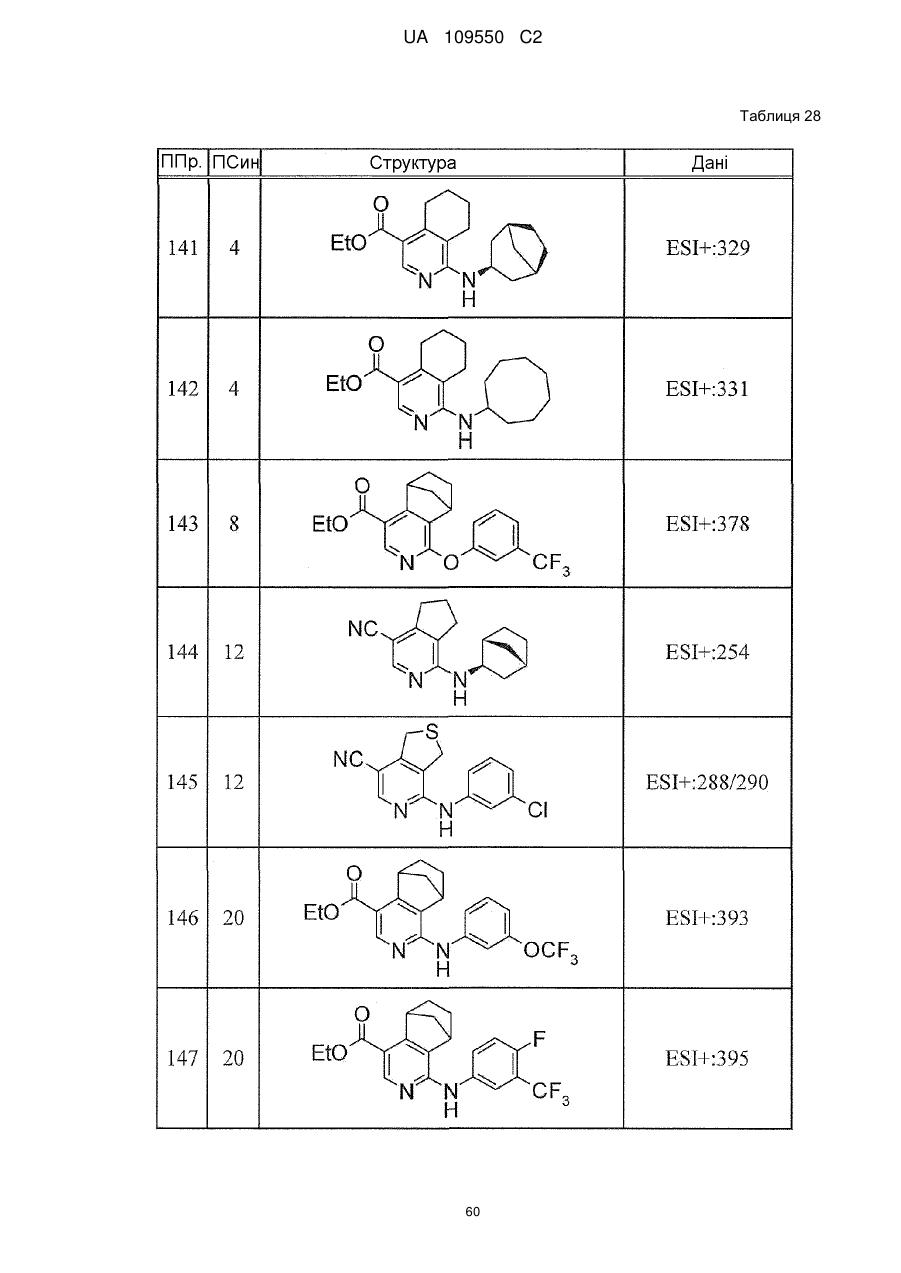
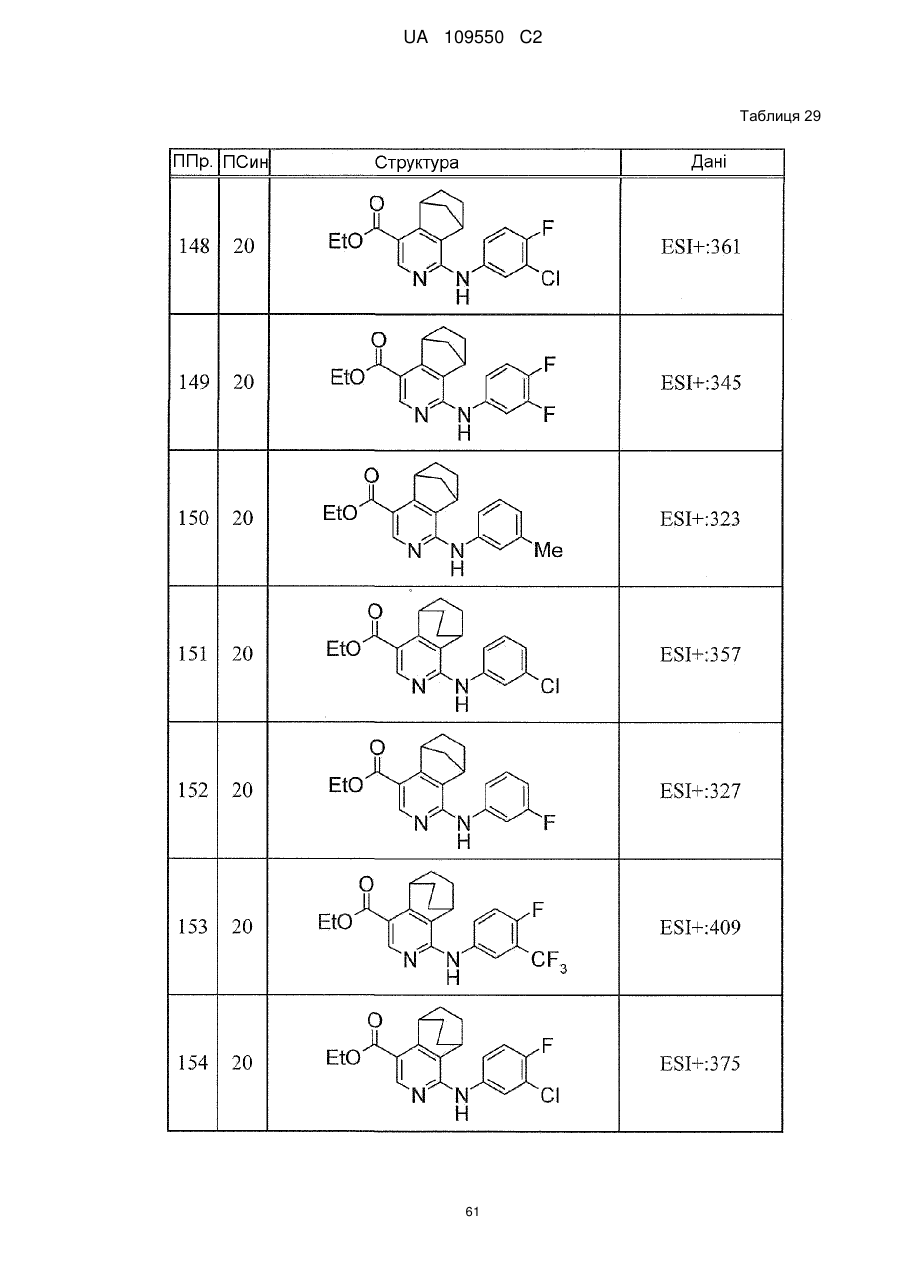
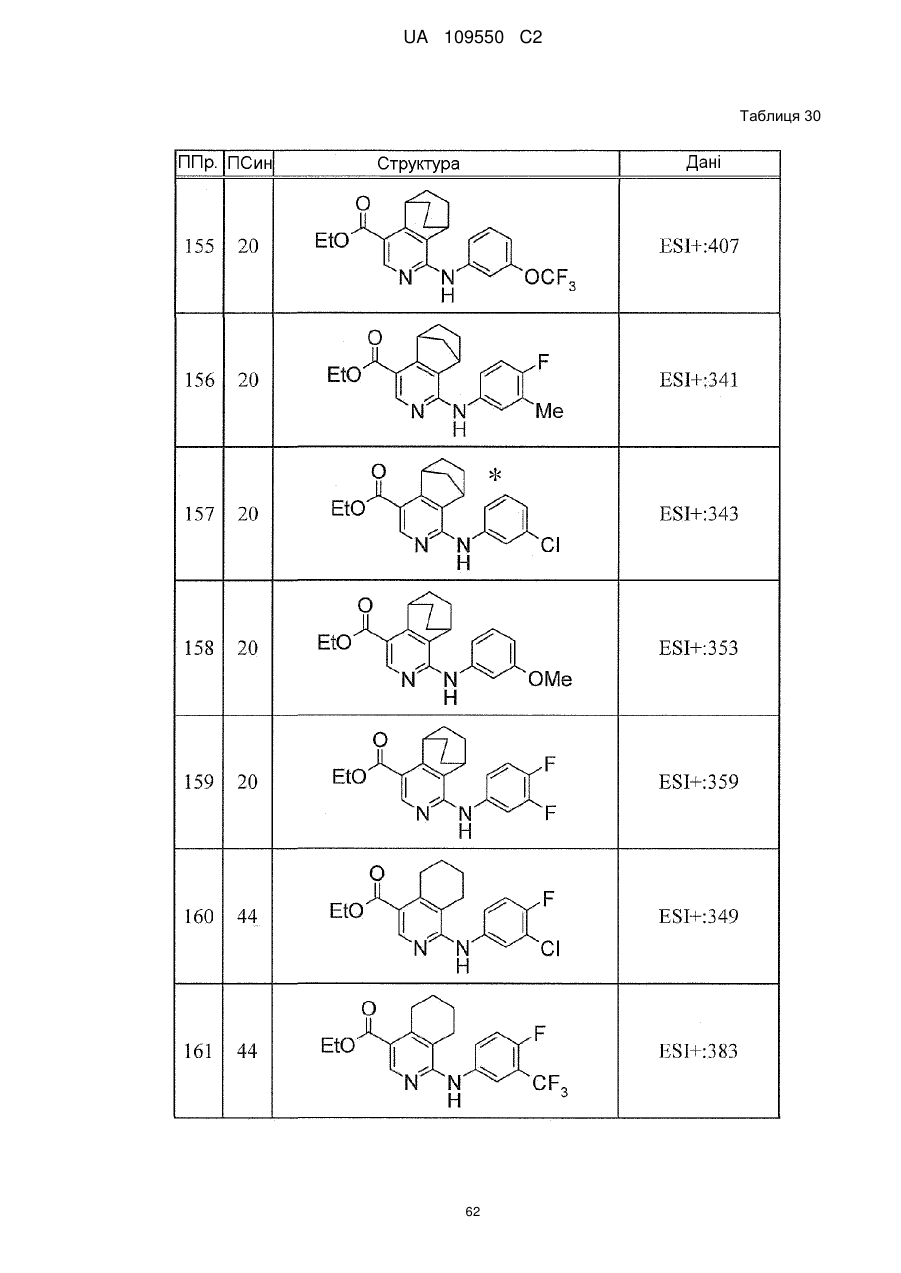
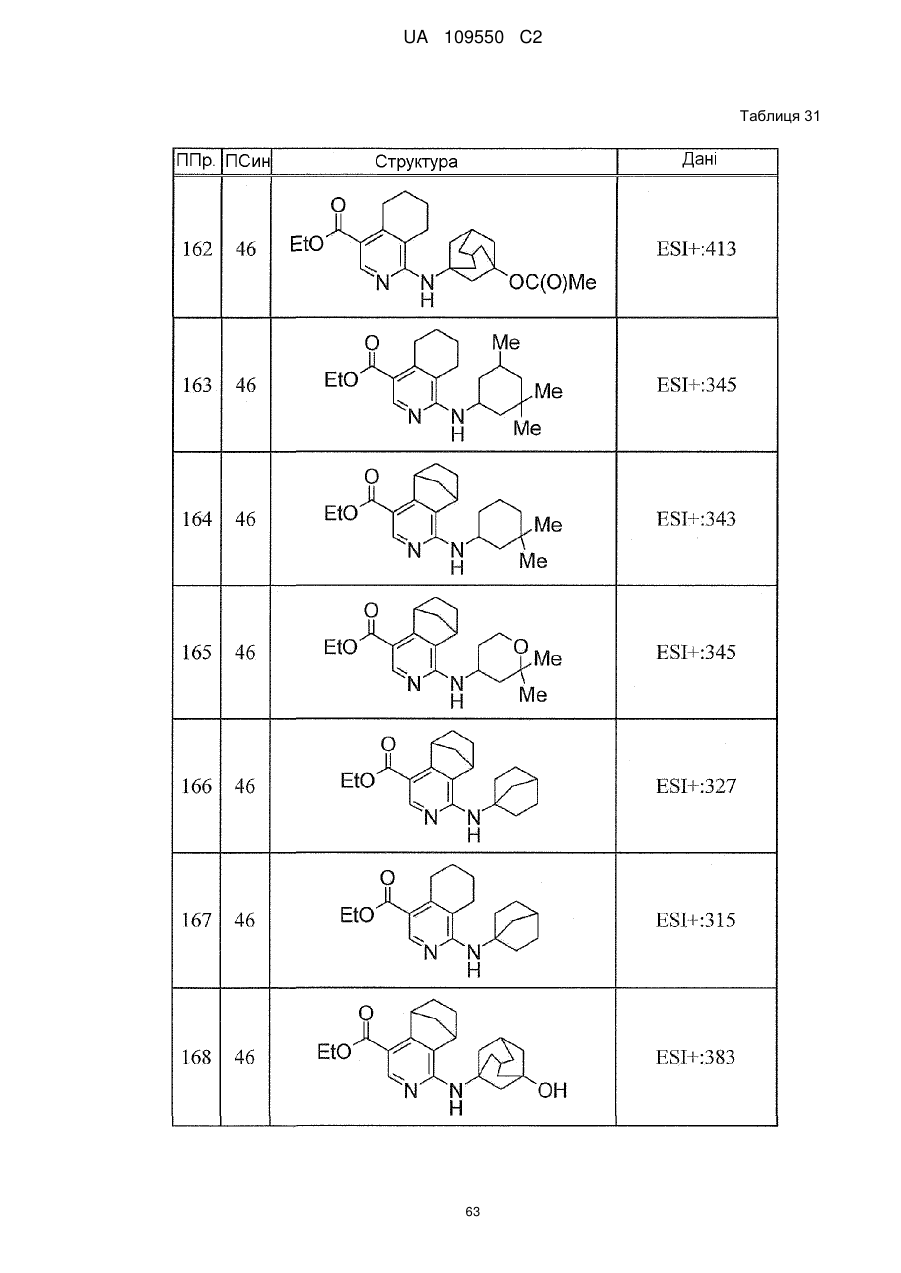
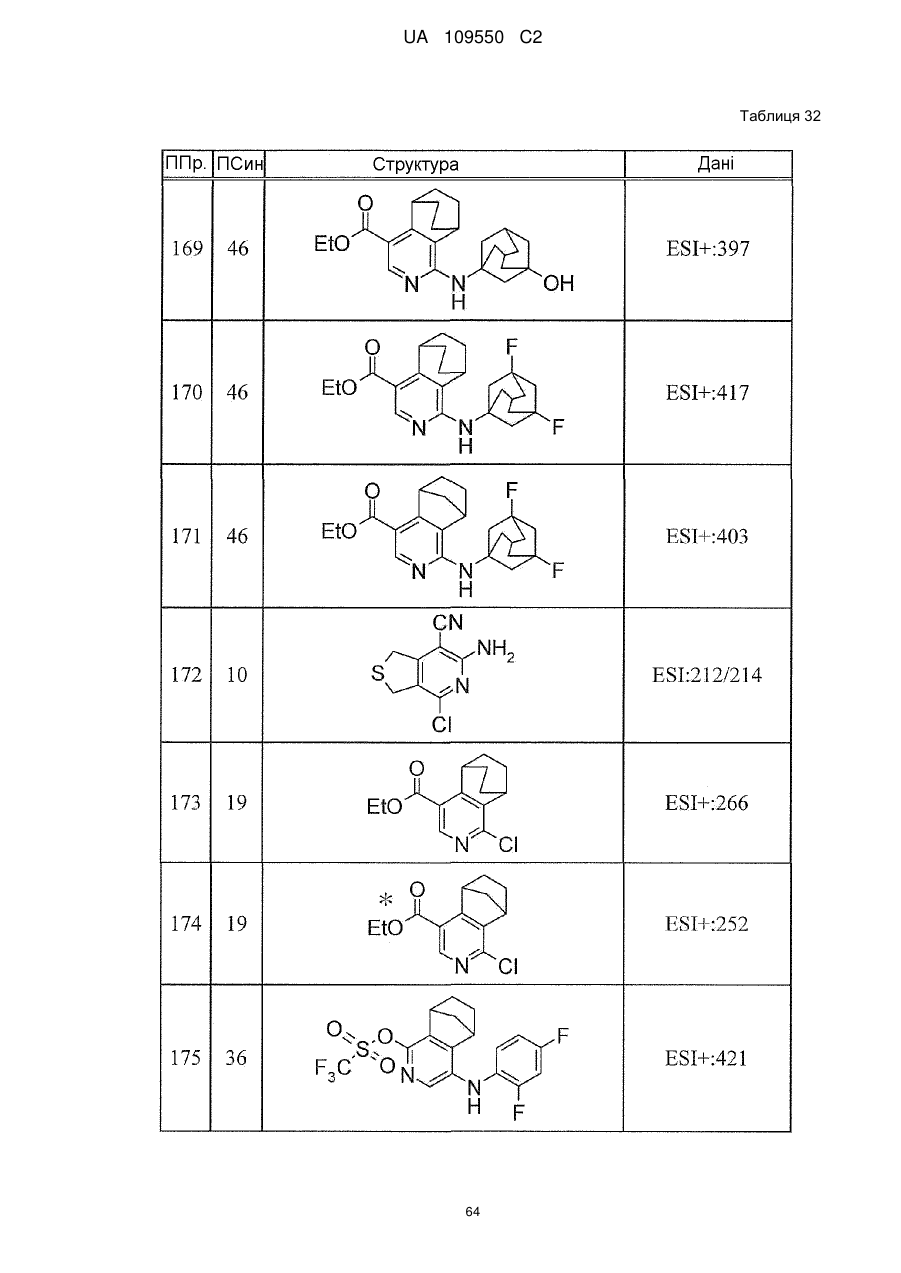
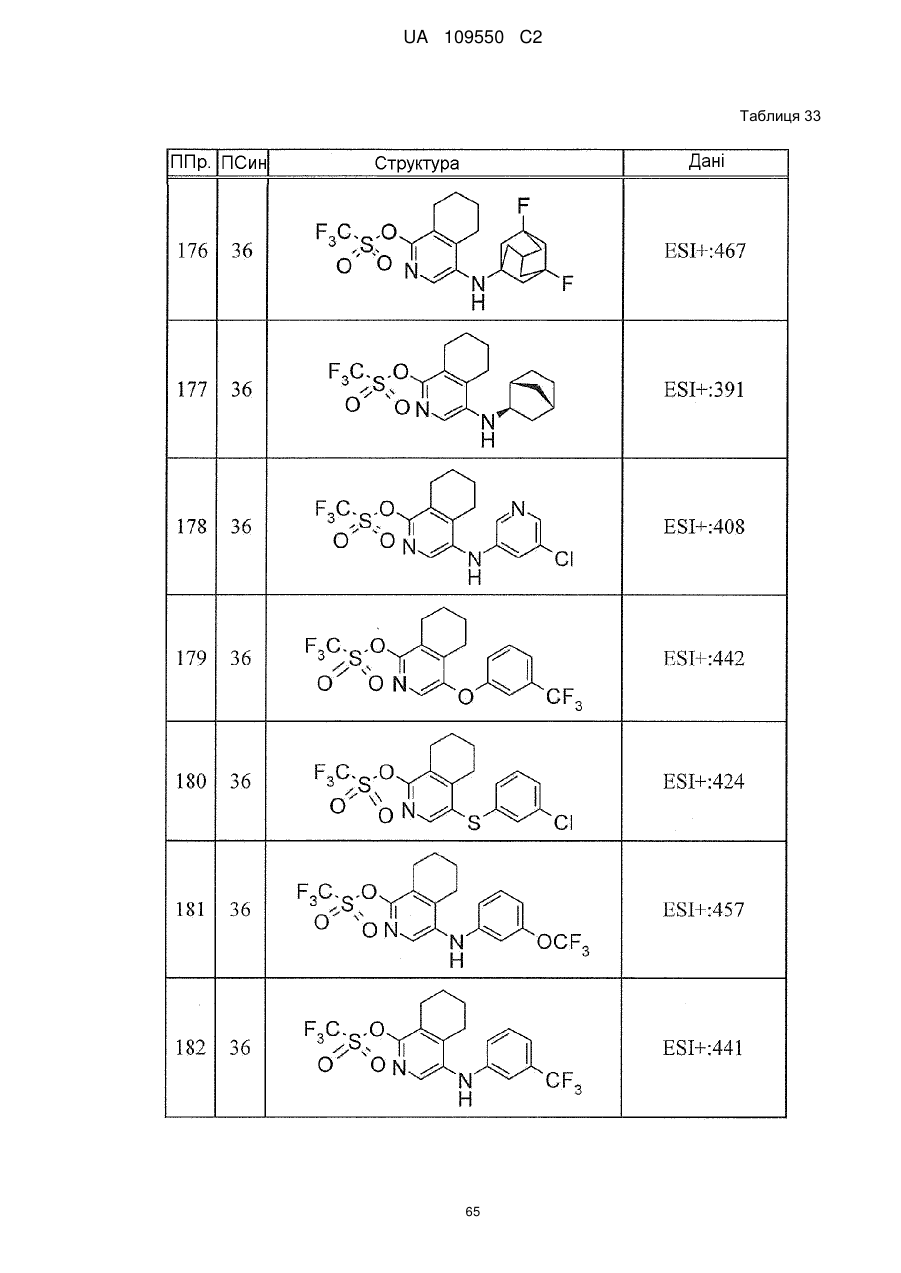
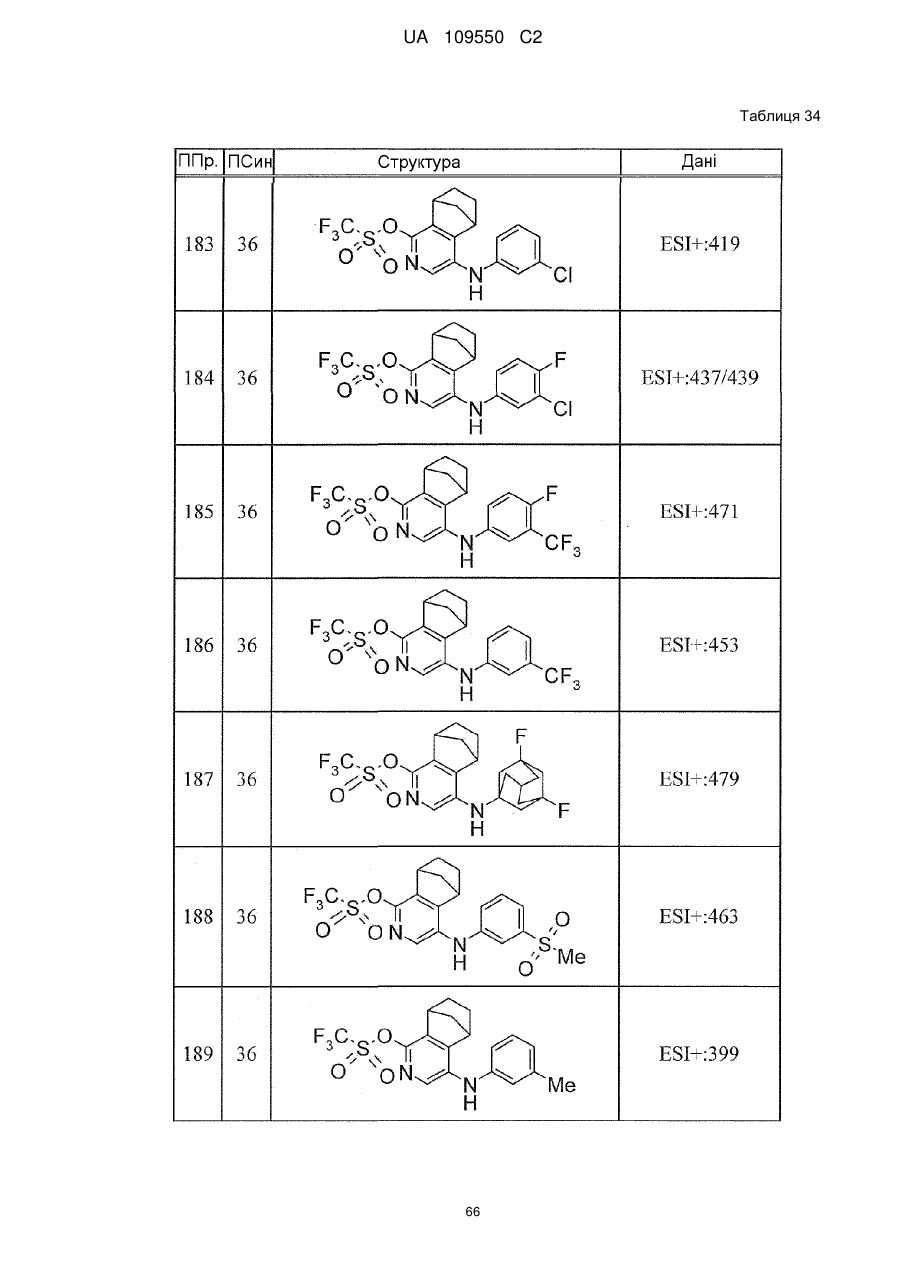
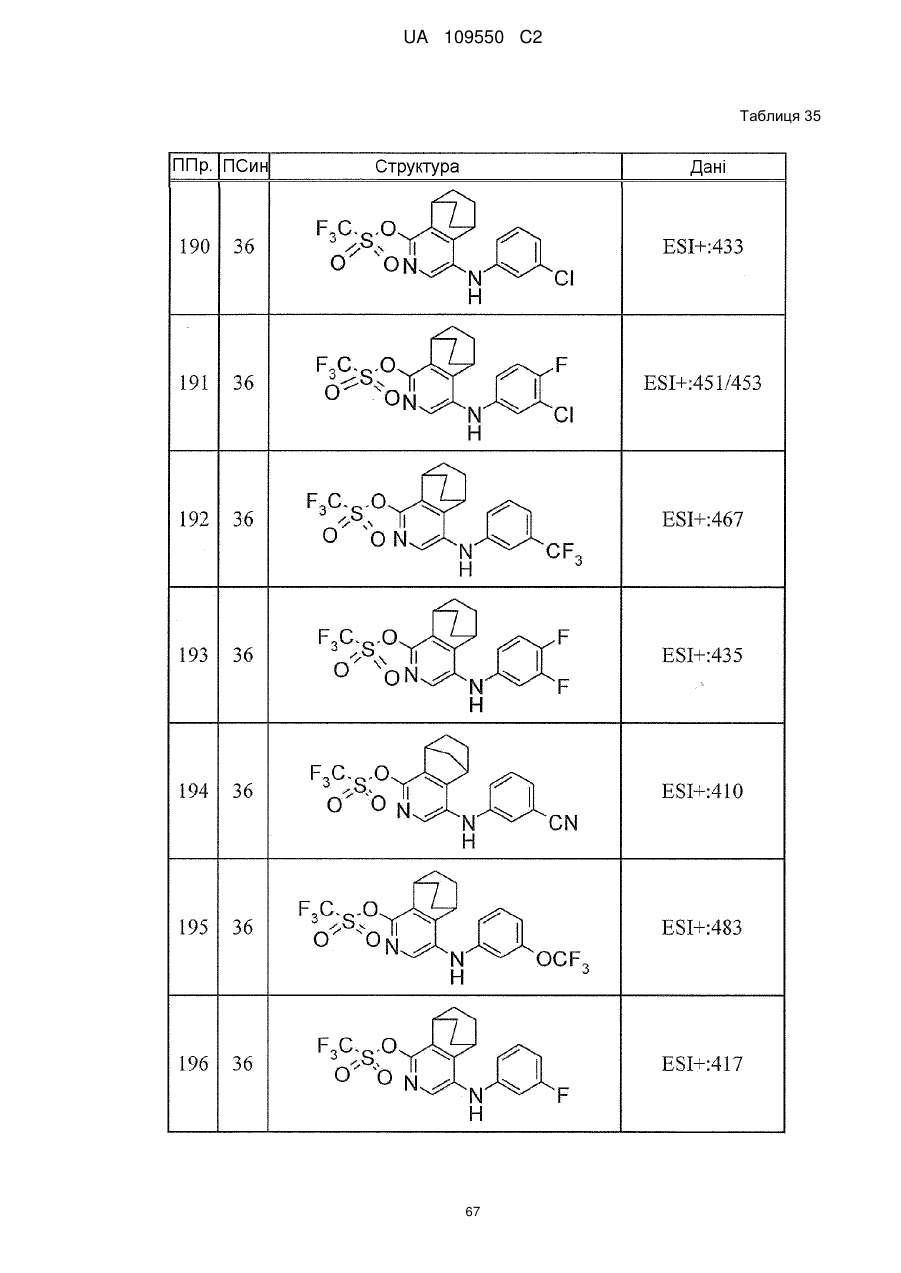
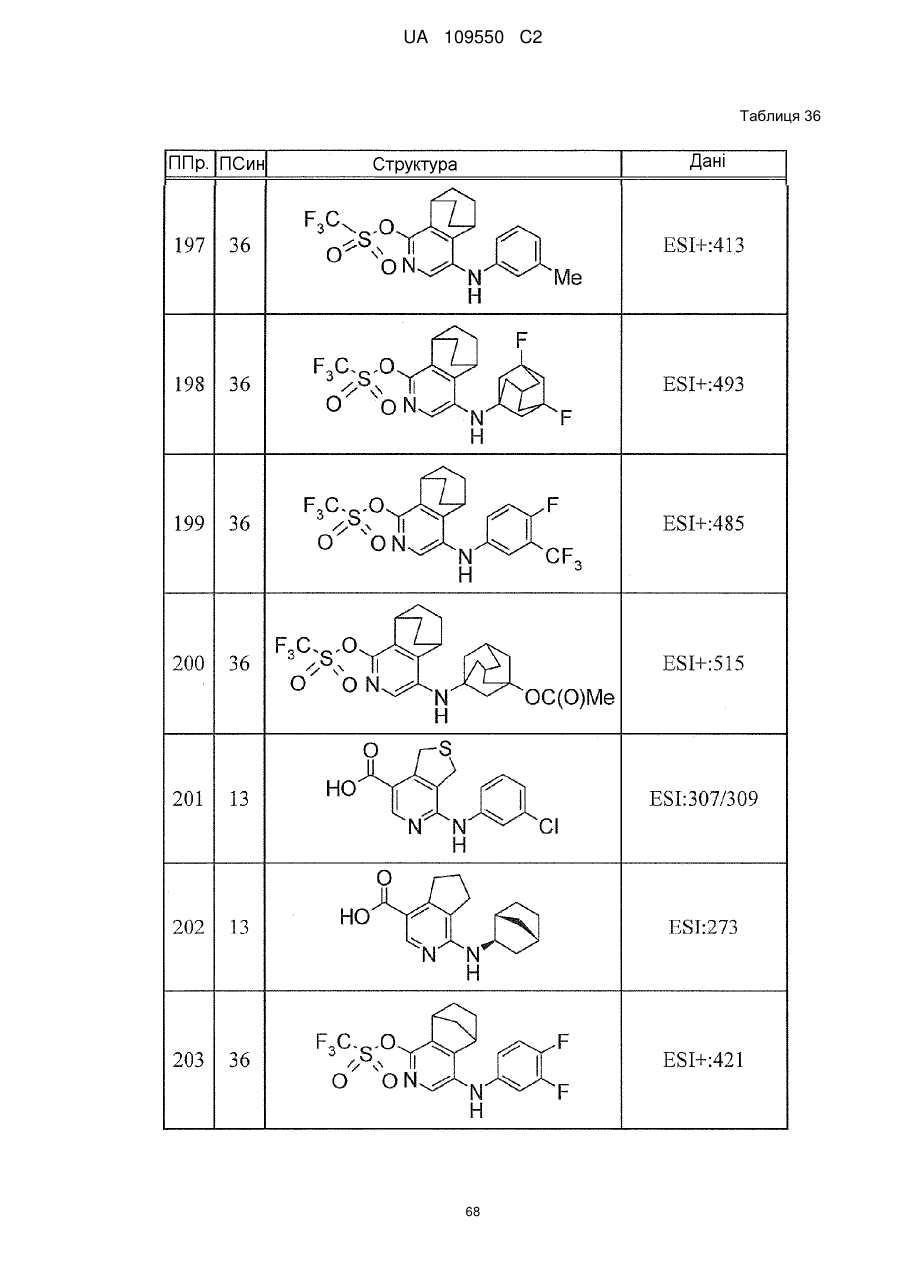
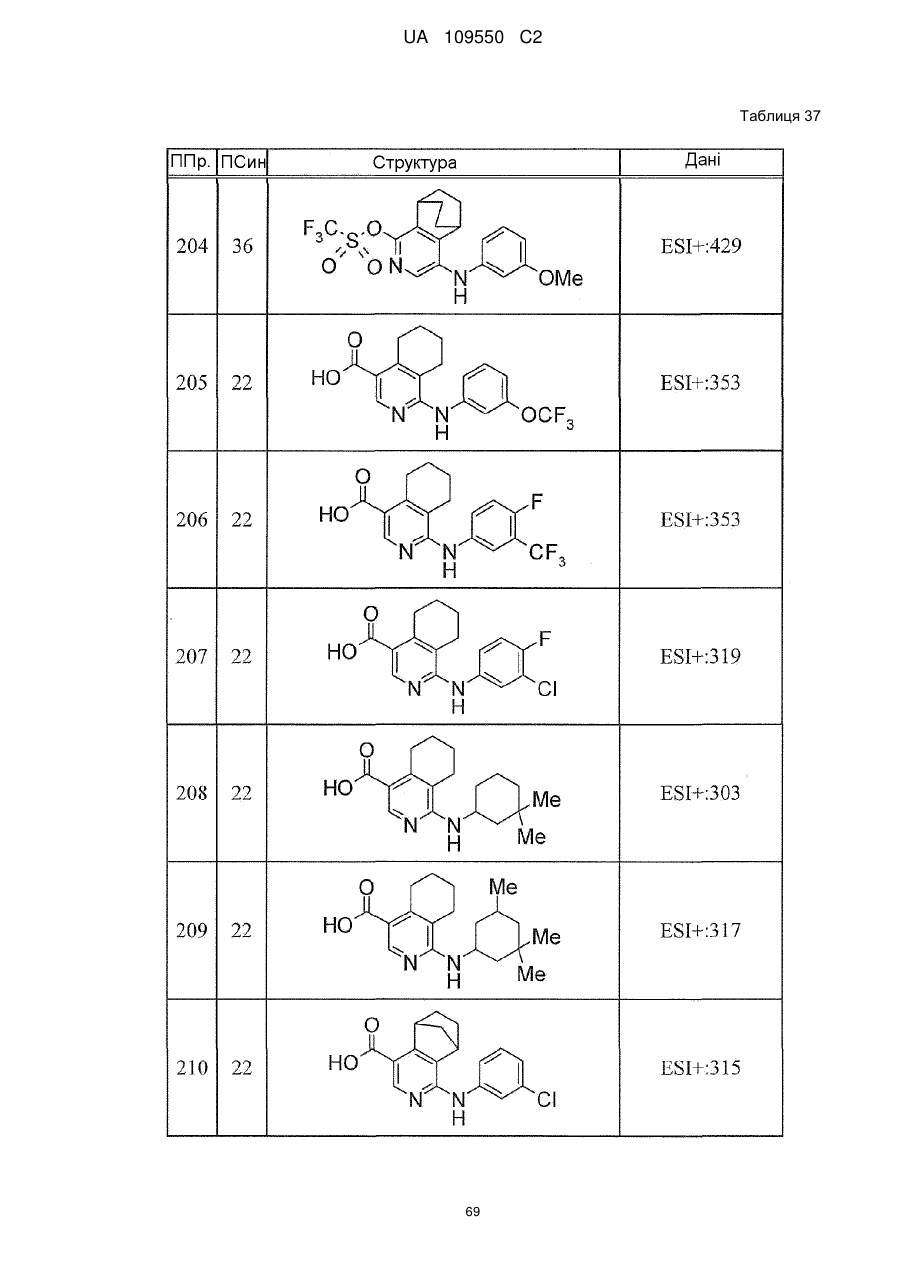
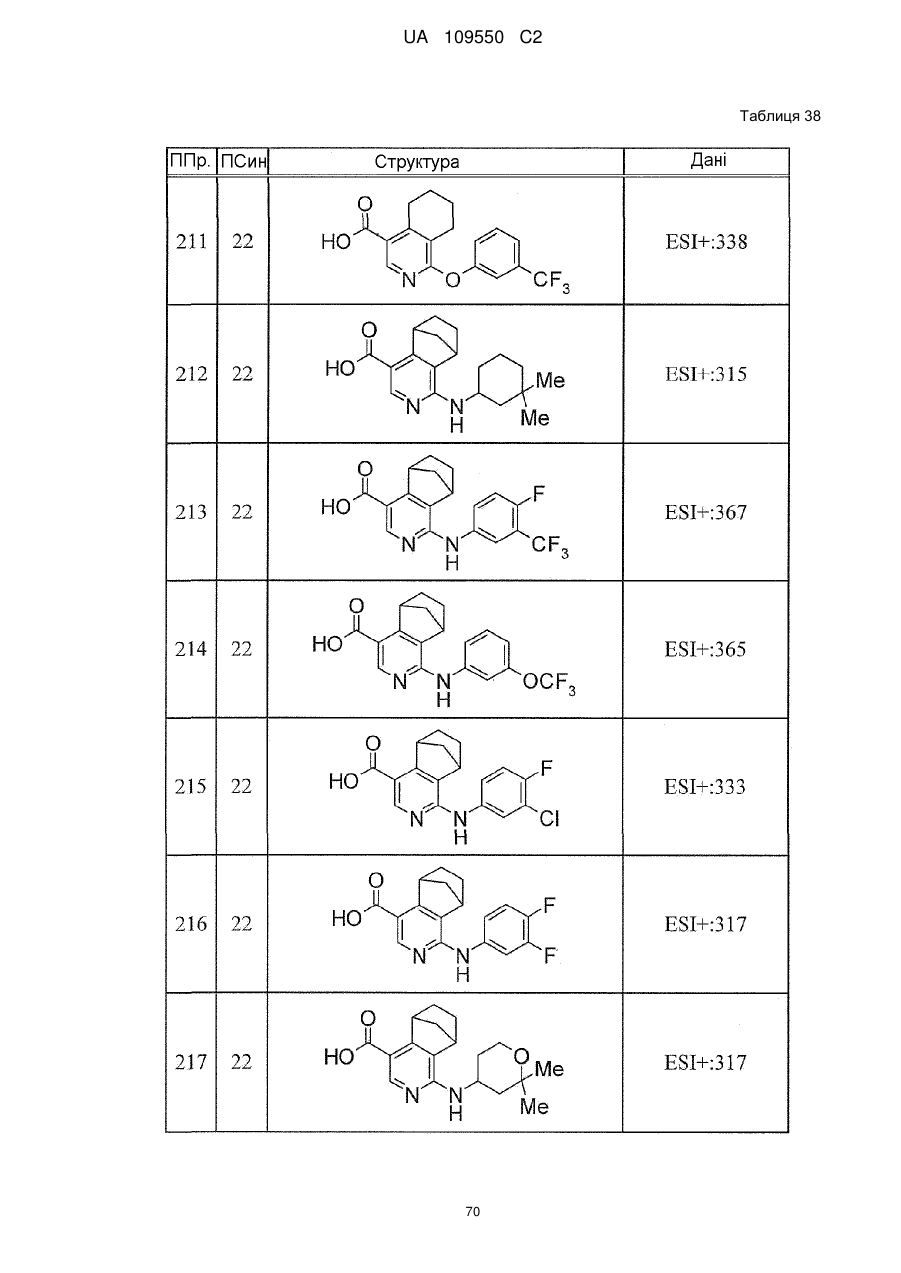
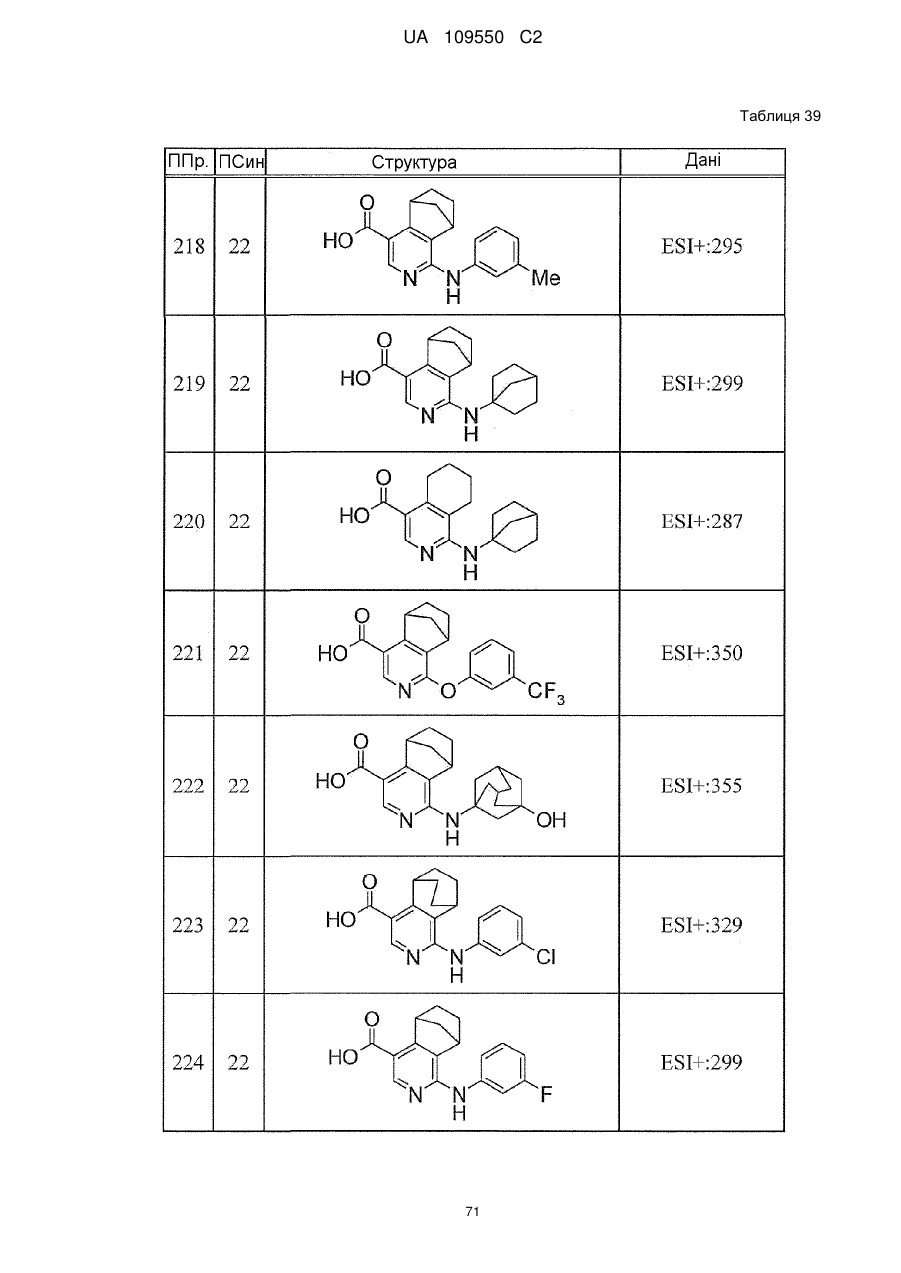
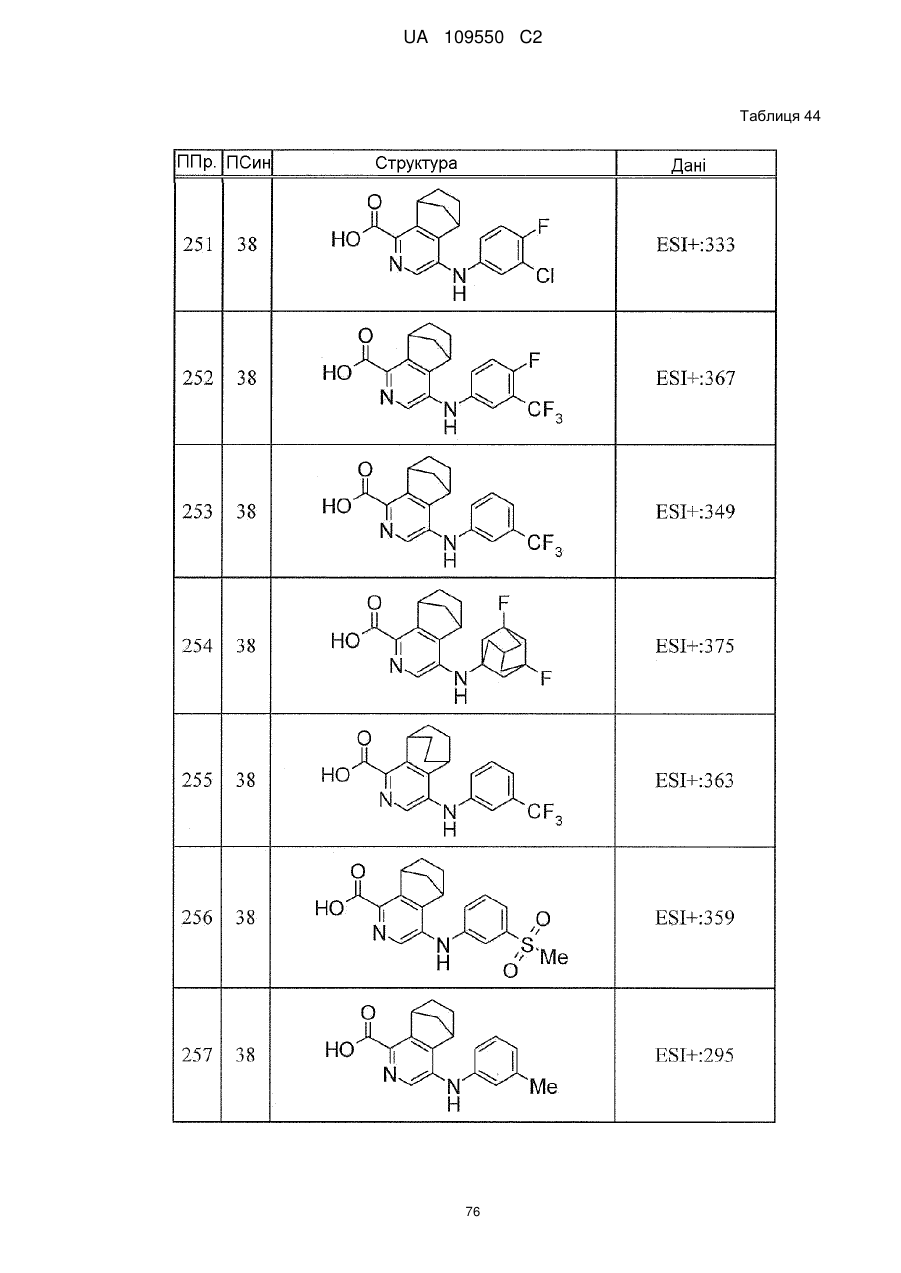
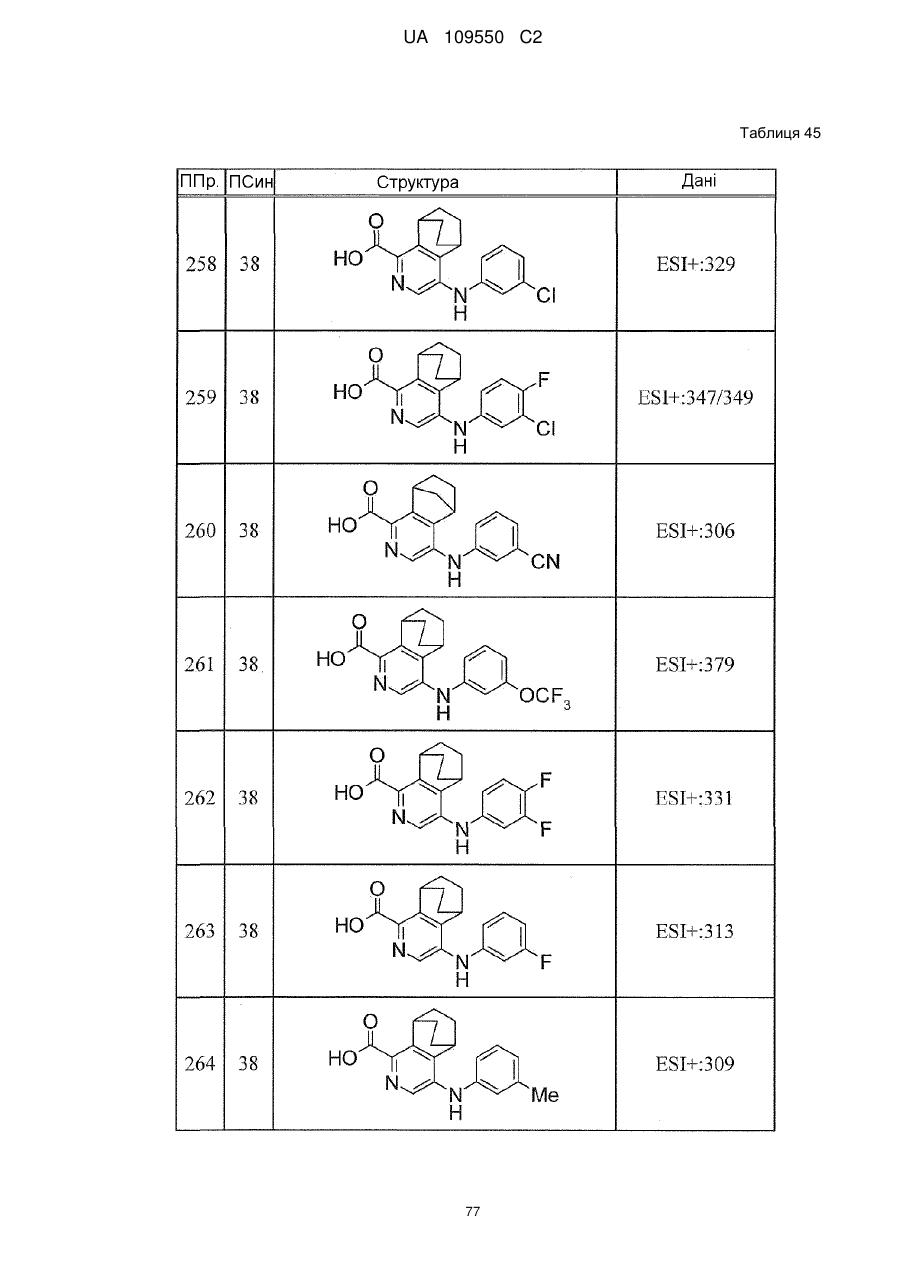
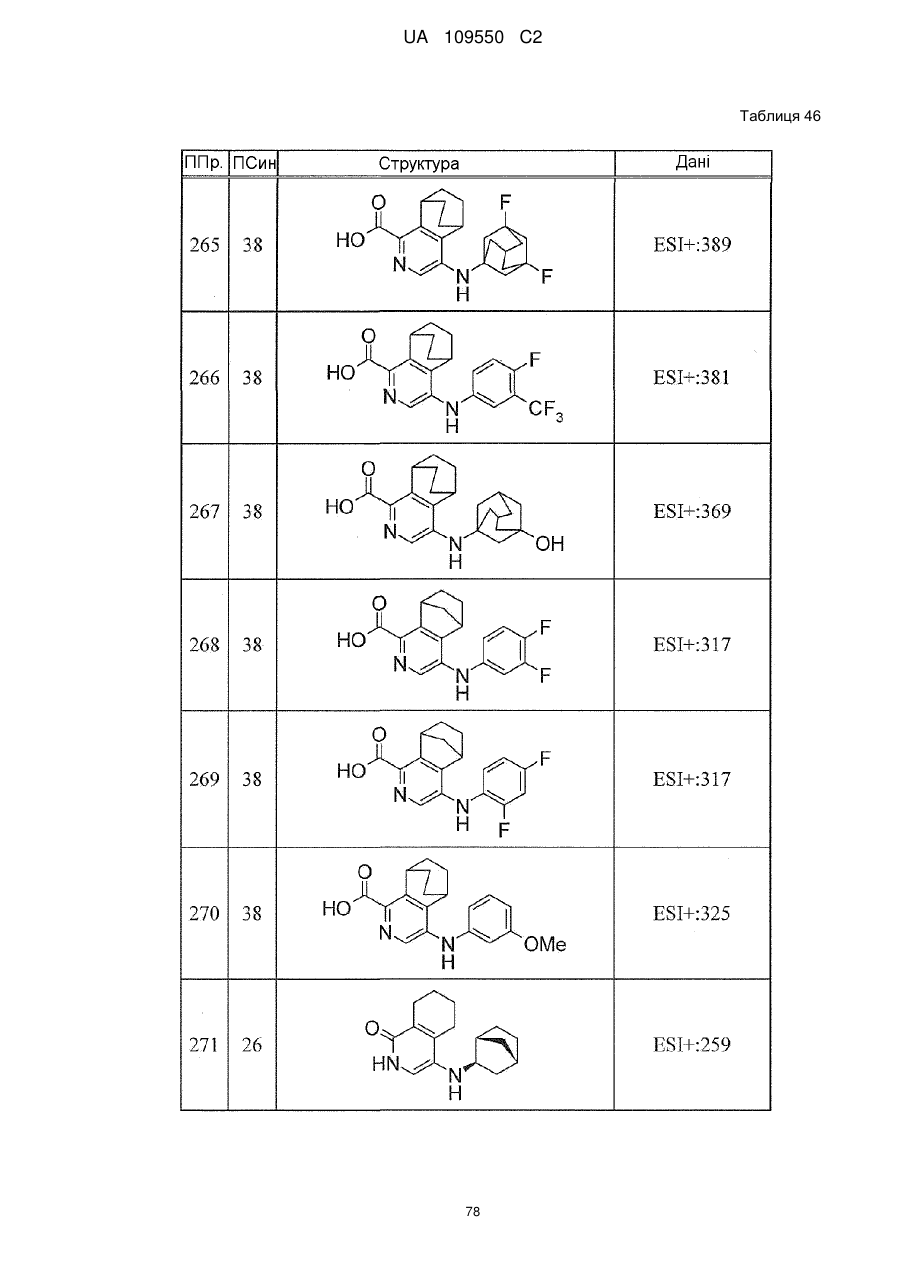
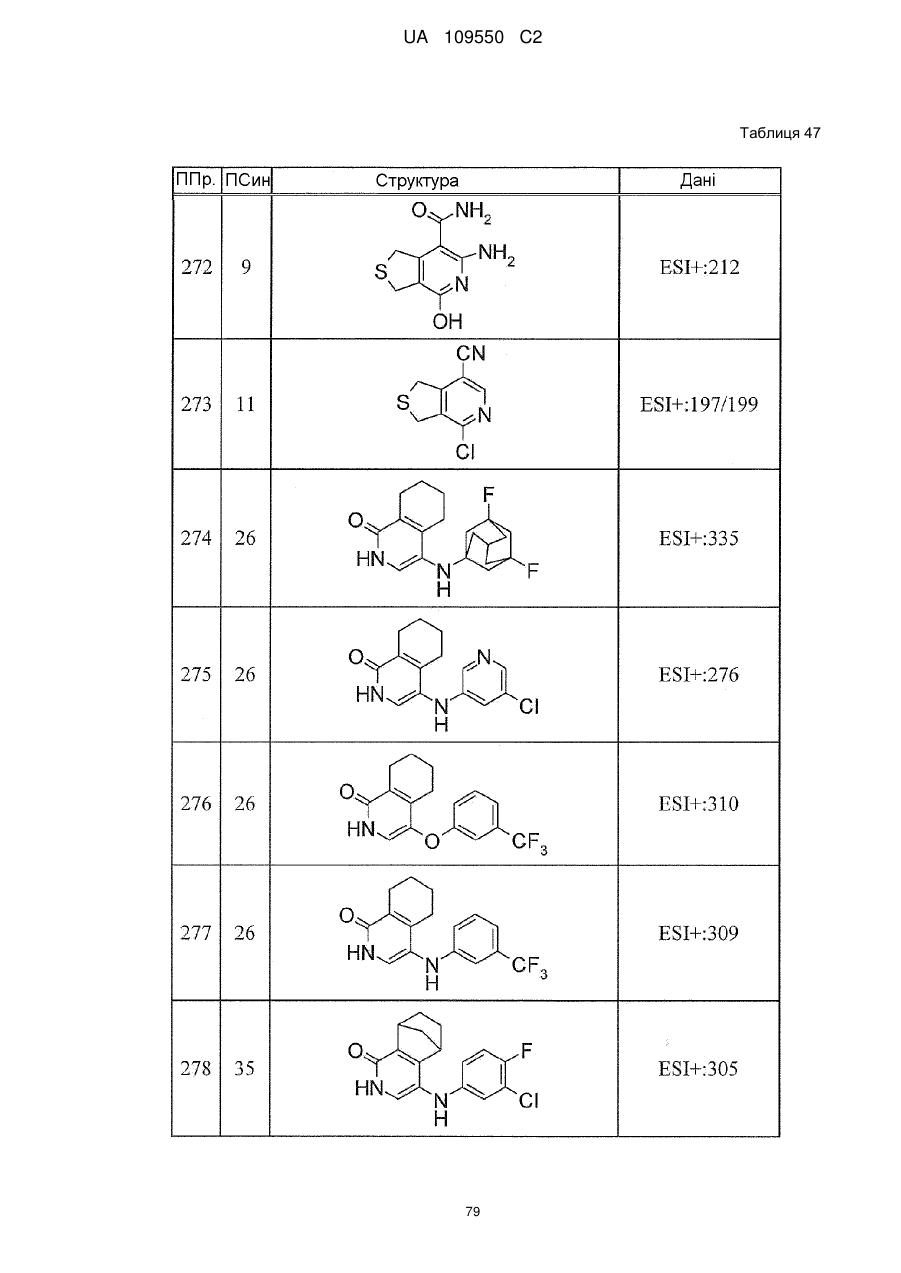
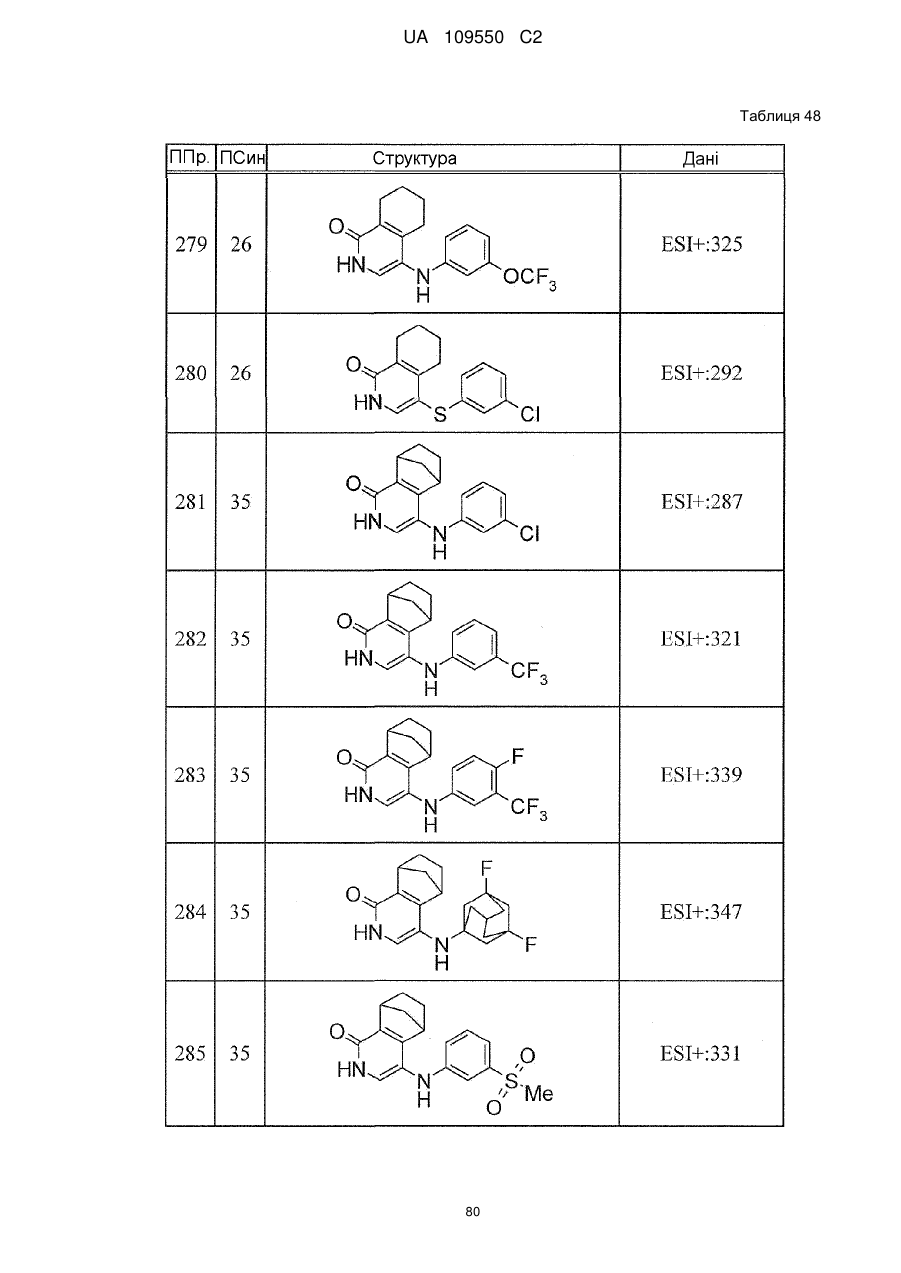
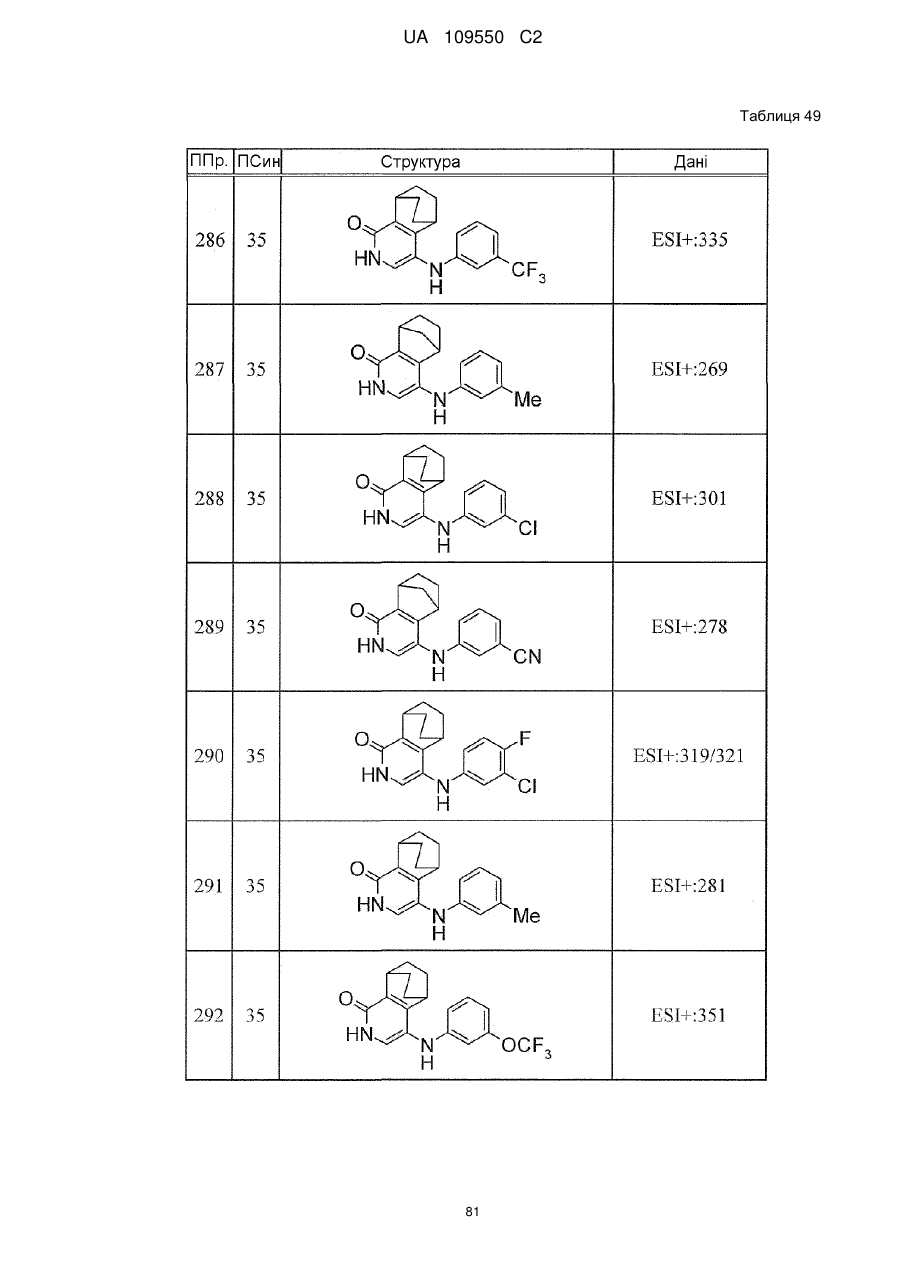
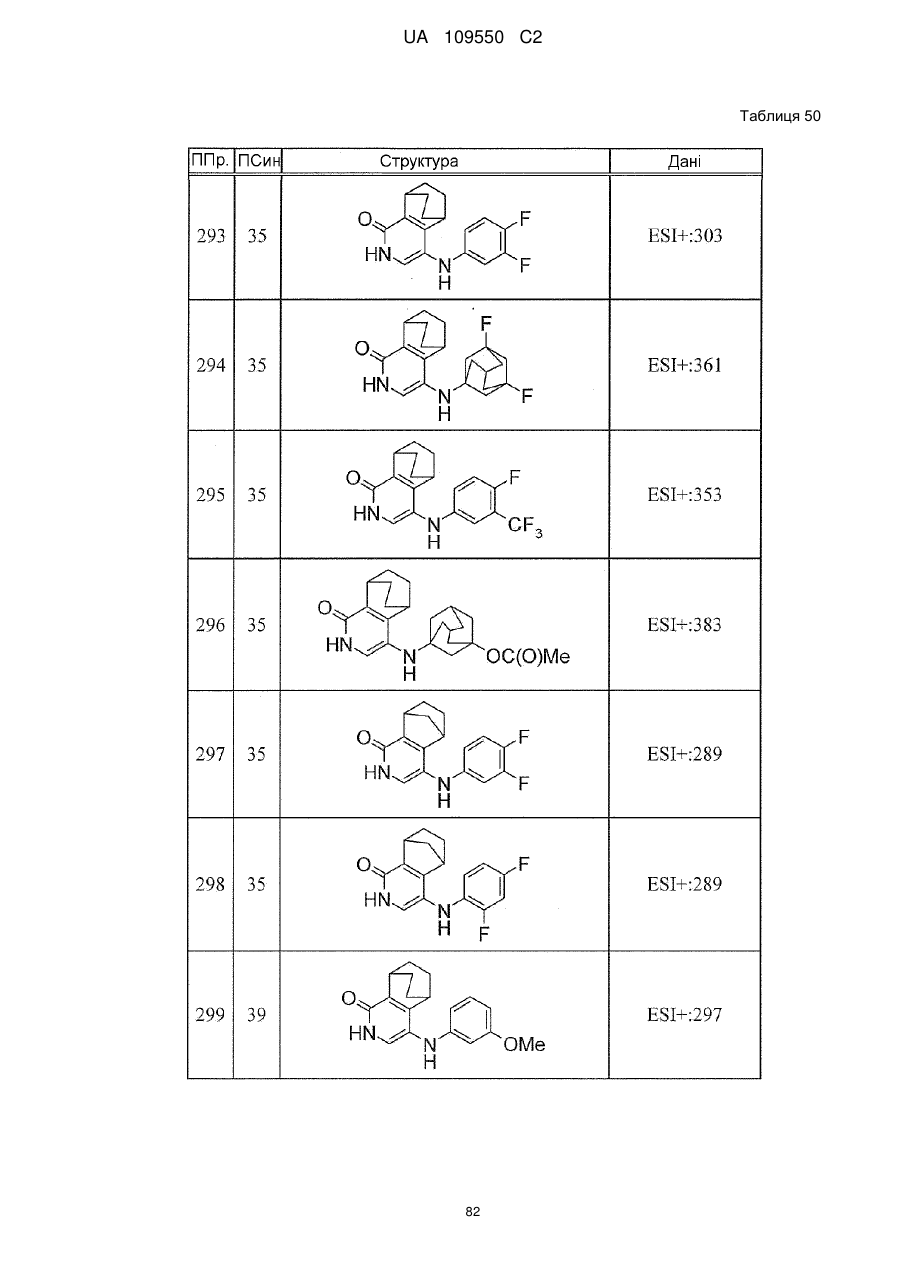
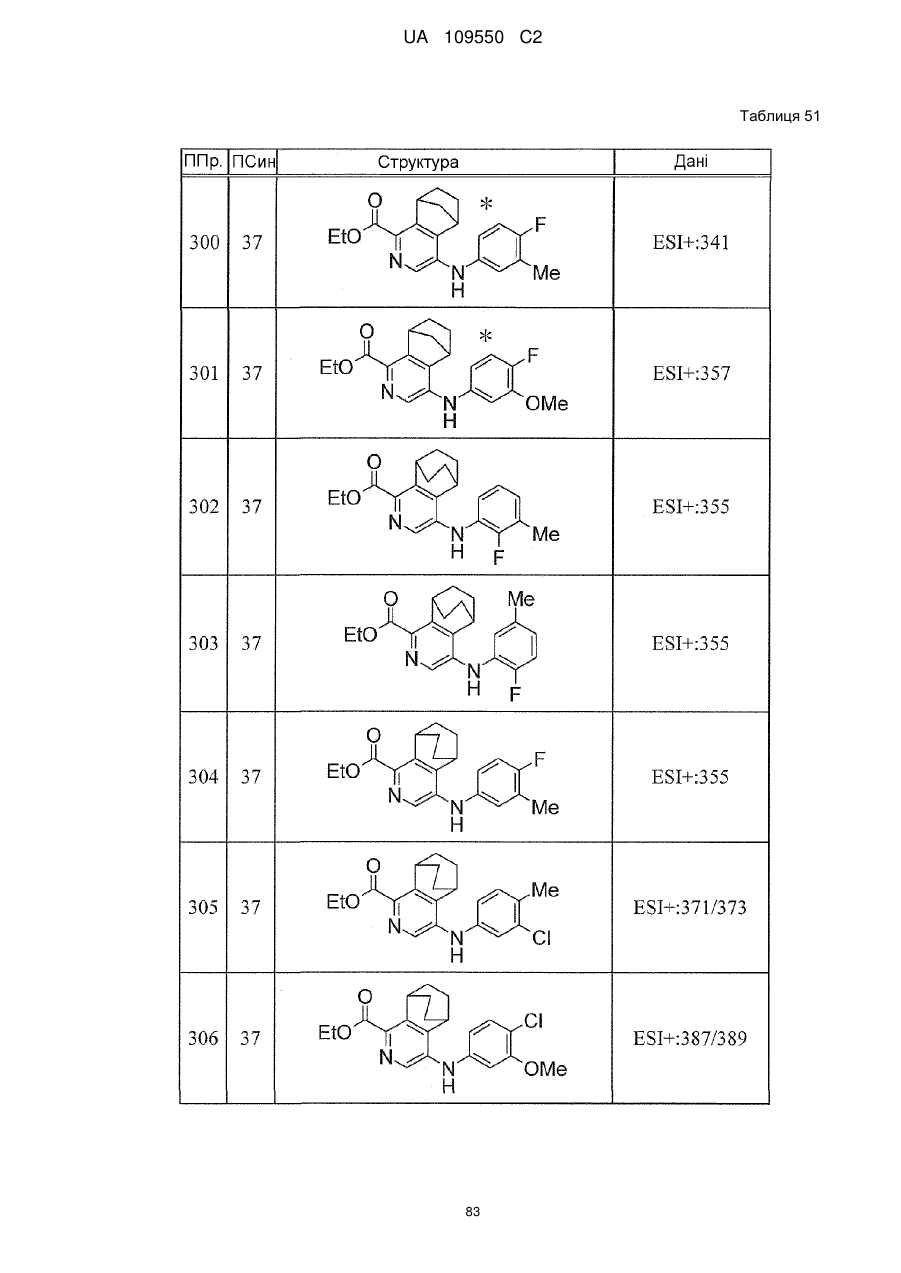
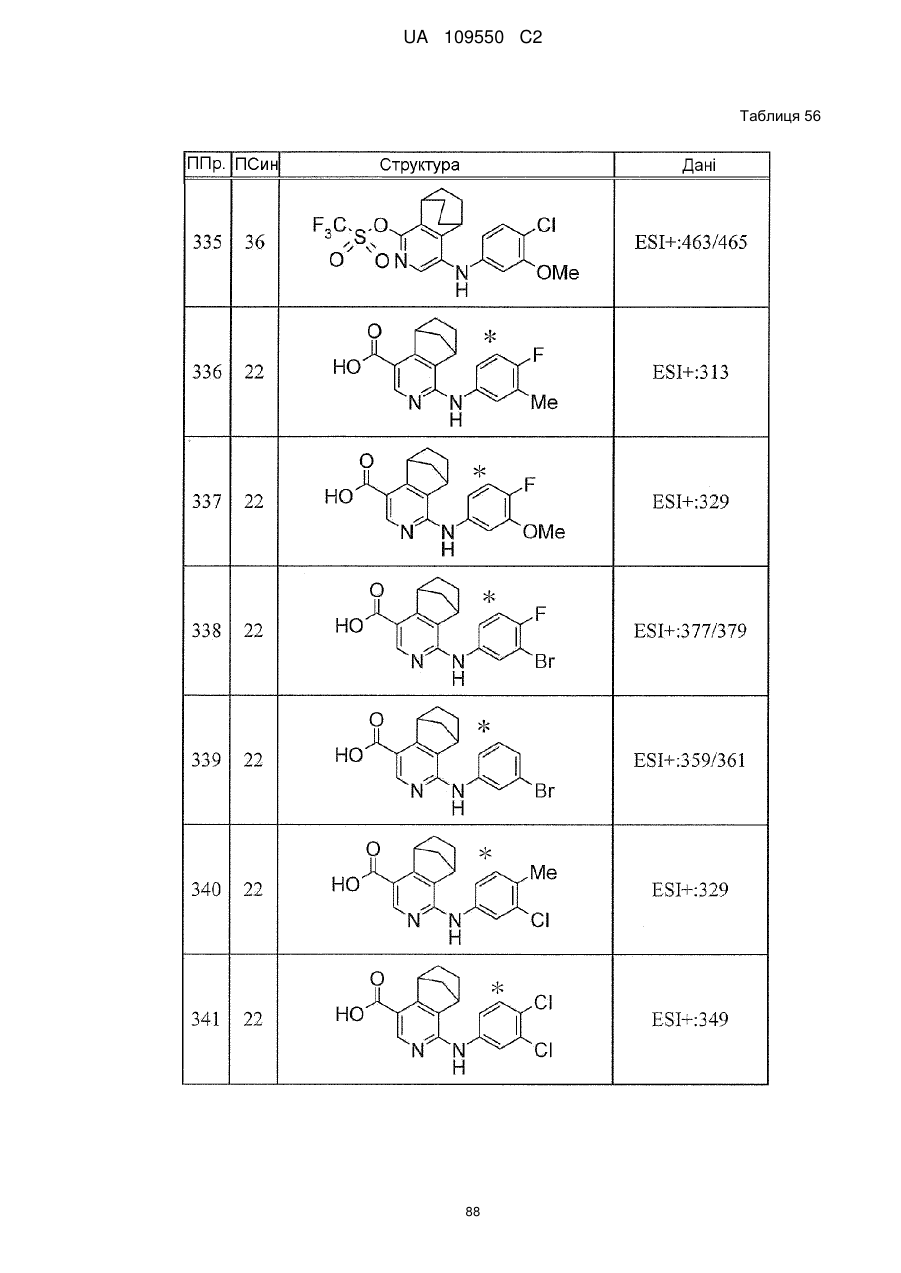
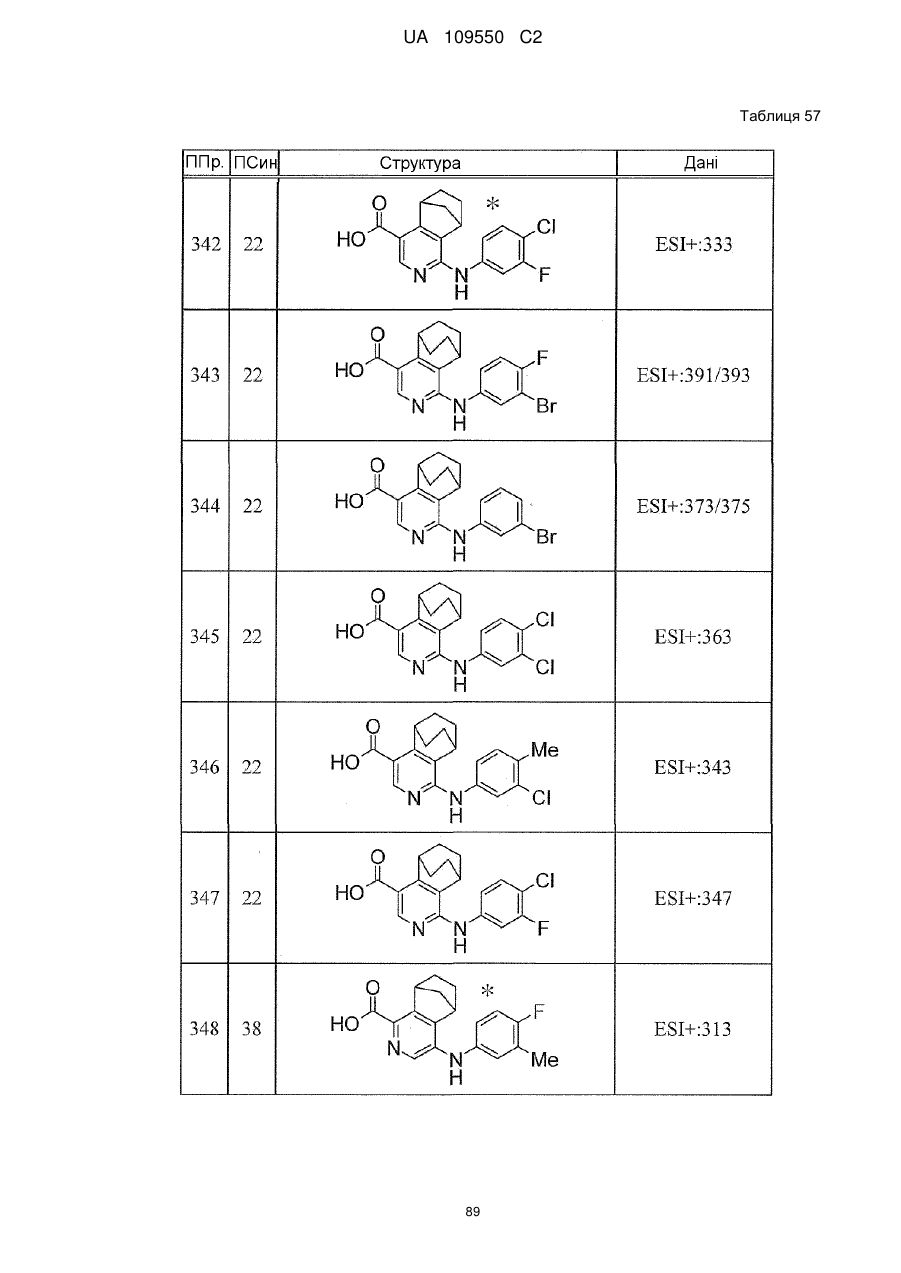
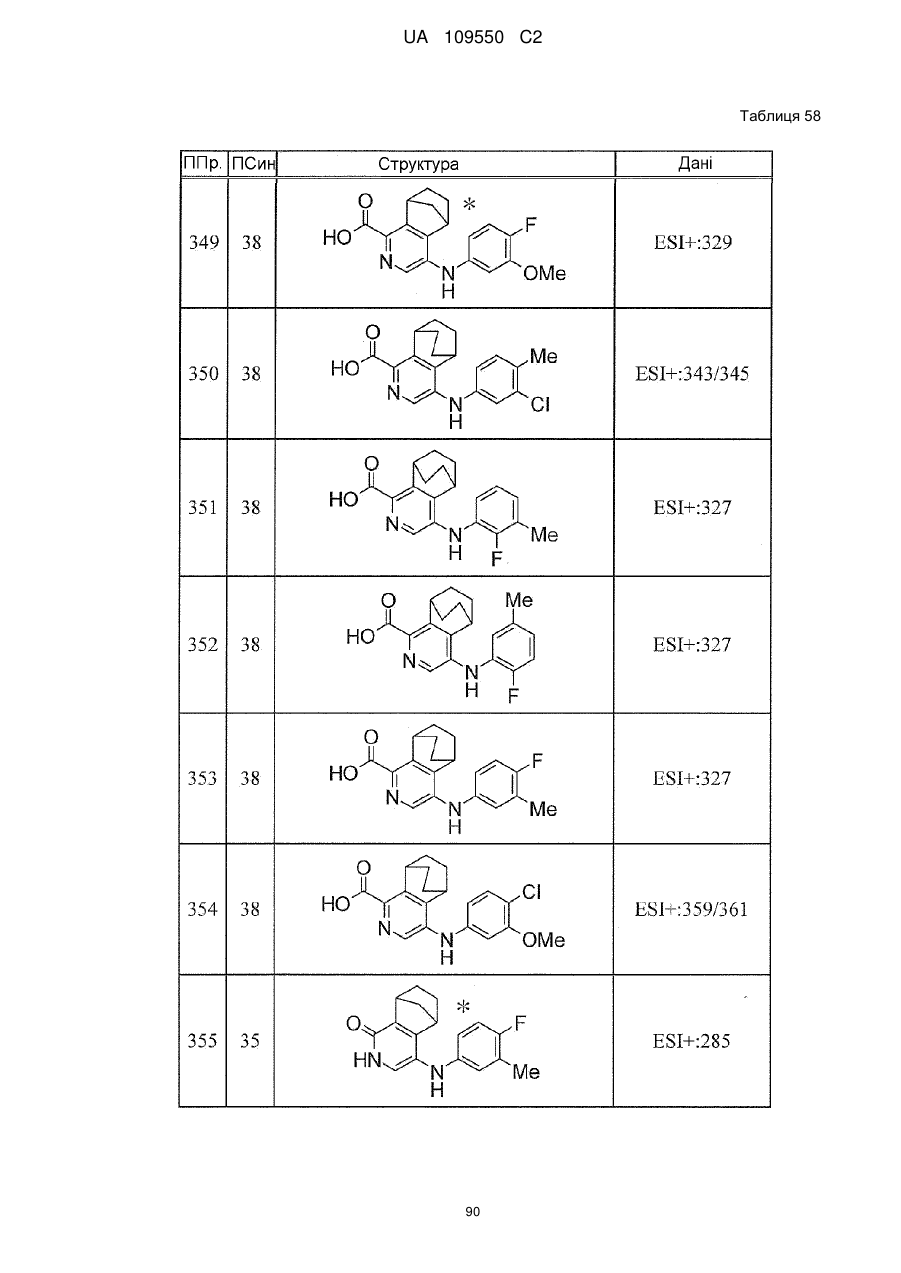
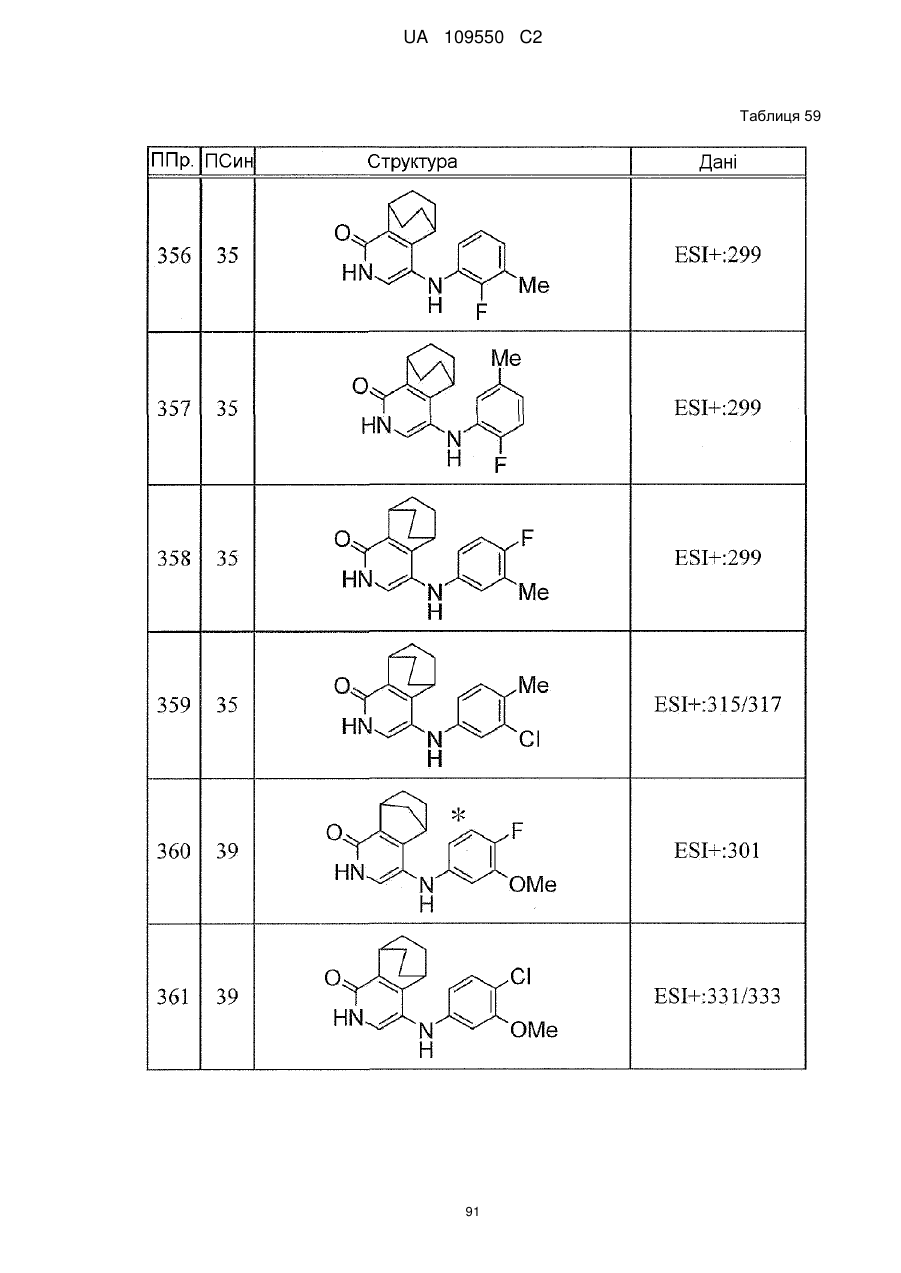
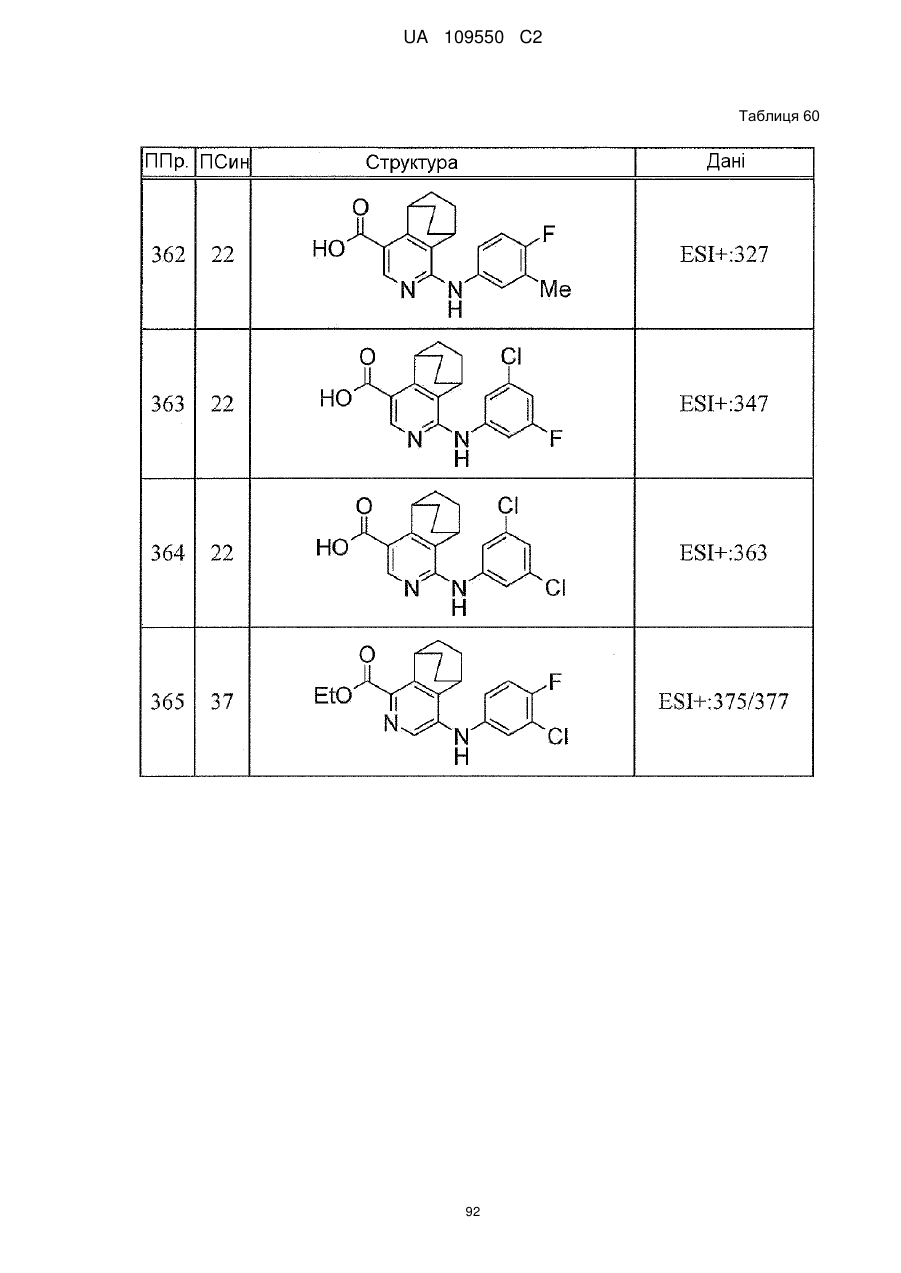
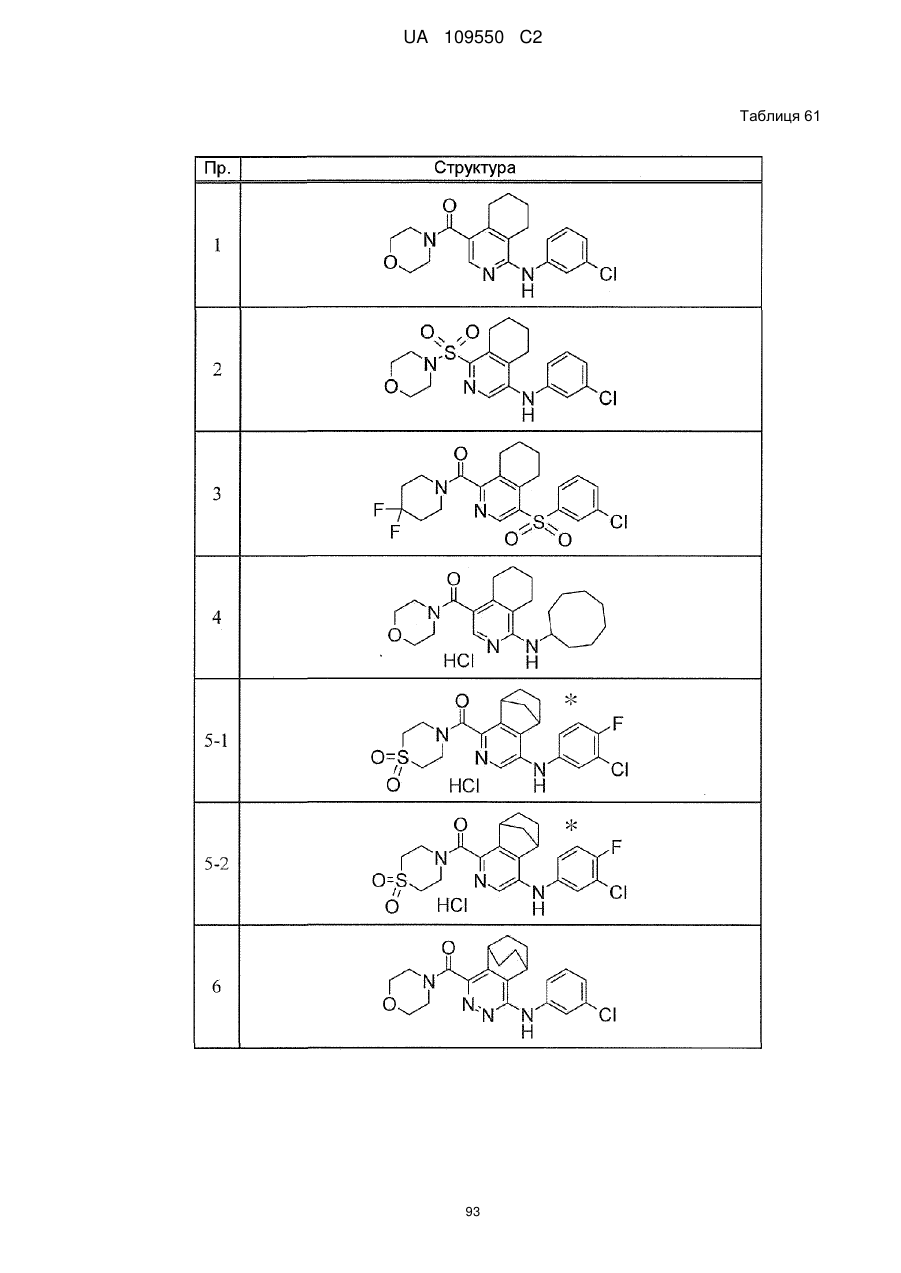
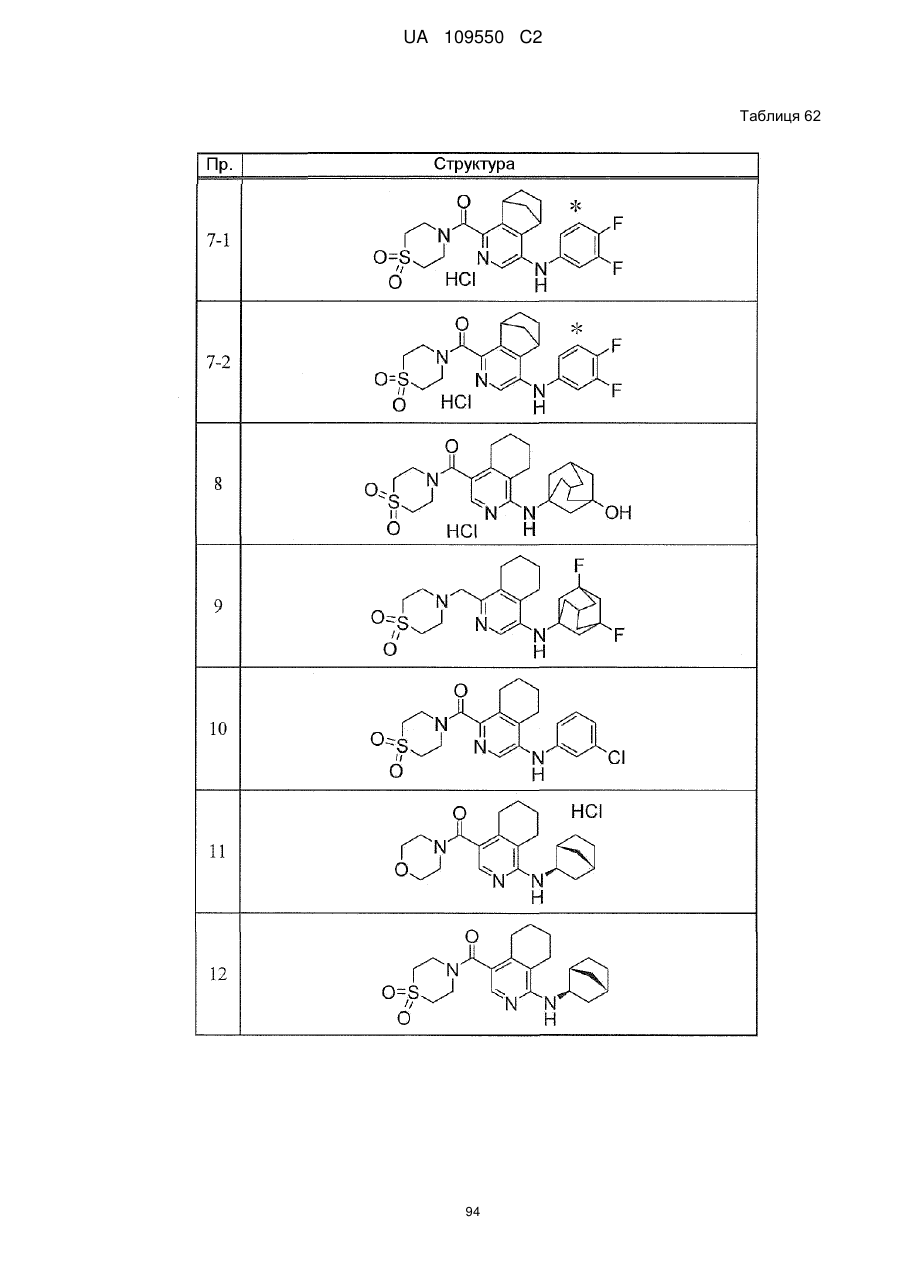
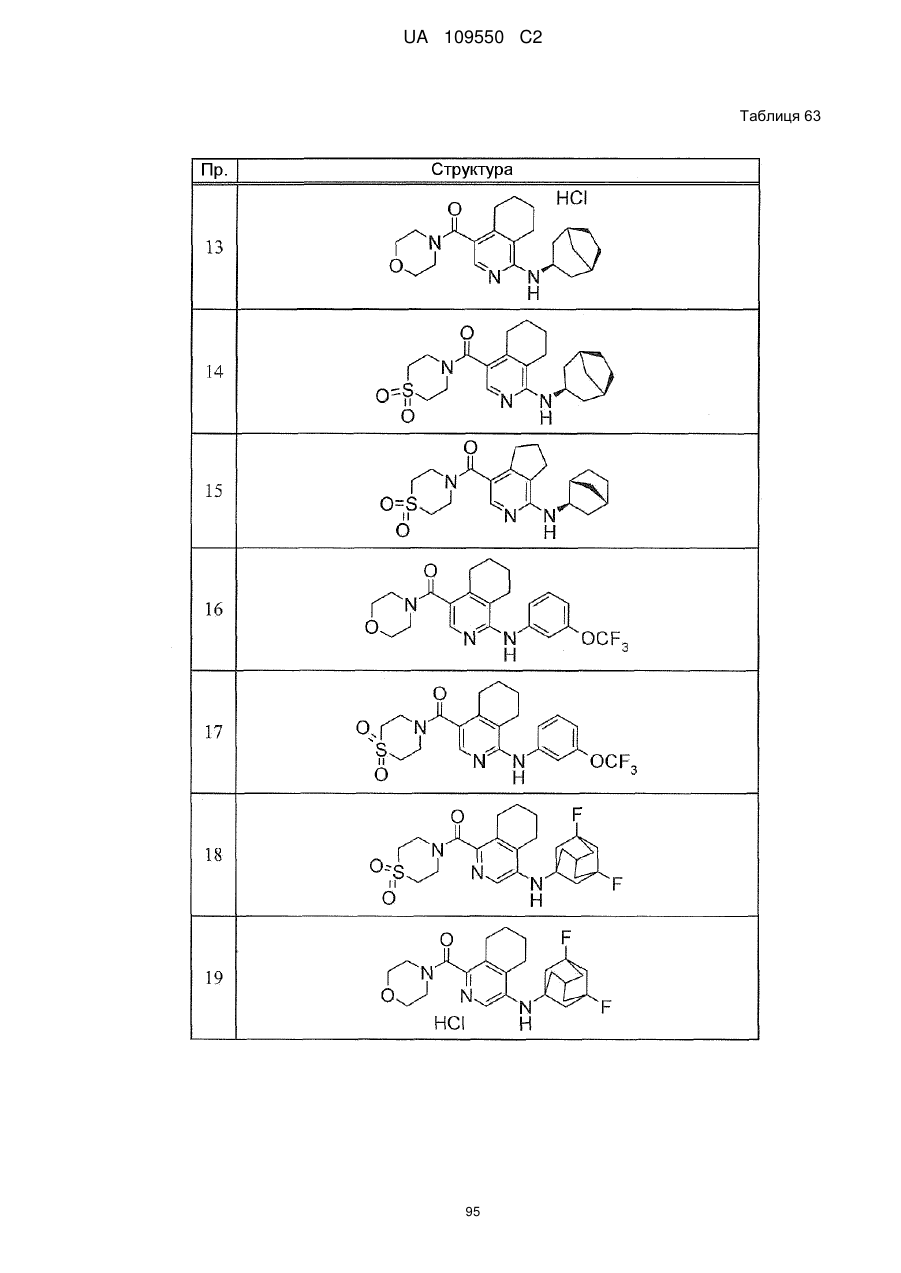
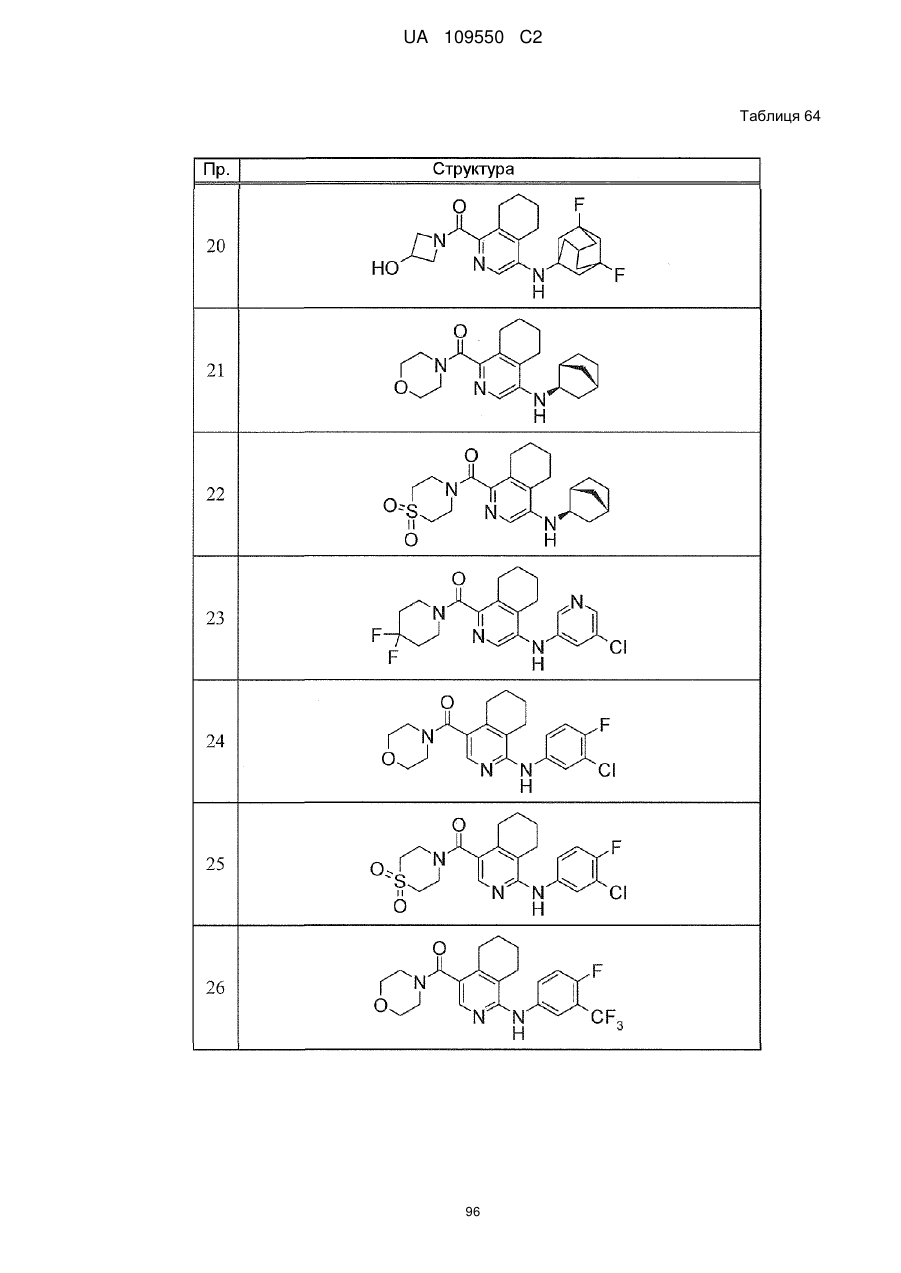
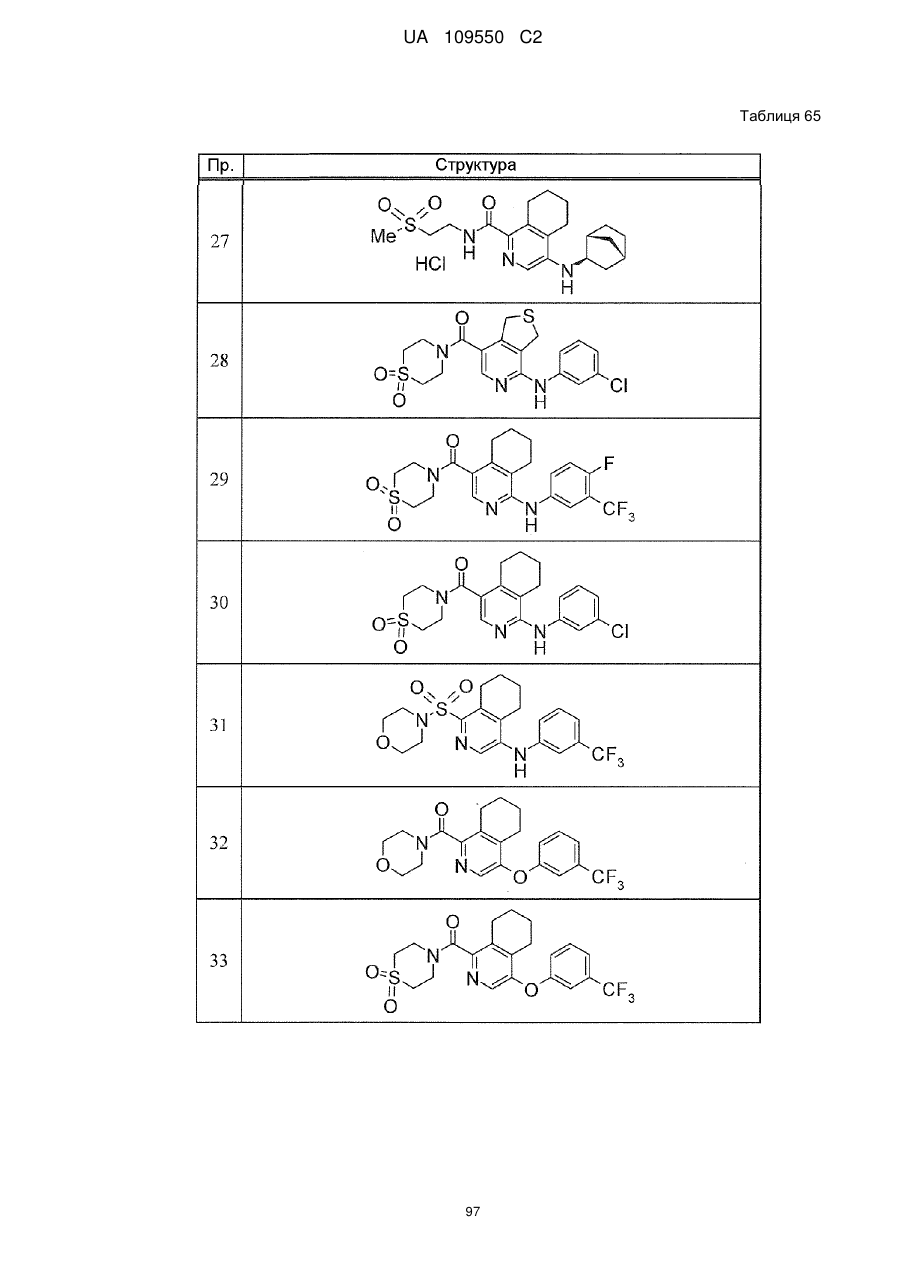
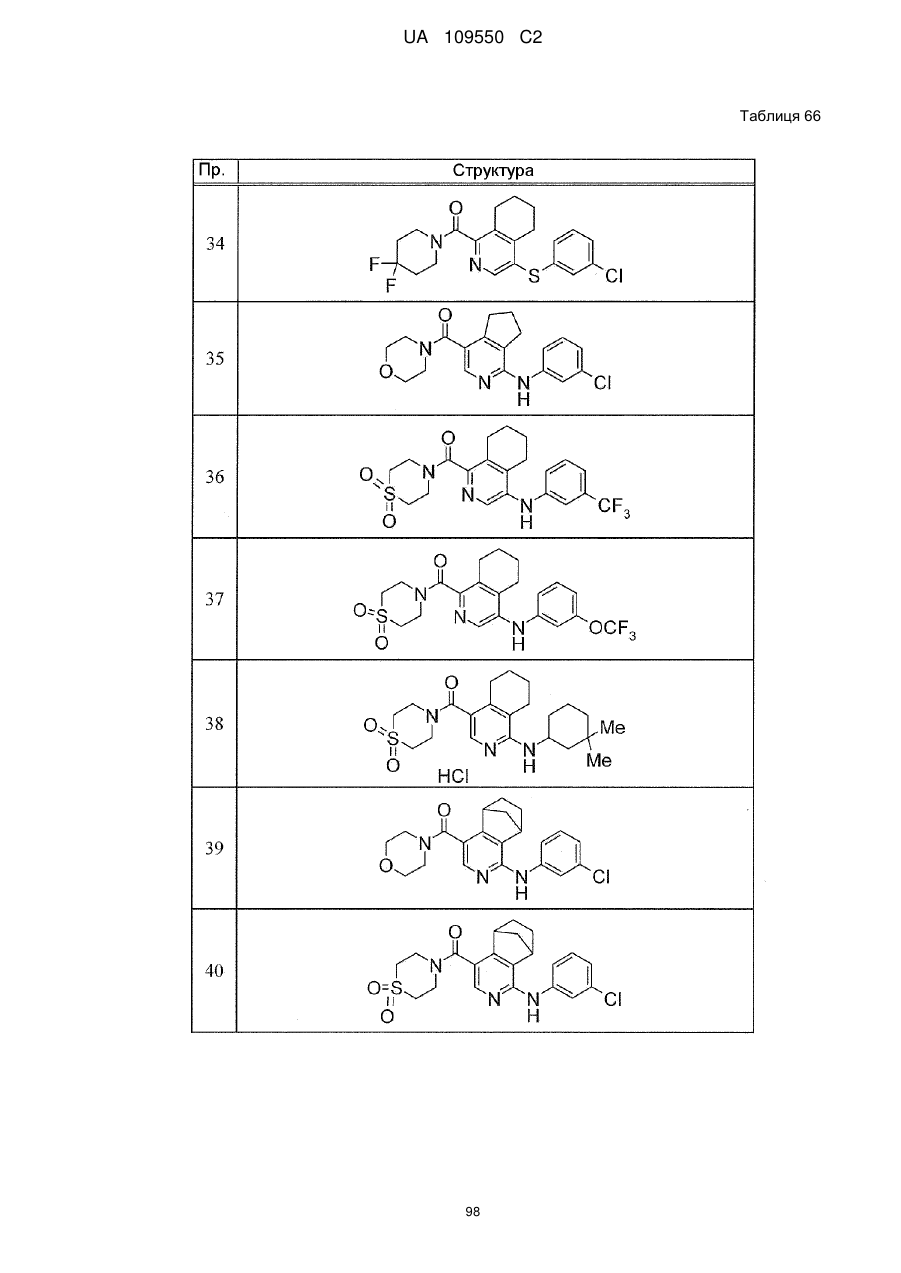
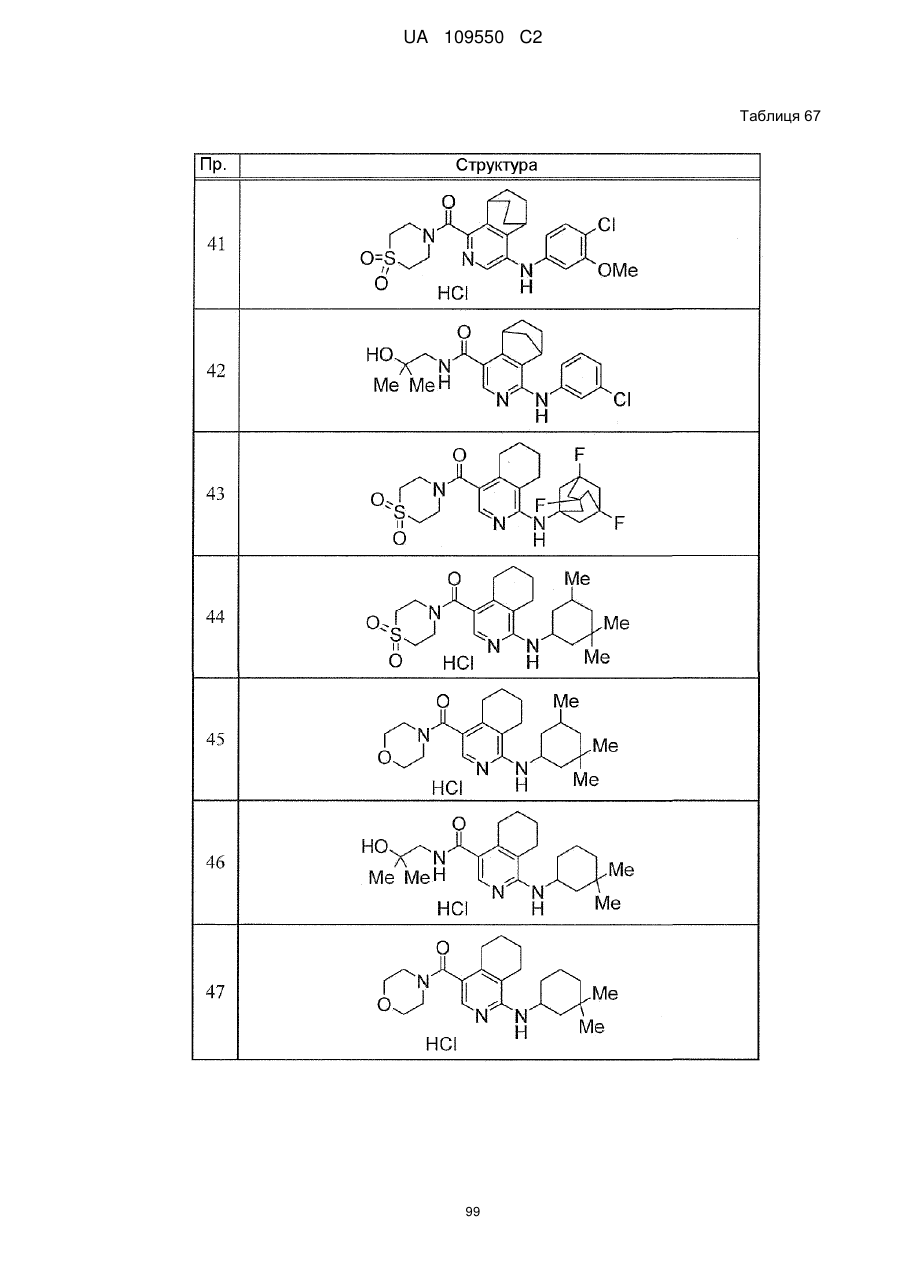
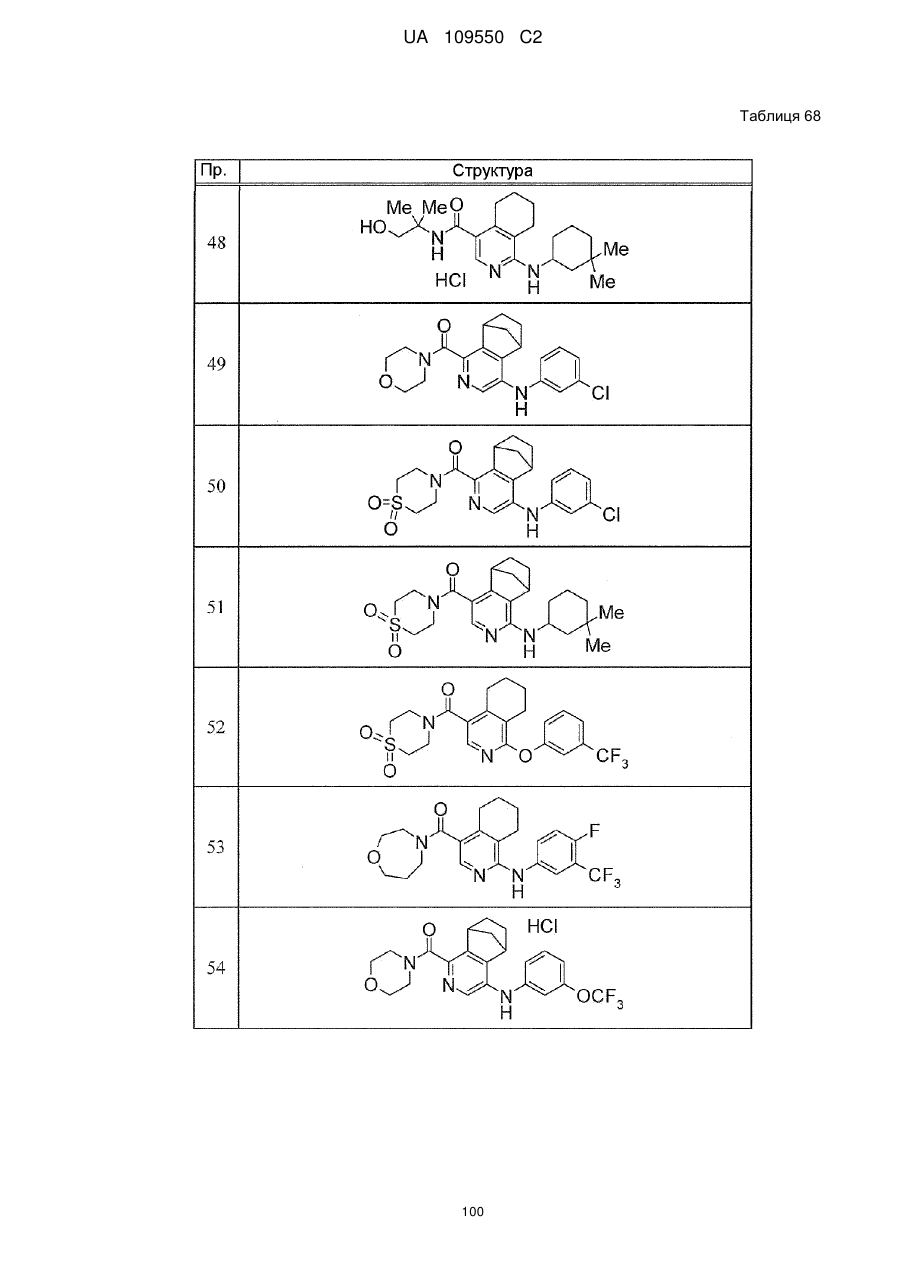
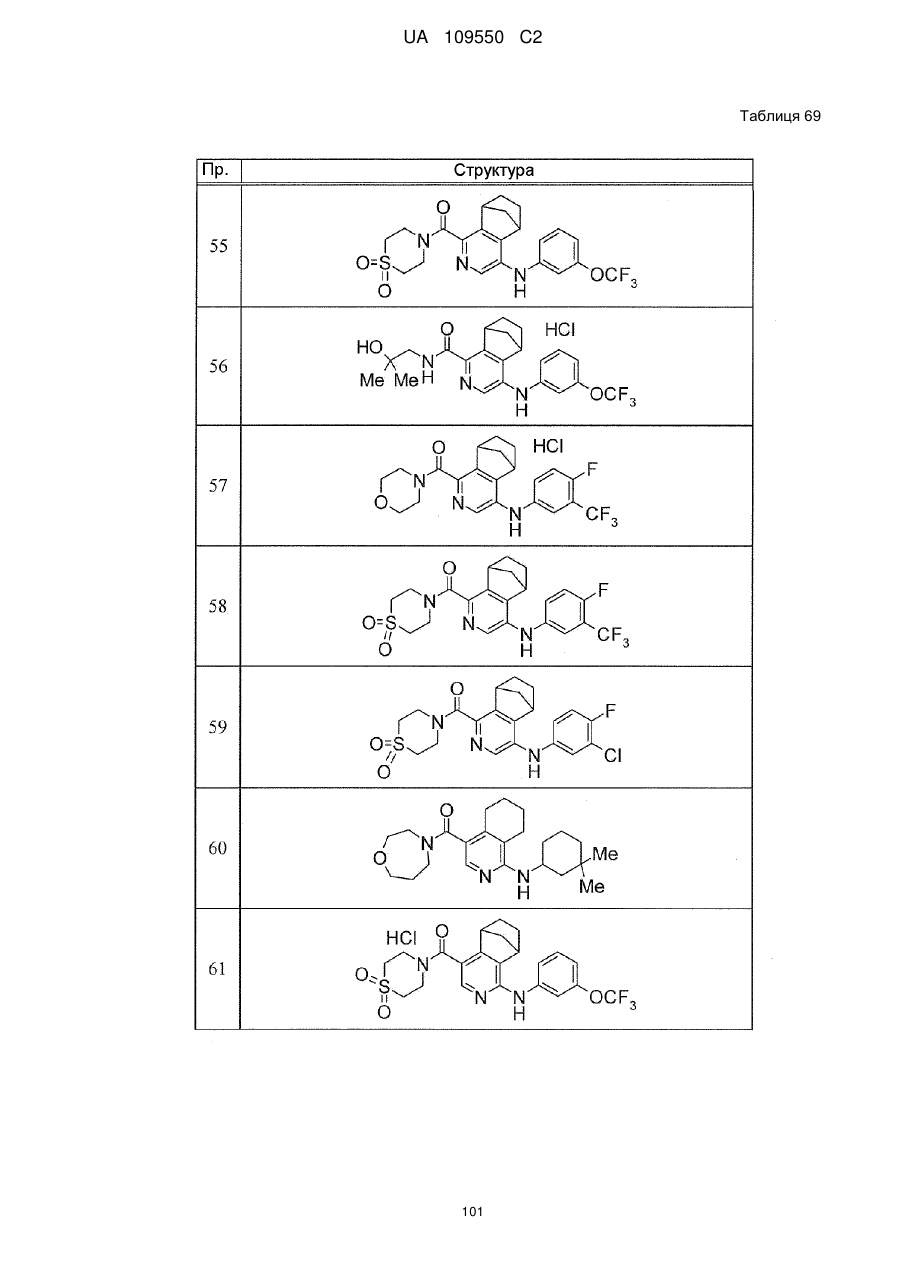
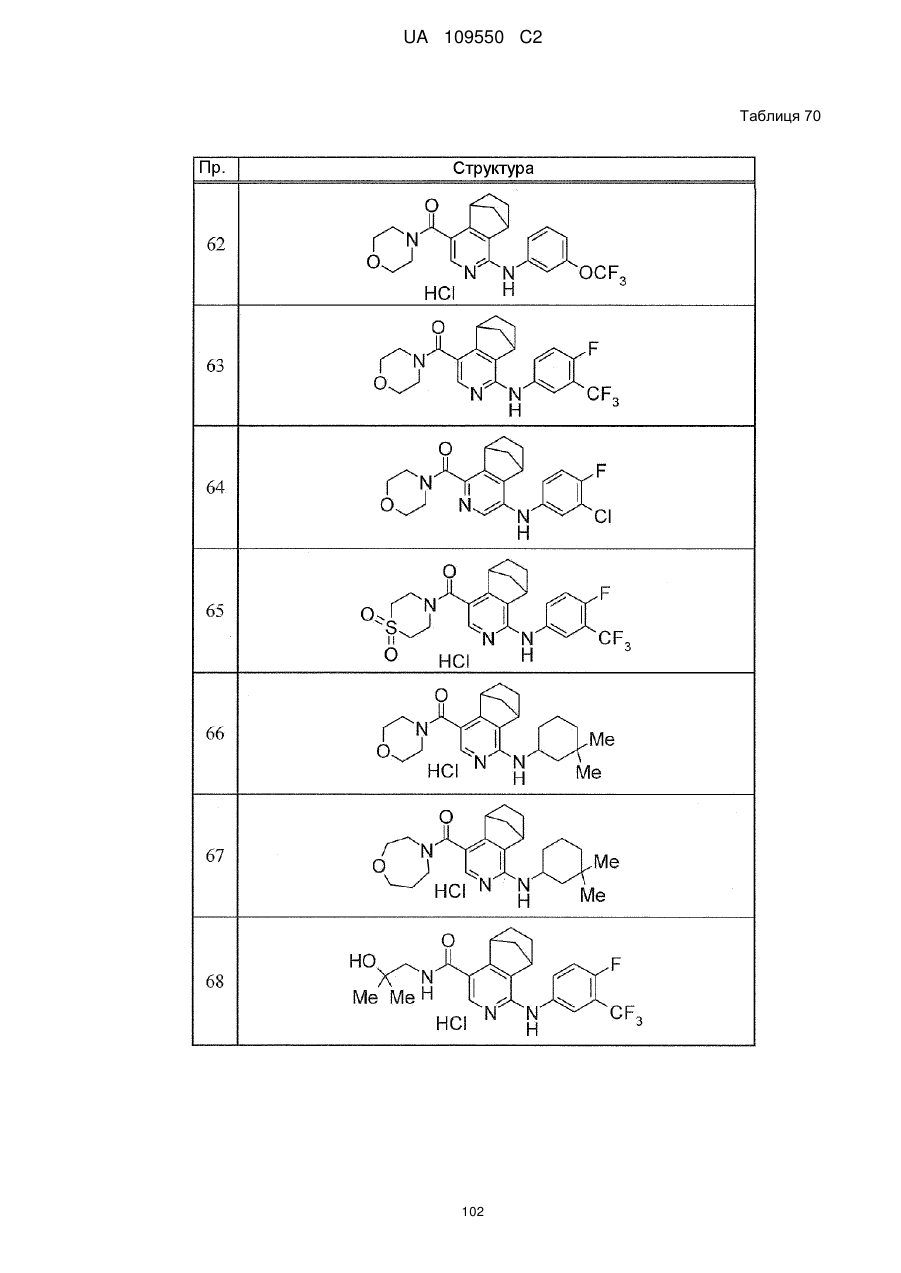
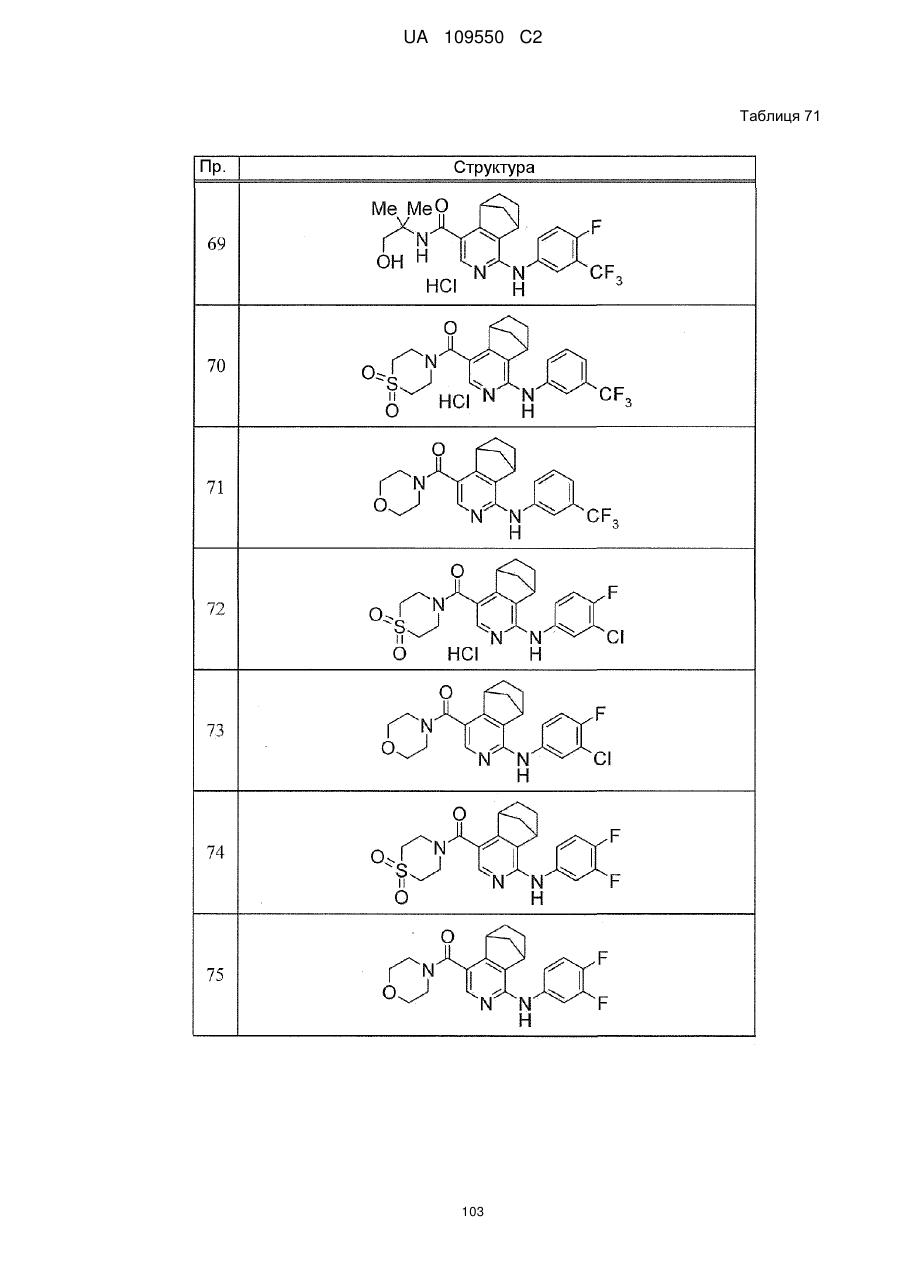
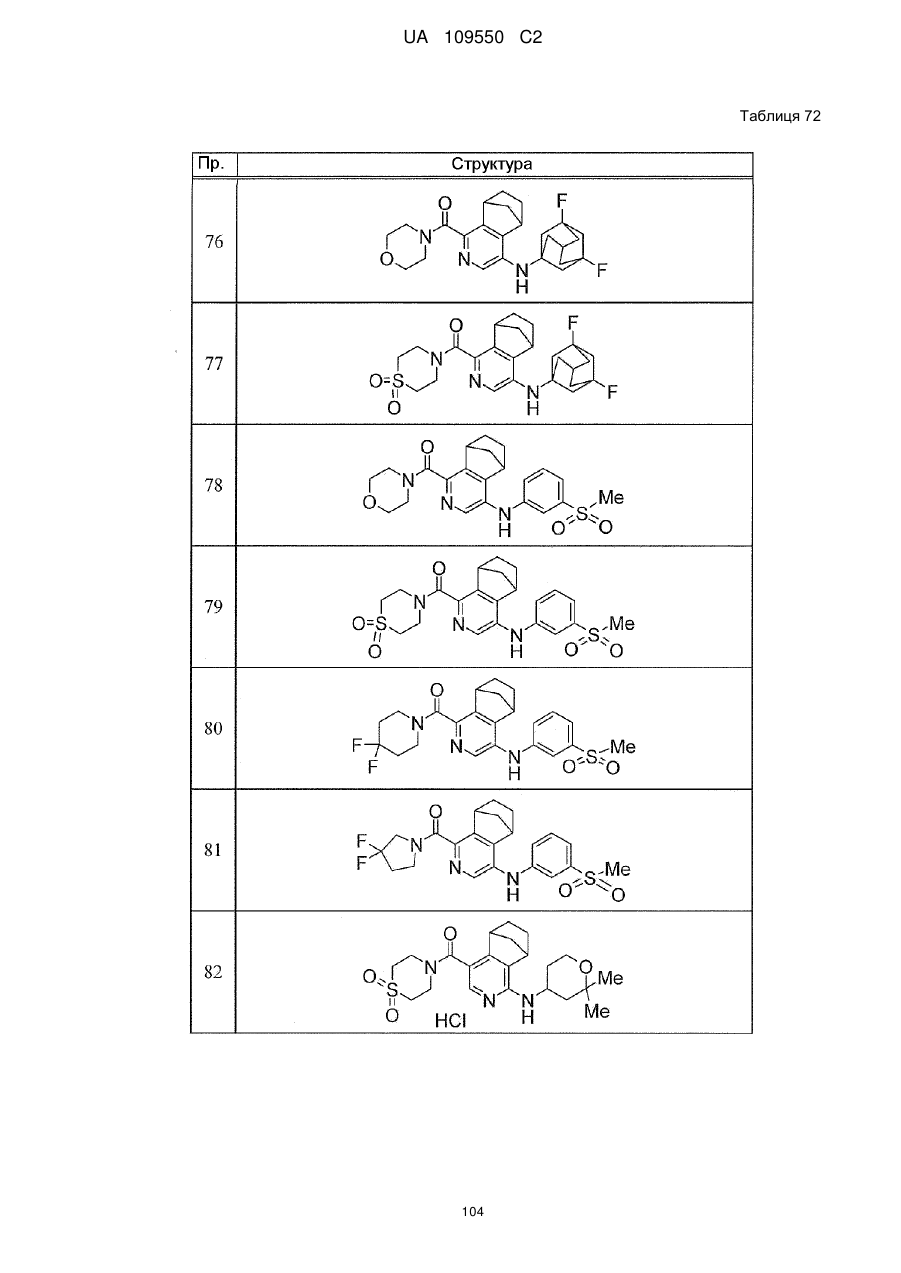
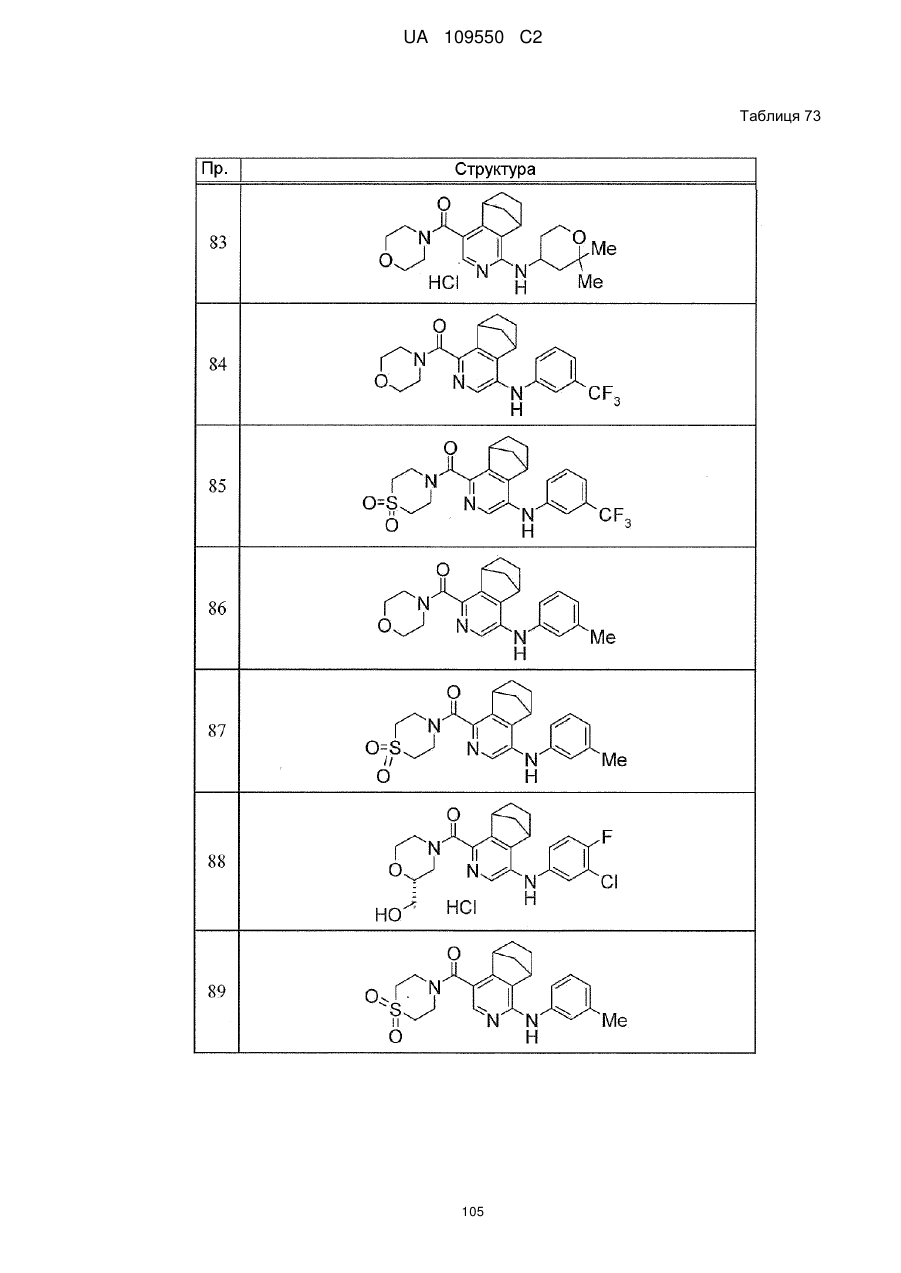
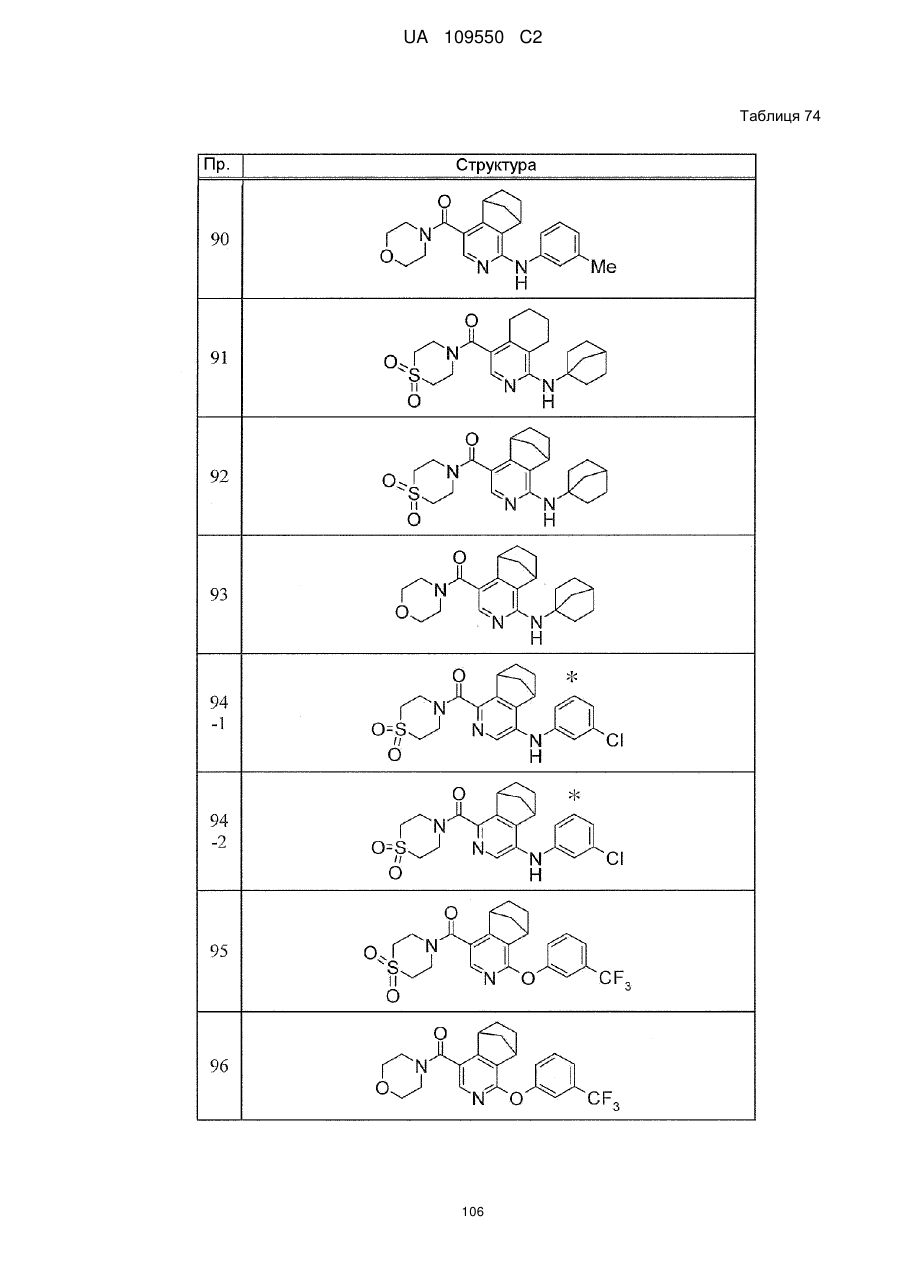
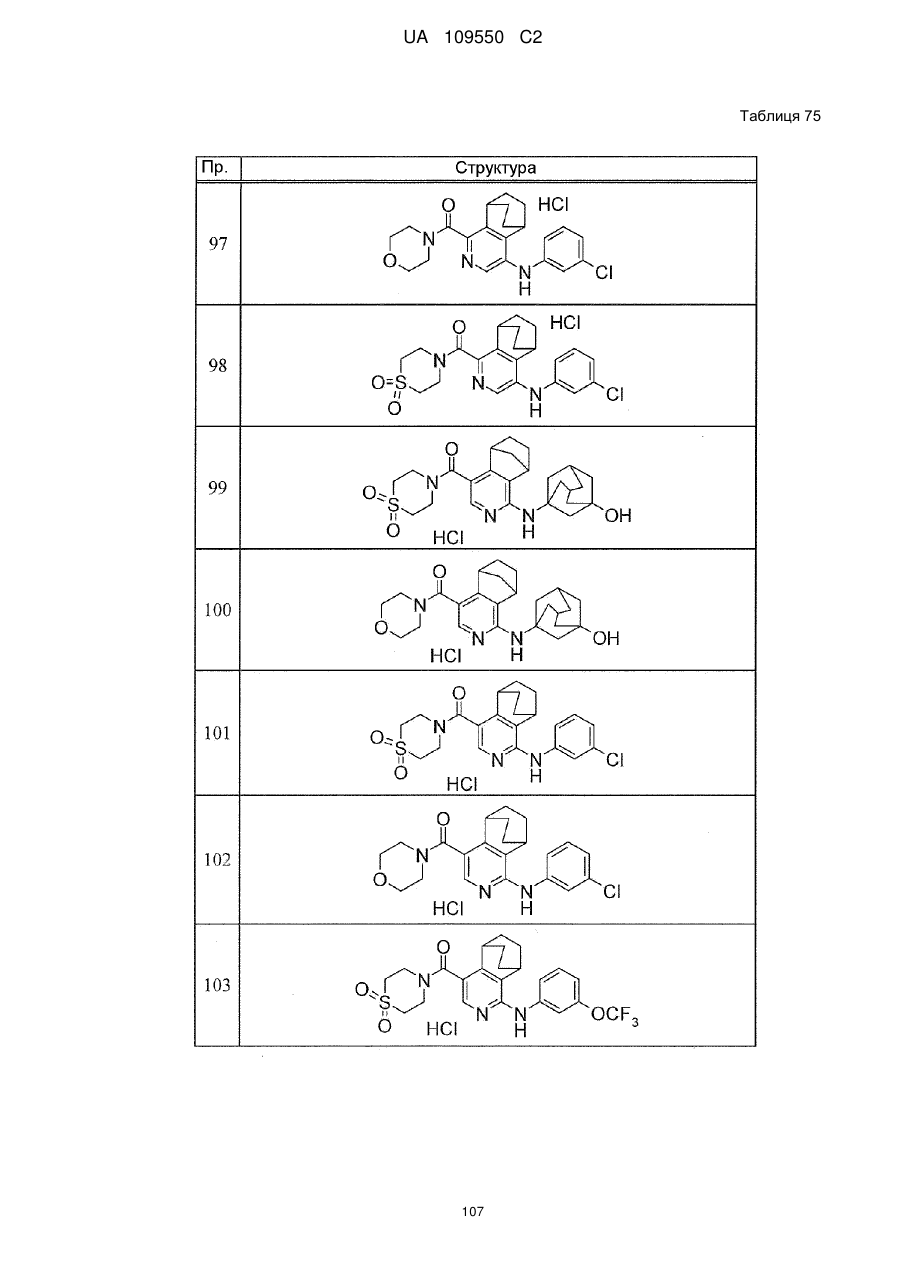
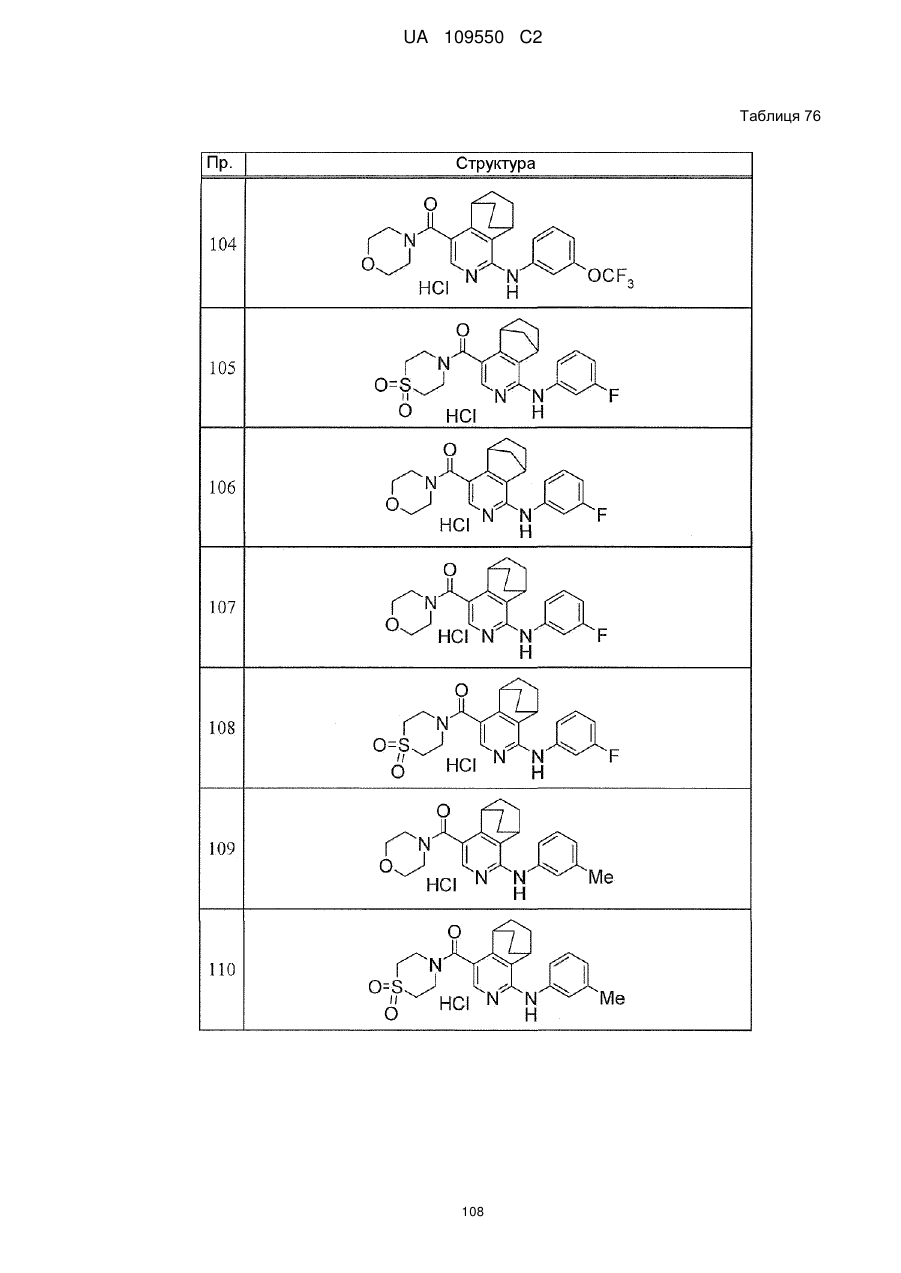
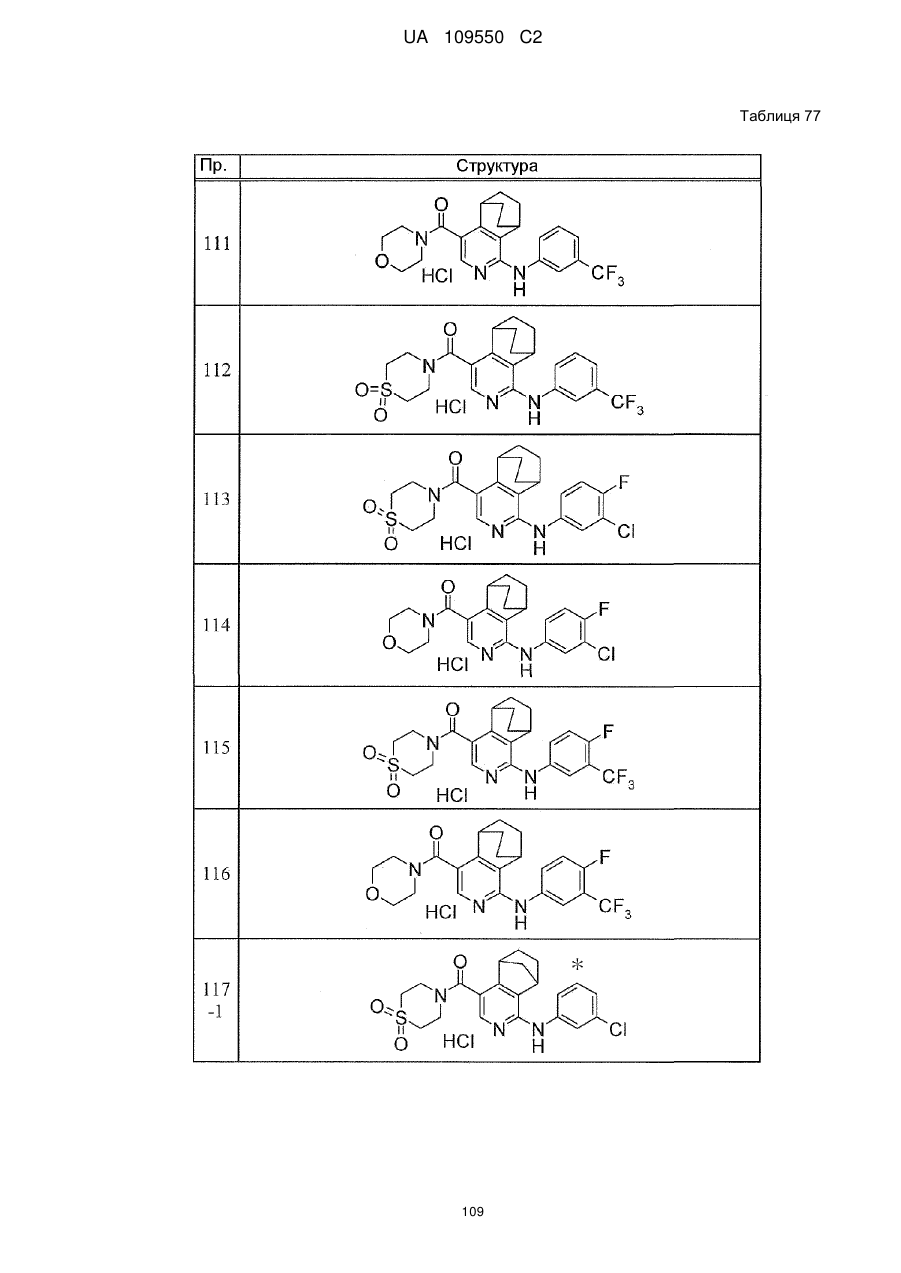
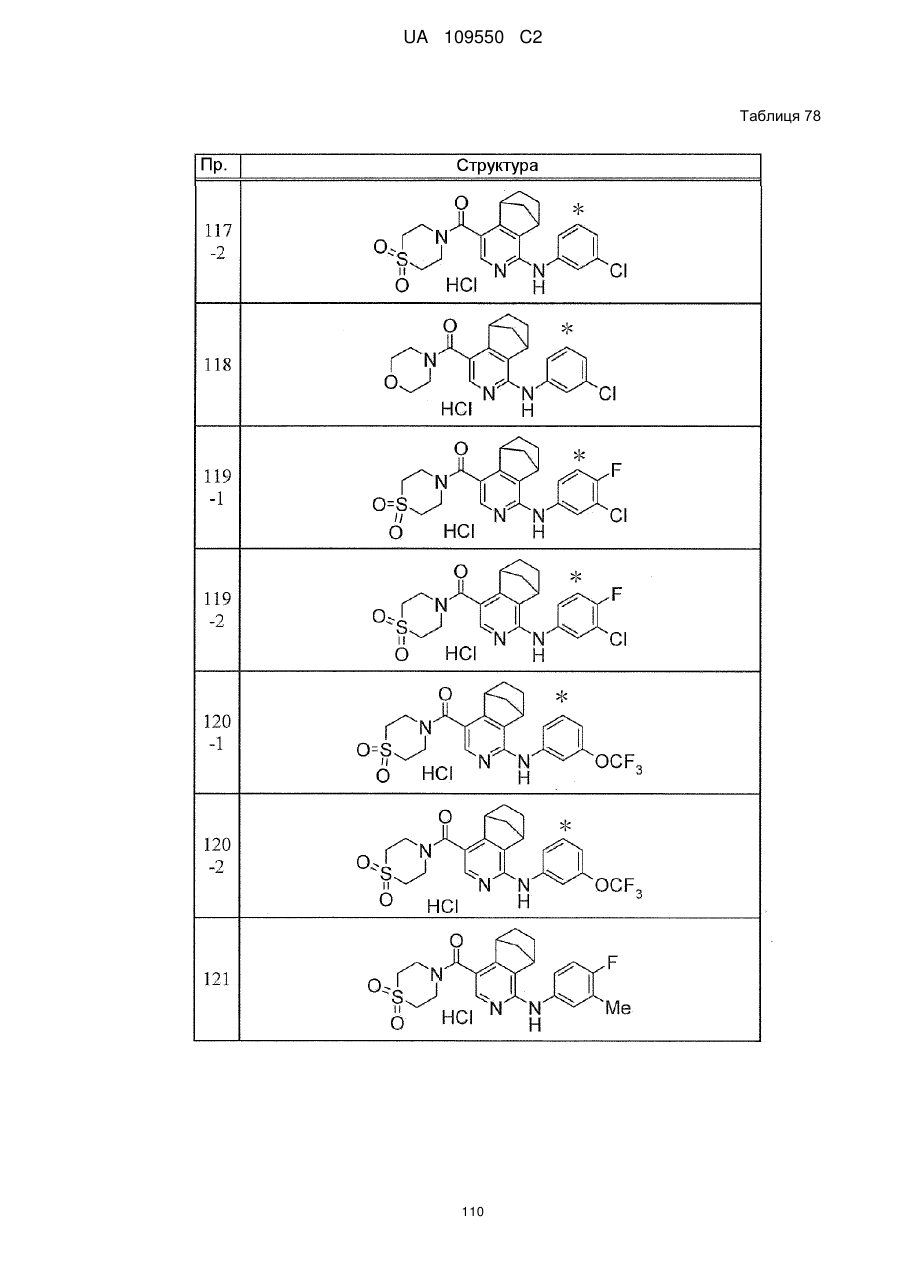
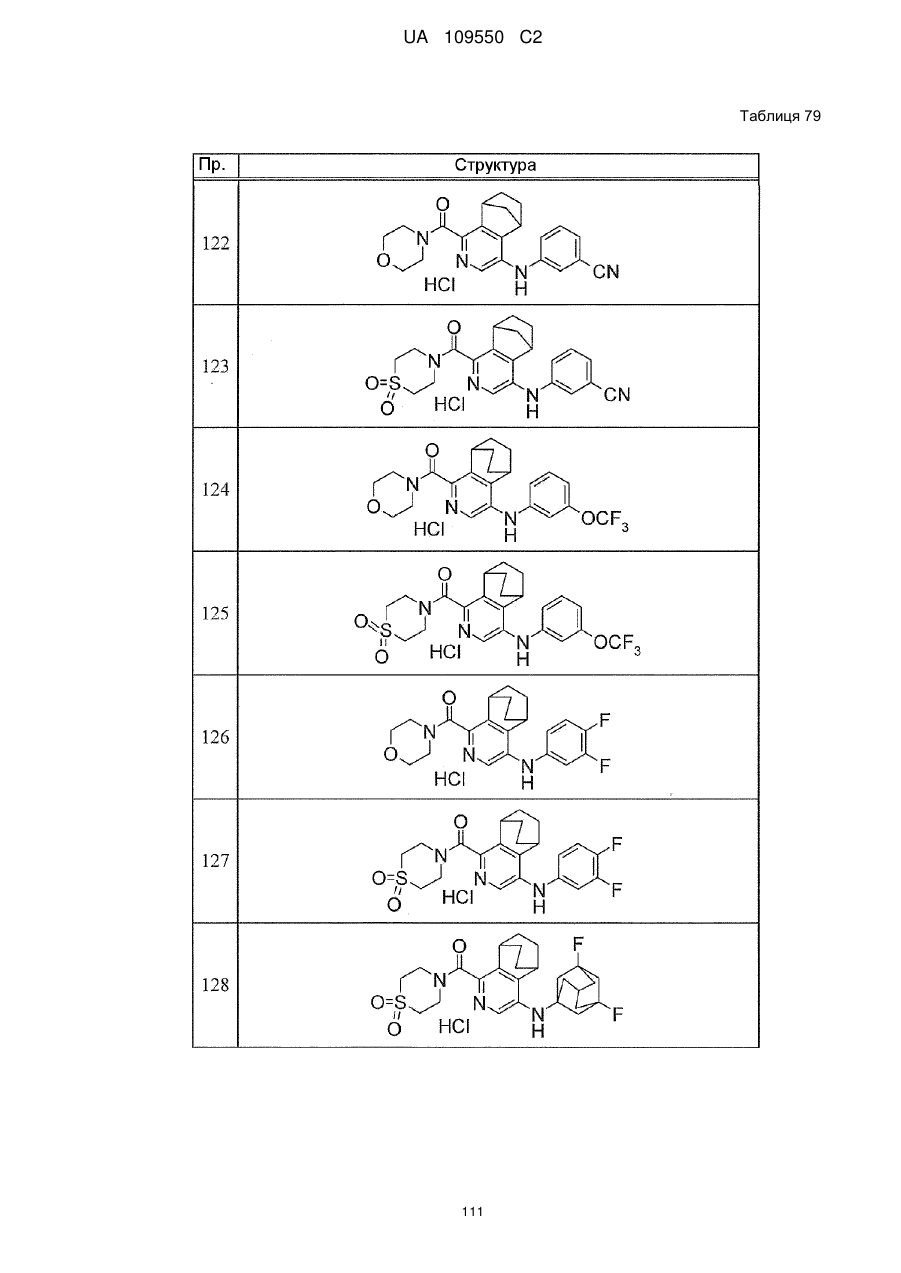
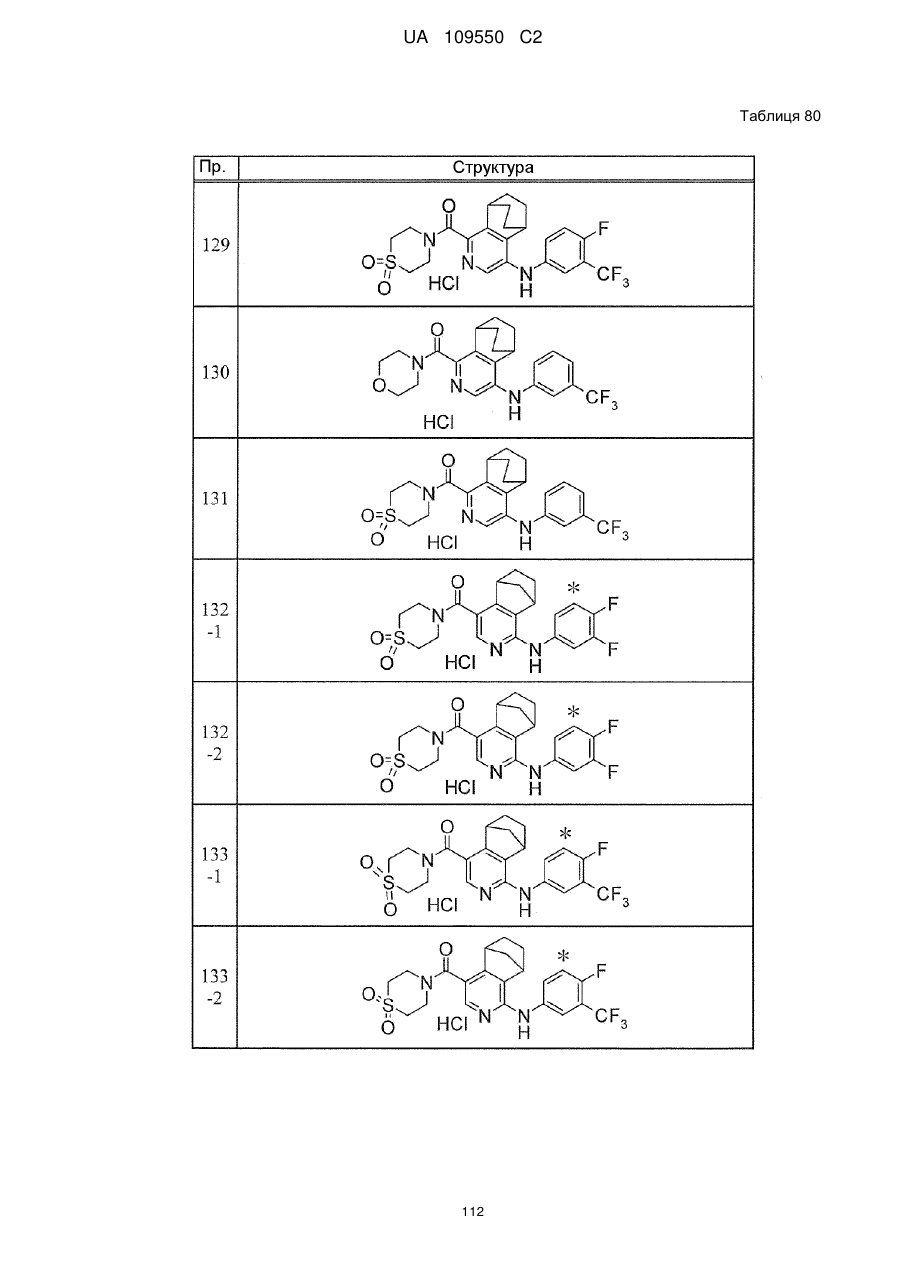
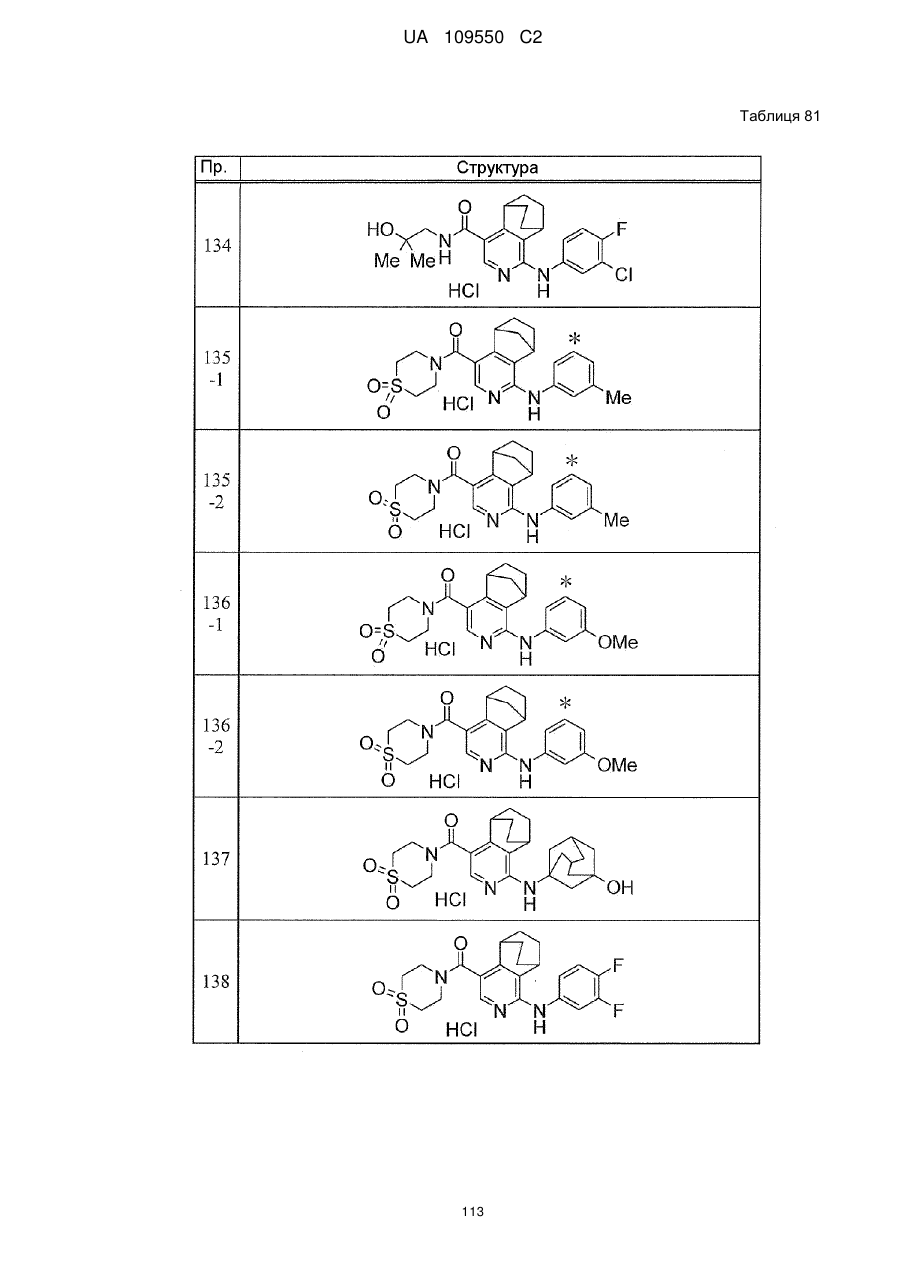
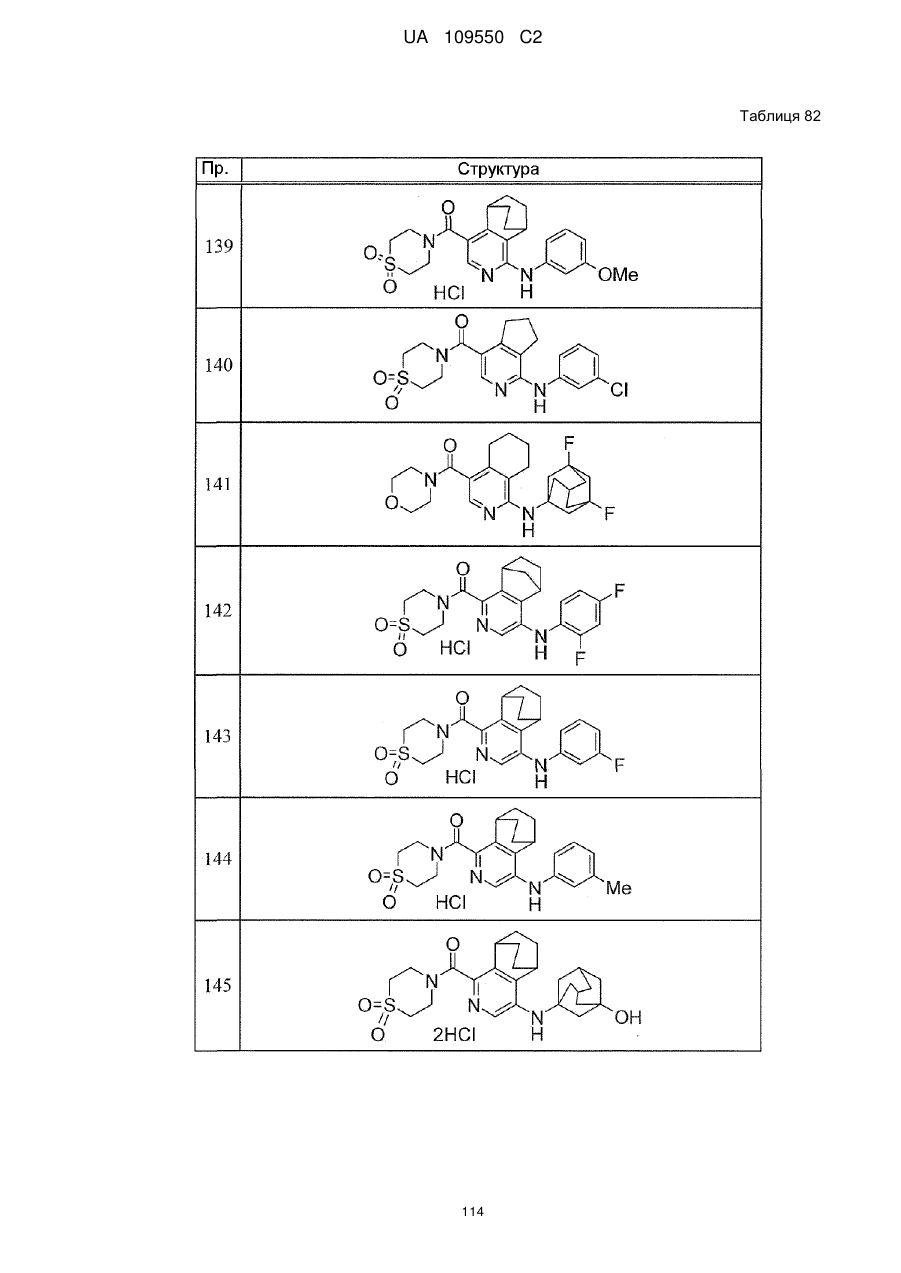
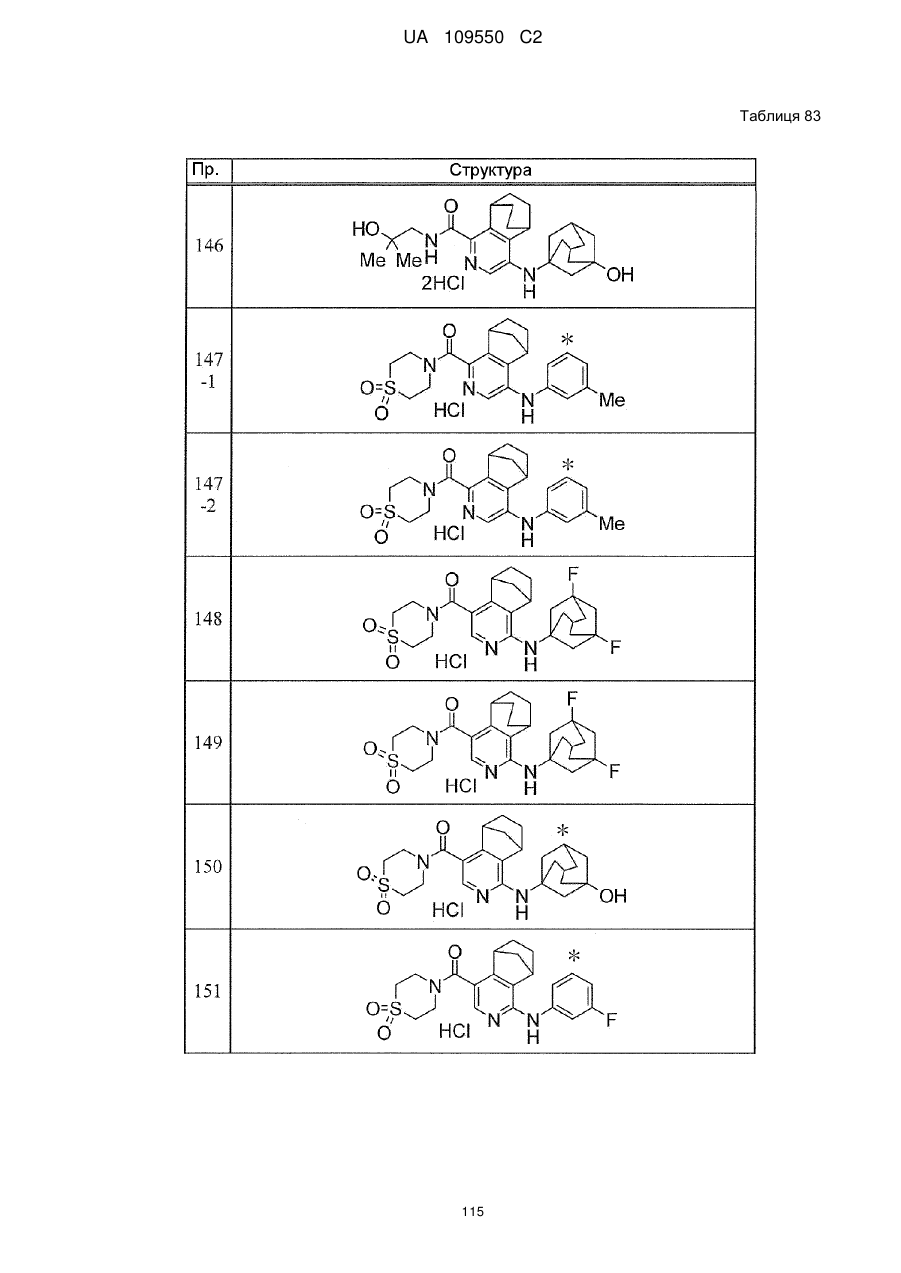
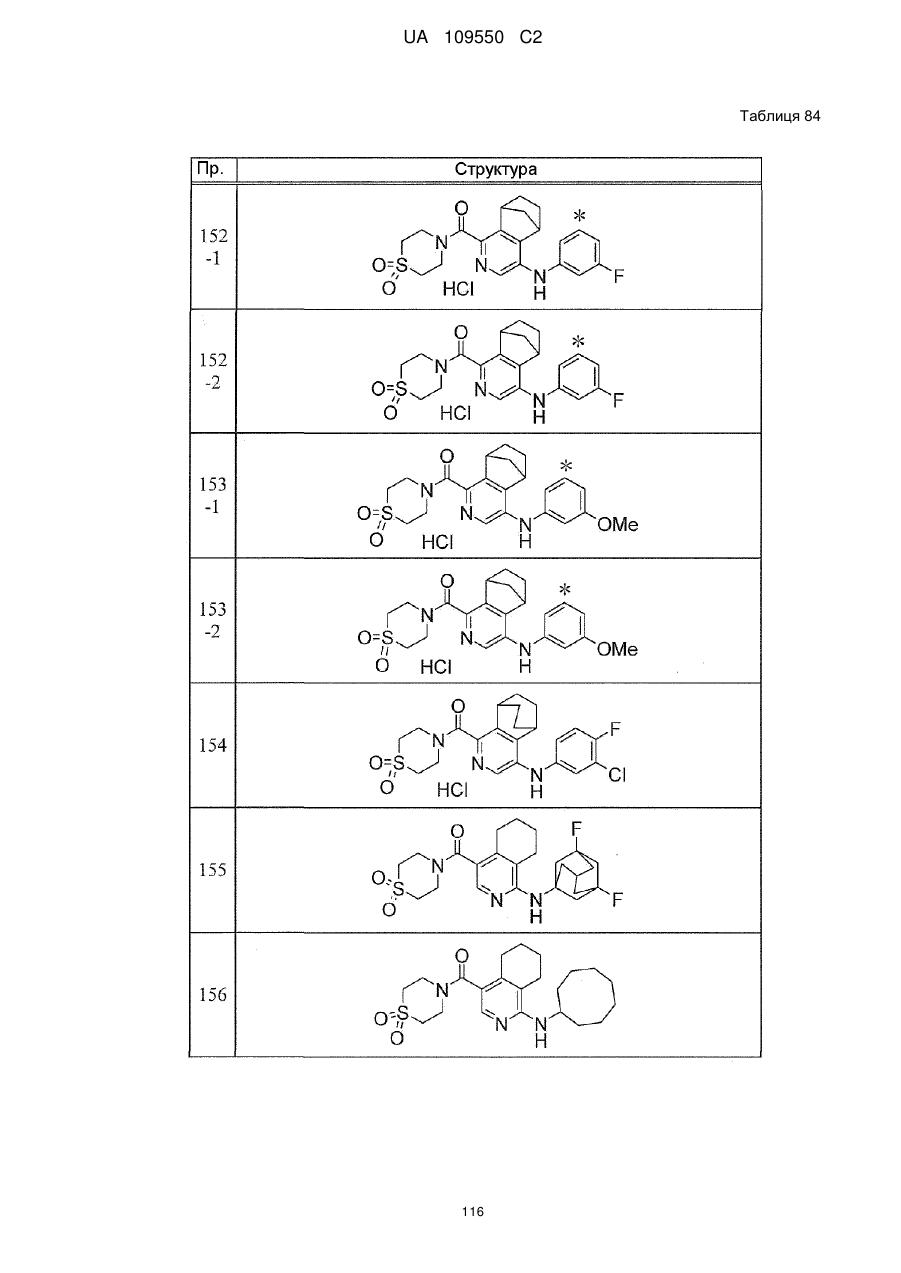
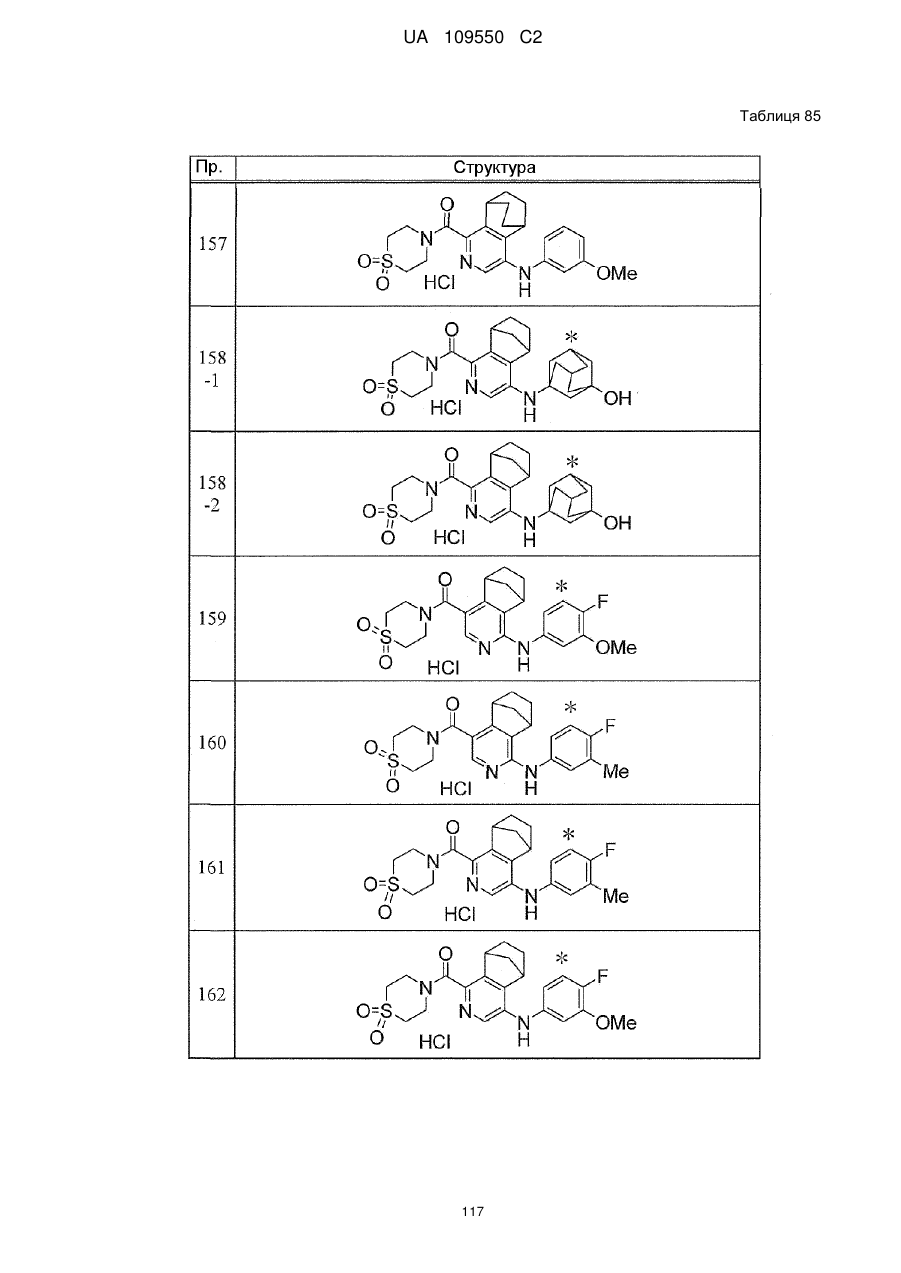
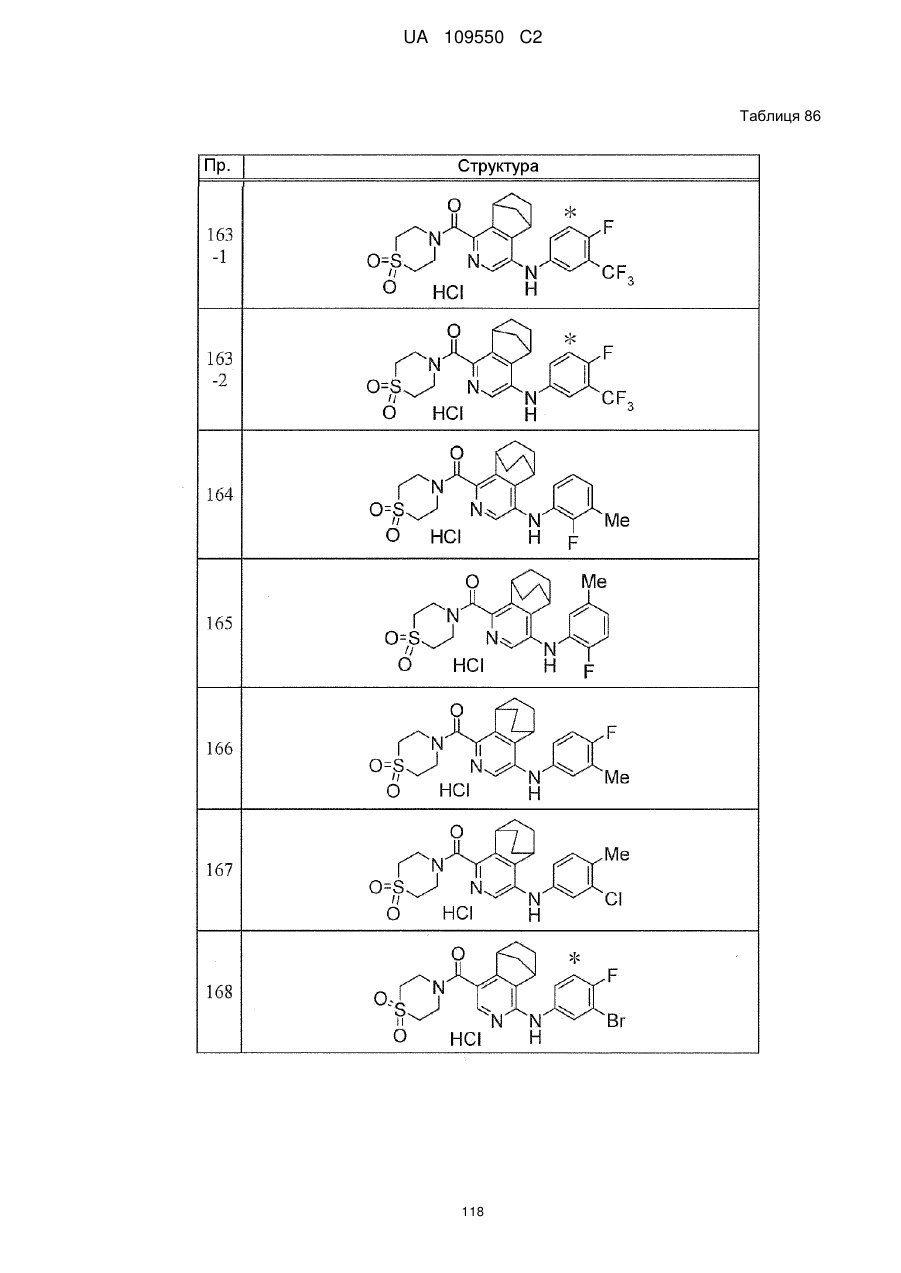
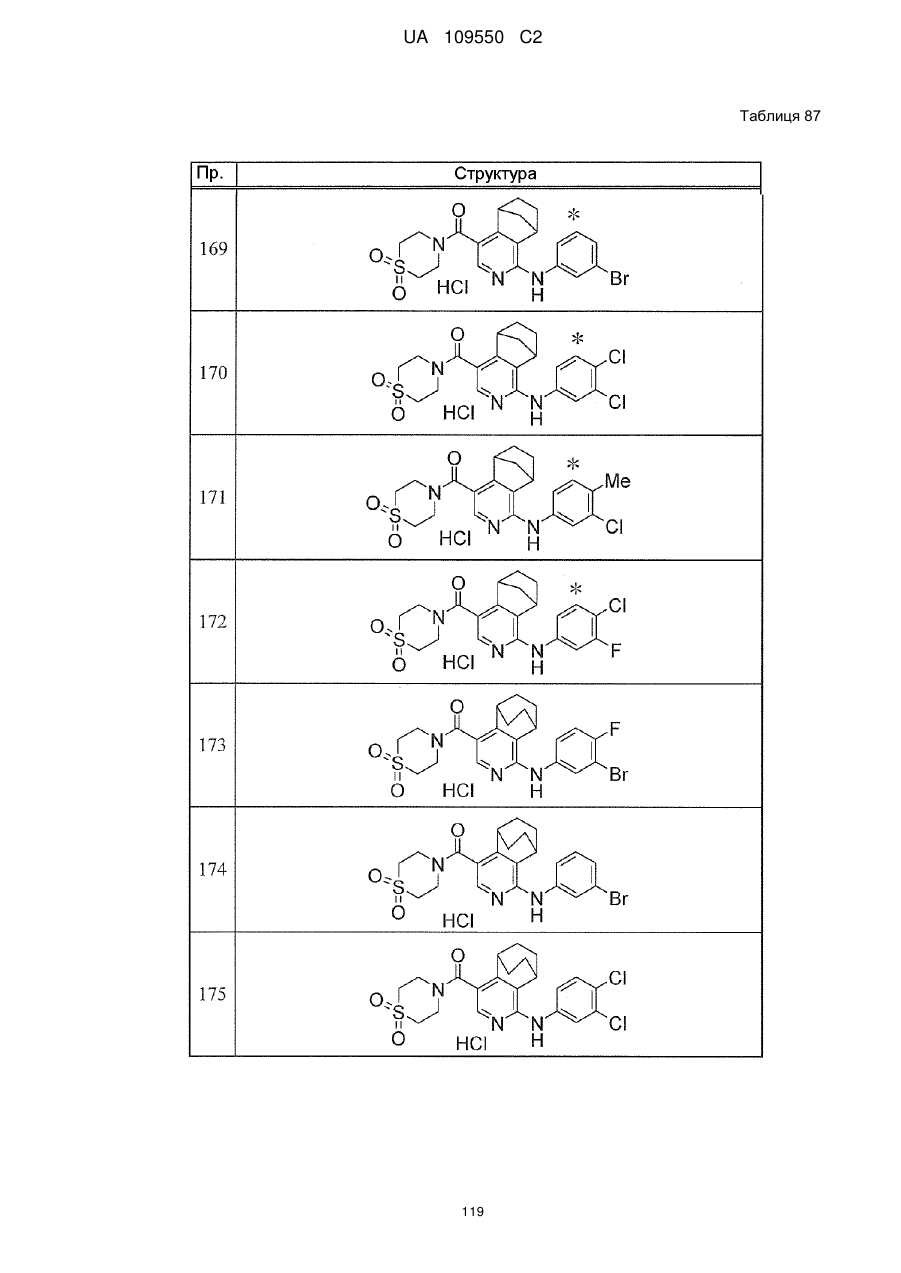
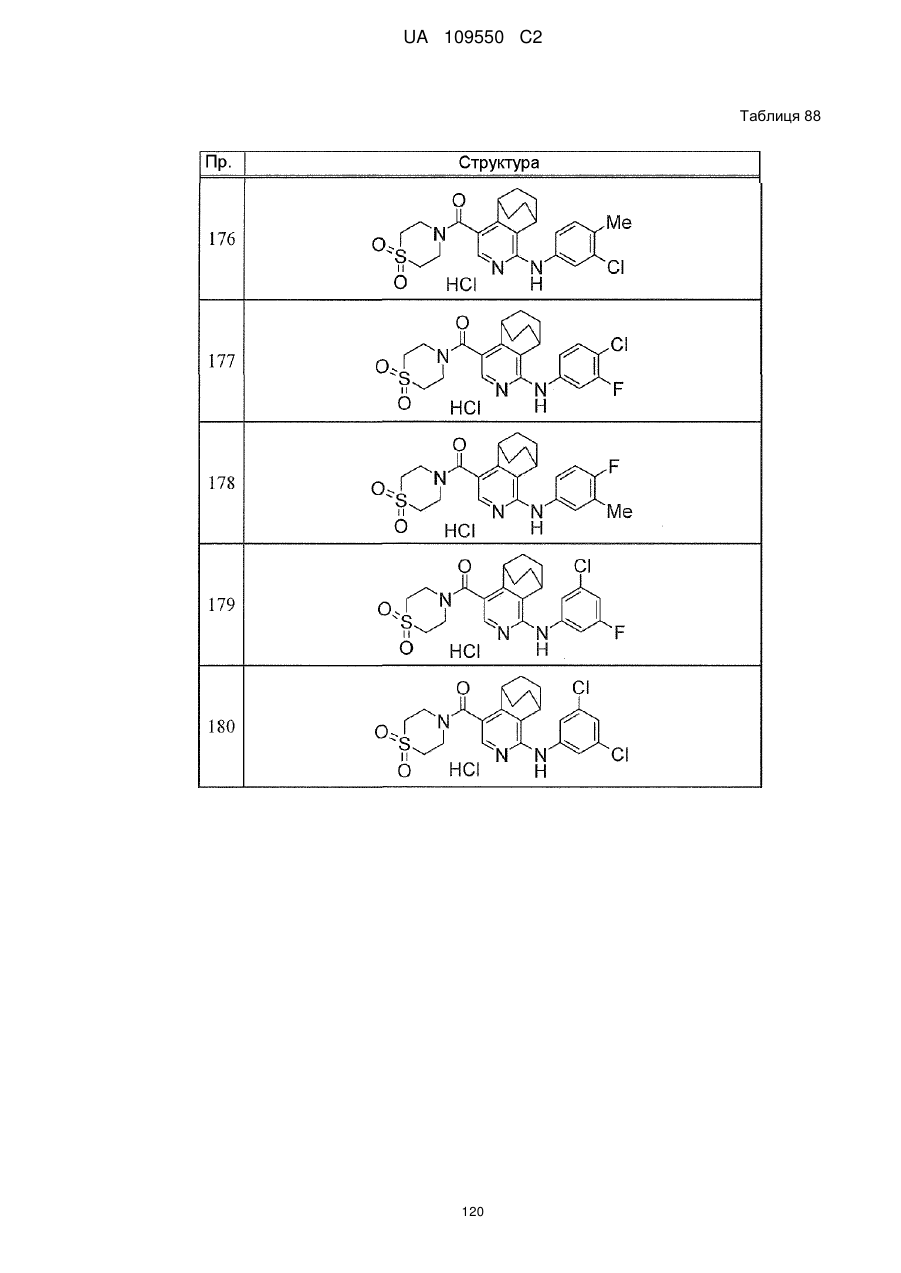
6. Сполука за п. 1 або її сіль, вибрана з групи:
{1-[(3-хлорфеніл)аміно]-5,6,7,8-тетрагідроізохінолін-4-іл}(1,1-діоксидотіоморфолін-4-іл)метанон,
{4-[(3-хлорфеніл)аміно]-5,6,7,8-тетрагідроізохінолін-1-іл}(1,1-діоксидотіоморфолін-4-іл)метанон,
морфолін-4-іл-(1-{[(3-трифторметокси)феніл]аміно}-5,6,7,8-тетрагідроізохінолін-4-іл)метанон,
(1,1-діоксидотіоморфолін-4-іл){4-[(3-трифторметил)фенокси]-5,6,7,8-тетрагідроізохінолін-1-іл}метанон,
(1,1-діоксидотіоморфолін-4-іл)(4-{[(3-трифторметил)феніл]аміно}-5,6,7,8-тетрагідроізохінолін-1-іл)метанон,
(1,1-діоксидотіоморфолін-4-іл){1-[(3-трифторметил)фенокси]-5,6,7,8-тетрагідроізохінолін-1-іл}метанон,
{4-[(3-хлорфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-1-іл}(1,1-діоксидотіоморфолін-4-іл)метанон,
{1-[(3-хлорфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-4-іл}(1,1-діоксидотіоморфолін-4-іл)метанон,
(1,1-діоксидотіоморфолін-4-іл)(1-{[(3-трифторметил)феніл]аміно}-5,6,7,8-тетрагідро-5,8-етаноізохінолін-4-іл)метанон,
(1,1-діоксидотіоморфолін-4-іл)(4-{[(3-трифторметокси)феніл]аміно}-5,6,7,8-тетрагідро-5,8-етаноізохінолін-1-іл)метанон,
{4-[(3,4-дифторфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-1-іл}(1,1-діоксидотіоморфолін-4-іл)метанон,
{1-[(3-хлор-4-фторфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-4-іл}(1,1-діоксидотіоморфолін-4-іл)метанон,
(1,1-діоксидотіоморфолін-4-іл)(1-{[3-(трифторметокси)феніл]аміно}-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-іл)метанон,
(1,1-діоксидотіоморфолін-4-іл)(1-{[4-фтор-3-(трифторметил)феніл]аміно}-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-іл)метанон,
{1-[(3-хлорфеніл)аміно]-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-іл}(1,1-діоксидотіоморфолін-4-іл)метанон,
{1-[(3,4-дифторфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-4-іл}(1,1-діоксидотіоморфолін-4-іл)метанон,
(1,1-діоксидотіоморфолін-4-іл){4-[(2-фтор-3-метилфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-1-іл}метанон,
(1,1-діоксидотіоморфолін-4-іл){4-[(2-фтор-5-метилфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-1-іл}метанон,
{4-[(3-хлор-4-метилфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-1-іл}(1,1-діоксидотіоморфолін-4-іл)метанон,
{1-[(3-хлор-5-фторфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-4-іл}(1,1-діоксидотіоморфолін-4-іл)метанон
і їх солі.
7. Сполука або її сіль за п. 6, де сполукою є {1-[(3-хлор-4-фторфеніл)аміно]-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-іл}(1,1-діоксидотіоморфолін-4-іл)метанон.
8. Сполука або її сіль за п. 6, де сполукою є (1,1-діоксидотіоморфолін-4-іл)(1-{[3-(трифторметокси)феніл]аміно}-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-іл)метанон.
9. Сполука або її сіль за п. 6, де сполукою є (1,1-діоксидотіоморфолін-4-іл)(1-{[4-фтор-3-(трифторметил)феніл]аміно}-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-іл)метанон.
10. Сполука або її сіль за п. 6, де сполукою є {1-[(3,4-дифторфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-4-іл}(1,1-діоксидотіоморфолін-4-іл)метанон.
11. Сполука або її сіль за п. 6, де сполукою є (-)-{1-[(3-хлор-4-фторфеніл)аміно]-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-іл}(1,1-діоксидотіоморфолін-4-іл)метанону моногідрохлорид.
12. Сполука або її сіль за п. 6, де сполукою є (-)-(1,1-діоксидотіоморфолін-4-іл)(1-{[3-(трифторметокси)феніл]аміно}-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-іл)метанону моногідрохлорид.
13. Сполука або її сіль за п. 6, де сполукою є (-)-(1,1-діоксидотіоморфолін-4-іл)(1-{[4-фтор-3-(трифторметил)феніл]аміно}-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-іл)метанону моногідрохлорид.
14. Сполука або її сіль за п. 6, де сполукою є {1-[(3,4-дифторфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохонолін-4-іл}(1,1-діоксидотіоморфолін-4-іл)метанону моногідрохлорид.
15. Фармацевтична композиція, що містить:
сполуку за п. 6 або її сіль і фармацевтично прийнятний ексципієнт.
16. Фармацевтична композиція для профілактики або лікування захворювань, пов'язаних з канабіноїдним рецептором 2 типу, що містить сполуку за п. 1 або її сіль.
17. Фармацевтична композиція за п. 16, де захворюванням, пов'язаним з канабіноїдним рецептором 2 типу, є запальне захворювання.
18. Фармацевтична композиція за п. 16, де захворюванням, пов'язаним з канабіноїдним рецептором 2 типу, є біль.
19. Застосування сполуки за п. 6 або її солі для виробництва фармацевтичної композиції для профілактики або лікування захворювань, пов'язаних з канабіноїдним рецептором 2 типу.
20. Застосування сполуки за п. 6 або її солі для профілактики або лікування захворювань, пов'язаних з канабіноїдним рецептором 2 типу.
21. Спосіб профілактики або лікування захворювань, пов'язаних з канабіноїдним рецептором 2 типу, який характеризується тим, що пацієнту вводять ефективну кількість сполуки за п. 6 або її фармацевтично прийнятної солі.
Текст
Реферат: Проблема. Отримати сполуку, що застосовується як новий агент, який чудово придатний для профілактики і/або лікування захворювань, пов'язаних з канабіноїдним рецептором 2 типу, на основі агоністичної дії до канабіноїдного рецептора 2 типу. Рішення. Проведене дослідження сполук, що мають агоністичну дію на канабіноїдний рецептор 2 типу, і підтверджено, що сполука піридину з конденсованим кільцем відповідно до даного винаходу має чудову агоністичну дію на канабіноїдний рецептор 2 типу. Така сполука піридину з конденсованим кільцем має агоністичну дію на канабіноїдний рецептор 2 типу і може застосовуватися як профілактичний і/або терапевтичний агент для лікування захворювань, пов'язаних з канабіноїдним рецептором 2 типу, таких як запальні захворювання і біль. UA 109550 C2 5 10 15 20 25 30 35 40 Галузь техніки Даний винахід стосується фармацевтичної композиції, зокрема, конденсованої циклічної сполуки піридину, яку застосовують як активний інгредієнт фармацевтичної композиції для профілактики і/або лікування захворювань, пов'язаних з канабіноїдним рецептором 2 типу. Рівень техніки Канабіноїд є загальним терміном для компонентів марихуани, що містяться в коноплі. На даний момент відомо близько 60 видів або більше компонентів, які в основному включають тетрагідроканабінол, канабінол, канабідіол і подібні. Марихуану застосовують тисячі років як лікарський засіб або подібне, вона викликає психологічні і нервові реакції, і викликає сенсорну дезорієнтацію, ейфорію, знеболюючу дію, галюцинації і подібне. Канабіноїди володіють різними типами фармакологічної дії, і було виявлено, що вони володіють імунодепресивною дією, протизапальною дією, знеболюючою дією і подібними в доповнення до дії на центральну нервову систему. Канабіноїд є сьомим рецептором трансмембранного G-зв'язаного білка, і в цей час ідентифіковані і скриновані два типи, включаючи канабіноїдні рецептори типу 1 (КБ1) і типу 2 (КБ2) (Nature, 1990, 346, 561-564;Nature, 1993, 365, 61-65). Людський КБ1 складається з 472 амінокислот і у високій мірі експресується в блідій кулі, смугастому тілі, чорній речовині, гіпокампі, мозочковому молекулярному шарі, корі головного мозку і подібним, в мозку. КБ1 також експресується в яєчках, сім'яному протоку, матці, тонкому кишечнику, кровоносних судинах і подібних, в доповнення до мозку. КБ2 складається з 360 амінокислот і демонструє 44 % гомологію до КБ1. КБ2 значною мірою експресується в селезінці, піднебінних мигдалинах і лімфатичних вузлах, а також в лейкоцитарних клітинах, таких як макрофаги, моноцити, Влімфоцити, ЕК-клітинах, еозинофілах і подібних. Недавно було описано, що КБ2 також експресується в мозку (Science, 2005, 310, 329-332). Було описано, що агоніст КБ2 володіє центральною знеболюючою дією (European Journal of Neuroscience, 2006, 23, 1530-1538) і периферійною знеболюючою дією (Proceedings of the National Academy of Sciences, 2005, 102, 3093-3098). У доповнення було виявлено, що, оскільки КБ2 значною мірою експресується в гематоцитах і імуноцитах, агоніст КБ 2 володіє імунодепресивною дією і протизапальною дією (British Journal of Pharmacology, 2003, 139, 775786). Було описано, що агоніст КБ2 володіє протисвербіжною дією при захворюваннях шкіри (Science, 2007, 316, 1494-1497) і може застосовуватися при атопічному дерматиті і подібних. Більше того, завдяки протизапальній дії і імунодепресивній дії агоніст КБ2 може бути ефективним при атеросклерозі (Nature, 2005, 434, 782-786), рефлюкс-езофагіті (European Journal of Pharmacology, 2007, 573, 206-213), захворюванні печінки (British Journal of Pharmacology, 2008, 153, 286-289) і хронічних захворюваннях печінки (Expert Opinion of Therapeutic Targets, 2007, 11, 403-409). Більше того, було описано, що КБ2 також експресується в остеобластах і остеокластах, і що агоніст КБ2 володіє дією, що підвищує активність остеобластів і інгібує активність остеокластів, тим самим надаючи дію інгібування остеоклазії (Proceedings of the National Academy of Sciences, 2006, 103, 696-701). Як сполуки, що надають КБ2 агоністичну дію, були описані сполуки, представлені наступними Формулою (А) (патентний документ 1), Формулою (В) (патентний документ 2), Формулою (С) (патентні документи 3 і 4), Формулою (D) (непатентний документ 1) і Формулою (Е) (патентний документ 5), відповідно. Однак жоден з цих документів не включає опис або участь сполуки формули (I), описаної нижче, або її солі відповідно до даного винаходу, 45 1 UA 109550 C2 12 13 11 (в формулах (А) і (В) Х1 зокрема є NR ; Х2 і Х3 є групою -CR =CR - в поєднанні або Х3 є 13 11 NR ; Х1 і Х2 є -CR =CR - в поєднанні, більш детально див. у відповідних джерелах, див. відповідне джерело для формули (С) і див. відповідне джерело для формули (D), в формулі (Е) 6 R є метилом, хлором або CHxFn, більш детально див. у відповідному джерелі). Посилання Патентний документ Патентний документ 1: публікація міжнародної заявки WO 2005/121140 Патентний документ 2: публікація міжнародної заявки WO 2007/017264 Патентний документ 3: публікація міжнародної заявки WO 2007/017237 Патентний документ 4: публікація міжнародної заявки WO 2008/116816 Патентний документ 5: публікація міжнародної заявки WO 2004/018433 Непатентний документ Непатентний документ 1: Journal of Medicinal Chemistry, 2009, Vol. 52, No. 19, pp 5785-5788 Опис винаходу Проблеми, що вирішуються винаходом У даному винаході представлена фармацевтична композиція, наприклад, фармацевтична композиція, що володіє КБ2 агоністичною дією, зокрема, фармацевтична композиція для профілактики і/або лікування пов'язаних з КБ2 захворювань, і сполуки, що застосовується як активний інгредієнт фармацевтичної композиції. Засоби розв'язання проблем Автори даного винаходу провели ретельне дослідження агоніста КБ2. У результаті вони виявили, що конденсована циклічна сполука піридину, показана нижче, володіє чудовою КБ2 агоністичною дією і може бути агентом для профілактики і/або лікування пов'язаних з КБ2 захворювань, тим самим завершуючи даний винахід. Тобто, даний винахід стосується сполуки формули (I) або її солі, і фармацевтичної композиції, що містить сполуку або її сіль і екципієнт, 12 5 10 15 20 25 30 35 (в формулі Х і Y є СН, С-нижчим алкілом або N, де або Х, або Y є N, W є -NH-, -N(нижчим алкілом)-, -О-, -S-, -S(О)- або -S(О)2-, 1 R є циклоалкілом, який може бути заміщений, арилом, який може бути заміщений, ароматичним гетероциклом, який може бути заміщений, або неароматичним гетероциклом, який може бути заміщений, 2 3 4 R є -Z-NR R або Z-циклічним аміно, який може бути заміщений, А частина є групою, представленою формулою (II), (III) або (IV), 40 3 45 R є Н або нижчим алкілом, 4 R є нижчим алкілом, заміщеним однією або більше групами, вибраними з групи, що включає -ОН-, -О-нижчий алкіл, галоген, циклоалкіл, ціано, -S-нижчий алкіл, -S(О)-нижчий алкіл, -S(О)2-нижчий алкіл і -О-галогено-нижчий алкіл, 5 R є однаковими або різними і є нижчим алкілом або галогеном, Z є однаковими або різними і є -С(О)-, -СН2- або -S(О)2-, m є однаковими або різними і дорівнюють цілому числу від 0 до 10, і n є однаковими або різними і дорівнюють цілому числу від 0 до 2). 2 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 55 60 Крім того, якщо не вказано інакше, якщо символи в хімічній формулі в даному описі також застосовують в іншій хімічній формулі, однакові символи мають однакове значення. Більше того, даний винахід стосується фармацевтичної композиції для профілактики і/або лікування пов'язаних з КБ2 захворювань, яка містить сполуку формули (I) або її сіль. Крім того, фармацевтична композиція включає агент для профілактики і/або лікування пов'язаних з КБ2 захворювань, який містить сполуку формули (I) або її сіль. Даний винахід також стосується застосування сполуки формули (I) або її солі для виробництва фармацевтичної композиції для профілактики і/або лікування пов'язаних з КБ2 захворювань, застосування сполуки формули (I) або її солі для профілактики і/або лікування пов'язаних з КБ2 захворювань, сполуки формули (I) або її солі для профілактики і/або лікування пов'язаних з КБ2 захворювань, і способу профілактики і/або лікування пов'язаних з КБ2 захворювань, який включає введення ефективної кількості сполуки формули (I) або її солі пацієнту. Крім того, "пацієнт" стосується людини або іншого ссавця, якому потрібна профілактика або лікування, і в іншому варіанті, пацієнт стосується людини, якій потрібна профілактика або лікування. Ефект даного винаходу Сполука формули (I) або її сіль володіє КБ2 агоністичною дією, і може застосовуватися як агент для профілактики і/або лікування пов'язаних з КБ2 захворювань. Приклади пов'язаних з КБ2 захворювань включають запальні захворювання (наприклад, ревматоїдний артрит і деформуючий артрит), біль (наприклад, гострий біль, хронічний біль, ноцицептивний біль, біль при запаленні, біль при ревматоїдній артропатії і біль при деформуючому артрозі), рак і пухлини (наприклад, рак імунної системи, рак легенів, рак ободової і прямої кишки і лейкемія), респіраторні захворювання (наприклад, респіраторний дистрес-синдром, легеневий туберкульоз, астма і хронічне обструктивне захворювання легенів), захворювання печінки, захворювання мозку, захворювання очей (наприклад, очну гіпертонію, катаракту, глаукому і захворювання сітківки), захворювання шкіри (наприклад, прурітичний дерматит і мікоз поверхні шкіри), хвороби кровообігу (наприклад, хвороба Руньон-Гебердена, інфаркт міокарда, артеріосклероз, гіпертонію, рестеноз після коронарного стентування і тромбоз), алергічні захворювання (наприклад, анафілактичний шок, алергічну астму, атопічну астму і лікарські алергії), хвороби травлення (наприклад, запор, діарею, блювання, пептичну виразку, синдром подразненого кишечника і виразковий коліт), імунологічні захворювання (наприклад, імунологічна некомпетентність, псоріаз, ревматоїдний артрит, остеопороз, септичний шок і системний червоний вовчак), нейрогенні захворювання (наприклад, нейродегенеративне захворювання, нудоту, невропатію, недоумство, хворобу Паркінсона, шизофренічне захворювання, синдром нав'язливих станів, посттравматичний стрес, розлад пам'яті, втрату апетиту, анорексію, циркадну аритмію, апное уві сні, залежність від хімічних сполук, дискінезію, конвульсії і парестезію), остеогенез, відновлення кісток, ожиріння і подібні. Варіанти здійснення даного винаходу Далі представлений докладний опис даного винаходу. "Нижчий алкіл" стосується лінійного або розгалуженого алкілу, що містить від 1 до 6 атомів вуглецю (далі позначений як С1-6), наприклад, метилу, етилу, н-пропілу, ізопропілу, н-бутилу, ізобутилу, втор-бутилу, трет-бутилу, н-пентилу, н-гексилу і подібним. В іншому варіанті, нижчим алкілом є С1-4 алкіл, в ще одному варіанті, нижчим алкілом є метил, етил або н-пропіл. "Нижчий алкілен" стосується лінійного або розгалуженого С 1-6 алкілену, наприклад, метилену, етилену, триметилену, тетраметилену, пентаметилену, гексаметилену, пропілену, бутилену, метилметилену, етилетилену, 1,1-диметилетилену, 2,2-диметилетилену, 1,2диметилетилену, 1,1,2,2-тетраметилетилену, 1-метилбутилену, і подібним. В іншому варіанті, нижчим алкіленом є С1-4 алкілен, в ще одному варіанті, нижчим алкіленом є метилен, етилен, триметилен, тетраметилен, пентаметилен або 1,2-диметилетилен. "Галоген" стосується F, Cl, Br і I. В іншому варіанті, галогеном є F або Cl, і в ще одному варіанті, галогеном є F, і в іншому варіанті, галогеном є Cl. "Галогено-нижчий алкіл" стосується нижчого алкілу, заміщеному одним або більше атомами галогену. В іншому варіанті, галогено-нижчим алкілом є нижчий алкіл, заміщений від 1 до 5 атомами галогену, і в іншому варіанті, галогено-нижчим алкілом є трифторметил. "Циклоалкіл" стосується С3-10 насиченої вуглеводневої циклічної групи. Циклоалкіл може мати місток. Альтернативно, частина зв'язків в кільці може бути ненасичена або конденсована з бензольним кільцем. Приклади циклоалкілу включають циклопропіл, циклобутил, циклопентил, циклогексил, циклогексеніл, циклогептил, циклооктил, біцикло[2.2.1]гептил, біцикло[2.2.2]октил, біцикло[3.2.1]октил, адамантил, інданіл і подібні. В іншому варіанті циклоалкілом є циклопентил, циклогексил, циклогептил, циклооктил, біцикло[2.2.1]гептил, біцикло[2.2.2]октил, 3 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 55 60 біцикло[3.2.1]октил або адамантил, і в ще одному варіанті, циклоалкілом є С 3-8 циклоалкіл. В іншому варіанті, циклоалкілом є С5-8 циклоалкіл, в іншому варіанті, циклоалкілом є циклогексил, і в іншому варіанті, циклоалкілом є адамантил. "Арил" стосується моноциклічної - трициклічної С6-14 ароматичної циклічної групи, наприклад, фенілу, нафтилу і подібним. В іншому варіанті, арилом є моноциклічна - біциклічна С6-10 ароматична циклічна група, і в іншому варіанті, арилом є моноциклічна С 6-8 ароматична вуглеводнева циклічна група. В іншому варіанті арилом є феніл, і в ще одному варіанті, арилом є нафтил. "Ароматичний гетероцикл" стосується 5-6-членного ароматичного гетероциклу, який містить один або більше гетероатомів, вибрану з О, N і S, як атоми кільця. Ароматичний гетероцикл може бути конденсований з бензольним кільцем або тіофеновим кільцем. Приклади ароматичного гетероциклу включають піридил, піроліл, піразиніл, піримідиніл, піридазиніл, імідазоліл, триазоліл, триазиніл, тетразоліл, тіазоліл, піразоліл, ізотіазоліл, оксазоліл, ізоксазоліл, тіадіазоліл, оксадіазоліл, тієніл, фурил, індоліл, ізоіндоліл, бензімідазоліл, індазоліл, хіноліл, ізохіноліл, хіназолініл, хіноксалініл, фталазиніл, бензотіазоліл, бензізотіазоліл, бензотіадіазоліл, бензоксазоліл, бензізоксазоліл, бензофураніл, бензотієніл, карбазоліл, дибензо[b, d]фураніл, дибензо[b, d]тієніл, тієнопіридил, тієнопіримідиніл, тієнопіразил, і подібні. В іншому варіанті, ароматичним гетероциклом є 5-6-членний моноциклічний ароматичний гетероцикл, і в ще одному варіанті, ароматичним гетероциклом є 6членний моноциклічний ароматичний гетероцикл. В іншому варіанті, ароматичним гетероциклом є піридил, піроліл, піразиніл, піримідиніл, піридазиніл, імідазоліл або триазоліл, і в ще одному варіанті, ароматичним гетероциклом є піридил. "Неароматичний гетероцикл" стосується 4-7-членного неароматичного гетероциклу, який містить один або більше гетероатомів, вибраних з О, N і S, як атоми кільця. Крім того, атом сірки як атом кільця може бути окиснений. Приклади неароматичного гетероцикла включають азетидиніл, піролідиніл, піперидиніл, піперазиніл, азепаніл, діазепаніл, морфолініл, тіоморфолініл, 1,1-діоксидотіоморфолініл, тетрагідропіридиніл, оксетаніл, тетрагідрофураніл, тетрагідротієніл, тетрагідропіраніл, діоксоланіл, діоксаніл або тетрагідротіопіраніл, і подібні. В іншому варіанті, неароматичним гетероциклом є 5-6-членний моноциклічний неароматичний гетероцикл, в ще одному варіанті, неароматичним гетероциклом є 6-членний моноциклічний неароматичний гетероцикл. В іншому варіанті, неароматичним гетероциклом є піперидиніл, морфолініл, тіоморфолініл, 1,1-діоксидотіомофролініл, тетрагідрофураніл, тетрагідропіраніл або тетрагідротіопіраніл, і в ще одному варіанті, неароматичним гетероциклом є піперидиніл, морфолініл, 1,1-діоксидотіоморфолініл або тетрагідропіраніл. "Циклічний аміно" стосується групи, що має атом азоту, що входить у вказані вище "неароматичні гетероцикли", і є неароматичним гетероциклом, що має зв'язок на атомі азоту. Приклади циклічного аміно включають азетидин-1-іл, піразолідин-1-іл, імідазолідин-1-іл, 1,4діазепан-1-іл, 3-азабіцикло[3.1.1]гепто-3-іл, 2-азабіцикло[2.2.2]окто-2-іл, піролідин-1-іл, піперидин-1-іл, азепан-1-іл, піперазин-1-іл, морфолін-4-іл, тіоморфолін-4-іл, 1оксидотіоморфолін-4-іл, 1,1-діоксидотіоморфолін-4-іл, 1,3-тіадіан-3-іл, 1-оксидо-1,3-тіадіан-3-іл, 1,1-діоксидо-1,3-тіадіан-3-іл, 1,4-оксаазепан-4-іл, і подібні. В іншому варіанті, циклічним аміно є піролідин-1-іл, піперидин-1-іл, азепан-1-іл, піперазин-1-іл, морофлін-4-іл, тіоморфолін-4-іл, 1,1діоксидотіоморфолін-4-іл або 1,4-оксаазепан-4-іл, в ще одному варіанті, циклічним аміно є піролідин-1-іл, піперидин-1-іл, морфолін-4-іл, 1,1-діоксидотіоморфолін-4-іл або 1,4-оксаазепан4-іл. У ще одному варіанті, циклічним аміно є 6-членний моноциклічний циклічний аміно. В іншому варіанті, циклічним аміно є піперидин-1-іл, морфолін-4-іл або 1,1-діоксидотіоморфолін-4іл. У даному описі фраза "може бути заміщений" означає, що група може бути не заміщена або мати від одного до п'яти замісників. В іншому варіанті, фраза означає, що група може бути не заміщена або мати від одного до трьох замісників, і в ще одному варіанті, фраза означає, що група може бути не заміщена або мати один замісник. В іншому варіанті, фраза означає, що група може бути не заміщена. Крім того, якщо група має множину замісників, ці замісники можуть бути однаковими або різними. У формулі (I) як замісники, прийнятні в "циклоалкілі, який може бути заміщений", "арилі, який може бути заміщений", ароматичному гетероциклі, який може бути заміщений" і 1 "неароматичному гетероциклі, який може бути заміщений", представлених R , і в "циклічному аміно, який може бути заміщений" в "Z-циклічному аміно, який може бути заміщений", 2 представленому R , звичайно застосовують замісники, що застосовуються. Їх приклади включають замісники з представленої нижче групи D. Група D 4 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 55 60 (1) галоген, (2) -ОН, -О-нижчий алкіл, -О-галогено-нижчий алкіл і -SH, (3) ціано і нітро, (4) циклоалкіл, -О-циклоалкіл і -С(О)-циклоалкіл, які можуть бути відповідно заміщені однією або більше групами, що включають нижчий алкіл, галоген, -ОН, -О-нижчий алкіл, -О-галогенонижчий алкіл і галогено-нижчий алкіл, (5) арил, -О-арил і -С(О)-арил, які можуть бути заміщені однією або більше групами, що включають нижчий алкіл, галоген, -ОН, -О-нижчий алкіл, -О-галогено-нижчий алкіл і галогенонижчий алкіл, (6) ароматичний гетероцикл, -О-ароматичний гетероцикл і -С(О)-ароматичний гетероцикл, які можуть бути заміщені однією або більше групами, що включають нижчий алкіл, галоген, -ОН, -О-нижчий алкіл, -О-галогено-нижчий алкіл і галогено-нижчий алкіл, (7) неароматичний гетероцикл, -О-неароматичний гетероцикл і -С(О)-неароматичний гетероцикл, які можуть бути заміщені однією або більше групами, що включають нижчий алкіл, галоген, -ОН, -О-нижчий алкіл, -О-галогено-нижчий алкіл і галогено-нижчий алкіл, (8) -С(О)-нижчий алкіл, -С(О)О-нижчий алкіл, -NH-C(О)-нижчий алкіл, -NH-нижчий алкіл, N(нижчий алкіл)2, -C(О)-NH-нижчий алкіл і -C(О)-N(нижчий алкіл)2, де групи нижчого алкілу можуть бути відповідно заміщені однією або більше групами, що включають галоген, -ОН, -Онижчий алкіл, -О-галогено-нижчий алкіл, (9) -NH2- і -C(О)-NH2, (10) -S-нижчий алкіл, -S(О)-нижчий алкіл і -S(О)2-нижчий алкіл, де групи нижчого алкілу можуть бути відповідно заміщені однією або більше групами, що включають галоген, -ОН, -Онижчий алкіл, -О-галогено-нижчий алкіл, і (11) нижчий алкіл і -О-нижчий алкіл, які можуть бути відповідно заміщені однією або більше групами, що включають замісники, описані у (1) - (10) вище. В одному варіанті група D включає (1) галоген, (2) -ОН, -О-нижчий алкіл і -О-галогено-нижчий алкіл, (3) ціано і нітро, (4) циклоалкіл і -О-циклоалкіл, які можуть бути відповідно заміщені однією або більше групами, що включають нижчий алкіл, галоген, -ОН, -О-нижчий алкіл, -О-галогено-нижчий алкіл і галогено-нижчий алкіл, (5) арил, -О-арил і -С(О)-арил, які можуть бути заміщені однією або більше групами, що включають нижчий алкіл, галоген, -ОН, -О-нижчий алкіл, -О-галогено-нижчий алкіл і галогенонижчий алкіл, (6) -С(О)-нижчий алкіл і -С(О)О-нижчий алкіл, де групи нижчого алкілу можуть бути відповідно заміщені однією або більше групами, що включають галоген, -ОН, -О-нижчий алкіл і О-галогено-нижчий алкіл, (7) -S-нижчий алкіл, -S(О)-нижчий алкіл і -S(О)2-нижчий алкіл, де групи нижчого алкілу можуть бути відповідно заміщені однією або більше групами, що включають галоген, -ОН, -Онижчий алкіл, -О-галогено-нижчий алкіл, і (8) нижчий алкіл і -О-нижчий алкіл, які можуть бути відповідно заміщені однією або більше групами, що включають замісники, описані у (1) - (7) вище. В іншому варіанті група D включає (1) галоген, (2) -ОН, (3) ціано, (4) -S-нижчий алкіл, -S(О)-нижчий алкіл і -S(О)2-нижчий алкіл, де групи нижчого алкілу можуть бути відповідно заміщені однією або більше групами, що включають галоген, -ОН, -Онижчий алкіл і -О-галогено-нижчий алкіл, і (5) нижчий алкіл і -О-нижчий алкіл, які можуть бути відповідно заміщені однією або більше групами, що включають замісники, описані у (1) - (4) вище. В іншому варіанті замісники в "циклоалкілі, який може бути заміщений", "ароматичному гетероциклі, який може бути заміщений" і "неароматичному гетероциклі, який може бути 1 заміщений", представленими R в формулі (I), представлені i) нижчим алкілом, який може бути заміщений однією або більше групами, що включають галоген, ОН і -О-нижчий алкіл, ii) галогеном, iii) нітро і iv) -ОН. У ще одному варіанті представлені одна або більше групи, вибрані з груп, що включають нижчий алкіл, галоген і -ОН, і в ще одному варіанті, представлені одна або більше групи, вибрані з метилу, F, Cl і -ОН. В іншому варіанті замісників "арилу, який може бути заміщений" в формулі (I) представлені 5 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 55 (1) нижчим алкілом або -О-нижчим алкілом, який може бути відповідно заміщений однією або більше групами, вибраними з групи, що включає галоген, -ОН, -О-нижчий алкіл і арил, (2) галогеном, (3) -ОН, (4) ціано, (5) циклоалкілом або -О-циклоалкілом, який може бути відповідно заміщений нижчим алкілом, (6) арилом, -О-арилом або -С(О)-арилом, який може бути відповідно заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген, -ОН, -О-нижчий алкіл О-(нижчий алкіл, заміщений галогеном) і нижчий алкіл, заміщений галогеном, (7) ароматичним гетероциклом або -О-ароматичним гетероциклом, який може бути відповідно заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл і галоген, (8) неароматичним гетероциклом або -О-неароматичним гетероциклом, який може бути відповідно заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл і галоген, (9) -С(О)-нижчим алкілом, -С(О)О-нижчим алкілом, -NH-C(О)-нижчим алкілом або -нижчий алкенілен-С(О)О-нижчим алкілом, де групи нижчого алкілу можуть бути відповідно заміщені однією або більше групами, що включають галоген і -ОН, (10) -NH2, -NH-нижчим алкілом або -N(нижчим алкілом)2, і (11) -S-нижчим алкілом, -S(О)-нижчим алкілом і -S(О)2-нижчим алкілом. Деякі варіанти сполуки формули (I) або її солі показані нижче. (1) Сполука або її сіль, в якій або Х, або Y є СН або його сіль; в іншому варіанті, сполука, в якій Х є СН і Y є N; в іншому варіанті, сполука або сіль, в якій Х є N і Y є СН або його сіль; (2) сполука або її сіль, в якій частина А представлена формулою (II) або (III); в іншому варіанті, сполука або її сіль, в якій частина А представлена формулою (II); в ще одному варіанті, сполука або її сіль, в якій частина А представлена формулою (III); (3) сполука або її сіль, в якій n в формулі (II) дорівнює 0 або 1; в іншому варіанті, сполука або її сіль, в якій n в формулі (II) дорівнює 1; (4) сполука або її сіль, в якій n в формулі (III) дорівнює 0 або 1; в іншому варіанті, сполука або її сіль, в якій n в формулі (III) дорівнює 0; в ще одному варіанті, сполука або її сіль, в якій n в формулі (III) дорівнює 1; (5) сполука або її сіль, в якій W є -NH-, -O-, -S- або -S(О)2-; в іншому варіанті, сполука або її сіль, в якій W є -NH-, -O - або -S-; в ще одному варіанті, сполука або її сіль, в якій W є -NH-, -O або -S(О)2-; в іншому варіанті, сполука або її сіль, в якій W є -NH- або -О-; в іншому варіанті, сполука або її сіль, в якій W є -NH- або -S-; в іншому варіанті, сполука або її сіль, в якій W є -NHабо -S(О)2-; в іншому варіанті, сполука або її сіль, в якій W є -NH-; в іншому варіанті, сполука або її сіль, в якій W є -О-; в іншому варіанті, сполука або її сіль, в якій W є -S(О)2-; 1 (6) сполука або її сіль, в якій R є циклоалкілом, арилом, ароматичним гетероциклом і неароматичним гетероциклом, який може бути відповідно заміщений однією або більше 1 групами, вибраними з групи D; в іншому варіанті, сполука або її сіль, в якій R є i) циклоалкілом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген і -ОН, ii) арилом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген, галогено-нижчий алкіл, -О-нижчий алкіл, -О-галогено-нижчий алкіл, -S-нижчий алкіл, -S(О)-нижчий алкіл, -S(О)2-нижчий алкіл, ціано, С(О)-нижчий алкіл, -С(О)О-нижчий алкіл, -NH2-, -NH-нижчий алкіл і -N(нижчий алкіл)2, iii) ароматичним гетероциклом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген і -ОН, або iv) неароматичним гетероциклом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, 1 галоген і -ОН; в ще одному варіанті, сполука або її сіль, в якій R є i) циклоалкілом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген і -ОН або ii) арилом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген, галогено-нижчий алкіл, -О-нижчий алкіл, -Огалогено-нижчий алкіл, -S-нижчий алкіл, -S(О)-нижчий алкіл, -S(О)2-нижчий алкіл, ціано, -С(О)нижчий алкіл, -С(О)О-нижчий алкіл, -NH2-, -NH-нижчий алкіл і -N(нижчий алкіл)2; в іншому 1 варіанті, сполука або її сіль, в якій R є i) циклоалкілом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген і -ОН, ii) арилом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген, галогено-нижчий алкіл, ціано, -S(О)2-нижчий алкіл і -О-галогено-нижчий алкіл; 6 UA 109550 C2 2 5 3 4 (7) сполука або її сіль, в якій R є Z-NR R або Z-циклічним аміно, який може бути заміщений 2 однією або більше групами, вибраними з групи D; в іншому варіанті, сполука або її сіль, в якій R є Z-циклічним аміно, який може бути заміщений однією або більше групами, вибраними з групи 2 D; в ще одному варіанті, сполука або її сіль, в якій R є групою, представленою формулою (V), 2 (VI) або (VII); в іншому варіанті, сполука або її сіль, в якій R є групою, представленою 2 формулою (V) або (VI); в іншому варіанті, сполука або її сіль, в якій R є групою, представленою 2 формулою (V); в іншому варіанті, сполука або її сіль, в якій R є групою, представленою 2 формулою (VI); і в іншому варіанті, сполука або її сіль, в якій R є групою, представленою формулою (VII) 10 6 15 20 25 30 35 40 45 50 (в формулах R однакові або різні є нижчим алкілом, який може бути заміщений однією або більше групами, вибраними з -ОН, -О-нижчого алкілу, галогену, циклоалкілу, ціано, -S-нижчого алкілу, -S(О)-нижчого алкілу, -S(О)2-нижчого алкілу і -О-галогено-нижчого алкілу, -ОН, -Онижчого алкілу, галогену, циклоалкілу, ціано, -О-нижчого алкілена-ОН, -S-нижчого алкілу, -S(О)нижчого алкілу, -S(О)2-нижчого алкілу і -О-галогено-нижчого алкілу); 6 (8) сполука або її сіль, в якій R в формулі (VI) є -нижчим алкіленом-ОН; в іншому варіанті, 6 сполука або її сіль, в якій R в формулі (VI) є С1-4 алкіленом-ОН; 6 (9) сполука або її сіль, в якій R в формулі (VII) є галогеном або -ОН; 5 5 (10) сполука або її сіль, в якій m в (R )m в формулі (II) дорівнює 0; або R є нижчим алкілом, 5 якщо m дорівнює 1 або 2; в іншому варіанті, сполука або її сіль, в якій m в (R )m в формулі (II) дорівнює 0; 5 (11) сполука або її сіль, в якій m в формулі (III) дорівнює 0, або m дорівнює 1 або 2 і R є нижчим алкілом; в іншому варіанті сполука або її сіль, в якій m в формулі (III) дорівнює 0; (12) сполука або її сіль, в якій Z є -С(О)- або -СН2-; в іншому варіанті, сполука або її сіль, в якій Z є -С(О)-; в ще одному варіанті, сполука або її сіль, в якій Z є -СН2-; (13) сполука, в якій n в формулі (VI) дорівнює 1 або 2, або її сіль; в іншому варіанті, сполука, в якій n в формулі (VI) дорівнює 1, або її сіль; (14) сполука або її сіль, в якій m в формулі (VI) дорівнює 0 або 1; в іншому варіанті, сполука або її сіль, в якій m в формулі (VI) дорівнює 0; (15) сполука або її сіль, в якій n в формулі (VII) дорівнює 1 або 2; в іншому варіанті, сполука або її сіль, в якій n в формулі (VII) дорівнює 2; (16) сполука або її сіль, яка є поєднанням двох або більше з варіантів, описаних вище в розділах (1) - (15) Як описано в представленому вище розділі (16), даний винахід включає сполуку або її сіль, яка являє собою поєднання двох або більше варіантів, описаних в представлених вище розділах (1) - (15). Конкретні приклади представлені нижче. (17) сполука або її сіль, в якій Х і Y є СН, С-нижчим алкілом або N; де або Х, або Y є N, W є -NH-, -N(нижчим алкілом)-, -О-, -S-, -S(О)- або -S(О)2-, 1 R є циклоалкілом, який може бути заміщений, арилом, який може бути заміщений, ароматичною гетероциклічною групою, яка може бути заміщена або неароматичною гетероциклічною групою, яка може бути заміщена, 2 3 4 R є -C(О)-NR R або групою, яку вибирають з формул (V), (VI) і (VII), частина А є групою, яку вибирають з формул (II), (III) і (IV), 3 R є Н або нижчим алкілом, 4 R є -нижчим алкіленом-ОН, -нижчим алкіленом-О-нижчим алкілом або -нижчим алкіленомS(О)2-нижчим алкілом, 5 R однакові або різні є нижчим алкілом або галогеном, 6 R однакові або різні є нижчим алкілом, галогеном, -ОН або нижчим алкіленом-ОН, Z однакові або різні є -С(О)-, -СН2- або -S(О)2-, m дорівнює цілому числу від 0 до 4, і n дорівнює цілому числу від 0 до 2. 7 UA 109550 C2 1 5 10 15 20 25 30 35 40 45 50 55 60 (18) сполука або її сіль, в якій R є циклоалкілом, арилом, ароматичним гетероциклом або неароматичним гетероциклом, які можуть бути відповідно заміщені одним або більше 2 3 4 замісниками, вибраними з групи D, R є -Z-NR R або Z-циклічним аміно, який може бути заміщений одним або більше замісниками, вибраними з групи D, 2 (19) сполука або її сіль по розділу (18), де R є групою, яку вибирають з формул (V), (VI) і 6 (VII), R однакові або різні є нижчим алкілом, який може бути заміщений одним або більше замісниками, вибраними з -ОН, -О-нижчого алкілу, галогену, циклоалкілу, ціано, -S-нижчого алкілу, -S(О)-нижчого алкілу, -S(О)2-нижчого алкілу і -О-галогено-нижчого алкілу, -ОН, -Онижчого алкілу, галогену, циклоалкілу, ціано, -О-нижчого алкілена-ОН, -S-нижчого алкілу, -S(О)нижчого алкілу, -S(О)2-нижчого алкілу і -О-галогено-нижчого алкілу, 2 (20) сполука або її сіль по розділу (19), де R є групою, яку вибирають з формул (V) або (VI), Z є -С(О)-, W є -NH-або -О-, і частина А є групою, яку вибирають з формул (II) або (III), 1 (21) сполука або її сіль по розділу (20), де Х є СН, Y є N, R є i) циклоалкілом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген і -ОН або ii) арилом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген, галогено-нижчий алкіл і -О-галогено-нижчий алкіл, частина А є групою, представленою формулою (II), де n дорівнює 0 або 1 і m дорівнює 0, n в формулі (VI) дорівнює 1 або 2, і m в формулі (VI) дорівнює 0, (22) сполука або її сіль по розділу (21), де n в формулі (II) дорівнює 0, n в формулі (VI) 1 дорівнює 1, R є фенілом, який може бути заміщений однією або більше групами, вибраними з групи, що включає галоген, -О-галогено-нижчий алкіл і галогено-нижчий алкіл, 1 (23) сполука або її сіль по розділу (20), де Х є СН, Y є N, R є i) циклоалкілом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген і -ОН або ii) арилом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген, галогено-нижчий алкіл, -О-нижчий алкіл і -Огалогено-нижчий алкіл, або неароматичним гетероциклом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген і -ОН, частина А є групою, представленою формулою (III), де n дорівнює 0 або 1 і m дорівнює 0, n в формулі (VI) дорівнює 1 або 2, і m в формулі (VI) дорівнює 0, 1 (24) сполука або її сіль по розділу (23), де R є фенілом, який може бути заміщений однією або більше групами, вибраними з групи, що включає галоген, -О-галогено-нижчий алкіл і 2 галогено-нижчий алкіл, R є групою, представленою формулою (V), і W є -NH-, 1 (25) сполука або її сіль по розділу (20), де Х є N, Y є СН, R є i) циклоалкілом, який може 0 бути заміщений однією або більше групами, вибраними з групи, що включає R , галоген і -ОН або ii) арилом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген, галогено-нижчий алкіл і -О-галогено-нижчий алкіл, частина А є групою, представленою формулою (II), де n дорівнює 1 і m дорівнює 0, n в формулі (VI) дорівнює 1, і m в формулі (VI) дорівнює 0, 1 (26) сполука або її сіль по розділу (25), де R є фенілом, який може бути заміщений однією або більше групами, вибраними з групи, що включає галоген і галогено-нижчий алкіл, Z є -С(О)-, 2 R є формулою (V), 1 (27) сполука або її сіль по розділу (20), де Х є N, Y є СН, R є i) циклоалкілом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген і -ОН або ii) арилом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, галоген, галогено-нижчий алкіл, -О-нижчий алкіл, -Огалогено-нижчий алкіл, -S-нижчий алкіл, -S(О)-нижчий алкіл, -S(О)2-нижчий алкіл, ціано, -С(О)нижчий алкіл, -С(О)О-нижчий алкіл, -NH2-, -NH-нижчий алкіл і -N(нижчий алкіл)2, частина А є групою, представленою формулою (III), де n дорівнює 0 або 1 і m дорівнює 0, n в формулі (VI) 6 дорівнює 1, R в формулі (VI) є -нижчим алкіленом-ОН, і m в формулі (VI) дорівнює 0 або 1, 1 (28) сполука або її сіль по розділу (28), де n в формулі (III) дорівнює 1, R є фенілом, який може бути заміщений однією або більше групами, вибраними з групи, що включає нижчий алкіл, 2 галоген і -О-галогено-нижчий алкіл, і R є формулою (V), Приклади конкретних сполук, включених в формулу (I) або їх солей, включають: {1-[(3-хлорфеніл)аміно]-5,6,7,8-тетрагідроізохінолін-4-іл}(1,1-діоксидотіоморфолін-4іл)метанон, {4-[(3-хлорфеніл)аміно]-5,6,7,8-тетрагідроізохінолін-1-іл}(1,1-діоксидотіоморфолін-4іл)метанон, морфолін-4-іл (1-{[(3-трифторметокси)феніл]аміно}-5,6,7,8-тетрагідроізохінолін-4-іл)метанон, (1,1-діоксидотіоморфолін-4-іл){4-[(3-трифторметил)фенокси]-5,6,7,8-тетрагідроізохінолін-1іл}метанон, 8 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 55 60 (1,1-діоксидотіоморфолін-4-іл)(4-{[(3-трифторметил)феніл]аміно}-5,6,7,8тетрагідроізохінолін-1-іл)метанон, (1,1-діоксидотіоморфолін-4-іл){1-[(3-трифторметил)фенокси]-5,6,7,8-тетрагідроізохінолін-1іл}метанон, {4-[(3-хлорфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-1-іл}(1,1-діоксидотіоморфолін4-іл)метанон, {1-[(3-хлорфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-4-іл}(1,1-діоксидотіоморфолін4-іл)метанон, (1,1-діоксидотіоморфолін-4-іл)(1-{[(3-трифторметил)феніл]аміно}-5,6,7,8-тетрагідро-5,8етаноізохінолін-4-іл)метанон, (1,1-діоксидотіоморфолін-4-іл)(4-{[(3-трифторметокси)феніл]аміно}-5,6,7,8-тетрагідро-5,8етаноізохінолін-1-іл)метанон, {4-[(3,4-дифторфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-1-іл}(1,1діоксидотіоморфолін-4-іл)метанон, {1-[(3-хлор-4-фторфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-4-іл}(1,1діоксидотіоморфолін-4-іл)метанон, (1,1-діоксидотіоморфолін-4-іл)(1-{[3-(трифторметокси)феніл]аміно}-5,6,7,8-тетрагідро-5,8метаноізохінолін-4-іл)метанон, (1,1-діоксидотіоморфолін-4-іл)(1-{[4-фтор-3-(трифторметил)феніл]аміно}-5,6,7,8-тетрагідро5,8-метаноізохінолін-4-іл)метанон, {1-[(3-хлорфеніл)аміно]-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-іл}(1,1діоксидотіоморфолін-4-іл)метанон, {1-[(3,4-дифторфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-4-іл}(1,1діоксидотіоморфолін-4-іл)метанон, (1,1-діоксидотіоморфолін-4-іл){4-[(2-фтор-3-метилфеніл)аміно]-5,6,7,8-тетрагідро-5,8етаноізохінолін-1-іл}метанон, (1,1-діоксидотіоморфолін-4-іл){4-[(2-фтор-5-метилфеніл)аміно]-5,6,7,8-тетрагідро-5,8етаноізохінолін-1-іл}метанон, {4-[(3-хлор-4-метилфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-1-іл}(1,1діоксидотіоморфолін-4-іл)метанон, {1-[(3-хлор-5-фторфеніл)аміно]-5,6,7,8-тетрагідро-5,8-етаноізохінолін-1-іл}(1,1діоксидотіоморфолін-4-іл)метанон, і їх солі. Сполука формули (I) має таутомери або геометричні ізомери, в залежності від типу замісників. У даному описі сполука формули (I) описана тільки в одній формі ізомеру в деяких випадках. Однак даний винахід включає інші ізомери, розділені ізомери або їх суміші. У доповнення, сполука формули (I) може мати асиметричні атоми вуглецю або осьову хіральність в деяких випадках, і в такому випадку можуть бути оптичні ізомери. Даний винахід також включає розділені оптичні ізомери сполуки формули (I) або їх суміші. Більше того, даний винахід включає фармацевтично прийнятні проліки сполуки, представленої формулою (I). Фармацевтично прийнятні проліки належать до сполук, що мають групу, яка може бути перетворена в аміногрупу, гідроксильну групу, карбоксильну групу або подібну сольволізом або в фізіологічних умовах. Приклади груп, які утворюють проліки, включають групи, описані в Prog. Med., 5, 2157-2161(1985) або в "Pharmaceutical Research and Development" (Hirokawa Publishing Company, 1990), Vol. 7, Drug Design 163-198. Сіль сполуки формули (I) стосується фармацевтично прийнятної солі сполуки формули (I), і солі утворюють кислотно-адитивні солі або сіль з основою в деяких випадках, в залежності від типу замісників. Конкретні приклади солі включають кислотно-адитивні солі з неорганічною кислотою, такою як хлористоводнева кислота, бромистоводнева кислота, йодистоводнева кислота, сірчана кислота, азотна кислота або фосфорна кислота, або з органічною кислотою, такою як мурашина кислота, оцтова кислота, пропіонова кислота, щавлева кислота, малонова кислота, янтарна кислота, фумарова кислота, малеїнова кислота, молочна кислота, яблучна кислота, мигдалева кислота, винна кислота, дибензоїлвинна кислота, дитолуоїлвинна кислота, лимонна кислота, метансульфонова кислота, етансульфонова кислота, бензолсульфонова кислота, п-толуолсульфонова кислота, аспартинова кислота або глутамінова кислота, солі з неорганічною основою, такою як натрій, калій, магній, кальцій або алюміній, або з органічною основою, такою як метиламін, етиламін, етаноламін, лізин або орнітин, солі з різними амінокислотами і похідними амінокислоти, такими як ацетиллейцин, солі амонію і подібні. Даний винахід також включає різні гідрати або сольвати і поліморфні речовини сполуки формули (I) і її солей. Крім того, даний винахід включає сполуки, мічені різними радіоізотопами або не радіоактивними ізотопами. 9 UA 109550 C2 5 10 15 20 Спосіб отримання Сполука формули (I) або її сіль може бути отримана із застосуванням різних відомих способів синтезу, із застосуванням характеристик на основі її лужної структури або типу замісників. У зв'язку з цим, в залежності від типу функціональних груп, в деяких випадках ефективно заміняти функціональну групу заздалегідь відповідною захисною групою (групою, яка може бути легко перетворена в функціональну групу) в момент перетворення вихідного матеріалу в проміжну сполуку, з урахуванням методики отримання. Приклади захисної групи включають захисні групи, описані у Wuts (P.G.M.Wuts) і Greene (T.W.Greene), "Greene's Protective Groups in Organic Synthesis" (4th edition, 2006) і подібних. Захисна група може застосовуватися при відповідному виборі відповідно до умов реакції. У цьому способі, захисну групу вводять для отримання реакції, і потім захисну групу необов'язково видаляють, з отриманням бажаної сполуки. Крім того, проліки сполуки формули (I) можуть бути отримані введенням конкретної групи на стадії від вихідного матеріалу до проміжної сполуки, як і вказаної вище захисної групи, або подальшою взаємодією із застосуванням отриманої сполуки формули (I). Реакція може проводитися методами, відомими фахівцям в даній галузі техніки, такими як етерифікація, амідування і дегідратація. Далі описаний типовий спосіб отримання сполуки формули (I). Кожний спосіб отримання може проводитися згідно з посилальним документом, включеним у відповідний опис. Більше того, кожний спосіб отримання відповідно до даного винаходу не обмежений наступними прикладами. Спосіб отримання 1 25 30 35 40 45 У формулі В є циклічною аміногрупою, яка може бути заміщена, W є -NH-, -N(нижчим алкілом)-, -О-, -S- або -S(О)2-. Сполука формули (I-1) або сполука формули (I-2) може бути отримана реакцією амідування між сполукою (1) і відповідною циклічною аміносполукою (2) або лінійною аміносполукою (3), яка може бути заміщена. Наприклад, в цій реакції сполуку (1) і відповідну циклічну аміносполуку (2) або лінійну аміносполуку (3), яка може бути заміщена, застосовують в еквівалентній кількості, або одну із сполук застосовують в надмірній кількості. Суміш цих сполук перемішують звичайно протягом від 0,1 години до 5 днів в умовах від охолоджування до нагрівання, переважно при від -20 °C до 100 °C, в розчиннику, не активному до реакції, в присутності конденсуючого агента. Не будучи особливо обмеженими, приклади розчинника, що застосовується, включають ароматичні вуглеводні, такі як бензол, толуол, ксилол і подібні, галогеновані вуглеводні, такі як дихлорметан, 1,2-дихлоретан, хлороформ і подібні, прості ефіри, такі як діетиловий ефір, тетрагідрофуран, діоксан, диметоксіетан і подібні, N, N-диметилформамід, N, Nдиметилімідазолідинон, диметилсульфоксид, етилацетат, ацетонітрил, етанол, воду і їх суміші. Приклади конденсуючого агента включають, але не обмежені ними, 3-оксид гексафторфосфату 1-[біс(диметиламіно)метилен]-1Н-1,2,3-триазоло[4,5-b]піридин-1-ія (ГАТУ), 1-(3диметиламінопропіл)-3-етилкарбодіімід (WCS), дициклогексилкарбодіімід (ДЦК), 1,1'карбонілдіімідазол (КДІ), азид дифенілфосфату і оксихлорид фосфору, і подібні. Переважно застосовувати добавку (наприклад, 1-гідроксибензотриазол (HOBt)) в деяких випадках для 10 UA 109550 C2 5 10 15 20 25 30 35 40 45 реакції. Іноді переважно провести реакцію в присутності органічної основи, такої як триетиламін, N, N-діізопропілетиламін. N-метилморфолін або подібні, або неорганічної основи, такої як карбонат калію, карбонат натрію, гідроксид калію або подібні, для більш нормального проходження реакції. Крім того, також можливо застосовувати спосіб перетворення карбоксильної групи похідного карбонової кислоти (1) в реакційноздатне похідне з подальшою його взаємодією з циклічною аміносполукою (2) або лінійною аміносполукою (3), яка може бути заміщена. Приклади реакційноздатного похідного карбонової кислоти включають галогеніди кислоти, отримані привзаємодії карбонової кислоти з галогенуючим агентом, таким як оксихлорид фосфору, тіонілхлорид або подібні, змішані ангідриди кислоти, отримані взаємодією карбонової кислоти з ізобутилхлорформіатом або подібними, і активні складні ефіри, отримані конденсуванням карбонової кислоти з 1-гідроксибензотриазолом або подібними. Реакція між цими реакційноздатними похідними і сполукою (2) або (3) може пройти в розчиннику, не активному до реакції, такому як галогеновані вуглеводні, ароматичні вуглеводні або прості ефіри, в умовах від охолоджування до нагрівання, переважно від -20 °C до 60 °C. Документ S. R. Sandler and W. Karo, "Organic Functional Group Preparations", 2nd edition, Vol. 1, Academic Press Inc., 1991 The Chemical Society of Japan., "Jikken Kagaku Koza (Courses in Experimental Chemistry) (5th edition)", Vol. 16, (2005) (MARUZEN Co., Ltd.) Спосіб отримання 2 У формулі р дорівнює 1 або 2 Сполука формули (I-4) може бути отримана реакцією окиснення сполуки формули (I-3), де W є -S-, серед сполук формули (I-1) або сполук формули (I-2), отриманих в способі отримання 1. Наприклад, сполука (I-3) може бути оброблена окисником, який застосовують в еквівалентній сполуці кількості, або застосовують в надмірній кількості в порівнянні із сполукою, звичайно протягом від 0,1 години до 3 днів, в розчиннику, не активному до реакції, в умовах від охолоджування до нагрівання, переважно від -20 °C до 80 °C. Приклади розчинника включають, але не обмежені ними, прості ефіри, такі як діетиловий ефір, тетрагідрофуран, діоксан, диметоксіетан і подібні, галогеновані вуглеводні, такі як дихлоретан, 1,2-дихлоретан, хлороформ і подібні, ароматичні вуглеводні, такі як бензол, толуол, ксилол і подібні, N, Nдиметилформамід, диметилсульфоксид і етилацетат, воду і їх суміші. Як окисник відповідним чином застосовують, наприклад, м-хлорпербензойну кислоту, періодат натрію і подібні. Документи B. M. Trost, "Comprehensive Organic Synthesis", Vol. 7, 1991 M. Hudlicky, "Oxidation in Organic Chemistry (ACS Monograph: 186), "ACS, 1990 The Chemical Society of Japan., "Jikken Kagaku Koza (Courses in Experimental Chemistry) (5th edition)", Vol. 17, (2005) (MARUZEN Co., Ltd.) Спосіб отримання 3 1 У формулі L є відхідною групою і Q є -NH- або -О-. 11 UA 109550 C2 5 10 15 20 25 30 Сполука формули (I-5) може бути отримана реакцією між сполукою (4) і сполукою (5). Приклади відхідної групи включають галоген, метансульфонілокси, п-толуолсульфонілоксигрупу і подібні. У реакції сполуку (4) і сполуку (5) використовують в еквівалентній кількості, або сполуки використовують в надмірній кількості. Їх суміш перемішують протягом від 0,1 години до 5 днів в розчиннику, не активному до реакції, в присутності основи і паладієвого каталізатора, в умовах від охолоджування до нагрівання із зворотним холодильником, переважно, від 0 °C до 100 °C. Не будучи особливо обмеженими, приклади розчинника, що застосовується, включають ароматичні вуглеводні, такі як бензол, толуол, ксилол і подібні, прості ефіри, такі як діетиловий ефір, тетрагідрофуран, діоксан, диметоксіетан і подібні, галогеновані вуглеводні, такі як дихлорметан, 1,2-дихлоретан, хлороформ і подібні, N, N-диметилформамід, диметилсульфоксид, етилацетат, ацетонітрил, і їх суміші. Іноді переважно провести реакцію в присутності органічної основи, такої як триетиламін, N, N-діізопропілетиламін, N-метилморфолін або подібного, або неорганічної основи, такої як карбонат калію, карбонат натрію, гідроксид калію, трет-бутоксид натрію, трет-бутоксид калію або подібні, для нормального проходження реакції. Приклади паладієвого каталізатора включають трис(дибензиліденацетон)дипаладій і подібні. Крім того, переважно в деяких випадках провести реакцію в присутності 2,2'біс(дифенілфосфіно)-1,1' бінафтилу або подібних як окремого ліганда для нормального проходження реакції. Більше того, в даному способі, якщо W є -О-, сполуку (5) і основу застосовують в еквівалентній кількості, або одне з них застосовують в надмірній кількості. Їх суміш перемішують протягом від 0,1 години до 5 днів в розчиннику, не активному до реакції, в умовах від охолоджування до нагрівання із зворотним холодильником, з подальшим доданням сполуки (4), з подальшим перемішуванням при нагріванні із зворотним холодильником від кімнатної температури, з отриманням сполуки I-5). Приклади основи, що застосовується, включають гідрид натрію. Також можливо застосовувати спосіб, в якому сполуку (4) і сполуку (5) застосовують в еквівалентній кількості, або одну з них застосовують в надмірній кількості, їх суміш нагрівають в розчиннику, не активному до реакції, з отриманням сполуки (I-5). У цьому випадку переважно провести реакцію в кислих умовах, наприклад, в присутності 4М розчину гідрохлориду/діоксану, для нормального проходження реакції. Спосіб отримання 4 35 40 45 Сполука формули (I-6) або (I-7) може бути отримана перетворенням гідроксильної групи сполуки (6) в відхідну групу з подальшою взаємодією відхідної групи з відповідною циклічною аміносполукою (2) або лінійною аміносполукою (3), яка може бути заміщена. Реакція може провестися перетворенням гідроксильної групи сполуки (6) в, наприклад, галоген, такий як хлор, бром або йод, або подібні, або сульфонілокси, такий як метансульфонілокси, етансульфонілокси, бензолсульфонілокси, 4-метилбензолсульфонілокси, трифторметансульфонілокси або подібні, або трифторметокси, і перемішуванням отриманої суміші протягом від 0,1 години до 5 днів в присутності відповідної основи, в розчиннику, не активному до реакції, або без застосування розчинника, в умовах від охолоджування до нагрівання, переважно, при кімнатній температурі або при нагріванні. Потім сполуку (7), в якій гідроксильна група перетворена у відхідну групу, і циклічну аміносполуку (2) або лінійну аміносполуку (3), яка може бути заміщена, застосовують в еквівалентній кількості, або одну з 12 UA 109550 C2 5 10 15 них застосовують в надмірній кількості, і сполуку перемішують протягом від 0,1 години до 5 днів в присутності основи, в розчиннику, не активному до реакції, в умовах від охолоджування до нагрівання із зворотним холодильником. Не будучи особливо обмеженими, приклади розчинника, що застосовується, включають ароматичні вуглеводні, такі як бензол, толуол, ксилол і подібні, прості ефіри, такі як діетиловий ефір, тетрагідрофуран, діоксан, диметоксіетан і подібні, галогеновані вуглеводні, такі як дихлорметан, 1,2-дихлоретан, хлороформ і подібні, N, N-диметилформамід, диметилсульфоксид, етилацетат, ацетонітрил, і їх суміші. Приклади основи включають органічні основи, такі як триетиламін, діізопропілетиламін, 1,8діазабіцикло[5.4.0]-7-ундецен, н-бутиллітій і подібні, і неорганічні основи, такі як карбонат натрію, карбонат калію, гідрид натрію, трет-бутоксид калію і подібні. Іноді переважно провести реакцію в присутності каталізатора міжфазного перенесення, такого як хлорид тетра-нбутиламонію. Документ S. R. Sandler, W. Karo, "Organic Functional Group Preparations", 2nd Edition, Vol. 1, Academic Press Inc., 1991 The Chemical Society of Japan., "Jikken Kagaku Koza (Courses in Experimental Chemistry) (5th edition)", Vol. 14, (2005) (MARUZEN Co., Ltd.) Синтез вихідного матеріалу 1 20 2 25 30 10 У формулі частина А є формулою (II) або (III), Т є NH, -O- або -S-, L є галогеном і R є ціано або -C(О) О-нижчим алкілом. Даний спосіб отримання являє собою спосіб отримання сполуки (17), в якій А частина представлена формулою (II) або (III), як вихідної сполуки (1) для способу отримання 1. Стадія 1 Ця стадія являє собою стадію отримання сполуки (9) окисненням сполуки (8), яку отримують способом, описаним в Tetrahedron, 1992, 48(36), 7663-7678, або способом на основі вказаного вище способу. Цю реакцію проводять по методиці способу отримання 2. Стадія 2 Ця стадія являє собою стадію отримання сполуки (10) введенням метоксигрупи в сполуку (9). 13 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 55 60 У цій реакції основу додають до суміші сполуки (9) і метанолу, і отриману суміш перемішують протягом від 0,1 години до 3 днів в умовах від охолоджування до нагрівання. Приклади основи включають метоксид натрію. Стадія 3 Ця стадія являє собою стадію отримання сполуки (11) галогенуванням сполуки (10). У цій реакції сполуку (10) і галогенуючий агент застосовують в еквівалентній кількості, або одне з них застосовують в надмірній кількості. Сполуку і агент перемішують протягом від 0,1 години до 5 днів в розчиннику, не активному до реакції, в умовах від охолоджування до нагрівання із зворотним холодильником, внаслідок чого відбувається реакція. Не будучи особливо обмеженими, приклади розчинника, що застосовується, включають галогеновані вуглеводні, такі як дихлорметан, 1,2-дихлоретан, хлороформ і подібні. Крім того, як галогенуючий агент може застосовуватися N-бромсукцинімід, N-хлорсукцинімід і подібні. Стадія 4 Ця стадія являє собою стадію отримання сполуки (12) ціанідуванням або етерифікацією сполуки (11). У цій реакції сполуку (11) і заздалегідь визначену сполуку ціано застосовують в еквівалентній кількості, або одну із сполук застосовують в надмірній кількості. Їх суміш перемішують від 0,1 години до 5 днів в розчиннику, не активному до реакції, в присутності паладієвого каталізатора, при нагріванні із зворотним холодильником від кімнатної температури, внаслідок чого відбувається реакція. Не будучи особливо обмеженими, приклади розчинника, що застосовується, включають ароматичні вуглеводні, такі як бензол, толуол, ксилол і подібні, прості ефіри, такі як діетиловий ефір, тетрагідрофуран, діоксан, диметоксіетан і подібні, галогеновані вуглеводні, такі як дихлорметан, 1,2-дихлоретан, хлороформ і подібні, N, N-диметилформамід, диметилсульфоксид, N-метилпіролідон, і їх суміші. Приклади сполуки ціано включають ціанід цинку, ціанід натрію, ціанід калію і подібні. Приклади паладієвого каталізатора включають трис(дибензиліденацетон)дипаладій і подібні. Також в деяких випадках переважно провести реакцію в присутності 1,1-біс(дифенілфосфіно)фероцену як додаткового ліганда, для нормального проходження реакції. Більше того, іноді переважно провести реакцію в присутності металевого порошку, наприклад, порошку цинку, для нормального проходження реакції. Крім того, замість ціанідування, окисень вуглеводу може бути введений в сполуку (11), і потім сполуку піддають реакції зі спиртом в реакційній системі, з отриманням сполуки (12) у вигляді похідного складного ефіру. У цій реакції сполуку (11) і окисень вуглеводу застосовують в еквівалентній кількості, або одну із сполук застосовують в надмірній кількості. Сполуку і окисень вуглеводу перемішують від 0,1 години до 5 днів в присутності паладієвого каталізатора і основи, в наступному розчиннику, в умовах від охолоджування до нагрівання із зворотним холодильником, для нормального проходження реакції. Не будучи особливо обмеженими, приклади розчинника, що застосовується, включають N, N-диметилформамід і подібні, спирти, такі як метанол, етанол і подібні, і їх суміші. Більше того, як паладієвий каталізатор застосовують, наприклад, ацетат паладію. Крім того, як основу застосовують триетиламін, наприклад. Більше того, в деяких випадках переважно провести реакцію в присутності ліганду, наприклад, дифенілфосфінофероцену, для нормального проходження реакції. Стадія 5 Ця стадія являє собою стадію отримання сполуки (13) деметилуванням сполуки (12). У цій реакції сполуку (12) і, наприклад, хлорид триметилсилілу застосовують в еквівалентній кількості, або одну із сполук застосовують в надмірній кількості. Суміш перемішують протягом від 0,1 години до 5 днів в розчиннику, не активному до реакції, при нагріванні із зворотним холодильником від кімнатної температури, внаслідок чого відбувається реакція. Не будучи особливо обмеженими, приклади розчинника, що застосовується, включають ацетонітрил і подібні. Крім того, в деяких випадках, переважно провести реакцію в присутності йодида калію, йодида натрію або подібних, для нормального проходження реакції. Більше того, замість хлориду триметилсилілу може застосовуватися концентрована хлористоводнева кислота або подібні. У цьому випадку, як розчинник може застосовуватися, наприклад, діоксан, вода і їх суміш. Стадія 6 Ця стадія являє собою стадію отримання сполуки (14) перетворенням гідроксильної групи сполуки (13) в заздалегідь визначену відхідну групу. У цій реакції гідроксильну групу сполуки (13) перемішують від 0,1 години до 5 днів в присутності галогенуючого агента або подібного і відповідної основи, в розчиннику, не 14 UA 109550 C2 5 10 15 20 25 30 активному до реакції або без розчинника, в умовах від охолоджування до нагрівання, переважно, при нагріванні від кімнатної температури, тим самим викликаючи перетворення гідроксильної групи сполуки в галоген, такий як хлор, бром, йод або подібні, або сульфонілоксигрупу, таку як метансульфонілокси, етансульфонілокси, бензолсульфонілокси, 4метилбензолсульфонілокси або трифторметансульфонілокси, або подібні, або в трифторметоксигрупу. Стадія 7 Ця стадія являє собою стадію отримання сполуки (16) взаємодією між сполукою (14) і сполукою (15). Ця реакція може провестися способом, описаним в способі отримання 3. 1 Крім того, якщо Т є -S-, сполуку (14) і R -SH застосовують в еквівалентній кількості, або одну із сполук застосовують в надмірній кількості. Суміш перемішують протягом від 0,1 години до 5 днів в розчиннику, не активному до реакції, в присутності паладієвого каталізатора, при нагріванні із зворотним холодильником від кімнатної температури, внаслідок чого відбувається реакція. Не будучи особливо обмеженими, приклади розчинника, що застосовується, включають діоксан і подібні. Як паладієвий каталізатор застосовують, наприклад, ацетат паладію. Більше того, в деяких випадках переважно провести реакцію в присутності ліганду, наприклад, біс[2-(дифенілфосфіно)фенілового]ефіру, для нормального проходження реакції. Стадія 8 Ця стадія являє собою стадію отримання сполуки (17) гідролізом сполуки (16). 10 У цій реакції, якщо R в сполуці є ціано, сполуку перемішують від 0,1 години до 5 днів в наступному розчиннику, при нагріванні із зворотним холодильником від кімнатної температури, переважно, при нагріванні із зворотним холодильником, в кислих або лужних умовах. Приклади розчинника, що застосовується, включають прості ефіри, такі як діетиловий ефір, тетрагідрофуран, діоксан, диметоксіетан і подібні, спирти, такі як метанол, етанол, і подібні, воду і їх суміші. Приклади кислоти, що застосовується при проведенні реакції в кислих умовах, включають хлористоводневу кислоту, сірчану кислоту, і подібні. Приклади основи, що застосовується при проведенні реакції в лужних умовах, включають водний розчин гідроксиду натрію, водний розчин гідроксиду калію, і подібні. 10 11 Якщо в сполуці R є CO2R , реакція може провестися, як описана у Greene and Wuts, "Protective Groups in Organic Synthesis", 3rd edition, John Wiley & Sons Inc, 1999. Синтез вихідного матеріалу 2 35 40 Даний спосіб отримання являє собою спосіб отримання сполуки (23), в якій А частина представлена формулою (II) або (III), як вихідна сполука (1) для способу отримання 1. Стадія 1 Ця стадія являє собою стадію отримання сполуки (19) амінуванням сполуки (18). Умови реакції такі ж, як в способі отримання 3. Стадія 2 15 UA 109550 C2 5 10 Ця стадія являє собою стадію отримання сполуки (20) деметилуванням сполуки (19). Умови реакції такі ж, як описані на стадії 5 синтезу вихідного матеріалу 1. Стадія 3 Ця стадія являє собою стадію отримання сполуки (21) перетворенням гідроксильної групи сполуки (20) в заздалегідь визначену відхідну групу. Умови реакції такі ж, як описані на стадії 6 синтезу вихідного матеріалу 1. Стадія 4 Ця стадія являє собою стадію отримання сполуки (22) ціанідуванням або етерифікацією 1 відхідної групи L сполуки (21). Умови реакції такі ж, як описані на стадії 4 синтезу вихідного матеріалу 1. Стадія 5 Ця стадія являє собою стадію отримання сполуки (23) гідролізом сполуки (22). Умови реакції такі ж, як описані на стадії 8 синтезу вихідного матеріалу 1. Синтез вихідного матеріалу 3 15 20 25 30 35 Даний спосіб отримання являє собою спосіб отримання сполуки (27) і сполуки (28), в яких -Z2 , представлений R , є -S(О)2-, як вихідної сполуки (4) для способу отримання 3. Стадія 1 Ця стадія являє собою стадію отримання сполуки (25) перетворенням гідроксильної групи сполуки (24) в тіольну групу. У цій реакції сполуку (24) обробляють реагентом Ловесона, який застосовують в еквівалентній із сполукою кількості або в надлишку в порівнянні із сполукою, протягом від 0,1 години до 3 днів в розчиннику, не активному до реакції, в умовах від охолоджування до нагрівання. Не будучи особливо обмеженими, приклади розчинника, що застосовується, включають ароматичні вуглеводні, такі як бензол, толуол, ксилол і подібні. Стадія 2 Ця стадія являє собою стадію отримання сполуки (26) перетворенням тіольної групи сполуки (25) в хлорид сульфонілхлориду. У цій реакції сполуку (25) обробляють окисником, який застосовують в еквівалентній із сполукою кількості або в надлишку в порівнянні із сполукою, протягом від 0,1 години до 3 днів в розчиннику, не активному до реакції, в умовах від охолоджування до нагрівання, в кислих умовах. Не будучи особливо обмеженими, приклади розчинника, що застосовується, включають галогеновані вуглеводні, такі як дихлорметан, 1,2-дихлоретан, хлороформ і подібні, воду і їх 16 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 суміші. Як окисник застосовують, наприклад, гіпохлорит натрію. Для отримання кислих умов, наприклад, застосовують концентровану хлористоводневу кислоту. Стадія 3 Ця стадія являє собою стадію отримання сполуки (27) або сполуки (28) амідуванням сполуки (26). Ця реакція може бути проведена способом, описаним в способі отримання 1. Синтез вихідного матеріалу 4 11 У формулі R є нижчим алкілом. Даний спосіб отримання являє собою спосіб отримання сполуки (6) як вихідної сполуки для способу отримання 4. Сполука (6) може бути отримана відновленням складної ефірної групи сполуки (29). У цій реакції сполуку (29) обробляють відновлюючим агентом, який застосовують в еквівалентній із сполукою кількості або в надлишку в порівнянні із сполукою, протягом від 0,1 години до 3 днів в розчиннику, не активному до реакції, в умовах від охолоджування до нагрівання, переважно від -20 °C до 80 °C. Не будучи особливо обмеженими, приклади розчинника, що застосовується, включають прості ефіри, такі як діетиловий ефір, тетрагідрофуран, діоксан, диметоксіетан і подібні, спирти, такі як метанол, етанол, 2-пропанол, і подібні, ароматичні вуглеводні, такі як бензол, толуол, ксилол, і подібні, N, N-диметилформамід, диметилсульфоксид, етилацетат, або їх суміш. Як відновлюючий агент застосовують гідридний відновлюючий агент, такий як боргідрид натрію, гідрид діізобутилалюмінію, або подібні, металеві відновлюючі агенти, такий як натрій, цинк, залізо або подібні, і інші відновлюючі агенти, описані в представлених нижче документах. Крім того, в деяких випадках переважно провести реакцію в присутності добавки, наприклад, хлориду кальцію, для нормального проходження реакції. Документи M. Hudlicky, "Reductions in Organic Chemistry, 2nd ed (ACS Monograph: 188), ACS, 1996 R. C. Larock, "Comprehensive Organic Transformations", 2nd edition, VCH Publishers, Inc., 1999 T. J. Donohoe, "Oxidation and Reduction in Organic Synthesis (Oxford Chemistry Primers 6), Oxford Science Publications, 2000 The Chemical Society of Japan., "Jikken Kagaku Koza (Courses in Experimental Chemistry) (5th edition)", Vol. 16, (2005) (MARUZEN Co., Ltd.) Фармакологічну дію сполуки формули (I) підтверджують в наступних тестах. Експериментальний приклад 1: тестування інгібування медийованого людським КБ2 утворення циклічного АМФ (цАМФ) Цей тест проводять із застосуванням клітин СНО, що викликають експресування людського КБ2 ("Molecular Pharmacology", 1995, Vol. 48, pp 443-450). 3 Суспензію клітин СНО, експресуючих людський КБ2 (2,5×10 /мл) і середовище для аналізу з доданням речовини, що тестується, і форсколіну (кінцева концентрація 0,5 мкМ) змішують разом в рівних кількостях з подальшим інкубуванням протягом 30 хвилин при кімнатній температурі, і потім додають 0,6 % Triton Х-100 з отриманням лізату клітин. Концентрацію цАМФ в лізаті клітин вимірюють із застосуванням набору цАМФ (виробництва Cisbio international). Середовище для дослідження отримують доданням до α-МЕМ виробництва Invitrogen 0,02 % CHAPS, 1 мМ ізобутилметилксантину і 0,5 мг/мл альбуміну бичачої сироватки. Концентрацію цАМФ в суспензії клітин, що не містить форс колін, беруть як 0 % підвищення цАМФ, і концентрацію цАМФ в суспензії клітин з доданням форсколіну беруть як 100 % підвищення цАМФ, що дозволяє розрахувати швидкість інгібування внутрішньоклітинного підвищення цАМФ в 30 нМ речовині, що тестується. 17 UA 109550 C2 Результати, отримані для декількох типових сполук, показані в таблиці 1. В таблиці пр. означає номер прикладу сполуки, що тестується, описаної нижче, і Інг. означає швидкість інгібування підвищення цАМФ. Таблиця 1 Пр. 10 11 16 30 33 36 38 52 59 94-1 98 101 Інг. (%) 73 77 87 82 81 82 77 96 93 97 96 99 Пр. 112 117-2 119-2 120-2 125 129 133-2 138 164 165 167 179 Інг. (%) 103 100 91 105 100 95 90 97 119 111 115 100 5 10 15 Експериментальний приклад 2: ефект інгібування розподілу маси задньої лапи у щурів з викликаним ад'ювантом артритом. Для цього тесту застосовують самиць щурів Льюїса (вік 7-8 тижнів). 50 мкл убитих Mycobacterium tuberculosis H37 Ra (виробництва DIFCO MICROBIOLOGY), суспендованих в рідкому парафіні в концентрації 10 мг/мл підшкірно вводять в подушечку стопи правої задньої лапи. На наступний день речовину, що тестується, вводять перорально і через деякий час навантаження на ліві і праві задні лапи вимірюють із застосуванням Incapacitance Tester (виробництва Linton Instruments), розраховуючи різницю навантаження між лівою і правою. Різниця навантаження групи, якій вводили носій, вважають як швидкість інгібування 0 %, і різницю навантаження в нормальній групі вважають як швидкість інгібування 100 %, що дозволяє розрахувати швидкість інгібування речовини, що тестується. Результати, отримані для декількох типових сполук, показані в таблиці 2. В таблиці пр. означає номер прикладу сполуки, що тестується, описаної нижче, і значення в дужках вказують дозу. 20 Таблиця 2 Приклад 10 16 30 36 119-2 120-2 133-2 138 25 30 Швидкість інгібування (%) 30 (0,1 мг/кг) 29 (0,1 мг/кг) 17 (0,1 мг/кг) 49 (0,1 мг/кг) 49 (0,3 мг/кг) 34 (0,3 мг/кг) 39 (0,3 мг/кг) 54 (0,3 мг/кг) Як показано в представлених вище тестах, декілька типових сполук володіють чудовою КБ2 агоністичною дією, і це показує, що сполуки можуть застосовуватися для профілактики і/або лікування наступних пов'язаних з КБ2 захворювань. Запальні захворювання, наприклад, захворювання, такі як дерматит, контактний дерматит, алергічний дерматит, атопічний дерматит, дерматити, такий як отруєння лаком і косметичний висип, алергічний риніт, сезонний алергічний риніт, хронічний бронхіт, бронхіт, пневмонія, несподівана інтерстиціальна пневмонія, рефлюкс-езофагіт, гастрит, атопічний гастрит, панкреатит, міокардит, перікардит, ендокардит, гепатит, запальні захворювання кишечнику, коліт, хронічні захворювання кишечнику, виразковий коліт, запальний ентерит, локалізований ілеїт, нефрит, гломерулонефрит, нефритичний синдром, ангіїт, алергічний гранулематозний ангіїт, виразковий ангіїт, васкуліт, ревматоїдний спондиліт, артрит, остеоартрит, псоріатичний артрит, подагричний артрит, юнацький артрит, реактивний артрит, недиференційований 18 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 55 спондилоартрит, ретиніт, увеїт, хороїдит увеального тракту, кон'юнктивіт, алергічний кон'юнктивіт, кератокон'юнктивіт, інфекційний кон'юнктивіт, вузелковий періартеріїт, тироїдит,поліміозит, гінгівіт, гіпертермія, тендиніт, бурсит, цистит, анкілозуючий спондиліт, енцефаліт, менінгіт, злоякісний менінгіт, бактерійний енцефаломенінгіт, цитомегаловірусний менінгіт, неврит, сонячний опік, ревматична лихоманка, вульварний вестибуліт, стоматит, гострий вагініт, баланіт, баланопостит, хронічне запалення слизової мембрани, дерматоміозит, тироїдит Хашімото, і хронічні запальні захворювання (біль, що супроводжується ревматоїдним артритом, деформуючий артроз, ревматоїдний спондиліт, подагричний артрит, юнацький артрит і розсіяний склероз). Біль, наприклад, біль при ревматоїдному артриті, біль при деформуючому артрозі, хронічний біль, запальний біль, гострий біль, гострий периферійний біль, люмбаго, хронічне люмбаго, головний біль, мігрень, зубний біль, запальний біль, ноцицептивний біль, нейрогенний біль, невропатичний біль, міалгія, фіброміалгія, вісцералгія, тазовий біль, невралгія, невралгія сідничного нерва, постгерпетична невралгія, діабетичний біль, біль, пов'язаний з ВІЛ, раковий біль, центральна невралгія трійникового нерва, нейрогенне люмбаго, тканинно-м'язовий і скелетний біль, психогенний біль, дисменорея, паралгезія, гіперпатія, гіпалгія, зубний біль, біль в шиї, біль, супроводжуючий вірусну інфекцію, біль, супроводжуючий запальну вірусну інфекцію, функціональний біль в животі (не виразковий шлунково-кишковий розлад, не серцевий біль, синдром подразненого кишечнику і подібні), біль, супроводжуючий ішемію міокарда, біль при травмі і токсині, алодинія і біль, викликаний ударом, і захворювання, такі як розтягнення і розтягнення м'язів. Рак і пухлини, наприклад, захворювання, такі як рак імунної системи, рак легенів, рак прямої і ободової кишки, злоякісна пухлина мозку, рак шкіри, рак матки, рак молочної залози, рак простати, лейкемія, доброякісна шкірна неоплазма, ракова пухлина, папілома, дрібноклітинний рак легенів, гліобластома, медулоепітеліома, медулобластома, нейробластома, пухлина ембріона, астроцитома, астробластома, епендимома, олігодендрогліома, пухлина сплетіння, нейроепітеліома, пухлина епіфізу, епендимобластома, нейроектодермальна пухлина, саркоматоз, злоякісна меланома, невринома, лімфома, нейрогліома, епітеліома щитовидної залози, нейробластома, лімфома Т-клітин шкіри, нейрогліома, пухлини, пінеальна пухлина і злоякісна мієлома. Респіраторні захворювання, наприклад, захворювання, такі як респіраторний дистрессиндром, гострий респіраторний дистрес-синдром, легеневий туберкульоз, кашель, бронхіальна астма, кашель, виникаючий при гіперчутливості дихальних шляхів (бронхіт, інфекція верхніх дихальних шляхів, астма, обструктивна легенева хвороба і подібні), холодові синдроми, протикашлевий ефект, гіперчутливість дихальних шляхів, туберкульозні пошкодження, астма (запальна клітинна інфільтрація в дихальний шлях, підвищена гіперчутливість дихальних шляхів, бронхоспазм, гіперсекреція слизу і подібні), хронічне обструктивне захворювання легенів, емфізема, фіброз легенів, ідіопатичний фіброз легенів, кашель, оборотна обструкція дихальних шляхів, респіраторний дистрес-синдром у дорослих, хвороба голуб'ятника, легені фермера, бронхо-легенева дисплазія, розлад дихальних шляхів і пневматоз. Захворювання печінки, наприклад, захворювання, такі як фіброз печінки, інфаркт печінки і хронічний цироз печінки. Захворювання мозку, наприклад, захворювання, такі як пошкодження мозку, ішемічний інсульт, удар, агент для лікування пухлин мозку, церебральна ішемія, гостра церебральна ішемія і цереброваскулярна ішемія. Захворювання очей, наприклад, захворювання, такі як очна гіпертонія, катаракта, глаукома, відшаровування сітківки, ретиноз, захворювання сітківки, розлади очного яблука і покриття виразками рогівки. Захворювання шкіри, наприклад, захворювання, такі як прурит, пахідермія, стареча ксеродермія і склеродермія. Захворювання кровообігу, наприклад, захворювання, такі як грудна жаба, нестабільна стенокардія, інфаркт міокарда, серцева недостатність, розсіяний склероз, артеріосклероз, атеросклероз, аритмія, гіпертонічний синдром, ішемічна хвороба серця, серцева криза, серцева ішемія, кардіоплегія, периферійна вазодилатація, гіпертонія, гіпотензія, рестеноз після коронарного стентування, тромбоз, захворювання судин і симптоми серцево-судинних захворювань, що супроводжуються ремоделюванням судин. Алергічні захворювання, наприклад, захворювання, такі як анафілаксія, алергія травного тракту, алергічні шлунково-кишкові захворювання, алергічна астма, атопічна астма, алергічний бронхо-легеневий аспергілоз, пилкова алергія і алергії на лікарські засоби. 19 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 55 60 Захворювання травлення, наприклад, захворювання, такі як запор, діарея, секреторна діарея, блювання (блювання, викликане протираковою хіміотерапією), нудота, зокрема, нудота, супроводжуюча хіміотерапію, нудота, супроводжуюча СНІД, гастроезофагеальна рефлюксна хвороба, пептична виразка, синдром подразненого кишечнику, функціональне шлунковокишкове подразнення, запальна хвороба кишечнику і виразковий коліт. Урогенітальні захворювання, наприклад, захворювання, такі як ускладнена менструація. Імунологічні захворювання, наприклад, захворювання, такі як імунологічна недостатність, імунорегулювання, аутоімунні захворювання, лімфома Т-клітин, псоріаз, звичайний псоріаз, ревматоїдний артрит, остеопороз, сепсис, септичний шок, системний червоний вовчак, аутоімунна гемолітична анемія і СНІД. Ускладнення, супроводжуючі трансплантацію, наприклад, захворювання, такі як відторгнення після трансплантації і захворювання "трансплантат проти хазяїна". Неврогенні захворювання, наприклад, захворювання, такі як нейродегенеративні захворювання, депресія, маніакальна депресія, нудота, вертіго, фантомна кінцівка, нервові розлади, периферійні нервові розлади, пошкодження нервів, травматичний невроз, недоумство, старече недоумство, деменція, стареча деменція, хвороба Альцгеймера, психоз, шизофренія, хвороба Піка, хорея Хантінгтона, хорея, хвороба Паркінсона, хвороба Крейтцфельдта-Якоба, захворювання відцентрового нерва, недоумство при множинному ішемічному інсульті, гіпоксія, авітаміноз, віковий розлад пам'яті, шизофренічний розлад, депресія, тривога, панічний розлад, агорафобія, соціальна фобія, обсесивно-компульсивний розлад, пост-травматичний стрес, розлад пам'яті, амнезія, апестат, втрата апетиту, анорексія, нервова булімія, функціональний розлад, циркадна аритмія, розлад сну, дисомнія, безсоння, гіперсомнія, апное уві сні, залежність від хімічних речовин, печія, дисфагія, гіперчутливість ниркової лоханки, нейродегенерація (супроводжуюча удар, зупинку серця, травматичний розлад мозку і мієлопатія), дискінезія, конвульсії, м'язові судоми, тремор, парестезія і гіперестезія. Інші захворювання, такі як синдром Гілайна-Барра, хвороба Педжета, хронічна хворобливість, аверсія, міастенія гравіс, діабет, цукровий діабет I типу, ішемічний стан, спонтанний пневмоторакс, нейродегенеративний синдром, круп, синдром Сйоргена, пошкодження спинного мозку, травматичне пошкодження хряща, епілепсія, скороминущі церебральні ішемічні приступи, опортуністичні інфекції (ВІЛ і подібні), червоний плоский лишай, пемфигіт, булезний епідермоліз, гіпертрофічний шрам, келоїдні рубці, артроз, ішемія серця, інфаркт, сироваткова хвороба, ниркова ішемія, афтозна виразка, хвороба Крона, целіакія, апластична анемія, хвороба Ходжкіна, нефротичний синдром, ендотоксичний шок, гіпотензивний шок, ослаблення фертильності, синдром Турета, інгібування пам'яті, екзема, саркоїдоз, респіраторний дистрес-синдром у дорослих, захворювання коронарної артерії, меланома, хвороба Грейвса, синдром Гудпасчера, амілоз, захворювання, що вражають колонії клітин плазми, відкладена або миттєва гіперчутливість, паразити, вірусна або бактерійна інфекція, пошкодження хребта, запаморочення, ожиріння, захворювання з'єднувальних тканин, захворювання, що вражають лімфатичну кроветворну систему, аміотрофічний бічний склероз, ускладнені м'язові судоми, ускладнена кахексія і бактерійний менінгіт. Фармацевтична композиція, що містить один або більше види сполуки формули (I) або її солі як активний інгредієнт, може бути отримана із застосуванням ексципієнтів, що звичайно застосовуються в даній галузі техніки, тобто із застосуванням ексципієнтів або носіїв для лікарських засобів, звичайними методами. Композиція може вводитися в будь-яких формах, таких як пероральне введення із застосуванням таблетки, пілюлі, капсули, гранул, порошку або рідин, і парентеральне введення із застосуванням препаратів для ін'єкцій, таких як внутрішньосуглобна ін'єкція, внутрішньовенна ін'єкція і внутрішньом'язова ін'єкція, супозиторій, очні краплі, очна мазь, черезшкірна рідина, мазь, черезшкірний пластир, черезмембранна рідина, черезмембранний пластир або інгаляція. Як тверду композицію для перорального введення застосовують таблетку, порошок, гранули і подібні. У такій твердій композиції один або два типи активних інгредієнтів змішують з, принаймні, одним видом неактивного ексципієнта. Композиція може містити неактивні добавки, наприклад, лубрикант, дезінтегруючий агент, стабілізатор і добавку для розчинення згідно із звичайними методами. Таблетка або пілюля необов'язково можуть бути покриті цукром або плівкою з розчинного в шлунку або кишечнику матеріалу. Рідка композиція для перорального введення включає фармацевтично прийнятний опалесціюючий агент, розчин, суспензію, сироп, еліксир або подібні, і містить звичайний неактивний розріджувач, наприклад, очищену воду або етанол. Рідка композиція може містити допоміжний агент, такий як солюбілізатор, зволожувач або суспензію, підсолоджувач, смакову добавку, ароматичний агент і консервант, в доповнення до неактивного розріджувача. 20 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 55 60 Препарат для ін'єкції для парентерального введення містить стерильний водний або неводний розчинник, суспензію або опалесціюючий агент. Приклади водного розчинника включають дистильовану воду для ін'єкцій і фізіологічний розчин. Приклади неводного розчинника включають спирти, такі як етанол. Ці композиції можуть також містити агент тонічності, консервант, зволожувач, емульгатор, диспергатор, стабілізатор або солюбілізатор. Їх стерилізують, наприклад, фільтруванням, при якому їх фільтрують через уловлюючий бактерії фільтр, змішуванням з антимікробним препаратом, або опроміненням. Більше того, вони можуть застосовуватися у вигляді композиції стерильного розчину і розчинятися або суспендуватися в стерильній воді або стерильному носії для ін'єкцій перед застосуванням. Застосування агентів для зовнішнього використання включає мазь, пластир, крем, желе, гарячий компрес, спрей, лосьйон, очні краплі, очну мазь і подібні. Агент для зовнішнього застосування містить звичайний субстрат для мазей і лосьйонів, водні або неводні рідкі композиції, суспензію, емульсію, і подібні. Черезслизові агенти, такі як інгаляції і трансназальні агенти, застосовують у вигляді рідини або напівтвердої речовини, і можуть бути отримані методами, відомими в даній галузі техніки. Наприклад, туди можуть бути відповідним образом додані відомі ексципієнти, рН коректор, консервант, поверхнево-активна речовина, лубрикант, стабілізатор, загусник або подібні. Для введення можуть застосовуватися відповідні пристрої для інгаляцій або інсуфляцій. Наприклад, при застосуванні відомого пристрою, такого як дозуючий інгалятор або розпилювач, сполука може вводитися окремо або вводитися у вигляді порошку або складової суміші або розчину або суспензії в поєднанні сполуки з фармацевтично прийнятним носієм. Сухий порошковий інгалятор і подібні можуть застосовуватися для одного введення або множини введень, і може застосовуватися сухий порошок або капсули, що містять порошок. Альтернативно, сполука може вводитися в формі стисненого аерозольного спрею із застосуванням відповідного викидаючого агента, наприклад, відповідного газу, такого як хлорфторалкан, гідрофторалкан або двоокис вуглецю. Звичайно для перорального введення відповідна добова доза складає від близько 0,001 мг/кг до 100 мг/кг на масу тіла, переважно від 0,1 мг/кг до 30 мг/кг, і більш переважно, від 0,1 мг/кг до 10 мг/кг, її вводять від одного-двох до чотирьох разів на добу окремими дозами. При внутрішньовенному введенні відповідна добова доза складає від 0,0001 мг/кг до 10 мг/кг на масу тіла, її вводять один або багато разів на добу окремими дозами. Крім того, черезслизовий агент вводять один раз на добу або багато разів на добу окремими дозами в дозі від близько 0,001 мг/кг до 100 мг/кг на масу тіла. Дозу відповідним чином визначають в кожному конкретному випадку з урахуванням симптомів, віку, статі і подібних. Фармацевтична композиція відповідно до даного винаходу містить один або більше види сполуки формули (I) і її солі як активний інгредієнт, в кількості від 0,01 % мас. до 100 % мас., і від 0,01 % мас. до 50 % мас. в одному варіанті, хоча кількість може варіюватися в залежності від способу введення, дозованої форми, місця введення і типу ексципієнта або добавки. Сполука формули (I) може застосовуватися одночасно з агентом для лікування або профілактики різних захворювань, що вважаються захворюваннями, для яких сполука формули (I) є ефективною. При спільному застосуванні сполука і агент можуть бути введені одночасно, введені послідовно в один час або введені з бажаним часовим інтервалом. Препарат для одночасного введення може бути виготовлений у вигляді окремих препаратів або фармацевтичної композиції, яка містить різні агенти для лікування або профілактики захворювань, що вважаються захворюваннями, для яких сполука формули (I) є ефективною, і сполуку формули (I). Приклади Далі спосіб отримання сполуки формули (I) описаний детально на основі прикладів, але даний винахід не обмежений сполукою, описаною в представлених нижче прикладах. Крім того, спосіб отримання вихідних сполук показаний, відповідно, в прикладах отримання. Спосіб отримання сполуки формули (I) не обмежений способами отримання в показаних нижче прикладах. Сполука формули (I) може бути отримана об'єднанням цих способів отримання, або способом, який відомий фахівцеві в даній галузі техніки. У прикладах отримання, прикладах і представлених нижче таблицях в деяких випадках застосовують наступні абревіатури. ППр: номер прикладу отримання (якщо номер прикладу отримання включає, наприклад, 391 і 39-2, це показує, що сполуки отримані у вигляді енантіомерів), Пр: номер прикладу (якщо номер прикладу включає, наприклад, 5-1 і 5-2, це показує, що сполуки отримані у вигляді енантіомерів), Стр: хімічна структурна формула, ПСин: спосіб отримання (показує, що відповідну сполуку отримують тим же способом отримання, як сполуку, відмічену номером 21 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 55 60 прикладу отримання, описаним в стовпці), Син: спосіб отримання (показує, що відповідну сполуку отримують тим же способом отримання, як сполуку, відмічену номером прикладу, 1 описаним в стовпці), дані: фізико-хімічні дані, ЯМР1: δ (ч./млн.) характеристичного піка в Н+ ЯМР в ДМСО-d6, ESI +: значення m/z в мас спектрометрії (іонізація ESI, (М+Н) , якщо не вказано інакше), ESI -: значення m/z в маси спектрометрии (іонізація ESI, (М+Н) , якщо не вказано інакше). Крім того, сполука, що має символ * в структурі, представляє єдиний енантіомер. [M] в прикладі отримання і прикладі означає [моль/л]. [α]D показує оптичне обертання, і с означає концентрацію в момент вимірювання оптичного обертання. Більше того, Темп. в таблиці означає температуру початку екстраполяції (°С) в диференціюючій скануючій калориметрії (ДСК). Приклад отримання 1 Суспензію N, N-диметилформаміду (25 мл), що містить 4-бром-1-метокси-5,6,7,8тетрагідроізохінолін (2,13 г), порошок цинку (115 мг), ціаніду цинку (2,07 г), трис(дибензиліденацетон)дипаладій (0) 9201 мг) і 1,1'-біс(дифенілфосфіно)фероцен (244 мг) перемішують протягом 2 годин при 120 °C в атмосфері азоту, з подальшим охолоджуванням до кімнатної температури. Потім туди додають етилацетат, нерозчинний продукт видаляють фільтрацією з целітом, і отриманий продукт промивають етилацетатом. Фільтрат промивають розбавленим водним аміаком, водою і насиченим розчином солі, і сушать над безводним сульфатом магнію з подальшою фільтрацією. Отриманий фільтрат концентрують, і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням 1метокси-5,6,7,8-тетрагідроізохінолін-4-карбонітрилу (992 мг) у вигляді блідо-коричневого порошку. Приклад отримання 2 Хлорид триметилсилілу (0,564 мл) додають до суспензії в ацетонітрилі (10 мл), що містить 1-метокси-5,6,7,8-тетрагідроізохінолін-4-карбонітрил (420 мг) і йодид калію (741 мг), і отриману суміш перемішують протягом 4 годин при 70 °C з подальшим охолоджуванням до кімнатної температури. Потім туди додають воду і екстрагують етилацетатом. Органічний шар промивають водою і насиченим розчином солі, і сушать над безводним сульфатом магнію з подальшою фільтрацією. Отриманий фільтрат концентрують, і залишок суспендують в хлороформі. Нерозчинні тверді речовини збирають фільтрацією з отриманням 1-оксо1,2,5,6,7,8-гексагідроізохінолін-4-карбонітрилу (74 мг) у вигляді блідо-жовтого порошку. Фільтрат концентрують, і залишок суспендують в етилацетаті. Нерозчинні тверді речовини збирають фільтрацією з отриманням 1-оксо-1,2,5,6,7,8-гексагідроізохінолін-4-карбонітрилу (201 мг) у вигляді червоного порошку. Отриманий фільтрат концентрують, і залишок очищають хроматографією на колонці з силікагелем (хлороформ-метанол) з отриманням 1-оксо1,2,5,6,7,8-гексагідроізохінолін-4-карбонітрилу (15 мг) у вигляді блідо-коричневого порошку. Приклад отримання 3 Суміш 1-оксо-1,2,5,6,7,8-гексагідроізохінолін-4-карбонітрилу (290 мг) і оксихлориду фосфору (8,23 г) нагрівають при кипінні із зворотним холодильником протягом 3 годин. Реакційну суміш концентрують, і воду додають до залишку, потім екстрагують етилацетатом. Органічний шар промивають водою і насиченим розчином солі, і сушать над безводним сульфатом магнію з подальшою фільтрацією. Отриманий фільтрат концентрують з отриманням 1-хлор-5,6,7,8тетрагідроізохінолін-4-карбонітрилу (320 мг) у вигляді жовтої твердої речовини. Приклад отримання 4 Суміш 1-хлор-5,6,7,8-тетрагідроізохінолін-4-карбонітрилу (315 мг), 3-хлораніліну 91 г) і Nметилпіролідону перемішують протягом 4 годин при 180 °C з подальшим охолоджуванням до кімнатної температури. Додають воду, потім екстрагують етилацетатом. Органічний шар промивають водою і насиченим розчином солі, і сушать над безводним сульфатом магнію з подальшою фільтрацією. Отриманий фільтрат концентрують, і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням 1-[(3хлорфеніл)аміно]-5,6,7,8-тетрагідроізохінолін-4-карбонітрилу (225 мг) у вигляді блідокоричневого порошку. Приклад отримання 5 Суміш 1-[(3-хлорфеніл)аміно]-5,6,7,8-тетрагідроізохінолін-4-карбонітрилу (125 мг) і 50 % водного розчину сірчаної кислоти (4 мл) нагрівають при кипінні із зворотним холодильником протягом 7 годин з подальшим охолоджуванням до кімнатної температури. Потім додають воду і хлороформ, перемішують протягом 10 хвилин при кімнатній температурі. Нерозчинний продукт збирають фільтрацією і промивають водою і хлороформом з отриманням 1-[(3хлорфеніл)аміно]-5,6,7,8-тетрагідроізохінолін-4-карбонової кислоти (59,3 мг) у вигляді блідокоричневої твердої речовини. Водний шар фільтрату виділяють і додають водний розчин 22 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 55 60 гідроксиду натрію для доведення рН до 3-4 з подальшою екстракцією з хлороформом/метанолом (20:1), сушать над безводним сульфатом магнію і фільтрують. Отриманий фільтрат концентрують, і додають невелику кількість хлороформу. Нерозчинні тверді речовини збирають фільтрацією і промивають діізопропіловим ефіром з отриманням 1[(3-хлорфеніл)аміно]-5,6,7,8-тетрагідроізохінолін-4-карбонової кислоти (39,4 мг) у вигляді блідокоричневої твердої речовини. Фільтрат концентрують, і залишок очищають хроматографією на колонці з силікагелем (хлороформ-метанол) з отриманням 1-[(3-хлорфеніл)аміно]-5,6,7,8тетрагідроізохінолін-4-карбонової кислоти (3 мг) у вигляді блідо-коричневого порошку. Приклад отримання 6 Ацетат паладію (76,8 мг), дифенілфосфінофероцен (189 мг) і триетиламін (3 мл) додають до суміші 4-бром-5,6,7,8-тетрагідроізохінолін-1(2Н)-ону (1,56 г), етанолу (15,6 мл) і N, Nдиметилформаміду (31,2 мл), і результат перемішують протягом 48 годин при 100 °C в атмосфері окислу вуглецю. До реакційної суміші додають воду, і нерозчинний матеріал видаляють фільтрацією, потім екстрагують етилацетатом. Органічний шар промивають водою і насиченим розчином солі, і сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням етил 1-оксо-1,2,5,6,7,8гексагідроізохінолін-4-карбоксилату (964 мг) у вигляді коричневої твердої речовини. Приклад отримання 7 Суміш етил 1-оксо-1,2,5,6,7,8-гексагідроізохінолін-4-карбоксилату (531 мг) і оксихлориду фосфору (7,1 мл) перемішують протягом 2 годин при 100 °C. Реакційний розчин концентрують при зниженому тиску, до залишку додають лід і водний розчин гідрокарбонату, потім екстрагують етилацетатом. Органічний шар промивають насиченим розчином солі і сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують з отриманням 1-хлор-5,6,7,8-тетрагідроізохінолін-4-карбоксилату (574 мг) у вигляді коричневої твердої речовини. Приклад отримання 8 3-(Трифторметил)фенол (340 мкл) додають до суміші 60 % гідриду натрію (120 мг) і N, Nдиметилформаміду (31,2 мл) при охолоджуванні на льоду з подальшим перемішуванням протягом 30 хвилин при кімнатній температурі. Потім додають 1-хлор-5,6,7,8тетрагідроізохінолін-4-карбоксилат (565 мг) з подальшим перемішуванням протягом 120 годин при 80 °C. До реакційної суміші додають воду при охолоджуванні на льоду, потім екстрагують етилацетатом. Органічний шар промивають насиченим розчином солі і сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують, і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням 1-[(3трифторметил)фенокси]-5,6,7,8-тетрагідроізохінолін-4-карбоксилату (193 мг) у вигляді коричневої твердої речовини. Приклад отримання 9 Метил 2-оксоциклопентанкарбоксилат (3,41 г) і метоксид натрію (1,77 г) додають в суспензію в етанолі (40 мл), що містить гідрохлорид 3-аміно-3-імінопропанаміду (3,00 г) з подальшим нагріванням при кипінні із зворотним холодильником протягом 4,5 годин. Реакційний розчин концентрують при зниженому тиску і додають воду, потім нейтралізують оцтовою кислотою. Осад збирають фільтрацією і промивають етанолом з отриманням 3-аміно-1-гідрокси-6,7дигідро-5Н-циклопента[с]піридин-4-карбоксаміду (1,66 г) у вигляді безбарвної твердої речовини. Приклад отримання 10 Суміш 3-аміно-1-гідрокси-6,7-дигідро-5Н-циклопента[с]піридин-4-карбоксаміду (1,65 г) і оксихлориду фосфору (8 мл) нагрівають при кипінні із зворотним холодильником протягом 3 годин. Реакційний розчин концентрують при зниженому тиску, і залишок додають в крижану воду з подальшою нейтралізацією карбонатом натрію і екстрагуванням хлороформом. Органічний шар концентрують при зниженому тиску і потім залишок очищають хроматографією на колонці з силікагелем (хлороформ:метанол = 10:1) з отриманням 3-аміно-1-хлор-6,7-дигідро5Н-циклопента[с]піридин-4-карбонітрилу (725 мг) у вигляді блідо-жовтої твердої речовини. Приклад отримання 11 Мідний порошок додають до суміші нітриту N-амілу і тетрагідрофурану (10 мл) при кімнатній температурі, і потім по краплях додають суміш 3-аміно-1-хлор-6,7-дигідро-5Нциклопента[с]піридин-4-карбонітрилу (598 мг), тетрагідрофурану (15 мл) і N, Nдиметилформаміду (15 мл). Через 15 хвилин продукт нагрівають до 80 °C і перемішують протягом 4 годин при тій же температурі. Додають воду, потім екстрагують етилацетатом. Органічний шар промивають насиченим розчином солі і сушать над безводним сульфатом магнію з подальшою фільтрацією. Отриманий фільтрат концентрують, і залишок очищають 23 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 55 хроматографією на колонці з силікагелем (гексан-етилацетат = 3:1) з отриманням 1-хлор-6,7дигідро-5Н-циклопента[с]піридин-4-карбонітрилу (394 мг) у вигляді білої твердої речовини. Приклад отримання 12 Суміш 1-хлор-6,7-дигідро-5Н-циклопента[с]піридин-4-карбонітрилу (452 мг), 3-хлораніліну (1,45 г) і 1-метил-2-піролідону (7 мл) перемішують протягом 4 годин при 180 °C. Воду додають до реакційної суміші, потім перемішують протягом години. Потім тверді речовини, що випали в осад збирають фільтрацією і промивають водою і потім сумішшю гексану:етилацетату (4:1) з подальшим сушінням при зниженому тиску з отриманням 1-[(3-хлорфеніл)аміно-6,7-дигідро-5Нциклопента[с]піридин-4-карбонітрилу (633 мг) у вигляді блідо-коричневої твердої речовини. Приклад отримання 13 Суміш 1-[(3-хлорфеніл)аміно-6,7-дигідро-5Н-циклопента[с]піридин-4-карбонітрилу (633 мг), сірчаної кислоти (6 мл) і води (6 мл) перемішують протягом 10 годин при 120 °C. Потім реакційну суміш охолоджують, додають крижану воду з подальшою нейтралізацією водним розчином гідроксиду натрію і перемішуванням протягом години при кімнатній температурі. Тверді речовини, що випали в осад, збирають фільтрацією і промивають водою і потім сумішшю гексану:етилацетату (3:1) з подальшим сушінням при зниженому тиску з отриманням 1-[(3хлорфеніл)аміно-6,7-дигідро-5Н-циклопента[с]піридин-4-карбонової кислоти (633 мг) у вигляді блідо-сірої твердої речовини. Приклад отримання 14 Суміш 1-(метилсульфоніл)-5,6,7,8-тетрагідро-5,8-метаноізохіноліну (280 мг) і хлороформу (5 мл) по краплях додають до суміші 3-хлорпербензойної кислоти (340 мг) і хлороформу (10 мл) при охолоджуванні на льоду. Реакційну суміш перемішують протягом 2 годин при кімнатній температурі і потім додають насичений водний розчин карбонату натрію. Водний шар екстрагують хлороформом і органічний шар промивають водою. Органічний шар сушать над безводним сульфатом магнію, потім фільтрують і концентрують з отриманням 1(метилсульфініл)-5,6,7,8-тетрагідро-5,8-метаноізохіноліну (303 мг) у вигляді блідо-жовтого масла. Приклад отримання 15 Метоксид натрію (4 мл) додають до суміші 1-(метилсульфініл)-5,6,7,8-тетрагідро-5,8метаноізохіноліну (303 мг) і метанолу (2 мл), і отриману суміш нагрівають при кипінні із зворотним холодильником протягом 15 хвилин. Реакційну суміш концентрують, і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням 1метокси-5,6,7,8-тетрагідро-5,8-метаноізохіноліну (363 мг) у вигляді блідо-жовтого масла. Приклад отримання 16 N-бромсукцинімід (286 мг) додають до суміші 1-метокси-5,6,7,8-тетрагідро-5,8метаноізохіноліну (256 мг) і хлороформу (4 мл), і отриману суміш перемішують протягом 36 годин при кімнатній температурі. Реакційну суміш концентрують, і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням 4-бром-1-метокси5,6,7,8-тетрагідро-5,8-метаноізохіноліну (286 мг) у вигляді безбарвного масла. Приклад отримання 17 Ацетат паладію (13 мг), дифенілфосфінофероцену (31 мг) і триетиламіну (470 мкл) додають до суміші 4-бром-1-метокси-5,6,7,8-тетрагідро-5,8-метаноізохіноліну (286 мг), етанолу (3 мл) і N, N-диметилформаміду (6 мл), і отриману суміш перемішують протягом 15 годин при 100 °C в атмосфері окислу вуглецю. До реакційної суміші додають воду, потім екстрагують етилацетатом. Органічний шар промивають водою і насиченим розчином солі і сушать над безводним сульфатом магнію з подальшою фільтрацією. Отриманий фільтрат концентрують, і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням етил 1-метокси-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-карбоксилату (140 мг) у вигляді безбарвного масла. Приклад отримання 18 Йодид натрію (96 мг) і хлорид триметилсилілу (18 мкл) додають до суміші етил 1-метокси5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-карбоксилату (140 мг) і ацетонітрилу (4 мл) з подальшим перемішуванням протягом 4 годин при кімнатній температурі і протягом 15 годин при 50 °C. До реакційної суміші додають воду і потім екстрагують етилацетатом. Органічний шар промивають водою і насиченим розчином солі і сушать над безводним сульфатом магнію з подальшою фільтрацією. Отриманий фільтрат концентрують з отриманням етил 1-оксо1,2,5,6,7,8-гексагідро-5,8-метаноізохінолін-4-карбоксилату (134 мг) у вигляді коричневої твердої речовини. Приклад отримання 19 24 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 55 60 Суміш етил 1-оксо-1,2,5,6,7,8-гексагідро-5,8-метаноізохінолін-4-карбоксилату (2,04 мг) і оксихлориду фосфору (12 мл) перемішують протягом години при 100 °C. Реакційний розчин концентрують при зниженому тиску, до залишку додають водний розчин гідрокарбонату натрію, потім екстрагують етилацетатом. Органічний шар промивають насиченим розчином солі і сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують з отриманням етил 1-хлор-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-карбоксилату (1,75 г) у вигляді коричневої твердої речовини. Приклад отримання 20 Суміш етил 1-хлор-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-карбоксилату (674 мг), 3(трифтометил)аніліну (1 мл) і 1-метил-2-піролідону (3,4 мл) перемішують протягом 12 годин при 180 °C. До реакційної суміші додають воду, потім екстрагують етилацетатом. Органічний шар промивають насиченим розчином солі і сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують, і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням етил 1-{[3-(трифторметил)феніл]аміно}5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-карбоксилату (1,0 г) у вигляді жовтої твердої речовини. Приклад отримання 21 Суміш етил 1-хлор-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-карбоксилату (700 мг), 3-хлор-4фтораніліну (486 мг), 4М розчину гідрохлориду/діоксану (139 мкл) і N-метилпіролідону (3,5 мл) перемішують протягом 48 годин при 120 °C. До реакційної суміші додають воду, потім екстрагують етилацетатом. Органічний шар промивають насиченим розчином солі і сушать над безводним сульфатом натрію, з подальшою фільтрацією. Отриманий фільтрат концентрують і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням 1-[(3-хлор-4-фторфеніл)аміно]-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-карбоксилату (878 мг) у вигляді білої твердої речовини. Приклад отримання 22 1М водний розчин гідроксиду натрію (6 мл) додають до суміші етил 1-{[3(трифторметил)феніл]аміно}-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-карбоксилату 91,0 г), етанолу (5 мл) і тетрагідрофурану (5 мл), і отриману суміш перемішують протягом 16 годин при кімнатній температурі. Реакційний розчин концентрують при зниженому тиску, до залишку додають воду, і суміш промивають ефіром. До водного шару додають 1М хлористоводневу кислоту доти, поки рН не стане 1, потім екстрагують хлороформом. Органічний шар промивають насиченим розчином солі і сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують і залишок промивають гексаном - етилацетатом (4:1) з отриманням етил 1-{[3-(трифторметил)феніл]аміно}-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4карбонової кислоти (659 мг) у вигляді жовтої твердої речовини. Приклад отримання 23 Біцикло[2.2.2]окта-2-ен (25 г) додають до суміші 3-(метилсульфаніл)-1,2,4-триазину (16.6 г) і толуолу (16.6 мл) з подальшим перемішуванням протягом 18 годин при 180 °C в герметичній закритій трубці. Отриману реакційну суміш очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням 1-(метилсульфаніл)-5,6,7,8-тетрагідро-5,8-метаноізохіноліну (10,4 г) у вигляді блідо-жовтого масла. Приклад отримання 24 Періодат натрію (12 г) додають до суміші 1-(метилсульфаніл)-5,6,7,8-тетрагідро-5,8етаноізохіноліну (10,4 г), тетрагідрофурану (40 мл), метанолу (40 мл) і води (40 мл) при охолоджуванні на льоду з подальшим перемішуванням протягом 15 годин при 50 °C. Після відділення нерозчинного продукту фільтрацією, органічний розчинник випаровують при зниженому тиску, і водний шар, що залишився, екстрагують етилацетатом. Органічний шар промивають водою і насиченим розчином солі і сушать над безводним сульфатом магнію з подальшою фільтрацією. Отриманий фільтрат концентрують з отриманням 1-(метилсульфініл)5,6,7,8-тетрагідро-5,8-етаноізохіноліну (8,05 г) у вигляді блідо-жовтого масла. Приклад отримання 25 2,2'-Біс(дифенілфосфіно)-1,1'-ібінафтил (205 мг), трет-бутоксиду натрію (794 мг) і трис(дибензиліденацетон)дипаладію (76 мг) додають до суміші 4-бром-1-метокси-5,6,7,8тетрагідроізохіноліну (1 г), 3-хлораніліну (518 мкл) і толуолу (15 мл) з подальшим перемішуванням протягом 16 годин при 100 °C в атмосфері аргону. До реакційного розчину додають насичений розчин солі, нерозчинний продукт відділяють фільтрацією, і потім фільтрат екстрагують етилацетатом. Органічний шар сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням N-(3-хлорфеніл)-1метокси-5,6,7,8-тетрагідроізохінолін-4-аміну (1,02 г) у вигляді червонувато-коричневого масла. 25 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклад отримання 26 Йодид калію (1,76 г) і хлорид триметисилілу (1,34 мл) додають до суміші N-(3-хлорфеніл)-1метокси-5,6,7,8-тетрагідроізохінолін-4-аміну (1,02 г) і ацетонітрилу (10 мл) з подальшим перемішуванням протягом 18 годин при 70 °C. До реакційного розчину додають воду, і отриману тверду речовину збирають фільтрацією і промивають етилацетатом. Потім отриманий продукт сушать при зниженому тиску з отриманням 4-[(3-хлорфеніл)аміно]-5,6,7,8-тетрагідроізохінолін1(2Н)-ону у вигляді білої твердої речовини. Фільтрат концентрують, і осад очищають хроматографією на колонці з силікагелем (метанол-хлороформ) і змішують з твердою речовиною, отриманою раніше, з отриманням 4-[(3-хлорфеніл)аміно]-5,6,7,8тетрагідроізохінолін-1(2Н)-ону (792 мг) у вигляді білої твердої речовини. Приклад отримання 27 Суміш 4-[(3-хлорфеніл)аміно]-5,6,7,8-тетрагідроізохінолін-1(2Н)-ону (792 мг) і оксихлориду фосфору (3 мл) перемішують протягом 20 годин при 120 °C. Потім реакційний розчин концентрують, до залишку додають воду, потім екстрагують етилацетатом. Органічний шар промивають насиченим розчином солі і сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням 1-хлор-N-(3-хлорфеніл)-5,6,7,8тетрагідроізохінолін-4-аміну (187 мг) у вигляді жовтого масла. Приклад отримання 28 Ціанід цинку (150 мг), дифенілфосфінофероцен (18 мг) і трис(дибензиліденацетон)дипаладію (15 мг) додають до суміші 1-хлор-N-(3-хлорфеніл)-5,6,7,8тетрагідроізохінолін-4-аміну (187 мг) і N-метилпіролідону (3 мл) з подальшим перемішуванням протягом 18 годин при 120 °C в атмосфері аргону. Воду додають до реакційного розчину, нерозчинний матеріал відділяють фільтрацією і потім фільтрат екстрагують етилацетатом. Органічний шар промивають насиченим розчином солі і сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням 4-[(3хлорфеніл)аміно]-5,6,7,8-тетрагідроізохінолін-1-карбонітрилу (99 мг) у вигляді блідо-жовтої твердої речовини. Приклад отримання 29 Водний розчин гідроксиду натрію (15 % маси, 3 мл) додають до суміші 4-[(3хлорфеніл)аміно]-5,6,7,8-тетрагідроізохінолін-1-карбонітрилу (98 мг) і етанолу (2 мл), і суміш перемішують протягом 2 днів при 80 °C. Реакційний розчин охолоджують до 0 °C і додають 1М хлористоводневу кислоту до того як рН стане 3. Отриману тверду речовину збирають фільтрацією, промивають водою і потім сушать при зниженому тиску з отриманням 4-[(3хлорфеніл)аміно]-5,6,7,8-тетрагідроізохінолін-1-карбонової кислоти (80 мг) у вигляді блідожовтої твердої речовини. Приклад отримання 30 Карбонат цезію (2,02 г), N, N-диметилгліцину (160 мг) і йодиду міді (98 мг) додають до суміші 4-бром-1-метокси-5,6,7,8-тетрагідроізохіноліну (500 мг), 3-(трифторметил)фенолу (369 мкл) і діоксану (7,5 мл), і отриману суміш перемішують протягом 3 днів при 100 °C в атмосфері аргону. Воду додають до реакційного розчину, потім екстрагують етилацетатом. Органічний шар промивають насиченим розчином солі і сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують, і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням 1-метокси-4-[3(трифторметил)фенокси]-5,6,7,8-тетрагідроізохіноліну (278 мг) у вигляді блідо-жовтого твердого масла. Приклад отримання 31 В атмосфері аргону суміш 3-хлорбензолтіолу (480 мкл) і діоксану (2 мл) додають до суміші 4-бром-1-метокси-5,6,7,8-тетрагідроізохіноліну (1 г), трет-бутоксиду натрію (595 мг), біс[2(дифенілфосфіно)фенілового]ефіру (133 мг), ацетату паладію (46 мг) і діоксану (8 мл) при кімнатній температурі з подальшим перемішуванням протягом 25 годин при 100 °C. До реакційного розчину додають воду, потім екстрагують етилацетатом. Органічний шар промивають насиченим розчином солі і сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують, і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням 4-[3-(хлорфеніл)сульфаніл]-1-метокси5,6,7,8-тетрагідроізохіноліну (628 мг) у вигляді безбарвного масла. Приклад отримання 32 Реагент Лавесона (620 мг) додають до суміші 4-бром-5,6,7,8-тетрагідроізохінолін-1(2Н)-ону (500 мг) і толуолу (20 мл) з подальшим перемішуванням протягом 4 годин при 130 °C в 26 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 55 60 атмосфері аргону. Після концентрації реакційного розчину залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) і потім промивають етилацетатом-гексаном (1:1) з отриманням 4-бром-5,6,7,8-тетрагідроізохінолін-1(2Н)-тіону (314 мг) у вигляді жовтої твердої речовини. Приклад отримання 33 10 % водний розчин гідрохлориту натрію (2 мл) по краплях додають до суміші 4-бром5,6,7,8-тетрагідроізохінолін-1(2Н)-тіону (150 мг), дихлорметану (2 мл), води (2 мл) і концентрованої хлористоводневої кислоти (600 мкл) протягом 5 хвилин при охолоджуванні на льоду і енергійному перемішуванні з подальшим перемішуванням протягом ще 45 хвилин. Реакційний розчин екстрагують дихлорметаном, і органічний шар промивають насиченим розчином солі і сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують з отриманням неочищеного продукту хлориду 4-бром-5,6,7,8тетрагідроізохінолін-1-сульфонілу. Суміш отриманого неочищеного продукту хлориду 4-бром5,6,7,8-тетрагідроізохінолін-1-сульфонілу і дихлорметану 92 мл) по краплях додають до суміші морфоліну (80 мкл), триетиламіну (257 мкл) і дихлорметану (2 мл) при охолоджуванні на льоду з подальшим перемішуванням протягом 18 годин при кімнатній температурі. Насичений водний розчин гідрокарбонату натрію додають до реакційного розчину з подальшим екстрагуванням хлороформом. Органічний шар промивають насиченим розчином солі і сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують, і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням 4-бром1-(морфолін-4-ілсульфоніл)-5,6,7,8-тетрагідроізохіноліну (131 мг) у вигляді білої твердої речовини. Приклад отримання 34 2,2'-Біс(дифенілфосфіно)-1,1'-бінафтил (126 мг), трет-бутоксид натрію (486 мг) і трис(дибензиліденацетон)дипаладію (46 мг) додають до суміші 4-бром-1-метокси-5,6,7,8тетрагідро-5,8-метаноізохіноліну (642 мг), 3-(трифторметокси)аніліну (388 мкл) і толуолу (10 мл) з подальшим перемішуванням протягом 16 годин при 100 °C в атмосфері аргону. До реакційного розчину додають насичений розчин солі, нерозчинний продукт відділяють фільтрацією, і фільтрат екстрагують етилацетатом. Органічний шар сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують, і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням 1метокси-N-[3-(трифторметокси)феніл]-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-аміну (839 мг) у вигляді червонувато-коричневої твердої речовини. Приклад отримання 35 Йодид натрію (896 мг) і хлориду триметилсилілу (756 мкл) додають до суміші 1-метокси-N[3-(трифторметокси)феніл]-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-аміну (838 мг) і ацетонітрилу (10 мл), і отриману суміш перемішують протягом ночі при 60 °C. До реакційного розчину додають водний розчин гідрокарбонату натрію, потім екстрагують етилацетатом. Органічний шар промивають насиченим розчином солі і сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують, і залишок очищають хроматографією на колонці з силікагелем (метанол-хлороформ) з отриманням 4-{[3(трифторметокси)феніл]аміно}-5,6,7,8-тетрагідро-5,8-метаноізохінолін-1(2Н)-ону (613 мг) у вигляді білої твердої речовини. Приклад отримання 36 Трифторметансульфоновий ангідрид (337 мкл) додають до суміші 4-{[3(трифторметокси)феніл]аміно}-5,6,7,8-тетрагідро-5,8-метаноізохінолін-1(2Н)-ону (613 мг), піридину (2 мл) і дихлорметану (6 мл) при охолоджуванні на льоду з подальшим перемішуванням протягом години. Реакційний розчин концентрують і до залишку додають етилацетат і насичений водний розчин гідрокарбонату натрію, потім екстрагують етилацетатом. Органічний шар промивають насиченим розчином солі і сушать над безводним сульфатом натрію з подальшою фільтрацією. До отриманого фільтрату додають толуол і фільтрат концентрують. Цю процедуру повторюють три рази з отриманням трифторметансульфонату 4{[3-(трифторметокси)феніл]аміно}-5,6,7,8-тетрагідро-5,8-метаноізохінолін-1-ілу (850 мг) у вигляді коричневого масла. Приклад отримання 37 Ацетат паладію (20 мг), дифенілфосфінофероцен (50 мг) і триетиламін (759 мкл) додають до суміші трифторметансульфонату 4-{[3-(трифторметокси)феніл]аміно}-5,6,7,8-тетрагідро-5,8метаноізохінолін-1-ілу (850 мг), етанолу (4 мл) і N, N-диметилформаміду (8 мл) з подальшим перемішуванням протягом 14 годин при 100 °C в атмосфері окислу вуглецю. До реакційної суміші додають воду, потім екстрагують етилацетатом. Органічний шар промивають водою і 27 UA 109550 C2 5 10 15 20 25 30 35 40 45 50 55 насиченим розчином солі і сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують, залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням етил 4-{[3-(трифторметокси)феніл]аміно}-5,6,7,8тетрагідро-5,8-метаноізохінолін-1-карбоксилату (665 мг) у вигляді білої твердої речовини. Приклад отримання 38 Водний розчин гідроксиду натрію (15 % мас., 3 мл) додають до суміші етил 4-{[3(трифторметокси)феніл]аміно}-5,6,7,8-тетрагідро-5,8-метаноізохінолін-1-карбоксилату (660 мг) і етанолу (8 мл) з подальшим перемішуванням протягом 3 годин при 60 °C. Після випаровування етанолу в реакційному розчині водний розчин, що залишився, охолоджують до 0 °C і додають 1М хлористоводневу кислоту доти, поки рН не стане дорівнювати 3. Потім додають хлорид натрію для насичення розчину, потім екстрагують сумішшю метанолу-хлороформу (1:10). Органічний шар сушать над безводним сульфатом натрію з подальшою фільтрацією і концентрацією з отриманням 4-{[3-(трифторметокси)феніл]аміно}-5,6,7,8-тетрагідро-5,8метаноізохінолін-1-карбонової кислоти (605 мг) у вигляді блідо-жовтої твердої речовини. Приклад отримання 39 Концентровану хлористоводневу кислоту (3 мл) додають до суміші 1-метокси-N-(3метоксифеніл)-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-аміну (526 мг), діоксану (1 мл) і води (1 мл) з подальшим перемішуванням протягом 36 годин при 100 °C. Водний розчин гідроксиду натрію (15 % мас.) додають до реакційного розчину доти, поки рН не стане 9, і отриману тверду речовину збирають фільтрацією і промивають водою і етилацетатом з отриманням 4-[(3тметоксифеніл)аміно]-5,6,7,8-тетрагідро-5,8-метаноізохінолін-1(2Н)-ону (407 мг) у вигляді білої твердої речовини. Приклад отримання 40 Суміш етил 1-оксо-1,2,5,6,7,8-гексагідро-5,8-метаноізохінолін-4-карбоксилату (171 мг) і оксихлориду фосфору (1,3 мл) перемішують протягом 3 годин при 110 °C. Реакційний розчин концентрують при зниженому тиску, до залишку додають толуол, і операцію азеотропної перегонки повторюють три рази. До залишку додають водний розчин гідрокарбонату натрію, потім екстрагують етилацетатом. Органічний шар промивають насиченим розчином солі і сушать над сульфатом натрію з подальшою фільтрацією і концентрацією. До отриманого жовтого масла додають 3-хлоранілін (77 мкл) і N-метилпіролідон (1,5 мл) з подальшим перемішуванням протягом 7 годин при 180 °C. До реакційної суміші додають воду, потім екстрагують етилацетатом. Органічний шар промивають насиченим розчином солі і сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують, і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням 1-{[3-хлорфеніл]аміно}-5,6,7,8-тетрагідро-5,8-метаноізохінолін-4-карбоксилату (262 мг) у вигляді блідо-жовтої твердої речовини. Приклад отримання 41 2,2'-Біс(дифенілфосфіно)-1,1'-бінафтил (118 мг), трет-бутоксид натрію (459 мг) і трис(дибензиліденацетон)дипаладію (43 мг) додають до суміші 4-бром-1-метокси-5,6,7,8тетрагідро-5,8-метаноізохіноліну (599 мг), 3-(трифторметил)аніліну (330 мкл) і толуолу (2 мл) з подальшим перемішуванням протягом 30 хвилин при 150 °C при обробці мікрохвилями в атмосфері аргону. До реакційного розчину додають насичений розчин солі, нерозчинний продукт відділяють фільтрацією, і фільтрат екстрагують етилацетатом. Органічний шар сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують, і залишок очищають хроматографією на колонці з силікагелем (гексанетилацетат) з отриманням 1-метокси-N-[3-(трифторметил)феніл]-5,6,7,8-тетрагідро-5,8метаноізохінолін-4-аміну (818 мг) у вигляді жовтого масла. Приклад отримання 42 Гідрохлорид 1,3-біс(2,6-діізопропілфеніл)-1Н-імідазол-3-ію (459 мг), ацетат паладію(II) (113 мг) і трет-бутоксид натрію (809 мг) додають до суміші 4-бром-1-метокси-5,6,7,8-тетрагідро-5,8метаноізохіноліну (1,5 г), ацетату 3-аміноадамантан-1-ілу (1,40 г) і толуолу (10 мл) з подальшим перемішуванням протягом 30 хвилин при 150 °C при опроміненні мікрохвилями в атмосфері аргону. До реакційного розчину додають насичений розчин солі, нерозчинний продукт відділяють фільтрацією, і фільтрат екстрагують етилацетатом. Органічний шар сушать над безводним сульфатом натрію з подальшою фільтрацією. Отриманий фільтрат концентрують, і залишок очищають хроматографією на колонці з силікагелем (гексан-етилацетат) з отриманням ацетату 3-[1-метокси-5,6,7,8-тетрагідро-5,8-етаноізохінолін-4-іл)аміно]адамантан-1-ілу (776 мг) у вигляді коричневої піни. Приклад отримання 43 28
ДивитисяДодаткова інформація
Назва патенту англійськоюCondensed ring pyridine compound
Автори англійськоюMatsushima, Yuji, Kameda, Minoru, Honda, Shugo, Sugano, Yukihito, Usuda, Hiroyuki, Terasaka, Tadashi, Terasawa, Takeshi, Nishigaki, Fusako
Автори російськоюМацусима Юдзи, Камеда Минору, Хонда Суго, Сугано Юкихито, Усуда Хироюки, Тарасака Тадаси, Терасава Такеси, Нисигаки Фусако
МПК / Мітки
МПК: A61P 29/00, A61K 31/541, C07D 237/34, A61K 31/4725, A61P 25/04, A61K 31/553, C07D 401/12, C07D 495/04, A61P 43/00, C07D 413/12, A61K 31/5377, C07D 217/26, C07D 405/12
Мітки: піридину, конденсовані, циклічні, сполуки
Код посилання
<a href="https://ua.patents.su/144-109550-kondensovani-ciklichni-spoluki-piridinu.html" target="_blank" rel="follow" title="База патентів України">Конденсовані циклічні сполуки піридину</a>
Попередній патент: Стійкі до розчинників поліамідні нанофільтраційні мембрани
Наступний патент: Пантенолу докозагексаєноат і його застосування для лікування і попередження серцево-судинних захворювань
Випадковий патент: Індикатор справності свічок розжарювання дизельного двигуна