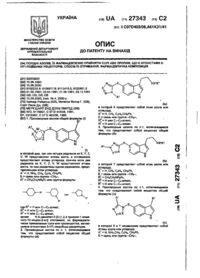
Похідні оксазолідинону, спосіб їх отримання, фармацевтична композиція та спосіб її отримання
Номер патенту: 54367
Опубліковано: 17.03.2003
Автори: Вурцігер Ханнс, ФІТТШЕН Клаус, Мельцер Гвідо, Раддатц Петер, Юрасцук Хорст, Віснер Маттіас, Ганте Йоахім, Бернотат-Даніловські Сабіне
Формула / Реферат
1. Производные оксазолидинона формулы I
, I
где
R1 означает амидинофенил,
R2 означает Н, А, С1-С10-алканоил, C1-C8-алкоксикарбонил, бензоил, нафтоил, С1-С6-алкилсульфонил, бензилсульфонил или монозамещенный C1-С6-алкилом фенилсульфонил,
R3 означает водород или С1-С6-алкил,
А означает алкил с 1-16 С-атомами,
а также их физиологически приемлемые соли.
2. Производные оксазолидинона формулы I по п. 1, отличающиеся тем, что представляют собой:
(a) 3-п-амидино-фенил-5-[п-(2-амино-2-карбокси-этил)-фенокси-метил]-оксазолидин-2-он,
(b) 3-п-амидино-фенил-5-[п-(2-амино-2-метоксикарбонилэтил)-фенокси-метил]-оксазолидин-2-он,
(c) 3-п-амидино-фенил-5-[п-(2-N-бутилсульфонил-амино-2-карбокси-этил)-фенокси-метил]-оксазолидин-2-он,
(d) 3-п-амидино-фенил-5-[п-(2-N-п-толуолсульфонил-амино-2-карбокси-этил)-фенокси-метил]-оксазолидин-2-он;
(е) 3-п-амидино-фенил-5-[п-(2-N-бутилсульфонил-амино-2-метоксикарбонил-этил)-фенокси-метил]-оксазолидин-2-он,
а также их физиологически приемлемые соли.
3. Способ получения соединений формулы I согласно пункту 1, отличающийся тем, что соединение формулы I выделяют из его функционального производного, содержащего соответствующие защищенные амино и/или гидроксигруппы, путем обработки сильной кислотой, возможно в присутствии инертного растворителя, или гидрогенолитически и полученное соединение переводят, в случае необходимости, в одну из его солей путем обработки кислотой или основанием.
4. Способ получения соединений формулы I согласно пункту 1, отличающийся тем, что соединение формулы II
, ІІ
где
R1 имеет значение, указанное в пункте 1,
Ζ - реакционноспособная этерифицированная группа ОН,
вводят во взаимодействие с соединением формулы III
, ІІІ
где
X означает OH или его соль,
R2 и R3 имеют указанные в п. 1 значения, и возможно соединение формулы I переводят в одну из его солей путем обработки кислотой или основанием.
5. Производные оксазолидинона формулы I по п. 1, отличающиеся тем, что их используют в качестве адгезионнорецепторных антагонистов.
6. Способ получения фармацевтической композиции, обладающей антагонистической активностью в отношении рецепторов адгезии, отличающийся тем, что соединение формулы I по пункту 1 и/или одну из его физиологически приемлемых солей вместе, по меньшей мере, с твердым, жидким или полужидким носителем или вспомогательным веществом переводят в пригодную для приема форму.
7. Фармацевтическая композиция, обладающая антагонистической активностью в отношении рецепторов адгезии, отличающаяся тем, что в качестве активного вещества она содержит эффективное количество, по меньшей мере, одного соединения формулы I по пункту 1 и/или одной из его физиологически приемлемых солей.
Текст
1 Производные оксазолидинона формулы І оксазолидин-2-он, а также их физиологически приемлемые соли 3 Способ получения соединений формулы I согласно пункту 1, отличающийся тем, что соединение формулы I выделяют из его функционального производного, содержащего соответствующие защищенные амино и/или гидроксигруппы, путем обработки сильной кислотой, возможно в присутствии инертного растворителя, или гидрогенолитически и полученное соединение переводят, в случае необходимости, в одну из его солей путем обработки кислотой или основанием 4 Способ получения соединений формулы I согласно пункту 1, отличающийся тем, что соединение формулы II R R1 N \ КОМПОЗИЦІЯ ТА l N о о Л> о R означает амидинофенил, R2 означает Н, А, С-і-С-ю-алканоил, C-i-Csалкокси карбон ил, бензоил, нафтоил, С-і-Сєалкилсульфонил, бензилсульфонил или монозамещенный СгСб-алкилом фенилсульфонил, R3 означает водород или Сі-Сє-алкил, А означает алкил с 1-16 С-атомами, а также их физиологически приемлемые соли 2 Производные оксазолидинона формулы І по п 1, отличающиеся тем, что представляют собой (a) 3-п-амидино-фенил-5-[п-(2-амино-2-карбоксиэтил)-фенокси-метил]-оксазолидин-2-он, (b) 3-п-амидино-фенил-5-[п-(2-амино-2метоксикарбонилэтил)-фенокси-метил]оксазолидин-2-он, (c) 3-п-амидино-фенил-5-[п-(2-г\І-бутилсульфониламино-2-карбокси-этил)-фенокси-метил]оксазолидин-2-он, (d) 3-п-амидино-фенил-5-[п-(2-Ы-птолуолсульфонил-амино-2-карбокси-этил)фенокси-метил]-оксазолидин-2-он, (є) 3-п-амидино-фенил-5-[п-(2-г\І-бутилсульфониламино-2-метоксикарбонил-этил)-фенокси-метил] А R имеет значение, указанное в пункте 1, Z - реакционноспособная этерифицированная группа ОН, вводят во взаимодействие с соединением формулы III coo где X означает ОН или его соль, R2 и R3 имеют указанные в п 1 значения, и возможно соединение формулы I переводят в одну из его солей путем обработки кислотой или основанием 5 Производные оксазолидинона формулы І по п 1, отличающиеся тем, что их используют в качестве адгезионнорецепторных антагонистов 6 Способ получения фармацевтической композиции, обладающей антагонистической активностью в отношении рецепторов адгезии, отличающийся тем, что соединение формулы I по пункту 1 и/или 1 (О го ю З 54367 одну из его физиологически приемлемых солей антагонистической активностью в отношении ревместе, по меньшей мере, с твердым, жидким или цепторов адгезии, отличающаяся тем, что в каполужидким носителем или вспомогательным вечестве активного вещества она содержит эффекществом переводят в пригодную для приема тивное количество, по меньшей мере, одного форму соединения формулы I по пункту 1 и/или одной из 7 Фармацевтическая композиция, обладающая его физиологически приемлемых солей Изобретение касается новых производных оксазолидинона формулы I (I) где R означает —V h о или R2 Н, А, Ас, A-SO2-, Ar-SO2- или аминозащитную группу, если она имеется, R3 Н, А, циклоалкил с 3-7 атомами С, Аг или Ar-(CH2)k -, А алкил с 1-46 атомами С, В Н,А или H2N-C(=NH)-, N2H-CH2-, H2N-C(=NH)- или H2-N-C(=NH)-NHСН2, причем первичные аминогруппы могут также иметь аминозащитные группы, Ас алканоил с 1-10 атомами С или ароил с 711 атомами С, Аг незамещенный или моно и/или дизамещенный A, CI, Вг, I, ОА, ОН, NO2, CN, ИН2, NHA или NA2 фенил или бензил, m 0, 1, 2, 3 или 4, п 2, 3 или 4, и к 1, 2, 3 или 4, а также их физиологически переносимых солей Аналогичные соединения известны из описания изобретения - ЕР-АІ-0 381 033 В основу изобретения положена задача найти новые соединения с ценными свойствами, в частности, такие, которые могут быть использованы для получения лекарственных средств Эта задача была решена с помощью изобретения Было обнаружено, что соединения формулы I, а также их сольваты и соли при хорошей переносимости обладают ценными фармакологическими свойствами Прежде всего, они действуют как интегрин-ингибиторы, при этом они, в частности, тормозят взаимодействие рецепторов Рз - или Рб, - интегрина с лигандами Особую эффективность соединения обнаруживают в случае интегринов и аурз, avPs, ацєРз Эта активность может быть, например, доказана по методу, который описывается J W Smith et al Biol Chem 2205,12267-12271 В частности, они тормозят связывание фибриногенов, фибронектина и фактора фон Виллебранда с фибриногенным ре цептором кровяных пластинок (гликопротеин llb/llla), а также связывание их и других адгезивных протеинов, таких как витронектин, коллаген и ламинин, с соответствующими рецепторами на поверхности различных типов клеток Таким образом, эти соединения влияют на взаимодействие типа клетка-клетка и клетка-матрица Они, в частности, предотвращают возникновение тромбов кровяных пластинок и поэтому могутприменяться для лечения тромбов, апоплексии, сердечного инфаркта, ангины ресішіз.остео-литических заболеваний, в частности, остеопороза, антиангиогенеза и рестеноза после ангиопластии, ишемии, воспалений, артериосклероза и острой почечной недостаточности Далее, соединения оказывают эффективное воздействие на раковые клетки, одерживал образование метастазов Таким образом, они могут также использоваться в качестве антиракового средства Имеются показания, что раковые клетки через микротромбы попадают в сосуды и, таким образом, защищают себя от обнаружения клетками иммуносистемы Микротромбы способствуют также привязыванию раковых клеток к стенкам сосудов Так как образование микротромбов находится во взаимосвязи с фибриногеннои привязанностью к фибриногенному рецептору (гликопротеин ПЬ/ш а), то ингибиторы фибриногеннои связи считаются также ингибиторами метастазов Соединения пригодны также в качестве антимикробных активных веществ, которые могут препятствовать развитию инфекций таких, например, которые вызваны бактериями, грибком или дрожжами Эти вещества можно давать, поэтому, предпочтительным образом, в качестве сопутствующих антимикробных активных веществ, если предпринимаются воздействия на организм, при которых используются вещества, чуждые организму, такие, как, например, биоматериалы, имплантаты, катетеры или стимуляторы сердца Они действуют как антисептические средства Антимикробная активность соединений может быть, например, доказана методом Р Valentin -Weigand et al который описан в Infection and Immunity, 28512855(1988) Другие свойства соединений могут быть определены по методике, описанной в описании изобретения ЕР-АІ-0 462 960 Торможение фибринной связи с фибриногенным рецептором может быть доказано по методике, указанной в описании изобретения ЕР-АІ-0 381 033 Действие подавления агрегации тромбоцитов может быть определено в лабораторных условиях по методике Борна (Natyre 4832, 927-929, 1962) Далее, предметом изобретения является спо 54367 соб получения соединения указанной формулы I, а также его солей, отличающийся тем, что а) соединение формулы I освобождают из одного из его функциональных производных путем обработки сольволизирующим или гидрогенолизирующим средством, или что б) соединение формулы II (II) где Z означает СІ, Вг, I, ОН или реакционноспособную этерифицированную ОН-группу, и R1 имеет указанное выше значение, вводят в реакцию взаимодействия с соединением формулы (III) где Л з R H R имеют указанные значения, а X означает ОН или остаток, образованный из ОН по типу соли, или что (в) соединение формулы IV (IV) где д1 R1, R2 и R3 имеет указанные выше значения, вводят в реакцию взаимодействия с реакционноспособным производным угольной кислоты, или что (г) соединена формулы V (V) где 'Ч 3 R и R имеют указанные значения, вводят во взаимодействие с соединением формулы VI «О где В имеет указанное значение» и У означает -8G яш )п -(С%)„ - X , где тип имеют уже указанные значения, а Xі означает CI, Вг, I иди другую легко нуклеофильно вытесняемую отходящую группу, (д) для получения гуанидинометильного соединения формулы I (R = фенильный остаток, однократно замещенный группой H2N-C(=NH)-NHСН2 -) аминное соединение, соответствующее формуле I, которое содержит, однако, вместо остатка R1 аминометилфенильную группу, обрабатывают амидинирующим средством, или что 6 3 (е) один остаток R превращают в другой ос3 таток R путем омыления сложного эфира формулы I, или карбоновую кислоту формулы I подвергают этерификации, или что 1 2 (ж) остаток (остатки) R и/или R превращают в 1 2 другой остаток (другие остатки) R и/или R , и/или что (з) соединение формулы I переводят в одну из его солей путем обработки кислотой или основанием Соединения формулы I обладают, по меньшей мере, одним хиральным центром и могут, поэтому, выступать в нескольких энантиомерных формах Все эти формы (например» формы D и L) и их смеси (например, формы OL ) включены в формулу I Выше и ниже остатки или соответственно параметры А, В, D, X, Y, R1-R3, Ac, Аг, К, т и п имеют значения, указанные в формулах I - VI, если четко не указано что-либо другое Если в молекуле имеются несколько одинаково обозначенных групп, то они могут независимо друг от друга принимать различные определения В вышеуказанных формулах группа А имеет 16, предпочтительно 1, 2, 3 или 4 атома С В частности, А означает предпочтительно метил, атил, пропил, изопропил, бутил, изобутил, вторичный бутил или третичный бутил, далее, также пентил, 1-, 2- иди 3-метидбутил, 1,1-, 1,2- или 2,2диметилпропил, 1-этилпропил, гексил, 1-, 2-, 3или 4-метил-пентил R1 является, предпочтительно фенильным остатком, замещенным в 4-ом положении, но также и во 2-ом или в Зем положении, в особенности, предпочтительно 2-, 3- или (в особенности) 4аминометилфенилом, 2-, 3- или (в особенности) 4амидофенил, 2-, 3- или 4-гуадинометилфенил, причем во всех случаях первичные аминогруппы могут иметь также аминозащитные группы Далее, R1 является также, предпочтительным образом, 4пиперидидьным, 4-пиперидилметильным, 4пиперидилэтильным, 1-амидино-4пиперид ильным, 1-амидино-4пиперидилметильным, 4-пиперазинилэтильным, 4пиперазинилпропильным, 4пиперазинилбутильным, 1-амидино-4пиперазинилэтильным или 1-амидино-4пиперазинилпропильным остатком 2 R представляет предпочтительно водород, метил, этил, метилсульфонил, этилсульфонил, нпропилсульфонил или н-бутилсульфонил, толуолсульфонил или аминозащитную группу, если она имеется R3 является предпочтительно водородом, метилом или этилом Аг является предпочтительно незамещенным фенилом или 4-метилфенилом, Ас означает, предпочтительно алканоил с 1-6 атомами С, как, например, формил, ацетил, пронионил, бутирил, изобутирил, валерил или капроил, далее, бензоил, толуил, 1- или 2-нафтоил или фенил ацетил Параметры к и т означают, предпочтительно О или 1 Параметр п - это, предпочтительно 2 или 3 Среда соединений формулы I предпочтительными являются те, в которых, по меньшей мере, 54367 один из указанных остатков, одна из указанных групп и/или один их указанных параметров имеет одно из указанных предпочтительных значений Некоторые группы предпочтительных соединений - это те из формуя 1а - If, которые соответствуют формуле I, где, однако, 1 в la R означает амидинофенил, 1 в 1 б R означает амидинофенил и 2 R означает водород, 1 в їв R означает аминометилфенил и 3 R означает водород или метил, 1 в Іг R означает амидинофенил и 3 R означает водород или метил, 1 в Ід R означает пиперидилметил и пиперидилэтил и 2 R означает водород или -A- SO2-, 1 le R означает 1 -амидинопиперидилметил и R2 означает водород или A- SO2-, їж R1 означает пиперазиноэтил или пиперазинопропил и R2 означает водород или A- SO2-, Із R1 означает i-амидинопиперазиноэтил или Iамидинопиперазинопропил и R2 означает водород или A- SO2 Соединения формулы 1, а также исходные вещества для их получения получают обычно по известным методикам, которые описаны в литературе (например, в Houben - Wey 1, Методы органической химии, издательство Georg - Thieme, Штуттгарт далее, описание изобретения - ЕР-АІ-0 381 033, ЕР-АІ-0 462 960), а именно, в условиях реакции, которые известны и пригодны для названных реакций обмена При этом можно использовать также сами по себе известные варианты, которые здесь более подробно не упоминаются Исходные вещества можно получать, при желании, in situ так что затем их не надо выделять из реакционной смеси, а можно вводить сразу же в реакцию обмена с образованием соединений формулы I Соединения формулы I могут быть получены путем их выделения из их функциональных производных путем сольволиза, в частности, гидролиза или гидрогенолиза Предпочтительными исходными веществами для сольволиза или соответственно гидрогенолиза являются такие вещества, которые обычно соответствуют формуле I, но вместо одной или нескольких свободных амино- и/или гидроксигрупп содержат соответствующие защищенные аминои/или гидроксигруппы, предпочтительным образом, такие, которые вместо атома Н, связанного с атомом N, несут аминозащитную группу, в частности, такие, которые вместо группы HN несут группу R'-N, где R' означает аминозащитную группу, и/или такие, которые вместо атома Н гидроксигруппы несут гидроксизащитную группу например, такие, которые соответствуют формуле I, однако вместо группы -СООН несут группу -COOR", где R" означает гидроксизащитную группу В молекуле исходного вещества могут также присутствовать несколько - одинаковых или разных - защищенных амино-и/или гидроксигрупп Если имеющиеся защитные группы отличаются друг от друга, то они могут во многих случаях селективно отщепляться 8 Выражение "аминозащитная группа" является общеизвестным и относится к группам, которые пригодны для защиты (блокирования) аминогруппы от химических превращений, но которые, к тому же, могут легко быть удалены, после того, как желаемая химическая реакция прошла на другом месте молекулы Типичными для таких групп являются, в частности, незамещенные или замещенные ацильные, арильные (например, 2,4динитрофенил, (DNP)), аралкоксиметильные (например, бензоилоксиметил (ВОМ)) или аралкильные (например, 4-нитро-бензил, трифенилметил) группы Так как аминозащитные группы удаляются после проведения желаемой реакции (или серии реакций), то их вид и размер, в общем, не являются критическими предпочтительными являются, однако, такие группы с 1-20, в частности, 1-8 атомами С Выражение "ацильная группа" следует воспринимать в связи с настоящим способом в самом широком смысле Оно включает ацильные группы, производные от алифатических, аралифатических, ароматических или гетероциклических карбонових кислот или сульфоновых кислот, а также, в частности, алкоксикарбонильные, арилоксикарбонильные и, прежде всего, аралкоксикарбонильные группы Примерами таких ациловых групп являются алканоил, такой как - ацетил, пропионил, бутирил, аралканоил, такой как -фенил ацетил, ароил, такой как - бензоил или толуил, арилоксиалканоил, такой как - феноксиацетил, ал кокси карбон ил, такой как - метоксикарбонил, этоксикарбонил, 2,2,2-трихворэтоксикарбонил, изопропоксикарбонил, трет-бутоксикарбонил (ВОС), 2-йодэтоксикарбонил, аралкилоксикарбонил, такой как -бензилоксикарбонил (CBZ), 4метоксибензилоксикарбонил, 9фторенил метоксикарбонил (FMOC) Предпочтительными защитными группами являются ВОС, DNP и ВОМ, далее CBZ, бензил и ацетил Выражение "гидроксизащитная группа" является также общеизвестным и относится к группам, которые пригодны для защиты гидроксигруппы от химических превращений, но которые могут быть легко удалены, после того, как желаемая химическая реакция прошла на другом месте молекулы Типичными для таких групп являются названные выше незамещенные иди замещенные арильные, аралкильные или ацильные группы, далее также алкильные группы Природа и размер гидроксизащитных групп не являются критическими, так как после завершения желаемой химической реакции иди последовательности реакций они вновь подлежат удалению, предпочтительными являются группы с 1-20, в частности, с 1-10 атомами С Примерами гидроксизащитных групп являются, кроме того, трет-бутил, бензил, р-нитробензоил, р-толуолсульфонил и ацетил, причем особое предпочтение отдается бензилу и ацетилу Используемые в качестве исходных веществ функциональные производные соединений формулы 1 могут быть получены по обычной методике, так как это описано в вышеназванных справочниках и заявках на выдачу патента, например, путем реакции обмена соединений, которые соответствуют формулам II и III, причем, однако, по меньшей мере, одно из этих соединений содержит защитную группу вместо атома Н Высвобождение соединений формулы I из их функциональных производных удается осуществить - в зависимости от использованной защитной группы - например, с помощью сильных шел от, целесообразным образом, с помощью трифторуксусной кислоты или хлорной кислоты, но и с помощью других сильных неорганических кислот, таких как соляная кислота или серная кислота, с помощью сильных органических карбонових кислот, таких как трихлоруксусная кислота, или сульфоновых кислот, таких как бензольная или п толуолсульфоновая кислота Возможно присутствие дополнительного инертного растворителя, но это требуется не всегда В качестве инертного растворителя пригодны, предпочтительно, органические, например, карбоновые кислоты, такие как уксусная кислота, пробой эфир, кактетрагидрофуран или диоксан, амиды, такие как - диметилформамид (DMF), галогенированные углеводороды, такие как дихлорметан, сульфоксиди, такие как - диметилсувьфоксид (DMSO), далее, также спирты, такие как метанол, этанол, или изопропанол, а также вода Далее, могут применяться смеси названных выше растворителей Три фтору ксусная кислота применяется предпочтительно в избыточном количестве без добавления другого растворителя, хлорная кислота - в форме смеси из уксусной кислоты и 70%-ной хлорной кислоты в соотношении 9 1 Реакционные температуры для расщепления лежат, целесообразным образом, в интервале между приблизительно 0 и приблизительно 50°С Работают предпочтительно, в интервале между 15 и 30°С (комнатная температура) Группа ВОС может отщепляться, например, предпочтительно, с помощью трифторуксусной кислоты в дихлорметане или с помощью приблизительно 3-5н НСІ в диоксане при 15-60°С, группа FMOC - с помощью приблизительно 5-20%-ного раствора диметиламина, диэтиламина или пиперидина в DMF при 15-60°С Отщепление группы DNP удается произвести, например, также с помощью приблизительно 3-10%-ного раствора 2меркаптоэтанола в DMF /вода при 15-30°С Защитные группы (например, BOM, CBZ или бензил), которые могут удаляться гидрогенолитически, могут быть, например, удалены путем обработки водородом в присутствии катализатора (например, катализатора благородного металла, как палладий, целесообразным образом, на носителе, таком как уголь) В качестве растворителя пригодны при этом названные выше растворители, в частности, например, спирты, такие как метанол, или этанол, или амиды, такие как DMF Гидрогенолиз проводится, как правило, при температурах между, приблизительно, 0 и 100°С и давлении между, приблизительно, 1 и 200 бар, предпочтительным образом, при 20-30°С и 1-10 бар Гидрогенолиз группы CBZ удается хорошо провести, например, на 5-10%-ном Pd-C в метаноле при 20-30°С Соединения формулы I могут быть получены, предпочтительным образом, также с помощью реакций соединения формулы II с производным фенола формулы III При этом пользуются целе 54367 10 сообразным образом, известными методиками получения простых эфиров Летучая группа Z означает, предпочтительным образом, Cl, Br, I, G r Сє-алкилсульфонилокси, как метан- или этансульфонилокси или Сє - С-юарилсульфонилокси, как бензол-, р-толуол- или 1или 2-нафталинсульфонилокси Реакция протекает предпочтительным образом, в присутствии дополнительного основания, например, гидроксида или карбоната щелочного или щелочноземельного металла, как то - гидроксид натрия, калия или кальция, карбонат натрия, калия или кальция, в инертном растворителе, например, в галогенированном углеводороде, как то - дихлорметан, в простом эфире, как то - TNF или диоксан, в амиде, как то -DMF или диметилацетамид, в нитриле, как то - ацетонитрил, при температурах между приблизительно -10 и 200, предпочтительным образом, между 0 и 120°С Если летучая группа Е отличается от 1, то рекомендуется добавление йодида, такого как йодид калия Исходные вещества формулы II являются, как правило, новыми Они могут быть получены, например, с помощью реакции замещенного анилина формулы R1 NH2 с соединением формулы R5CH2 - CHR6 - СН2ОН (где RfeZ, R6OH или R5 и R6 вместе означают также 0) с образованием соединения формулы R1 - NH - СН 2 - CHR8 СН2ОН (где R8 означает ОН), с помощью реакции с производным угольной кислоты, таким как - диэтилкарбонат с получением 3^1-5-гидроксиметил-2оксазолидинонов и, при необходимости, с помощью превращения гидроксиметиловой группы в группу CH2Z, например, с помощью SOCb, SOBr2, метансульфонилхлорида или n толуолсульфонилхлорида Соединения формулы III, как правило, известии или могут быть получены по аналогии с известными соединениями из подходящих фенольных производных или из фенола Соединения формулы I могут быть, далее, получены посредством реакции соединения формулы IV (или его реакционноспособного производного) с реакционным производным угольной кислоты В качестве производных угольной кислоты пригодны, в частности, диалкилкарбонаты, такие как диэтилкарбонат, далее также алкиловый эфир хлормуравьиной кислоты, как то - этилхлорформиат Предпочтительным образом, производное уксусной кислоты, которое, целесообразным образом, используется в избыточном количестве, сложит также растворителем или суспензионным средством Но может присутствовать также один из указанных растворителей, если он в данной реакции обмена является инертным Далее, рекомендуется добавлять основание, в частности, алкоголят щелочного металла, как то - трет -бутилат калия Работа ведется предпочтительным образом, при реакционных температурах между 0 и 150°С, предпочтительным образом, между 70 и 120°С Исходные вещества формулы IV являются, как правило, новыми Их можно, например, получать за счет функционализирования названных выше соединений формулы R1 - NH - СН 2 СН(ОН) - СН2ОН соединения формулы R1 - NH 12 11 54367 СЬІ2 -СН(ОН) - СЬІ2 - Z и реакции с соединениями из этих продуктов могут быть получены производформулы III ные, в процессе восстановления их, например, с 1 помощью газообразного водорода Для получения соединении формулы где R означает гуадинофенильную группу, можно обраОснование формулы I с помощью кислоты ботать соответствующее аминофенильное соедиможет переводиться в соответствующую кислотнение амидинирующим средством В качестве но-аддитивную соль Дня этого взаимодействия амидинирующего средства предпочтение отдаетприменяются, в частности, кислоты, которые обся 1-ами-дино-3,5-диметилпиразолилу, который, в разуют физиологически приемлемые соли Так, частности, используется в форме своего нитрата могут использоваться неорганические кислоты, Работают, целесообразным образом, с добавленапример, серная кислота, азотная кислота, галонием основания, такого как триэтиламин или, геноводородные кислоты, такие как, хлорводородэтил-диизопропиламин в инертном растворителе ная кислота или бромводородная кислота, фосили смеси растворителей, например, вофорные кислоты, такие как ортофосфорная да/диоксан при температурах между 0 и 120°С, кислота, сульфаминовая кислота, далее, органипредпочтительно, между 60 и 120°С ческие кислоты, в частности, алифатические, алициклические, ароматические или гетероцикличесДалее, имеется возможность в соединении 3 кие одноосновные или многоосновные формулы I превратить один остаток R в другой карбоновые, сульфоновые или серные кислоты, остаток R3, путем омыления сложного эфира например, муравьиная кислота, уксусная кислота, формулы I или с помощью этерификаций карботри фтору ксусная кислота, пропионовая кислота, новой кислоты формулы I пивал иновая кислота, диэтилуксуская кислота, Для осуществления этерификаций можно обмалоновая кислота, янтарная кислота, пимелино3 работать кислоту формулы I (R =H) избыточным вая кислота, фумарная кислота, малеиновая кис3 3 количеством спирта формулы R -OH (R =A или лота, молочная кислота, винная кислота, яблочбензил), целесообразно, в присутствии сильной ная кислота, лимонная кислота, глюконовая кислоты, такой как соляная кислота или серная кислота, аскорбиновая кислота, никотиновая кискислота, при температурах между 0 и 100, предлота, метан- или этансульфоновая кислота, этанпочтительным образом между 20 и 50°С дасульфоновая кислота, 2И наоборот, сложный эфир формулы I (R3 = А или бензил) можно превратить в соответствуюгидроксиэтансульфоновая кислота, бензолсульщую кислоту формулы (R3=H), целесообразно, с фоновая кислота п -толуолсульфоновая кислота, помощью сольволиза или гидрогенолиза в соотнафталиновая моно- и дисульфоновая кислоты, ветствии с одной из указанных выше методик, лаурилсерная кислота Соли с физиологически например, с помощью NaOH или КОН в смеси вонепроницаемыми кислотами Например, пикраты, ды и диоксана при температурах между 0 и 40°С, могут применяться для выделения и/или очистки предпочтительно, между 10 и 30°С соединений формулы I Кроме того, имеется возможность превращеСвободные основания формулы I могут освония одного остатка R1 и/или R2 в другой остаток R1 бождаться, при желании, из их солей после обраи/или R2 ботки сильными основаниями, такими как гидроксид натрия или калия, карбонат натрия или В частности, можно первичные или вторичные калия аминогруппы алкилировать, ацилировать, амидинировать или снабжать временными аминозащитМожно также превращать карбоновые кислоты ными группами или алкил- или арилсульфонилформулы I (R3 = Н) путем реакции обмена с соотгруппами или, наоборот, освобождать их путем ветствующими основаниями в их соли металлов удаления этих групп или аммония, например, соли натрия, калия или кальция Для получения амидина формулы I (R1 = амидинофенил) можно присоединять к нитрилу форСоединения формулы I содержат один или 1 мулы I (R = цианфенил) аммиак Присоединение несколько хиральных центров и могут, поэтому, осуществляется в процессе нескольких этапов, присутствовать в рацемической или в оптически путем превращения известным способом а) нитактивной форма Полученные рацематы с испольрила с помощью bbS в тиоамид, который с помозованием известных методик могут разделяться щью алкилирующего средства, например, СНзІ, механически или химически на энантиомеры переводится в соответствующий сложный SПредпочтительным образом, из рацемической алкил-имидотиоэфир, который, со своей стороны смеси с помощью реакции обмена с оптически реагирует с ІЧНз с образованием амидина, спосоактивным разделяющим средством образуются бом б) нитрила с помощью спирта, например, этадиастереомеры В качестве разделяющего среднола, в присутствии НСІ в соответствующий сложства пригодны, например, оптически активные ный имидоэфир, который подвергается обработке кислоты, такие как - D -формы и L -формы винной аммиаком, и способом в) путем вступления нитрикислоты, диацетилвинная кислота, дибензоилвинла в реакцию обмена с бис-(триметилсилил)ная кислота, миндальная кислота, яблочная киамидомлития и доследующим гидролизом продукслота, молочная кислота или различные оптичета ски-активные камфарно-сульфоновые кислоты, такие как - р -сул ьфо камфарная кислота ПредАналогичным образом можно получать соотпочтительным является также разделение энанветствующие N-гидрокси-амидины формулы I (R1 тиомеров с помощью колонки, наполненной опти= фенил, замещенный HO-NH-C(=NH)) из нитрически активным разделительным средством лов, если работать по методике а) или б), но вме(например, динитробензоил-фенил-глицином), в сто аммиака использовать гидроксиламин Далее, 14 13 54367 качестве растворителя (в хроматографии) пригодкак правило, по аналогии с другими известными, на, например, смесь гексаимеющимися в продаже, фармацевтическими на/изопропанола/ацетонитрила, например, в объсредствами, в частности, по аналогии с соединеемном соотношении 82 15 3 ниями, описанными в ЕР-А-459 256, предпочтительным образом, в виде дозировок, составляюЕстественно, имеется возможность получения щих приблизительно 5мг и 1г, в частности, 50 и оптически активных соединений формулы I со500мг на дозировочную единицу Ежедневная догласно описанным выше методикам, когда использировка составляет, предпочтительным образом, зуют исходные вещества (например, такие вещеприблизительно 0,1 и 20мг/кг, в частности, 1 и ства формулы II), которые уже являются 10мг/кг веса тела Специальная доза, для каждого оптически активными определенного пациента зависит, однако, от разНовые соединения формулы I и их физиололичных факторов, например, от активности исгически приемлемые соли могут применяться для пользованного специального соединения, от возполучения фармацевтических препаратов, если их раста, веса тела, общего состояния здоровья, вместе с, по меньшей мере, одним веществомпола, от времени и способа приема, от скорости носителем или вспомогательным веществом и, выведения, от комбинаций лекарств и тяжести при желании, вместе с одним или несколькими соответствующего заболевания, которое подвердругими активными веществами, перевести в согается терапии Предпочтительным является ответствующую дозировочную форму Полученоральное введение ные таким образом препараты могут использоваться в качестве лекарственного средства в Выше и ниже температура указывается в грамедицине и ветеринарии В случае веществдусах Цельсия В приводимых ниже примерах выносителей речь идет об органических и неорганиражение "приготовление обычным способом" озческих веществах, которые пригодны для энтеначает При необходимости добавляют воду, в рального (например, орального или ректального) зависимости от конституции конечного продукта или парентерального введения или для введения устанавливают значение рН между 2 и 8, проводят в форме спрея для ингаляций, и не реагируют с фильтрацию ионообменную колонку, органиченовыми соединениями, например, вода, растискую фазу высушивают над сульфатом натрия, тельные масла, бензиловые спирты, полиэтиленгупаривают, при необходимости лиофилизируют и ликоли, глицеринтриацетаты и другие глицериды очищают с помощью хроматографии на силикагежирных кислот, желатины, соевый лецитин, углеле и/или с помощью кристаллизации В послеводы, такие как - лактоза или крахмал, стеарат дующих примерах выражение "4-пмперидилэтил" магния, тальк, целлюлоза Для орального примеозначает всегда "2-(4-пиперидил)-этил", выраженения служат, в частности, таблетки, драже, капние "4-пиперидилпропил" всегда "3-(4-пиперидил)сулы, сиропы, соки или капли, интерес представпропил" и выражение "4-пиперидилбутил" всегда ляют таблетки, имеющие лаковое покрытие, и "4-(4-пиперидил)-бутил" Точно так же выражение капсулы с оболочками, обладающими устойчиво"4-пиперазинил-этил" означает всегда "2-(4стью против воздействия желудочного сока Для пиперазинил)-этил", выражение "4ректального применения служат суппозитории, пиперазинилпропил" - "3-(4-пиперазинил)-пропил" для парентерального введения -растворы, преди выражение "4-пиперазинилбутил" - "4-(4почтительным образом, маслянистые или водные пиперазинил)-бутил" Включены также и снабженрастворы, далее суспензии, эмульсии или имные защитными группами производные, например, плантаты ВОС-защищенные соединения Для введения в виде спрея дня ингаляций моПример 1 гут применяться спреи, которые содержат активК раствору 1,9г метилового эфира 2-N-BOCное вещество либо в растворенном виде, либо в амино-3-(4-гидрокси-фенил)-пропановой кислоты виде суспензии в смеси рабочего газа При этом, ("А") (получаемого из тирозина путем этерификацелесообразным образом, применяют активное ции с метанолом и введения защитной группы вещество в микронизированной форме, причем ВОС) в 20мл диметилформамида (DMF) добавлямогут добавляться одно или несколько дополниют 1 эквивалент NaH и перемешивают в течение тельных физиологически приемлемых раствори30 минут при комнатной температуре После этого телей, например, этанол Ингаляционные растводобавляют 1,8г 3-п-І\І-ВОС-амидино-фенил-5ры могут приготовляться с помощью обычных метан-сульфонилокси-метил-оксазолидин-2-она ингаляторов Новые соединения могут также лио(получаемого в результате реакции п филизироваться, а полученные лиофилизаты моаминобензонитрила с 2,3-эпоксипропан-1-олом с гут использоваться, например, для получения образованием р-(І\І-2,3-дигидроксипропил-аміно)инъекционных препаратов Указанные композиции бензонитрила, реакции обмена с диэтилкарбонамогут быть стерилизованы и/или могут содержать том в присутствии трет-бутилатакалия с образовспомогательные вещества, такие как консерванванием З-п-цианфенил-5-гидроксиметилты, стабилизаторе и/или смачиватели, эмульгатооксазолидин-2-она, реакции обмена с H2S, меры, соли для оказания влияния на осмотическое тилйодидом и ацетатом аммония с получением давление, буферные вещества, красители и/или амидина, путем введения защитной группы ВОС в ароматические вещества При желании, они могут амидин и последующей этерификации с помощью содержать также одно или несколько дополниметансульфонил-хлорида), растворенного в 10мл тельных активных веществ, например, один DMF, и снова перемешивают в течение 15 минут витамин или несколько витаминов при комнатной температуре После удаления растворителя и осуществления "приготовления обычСоединения по изобретению принимаются, 16 15 54367 ным способом" получают З-n -ВОС-амидино33-(І-изопропил-4-пиперидилметил) -5- [п -(2фенил-5-[п -(2-меток-сикарбонил-2-І\І-ВОС-аминометоксикарбонил-2-М-ВОС-аминоэтил) -фенокси] этил) -фенокси] -метилоксазоли-дин-2-он метил-оксазолидин-2-он, Анадогино посредством реакции обмена "А" с помощью 3-(4-1Ч-ВОС-пиперазинилэтил)-5получают с помощью 3-(4-ІЧ-ВОС-пиперидил)-5метансульфонилокси-метил-оксазолидин-2-она метансульфонилокси-метил-оксазолидин-2-она 3-(4-1Ч-ВОС-пиперазинилэтил) -5-[п-(23-(4-І\І-ВОС-пиперидил) -5[п -(2метоксккарбонил-2-М-ВОС-аминоэтил)-фенокси] метоксикарбонил-2-М-ВОС-аминоэтил)-фенокси] метил-оксазолидин-2-он, метил-оксазолидин-2-он, с помощью 3-(4-ІЧ-ВОС-пиперазинилпропил)5-метансульфонилокси-метил-оксазолидин-2-она с помощью 3-(4-ІЧ-ВОС-пиперидилметил)-5метансульфонилокси-метил-оксазолидкн-2-она 3-(4-М-ВОС-пиперазинилпропил)-5-[п-(23-(4-І\І-ВОС-пиперидилметил)-5-[п -(2метоксикарбонил-2-Н-ВОС-аминоэтил)-фенокси] метил-оксазолидин-2-он, метоксикарбонил-2-11 -ВОС-амино-этйл)-фенокси]метил-оксазолидин-2-он, с помощью 3-(4-І\І-ВОС-пиперазинилбутил)-5метансульфонилокси-метил-оксазолидин-2-она с помощью 3-(4-1Ч-ВОС-пиперидилэтил)-5метансульфонилокси-метил-оксазолидин-2-она 3-(4-М-ВОС-пиперазинилбутил) -5-[п-(23-(4-1\1-ВОС-пиперидилэтил) -5-[п -(2метоксикарбонил-2-М-ВОС-аминоэтил)-фенокси] метоксикарбонил-2-М-ВОС-амино-этил)-фенокси] метил-оксазолидин-2-он, метил-оксазолидин-2-он, с помощью 3-(1 -ІЧ-ВОС-амидино-4с помощью 3-(4-ІЧ-ВОС-пиперидилпропил)-5пиперазинилэтил)-5-метансульфонилокси-метилметансульфонилокси-метил-оксазолидин-2-она оксазолидин-2-она 3-(4-І\І-ВОС-пиперидиллропил)-5-[п-(23-(1-М-ВОС-амидино-4-пиперазинилэтил)-5-[пметоксикарбонил-2-М-ВОС-аминонэтил)-фенокси] (2-метоксикарбонил-2-М-ВОС-аминоэтил)-метил-оксазолидин-2-он, фенокси] -метил-оксазолидин-2-он, с помощью 3-(4-І\І-ВОС-пиперидилбутил)-5с помощью 3-(І-М-ВОС-амидино-4метансульфонилокси-метил-оксазолидин-2-она пиперазинилпропил)-5-метансульфонилоксиметил-оксазолидин-2-она 3-(4-І\І-ВОС-пиперидилбутил)-5[п -(2метоксикарбонил-2-1\1-ВОС-аминоэтил) -фенокси] 3-(1-М-ВОС-амидино-4-пиперазинил пропил) метил-оксазолидин-2-он, 5-[п -(2-метоксикарбонил-2-М-ВОС-аминоэтил) фенокси] -метил-оксазолидин-2-он, с помощью 3-(1 -ІЧ-ВОС-амидино-4пиперидил)-5-метансуль-фонилокси-метилс помощью 3-(1 -Ы-ВОС-амидино-4оксазолидин-2-она пиперазинилбутил)-5-метансульфонилокси-метилоксазолидин-2-она 3-(1-1\1-ВОС-амидино-4-пиперидил) -5-[п-(2метоксикарбонил-2-1Ч-ВОС-аминоэтил) -фенокси] 3-(1-М-ВОС-амидино-4-пиперазинилбутил) -5-метил-оксазолидин-2-он, [п -(2-метоксикарбонил-2-М-ВОС-амино-этил)фенокси] -метил-оксазолидин-2-он, с помощью 3-(1 -І\І-ВОС-амидино-4пиперидилметил)-5-метансульфонилокси-метилПример 2 оксазодидин-2-она Раствор 0,9г 3-п-циан-фенил-5-[п-(2метоксикарбонил-2-М-ВОС-аминоэтил)-фенокси] 3-(1-1\1-ВОС-амидино-4-пиперид ил метил)- 5-[п метил-оксазолидин-2-она получаемый по примеру (2-метоксикарбонил-2-1\1-ВОС-аминоэтил)1 с помощью реакции обмена метилового эфира фенокси] -метил-оксазолидин-2-он, 2-Т-ВОС-амино-3-(4-гидрокси-фенил)-пропановой с помощью 3-(1-11-ВОС-амидино-4- пиперидикислоты с 3-п -циан-фенил-5лэтил)-5-метансульфонилокси-метилоксазолидин-2-она метансувьфонилокси-метил-оксазолидин-2-оном] в 40мл 10%-ного метанольного раствора ІЧНз гид3-(1-11-ВОС-амидино-4- пиперидилэтил)-5- [п рируются на 0,6г никеля Ренея при комнатной (2-метокси-карбонил-2-П-ВОС-аминоэтил)температуре и давлении в I бар до окончания пофенокси] -метил-оксазолидин-2-он, глощения ЬІ2 После фильтрации и упаривания с помощью 3-(1-П-ВОС-амидино-4получают, используя "приготовление обычным пиперидилпропил)-5-метансульфонилокси-метилспособом", 3-п -аминометил-фенил-5-[р-(2оксазолидин-2-она метокси-карбонил-2-І\І-ВОС-аминозтил) -фенокси] 3-(l-N- ВОС-амидино-4-пиперидилпропил) -5-[п -метил-оксазолидин-2-он -(2-метоксикарбонил-2-П-ВОС-амино-этил)фенокси] -метил-оксазолидин-2-он, По аналогии получают, с помощью 3-(lNВОС-амидино-4из 3-м -циан-фенил-5-[п -(2-метоксикарбонилпиперидилбутил)-5-метансульфонилокси-метил2-1\1-ВОС-аминоэтил) -фенокси] -метилоксазолидин-2-она оксазолидин-2-она 3-(l- N- ВОС-амидино-4-пиперидилбутил)-5-[п 3-м -аминометил-фенил-5-[п -(2(2-метоксикарбонил-2-М-ВОС-амино-этил) метоксикарбонил-2-М-ВОС-аминоэтил) -фенокси] фенокси] -метил-оксазолидин-2-он, метилоксазолидин-2-он, с помощью 3-(І-изопропил-4-пиперидил)-5из З-м-циан-фенил-5- [п-(2-метоксикарбонилметансульфонилокси-метил-оксазолидин-2-она 2-М-бутилсульфонил-аминоэтил) -фенокси] метил-оксазолидин-2-она 3-(І-изопропил-4-пиперидил) -5[п -(2метоксикарбонил-2-М-ВОС-аминоэтил)-фенокси] 3-м-аминометил-фенил-5-[п-(2метил-оксазолидин-2-он, метоксикарбонил-2-г\І-бутилсульфониламиноэтил)-фенокси]-метилоксазолидин-2-он, с помощью 3-(І-изопропил-4-пиперидилметил)5-метансульфонилокси-меил-оксазолидин-2-она из 3-П -циан-фенил-5-[п -(2-метоксикарбонил 18 17 54367 2-г\1-бутилсульфонил-аминоэтил) -фенокси] 3-(І-етил-4-пиперидил) -5-[п -(2метил-оксазолидин-2-она метоксикарбонил-2-М-бутилсульфониламиноэтил)-фенокси] -метил-оксазолидин-2-он, 3-П -аминометил-фенил-5-[п -(2метоксикарбонил-2-г\І-бутилсульфонилс помощью 3-(1 -І\І-ВОС-амидино-4аминоэтил)-фенокси] -метилоксазолидин-2-он, пиперидилметил)-5-метансульфонилокси-метилоксазолидин-2-она из 3- о -циан-фенил-5-[п -(2-метоксикарбонил2-г\1-бутилсульфонил-аминоэтил) -фенокси] 3-(1-М-ВОС-амидино-4-пиперидилметил)-5-[пметил-оксазолидин-2-она (2-метоксикарбонил-2-М-бутилсульфониламиноэтил)-фенокси] -метил-оксазолидин-2-он, 3-о-аминометил-фенил-5-5-[п -(2метоксикарбонил-2-г\І-бутилсульфонилс помощью 3-(1 -І\І-ВОС-амидино-4аминоэтил) -фенокси] -метилоксазолидин-2-он, пиперидилэтил)-5-метансульфонилокси-метилоксазолидан-2-она из 3-о-циан-фенил-5-[п -(2-метоксикарбонил-2г\|-ВОС-аминоэтил)-фенокси] -метил-оксазолидин3-(1-М-ВОС-амидино-4-пиперидилэтил)-5-[п-(22-она метоксикарбонил-2-М-бутилсульфониламиноэтил)-фенокси] -метил-оксазолидин-2-он, З-о-аминометил-фенил-5[р-(2с помощью -(1 -N-BOC-амидино -4метоксикарбонил-2-М-ВОС-аминоэтил)-фенокси] пиперидилпропил)-5-метансульфонилокси-метилметилоксазолидин-2-он оксазолидин-2-она Пример 3 Аналогично примеру 1, исходя из метилового 1-(N-BOC-амидино -4-пиперидилпропил) -5-[п эфира 2-Т-бутилсульфонил-амино-3-(4-гидрокси(2-метоксикарбонил-2-М-бутилсульфонилфенил)-пропановой кислоты ("В") [получаемого из аминоэтил) -фенокси] -метил-оксазолидин-2-он, тирозина путем этерификации метанолом и с пос помощью 3-(1 -І\І-ВОС-амидино-4мощью реакции обмена с бутилсульфонилхлорипиперидилбутил)-5-метансульфонилокси-метилдом], с помощью реакции обмена с 3-(1-N-BOCоксазолидин-2-она амидино-4-пиперидил) -5-метансульфонилокси3-(1-М-ВОС-амидино-4-пиперидилбутил)-5-[п метил-оксазолидин-2-оном [получаемым реакцией (2-метоксикарбонил-2-г\І-бутилсульфонил1-Н-ВОС-амидино-4-амино-пилеридина с 2,3аминоэтил) -фенокси] -метил-оксазолидин-2-он, эпоксипропан-1-олом с образованием I-IN-BOCс помощью 3-(1-изопропил-4-пиперидил)-5амидино-4-(І\І-2,3-дигидрокси-пропил-амино) метансульфонилокси-метил-оксазолидин-2-она пиперидина, взаимодействием с диэтилкарбона3-(1-изопропил-4-пиперидил)-5(п -(2том в присутствии трет-бутилатакалия с образометоксикарбонил-2-М-бутилсульфонилванием 3-( І-І\І-ВОС-амидино-4-пиперидил) -5аминоэтил)-фенокси] -метил-оксазолидин-2-он, гидрокси-метил-оксазолидин-2-она и последуюс помощью 3-(1-метил-4-пиперидилметил)-5щей этерификацией с метансульфонилхлоридом] метансульфонилокси-метил-оксазолидин-2-она получают 3-(1-1\1-ВОС-амидино-4-пиперидил)-5-[п3-( І-метил-4-пиперид ил метил) -5-[п -(2(2-метоксикарбонил-2-г\І-бутилсульфонилметоксикарбонил-2-М-бутилсульфониламиноэтил) -фенокси] -метил-оксазолидин-2-он аминоэтил)-фенокси] -метил-кжсазолидин-2-он, Аналогичным образом посредством реакции с помощью 3-(4-М-ВОС-пиперазинилэтил)-5обмена "В" получают метансульфо-килокси-метил-оксазолидин-2-она с помощью 3-(4-І\І-ВОС-пиперидил)-53-(4-М-ВОС-пиперазинилэтил) -5-[п -(2метансульфонилокси-метил -оксазолидин-2-она метоксикарбонил-2-М-бутилсульфониламиноэтил)-фенокси] -метил-оксазолидин-2-он, 3-(4-І\І-ВОС-пиперидил)-5 [п-(2метоксикарбонил-2-г\І-бутилсульфонилс помощью 3-(4-М-ВОС-пиперазинилпропил)аминоэтил)-фенокси]-метил-оксазолидин-2-он, 5-метансуль-фонилокси-метил-оксазолидин-2-она с помощью 3-(4-г\І-ВОС-пиперидилметил)-53-(4-М-ВОС-пиперазинилпропил)-5-[п-(2метансульфонилокси-метил-оксазолидин-2-она метоксикарбонил-2-М-бутилсуиьфонил-аминоэтил) -фенокси] -метил-оксазолидин-2-он, 3-(4-г\І-ВОС-пиперидилметил)-5-[п .(2метоксикарбонил-2-Nбутил сул ьфонилс помощью 3-(4-г\І-ВОС-пиперазинилбутил)-5метансульфонилокси-метил-оксазолидин-2-она аминоэтил)-фенокси] -метил-оксазолидин-2-он, с помощью 3-(4-г\1-ВОС-пиперидилэтил)-53-(4-М-ВОС-пиперазинилбутил)-5-[п -(2метансульфонилокси-метил-оксазолидин-2-она метоксикарбонил-2-М-бутилсульфонил3-(4-1\1-ВОС-пиперидилэтил) -5[п -(2аминоэтил) -фенокси] -метил-оксазолидин-2-он, метокоикарбонил-2-Nбутил сул ьфонилс помощью 3-(1 -Ы-ВОС-амидино-4пиперазинилэтил)-5-меметансульфонилоксиаминоэтил)-фенокси] -метил-оксазолидин-2-он, метил-оксазолидин-2-она с помощью 3-(4-г\І-ВОС-пиперидилпропил)-5метансульфонилокси-метил-оксазолидин-2-она 3-(1-М-ВОС-амидино-4-пиперазинилэтил) -5- [п -(2-метоксикарбокил-2-М-бутилсульфонил3-(4-г\І-ВОС-пиперидилпропил)-5-[п -(2аминоэтил) -фенокси] -метил-оксазолидин-2-он, метоксикарбонил-2-М-бутилсульфониламиноэтил)-фенолокси] -метил-оксазолидин-2-он, с помощью 3-(1 -І\І-ВОС-амидино-4с помощью 3-(4-г\І-ВОС-пиперидилбутил)-5пиперазинилпропил)-5-метансульфонилоксиметансульфонилокси-метил-оксазолидин-2-она метил-оксазолидин-2-она 3-(4-г\І-ВОС-пиперидилбутил) _5- [п -(23-(І-М-ВОС-амидано-4-пиперазинилпропил) -5[п-(2-метоксикарбонил-2-М-бутилсульфонилметоксикарбонил-2-Nбутил сул ьфониламино-этил)-фенокси] -метил-оксазолидин-2-он, аминоэтил)-фенокси] -метил-оксазолидин-2-он, с помощью 3-(1 -этил-4-пиперидил)-5с помощью 3-(І-І\І-ВОС-амидино-4метансульфонилокси-метил-оксазолидин-2-она пиперазинилбутил)-5-метансульфонилонси-метил 19 54367 оксазолидин-2-она 3-(І-г\І-ВОС-амидино-4-пиперазинилбутил)-5-[п -(2-метоксикарбонил -2-г\І-бутилсульфониламиноэтил)-фенокси]-метил-оксазолидин-2-он, Пример 4 1,2г 3-П -Амидано-фенил-5-[п -(2метоксикарбонил-2-М-ВОС-амино-этил)-фенокси] метилоксазолидин-2-она [получаемого в соответствии с примером 1] суспендируются в 60мл метанола, смешивают с 4мл 2 N раствора НаОН и перемешивают в течение 4 часов при комнатной температуре После удаления растворителя осадок поглощают водой, значение рН устанавливают равным 3 путем добавления разбавленной HCI и фильтруют через кислый ионообменник Фильтрат высушивают над MSO4 После удаления растворителя и после дополнительной лиофилизации получают 3- п -амидино-фенил-5- [п -(2-карбокси2-1\1-ВОС-амино-этил) -фенокси] -метилоксазолидин-2-она Аналогичным образом с помощью омыления продуктов из примера 1 получают 3-(4-г\І-ВОС-пиперидил) _5- [п -(2-карбокси-2-ІЧВОС-амино-этил) -фенокси] -метил-оксазолидин2-он, 3-(4-г\І-ВОС-пиперидилметил)-5-[п .(2карбокси-2-1\1-ВОС-аминоэтил)-фенокси] -метилоксазолидин-2-он, 3-(4-г\1-ВОС-пиперидилэтил)-5-[п -(2-карбокси2-1\1-ВОС~аминоэтил)-фенокси] -метилоксазолидин-2-он, 3-(4-г\І-ВОС-пиперидилпропил) -5- [п -(2карбокси-2-1\1-ВОС-аминоэтил)-фенокси] -метилоксазолидин-2-он, 3-(4-г\І-ВОС-пиперидилбутил)-5-[п -(2карбокси-2-1\1-ВОС-аминоэтил)-фенокси] -метилоксазолидин-2-он, 3-(1-г\1-ВОС-амидино-4-пиперидил)-5-[п -(2карбокси-2-1\1-ВОС-аминоэтил)-фенокси] -метилоксазолидин-2-он, 3-(І-г\І-ВОС-амидино-4-пиперидилметил) -5- [п(2-карбокси-2-М-ВОС-аминоэтил)-фенокси] -метилоксазолидин-2-он, 3-(1-г\1-ВОС-амидино-4-пиперидилэтил)-5-[п-(2карбокси-2-1\1-ВОС-аминоэтил)-фенокси] -метилоксазолидин-2-он, 3-(І-г\І-ВОС-амидино-4-пиперидилпропил) -5- [п -(2-карбокси-2-1\1-ВОС-аминоэтил) -фенокси] метил-оксазолидин-2-он, 3-(І-г\І-ВОС-амидино-4-пиперидилбутил) -5- [п (2-карбокси-2-М-ВОС-аминоэтил)-фенокси] -метилоксазолидин-2-он, 3-(І-зопропил-4-пиперидил)-5- [п -(2-карбокси2-1\1-ВОС-аминоэтил) -фенокси] -метилоксазолидин-2-он, 3-(І-метйл-4-пиперидилметил)-5[п -(2карбокси-2-М-ВОС-аминоэтил)-фенокси] -метилоксазолидин-2-он, 3-(4-г\1-ВОС-пиперазинилэтил) _5- [п -(2карбокеи-2-М-ВОС-аминоэтил) -фенокси 3 -метилоксазолидан2-он, 3-(4-М-ВОС-пиперазинил пропил) -5-[п -(2карбокси-2-М-ВОС-аминоэтил) -фенокси] -метилоксазолидин-2-он, 3-(4-М-ВОС-пиперазинилбутил)-5-[п -(2карбокси-2-М-ВОС-аминоэтил)-фенокси] -метил 20 оксазолидин-2-он, 3-(1-М-ВОС-амидино-4-пиперазинилэтил)-5-[п(2-карбокси-2-М-ВОС-аминоэтил)-фенокси] -метилоксазолидин-2-он, 3-(І-М-ВОС-амидино-4-пиперазинилпропил)-5[п -(2-карбокси-2-М-ВОС-аминоэтил)-фенокси] метил-оксазолидин-2-он, 3-(І-г\І-ВОС-амидино-4-пиперазинилбутил)-5-[п -(2-карбокси-2-М-ВОС-аминоэтил)-фенокси] метил-оксазолидин-2-он Пример 5 0,6г 3-п -М-ВОС-амидино-фенйл-5-[п -(2карбокси-2-М-ВОС-аминоэтил)-фенокси] -метилоксазолидин-2-она [получаемого в соответствии с примером 4] суспендируются в 40мл 2Н раствора HCI на основе диоксана и перемешиваются в течение трех часов при комнатной температуре После удаления растворителя и проведения "приготовления обычным способом" получают 3- п амидино-фенил-5- [п -(2-карбокси-2-аминоэтил)фенокси] -метил-оксазолидин-2-он, дигидрохлорид, т пд 165° (разл ) Аналогичным образом после удаления защитной группы ВСС продуктов получают из примера 4 3-(4-пиперидил) -5[п -(2-карбокси-2аминоэтил) -фенокси] -метил-оксазолидин-2-он, дигидрохлорид, 3-(4-пиперид ил метил) -5- [п -(2-карбокси-2аминоэтил)-фенокси] -метил-оксазолидин-2-он, дигидрохлорид, 3-(4-пиперидил) -5[п -(2-карбокси-2аминоэтил) -фенокси] -метил-оксазолидин-2-он, дигидрохлорид, 3-(4-пиперидилпролил) -5- [п -(2-карбокси-2аминоэтил) -фенокси] -метил-оксазолидин-2-он, дигидрохлорид, 3-(4 -пиперидилбутил)-5-[п -(2-карбокси-2аминоэтил)-фенокси] -метил-оксазолидин-2-он, дигидрохлорид, 3-(І-амидино-4-пиперидил) -5- [п -(2-карбокси2-аминоэтил)-фенокси] -метил-оксазолидин-2-он, дигидрохлорид, 3-(І-амидино-4-пиперидилметил)-5-[п -(2карбокси-2-аминоэтил) -фенокси] -метилоксазолидин-2-он, дигидрохлорид, 3-(1-амидино-4-пиперидилэтил)-5-[п-(2карбокси-2аминоэтил) -фенокси] -метилоксазолидин-2-он, дигидрохлорид, 3-(І-амидино-4-пиперидилпропил) -5-[п -(2карбокси-2-аминоэтил) -фенокси] -метилоксазолидин-2-он, дигидрохлорид, 3-(І-амидино-4-пилеридилбутил) -5- [п -(2карбокси-2-аминоэтил)-фенокси] -метилоксазолидин-2-он, дигидрохлорид, 3-(І-изопропил-4-пиперидил) -5[п -(2карбокси-2-аминоэтил)-фенокси] -метилоксазолидин-2-он, дигидрохлорид, 3-(І-метил-4-пиперидилметил)-5[п -(2карбокси-2-аминоэтил)-фенокси] -метилоксазолидин-2-он, дигидрохлорид, 3-(4-пиперазинилэтил)-5-[п -(2-карбокси-2аминоэтил)-фенокси] -метил-оксазолидин-2-он, дигидрохлорид, 3-(4-пиперазинилпропил) -5- [п -(2-карбокси-2аминоэтил)-фенокси] -метил-оксазолидин-2-он, 54367 22 21 дигидрохлорид, 3-(4-пиперазинилпропил)-5-[п (2метоксикарбонил-2-аминоэтил)-фенокси]-метил3-(4-пиперазинилбутил)-5-[п-(2-карбокси-2оксазолидин-2-он, дигидрохлорид, аминоэтил)-фенокси]-метил-оксазолидин-2-он, дигидрохлорид, 3-(4-пиперазинилбутил)-5-[п -(23-(1-амидино-4-пиперазинилэтил)-5-[п-(2метоксикарбонил -2-аминоэтил)-фенокси 3-метилкарбокси-2-аминоэтил)-фенокси]-метилоксазолидин-2-он, дигидрохлорид, оксазолидин-2-он, дигидрохлорид, 3-(1-амидино-4-пиперазинилэтил)-5-[п -(23-(І-амидино-4-пиперазинилпропил)-5-[п -(2метоксикарбонил-2-аминоэтил)-фенокси] -метилкарбокси-2-аминоэтил) -фенокси]-метилоксазолидин-2-он, дигидрохлорид, оксазолидин-2-он, дигидрохлорид, 3-(1-амидино-4-пиперазинилпропил)-5-[п-(2метоксикарбонил-2-аминоэтил)-фенокси] -метил3-(І-амидино-4-пиперазинилбутил)-5-[п -(2оксазолидин-2-он, дигидрохлорид, карбокси-2-аминоэтил) -фенокси] -метилоксазолидин-2-он, дигидрохлорид 3-(1-амидино-4-пиперазинилбутил)-5-[п-(2метоксикарбонил-2-аминоэтил)-фенокси]-метилПример 6 оксазолидин-2-он, дигидрохлорид 0,6г 3-п-м-ВОС-амидино-фенил-5-[п-(2метокси-карбонил-2-М-ВОС-аминоэтил)-фенокси]Пример 7 метил-оксазолидин-2-она [полученного в соответАналогично примеру 4, исходя из 3-(1-N-BOCствии с примером 1] суспендируют в 40мл 2N расамидино-4-пиперидил)-5-[п-(2-метокси-карбонил-2твора HCI на основе диоксана и перемешивают в М-бутилсульфонил-аминоэтил)-фенокси]-метилтечение трех часов при комнатной температуре оксазолидин-2-она [получаемого в соответствии с примером 3], омылением получают 3-(І-Н-ВОСПосле удаления растворителя и проведения амидино-4-пиперидил)-5[п-(2-карбокси-2-І\І"приготовления обычным способом" получают 3-п бутилсульфонил-аминоэтил)-фенокси] -метил-амидино-фенил-5-[п-метоксикарбонил-2оксазолидин-2-он аминоэтил) -фенокси] -метил-оксазолидан-2-он, дигидрохлорид, т пл 132-133°С Аналогичным образом получают с помощью омыления 3-(4-І\І-ВОС-пиперидил)-5-[п-(2Аналогичным образом после удаления защитной группы ВОС продуктов получает из примера 1 метоксикарбонил-2-г\І-бутилсульфонил3-(4-пиперидил)-5-[п-(2-ыетоксикарбонил-2аминоэтил)-фенокси]-метил-оксазолидин-2-он аминоэтил)-фенокси] -метил-оксазолидин-2-он, 3-(4-Ы-ВОС-пиперидил-5-[п -(2-карбокси-2-Ыдигидрохлорид, бутилсульфонил-аминоэтил)-фенокси] -метилоксазолидин-2-он, 3-(4-пиперидилметил)-5-[п-(2метоксикарбонил-2-амино-этил)-фенокси]-метил3-(4-М-ВОС-пиперидилметил)-5-[п -(2оксазолидин-2-он, дигидрохлорид, метоксикарбонил-2-Nбутил сул ьфонил3-(4-пиперидилэтил)-5-[п-(2-метоксикарбониламиноэтил)-фенокси]-метил-оксазолидин-2-он, 2-амино-этил)-фенокси]-метил-оксазолидин-2-он, 3-(4-г\І-ВОС-пиперидилметил)-5-[п-(2-карбоксидигидрохлорид, 2-М-бутилсульфонил-аминоэтил)-фенокси]-метилоксазолидин-2-он, 3-(4-пилеридилпропил)-5-[п-(2метоксикарбонил-2-аминозтил)-фенокси] -метил3-(4-М-ВОС-пиперидилэтил)-5-[п-(2оксазолидин-2-он, дигидрохлорид, метоксикарбонил-2-М-бутилсульфониламиноэтил)-фенокси]-метил-оксазолидин-2-он 3-(4-пиперидилбутил)-5-[п-(2метоксикарбонил-2-аминоэтил)-фенокси]-метил3-(4-М-ВОС-пиперидилэтил)-5-[п-(2-карбоксиоксазолидин-2-он, дигидрохлорид, 2-М-бутилсульфонил-аминоэтил)-фенокси] -метилоксазолидин-2-он, 3-(І-амидино-4-пиперидил)-5-[п-(23-(4-г\І-ВОС-пиперидилпропил) _5- [п -(2метоксикарбонил-2-аминоэтил)-фенокси]-метилоксазолидин-2-он, дигидрохлорид, метоксикарбонил-2-М-бутилсульфониламиноэтил)-фенокси] -метил- оксазолидин -2-он 3-(І-амидино-4-пиперидилметил)-5-[п-(2метоксикарбонил-2-аминоэтил)-фенокси] -метил3-(4-М-ВОС-пиперидилпропил)-5-[п-(2оксазолидин-2-он, дигидрохлорид, карбокси-2-г\1-бутилсульфонил-аминоэтил)фенокси]-метил- оксазолидин-2-он, 3-(1-амидино-4-пиперидилэтил)-5-[п-(2метоксикарбонил-2-аминоэтил)-фенокси] -метил3-(4-М-ВОС-пиперидилбутил)-5-[п-(2оксазолидин-2-он, дигидрохлорид, метоксикарбонил-2-М-бутилсульфониламиноэтил)-фенокси]-метил- оксазолидин-2-он 3-(І-амидино-4-пиперидилпропил)-5-[п -(2метоксикарбонил-2-аминоэтил)-фенокси]-метил3-(4-М-ВОС-пиперидилбутил)-5-[п -(2оксазолидин-2-он, дигидрохлорид, карбокси-2-М-бутилсульфонил-аминоэтил)фенокси]-метил- оксазолидин -2-он, 3-( І-амидино-4-пиперидилбутил) -5-[п -(2метоксикар-бонил-2-аминоэтил)-фенокси] -метил3-(1 -этил-4-пиперидил)-5-[п-(2оксазолидин-2-он, дигидрохлорид, метоксикарбонил-2-г\І-бутилсульфониламиноэтил)-фенокси]-метил- оксазолидин -2-он 3-(І-изопропил-4-пиперидил)-5[п -(2метоксикарбонил-2-аминоэтил)-фенокси]-метил3-(1-этил-4-пиперидил)-5-[п -(2-карбокси-2-І\Іоксазолидан-2-он, дигидрохлорид, бутилсульфонил-аминоэтил)-фенокси] -метилоксазолидин -2-он, 3-(І-метил-4-пиперидилметил)-5[п -(2метоксикарбонил-2-аминоэтил)-фенокси] -метил3-(1-г\1-ВОС-амидино-4-пиперидилметил)-5-[поксазолидин-2-он, дигидрохлорид, (2-метоксикарбонил-2-М-бутилсульфонил3-(4-пиперазинилэтил) -5[п -(2аминоэтил)-фенокси]-метил-оксазолидин-2-он метоксикарбонил-2-аминозтил)-фенокси]-метил3-(І-М-ВОС-амидино-4-пиперидилметил)-5-[поксазолидин-2-он, дигидрохлорид, (2-карбокси-2-М-бутилсульфонил-аминоэтил) 24 23 54367 фенокси] -метил- оксазолидин -2-он фенокси]-метил-оксазолидан-2-он 3-(1-1\1-ВОС-амидино-4-пиперидилэтил)-5-[п-(2Пример 8 меток-сикарбонил-2-г\І-бутилсульфонилК раствору 0,6г 3-п-амидино-фенил-(2аминоэтил)-фенокси] -метил- оксазолидин-2-он метоксикарбонил-2-М-ВОС-амино-этил)-фенокси]метил-оксазолидин-2-она в 20мл THF добавляют 3-(1-1\1-ВОС-амидино-4-пиперидилэтил)-5-[п 20мл 20%-ного раствора NaOH и перемешивают в (2-карбокси-2-И-бутилсульфонил-аминоэтил) течение 24 часов при комнатной температуре фенокси] -метил-оксазолидан-2-он, После удаления растворителя и сублимационной 3-(І-Г\І-ВОС-амилино-4-пиперидиллропил)-5-[псушки получают Na-соль 3-п -амидино-фенил-5-[п(2-метоксикарбонил-2-г\І-бутилсульфонил(карбокси-2-1Ч-ВОС-аминоэтил) -фенокси] -метиламиноэтил)-фенокси]-метил -оксазолидин-2-он оксазолидин-2-она, т пл 120-121 °С 3-(І-І\І-ВОС-амилино-4-пиперидиллропил)-5-[п(2-карбокси-2-г\1-бутилсульфонил-аминоэтил)Аналогичным образом получают фенокси]-метил -оксазолидин-2-он, натриевую соль 3-п-аминометил-фенил-5-[п(карбокси-2-М-ВОС-аминоэтил)-фенокси]-метил3-(І-г\І-ВОС-амидано-4-пиперидилбутил)-5-[поксазолидин-2-она, (2-метоксикарбонил-2-И-бутилсульфониламиноэтил)-фенокси] -метил-оксазолидин-2-он натриевую соль 3-п-амидино-фенил-5-[п(карбокси-2-М-бутилсульфониламино-этил)3-(І-г\І-ВОС-амидино-4-пиперидилбутил)-5-[пфенокси]-метил-оксазолидин-2-она, (2-карбокси-2-г\1-бутилсульфонил-аминоэтил)фенокси]- метил-оксазолидин-2-он, натриевую соль 3-п-аминометил-фенил-5-[п3-(І-изопропил-4-пиперидил)-5-[п-(2(2-карбокси-2-М-бутилсульфонил-аминоэтил)метоксикарбонил-2-Nбутил сул ьфонилфенокси]-метил-оксазолидин-2-она аминоэтил)-фенокси]-метил-оксазолидан-2-он Пример 9 3-(І-изопропил-4-пиперидил)-5-[п-(2-карбоксиРаствор 0,2г 1-амидино-3,5-диметилпиразол2-г\1-бутилсульфонил-аминоэтил)-фенокси]-метилнитрата в 17мл диоксана и 5мл воды смешивается оксазолидан-2-он, с 0,7мл этилдиизопропиламина и перемешивают в течение 15минут После этого добавляют 0,4г 3-п 3-(1-метил-4-пиперидилметил)-5-[п-(2аминометил-фенил-5-[п -(2-метокси-карбонил-2-І\Іметокоикарбонил-2-г\І-бутилсульфонилВОС-аминоэтил)-фенокси]-метил-оксазолидин-2аминоэтил)-фенокси]-метил- оксазолидан-2-он, она, смесь кипятят в течение 30 часов, упаривают, 3-(І-метил-4-пиперидилметил)-5-[п-(2а "приготовление ведут обычным способом" Покарбокси-2-г\1-бутилсульфонил-аминоэтил)лучают 3-п -гуадано-метил-фенил-5-[п-(2-метоксифенокси]-метил- оксазолидан-2-он, карбонил-2-1\1-ВОС-аминоэтил)-фенокси]-метил3-(4-1\1-ВОС-пиперазинилэтил)-5-[п-(2оксазолидин-2-он метоксикарбонил-2-І\І-бутилсульфониламиноэтил)-фенокси] -метил- оксазолидан-2-он Аналогичным образом получают 3-(4-1\1-ВОС-пиперазинилэтил)-5-[п-(2из 3-М-аминометил-фенил-5-[п-(2карбокси-2-1\1-бутилсульфонил-аминоэтил)метоксикарбонил-2-М-ВОС-аминоэтил)-фенокси]фенокси]-метил- оксазолидан-2-он, метил-оксазолидин-2-она, 3-(4-І\І-ВОС-пиперазинилпропил)-5-[п-(23-м-гуадинометил-фенил-5-[п-(2метоксикарбонил-2-г\І-бутилсульфонилметоксикарбонил-2-М-ВОС-аминоэтил)-фенокси]аминоэтил)-фенокси] -метил- оксазолидан-2-он метил-оксазолидин-2-он, 3-(4-І\І-ВОС-пиперазинилпропил)-5-[п-(2из 3-м-аминометил-фенил-5-[п-(2карбокси-2-М-бутилсульфонил-аминоэтил)метоксикарбонил-2-г\І-бутилсульфониламинофенокси] -метил- оксазолидан-2-он, этил)-фенокси]-метил-оксазолидин-2-она, 3-(4-М-ВОС-пиперазинилбутил)-5-[п-(23-м-гуадинометил-фенил-5-[п-(2метоксикарбонил-2-М-бутилсульфонилметоксикарбонил-2-М-бутилсульфониламиноэтил)-фенокси] -метил- оксазолидан-2-он аминоэтил)-фенокси]-метил-оксазолидин-2-он, 3-(4-М-ВОС-пиперазинилбутил)-5-[п-(2из 3п -аминометил-фенил-5-[п-(2карбокси-2-М-бутилсульфонил-аминоэтил)метоксикарбонил-2-М-бутилсульфонилфенокси] -метил- оксазолидан-2-он, аминоэтил)-фенокси]-метил-оксазолидин-2-она, 3-(1-1\1-ВОС-амидино-4-пиперазинилэтил)-5-[п3п-гуадонометил-фенил-5-[п-(2(2-метоксикарбонил-2-М-бутилсульфонилметоксикарбонил-2-М-бутилсульфониламиноэтил)-фенокси]-метил-оксазолидан-2-он аминоэтил)-фенокси]-метил-оксазолидин-2-она, 3-(1-М-ВОС-амидино-4-пиперазинилэтил)-5-[пиз 3-о-аминометил-фенил-5-[п-(2(2-карбокси-2-М-бутилсульфонил-аминоэтил)метоксикарбонил-2-М-бутилсульфонилфенокси]-метил-оксазолидан-2-он, аминоэтил)-фенокси]-метил-оксазолидин-2-она, 3-(І-Г\І-ВОС-амидино-4-пиперазинилпропил)-53-о-гуадинометил-фенил-5-[п-(2-2[п-(2-метоксикарбонил-2-І\І-бутилсульфонилметоксикарбонил-2-г\І-бутилсульфониламиноаминоэтил)-фенокси]-метил-оксазолидан-2-он этил)-фенокси]-метил-оксазолидин-2-она, 3-(І-М-ВОС-амидино-4-пиперазинилпропил)-5из 3-о-аминометил-фенил-5-[п-(2[п-(2-карбокси-2-М-бутилсульфонил-аминоэтил)метоксикарбонил-2-М-ВОС-аминоэтил)-фенокси]фенокси]-метил-оксазолидан-2-он, метил-оксазолидин-2-она, 3-(І-І\І-ВОС-амидино-4-пиперазинилбутил)-53-о-гуадинометил-фенил-5-[п-(2[п-(2-метоксикарбонил-2-М-бутилсульфонилметоксикарбонил-2-М-ВОС-аминоэтил)-фенокси]аминоэтил)-фенокси]-метил-оксазолидан-2-он метил-оксазолидин-2-она, 3-(І-М-ВОС-амидино-4-пиперазинилбутил)-5Пример 10 [п-(2-карбокси-2-М-бутилсульфонил-аминоэтил)В раствор 1,2г 3-п -циан-фенил-5-[п-(2 26 25 54367 метоксикарбонил-2-г\І-бутилсольфонил3-М -амидино-фенил-5-[п-(2-карбокси-2-М-паминоэтил)-фенокси]-метил-оксазолидин-2-она, толуолсульфонил-аминоэтил)-фенокси]-метил[получаемого в соответствии с примером 1 путем оксазолидин-2-он, реакции обмена метилового эфира 2-Nиз 3-М -амидино-фенил-5-[п-(2бутилсульфонил-амино-3-(4-гидрокси-фенил)метоксикарбонил-2-І\І-п-толуолсульфонилпропановой кислоты с З-п-циан-фенил-5аминоэтил)-фенокси]-метил-оксазолидин-2-она, метансульфонилокси-метил-оксазолидан-2-он] в 3-М -амидино-фенил-5-[п-(2-карбокси-2-М-п50мл пиридина и 7мл триэтиламина при -10° ввотолуолсульфонил-аминоэтил)-фенокси]-метилдят газ% bbS до насыщения После этого переоксазолидин-2-он, мешивают 14 часов при комнатной температуре, Пример 12 упаривают, растворяют осадок в 50мл ацетона и 1,37г 3-п-(5-оксо-1,2,4-оксадиазолин-З-ил)смешивают с 9мл метилйодада После этого профенил-5-[п-(2-метоксикарбонил-2-М-этилводят повторное перемешивание в течение 6 чааминоэтил)-фенокси]-метил-оксазолидин-2-она сов, фильтруют, осадок промывают 5мл ацетона, [полученного в соответствии с примером 1 порастворяют его в 30мл метанола, добавляют 4,6г средством реакций обмена метилового эфира 2ацетата аммония и перемешивают при комнатной |\|-этил-амино-3-(4-гидрокси-фенйл)-пропановой температуре в течение 24 часов После "пригокислоты с 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил)товления обычным способом" получают амидинофенил-5-метан-сульфонилметил-оксазолидин-2фенил-5-[п-(2-метоксикарбонил-2-І\Іон], растворяют в 50мл метанола и гидрируют на бутилсульфонил-аминоэтил)-фенокси никеле Ренея После єтого реакционную смесь оксазолидин-2-он, т пд 162-163° фильтруют, а фильтрат упаривают в вакууме Полученный продукт обрабатывают 20мл этилового Аналогичным образом получают эфира уксусной кислоты при нагревании, и после из 3-м-циан-фенил-5-[п-(2-метосикарбонил-2охлаждения продукт отсасывают Получают 3-пг\|-бутилсульфонил-аминоэтил)-фенокси]метиламидинофенил-5-[п-(2-метоксикарбонил-2-І\І-етилоксазолидин-2-она, аминоэтил) -фенокси]-метил-оксазолидин-2-она 3-м-амидино-фенил-5-[п-(2-метосикарбонил-2г\|-бутилсульфонил-аминоэтил)-фенокси]метилоксазолидин-2-он, из 3-п-циан-фенил-5-[п-(2-метоксикарбонил-2М-(ВОС-аминоетил)-фенокси]-метил-оксазолидин2-она, 3-п-амидино-фенил-5-[п-(2-метоксикарбонил2-І\І-(ВОС-аминоєтил)-фенокси]-метилоксазолидин-2-он, из 3-п-циан-фенил-5-[п-(2-метоксикарбонил-2N-п-толуолсульфонил-аминоэтил) -фенокси]метил-оксазолидин-2-она, 3-п-амидино-фенил-5-[п-(2-метоксикарбонил2-І\І-п-толуолсульфонил-аминоєтил)-фенокси]метил-оксазолидин-2-он, из 3-м-циан-фенил-5-[п-(2-метоксикарбонил-2|\|-п-толуолсульфониламино-єтил)-фенокси]метил-оксазолидин-2-он, из 3-м-амидино-фенил-5-[п-(2метоксикарбонил-2-І\І-п-толуолсульфониламиноэтил)-фенокси]-метил-оксазолидин-2-он Пример 11 Аналогично примеру 4, исходя из 3-памидино-фенил-5-[п-(2-метоксикарбонил-2-І\Ібутилсульфонил-2-г\1-аминоэтил)-фенокси]-метилоксазолидин-2-она [получаемого в соответствии с примером 10], путем омыления получают 3-памидино-фенил-5-[п-(2-карбокси-2-І\Ібутилсульфонил-амино-этил)-фенокси]-метилоксазолидин-2-он, т пл 236-237° Аналогичным образом получают с помощью омыления из 3-М-аминометил-фенил-5-[п-(2метилкарбонил-2-г\1-бутилсульфонил-аминоэтил)фенокси]-метил-оксазолидкн-2-она, 3-М -амидино-фенил-5-[п-(2-карбокси-2-І\Ібутилсульфонил-аминоэтил)-фенокси]-метилоксазолидин-2-он, из 3-М -амидино-фенил-5-[п-(2метоксикарбонил-2-І\І-п-толуолсульфониламиноэтил)-фенокси]-метил-оксазолидин-2-она, Аналогично восстановительным расщеплением группы-5-оксо-1,2,4-оксадиазолина получают из 3-п -(5-оксо-1,2,4-оксадиазолин-3-ил)фенил-5-[п-(2-метоксикарбонил-2-І\І-изопропиламино-этил)-фенокси]-метил-оксазолидин-2-она, 3-п -амидинофенил-5-[п-(2-метоксикарбонил2-1\1-изопропил-аминоэтил)-фенокси]-метилоксазолидин-2-она, из 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил)фенил-5-[п-(2-метоксикарбонил-2-І\І-ацетиламиноэтил)-фенокси]-метил-оксазолидин-2-она, 3-п -амидинофенил-5-[п-(2-метоксикарбонил2-М-ацетил-аминоэтил)-фенокси]-метилоксазолидин-2-она, из 3-п -(5-оксо-1,2,4-оксадиазолин-3-ил)фенил-5-[п-(2-метоксикарбонил-2-М-пропиониламиноэтил)-фенокси]-метил-оксазолидин-2-она, 3-п -амидинофенил-5-[п-(2-метоксикарбонил2-М-пропионил-аминоэтил)-фенокси]-метилоксазолидин-2-она, 3-п -(5-оксо-1,2,4-оксадиазолин-3-ил)-фенил-5[п-(2-метоксикарбонил-2-М-ВОС-аминоэтил)фенокси]-метил-оксазолидин-2-она, из 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил)фенил-5-[п-(2-метоксикарбонил-2-М-трет -бутиламиноэтил)-фенокси]-метил-оксазолидин-2-она, 3-п -амидинофенил-5-[п-(2-метоксикарбонил2-Ы-трет -бутил-аминоэтил)-фенокси]-метилоксазолидин-2-она Пример 13 Аналогично примеру 4 омылением соответствующих сложных эфиров из примера 12 получают следующие карбоновые кислоты 3-п -амидинофенил-5-[п-(2-карбокси-2-1\1-этиламиноэтил)-фенокси]-метил-оксазолидин-2-он, 3-п -амидинофенил-5-[п-(2-карбоси-2-І\Іизопропил-аминоэтил)-фенокси]-метилоксазолидин-2-он, 3-п -амидинофенил-5-[п-(2-карбокси-2-І\Іацетил-аминоэтил)-фенокси]-метил-оксазолидин 27 2-он, 3-п -амидинофенил-5-[п-(2-карбокси-2-1\1пропионил-аминоэтил)-фенокси]-метилоксазолидин-2-он, 3-п -амидинофенил-5-[п-(2-карбокси-2-1\1аминоэтил)-фенокси]-метил-оксазолидин-2-он, 3-п -амидинофенил-5-[п-(2-карбокси-2-1\1-трет бутил-аминоэтил)-фенокси]-метил-оксазолидин-2он Пример 14 Аналогично примеру 4 путем омыления соответствующих сложных эфиров из примера 9 получают следующие карбоновые кислоты 3-п-гуадинометил-фенил-5-[п-(2-карбокси-2-ІЧВОС-аминоэтил)-фенокси]-метил-оксазолидин-2он, 3-м-гуадинометил-фенил-5-[п-(2-карбокси-2-ІЧВОС-аминоэтил)-фенокси]-метил-оксазолидин-2он, 3-м-гуадинометил-фенил-5-[п-(2-карбокси-2-І\Ібутилсульфонил-аминоэтил)-фенокси]-метилоксазолидин-2-он, 3-п-гуадинометил-фенил-5-[п-(2-карбокси-2-І\Ібутилсульфонил-аминоэтил)-фенокси]-метилоксазолидин-2-он, 3-о-гуадинометил-фенил-5-[п-(2-карбокси-2-І\Ібутилсульфонил-аминоэтил)-фенокси]-метилоксазолидин-2-он, 3-о-гуадинометил-фенил-5-[п-(2-карбокси-2-ІЧВОС-аминоэтил)-фенокси]-метил-оксазолидин-2он Пример 15 Аналогично примеру 5 путем отщепления защитной группы ВОС, исходя из продуктов примера 14, получают следующие соединения 3-п-гуадинометил-фенил-5-[п-(2-карбокси-2аминоэтил)-фенокси]-метил-оксазолидин-2-он, 3-м-гуадинометил-фенил-5-[п-(2-карбокси-2аминоэтил)-фенокси]-метил-оксазолидин-2-он, 3-о-гуадинометил-фенил-5-[п-(2-карбокси-2аминоэтил)-фенокси]-метил-оксазолидин-2-он Пример 16 0,5г 3-п -(5-оксо-1,2,4-оксадиазолин-3-ил)фенил-5-[п-(2-бензилоксикарбонил-2-аминоэтил)фенокси]-метил-оксазолидин-2-она [получаемые путем реакции обмена бензилового эфира 2-NВОС-амино-3-(4-гидрокси-фенил)-пропановой кислоты, который получают из тирозина путем введения защитной группы ВОС и этерификации с помощью бензилового спирта, с 3-п-(5-ксо-1,2,4оксадиазолин-3-ил)-фенил-5-метансульфонилметил-оксазолидин-2-оном с получением 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил)-фенил-5[п-(2-бензилоксикарбонил-2-1\1-ВОС-амино-этил)фенокси]-метил-оксазолидан-2-она и последующей обработки трифторуксусной кислотой] растворяют в 10мл дихлорметана и вводят в реакцию обмена с 1 эквивалентом хлорида пропансульфокислоты при ледяном охлаждении Спустя 1 час реакционный раствор промывают разбавленной соляной кислотой (2 раза) и водой, а органическую фазу упаривают после сушки над сульфатом магния Продукт очищают путем кристаллизации из этилацетат/петролейного эфира и путем хроматографии на силикагеле (толуол/ацетон 4 1) Получают 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил) 54367 28 фенил-5-[п-(2-бензилокси-карбонил-2-І\Іпропилсульфонил-аминоэтил) -фенокси]-метилоксазолидин-2-он, FAB-MS т/е 635 (М+Н+) По аналогии путем реакции обмена 3-п-(5оксо-1,2,4-оксадиазолин-3-ил)-фенил-5-[п-(2бензилоксикарбонил-2-амино-этил)-фенокси]метил-оксазолидин-2-он получают с помощью хлорида этан сул ьфоки слоты 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил)-фенил-5[п-(2-бензилоксикарбонил-2-1\1-этилсульфониламино-этил)-фенокси]-метил-оксазолидин-2-он, с помощью хлорида толуол сул ьфоки слоты 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил)-фенил-5[п-(2-бензилоксикарбонил-2-І\І-толуолсульфониламиноэтил)-фенокси]-метил-оксазолидин-2-он, с помощью хлорида бензилсульфокислоты 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил)-фенил-5[п-(2-бензилоксикарбонил-2-М-бензилсульфониламиноэтил)-фенокси]-метил-оксазолидин-2-он, с помощью хлорида гексансульфокислоты 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил)-фенил-5[п-(2-бензилоксикарбонил-2-1\1-гексилсульфониламиноэтил)-фенокси]-метил-оксазолидин-2-он, с помощью хлорида пентансульфокислоты 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил)-фенил-5[п-(2-бензилоксикарбонил-2-М-пентилсульфониламиноэтил)-фенокси]-метил-оксазолидин-2-он, ты с помощью хлорида гексадекансульфокисло 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил)-фенил-5[п-(2-бензилоксикарбонил-2-І\Ігексадеканилсульфонил-аминоэтил)-фенокси]метил-оксазолидин-2-он, с помощью хлорида бутановой кислоты 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил)-фенил-5[п-(2-бензилоксикарбонил-2-І\І-бутаноиламиноэтил)-фенокси]-метил-оксазолидин-2-он, с помощью хлорида пентановой кислоты 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил)-фенил-5[п-(2-бензилоксикарбонил-2-М-пентаноиламиноэтил)-фенокси]-метил-оксазолидин-2-он, с помощью хлорида гексановой кислоты 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил)-фенил-5[п-(2-бензилоксикарбонил-2-І\І-гексаноиламиноэтил)-фенокси]-метил-оксазолидин-2-он, с помощью хлорида бензойной кислоты 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил)-фенил-5[п-(2-бензилоксикарбонил-2-М-бензоиламиноэтил)-фенокси]-метил-оксазолидин-2-он, с помощью хлорида І-нафталиновой кислоты 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил)-фенил-5[п-(2-бензилоксикарбонил-2-М-(І-нафтоил-амино)этил)-фенокси]-метил-оксазолидин-2-он, с помощью хлорида 2-нафталиновой кислоты 3-п-(5-оксо-1,2,4-оксадиазолин-3-ил)-фенил-5[п-(2-бензилоксикарбонил-2-М-(2нафтоил-амино)этил)-фенокси]-метил-оксазолидин-2-он Пример 17 Для расщепления бензилового эфира и оксадиазолинового кольца 0,4г 3-п -(5-ксо-1,2,4оксадиазолин-3-ил)-фенил-5-[п-(2-бензилоксикарбонил-2-1\1-пропилсульфонил-аминоэтил)фенокси]-метил-оксазолидин-2-она растворяют в 10мл дихлорметана и после добавления 1мл уксусной кислоты, 0,5мл воды и 5мл метанола, а также 0,1 г палладия/активированного угля (10%) 30 29 54367 обрабатывают при комнатной температуре водоинъекционные пузырьки, лиофилизуют в стерильродом Спустя 30 минут катализатор фильтруют, ных условиях, и стерильно закупоривают Каждый реакционный раствор концентрируют и получают инъекционный пузырек содержит 5мг активного 3-п-амидино-фенил-5-[п-(2-карбокси-2-1Чвещества пропилсульфонил-аминоэтил)-фенокси]-метилПример Б оксазолидин-2-она, температура вспышки 200° Суппозитории (плавление) Смесь из 20г активного вещества формулы 1 Аналогичным образом с помощью гидрировасо ЮОг соевого лецитина и 1400г масла какао ния продуктов из примера 16 получают расплавляют, выливают в формы и оставляют охлаждаться Каждый суппозиторий содержит 3-п -амидино-фєнил-5-[п-(2-карбокси-2-І\І20мг активного вещества этилсульфонил-аминоэтил)-фенокси]-метилоксазолидин-2-он, т пл 212 (разл), Пример В 3-п -амидино-фєнил-5-[п-(2-карбокси-2-І\ІРаствор тулуолсульфонил-аминоэтил)-фенокси]-метилПриготавливают раствор из 1г активного веоксазолидин-2-он, т пл 205° (разл ), щества формулы 1, 9,3г NaH2PO4-2H2O, 28,48г Na2HPO-12H2O, и 0,1 бензалкониумхлорида в 3-п -амидино-фєнил-5-[п-(2-карбокси-2-І\І940мл дважды дистиллированной воды Значение бензилсульфонил-аминоэтил)-фенокси]-метилрН устанавливают равным 6,8, раствор доводят оксазолидин-2-он, т пл 211° (разл), до 1л, стерилизуют с помощью облучения Рас3-п -амидино-фєнил-5-[п-(2-карбокси-2-І\Ітвор может применяться в форме глазных капель гегсилсульфонил-аминоэтил)-фенокси]-метилоксазолидин-2-он, т пл 198° (разл), Пример Г 3-п -амидино-фєнил-5-[п-(2-карбокси-2-І\ІМазь пентилсульфонил-аминоэтил)-фенокси]-метилСмешивают 500мг активного вещества фороксазолидин-2-он, т пл 215° (разл), мулы 1с 99,5г вазелина в антисептических усло3-п -амидино-фєнил-5-[п-(2-карбокси-2-І\Івиях гегсадеканилсульфонил-аминоэтил)-фенокси]Пример Д метил-оксазолидин-2-он, т пл 220° (разл ), Таблетки 3-п -амидино-фєнил-5-[п-(2-карбокси-2-І\ІСмесь из 1кг активного вещества формулы бутаноил-аминоэтил)-фенокси]-метил1,4кг лактозы, 1,2кг картофельного крахмала, 0,2кг оксазолидин-2-он, т пл 190° (разл), талька и 0,1кг стеарата магния спрессовывают 3-п -амидино-фєнил-5-[п-(2-карбокси-2-І\Іобычным образом, так, что каждая таблетка сопентаноил-аминоэтил)-фенокси]-метилдержит 10мг активного вещества оксазолидин-2-он, т пл 195° (разл), Пример У 3-п -амидино-фєнил-5-[п-(2-карбокси-2-І\ІДраже гексаноил-аминоэтил)-фенокси]-метилАналогично примеру Е прессуют таблетки, кооксазолидин-2-он, т пл 188° (разл), торые затем обычным образом покрывают обо3-п -амидино-фєнил-5-[п-(2-карбокси-2-І\Ілочкой из сахарозы, картофельного крахмала, бензоил-аминоэтил)-фенокси]-метил-оксазолидинталька траганте и красителя 2-он, т пл 204° (разл ), Пример Ж 3-п -амидино-фєнил-5-[п-(2-карбокси-2-І\І-(ІКапсулы нафтоил-амино)-этил)-фенокси]-метил2кг активного вещества формулы 1 обычным оксазолидин-2-он, образом наполняют капсулы из твердого желати3-п -амидино-фєнил-5-[п-(2-карбокси-2-І\І-(2на, ток что каждая капсула содержит 20мг активнафтоил-амино)-этил)-фенокси]-метилного вещества оксазолидин-2-он, т пл 226° (разл ) Пример 3 Приводимые ниже примеры касаются фармаАмпулы цевтических препаратов Раствор из 1 кг активного вещества формулы 1 Пример А в 60л дважды дистиллированной воды фильтруют Пузырьки для инъекций в стерильных условиях, разливают в ампулы, В растворе ЮОг активного вещества формулы лиофилизуют и закрывают в стерильных услови1 и 5г динатрийгидрогенфосфата в Зл дважды ях Каждая ампула содержит 10мг активного ведистиллированной вода с 2н соляной кислоты щества устанавливают значение рН, равное 6,5, раствор фильтруют в стерильных условиях, разливают в Підписано до друку 03 04 2003 р Тираж 39 прим ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)236-47-24
ДивитисяДодаткова інформація
Назва патенту англійськоюOxasolyldinone derivatives, methods for their production, pharmaceutical composition and method for its preparation
Автори англійськоюGante Joachim, Jurascuk Horst, Raddatz Peter, Wurziger Hanns, Bernotat-Danelowski Sabine, Melzer Guido
Назва патенту російськоюПроизводные оксазолидинона, способ их получения, фармацевтическая композиция и способ ее получения
Автори російськоюГанте Йоахим, Юрасцук Хорст, Раддатц Петер, Вурцигер Ханнс, Бернотат-Даниловськи Сабине, Мельцер Гвидо
МПК / Мітки
МПК: A61P 35/00, A61P 9/08, C07D 263/24, A61P 9/00, A61P 9/10, A61P 7/02, A61P 15/00, A61K 31/421, C07D 413/04, A61K 31/495, A61P 43/00, A61K 31/496, A61K 31/42, A61P 19/10, C07D 413/10, A61K 31/445, C07D 413/06, A61P 13/02
Мітки: отримання, композиція, похідні, фармацевтична, спосіб, оксазолідинону
Код посилання
<a href="https://ua.patents.su/15-54367-pokhidni-oksazolidinonu-sposib-kh-otrimannya-farmacevtichna-kompoziciya-ta-sposib-otrimannya.html" target="_blank" rel="follow" title="База патентів України">Похідні оксазолідинону, спосіб їх отримання, фармацевтична композиція та спосіб її отримання</a>
Попередній патент: Порошковий дріт для десульфурації чавуну
Наступний патент: N-аміно-1-гідроксіалкіліден-1,1-біфосфорні кислоти та спосіб їх безперервного отримання
Випадковий патент: Склад для одержання зносостійких композиційних електролітичних покриттів на основі нікелю