Спосіб одержання 1-бензил-3-гідроксиметил-1н-індазолу і його похідних та проміжні сполуки магнію
Номер патенту: 106886
Опубліковано: 27.10.2014
Автори: Якоанджелі Томмазо, Караччоло Торкяроло Джуліано, Фурлотті Гвідо
Формула / Реферат
1. Спосіб одержання 1-бензил-3-гідроксиметил-1Н-індазолу, представленого наступною формулою (II):
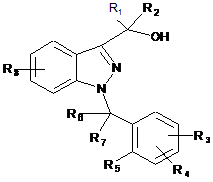 , (II)
, (II)
у якій
R1 і R2, які можуть бути однаковими або різними, являють собою водень або алкільну групу, яка включає від 1 до 6 атомів вуглецю,
R3, R4 і R8, які можуть бути однакові або різні, можуть являти собою водень, алкільну групу, яка включає від 1 до 5 атомів вуглецю, алкоксильну групу, яка включає від 1 до 3 атомів вуглецю, та атом галогену,
R5 може являти собою водень, алкільну групу, яка включає від 1 до 5 атомів вуглецю, алкоксильну групу, яка включає від 1 до 3 атомів вуглецю, атом галогену, або разом з одним з R6 і R7 може утворювати кільце, яке включає 5 або 6 атомів вуглецю, і
R6 і R7, які можуть бути однакові або різні, можуть являти собою водень, алкільну групу, яка включає від 1 до 5 атомів вуглецю, або один з R6 і R7 разом з R5 може утворювати кільце, яке включає 5 або 6 атомів вуглецю.
у якому
а) 1-бензил-3-галоген-1H-індазол формули (III):
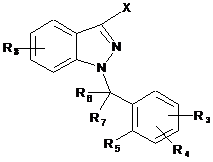 , (III)
, (III)
у якій X являє собою атом галогену, вибраний з йоду та брому, краще - йоду,
вводять у реакцію з галоїдом алкілмагнію формули RMgX', де R являє собою алкільну групу з 1 до 6 атомами вуглецю і X' являє собою атом галогену, вибраний з брому і хлору, краще - хлору, з утворенням проміжної сполуки (IV):
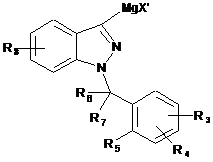 , (IV)
, (IV)
b) вказану проміжну сполуку (IV) вводять у реакцію з карбонільною сполукою формули R1-CO-R2, з утворенням сполуки формули (II), або, альтернативно до стадії b),
b') вказану проміжну сполуку (IV) вводять у реакцію з амідом формули R'R''N-CO-R1, де R' і R", які можуть бути однакові або різні, являють собою алкільну групу, яка включає від 1 до 3 атомів вуглецю,
з утворенням проміжної сполуки (VIII):
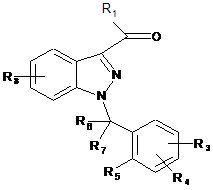 , (VIII)
, (VIII)
яку вводять в реакцію з відновлювальним агентом карбонільної групи з утворенням сполуки формули (II).
2. Спосіб одержання 1-бензил-3-гідроксиметил-1Н-індазолу, представленого формулою (II) за п. 1, у якому вказані етапи а) і b) проводять в присутності розчинника, вибраного з групи, яка включає тетрагідрофуран, 2-метилтетрагідрофуран, діетиловий етер, діоксан, t-бутилметиловий етер, дибутиловий етер, ксилен, толуол, дихлорметан, хлороформ, n-гексан, n-гептан і їх суміші, і вказаний етап b') проводять в присутності розчинника, вибраного з групи, яка включає тетрагідрофуран, 2-метилтетрагідрофуран, діетиловий етер, діоксан, t-бутилметиловий етер, дибутиловий етер, ксилен, толуол, дихлорметан, хлороформ, n-гексан, n-гептан, метанол, етанол, n-пропанол, і-пропанол, диглім, піридин, ДМСС, оцтову кислоту і їх суміші.
3. Спосіб одержання 1-бензил-3-гідроксиметил-1Н-індазолу, представленого формулою (II) за п. 1, у якому вказаний галоїд алкілмагнію формули RMgX' вибирають з групи, яка включає метилMgCl, етилMgCl, n-пропілMgCl, i-пропілMgCl, n-бутилMgCl, і-бутилMgCl, сек-бутилMgCl, t-бyтилMgCl, n-пeнтилMgCl, n-гексилMgCl, алілMgCl, циклoгeкcилMgCl, мeтилMgBr, етилMgBr, n-пропілMgBr, i-пpoпiлMgBr, n-бутилMgВr, i-бутилMgBr, sec-бyтилMgBr, t-бутилMgBr, n-пентилМgВr, n-гексилMgВr, aлiлMgBr, циклoгeкcилMgBr, де кращим є i-пропілMgCl.
4. Спосіб одержання 1-бензил-3-гідроксиметил-1Н-індазолу, представленого формулою (II) за п. 1, у якому вказаний етап а) проводять при молярному співвідношенні між галоїдом алкілмагію формули RMgX' і 1-бензил-3-галогено-1Н-індазолом формули (III) між 1 і 4, краще - між 1,5 і 4.
5. Спосіб одержання 1-бензил-3-гідроксиметил-1Н-індазолу, представленого формулою (II) за п. 1, у якому вказану карбонільну сполуку формули R1-CO-R2 вибирають з групи, яка включає альдегіди і кетони.
6. Спосіб одержання 1-бензил-3-гідроксиметил-1Н-індазолу, представленого формулою (II) за п. 1, у якому вказану карбонільну сполуку формули R1-CO-R2 вибирають з групи, яка включає формальдегід, ацетальдегід, пропанал, бутанал, пентанал, гексанал, ацетон, метилетилкетон і ізобутилметилкетон, де кращим є формальдегід.
7. Спосіб одержання 1-бензил-3-гідроксиметил-1Н-індазолу, представленого формулою (II) за п. 1, у якому вказаний етап b) проводять при молярному співвідношенні між 1-бензил-3-галогено-1Н-індазолом формули (III) і карбонільною сполукою формули R1-CO-R2 між 1 і 6.
8. Спосіб одержання 1-бензил-3-гідроксиметил-1H-індазолу, представленого формулою (II) за п. 1, у якому вказаний амід формули R'R''N-CO-R1 вибирають з групи, яка включає Ν,Ν-диметилформамід, Ν,Ν-діетилформамід, Ν,Ν-ди-n-пропілформамід, Ν,Ν-диметилацетамід, Ν,Ν-діетилацетамід, Ν,Ν-ди-n-пропілацетамід, Ν,Ν-диметилпропіонамід, N,N-діетилпропіонамід і Ν,Ν-ди-n-пропілпропіонамід, де кращим є Ν,Ν-диметилформамід.
9. Спосіб одержання 1-бензил-3-гідроксиметил-1H-індазолу, представленого формулою (II) за п. 1, у якому вказаний етап b') проводять при молярному співвідношенні між 1-бензил-3-галогено-1H-індазолом формули (III) і амідом формули R'R''N-CO-R1 між 1 і 4.
10. Спосіб одержання 1-бензил-3-гідроксиметил-1H-індазолу, представленого формулою (II) за п. 1, у якому вказаний відновлювальний агент карбонільної групи, який використовують на етапі b'), вибирають з групи, яка включає NaBH4, KBH4, LiBH4, Zn(BH4)2, Ca(BH4)2, NaAlH4, LiAlH4, Et3SiH, Bu3SnH, i-Bu2AlH, 70 % NaAlH2(OCH2CH2OCH3)2 у толуолі, де кращим є 70 % NaAlH2(OCH2CH2OCH3)2 у толуолі.
11. Спосіб одержання 1-бензил-3-гідроксиметил-1Н-індазолу, представленого формулою (II) за п. 1, у якому групи R1-R8 у формулах (II), (III), (IV) і (VIII), вказаних вище, можуть мати наступні значення:
R1 і R2, які можуть бути однаковими або різними, представлені атомом водню, алкільною групою, яка включає від 1 до 3 атомів вуглецю,
R3, R4 і R8, які можуть бути однаковими, або різними, можуть являти собою водень, метильну групу, етильну групу, метоксигрупу, етоксигрупу, атом хлору і атом фтору,
R5 може являти собою водень, метильну групу, етильну групу, метоксигрупу, етоксигрупу, атом хлору, атом фтору, або разом з одним з R6 і R7 може утворювати кільце, яке включає 6 атомів вуглецю, і
R6 і R7, які можуть бути однаковими або різними, можуть являти собою водень, метильну групу, етильну групу, або один з R6 і R7 разом з R5 може утворювати кільце, яке включає 6 атомів вуглецю.
12. Проміжна сполука, представлена наступною формулою (IV):
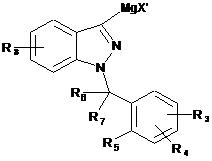 , (IV)
, (IV)
у якій
X' являє собою атом галогену, вибраний з брому і хлору,
R3, R4 і R8, які можуть бути однакові або різні, можуть являти собою водень, алкільну групу, яка включає 1-5 атомів вуглецю, алкоксильну групу, яка включає 1-3 атоми вуглецю, і атом галогену,
R5 може являти собою водень, алкільну групу, яка включає 1-5 атомів вуглецю, алкоксильну групу, яка включає 1-3 атоми вуглецю, атом галогену, або разом з одним з R6 і R7 може утворювати кільце, яке включає 5 або 6 атомів вуглецю, і
R6 і R7, які можуть бути однакові або різні, можуть являти собою водень, алкільну групу, яка включає 1-5 атомів вуглецю, або один з R6 і R7 разом з R5 може утворювати кільце, яке включає 5 або 6 атомів вуглецю.
13. Проміжна сполука, представлена формулою (IV) за п. 12, у якій:
X' являє собою атом хлору,
R3, R4 і R8, які можуть бути однакові або різні, можуть являти собою водень, метильну групу, етильну групу, метоксигрупу, етоксигрупу, атом хлору і атом фтору,
R5 може являти собою водень, метильну групу, етильну групу, метоксигрупу, етоксигрупу, атом хлору і атом фтору, або разом з одним з R6 і R7 може утворювати кільце, яке включає 6 атомів вуглецю,
R6 і R7, які можуть бути однакові або різні, можуть являти собою водень, метильну групу, етильну групу, або один з R6 і R7 разом з R5 може утворювати кільце, яке включає 6 атомів вуглецю.
Текст
Реферат: Даний винахід стосується способу одержання 1-бензил-3-гідроксиметил-1H-індазолу формули (II) для застосування у наступному способі одержання 1-бензил-3-гідроксиметил-1Н-індазолу формули (І). UA 106886 C2 (12) UA 106886 C2 UA 106886 C2 5 10 15 20 25 30 35 40 45 ГАЛУЗЬ ВИНАХОДУ Даний винахід стосується одержання 1-бензил-3-гідроксиметил-1H-індазолу. Зокрема даний винахід стосується способу одержання 1-бензил-3-гідроксиметил-1Hіндазолу формули (II), яка наведена нижче, для застосування у наступному способі одержання 1-бензил-3-гідроксиметил-1H-індазолу формули (I), яка наведена нижче. РІВЕНЬ ТЕХНІКИ Європейський патент EP-B-O 382 276 описує деякі похідні 1-бензил-3-гідроксиметил-1Hіндазолу формули (A), які мають аналгетичну активність: у якій R і R', які можуть бути однаковими або різними, являють собою H або C1-5 алкіл, і R'' являє собою H або C1-4 алкіл, можливо у формі його солі з фармацевтично прийнятною органічною або неорганічною основою, коли R" являє собою H. В свою чергу Європейський патент EP-B-O 510 748 з іншої сторони описує застосування тих же похідних для приготування фармацевтичної композиції, активної у лікуванні аутоімунних захворювань. На додаток до цього документ EP-B1-0 858 337 описує фармацевтичну композицію, яка містить сполуку формули (A), у якій R=R' = CH3 і R" = H, та імуносупресант. Європейський патент EP-B-1 005 332 описує застосування тих же похідних для приготування фармацевтичної композиції для лікування станів, обумовлених утворенням MCP-1. Нарешті міжнародна заявка WO 2008/061671 описує застосування сполуки (A) для зниження рівнів тригліцеридів, холестерину і глюкози у крові. Різні способи одержання сполук формули (A) описані у вищевказаному патенті EP-B-O 382 276. Способи, описані в патенті EP-B-O 382 276, мають як ключову стадію одержання 1-бензил-3гідроксиметил-1H-індазолу, з якої можуть бути одержані сполуки формули (A) за допомогою трьох різних видів реакцій: Перший вид реакції передбачає конверсію 1-бензил-3-гідроксиметил-1H-індазолу у відповідний алкоголят, який у свою чергу потім вступає в реакцію з X-CRR'-COOR", де X являє собою відхідну групу, вибрану з групи, яка включає галогени, арилен-SO2-O-, або алкілен-SO2O-, для одержання сполук формули (A). Другий вид реакції передбачає конверсію 1-бензил-3-гідроксиметил-1H-індазолу у відповідне похідне 3-галогенометилу, яке потім вступає в реакцію з алкоголятом формули MeOCRR'-COOR", де Me являє собою лужний метал, для одержання сполук формули (A). Третій вид реакції передбачає проведення реакції 1-бензил-3-гідроксиметил-1H-індазолу з хлороформом і кетоном формули O=CRR' в присутності лужної основи, такої як гідроксид натрію для одержання сполук формули (A), де R" являє собою водень. Одержання ключової проміжної сполуки 1-бензил-3-гідроксиметил-1H-індазолу за допомогою способу, описаного у патенті EP-B-O 382 276, проводять шляхом відновлення відповідної 3-карбонової кислоти за допомогою придатного відновлювального агента, такого як, наприклад, гідрид алюміній-літію (LiAIH4). КОРОТКИЙ ОПИС ВИНАХОДУ Заявнику відомо, що спосіб синтезу, відомий з рівня техніки і описаний у вищевказаному патенті EP-B-O 382 276, має ряд недоліків. По-перше, 1-бензил-1 (H)-індізол-3-карбонова кислота не є продуктом, який можна легко одержати на ринку, і він є доволі дорого коштує. Зокрема є мало постачальників і способи синтезу, описані в літературі, передбачають бензилування відповідної 1 (H)-індазол-3-карбоної кислоти, яка також дорого коштує і її також не можна легко одержати. На другому місці 1 UA 106886 C2 5 10 15 відновлення 1-бензил-1 (H)-індазол-3-карбонової кислоти для одержання 1-бензил-3гідроксиметил-1H-індазол проходить з високими факторами розведення. Крім того реакція другого виду передбачає застосування тіоніл хлориду для перетворення 1бензил-3-гідроксиметил-1H-індазолу у відповідне похідне 3-хлорметилу. Застосування тіоніл хлориду – високотоксичної речовини приводить до росту проблем безпеки та управління у промислових процесах. Нарешті, реакція третього виду (реакція Баргеліні) показала недоліки у промисловому виробництві, пов'язані з низьким виходом (менше ніж 50 %), утворенням моноксиду вуглецю – токсичного і легкозаймистого газу і утворенням значного екзотермічного явища, якими важко управляти у промисловому масштабі (Davis et al. Synthesis, 12, (2004), 1959-1962). Крім того реакція Баргеліні знаходить краще застосування у синтезі етерів з фенолів, а не з аліфатичних спиртів (US 3,262,850; Cvetovich et al., J. Org. Chem., (2005), 70, 8560-8563). Заявник таким чином розглянув проблему розробки нового способу приготування 1-бензил3-гідроксиметил-1H-індазолу для одержання сполук формули (A), здатного подолати вищевказані недоліки. Зокрема Заявник розширив проблему до одержання 1-бензил-3гідроксиметил-1H-індазолів наступної формули (II). для одержання сполук наступної формули (I) 20 25 30 35 40 у якій замісники від R1 до R12 мають такі ж, як вказані далі у докладному описі та формулі винаходу. Заявник винайшов новий спосіб одержання 1-бензил-3-гідроксиметил-1H-індазолів формули (II) для одержання сполук формули (I), що значно покращує, з однієї сторони, промислову придатність, вихід продуктів та вартість нового способу у порівнянні з відомими способами і, з іншої сторони, якість продуктів, отриманих за допомогою цього способу. Заявник несподівано винайшов, що 1-бензил-3-гідроксиметил-1H-індазол, або його похідні формули (II) можна легко одержати шляхом реакції реактиву Гриньяра формули (IV), яка наведена нижче, з придатною електрофільною сполукою, такою як, наприклад, альдегіди, кетони або аміди, з наступним відновленням, якщо це необхідно, проміжної карбонільної сполуки. Зокрема, Заявник несподівано винайшов, що реактив Гриньяра формули (IV) легко одержуються з 1-бензил-3-галогено-1H-індазолу або його похідних формули (III), описаних нижче, через обмінну реакцію галогену/магнію з реактивами Гриньяра типу галоїду алкіл магнію при низький температурі. Заявник також вважає, що реактиви Гриньяра формули (IV) невідомі у галузі. Фактично, у галузі відомі лише органометалеві похідні індазолу з металом у 3 положенні з такими металами як цинк (Knochel et al., Synlett 2005, 267) або мідь (Knochel et al., Synthesis 2006, 15, 2618 і Knochel et al., Synlett 2004, 13, 2303-2306), тоді як реакції руйнування індазольного кільця у спробі приготувати відповідні 3-органолітієві сполуки (Welch et al., Synthesis, 1992, 937) і 3-органонатриєві похідні (Tertov et al., Zhurnal Organicheskoi Khimii 1970, 6; 2140) відомі. 2 UA 106886 C2 5 10 15 20 25 30 Вказані похідні 1-бензил-3-галогено-1H-індазолу формули (III), які є широко відомими у літературі, можна легко одержати шляхом галогенування 1H-індазолу у 3 положенні з наступним бензилуванням у 1 положенні (Collot et al., Tetrahedron, 1999, 55, 6917; Coller et al., Aust. J. Chem. 1974, 27, 2343). Заявник несподівано винайшов, що 1-бензил-3-гідроксиметил-1H-індазол, або його похідні формули (II) можна легко перетворити у відповідні похідні 3-галогенметилу шляхом простої обробки гідрогалогеновими кислотами і потім у сполуки у сполуки формули (I) шляхом етерифікації відповідною гідроксикарбоновою кислотою або естером формули (Vl). Альтернативно, Заявник несподівано винайшов, що 1-бензил-3-гідроксиметил-1H-індазол, або його похідні формули (II) можна легко перетворити у сполуки формули (I) шляхом етерифікації відповідною α-галогенкарбоновою кислотою або естером формули (VII), описаним нижче. Таким чином, у першому аспекті даний винахід стосується способу одержання 1-бензил-3гідроксиметил-1H-індазолу і його похідних, представлених наступною формулою (II): де замісники від R1 до R8 мають значення, вказані далі у докладному описі та формулі винаходу, де a) 1-бензил-3-галоген-1H-індазол формули де X являє собою атом галогену, вибраний з йоду і брому, краще - йод вводять у реакцію з галоїдом алкіл магнію формули RMgX', де R являє собою алкільну групу, яка має від 1 до 6 атомів вуглецю і X' являє собою атом галогену, вибраний з брому та хлору, краще - хлор, для утворення проміжної сполуки (IV): b) вказану проміжну сполуку (IV) вводять в реакцію з карбонільною сполукою формули R 1CO-R2 для утворення сполуки формули (II), або альтернативно b') вказану проміжну сполуку формули (IV) вводять у реакцію з амідом формули R'R''N-COR1, де R' і R", які можуть бути однаковими або різними, являють собою алкільну групу, яка включає 1-3 атоми вуглецю, для утворення проміжної сполуки (VIII): 3 UA 106886 C2 5 10 яку вводять у реакцію з відновлювальним агентом карбонільної групою для утворення сполуки формули (II). Сполуку формули (II), яку одержують зі способом даного винаходу, можна легко застосувати у способі одержання похідних 1-бензил-3-гідроксиметил-1H-індазолу, представлених наступною формулою (I): де замісники від R1 до R12 мають значення, вказані далі у докладному описі та формулі винаходу. Нарешті, у другому аспекті даний винахід стосується проміжної сполуки, представленої наступною формулою (IV): 15 де X' являє собою атом галогену, вибраний з брому та хлору, краще – хлор і замісники від R3 до R8 мають значення, вказані у докладному описі та формулі винаходу. Докладний опис винаходу У першому аспекті даний винахід стосується способу одержання 1-бензил-3-гідроксиметил1H-індазолу та його похідних, представлених наступною формулою (II): 20 у якій R1 і R2, які можуть бути однакові або різні, являють собою водень або алкільну групу, яка включає від 1 до 6 атомів вуглецю, 4 UA 106886 C2 5 10 15 20 25 30 35 R3, R4 і R8, які можуть бути однакові або різні, можуть являти собою водень, алкільну групу, яка включає від 1 до 5 атомів вуглецю, алкоксильну групу, яка включає від 1 до 3 атомів вуглецю, та атом галогену, R5 може являти собою водень, алкільну групу, яка включає від 1 до 5 атомів вуглецю, алкоксильну, яка включає від 1 до 3 атомів вуглецю, атом галогену, або разом з одним R 6 і R7 може утворювати кільце, яке включає 5 або 6 атомів вуглецю, і R6 і R7, які можуть бути однакові або різні, можуть являти собою водень, алкільну групу, яка включає від 1 до 5 атомів вуглецю, або один з R6 і R7 разом з R5 може утворювати кільце, яке включає 5 або 6 атомів вуглецю. Спосіб одержання 1-бензил-3-гідроксиметил-1H-індазолу та його похідних, представлених вищевказаною формулою (II) згідно з винаходом передбачає, що: a) a 1-бензил-3-галогено-1H-індазол формули (ІІІ) у якій X являє собою атом галогену, вибраний з йоду та брому, краще – йод, і R3-R8 мають вищевказані значення, вводять у реакцію з галоїдом алкілмагнію формули RMgX', де R являє собою алкільну групу з 1 до 6 атомами вуглецю і X' являє собою атом галогену, вибраний з брому і хлору, краще – хлор, для утворення проміжної сполуки (IV): b) вказану проміжну сполуку (IV) вводять у реакцію з карбонільною сполукою формули R 1CO-R2, де R1 і R2 мають вищевказані значення для утворення сполуки формули (II), або альтернативно до b) b') вказану проміжну сполуку (IV) вводять у реакцію з амідом формули R'R''N-CO-R1, де R' і R", які можуть бути однакові або різні, являють собою алкільну групу, яка включає від 1 до 3 атомів вуглецю і R1 має вищевказані значення, для утворення проміжної сполуки (VIII): яку вводять у реакцію з відновлювальним агентом карбонільної групи для одержання сполуки формули (II). Краще етап a) проводити в присутності придатного розчинника, такого як, наприклад, тетрагідрофуран, 2-метил-тетрагідрофуран, діетиловий етер, діоксан, t-бутил-метиловий етер, дибутиловий етер, ксилен, толуол, дихлорметан, хлороформ, n-гексан, n-гептан і їх суміші і т.п., краще - 2-метил-тетрагідрофуран, тетрагідрофуран, толуол, ксилен і їх суміші і кращим є 2метил-тетрагідрофуран. Галоїд алкілмагнію формули RMgX', який використовують на етапі a), може являти собою метилMgCI, етилMgCI, n-пропілMgCI, i-пропілMgCI, n-бутилMgCI, i-бутилMgCI, сек-бутилMgCI, t 5 UA 106886 C2 5 10 15 20 25 30 35 40 45 50 55 бутилMgCI, n-пентилMgCI, n-гексилMgCI, алілMgCI, циклогексилMgCI, метилMgBr, етилMgBr, n пропіл Mg Br, i-пропілMgBr, n-бутилMgBr, i-бутилMgBr, sec-бутилMgBr, t-бутилMgBr, nпентилMgBr, n-гексилMgBr, алілMgBr, циклогексилMgBr, і краще - i-пропілMgCI. Ці реагенти можна одержати на комерційній основі або приготувати згідно зі способами, широко описаними в літературі (Silverman et al., Handbook of Grignard reagents, Chapter 2, CRC Press). Краще реакцію обміну на етапі a) можна проводити з використанням каталізатора шляхом додавання солей літію, наприклад, LiCI, як описано в літературі (Knochel et al., Chem. Commun., 2005, 543). Краще реакцію на етапі a) проводити при температурі у межах -30 °C і +30 °C, краще – при температурі між -20 °C і -10 °C. Краще етап a) проводити при молярному співвідношенні між галоїдом алкілмагнію формули RMgX' і 1-бензил-3-галогено-1H-індазолом формули (III) між 1 і 4, краще – між 1,5 і 4. Краще етап b) проводити в присутності придатного розчинника, такого як, наприклад, тетрагідрофуран, 2-метил-тетрагідрофуран, діетиловий етер, діоксан, t-бутилметиловий етер, дибутиловий етер, ксилен, толуол, дихлорметан, хлороформ, n-гексан, n-гептан та їх суміші і т.п., краще - 2-метил-тетрагідрофуран, тетрагідрофуран, толуол, ксилен і їх суміші, але кращим є 2-метил-тетрагідрофуран. Краще етап b) проводити з використанням карбонільної сполуки, вибраної з групи альдегідів, таких як, наприклад, формальдегід, ацетальдегід, пропанал, бутанал, пентанал, гексанал і т.п. і кетонів, таких як, наприклад, ацетон, етилметил кетон, ізобутилметил кетон і т.п. Краще використовувати формальдегід і як джерело формальдегіду використовувати зокрема полімери, такі як деполімеризовані у зручний спосіб параформальдегід або триоксан. Краще етап b) проводити, використовуючи молярне співвідношення між 1-бензил-3галогено-1H-індазолом формули (III) і карбонільною сполукою формули R1-CO-R2 між 1 і 6. Краще етап b) проводити при температурі між -30 °C і +30 °C, краще при температурі між 10 °C і 0 °C. Краще етап b') проводити, використовуючи алкіламід, вибраний з групи, яка включає N,Nдиметилформамід, N,N-діетилформамід, N,N-ди-n-пропілформамід, N1N-диметилацетамід, N,Nдіетилацетамід, N,N-ди-n-пропілацетамід, N,N-диметилпропіонамід, N,N-діетилпропіонамід, N,N-ди-n-пропілпропіонамід, краще - N,N-диметилформамід. Краще етап b') проводити при температурі між -30 °C і +30 °C, краще – при температурі між 10 °C і 0 °C. Зокрема, етап b') проводять, використовуючи молярне співвідношення між 1-бензил-31 11 галоген-1H-індазолом формули (III) і амідом R R N-CO-Ri між 1 і 4. Краще, коли відновлювальний агент карбонільної групи, який використовують на етапі b') вибирати з групи, яка включає гідриди, такі як, наприклад, NaBH 4, KBH4, LiBH4, Zn(BH4)2, Ca(BH4)2, NaAIH4, LiAIH4, Et3SiH, Bu3SnH, i-Bu2AIH, 70 % NaAIH2(OCH2CH2OCH3)2 у толуолі та похідні. Відновлювальний агент карбонільної групи краще являє собою 70 % NaAlH2(OCH2CH2OCH3)2 у толуолі. Відновлювальні агенти карбонільної групи широко висвітлюються в літературі (описані, наприклад, у Smith, March, March's Advanced Organic Chemistry, 5th ed., pages 1197-1205, John Wiley & Sons, Inc. і Carey, Sundberg, Advanced Organic Chemistry, 4th ed., pages 262-290). Краще відновлення на етапі b') проводити в присутності придатного розчинника, такого як, наприклад, тетрагідрофуран, 2-метил-тетрагідрофуран, діетиловий етер, діоксан, tбутилметиловий етер, дибутиловий етер, ксилен, толуол, дихлорметан, хлороформ, n-гексан, nгептан, метанол, етанол, n-пропанол, i-пропанол, диглім (біс-(2-метоксиетиловий)етер), піридин, диметилсульфоксид (DMSO), оцтова кислота, їх суміші і т.п., краще - толуол, ксилен, тетрагідрофуран, 2-метил-тетрагідрофуран і їх суміші. Краще відновлення на етапі b') проводити при температурі між 10° і 100 °C, краще - при температурі між 20 °C і 60 °C. Зокрема відновлення карбонільної групи на етапі b') проводити, використовуючи число еквівалентів гідриду між 1 і 3, краще - 2. Краще групи R1-R8 у формулах (II), (III), (IV) і (VIII), вказаних вище, можуть мати наступні значення. Краще, коли R1 і R2, які можуть бути однаковими або різними, представлені атомом водню, алкільною групою, яка включає від 1 до 3 атомів вуглецю. Краще, коли R3, R4 і R8, які можуть бути однаковими або різними, можуть являти собою водень, метильну групу, етильну групу, метокси групу, етокси групу, атом хлору і атом фтору. 6 UA 106886 C2 5 10 15 20 Краще R5 може бути воднем, метильною групою, етильною групою, метокси групою, етокси групою, атомом хлору і атомом фтору, або разом з a атомом фтору, або разом з одним з R 6 і R7 може утворювати кільце, яке містить 6 атомів вуглецю. Краще, коли R6 і R7, які можуть бути однаковими або різними, можуть являти собою водень, метильну групу, етильну групу, або один з R6 і R7 разом з R5 може утворювати кільце, яке включає 6 атомів вуглецю. Краще, коли сполуку (II), одержану згідно зі способом даного винаходу, використовують у способі для одержання похідних 1-бензил-3-гідроксиметил-1H-індазолу, представлених наступною формулою (I): у якій R1-R8 мають значення вказані у формулі (II) вище, R10 і R11, які можуть бути однаковими або різними, являють собою водень або алкільну групу, яка включає від 1 до 5 атомів вуглецю. R12 являє собою алкільну групу, яка включає від 1 до 4 атомів вуглецю. Краще, коли спосіб одержання похідних 1-бензил-3-гідроксиметил-1H-індазол, наведених у вищевказаній формулі (I) передбачає, що a) 1-бензил-3-гідроксиметил-1H-індазол або його похідне, представлені наступною формулою (II): 25 у якій R1-R8 мають вищевказані і значення, вводять у реакцію з галоїдводневою кислотою формули HX", де X" являє собою атом галогену, вибраний з групи, яка складається з хлору, брому і йоду, краще – хлор, для утворення 1-бензил-3-галоїдметил-1H-індазолу або його похідного, представлених наступною формулою (V): 30 у якій R1-R8 і X" мають вищевказані значення, b)1-бензил-3-галоїдметил-1H-індазол або його похідне, представлені вищенаведеною формулою (V), вводять у реакцію у присутності сильної основи зі сполукою, представленою наступною формулою (Vl): 7 UA 106886 C2 5 10 15 20 25 30 35 40 45 50 у якій R10, R11, які можуть бути однаковими або різними, і R12 мають вищевказані значення, для утворення похідних 1-бензил-3-гідроксиметил-1H-індазолу, представлених вищенаведеною формулою (I). Альтернативно, спосіб одержання похідних 1-бензил-3-гідроксиметил-1H-індазолу, представлених вищенаведеною формулою (I) передбачає, що: a') 1-бензил-3-гідроксиметил-1H-індазол або його похідне, представлені вищенаведеною формулою (II), вводять в реакцію в присутності сильної основи з сполукою, представленою наступною формулою (VII) у якій R10, R11, які можуть бути однаковими або різними, і R12 мають вищевказані значення, і X'" являє собою атом галогену, вибраний з групи, яка складається з хлору, брому і йоду, краще – бром, для утворення похідних 1-бензил-3-гідроксиметил-1H-індазолу, представлених вищенаведеною формулою (I). Краще, коли вищевказаний спосіб одержання похідних 1-бензил-3-гідроксиметил-1Hіндазолу, представлених формулою (I), може включати утворення солі карбоксильної групи, представленою формулою -COOR12, шляхом обробки фармацевтично прийнятною органічною або неорганічною основою. Цю обробку можна проводити безпосередньо на відповідній кислоті, коли R12 є воднем, або після реакції гідролізу естеру, коли R12 являє собою алкільну групу, яка включає від 1 до 4 атомів вуглецю. Краще, коли етап a) проводять у водному розчині або органічному розчиннику. Гідридводнева кислота формули HX", яку використовують, являє собою концентровану або розведену соляну кислоту, бромистоводневу кислоту або йодистоводневу кислоту у такій концентрації, щоб мати молярне співвідношення між кислотою і сполукою формули (II) між 1 і 20, краще - між 1 і 5, і найкраще - приблизно 3. Краще, коли етап a) проводять при температурі між 25 °C і 100 °C, краще при температурі між 60 °C і 90 °C. Органічний розчинник, який краще використовувати на етапі a), вибирають з групи, яка включає толуол, ксилен, оцтову кислоту, діоксан, дибутиловий етер, 2-метил-тетрагідрофуран. Краще, коли етап b) проводять в апротонних розчинниках, таких як, наприклад, тетрагідрофурані, діоксані, N,N-диметилформаміді, толуолі, N-метилпіролідоні, диметилсульфорксиді, гексаметилфосфаміді, ацетоні, ізобутилметил кетоні, метилетил кетоні, або їх суміші, краще – толуолі або N,N-диметилформаміді і їх сумішах. Сильну основу, яку використовують на етапі b), краще вибрати з групи, яка включає гідрид натрію, металевий натрій, металевий калій, бутил літій, літій-диізопропіл амід, амід натрію, гідрид калію, кращим є гідрид натрію. Краще етап b) проводити, використовуючи α-гідрокси кислоту, вибрану з групи, яка включає гідроксиоцтову кислоту, молочну кислоту, α-гідроксиізомасляну кислоту, α-гідроксимасляну кислоту, 2-етил-гідроксимасляну кислоту, 2-гідроксиізовалеріанову кислоту, 2-гідрокси-3,3диметилмасляну кислоту, 2-гідроксиізокапронову кислоту, кращою є α-гідроксиізомасляна кислота. Краще етап b) проводити, використовуючи α-гідроксиестер, вибраний з групи, яка включає метил гліколят, етил гліколят, бутил гліколят, метил лактат, етил лактат, бутил лактат, t-бутил лактат, ізопропіл лактат, ізобутил лактат, метил-2-гідроксиізобутират, етил-2-гідроксиізобутират, етил-2-гідроксивалеріат, t-бутил-2-гідроксибутират, кращим є етил-2-гідроксиізобутират. Краще, коли молярне співвідношення між 1-бензил-3-галометил-1H-індазололом формули (V) і α-гідроксикислотою або естером формули (Vl) знаходиться між 1 і 2, краще – приблизно 1,2. Зокрема, молярне співвідношення між α-гідроксикислотою формули (Vl) і сильною основою знаходиться між 1 і 3, краще – приблизно 2. Подібним чином молярне співвідношення між αгідроксиестером формули (Vl) і сильною основою знаходиться між 1 і 1.5, краще – приблизно 1. Краще, коли сполука, представлена формулою (VII), яку використовують на етапі a') являє 8 UA 106886 C2 5 10 15 20 25 30 35 40 45 50 55 60 собою α-галоїдкислоту, вибрану з групи, яка включає бромоцтову кислоту, 2-бромпропіонову кислоту, 2-броммасляну кислоту, 2-бромізомасляну кислоту, 2-бром-2-бутилпропіонову кислоту, 2-бромвалеріанову кислоту, α-бромізовалеріанову кислоту, кращою є α-бромізомасляна кислота. Краще етап a') проводити з молярним співвідношенням 1-бензил-3-гідроксиметил-1Hіндазолом формули (II) і α-галоїдкислотою або естером формули (VII) між 1 і 3, краще приблизно 3. Краще етап a') проводити у апротонних розчинниках, таких як, наприклад, тетрагідрофуран, діоксан, N,N-диметилформамід, толуол, N-метилпіролідон, диметилсульфоксид, гексаметилфосфорамід, ацетон, ізобутилметил кетон, метилетил кетон, або їх сумішах, краще – метилетилкетоні. Сильну кислоту, яку використовують на етапі a'), краще вибрати з групи, яка включає гідрид натрію, гідрид калію, металевий натрій, металевий калій, гідроксид натрію, гідроксид калію, кращим є гідроксид натрію. Молярне співвідношення між 1-бензил-3-гідроксиметил-1H-індазолом формули (II) і сильною основою краще знаходиться між 1 і 15, і краще - приблизно 9. Краще, коли етап a') проводять при температурі між 25 °C і 100 °C, краще – при температурі між 50 °C і 70 °C. Краще, коли групи R1-R12 у формулах (I), (II), (V), (Vl) і (VII), вказаних вище, можуть мати наступні значення. Краще, коли, R1 і R2, які можуть бути однаковими, або різними, представлені атомом водню, або алкільною групою, яка включає від 1 до 3 атомів вуглецю. Краще, коли R3, R4 і R8, які можуть бути однаковими, або різними, можуть являти собою водень, метильну групу, етильну групу, метокси групу, етокси групу, атом хлору і атом фтору. Краще, коли R5 може являти собою водень, метильну групу, етильну групу, метокси групу, етокси групу, атом хлору, атом фтору, або разом з одним з R 6 і R7 може утворювати кільце, яке включає 6 атомів вуглецю. Краще, коли R6 і R7, які можуть бути однаковими, або різними, можуть являти собою водень, метильну групу, етильну групу, або один з R6 і R7 разом з R5 може утворювати кільце, яке включає 6 атомів вуглецю. Краще, коли R10 і R11, які можуть бути однаковими, або різними, являють собою водень або алкільну групу, яка включає 1-3 атоми вуглецю і R12 являє собою водень або алкільну групу, яка включає 1-3 атоми вуглецю. Наступні приклади призначені лише для ілюстрації даного винаходу без обмеження його у будь-який спосіб. ЕКСПЕРИМЕНТАЛЬНА ЧАСТИНА Сполуки 3-йод-1H-індазолу і 1-бензил-3-йод-1H-індазолу були одержані згідно зі способом, описаним Collot et al. (Tetrahedron, 55, 6917, 1999). Сполука 3-бром-1H-індазолу була одержана згідно зі способом, описаним Coller et al. [Aust. J. Chem. 1974, 27, 2343). Приклад 1 Одержання 1-бензил-3-броміндазолу 3-бром-1H-індазол (90,4 г, 0,459 моль, 1,0 екв.) і толуол (450 мл) помістили в колбу ємністю 1 літр з механічною мішалкою в атмосфері азоту. Потім при кімнатній температурі протягом більше ніж півгодини додавали калій t-бутоксид (t-BuOK, 54,2 г, 0,483 моль, 1,05 екв.) і протягом більше, ніж приблизно 1,5 години додавали бензилбромід (86,3 г, 0,505 моль, 1,1 екв.). Суміш залишили перемішуватись при такій же температурі до повного завершення реакції (визначено за допомогою ТШХ, приблизно 3 години). Потім додавали 0,1 M HCI (45 мл) і воду (90 мл) і одержані фази розділяли. Органічну фазу промивали водою і розчинник випаровували при зниженому тиску для одержання червоного залишку. Потім продукт осаджували шляхом додавання n-гептану і висушували в умовах вакууму при кімнатній температурі Вихід: 65,9 г бежевого твердого залишку (вихід 50 %). 1 H ЯМР (300 MHz, DMSO-d6) δ (ppm) 5,67 (s, 2H), 7,29 (m, 6H), 7,50 (ddd, 1H, J=8,6 Hz, 6,9 Hz, 1,0 Hz), 7,60 (dd, 1H, J=8,2 Hz, 0,7 Hz), 7,80 (dd, 1H, J=8,6 Hz, 0,7 Hz). 13 C ЯМР (300 MHz, DMSO-d6) δ (ppm) 52,2, 1 10,4, 1 19,5, 121,7, 122,9, 127,4, 127,4, 127,6, 127,7, 128,6, 128,6, 129,6, 136,9, 140,5. Приклад 2 Одержання 1-бензил-3-гідроксиметил-1H-індазолу Приготували розчин i-пропілмагній хлориду (i-PrMgCI) в 2-метилтетрагідрофурані (Me-ТГФ) в придатній ретельно висушеній колбі, яку витримували в атмосфері азоту, з металевого магнію (Mg, 10,91 г, 0,4489 моль, 1,5 екв.), активованого кристалами йоду і розчині ізопропіл хлориду (i 9 UA 106886 C2 5 10 15 20 25 30 35 40 45 50 55 60 PrCI, 41,0 мл, 0,4489 моль, 1,5 екв.) безводному Me-ТГФ(185 мл). Після охолодження до приблизно -10 °C додавали розчин 1-бензил-3-йод-1H-індазолу (100 г, 0,2993 моль, 1,0 екв.) в безводному Me-ТГФ (120 мл) протягом більше 1 години, підтримуючи постійною кімнатну температуру. Реакційну суміш перемішували ще годину для завершення обміну галоген/магній і одержали жовту суспензію. Пропускали газоподібний формальдегід (генерований нагріванням суспензії 54 г параформальдегіду в 150 мл ксилену при приблизно 115 °C) протягом приблизно двох годин при температурі нижче 0 °C. Коли реакція завершилась, додавали розведену H 3PO4 і надлишок ре-полімеризованого параформальдегіду видаляли шляхом фільтрації. Фази розділяли і органічну фазу потім промивали розведеним розчином NaHCO3 і потім концентрували. Продукт, осаджений шляхом додавання n-гексану, збирали шляхом фільтрації і висушували. Вихід: 56,8 г білого твердого залишку (79,6 %). Температура плавлення: 85-86 °C 1 H ЯМР (300 MHz, DMSO-d6) δ (ppm) 4,79 (d, 2H, J=5,8 Hz), 5,27 (t, 1H, J=5,8 Hz), 5,6 (s, 2H), 7,12 (t, 1H, J=7,5 Hz), 7,28 (m, 5H), 7,36 (t, 1H, J=7,2 Hz), 7,64 (d, 1H, J=8,5 Hz), 7,86 (d, 1H, J=8,2 Hz). 13 C ЯМР (300 MHz, DMSO-d6) δ (ppm) 51,6, 56,6, 109,6, 120,0, 120,9, 122,2, 126,2, 127,3, 127,3, 127,4, 128,5, 128,5, 137,7, 140,3, 145,2. Приклад 3 Одержання 1-бензил-3-гідроксиметил-IH-індазолу Розчин 2M i-PrMgCI в ТГФ (69 мл, 138 ммоль, 4.0 екв.) додавали до придатної ретельно висушеної колби в атмосфері азоту. Розчин охолоджували до приблизно -10 °C. Протягом більше ніж однієї години при постійній температурі додавали розчин 1-бензил-3-бром-1Hіндазолу (10 г, 34,8 ммоль, 1,0 екв.) в безводному ТГФ (40 мл). Реакційну суміш перемішували протягом принаймні 6 годин і одержали жовту суспензію. При температурі нижче 0 °C протягом приблизно двох годин над цим пропускали газоподібний формальдегід (одержаний нагріванням суспензії 16,7 г параформальдегіду у 60 мл ксилену при приблизно 115 °C). Після повної завершення реакції додавали розведену H3PO4 і залишок ре-полімеризованого параформальдегіду видаляли за допомогою фільтрації. До суміші додавали Me-ТГФ (60 мл) і фази розділяли. Органічну фазу промивали розведеним розчином NaHCO 3. Після концентрування органічної фази одержали олійний, який містив продукт. Наступне очищення сирого продукті з допомогою хроматографії на силікагелі дало 2,8 г білого твердого продукту (вихід: 34 %). Температура плавлення: 85-86 °C 1 H ЯМР (300 MHz, DMSO-d6) δ (ppm) 4,79 (d, 2H, J=5,8 Hz), 5,27 (t, 1H, J=5,8 Hz), 5,6 (s, 2H), 7,12 (t, 1H, J=7,5 Hz), 7,28 (m, 5H), 7,36 (t, 1H, J=7,2 Hz), 7,64 (d, 1H, J=8,5 Hz), 7,86 (d, 1H, J=8,2 Hz). 13 C ЯМР (300 MHz, DMSO-d6) δ (ppm) 51,6, 56,6, 109,6, 120,0, 120,9, 122,2, 126,2, 127,3, 127,3, 127,4, 128,5, 128,5, 137,7, 140,3, 145,2. Приклад 4 Одержання 1-бензил-3-хлорметил-1H-індазолу 1-бензил-3-гідроксиметил-1H-індазол (400 г, 1,7 моль, 1 екв.), толуол (1,6 л) і концентровану HCI (422 мл, 5,1 моль, 3,0 екв.) додавали до колби з трьома горлечками, обладнаною механічною мішалкою і конденсатором зі зворотним холодильником. Реакційну суміш нагрівали до приблизно 90 °C і перемішували до повного завершення реакції (визначено за допомогою ТШХ, приблизно дві години). Після охолодження до кімнатної температури додавали NaCI (приблизно 10 г), фази розділяли і водну фазу вивантажували. Органічну фазу промивали насиченим розчином NaHCO 3 (приблизно 100 мл) і потім концентрували. Продукт осаджували шляхом додавання n-гексану (приблизно 500 мл), фільтрували і висушували. Вихід: 398,2 г білого твердого продуту (91 %). температура плавлення: 89-91 °C 1 H ЯМР (300 MHz, DMSO-d6) δ (ppm) 5,14 (s, 2H), 5,65 (s, 2H), 7,27 (m, 6H), 7,43 (m, 1H), 7,12 (d, 1H, J=8,5 Hz), 7,88 (d, 1H, J=8,2 Hz) 13 C ЯМР (300 MHz, DMSO-d6) δ (ppm) 38,2, 51,8, 110,2, 120,1, 120,9, 121,7, 126,7, 127,3, 127,3, 127,5, 128,5, 128,5, 137,2, 140,4, 140,6. Приклад 5 Одержання 2-[(1-бензил-1H-індазол-3-іл)метокси]-2-метилпропанової кислоти Етил-2-гідроксиізобутират (18,5 г, 140 ммоль, 1,2 екв.), толуол (100 мл) і ДМФ (20 мл) поміщали до колби з трьома горлечками, обладнаної механічною мішалкою і конденсатором зі зворотним холодильником в інертній атмосфері. До суміші частинами протягом періоду приблизно 1,5 години додавали дисперсію 60 % NaH (5,6 г, 140 ммоль, 1,2 екв.). Потім по 10 UA 106886 C2 5 10 15 20 25 30 35 40 45 50 55 краплинах додавали 1-бензил-3-хлорметил-1H-індазол (30 г, 117 ммоль, 1 екв.) у толуолі (90 мл) і ДМФ (60 мл). Реакційну суміш нагрівали до приблизно 90 °C і витримували при цій же температурі до повного завершення реакції (визначено за допомогою ТШХ, приблизно 10 годин). Після охолодження до кімнатної температури суміш промивали підкисленою водою і водою. Органічну фазу концентрували при зниженому тиску і одержаний олійний залишок обробляли 10 M NaOH (36 мл) при температурі кип'ятіння зі зворотним холодильником протягом принаймні 3 годин. Продукт, який осаджували за допомогою концентрованої HCI, фільтрували і висушували. Вихід: 32,3 г білого твердого продукту (85 %). Температура плавлення: 133-134 °C. Елементарний аналіз: Розраховано: C (70,35), H (6,21), N (8,64), Визначено: C (70,15), H (6,17), N (8,63). 1 H ЯМР (300 MHz, DMSO-d6) δ (ppm) 1,44 (s, 6H), 4,76 (s, 2H), 5,60 (s, 2H), 7,14 (t, 1H, J=7,6 Hz), 7,20-7,34 (m, 5H), 7,37 (ddd, 1H, J=8,3 Hz, 7,0 Hz, 1,1Hz), 7,66 (d, 1H, J=8,4 Hz), 7,94 (d, 1H, J=8,1Hz), 12,77 (s, 1H). 13 C ЯМР (300 MHz, DMSO-d6) δ (ppm) 24,48, 24,48, 51,63, 59,65, 76,93, 109,69, 120,22, 121,06, 122,62, 126,28, 127,36, 127,36, 127,44, 128,46, 128,46, 137,49, 140,31, 141,97, 175,46. Приклад 6 Одержання 1-бензил-IH-індазол-3-карбальдегіду Розчин i-PrMgCI в ТГФ готували у придатній ретельно висушеній колбі в атмосфері азоту з металевого магнію (Mg, 164 мг, 6,75 ммоль, 1,5 екв.), активованого кристалами йоду, і розчині iPrCI (0,62 мл, 6,75 ммоль, 1,5 екв.) в безводному ТГФ (2,8 мл). Після охолодження до приблизно -10 °C до реакційної суміші протягом більше ніж однієї години додавали розчин 1-бензил-3-йод-1H-індазолу (1,5 г, 4,5 моль, 1,0 екв.) в безодному ТГФ(5 мл) при постійній температурі. Реакційну суміш перемішували ще одну додаткову годину до завершення обміну галоген/магній, в результаті одержали жовту суспензію. При перемішуванні до суспензії протягом більше ніж однієї години при температурі нижче 0 °C додавали диметилформамід (ДМФ) (1,4 мл, 18 моль, 4 екв.) і реакційну суміш перемішували протягом ще однієї години при цій же температурі до повного завершення реакції (визначено за допомогою ТШХ). До реакційної суміші додавали розведену H 3PO4 і толуол і фази розділяли. Органічну фазу промивали розведеним розчином NaHCO3. Після концентрування органічної фази продукт осаджували шляхом додавання n-гексану, фільтрували і висушували. Вихід: 1,0 г жовтуватого твердого продукту (94 %). 1 H ЯМР (300 MHz, DMSO-d6) δ (ppm) 5,84 (s, 2H), 7,32 (m, 5H), 7,39 (ddd, 1H, J=8,1Hz, 7,0 Hz, 1,0 Hz), 7,53 (ddd, 1H, J=8,4 Hz, 7,0 Hz, 1,2 Hz) 7,90 (dt, 1H, J=8,5 Hz, 1,0 Hz), 8,16 (dt, 1H, J=8,1Hz, 1,2 Hz), 10,19 (s, 1H). 13 C ЯМР (300 MHz, DMSO-d6) δ (ppm) 52,9, 111,0, 121,0, 121,2, 124,2, 127,5, 127,6, 127,6, 127,9, 128,6, 128,6, 136,2, 140,7, 142,4, 186,8. Приклад 7 Одержання 1-бензил-3-гідроксиметил-IH-індазолу 1-бензил-I H-індазол-3-карбальдегід (2,36 г, 10 ммоль, 1 екв.) і толуол (12 мл) поміщали в ретельно висушену 100 мл колбу, обладнану магнітною мішалкою в інертній атмосфері азоту. Потім до розчину при кімнатній температурі повільно додавали 70 % розчин натрій дигідробіс(2-метоксиетокси)алюмінату в толуолі (2,8 мл, 10 ммоль, 2 екв.). Після повного завершення реакції (після приблизно 15 хвилин) додавали 2 M HCI (10 мл), H 2O (10 мл) і толуол (15 мл). Фази розділяли і водну фазу двічі екстрагували толуолом. Об'єднані органічні фази промивали водою і концентрували. Потім продукт осаджували шляхом додавання n-гексану, фільтрували і висушували. Вихід: 1,95 г білого твердого продукту (82,0 %). Температура плавлення: 85-86 °C. 1 H ЯМР (300 MHz, DMSO-d6) δ (ppm) 4,79 (d, 2H, J=5,8 Hz), 5,27 t, 1H, J=5,8 Hz), 5,6 (s, 2H), 7,12 (t, 1H, J=7,5 Hz), 7,28 (m, 5H) 7,36 (t, 1H, J=7,2 Hz), 7,64 (d, 1H, J=8,5 Hz), 7,86 (d, 1H, J=8,2 Hz). 13 C ЯМР (300 MHz, DMSO-d6) δ (ppm) 51,6, 56,6, 109,6, 120,0, 120,9, 122,2, 126,2, 127,3, 127,3, 127,4, 128,5, 128,5, 137,7, 140,3, 145,2. 11 UA 106886 C2 ФОРМУЛА ВИНАХОДУ 5 1. Спосіб одержання формулою (II): 1-бензил-3-гідроксиметил-1Н-індазолу, представленого наступною R2 R1 OH N R8 N R6 R3 R7 R5 10 15 20 R4 , (II) у якій R1 і R2, які можуть бути однаковими або різними, являють собою водень або алкільну групу, яка включає від 1 до 6 атомів вуглецю, R3, R4 і R8, які можуть бути однакові або різні, можуть являти собою водень, алкільну групу, яка включає від 1 до 5 атомів вуглецю, алкоксильну групу, яка включає від 1 до 3 атомів вуглецю, та атом галогену, R5 може являти собою водень, алкільну групу, яка включає від 1 до 5 атомів вуглецю, алкоксильну групу, яка включає від 1 до 3 атомів вуглецю, атом галогену, або разом з одним з R6 і R7 може утворювати кільце, яке включає 5 або 6 атомів вуглецю, і R6 і R7, які можуть бути однакові або різні, можуть являти собою водень, алкільну групу, яка включає від 1 до 5 атомів вуглецю, або один з R6 і R7 разом з R5 може утворювати кільце, яке включає 5 або 6 атомів вуглецю, у якому а) 1-бензил-3-галоген-1H-індазол формули (III): X N R8 N R6 R3 R7 R5 25 R4 , (III) у якій X являє собою атом галогену, вибраний з йоду та брому, краще - йоду, вводять у реакцію з галоїдом алкілмагнію формули RMgX', де R являє собою алкільну групу з 1 до 6 атомами вуглецю і X' являє собою атом галогену, вибраний з брому і хлору, краще - хлору, з утворенням проміжної сполуки (IV): MgX' N R8 N R6 R3 R7 R5 R4 , (IV) b) вказану проміжну сполуку (IV) вводять у реакцію з карбонільною сполукою формули R1-COR2, з утворенням сполуки формули (II), або, альтернативно до стадії b), 12 UA 106886 C2 b') вказану проміжну сполуку (IV) вводять у реакцію з амідом формули R'R''N-CO-R1, де R' і R", які можуть бути однакові або різні, являють собою алкільну групу, яка включає від 1 до 3 атомів вуглецю, з утворенням проміжної сполуки (VIII): R1 O N R8 N R6 R3 R7 5 10 15 20 25 30 35 40 45 R5 R4 , (VIII) яку вводять в реакцію з відновлювальним агентом карбонільної групи з утворенням сполуки формули (II). 2. Спосіб одержання 1-бензил-3-гідроксиметил-1Н-індазолу, представленого формулою (II) за п. 1, у якому вказані етапи а) і b) проводять в присутності розчинника, вибраного з групи, яка включає тетрагідрофуран, 2-метилтетрагідрофуран, діетиловий етер, діоксан, t-бутилметиловий етер, дибутиловий етер, ксилен, толуол, дихлорметан, хлороформ, n-гексан, n-гептан і їх суміші, і вказаний етап b') проводять в присутності розчинника, вибраного з групи, яка включає тетрагідрофуран, 2-метилтетрагідрофуран, діетиловий етер, діоксан, t-бутилметиловий етер, дибутиловий етер, ксилен, толуол, дихлорметан, хлороформ, n-гексан, n-гептан, метанол, етанол, n-пропанол, і-пропанол, диглім, піридин, ДМСС, оцтову кислоту і їх суміші. 3. Спосіб одержання 1-бензил-3-гідроксиметил-1Н-індазолу, представленого формулою (II) за п. 1, у якому вказаний галоїд алкілмагнію формули RMgX' вибирають з групи, яка включає метилMgCl, етилMgCl, n-пропілMgCl, i-пропілMgCl, n-бутилMgCl, і-бутилMgCl, сек-бутилMgCl, tбyтилMgCl, n-пeнтилMgCl, n-гексилMgCl, алілMgCl, циклoгeкcилMgCl, мeтилMgBr, етилMgBr, nпропілMgBr, i-пpoпiлMgBr, n-бутилMgВr, i-бутилMgBr, sec-бyтилMgBr, t-бутилMgBr, nпентилМgВr, n-гексилMgВr, aлiлMgBr, циклoгeкcилMgBr, де кращим є i-пропілMgCl. 4. Спосіб одержання 1-бензил-3-гідроксиметил-1Н-індазолу, представленого формулою (II) за п. 1, у якому вказаний етап а) проводять при молярному співвідношенні між галоїдом алкілмагію формули RMgX' і 1-бензил-3-галогено-1Н-індазолом формули (III) між 1 і 4, краще - між 1,5 і 4. 5. Спосіб одержання 1-бензил-3-гідроксиметил-1Н-індазолу, представленого формулою (II) за п. 1, у якому вказану карбонільну сполуку формули R1-CO-R2 вибирають з групи, яка включає альдегіди і кетони. 6. Спосіб одержання 1-бензил-3-гідроксиметил-1Н-індазолу, представленого формулою (II) за п. 1, у якому вказану карбонільну сполуку формули R1-CO-R2 вибирають з групи, яка включає формальдегід, ацетальдегід, пропанал, бутанал, пентанал, гексанал, ацетон, метилетилкетон і ізобутилметилкетон, де кращим є формальдегід. 7. Спосіб одержання 1-бензил-3-гідроксиметил-1Н-індазолу, представленого формулою (II) за п. 1, у якому вказаний етап b) проводять при молярному співвідношенні між 1-бензил-3-галогено1Н-індазолом формули (III) і карбонільною сполукою формули R1-CO-R2 між 1 і 6. 8. Спосіб одержання 1-бензил-3-гідроксиметил-1H-індазолу, представленого формулою (II) за п. 1, у якому вказаний амід формули R'R''N-CO-R1 вибирають з групи, яка включає Ν,Νдиметилформамід, Ν,Ν-діетилформамід, Ν,Ν-ди-n-пропілформамід, Ν,Ν-диметилацетамід, Ν,Νдіетилацетамід, Ν,Ν-ди-n-пропілацетамід, Ν,Ν-диметилпропіонамід, N,N-діетилпропіонамід і Ν,Ν-ди-n-пропілпропіонамід, де кращим є Ν,Ν-диметилформамід. 9. Спосіб одержання 1-бензил-3-гідроксиметил-1H-індазолу, представленого формулою (II) за п. 1, у якому вказаний етап b') проводять при молярному співвідношенні між 1-бензил-3-галогено1H-індазолом формули (III) і амідом формули R'R''N-CO-R1 між 1 і 4. 10. Спосіб одержання 1-бензил-3-гідроксиметил-1H-індазолу, представленого формулою (II) за п. 1, у якому вказаний відновлювальний агент карбонільної групи, який використовують на етапі b'), вибирають з групи, яка включає NaBH4, KBH4, LiBH4, Zn(BH4)2, Ca(BH4)2, NaAlH4, LiAlH4, Et3SiH, Bu3SnH, i-Bu2AlH, 70 % NaAlH2(OCH2CH2OCH3)2 у толуолі, де кращим є 70 % NaAlH2(OCH2CH2OCH3)2 у толуолі. 13 UA 106886 C2 5 10 11. Спосіб одержання 1-бензил-3-гідроксиметил-1Н-індазолу, представленого формулою (II) за п. 1, у якому групи R1-R8 у формулах (II), (III), (IV) і (VIII), вказаних вище, можуть мати наступні значення: R1 і R2, які можуть бути однаковими або різними, представлені атомом водню, алкільною групою, яка включає від 1 до 3 атомів вуглецю, R3, R4 і R8, які можуть бути однаковими, або різними, можуть являти собою водень, метильну групу, етильну групу, метоксигрупу, етоксигрупу, атом хлору і атом фтору, R5 може являти собою водень, метильну групу, етильну групу, метоксигрупу, етоксигрупу, атом хлору, атом фтору, або разом з одним з R6 і R7 може утворювати кільце, яке включає 6 атомів вуглецю, і R6 і R7, які можуть бути однаковими або різними, можуть являти собою водень, метильну групу, етильну групу, або один з R6 і R7 разом з R5 може утворювати кільце, яке включає 6 атомів вуглецю. 12. Проміжна сполука, представлена наступною формулою (IV): MgX' N R8 N R6 R3 R7 15 20 25 30 35 R5 R4 , (IV) у якій X' являє собою атом галогену, вибраний з брому і хлору, R3, R4 і R8, які можуть бути однакові або різні, можуть являти собою водень, алкільну групу, яка включає 1-5 атомів вуглецю, алкоксильну групу, яка включає 1-3 атоми вуглецю, і атом галогену, R5 може являти собою водень, алкільну групу, яка включає 1-5 атомів вуглецю, алкоксильну групу, яка включає 1-3 атоми вуглецю, атом галогену, або разом з одним з R6 і R7 може утворювати кільце, яке включає 5 або 6 атомів вуглецю, і R6 і R7, які можуть бути однакові або різні, можуть являти собою водень, алкільну групу, яка включає 1-5 атомів вуглецю, або один з R6 і R7 разом з R5 може утворювати кільце, яке включає 5 або 6 атомів вуглецю. 13. Проміжна сполука, представлена формулою (IV) за п. 12, у якій: X' являє собою атом хлору, R3, R4 і R8, які можуть бути однакові або різні, можуть являти собою водень, метильну групу, етильну групу, метоксигрупу, етоксигрупу, атом хлору і атом фтору, R5 може являти собою водень, метильну групу, етильну групу, метоксигрупу, етоксигрупу, атом хлору і атом фтору, або разом з одним з R6 і R7 може утворювати кільце, яке включає 6 атомів вуглецю, R6 і R7, які можуть бути однакові або різні, можуть являти собою водень, метильну групу, етильну групу, або один з R6 і R7 разом з R5 може утворювати кільце, яке включає 6 атомів вуглецю. Комп’ютерна верстка Л. Литвиненко Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 14
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 1-benzyl-3-hydroxymethyl-1h-indazole and its derivatives and required magnesium intermediates
Автори англійськоюCaracciolo Torchiarolo, Giuliano, Iacoangeli, Tommaso, Furlotti, Guido
Автори російськоюКараччоло Торкяроло Джулиано, Якоанджели Томмазо, Фурлотти Гвидо
МПК / Мітки
МПК: C07D 231/56, C07F 3/00
Мітки: 1-бензил-3-гідроксиметил-1н-індазолу, магнію, проміжні, похідних, спосіб, сполуки, одержання
Код посилання
<a href="https://ua.patents.su/16-106886-sposib-oderzhannya-1-benzil-3-gidroksimetil-1n-indazolu-i-jjogo-pokhidnikh-ta-promizhni-spoluki-magniyu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 1-бензил-3-гідроксиметил-1н-індазолу і його похідних та проміжні сполуки магнію</a>
Попередній патент: Dig-3 інсектицидні cry-токсини
Наступний патент: Похідні спіроциклічних амідів
Випадковий патент: Установка для електрогідравлічної очистки відливок












