Заміщені (2s)-2-етокси-3-фенілпропанові кислоти
Номер патенту: 80729
Опубліковано: 25.10.2007
Автори: Мінідіс Анна, Дальстром Мікаель Ульф Йоган, Орелль Карл-Йоган, Ліндстедт Альстермарк Ева-Лотт, Лі Ланна, Ольссон Анна Крістіна, Юсефі-Салакдех Есмаіл
Формула / Реферат
1. S-енантіомер сполуки формули І

де R1 представляє хлор, трифлуорметил або трифлуорметоксил, R2 представляє Н або флуор, a R3 представляє С2-4алкіл, а також його фармацевтично прийнятні солі, сольвати та проліки.
2. Сполука, яку вибирають з групи:
(2S)-3-[4-(2-{бутил[2-флуор-4-(трифлуорметил)бензил]аміно}-2-оксоетокси)феніл]-2-етоксипропанова кислота;
(2S)-3-(4-{2-[(4-хлорбензил)(етил)аміно]-2-оксоетокси}феніл)-2-етоксипропанова кислота;
(2S)-2-етоксі-3-[4-(2-{етил[4-(трифлуорметокси)бензил]аміно}-2-оксоетокси)феніл]пропанова кислота;
(2S)-2-етоксі-3-[4-(2-{етил[4-(трифлуорметил)бензил]аміно}-2-оксоетокси)феніл]пропанова кислота та
(2S)-3-[4-(2-{бутил[4-(трифлуорметил)бензил]аміно}-2-оксоетокси)феніл]-2-етоксипропанова кислота;
та її фармацевтично прийнятні солі та сольвати.
3. (2S)-3-[4-(2-{бутил[2-флуор-4-(трифлуорметил)бензил]аміно}-2-оксоетокси)феніл]-2-етоксипропанова кислота та її фармацевтично прийнятні солі.
4. (2S)-3-(4-{2-[(4-хлорбензил)(етил)аміно]-2-оксоетокси}феніл)-2-етоксипропанова кислота та її фармацевтично прийнятні солі.
5. (2S)-2-етоксі-3-[4-(2-{етил[4-(трифлуорметокси)бензил]аміно}-2-оксоетокси)феніл]пропанова кислота та її фармацевтично прийнятні солі.
6. (2S)-2-етоксі-3-[4-(2-{етил[4-(трифлуорметил)бензил]аміно}-2-оксоетокси)феніл]пропанова кислота та її фармацевтично прийнятні солі.
7. (2S)-3-[4-(2-{бутил[4-(трифлуорметил)бензил]аміно}-2-оксоетокси)феніл]-2-етоксипропанова кислота та її фармацевтично прийнятні солі.
8. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-7 у суміші з фармацевтично прийнятними ад'ювантами, розріджувачами та/або носіями.
9. Спосіб лікування або попередження ліпідних розладів (дисліпідемії), асоційованих або не асоційованих з резистентністю до інсуліну, шляхом введення сполуки за будь-яким з пп. 1-7 ссавцю, що цього потребує.
10. Застосування сполуки за будь-яким з пп. 1-7 у виробництві медикаменту для лікування ліпідних розладів (дисліпідемії), асоційованих або не асоційованих з резистентністю до інсуліну.
11. Спосіб лікування або попередження діабету типу 2, шляхом введення ссавцю, що цього потребує, ефективної кількості сполуки формули І за будь-яким з пп. 1-7.
12. Спосіб отримання сполуки формули І, в якому проводять реакцію S-енантіомера сполуки формули II

у котрій R1, R2 та R3 визначено вище, a R4 представляє захисну групу для карбоксильної гідроксигрупи, із засобом зняття захисту.
13. Сполука формули II

у котрій R1, R2 та R3 визначено вище, a R4 представляє захисну групу для карбоксильної гідроксигрупи.
14. Сполука формули III
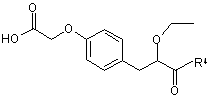 ІІІ,
ІІІ,
у котрій R4 представляє захисну групу для карбоксильної гідроксигрупи.
15. Спосіб отримання сполуки формули І, в якому проводять реакцію сполуки формули V

у котрій R1 та R2 визначено вище, a R представляє Н, або OR представляє захисну групу для карбоксильної гідроксигрупи, зі сполукою формули VI
R3X
VI,
де R3 визначено вище, а X представляє відщеплювану групу, у присутності основи, у присутності інертного розчинника при температурі у межах -25 °С-150 °С та, як варіант, коли OR представляє захисну групу, з подальшим видаленням захисної групи.
16. Сполука формули V, яку вибирають з групи:
(2S)-3-[4-(2-{[2-флуор-4-(трифлуорметил)бензил]аміно}-2-оксоетокси)феніл]-2-етоксипропанова кислота;
(2S)-3-(4-{2-[4-хлорбензиламіно]-2-оксоетокси}феніл)-2-етоксипропанова кислота;
(2S)-2-етокси-3-[4-(2-{4-(трифлуорметокси)бензиламіно}-2-оксоетокси)феніл]пропанова кислота
та (2S)-2-етокси-3-[4-(2-{4-(трифлуорметил)бензиламіно}-2-оксоетокси)феніл]пропанова кислота.
17. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-7 у комбінації з ще одним терапевтичним засобом, що є корисним у лікуванні розладів, асоційованих з розвитком та прогресом атеросклерозу, як-то гіпертензія, гіперліпідемії, дисліпідемії, діабет та ожиріння.
18. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-7 у комбінації з ще одним модулятором АППР.
19. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-7 у комбінації з холестеринзнижувальним засобом.
20. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-7 у комбінації з інгібітором HMG-CoA редуктази.
21. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-7 у комбінації з аторвастатином або його фармацевтично прийнятними сіллю, сольватом, кристалічною формою або проліками.
22. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-7 у комбінації з розувастатином або його фармацевтично прийнятною сіллю.
23. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-7 у комбінації з інгібітором ТКЖК.
24. Фармацевтична композиція за п. 23, де інгібітор ТКЖК вибирають з групи:
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-1'-феніл-1'-[N'-(карбоксиметил)карбамоїл]метил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N'-
(карбоксиметил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-1'-феніл-1'-[N'-(2-сульфоетил)карбамоїл]метил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N-{(R)-1'-феніл-1'-[N'-(2-сульфоетил)карбамоїл]метил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N'-(2-
сульфоетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N'-(2-сульфоетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-дiоксо-3-бутил-3-етил-5-феніл-7-метилтiо-8-(N-{(R)-a-[N'-(2-карбоксіетил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл7-метилтіо-8-(N-{(R)-a-[N'-(2карбоксіетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N'-(5-карбоксипентил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N'-(2-карбоксіетил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-(N-{a-[N'-(2-cyльфoeтил)кapбaмоїл]-2-флуорбензил)карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N'-(R)-(2-гідрокси-1-карбоксіетил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-(N-{(R)-a-[N'-(R)-(2-гідрокси-1-карбоксіетил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-{N-[(R)-a-(N'-{(R)-1-[N"-(R)-(2-гідрокси-1-карбоксіетил)карбамоїл]-2-гідроксіетил}карбамоїл)бензил]карбамоїлметокси}-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N-{a-[N'-(карбоксиметил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3-бутил-3-етил-5-[феніл-7-метилтіо-8-(N-{a-[N'-
((етокси)(метил)фосфорилметилкарбамоїл)бензил]карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-дioкco-3-бyтил-3-eтил-5-фeнiл-7-мeтилтio-8-{N-[(R)-a-(N'-{2-[(гідрокси)(метил)фосфорил]етил}карбамоїл)бензил]карбамоїлметокси}-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-(N-{(R)-a-[N'-(2-мeтилтio-1-карбоксіетил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-{N-[(R)-a-(N'-{2-
[(метил)(етил)фосфорил]етил}карбамоїл)-4-гідроксибензил]карбамоїлметокси}-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-{N-[(R)-a-(N'-{2-[(метил)(гідрокси)фосфорил]етил}карбамоїл)-4-гідроксибензил]карбамоїлметокси}-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-(N-{(R)-a-[(R)-N'-(2-мeтилcyльфiнiл-1-каpбoкcieтил)каpбамoїл]бeнзил}каpбамoїлмeтoкcи)-2,3,4,5-тeтpагiдpo-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метокси-8-[N-{(R)-a-[N'-(2-
сульфоетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси]-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N-((R)-1-карбокси-2-метилтіоетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N-((S)-1-карбокси-2-(R)-гідроксипропіл)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-дiоксо-3,3-дибутил-5-фенiл-7-метилтiо-8-(N-{(R)-a-[N-((S)-1-карбокси-2-метилпропіл)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N-((S)-1-карбоксибутил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N((S)-1-карбоксипропіл)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N((S)-1-карбоксіетил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-дioксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N-((S)-1-карбокси-2-(R)-гідроксипропіл)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-дiоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N-(2-
сульфоетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N-((S)-1-карбоксіетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N-((R)-1-карбокси-2-метилтіоетил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N-{(S)-1-[N-((S)-2-гідрокси-1-карбоксіетил)карбамоїл]пропіл}карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-(N-{(R)-a-[N-((S)-1-карбокси-2-метилпропіл)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N-((S)-1-карбоксипропіл)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-[N-((R/S)-a-{N-[1-(R)-2-(S)-1-гідрокси-1-(3,4-дигідроксифеніл)проп-2-іл]карбамоїл}-4-гідроксибензил)карбамоїлметокси]-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-a-[N-(2-(S)-3-(R)-4-(R)-5-(R)-2,3,4,5,6-пентагідроксигексил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін та
1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-(N-{(R)-a-[N-(2-(S)-3-(R)-4-(R)-5-(R)-2,3,4,5,6-пентагідроксигексил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
або його фармацевтично прийнятної солі, сольвату, сольвату такої солі або проліків.
Текст
C2 2 UA 1 O , II у котрій R , R та R визначено вище, a R4 представляє захисну групу для карбоксильної гідроксигрупи, із засобом зняття захисту. 13. Сполука формули II 3 80729 O R1 CH2 N O R4 R3 R2 1 O , II O у котрій R , R та R визначено вище, a R4 представляє захисну групу для карбоксильної гідроксигрупи. 14. Сполука формули III O HO 2 3 O O R4 O ІІІ, у котрій R4 представляє захисну групу для карбоксильної гідроксигрупи. 15. Спосіб отримання сполуки формули І, в якому проводять реакцію сполуки формули V O R1 CH2 N H O O OR R2 O ,V у котрій R1 та R2 визначено вище, a R представляє Н, або OR представляє захисну груп у для карбоксильної гідроксигрупи, зі сполукою формули VI R3X VI, де R3 визначено вище, а X представляє відщеплювану гр упу, у присутності основи, у присутності інертного розчинника при температурі у межах -25 °С-150 °С та, як варіант, коли OR представляє захисну груп у, з подальшим видаленням захисної групи. 16. Сполука формули V, яку вибирають з групи: (2S)-3-[4-(2-{[2-флуор-4(трифлуорметил)бензил]аміно}-2оксоетокси)феніл]-2-етоксипропанова кислота; (2S)-3-(4-{2-[4-хлорбензиламіно]-2оксоетокси}феніл)-2-етоксипропанова кислота; (2S)-2-етокси-3-[4-(2-{4(трифлуорметокси)бензиламіно}-2оксоетокси)феніл]пропанова кислота та (2S)-2-етокси-3-[4-(2-{4(трифлуорметил)бензиламіно}-2оксоетокси)феніл]пропанова кислота. 17. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-7 у комбінації з ще одним терапевтичним засобом, що є корисним у лікуванні розладів, асоційованих з розвитком та прогресом атеросклерозу, як-то гіпертензія, гіперліпідемії, дисліпідемії, діабет та ожиріння. 18. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-7 у комбінації з ще одним модулятором АППР. 19. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-7 у комбінації з холестеринзнижувальним засобом. 4 20. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-7 у комбінації з інгібітором HMG-CoA редуктази. 21. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-7 у комбінації з аторвастатином або його фармацевтично прийнятними сіллю, сольватом, кристалічною формою або проліками. 22. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-7 у комбінації з розувастатином або його фармацевтично прийнятною сіллю. 23. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-7 у комбінації з інгібітором ТКЖК. 24. Фармацевтична композиція за п. 23, де інгібітор ТКЖК вибирають з групи: 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-1'-феніл-1'-[N'(карбоксиметил)карбамоїл]метил}карбамоїлметокс и)-2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-a-[N'(карбоксиметил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-1'-феніл-1'-[N'-(2сульфоетил)карбамоїл]метил}карбамоїлметокси)2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N{(R)-1'-феніл-1'-[N'-(2сульфоетил)карбамоїл]метил}карбамоїлметокси)2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-a-[N'-(2сульфоетил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N{(R)-a-[N'-(2-сульфоетил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,5-бензотіазепін; 1,1-дiоксо-3-бутил-3-етил-5-феніл-7-метилтiо-8-(N{(R)-a-[N'-(2карбоксіетил)карбамоїл]бензил}карбамоїлметокси) -2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл7-метилтіо-8-(N{(R)-a-[N'-(2карбоксіетил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N{(R)-a-[N'-(5карбоксипентил)карбамоїл]бензил}карбамоїлметок си)-2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-a-[N'-(2карбоксіетил)карбамоїл]бензил}карбамоїлметокси) -2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-(N-{a[N'-(2-cyльфoeтил)кapбaмоїл]-2флуорбензил)карбамоїлметокси)-2,3,4,5тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N{(R)-a-[N'-(R)-(2-гідрокси-1 5 карбоксіетил)карбамоїл]бензил}карбамоїлметокси) -2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-(N{(R)-a-[N'-(R)-(2-гідрокси-1карбоксіетил)карбамоїл]бензил}карбамоїлметокси) -2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-{N[(R)-a-(N'-{(R)-1-[N"-(R)-(2-гідрокси-1карбоксіетил)карбамоїл]-2гідроксіетил}карбамоїл)бензил]карбамоїлметокси}2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N{a-[N'(карбоксиметил)карбамоїл]бензил}карбамоїлметок си)-2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3-бутил-3-етил-5-[феніл-7-метилтіо-8(N-{a-[N'((етокси)(метил)фосфорилметилкарбамоїл)бензил ]карбамоїлметокси)-2,3,4,5-тетрагідро-1,5бензотіазепін; 1,1-дioкco-3-бyтил-3-eтил-5-фeнiл-7-мeтилтio-8-{N[(R)-a-(N'-{2[(гідрокси)(метил)фосфорил]етил}карбамоїл)бензи л]карбамоїлметокси}-2,3,4,5-тетрагідро-1,5бензотіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-(N{(R)-a-[N'-(2-мeтилтio-1карбоксіетил)карбамоїл]бензил}карбамоїлметокси) -2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-{N[(R)-a-(N'-{2[(метил)(етил)фосфорил]етил}карбамоїл)-4гідроксибензил]карбамоїлметокси}-2,3,4,5тетрагідро-1,5-бензотіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-{N[(R)-a-(N'-{2[(метил)(гідрокси)фосфорил]етил}карбамоїл)-4гідроксибензил]карбамоїлметокси}-2,3,4,5тетрагідро-1,5-бензотіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-(N{(R)-a-[(R)-N'-(2-мeтилcyльфiнiл-1каpбoкcieтил)каpбамoїл]бeнзил}каpбамoїлмeтoкcи) -2,3,4,5-тeтpагiдpo-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метокси-8-[N{(R)-a-[N'-(2сульфоетил)карбамоїл]-4гідроксибензил}карбамоїлметокси]-2,3,4,5тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-a-[N-((R)-1-карбокси-2метилтіоетил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-a-[N-((S)-1-карбокси-2-(R)гідроксипропіл)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; 1,1-дiоксо-3,3-дибутил-5-фенiл-7-метилтiо-8-(N{(R)-a-[N-((S)-1-карбокси-2метилпропіл)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; 80729 6 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-a-[N-((S)-1-карбоксибутил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-a-[N((S)-1карбоксипропіл)карбамоїл]бензил}карбамоїлметок си)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-a-[N((S)-1карбоксіетил)карбамоїл]бензил}карбамоїлметокси) -2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін; 1,1-дioксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-a-[N-((S)-1-карбокси-2-(R)гідроксипропіл)карбамоїл]бензил}карбамоїлметокс и)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін; 1,1-дiоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-a-[N-(2сульфоетил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-a-[N-((S)-1-карбоксіетил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-a-[N-((R)-1-карбокси-2метилтіоетил)карбамоїл]бензил}карбамоїлметокси )-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-a-[N-{(S)-1-[N-((S)-2-гідрокси-1карбоксіетил)карбамоїл]пропіл}карбамоїл]бензил}к арбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5бензотіадіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-(N{(R)-a-[N-((S)-1-карбокси-2метилпропіл)карбамоїл]бензил}карбамоїлметокси) -2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-a-[N-((S)-1-карбоксипропіл)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-[N((R/S)-a-{N-[1-(R)-2-(S)-1-гідрокси-1-(3,4дигідроксифеніл)проп-2-іл]карбамоїл}-4гідроксибензил)карбамоїлметокси]-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-a-[N-(2-(S)-3-(R)-4-(R)-5-(R)-2,3,4,5,6пентагідроксигексил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін та 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-(N{(R)-a-[N-(2-(S)-3-(R)-4-(R)-5-(R)-2,3,4,5,6пентагідроксигексил)карбамоїл]бензил}карбамоїлм етокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін; або його фармацевтично прийнятної солі, сольвату, сольвату такої солі або проліків. 7 80729 Представлений винахід стосується деяких нових похідних (2S)-3-(4-{2-[аміно]-2оксоетокси}феніл)-2-етоксипропанової кислоти, способів отримання таких сполук, їх корисності у лікуванні клінічних станів, залучаючи ліпідні розлади (дисліпідемії) асоційовані або не асоційовані з резистентністю до інсуліну та іншими виявами метаболічного синдрому, способів їх терапевтичного застосування та фармацевтичних композицій, що їх містять. Метаболічний синдром, залучаючи цукровий діабет типу 2, стосується сукупності виявів, залучаючи резистентність до інсуліну з супутньою гіперінсулінемією, можливо цукровий діабет типу 2, артеріальну гіпертензію, центральне (вісцеральне) ожиріння, дисліпідемію, спостережену як порушені рівні ліпопротеїнів, що характеризуються типово підвищеними ЛДНГ (ліпопротеїни дуже 1 низької густини), частинки ЛНГ низької густини та зменшеними ЛВГ (ліпопротеїн високої густини) концентрації та зменшеним фібринолізом. Нещодавнім епідеміологічним дослідженням документовано, що особи з резистентністю до інсуліну мають значно збільшений ризик серцевосудинної захворюваності та смертності, дуже потерпаючи від інфаркту міокарду та інсульту. У цукровому діабеті типу 2 атеросклеротичні стани викликають до 80% усіх смертей. У клінічній медицині відома необхідність підвищення чутливості до інсулін у у пацієнтів з метаболічним синдромом, а відтак корекції дисліпідемії, котра, як вважають, викликає прискорений прогрес атеросклерозу. Однак, зараз це не є універсально прийнятим діагнозом з добре визначеними фармакотерапевтичними показаннями. S-енантіомер сполуки формули С нижче С 2-етокси-3-[4-(2-(4метансульфонілоксифеніл}етокси)феніл]пропанов ої кислоти розкрито [у Міжнародній публікації WO 99/62872]. Ця сполука, як повідомлено, є модулятором активованих проліфератором пероксисоми рецепторів (АППР, для огляду АППР [дивись Т. M.Willson et al, J Med Chem 2000, Vol 43, 527]) та мають поєднану ΑΠΠΡα/ΑΠΠΡgагоністичну активність [Structure, 2001, Vol 9, 699, P. Cronet et al.]. Ця сполука є ефективною у лікуванні станів, асоційованих з резистентністю до інсуліну. Несподівано зараз винайдено серії сполук, котрі є селективними модуляторами АППРα. Представлений винахід стосується Sенантіомеру сполуки формули І 8 I де R1 представляє хлор, трифлуорметил або трифлуорметоксил, R2 представляє Η або флуор, a R3 представляє С 2-4алкіл, а також його фармацевтично прийнятних солей, сольватів та проліків. Термін "проліки", як застосовано у цьому описі, охоплює похідні карбонової кислоти, котрі перетворюються у ссавці, особливо людині, у карбонову кислоту або сіль або її кон'югат. Слід розуміти що, не торкаючись теорії, вважають, що більшість активності, асоційованої з проліками, походить від активності сполуки формули І, у котру проліки перетворюються. Проліки можна отримувати звичайними способами, добре відомими фахівцю. Різні карбоксипроліки відомі у рівні техніки. Наприклад, про похідні таких проліків дивись: [a) Design of Prodrugs, edited by Η. Bundgaard, (Elsevier, 1985) та Methods in Enzymology. 42: 309396, edited by K. Widder, et al. (Academic Press, 1985); b) A Textbook Drugs Design та Development, edited by Krogsgaard-Larsen та Н. Bundgaard, Chapter 5 "Design та Application of Prodrugs", by H. Bundgaard р.НЗ-191(1991); c) Н. Bundgaard, Ad vanced Drugs Delivery Reviews, 8:1-38 (1992); d) H. Bundgaard, et al, Journal of Pharmaceutical Sciences, 77:285 (1988); та N. Kakeya, et al., Chem Pharm Bull, 32:692 (1984)]. Вищенаведені документи уведено тут як посилання. In vi vo розщеплювані естери є як раз одним типом проліків вихідноїмолекули. In vivo здатним до гідролізу (або розщеплюваним) естером сполуки формули (І), що містить карбоксигрупу, є, наприклад, фармацевтично прийнятний естер, котрий гідролізується у тілі людини або тварини для продукування вихідної кислоти. Придатні фармацевтично прийнятні естери для карбоксигрупи охоплюють С 1-4алкоксиметилові естери, наприклад, метоксиметилові; С1естери, наприклад, 6алкеноїлоксиметилові метоксиметилові; С1-6алкеноїлоксиметилові естери, наприклад, півалоїлоксиметилові; фталідилові естери; С3естери, 8ЦиклоалкоксикарбонілоксиС 1-6алкілові наприклад, 1-циклогексилкарбонілоксіетилові; 1,3діоксолен-2-онілметилов естери, наприклад, 5метил-1,3-діоксолен-2-онілметилові; та С16алкоксикарбонілоксіетилові естери, наприклад, 1метоксикарбонілоксіетилові; та можуть бути утвореними на будь-якій карбоксигрупі у сполуках цього винаходу. Конкретними сполуками винаходу є: 9 80729 (2S)-3-[4-(2-{Бутил(2-флуор-4(трифлуорметил)бензил)аміно}-2оксоетокси)феніл]-2-етоксипропанова кислот; (2S)-3-(4-[2-[(4-хлорбензил)(етил)аміно]-2оксоетокси}феніл)-2-етоксипропанова кислота, (2S)-2-Етокси-3-[4-(2-{етил[4(трифлуорметокси)бензил]аміно}-2оксоетокси)феніл]пропанова кислота; (2S)-2-Етокси-3-[4-(2-{етил[4(трифлуорметил)бензил]аміно}-2оксоетокси)феніл]пропанова кислота; та (2S)-3-[4-(2-{Бутил[4(трифлуорметил)бензил]аміно}-2оксоетокси)феніл]-2-етоксипропанова кислота; та їх фармацевтично прийнятні солі та сольвати. Слід розуміти що кожна з вищенаведених сполук індивідуально та також будь-яка комбінація цих сполук наприклад двох, трьох, чотирьох або усі х з вищенаведених сполук утворює частину представленого винаходу. Слід також розуміти що представлений винахід стосується п'яти втілень, у котрих кожна з вищенаведених п'яти сполуки є у свою чергу виключена із загальної патентної формули до сполук формули І, які описано вище, за допомогою застереження щодо сполуки. Представлений винахід стосується також втілення, де будь-яку комбінацію п'яти вищенаведених сполук виключена із загальної патентної формули до сполук формули І, які описано вище, допомогою застереження щодо комбінації сполук. У представленому описі вираз "фармацевтично прийнятні солі" визначають, але без обмеження, солі основ, як-то солі лужного металу, солі лужноземельного металу, солі амонію, солі з основними амінокислотами та солі з органічними амінами, особливо трет-бутиламіном. У ще одному аспекті представлений винахід стосується одного або більше з наступного: сіль (2S)-3-[4-(2-{Бутил[2-флуор-4(трифлуорметил)бензил]аміно}-2оксоетокси)феніл]-2-етоксипропанової кислоти трет-бутиламіну; сіль (2S)-3-(4-{2-[(4-Хлорбензил)(етил)аміно]-2оксоетокси}феніл)-2-етоксипропанової кислоти трет-бутиламіну; сіль (2S)-2-Етокси-3-[4-(2-{етил[4(трифлуорметокси)бензил]аміно}-2оксоетокси)феніл]пропанової кислоти третбутиламіну; сіль (2S)-2-Етокси-3-[4-(2-{етил[4(трифлуoрметил)бензил]аміно}-2оксоетокси)феніл]пропанової кислоти третбутиламонію; та сіль (2S)-3-[4-(2-{Бутил[4(трифлуорметил)бензил]аміно}-2оксоетокси)феніл]-2-етоксипропанової кислоти трет-бутиламонію. Ці солі можна отримувати реакцією кислоти з трет-бутиламіном (наприклад, приблизномолярним еквівалентом з огляду на кислоту) у розчиннику, наприклад, етері, наприклад, діізопропіловому етері або третбутилметиловому етері, або естері, наприклад, 10 трет-бутилацетаті, або їх суміші або з суміші одного з цих розчинників та анти-розчиннику, наприклад, вуглеводню, наприклад, ізооктану, та виділення солі способами, відомими фахівцю, наприклад, фільтруванням. Слід також розуміти, що деякі сполуки представленого винаходу можуть існувати у сольватованій, наприклад, гідратованій, а також несольватованій формах. Слід розуміти, що представлений винахід стосується усіх таких сольватованих форм. Деякі сполуки представленого винаходу можуть існувати як таутомери. Слід розуміти, що представлений винахід стосується усі х таких та утомерів. Способи створення Сполуки винаходу можна отримувати ям показано нижче. Однак, винахід не обмежено цими способами. Сполуки можна також отримувати як описано для структурно споріднених сполук у попередньому рівні техніки. Реакції можна проводити стандартними способами або як описано у розділі експерименту. Сполуки формули І можна отримувати реакцією S-енантіомеру сполуки формули II II у котрій R1, R2 та R3 визначено вище, а В4 представляє захисну групу для карбоксильної гідроксигрупи, як описано у стандартному тексті "Protective Groups in Organic Synthesis", 3rd Edition (1999) by Greene та Wuts, з засобом зняття захисту. За хисна група може також бути смолою, як-то смола Ванга або 2-хлортритил-хлоридна смол. Захисні групи можна видаляти способами, що добре відомі фахівцю. Одною такою захисною групою є та , де R4 представляє С 1-6алкоксигрупу, наприклад, метоксил або етоксил, або арилалкоксигрупу, наприклад, бензилоксил, так що COR представляє естер. Такі естери можуть реагувати із засобом зняття захисту, наприклад, засобом гідролізу, наприклад, літій гідроксидом, у суміші ТГФ та води, при температурі у межах 0100°С, даючи сполуки формули І. Сполуки формули II можна отримувати реакцією S-енантіомеру сполуки формули III III у котрій R4 визначено вище, зі сполукою формули IV IV у котрій R1, R2 та R3 визначено вище, в інертному розчиннику, наприклад, дихлорметані, у присутності засобу сполучення, наприклад, карбодііміду, наприклад, 1-(3диметиламінопропіл)-3-етилкарбодііміду, та, як варіант, у присутності каталізатору, наприклад, 11 80729 основного каталізатору, наприклад, 4диметиламінопіридину, при температурі у межах 25°С-150°C. Сполуки формули III та IV можна отримувати способами, описаними у прикладях або аналогічними способами, відомими фахівцю. Сполуки формули II та III є корисними інтермедіатами у створенні сполук формули І та, можна вважати, є нов. Сполуки формули II та III тут заявлено як наступний аспект представленого винаходу. S-енантіомери сполук формули II та III є кращими. Сполуки формули І можна також отримувати реакцією сполуки формули V 12 метилпіролідон або толуол або суміші їх, особливо диметилсульфоксид. Відповідно X представляє бром, хлор, OSO2CH, ОТозил, OSO 2CF3, OC(O)OR, OP(O)(OR)2 або OSO2OR. Особливо X представляє хлор або бром. Можна застосовувати, як варіант, каталізатор фазо-переносу, наприклад, сіль алкіламонію, наприклад, галогенід тетраалкігіамонію, наприклад, тетрабутиламонію бромід. Сполуки формули V, у котрій R представляє Η (або сполука VII) можна отримувати реакцією сполуки формули V V V у котрій R1 та R 2 визначено вище, R предртавляє Η, або OR представляє захисну групу для карбоксильної гідроксигрупи, зі сполукою формули VI R3X VI де R3 визначено вище, а X представляє відщеплювану груп у, у присутності основи у присутності інертного розчиннику при температурі у межах -25°С до 150°С, та, як варіант, коли OR представляє захисну гр упу, видалення захисної групи. Зокрема сполуку формули І можна отримувати реакцією сполуки формули VII у котрій R1 та R2 визначено вище, a OR представляє захисну групу для карбоксильної гідроксигрупи, із засобом зняття захисту. Зокрема, OR представляє С 1-6алкоксигрупу, наприклад, етоксигрупу або арилалкоксигрупу, наприклад, бензилок-сил, так що COOR представляє естер. Такі естери можуть реагувати із засобом зняття захисту, наприклад, засобом гідролізу, наприклад, літій гідроксидом у суміші ТГФ та води, при температурі у межах 0-100°С Сполуки формули V, у котрій OR представляє захисну груп у для карбоксильної гідроксигрупи, можна отримувати реакцією сполуки формули VIII VII VIII у котрій R1 та R2 визначено вище, зі сполукою формули VI R3X VI де R3 визначено вище, а X представляє відщеплювану груп у, у присутності основи у присутності інертного розчиннику при температурі у межах -25°С-150°С. Захисні групи OR та зняття захисту засоби описано [у стандартному тексті "Protective Groups in Organic Synthesis", 3rd Edition (1999) by Greene та Wuts], котрий уведено тут як посилання. Придатні захисні групи охоплюють ті, де OR представляє С 1-6алкоксигрупу, наприклад, метоксил або етоксил, або арилалкоксигрупу, наприклад, бензилоксил. Зокрема, коли OR представляє С 1-6алкоксигрупу, наприклад, етоксигрупу або арилалкоксигрупу, наприклад, бензилоксил, так, що COOR представляє естер, тоді такі естери можуть реагувати із засобом зняття захисту, наприклад, засобом гідролізу, наприклад, літій гідроксидом у суміші ТГФ та води, при температурі у межах 0-100°С. Придатні основи охоплюють калій гідроксид, натрій гідроксид, літій гідроксид, натрій гідрид, калій трет-бутоксид, цезій карбонат, калій карбонат, або натрій карбонат особливо калій гідроксид. Придатні інертні розчинники охоплюють диметилсульфоксид, Ν,Ν-диметилформамід, М у котрій OR визначено вище, зі сполукою формули IX IX у котрій R1 та R2 визначено вище, a Y представляє відщеплювану гр упу, наприклад, галоген, особливо хлор, в інертному розчиннику, наприклад, ацетонітрилі або метил ізобутилкетон і, у присутності основи, наприклад, калій карбонату, при температурі у межах 0°С-150°С. Вважають, що сполуки формули V, у котрій R представляє Η (сполука VII), наприклад, (2S)-3-[4-(2-{[2-флуор-4(трифлуоргметил)бензил]аміно)-2оксоетокси)феніл]-2-етоксипропанова кислота; (2S)-3-(4-{2-[4-Хлорбензиламіно]-2оксоетокси}феніл)-2-етоксипропанова кислота, (2S)-2-Етокси-3-[4-(2-{4(трифлуорметокси)бензиламіно}-2оксоетокси)феніл]пропанова кислота; та (2S)-2-Етокси-3-[4-(2-{4(трифлуорметил)бензиламіно}-2оксоетокси)феніл]пропанова кислота; є новими та заявлені тут як подальша частина представленого винаходу Ці сполуки мають перевагу, що є твердими, а тому дають 13 80729 можливість очистки та виділення протягом послідовних реакцій, якщо бажано. Ці сполуки є також модуляторами АППР-альфа та/або АППРгамма та, можна вважати, є корисними у лікуванні показань, описаних тут. Також тут заявлено сполуку формули V, у котрій OR представляє захисну гр уп у для карбоксильної гідроксигрупи, зокрема OR представляє, наприклад, С1-6алкоксигрупу, наприклад, метоксил, етоксил або пропоксил, або арилалкоксигрупу де арилом є феніл, як варіант, заміщений С 1-6алкілом, С1-6алкоксилом або галогеном, наприклад, бензилоксил, наприклад, сполука формули X X у котрій R1 та R2 визначено вище. У ще одному аспекті представлений винахід стосується способу отримання фармацевтично прийнятної солі сполуки формули І, що залучає реакцію кислоти, отриманої одним зі способів представленого винаходу, з основою, як варіант, у присутності розчиннику, та виділення солі. Переважно сполука формули І, отримана способом є (2S)-енантіомером. Подібним чином кращі сполуки формули V тa X представляють (2S)-енантіомер Сполуки винаходу можна виділяти з їх реакційної суміші, застосовуючи звичайні способи. Фахівцю ясно, що для отримання сполуки винаходу альтернативними, а у деяких випадках більш зручними способами, індивідуальні етапи способу можна проводити у відмінному порядку, та/або індивідуальні реакції можна проводити на відмінному етапі у загальному шляху (тобто хімічні перетворення можна проводити з інтермедіатами, відмінними від тих, що асоційовані тут з конкретною реакцією). Вираз "інертний розчинник" стосується розчиннику, що не реагує з вихідними матеріалами, реагентами, інтермедіатами або продуктами таким чином, що шкідливо впливає на вихід бажаного продукту. Фармацевтичні препарати Сполуки винаходу звичайно застосовують перорально, парентерально, внутрішньовенно, внутрішньом'язово, підшкірно або іншими ін'єкціями, букально, ректально, вагінально, трансдермально та/або назально, та/або інгаляціями, у формі фармацевтичних препаратів, що містять активний інгредієнт як вільну кислоту або фармацевтично прийнятну органічну або інеорганічну основно-адитивну сіль, у фармацевтично прийнятній дозовані формі. Залежно від розладу та пацієнта, якого лікують, та шляху застосування композиції можна застосовувати у різних дозах. Придатними добовими дозами сполук винаходу у терапевтичному лікуванні людей є приблизно 0,0001-100мг/кг маси тіла, переважно 0,001-10мг/кг маси тіла. Пероральні композиції є кращими, особливо таблетки або капсули, котрі 14 можна формувати способами, відомими фахівцю, для забезпечення дози активної сполуки у межах 0,5-500мг, наприклад, 1мг, 3мг, 5мг, 10мг, 25мг, 50мг, 100мг та 250мг. Згідно з наступним аспектом винаходу відтак запропоновано фармацевтичну композицію, що містить будь-яку сполуку винаходу або її фармацевтично прийнятні похідні у суміші з фармацевтично прийнятними ад'ювантами, розріджувачами та/або носіями. Фармакологічні властивості Представлені сполуки формули (І) є корисними для профілактики та/або лікування клінічних станів, асоційованих з уродженою або індукованою зменшеною чутливістю до інсуліну (резистентність до інсуліну) та асоційованих метаболічних розладів (також відомих як метаболічний синдром). Ці клінічні стани охоплюють, але без обмеження, загальне ожиріння, абдомінальне ожиріння, артеріальну гіпертензію, гіперінсулінемію, гіперглікемію, діабет типу 2 та дисліпідемію, що характеристично з'являється з резистентністю до інсуліну. Ця дисліпідемія, також відома як атероген-ний ліпопротеїновий профіль, характеризується помірно підвищеними неестерифіко-ваними жирними кислотами, підвищеним ліпопротеїном дуже низької густини (ЛДНГ) багатими тригліцеридами частинками, високими рівнями Аро В, низькими рівнями лі-попротеїну високої густини (ЛВГ), асоційованими з низькими рівнями частинок ароАІ та високими рівнями Аро В у присутності невеликих, густи х частинок ліпопротеїнів низької густини (ЛНГ), фенотипу В. Сполуки представленого винаходу, як очікують, є корисними у лікуванні пацієнтів з поєднаними або змішаними гіперліпідеміями або різними ступенями гіпертригліцеридемій та післяобідньої дисліпідемії з іншими виявами метаболічного синдрому або без них. Лікування представленими сполуками, як очікують, знизить серцево-судинні захворюваності та смертності, асоційовані з атеросклерозом внаслідок їх антидисліпідемічних, а також антизапальних властивості. Стани серцевосудинних хвороб охоплюють макро-ангіопатії різних вн утрішніх органів, викликаючи інфаркт міокарду, застійну серцеву недостатність, церебрально-васкулярну хворобу та периферійну артеріальну недостатність нижніх кінцівок. Внаслідок їх інсулін-сенсибілізувальної дії сполуки формули І, як також очікують, попереджатимуть або затримуватимуть розвиток діабету типу 2 від метаболічного синдрому та діабету вагітних. Тому розвиток довготермінових ускладнень, асоційованих з хронічною гіперглікемією у цукровому діабеті, як-то мікро-ангіопатії, що викликають ниркову хворобу, пошкодження сітчатки та хворобу периферійних судин нижніх кінцівок, як очікують, буде затриманим. Більш того сполуки можуть бути корисними у лікуванні різних станів поза серцево-судинною системою, асоційованих або не асоційованих з резистентністю до інсуліну, синдрому типу полікистозного яєчника, ожирінням, раком та 15 80729 станами запальних хвороб, залучаючи нейродегенеративні розлади, як-то м'яке когнітивне погіршання, хвороба Альцгеймера, хвороба Паркінсона та розсіяний склероз. Сполуки представленого винаходу, як очікують, є корисними у контролі рівнів глюкози у пацієнтів, що потерпають від діабету типу 2. Представлений винахід стосується способу лікування або попередження дисліпідемій, синдрому резистентності до інсуліну та/або метаболічних розладів (як визначено вище), що залучає застосування сполуки формули І до ссавця (особливо людини), що цього потребує. Представлений винахід стосується способу лікування або попередження діабет типу 2, що залучає застосування ефективної кількості сполуки формули І до ссавця (особливо людини), що цього потребує. Представлений винахід стосується способу лікування або попередження атеросклерозу, що залучає застосування ефективної кількості сполуки формули І до ссавця (особливо людини), що цього потребує. Згідно з наступним аспектом представлений винахід стосується застосування сполуки формули І як медикаменту. Згідно з наступним аспектом представлений винахід стосується застосування сполуки формули І у виробництві медикаменту для лікування резистентності до інсуліну та/або метаболічних розладів. Комбінована терапія Сполуки винаходу можуть бути поєднаними з ще одним терапевтичним засобом, що є корисним у лікуванні розладів, асоційованих з розвитком та прогресом атеросклерозу, як-то гіпертензії, гіперліпідемії, дисліпідемій, діабету та ожиріння. Сполуки винаходу можуть бути поєднаними з ще одним терапевтичним засобом, що зменшує співвідношення ЛНГ:ЛВГ або засобом, що викликає зменшення рівнів циркуляції ЛНГхолестерину. У пацієнтів з цукровим діабетом сполуки винаходу можуть також бути поєднаними з терапевтичними засобами, застосовуваними для лікування ускладнень, споріднених з мікроангіопатіями. Сполуки винаходу можна застосовувати разом з іншими терапіями для лікування метаболічного синдрому або діабету типу 2 та асоційованих з цим ускладнень, це охоплює бігуанідні ліки, наприклад, метформін, фенформін та буформін, інсулін (синтетичні аналоги інсуліну, амілін) та пероральні антигіпергліцемічні засоби (це є поділеним на обідні регулятори глюкози та інгібітори альфа-глюкозідази). Прикладом інгібітору альфа-глюкозідази є акарбоза або воглібоза або міглітол. Прикладом обіднього регулятору глюкози є репаглінід або натеглінід. У ще одному аспекті винаходу, сполук у формули І, або її фармацевтично прийнятні сіль, сольват, сольват такої солі або проліки, можна застосовувати у поєднанні з ще одним модулятором АППР. Модулятори АППР охоплюють, але без обмеження, агоніст АППРальфа та/або гамма, або фармацевтично його 16 прийнятні солі, сольвати, сольвати таких солей або проліки. Придатні агоністи АППР-альфа та/або гамма, їх фармацевтично прийнятні солі, сольвати, сольвати таких солей або проліки добре відомі у рівні техніки. Це охоплює сполуки, [описані у WO 01/12187, WO 01/12612, WO 99/62870, WO 99/62872, WO 99/62871, WO 98/57941, WO 01/40170, J Med. Chem, 1996, 39, 665, Expert Opinion on Therapeutic Patents, 10 (5), 623-634 (зокрема сполуки, описані у патентних заявках представлено на с 634) та J Med Chem, 2000, 43, 527], котрі уведено тут як посилання. Особливо агоніст АППР-альфа та/або гамма стосується NN622/рагаглітазару, BMS 298585, WY-14643, клофібрату, фенофібрату, безафібрату, гемфіброзилу та ципрофіерату; GW 9578, циглітазону, троглітазону,) піоглітазону, розиглітазону, еглітазону, проглітазону, BRL49634, KRP-297, ЛТ-501, SB 213068, GW 1929, GW 7845, GW 0207, L-796449, L-165041 та GW 2433. Особливо агоніст АППР-альфа та/або гамма стосується (S)-2-етокси-3-[4-(2-{4метансульфонілоксифеніл}етокси)феніл]пропанової кислоти та її фармацевтично прийнятних солей. На додаток комбінацію винаходу можна застосовувати у поєднанні з сульфонілсечовиною, наприклад: глімеперид, глібенкламід (глібурид), гліклазид, гліпізид, гліквідон, хлорпропамід, толбутамід, ацетогексамід, глікопірамід, карбутамід, глібонурид, глізоксепід, глібутіііазол, глібузол, глігексамід, глімідин, гліпінамід, фенбутамід, толциламід та толазамід. Переважно сульфонілсечовиною є глімеперид або глібенкламід (глібурид). Більш переважно сульфонілсечовиною є глімеперид. Тому представлений винахід стосується застосування сполуки представленого винаходу у поєднанні з одною, двома або більше існуючими терапіями, описаними у цьому розділі. Дози інших існуючих терапій для лікування діабету тип у 2 та асоційованих з ним ускладнень відомі у рівні техніки та затверджені для застосування регуляторними органами, наприклад, FDA, їх можна знайти у Orange Book, опубліковано FDA. Альтернативно як результат корисності комбінації можна застосовувати менші дози. Представлений винахід стосується також сполук представленого винаходу у комбінації з холестерин-знижувальним засобом. Холестерин-знижувальні засоби, розглянуті у цій заявці охоплюють, але без обмеження інгібітори HMG-CoA-редуктази (3гідрокси-3-метилглутарил кофермент А редуктаза). Відповідно інгібітором HMG-CoA редуктази є статин що вибирають з групи: аторвастатин, бервастатин, церивастатин, далвастатин, флувастатин, ітаваста тин, ловастатин, мевастатин, нікостатин, нівастатин, правастатин та симвастатин, або його фармацевтично прийнятна сіль, особливо натрію чи кальцію, або сольват, або сольват такої солі. Конкретним статином є аторвастатин, або його фармацевтично прийнятна сіль, сольват, сольват такої солі або проліки. Особливим статином є кальцієва сіль аторвастатину. Особливо кращим 17 80729 статином є, однак, сполука з хімічною назвою (Е)7-[4-(4-флуорфеніл)-6-ізопропіл-2[метил(метилсульфоніл)-аміно]-піримідин-5іл](3R,5S)-3,5-дигідроксигепт-6-енова кислота, [також відома як (Е)-7-[4-(4-флуорфеніл)-6ізопропіл-2-[N-метил-N-(метилсульфоніл)аміно]піримідин-5-іл](3R,5S)-3,5-дигідроксигепт-6енова кислота] або її фармацевтично прийнятні сіль або сольват, або сольват такої солі. Сполуку (Е)-7-[4-(4-флуорфеніл)-6-ізопропіл-2-[метил(метилсульфоніл)-аміно]піримідин-5-іл](3R,5S)-3,5дигідроксигепт-6-енова кислота, та її солі натрію та кальцію розкрито [у публікації Європейської патентної заявки. ЕР-А-0521471, та у Bioorganic та Medicinal Chemistry, (1997), 5(2), 437-444]. Цей останній статин зараз відомий як розувастатин. У представленій заявці, термін "холестеринзнижувальний засіб" також охоплює хімічні модифікації інгібіторів HMG-CoA редуктази, як-то естери, проліки та метаболіти, активні або неактивні. Представлений винахід стосується також сполук представленого винаходу у комбінації із засобом зв'язування жовчних кислот, наприклад, колитипол або холітирамін або холітагель. Представлений винахід стосується також сполук представленого винаходу у комбінації з інгібітором транспортної системи жовчної кислоти клубової кишки (інгібітор ТКЖК). Придатні сполуки, виявляючі інгібувальну активність стосовно ТКЖК, описано, [дивись, наприклад, сполуки, описані у WO 93/16055, WO 94/18183, WO 94/18184, WO 96/05188, WO 96/08484, WO 96/16051, WO 97/33882, WO 98/07449, WO 98/03818, WO 98/38182, WO 99/32478, WO 99/35135, WO 98/40375, WO 99/35153, WO 99/64409, WO 99/64410, WO 00/01687, WO 00/47568, WO 00/61568, WO, 00/62810, WO 01/68906, DE 19825804, WO 00/38725, WO 00/38726, WO 00/38727, WO 00/38728, WO 00/38729, WO 01/68906, WO 01/66533, WO 02/32428, WO 02/50051, ЕР 864 582, ЕР489423, ЕР549967, ЕР573848, ЕР624593, ЕР624594, ЕР624595 та ЕР624596], вміст цих патентних заявок уведено тут як посилання. Особливими класами інгібіторів ТКЖК, придатних для застосування у представленому винаході, є бензотієпіни та сполуки, [описані у формулі винаходу, особливо п.1 WO 00/01687, WO 96/08484 та WO 97/33882], що уведено тут як посилання. Іншими придатним класами інгібіторів ТКЖК є 1,2-бензотіазепіни, 1,4-бензотіазепіни та 1,5-бензотіазепіни. Наступним придатним класом інгібіторів ТКЖК є 1,2,5-бензотіадіазепіни. Одною конкретною придатною сполукою, виявляючою інгібувальну активність стосовно ТКЖК, є (3R,5R)-3-бутил-3-етил-1,1-діоксидо-5феніл-2,3,4,5-тетрагідро-1,4-бензотіазеріп-8-іл β-Dглюкопіранозидуронова кислота [ЕР 864 582]. Інші придатні інгібітори ТКЖК охоплюють одну зі сполук: 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-1'-феніл-1'-[N'(карбоксиметил)карбамоїл]метил}карбамоїлметокс и)-2,3,4,5-тетрагідро-1,5-бензотіазепін; 18 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-α-[Ν'-(карбоксиметил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-3,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-1'-феніл-1'-[N'-(2сульфоетил)карбамоїл]метил}карбамоїлметокси)2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-дioкco-3-бyтил-3-eтил-5-фeнiл-7-мeтилтio8-(N-{(R)-1'-феніл-1'-[N'-(2сульфоетил)карбамоїл]метил}карбамоїлметокси)2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-α-[Ν'-(2-сульфоетил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо8-(N-{(R)-α-[N'-(2-сульфоетил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,5-бензотіазепін; 1,1-дioкco-3-бyтил-3-eтил-5-фeнiл-7-мeтилтio8-(N-{(R)-α-[N'-(2карбоксіетил)карбамоїл]бензил}карбамоїлметокси) -2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8(N-{(R)-α-[N'-(2-карбоксіетил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,5-бензотіазепін; 1,1-дioкco-3-бyтил-3-eтил-5-фeнiл-7-мeтилтio8-(N-{(R)-α-[N'-(5карбоксипентил)карбамоїл]бензил}карбамоїлметок си)-2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8(N-{(R)-α-[N'-(2карбоксіетил)карбамоїл]бензил}карбамоїлметокси) -2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-α-[N'-(2-сульфоетил)карбамоїл]-2флуорбензил)карбамоїлметокси)-2,3,4,5тетрагідро-1,5-бензотіазепін; 1,1-дioкco-3-бyтил-3-eтил-5-фeнiл-7-мeтилтio8-(N-{(R)-α-[N'-(R)-(2-гідрокси-1карбоксіетил)карбамоїл]бензил}карбамоїлметокси) -2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-α-[N'-(2-гідрокси-1карбоксіетил)карбамоїл]бензил}карбамоїлметокси) -2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8{N-[(R)-α-(N'-{(R)-1-[N"-(R)-(2-гідpoкcи-1карбоксіетил)карбамоїл]-2гідроксіетил}карбамоїл)бензил]карбамоїлметокси}2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо8-(Ν-{α-[Ν'(карбоксиметил)карбамоїл]бензил}карбамоїлметок си)-2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-дioкco-3-бyтил-3-eтил-5-фeнiл-7-мeтилтio8-(N-{α-[N'((етокси)(метил)фосфорилметил)карбамоїл]бензи л}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5бензотіазепін; 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо8-{N-[(R)-α-(N-{2[(гідрокси)(метил)фосфорил]етил)карбамоїл)бензи 19 л]карбамоїлметокси}-2,3,4,5-тетрагідро-1,5бензотіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8(N-{(R)-α-[N'-(2-метилтіо-1карбоксіетил)карбамоїл]бензил}карбамоїлметокси) -2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8{N-[(R)-α-(N'-{2[(метил)(етил)фосфорил]етил}карбамоїл)-4гідроксибензил]карбамоїлметокси)-2,3,4,5тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8{N-[(R)-α-(N'-{2[(метил)(гідрокси)фосфорил]етил}карбамоїл)-4гідроксибензил]карбамоїлметокси}-2,3,4,5тетрагідро-1,5-бензотіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8(N-{(R)-α-[(R)-N'-(2-мeтилcyльфiн iл-1карбоксіетил)карбамоїл]бензил}карбамоїлметокси) -2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтoкcи-8-[N{(R)-α-[N'-(2-сульфоетил)карбамоїл]-4гідроксибензил}карбамоїлметокси]-2,3,4,5тетрагідро-1,5-бензотіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8(N-{(R)-α-[N-((R)-1-карбокси-2метилтіоетил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-α-[N-((S)-1-карбокси-2-(R)гідроксипропіл)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-α-[N-((S)-1-карбокси-2метилпропіл)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-α-[N-((S)-1-карбоксибутил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8(N-{(R)-α-[N((S)-1карбоксипропіл)карбамоїл]бензил}карбамоїлметок си)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-α-[N-((S)-1карбоксіетил)карбамоїл]бензил}карбамоїлметокси) -2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-α-[N-((S)-1-карбокси-2-(R)гідроксипропіл)карбамоїл]бензил}карбамоїлметокс и)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-α-[N-(2-сульфоетил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-α-[N-((S)-1-карбоксіетил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8(N-{(R)-α-[N-((R)-1-каpбoкcи-2 80729 20 метилтіоетил)карбамоїл]бензил}карбамоїлметокси )-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-α-[N-{(S)-1-[-((S)-2-гідрокси-1карбоксіетил)карбамоїл]пропіл}карбамоїл]бензил}к арбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-α-[N-{(S)-1-карбокси-2метилпропіл)карбамоїл]бензил)карбамоїлметокси) -2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-α-[N-{(S)-1-карбоксипропіл)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8[N-((R/S)-α-{N-[1-(R)-2-(S)-1-гідрокси-1-(3,4дигідроксифеніл)проп-2-іл]карбамоїл}-4гідроксибензил)карбамоїлметокси]-2,3,4,5тетрдгідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-α-[N-(2-(S)-3-(R)-4-(R)-5-(R)-2,3,4,5,6пентагідроксигексил)карбамоїл]-4гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; та 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)-α-[N-(2-(S)-3-(R)-4-(R)-5-(R)-2,3,4,5,6пентагідроксигексил)карбамоїл]бензил}карбамоїлм етокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін; або її фармацевтично прийнятні сіль, сольват, сольват такої солі або проліки. Згідно з додатковим наступним аспектом представленого винаходу запропоновано комбіноване лікування, що залучає застосування ефективної кількості сполуки формули І, або її фармацевтично прийнятної солі, сольвату, сольвату такої солі або проліків, як варіант, разом з фармацевтично прийнятним розріджувачем або носієм, з одночасним, послідовним або окремим застосуванням одного або більш наступних засобів що вибирають з групи: інгібітор БПХЕ (білок переносу холестерилового естеру), наприклад, [описаний у WO 00/38725 раgе 7 line 22 - раgе 10, line 17], котре уведено тут як посилання; антагоніст поглинання холестерину, наприклад, азетидинони, як-то SCR 58235 та [описані у US 5,767,115], котре уведено тут як посилання; інгібітор БМП (білок мікросомного переносу), наприклад, що [описано у Science, 282, 751-54, 1998], котре уведено тут як посилання; похідне нікотинової кислоти, залучаючи уповільнене вивільнення та комбіновані продукти, наприклад, нікотинова кислота (ніацин), аципімокс та нуцеритрол; фітостеринова сполука, наприклад, стандс; пробукол; омега-3 жирна кислота, наприклад, ОтасоrrМ; сполука проти ожиріння, наприклад, ористат [ЕР 129,748] та сибутрамін [GB 2,184,122 та US 4,929,629]; антигіпертензивна сполука, наприклад, інгібітор ферменту перетворення ангіотензину (ФПА), антагоніст рецептору ангіотензину II, 21 80729 андренергічний блокатор, альфа андренергічний блокатор, бета андренергічний блокатор, наприклад, метопролол, змішаний альфа/бета андренергічний блокатор, андренергічний стимулятор, блокатор каналів кальцію, блокатор АТ-1, салуретичний засіб, діуретичний засіб або судинорозширювальний засіб; антагоніст або інверсивний агоніст СВ1, наприклад, що [описано у WO 01/70700 та ЕР 65635]; аспірин; антагоніст меланін-концентруючого гормону (МСН); інгібітор PDK; або модулятори ядерних рецепторів, наприклад, LXR, FXR, R XR, та RORaльфa; або їх фармацевтично прийнятна сіль, сольват, сольват такої солі або проліки, як варіант, разом з фармацевтично прийнятним розріджувачем або носієм до теплокровних тварин, як-то людини, що потребує такого терапевтичного лікування. Конкретні інгібітори ФПА або їх фармацевтично прийнятні солі, сольвати, сольвати таких солей або проліки, залучаючи активні метаболіти, які можна застосовувати у комбінації зі сполукою формули І охоплюють, але без обмеження, наступні сполуки: алацеприл, алатриоприл, алтіоприл кальцій, анковенін, беназеприл, беназеприл гідрохлорид, беназеприлат, бензоїлкаптоприл каптоприл, каптоприл-цистеїн, каптоприл-глутатіон, церанаприл, цераноприл, церонаприл, цилазаприл, цилазаприлат, делаприл, делаприлдіацид, еналаприл, еналаприлат, енаприл, епікаптоприл, фороксимітин, фосфеноприл, фосеноприл, фосеноприл натрій, фоциноприл, фоциноприл натрій, фоциноприлат, фоциноприлова кислота, глікоприл, геморфін-4, ідраприл, імідаприл, індолаприл, індолаприлат, лібензаприл, лізиноприл, ліціумін А, ліціумін В, міксанприл, моексиприл, моексиприлат, мовелтиприл, мурацеїн А, мурацеїн В, мурацеїн С, пентоприл, периндоприл, периндоприлат, півалоприл, півоприл, квінаприл, квінаприл гідрохлорид, квінаприлат, раміприл, раміприлат, спіраприл, спіраприл гідрохлорид, спіраприлат, спіроприл, спіроприл гідрохлорид, темокаприл, темокаприл гідрохлорид, тепротид, трандолаприл, трандолаприлат, утибаприл, забіциприл, забіциприлат, зофеноприл та зофеноприлат. Кращими інгібіторами ФПА для застосування у представленому винаході є раміприл, раміприлат, лізиноприл, еналаприл та еналаприлат. Більш кращими інгібіторами ФПА для застосування у представленому винаході є раміприл та раміприлат. Кращі антагоністи ангіотензину II, їх фармацевтично прийнятні солі, сольвати, сольвати таких солей або проліки для застосування у комбінації зі сполукою формули І охоплюють, але без обмеження, сполуки: кандесартан, кандесартан цилексетил, лосартан, валсартан, ірбесартан, тазосартан, телмісартан та епросартан. Особливо кращими антагоністами ангіотензину II або їх фармацевтично прийнятними 22 похідними їх для застосування у представленому винаході є кандесартан та кандесартан цилексетил. Тому як додаткову особливість винаходу, запропоновано спосіб лікування діабету типу 2 та асоційованих з ним ускладнень у теплокровних тварин, як-то людини, що потребує такого лікування, котрий містить застосування до вказаної тварини ефективної кількості сполуки формули І, або її фармацевтично прийнятної солі, сольвату, сольвату такої солі або проліків в одночасному, послідовному або окремому застосуванні з ефективною кількістю одної іншої сполуки, описаної у цьому комбінаційному розділі, або її фармацевтично прийнятної солі, сольвату, сольвату такої солі або проліків. Тому як додаткову особливість винаходу, запропоновано спосіб лікування гіперліпідемічних станів у теплокровних тварин, як-то людини, що потребує такого лікування, котрий містить застосування до вказаної тварини ефективної кількості сполуки формули І, або її фармацевтично прийнятної солі, сольвату, сольвату такої солі або проліків в одночасному, послідовному або окремому застосуванні з ефективною кількістю одної іншої сполуки, описаної у цьому комбінаційному розділі, або її фармацевтично прийнятної солі, сольвату, сольвату такої солі або проліків. Згідно з наступним аспектом винаходу запропоновано фармацевтичну композицію, котра містить сполуку формули І, або її фармацевтично прийнятні сіль, сольват, сольват такої солі або проліки, та одної іншої сполуки, описаної у цьому комбінаційному розділі, або її фармацевтично прийнятної солі, сольвату, сольвату такої солі або проліків, у поєднанні з фармацевтично прийнятним розріджувачем або носієм. Згідно з наступним аспектом представленого винаходу запропоновано комплект, що містять сполуку формули І, або її фармацевтично прийнятну сіль, сольват, сольват такої солі або проліки, та одної іншої сполуки, описаної у цьому комбінаційному розділі, або її фармацевтично прийнятної солі, сольвату, сольвату такої солі або проліків. Згідно з наступним аспектом представленого) винаходу запропоновано комплект, що містить: а) сполуку формули І, або фармацевтично прийнятну сіль, сольват, сольват такої солі або проліки, у першій одиничній дозованій формі; b) одну іншу сполуку, описану у цьому комбінаційному розділі, або її фармацевтично прийнятні сіль, сольват, сольват такої солі або проліки; у другій одиничній дозованій формі; та c) контейнери, що містять вказані першу та другу дозовані форми. Згідно з наступним аспектом представленого винаходу запропоновано комплект, що містить: a) сполуку формули І, або її фармацевтично прийнятні сіль, сольват, сольват такої солі або проліки, разом з фармацевтично прийнятним розріджувачем або носієм, у першій одиничній дозованій формі; b) одну іншу сполуку, описану у цьому комбінаційному розділі, або її фармацевтично 23 80729 прийнятні сіль, сольват, сольват такої солі або проліки, у другій одиничній дозованій формі; та c) контейнери, що містять вказані першу та другу дозовані форми. Згідно з ще одною особливістю винаходу запропоновано застосування сполуки формули І, або її фармацевтично прийнятної ,солі, сольвату, сольвату такої солі або проліків, та одної іншої сполуки, описаної у цьому комбінаційному розділі, або її фармацевтично прийнятної солі, сольвату, сольвату такої солі або проліків, у виробництві медикаменту для застосування у лікуванні метаболічного синдрому або діабету типу 2 та асоційованих з ним ускладнень у теплокровних тварин, як-то людини. Згідно з ще одною особливістю винаходу запропоновано застосування сполуки формули І, або її фармацевтично прийнятної солі, сольвату, сольвату такої солі або проліків, та одної іншої сполуки, описаної у цьому комбінаційному розділі, або її фармацевтично прийнятної солі, сольвату, сольвату такої солі або проліків, у виробництві медикаменту для застосування у лікуванні гіперліпідемічних станів у теплокровних тварин, якто людини. Згідно з наступним аспектом представленого винаходу запропоновано комбіноване лікування, що містить застосування ефективної кількості сполуки формули І, або її фармацевтично прийнятної солі, сольвату, сольвату такої солі або проліків, як варіант, разом з фармацевтично прийнятним розріджувачем або носієм, з одночасним, послідовним або окремим застосуванням ефективної кількості одної іншої сполуки, описаної у цьому комбінаційному розділі, або її фармацевтично прийнятної солі, сольвату, сольвату такої солі або проліків, як варіант, разком з фармацевтично прийнятним розріджувачем або носієм, до теплокровних тварин, як-то людина, при необхідності такого терапевтичного лікування. Приклади Виміри 1Н ЯМР та 13С Я МР проводять на спектрометрах Varian Mercury 300 або Varian UNITY plus 400, 500 або 600, при частотах 1Н 300, 400, 500 та 600МГц, відповідно, та при частотах 13 С 75, 100, 125 та 150МГц, відповідно. Виміри виконують на дельта шкалі (8). якщо не встановлено інше, хімічні зсуви надано умлн.-1 з розчинником як внутрішнім стандартом. ДМСО ТГФ Pd/C ДМАП t s d q m bs dm bt dd Скорочення диметилсульфоксид тетрагідрофуран паладій на вугіллі диметиламінопіридин триплет синглет дублет квартет мультиплет широкий синглет дублет м ультиплетів широкий триплет дублет of дублет 24 Приклад 1 (2S)-3-[4-(2-(бутил)2-флуор-4(трифлуорметил)бензил]аміно)-2оксоетокси)феніл]-2-етоксипропанова кислота (і) Етил (2S)-3-{4-[2-[бензилокси)-2оксoетокси]фенілї-2-етоксипропаноат До розчину етил (2S)-2-етокси-3-(4гідроксифеніл)пропаноату (23,8г, 100ммоль, отримано як описано [у WO 99/62872]) в ацетонітрилі (200мл) додають безводний калій карбонат (31,9г, 231ммоль) а потім бензилбромацетат (17,4мл, 110ммоль) та реакційну суміш гріють при кипінні під зворотним холодильником протягом ночі. Реакційній суміші дозволяють охолонути до кімнатної температури, нерозчинні солі відфільтровують та розчин концентрують у вакуумі. Залишок переміщають в етилацетат (300мл), та органічну фазу промивають водним натрій гідрогенкарбонатом (3´100мл) та розсолом (100мл), сушать безводним магній сульфатом та концентрують у вакуумі. Очистка на силікагелі з метиленхлоридом як елюентом та збирання чистих фракцій, дають 22,4г (58%) жовтого масла. 1 Н ЯМР (400МГц, CDCI3): δ 1,16 (t, 3Н), 1,22 (t, 3Н), 2,93-2,97 (m, 2H), 3,35 (m, 1H), 3,60 (m, 1H), 3,97 (m, 1H), 4,16 (q, 2H), 4,64 (s, 2H), 5,23 (s, 2H), 6,82 (d, 2H), 7,15 (d, 2H), 7,32-7,39 (m, 5H). 13 C ЯМР (100МГц, CDCI3): δ 14,3, 15,2, 38,6, 60,9, 65,6, 66,3, 67,0, 80,4, 114,6, 128,5, 128,6, 128,7, 130,6, 135,3, 156,7, 169,0, 172,6. (іі) (4-[(2S)-2,3-діетокси-3оксопропіл]фенікси}оцтова кислота До розчину етил (2S)-3-{4-[2-(бензилокси)-2оксоетокси]феніл}-2-етоксипропаноату (22,33г, 57,8ммоль) у свіжо перегнаному ТГФ (290мл) додають Pd/C (10%, 3,1г) та реакційну суміш гідрують під атмосферним тиском при кімнатній температурі протягом ночі. Суміш фільтрують, через шар целіту та фільтрат концентрують у вакуумі, отримуючи 16,6г (97%) світло-жовтого масла. 1 Н ЯМР (400МГц, CDCI3): δ 1,15 (t, 3Н), 1,21 (t, 3Н), 2,93-2,98 (m, 2H), 3,35 (m, 1H), 3,60 (m, 1H), 3,97 (m, 1H), 4,16 (q, 2H), 4,65 (s, 2H), 6,84 (d, 2H), 7,17 (d, 2H), 8,48 (bs, 1H). 13 C ЯМР (100МГц, CDCI3): δ 14,3, 15,1, 38,5, 61,0, 65,1, 66,4, 80,3, 114,6, 130,7, 130,9, 156,4,172,7, 173,7. (ііі) N-Бутил-N-[2-флуор-4(трифлуорметил)бензил]амін До розчину 2-флуор-4(трифлуорметил)бензальдегіду (3,84г, 20,0ммоль) та н-бутиламіну (1,46г, 20,0ммоль) у метанолі (100мл) додають оцтову кислоту (4,6мл, 80ммоль) та натрій ціаноборогідрид (1,51г, 24,0ммоль) та розчин перемішують при кімнатній температурі протягом 3 діб. Воду (10мл) додають та суміш концентрують у вакуумі. Залишок переміщають у водний 1Μ КОН (125мл) та етилацетат (100мл) та фази розділяють. Водну фазу екстрагують етилацетатом (2´100мл) та поєднану органічну фазу сушать натрій сульфатом та концентрують у вакуумі. Очистка на попередньо упакованій колонці силікагелю (Колонка Isolute® SPE, 25 80729 70г/150мл) з етилацетатом (33-100% градієнт) та гептаном як елюентом та збирання чистих фракцій, дають 1,28г (26%) безбарвного масла низької в'язкості. 1 Н ЯМР (400МГц, CDCI3): δ 0,91 (t, 3Н), 1,281,41 (m, 2H), 1,44-1,55 (m, 2H), 2,62 (t, 2H), 3,88 (s, 2H), 7,29 (m, 1H), 7,38 (m, 1H), 7,51 (m, 1H). 13 С ЯМР (100МГц, CDCI3): δ 14,1, 20,6, 32,4, 47,0, 49,3, 112,8 (m), 121,1 (m), 123,5 (q), 130,5131,6 (m), 130,8 (m), 132,0 (d), 160,8 (d). (iv) Етил (2S)-3-[4-(2-(бутил)-2-флуор-4(трифлуорметил)бензил]аміно)-2-оксоетокси) фенілі-2-етоксипропаноат До розчину N-бутил-N-[2-флуор-4(трифлуорметил)бензил]аміну (0,598г, 2,40ммоль) та {4-[(2S)-2,3-діетокси-3оксопропіл]фенокси}оцтової кислоти (0,593г, 2,00ммоль) у метиленхлориді (20мл) додають Ν,Νдіізопропілетиламін (0,80мл, 4,6ммоль) та О(бензотриазол-1-іл)-N,N,N',N'-тетраметилуроній тетрафлуорборат (0,674г, 2,10ммоль) та реакційну суміш перемішують при кімнатній температурі протягом ночі. Утворений розчин розбавляють метиленхлоридом (100мл) та органічну фазу промивають 2Μ НСІ (3´75мл), насиченим водним розчином натрій гідрогенкарбонату (2´75мл), та розсолом (75мл), сушать натрій сульфатом, та концентрують у вакуумі. Очистка на попередньо упакованій колонці силікагелю (Колонка Isolute® SPE, 20г/70мл) з метанолом (0-2% градієнт) у метиленхлориді як елюентом, дає 0,785г (74%) блідого жовтувато-білого масла. 1 Н ЯМР (400МГц, CDCI3): δ 0,84-0,97 (m, 3Н), 1,11-1,19 (m, 3Н), 1,19-1,40 (m, 5Н), 1,45-1,65 (m, 2Н), 2,90-2,99 (m, 2Н), 3,29-3,40 (m, 3Н), 3,60 (m, 1H), 3,96 (m, 1H), 4,16 (q, 2Н), 4,68 (s, 2Н), 4,72 та 4,74 (2s, 2Н, утримання), 6,70 та 6,86 (2d, 2Н, ротамери), 7,10 та 7,17 (2d, 2Н, ротамери), 7,217,40 (m, 3Н). 1З С ЯМР (100МГц, CDCI3): δ 13,8, 14,3, 15,2, 20,2, 29,2, 30,9, 38,5, 42,1 (d), 44,6 (d), 46,2, 47,5, 60,9, 66,3, 67,6, 68,3, 80,4, H3,0(m), 114,3, 114,6, 121,4 (m), 123,3 (q), 128,5 (m), 129,1 (d), 130,6, 130,6, 130,7, 131,0 (d), 131,0-132,2 (m), 156,6, 156,8, 160,3 (d), 160,5 (d), 168,5, 168,6, 172,6. (Число піків більше числа атомів карбону внаслідок ротамерів.) (ν) (2S)-3-[4-(2-{Бутил[2-флуор-4(трифлуорметил)бензил]аміно}-2оксоетокси)феніл]-2-етоксипропанова кислота До розчину етил (2S)-3-[4-(2-{Бутил[2-флуор-4(трифлуорметил)бензил]аміно}-2оксоетокси)феніл]-2-етоксипропаноату (0,748г, 1,42ммоль) в ацетонітрилі (70мл) додають водний 0,10Μ LiOH (35мл) та реакційну суміш перемішують при кімнатній температурі протягом ночі. Після нейтралізації 5% НСІ, об'єм розчиннику зменшують у вакуумі та залишкову водну фазу підкислюють 5% НСІ та екстрагують етилацетатом (3´100мл). Поєднану органічну фазу промивають розсолом (100мл), сушать натрій сульфатом, та концентрують у вакуумі, отримуючи 0,688г (97%) блідого жовтого масла. 1 Н ЯМР (400МГц, CDCI3): δ 0,84-0,96 (у, 3Н), 1,16 (t, 3H), 1,21-1,40 (m, 2H), 1,45-1,66 (m, 2Н), 26 2,88-3,11 (m, 2Н), 3,29-3,46 (m, 3Н), 3,61 (m, 1Н), 4,02 (m, 1Н), 4,69 (s, 2H), 4,73 та 4,75 (2s, 2H, ротамери), 6,70 6,86 (2d, 2H, ротамери), 7,12 та 7,18 (2d, 2H, ротамери), 7,22-7,41 (m, 3Н), 8,66 (bs, 1H). 13 С ЯМР (100МГц, CDCI3): δ 13,8, 15,1, 20,1, 29,2, 30,8, 38,0, 42,2 (d), 44,6 (d), 46,3, 47,5, 66,8, 67,4, 68,1, 79,8, 113,0 (m), 114,4, 114,6, 121,4 (m), 123,3 (q), 128,3 (m), 129,1 (d), 130,2, 130,7, 130,8,131,0 (d), 131,0-132,2 (m), 156,7, 156,9, 160,3 (d), 160,5 (d), 168,8, 168,9, 175,6. (Число піків більше числа атомів карбону внаслідок ротамерів.) Приклад 2 (2S)-3-(4-{2-[(4-хлорбензил)(етил)аміно]-2оксоетокси}феніл)-2-етоксипропанова кислота (і) Етил (2S)-3-(4-{2-[(4-хлорбензил)етил)аміно]-2-оксоетокси}феніл)-2етоксипропаноат До розчину N-(4-хлорбензил)-N-етиламіну (0,150г, 0,88ммоль) та {4-[(2S)-2,3-діетокси-3оксопропіл]фенокси}оцтової кислот (0,270г, 0,91ммоль) у метиленхлориді (10мл) додають Ν,Νдіізопропілетиламін (0,34мл, 1,9ммоль) та О(бензотриазол-1-іл)-N,N,N',N'-тетраметилуроній тетрафлуорборат (0,320г, 1,00ммоль) та реакційну суміш перемішують при кімнатній температурі протягом ночі. Утворений розчин розбавляють метиленхлоридом (40мл) та органічну фазу промивають 5% НСІ (50мл), насиченим водним розчином натрій гідрогенкарбонату (50мл), та розсолом (50мл), сушать натрій сульфатом та концентрують у вакуумі. Очистка на попередньо упакованій колонці силікагелю (Колонка Isolute® SPE, 50г/150мл) з метиленхлоридом/етилацетатом 10:1 як елюентом, дає 0,24г (61%) безбарвного масла. 1 Н ЯМР (500МГц, CDCI3): δ 1,05-1,24 (m, 9H), 2,88-3,00 (m, 2H), 3,28-3,42 (m, 3Н), 3,60 (m, 1H), 3,96 (m, 1H), 4,12-4,20 (m, 2H), 4,56 та 4,58 (2s, 2H, ротамери), 4,64 та 4,73 (2s, 2Н, ротамери), 6,75 та 6,88 (2d, 2Н, ротамери), 7,09-7,20 (у, 4Н), 7,24 та 7,30 (2d, 2H, ротамери). (іі) (2S)-3-(4-{2-[(4-Хлорбензил)-етил)амінo]-2оксоетокси}феніл)-2-етоксипропанова кислота До розчину етил (2S)-3-(4-{2-[(4хлорбензил)(етил)аміно]-2-оксоетокси}феніл)-2етоксипропаноату (0,240г, 0,54ммоль) у ТГФ (30мл) додають водний 0,10Μ LiOH (15мл) та розчин перемішують при кімнатній температурі протягом ночі. Після нейтралізації 5% НСІ, об'єм розчиннику зменшують у вакуумі та залишкову водну фазу підкислюють 5% НСІ та екстрагують метиленхлоридом (2´50мл). Поєднану органічну фазу промивають розсолом (50мл), сушать натрій сульфатом, та концентрують у вакуумі. Очистка на попередньо упакованій колонці силікагелю (Колонка Isolute® SPE, 2г/15мл) з етилацетатом як елюентом дає 0,138г (61%) блідого жовтого масла. 1 Н ЯМР (500МГц, CDCI3): δ 1,05-1,21 (m, 6H), 2,94 (m, 1H), 3,04 (m, 1H), 3,30-3,45 (m, 3Н), 3,61 (m, 1H), 4,01 (m, 1H), 4,57 та 4,58 (2s, 2H, ротамери), 4,66 та 4,73 (2s, 2H, ротамери), 6,74 та 6,87 (2d, 2H, ротамери), 7,10-7,20 (m, 4H), 7,24 та 7,30 (d, 2H), 7,98 (bs, 1H). 27 13 80729 С ЯМР (100МГц, CDCI3): δ 12,3, 13,9, 15,1, 38,0, 41,2, 41,5, 47,6, 49,8, 66,7, 67,4, 68,0, 79,8, 114,5, 114,6, 128,3, 128,8, 129,1, 129,5, 130,2, 130,7, 133,3, 133,6, 135,0, 135,7, 156,7, 156,9, 168,4, 168,4, 175,5. (Число піків більше числа атомів карбону внаслідок ротамерів.). Приклад 3 (2S)-2-Етокси-3-[4-(2-{етил[4(трифлуорметокси)бензил]аміно}-2оксоетокси)феніл]-пропанова кислота (і) N-[4-(Трифлуорметокси)бензил]ацетамід До розчину 4-(трифлуорметокси)бензиламіну (3,46г, 57,6ммоль) у ДМФ (75мл) та оцтової кислоти (10,0г, 52,3ммоль) при -10°С додають (бензотриазол-1-іл)-Ν,Ν,Ν',Ν'-тетраметилуроній тетрафлуорборат (20,2г, 62,8ммоль) та Ν,Νдіізопропілетиламін (20,0мл, 115ммоль) та реакційну суміш перемішують при кімнатній температурі протягом ночі. Етилацетат (200мл) додають та органічну фазу промивають водою (100мл), 0,25Μ NaOH (100мл), насиченим водним розчином натрій гідрогенкарбонату (100мл), водою (100мл), 0,5Μ НСІ (100мл), та водою (100мл), сушать магній сульфатом, та концентрують у вакуумі, отримуючи 11,2г (92%) безбарвного масла. 1 Н ЯМР (600МГц, CDCI3): δ 2,03 (s, 3Н), 4,43 (d, 2H), 5,83 (bs, 1H), 7,17 (d, 2H), 7,31 (d, 2H). 1З С ЯМР (125 МГц, CDCI3): δ 22,9, 42,8, 120,5 (q), 121,1, 129,0, 137,3, 148,4, 170,6. (ii) N-етил-N-[4-(Трифлуорметокси)бензил]амін N-[4-(Трифлуорметокси)бензил]ацетамід (10,4г, 44,6ммоль) розчиняють у ТГФ (100мл) та охолоджують до -10°С. Боран (56мл 2Μ розчин диметилсульфідного комплексу у діетиловому етері) додають та реакційну суміш перемішують при -10°С протягом 15 хвилин та тоді дозволяють нагрітися до кімнатної температури. Реакційну суміш гріють при кипінні під зворотним холодильником протягом ночі та тоді дозволяють охолонути до кімнатної температури. Реакцію гасять обережним додаванням 10% НСІ (30мл) при 0°С та суміш перемішують при кімнатній температурі протягом ночі та тоді концентрують у вакуумі. Залишок переміщають у воду (200мл) та діетиловий етер (200мл) та фази розділяють. Концентрація у вакуумі етерної фази дає 1,9г (21%) заголовної сполуки як безбарвне масло. 1 Н ЯМР (300МГц, CDCI3): δ 1,28 (t, 3Н), 2,72 (q, 2H), 3,83 (s, 2H), 3,86 (bs, 1H), 7,18 (d, 2H),7,40 (d, 2H). iii) Етил (2S)-2-етокси-3-[4-[2-(етил[4(трифлуорметокси)бензил]аміно)-2оксоетоксифеніл]пропаноат До розчину N-етил-N-[4(трифлуорметокси)бензил]амін (0,438г, 2,00ммоль) та {4-[(2S)-2,3-діетокси-3оксопропіл]фенокси}оцтової кислоти (0,593г, 2,00ммоль) у метиленхлориді (20мл) додають Ν,Νдіізопропілетиламін (0,80мл, 4,6ммоль) та О(бензотриазол-1-іл)-N,N,N',N'-тетраметилуроній тетрафлуорборат (0,674г, 2,10ммоль) та реакційну суміш перемішують при кімнатній температурі протягом ночі. Утворений розчин розбавляють метиленхлоридом (40мл) та органічну фазу 28 промивають 5% НСІ (50мл), насиченим водним розчином натрій гідрогенкарбонату (50мл), та розсолом (50мл), сушать натрій сульфатом, та концентрують у вакуумі. Очистка на попередньо упакованій колонці силікагелю (Колонка Isolute® SPE, 50г/150мл) з метиленхлоридом/етилацетатом 10:1 як елюентом, дає 0,57г (58%) безбарвного масла. 1 Н ЯМР (500МГц, CDCI3): δ 1,08-1,28 (m, 9H), 2,88-3,00 (m, 2H), 3,28-3,44 (m, 3Н), 3,60 (m, 1H), 3,96 (m, 1H), 4,12-4,20 (m, 2H), 4,60 та 4,62 (2s, 2H, ротамери), 4,66 та 4,74 (2s, 2H, ротамери), 6,74 та 6,89 (2d, 2Н, ротамери), 7,08-7,27 (m, 6H). 13 С ЯМР (100МГц, CDCI3): δ 12,4, 14,0, 14,4, 15,2, 38,6, 41,1, 41,5, 47,5, 49,7, 61,0, 66,3, 67,7, 68,3, 80,4, 114,5, 114,6, 121,2, 121,5, 128,3, 129,5, 130,6, 130,7, 130,7, 135,6, 136,1, 148,6, 156,9, 168,1, 168,2, 172,6. (Число піків більше числа карбонів внаслідок ротамерів. Трифлуорований карбон не показано.) (iv) (2S)-2-етокси-3-[4-[2-(етил-4(трифлуорметокси)бензил]аміно)-2оксоетокси)феніл1-пропанова кислота. До розчину етил (2S)-2-етокси-3-[4-(2-(етил[4(трифлуорметокси)бензил]аміно}-2оксоетокси)феніл]пропаноату (0,560г, 1,13ммоль) у ТГФ (50мл) додають водний 0,10Μ LiOH (25мл) та розчин перемішують при кімнатній температурі протягом ночі. Після нейтралізації 5% НСІ, об'єм розчиннику зменшують у вакуумі та залишкову водну фазу підкислюють 5% НСІ та екстрагують етилацетатом (2´50мл). Поєднану органічну фазу промивають розсолом (50мл), сушать натрій сульфатом, та концентрують у вакуумі. Очистка на попередньо упакованій колонці силікагелю (Колонка Isolute® SPEa, 10г/70мл) з етилацетатом як елюентом дає 0,457г (87%) безбарвного масла. 1 Н ЯМР (500МГц, CDCI3): δ 1,08-1,23 (m, 6H), 2,96 (m, 1H), 3,08 (m, 1H), 3,33-3,43 (m, 2H), 3,48 (m, 1H), 3,59 (m, 1H), 4,05 (m, 1H), 4,60 та 4,62 (2s, 2Н, ротамери), 4,67 та 4,75 (2s, 2H, ротамери), 6,75 та 6,89 (2d, 2H, ротамери), 7,09-7,27 (m, 6H). 13 С ЯМР (100МГц, CDCI3): δ 12,4, 14,0, 15,2, 37,8, 41,2, 41,6, 47,5, 49,7, 67,0, 67,6, 68,2, 79,8, 114,6, 114,8, 121,2, 121,5,128,3, 129,5, 129,9, 130,8, 130,8, 135,4, 136,0, 148,7, 148,8, 156,9, 157,0, 168,3, 168,3, 174,2. (Число піків більше числа карбонів внаслідок ротамерів. Трифлуорований карбон не показано.) Приклад 4 (2S)-2-Етокси-3-[4-(2-(етил[4(трифлуорметил)бензил]аміно]-2оксоетокси)феніл]пропанова кислота (і) Етил (2S)-2-етокси-3-[4-[2-(етил[4(трифлуорметил)бензил]аміно)-2-оксоетокси) феніл]пропаноат До розчину N-етил-N-[4(трифлуорметил)бензил]аміну (0,213г, 1,05ммоль) та {4-[(2S)-2,3-діетокси-3оксопропіл]фенокси}оцтової кислоти (0,296г, 1,00ммоль) у метиленхлориді (10мл) додають Ν,Νдіізопропілетиламін (0,40мл, 2,3ммоль) та О(бензотіазол-1-іл)-N,N,N',N'-тетраметилуроній тетрафлуорборат (0,337г, 1,05ммоль) та реакційну суміш перемішують при кімнатній температурі 29 80729 протягом ночі. Утворений розчин розбавляють метиленхлоридом (90мл) та органічну фазу промивають 5% НСІ (2 χ 50мл), насиченим водним розчином натрій гідрогенкарбонату (2´50мл), та розсолом (50мл), сушать натрій сульфатом, та концентрують у вакуумі. Очистка на попередньо упакованій колонці силікагелю (Колонка Isolute® SPEa, 50г/150мл) з метанолом (0-1% градієнт) у метиленхлориді як елюентом, дає 0,339г (70%) безбарвного масла. 1 Н ЯМР (400МГц, CDCI3): δ 1,06-1,24 (m, 9H), 2,88-3,00 (m, 2H), 3,28-3,44 (m, 3Н), 3,59 (m, 1H), 3,96 (m, 1H), 4,10-4,19 (m, 2H), 4,64, 4,67, та 4,74 (3s, 4H, ротамери), 6,71 та 6,88 (2d, 2H, ротамери), 7,10 та 7,17 (2d, 2H, ротамери), 7,30 (d, 2H), 7,52 та 7,57 (2d, 2H, ротамери). 13 С ЯМР (100МГц, CDCI3): δ 12,3, 13,9, 14,3, 15,1, 38,5, 41,2, 41,7, 47,8, 49,9, 60,8, 66,2, 67,6, 68,2, 80,3, 114,4, 114,5, 125,5 (m), 125,8 (m), 127,1, 128,2, 129,2-130,6 (у), 130,5, 130,6, 130,6, 141,0, 141,5, 156,6, 156,8, 168,1, 168,2, 172,5. (Число піків більше числа атомів карбону внаслідок ротамерів. Трифлуорований карбон не показано.) (іі) (2S)-2-Етокси-3-[4-(2-(етил[4(трифлуорметил)бензил]аміно)-2оксоетокси)феніл]пропанова кислота До розчину етил (2S)-2-етокси-3-[4-(2-{етил[4(трифлуорметил)бензил]аміно}-2оксоетокси)феніл]пропаноату ((0,308г, 0,64ммоль) в ацетонітрилі (32мл) додають водний 0,10Μ LiOH (16мл) та розчин перемішують при кімнатній температурі протягом ночі. Після нейтралізації 5% НСІ, об'єм розчиннику зменшують у вакуумі та залишкову водн у фазу розбавляють водою та водним 0,10Μ LiOH (до повного об'єму 100мл, рН10) та промивають діетиловим етером (2´100мл). Водну фазу підкислюють 5% НСІ та екстрагують етилацетатом (3´100мл). Поєднану органічну фазу промивають 5% НСІ (100мл) та розсолом (100мл), сушать натрій сульфатом, та концентрують у вакуумі, отримуючи 0,279г (96%) безбарвного масла. 1 H ЯМР (400МГц, CDCI3): δ 1,08-1,24 (m, 6H), 2,88-3,12 (m, 2H), 3,34-3,47 (m, 3Н), 3,61 > (m, 1H), 4,02 (m, 1H), 4,66, 4,67, 4,69, та 4,76 (4s, 4H, ротамери), 6,72 та 6,89 (2d, 2H, ротамери), 7,12 та 7,19 (2d, 2H, ротамери), 7,32 (d, 2H), 7,53 та 7,58 (2d, 2Н, ротамери), 8,08 (bs, 1H). 13 С ЯМР (100МГц, CDCI3): δ 12,3, 13,9, 15,1, 38,0, 41,4, 41,9, 48,0, 50,1, 66,8, 67,5, 68,1, 79,8, 114,5, 114,7, 125,6 (m), 125,9 (m), 127,2, 128,2, 129,2-130,6 (m), 130,2, 130,7, 130,8, 140,8, 141,3, 156,7, 156,9, 168,6, 168,6, 175,5. (Число піків більше числа атомів карбону внаслідок ротамерів. Трифлуорований карбон не показано.) Приклад 5 (2S)-3-{4-(2-(Бутил[4(трифлуорметил)бензил]аміно)-2оксоетокси)феніл]-2-етоксипропанова кислота (і) Етил (2S)-3-[4-[2-(бутил[4(трифлуорметил)бензил]аміно)-2оксоетокси)феніл]-2-етоксипропаноат До розчину N-бутил-N-[4(трифлуорметил)бензил]аміну (0,486г, 2,10ммоль) та {4-[(2S)-2,3-діетокси-3 30 оксопропіл]фенокси}оцтової кислоти (0,593г, 2,00ммоль) у метиленхлориді (20мл) додають Ν,Νдіізопропілетиламін (0,80мл, 4,6ммоль) та О(бензотриазол-1-іл)-Ν,Ν,Ν',Ν'-тетраметилуроній тетрафлуорборат (0,674г, 2,10ммоль) та реакційну суміш перемішують при кімнатній температурі протягом ночі. Утворений розчин розбавляють метиленхлоридом (80мл) та органічну фазу промивають 5% НСІ (3´50мл), насиченим водним розчином натрій гідрогенкарбонату (2´50мл), та розсолом (50мл), сушать натрій сульфатом, та концентрують у вакуумі. Очистка на попередньо упакованій колонці силікагелю (Колонка Isolute® SPEa, 70г/150мл) з метанолом (0-1% градієнт) у метиленхлориді як елюентом та збирання чистих фракцій, дають 0,355г (35%) безбарвного масла. 1 Н ЯМР (400МГц, CDCI3): δ 0,82-0,93 (m, 3Н), 1,09-1,17 (m, 3Н), 1,20 (t, 3Н), 1,22-1,38 (m, 2H), 1,44-1,61 (m, 2H), 2,87-3,00 (m, 2H), 3,25-3,39 (m, 3H), 3,59 (m, 1H), 3,96 (m, 1H), 4,08-4,18 (m, 2H), 4,64, 4,68, та 4,75 (3s, 4H, ротамери), 6,72 та 6,87 (2d, 2H, ротамери), 7,10 та 7,17 (2d, 2H, ротамери), 7,29 (d, 2Н), 7,51 та 7,56 (2d, 2H, ротамери). 13 С ЯМР (100МГц, CDCI3): δ 13,5, 14,0, 14,9, 19,9, 29,0, 30,5, 38,3, 45,9, 46,7, 48,1, 50,1, 60,6, 66,0, 67,3, 67,9, 80,1, 114,2, 114,3, 125,3 (m), 125,6 (m), 126,9, 127,9, 128,8-130,5 (m), 130,2, 130,3, 130,4, 141,0, 141,4, 156,5, 156,7, 168,1, 172,2. (Число піків є більше числа атомів карбону внаслідок ротамерів. Трифлуорований карбон не показано.) (іі) (2S)-3-[4-(2-(Бутил[4[трифлуорметил)бензил]аміно)-2оксоетокси)феніл]-2-етоксипропанова кислота До розчину етил (2S)-3-[4-(2-{бутил[4(трифлуорметил)бензил]аміно}-2оксоетокси)феніл]-2-етоксипропаноату (0,311г, 0,61ммоль) в ацетонітрилі (30мл) додають водний 0,10Μ LiOH (15мл) та розчин перемішують при кімнатній температурі протягом ночі. Після підкислення 5% НСІ, суміш екстрагують етилацетатом (3´100мл) та поєднану органічну фазу промивають 5% НСІ (100мл) та розсолом (100мл), сушать натрій сульфатом, та концентрують у вакуумі, отримуючи 0,232г (79%) безбарвного масла. 1 H ЯМР (400МГц, CDCI3): δ 0,84-0,94 (m, 3Н), 1,10-1,19 (m, 3Н), 1,20-1,36 (m, 2H), 1,46-1,62 (m, 2H), 2,87-3,10 (m, 2H), 3,25-3,45 (m, 2H), 3,61 (m, 1H), 4,01 (m, 1H), 4,66, 4,69 та 4,76 (3s, 4H, ротамери), 6,72 та 6,88 (2d, 2H, ротамери), 7,12 та 7,19 (2d, 2Н, ротамери), 7,30 (d, 2h), 7,53 та 7,59 (2d, 2H, ротамери), 8,27 (bs, 1H). 13 С ЯМР (100МГц, CDCI3): δ 13,8, 15,1, 20,1, 29,2, 30,7, 38,0, 46,3, 47,0, 48,4, 50,4, 66,7, 67,4, 68,1, 79,8, 114,5, 114,6, 125,6 (m), 125,9 (m), 127,1, 128,2, 129,2-130,5 (m), 130,2, 130,7, 130,8, 140,8, 141,2, 156,7, 156,9, 168,8, 175,6. (Число піків більше числа атомів карбону внаслідок ротамерів. Трифлуорований карбон не показано.) Біологічна активність Сполуки винаходу тестують в аналізах, описаних [у WO03/051821]. Сполуки формули І мають ЕK50 менше 0,1мкмоль/л стосовно АППРα, а особливі сполуки мають ЕK50 менше 0,01 31 80729 мкмоль/л. Додатково у конкретних сполуках співвідношення ЕK50 (ΑΠΠΡg): ΕΚ50 (ΑΠΠΡα) більше 150:1. Вважають, що це співвідношення є важливим з огляду на фармакологічну активність сполук та їх терапевтичного профілю. На додаток сполуки представленого винаходу виявляють поліпшені МЛФК (метаболізм ліків та фармакокінетика) властивості, наприклад, вони виявляють поліпшену метаболічну стабільність in vitro. Сполуки також мають багатообіцяючий токсикологічний профіль. ЕK50 з прикладів для людини АППР альфа є; Приклад 1 Приклад 2 Приклад 3 Приклад 4 Приклад 5 0,001мкмоль/л 0,003мкмоль/л 0,003мкмоль/л 0,005мкмоль/л 0,003мкмоль/л. 32
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted (2s)-2-ethoxy-3-phenylpropanoic acids
Автори англійськоюOlsson Anna Christina, Li Lanna, Aurell Carl-Johan, Minidis Anna, Yousefi-Salakdeh Esmail, Dahlstrom Mikael Ulf Johan
Назва патенту російськоюЗамещенные (2s)-2-этокси-3-фенилпропановые кислоты
Автори російськоюОльссон Анна Кристина, Ли Ланна, Орелль Карл-Йоган, Минидис Анна, Юсефи-Салакдех Эсмаил, Дальстром Микаэль Ульф Йоган
МПК / Мітки
МПК: C07C 235/20, A61K 31/16
Мітки: заміщені, 2s)-2-етокси-3-фенілпропанові, кислоти
Код посилання
<a href="https://ua.patents.su/16-80729-zamishheni-2s-2-etoksi-3-fenilpropanovi-kisloti.html" target="_blank" rel="follow" title="База патентів України">Заміщені (2s)-2-етокси-3-фенілпропанові кислоти</a>
Попередній патент: Теплова дискретна вимірювальна лінія
Наступний патент: Спосіб одержання активованих рідин
Випадковий патент: Лінія гідрозмиву окалини












