Заміщені похідні фенілпропіонової кислоти як агоністи активованого пероксизомним проліфератором рецептора альфа (аппр) людини, спосіб їх одержання, фармацевтична композиція на їх основі, проміжна сполука (варіанти)
Номер патенту: 77460
Опубліковано: 15.12.2006
Автори: Альстермарк Ліндстедт Ева-Лотте, Ольссон Анна Крістіна, Лі Ланна
Формула / Реферат
1. S-енантіомер сполуки формули І
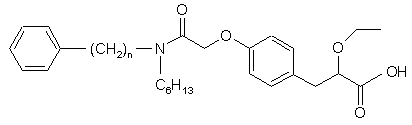 , I
, I
де n дорівнює 1 або 2, та її фармацевтично прийнятні солі, сольвати, кристалічні форми та проліки.
2. Сполука, яку вибрано з групи, що складається з
(2S)-3-(4-{2-[бензил(гексил)аміно]-2-оксоетокси}феніл)-2-етоксипропанової кислоти,
(2S)-2-етокси-3-(4-{2-[гексил(2-фенілетил)аміно]-2-оксоетокси}феніл)пропанової кислоти та їх фармацевтично прийнятних солей, сольватів і кристалічних форм.
3. (2S)-3-(4-{2-[бензил(гексил)аміно]-2-оксоетокси}феніл)-2-етоксипропанова кислота та її фармацевтично прийнятні солі, сольвати і кристалічні форми.
4. (2S)-2-етокси-3-(4-{2-[гексил(2-фенілетил)аміно]-2-оксоетокси}феніл)пропанова кислота та її фармацевтично прийнятні солі, сольвати і кристалічні форми.
5. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-4 у суміші з фармацевтично прийнятними ад'ювантами, розріджувачами та/або носіями.
6. Спосіб лікування або профілактики ліпідних розладів (дисліпідемії), пов'язаних або ні з резистентністю до інсуліну, який передбачає введення сполуки за будь-яким з пп. 1-4 ссавцю, що потребує цього.
7. Використання сполуки за будь-яким з пп. 1-4 у виготовленні медикаменту, призначеного для лікування ліпідних розладів (дисліпідемії), пов'язаних або ні з резистентністю до інсуліну.
8. Спосіб лікування або профілактики діабету типу 2, який полягає в уведенні ефективної кількості сполуки формули І за будь-яким з пп. 1-4 ссавцю, що потребує цього.
9. Спосіб отримання сполуки формули І, в якому піддають реакції сполуку формули II
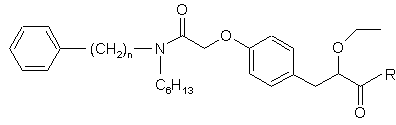 , II
, II
в якій n визначено раніше, a R представляє захисну групу для гідроксилу карбоксильної групи, із засобом зняття захисту.
10. Сполука формули II
 , II
, II
в якій n визначено раніше, a R представляє захисну групу для гідроксилу карбоксильної групи.
11. Сполука формули III
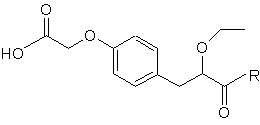 , III
, III
у якій R має значення, визначене вище.
12. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-4 у комбінації з іншим терапевтичним засобом, корисним у лікуванні розладів, пов'язаних з виникненням і перебігом атеросклерозу, наприклад, гіпертензії, гіперліпідемій, дисліпідемій, діабету і ожиріння.
13. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-4 у комбінації з іншим засобом, що модулює ПАРП.
14. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-4 у комбінації з засобом, що знижує рівень холестерину.
15. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-4 у комбінації з інгібітором HMG-CoA-редуктази.
16. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-4 у комбінації з аторвастатином або його фармацевтичнo прийнятною сіллю, сольватом, кристалічною формою або проліками.
17. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-4 у комбінації з розувастатином або його фармацевтичнo прийнятною сіллю.
18. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-4 у комбінації з інгібітором ТЖККК.
19. Фармацевтична композиція за п. 18, яка відрізняється тим, що її інгібітор ТЖККК вибрано із таких сполук:
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-1'-феніл-1'-[N'-(карбоксиметил)-карбамоїл]метил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N'-(карбоксиметил)карбамоїл]-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-[N'-(карбоксиметил)карбамоїл]-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-1'-феніл-1'-[N'-(2-сульфоетил)-карбамоїл]метил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N'-{(R)-1'-феніл-1'-[N'-(2-сульфоетил)-карбамоїл]метил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N'-(2-сульфоетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-[N'-(2-сульфоетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N’-(2-сульфоетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-[N’-(2-сульфоетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N’-(2-карбоксіетил)-карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-[N’-(2-карбоксіетил)-карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N'-(2-карбоксіетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-[N'-(2-карбоксіетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N'-(5-карбоксипентил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-[N'-(5-карбоксипентил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N’-(2-карбоксіетил)карбамоїл]-бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-[N’-(2-карбоксіетил)карбамоїл]-бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{![]() -[N’-(2-сульфоетил)карбамоїл]-2-флуорбензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-[N’-(2-сульфоетил)карбамоїл]-2-флуорбензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N’-(R)-(2-гідрокси-1-карбоксіетил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-[N’-(R)-(2-гідрокси-1-карбоксіетил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N’-(R)-(2-гідрокси-1-карбоксіетил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-[N’-(R)-(2-гідрокси-1-карбоксіетил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-{N-[(R)-![]() -(N'-{(R)-1-[N"-(R)-(2-гідрокси-1-карбоксіетил)карбамоїл]-2-гідроксиетил}карбамоїл)бензил]карбамоїлметокси}-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-(N'-{(R)-1-[N"-(R)-(2-гідрокси-1-карбоксіетил)карбамоїл]-2-гідроксиетил}карбамоїл)бензил]карбамоїлметокси}-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N-{![]() -[N’-(карбоксиметил)карбамоїл]-карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-[N’-(карбоксиметил)карбамоїл]-карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8-(N-{![]() -[N’-((етокси)(метил)фосфорилметил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-[N’-((етокси)(метил)фосфорилметил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8{N-[(R)-![]() -(N'{2-[(гідрокси)(метил)фосфорил]етил}карбамоїл)бензил]карбамоїлметокси}-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-(N'{2-[(гідрокси)(метил)фосфорил]етил}карбамоїл)бензил]карбамоїлметокси}-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N'-(2-метилтіо-1-карбоксіетил)-карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-[N'-(2-метилтіо-1-карбоксіетил)-карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-{N(R)-![]() -(N'-{2-[(метил)(етил)фосфорил]-етил}карбамоїл)-4-гідроксибензил]карбамоїлметокси}-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-(N'-{2-[(метил)(етил)фосфорил]-етил}карбамоїл)-4-гідроксибензил]карбамоїлметокси}-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-{N-[(R)-![]() -(N'-{2-[(метил)(гідрокси)фосфорил]етил}карбамоїл)-4-гідроксибензил]карбамоїлметокси}-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-(N'-{2-[(метил)(гідрокси)фосфорил]етил}карбамоїл)-4-гідроксибензил]карбамоїлметокси}-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-(N-{(R)-![]() -[(R)-N'-(2-мeтилcyльфoнiл-1-карбоксіетил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-[(R)-N'-(2-мeтилcyльфoнiл-1-карбоксіетил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтoкcи-8-[N-{(R)-![]() -[N'-(2-cyльфoeтил)каpбамoїл]-4-гідроксибензил}карбамоїлметокси]-2,3,4,5-тетрагідро-1,5-бензотіазепін;
-[N'-(2-cyльфoeтил)каpбамoїл]-4-гідроксибензил}карбамоїлметокси]-2,3,4,5-тетрагідро-1,5-бензотіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N-((R)-1-карбокси-2-метилтіоетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
-[N-((R)-1-карбокси-2-метилтіоетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-8-феніл-7-метилтіо-8-(N-{(R)-![]() -[N-((S)-1-карбокси-2-(R)-гідроксипропіл)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
-[N-((S)-1-карбокси-2-(R)-гідроксипропіл)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N-((S)-1-карбокси-2-метилпропіл)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
-[N-((S)-1-карбокси-2-метилпропіл)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N-((S)-1-карбоксибутил)-карбамоїл]-4-гідроксибензил}карбамоїлметокси)2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
-[N-((S)-1-карбоксибутил)-карбамоїл]-4-гідроксибензил}карбамоїлметокси)2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N-((S)-1-карбоксипропіл)-карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
-[N-((S)-1-карбоксипропіл)-карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N-((S)-1-карбоксіетил)-карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
-[N-((S)-1-карбоксіетил)-карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N-((S)-1-карбокси-2-(R)-гідроксипропіл)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
-[N-((S)-1-карбокси-2-(R)-гідроксипропіл)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N-(2-сульфоетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
-[N-(2-сульфоетил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N-((S)-1-карбоксіетил)-карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
-[N-((S)-1-карбоксіетил)-карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N-((R)-1-карбокси-2-метилтіоетил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
-[N-((R)-1-карбокси-2-метилтіоетил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-![]() -[N-{(S)-1-[N-((S)-2-гідрокси-1-карбоксіетил)карбамоїл]пропіл}карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
-[N-{(S)-1-[N-((S)-2-гідрокси-1-карбоксіетил)карбамоїл]пропіл}карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)-![]() -[N-((S)-1-карбокси-2-метилпропіл)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
-[N-((S)-1-карбокси-2-метилпропіл)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N-((S)-1-карбоксипропіл)-карбамоїл]4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
-[N-((S)-1-карбоксипропіл)-карбамоїл]4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-[N-((R/S)-![]() -{N-[1-(R)-2-(S)-1-гідрокси-1-(3,4-дигідроксифеніл)проп-2-іл]карбамоїл}-4-гідроксибензил)карбамоїлметокси]-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
-{N-[1-(R)-2-(S)-1-гідрокси-1-(3,4-дигідроксифеніл)проп-2-іл]карбамоїл}-4-гідроксибензил)карбамоїлметокси]-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N-(2-(S)-3-(R)-4-(R)-5-(R)-2,3,4,5,6-пентагідроксигексил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін і
-[N-(2-(S)-3-(R)-4-(R)-5-(R)-2,3,4,5,6-пентагідроксигексил)карбамоїл]-4-гідроксибензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін і
1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N-{(R)-![]() -[N-(2-(S)-3-(R)-4-(R)-5-(R)-2,3,4,5,6-пентагідроксигексил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
-[N-(2-(S)-3-(R)-4-(R)-5-(R)-2,3,4,5,6-пентагідроксигексил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін;
або їх фармацевтично прийнятна сіль, сольват, сольват такої солі або проліки.
Текст
1. S-енантіомер сполуки формули І 2 (11) 1 UA (54) ЗАМІЩЕНІ ПОХІДНІ ФЕНІЛПРОПІОНОВОЇ КИСЛОТИ ЯК АГОНІСТИ АКТИВОВАНОГО ПЕРОКСИЗОМНИМ ПРОЛІФЕРАТОРОМ РЕЦЕПТОРА АЛЬФА (АППР) ЛЮДИНИ, СПОСІБ ЇХ ОДЕРЖАННЯ, ФАРМАЦЕВТИЧНА КОМПОЗИЦІЯ НА ЇХ ОСНОВІ, ПРОМІЖНА СПОЛУКА (ВАРІАНТИ) C2 ДО ПАТЕНТУ НА ВИНАХІД (19) ДЕРЖАВНИЙ ДЕПАРТАМЕНТ ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ 3 77460 4 розладів (дисліпідемії), пов'язаних або ні з резис{(R)-1'-феніл-1'-[N'-(карбоксиметил)тентністю до інсуліну, який передбачає введення карбамоїл]метил}карбамоїлметокси)-2,3,4,5сполуки за будь-яким з пп.1-4 ссавцю, що потрететрагідро-1,5-бензотіазепін; бує цього. 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N7. Використання сполуки за будь-яким з пп.1-4 у {(R)- -[N'-(карбоксиметил)карбамоїл]виготовленні медикаменту, призначеного для гідроксибензил}карбамоїлметокси)-2,3,4,5лікування ліпідних розладів (дисліпідемії), пов'ятетрагідро-1,5-бензотіазепін; заних або ні з резистентністю до інсуліну. 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N8. Спосіб лікування або профілактики діабету {(R)-1'-феніл-1'-[N'-(2-сульфоетил)типу 2, який полягає в уведенні ефективної кількарбамоїл]метил}карбамоїлметокси)-2,3,4,5кості сполуки формули І за будь-яким з пп.1-4 тетрагідро-1,5-бензотіазепін; ссавцю, що потребує цього. 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-89. Спосіб отримання сполуки формули І, в якому (N'-{(R)-1'-феніл-1'-[N'-(2-сульфоетил)піддають реакції сполуку формули II карбамоїл]метил}карбамоїлметокси)-2,3,4,5O тетрагідро-1,5-бензотіазепін; O O (CH ) N 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(NR CH {(R)- -[N'-(2-сульфоетил)карбамоїл]-4O , II гідроксибензил}карбамоїлметокси)-2,3,4,5в якій n визначено раніше, a R представляє захитетрагідро-1,5-бензотіазепін; сну групу для гідроксилу карбоксильної групи, із 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8засобом зняття захисту. (N-{(R)- -[N’-(2-сульфоетил)карбамоїл]-410. Сполука формули II гідроксибензил}карбамоїлметокси)-2,3,4,5O тетрагідро-1,5-бензотіазепін; O O (CH ) N 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8R CH (N-{(R)- -[N’-(2-карбоксіетил)O , II карбамоїл]бензил}карбамоїлметокси)-2,3,4,5в якій n визначено раніше, a R представляє захитетрагідро-1,5-бензотіазепін; сну групу для гідроксилу карбоксильної групи. 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N11. Сполука формули III {(R)- -[N'-(2-карбоксіетил)карбамоїл]-4O гідроксибензил}карбамоїлметокси)-2,3,4,5O O HO тетрагідро-1,5-бензотіазепін; R 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8O (N-{(R)- -[N'-(5, III у якій R має значення, визначене вище. карбоксипен12. Фармацевтична композиція, яка містить спотил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5луку за будь-яким з пп.1-4 у комбінації з іншим тетрагідро-1,5-бензотіазепін; терапевтичним засобом, корисним у лікуванні 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(Nрозладів, пов'язаних з виникненням і перебігом {(R)- -[N’-(2-карбоксіетил)карбамоїл]атеросклерозу, наприклад, гіпертензії, гіперліпібензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5демій, дисліпідемій, діабету і ожиріння. бензотіазепін; 13. Фармацевтична композиція, яка містить спо1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(Nлуку за будь-яким з пп.1-4 у комбінації з іншим { -[N’-(2-сульфоетил)карбамоїл]-2засобом, що модулює ПАРП. флуорбензил}карбамоїлметокси)-2,3,4,514. Фармацевтична композиція, яка містить спотетрагідро-1,5-бензотіазепін; луку за будь-яким з пп.1-4 у комбінації з засобом, 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-8що знижує рівень холестерину. (N-{(R)- -[N’-(R)-(2-гідрокси-115. Фармацевтична композиція, яка містить спокарбоксіелуку за будь-яким з пп.1-4 у комбінації з інгібітотил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5ром HMG-CoA-редуктази. тетрагідро-1,5-бензотіазепін; 16. Фармацевтична композиція, яка містить спо1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(Nлуку за будь-яким з пп.1-4 у комбінації з аторвас{(R)- -[N’-(R)-(2-гідрокси-1татином або його фармацевтичнo прийнятною карбоксіесіллю, сольватом, кристалічною формою або тил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5проліками. тетрагідро-1,5-бензотіазепін; 17. Фармацевтична композиція, яка містить спо1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-{Nлуку за будь-яким з пп.1-4 у комбінації з розувас[(R)- -(N'-{(R)-1-[N"-(R)-(2-гідрокси-1татином або його фармацевтичнo прийнятною карбоксіетил)карбамоїл]-2сіллю. гідроксие18. Фармацевтична композиція, яка містить спотил}карбамоїл)бензил]карбамоїлметокси}-2,3,4,5луку за будь-яким з пп.1-4 у комбінації з інгібітотетрагідро-1,5-бензотіазепін; ром ТЖККК. 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-819. Фармацевтична композиція за п.18, яка відрі(N-{ -[N’-(карбоксиметил)карбамоїл]зняється тим, що її інгібітор ТЖККК вибрано із карбамоїлметокси)-2,3,4,5-тетрагідро-1,5таких сполук: бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо-82 n 6 13 2 n 6 13 5 77460 6 (N-{ -[N’{(R)- -[N-((S)-1-карбоксіетил)((етоккарбамоїл]бензил}карбамоїлметокси)-2,3,4,5си)(метил)фосфорилметил)карбамоїл]бензил}кар тетрагідро-1,2,5-бензотіадіазепін; бамоїлметокси)-2,3,4,5-тетрагідро-1,51,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(Nбензотіазепін; {(R)- -[N-((S)-1-карбокси-2-(R)1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіогідроксипро8{N-[(R)- -(N'{2піл)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5[(гідроктетрагідро-1,2,5-бензотіадіазепін; си)(метил)фосфорил]етил}карбамоїл)бензил]кар 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(Nбамоїлметокси}-2,3,4,5-тетрагідро-1,5{(R)- -[N-(2-сульфоетил)карбамоїл]-4бензотіазепін; гідроксибензил}карбамоїлметокси)-2,3,4,51,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(Nтетрагідро-1,2,5-бензотіадіазепін; {(R)- -[N'-(2-метилтіо-1-карбоксіетил)1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(Nкарбамоїл]бензил}карбамоїлметокси)-2,3,4,5{(R)- -[N-((S)-1-карбоксіетил)-карбамоїл]-4тетрагідро-1,5-бензотіазепін; гідроксибензил}карбамоїлметокси)-2,3,4,51,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8тетрагідро-1,2,5-бензотіадіазепін; {N(R)- -(N'-{2-[(метил)(етил)фосфорил]1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(Nетил}карбамоїл)-4{(R)- -[N-((R)-1-карбокси-2гідроксибензил]карбамоїлметокси}-2,3,4,5метилтіоететрагідро-1,5-бензотіазепін; тил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,51,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-{Nтетрагідро-1,2,5-бензотіадіазепін; [(R)- -(N'-{21,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8[(метил)(гідрокси)фосфорил]етил}карбамоїл)-4(N{(R)- -[N-{(S)-1-[N-((S)-2-гідрокси-1гідроксибензил]карбамоїлметокси}-2,3,4,5карбоксіететрагідро-1,5-бензотіазепін; тил)карбамоїл]пропіл}карбамоїл]бензил}карбамої 1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтилтio-8-(Nлметокси)-2,3,4,5-тетрагідро-1,2,5{(R)- -[(R)-N'-(2-мeтилcyльфoнiл-1бензотіадіазепін; карбоксіе1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8тил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5(N{(R)- -[N-((S)-1-карбокси-2тетрагідро-1,5-бензотіазепін; метилпро1,1-дioкco-3,3-дибyтил-5-фeнiл-7-мeтoкcи-8-[Nпіл)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5{(R)- -[N'-(2-cyльфoeтил)каpбамoїл]-4тетрагідро-1,2,5-бензотіадіазепін; гідроксибензил}карбамоїлметокси]-2,3,4,51,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(Nтетрагідро-1,5-бензотіазепін; {(R)- -[N-((S)-1-карбоксипропіл)-карбамоїл]41,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(Nгідроксибензил}карбамоїлметокси)-2,3,4,5{(R)- -[N-((R)-1-карбокси-2тетрагідро-1,2,5-бензотіадіазепін; метилтіоетил)карбамоїл]-41,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-[Nгідроксибензил}карбамоїлметокси)-2,3,4,5((R/S)- -{N-[1-(R)-2-(S)-1-гідрокси-1-(3,4тетрагідро-1,2,5-бензотіадіазепін; дигідроксифеніл)проп-2-іл]карбамоїл}-41,1-діоксо-3,3-дибутил-8-феніл-7-метилтіо-8-(Nгідроксибензил)карбамоїлметокси]-2,3,4,5{(R)- -[N-((S)-1-карбокси-2-(R)тетрагідро-1,2,5-бензотіадіазепін; гідроксипропіл)карбамоїл]-41,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(Nгідроксибензил}карбамоїлметокси)-2,3,4,5{(R)- -[N-(2-(S)-3-(R)-4-(R)-5-(R)-2,3,4,5,6тетрагідро-1,2,5-бензотіадіазепін; пентагідроксигексил)карбамоїл]-41,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(Nгідроксибензил}карбамоїлметокси)-2,3,4,5{(R)- -[N-((S)-1-карбокси-2тетрагідро-1,2,5-бензотіадіазепін і метилпропіл)карбамоїл]-41,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(Nгідроксибензил}карбамоїлметокси)-2,3,4,5{(R)- -[N-(2-(S)-3-(R)-4-(R)-5-(R)-2,3,4,5,6тетрагідро-1,2,5-бензотіадіазепін; пентагідроксигек1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(Nсил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5{(R)- -[N-((S)-1-карбоксибутил)-карбамоїл]-4тетрагідро-1,2,5-бензотіадіазепін; гідроксибензил}карбамоїлметокси)2,3,4,5або їх фармацевтично прийнятна сіль, сольват, тетрагідро-1,2,5-бензотіадіазепін; сольват такої солі або проліки. 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N{(R)- -[N-((S)-1-карбоксипропіл)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-(N 7 Винахід стосується певних нових похідних (2S)-3-(4-{2-[аміно]-2-оксоетокси}феніл)-2етоксипропанової кислоти, способів отримання таких сполук, їх використання у лікуванні клінічних станів, включаючи ліпідні розлади (дисліпідемії), пов'язані або ні з резистентністю до інсуліну і іншими проявами метаболічного синдрому, способів їх терапевтичного використання і фармацевтичних композицій, що їх містять. Метаболічним синдромом, що охоплює цукровий діабет типу 2, називають прояви, що включають резистентність до інсуліну із супроводжуючими гіперінсулінемією, можливо, цукровим діабетом типу 2, артеріальною гіпертензією, центральним (вісцеральним ожирінням), дисліпідемією, що спостерігається як порушення рівнів ліпопротеїну і характеризується підвищеними концентраціями ЛДНГ (ліпопротеїни дуже низької густини), частинок низької густини (ЧНГ) і зниженням концентрації ліпопротеїну високої густини і зниженим фібринолізом. Сучасні епідеміологічні дослідження показали, що особам з резистентністю до інсуліну властивий високий ризик серцево-судинної захворюваності і смерті, зокрема, виникнення інфаркту міокарду і інсульту. Стани, пов'язані з атеросклерозом, викликаним цукровим діабетом типу 2, спричиняють до 80% всіх смертей. У клінічній медицині усвідомлюють необхідність підвищувати чутливість до інсуліну у пацієнтів з метаболічним синдромом і цим коригувати дисліпідемію, яку вважають причиною прискореного прогресування атеросклерозу. Однак, зараз це не є загальноприйнятим діагнозом з добре визначеними фармакотерапічними показаннями. Було виявлено, що S-енантіомер сполуки формули С: тобто 2-етокси-3-[4-(2-{4метансульфонілоксифеніл}етокси)феніл]пропанова кислота, [описана у Публікації РСТ WO 99/62872], є модулятором активованих пероксизомним проліфератором рецепторів [АППР, огляд яких можна знайти у T.M.Willson et al., J Med Chem 2000, Vol 43,527] і має комбіновану агоністичну активність стосовно АППР /АППР [Structure, 2001, Vol 9699, P.Cronet et al.]. Ця сполука є ефективною при лікуванні станів, пов'язаних з резистентністю до інсуліну. Несподівано була винайдена серія сполук, які є потужними модуляторами АППР. Винахід стосується S-енантіомеру сполуки формули І у якій п дорівнює 1 або 2, і її фармацевтично прийнятних солей, сольватів, кристалічних форм і проліків. Термін "проліки" у цьому документі охоплює похідні карбоксильної групи, які у ссавці, зокрема, 77460 8 у людині перетворюються у карбоксильну групу або її сіль або кон'югат. Хоча це не пов'язано з теорією, вважають, що більша частина активності, пов'язаної з проліками, зумовлюється активністю сполуки формули І, в яку перетворюються ці проліки. Проліки можна отримувати звичайними способами, добре відомими фахівцям. Відомими є різні карбокси-проліки, наприклад, див.: a) Design of prodrugs, ed. by Η. Bundgaard, (Elsevier, 1985) і Methods in Enzymology. 42:309396, ed. by K. Widder, et al. (Academic Press, 1985); b) Textbook of Drug Design and Development, ed. by Krogsgaard-Larsen and H. Bundgaard, Chapter 5 "Design and Application of Prodrugs", by H. Bundgaard, pp.113-191 (1991); c) Н. Bundgaard, Advanced Drug Delivery Reviews, 8:1-38 (1992); d) H. Bundgaard, et al., Journal of Pharmac. Sciences, 77:285 (1988); і e) N. Kakeya, et al., Chem Pharm Bull, 32:692 (1984). Зазначені документи включено посиланням. Розщеплюванні in vivo естери є лише одним типом проліків вихідної молекули. Гідролізованою in vivo (або розщеплюванню) естерною сполукою формули (І), яка містить карбоксигрупу, є, наприклад, фармацевтично прийнятний естер, який у людині або у тварині гідролізується з утворенням вихідної кислоти. Фармацевтично прийнятні естери для карбоксигрупи включають С1-6апкоксиметилов! естери, наприклад, метоксиметиловий; С1-6-алканоїлоксиметилові естери, наприклад, півалоїлоксиметиловий; фталідилові естери; С3-8-циклоалкоксикарбонілоксиС1-6-алкілові естери, наприклад, 1-циклогексилкарбонілоксіетиловий; 1,3-діоксолен-2-онілметилові естери, наприклад, 5-метил-1,3-діоксолен-2-онілметиловий; і С1-6алкоксикарбонілоксіетилові естери, наприклад, 1метоксикарбонілоксіетиловий; і можуть бути утворені на будь-якій карбоксигрупі у сполуках винаходу. Сполуки формули І мають активність як медикаменти. Зокрема, сполуки формули І є потужними агоністами АППР . Крім того, сполуки формули І є також агоністами ΑΠΠΡ . Термін "агоністи" тут охоплює часткові агоністи. Окремими сполуками винаходу є: (2S)-3-(4-{2-[бензил(гексил)аміно]-2оксоетокси}феніл)-2-етокси-пропанова кислота; і (2S)-2-етокси-3-(4-{2-[гексил(2фенілетил)аміно]-2-оксоетокси}феніл)пропанова кислота; і їх фармацевтично прийнятні солі, сольвати і кристалічні форми. У цьому документі вираз "фармацевтично прийнятні солі" стосується (але без обмеження) солей основ, наприклад, солей лужних металів, солей лужноземельних металів, солей амонію, солей, утворених з основними амінокислотами, і солей, утворених з органічними амінами. Зрозуміло, що певні сполуки винаходу можуть існувати у сольватованих, наприклад, гідратованих, а також у несольватованих формах. Зрозуміло також, що винахід охоплює всі такі сольватовані форми. Деякі сполуки винаходу можуть існувати 9 77460 10 як таутомери. Винахід також охоплює всі такі таусполуки винаходу в інший, а у деяких випадках томери. більш зручний спосіб, описані вище окремі етапи Способи отримання процесу отримання можуть бути виконані у іншому Сполуки винаходу можна отримувати, як це порядку і/або окремі реакції можуть бути проведені описано нижче. Винахід, однак, не обмежується на інших етапах процесу (тобто хімічні перетвоцими способами. Сполуки можна також отримуварення можуть бути проведені з інтермедіатами, ти, як це описано для відомих структурно близьких відмінними від зазначених вище для цієї реакції). сполук. Реакції можна проводити стандартними Вираз "інертний розчинник" стосується розчиспособами або так, як це описано у розділі, присну, який не реагує з вихідними матеріалами, реавяченому експериментам. гентами, інтермедіатами або продуктами, що може Сполуки формули І можна отримувати реакцішкідливо вплинути на вихід бажаного продукту. єю S-енантіомеру сполуки формули II Фармацевтичні препарати Сполуки винаходу вводять пацієнту перорально, парентерально, внутрішньовенно, внутрішньом'язово, підшкірно або іншим шляхом ін'єкції, букально, ректально, вагінально, трансдермально і/або через ніс, і/або інгаляцією, у формі фармацеу якій n визначено вище, a R є захисною грувтичної композиції, яка містить активний інгредієнт пою для карбоксильної гідроксигрупи, як це описау вигляді вільної кислоти або фармацевтично прино у стандартному документі "Protective Groups in йнятної органічної або неорганічної основноOrganic Synthesis (Захисні групи у органічному адитивної солі у фармацевтично прийнятній дозосинтезі)", 2nd Edition (1991) by Greene and Wuts, із ваній формі. Композиції можна вводити у змінних засобом позбавлення захисту. Захисна група може дозах залежно від розладу і пацієнта, що одержує бути також смолою, наприклад, смолою Ванга або лікування. 2-хлортритилхлоридною смолою. Захисні групи Придатні денні дози сполуки винаходу при теможуть бути видалені способами, добре відомими рапевтичному лікуванні людини становлять прибфахівцям. В одній з таких захисних груп R2 є С1-6лизно 0,0001-100мг/кг маси тіла, бажано 0,001алкоксигрупою або арилалкоксигрупою, напри10мг/кг маси тіла. клад, бензилоксигрупою, у якій COR2 представляє Бажаними пероральними формами є, зокрема, естер. Такі естери можуть бути введені у реакцію таблетки або капсули, які можуть бути виготовлені із засобом позбавлення захисту, наприклад, гідровідомими способами і містять дози активної сполулізувальним засобом, наприклад, гідроксидом ліки у межах від 0,5мг до 500мг, наприклад, 1мг, 3мг, тію у суміші ТГФ і води, при температурі 0-100°С, з 5мг, 10мг, 25мг, 50мг, 100мг і 250мг. одержанням сполуки формули І. Подальшим об'єктом винаходу є фармацевтиСполуки формули II можна отримувати реакцічні композиції, що включають будь-які сполуки єю S-енантіомеру сполуки формули III винаходу або їх фармацевтично прийнятні похідні, у суміші з фармацевтично прийнятними ад'ювантами, розріджувачами і/або носіями. Фармацевтичні властивості Сполуки формули (І) можуть бути використані III для профілактики і/або лікування клінічних станів, 2 де R визначено вище, з сполукою формули пов'язаних з природною або набутою зниженою IV. чутливістю до інсуліну (резистентність до інсуліну) і асоційованими метаболічними розладами (відомими також як метаболічний синдром). Ці клінічні стани включають (але без обмеження) загальне ожиріння, абдомінальне ожиріння, артеріальну 1 де R визначено вище, у інертному розчині, гіпертензію, гіперінсулінемію, гіперглікемію, діабет наприклад, ДХМ, у присутності засобу сполучення, типу 2 і дисліпідемію, яка звичайно супроводжує наприклад, карбодііміду, наприклад, 1-(3резистентність до інсуліну. Ця дисліпідемія, відома диметиламінопропіл)-3-етилкарбодііміду, і, як ватакож як атер-генний ліпопротеїновий профіль, ріант, у присутності каталізатору, наприклад, осхарактеризується помірним підвищенням рівня новного каталізатору, наприклад, 4неестерифі-кованих жирних кислот, багатих на диметиламінопіридину, при температурі від -25°С тригліцерид часток ліпопротеїну дуже низької гусс до 150 С. тини (ЛДНГ), високими рівнями Аро В, низькими Сполуки формул III і IV можна отримувати рівнями ліпопротеїну високої густини, пов'язаними способами, описаними у Прикладах або подібними з низькими рівнями частинок ароАІ, і високими способами, відомими фахівцям. рівнями Аро В у присутності невеликих компактних Сполуки формул II і III можуть бути корисними частинок ліпопротеїнів низької густини, фенояк інтермедіати при отриманні сполуки формули І, типу В. вважаються новими і розглядаються як ще один Сполуки винаходу, як вважають, можуть викоаспект винаходу. Бажаними є S-енантіомери спористовуватись для лікування пацієнтів з комбінолуки формул II і III. Сполуки винаходу можуть бути ваними або змішаними гіперліпідеміями або різвиділені з реакційних сумішей звичайними спосоними рівнями гіпертригліцеридемії і післяобідньої бами. дисліпідемії, і з іншими проявами метаболічного Для фахівця зрозуміло, що для одержання синдрому або без них. 11 77460 12 Можна сподіватись, що застосування сполук ньої глюкози і інгібітори альфа-глюкозидази). Привинаходу знизить серцево-судинну захворюваність кладами інгібітору альфа-глюкозидази є акарбоза і смертність, пов'язані з атеросклерозом, завдяки або воглібоза, або мігитол. Прикладом регуляторів їх антидисліпідемічним і протизапальним властиобідньої глюкози є репаглінід або натеглінід. востям. Серцево-судинні хворобливі стани вклюЗгідно з іншим аспектом винаходу, сполуку чають макроангіопатії різних внутрішніх органів, які формули І, або її фармацевтично прийнятну сіль, є причиною інфаркту міокарду, застійної серцевої сольват, сольват такої солі або проліки можна недостатності, цереброваскулярної хвороби і певводити разом з іншим модулятором АППР, вклюриферійної артеріальної недостатності кінцівок. чаючи (без обмеження) агоністи АППР і/або Вважається також, що завдяки підвищенню чутлиΑΠΠΡ , або з їх фармацевтично прийнятними совості до інсуліну сполуками формули І ці сполуки лями, сольватами, сольватами таких солей або їх відвернуть або затримають розвиток діабету типу проліками. Фахівцям добре відомі придатні агоніс2 з метаболічного синдрому і діабету вагітності. ти АППР і/або ΑΠΠΡ , їх фармацевтично прийняОтже, можна сподіватись на затримання розвитку тні солі, сольвати, сольвати таких солей або продовготривалих ускладнень, пов'язаних з хронічною ліки. Прикладами є сполуки, [описані у WO гіперглікемією при цукровому діабеті, наприклад, 01/12187, WO 01/12612, WO 99/62870, WO мікроангіопатій, які викликають ниркові захворю99/62872, WO 99/62871, WO 98/57941, WO вання, пошкодження сітківки і захворювання пе01/40170, J Med Chem, 1996,39, 665, Expert риферійних судин нижніх кінцівок. Крім того, ці Opinion on Therapeutic Patents, 10 (5), 623-634 (зосполуки можуть бути корисними при лікуванні різкрема заявки на cтop.634) і J Med Chem, 2000, 43, них станів, не пов'язаних з серцево-судинною сис527], включені посиланням. Зокрема, агоністами темою або з резистентністю до інсуліну, як-то поАППР і/або ΑΠΠΡ є MN622/Ragaglitazar, BMS лікистозний яєчниковий синдром, ожиріння, рак і 298585, WY-14643, клофібрат, фенофібрат, безазапальні хвороби, включаючи нейродегенеративні фібрат, гемфіброзилі і ципрофібрат; GW 9578, розлади, наприклад, помірне порушення розпізнациглітазон, троглітазон, піоглітазон, розиглітазон, вальної здатності, хворобу Альцгеймера, хворобу еглітазон, проглітазон, BRL-49634, KRP-297, JTTПаркінсона і множинний склероз. 501, SB 213068, GW 1929, GW 7845, GW 0207, LМожна сподіватись, що сполуки винаходу мо796449, L-165041 і GW 2433. Зокрема, агоністами жуть бути корисними для контролю рівнів глюкози АППР і/або ΑΠΠΡ є (S)-2-етокси-3-[4-(2-{4у пацієнтів, що страждають від діабету типу 2. метансульфонілоксифеніл}етокси)-феніл]Винахід охоплює спосіб лікування і профілакпропанова кислота і її фармацевтично прийнятні тики дисліпідемій, синдрому резистентності до солі. інсуліну і/або метаболічних розладів (згаданих Згідно з винаходом, комбіноване лікування вище), який полягає в уведенні сполуки формули І можна проводити у сполученні з сульфонілссавцю (зокрема, людині), що потребує цього. мочевиною, наприклад, глімепіридом, глібенкламіВинахід охоплює спосіб лікування або профідом (глібуридом), гліклазидом, гліпізидом, гліхідолактики діабету типу 2, який полягає в уведенні ном, хлорпропамідом, толбутамідом, асетогексаефективної кількості сполуки формули І ссавцю мідом, глікопірамідом, карбутамідом, (зокрема, людині), що потребує цього. глібониридом, глізоксеридом, глібутіазолом, глібуЗгідно з іншим аспектом, винахід охоплює золом, глігексамідом, глімідином, гліпінамідом, сполуки формули І як медикамент. фенбутамідом, толциламідом і толазамідом. БаЗгідно з подальшим аспектом, винахід охопжаною сульфонілмочевиною є глімепірид або глілює використання сполуки формули І у виготовбенкламід (глібурид). Найкражою сульфонілмочеленні медикаменту для лікування резистентності виною є глімепірид. Отже, винахід охоплює до інсуліну і/або метаболічних розладів. застосування сполуки винаходу разом з однією, Комбінована терапія двома або більше терапій, зазначених вище. ДоСполуки винаходу можна комбінувати з іншизування для інших існуючих терапій для лікування ми терапевтичними засобами, корисними для лідіабету типу 2 і пов'язаних з ним ускладненнями є кування розладів пов'язаних виникненням і перебівідомим фахівцям і схвалюється регулюючими гом атеросклерозу, наприклад, гіпертензії, органами, наприклад, FDA і можуть бути знайдені гіперліпідемії, дисліпідемії, діабету і ожиріння. у Orange Book від FDA. Перевагою комбінованого Сполуки винаходу можна комбінувати з іншими лікування є можливість застосовувати менші дози. терапевтичними засобами, які знижують відноВинахід охоплює також сполуку винаходу у комбішення ЧНГ/ЧВГ або з засобами, що викликають нації з знищуючими холестерол засобами, які зниження рівнів циркуляції ЧНГ-холестеролу. Для включають (без обмеження) інгібітори HMG-CoAпацієнтів з цукровим діабетом сполуки винаходу редуктази (редуктази співферменту 3-гідрокси-3можна також комбінувати з терапевтичними засометилглютарилу). Прикладом інгібітору HMG-CoAбами, призначеними для лікування ускладнень, редуктази є статин, вибраний з групи, яку складапов'язаних з мікроангіопатіями. ють аторвастатин, бервастатин, церивастатин, Сполуки винаходу можна використовувати радальвастатин, флувастатин, ітавастатин, ловастазом з іншими терапіями для лікування метаболічтин, мевастатин, нікостатин, нівастатин, провастаного синдрому або діабету типу 2 і пов'язаних з тин і симвастатин, або їх фармацевтично прийнятним ускладнень, включаючи бігуанідні ліки, наприні солі, зокрема, солі натрію і кальцію, або їх клад, метморфін, фенморфін і буформін, інсулін сольвати, або сольвати таких солей. Зокрема, ста(синтетичні аналоги інсуліну, амілін) і оральні антином є аторвастатин або його фармацевтично тигіперглікеміки (їх розділяють на регулятори обідприйнятна сіль, сольват, сольват такої солі або 13 77460 14 відповідні проліки. Бажаним статином є аторваста8-(N-{(R)-1'-феніл-1'-[N'-(2тинова сіль кальцію, найкращим же статином є сульфоетил)карбамоїл]метил}карбамоїлметокси)сполука (Е)-7-[4-(4-флуорфеніл)-6-ізопропіл-22,3,4,5-тетрагідро-1,5-бензотіазепін; [метил(метилсульфоніл)-аміно]-піримщин-51,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8іл](3R,5S)-3,5-дигідроксигепт-6-енойна кислота, (N-{(R)- -[N'-(2-сульфоетил)карбамоїл]-4[відома також як (Е)-7-[4-(4-флуорфеніл)-6гідроксибензил}карбамоїлметокси)-2,3,4,5ізопропіл-2-[N-метил-N-(метилсульфоніл)-аміно]тетрагідро-1,5-бензотіазепін; піримідин-5-іл](3R,5S)-3,5-дигідроксигепт-6-енойна 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіокислота] або її фармацевтично прийнятна сіль або 8-(N-{(R)- -[N'-(2-сульфоетил)карбамоїл]-4сольват, або сольват такої солі. (Е)-7-[4-(4гідроксибензил}карбамоїлметокси)-2,3,4,5флуорфеніл)-6-ізопропіл-2-[метилтетрагідро-1,5-бензотіазепін; (метилсульфоніл)-аміно]-піримідин-5-іл](3R,5S)1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо3,5-дигідроксигепт-6-енойну кислоту, і її кальцієву і 8-(N-{(R)- -[N'-(2-карбоксіетил)-карбамоїл]натрієву солі [описано у Європейській заявці ЕР-Абензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,50521471, і у Bioorganic and Medicinal Chemistry, бензотіазепін; (1997), 5(2), 437-444]. Останній статин відомий 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8також як розувастатин. (N-{(R)-а-[N'-(2-карбоксіетил)карбамоїл]-4У цій заявці термін "засіб, що знижує рівень гідроксибензил}карбамоїлметокси)-2,3,4,5холестерину" охоплює також хімічні модифікації тетрагідро-1,5-бензотіазепін; інгібіторів HMG-CoA-редуктази, наприклад, естери, 1,1-д1оксо-3-бутил-3-етил-5-феніл-7-метилтіопроліки і метаболіти, активні або неактивні. 8-(N-{(R)- -[N'-(5-карбоксипентил)Винахід також охоплює сполуку винаходу у карбамоїл]бензил}карбамоїлметокси)-2,3,4,5комбінації з інгібітором транспортної системи жовтетрагідро-1,5-бензотіазепін; чної кислоти клубової кишки (інгібітор ТЖККК). 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8Сполуки-інгібітори ІВАТ були описані; [див., (N-{(R)- -[N'-(2-карбоксіетил)наприклад, WO 93/16055, WO 94/18183, WO карбамоїл]бензил}карбамоїлметокси)-2,3,4,594/18184, WO 96/05188, WO 96/08484, WO тетрагідро-1,5-бензотіазепін; 96/16051, WO 97/33882, WO 98/07449, WO 1,1-діоксо-3-дибутил-5-феніл-7-метилтіо-8-(N98/03818, WO 98/38182, WO 99/32478, WO { -[N-(2-сульфоетил)карбамоїл]-299/35135, WO 98/40375, WO 99/35153, WO флуорбензил}карбамоїлметокси)-2,3,4,599/64409, WO 99/64410, WO 00/01687, WO тетрагідро-1,5-бензотіазепін; 00/47568, WO 00/61568, WO 00/62810, WO 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо01/68906, DE 19825804, WO 00/38725, WO 8-(N-{(R)- -[N'-(R)-(2-гідрокси-100/38726, WO 00/38727, WO 00/38728, WO карбоксіе00/38729, WO 01/68906, WO 01/66533, WO тил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,502/32428, WO 02/50051, ЕР 864 582, ЕР 489423, тетрагідро-1,5-бензотіазепін; ЕР 549967, ЕР 573848, ЕР 624593, ЕР 624594, ЕР 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8624595 і ЕР 624596]. Зміст цих заявок включено (N-{(R)- -[N'-(R)-(2-гідрокси-1посиланням. карбоксіетил)карбамот]бензил}карбамоїлметокси)Зокрема, класами інгібіторів ТЖККК, придат2,3,4,5-тетрагідро-1,5-бензотіазепін; ними для використання згідно з винаходом є бен1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8зотієпіни і сполуки, описані у Формулі винаходу, {N-[(R)- -(N'-{(R)-1-[N"-(R)-(2-гідрокси-1зокрема, у п.1 Формули [WO 00/01687, WO карбоксіетил)карбамот]-296/08484 і WO 97/33882], включених посиланням. гідроксіетил}карбамоїл)бензил]Іншими придатними класами інгібіторів ТЖККК є карбамоїлметокси}-2,3,4,5-тетрагідро-1,51,2-бензотіазепіни, 1,4-бензотіазепіни і 1,5бензотіазепін; бензотіазепіни. Придатними класами інгібіторів 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіоТЖККК є також 1,2,5-бензотіадіазепіни. 8-(N-{ -[N'-(карбоксиметил)-карбамоїл]Конкретними сполуками-інгібіторами ТЖККК є: бензил}карбамоїлметокси)-2,3,4,5-тетрагідро-1,5(3R,5R)-3-бутил-3-eтил-1,1-діоксид-5-фенілбензотіазепін; 2,3,4,5-тетрагідро-1,4-бензотіазепін-8-іл β-D1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіоглюкопіранозидуронова кислота (ЕР 864 582). 8-(N-{ -[N'-((етокси)-(метил)Іншими інгібіторами ТЖККК є: фосфорилме1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-Nтил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5{(R)-1'-феніл-[N'-(карбоксиметил)тетрагідро-1,5-бензотіазепін; карбамоіл]метил}карбамоїлметокси)-2,3,4,51,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіотетрагідро-1,5-бензотіазепін; 8-{N-[(R)- -(N'-{2-[(гідрокси)(метил)1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8фосфо(N-{(R)- -[N'-(карбоксиметил)карбамоїл]-4рил]етил}карбамоїл)бензил]карбамоїлметокси}гідроксибензил}карбамоїлметокси)-2,3,4,52,3,4,5-тетрагідро-1,5-бензотіазепін; тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-81,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)- -(N'-(2-метилтіо-1(N-{(R)-1'-феніл-1'-[N'-(2карбоксіесульфоетил)карбамоїл]метил}карбамоїлметокси)тил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,52,3,4,5-тетрагідро-1,5-бензотіазепін; тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо 15 77460 16 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)- -[N-{(R)-1-[N-((R)-2-гідрокси-1{N-[(R)- -(N'-{2-[(метил)-(етил)фосфорил]карбоксіеетил}карбамоїл)-4тил)карбамоїл]пропіл}карбамоїл]бензил)карбамоїл гідроксибензил]карбамоїлметокси}-2,3,4,5метокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін; тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-81,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)- -[N-((R)-1-карбокси-2{N-[(R)-L-(N'-{2-[(метил)(гідрокси)метилпрофосфорил]етил}карбамоїл)-4-гідроксибензил]піл)карбамоїп]бензил}карбамоїлметокси)-2,3,4,5карбамоїлметокси}-2,3,4,5-тетрагідро-1,5тетрагідро-1,2,5-бензотіадіазепін; бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-81,1-(діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)- -[N-((R)-1-карбоксипропіл)карбамоїл]-4(N-{(R)- -[(R)-N'-(2-метилсульфініл-1гідроксибензил}карбамоїлметокси)-2,3,4,5карбоксіететрагідро-1,2,5-бензотіадіазепін; тил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,51,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8тетрагідро-1,5-бензотіазепін; [N-((R)- -{N-[1-(R)-2-(S)-1-гідрокси-1-(3,41,1-діоксо-3,3-дибутил-5-феніл-7-метокси-8-[Nдигідроксифеніл)проп-2-іл]карбамоїл}-4{(R)- -[N'-(2-сульфоетил)карбамоїл]-4гідроксибензил)-карбамоїлметокси]-2>3,4,5гідроксибензил}карбамоїлметокси]-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-81,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8[N-{(R)- -[N-(2-(R)-3-(R)-4-(R)-5-(R)-2,3,4,5,6(N-{(R)- -[N-((R)-1-карбокси-2-метилтіопентагідроксигексил)карбамоїл]-4етил)карбамоїл]-4гідроксибензил}карбамоїл-метокси)-2,3,4,5гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; і тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-81,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N{(R)- -[N-(2-(R)-3-(R)-4-(R)-5-(R)-2,3,4,5,6(N-{(R)- -[N-((R)-1-карбокси-2-(R)пентагідроксигексил)карбамоїл]бензил}карбамоїлгідроксипропіл)карбамоїл]-4-гідроксибензил}метокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін; карбамоїлметокси)-2,3,4,5-тетрагідро-1,2,5або їх фармацевтично прийнятні сіль, сольват, бензотіадіазепін; сольват такої солі або проліки. 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8-NЗгідно з ще одним аспектом, в рамки винаходу {(R)- -[N-((R)-1-карбокси-2входить комбіноване лікування, яке полягає в увеметилпропіл)карбамоїл]-4денні ефективної кількості сполуки формули І або гідроксибензил}карбамоїлметокси)-2,3,4,5її фармацевтично прийнятної солі, сольвату, сольтетрагідро-1,2,5-бензотіадіазепін; вату такої солі або проліків, як варіант, разом з 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8фармацевтично прийнятним розріджувачем або носієм, з одночасним, послідовним або окремим (N-{(R)- -[N-((R)-1-карбоксибутил)карбамоїл]-4введенням одного або більше засобів, вибраних з гідроксибензил}карбамоілметокси)-2,3,4,5групи, яку складають: тетрагідро-1,2,5-бензотіадіазепін; інгібітор БПХЕ (білок переносу холестериново1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8го естеру), наприклад, згаданий і [описаний у до(N-{(R)- -[N-((R)-1-карбоксипропіл)карбамоїл]кументі WO 00/38725 стор.7 ряд.22 - cтop.10, бензил}карбамоїлметокси)-2,3,4,5-тетрагідроряд.17], включеному посиланням; 1,2,5-бензотіадіазепін; антагоніст абсорбції холестеролу, наприклад, 1,1-діоксо-3,3-дибутил-5-фент-7-метилтіо-8-(Nацетидинони, наприклад, SCH 58235 і [описані у {(R)- -[N-((R)-1-карбоксіетил)карбамоїл]документі US 5 767 115], включеному посиланням; бензил}карбамоїпметокси)-2,3,4,5-тетрагідро-1,2,5інгібітор БМП (білок мікросомного переносу), бензотіадіазепін; наприклад, [описаний у Science, 282, 751-54,1998], 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8включеній посиланням; (N-{(R)- -[N-((R)-1-карбокси-2-(R)похідне нікотинової кислоти, включаючи прогідроксипродукти з уповільненим вивільненням і комбіновані піл)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5продукти, наприклад, нікотинова кислота (ніацин), тетрагідро-1,2,5-бензотіадіазепін; ацимпокс і ніцеритрол; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8фітостерольна сполука, наприклад, етаноли; (N-{(R)- -[N-(2-сульфоетил)карбамоїл]-4пробукол; гідроксибензил}карбамоїлметокси)-213,4,5сполука проти ожиріння, наприклад, орлістат тетрагідро-1,2,5-бензотіадіазепін; [ЕР 129748] і сибутрамін [GB 2 184 122 і US 4 929 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8629]; (N-{(R)- -[N-((R)-1-карбоксіетил)карбамоїл]-4антигіпертензивна сполука, наприклад, інгібігідроксибензил}карбамоїлметокси)-2,3,4,5тор ферменту перетворення ангіотензину(КЕА), тетрагідро-1,2,5-бензотіадіазепін; антагоніст рецептору ангіотензину, андренергічний 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8блокатор, альфа-андренергічний блокатор, бета(N-{(R)- -[N-((R)-1-карбокси-2андренергічний блокатор, змішаний альфа/бета метилтіоеандренергічний блокатор, андренергічний стимутил)карбамот]бензил}карбамоїлметокси)-2,3,4,5лятор, блокатор каналу кальцію, блокатор АТ-1, тетрагідро-1,2,5-бензотіадіазепін; салуретик, діуретик або судинорозширювальний 1,1-діоксо-3,3-(дибутил-5-феніл-7-метилтіо-8засіб; 17 77460 18 антагоніст або інверсний антагоніст СВ1, наклад, людини, що потребують такого лікування, приклад, [описаний у WO01/70700 і ЕР 65635]; який полягає в уведенні зазначеній тварині ефекантагоніст гормону концентрування меланіну тивної кількості сполуки формули І або її фарма(ГКМ); цевтично прийнятної солі, сольвату, сольвату таінгібітор PDK; або кої солі або проліків з одночасним, послідовним модулятори ядерних рецепторів, наприклад, або роздільним застосуванням з ефективною кільLXR, FXR, RXR, і ROR-альфа; або їх фармацевтикістю іншої сполуки, описаної у цьому розділі, або чно прийнятні солі, сольвати, сольвати таких соїї фармацевтично прийнятної солі, сольвату, сольлей або проліки, як варіант, разом з фармацевтивату такої солі або проліків. чно прийнятним розріджувачем або носієм, Іншим аспектом винаходу є фармацеватична теплокровній тварині, наприклад, людині, що поткомпозиція, яка містить сполуку формули І або її ребує такого терапевтичного лікування. фармацевтично прийнятну сіль, сольват, сольват Інгібітори ΚΕΑ або їх фармацевтично прийняттакої солі або проліки, і одну з інших сполук, опині солі, сольвати, сольвати таких солей або пролісаних у цьому розділі, або її фармацевтично прики, включаючи активні метаболіти, які можна викойнятної солі, сольвату, сольвату такої солі або ристовувати у комбінації з сполуками формули І, проліків разом з фармацевтично прийнятним розвключають (без обмеження) такі сполуки: алацепріджувачем або носієм. рил, алатриоприл, алтіоприл кальцію, анковенін, Згідно з ще одним аспектом, в рамки винаходу беназеприл, беназеприлгідрохлорид, беназепривходить комплект, який містить сполуку формули І лат, бензоїлкаптоприл, каптоприл, еаптоприлабо фармацевтично прийнятну сіль, сольват, социстеїн, капртприл-глютатіон, церанаприл, церальват такої солі або проліки, і одну з інших сполук, ноприл, цернаприл, цилізаприл, цилазаприлат, описаних у цьому розділі, або її фармацевтично делаприл, делаприл-дикислота, еналаприл, енаприйнятної солі, сольвату, сольвату такої солі або лаприлат, енаприл, епікаптоприл, фороксимітин, проліків. фостеноприл, фосеноприл, фосеноприл натрію, Згідно з подальшим аспектом, в рамки винафосиноприл, фосиноприл натрію, фосиноприлат, ходу входить комплект, який містить: фосиноприлова кислота, глікоприл, геморфін-4, a) сполуку формули І або фармацевтично ідраприл, імідаприл, індолаприл, індолаприлат, прийнятну сіль, сольват, сольват такої солі або лібензаприл, лізиноприл, ліціумін А, ліціумін В, проліки, у першій одиничній дозованій формі; міксанприл, моекзиприл, моекзиприлат, мовелтипb) одну з інших сполук, описаних у цьому розрил, мурацеїн А, мурацеїн В, мурацеїн С, пентопділі, або її проліки у другій одиничній дозованій рил, периндоприл, периндоприлат, півалоприл, формі; і півоприл, хінаприл, хінаприлгідрохлорид, хінаприc) контейнерний засіб для зберігання зазначелат, раміприл, раміприлат, спіраприл, спіраприлгіних першої і другої одиничних дозованих форм. дрохлорид, спіраприлат, спіроприл, спіроприлгідЗгідно з іншим аспектом, в рамки винаходу рохлорид, темокаприл, темокаприлгідрохлорид, входить комплект, який містить: тепротид, трандолаприл, трандолаприлат, утабаa) сполуку формули І або її фармацевтично прил, забіциприл, забіциприлат, зофеноприлі і прийнятну сіль, сольват, сольват такої солі або зофеноприлат. Бажаними інгібіторами ΚΕΑ згідно проліки, разом з фармацевтично прийнятним розз винаходом є раміприл, раміприлат, лізиноприл, ріджувачем або носієм, у першій одиничній дозоеналаприл і еналаприлат. Найкращими інгібітораваній формі; ми ΚΕΑ є раміприл і раміприлат. b) одну з інших сполук, описаних у цьому розБажані антагоністи ангіотензину II, їх фармаділі, або її проліки у другій одиничній дозованій цевтично прийнятні солі, сольвати, сольват таких формі; і солей або проліки, придатні для комбінування з c) контейнерний засіб для зберігання зазначесполуками формули І, включають (але без обмених першої і другої одиничних дозованих форм. ження) такі сполуки: кандезартан, кандезартанціВинахід охоплює також використання сполуки лексетил, лосартан, вальзартан, ірбезартан, тазоформули І або її фармацевтично прийнятної солі, зартан, тельмізартан і епрозартан. Більш сольватів, сольватів такої солі або проліків, і однієї бажаними антагоністами ангіотензину І або їх фаз інших сполук, описаних у цьому розділі, або її рмацевтично прийнятними похідними, згідно з вифармацевтично прийнятної солі, сольвату, сольнаходом, є кандезартан і кандезартанцілексетил. вату такої солі або проліків, у виготовленні медиОтже, винахід охоплює також спосіб лікування каменту, призначеного для лікування метаболічнодіабету типу 2 і пов'язаних з ним ускладнень у тего синдрому або діабету типу 2 і пов'язаних з ним плокровної тварини, наприклад, людини, що потускладнень у теплокровної тварини, наприклад, ребують такого лікування, який полягає в уведенні людини. зазначеній тварині ефективної кількості сполуки Згідно з іншим аспектом, винахід охоплює виформули І або її фармацевтично прийнятної солі, користання сполуки формули І або її фармацевтисольвату, сольвату такої солі або проліків з одночно прийнятної солі, сольватів, сольватів такої солі часним, послідовним або роздільним застосуванабо проліків, і однієї з інших сполук, описаних у ням з ефективною кількістю одної іншої сполуки, цьому розділі, або її фармацевтично прийнятної описаної у цьому розділі, або її фармацевтично солі, сольвату, сольвату такої солі або проліків, у прийнятної солі, сольвату, сольвату такої солі або виготовленні медикаменту, призначеного для лікупроліків. вання гіперліпідемічних станів у теплокровної тваВинахід охоплює також спосіб лікування гіперрини, наприклад, людини. ліпідемічних станів у теплокровної тварини, наприЗгідно з ще одним аспектом, винахід охоплює 19 77460 20 комбіноване лікування, яке полягає в уведенні оксопропіл]фенокси}оцтова кислота ефективної кількості сполуки формули І або її фаДо розчину етил (2S)-3-{4-[2-(бензилокси)-2рмацевтично прийнятної солі, сольвату, сольвату оксоетокси]феніл}-2-етоксипропаноату (22,33г, такої солі або проліків, як варіант, разом з фарма57,8ммоль) у щойно дистильованому ТГФ (290мл) цевтично прийнятним розріджувачем або носієм, з додають Pd/C (10%, 3,1г) і реакційну суміш гідроодночасним, послідовним або роздільним застосугенують під атмосферним тиском при кімнатній ванням ефективної кількості іншої сполуки, описатемпературі протягом ночі. Суміш фільтрують ченої у цьому розділі, або її фармацевтично прийнярез броунмілерит і фільтрат концентрують у вакутної солі, сольвату, сольвату такої солі або умі, одержуючи 16,6г (97%) світло-жовтого масла. 1 проліків, як варіант, разом з фармацевтично приН ЯМР (400МГц, CDCI3): δ 1,15 (t, 3Н), 1,21 (t, йнятним розріджувачем або носієм, теплокровній 3Н), 2,93-2,98 (m, 2H), 3,35 (m, 1H), 3,60 (m, 1H), тварині, наприклад, людині, що потребує такого 3,97 (m, 1H), 4,16 (q, 2H), 4,65 (s, 2H), 6,84 (d, 2H), лікування. 7,17 (d, 2H), 8,48 (bs, 1H) 13 Приклади C ЯМР (100МГц, CDCI3): δ 14,3, 15,1, 38,5, 1 13 Вимірювання Н ЯМР і С ЯМР виконано на 61,0, 65,1, 66,4, 80,3, 114,6, 130,7, 130,9, 156,4, спектрометрах Varian Mercury 300 або Varian 172,7, 173,7 UNITY plus 400, 500 або 600, на частотах 1Н 300, (ііі) Етил (2S)-3-(4-{2-[бензил(гексил)аміно]-2400, 500 і 600МГц, відповідно, і на частотах 13С оксоетокси}феніл)-2-етоксипропаноат 75,100,125 і 150МГц, відповідно. Вимірювання буДо розчину {4-[(2S)-2,3-діетокси-3ли проведені на дельта-шкалі (δ). оксопропіл]фенокси}оцтової кислоти (0,110г, Якщо не визначено інше, хімічні зсуви наведе0,37моль) у метиленхлориді (3,7мл) додають Nно умлн~1 відносно розчиннику як внутрішнього гексилбензиламін (0,079г, 0,41ммоль) і ДМАП стандарту. (0,045г, 0,37ммоль) і потім гідрохлорид 1-етил-3Абревіатури (3-диметил-амінопропіл)карбодііміду (0,071г, ДМСО - диметилсульфоксид 0,37ммоль) і реакційну суміш перемішують при ТГФ - тетрагідрофуран кімнатній температурі протягом ночі. Суміш розбаPd/C - паладій на вугіллі вляють метиленхлоридом (25мл), і органічну фазу ДМАП - диметиламінопіридин промивають 5%-ю НСІ (3 25мл), водним натрій t триплет гідрокарбонатом (25мл) і розсолом (25мл), сушать s синглет натрій сульфатом і концентрують у вакуумі. Очиd дублет щення на пакетній колонці силікагелю (Ізolute® q квартет SPE Column, 5г Si/25мл) з метанолом (0-1% градіm мультиплет єнт) у метиленхлориді як елюентом дає 0,139г bs широкий синглет (80%) безбарвного масла. 1 dm дублет мультиплету Н ЯМР (400МГц, CDCI3): δ 0,81-0,90 (m, 3Н), bt широкий триплет 1,11-1,32 (m, 12Н), 1,46-1,62 (m, 2H), 2,88-3,00 (m, dd дублет дублету 2H), 3,21-3,29 і 3,29-3,40 (2m, 3Н, ротамери), 3,59 Приклад 1 (m, 1H), 3,95 (m, 1H), 4,10419 (m, 2Н), 4,60 і 4,61 (2S)-3-(4-{2-[бензил(гексил)аміно1-2(2s, 2Н, ротамери), 4,65 і 4,73 (2s, 2H, фікс), 6,77 і оксоетокси}феніл)-2-етоксипропанова кислота 6,87 (2d, 2H, ротамери), 7,07-7,37 (m, 7H). 13 (і) Етил (2S)-3-{4-[2-(бензилокси)-2С ЯМР (100МГц, CDCI3): δ 13,9, 14,2, 15,1, оксоетокси]феніл}-2-етоксипропаноат 22,5, 26,5, 27,1, 28,4, 31,4, 31,5, 38,4, 46,3, 46,5, До розчину етил (2S)-2-етокси-3-(448,2, 50,5, 60,7, 66,1, 67,5, 67,8, 80,3, 114,4, 114,5, гідроксифеніл)пропаноату (23,8г, 100ммоль, отри126,6, 127,3, 127,6, 128,0, 128,5, 128,8, 130,2, маного [згідно з WO 99/62872]) у ацетонітрилі 130,2, 130,4, 130,5, 136,6, 137,2, 156,8, 156,9, (200мл) додають безводний карбонат калію (31,9г, 168,0, 168,1, 172,4. (Кількість піків перевищує кіль231ммоль) і потім бензилбромацетат (17,4мл, кість атомів карбону внаслідок ротамерів) 110ммоль) і реакційну суміш витримують під зво(іv) (2S)-3-(4-{2-[бензил(гексил)аміно]-2ротним холодильником протягом ночі. Реакційну оксоетокси}феніл)-2-етоксипропанова кислота суміш залишають охолонути до кімнатної темпеДо розчину етил (2S)-3-(4-{2ратури, нерозчинні солі відфільтровують і розчин [бензил(гексил)аміно]-2-оксоетокси}феніл)-2концентрують у вакуумі. Залишок вносять у етилаетокси-пропаноату (0,080г, 0,17ммоль) у ТГФ цетат (300мл), і органічну фазу промивають вод(8,6мл) додають 4,3мл 0,10М розчину LiOH і реакним натрій гідрокарбонатом (3 100мл) і розсолом ційну суміш перемішують при кімнатній темпера(100мл), сушать безводним магній сульфатом і турі протягом ночі. Реакційну суміш підкислюють концентрують у вакуумі. Очищення на силікагелі 2М НСІ і екстрагують етилацетатом (3 25мл). метиленхлоридом як елюентом і збирання чистих Об'єднану органічну фазу промивають розсолом фракцій дають 22,4г (58%) жовтого масла. (25мл), сушать натрій сульфатом, і концентрують у 1 Н ЯМР (400МГц, CDCI3): δ 1,16 (t, 3Н), 1,22 (t, вакуумі, одержуючи 0,068г (90%) безбарвного ма3Н), 2,93-2,97 (m, 2H), 3,35 (m, 1H), 3,60 (m, 1H), сла. 1 3,97 (m, 1H), 4,16 (q, 2H), 4,64 (s, 2H), 5,23 (s, 2H), Н ЯМР (400МГц, CDCI3): δ 0,80-0,92 (m, 3Н), 6,82 (d, 2H), 7,15 (d, 2H), 7,32-7,39 (m, 5H). 1,11-1,18 (m, 3Н), 1,18-1,33 (m, 6H), 1,46-1,63 (m, 13 C ЯМР (100МГц, CDCI3): δ 14,3, 15,2, 38,6, 2H), 2,87-3,11 (m, 2H), 3,20-3,30 і 3,32-3,45 (2m, 3Н, 60,9, 65,6, 66,3, 67,0, 80,4, 114,6, 128,5, 128,6, ротамери), 3,61 (m, 1Н), 4,01 (гл, 1Н), 4,61 і 4,63 128,7, 130,6, 135,3, 156,7, 169,0, 172,6. (2s, 2Н, ротамери), 4,67 і 4,75 (2s, 2H, ротамери), (іі) {4-[(2S)-2,3-діетокси-36,77 і 6,88 (2d, 2H, ротамери), 7,10-7,40 (m, 7H), 21 77460 22 13 8,79 (bs, 1H). С ЯМР (100МГц, CDC3): δ 14,0, 14,1, 15,1, 13 С ЯМР (100МГц, CDC13): δ 14,0, 15,1, 22,6, 22,6, 22,6, 26,6, 26,7, 27,3, 28,9, 31,5, 31,6, 33,8, 26,6, 27,1, 28,4, 31,5, 31,5, 31,6, 38,1, 46,5, 46,6, 35,2, 38,1, 46,1, 48,3, 48,4, 49,0, 66,7, 67,4, 79,9, 48,5, 50,7, 66,7, 67,4, 67,7, 79,9, 114,6, 114,7, 126,7, 114,6, 126,4, 127,0, 128,6, 128,9, 130,0, 130,1, 127,5, 127,8, 128,2, 128,7, 129,0, 130,1, 130,1, 130,6, 130,7, 138,2, 139,1, 156,9, 157,0, 168,1, 130,6, 130,7, 136,5, 137,0, 156,9, 157,0, 168,5, 168,2, 175,6 (Кількість піків перевищує кількість 168,6, 175,6. (Кількість піків перевищує кількість атомів карбону внаслідок ротамерів). атомів карбону внаслідок ротамерів) Біологічна активність Приклад 2 Композиції (2S)-2-етокси-3-(4-{2-{гексил(2Сполуки були розчинені у ДМСО для одерфенілетил)аміно]-2-оксоетокси}-феніл)-пропанова жання 16мМ маточних розчинів. Перед аналізом кислота маточні розчини розбавляли ДМСО і середовища(і) Етил (2S)-2-етокси-3-(4-{2-[гексил(2ми культури. фенілетиламіно]-2-оксоетокси}феніл)пропаноат Загальні хімікати і реагенти До розчину {4-[(2S)-2,3-діетокси-3Реагент для люциферазного аналізу був приоксопропіл]фенокси}оцтової кислоти (0,110г, дбаний від Packard, USA. Рестрикційні ферменти 0,37ммоль) у метиленхлориді (3,7мл) додають Nвід Boehringer and Vent, полімераза - від New гексил-2-фенілетиламін (0,080г, 0,39ммоль) і England Biolabs. ДМАП (0,045г, 0,37ммоль) і потім 1-етил-3-(3Клітинні лінії і умови для культур клітин диметиламінопропіл)-карбодіімідгідрохлорид U2-OS (остеогенна саркома людини) була (0,071г, 0,37ммоль), і реакційну суміш перемішупридбана від АТСС, USA, клітини були розширені і ють при кімнатній температурі протягом ночі. Суповторно заморожені порціями з проходу 6. Кульміш розбавляють метиленхлоридом (25мл), і оргатуру клітин вирощували у модифікованому середовищі Dulbecco's Eagle (DMEM) з 25мМ глюкози, нічну фазу промивають 5%-ю НСІ (3 25мл), 2мМ глютаміну або 4мМ L-аланіл-L-глютаміну, водним натрій гідрокарбонатом (25мл) і розсолом 10% сироватки зародка теляти при 5% СО2. Вико(25мл), сушать натрій сульфатом і концентрують у ристовували буферований фосфатом розсіл (PBS) вакуумі. Очищення на пакетній колонці силікагелю без додання кальцію або магнію. Всі реагенти для (Ізоlutе® SPE Column, 5г Si/25мл) з метанолом (0культури клітин - від Gibco (USA) і 96-коміркові 1% градієнт) у метиленхлориді як елюентом дає планшети для культур - від Wallach. 0,125г (70%) безбарвного масла. 1 Плазмідні констракти для гетерологічної ексН ЯМР (400МГц, CDCI3): δ 0,82-0,92 (m, 3Н), пресії 1,16 (t, 3Н), 1,19-1,33 (m, 9H), 1,45-1,65 (m, 2H), Була застосована стандартна процедура ре2,82-2,90 (m, 2H), 2,91-2,98 (m, 2H), 3,12-3,21 і комбінантної ДНК, описана у Ausubel (7). Репорте3,29-3,42 (2m, 3Н, ротамери) 3,50-3,65 (m, 3Н), рний вектор люциферази, pGLSUAS (клон склада3,95 (m,IH), 4,16 (q, 2Н), 4,39 і 4,65 (2s, 2H, ротається з 5 копій зв'язуючої послідовності GAM ДНК, мери), 6,75 і 6,86 (2d, 2H, ротамери), 7,10-7,34 (m, 5'-CGACGGAGTACTGTCCTCCGAGCT-3') був кло7H). 13 нованої у сайти Sacl/Xhol pGL3-Promoter С ЯМР (100МГц, CDCI3): δ 14,0, 14,1, 14,3, (Promega). Фрагмент Sacl/Xhol, що несе сайти 15,1, 22,6, 26,5, 26,7, 27,4, 29,0, 31,5, 31,6, 33,9, UAS, був конструктований з використанням гібри35,3, 3,8,5, 45,9, 48,1, 48,3, 48,9, 60,8, 66,2, 67,5, дизованих олігонуклеотидів, що перекриваються. 80,4, 114,5, 126,4, 126,9, 128,5, 128,9, 130,1, 130,2, Вектори експресії базуються на pSG5 (Stratagene). 130,5, 130,5, 138,3, 139,2, 156,9, 157,0, 167,6, Всі вектори містять фрагмент EcoRI/Nhel, який 167,8, 172,5 (Кількість піків перевищує кількість кодує зв'язуючий домен ДНК GAL4 (кодує позиції атомів карбону внаслідок ротамерів). 1-145 амінокислот з номером входу бази даних (іі) (2S)-2-етокси-3-(4-{2-[гексил(2Р04386) з подальшим злиттям у рамці з фрагменфенілетил)аміно]-2-оксоетокси}феніл)-пропанова том, що кодує ядерну локалізаційну послідовність кислота від антигену Τ Polyoma Virus. Ця послідовність До розчину етил (2S)-2-етокси-3-(4-{2конструктована з використанням гібридизованих [гексил(2-фенілетил)аміно]-2-оксоетокси}-феніл)охолодженням олігонуклеотидів, що перекривапропаноату (0,081г, 0,17ммоль) у ТГФ (8,6мл) доються, і створює клейкі кінці Nhel/Kpnl (5'дають 4,3мл 0,10М розчину LiOH і реакційну суміш CTAGCGCTCCTAGAAGAAACGCAAGGTTGGTACперемішують при кімнатній температурі протягом ночі. Реакційну суміш підкислюють 2М НСІ і екст3'). Зв'язуючі ліганд домени від АППР людини і рагують етилацетатом (3 25мл). Об'єднану органімиші і ΑΠΠΡ людини і миші були PCRчну фазу промивають розсолом (25мл), сушать ампліфіковані як фрагменти Kpnl/BamHI і кпонованатрій сульфатом і концентрують у вакуумі, одерні у рамці у домен, що зв'язує GAL4 ДНК і ядерну жуючи 0,073г (96%) безбарвного масла. локалізаційну послідовність. Послідовність всіх 1 Н ЯМР (400МГц, CDCI3): δ 0,82-0,93 (m, 3Н), плазмідних констрактів була підтверджена секвен1,15 (t, 3Н), 1,20-1,35 (m, 6H), 1,47-1,62 (m, 2H), суванням. Для перехідних трансфекцій були вико2,80-2,99 (m, 3Н), 3,00-3,09 (m, 1H), 3,11-3,21 і ристані такі вектори експресії. 3,31-3,44 (2m, 3Н, ретейнери), 3,50-3,67 (m, 3Н), 4,01 (m, 1Н), 4,40 і 4,66 (2s, 2H, ротамери), 6,75 і 6,85 (2d, 2H, ротамери), 7,10-7,35 (m, 7H), 8,86 (bs, 1H). 23 77460 24 ний фільтр, щоб видалити залишки вугілля та смоли. Субтип кодова- Тип послідовності Вектор Процедура аналізу ної АППР 1 Маточні розчини сполуки у ДМСО розбавляS74349,nt 625pSGGALhPPa ΑΠΠΡ людини ють до належної концентрації у основних планше1530 тах. Сполуки з основних планшетів розбавляють у X57638,nt 668pSGGALmPPa ΑΠΠΡ миші середовищі культури для отримання розчину тест1573 сполуки для кінцевих доз. U63415,nt 613pSGGALhPPg ΑΠΠΡ людини Після корекції кількості клітинного середовища 1518 до 75мкл у кожній комірці додають 50мкл розчину U09138,nt 652pSGGALmPPg ΑΠΠΡ миші тест-сполуки. Тимчасово трансфіковані клітини 1577 піддають дії сполуки протягом приблизно 24год. 1 перед проведенням аналізу виявлення люциферануклеотидні позиції входів бази даних, викози. Для цього аналізу додають 100мкл аналітичнористані для вираження домену, що зв'язує ліго реагенту до кожного комірки і планшети залиганди. шають приблизно на 20хвил. для забезпечення лізису клітин. Після лізису виміряють активність люциферази лічильником 1420 Multiwell counter, Перехідні транзакції Victor, від Wallach. Заморожені групи клітин з прогону шість були Еталонні сполуки розморожені і розширені до прогону 8 перед транДля активування ΑΠΠΡ як людини, так і миші, сфекцією. Злиті клітини були трипсинізовані, прояк еталонну речовину використовували TZDмиті і гранульовані у центрифузі при 270хg протяпіоглітазон. Для активування АППР людини і мигом 2хвил. Клітинні гранули були ресуспендовані у ші як еталонну речовину використовували 5, 8, 11, холодному БФФР (буферованому фосфатом фізі14-ейкозатетраіонову кислот (ЕТІK). ологічному розчині) до концентрації клітин приблиОбчислення і аналіз зно 18 106клітин/мл. Після додавання ДНК суспенДля обчислення значень ЕС50 була побудовазію інкубували на льоду протягом приблизно на крива залежності "концентрація-відгук". Необ5хвил.перед електропорацією при 230В, 960пкФ у хідні значення одержували усередненням двохBiorad's Gene Pulser™ у 0,5мл зразках. До кожного трьох незалежних вимірювань (після віднімання зразка були додані 50мкг ДНК, включаючи 2,5мкг середнього фонового значення) і репрезентували вектору експресії, 25мкг репортерного вектора і як процент від максимального активування ета22,5мкг неспецифічної ДНК (pBluescript, лонною сполукою. Значення наносили на графік як Stratagene). функцію логарифма концентрації тест-сполуки. Після електропорації клітини були розбавлені Значення EC50 оцінювали лінійною інтерполяцією до концентрації 320'000клітин/мл у DMEM без феміж точками даних і обчисленням концентрації, нольного червоного, і у 96-коміркових планшетах потрібної для одержання 50% максимального акбули посіяні приблизно 25'000клітин/комірку. Для тивування еталонною сполукою. відновлення клітин засіяні планшети були інкубоСполуки формули І мають EC50 нижче вані при 37°С протягом 3-4год. перед доданням 0,5мкмоль/л, а бажані сполуки - нижче тест-сполуки. У аналізах для ΑΠΠΡ клітинне се0,05мкмоль/л для АППР . Сполуки формули І є редовище доповнюють десорбованою зі смолиобраною групою сполук, які виявляють більш повугілля сироваткою зародка теляти (СЗТ), щоб тужну дію на АППР , ніж на ΑΠΠΡ . Вважається, уникнути фонового активування компонентами що таке співвідношення є важливим, оскільки хажирних кислот СЗТ. Цю СЗТ одержували таким рактеризує фармакологічну активність сполук і їх чином: на 500мл активованої нагріванням СЗТ терапевтичний профіль. додають 10г вугілля і 25г Bio-Rad Analytical Grade Крім того, сполуки винаходу мають поліпшені Anion Exchange Resin 200-400 mesh і розчин виякості щодо метаболізму ліків і фармакокінетики, тримують з магнітним перемішуванням при кімнанаприклад, вони виявляють поліпшену метаболічтній температурі протягом ночі. Наступного дня ну стабільність in vitro, а також сприятливу реакцію СЗТ центрифугують і повторюють процедуру обна дозу in vivo. Сполуки також мають багатообіцяробки протягом 4-6 годин. Після другої обробки ючий токсикологічний профіль. СЗТ центрифугують і фільтрують через стериль Комп’ютерна верстка Т. Чепелева Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted derivatives of phenylpropionic acid as agonists of alpha-receptor activated by peroxysome proliferator, method of preparation, pharmaceutical composition, intermediate (variants)
Автори англійськоюAlstermark Lindstedt Eva-Lotte, Olsson Anna Christina, Li Lanna
Назва патенту російськоюЗамещенные производные фенилпропионовой кислоты в качестве агонистов активированного пероксисомным пролифератором рецептора альфа (аппр) человека, способ их получения, фармацевтическая композиция на их основе, промежуточное соединение (варианты)
Автори російськоюАльстермарк Линдстедт Эва-Лотте, Ольссон Анна Кристина, Ли Ланна
МПК / Мітки
МПК: A61P 9/12, A61P 9/10, A61K 31/554, C07C 69/736, A61K 31/195, A61P 3/10, C07C 69/734, A61K 45/00, A61K 31/16, A61K 31/192, A61P 3/04, A61K 45/06, A61K 31/505, C07C 231/00, C07C 235/20, A61P 43/00, A61K 31/40, A61P 3/00, A61P 3/06
Мітки: агоністи, альфа, сполука, одержання, рецептора, заміщені, похідні, пероксизомним, фенілпропіонової, активованого, основі, спосіб, фармацевтична, аппр, людини, варіанти, кислоти, композиція, проміжна, проліфератором
Код посилання
<a href="https://ua.patents.su/12-77460-zamishheni-pokhidni-fenilpropionovo-kisloti-yak-agonisti-aktivovanogo-peroksizomnim-proliferatorom-receptora-alfa-appr-lyudini-sposib-kh-oderzhannya-farmacevtichna-kompoziciya-na-k.html" target="_blank" rel="follow" title="База патентів України">Заміщені похідні фенілпропіонової кислоти як агоністи активованого пероксизомним проліфератором рецептора альфа (аппр) людини, спосіб їх одержання, фармацевтична композиція на їх основі, проміжна сполука (варіанти)</a>
Попередній патент: Тонкоплівковий конденсатор і спосіб його одержання
Наступний патент: Колонний екстрактор
Випадковий патент: Пробка-дозатор для пляшки з рідиною












