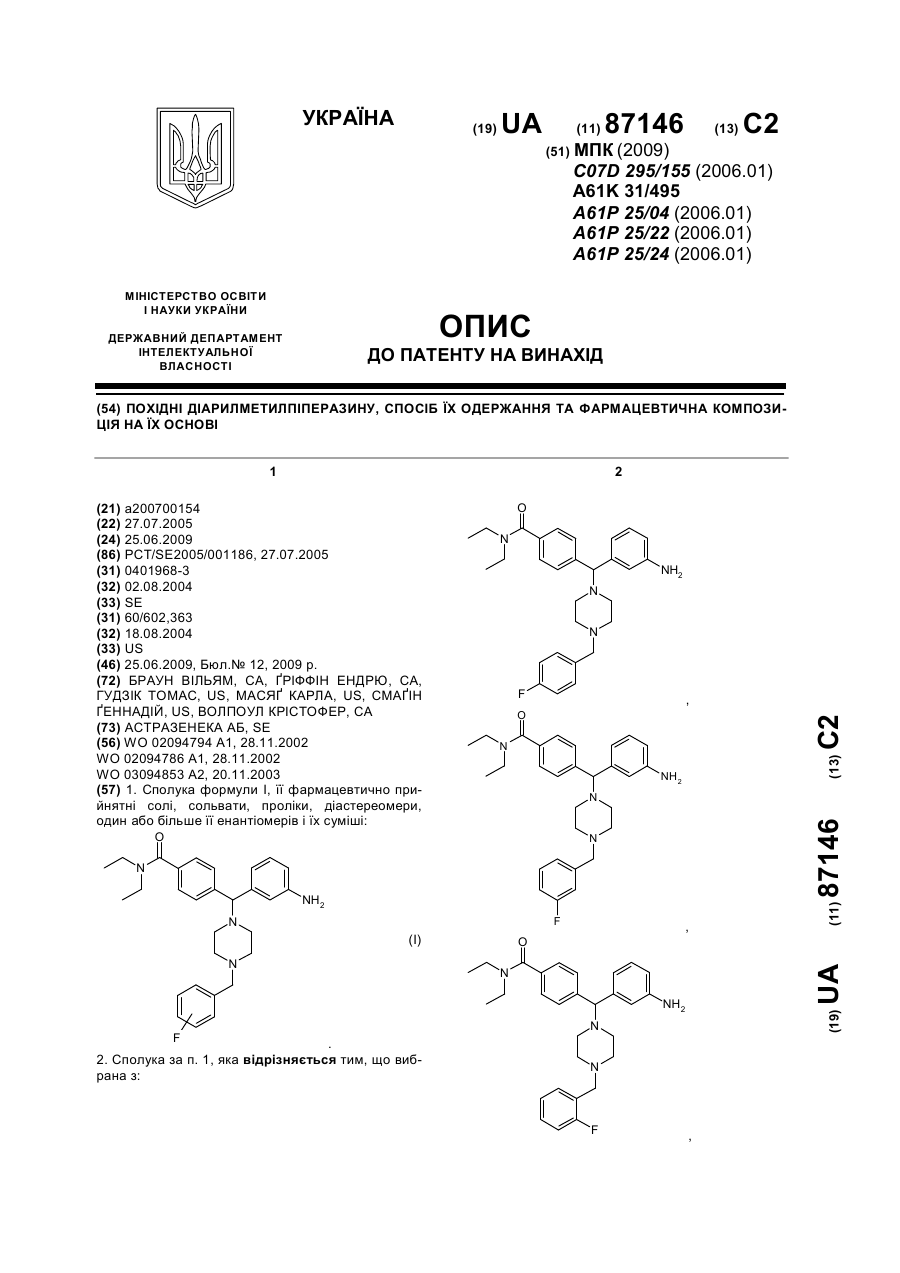
Похідні діарилметилпіперазину, спосіб їх одержання та фармацевтична композиція на їх основі
Номер патенту: 87146
Опубліковано: 25.06.2009
Автори: Гудзік Томас, Масяґ Карла, Смаґін Ґеннадій, ріффін Ендрю, Браун Віл'ям, Волпоул Крістофер
Формула / Реферат
1. Сполука формули І, її фармацевтично прийнятні солі, сольвати, проліки, діастереомери, один або більше її енантіомерів і їх суміші:
 . (I)
. (I)
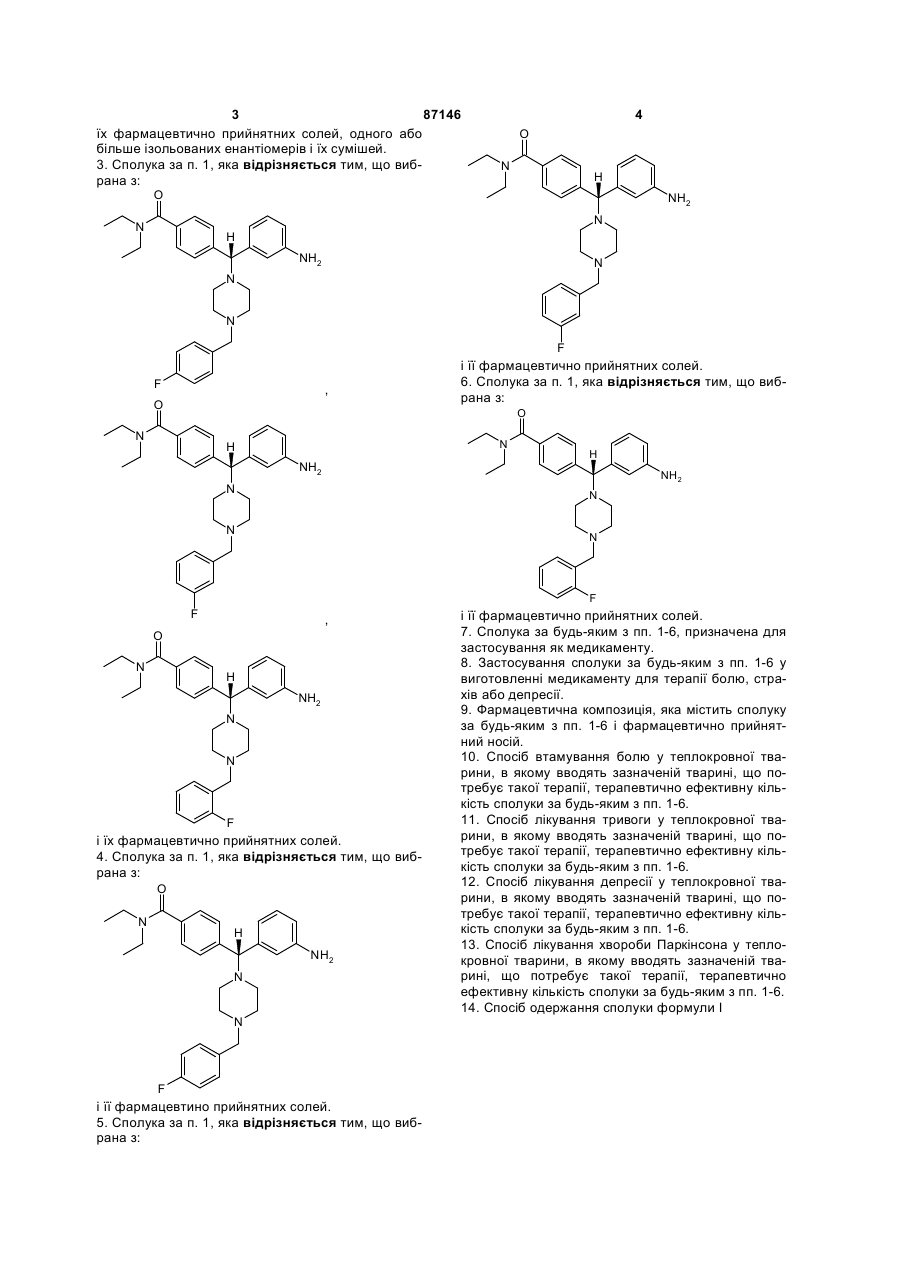
2. Сполука за п. 1, яка відрізняється тим, що вибрана з:
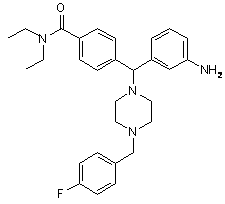 ,
,  ,
,
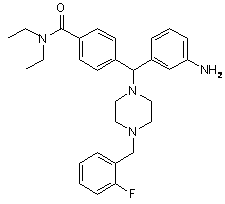 ,
,
їх фармацевтично прийнятних солей, одного або більше ізольованих енантіомерів і їх сумішей.
3. Сполука за п. 1, яка відрізняється тим, що вибрана з:
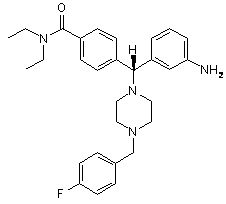 ,
,  ,
,
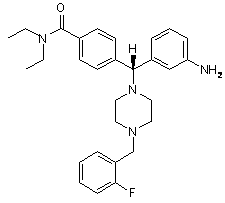
і їх фармацевтично прийнятних солей.
4. Сполука за п. 1, яка відрізняється тим, що вибрана з:
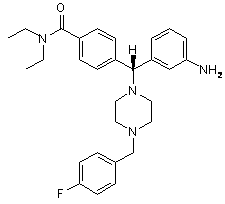
і її фармацевтино прийнятних солей.
5. Сполука за п. 1, яка відрізняється тим, що вибрана з:

і її фармацевтично прийнятних солей.
6. Сполука за п. 1, яка відрізняється тим, що вибрана з:

і її фармацевтично прийнятних солей.
7. Сполука за будь-яким з пп. 1-6, призначена для застосування як медикаменту.
8. Застосування сполуки за будь-яким з пп. 1-6 у виготовленні медикаменту для терапії болю, страхів або депресії.
9. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-6 і фармацевтично прийнятний носій.
10. Спосіб втамування болю у теплокровної тварини, в якому вводять зазначеній тварині, що потребує такої терапії, терапевтично ефективну кількість сполуки за будь-яким з пп. 1-6.
11. Спосіб лікування тривоги у теплокровної тварини, в якому вводять зазначеній тварині, що потребує такої терапії, терапевтично ефективну кількість сполуки за будь-яким з пп. 1-6.
12. Спосіб лікування депресії у теплокровної тварини, в якому вводять зазначеній тварині, що потребує такої терапії, терапевтично ефективну кількість сполуки за будь-яким з пп. 1-6.
13. Спосіб лікування хвороби Паркінсона у теплокровної тварини, в якому вводять зазначеній тварині, що потребує такої терапії, терапевтично ефективну кількість сполуки за будь-яким з пп. 1-6.
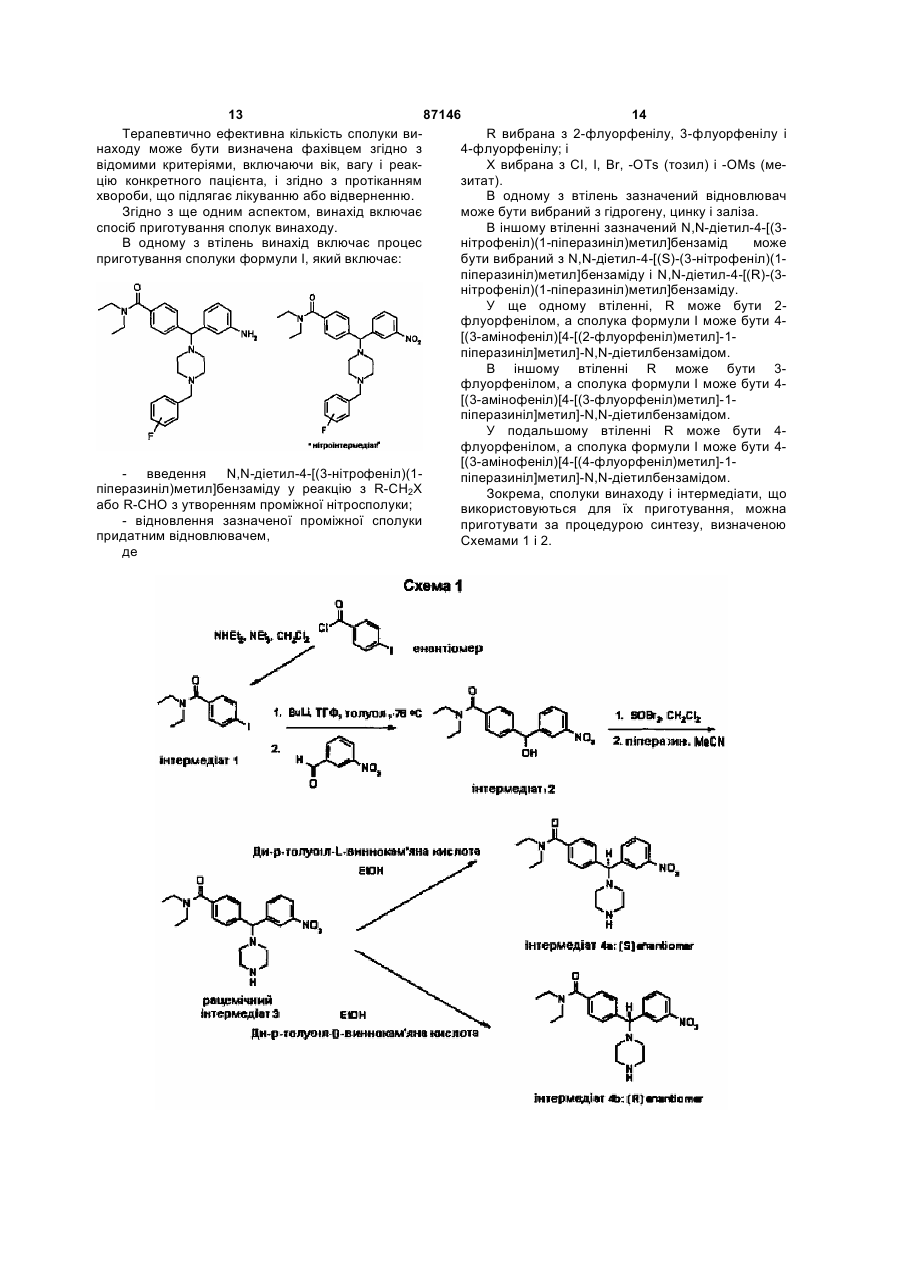
14. Спосіб одержання сполуки формули І
 , (I)
, (I)
в якому здійснюють:
- введення N,N-діетил-4-[(3-нітрофеніл)(1-піперазиніл)метил]бензаміду у реакцію з R-СН2Х або R-CHO з отриманням проміжної сполуки;
- відновлення зазначеної проміжної сполуки відповідним відновлювачем,
де
R вибрана з 2-флуорфенілу, 3-флуорфенілу і 4-флуорфенілу; а
Х вибрана з Сl, І, Br, -OTs (тозил) і -OMs (мезилат).
15. Спосіб за п. 14, який відрізняється тим, що зазначений відновлювач може бути вибраний з гідрогену, цинку і заліза.
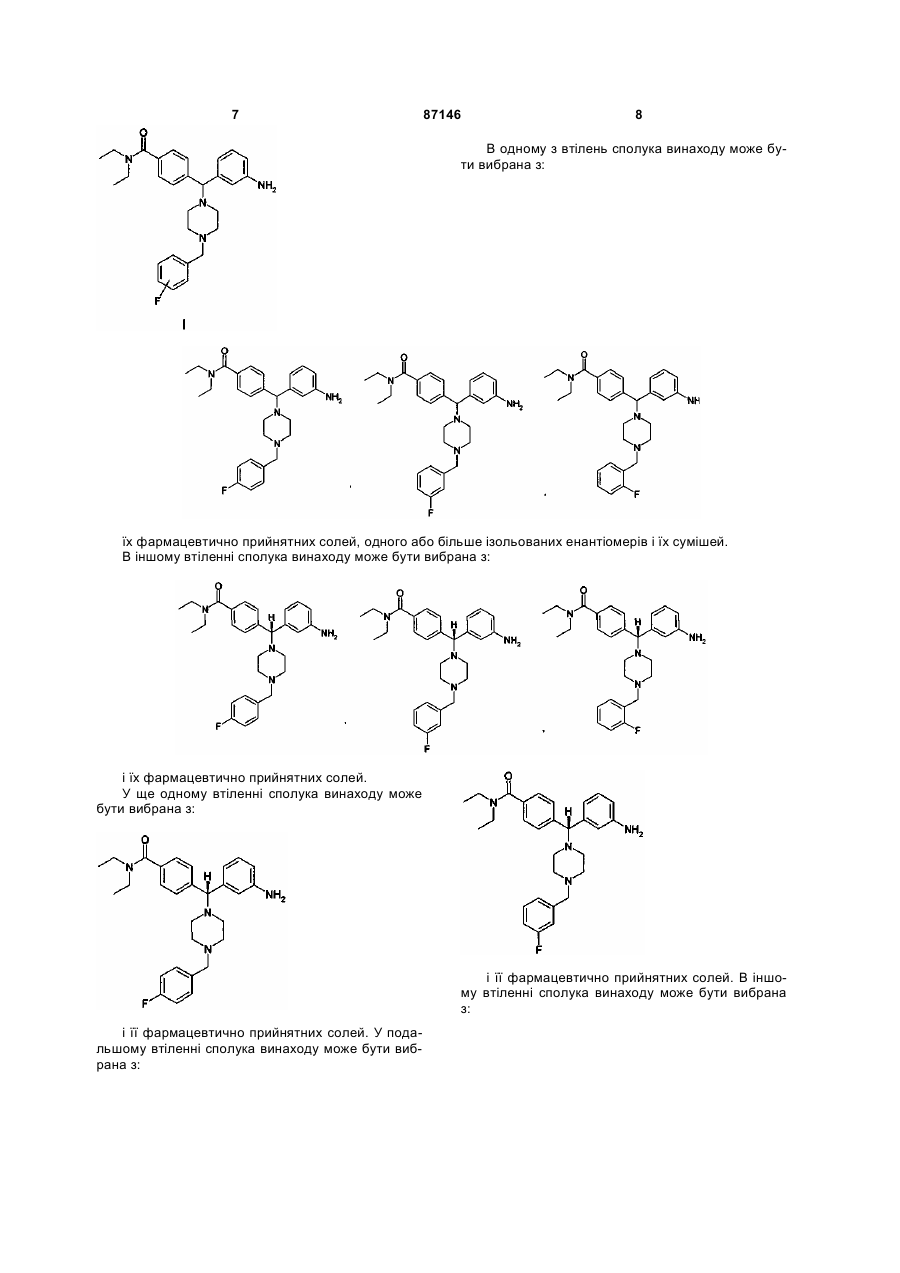
16. Сполука, вибрана з
енантіомерно чистого 4-{(S)-(3-амінофеніл)[4-(4-флуорбензил)піперазин-1-іл]метил}-N,N-діетилбензаміду,
енантіомерно чистого 4-{(R)-(3-амінофеніл)[4-(4-флуорбензил)піперазин-1-іл]метил}-N,N-діетилбензаміду,
енантіомерно чистого 4-[(R)-(3-амінофеніл)[4-[(2-флуорфеніл)метил]-1-піперазиніл]метил]-N,N-діетилбензаміду,
енантіомерно чистого 4-[(R)-(3-амінофеніл)[4-[(3-флуорфеніл)метил]-1-піперазиніл]метил]-N,N-діетилбензаміду
і їх фармацевтично прийнятних солей.
Текст
1. Сполука формули І, її фармацевтично прийнятні солі, сольвати, проліки, діастереомери, один або більше її енантіомерів і їх суміші: N N F , 3 87146 їх фармацевтично прийнятних солей, одного або більше ізольованих енантіомерів і їх сумішей. 3. Сполука за п. 1, яка відрізняється тим, що вибрана з: 4 O N H O NH2 N N H NH2 N N N F F , O і її фармацевтично прийнятних солей. 6. Сполука за п. 1, яка відрізняється тим, що вибрана з: O N N H NH2 H NH2 N N N N F F , O N H NH2 N N F і їх фармацевтично прийнятних солей. 4. Сполука за п. 1, яка відрізняється тим, що вибрана з: O N H NH2 N N F і її фармацевтино прийнятних солей. 5. Сполука за п. 1, яка відрізняється тим, що вибрана з: і її фармацевтично прийнятних солей. 7. Сполука за будь-яким з пп. 1-6, призначена для застосування як медикаменту. 8. Застосування сполуки за будь-яким з пп. 1-6 у виготовленні медикаменту для терапії болю, страхів або депресії. 9. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-6 і фармацевтично прийнятний носій. 10. Спосіб втамування болю у теплокровної тварини, в якому вводять зазначеній тварині, що потребує такої терапії, терапевтично ефективну кількість сполуки за будь-яким з пп. 1-6. 11. Спосіб лікування тривоги у теплокровної тварини, в якому вводять зазначеній тварині, що потребує такої терапії, терапевтично ефективну кількість сполуки за будь-яким з пп. 1-6. 12. Спосіб лікування депресії у теплокровної тварини, в якому вводять зазначеній тварині, що потребує такої терапії, терапевтично ефективну кількість сполуки за будь-яким з пп. 1-6. 13. Спосіб лікування хвороби Паркінсона у теплокровної тварини, в якому вводять зазначеній тварині, що потребує такої терапії, терапевтично ефективну кількість сполуки за будь-яким з пп. 1-6. 14. Спосіб одержання сполуки формули І 5 87146 6 R вибрана з 2-флуорфенілу, 3-флуорфенілу і 4флуорфенілу; а Х вибрана з Сl, І, Br, -OTs (тозил) і -OMs (мезилат). N 15. Спосіб за п. 14, який відрізняється тим, що зазначений відновлювач може бути вибраний з NH2 гідрогену, цинку і заліза. N 16. Сполука, вибрана з (I) енантіомерно чистого 4-{(S)-(3-амінофеніл)[4-(4флуорбензил)піперазин-1-іл]метил}-N,NN діетилбензаміду, енантіомерно чистого 4-{(R)-(3-амінофеніл)[4-(4флуорбензил)піперазин-1-іл]метил}-N,Nдіетилбензаміду, F енантіомерно чистого 4-[(R)-(3-амінофеніл)[4-[(2, флуорфеніл)метил]-1-піперазиніл]метил]-N,Nв якому здійснюють: діетилбензаміду, введення N,N-діетил-4-[(3-нітрофеніл)(1енантіомерно чистого 4-[(R)-(3-амінофеніл)[4-[(3піперазиніл)метил]бензаміду у реакцію з R-СН2Х флуорфеніл)метил]-1-піперазиніл]метил]-N,Nабо R-CHO з отриманням проміжної сполуки; діетилбензаміду - відновлення зазначеної проміжної сполуки відпоі їх фармацевтично прийнятних солей. відним відновлювачем, де O Ця заявка пов'язана з попередньою заявкою США 60/602 363 від 18/08/2004, включеною посиланням і має пріоритет згідно з 35 U.S.C., § 119(a)(d), для шведської заявки No. 0401968-3 від 2/08/2004. Винахід стосується нових сполук, способу їх приготування, їх застосування і фармацевтичних композицій, що містять ці сполуки, а також їх використання у терапії, зокрема, для лікування болю, страхів і функціональних шлунково-кишкових розладів. Було встановлено, що дельта("d")-рецептор грає роль у багатьох тілесних функціях, наприклад, систем кровообігу і больових систем. Тому ліганди для d-рецептора можуть знайти потенційне застосування як аналгетикЬ і/або антигіпертонічні агенти. Було показано, що ліганди для dрецептора виявляють імуномодуляторну активність. На сьогоднішній день ідентифіковано щонайменше три різні популяції опіоїдних рецепторів (m, d і k), і всі три були знайдені у центральній і периферійній нервових системах багатьох видів, включаючи людину. У багатьох тваринних моделях спостерігали аналгезію при активуванні одного або більше цих рецепторів. За небагатьма винятками, наявні селективні опіоїдні d-ліганди є пептидними за природою і є непридатними для введення пацієнту системними шляхами. Одним з прикладів не-пептидного dагоніста є SNC80 [Bilsky E.J. et al., Journal of Pharmacology and Experimental Therapeutics, 273(1), pp. 359-366 (1995)]. Були ідентифіковані численні d-агоністичні сполуки, але вони мають багато вад, зокрема, погану фармакокінетику і не діють як аналгетики при введенні системними шляхами. Крім того, було підтверджено, що багатьом з цих d-агоністичних сполук властива значна конвульсивна дія при системному введенні. Деякі d-агоністи були описані у публікації РСТ WO02/094794. Проте існує потреба у поліпшених d-агоністах. Ми несподівано виявили, що деякі сполуки мають одну або більше поліпшених якостей, тобто поліпшені d-агоністичну активність, активність in vivo, фармакокінетику, біозасвоюваність, стабільність in vitro і in vivo, здатність проникати у мозок і/або нижчу токсичність. Якщо не визначено інше, номенклатура у цьому описі взагалі відповідає прикладам і вимогам документа Nomenclature of Organic Chemistry, Sections A, B, C, D, E, F, H, Pergamon Press, Oxford, 1979, включеному у цей опис посиланням стосовно правил для типових назв хімічних структур; як варіант, назва сполуки може бути утворена з використанням програми хімічних найменувань ACD/ChemSketch, Version 5,09/September 2001, Advanced Chemistry Development, Inc., Toronto, Canada. "Енантіомерно чистий" стосується сполуки, яка містить щонайменше 75% даного енантіомеру від повної кількості двох можливих енантіомерів. Зокрема, "енантіомерно чистий" стосується сполуки, яка містить щонайменше 90% даного енантіомеру від повної кількості двох можливих енантіомерів. У деяких втіленнях, "енантіомерно чистий" стосується сполуки, яка містить щонайменше 96% даного енантіомеру від повної кількості двох можливих енантіомерів. "Теплокровні тварини" включають людину. Згідно з одним з аспектів, винахід стосується сполук формули І, їх фармацевтично прийнятних солей, сольватів, проліків, діастереомерів, одного або більше енантіомерів і їх сумішей: 7 87146 8 В одному з втілень сполука винаходу може бути вибрана з: їх фармацевтично прийнятних солей, одного або більше ізольованих енантіомерів і їх сумішей. В іншому втіленні сполука винаходу може бути вибрана з: і їх фармацевтично прийнятних солей. У ще одному втіленні сполука винаходу може бути вибрана з: і її фармацевтично прийнятних солей. В іншому втіленні сполука винаходу може бути вибрана з: і її фармацевтично прийнятних солей. У подальшому втіленні сполука винаходу може бути вибрана з: 9 87146 10 карбонової кислоти або фенолу, одним еквівалентом гідроксиду або алкоксиду лужного або лужноземельного металу (наприклад, етоксиду або метоксиду), або належним основним органічним аміном (наприклад, холіном або меглуміном) у водному середовищі, з подальшим звичайним очищенням. В одному з втілень сполука формули І може бути перетворена у її фармацевтично прийнятну сіль або сольват, зокрема, у кислото-адитивну сіль, наприклад, гідрохлорид, гідробромід, фосфат, ацетат, фумарат, малеат, тартрат, цитрат, метансульфонат або р-толуолсульфонат. і її фармацевтично прийнятних солей. Нові сполуки винаходу можуть бути викорисВ іншому втіленні сполука винаходу може бути вибрана з групи, яку складають 4-{S)-(3тані у терапії, зокрема, для лікування різних больових станів, наприклад, хронічного болю, нейамінофеніл)[4-(4-флуорбензил)піперазин-1ропатичного болю, гострого болю, ракового болю, іл]метил}-N,N-діетилбензамід; 4-{(R)-(3болю, викликаного ревматоїдним артритом, мігамінофеніл)[4-(4-флуорбензил)піперазин-1ренню, вісцерального болю тощо. Цей перелік не є іл]метил}-N,N-діетилбензамід; 4-[(R)-(3вичерпним. амінофеніл)[4-[(2-флуорфеніл)метил]-1Сполуки винаходу можуть бути використані піперазиніл]метил]-N,N-діетилбензамід; 4-[(R)-(3для лікування діареї, депресії, страхів і/або стреамінофеніл)[4-[(3-флуорфеніл)метил]-1піперазиніл]метил]-N,N-діетил-бензамід і їх фарсових розладів, наприклад, посттравматичного стресу, панічного розладу, загально тривожного мацевтично прийнятні солі. розладу, соціальної фобії і обсесивноУ ще одному втіленні сполук винаходу може компульсивного розладу, нетримання сечі, передбути вибрана з групи, яку складатють енантіомерчасної еякуляції, різних ментальних захворювань, но чистий 4-{(S)-(3-амінофеніл)[4-(4кашлю, легеневого набряку, різних шлунковофлуорбензил)піперазин-1-іл]метил}-N,Nкишкових розладів, наприклад, констипації, функдіетилбензамід; енантіомерно чистий 4-{(R)-(3ціональних шлунково-кишкових розладів, наприамінофеніл)[4-(4-флуорбензил)піперазин-1іл]метил}-N,N-діетилбензамід; енантіомерно чисклад, синдрому подразнення кишечнику і функціотий 4-[(R)-(3-амінофеніл)[4-[(2-флуорнальної диспепсії, хвороби Паркінсона і інших моторних розладів, травматичних пошкоджень феніл)метил]-1-піперазиніл]метил]-N,Nмозку, інсульту, для кардіозахисту після інфаркту діетилбензамід; енантіомерно чистий 4-[(R)-(3міокарду, травм спини і залежностей, включаючи амінофеніл)[4-[(3-флуорфеніл)метил]-1залежності від спирту, нікотину, опіоїду, і інших піперазиніл]метил]-N,N-діетилбензамід і їх фармазловживань і розладів симпатичної нервової сисцевтично прийнятні солі. теми, наприклад, гіпертонії. Зрозуміло, що, коли сполуки винаходу мають Сполуки винаходу можуть бути використані як один або більше хіральних центрів, ці сполуки можуть існувати і бути ізольовані як епантіомерні або імуномодулятори, зокрема, для аутоімунних хвороб, наприклад, артриту, длятрансплантації шкіри діастереомерні форми або як рацемічні суміші. і органів і для подібних хірургічних потреб, для Винахід включає будь-який можливий енантіомер, хвороб колагену, різних алергій, для використання діастереомери, рацемати або їх суміші від сполук як антипухлинних і антивірусних агентів. формули І. Оптично активні форми сполуки винаСполуки винаходу можуть бути використані ходу можуть бути приготовлені, наприклад, хорапри хворобливих станах, в яких має місце дегенальним хроматографічним розділенням рацемату, рація або дисфункція опіоїдних рецепторів або в синтезом з оптично активних вихідних матеріалів або асиметричним синтезом, базованим на описаяких існує зв'язок з цими явищами. Це може потребувати використання ізотопічно мічених версій них далі процедурах. сполук винаходу у діагностиці і при застосуванні Зрозуміло також, що деякі сполуки винаходу зображень, наприклад, у позитронно-емісійній томожуть існувати у сольватованій, наприклад, гідмографії. ратованій, а також несольватованій формах. ВиСполуки винаходу можуть бути використані як нахід включає всі такі сольватовані форми сполуки аналгетики при застосуванні загальної анестезії і формули І. нагляду під анестезією. Для отримання балансу В об'єм винаходу входять також солі сполуки формули І. Взагалі фармацевтично прийнятні солі результатів, необхідних для підтримання анестетичного стану (наприклад, амнезії, аналгезії, м'ясполук винаходу можуть бути отримані з застосузової релаксації і заспокоєння) часто використованням стандартних процедур, наприклад, реакцівують комбінації агентів з різними властивостями. єю достатньо основної сполуки, наприклад, алкіл Такі комбінації включають інгаляційні анестетики, аміну, з придатною для цього кислотою, напригіпнотики, транквілізатори, нейром'язові блокери і клад, НСІ або оцтовою, отримуючи фізіологічно опіоїди. прийнятний аніон. Можна також отримати сіль відВ об'єм винаходу входить застосування будьповідного лужного металу (наприклад, натрію, калію або літію) або лужно-земельного металу (наякої сполуки формули І для виготовлення медикаменту. приклад, кальцію) обробкою сполуки винаходу, що має відповідний кислотний протон, наприклад, 11 87146 12 Крім того, в об'єм винаходу входить застосуз фармацевтично прийнятним носієм, для викоривання будь-якої сполуки винаходу для виготовстання у терапії болю і страхів. лення медикаменту, призначеного для терапії боКрім того, винахід включає фармацевтичну лю, включаючи, але без обмеження, гострий біль, композицію, що містить сполуку винаходу, її сольхронічний біль, невропатичній біль, біль у спині, вати або її фармацевтично прийнятну сіль, разом раковий біль і вісцеральний біль. з фармацевтично прийнятним носієм для викорисТакож в об'єм винаходу входить застосування тання при будь-яких описаних вище станах. сполуки винаходу для виготовлення медикаменту, Для приготування фармацевтичної композиції призначеного для терапії страхів, включаючи, але з сполуками винаходу можуть бути використані без обмеження, соціальну фобію, загальний тритверді або рідкі фармацевтично прийнятні носії. вожний розлад, гостру тривожність. Тверді препарати включають порошки, таблетки, Крім того, в об'єм винаходу входить застосудисперсні гранули, капсули, каше і супозиторії. вання будь-якої сполуки винаходу для виготовТвердими носіями можуть бути одна або більлення медикаменту, призначеного для терапії деше речовин, які можуть бути також розріджувачапресії. ми, смаковими агентами, солюбілізаторами, змаТакож в об'єм винаходу входить застосування щувачами, суспендуючи ми або зв'язуючими будь-якої сполуки винаходу для виготовлення меагентами або дезінтеграторами таблетки; вони дикаменту, призначеного для терапії хвороби Парможуть бути також інкапсуляторами. кінсона. У порошках носій є подрібненою твердою реКрім того, в об'єм винаходу входить застосучовиною у суміші з подрібненою сполукою винаховання будь-якої сполуки винаходу для виготовду або активним компонентом. У таблетках активлення медикаменту, призначеного для лікування ний компонент змішаний з носієм, який має будь-якого з розглянутих вище станів. необхідні зв'язувальні якості, у потрібній пропорції Одним з аспектів винаходу є спосіб лікування і сформований у бажані форму і розмір. суб'єкту, що страждає від будь-якого з зазначених Для приготування супозиторної композиції вище станів, згідно з яким ефективну кількість розплавляють легкоплавкий віск, наприклад, суміш сполуки винаходу вводять пацієнту, що потребує гліцеридів жирних кислот і масла какао і диспертакого лікування. гують активний інгредієнт з перемішуванням. РозОтже, винахід включає сполуку формули І або плавлену гомогенну суміш вливають у форми баїї фармацевтично прийнятну сіль або сольват, жаного розміру і залишають для отвердіння. визначені вище, для використання у терапії. Придатними носіями є карбонат магнію, стеаТут термін "терапія" включає "профілактику", рат магнію, тальк, лактоза, цукор, пектин, декякщо спеціально не зазначено інше. Термін "терастрин, крохмаль, трагакант, метилцелюлоза, напевтичний" і "терапевтично" слід інтерпретувати трій-карбоксиметилцелюлоза, легкоплавкий віск, відповідно. Термін "терапія" включає введення масло какао тощо. пацієнту ефективної кількості сполуки винаходу Термін "композиція" також включає рецептури для полегшення вже існуючого хворобливого стаактивного компонента з інкапсулюючим матеріал ну, гострого або хронічного, або рекурентного стаяк носієм з утворенням капсул, в яких активний ну. Це визначення також включає профілактичні компонент (з іншими носіями або без них) замкнетерапії для відвернення рекурентних станів і поний у носії. Подібні операції проводять з каше. довження терапії для хронічних розладів. Таблетки, порошки, каше і капсули можна виПри використанні для терапії у теплокровних користовувати як тверді дозовані форми для петварин, наприклад, людини, сполуку винаходу морорального введення пацієнту. жна вводити у формі звичайної фармацевтичної Рідкі композиції включають розчини, суспензії і композиції будь-яким шляхом, включаючи перораемульсії. Прикладом можуть бути водні або воднольне, внутрішньом'язове, підшкірне, локальне, пропіленгліколеві розчини активних сполук для внутрішньоносове, внутрішньочеревне, інтраторапарентерального введення пацієнту. Рідкими комкальне, внутрішньовенне, епідуральне, інтратекапозиціями також можуть бути водні розчини рецельне, інтрацереб-ровентрикулярне введення і птури у водному поліетиленгліколевому розчині. введення ін'єкцією у суглоби. Водні розчини для перорального введення В одному з втілень винаходу шлях введення можуть бути приготовлені розчиненням активного пацієнту може бути пероральним, внутрішньовенкомпонента у воді з доданням за бажанням приданим або внутрішньом'язовим. тних для цього забарвлювачів, смакових агентів, Дози залежать від способу введення пацієнту, стабілізаторів і загущувачів. Водні суспензії для важкості хвороби, віку і ваги пацієнта і інших факперорального застосування можуть бути пригототорів, які звичайно бере до уваги лікар, коли вивлені диспергування тонко подрібненого активного значає режим лікування і дози для конкретного компонента у воді разом з в'язким матеріалом, пацієнта. наприклад, природною або синтетичною кумою, Отже, винахід включає фармацевтичну компосмолою, метилцелюлозою, натрійзицію, що містить сполуку винаходу, її сольвати карбоксиметилцелюлозою і іншими відомими у або її фармацевтично прийнятну сіль, разом з фагалузі суспендуючими агентами. рмацевтично прийнятним носієм. Залежно від способа введення пацієнту фарЗокрема, винахід включає фармацевтичну мацевтична композиція, бажано, містить від 0,05% композицію, що містить сполуку винаходу, її сольдо 99%, більше бажано, від 0,10 до 50% (за мавати або її фармацевтично прийнятну сіль, разом сою), сполуки винаходу від повного складу композиції. 13 87146 14 Терапевтично ефективна кількість сполуки виR вибрана з 2-флуорфенілу, 3-флуорфенілу і находу може бути визначена фахівцем згідно з 4-флуорфенілу; і відомими критеріями, включаючи вік, вагу і реакX вибрана з СІ, І, Br, -OTs (тозил) і -OMs (мецію конкретного пацієнта, і згідно з протіканням зитат). хвороби, що підлягає лікуванню або відверненню. В одному з втілень зазначений відновлювач Згідно з ще одним аспектом, винахід включає може бути вибраний з гідрогену, цинку і заліза. спосіб приготування сполук винаходу. В іншому втіленні зазначений N,N-діетил-4-[(3В одному з втілень винахід включає процес нітрофеніл)(1-піперазиніл)метил]бензамід може приготування сполуки формули І, який включає: бути вибраний з N,N-діетил-4-[(S)-(3-нітрофеніл)(1піперазиніл)метил]бензаміду і N,N-діетил-4-[(R)-(3нітрофеніл)(1-піперазиніл)метил]бензаміду. У ще одному втіленні, R може бути 2флуорфенілом, а сполука формули І може бути 4[(3-амінофеніл)[4-[(2-флуорфеніл)метил]-1піперазиніл]метил]-N,N-діетилбензамідом. В іншому втіленні R може бути 3флуорфенілом, а сполука формули І може бути 4[(3-амінофеніл)[4-[(3-флуорфеніл)метил]-1піперазиніл]метил]-N,N-діетилбензамідом. У подальшому втіленні R може бути 4флуорфенілом, а сполука формули І може бути 4[(3-амінофеніл)[4-[(4-флуорфеніл)метил]-1- введення N,N-діетил-4-[(3-нітрофеніл)(1піперазиніл]метил]-N,N-діетилбензамідом. піперазиніл)метил]бензаміду у реакцію з R-СН2Х Зокрема, сполуки винаходу і інтермедіати, що або R-CHO з утворенням проміжної нітросполуки; використовуються для їх приготування, можна - відновлення зазначеної проміжної сполуки приготувати за процедурою синтезу, визначеною придатним відновлювачем, Схемами 1 і 2. де 15 Біологічне оцінювання і властивості Була виявлена активність сполук винаходу до d-рецепторів у теплокровних тварин, включаючи людину. Зокрема, було виявлено, що сполуки винаходу є ефективними лігандами d-рецептора. Аналізи in vitro, infra, підтвердили цю активність, особливо ефективність і потужність агоністів, показану в аналізі функцій мозку щура і/або функціональним аналізом d-рецептора людини (низька). Це може бути віднесено до активності in vivo і може не бути лінійно корельовано з зв'язувальною спорідненістю. У цих аналізах in vitro сполуку випробували на активність до d-рецепторів і визначали IК50 для оцінювання селективної активності певної сполуки до d-рецепторів. У даному випадку IК50 є концентрацією сполуки, при якій спостерігається 50%-е видалення ліганду радіоактивного dрецептора. У подібних аналізах були виміряні активності сполук до k- і m-рецепторів. Моделі in vitro Клітинна культура Клітини 293S людини, що експресують клоновані людські k-, d- і m-рецептори і стійкі до неоміцин у вирощували у суспензії при 37°С і 5% СО2 у шейкерних колбах з вільним від кальцію DMEM10% FBS, 5% BCS, 0,1% Pluronic F-68 і 600мг/мл генетицину. Мозки щура були зважені і промиті льодяним PBS (з 2,5мМ EDTA, рН 7,4). Мозки гомогенізували полі троном протягом 30сек. (щур) у льодяному лізисному буфері (50мМ Tris, рН 7,0, 2,5мМ EDTA, з фенілметилсульфонілфлуоридом (PMSF), доданим перед використанням, до 0,5МмМ з 0,5М материнського запасу у ДМСО/етанолі). Приготування мембрани Клітини гранулювали і ре суспендували у лізисному буфері (50мМ Tris, pH 7,0, 2,5мМ EDTA, з PMSF, доданим перед використанням, до 0,1МмМ з 0,1Μ материнського запасу в етанолі), інкубували на льоду протягом 15хвил., потім гомогенізували полі троном протягом 30сек. Суспензію 87146 16 центрифугували при 1000g (max) 10хвил. при 4°С. Надосадову рідину зберігали на льоду і гранули ресуспендували, як раніше. Надосадові рідини з обох центрифугувань об'єднували центрифугували при 46000g (max) 30хвил. Гранули ресуспендували у холодному Tris-буфері (50мМ Tris/CI, pH 7,0) і центрифугували. Отримані гранули ресуспендували у мембранному буфері (50мМ Tris, 0,32M сахароза, рН 7,0). Аліквоти (1мл) у поліпропіленових пробірках заморожували у сухому льоді/етанолі і зберігали при -70°С до подальшого використання. Концентрації протеїну визначали модифікованим аналізом Лоурі (Lowry) з додецилсульфатом натрію. Аналізи на зв'язування Мембрани розморожували при 37°С і зберігали на льоду, пропускали тричі через 25-каліброву голку і розбавляли зв'язувальним буфером (50мМ Tris, 3мМ МgСІ2, 1мг/мл BSA (Sigma А-7888), рН 7,4), зберігали при 4°С після фільтрування через фільтр 0,22m і додавали свіжим 5мкг/мл апротоніну, 10мкМ бестатину, 10мкМ дипротину А, якщо мембрани були отримані з тканин (щура, миші, мавпи, без DTT). Аліквоти по 100мкл додавали до охолоджених льодом поліпропіленових пробірок 12x75мм з 100мкл відповідного радіоліганду і 100мк випробуваної сполуки при різних концентраціях. Повне (ТВ) і неспецифічне (NS) зв'язування визначали у присутності і відсутності 10мкМ налоксону. Пробірки струшували і інкубували при 25°С протягом 60-75хвил., після чого швидко вакуум-фільтрували і промивали приблизно 12мл/пробірка промивним буфером (50мМ Tris, рН 7,0, 3мМ МgСІ2) через фільтри GF/B (Whatman), просочуючи протягом щонайменше 2год. у 0,1%му полiетиленейміні. Радіоактивність (dpm) на фільтрах виміряли бета-лічильником після просочування фільтрів протягом щонайменше 12год. у мініколбах з 6-7мл сцинтиляційної рідини. Аналіз проводили у 96-коміркових глибоких планшетах з фільтруванням через 96-коміркові уніфільтри, про 17 87146 18 Мембрани мозку щура розморожували при сочені РЕІ, які промивали тричі 1мл промивного 37°С, пропускали тричі через голку калібру 25 з буфера і сушили у печі при 55°С 2год. Відлік на фільтрі проводили лічильником TopCount тупим кінцем і розбавляли зв'язувальним GTPgS (Packard) після додання 50мкл сцинтиляційної рі(50мМ Hepes, 20мМ NaOH, 100мМ NaCI, 1мМ дини MS-20 на комірку. IКC50 сполук оцінювали на EDTA, 5мМ МgСІ2, рН 7,4, з доданням свіжих: 1мМ 10-точкових кривих видалення для d і 5-точкових DTT, 0,1% BSA). Мембрани розбавляли доданням 120мкМ GDP. EК50 і Еmах сполук оцінювали з 10кривих для m і k. Аналіз проводили в об'ємі 300мкл точкових кривих залежності від дози в об'ємі з належною кількістю протеїну мембрани (2мкг, 300мкл з належною кількістю протеїну мембрани 35мкг і 1мкг для d, m і k, відповідно) і 50000-80000 (20мкг/комірка) і 100000-130000dpm GTPg35S на dpm/комірка належного індикатора (1251комірку (0,11-0,14нМ). Базове і максимально стиDeltorphin II, 125I-FK33824 і 125I-DPDYN для d, m і мульоване зв'язування визначали у присутності і k, відповідно). Повне і неспецифічне зв'язування відсутності 3мкМ SNC80. Аналіз проводили на визначали у присутності і відсутності 10мкМ налоклітинах НЕК 293S, що стабільно експресували ксону. клоновані d-рецептори у трохи різних буферах Функціональні аналізи (50мМ Hepes, 20мМ NaOH, 200мМ NaCI, 1мМ Агоністичну активність сполук виміряють, виEDTA, 5мМ МgСІ2, рН 7,4, з доданням свіжих: 0,5% значаючи рівень, з яким рецепторний комплекс BSA, без DTT) і з GDP з кінцевою концентрацією сполук зв'язує GTP з G-априєїнами, до яких при3мкМ. єднані рецептори. В аналізі на зв'язування GTP, Аналіз даних GTP[g]35S з'єднували з випробуваними сполуками і Специфічне зв'язування обчислювали як TBмембранами з клітин HEK-293S, що експресують NS, і у присутності різних випробуваних сполук клоновані опіоїдні рецептори людини або з гоморепрезентували як % від контрольного специфічгенізованого мозку щура або миші. Агоністи стиного зв'язування. Значення IК50 і коефіцієнт Гілла мулюють зв'язування GTP[g]35S у цих мембранах. (Hill) (nН) для лігандів у видаленні специфічно зв'яЗначення EК50 і Еmах сполук визначали з кривих заних лігандів обчислювали з логарифмічної кризалежності від дози. Зсувом праворуч цих кривих вою або програмою, наприклад, Ligand GraphPad d-антагоністом налтриндолом перевіряли, чи опоPrism, SigmaPlot або ReceptorFit. Значення Κi обсередковується агоністична активність dчислювали з рівняння Чена-Пруссоффа. Середрецепторами. У функціональному аналізі dнє±стандартне відхилення для IК50, Ki і nН були рецептора людини, EК50 (низьку) виміряли, коли ці визначені для лігандів з щонайменше трьох кривих d-рецептора людини експресувались на низьких видалення. рівнях порівняно екс пресуванням при високих Таблиця містить біологічні дані деяких сполук EК50. Значення Еmах визначали відносно стандартвинаходу, досліджених описаними аналізами. ного d-агоніста SNC80, тобто більше 100% є сполуками з вищою ефективністю, ніж SNC80. Процедура для GTP мозку щура 19 Експерименти з насиченням рецептора Значення Kd радіолігандів визначають аналізом на зв'язування на клітинних мембранах з відповідними радіолігандуми при концентраціях (0,25)Kd (до 10 при наявності достатньої кількості лігандів). Специфічне зв'язування радіоліганду репрезентують як пкмоль/мг протеїну мембрани. Значення Kd і Вmax з окремих експериментів були отримані нелінійним співставленням специфічно зв'язаних (В) з нМ вільних радіолігандів (F) згідно з односторонньою моделлю. Визначення механо-алодинії тестом Фон Фрея (Фон Фрей) Тестування проводили між 08:00 і 16:00год. методом, описаним у [Chaplan et al. (1994)]. Щурів розміщували у плексигласових клітках з сітчастою підлогою, яка дозволяє доступ до лап, і залишали звикати на 10-15хвил. Зоною тесту була середня частини підошви задньої лапи, з униканням чутливих подушечок лапи. До лапи торкались декількома з серії 8 волосків фон Фрея, які мають жорсткість, що зростає логарифмічно (0,41, 0,69, 1,20, 2,04, 3,63, 5,50, 8,51, і 15,14г; Stoelting, III, USA). Волосок фон Фрея притискають кінчиком знизу через сітку перпендикулярно до підошви лапи з силою, достатньою для легкого згинання волоска, протягом приблизно 6-8хвил. Позитивною реакцією вважається різке відсмикування лапи. Відсмикування негайно після прибирання волоска також вважається позитивною реакцією. Переміщення вважається невизначеною реакцією, і у таких випадках стимулювання повторюють. Протокол тесту ***Тварин тестували через день після операції для груп, що отримали FCA. 50%-й поріг відсмикування визначали методом "вище-нижче" Диксона (Dixon, 1980). Тест починали з волоска жорсткістю 2,04г і стимулювання проводили згідно з послідовністю, зростаючою або убутковою. Якщо реакції відсмикання не було, застосовували більш сильний стимул, якщо реакція була застосовували слабший. Обчислення порогу цим методом потребує 6 реакцій поблизу 50%-го порогу, і відлік цих 6 реакцій починали з появи першої зміни реакції, наприклад, при перетинання першого порогу. У випадках потрапляння порогу за межі стимулів, призначаються значення 15,14 (нормальна чутливість) або 0,41 (максимальна алодинія), відповідно. Отриману сукупність позитивних і негативних реакцій табулювали, позначаючи: X - відсутність відсмикання; О - відсмикання, і 50%-й поріг відсмикання визначали інтерполяцією за формулою 50%-й поріг (г)=10(Xf+kd)/10000, де Xf - значеня жорсткості останнього волоска фон Фрея (у логарифмічних одиницях); k - табличне значеня [з Chaplan et al. (1994)] для сукупності позитивних/негативних реакцій; і d - середня різниця між стимулами (у логарифмічних одиницяхэ). Тут d=0,224. Поріг фон Фрей перераховують у %% від максимального можливого ефекту (% МРЕ) згідно з [Chaplan et al., 1994], за формулою % МРЕ=(поріг (г) при введенні ліків-поріг (г) алодинії´100)/контрольний поріг (г)-поріг (г) алодинії. 87146 20 Введення пацієнту випробуваної сполуки Щури отримували (ін'єкцією підшкірно, внутрішньочеревно або внутрішньовенно, або перорально) випробувану сполуку перед тестом фон Фрея з інтервалом між цими діями, залежним від випробуваної сполуки. Тест на контракцію Внутрішньочеревне введення оцтової кислоти викликає абдомінальні контракції у мишей, тіла яких при цьому зазнають характерного розтягання. Якщо введення аналгетика знижує частоту таких проявів, він вважається перспективним. Повний і типовий контракційний рефлекс реєструють, коли: тварина не рухається, нижня частина спини трохи опускається, спостерігається підошвений аспект обох лап. Згідно з цим аналізом, сполуки винаходу показали значне зниження контракційної реакції після перорального введення 1-100мкмоль/кг. (і) Приготування розчинів Оцтова кислота (АсОН): 120мкл оцтової кислоти додають до 19,88мл дистильованої води для отримання 20мл з кінцевою концентрацією 0,6% АсОН, після чого розчин перемішують і готують для ін'єкції. Сполука (ліки): кожну сполуку приготовляють і розчиняють у найпридатнішому носи за стандартними процедурами. (іі) Введення розчину пацієнту Сполуку (ліки) вводять перорально, внутрішньочеревно, підшкірно або внутрішньовенно дозою 10мл/кг (відповідно до середньої ваги миші) за 20, 30 або 40хвил. (залежно від класу сполуки і її характеристик) перед тестом. Коли сполуку вводять центрально: інтравентрикулярно або інтратекально, доза становить 5мкл. АсОН вводять внутрішньочеревно у двох місцях дозою 10мл/кг (відповідно до середньої ваги миші) безпосередньо перед тестом. (ііі) Тест Тварину (мишу) спостерігають протягом 20хвил. і відзначають кількість контракційних реакцій до кінця експерименту. Мишей тримають в окремих клітках з контактною підлогою. Звичайно спостерігають 4 миші: одну контрольну і трьох, що отримали ліки. Для ознак тривожності і подібних ознак ефективність визначали конкурентним тестом ГеллераЗайфтера (Geller-Seifter) для щурів. Для ознак шлунково-кишкового розладу ефективність може бути визначена в аналізі, описаному [Coutinho SV et al, у American Journal of Physiology - Gastrointestinal & Liver Physiology. 282(2):G30716, 2002 Feb], для щурів. Додаткові протоколи тестів in vivo Суб'єкти і утримання Незаражені самці щура Sprague Dawley (175200] г) утримувались у групах по 5 з контролем температури (22°С, вологість 40-70%, 12-годинна зміна світло/темрява). Експерименти проводили у світловій фазі циклу. Тварини отримували їжу і воду досхочу, і їх вбивали негайно після отримання даних. Зразок 21 87146 22 Тест сполуки (ліків) проводили на групах щуВ усіх сполуках (ліки) було встановлено рН від рів, що не отримували ніяких ліків, і на групах, які 6,5 до 7,5 і їх вводили у кількості 4мл/кг. Після отримували Е. соlі-ліпосахарид (LPS). Чотири грувведення сполуки (ліків) тварин повертали у їх пи отримували ін'єкцію LPS, одній з чотирьох груп клітки до початку тестів. вводили носій, а іншим - ліки з носієм. Другий наАналіз бір експериментів проводили на п'яти групах щуЗаписи були піддані ряду статистичних аналірів; всі вони не отримували LPS. Незаражена грузів і аналізів Фур'є для фільтрування (від 20 до па не приймала ніяких сполук (ліків) або носія; інші 24кГц) і обчислення бажаних параметрів. Дані бучотири групи отримували носій з ліками або без ли репрезентовані як середнє ± стандартне відхиних. Ці експерименти проводили для визначення лення. Статистичну значущість оцінювали Танксіолітичної або заспокоюючої дії ліків, тобто тестом для порівняння між неза-раженими щурами внеску у зниження USV. і щурами, що отримали LPS, і однонапрямним тесВведення LPS пацієнту том ANOVA і потім тестом (post-hoc) Данета Щурів витримували в експериментальній ла(Dunnett) множинного порівняння на ефективність бораторії 15-20хвил. перед лікуванням. Запалення ліків. Різниця між групами вважається значущою з викликали введенням LPS (ендотоксин граммінімальним значенням p£0,05. Експерименти понегативного серотипу бактерії Е. coli, 0111 :В4, вторювали мінімум двічі. Sigma). LPS (2,4мг) вводили ін'єкцією інтрацеребВизначення термічної гіпералгезії з звикорисро-інтравентрикулярно в об'ємі 10мл, використотанням підошвеного тесту Харгривза (Hargreaves) вуючи стандартні стереотаксичні хірургічні процеВведення пацієнту FCA або карагену дури під ізофлурановою анестезією. Шкіру між Повний ад'ювант Фройнда (Freund) (FCA): вухами зсували рострально і робили повздовжній SIGMA кат. # F 5881, Mycabacterium tuberculosis надріз довжиною приблизно 1см для оголення (H37Ra, ATCC 25177), 1мг/мл, вбитий теплом суповерхні черепа. Місце пункції визначали за кооршений, 0,85мл парафіну, 0,15мл манідмоноолеату динатами: 0,8мм за тем'ям, 1,5мм ліворуч до ламабо караген типу Lambda, IV(Cg): SIGMA кат. # Сбди (сагітальний шов) і 5мм нижче поверхні чере3889, (Желатин рослинний; Ірландський мох), па (вертикально) у бічному шлуночку. LPS вводили (1,0% розчин у NaCI). стерильної голкою з нержавіючої сталі (26-G 3/8) Ін'єкції робили шприцем Гамільтона (Hamilton) довжиною 5мм, приєднаною до шприца 100мл стерильною голкою 26G5/8". Щура розміщували у Гамільтона поліетиленовою трубкою (РЕ20; 10камері для анестезії ізофураном. Після досягнення 15см). 4-міліметровий стопер, зроблений з відрізку бажаного результату щура видаляли і укладали у голки (20-G), закріпляли силіконовим клеєм на черевне горизонтальне положення (грудинне). голці 26-G для забезпечення бажаної глибини Задню лапу ухоплю-вали і підшкірно вводили гол5мм. ку, між подушечками пальців 2 і 3 щоб досягти Після ін'єкції LPS голку залишали ще на 10сек. середини лапи (метатарсальної зони). Повільно у для забезпечення дифузії сполуки, потів видалялапу вводили 100мкл FCA або 100мкл розчину ли, надріз закривали, щура повертали у його клітку карагену і трохи стискали протягом 3-4сек. після давали йому відпочити протягом щонайменше видалення голки. 3,5год. перед тестом. Якщо тварина прокидалась під час цієї процеЕкспериментальна стимуляція вдуванням подури, її повертали в інгаляційну камеру до досягвітря нення бажаного результату. Щурів залишали у лабораторії після ін'єкцій Після цієї підпідошвеної ін'єкції, тварин залиLPS і сполуки (ліків). На час тесту щурів видаляли і шали прокинутись у їх клітках під наглядом. розміщували поза лабораторією. Щурів по одному При введенні FCA щура залишали на 48год., а приносили у лабораторію і розміщували у прозорій при введенні карагену - на 3год. для розвитку закоробці (9´9´18см), яку потім переносили у звукопального процесу. Вранці щурів переносили до лабораторії (у клітках) і залишали щонайменше на підсилюючу вентильовану камеру (62´35´46см, 30хвил. для звикання. BRS/LVE, Div. Tech-Serv Inc). Повітря вдували чеМісце тесту рез вихідну повітряну форсунку діаметром 0,32см Теплове стимулювання прикладали до центру під контролем системи AirStim (San Diego поверхні підошви, між подушечками. Місце тесту Intruments), здатної вдувати повітря порціями тримає контактувати з склом, без сечі або фекалій між валістю 0,2сек. з постійною інтенсивністю і частоними, для забезпечення нормальної теплопередатою 1 вдування за 10сек. Виконували максимум 10 чі від скла до шкіри. вдувань або до початку вокалізації. Реєстрацію Підошвений апарат складається з коробки з починали з першим вдуванням. скляною кришкою/платформою, температуру Експерименти з записом ультазвуків скляної поверхні підтримують на рівні 30°С за доВокалізації записували протягом 10хвил. мікпомогою механізму внутрішнього зворотного зв'язрофонами (G.R.A.S., Sound and Vibrations, ку. Під цією скляною платформою на рухомому Vedbaek, Denmark), встановленими у кожній камекронштейні була встановлена лампа, a під нею рі і контрольованими програмою (LMS CADA-X дзеркало для спрямовування світла під лапи щура 3,5В, Data Acquisition Monitor, Troy, Michigan). Були через отвір діаметром приблизно 2мм. Після вмизаписані частоти від 0 до 32000Гц, записи зберігакання світла автоматичні датчики вимикають світли і аналізували тією ж програмою (LMS CADA-X ло при прибиранні лапи; якщо щур прибирає лапу, 3,5В, Time Data Processing Monitor i UPA (User світло вимикається через 20,48сек. для уникнення Programming and Analysis)). травмування лапи. Експериментатор може також Сполуки (Ліки) 23 87146 24 вимкнути світло у будь-який момент. Таймер ре- тварина знаходиться у такому положенні, що єструє час, коли світло є включеним. лапа не контактує безпосередньо з склом (лапа Флюксметр виміряє світловий потік лежить на хвості); (флюкс/см2), який має становити приблизно 97-98; - лапа тварини з'являється синіє в результаті потік можна коригувати, але не під час експеримепоганої ін'єкції; у такому тварину усувають повніснту. тю (з початку). Часові співвідношення При наявності сечі або екскрементів тварину Експеримент можна проводити через різні видаляють, поверхню скла чисто витирають і твапроміжки часу після викликання запалення. Гіперрину повертають. Якщо тварина спить або виявалгезію виміряють через 48год. після ін'єкції FCA ляє напружену нерухомість, експериментатор моабо 3год. після ін'єкції карагену. же обережно пересунути коробку або зробити рухи Процедура тесту рукою перед коробкою, щоб привернути увагу. Незаражені щури: Для отримання кривої заТварини мають знаходитись під уважним наглядом лежності реакції від дози одну групу з 7 щурів випротягом тесту. користовували як контрольну; їх анестезували Повторні тести разом з іншими 28 щурами, але не вводили нічого Якщо на будь-якій стадії експерименту експеін'єкцією. Тестування цієї групи можна проводити риментатор не має впевненості у тому, що прибидо або негайно після експерименту, спричиняючи рання лапи є реакцією на нагрівання, тварина момінімальний стрес. Щурів розміщували в індивідуже бути піддана повторному тесту через 5-8хвил. Це може бути викликано несподіваним рухом тваальних плексигласових коробках (14´21´9см) на рин або сечовиділенням, або дефекацією під час підошвеному пристрої; їх залишали на 30хвил. для стимулювання. звикання, світло розміщували під місцем тесту і Прийнятні реакції вмикали, латентність прибирання лапи реєструваРеакцією на нагрівання можна вважати: ли. Через 5-8хвил. (щоб дозволити температурі - прибирання лапи з скла (часто з подальшим шкіри нормалізуватись) проводили друге вимірюоблизуванням лапи), вання і щурів повертали до їх кліток. - бічні рухи тіла (у бік від стимульованої лапи), Основні дані: іншим 28 щурам (розділеним 4 - прибирання пальців з скла, групи) ін'єкцією вводили FCA (або караген) розмі- прибирання з скла центральної частини піщували в індивідуальних коробках на машині і дошви запаленої лапи. залишали звикати на 30хвил. Експериментатор Аналіз має визначити рівень запалення лапи і знебарвДані були репрезентовані як середлення. Джерело тепла розміщували під місцем нє±стандартне відхилення. Статистичну значутесту і реєстрували латентність прибирання лапи щість оцінювали Т-тестом для порівняння між кондвома вимірюваннями. Наявність гіпералгезії трольними і запаленими щурами, і однонапрямним встановлюють, порівнюючи основні дані з даними тестом ANOVA і потім тестом (post-hoc) Данета для незаражених щурів. (Dunnett) множинного порівняння на ефективність Тести після введення ліків: після встановлення ліків. Різниця між групами вважається значущою гіпералгезії, щурам ін'єкцією вводили випробувані мінімальним значенням p£0,05. Експерименти посполуки. Кожну сполуку приготовляли і розчиняли у найбільш придатному носії згідно з стандартнивторювали мінімум двічі. ми процедурам. Спосіб введення, дози, об'єм і час Метаболічні і фармакокінетичні властивості тесту після ін'єкції є специфічними для цієї сполуки Було несподівано виявлено, що метаболічні і (або класу сполук). Після введення сполук через фармакокінетичні властивості сполук поліпшують20-30хвил. після ін'єкції, щурів розміщували у піся внаслідок заміщення флуором нижнього бензидошвеному апараті і залишали до появи дії ліків. лу бензилпіперазинільного компонента формули І. Через 60хвил. або більше після ін'єкції, щурів пеВ одному з втілень було виявлено, що деякі реакреносили до їх кліток разом з сусідами по клітці. тивні метаболіти знижуються за рівнем або видаЩурів завжди повертати у їх первісні клітки разом ляються з сполук винаходу. В іншому втіленні дез сусідами для мінімізації стресу і відновлення які сполуки винаходу показали поліпшену соціальної структури у групі. Через 30хвил. щурів біозасвоюваність, що може бути результатом їх розміщували на підошвеній машині, залишали на слабкої спорідненості з 2D6- і 3А4-цитохромом 30 хвилю звикнути і проводили тести, як це було Р450. Наведені далі дані підтверджують ці властиописано вище, виконуючи два вимірювання. вості сполук. Критерії для тесту Мікросомні інкубації Тварини мають бути спокійними але уважниСполуку винаходу (початкова концентрація ми, у правильному положення, без сечі або екс10мкМ) інкубували індивідуально з мікросомами крементів між лапами і склом машини. Тест не печінки щура (0,5мг/мл протеїну) у буфері з 0,1Μ проводять, якщо: ΚΗ2ΡΟ4 (рН 7,4) і 5мМ МgСІ2 і 5мМ захоплюючого - тварина рухається, нюхає, чистить себе і реагента (глютатіон(GSH), N-ацетилцистеїн (NAC), знайомиться з довкіллям, або CH3ONH2) протягом 60хвил. при 37°С. Реакції - тварина спить, були ініційовані доданням NADPH (1мМ) і їх при- тварина виявляє явні ознаки стресу (напрупиняли доданням такого ж об'єму підкислювана жена нерухомість, вокалізації, вуха у положенні (0,1% мурашина кислота вацетонітрилі). лежачи), якщо вони не є можливим побічним реІнкубації гепатоцитів зультатом дії сполуки і їх не можна уникнути. Сполуку винаходу (початкова концентрація 10мкМ) інкубували індивідуально з свіжими гепа 25 87146 26 тоцитами щура (Sprague Dawley) і кріозбереженого лінії відліку. Для визначення лінії відліку були відібрані три 20-хвилинні зразки, тваринам ін'єкцією собаки (Beagle) (1´106клітин/мл) при рН 7,4 і 37°С внутрішньочеревно вводили носій або сполуки і протягом 1год. Гепатоцитна інкубаційна суміш місзразки збирали протягом 5год. Програму парадигтила середовище Ε Вільямса з 25мМ НЕРЕР, 1%ми стресу починали через 20хвил. після введення м розчином ITS-G (Life Technologies, Cat. No сполук. Зразки негайно уприскували у систему 41400-045), 10мМ НЕРЕР (рН 7,4), і 2мМ LВЕРХ для аналізу на концентрації моно аміну. глютаміну. Інкубації припиняли доданням такого ж Концентрації нейротрансмітерів у 3 зразках, взяоб'єму підкислювана (0,1% мурашина кислота в тих перед введенням пацієнту сполук/носія усереацетонітрилі). днювали і використовували як еталон (100%). Аналіз РХ-МС Концентрації нейротрансмітерів у подальших мікро Після осадження протеїну над осадові рідини діалізатах репрезентували як %% від еталону. зразків були аналізовані на метаболіти повноскаПроцедура стресу нувальними РХ-МС. Були отримані дані про молеДля цих процедур були використані стандартні кулярну масу кожного метаболіту. Були аналізовабокси пасивного уникнення, обладнані засобами ні фрагментаційні картини від додаткових світла, тону і електричних ударів (Med Associates, вимірювань РХ-МС/МС для визначення структур Inc). Бокси розміщували у звукопідсилюючих камепервісних метаболітів. рах. Стресову парадигму проводили протягом 1 Інструменти: дня. Тварин акліматизували у камерах протягом ВЕРХ HP 1100 ВЕРХ System (Hewlett 2год., потім протягом 6хвил. піддавали у послідовPackard, D-76337 Waldbronn, Germany) ності дії світла, електричному удару на лапах МС LCQ (Finnigan Corporation, 355 River (0,5сек. 1,5мА, 10 ударів). "Спокійну" групу у камеOaks Parkway, San Jose, CA) рах піддавали дії світла але без електричних удаУмови мас-спектрографії (МС: LCQ): рів. Через 40хвил. тварин повторно піддавали дії Напруга джерела 4,5кВ світла, без електричних ударів. Темп, капілярів 180°С Введення ліків Потік газу 80 Всі сполуки розчиняли у стерильній дистильоДопоміжний потік газу 5 ваній воді (носій) і вводили внутрішньочеревно за Тип джерела ЕРІ 20хвил. до процедури стресу. Режим іонізації Позитивний ВЕРХ і електрохімічне виявлення. Умови ВЕРХ: Система ВЕРХ складається з насосу 5041, деКолонка Phenomenex Synergi MAXтектора Model 5200A Coulochem II, колонки MDRP, 4m, 2,0´150мм 150 3´150мм, амперметричної комірки model 5041 (Phenomenex, Torrance, CA) (всі від ЕРА Іnс) і іжектора (від BAS Іпс). Мобільна Мобільна фаза A=0,1% мурашина кислота у фаза: 75мМ Na2HPO4, 25мМ EDTA, 1,7мМ 1воді, В=ACN октансульфонова кислота, 100мкл триетиламіну, Потік 0,2мл/хвил. 10%-й ацетонітрил, рН 3,0. Потенціал - +0,65В, Температура 45°С потік з витратою 0,3мл/хвил. Дані отримують базоВиявлення Мас-спектрометр LCQ ваною на ПК прийомно-аналітичною системою Метод градієнта: (комп'ютер 501 і програмне забезпечення A/D, Час А В ЕРА, Іпс) з інтегрованим графічним програмним 0 90 10 забезпеченням для подальшого аналізу. 30 40 60 Групи з 6-8 щурів з інтрацеребральними мік30,1 10 90 родіалізними зондами у медіальній префронталь33 10 90 ній корі (де нейрохімічний сигнал є найсильнішим) 33,1 90 10 піддавали кондиціонуванню, описаному вище, і 40 90 10 спостерігали підвищення норепіферину і допаміну Результати тестів у тварин, що отримували носій. Деякі сполуки стійПервісними спостереженими шляхами біотрако блокували підвищення норепіферину і допамінсформації сполук були N-деетилування, Nну. дееалкілувагння і гідроксилування. Для сполук Геллер-Зіфтер - метод моделі тривожності винаходу з заміщеним флуором бензилУ тесті на конфліктність голодних тварин напіперазинільним компонентом продуктів приєдвчали натискати важіль для отримання їжі у станнання глютатіону на бензолі в інкубатах гепадартній оперантній камері у двох режимах. Згідно з тоцитів щура не було виявлено, але деякі продукпершим (не подавлений компонент) їжу дають у ти приєднання глютатіону на бензолі були виявлесередньому після 17 натискань важеля (програма ні у цих інкубатах для подібних сполук без заміщепідсилення VR17). Згідно з другим режимом (поного флуором бензильного кільця. давлений компонент), яка супроводжується світМетоди мікродіалізу in vivo ловим спалахом в оперантній камері, їжу також Процедура дають у середньому після 17 натискань важеля, Щурів рандомізовано розділили на 8 груп: споале супроводжують електричним ударом на підлокійні з носієм, з носієм під стресом, спокійні з ліказі камери згідно з окремою процедурою VR17. ми, з ліками під стресом. У мозок за 2год. перед Денні сеанси включають 5 почергових виконань експериментом були імплантовані діалізні зогди компонентів кожного типу: подавлені (3хвил.) і не (СМА/12, мембрана 4мм для mPFC) і заливались подавлені (3хвил.). Кількість натискань важеля у штучною CSF (aCSF, СМА Microdialysis AB) потоподавленому компоненті була нижчою порівняно з ком 1,1мл/хвил. протягом 2год. для стабілізації 27 87146 28 не подавленим компонентом. Антитривожні агенфільтруванням, обробляють водним гідроксидом ти, наприклад, діазепам, підвищували кількість натрію (2М) і екстрагують етилацетатом. Органічні натискань у подавленому компоненті, але не екстракти сушать (Na2SO4), фільтрують і концентвпливали на кількість натискань у не подавленому рують, отримуючи 1,986г інтермедіату 4b. 1Н ЯМР компоненті. Деякі сполуки винаходу мали анксіолі(400МГц, CDCI3) dΗ 1,11 (br s, 3H), 1,25 (br s, 3H), тичний профіль. 2,37 (br s, 4H), 2,91 (t, J=5Гц, 4H), 3,23 (br s, 2H), Далі наведено приклади приготування, очи3,52 (br s, 2H), 4,38 (s, 1H), 7,31-7,33 (m, 2H), 7,41щення, аналізу і біологічних тестів, які ілюструють 7,43 (m, 2H), 7,47 (t, J=8Гц, 1H), 7,75-7,79 (m, 1H), винахід, не обмежуючи його об'єму. 8,06-8,09 (m, 1H), 8,30-8,32 (m, 1H). Інтермедіат 1: 4-йодо-N,N-діетилбензамід Хіральну чистоту визначають ВЕРХ при таких До суміші 4-йодобензоїлхлориду (75г) у 500мл умовах: СН2СІ2 додають суміш Et3N (50мл) і Et2NH (100мл) Колонка Chiralpack AD (Daicel Chemical при 0°С. Отриману реакційну суміш гріють при Industries) кімнатній температурі 1год. і потім промивають Низький потік - 1мл/хвил. насиченим хлоридом амонію. Органічні екстракти Час - 30хвил. при 25°С сушать (Na2SO4), фільтрують і концентрують. ЗаІзократний 15%-й етанол (з 0,1% за об'ємом) лишок рекристалізують з гарячих гексанів і отридіетиламіну), 85%-і гексани (з 0,1% (за об'ємом) мують 80г інтермедіату 1. діетиламіну) Інтермедіат 2: 4-[гідрокси(3-нітрофеніл)метил]Час ретенції молекули - 20хвил. N,N-діетилбензамід Інтермедіат 4а: N,N-діетил-4-[(S)-(3N,N-діетил-4-йодобензамід (5,0г, 16ммоль) нітрофеніл)(1-піперазиніл)метил]бензамід розчиняють у ТГФ (150мл) і охолоджують до -78°С (S)-енантіомерний інтермедіат 4а можна під нітрогеном. Краплями протягом 10хвил. при отримати процедурою розчинення з ди-р-толуоїл(65-78)°С додають n-BuLi (15мл, 1,07М розчин у 1-виннокам'яною кислотою. гексані, 16ммоль). Розчин канюлюють у 3Сполука 1: 4-{(S)-(3-амінофеніл)[4-(4нітробензальдегід (2,4г, 16ммоль) у толуолі/ТГФ флуорбензил)піперазин-1-іл]метил}-N,N(прибл. 1:1, 100мл) при -78°С. Через 30хвил. додіетилбензамід дають NH4CI (водн.). Після концентрування in vacuo, екстрагування EtOAc/водою, сушіння (MgSO4) і випарювання органічної фази, залишок очищають хроматографією на кремнеземі (0-75% EtOAc/гептан) і отримують інтермедіат 2 (2,6г, 50%), 1Н ЯМР (400МГц, CDCI3) dΗ 1,0-1,3 (m, 6H), 3,2 (m, 2H), 3,5 (m, 2H), 5,90 (s, 1H), 7,30-7,40 (m, 4H), 7,50 (m, 1H), 7,70 (d, J=8Гц, 1H), 8,12 (m, 1H), 8,28 (m, 1Η). Інтермедіат 3: N,N-діетил-4-[(3-нітрофеніл)(1піперазиніл)метил]бензамід До розчину спиртового інтермедіату 2 (10,01г, 30,5ммоль) у ДХМ (200мл) додають тіонілбромід До розчину Інтермедіату 4а (467мг) у 1,2(2,58мл, 33,6ммоль). Через 1год. при кімнатній дихлоретані (13мл) додають 4-флуорбензальдегід температурі реакцію промивають насиченим вод(252мкл; 2екв.) і триацетоксиборгідрид натрію ним бікарбонатом натрію (100мл) і органічний шар (498мг; 2екв.). Реакцію перемішують при кімнатній відділяють. Водний шар промивають ДХМ температурі під нітрогеном 18год. і концентрують. (3´100мл) і об'єднані органічні екстракти сушать Додають насичений бікарбонат натрію і водний (Na2SO4), фільтрують і концентрують. розчин екстрагують трьома порціями ДХМ і об'єдСирий бензилбромід розчиняють в ацетонітнану органіку сушать над безводним сульфатом рилі (350мл) і додають піперазин (10,5г, натрію, фільтрують і концентрують. Сполуку роз122ммоль). Після нагрівання протягом 1год. при чиняють у суміші етанолу, ТГФ, води і насиченого 65°С реакцію промивають насиченим хлоридом хлориду амонію (4мл; відношення 4:2:1:1 за об'ємом). Додають наночастки заліза (тричі на кінчику амонію/етилацетатом і органічний шар відділяють. спатули) і розчин нагрівають при 150°С протягом Водний шар екстрагують етилацетатом (3´100мл) і 10хвил. у мікрохвильовій печі. Отриману суміш об'єднані органічні екстракти сушать (Na2SO4), охолоджують, фільтрують через броунмілерит і фільтрують і концентрують, отримуючи рацемічконцентрують. Залишок очищають флешний інтермедіат 3. хроматографією на силікагелі, з елюентом з градіІнтермедіат 4b: N,N-діетил-4-[(R)-(3єнтом від 1% до 5% МеОН у ДХМ. Отриманий нітрофеніл)(1-піперазиніл)метил]бензамід продукт розчиняють у ДХМ з 1,2мл 1М НСІ в етері. Рацемічний інтермедіат 3 розчиняють в етаРозчинник видаляють і продукт ізолюють як гідронолі (150мл) і додають ди-р-толуоїл-Dхлоридну сіль, отримуючи Сполуку 1 (164мг, 30% виннокам'яну кислоту (11,79г, 1екв.). Продукт осавихід) як безбарвну тверду речовину. Чистота джується протягом 12год. Тверду речовину зби(ВЕРХ) вище 99%; Оптична чистота (хіральна рають фільтруванням і розчиняють в етанолі під ВЕРХ) вище 99%; 1Н ЯМР (400МГц, CD3OD), 1,08 зворотним холодильником до розчинення всієї (t, J=6,5Гц, 3H), 1,21 (t, J=6,5Гц, 3H), 3,20-3,26 (m, твердої речовини (прибл. 1200мл етанолу). Після 4H), 3,51-3,54 (m, 6H), 4,43 (s, 2H), 7,19-7,23 (m, охолодження тверду речовину збирають фільтру2Н), 7,34 (d, J=8,0Гц, 1H), 7,40 (d, J=8,0Гц, 2H), ванням і рекристалізують двічі, потім збирають 29 87146 30 7,54-7,63 (m, 3H), 7,70-7,82 (m, 4H). Отримано: С, Сполука 3: 4-[(R)-(3-амінофеніл)[4-[(254,63; Η, 6,49; Ν, 8,68. флуорфеніл)метил]-1-піперазиніл]метил]-Ν,Νдіетилбензамід C29H36N4OF´4,1НСІ´0,8Η2Ο´0,1С4Н10О має С, 57,67; Η, 6,51 ;Ν, 8,67%. Сполука 2: 4-{(R)-(3-амінофеніл)[4-(4флуорбензил)піперазин-1-іл]метил}-N,Nдіетилбензамід До розчину Інтермедіату 4b (5,790г, 14,6ммоль) у 1,2-дихлоретані (60мл) додають 4флуорбензальдегід (2,04мл, 19,0ммоль) і триацетоксиборгідрид натрію (4,02г, 19,0ммоль). Через 20год. при кімнатній температурі реакцію гасять водним бікарбонатом натрію і органічний шар розділяють. Водний шар екстрагують ДХМ (3´100мл) і об'єднані органічні екстракти сушать (Nа2SО4), фільтрують і концентрують. Залишок очищають флеш-хроматографією з елюентом 30% до 50% ацетону у гексанах, отримуючи безбарвну піну (5,285г, 71%), тобто нітроінтермедіат (5,285г, 10,4ммоль), який розчиняють у суміші етанолу, ТГФ, воді і водного насиченого хлориду (4:2:1:1, за об'ємом) (100мл) і додають гранули заліза (0,63мг, 11,5ммоль). Реакцію нагрівають під зворотним холодильником і періодично додають гранули заліза. Через 24год. (90°С) реакцію охолоджують до кімнатної температури і фільтрують через броунмілерит і концентрують. До залишку додають водний бікарбонат натрію і ДХМ. Органічний шар відділяють і водний шар екстрагують ДХМ (3´100мл) і об'єднані органічні екстракти сушать (Na2SO4), фільтрують і концентрують. Продукт очищають на силікагелі з елюентом від 1% до 5% метанолу у ДХМ, отримуючи Сполуку 2 (3,505г) як блідожовту піну. Нечистий матеріал додатково отримують флеш-хроматографію і очищають другою флешхроматографією з елюентом 100% етилацетат до 5% метанолу в етилацетаті, отримуючи ще 0,949г Сполуки 2. Отримано об'єднаного матеріалу 4,454г (вихід 90%). Чистота (ВЕРХ) вище 99%; оптична чистота (хіральна ВЕРХ) вище 99%; 1Н ЯМР (400МГц, CD3OD), 1,08 (t, J=6,5Гц, 3H), 1,21 (t, J=6,5Гц, 3H), 3,20-3,26 (m, 4H), 3,51-3,54 (m, 6H), 4,43 (s, 2H), 7,19-7,23 (m, 2H), 7,34 (d, J=8,0Гц, 1Н), 7,40 (d, J=8,0Гц, 2Н), 7,54-7,63 (m, 3H), 7,70-7,82 (m, 4Н). Отримано: С, 54,00; Η, 6,34; Ν, 8,47. C29H35FN4O´4,7НСІ´0,2С4Н10О´0,1Η2Ο має С, 54,02; Η, 6,37; Ν, 8,46%. До розчину Інтермедіату 4b (298мг, 0,752ммоль) у 1,2-дихлоретані (8,5мл) додають 2флуорбензальдегід (160мг, 1,503ммоль, 2екв.) і триацетоксиборгідрид натрію (319мг, 1,503ммоль, 2екв.). Реакцію перемішують при кімнатній температурі під нітрогеном протягом 18год. і концентрують. Додають насичений бікарбонат натрію і водний розчин екстрагують трьома порціями ДХМ і об'єднану органіку сушать над безводним сульфатом натрію, фільтрують і концентрують. Сполуку розчиняють у суміші етанолу, ТГФ, води і насиченого хлориду амонію (3мл; відношення 4:2:1:1, за об'ємом). Додають наночастки заліза (тричі на кінчику спатули) і розчин нагрівають при 150°С 10хвил. у мікрохвильовій печі. Отриману суміш охолоджують, фільтрують через броунмілерит і концентрують. Сирий продукт розчиняють у СН2СІ2 і промивають водою. Органічний шар відділяють і водний, шар екстрагують ДХМ. Об'єднані органічні екстракти сушать (Na2SO4), фільтрують і концентрують. Продукт очищають зворотно-фазовою ВЕРХ (градієнт 5-50% CH3CN у Н2О з 0,1% ТФК), отримуючи Сполуку 3 (0,28г, 46%) як сіль ТФК, яку ліофілізують з CH3CN/H2O, отримуючи блідожовтий порошок. 1Н ЯМР (400МГц, CD3OD) 1,08 (t, J=6,6Гц, 3H), 1,22 (t, J=6,6Гц, 3H), 2,39 (br s, 2H), 3,02 (br s, 2H), 3,18-3,38 (m, 4H), 3,43 (br s, 2H), 3,52 (q, J=6,8Гц, 2H), 4,43 (s, 2H), 4,53 (s, 1H), 7,09 (dt, J=2,3, 6,8Гц, 1H), 7,24-7,30 (m, 1H), 7,30-7,41 (m, 6H), 7,52-7,60 (m, 4H). Обчислення для С29Н35FN4О´2,8ТФК´0,4Η2Ο: С, 51,88; Η, 4,86; Ν, 6,99. Отримано: С, 51,89; Η, 4,89; Ν, 6,97%. МС (обчисл.): 475,3 (МН+), МС. (отримано): 475,2 (МН+). ВЕРХ: k': 2,35; чистота: вище 99% (215нм), вище 99% (254нм), вище 99% (280нм). Умови ВЕРХ: Zorbax С-18, градієнт 10-95% В, потік 1мл/хвил., 25°С, А: 0,1% TFA in H2O, В: 0,1% ТФК у MeCN. Ротація: [a]16D=-8,91 (с=1,179, МеОН). Сполука 4: 4-[(R)-(3-амінофеніл)[4-[(3флуорфеніл)метил]-1-піперазиніл]метил]-Ν,Νдіетилбензамід 31 87146 32 і розчин нагрівають при 150°С 10хвил. у мікрохвильовій печі. Отриману суміш охолоджують, фільтрують через броунмілерит і концентрують. Отриманий продукт розчиняють у СН2СІ2 і промивають водою. Органічний шар відділяють і водний шар екстрагують ДХМ. Об'єднані органічні екстракти сушать (Na2SO4), фільтрують і концентрують. Продукт очищають зворотно-фазовою ВЕРХ (градієнт 5-50% CH3CN у Н2О з 0,1% ТФК), отримуючи Сполуку 4 (0,375г, 65%) як сіль ТФК, яку ліофілізують з CH3CN/H2O, отримуючи блідожовтий порошок. 1Н ЯМР (400МГц, CD3OD) 1,08 (t, J=6,4Гц, 3H), 1,21 (t, J=6,8Гц, 3H), 2,38 (br s, 2H), 3,00 (br s, 2H), 3,163,28 (m, 4H), 3,40 (br s, 2H), 3,51 (q, J=6,8Гц, 2H), До розчину Інтермедіату 4b (281мг, 4,37 (s, 2H), 4,56 (s, 1H), 7,18 (ddd, J=1,2, 2,3, 0,709ммоль) у 1,2-дихлоретані (8мл) додають 37,8Гц, 1H), 7,24 (ddd, J=1,0, 2,7, 8,8Гц, 1H), 7,28флуорбензальдегід (180мг, 1,417ммоль, 2екв.) і 7,38 (m, 4H), 7,55 (d, J=8,2Гц, 2H). Обчислено для триацетоксиборгідрид натрію (300мг, 1,417ммоль, C29H35FN4O´2,7ТФК´1,1Н2О: С, 51,50; Η, 5,01; Ν, 2екв.). Реакцію перемішують при кімнатній темпе6,98. Отримано: С, 51,52; Η, 5,01; Ν, 6,87%. МС ратурі під нітрогеном 18год. і концентрують. Дода(обчисл): 475,3 (ΜΗ+), M.S. (отримано): 475,2 ють насичений бікарбонат натрію і водний, розчин (МН+). ВЕРХ: k': 2,43; Чистота: вище 99% (215нм), екстрагують трьома порціями ДХМ і об'єднану орвище 99% (254нм), вище 99% (280нм). Умови ганіку сушать над безводним сульфатом натрію, ВЕРХ: Zorbax С-18, градієнт 10-95% В, потік фільтрують і концентрують. Продукт розчиняють у 1мл/хвил., 25°С, А: 0,1% ТФК у Н2О, В: 0,1% ТФК у суміші етанолу, ТГФ, води і насиченого хлориду MeCN. Ротація: [a]1βD=-8,94 (с=1,04, МеОН). амонію (3мл; відношення 4:2:1:1 за об'ємом). Додають наночастки заліза (тричі на кінчику спатули) Комп’ютерна верстка О. Гапоненко Підписне Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюDiarylmethyl piperazine derivatives, preparation thereof and pharmaceutical composition based thereon
Автори англійськоюBrown William, Griffin Andrew, Hudzik Thomas, Maciag Carla, Smagin Gennady, Walpole Christopher
Назва патенту російськоюПроизводные диарилметилпиперазина, способ их получения и фармацевтическая композиция на их основе
Автори російськоюБраун Вильям, Гриффин Эндрю, Гудзик Томас, Масяг Карла, Смагин Геннадий, Волпоул Кристофер
МПК / Мітки
МПК: A61P 25/22, A61P 25/04, C07D 295/155, A61K 31/495, A61P 25/24
Мітки: основі, похідні, фармацевтична, композиція, одержання, діарилметилпіперазину, спосіб
Код посилання
<a href="https://ua.patents.su/16-87146-pokhidni-diarilmetilpiperazinu-sposib-kh-oderzhannya-ta-farmacevtichna-kompoziciya-na-kh-osnovi.html" target="_blank" rel="follow" title="База патентів України">Похідні діарилметилпіперазину, спосіб їх одержання та фармацевтична композиція на їх основі</a>
Попередній патент: Тонкошаровий відстійник
Наступний патент: Спосіб настройки системи скидання тиску газів наддування з паливних баків літального апарата
Випадковий патент: Вагон для перевезення бензину та інших рідин