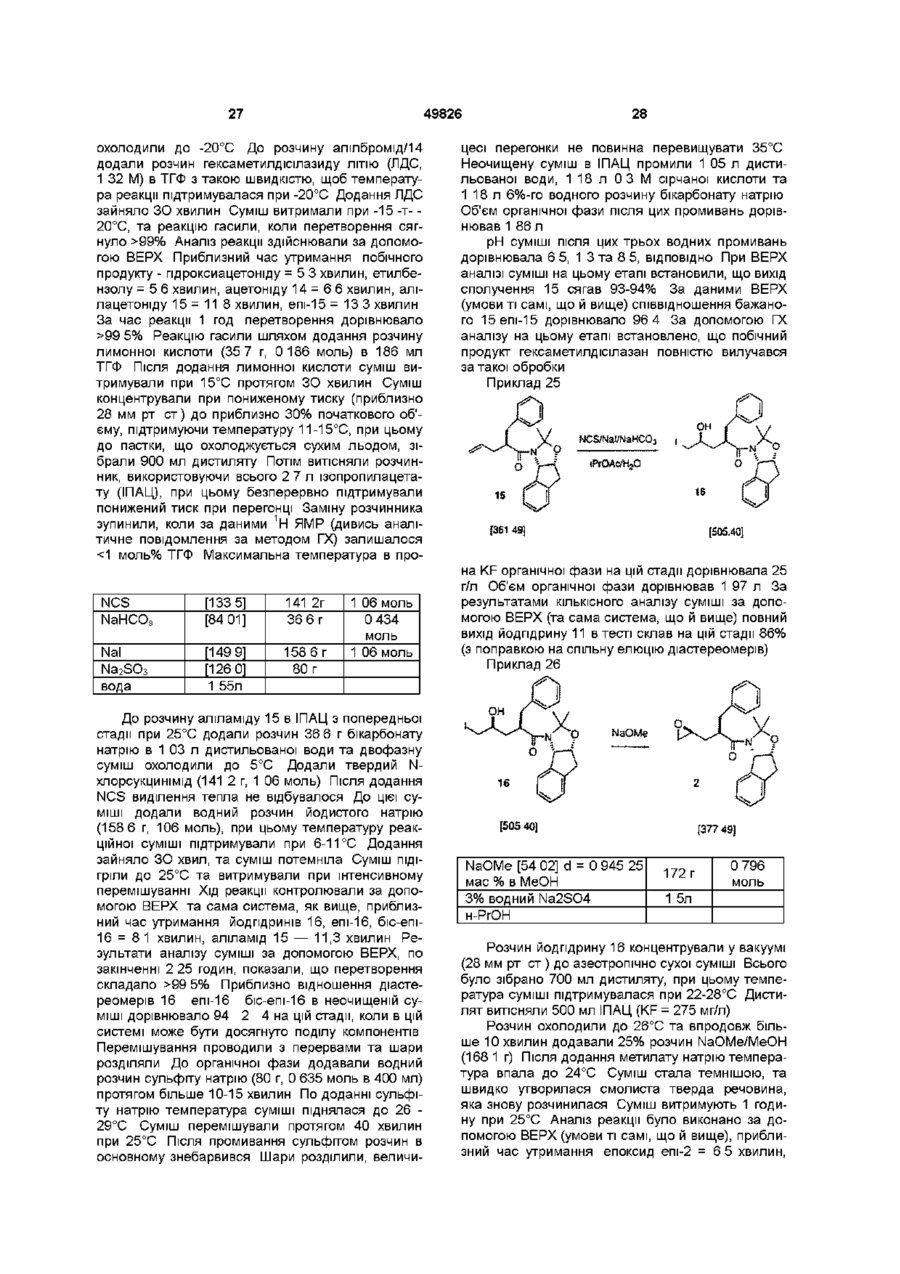
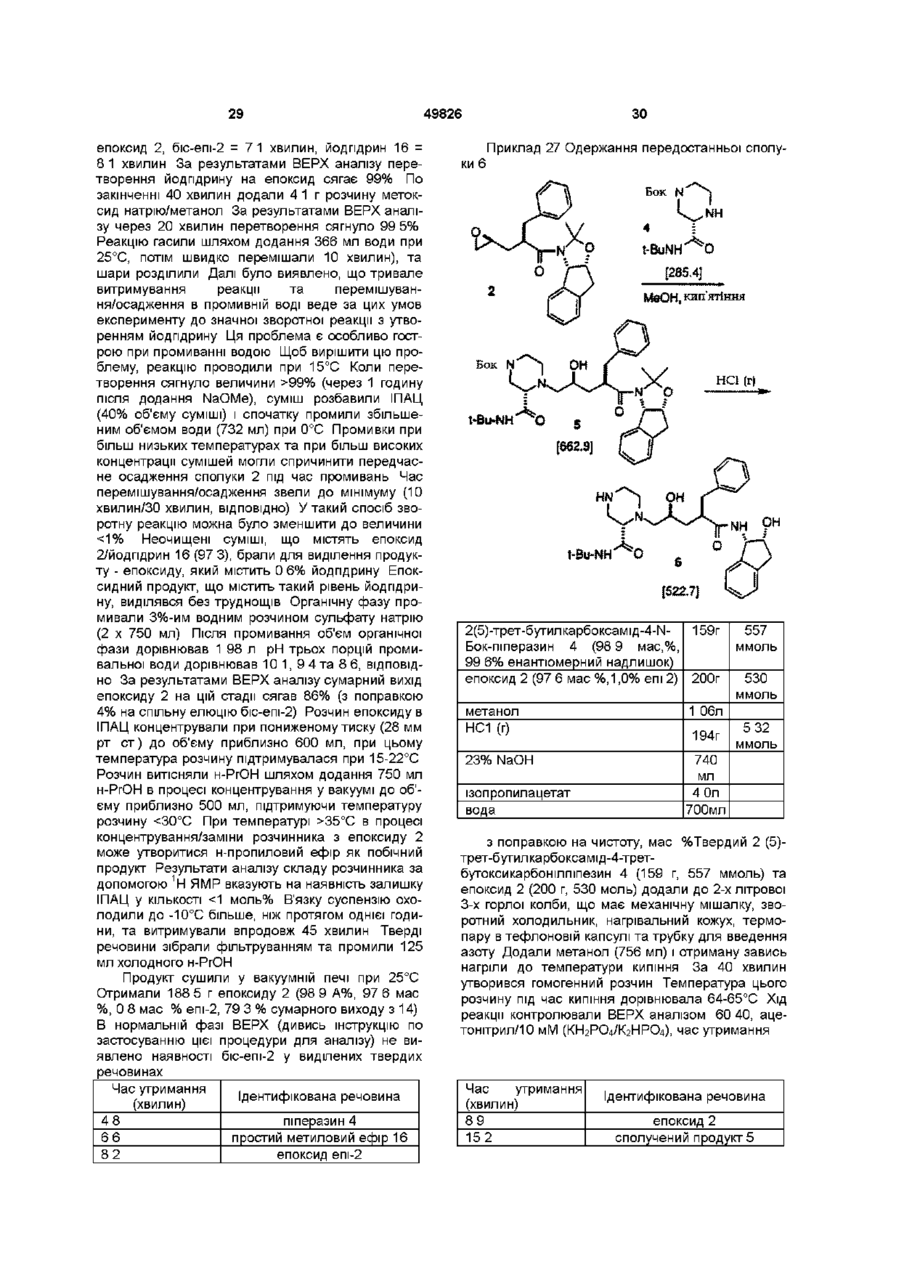
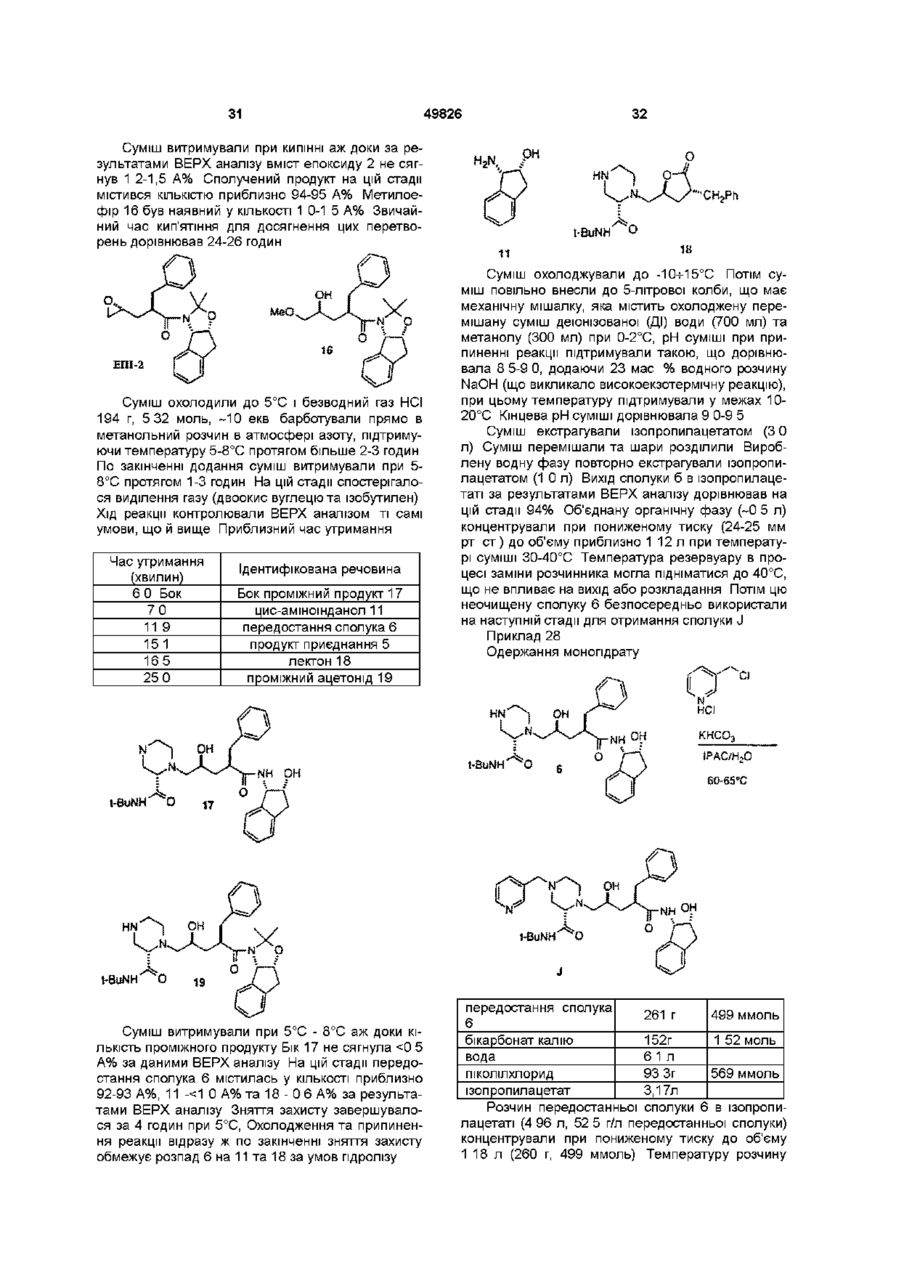
Спосіб одержання інгібітору протеази віл з 2(s)-4-піколіл-2-піперазин-трет-бутилкарбоксаміду
Номер патенту: 49826
Опубліковано: 15.10.2002
Автори: Аскін Девід, Волант Ральф П., Єнг Кан К., Рідер Пол
Формула / Реферат
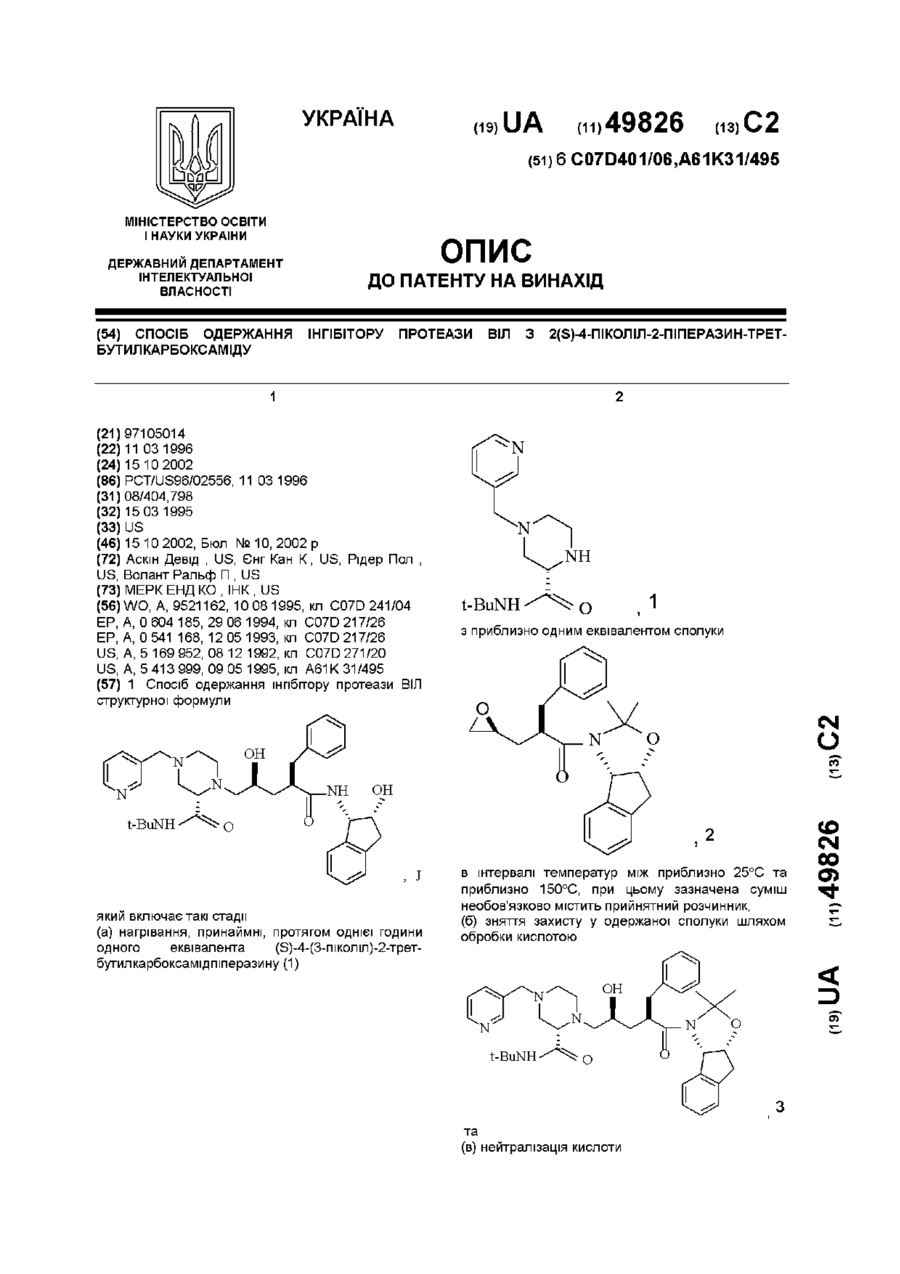
1. Спосіб одержання інгібітору протеази ВІЛ структурної формули
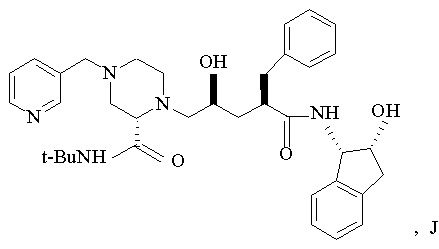
який включає такі стадії:
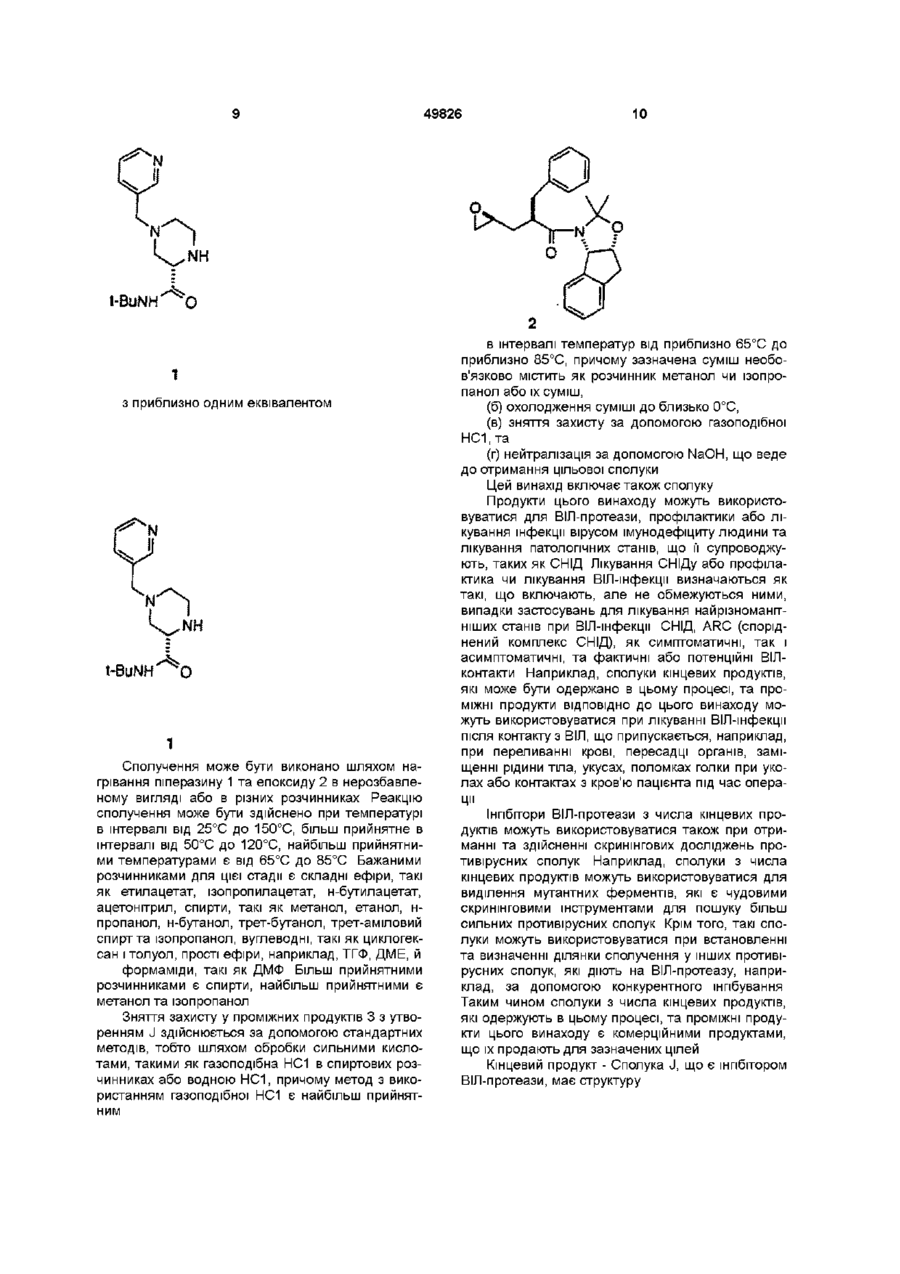
(а) нагрівання, принаймні, протягом однієї години одного еквівалента (S)-4-(3-піколіл)-2-трет-бутилкарбоксамідпіперазину (1)
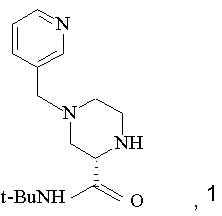
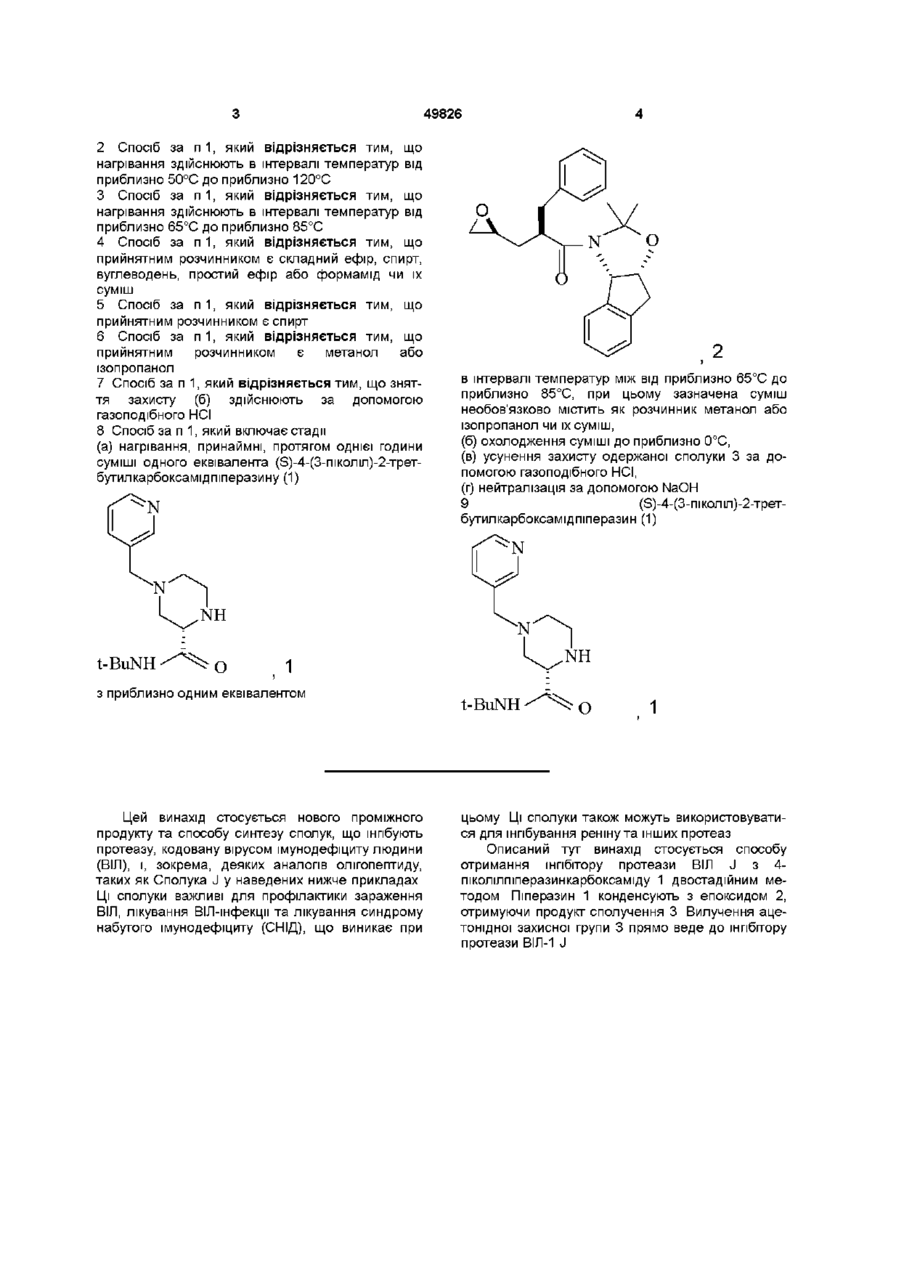
з приблизно одним еквівалентом сполуки
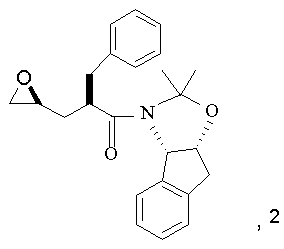
в інтервалі температур між приблизно 25°C та приблизно 150°C, при цьому зазначена суміш необов'язково містить прийнятний розчинник;
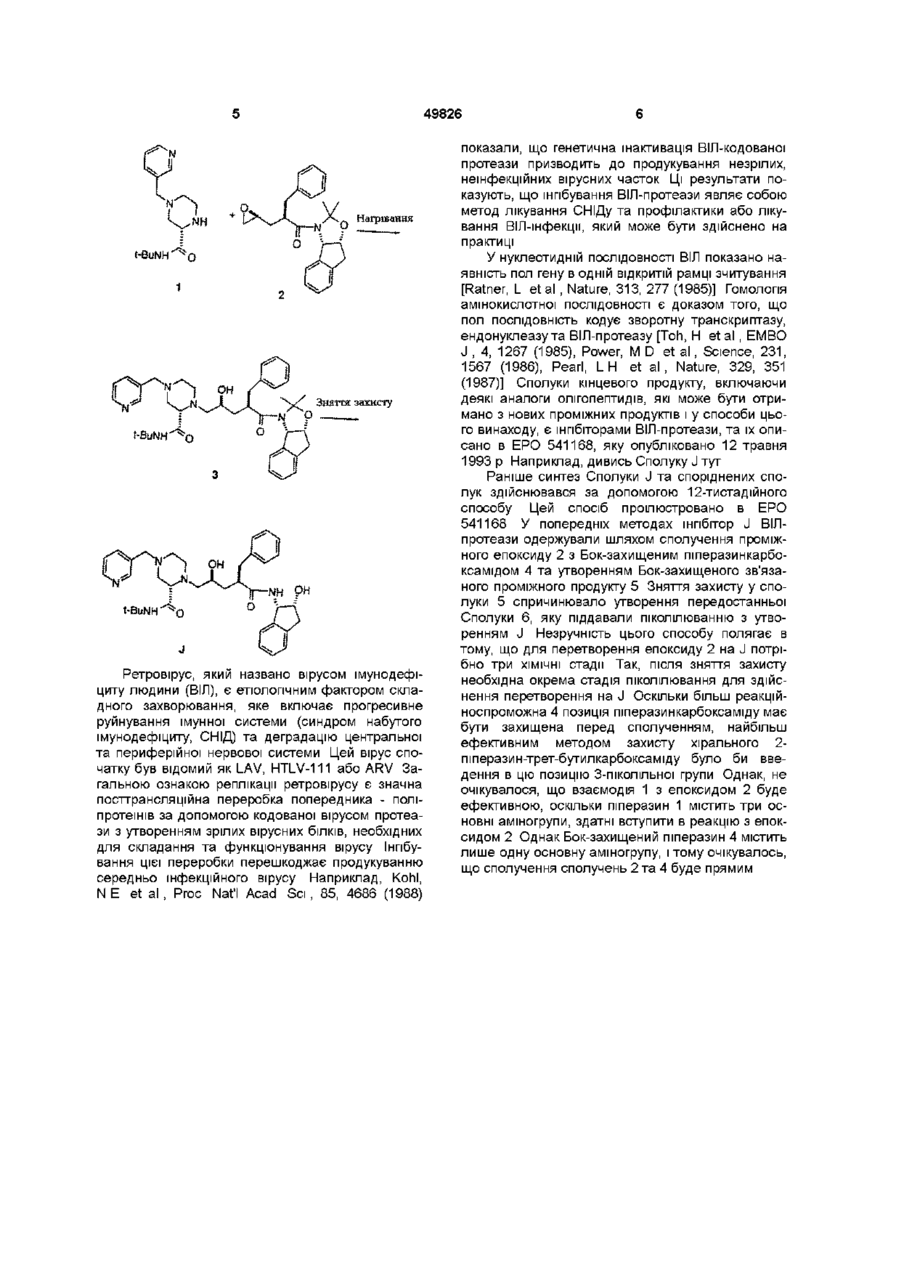
(б) зняття захисту у одержаної сполуки шляхом обробки кислотою
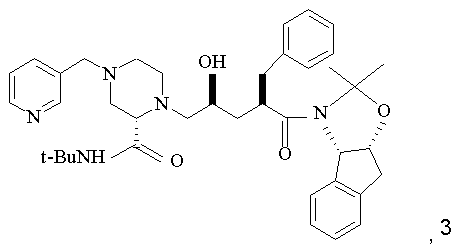 та
та
(в) нейтралізація кислоти.
2. Спосіб за п.1, який відрізняється тим, що нагрівання здійснюють в інтервалі температур від приблизно 50°C до приблизно 120°C.
3. Спосіб за п.1, який відрізняється тим, що нагрівання здійснюють в інтервалі температур від приблизно 65°С до приблизно 85°С.
4. Спосіб за п.1, який відрізняється тим, що прийнятним розчинником є складний ефір, спирт, вуглеводень, простий ефір або формамід чи їх суміш.
5. Спосіб за п.1, який відрізняється тим, що прийнятним розчинником є спирт.
6. Спосіб за п.1, який відрізняється тим, що прийнятним розчинником є метанол або ізопропанол.
7. Спосіб за п.1, який відрізняється тим, що зняття захисту (б) здійснюють за допомогою газоподібного НСl.
8. Спосіб за п.1, який включає стадії:
(а) нагрівання, принаймні, протягом однієї години суміші одного еквівалента (S)-4-(3-піколіл)-2-трет-бутилкарбоксамідпіперазину (1)
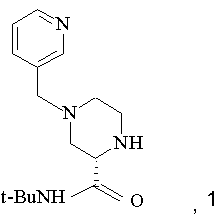
з приблизно одним еквівалентом
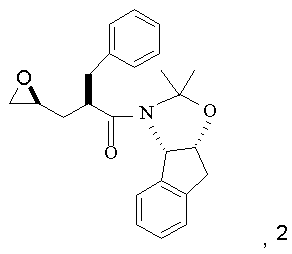
в інтервалі температур між від приблизно 65°С до приблизно 85°С, при цьому зазначена суміш необов'язково містить як розчинник метанол або ізопропанол чи їх суміш;
(б) охолодження суміші до приблизно 0°С;
(в) усунення захисту одержаної сполуки 3 за допомогою газоподібного НСl;
(г) нейтралізація за допомогою NaOH.
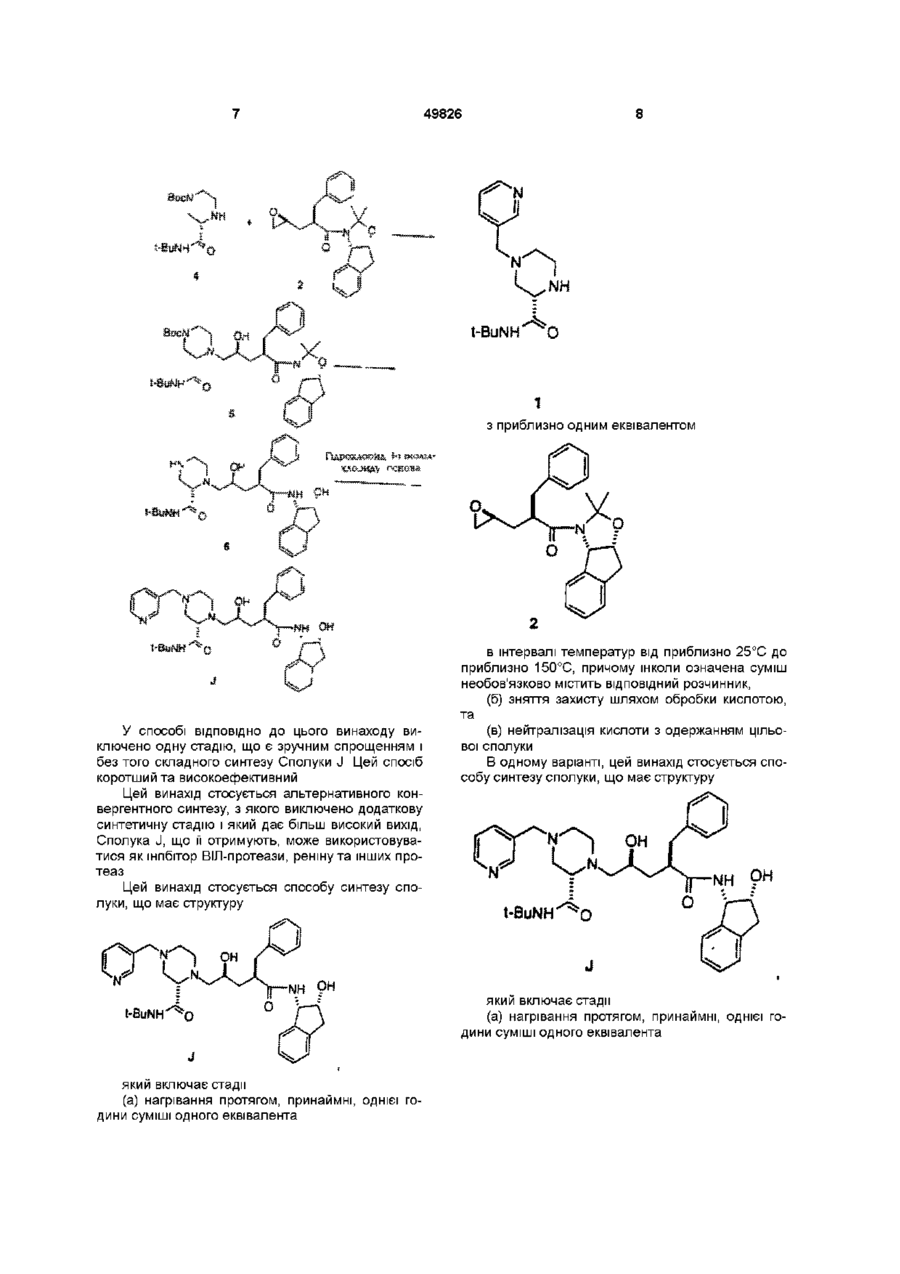
9. (S)-4-(3-піколіл)-2-трет-бутилкарбоксамідпіперазин (1):
 .
.
Текст
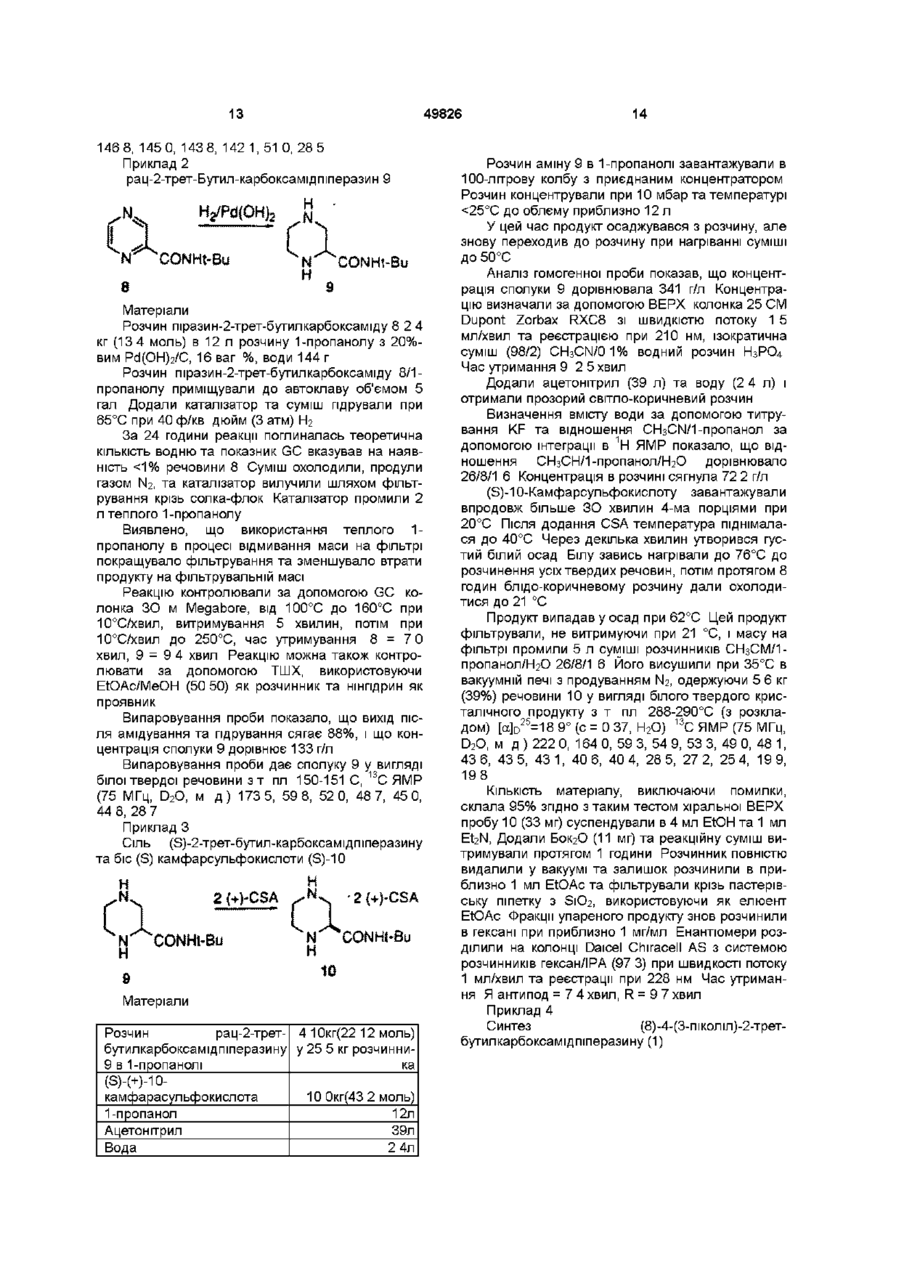
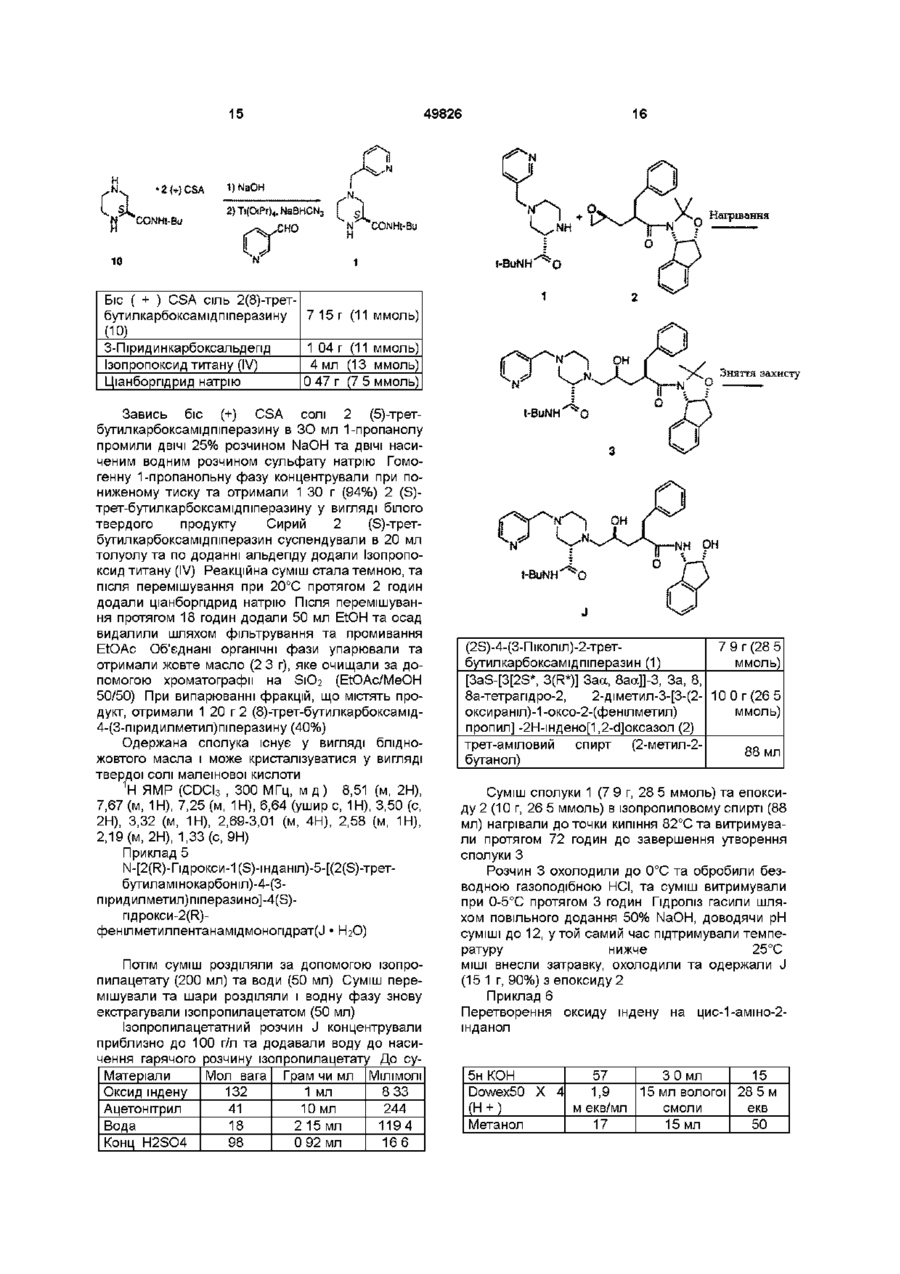
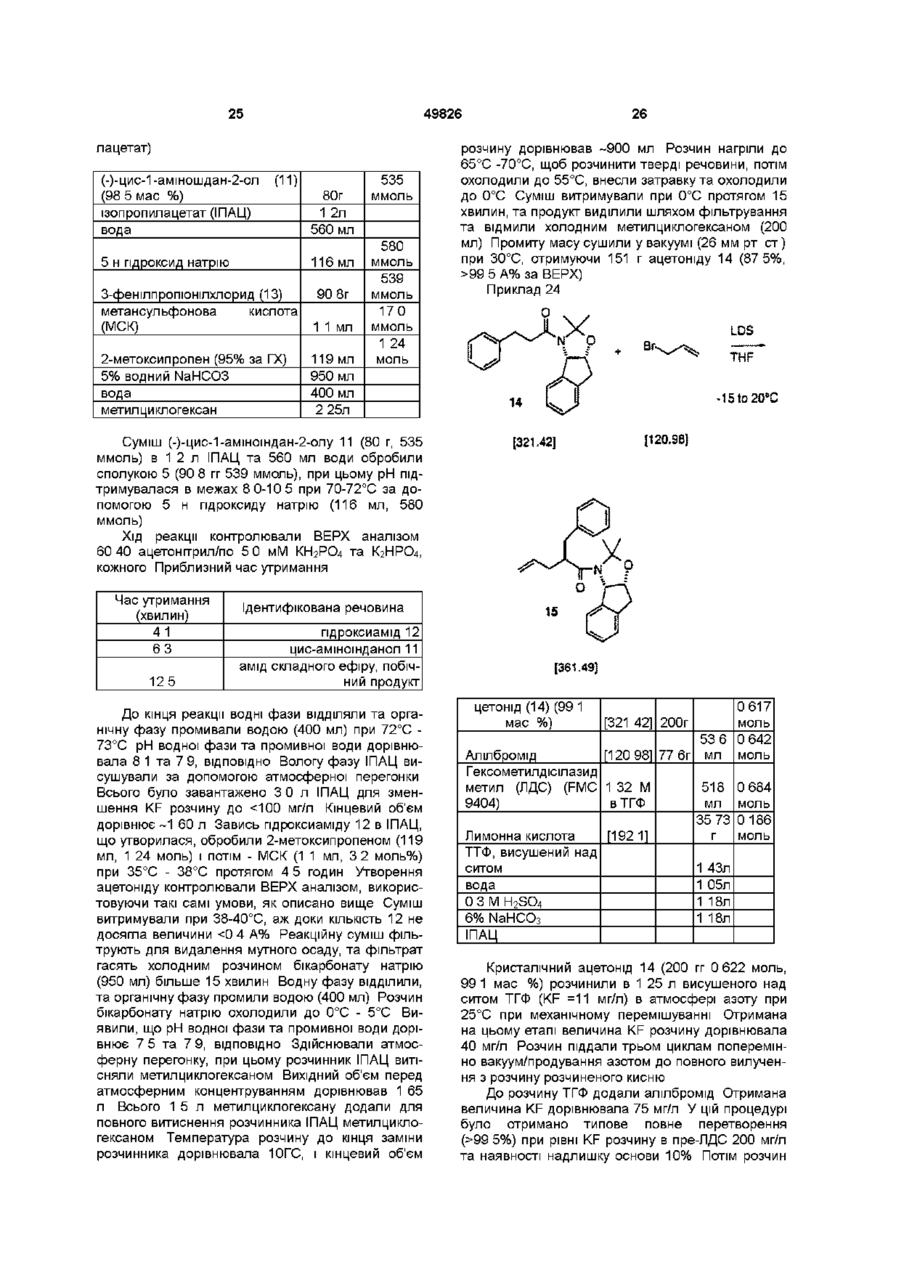
1 Спосіб одержання інгібітору протеази ВІЛ структурної формули NH 1 t-BuNH з приблизно одним еквівалентом сполуки О N .NH О о ОН (О t-BuNH ,J який включає такі стадії (а) нагрівання, принаймні, протягом однієї години одного еквівалента (3)-4-(3-піколіл)-2-третбутилкарбоксамідпіперазину (1) в інтервалі температур між приблизно 25°С та приблизно 150°С, при цьому зазначена суміш необов'язково містить прийнятний розчинник, (б) зняття захисту у одержаної сполуки шляхом обробки кислотою t-BuNH та (в) нейтралізація кислоти 00 49826 2 Спосіб за п 1 , який відрізняється тим, що нагрівання здійснюють в інтервалі температур від приблизно 50°С до приблизно 120°С 3 Спосіб за п 1 , який відрізняється тим, що нагрівання здійснюють в інтервалі температур від приблизно 65°С до приблизно 85°С 4 Спосіб за п 1 , який відрізняється тим, що прийнятним розчинником є складний ефір, спирт, вуглеводень, простий ефір або формамід чи їх суміш 5 Спосіб за п 1 , який відрізняється тим, що прийнятним розчинником є спирт 6 Спосіб за п 1 , який відрізняється тим, що прийнятним розчинником є метанол або ізопропанол 7 Спосіб за п 1, який відрізняється тим, що зняття захисту (б) здійснюють за допомогою газоподібного НСІ 8 Спосіб за п 1, який включає стадії (а) нагрівання, принаймні, протягом однієї години суміші одного еквівалента (3)-4-(3-піколіл)-2-третбутилкарбоксамідпіперазину (1) О в інтервалі температур між від приблизно 65°С до приблизно 85°С, при цьому зазначена суміш необов'язково містить як розчинник метанол або ізопропанол чи їх суміш, (б) охолодження суміші до приблизно 0°С, (в) усунення захисту одержаної сполуки 3 за допомогою газоподібного НСІ, (г) нейтралізація за допомогою NaOH 9 (3)-4-(3-піколіл)-2-третбутилкарбоксамідпіперазин (1) NH t-BuNH^ " ^ o NH 1 з приблизно одним еквівалентом Цей винахід стосується нового проміжного продукту та способу синтезу сполук, що інгібують протеазу, кодовану вірусом імунодефіциту людини (ВІЛ), і, зокрема, деяких аналогів олігопептиду, таких як Сполука J у наведених нижче прикладах Ці сполуки важливі для профілактики зараження ВІЛ, лікування ВІЛ-інфекцм та лікування синдрому набутого імунодефіциту (СНІД), що виникає при t-BuNH О цьому Ці сполуки також можуть використовуватися для інгібування реніну та інших протеаз Описаний тут винахід стосується способу отримання інгібітору протеази ВІЛ J з 4піколілпіперазинкарбоксаміду 1 двостадійним методом Піперазин 1 конденсують з епоксидом 2, отримуючи продукт сполучення 3 Вилучення ацетонідної захисної групи 3 прямо веде до інгібітору протеази ВІЛ-1 J 49826 Нагрівання Зняття захисту t-BuNH NN ОН Ретровірус, який названо вірусом імунодефіциту людини (ВІЛ), є етіологічним фактором складного захворювання, яке включає прогресивне руйнування імунної системи (синдром набутого імунодефіциту, СНІД) та деградацію центральної та периферійної нервової системи Цей вірус спочатку був відомий як LAV, HTLV-111 або ARV Загальною ознакою реплікації ретровірусу є значна посттрансляційна переробка попередника - поліпротешів за допомогою кодованої вірусом протеази з утворенням зрілих вірусних білків, необхідних для складання та функціонування вірусу Інгібування цієї переробки перешкоджає продукуванню середньо інфекційного вірусу Наприклад, Kohl, N Е et al , Proc Nat'l Acad Sci , 85, 4686 (1988) показали, що генетична інактивація ВІЛ-кодованої протеази призводить до продукування незрілих, неінфекційних вірусних часток Ці результати показують, що інгібування ВІЛ-протеази являє собою метод лікування СНІДу та профілактики або лікування ВІЛ-інфекцм, який може бути здійснено на практиці У нуклеотидніи ПОСЛІДОВНОСТІ ВІЛ показано наявність пол гену в одній відкритій рамці зчитування [Ratner, L et al , Nature, 313, 277 (1985)] Гомологія амінокислотної ПОСЛІДОВНОСТІ Є доказом того, що пол ПОСЛІДОВНІСТЬ кодує зворотну транскриптазу, ендонуклеазута ВІЛ-протеазу [Топ, Н et al , EMBO J , 4, 1267 (1985), Power, M D et a l , Science, 231, 1567 (1986), Pearl, L H et al , Nature, 329, 351 (1987)] Сполуки кінцевого продукту, включаючи деякі аналоги олігопептидів, які може бути отримано з нових проміжних продуктів і у способи цього винаходу, є інгібіторами ВІЛ-протеази, та їх описано в ЕРО 541168, яку опубліковано 12 травня 1993 р Наприклад, дивись Сполуку J тут Раніше синтез Сполуки J та споріднених сполук здійснювався за допомогою 12-тистадійного способу Цей спосіб проілюстровано в ЕРО 541168 У попередніх методах інгібітор J ВІЛпротеази одержували шляхом сполучення проміжного епоксиду 2 з Бок-захищеним піперазинкарбоксамідом 4 та утворенням Бок-захищеного зв'язаного проміжного продукту 5 Зняття захисту у сполуки 5 спричинювало утворення передостанньої Сполуки 6, яку піддавали піколілюванню з утворенням J Незручність цього способу полягає в тому, що для перетворення епоксиду 2 на J потрібно три ХІМІЧНІ стадії Так, після зняття захисту необхідна окрема стадія піколілювання для здійснення перетворення на J Оскільки більш реакційноспроможна 4 позиція піперазинкарбоксаміду має бути захищена перед сполученням, найбільш ефективним методом захисту хірального 2піперазин-трет-бутилкарбоксаміду було би введення в цю позицію 3-ПІКОЛІЛЬНОІ групи Однак, не очікувалося, що взаємодія 1 з епоксидом 2 буде ефективною, оскільки піперазин 1 містить три основні аміногрупи, здатні вступити в реакцію з епоксидом 2 Однак Бок-захищений піперазин 4 містить лише одну основну аміногрупу, і тому очікувалось, що сполучення сполучень 2 та 4 буде прямим 49826 1 з приблизно одним еквівалентом У способі ВІДПОВІДНО до цього винаходу виключено одну стадію, що є зручним спрощенням і без того складного синтезу Сполуки J Цей спосіб коротший та високоефективний Цей винахід стосується альтернативного конвергентного синтезу, з якого виключено додаткову синтетичну стадію і який дає більш високий вихід, Сполука J, що її отримують, може використовуватися як інгібітор ВІЛ-протеази, реніну та інших протеаз Цей винахід стосується способу синтезу сполуки, що має структуру в інтервалі температур від приблизно 25°С до приблизно 150°С, причому інколи означена суміш необов'язково містить ВІДПОВІДНИЙ розчинник, (б) зняття захисту шляхом обробки кислотою, та (в) нейтралізація кислоти з одержанням цільової сполуки В одному варіанті, цей винахід стосується способу синтезу сполуки, що має структуру NH РН 1-BuNH який включає стадії (а) нагрівання протягом, принаймні, однієї години суміші одного еквівалента який включає стадії (а) нагрівання протягом, принаймні, однієї години суміші одного еквівалента 49826 1 з приблизно одним еквівалентом 1 Сполучення може бути виконано шляхом нагрівання піперазину 1 та епоксиду 2 в нерозбавленому вигляді або в різних розчинниках Реакцію сполучення може бути здійснено при температурі в інтервалі від 25°С до 150°С, більш прийнятне в інтервалі від 50°С до 120°С, найбільш прийнятними температурами є від 65°С до 85°С Бажаними розчинниками для цієї стадії є складні ефіри, такі як етилацетат, ізопропилацетат, н-бутилацетат, ацетонітрил, спирти, такі як метанол, етанол, нпропанол, н-бутанол, трет-бутанол, трет-аміловий спирт та ізопропанол, вуглеводні, такі як циклогексан і толуол, прості ефіри, наприклад, ТГФ, ДМЕ, й формаміди, такі як ДМФ Більш прийнятними розчинниками є спирти, найбільш прийнятними є метанол та ізопропанол Зняття захисту у проміжних продуктів 3 з утворенням J здійснюється за допомогою стандартних методів, тобто шляхом обробки сильними кислотами, такими як газоподібна НС1 в спиртових розчинниках або водною НС1, причому метод з використанням газоподібної НС1 є найбільш прийнятним 10 в інтервалі температур від приблизно 65°С до приблизно 85°С, причому зазначена суміш необов'язково містить як розчинник метанол чи ізопропанол або їх суміш, (б) охолодження суміші до близько 0°С, (в) зняття захисту за допомогою газоподібної НС1, та (г) нейтралізація за допомогою NaOH, що веде до отримання цільової сполуки Цей винахід включає також сполуку Продукти цього винаходу можуть використовуватися для ВІЛ-протеази, профілактики або лікування інфекції вірусом імунодефіциту людини та лікування патологічних станів, що її супроводжують, таких як СНІД Лікування СНІДу або профілактика чи лікування ВІЛ-інфекцм визначаються як такі, що включають, але не обмежуються ними, випадки застосувань для лікування найрізноманітніших станів при ВІЛ-інфекцм СНІД, ARC (споріднений комплекс СНІД), як симптоматичні, так і асимптоматичні, та фактичні або потенційні ВІЛконтакти Наприклад, сполуки кінцевих продуктів, які може бути одержано в цьому процесі, та проміжні продукти ВІДПОВІДНО до цього винаходу можуть використовуватися при лікуванні ВІЛ-інфекцм після контакту з ВІЛ, що припускається, наприклад, при переливанні крові, пересадці органів, заміщенні рідини тіла, укусах, поломках голки при уколах або контактах з кров'ю пацієнта під час операції Інгібітори ВІЛ-протеази з числа кінцевих продуктів можуть використовуватися також при отриманні та здійсненні скринінгових досліджень противірусних сполук Наприклад, сполуки з числа кінцевих продуктів можуть використовуватися для виділення мутантних ферментів, які є чудовими скринінговими інструментами для пошуку більш сильних противірусних сполук Крім того, такі сполуки можуть використовуватися при встановленні та визначенні ділянки сполучення у інших противірусних сполук, які діють на ВІЛ-протеазу, наприклад, за допомогою конкурентного інгібування Таким чином сполуки з числа кінцевих продуктів, які одержують в цьому процесі, та проміжні продукти цього винаходу є комерційними продуктами, що їх продають для зазначених цілей Кінцевий продукт - Сполука J, що є інгібітором ВІЛ-протеази, має структуру 11 49826 ОН або и фармацевтичне прийнятні солі чи гідрати Сполука J має назву N- (2 (R) -пдрокси-1 (S) -інданіл) -2 (R) феніл метил-4(3) -пдрокси-5- (1 - (4- (3тридилметил)-2(3)-І\Г-(третбутилкарбоксамідо)піперазиніл))пентанамід, [1 S-[1 a[aS",yR",5(R")],2a]]-N-(2,3-fliriflpo-2пдрокси-1Н-шден-1-іл)-2[[(1,1діметилетил)амшо]карбоніл]-у-пдрокси-а- (фенілметил) -4(3-піридинілметил)-2піперазинпентанамід, або Н-(1 (S)-2(3-fliriflpo-2(R)-riflpoKCH-1 Н-інденіл)4(3)-пдрокси-2^)-фенілметил-5-[4-(3піридилметил)-2(3)-третбутилкарбамоіл)піперазиніл]пентанамід Сполуки-шпбітори ВІЛ-протеази, що їх може бути отримано у способи ВІДПОВІДНО ДО ЦЬОГО винаходу, описані в ЕРО 541164 Ці сполуки, які інгібують ВІЛ-протеазу, може бути введено пацієнтам, які потребують такого лікування, у фармацевтичних сполуках, що включають фармацевтичний носій та терапевтичне ефективну КІЛЬКІСТЬ сполуки або и фармацевтичне прийнятної солі В ЕРО 541164 описано прийнятні фармацевтичні сполуки, шляхи введення, сольові форми та солі й дози для цих сполук Сполуки ВІДПОВІДНО до цього винаходу, що можуть мати асиметричні центри та трапляються у вигляді рацематів, рацемічних сумішей та у вигляді індивідуальних діастереомерів або енантюмерів з усіма ізомерними формами, входять до обсягу цього винаходу Коли якась змінна (наприклад, арил) трапляється більш одного разу в будь-якому структурному елементі, и визначення в кожному випадку не залежить від и визначення в будь-якому іншому випадку Крім того, поєднання замісників та/або змінних є припустимими лише в такому вигляді, коли такі поєднання ведуть до стабільних сполук Далі докладно описуються показові експериментальні методи використання нового способу Ці методи є тільки ілюстративними прикладами, та ними не обмежують новий спосіб ВІДПОВІДНО до винаходу Приклад 1 Піразин-2-трет-бутилкарбоксамід 8 N (7) Оксалілхлорид трет-Бутиламш (КР=460мкг/мл) ЕЮАс (КР=56мкг/мл) ДМФ 1-Пропанол кислота 3 35кг (27моль)| 3 46кг (27 2моль) 9 36л (89моль) 27л 120мл 30л Карбонову кислоту 7 суспендували в 27 л ЕЮАс та 120 мл ДМФ при механічному перемішуванні в N2 в 3-хгорлій колбі об'ємом 72 л, та суспензію охолоджують до 2°С Додали оксалілхлориду, підтримуючи температуру між 5 та 8°С Додання завершують протягом 5 годин В процесі екзотермічного додання виділяється СО та СО2 НСІ, що утворилася, в основному залишається у розчині Є осад, який, певно, є НСІ сіллю хлорангідриду піразинової кислоти Аналіз утворення цього хлорангідриду здійснюють шляхом гасіння безводної реакційної проби за допомогою терт-бутиламшу По закінченні реакції залишається 99 5% енантюмерного надлишку) моногідрат карбонату натрію 900г 6 02 моль 760 г 613 моль діетоксиметан (ДЕМ) 3-фенілпропюнілхлорид (1 3) 56 3л 1 05кг метансульфонова кислота (МСК) 2-метоксипропен (95% за ГХ) 186г 5% водний NaHCO3 вода 10 8л 26 2л 1 28л 6 23 моль 019 моль 133 моль Завись суміші, що містить (-)-цис-і-аміношдан2-ол (11, 900 г, 6 02 моль) в 40 л ДЕМ та водний розчин карбонату натрію (760 г, 6,13 моль ЫагСОз • НгО в 6 4 л води) в реакторі об'ємом 100 л з 4-ма впускними отворами, що має термопарний вимірювальний датчик, механічну мішалку, та з'єднувальну муфту для введення азоту і барбатер, нагрівали до 46-47°С й витримували протягом 15 хвилин Реакційну суміш нагріли до 46-47°С і витримували 15 хвилин, щоб розчинити тверді речовини Водна фаза мала рН 11 5, Додали нерозбавлений 3-фенілпропюнілхлорид 13 (1 05 кг, 6 23 моль) впродовж більше 2 годин при 47-59°С В процесі додання 13 внутрішня температура збільшилася від 47°С до 59°С, в процесі додання хлорангідриду з розчину кристалізувався гідроксид аміду 12 По закінченні додання реакційну суміш витримували при 59°С протягом 0 5 години і потім нагрівали до 72°С для розчинення твердих речовин Температуру підняли до 72°С для розчинення гідроокису аміду так, щоб можна було отримати гомогенний зразок для аналізу ВЕРХ й спростити до 80°С протягом 1 години, отримуючи водний розчин цис-1-аміно-2-шданолу Приклад 21 Одержання аміду 14 о NH ОН 231 35] MSOH. 2 -Метоксипронен поділ фаз Хід реакції контролювали за допомогою аналізу ВЕРХ 60 40 Ацетонітрил/по 5 0 мМ КН2РО4 та К2НРО4, кожного Приблизний час утримання Час утримання (хвилин) 41 63 125 Ідентифікована речовина пдроксиамід 12 цис-аміноінданол 11 амід складного ефіру, побічний продукт По закінченні додання хлорангідриду та витримування при 72°С 0 5 години аналіз реакційної суміші за допомогою ВЕРХ показав наявність ~0 6 А% сполуки 11, -0 2 А% побічного продукту, складного ефіру аміду, та 98 7 А% пдроксиаміду Пдроксиамід 12 не ефективно відводився при виділенні ацетоніду 14 Водну фазу ВІДДІЛЯЛИ, а органічну фазу ДВІЧІ промивали 4 5 л води Промиту органічну фазу концентрували та висушували за допомогою атмосферної азеотропної перегонки Вихідний об'єм -40 л концентрували до 27 л Всього 16 л свіжого ДЕМ було завантажено до перегінного апарату і всю порцію концентрували при 88°С - 89°С до об'єму 40 л Висушену завись пдроксиаміду 12 в ДЕМ обробили 1 28 л 2-метоксипропену і потім 18 6 г МСК при 30°С Додання МСК за відсутності 2метоксипропену спричинювало утворення складного ефіру аміну Ця домішка знову перетворюється на пдроксиамід 12 у процесі обробки в лужному середовищі до кінця утворення ацетоніду Було виявлено, що рН 1 0 мл зразка, розведеного в 1 мл води, була 2 8-3 0 Одержану суміш витримували при 39°С - 40°С протягом 3 годин Утворення ацетоніду контролювали за допомогою ВЕРХ аналізу за тих самих умов, як описано вище у цьому прикладі Приблизний час утримання 23 Час утримання (хвилин) 41 69 90 125 49826 Ідентифікована речовина пдроксиамід 12 домішка метиленкеталю ацетон ід 14 складний ефір аміду, побічний продукт Суміш витримували при 38-40°С аж доки КІЛЬКІСТЬ сполучення 12 не стала 99% (через 1 годину після додання NaOMe), суміш розбавили ІПАЦ (40% об'єму суміші) і спочатку промили збільшеним об'ємом води (732 мл) при 0°С Промивки при більш низьких температурах та при більш високих концентрації сумішей могли спричинити передчасне осадження сполуки 2 під час промивань Час перемішування/осадження звели до мінімуму (10 хвилин/30 хвилин, ВІДПОВІДНО) У такий спосіб зворотну реакцію можна було зменшити до величини < 1 % Неочищені суміші, що містять епоксид 2/йодпдрин 16 (97 3), брали для виділення продукту - епоксиду, який містить 0 6% йодпдрину Епоксидний продукт, що містить такий рівень йодпдрину, виділявся без труднощів Органічну фазу промивали 3%-им водним розчином сульфату натрію (2 х 750 мл) Після промивання об'єм органічної фази дорівнював 1 98 л рН трьох порцій промивальної води дорівнював 10 1, 9 4 та 8 6, ВІДПОВІДНО За результатами ВЕРХ аналізу сумарний вихід епоксиду 2 на цій стадії сягав 86% (з поправкою 4% на спільну елюцію біс-епі-2) Розчин епоксиду в ІПАЦ концентрували при пониженому тиску (28 мм рт ст) до об'єму приблизно 600 мл, при цьому температура розчину підтримувалася при 15-22°С Розчин витісняли н-РЮН шляхом додання 750 мл н-РЮН в процесі концентрування у вакуумі до об'єму приблизно 500 мл, підтримуючи температуру розчину 35°С в процесі концентрування/заміни розчинника з епоксиду 2 може утворитися н-пропиловий ефір як побічний продукт Результати аналізу складу розчинника за допомогою 1Н ЯМР вказують на наявність залишку ІПАЦ у КІЛЬКОСТІ
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for making hiv protease inhibitor using 2(s)-4-picolyl-2-piperazine-t-butylcarboxamide
Назва патенту російськоюСпособ получения ингибитора протеазы вич с 2(s)-4-пиколил-2-пиперазин-трет-бутилкарбоксамида
МПК / Мітки
МПК: C07D 401/06
Мітки: одержання, віл, спосіб, 2(s)-4-піколіл-2-піперазин-трет-бутилкарбоксаміду, протеази, інгібітору
Код посилання
<a href="https://ua.patents.su/17-49826-sposib-oderzhannya-ingibitoru-proteazi-vil-z-2s-4-pikolil-2-piperazin-tret-butilkarboksamidu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання інгібітору протеази віл з 2(s)-4-піколіл-2-піперазин-трет-бутилкарбоксаміду</a>
Попередній патент: Стартерна акумуляторна батарея
Наступний патент: Спосіб діагностики шизофренії, пара праймерів для використання в способі, набір для визначення алелі er
Випадковий патент: Спосіб планування норм садіння картоплі