Композиція гліколіпідного ад’юванту (варіанти) та спосіб її отримання
Номер патенту: 90569
Опубліковано: 11.05.2010
Автори: Доміновскі Пол Жозеф, Маннан Рамасамі Маннар, Медіратта Санґіта
Формула / Реферат
1. Композиція, що містить:
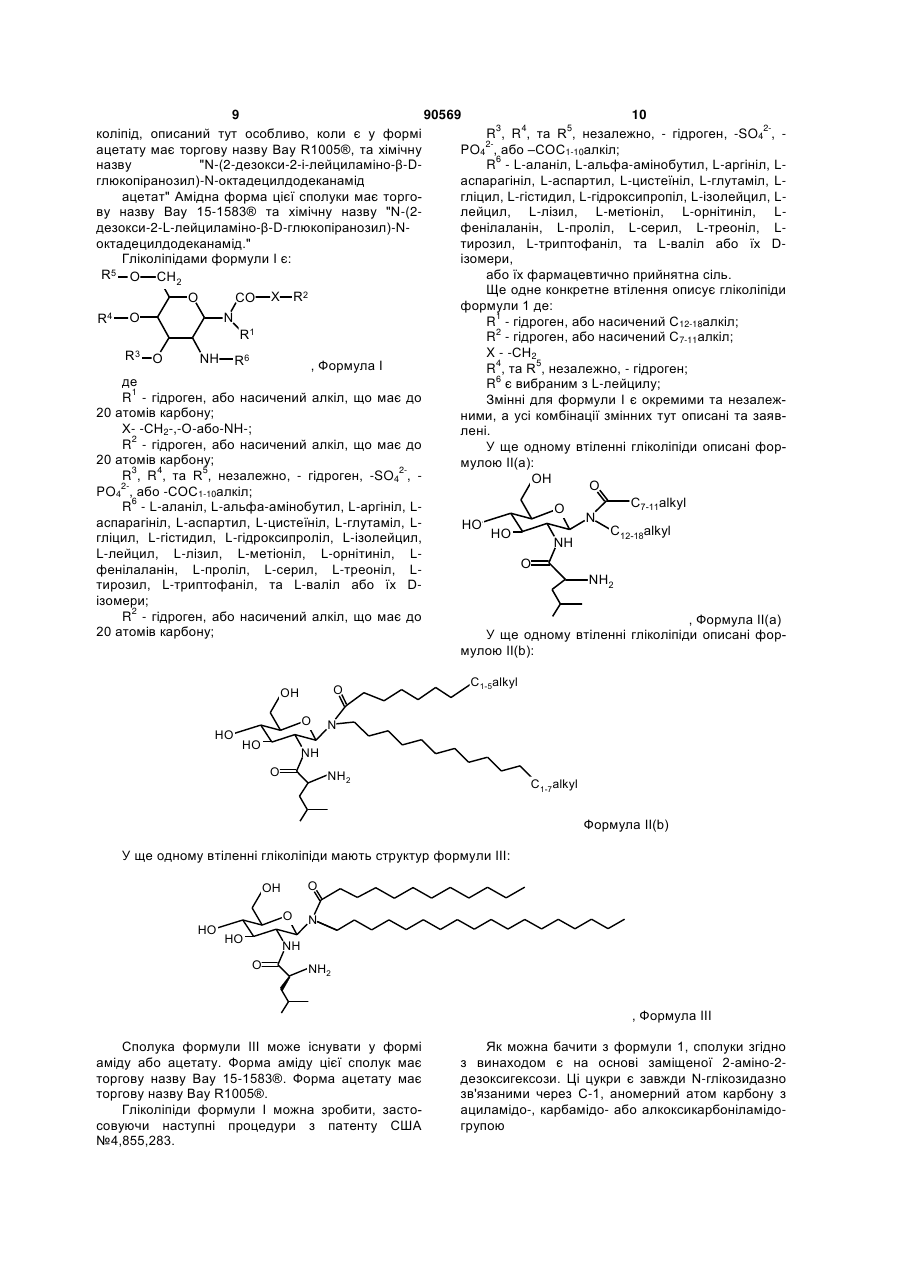
а) гліколіпід формули І
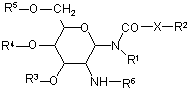 , Формула І
, Формула І
де
R1 та R2, незалежно - гідроген або насичений алкіл, що має до 20 атомів карбону;
X - -СН2-, -О- або -NH-;
R3, R4 та R5, незалежно - гідроген, -SO42-, -РО42-, -СОС1-10алкіл;
R6 - L-аланіл, L-альфа-амінобутил, L-аргініл, L-аспарагініл, L-аспартил, L-цистеїніл, L-глутаміл, L-гліцил, L-гістидил, L-гідроксипроліл, L-ізолейцил, L-лейцил, L-лізил, L-метіоніл, L-орнітиніл, L-фенілаланіл, L-проліл, L-серил, L-треоніл, L-тирозил, L-триптофаніл та L-валіл або їх D-ізомери;
у формі солі, де сіль є похідною від слабкої кислоти,
b) спирт, де спиртом є НО-С1-3алкіл;
c) слабку кислоту, де слабка кислота 1) є у молярному надлишку відносно вмісту гліколіпіду, та 2) є будь-якою кислотою, що має значення рКа (-log Ka) між 1,0 та 9,5, застосовуючи стандартні таблиці або значення;
d) неіонну ПАР, де неіонною ПАР є агент, що зменшує поверхневий натяг матеріалу, він є розчинним та має компонент, що є гідрофобним, та ще один компонент, що є гідрофільним.
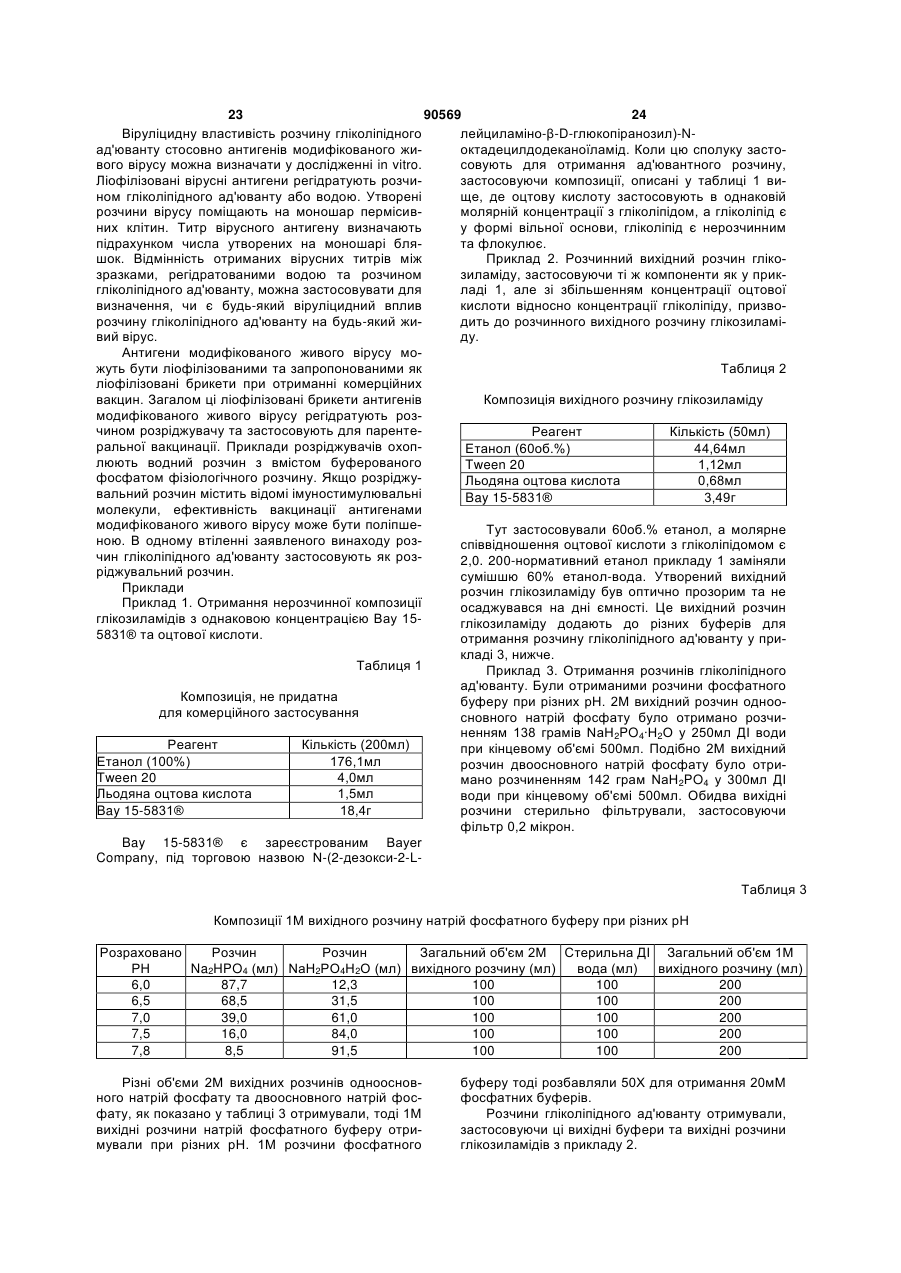
2. Композиція за п. 1, де гліколіпідом є сполука формули ІІ(а)
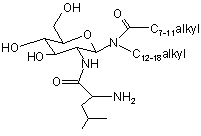 , Формула ІІ(а)
, Формула ІІ(а)
а слабка кислота є вибраною з одної з наступних слабких кислот або будь-якої їх комбінації: оцтова кислота, Н(С2Н3О2) (рКа 4,76); аскорбінова кислота (1), Н2(С6Н6О6) (рКа 4,10); ацетилсаліцилова кислота, Н8(С9О4), (рКа 3,5); бутанова кислота Н(С4Н7О2) (рКа 4,83); карбонатна кислота, форма 1, Н2СО3, (рКа 4,83); хромова кислота, форма 2, HCrO4-, (рКа 6,49); лимонна кислота, форма 1, Н3(С6Н5О7), (рКа 3,14); лимонна кислота, форма 2, Н2С6Н5О7)-, (рКа 4,77); лимонна кислота, форма 3, (НС6Н5О7)2-, (рКа 6,39); мурашина кислота, Н(СНО2), (рКа 3,75); фумарова кислота, Н4(С4О4), (рКа 3,03); гептанова кислота, Н(С7Н13О2), (рКа 4,89); гексанова кислота, Н(С6Н11О2), (рКа 4,84); флуоридна кислота, HF, (рКа 3,20); ізолимонна кислота, Н8(С6О7), (рКа 3,29); молочна кислота, Н(С3Н5О3), (рКа 3,08); малеїнова кислота, Н4(С4О4), (рКа 1,83); нікотинова кислота, H5(C6NO2), (pK3,39); щавлева кислота, форма 1, Н2(С2О4), (рКа 1,23); щавлева кислота, форма 2, (НС2О4)-, (рКа 4,19); пентанова кислота, Н(С5Н9О2), (рКа 4,84); фосфатна кислота, форма 1, Н3РО4, (рКа 2,16); пропанова кислота, Н(С3Н5О2), (рКа 4,86); піровиноградна кислота, Н4(С3О3), (рКа 2,39); бурштинова кислота Н6(С4О4), (рКа 4,19) та трихлороцтова кислота, Н(С2С13О2), (рКа 0,70).
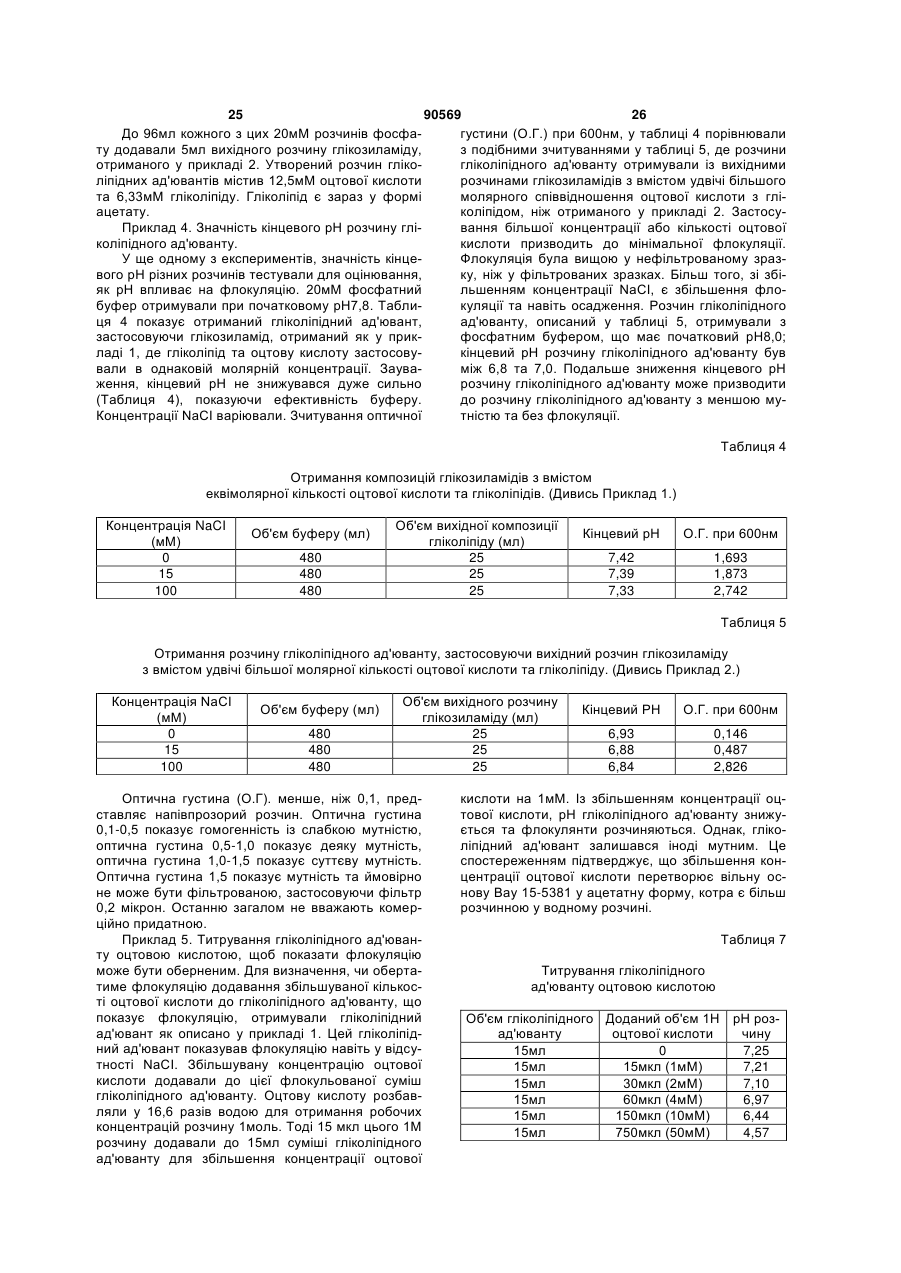
3. Композиція за п. 2, де гліколіпідом є сполука формули II(b)
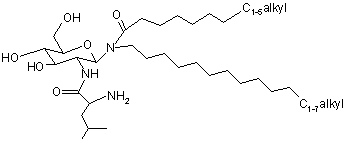 , Формула II(b)
, Формула II(b)
а слабка кислота є вибраною з одної з наступних слабких кислот або будь-якої їх комбінації: оцтова кислота, ацетилсаліцилова кислота; лимонна кислота; мурашина кислота; фумарова кислота; флуоридна кислота; ізолимонна кислота; малеїнова кислота; нікотинова кислота; фосфатна кислота; піровиноградна кислота; бурштинова кислота та трихлороцтова кислота.
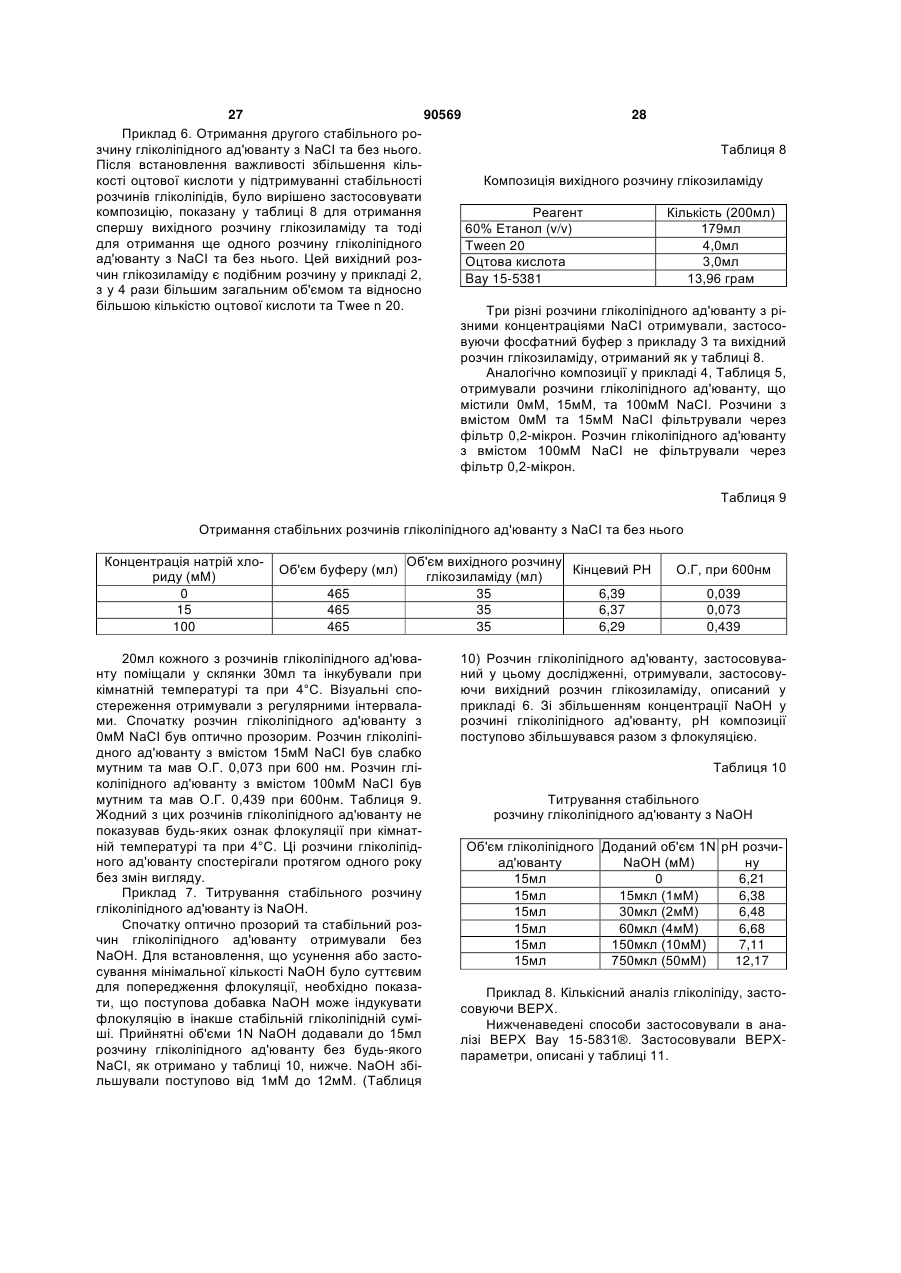
4. Композиція за п. 3, де гліколіпідом є -N-(2-дезокси-2-L-лейциламіно-β-D-глюкопіранозил)-N-октадецилдодеканамід ацетат, що має структуру формули III:
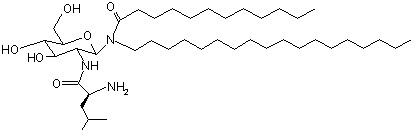 , Формула III
, Формула III
а слабкою кислотою є оцтова кислота.
5. Композиція за п. 2, де слабка кислота є вибраною з групи: оцтова кислота; ацетилсаліцилова кислота; лимонна кислота, форма 1; лимонна кислота, форма 2; лимонна кислота, форма 3; мурашина кислота; фумарова кислота; флуоридна кислота; ізолимонна кислота; малеїнова кислота; нікотинова кислота; фосфатна кислота, форма 1; піровиноградна кислота, бурштинова кислота та трихлороцтова кислота.
6. Композиція за будь-яким з пп. 1-5, де вказана слабка кислота є у кількості, що більше, ніж молярний еквівалент гліколіпіду, або більше у нижченаведену кількість разів, ніж молярний еквівалент гліколіпіду:
a) у 1,25 разу більше,
b) у 2,0 разу більше,
c) у 2,5 разу більше,
d) у 2,7 разу більше,
е) 3,0 разу більше,
f) у 5,0 разу більше, ніж молярний еквівалент кількості гліколіпіду.
7. Композиція за будь-яким з пп. 1-6, де спирт - етиловий спирт.
8. Композиція за будь-яким з пп. 1-7, де вказана неіонна ПАР є вибраною з будь-якої ПАР або їх комбінації: сорбітан монолаурат, сорбітан монопальмітат, сорбітан моностеарат, сорбітан тристеарат, сорбітан моноолеат, сорбітан триолеат, поліоксіетиленсорбітан монолаурат, поліоксіетиленсорбітан монопальмітат, поліоксіетиленсорбітан моностеарат, поліоксіетиленсорбітан моноолеат, поліоксіетиленсорбітан триолеат та інші сорбітани та поліоксіетиленсорбітани, звичайно застосовувані у вакцинах.
9. Композиція, що містить: а) гліколіпід формули І:
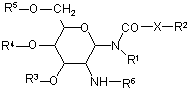 , Формула I
, Формула I
де
R1 та R2, незалежно - гідроген або насичений алкіл, що має до 20 атомів карбону;
X - -СН2-, -О- або -NH-;
R3, R4 та R5, незалежно - гідроген, -SO42-, -PO42-, -СОС1-10алкіл;
R6 - L-аланіл, L-альфа-амінобутил, L-аргініл, L-аспарагініл, L-аспартил, L-цистеїніл, L-глутаміл, L-гліцил, L-гістидил, L-гідроксипроліл, L-ізолейцил, L-лейцил, L-лізил, L-метіоніл, L-орнітиніл, L-фенілаланіл, L-проліл, L-серил, L-треоніл, L-тирозил, L-триптофаніл та L-валіл або їх D-ізомери;
у формі солі, де сіль є похідною від слабкої кислоти,
b) спирт, де спиртом є НО-С1-3алкіл;
c) слабку кислоту, де слабка кислота 1) є у молярному надлишку відносно вмісту гліколіпіду, та 2) є будь-якою кислотою, що має значення рКа (-log Ka) приблизно 1,0-9,5, застосовуючи стандартні таблиці або значення;
d) неіонну ПАР, де неіонна ПАР є агентом, що зменшує поверхневий натяг матеріалу, він є розчинним та має компонент, що є гідрофобним, та ще один компонент, що є гідрофільним; та
е) водний буфер, де підхожий буфер є придатним для застосування у вакцинах та може підтримувати рН інших інгредієнтів у межах рН приблизно 6-8, за умови, що застосовують не більше, ніж 50 мМ NaCl.
10. Композиція за п. 9, де рН розчину доводять до відносно постійного значення рН у водному розчині приблизно 6-7, а буфер є вибраним з групи: фосфатні буфери, що мають одноосновні та двоосновні солі натрійфосфату та/або калійфосфату при однакових або різних пропорціях.
11. Композиція за п. 9, де вказаний буфер є вибраним з групи:
a) 2-(N-морфоліно)етансульфонова кислота (також відома як МЕС);
b) 3-(N-морфоліно)пропансульфонова кислота (також відома як МПС);
c) н-[трис(гідроксиметил)]-2-аміноетансульфонова кислота (також відома як ТЕС);
d) 4-(2-гідроксіетил)піперазин-1-етансульфонова кислота (також відома як ГЕПЕС); та
e) [трис(гідроксиметил)метил]гліцин (також відомий як ТРИС);
або будь-яка їх комбінація.
12. Композиція за будь-яким з пп. 1-11, що містить крім того антиген, вибраний з антигену або будь-якої їх комбінації з групи: модифікований живий вірус герпесу корів, модифікований живий респіраторно-синцитіальний вірус корів та модифікований живий вірус парагрипу 3.
13. Композиція, що містить:
а) N-(2-дезокси-2-L-лейциламіно-β-D-глюкопіранозил)-N-октадецилдодеканамід ацетат, що має структуру формули III:
 , Формула III
, Формула III
b)етанол;
c) оцтову кислоту; де кількість становить молярний надлишок по відношенню до вмісту гліколіпіду;
d) неіонну ПАР, вибрану з групи: сорбітан монолаурат, сорбітан монопальмітат, сорбітан моностеарат, сорбітан тристеарат, сорбітан моноолеат, сорбітан триолеат, поліоксіетиленсорбітан монолаурат, поліоксіетиленсорбітан монопальмітат, поліоксіетиленсорбітан моностеарат, поліоксіетиленсорбітан моноолеат, поліоксіетиленсорбітан триолеат,
e) водний буфер, де рН розчину доводять до відносно постійного значення рН у водному буферованому розчині приблизно 6-7, а буфер є вибраним з групи:
a) 2-(N-морфоліно)етансульфонову кислоту (також відома як МЕС),
b) 3-N-морфоліно)пропансульфонову кислоту (також відома як МПС),
c) н-[трис(гідроксиметил)]-2-аміноетансульфонову кислоту (також відома як ТЕС),
d) 4-(2-гідроксіетил)піперазин-1-етансульфонову кислоту (також відома як ГЕПЕС), та
e) [трис(гідроксиметил)метил]гліцин (також відомий як ТРИС),
або будь-яку їх комбінацію,
за умови, що застосовують не більше, ніж 15 мМ NaCl; a
f) антигеном є по суті модифікований живий вірус герпесу корів, модифікований живий респираторно-синцитіальний вірус корів, та модифікований живий вірус парагрипу 3.
14. Спосіб отримання композиції, який полягає у змішуванні разом наступного:
A) гліколіпіду формули І;
B) спирту, де спиртом є НО-С1-3алкіл;
C) слабкої кислоти, де кількість слабкої кислоти є у молярному надлишку відносно вмісту гліколіпіду; та
D) неіонної ПАР.
15. Спосіб отримання композиції, який полягає у змішуванні разом наступного:
A) гліколіпіду формули І;
B) спирту, де спиртом є НО-С1-3алкіл;
C) слабкої кислоти, де кількість слабкої кислоти є у молярному надлишку відносно вмісту гліколіпіду;
D) неіонної ПАР; а тоді додавання
E) придатного буферу.
Текст
1. Композиція, що містить: а) гліколіпід формули І R5 O CH2 2 (19) 1 3 90569 4 (рКа 2,16); пропанова кислота, Н(С3Н5О2), (рКа 3. Композиція за п. 2, де гліколіпідом є сполука 4,86); піровиноградна кислота, Н4(С3О3), (рКа формули II(b) 2,39); бурштинова кислота Н6(С4О4), (рКа 4,19) та трихлороцтова кислота, Н(С2С13О2), (рКа 0,70). O OH O HO HO C1-5alkyl N NH O NH2 C1-7alkyl , Формула II(b) а слабка кислота є вибраною з одної з наступних слабких кислот або будь-якої їх комбінації: оцтова кислота, ацетилсаліцилова кислота; лимонна кислота; мурашина кислота; фумарова кислота; флуоридна кислота; ізолимонна кислота; малеїнова кислота; нікотинова кислота; фосфатна кислота; O OH O HO HO піровиноградна кислота; бурштинова кислота та трихлороцтова кислота. 4. Композиція за п. 3, де гліколіпідом є -N-(2дезокси-2-L-лейциламіно-β-D-глюкопіранозил)-Nоктадецилдодеканамід ацетат, що має структуру формули III: N NH O NH2 , Формула III а слабкою кислотою є оцтова кислота. 5. Композиція за п. 2, де слабка кислота є вибраною з групи: оцтова кислота; ацетилсаліцилова кислота; лимонна кислота, форма 1; лимонна кислота, форма 2; лимонна кислота, форма 3; мурашина кислота; фумарова кислота; флуоридна кислота; ізолимонна кислота; малеїнова кислота; нікотинова кислота; фосфатна кислота, форма 1; піровиноградна кислота, бурштинова кислота та трихлороцтова кислота. 6. Композиція за будь-яким з пп. 1-5, де вказана слабка кислота є у кількості, що більше, ніж молярний еквівалент гліколіпіду, або більше у нижченаведену кількість разів, ніж молярний еквівалент гліколіпіду: a) у 1,25 разу більше, b) у 2,0 разу більше, c) у 2,5 разу більше, d) у 2,7 разу більше, е) 3,0 разу більше, f) у 5,0 разу більше, ніж молярний еквівалент кількості гліколіпіду. 7. Композиція за будь-яким з пп. 1-6, де спирт етиловий спирт. 8. Композиція за будь-яким з пп. 1-7, де вказана неіонна ПАР є вибраною з будь-якої ПАР або їх комбінації: сорбітан монолаурат, сорбітан монопальмітат, сорбітан моностеарат, сорбітан тристеарат, сорбітан моноолеат, сорбітан триолеат, поліоксіетиленсорбітан монолаурат, поліоксіетиленсорбітан монопальмітат, поліоксіетиленсорбітан моностеарат, поліоксіетиленсорбітан моноолеат, поліоксіетиленсорбітан триолеат та інші сорбітани та поліоксіетиленсорбітани, звичайно застосовувані у вакцинах. 9. Композиція, що містить: а) гліколіпід формули І: R5 O CH2 CO O R4 O X R2 N R1 R3 O NH R6 , Формула I де R1 та R2, незалежно - гідроген або насичений алкіл, що має до 20 атомів карбону; X - -СН2-, -О- або -NH-; R3, R4 та R5, незалежно - гідроген, -SO42-, -PO42-, СОС1-10алкіл; R6 - L-аланіл, L-альфа-амінобутил, L-аргініл, Lаспарагініл, L-аспартил, L-цистеїніл, L-глутаміл, Lгліцил, L-гістидил, L-гідроксипроліл, L-ізолейцил, L-лейцил, L-лізил, L-метіоніл, L-орнітиніл, Lфенілаланіл, L-проліл, L-серил, L-треоніл, Lтирозил, L-триптофаніл та L-валіл або їх Dізомери; у формі солі, де сіль є похідною від слабкої кислоти, b) спирт, де спиртом є НО-С1-3алкіл; c) слабку кислоту, де слабка кислота 1) є у молярному надлишку відносно вмісту гліколіпіду, та 2) є будь-якою кислотою, що має значення рКа (-log Ka) приблизно 1,0-9,5, застосовуючи стандартні таблиці або значення; d) неіонну ПАР, де неіонна ПАР є агентом, що зменшує поверхневий натяг матеріалу, він є роз 5 90569 6 чинним та має компонент, що є гідрофобним, та c) н-[трис(гідроксиметил)]-2-аміноетансульфонова ще один компонент, що є гідрофільним; та кислота (також відома як ТЕС); е) водний буфер, де підхожий буфер є придатним d) 4-(2-гідроксіетил)піперазин-1-етансульфонова для застосування у вакцинах та може підтримувакислота (також відома як ГЕПЕС); та ти рН інших інгредієнтів у межах рН приблизно 6-8, e) [трис(гідроксиметил)метил]гліцин (також відоза умови, що застосовують не більше, ніж 50 мМ мий як ТРИС); NaCl. або будь-яка їх комбінація. 10. Композиція за п. 9, де рН розчину доводять до 12. Композиція за будь-яким з пп. 1-11, що містить відносно постійного значення рН у водному розчикрім того антиген, вибраний з антигену або будьні приблизно 6-7, а буфер є вибраним з групи: фоякої їх комбінації з групи: модифікований живий сфатні буфери, що мають одноосновні та двоосвірус герпесу корів, модифікований живий респірановні солі натрійфосфату та/або калійфосфату торно-синцитіальний вірус корів та модифікований при однакових або різних пропорціях. живий вірус парагрипу 3. 11. Композиція за п. 9, де вказаний буфер є виб13. Композиція, що містить: раним з групи: а) N-(2-дезокси-2-L-лейциламіно-β-Da) 2-(N-морфоліно)етансульфонова кислота (також глюкопіранозил)-N-октадецилдодеканамід ацетат, відома як МЕС); що має структуру формули III: b) 3-(N-морфоліно)пропансульфонова кислота (також відома як МПС); O OH O HO HO N NH O NH2 , Формула III b)етанол; c) оцтову кислоту; де кількість становить молярний надлишок по відношенню до вмісту гліколіпіду; d) неіонну ПАР, вибрану з групи: сорбітан монолаурат, сорбітан монопальмітат, сорбітан моностеарат, сорбітан тристеарат, сорбітан моноолеат, сорбітан триолеат, поліоксіетиленсорбітан монолаурат, поліоксіетиленсорбітан монопальмітат, поліоксіетиленсорбітан моностеарат, поліоксіетиленсорбітан моноолеат, поліоксіетиленсорбітан триолеат, e) водний буфер, де рН розчину доводять до відносно постійного значення рН у водному буферованому розчині приблизно 6-7, а буфер є вибраним з групи: a) 2-(N-морфоліно)етансульфонову кислоту (також відома як МЕС), b) 3-N-морфоліно)пропансульфонову кислоту (також відома як МПС), c) н-[трис(гідроксиметил)]-2-аміноетансульфонову кислоту (також відома як ТЕС), d) 4-(2-гідроксіетил)піперазин-1-етансульфонову кислоту (також відома як ГЕПЕС), та e) [трис(гідроксиметил)метил]гліцин (також відомий як ТРИС), або будь-яку їх комбінацію, за умови, що застосовують не більше, ніж 15 мМ NaCl; a f) антигеном є по суті модифікований живий вірус герпесу корів, модифікований живий респираторно-синцитіальний вірус корів, та модифікований живий вірус парагрипу 3. 14. Спосіб отримання композиції, який полягає у змішуванні разом наступного: A) гліколіпіду формули І; B) спирту, де спиртом є НО-С1-3алкіл; C) слабкої кислоти, де кількість слабкої кислоти є у молярному надлишку відносно вмісту гліколіпіду; та D) неіонної ПАР. 15. Спосіб отримання композиції, який полягає у змішуванні разом наступного: A) гліколіпіду формули І; B) спирту, де спиртом є НО-С1-3алкіл; C) слабкої кислоти, де кількість слабкої кислоти є у молярному надлишку відносно вмісту гліколіпіду; D) неіонної ПАР; а тоді додавання E) придатного буферу. Заявлений винахід стосується нових композицій гліколіпідних ад'ювантів, способів їх застосування та їх отримання. Нові композиції заявленого винаходу є стабільними протягом довгого часу без флокуляції. Вони є особливо корисними у виробленні різних медикаментів, охоплюючи вакцини. Вакцини звичайно застосовують для захисту людей та тварин від інфекційних хвороб, викликаних бактеріями, вірусами та паразитами. Антигени, застосовувані у вакцинах можуть бути будь-яким рядом агентів, але звичайно складаються з вбитих патогенних організмів, патогенних організмів, котрі є живими, але модифікованими чи послабленими, 7 90569 8 білків, рекомбінантних білків або їх фрагментів. міду у "придатний буфер." рН кінцевих стабільних Яким би не було джерело антигену, часто необхідрозчинів гліколіпідного ад'юванту, описаних тут, но додавати ад'ювант для посилення імунної реаслід бути приблизно 6-8. Кінцевий рН приблизно 6кції хазяїна на антиген. 7 є кращим. Описано кінцевий рН приблизно 6,3Ад'юванти застосовують для досягнення двох 6,4. Високі концентрації солей гліколіпідного ад'юцілей: вони повільно вивільняють антигени з діляванту у надлишку 30мМ NaCI, слід усувати. нок ін'єкції та стимулюють імунну систему. Ці два розчини представлені більш детально Першим ад'ювантом представленим у літератаким чином: турі був повний ад'ювант Фрейнда (ПАФ). ПАФ вихідний розчин глікозиламіду є композицією, містить емульсію вода-в-олії та екстракти мікобакщо містить: терій. Екстракти мікобактерій забезпечують імуноa) гліколіпід формули І: стимулювальні молекули у сирій формі. Емульсія вода-в-олії діє для створення ефекту депо, де антигени повільно вивільняються. На жаль ПАФ є погано толерантним і це може викликати неконтрольоване запалення. Після знаходження ПАФ протягом 80 років зроблено спроби зменшення небажаної побічної дії ад'ювантів. Гліколіпідні аналоги, що містять новий клас де сполук, що має властивості ад'ювантів є зараз R1 - гідроген, або насичений алкіл, що має до відомими. Патент США №4,855,283, (далі '283') 20 атомів карбону; розкриває синтез аналогів гліколіпідів, охоплюючи Х- -СН2-,-О-або-NH-; N-глікозиламіди, N-глікозилсечовини, NR2 - гідроген, або насичений алкіл, що має до глікозилкарбамати, а особливо: N-(2-дезокси-2-L20 атомів карбону; лейциламiно-β-D-глюкотранозил)-NR3, R4, та R5, незалежно, - гідроген, -SO42-, октадецилдодеканамiд ацетат (відомий як Bay PO42-, -СОС1-10алкіл; R1005, О Lockhoff, Angew. Chem. Int. Ed. Engl. R6 - L-аланіл, L-альфа-амінобутил, L-аргініл, L(1991) 30:1611-1620. Сполуки, описані у патенті аспарагініл, L-аспартил, L-цистеїніл, L-глутаміл, L'283' є особливо придатними для застосування як гліцил, L-гістидил, L-гідроксипроліл, L-ізолейцил, ад'юванти. L-лейцил, L-лізил, L-метіоніл, L-орнітиніл, LКомпозиції гліколіпідних ад'ювантів повинні буфенілаланін, L-проліл, L-серил, L-треоніл, Lти легкими для виробництва та стабільними при тирозил, L-триптофаніл, та L-валіл або їх Dзберіганні протягом довгого періоду часу без флоізомери; куляції ліпіду. Неацетатні форми амідів або глікоу формі солі, де сіль є похідною слабкої кислозиламідів гліколіпіду є дуже нерозчинними та звити; чайно флокулюють з розчину при зберіганні при b) спирт, де спиртом є НО-С1-3алкіл; кімнатній або нижчій температурі. c) слабку кислоту, де 1) слабка кислота є у Розчини та ад'юванти, що містять глікозиламімолярному надлишку відносно вмісту гліколіпіду, ди, запропоновані тут, показують малу флокуляцію та 2) будь-яка кислота, що має значення рКа прита є цілком стабільними. Вони є легкими для вироблизно 1,0-9,5, застосовуючи стандартні таблиці бництва та їх можна отримувати у комерційному або значення; та масштабі. Рідкі композиції гліколіпідних ад'ювантів d) неіонну ПАР, де неіонна ПАР є агентом, що можна застосовувати як розріджувач для отризменшує поверхневий натяг матеріалу, вона є романня регідратованого ліофілізованого антигену, зчинною та має один компонент, що є гідрофобприскореного тестування стабільності є запропоним, та ще один компонент, що є гідрофільним. нованими також. Розчин гліколіпідного ад'юванту є композиціЦей винахід стосується композиції та способу єю, що містить: створення або виробництва вихідного розчину a) вихідний розчин глікозиламіду; та глікозиламіду та розчин гліколіпідного ад'юванту. b) придатний буфер, де буфер є прийнятним вихідного розчину глікозиламіду отримують розчидля ветеринарного або медичного застосування та ненням гліколіпіду формули 1 у спирті та комбінуможе підтримувати відносно постійний рН у водванням цього з прийнятною кількістю слабкої кисному розчин приблизно 6,0-8,0. лоти плюс "неіонна" ПАР. Слабку кислоту додають Якщо не вказане інше, наступні терміни, задо спиртового розчину гліколіпіду, у молярному стосовувані в описі та формулі винаходу, мають надлишку слабкої кислоти відносно гліколіпіду. В нижченаведені значення. одному втіленні гліколіпідом є N-(2-дезокси-2-LТермін "спирт" стосується сполук формули: лейциламіно-β-D-глюкопіранозил)-NНО-С1-3алкіл. Це може бути метанол, етанол, або октадецилдодеканоїламід гідроацетат. В одному пропанол у будь-якій формі, як-то н-пропанол або втіленні спирт -етанол. В одному втіленні слабкою ізо-пропанол. Етанол є кращим. кислотою є оцтова кислота. В одному втіленні неіТермін "алкіл" стосується з насичених вуглеонні ПАР є різними сорбітанами (Span®) або поліводневих груп лінійним та нелінійним ланцюгом. оксіетиленсорбітанами (Tween®), зокрема, моноТермін "гліколіпіди" стосується сполук формулаурат сорбітанами (Span 20®) та монолаурат ли І нижче. Ці сполуки є описаними у патенті США поліоксіетиленсорбітанами (Tween 20®). Розчин №6,290,971, та патенті США №4,855,283, issued гліколіпідного ад'юванту отримують уведенням August 8, 1989. Патент США №6,290,971, та паприйнятної кількості вихідного розчину глікозилатент США №4,855,283 уведено тут як довідку. Глі 9 90569 10 коліпід, описаний тут особливо, коли є у формі R3, R4, та R5, незалежно, - гідроген, -SO42-, ацетату має торгову назву Bay R1005®, та хімічну PO42-, або –СОС1-10алкіл; назву "N-(2-дезокси-2-і-лейциламіно-β-DR6 - L-аланіл, L-альфа-амінобутил, L-аргініл, Lглюкопіранозил)-N-октадецилдодеканамід аспарагініл, L-аспартил, L-цистеїніл, L-глутаміл, Lацетат" Амідна форма цієї сполуки має торгогліцил, L-гістидил, L-гідроксипропіл, L-ізолейцил, Lву назву Bay 15-1583® та хімічну назву "N-(2лейцил, L-лізил, L-метіоніл, L-орнітиніл, Lдезокси-2-L-лейциламіно-β-D-глюкопіранозил)-Nфенілаланін, L-проліл, L-серил, L-треоніл, Lоктадецилдодеканамід." тирозил, L-триптофаніл, та L-валіл або їх DГліколіпідами формули І є: ізомери, або їх фармацевтично прийнятна сіль. R5 O CH2 Ще одне конкретне втілення описує гліколіпіди CO X R2 O формули 1 де: N R4 O R1 - гідроген, або насичений С12-18алкіл; 1 R R2 - гідроген, або насичений С7-11алкіл; X - -СН2 R3 O NH R6 , Формула І R4, та R5, незалежно, - гідроген; де R6 є вибраним з L-лейцилу; R1 - гідроген, або насичений алкіл, що має до Змінні для формули І є окремими та незалеж20 атомів карбону; ними, а усі комбінації змінних тут описані та заявХ- -СН2-,-О-або-NH-; лені. R2 - гідроген, або насичений алкіл, що має до У ще одному втіленні гліколіпіди описані фор20 атомів карбону; мулою ІІ(а): R3, R4, та R5, незалежно, - гідроген, -SO42-, OH 2O PO4 , або -СОС1-10алкіл; C7-11alkyl R6 - L-аланіл, L-альфа-амінобутил, L-аргініл, LO N аспарагініл, L-аспартил, L-цистеїніл, L-глутаміл, LHO C12-18alkyl HO гліцил, L-гістидил, L-гідроксипроліл, L-ізолейцил, NH L-лейцил, L-лізил, L-метіоніл, L-орнітиніл, LO фенілаланін, L-проліл, L-серил, L-треоніл, LNH2 тирозил, L-триптофаніл, та L-валіл або їх Dізомери; R2 - гідроген, або насичений алкіл, що має до , Формула ІІ(а) 20 атомів карбону; У ще одному втіленні гліколіпіди описані формулою ІІ(b): O OH O HO HO C1-5alkyl N NH O NH2 C1-7alkyl Формула ІІ(b) У ще одному втіленні гліколіпіди мають структур формули III: O OH O HO HO N NH O NH2 , Формула III Сполука формули III може існувати у формі аміду або ацетату. Форма аміду цієї сполук має торгову назву Bay 15-1583®. Форма ацетату має торгову назву Bay R1005®. Гліколіпіди формули І можна зробити, застосовуючи наступні процедури з патенту США №4,855,283. Як можна бачити з формули 1, сполуки згідно з винаходом є на основі заміщеної 2-аміно-2дезоксигексози. Ці цукри є завжди N-глікозидазно зв'язаними через С-1, аномерний атом карбону з ациламідо-, карбамідо- або алкоксикарбоніламідогрупою 11 90569 (I) з вищезгаданими значеннями для R1, R2 та X. 2-аміногрупа аміноцукрів у сполуках згідно з винаходом, формули І, є амідно зв'язаною з αамінокислотою або похідним α-амінокислоти. Амінокислотами є природні L-амінокислоти, якто гліцин, саркозин, гіпурова кислота, аланін, валін, лейцин, ізолейцин, серин, треонін, цистеїн, метіонін, орнітин, цитрулін, аргінін, аспарагінова кислота, аспарагін, глутамінова кислота, глутамін, фенілаланін, тирозин, пролін, триптофан та гістидин. Також описаними є D-амінокислоти, як-то Dаланін, або амінокарбонові кислоти, як-то альфааміномасляна кислота, α-аміновалеріанова кислота, α-амінокапронова кислота або αаміногептанова кислота, у D- та L-формі, що діють як замісники на аміноцукрі. Способи отримання сполуки формули І є запропонованими також. Це стосується вихідних від 2-аміно-2-дезоксиглікопіранози похідних (формула IV), котрі є захищеними на аміногрупі, (IV) де R10 представляє захисну групу для захисту аміногрупи, котра є відомою з синтезу пептидів та може, де прийнятно, бути селективно усуненою. Прикладами придатних захисних груп є ацилгрупи, як-то трифлуорацетил або трихлорацетил, о-нітрофенілсульфеніл, 2,4динітрофенілсульфеніл або необов'язково заміщені нижчі алкоксикарбонільні групи, як-то метоксикарбоніл, т-бутилоксикарбоніл, бензилоксикарбоніл, п-метоксибензилоксикарбоніл або 2,2,2трихлоретилоксикарбоніл. Придатні N-захищені похідні аміно-гексоз є відомими. Наприклад, М. Bergmann та L. Zervas, Вег. 64, 975 (1931); D. Horton, J. Org. Chem. 29, 1776 (1964); Ρ. Η. Gross та R. W. Jeanloz, J. Org. Chem. 32, 2759 (1967); M. L. Wolfrom та Η. Β. Bhat, J. Org. Chem. 32, 1821 (1967); загально: J. F. W. McOmie (Editor). Prot. Prot. Groups. Org. Chem., Plenum Press (1973); Geiger in "The Peptides" Vol. З, р 1-99, (1981) Academic Press; та література, цитована там). Кращими амінозахисними групами для отримання сполуки формули І є ВОС (третбутилоксикарбоніл) або Ζ (бензилоксикарбоніл). Блоковані похідні аміноцукру (IV) реагують, на першому етапі реакції, з амінами (формула V), H2N-R1 (V) де R1 має вищезгадані значення, даючи глікозиламіни (формули VI) (VI) 12 Глікозиламіни цього типу є відомими (ELLIS, Advances in Carbohydrate Chemistry 10, 95 (1955)) та є конкретно описаними у DE-OS (German Published Specification) No.3,213,650. На другому етапі реакції глікозиламіни (VI) реагують з придатними похідними карбонової кислоти (формула VII), як-то карбоксил галогеніди, або ангідриди карбонових кислот, R11-CO-CH2-R4 (VII) R2 має вищезгадані значення, a R11 представляє галоген як-то, наприклад, хлор, або представляє -O-CO-R2 з вищезгаданими значеннями для R2, або представляє -О-СО-О-нижчий алкіл. Цим шляхом, отримують глікозиламіди (формула VIII) (VIII) де R1 та R2 мають вищезгадані значення, R10 такий же, як R6, а X представляє -СН2Умови для N-ацилування цього типу є показаними у DE-OS (German Published Specification) No.3,213,650. У кращому втіленні глікозиламіни формули VI реагують з одним - двома еквівалентами карбонілхлориду (формула VII) або з одним - двома еквівалентами змішаного ангідриду, котрий отримано з важливої карбонової кислоти R2--CH2--CO2H та етил хлороформіату або ізобутил хлороформіату, у присутності органічної допоміжної основи, способами, відомими з літератури, отримуючи глікозилформаміди VIII з Х=-СН2-. Це проводять в органічних або водноорганічних розчинниках між 0°С та 50°С, де прийнятно, у присутності неорганічної або органічної основи. Придатними розріджувачами є спирти, якто метанол, етанол, 1-пропанол або 2-пропанол, або етери, як-то діетил-етер, тетрагідрофуран або 1,4-діоксан, або галогеновані вуглеводні, як-то дихлорметан, трихлорметан або 1,2-дихлоретан, або Ν,Ν-диметилформамід. Коли глікозиламіни (VI), котрі отримують на першому етапі, реагують із галогеномурашиними естерами (IX) R12-CO-O-R2 (IX) R12- галоген як-то, наприклад, хлор або бром, a R2 має вищезгадані значення, тоді отримують глікозилкарбамати (VIII), X у формулі VIII представляє оксиген. В одному втіленні глікозиламіни формули VIII реагують з одним - двома еквівалентами хлоркарбонового естеру IX, даючи глікозилкарбамат. Це переважно проводять в органічних або водноорганічних розчинниках при температурі між 0°С та 50°С, але особливо переважно при кімнатній температурі. Придатними розчинниками є спирти, етери, галогеновані вуглеводні або диметилформамід, як-то вищезгадані. Коли глікозиламіни (VI), котрі отримують на першому етапі, реагують з одним -двома еквівалентами органічного ізоціанату (формула X) R2-NCO (X) із R2, що має вищезгадані значення, отримують глікозилсечовини формули VIII, а X - -NH-. Цю 13 90569 14 реакцію ацилування типу вищезгаданих реакцій органічними розчинниками, як-то тетрагідрофуранпереважно проводять в органічних розчинниках, з метанол, тетрагідрофуран-вода, етанол-вода та температурою реакції, що є -20-60°С, переважно ізопропанол-вода. Триестери (формула XI), котрі 0-25°С Придатними розчинниками є вищезгадані очищеними одиничною або, де прийнятно, багатоспирти, етери, галогеновані вуглеводні або димекратною перекристалізацією, повертають до триотилформамід. лів (формула VIII) гідролізом або трансестерифіГлікозиламіди (формула VIII, Х=-СН2-), глікокацією трьох О-ацетил-груп. Різноманітність типів зилкарбамати (формула VIII, Х=-О-) або глікозилрозщеплень естерів є відомими в органічній хімії. сечовини (формула VIII, X=-NH-), отримані цим Для отримання триолів (формула VIII) з триестерів шляхом виділяють у формі кристалічних або амо(формула XI) це можна зробити трансестерифікарфних твердих продуктів відомими способами та, цією ацил-групи у присутності метанолу та каталіякщо необхідно, очищають стандартними процетичної кількості натрій метаноляту, що є відомим дурами, як-то перекристалізація, хроматографія, як гідроліз ZEMPLEN в органічній хімії. екстракція, тощо. Третій етап реакції при отриманні сполук форУ багатьох випадках, також краще проводити мули І згідно з винаходом полягає у селективному паралельно або замість вищезгаданих етапів очивідщепленні захисної групи 2-аміногрупи на цукрі у стки хімічну дериватизацію, котра дає похідні глісполуках формули VIII. У цій реакції треба бути козиламідів, карбаматів та сечовин формули VIII, обережним, щоб не було одночасного усунення 1котрі мають гарні властивості стосовно кристаліамідо-або 1-карбамідоабо 1зації. Хімічні дериватизації цього типу є, у випадку (алкоксикарбоніламідо)-груп на цукрі у сполуках глікозиламідів, глікозилкарбаматів та глікозилсеформули VIII. човин згідно з винаходом, наприклад, реакціями Бензилоксикарбоніл-групу, котра є переважно естерифікації на гідроксильних групах залишків застосовуваною, на С-2 аміногексанів можна кільцукру. Приклади придатних естерних груп є ацекісно та селективно відщеплювати, із збереженням тил, бензоїл або п-нітробензоїл. 1-амідо-, 1-карбамідоабо 1Для отримання три-О-ацил-похідних глікозиалкоксикарбоніламідогруп, в умовах гідрогенолізу. ламідів, глікозилсечовин або глікозилкарбаматів, Цей гідрогеноліз забезпечує глікозиламіди, гліковідповідні триоли (Формул VIII) реагують із ацилузилсечовини або глікозилкарбамати з вільною 2вальними агентами у присутності неорганічних або аміногрупою на цукрі формули (XII) органічних допоміжних основ. Придатними ацилувальними агентами є хлоридангідриди кислот, якто ацетилхлорид, бензоїлхлорид або п(XII) нітробензилхлорид, або ангідриди, як-то, наприклад, оцтовий ангідрид. Це призводить до утворення естерів формули XI (XI) де R1, R2, R10 та X мають вищезгадані значення, а R13 представляє ацетил, бензоїл або пнітробензоїл. Реакції О-ацилування переважно проводять в інертних органічних розчинниках, якими є галогеновані вуглеводні, як-то дихлорметан, трихлорметан або 1,2-дихлоретан, етери, як-то тетрагідрофуран, або 1,4-діоксан, естери, як-то етилацетат, та аміди, як-то диметилформамід. Також можливо для органічних основ поодинці, як-то триетиламін або піридин, бути придатними розчинниками. Основи, котрі можна застосовувати, є усі основами, застосовуваними в органічній хімії для О-ацилування. Переважно, застосовують триетиламін, піридин або суміш піридин/4диметиламінопіридин. Триестери (формула XI) можна легко кристалізувати з органічних розчинників. Особливо кращими для кристалізації є полярні розчинники, як-то коротко-ланцюгові спирти, як-то метанол, етанол, н-пропанол або ізопропанол. Іншими розчинниками, придатними для кристалізації триестерів (формула XI) є суміші органічних розчинників з полярними неорганічними або з вищезгаданими значеннями для R1, R2 та X. Приклади придатних каталізаторів для гідрогенолізу є благородні метали, як-то платина або паладій на активованому вугіллі. Паладій/активоване вугілля (5% або 10%) є застосовуваним переважно. Гідрогеноліз можна проводити під атмосферним тиском або підвищеним тиском у придатній герметичній посудині. Інертні розчинники є придатними для гідрування, як-то, наприклад, спирти, як-то метанол, етанол, або пропанол, етери, як-то тетрагідрофуран або 1,4-діоксан, або карбонові кислоти, як-то оцтова кислота, або їх суміші. Де прийнятно, розчинником є змішуваним з водою або розбавленими кислотами, як-то хлоридна кислота або сульфатна кислота. Безумовно, коли так кислоти додають, 2-аміно-2-дезоксиглікозиламіди, -карбамати та -сечовини формули XII отримують як солі амонію цих кислот. Тбутилоксикарбонільну захисну групу, котра є подібно переважно застосовуваною у сполуках формули VIII, можна відщеплювати способами, відомими з літератури, застосовуючи мінеральні кислоти, як-то хлоридна кислота або сульфатна кислота. У цьому випадку також, 2-аміно-2дезокси-глікозиламіди, -карбамати та -сечовини формули XII селективно отримують як солі амонію кислот, застосовуваних для розщеплення. Четвертий етап реакції для синтез сполук формули І, згідно з винаходом, полягає у зв'язуванні аміноглікозил-амідів, амідів, -карбаматів абосечовин формули XII, або їх солей, з придатним 15 90569 16 амінокислотним похідним. Придатні амінокислотні або сечовинні групи. Карбобензоксигрупу можна похідні є N-блокованими амінокислотами (формуселективно усувати гідрогенолізом у присутності ла XIII) благородного металу як-то, наприклад, паладій на активованому вугіллі, у придатному розчиннику, (XIII) як-то етанол, метанол, льодяна оцтова кислота або тетрагідрофуран. Розчинники можна застосо7 з R , що має вищезгадане значення, вувати як чисті розчинники або комбіновані один з 8 R представляє гідроген або метил, а одним або з водою. Реакцію можна проводити під 14 R представляє захисну групу, котру звичайно атмосферним тиском або під підвищеним тиском. застосовують у синтезі пептидів та котру можна Трет-бутилоксикарбоніл R14 у сполуках формули селективно усувати знов, залишаючи пептидний XIV можна усувати ацидолітичними способами. зв'язок. Прикладами придатних умови застосування гідроЗахисні групи для аміногруп у формулі XIII, когенхлориду у придатних розчинниках як-то, напритрі є переважно застосовуваними є вищезгаданиклад, льодяна оцтова кислота, діетил-етер, діокми, а бензилоксикарбонілабо тсан або етилацетат, при кімнатній температурі. бутилоксикарбоніл-групи є особливо кращими. Способи цього типу для відщеплення т-бутил карЗв'язування 2-аміно-2-дезокси-глікозиламіду, баматів є відомими. Пептидоглікозиламіди, карбамату або -сечовини формули XII з амінокискарбамати та -сечовини формули І, котрі отримулотним похідним формули XIII можна проводити ють таким чином, виділяють у формі кристалічних звичайними способами синтезу пептидів (Е. або аморфних твердих продуктів, відомими спосоWunsch et al.: Synthese von Peptiden (Synthesis of бами, та якщо необхідно, очищають стандартними peptides) in: Methoden der Org. Chemie (Methods of способами, як-то перекристалізація, хроматограorg. chemistry) (Houben-Weyl) (E. Muller, Editor), Vol фія, екстракція тощо. XV/1 and XV/2, 4th Edition, published by Thieme, Сполуки згідно з винаходом, формули І, можна Stuttgart (1974). також отримувати другим шляхом синтезу з подібПрикладами звичайних способів є конденсація ними гарними результатами. Цей другий шлях аміногрупи у сполуці формули XII із амінокислотсинтезу відрізняється від першого, що є описаним ним похідним формули XIII у присутності водовідвище, тим, що послідовність зв'язування синтонів німальних агентів, наприклад, дициклогексилкарамінокислоти аміноцукру, аміну R1-NH2 та карбободііміду або діізопропілкарбодііміду. нової кислоти R2-CH2-CO2-H, або похідного карбоКонденсацію сполук формули XII із сполуками натної кислоти R2-O-CO-ranoreH, чи R2-NCO, з формули XIII можна також проводити, коли карбовищезгаданими значеннями R1 та R2, є різними. У ксильна група є активованою. Можливою активоцьому другому шляху придатні 2-Nваною карбоксильною групою є, наприклад, ангід(аміноацил)аміноцукри формули XV рид кислоти, переважно змішаний ангідрид, як-то ацетангідрид кислоти, або амід кислоти, як-то імідазолід, або активований естер. Прикладами активованих естерів є ціанометилові естери, пентах(XV) лорфеніл-естери, та N-гідроксифталімідні естери. Активовані естери можна також отримувати з кислот (формула XIII) та N-гідроксисукциніміду або 1гідроксибензотіазолу у присутності водовіднімального агенту, як-то карбодіімід. Похідні амінокислот з вищезгаданими значеннями для R7 та R8, та, є відомими та їх можна отримувати відомим чиде R14 представляє амінозахисну групу, відому у ном. Конденсація аміносполуки формули XII із хімії пептидів, переважно бензилоксикарбоніл або необов'язково активованими карбоксильними спот-бутилоксикарбоніл, застосовують як вихідний луками формули XIII забезпечує пептидогліколіпікомпонент. Сполуки формули XV, котрі таким чиди формули XIV. ном отримують, тоді конденсують із аміносполуками формули III, отримуючи глікозиламіни загальної формули XVI (XIV) (XVI) 1 2 7 з вищезгаданими значеннями для R , R , R , R8, R14 та X. На кінцевому етапі способу отримання сполуки формули І, усувають захисну групу R14 у сполуках формули XIV. Треба бути обережним на цьому етапі, щоб інші амідні, уретанові або сечовинні групи у сполуках формули XIV не були відщепленими. Захисні групи R14, котрі є переважно застосовуваними у сполуках формули XIV, Nкарбобензоксигрупа та N-трет-бутилоксикарбонілгрупа, можна усувати, утримуючи амідні, уретанові з R1, R7, R8 та R14, що мають значення, відповідні формулі І та визначенню R6. Усі описані вище способи отримання сполук загальної формули VI можна застосовувати для отримання сполук загальної формули XVI. Сполуки формули XVI тоді реагують з вищезгаданими похідними карбонових кислот (формула VII) або з галогеномурашиними естерами (формула IX) або 17 90569 18 з органічними ізоціанатами (формула X), даючи 2Оцтова кислота є кращою. Ацетилсаліцилова (аміноацил)-аміноглікозиламіди формули XIV (з кислота, лимонна кислота, мурашина кислота, Х=-СН2--), або -карбамати формули XIV (з Х=-О-), фумарова кислота, флуоридна кислота, ізолимонабо -сечовини формули XIV (з X=-NH-). Ці реакції на кислота, малеїнова кислота, нікотинова кислоацилування можна загалом проводити описаними та, фосфатна кислота, піровиноградна кислота, вище способами для реакції глікозиламінів з похібурштинова кислота та трихлороцтова кислота є дними карбонових або карбонатної кислот. більш загальними слабкими кислотами, що застоІнтермедіати (формула XIV), котрі отримують совують індивідуально, у комбінації та як сукупцим шляхом, можна очищати вищезгаданим фізиність. чним способом очистки. Однак, краще перетворюТермін "неіонна ПАР" означає ПАР, котра є вати сполуки формули XIV, описаними вище споречовиною, що зменшує поверхневий натяг матесобами О-ацилування у три-О-ацетати або три-Оріалу, вона є розчинною, а неіонна означає, що бензоати загальної формули XVII вона має полярну групу, що не є електрично зарядженою. Термін амфіфільна ПАР означає ПАР, де частина молекули ПАР є гідрофобною, а частина є гідрофільною. Придатні ПАР повинні бути неіонними та амфіфільними та прийнятними для вете(XVII) ринарного або медичного застосування. Будь-які або не певні неіонні ПАР, що є прийнятними для ветеринарного або медичного застосування, можна легко визначати фахівцями. Є багато придатзі значеннями змінних відповідними формулі 1. них неіонних ПАР, що можна застосовувати згідно Ці сполуки можна легко кристалізувати, перез цим винаходом та запропонованими нижче прикважно з полярних розчинників, як-то метанол або ладами. етанол, та таким чином очищати. Очищені кристаДва добре відомих типи неіонних ПАР застолічні похідні формули XVII тоді перетворюють у совані тут. Вони є відомими як сорбітани, звичайно триоли формули XIV вищезгаданими способами під торговою маркою Span®, та поліоксіетиленгідролізу естерів, котрі є широко застосовуваними, сорбітани, звичайно під торговою маркою Tween®. особливо у хімії цукрів. Кінцеве усунення захисних Особливо застосованими тут є: груп у амінокислот у сполуках формули XIV вже Сорбітан монолаурат (Span 20®), сорбітан описано вище для отримання сполук формули І. монопальмітат (Span 40®), сорбітан моностеарат Винахід також стосується солей сполук формули І. (Span 60®), сорбітан тристеарат (Span 65®), сорНими є перед усім нетоксичні солі, котрі можна бітан моноолеат (Span 80®), сорбітан триолеат звичайно застосовувати у фармацевтиці, напри(Span 85®), поліоксіетиленсорбітан монолаурат клад, хлориди, ацетати та лактати, або інертні солі (Tween 20®), поліоксіетиленсорбітан монопальмісполук формули І. тат (Tween 40®), поліоксіетиленсорбітан моностеТермін "слабка кислота" означає будь-яку кисарат (Tween 60®), поліоксіетиленсорбітан моноолоту, що має значення рКа (-log Ka) приблизно 1,0 леат (Tween 80), та поліоксіетиленсорбітан - 9,5, застосовуючи стандартні таблиці або знатриолеат (Tween 85). Ці описи охоплюють торгові чення. Без обмеження рамок винаходу, наступні марки інгредієнтів, або еквівалентних інгредієнтів. приклади слабких кислот, є описаними з назвою, ПАР можна застосовувати індивідуально або у формулою, та приблизним рКа. Оцтова кислота, будь-якій комбінації. Н(С2Н3О2) (рКа 4,76); аскорбінова кислота(1), Сорбітан монолаурат (Span 20®), поліоксіетиН2(С6Н6О6) (рКа 4,10); ацетилсаліцилова кислота, ленсорбітан монолаурат (Tween 20®), сорбітан Н8(С9О4), (рКа 3,5,); бутанова кислота Н(С4Н7О2) моноолеат (Span 80®), сорбітан триолеат (Span (рКа 4,83); карбонатна кислота, Н2СО3, (рКа 4,83 85®), поліоксіетиленсорбітан моноолеат (Tween форма 1); хромова кислота, НСrO4-, (рКа 6,49 фо80), поліоксіетиленсорбітан триолеат (Tween 85) є рма 2); лимонна кислота, Н3(С6Н5О7), (рКа 3,14 описаними особливо. форма 1); лимонна кислота, Н2С6Н5О7-, (рКа 4,77 Термін "придатний буфер" означає буфер, що форма 2); лимонна кислота, (НС6Н5О7)-, (рКа 6,39 є придатним для ветеринарного або медичного форма 3); мурашина кислота, Н(СНО2), (рКа 3,75); застосування та може підтримувати відносно посфумарова кислота, Н4(С4О4) (рКа 3,03); гептанова тійний рН у водному розчин приблизно 6-8. Фоскислота, Н(С7Н13О2), (рКа 4,89); гексанова кислота, фатні буфери є одним втіленням, описаним тут. Н(C6H11O2), (рКа 4,84); флуоридна кислота, HF, Фосфатні буфери можна зробити з рН у широких (рКа 3,20); ізолимонна кислота, Н8(С6О7) (рКа межах змішуванням одноосновного та двооснов3,29); молочна кислота, Н(С3Н5О3), (рКа 3,08); маного натрій фосфатів та/або калій фосфатів у різлеїнова кислота, Н4(С4О4) (рКа 1,83); нікотинова них пропорціях. Створення та застосування різних кислота, H5(C6NO2), (pK3,39); щавлева кислота, буферів є добре відоме фахівцю. Н2(С2О4), (рКа 1,23 форма 1); щавлева кислота, Інші приклади буферів: (НС2О4)-, (рКа 4,19 форма 2); пентанова кислота, 2-(N-морфоліно) етансульфонова кислота (таН(С5Н9О2), (рКа 4,84); фосфатна кислота, Н3РО4, кож відома як МЕС); (рКа 2,16 форма 1); пропанова кислота, Н(С3Н5О2), 3-(N-морфоліно) пропансульфонова кислота (рКа 4,86); піровиноградна кислота, Н4(С3О3) (рКа (також відома як МПС); 2,39); бурштинова кислота Н6(С4О4) (рКа 4,19) та n-[трис(гідроксиметил]-2трихлороцтова кислота, Н(С2С13О2) (рКа 0,70). аміноетансульфонова кислота (також відома як Будь-які комбінації цих кислот є прикладами також. ТЕС); 19 90569 20 4-(2-гідроксіетил)піперазин-1-етансульфонова що може перетворювати ацетат гліколіпіду назад кислота (також відома як ГЕПЕС); до неацетатної форми, може викликати флокуля[трис(гідроксиметил)метил]гліцин (також відоцію гліколіпідів у водному розчині. Коли відбувамий як ТРИС). ється флокуляція гліколіпіду, молекули гліколіпіду Частина І. Отримання розчинів. виходять з розчину як тонкі пластівці, осідаючи на Новими композиціями, розкритими тут є 1) видно ємності. хідні розчини глікозиламідів та 2) розчини гліколіПочаткова концентрація слабкої кислоти у випідного ад'юванту. хідному розчині глікозиламіду гліколіпіду та спирт 1) Вихідний розчин глікозиламіду отримують визначають, чи буде флокуляція гліколіпіду. Слаброзчиненням гліколіпіду у спирті та комбінуванням ка кислота повинна бути у молярному надлишку прийнятної кількості слабкої кислоти. Слабку кисвідносно гліколіпіду для запобігання флокуляції. лоту додають до спиртового розчину гліколіпіду у 2) розчини гліколіпідного ад'юванту отримують молярному надлишку слабкої кислоти відносно уведенням прийнятної кількості вихідного розчину гліколіпіду. Неіонну ПАР додають до суміші глікоглікозиламіду у "придатний буфер." рН описаних ліпід-спирт-кислота для створення вихідного розтут кінцевих стабільних розчинів гліколіпідного чину глікозиламіду. Гліколіпідом є N-(2-дезокси-2ад'юванту повинен бути приблизно 6-8. Кінцевий L-лейциламіно-β-D-глюкопіранозил)-NрН приблизно 6 - 7 є кращим. Кінцевий рН є прибоктадецилдодеканоїламід ацетат. Спирт - етанол. лизно 6,3-6,4. Слабкою кислотою є оцтова кислота. Неіонні ПАР Вихідний розчин глікозиламіду містить надлиописані вище. шок кислоти та повинен бути буферованим для Отримання вихідних розчинів глікозиламідів. застосування як ад'юванту. Наприклад, фосфатСлабку кислоту додають до спиртового розчиний буфер можна зробити при певних рН у широну з вмістом гліколіпіду. Слабку кислоту додають у ких межах змішуванням одноосновних та двоосномолярному надлишку відносно вмісту гліколіпіду. вних солей натрій фосфат або калій фосфат у Слабку кислоту слід додавати у кількості від 1,25 різних пропорціях. Якщо застосовують фосфатний до 5 молярних еквівалентів відносно гліколіпіду. У буфер, його можна зробити приблизно при 20мМ, деяких втіленнях рекомендовані наступні відносні та він має рН приблизно 7,8. Коли вихідний розчин кількості кислоти. Слабкій кислоті слід бути у 2,0 глікозиламіду додають до буферу, рН буферу рази, 2,5 рази, 2,7 рази, 3,0 рази та 5,0 разів, а знижується. Буферований фосфатом розчин при найкраще у 2,7 рази більше за молями кислоти, рН7,8 призводить до кінцевого розчину гліколіпідніж молей гліколіпіду. ного ад'юванту з рН приблизно 6,4. Кінцеве довеНеіонну ПАР додають до суміші спиртдення рН можна зробити, але звичайно не необгліколіпід, перед або після добавки слабкої кислохідно. ти для створення кінцевого вихідного розчину гліВихідний розчин глікозиламіду з вмістом слабкозиламіду. кої кислоти та гліколіпіду має дуже низький рН. У присутності слабкої кислоти, глікозиламід Може бути необхідним доведення рН до прийнятперетворюється в ацетатну форму гліколіпіду. ного рівня. Сильна основа не підходить для цього, Гліколіпіди формули І не є повністю розчинними оскільки добавка сильної основи може перетворюпри уведенні безпосередньо у буферовані водні вати сольову форму гліколіпіду назад до несольорозчини. Розчин, звичайно отриманий від розчивої форми, призводячи до осадження (флокуляції) нення гліколіпіду формули І у буферованому воднесольової форми у водному середовищі. Однак, ному розчині є молочною сумішшю. Попередні якщо є бажаною сильна основа, слід застосовувадослідники намагалися отримати такі розчини готи тільки невеликі кількості. Наприклад, рекоменмогенних сумішей обробкою ультразвуком молочдують застосовувати не більше, ніж 100мМ NaOH, ного розчину. Однак, обробка ультразвуком не тоді як 4,0мМ або менше є оптимальними. гарантує, що розчин залишається гомогенним при Буферувальний розчин може необов'язково зберіганні. Хімічний підхід до суспендування цих містити трохи NaCI, але це не є потрібним. Концесполук призводить до повністю розчинного майже нтрації NaCI може бути приблизно 1 - 50мМ. Нижчі оптично прозорого розчину водного буферованого кількості NaCI є кращими. Приклади тут не мають гліколіпіду при прийнятному рН. Коли слабку кисNaCI або мають 15мМ NaCI. 100мМ NaCI не є лоту додають у надлишку у порівнянні з гліколіпіпридатним, оскільки відбувається флокуляція. дом, це гарантує, що усі гліколіпіди перетворюЖодної флокуляції не очікують з концентраціями ються у розчинну форму, та їх повернення назад NaCI 15мМ або менше. Жодної флокуляції не очідо нерозчинної форми є попередженим. кують з концентраціями NaCI 30мМ або менше. Слабка кислота перетворює гліколіпід у фарЖодної флокуляції не очікують з концентраціями мацевтично прийнятну сіль. Кращими солями є NaCI 50мМ або менше. нетоксичні солі, котрі звичайно застосовують у Частин II. Характеристика розчину гліколіпідфармацевтичних та біологічних препаратах. Наного ад'юванту. приклад, хлориди, ацетати, лактати та інертні солі Стабільність розчину гліколіпідного ад'юванту сполук формули І, отримують зі слабких кислот, при зберіганні можна відстежувати простим візуаописаних тут. льним спостереженням або застосуванням прийнСпиртами, застосовуваними для розчинення ятних аналітичних приладів. Молекули гліколіпіду гліколіпіду, можуть бути метанол, етанол, будь-які утворюють міцели у водному розчин та можливо ізомери пропанолу, або будь-яка їх комбінація. точно визначати розмір міцел лазерним дифракУтворений спиртовий розчин гліколіпіду повинен тометром. Такий вимір можна застосовувати для бути оптично прозорим. Будь-яка хімічна реакція, 21 90569 22 визначення будь-якої флокуляції молекул гліколірилової кислоти, що є перехресно зв'язаним із піду. поліалкеніл-етером. Альтернативний підхід до виміру стабільності Частина III. Застосування розчину гліколіпідноу реальному часі полягає у прискореному тестуго ад'юванту. ванні стабільності. У прискореному тестуванні Розчин гліколіпідного ад'юванту у фармацевстабільності ад'ювантний розчин піддають дії до тично прийнятній сольовій формі, можна змішуватемператури приблизно 37°С протягом приблизно ти з антигеном. Зручні антигени охоплюють: білки, 7 діб, а потім інкубують приблизно при 4°С протягл і ко протеїни, ліпопротеїни, пептиди, глікопептигом приблизно двох діб при постійному струшуди, ліпопептиди, токсоїди, вуглеводи мікробних ванні. Інкубування приблизно при 37°С протягом патогенів, та специфічні антигени пухлин. Антіанприблизно 7 діб представляє зберігання приблизтиген може бути похідним з багатьох джерел. Анно при 4°С протягом приблизно одного року. Інкутіантигени від мікробних патогенів стосується хвобування приблизно при 4°С протягом приблизно роб, що спричинюють бактерії, віруси, та паразити. двох діб з постійним струшуванням представляє Суміші двох або більш антигени можна застосовунапружений стан розчину гліколіпідного ад'юванту вати. Антиген може бути вбитим, природним поспри транспортуванні. лабленим, модифікованим живим, або білковим Для визначення, чи є розчин гліколіпідного екстрактом, рекомбінантно продукованим білком, ад'юванту ізотонічним з цитоплазмою, можна вихімічно синтезованим пептидом або будь-чим, що значати осмолярність. Різні концентрації натрій стимулює імунну реакцію. Пептидний антиген мохлориду можна додавати та осмолярність утвореже бути вільним пептидом або кон'югованим з гліного розчину визначати, застосовуючи осмометр. коліпідом або кон'югованим з іншими відомими Збільшення концентрації натрій хлориду, окрім епітопами В-клітин або Т-клітин. збільшення осмолярності також стимулює помутСтабільний розчин гліколіпідного ад'юванту ніння. Мутність, як вважають, є викликаною агреможна комбінувати із додатковими ад'ювантами гуванням міцел у більші частинки. Розчини, що або компонентами, котрі є відомими як такі, що важко або неможливо фільтрувати, застосовуючи мають властивості ад'юванту. Додаткові ад'юванфільтр 0,2 мкМ є загалом не прийнятними для ти, що можна комбінувати з розчином гліколіпіднокомерційного застосування, оскільки кінцеве фільго ад'юванту, охоплюють полімери, природно істрування є часто застосовуваним для гарантуваннуючі терпеноїдні сполуки у їх сирій або частково ня стерильності ад'ювантних розчинів, отриманих очищеній формі, амфіфільні четвертинні аміни, у комерційному масштабі. Електронний мікроскопохідні стінок бактеріальних клітин та синтетичні пічний аналіз можна застосовувати для визначенаналоги стінок бактеріальних клітин або компонення, чиє агрегування міцел результатом кількості ти ДНК. Розчин гліколіпідного ад'юванту можна солі. застосовувати разом або комбінованим з одним Додаткові негліколіпідні ад'юванти можна заабо більше агентами, як-то антибіотики або різні стосовувати у розчині гліколіпідного ад'юванту у антигени. Бактеріальні або вірусні антигени мокомбінації з описаними вище. У ще одному втіленжуть бути вбитими, чи модифікованими живими. ні винаходу додаткові імуностимулювальн молекуВбиті вірусні антигени отримують вирощуванням ли додають до розчину гліколіпідного ад'юванту. вірусів у культурі тканин та інактивуванням вірусів Імуностимулювальні молекули є добре відомими у хімічною обробкою. Деякі віруси можна вирощуварівні техніки та охоплюють сапоніни, Quil А, димети в ембріонах яєць. Вбитий вірусний антиген мотилдіоктадециламоній бромід (DDA) та Карбопол. жна додавати до розчину з вмістом розчину глікоQuil А є очищеним екстрактом кори південноліпідного ад'юванту, а утворений розчин можна американського дерева Quillaja saponaria. Quil А застосовувати для вакцинації тварини для досягіндукує гуморальні та опосередковані клітинами нення захисту проти вірусної інфекції. реакції. Quil А є часто застосовуваним з холестеВ одному втіленні цього винаходу, розчин глірином, оскільки холестерин усуває менш бажану коліпідного ад'юванту можна застосовувати як побічну дію, коли є доданим у прийнятних пропоррозріджувач для модифікованих живих вірусних ціях. Холестерин утворює нерозчинні комплекси із антигенів. Вірусні патогени можуть бути послаблеQuil А, що утворюють спірального типу структури, ними у вірулентності їх пасажуванням у культурі оскільки холестерин зв'язується з Quil А, таким тканин протягом кількох генерацій або певними чином оголюючи елементи молекул цукру, що доманіпуляціями з вірусним геномом. Такі послаблепомагають стимулювати імунну реакцію. ні штами вірусів можна вирощувати до дуже висоДиметилдіоктадециламоній бромід, DDA, є каких титрів у культурі тканин та можна застосовуватіонною ПАР з алкіл-ланцюгами з 18 атомів карботи як вакцинні антигени. Послаблені вірусні штами ну. Він є амфіфільним четвертинним аміном. Безпозначені як модифіковані живі вірусні антигени. посередня взаємодія DDA та антигену є Тоді як ці штами є менш вірулентними, вони є ще необхідною для отримання оптимальної імунної високо імуногенними при застосуванні як антигенів реакції, оскільки функції DDA як носія антигену у вакцині та дають захист проти інфекції вірулентбезпосереднім зв'язуванням антигену на поверхні ними штамами. Слід застосовувати розчин гліколірозділу олія/вода. Це стимулює гуморальні та опопідного ад'юванту як розріджувач для антигенів середковані клітинами імунні реакції. модифікованого живого вірусу, розчин гліколіпідКарбопол є ще одним корисним імуностимуного ад'юванту слід тестувати для гарантії, що це лювальним засобом, що можна застосовувати не матиме будь-якого віруліцидного впливу на згідно з цим винаходом. Він є гомополімером акконкретний розглянутий вірус. 23 90569 24 Віруліцидну властивість розчину гліколіпідного лейциламіно-β-D-глюкопіранозил)-Nад'юванту стосовно антигенів модифікованого жиоктадецилдодеканоїламід. Коли цю сполуку застового вірусу можна визначати у дослідженні in vitro. совують для отримання ад'ювантного розчину, Ліофілізовані вірусні антигени регідратують розчизастосовуючи композиції, описані у таблиці 1 вином гліколіпідного ад'юванту або водою. Утворені ще, де оцтову кислоту застосовують в однаковій розчини вірусу поміщають на моношар пермісивмолярній концентрації з гліколіпідом, а гліколіпід є них клітин. Титр вірусного антигену визначають у формі вільної основи, гліколіпід є нерозчинним підрахунком числа утворених на моношарі блята флокулює. шок. Відмінність отриманих вірусних титрів між Приклад 2. Розчинний вихідний розчин глікозразками, регідратованими водою та розчином зиламіду, застосовуючи ті ж компоненти як у прикгліколіпідного ад'юванту, можна застосовувати для ладі 1, але зі збільшенням концентрації оцтової визначення, чи є будь-який віруліцидний вплив кислоти відносно концентрації гліколіпіду, призворозчину гліколіпідного ад'юванту на будь-який жидить до розчинного вихідного розчину глікозиламівий вірус. ду. Антигени модифікованого живого вірусу можуть бути ліофілізованими та запропонованими як Таблиця 2 ліофілізовані брикети при отриманні комерційних вакцин. Загалом ці ліофілізовані брикети антигенів Композиція вихідного розчину глікозиламіду модифікованого живого вірусу регідратують розчином розріджувачу та застосовують для парентеРеагент Кількість (50мл) ральної вакцинації. Приклади розріджувачів охопЕтанол (60об.%) 44,64мл люють водний розчин з вмістом буферованого Tween 20 1,12мл фосфатом фізіологічного розчину. Якщо розріджуЛьодяна оцтова кислота 0,68мл вальний розчин містить відомі імуностимулювальні Bay 15-5831® 3,49г молекули, ефективність вакцинації антигенами модифікованого живого вірусу може бути поліпшеТут застосовували 60об.% етанол, а молярне ною. В одному втіленні заявленого винаходу розспіввідношення оцтової кислоти з гліколіпідомом є чин гліколіпідного ад'юванту застосовують як роз2,0. 200-нормативний етанол прикладу 1 заміняли ріджувальний розчин. сумішшю 60% етанол-вода. Утворений вихідний Приклади розчин глікозиламіду був оптично прозорим та не Приклад 1. Отримання нерозчинної композиції осаджувався на дні ємності. Це вихідний розчин глікозиламідів з однаковою концентрацією Bay 15глікозиламіду додають до різних буферів для 5831® та оцтової кислоти. отримання розчину гліколіпідного ад'юванту у прикладі 3, нижче. Таблиця 1 Приклад 3. Отримання розчинів гліколіпідного ад'юванту. Були отриманими розчини фосфатного Композиція, не придатна буферу при різних рН. 2Μ вихідний розчин одноодля комерційного застосування сновного натрій фосфату було отримано розчиненням 138 грамів NaH2PO4·H2O у 250мл ДІ води Реагент Кількість (200мл) при кінцевому об'ємі 500мл. Подібно 2М вихідний Етанол (100%) 176,1мл розчин двоосновного натрій фосфату було отриTween 20 4,0мл мано розчиненням 142 грам NaH2PO4 у 300мл ДІ Льодяна оцтова кислота 1,5мл води при кінцевому об'ємі 500мл. Обидва вихідні Bay 15-5831® 18,4г розчини стерильно фільтрували, застосовуючи фільтр 0,2 мікрон. Bay 15-5831® є зареєстрованим Bayer Company, під торговою назвою N-(2-дезокси-2-LТаблиця 3 Композиції 1М вихідного розчину натрій фосфатного буферу при різних рН Розраховано Розчин Розчин Загальний об'єм 2М Стерильна ДІ Загальний об'єм 1М РН Na2HPO4 (мл) NаН2РО4Н2О (мл) вихідного розчину (мл) вода (мл) вихідного розчину (мл) 6,0 87,7 12,3 100 100 200 6,5 68,5 31,5 100 100 200 7,0 39,0 61,0 100 100 200 7,5 16,0 84,0 100 100 200 7,8 8,5 91,5 100 100 200 Різні об'єми 2М вихідних розчинів одноосновного натрій фосфату та двоосновного натрій фосфату, як показано у таблиці 3 отримували, тоді 1М вихідні розчини натрій фосфатного буферу отримували при різних рН. 1М розчини фосфатного буферу тоді розбавляли 50Х для отримання 20мМ фосфатних буферів. Розчини гліколіпідного ад'юванту отримували, застосовуючи ці вихідні буфери та вихідні розчини глікозиламідів з прикладу 2. 25 90569 26 До 96мл кожного з цих 20мМ розчинів фосфагустини (О.Г.) при 600нм, у таблиці 4 порівнювали ту додавали 5мл вихідного розчину глікозиламіду, з подібними зчитуваннями у таблиці 5, де розчини отриманого у прикладі 2. Утворений розчин глікогліколіпідного ад'юванту отримували із вихідними ліпідних ад'ювантів містив 12,5мМ оцтової кислоти розчинами глікозиламідів з вмістом удвічі більшого та 6,33мМ гліколіпіду. Гліколіпід є зараз у формі молярного співвідношення оцтової кислоти з гліацетату. коліпідом, ніж отриманого у прикладі 2. ЗастосуПриклад 4. Значність кінцевого рН розчину глівання більшої концентрації або кількості оцтової коліпідного ад'юванту. кислоти призводить до мінімальної флокуляції. У ще одному з експериментів, значність кінцеФлокуляція була вищою у нефільтрованому зразвого рН різних розчинів тестували для оцінювання, ку, ніж у фільтрованих зразках. Більш того, зі збіяк рН впливає на флокуляцію. 20мМ фосфатний льшенням концентрації NaCI, є збільшення флобуфер отримували при початковому рН7,8. Табликуляції та навіть осадження. Розчин гліколіпідного ця 4 показує отриманий гліколіпідний ад'ювант, ад'юванту, описаний у таблиці 5, отримували з застосовуючи глікозиламід, отриманий як у прикфосфатним буфером, що має початковий рН8,0; ладі 1, де гліколіпід та оцтову кислоту застосовукінцевий рН розчину гліколіпідного ад'юванту був вали в однаковій молярній концентрації. Зауваміж 6,8 та 7,0. Подальше зниження кінцевого рН ження, кінцевий рН не знижувався дуже сильно розчину гліколіпідного ад'юванту може призводити (Таблиця 4), показуючи ефективність буферу. до розчину гліколіпідного ад'юванту з меншою муКонцентрації NaCI варіювали. Зчитування оптичної тністю та без флокуляції. Таблиця 4 Отримання композицій глікозиламідів з вмістом еквімолярної кількості оцтової кислоти та гліколіпідів. (Дивись Приклад 1.) Концентрація NaCI (мМ) 0 15 100 Об'єм буферу (мл) 480 480 480 Об'єм вихідної композиції гліколіпіду (мл) 25 25 25 Кінцевий pН О.Г. при 600нм 7,42 7,39 7,33 1,693 1,873 2,742 Таблиця 5 Отримання розчину гліколіпідного ад'юванту, застосовуючи вихідний розчин глікозиламіду з вмістом удвічі більшої молярної кількості оцтової кислоти та гліколіпіду. (Дивись Приклад 2.) Концентрація NaCI (мМ) 0 15 100 Об'єм буферу (мл) 480 480 480 Об'єм вихідного розчину глікозиламіду (мл) 25 25 25 Оптична густина (О.Г). менше, ніж 0,1, представляє напівпрозорий розчин. Оптична густина 0,1-0,5 показує гомогенність із слабкою мутністю, оптична густина 0,5-1,0 показує деяку мутність, оптична густина 1,0-1,5 показує суттєву мутність. Оптична густина 1,5 показує мутність та ймовірно не може бути фільтрованою, застосовуючи фільтр 0,2 мікрон. Останню загалом не вважають комерційно придатною. Приклад 5. Титрування гліколіпідного ад'юванту оцтовою кислотою, щоб показати флокуляцію може бути оберненим. Для визначення, чи обертатиме флокуляцію додавання збільшуваної кількості оцтової кислоти до гліколіпідного ад'юванту, що показує флокуляцію, отримували гліколіпідний ад'ювант як описано у прикладі 1. Цей гліколіпідний ад'ювант показував флокуляцію навіть у відсутності NaCI. Збільшувану концентрацію оцтової кислоти додавали до цієї флокульованої суміш гліколіпідного ад'юванту. Оцтову кислоту розбавляли у 16,6 разів водою для отримання робочих концентрацій розчину 1моль. Тоді 15 мкл цього 1М розчину додавали до 15мл суміші гліколіпідного ад'юванту для збільшення концентрації оцтової Кінцевий РН О.Г. при 600нм 6,93 6,88 6,84 0,146 0,487 2,826 кислоти на 1мМ. Із збільшенням концентрації оцтової кислоти, рН гліколіпідного ад'юванту знижується та флокулянти розчиняються. Однак, гліколіпідний ад'ювант залишався іноді мутним. Це спостереженням підтверджує, що збільшення концентрації оцтової кислоти перетворює вільну основу Bay 15-5381 у ацетатну форму, котра є більш розчинною у водному розчині. Таблиця 7 Титрування гліколіпідного ад'юванту оцтовою кислотою Об'єм гліколіпідного Доданий об'єм 1Η рН розад'юванту оцтової кислоти чину 15мл 0 7,25 15мл 15мкл (1мМ) 7,21 15мл 30мкл (2мМ) 7,10 15мл 60мкл (4мМ) 6,97 15мл 150мкл (10мМ) 6,44 15мл 750мкл (50мМ) 4,57 27 90569 28 Приклад 6. Отримання другого стабільного розчину гліколіпідного ад'юванту з NaCI та без нього. Таблиця 8 Після встановлення важливості збільшення кількості оцтової кислоти у підтримуванні стабільності Композиція вихідного розчину глікозиламіду розчинів гліколіпідів, було вирішено застосовувати композицію, показану у таблиці 8 для отримання Реагент Кількість (200мл) спершу вихідного розчину глікозиламіду та тоді 60% Етанол (v/v) 179мл для отримання ще одного розчину гліколіпідного Tween 20 4,0мл ад'юванту з NaCI та без нього. Цей вихідний розОцтова кислота 3,0мл чин глікозиламіду є подібним розчину у прикладі 2, Bay 15-5381 13,96 грам з у 4 рази більшим загальним об'ємом та відносно більшою кількістю оцтової кислоти та Twee n 20. Три різні розчини гліколіпідного ад'юванту з різними концентраціями NaCI отримували, застосовуючи фосфатний буфер з прикладу 3 та вихідний розчин глікозиламіду, отриманий як у таблиці 8. Аналогічно композиції у прикладі 4, Таблиця 5, отримували розчини гліколіпідного ад'юванту, що містили 0мМ, 15мМ, та 100мМ NaCI. Розчини з вмістом 0мМ та 15мМ NaCI фільтрували через фільтр 0,2-мікрон. Розчин гліколіпідного ад'юванту з вмістом 100мМ NaCI не фільтрували через фільтр 0,2-мікрон. Таблиця 9 Отримання стабільних розчинів гліколіпідного ад'юванту з NaCI та без нього Концентрація натрій хлориду (мМ) 0 15 100 Об'єм буферу (мл) 465 465 465 Об'єм вихідного розчину Кінцевий РН глікозиламіду (мл) 35 6,39 35 6,37 35 6,29 20мл кожного з розчинів гліколіпідного ад'юванту поміщали у склянки 30мл та інкубували при кімнатній температурі та при 4°С. Візуальні спостереження отримували з регулярними інтервалами. Спочатку розчин гліколіпідного ад'юванту з 0мМ NaCI був оптично прозорим. Розчин гліколіпідного ад'юванту з вмістом 15мМ NaCI був слабко мутним та мав О.Г. 0,073 при 600 нм. Розчин гліколіпідного ад'юванту з вмістом 100мМ NaCI був мутним та мав О.Г. 0,439 при 600нм. Таблиця 9. Жодний з цих розчинів гліколіпідного ад'юванту не показував будь-яких ознак флокуляції при кімнатній температурі та при 4°С. Ці розчини гліколіпідного ад'юванту спостерігали протягом одного року без змін вигляду. Приклад 7. Титрування стабільного розчину гліколіпідного ад'юванту із NaOH. Спочатку оптично прозорий та стабільний розчин гліколіпідного ад'юванту отримували без NaOH. Для встановлення, що усунення або застосування мінімальної кількості NaOH було суттєвим для попередження флокуляції, необхідно показати, що поступова добавка NaOH може індукувати флокуляцію в інакше стабільній гліколіпідній суміші. Прийнятні об'єми 1N NaOH додавали до 15мл розчину гліколіпідного ад'юванту без будь-якого NaCI, як отримано у таблиці 10, нижче. NaOH збільшували поступово від 1мМ до 12мМ. (Таблиця О.Г, при 600нм 0,039 0,073 0,439 10) Розчин гліколіпідного ад'юванту, застосовуваний у цьому дослідженні, отримували, застосовуючи вихідний розчин глікозиламіду, описаний у прикладі 6. Зі збільшенням концентрації NaOH у розчині гліколіпідного ад'юванту, рН композиції поступово збільшувався разом з флокуляцією. Таблиця 10 Титрування стабільного розчину гліколіпідного ад'юванту з NaOH Об'єм гліколіпідного Доданий об'єм 1N рН розчиад'юванту NaOH (мM) ну 15мл 0 6,21 15мл 15мкл (1мМ) 6,38 15мл 30мкл (2мМ) 6,48 15мл 60мкл (4мМ) 6,68 15мл 150мкл (10мМ) 7,11 15мл 750мкл (50мМ) 12,17 Приклад 8. Кількісний аналіз гліколіпіду, застосовуючи ВЕРХ. Нижченаведені способи застосовували в аналізі ВЕРХ Bay 15-5831®. Застосовували ВЕРХпараметри, описані у таблиці 11. 29 90569 30 Таблиця 11 Параметри, застосовувані у способі кількісного аналізу за допомогою ВЕРХ Bay 15-5381 Параметр Колонка Деталі Hamilton PRP-1, 7 мікрон, 250 4,6мм Потік 1,5мл/хвилин Об'єм ін'єкції 10мкл Довжина хвилі детек- 210нм тора Мобільна фаза А 0,4об.% перхлоратна кислота Мобільна фаза В Ацетонітрил Градієнт 0 хвилин 40% А/60% В 15 хвилин 30% А/70% В 20 хвилин 30% А/70% В 35 хвилин 10% А/90% В 50 хвилин 10% А/90% В 51 хвилин 40% А Час перебігу 65 хвилин Час утримання Bay 15- Приблизно 25 хвилин 5381 Таблиця 12 Стандарти Bay 15-5831® Стандарт 1 2 3 4 5 6 Концентрація 0,103мМ 0,206мМ 0,412мМ 0,618мМ 0,824мМ 1,03мМ Стандарти у межах 0,10-1,03мМ отримували та ін'єктували у ВЕРХ. Стандарти показано у таблиці 12. Зразки нагрівали до кімнатної температури та інвертували 5 разів перед застосуванням. Один мл зразку додавали до 6мл метанолу у 10мл мірній колбі. Зразки тоді обробляли ультразвуком протягом 10 хвилин та тоді розбавляли до об'єму та змішували. Нелінійну регресію проводили на стандартах з площами піків проти концентрації. Зразки були тоді розраховані за кривими. Приклад 9. Масштаб отримання 30л. Отримували 30л розчину гліколіпідного ад'юванту зі складом, описаним у прикладі 6. Ця партія містила 15мМ NaCI. Застосовуючи ці 30л, отримували 5 різних розчинів зі збільшенням концентрації NaOH. Концентрація. NaOH збільшували від 0мМ до 1мМ, 2мМ, 4мМ, 8мМ та 12мМ. Зразок для кожної концентрації NaOH аліквотували для виміру рН та візуального спостереження. Зі збільшенням кількості NaOH, рН гліколіпідного ад'юванту збільшувався разом зі збільшенням флокуляції. Флокуляція при концентрації NaOH 2мМ при кімнатній температурі, а при 4 °С, флокуляція починалася при 4мМ NaOH. Таблиця 13 Характеристики партії 30л гліколіпідного ад'юванту зі збільшенням концентраці NaOH Зразок № 30л зразку 1 30л зразку 2 30л зразку 3 30л зразку 4 30л зразку 5 30л зразку 6 Опис 15мМ NaCI, ОмМ NaOH 15мМ NaCI, 1мМ NaOH 15мМ NaCI, 2мМ NaOH 15мМ NaCI, 4мМ NaOH 15мМ NaCI, 8мМ NaOH 15мМ NaCI, 12мМ NaOH Виміряна концентрація (мМ) 6,21 6,3 6,24 6,17 6,26 6,15 Кількість Bay 15-5381 в усіх 6 зразках показана у таблиці 13 аналізували, застосовуючи спосіб ВЕРХ, описаний у прикладі 8. Зразки з різними рН показували ті ж концентрації Bay 15-5381, вказуючи, що ад'ювант не розкладається при збільшенні рН при добавці NaOH та флокуляції. Приклад 10. Оцінки стабільності, застосовуючи прискорене тестування в обважненому режимі. Цей приклад описує способи та результати прискореного тестування в обважненому режимі розчину гліколіпідного ад'юванту. Три партії розчинів гліколіпідного ад'юванту отримували, як описано у прикладі 6, у масштабі 500л. Усі три партії мали 15мМ NaCI та не містили NaOH. Розчини гліколіпідного ад'юванту з цих трьох партій по 500л О.Г. при 600нМ 0,218 0,137 0,137 0,15 0,129 0,062 РН 6,42 6,52 6,59 6,80 7,06 7,54 застосовували для дослідження стабільності гліколіпіду, застосовуючи прискорене тестування стабільності. Для прискореного тестування в обважненому режимі розчин гліколіпідного ад'юванту піддавали дії струшування протягом 7 діб при 37°С, а потім струшування при 4°С протягом двох діб. 7 діб струшування при 37°С представляє старіння при 4°С протягом року. Струшування при 4°С протягом двох діб представляє обважнення при транспортуванні. Один розчин гліколіпідного ад'юванту тримали статичним при 37°С протягом 7 діб, тоді струшували при 100об./хвил. при 4 °С протягом ще 2 діб. При чотирьох моментах часу, тобто Т=0, 3, 7, та 9 31 90569 32 доби, спостереженням та фотозображення реєстУ таблиці 15, контрольні зразки тримали при рували. При 2 моменти часу, тобто Т=0 та 9 доби, 4°С протягом 7 діб, тоді як тест-зразки струшували Індекс рефракції та розмір частинок аналіз тоді при 37°С протягом 7 діб. Зразки, що струшували проводили. при 37°С протягом 7 діб мають концентрації подібДругий розчин гліколіпідного ад'юванту струну концентрації, що зберігали при 4°С. шували при 100об./хвил. при 37°С протягом 7 діб; Приклад 11. Віруліцидне тестування розчину тоді струшували при 100 об/хвил при 4°С протягом гліколіпідного ад'юванту. ще 2 діб. При чотирьох моментах часу, тобто Т=0, Віруліцидне тестування проводили на розчині 3, 7, та 9 діб, спостереження та фотозображення гліколіпідного ад'юванту, отриманому у масштабі реєстрували. При 2 моментах часу, тобто Т=0 та 9 30 л, як описано вище у прикладі 9. Цей розчин діб, тоді проводили аналіз індексу рефракції та гліколіпідного ад'юванту містив 15мМ NaCI та не розміру частинок. містив NaOH. Третій розчин гліколіпідного ад'юванту тримаГліколіпідний ад'ювант тестували на його прили статичним при 4 °С протягом 9 діб як контроль. датність для застосування як розріджувачу з моУ чотири моменти часу, тобто Т=0, 3, 7, та 9 діб, дифікованими живими вірусами. Антигени модифіреєстрували спостереження та фотозображення. кованого живого вірусу отримують як висушені У 2 моменти часу, тобто Т=0 та 9 діб проводили сублімацією пробки. При регідратації цих пробок з аналіз індексу рефракції та розміру частинок. придатним розчином гліколіпідного ад'юванту, буНе було змін розміру частинок як результату ло підтверджено, що застосовуваний розчин глікотестування в обважненому режимі. Усі зразки підліпідного ад'юванту не знищує модифікованих житримували субмікронний розмір частинок, як спових вірусів. Розчин гліколіпідного ад'юванту стерігали у зразках негайно після їх отримання. тестували проти трьох вірусних антигенів корів: Більш того, вимір компоненту Bay 15-5831® за респираторно-синцитіальний вірус корів (BRSV), допомогою ВЕРХ у зразках, що тримали при 4°С вірус парагрипу З (РІЗ), та вірус інфекційного риабо піддавали обважненню при 37°С протягом 7 нотрахеїту корів (IBR). діб, не показував будь-як змін кількості Bay 15Вірусні пробки регідратували, застосовуючи 5831®. розчин гліколіпідного ад'юванту. Після інкубування при кімнатній температурі (RT) протягом 1 годин, Таблиця 15 зразки поміщали на моношар лінії пермісивних клітин з серійними розбавленнями. Підрахунком Кількісний аналіз Bay 15-5831® числа вірусних пробок, що виявляються на монопісля тестування в обважненому режимі шарі отримували 50% значення інфекційної дози на мл культур тканин (ТСID50/мл) для кожного вірусного антигену, ре гідратованого стерильною Номер партії розчину гліколіпід- Виміряна конценводою або розчином гліколіпідного ад'юванту. У ного ад'юванту та обробка трація (мМ) цьому аналізі зниження титру 0,7 після регідратації Партія 1-4°С 6,23 тест-розчином гліколіпідного ад'юванту вважали Партія 1-37°С Струшування 6,29 віруліцидним. Партія 2-4°С 6,32 Результати представлені у таблиці 16. Розчин Партія 2-37°С Струшування 6,30 гліколіпідного ад'юванту не показував будь-якого Партія 3-4°С 6,28 віруліцидного впливу на ці три віруси корів. Партія 3-37°С Струшування 6,29 Таблиця 16 Віруліцидний аналіз розчину гліколіпідного ад'юванту Вірус tslBR 051404 tsPI3 052604 BRSV 081103 Вихідний титр 7,3±0,5 Кінцевий титр з гліколіпід- Кінцевий титр зі стериним ад'ювантом льною водою 7,08 7,49 Втрата титру 0,42 7,6±0,5 7,74 7,49 -0,25 6,4±0,5 6,57 6,82 0,25 Цей приклад показує, що розчин гліколіпідного ад'юванту можна застосовувати у комерційній композиції вакцини для тварин. Rispoval® є обмеженим трьома різними вірусними хворобами корів, застосовуючи три модифіковані живі вірусні антигени. Цими вірусними антигенами корів є модифікований живий вірус герпесу корів, модифікований живий респираторно-синцитіальний вірус корів, та модифікований живий вірус парагрипу 3. Ці вірусні антигени продукують як ліофілізовані брикети та розчин гліколіпідного ад'юванту, продукований згідно з цим винаходом, можна застосовувати як розріджувальний розчин для цих антигенів. Застосовуваним гліколіпідом був N-(2-дезокси-2-Lлейциламіно-β-D-глюкопіранозил)-Nоктадецилдодеканамід ацетат. 33 90569 34 Приклади представлені для ілюстрації винацього винаходу повинні бути зрозумілими фахівходу. Вони не обмежують рамок винаходу. Багато цям. змін, варіацій, модифікацій, та інших застосувань Комп’ютерна верстка Т. Чепелева Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюGlycolipid adjuvant composition and process for the preparation thereof
Автори англійськоюDominowski Paul Joseph, Mannan Ramasamy Mannar, Mediratta Sangita
Назва патенту російськоюКомпозиция гликолипидного адьюванта (варианты) и способ ее получения
Автори російськоюДоминовски Поль Жозеф, Маннан Рамасами Маннар, Медиратта Сангита
МПК / Мітки
МПК: C07H 13/00, A61K 39/39, C07H 15/12
Мітки: спосіб, варіанти, гліколіпідного, композиція, ад'юванту, отримання
Код посилання
<a href="https://ua.patents.su/17-90569-kompoziciya-glikolipidnogo-adyuvantu-varianti-ta-sposib-otrimannya.html" target="_blank" rel="follow" title="База патентів України">Композиція гліколіпідного ад’юванту (варіанти) та спосіб її отримання</a>
Попередній патент: Безконтактна синхронна машина суміщеного типу
Наступний патент: Спосіб переробки нафтопродуктів
Випадковий патент: Пристрій для аналізу газів (варіанти) та пристрій для взяття проби газу