Екстракція молочної кислоти
Номер патенту: 113530
Опубліковано: 10.02.2017
Автори: Декіч Живковіч Таня, ван Крікен Ян, де Хан Андре Бан'є
Формула / Реферат
1. Спосіб регенерації молочної кислоти з водної суміші, який включає наступні етапи:
- забезпечення водної суміші, яка містить молочну кислоту та принаймні 5 мас. % розчиненого магнію хлориду, базованого на загальній масі води, та розчинення матеріалу у водній суміші,
- екстрагування молочної кислоти з водної суміші в першу органічну рідину, яка містить принаймні 90 мас. % органічного розчинника, вибраного із групи, яка складається з наступного: кетони С5+, діетилетер та метил-третинний-бутил-етер, отримуючи, таким чином, органічний розчин молочної кислоти та водну відпрацьовану рідину, яка містить магнію хлорид, та
- екстрагування молочної кислоти з органічного розчину молочної кислоти у водну рідину, отримуючи, таким чином, водний розчин молочної кислоти та другу органічну рідину.
2. Спосіб за п. 1, де водна суміш містить принаймні 15 мас. % розчиненого магнію хлориду, базованого на загальній масі води та розчиненого матеріалу у водній суміші.
3. Спосіб за п. 1 або 2, де органічний розчинник - кетон С5-С8.
4. Спосіб за п. 3, де органічний розчинник є метил-ізобутил-кетоном.
5. Спосіб за будь-яким із попередніх пунктів, де перший етап екстракції здійснюють при температурі принаймні 30 °C.
6. Спосіб за будь-яким із пп. 1-5, де другий етап екстракції здійснюють при температурі, яка є нижчою, ніж температура, при якій здійснено першу екстракцію.
7. Спосіб за п. 6, де другий етап екстракції здійснено при температурі на 10-50 °C нижче, ніж температура, при якій здійснено першу екстракцію.
8. Спосіб за будь-яким із пп. 1-6, де другий етап екстракції здійснено в межах 10 °C температури, при якій здійснено першу екстракцію.
9. Спосіб за будь-яким із пп. 1-8, де органічна рідина не містить екстрагентів.
10. Спосіб за будь-яким із пп. 1-8, де органічна рідина не містить екстрагентів аміну.
11. Спосіб за будь-яким із пп. 1-10, де органічна рідина, по суті, є вільною від амінів, етерів та спиртів, що означає, що ці сполуки, якщо присутні повністю, кожна присутня в кількості, меншій 2 мас. %, обчисленій щодо маси органічної рідини.
12. Спосіб за будь-яким із пп. 1-11, де водна суміш має рН 2 або нижче.
13. Спосіб за будь-яким із пп. 1-12, який додатково включає:
- піддавання розчину магнію хлориду етапу термічного розкладу при температурі принаймні 300 °C, розкладаючи, таким чином, сіль магнію хлориду до магнію оксиду та НСl, та
- розчинення НСl, утвореної в етапі термічного розкладу у воді, отримуючи, таким чином, розчин НСl.
14. Спосіб за будь-яким із пп. 1-12, що додатково включає:
- піддавання розчину магнію хлориду етапу термічного розкладу при температурі принаймні 300 °C, розкладаючи, таким чином, сіль магнію хлориду до магнію оксиду та НСl, та
- розчинення НСl, утвореної в етапі термічного розкладу у воді, отримуючи, таким чином, розчин НСl, та
- рециркуляція магнію оксиду в етапі ферментації як засобу нейтралізації або попередника цього.
15. Спосіб за будь-яким із пп. 1-14, що додатково включає етап ферментації для створення молочної кислоти, причому етап ферментації включає етапи бродіння джерела карбону за допомогою мікроорганізму у ферментаційному бульйоні для створення молочної кислоти та нейтралізації принаймні частини молочної кислоти додаванням магнієвої основи, отримуючи, таким чином, відповідний лактат.
16. Спосіб за п. 15, який додатково включає етап отримання водної суміші підкислюванням солі лактату HCl, отримуючи, таким чином, водну суміш.
17. Спосіб за п. 16, який додатково включає етап концентрування цієї отриманої водної суміші до екстракції до концентрації розчиненої солі принаймні 5 мас. %, що базовано на загальній масі води та розчиненого матеріалу у водній суміші.
Текст
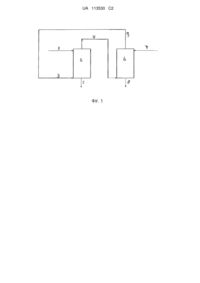
Реферат: Винахід стосується способу регенерації молочної кислоти з водної суміші, який охоплює наступні етапи: - забезпечення водної суміші, яка містить молочну кислоту та принаймні 5 мас. % розчиненого магнію хлориду, що базовано на загальній масі води та розчиненого матеріалу у водній суміші, - екстрагування молочної кислоти з водної суміші в першу органічну рідину, яка містить органічний розчинник, вибраний із групи, яка складається з наступного: кетони С5+, діетилетер та метил-третинний-бутил-етер, отримуючи, таким чином, органічний розчин молочної кислоти та водної відпрацьованої рідини, яка містить магній хлорид, та - екстрагування молочної кислоти з органічного розчину молочної кислоти у водну рідину, отримуючи, таким чином, водний розчин молочної кислоти та другу органічну рідину. Спосіб, згідно з винаходом, дозволяє комбіноване очищення та етап концентрації розчинів молочної кислоти вихідної реакційної суміші. UA 113530 C2 (12) UA 113530 C2 UA 113530 C2 5 10 15 20 25 30 35 40 45 50 55 Екстракція молочної кислоти Винахід стосується способу отримання розчину молочної кислоти, застосовуючи екстракцію. Виділення молочної кислоти з водної суміші, яка містить домішки, як-то солі, може бути важким. Молочну кислоту можна виготовляти через ферментацію мікроорганізмами джерела карбону, як-то вуглеводи або гліцерин. У такому способі джерело ферментації вуглеводу типово зброджують мікроорганізмом для створення молочної кислоти. Рідину, де завершено бродіння джерела вуглеводу, названо ферментаційним бульйоном або середовищем ферментації. Формування молочної кислоти протягом ферментації призводить до зменшення pH ферментаційного бульйону. Оскільки таке зменшення pH може пошкоджувати процес метаболізму мікроорганізмів, існує загальна практика додавати засіб нейтралізації, тобто основу, у середовище ферментації, щоб нейтралізувати pH. Як результат, отримана в середовищі ферментації молочна кислота типово присутня у вигляді солі лактату. Хоч є мікроорганізми, які достатньо стійкі до кислотних середовищ, за умови, щоб ферментацію можна робити при низькому pH (наприклад, при pH 3), навіть у таких процесах, принаймні, частину молочної кислоти отримують як сіль лактату. Щоб виділяти молочну кислоту з ферментаційного бульйону після ферментації, потрібна обробка спадним потоком. У такій обробці сіль лактату у ферментаційному бульйоні треба перетворювати до молочної кислоти. Також, молочну кислоту (або лактат, якщо ще не перетворено) треба виділяти з ферментаційного бульйону. Оскільки ферментаційний бульйон містить багато сполук, охоплюючи значні кількості біомаси (як-то мікроорганізми) та солі (походженням із засобу нейтралізації), отримання знову та виділення молочної кислоти може бути досить складним, типово потребуючи багаторазових етапів обробки, та призводячи до відходів, зокрема, втрати солі. У WO95/03268 описано спосіб регенерації органічної кислоти з ферментаційного бульйону очищенням бульйону для видалення, принаймні, суттєвої порції домішок, продукуючи вихідну реакційну суміш; підкислюючи вихідну реакційну суміш додаванням кількості мінеральної кислоти, ефективної для зниження pH вихідної реакційної суміші, приблизно, між 1,0 - 4,5, продукуючи підкислену вихідну реакційну суміш, котра є істотно насиченою стосовно, принаймні, одного електроліту, вибраного з групи, яка складається з MHSO 4, M2SO4, M3PO4, M2HPO4, MH2PO4, та MNO3, де M вибрано з групи, яка складається з Na, NH 4, та K; екстрагуючи підкислену вихідну реакційну суміш екстракційною сумішшю, котра містить (a) воду, (b) мінеральну кислоту в кількості, ефективній для втримання pH вихідної реакційної суміші, приблизно, між 1,0 − 4,5, та (c) насичений киснем розчинник, котрий має обмежену змішуваність з водою. Екстракція продукує екстракт розчиннику та перший рафінат. Екстракт розчиннику піддано зворотній екстракції водною рідиною, таким чином, продукуючи збагачений органічною кислотою водний екстракт та рафінат розчиннику, збіднений органічною кислотою. У WO00/17378 описано виготовлення молочної кислоти через ферментацію, регулювання pH за допомогою Ca(OH)2 або Mg(OH), додавання HCl, та екстракцію розчинником, вибраним із наступного: аміни, спирти та етери, краще - ізоаміловий спирт, діізопропіловий етер та Аламін 336. Тоді розчинник, який містить молочну кислоту, контактує з водою для генерування розчину молочної кислоти, котру оброблено далі. У CN101979368 описано екстракцію кислоти з розчину, який містить сіль. Сіллю може бути натрій хлорид. Екстрагент − метанол, етанол, н-пропанол, ізопропанол, н-бутанол, ізобутанол, ацетон, етиленгліколь, діетилетер, метилацетат або етилацетат. У JP8-337552 описано перетворення солі кислоти до кислоти, застосовуючи сульфатну кислоту або HCl. Кислотою може бути, наприклад, молочна кислота. Екстракція відбувається оксигенованим насиченим гетероциклічним типом сполук, наприклад, тетрагідрофураном. Існують різні проблеми, пов'язані зі способами, описаними в наведених вище посиланнях. Конкретною проблемою щодо послідовності екстракції, а потім − зворотної екстракції є формування розбавлених рідин. Звичайно, коли сполуку екстраговано з води, застосовуючи органічну рідину, а потім екстраговано з органічної рідини, застосовуючи воду, концентрація сполуки у водній рідині продукту є нижчою ніж у вихідній водній рідині. Це, звичайно, є несприятливим, оскільки генерує розбавлені рідини, котрі потребують подальшої концентрації. Отже, існує потреба в рівні техніки щодо способу екстракції/зворотної екстракції для молочної кислоти, котрий дозволяє виділення молочної кислоти з розчину солі без формування розбавлених розчинів кислоти, та без формування кристалів солі. Згідно із заявленим винаходом запропоновано такий спосіб. Заявлений винахід стосується способу регенерації молочної кислоти з водної суміші, який охоплює наступні етапи: 1 UA 113530 C2 5 10 15 20 25 30 35 40 45 50 55 - забезпечення водної суміші, яка містить молочну кислоту та, принаймні, 5 мас. % розчиненого магній хлориду, базоване на загальній масі води та розчиненого матеріалу у водній суміші, - екстрагування молочної кислоти з водної суміші в першу органічну рідину, яка містить органічний розчинник, вибраний із групи, яка складається з наступного: кетони C5+, діетилетер та метил-третинний-бутил-етер, отримуючи, таким чином, органічний розчин молочної кислоти та водну відпрацьовану рідину, яка містить магній хлорид, та - екстрагування молочної кислоти з органічного розчину молочної кислоти у водну рідину, отримуючи, таким чином, водний розчин молочної кислоти та другу органічну рідину. Знайдено, що спосіб згідно із винаходом, котрий полягає в застосуванні конкретної кислоти, тобто молочної кислоти, в комбінації з конкретною сіллю, тобто магній хлоридом, у конкретній кількості, тобто у кількості, принаймні, 5 мас. % розчиненого магній хлориду, в комбінації з конкретним розчинником, призводить до способу, де концентрація молочної кислоти у водному розчині, отриманому після подальшої екстракції та зворотної екстракції, є вищою ніж у водній суміші до екстракції. Цей ефект концентрації, наприклад, є сприятливим, коли водний розчин молочної кислоти, отриманий після зворотної екстракції, є концентрованим, у цьому випадку заощаджено вартість енергії випаровуванням меншої кількості води для отримання певної концентрації молочної кислоти. Крім того, переваги способу згідно з винаходом стають очевидним із наступного опису. Відомо, що в US2710880 описано вилучення молочної кислоти з водного розчину, застосовуючи розчинник вода-розчинний у воді спирт або кетон, котрий має краще 3-4 атоми карбону. Розчин містить сіль, краще - сульфат. Розчинник видаляють з екстракту дистиляцією. У GB280969 описано екстракцію молочної кислоти, застосовуючи етер або вищий спирт у присутності розчинного сульфату, отриманого із сульфатної кислоти. Фосфатну кислоту та щавлеву кислоту згадано як альтернативні. Відомо, що в CN101979368 описано екстракцію кислоти з розчину, який містить сіль. Екстрагент − метанол, етанол, н-пропанол, ізопропанол, н-бутанол, ізобутанол, ацетон, етиленгліколь, діетилетер, метилацетат або етилацетат. У JP8-337552 описано перетворення солі кислоти до кислоти, супроводжуване екстракцією оксигенованим насиченим гетероциклічним типом розчиннику. У GB173479 описано реакцію магній лактату із придатною кислотою, а потім − екстракція. Підкислення робили сульфатною кислотою; екстракцію робили ацетоном або етером, пристосованим розчиняти молочну кислоту. Розчинник видалено випаровуванням або дистиляцією. У розглянутих вище посиланнях не описано спосіб зворотної екстракції. Отже, ці посилання не є доречними. Не бажаючи бути пов'язаними теорією, уважаємо, що один або більше з наступних ефектів можуть виникати в способі екстракції згідно з винаходом. Це може бути, коли присутність магній хлориду у водній суміші підсилює екстракцію молочної кислоти з водної суміш у першу органічну рідину. Це буде сприяти описаному вище ефекту концентрації. Друге, це може бути, коли розчинений магній хлорид зменшує розчинність органічного розчинника у воді.Зокрема, при вищих концентраціях розчиненого магній хлориду менше розчинника (як-то, наприклад, MIBK) може розчинятися у водній суміші. Цей ефект може підсилюватися при вищих температурах, зокрема, при температурі в діапазоні 20°-100 °C. Відповідно, попередню та/або зворотну екстракцію краще проводити при температурі, принаймні, при 25 °C, краще, принаймні, при 30 °C, ще краще, принаймні, при 40 °C. Уважаємо, що цей ефект взагалі є вірним для кетонів та етерів. Нижча розчинність органічної рідини у воді буде призводити до потоків із вищою чистотою та меншими втратами розчиннику в попередній та зворотній екстракції, та, отже, може призводити до більш ефективного способу. На відміну, розчинність води в спирті та розчинність спирту у воді збільшується при підвищенні температури в діапазоні 25 °C та 100 °C. Третє, розчинність води в органічному розчиннику протягом екстракції також може бути зменшено присутністю розчиненого магній хлориду. Четверте, знайдено, що розчинений магній хлорид може стримувати формування емульсії, таким чином, посилюючи відокремлення фази між водною та органічною рідинами. Зокрема, це є сприятливим, коли водна суміш містить сліди біомаси. Біомаса, яка виникає зі способу ферментації, типово містить сполуки, які можуть діяти як поверхнево-активні речовини. Отже, коли водна суміш, яка містить біомасу, контактує з органічним розчинником, типово, буде 2 UA 113530 C2 5 10 15 20 25 30 35 40 45 50 55 утворено емульсію. Таке формування емульсії є небажаним, оскільки це може порушувати спосіб екстракції та відокремлення фази. Далі нижче буде описано переважні втілення заявленого винаходу. На фігурі 1 надано схематичне відображення втілення заявленого винаходу. На фігурі 1, (1) - вихідна водна суміш, котра, коли її постачено до екстракційного реактору (2), вона контактує з органічною рідиною (3). Потік (4), котрий містить карбонову кислоту в органічній рідині, відведено з екстракційного реактора (2). Відпрацьовану водну рідину (5) також відведено з екстракційного реактора (2). Потік (4), який містить карбонову кислоту в органічній рідині, надано до зворотного екстракційного реактора (6), де він контактує з водною рідиною, надано лінією (7). Розчин продукту водної карбонової кислоти відведено через лінію (8). Органічну рідину відведено через лінію (9), та рециркульовано до екстракційного реактору (2) через лінію (3), необов'язково після проміжних етапів очищення (не показано). Термін "екстракція", який тут застосовано, стосується екстракції рідина-рідина, також відомий як екстракція розчинником. Екстракція розчинником є способом екстракції, базованим на відмінності розчинності сполуки в двох різних рідинах, тобто в даному випадку розчинність молочної кислоти у воді (присутньої у водній суміші та водній рідині) стосовно розчинності молочної кислоти в органічному розчиннику (присутньому в органічній рідині). Попередня екстракція - спосіб, де сполуку екстраговано із водної суміші в органічну рідину. Зворотна екстракція - спосіб, де сполуку екстраговано з органічної рідини до водної рідини. Термін "розчинність", який тут застосовано, стосується максимальної кількості сполуки, яка може бути розчиненою в певній кількості водної суміші при певній температурі. Попередня екстракція та зворотна екстракція, які застосовано в способі винаходу, базовані на відмінності в розчинності молочної кислоти у воді та органічному розчиннику при різних температурах. Розчинність сполуки в одному розчиннику стосовно іншого розчинника можна відображати в термінах коефіцієнту розподілу (DR). Це співвідношення надає позначку того, як сполуку розподілено між водною фазою (наприклад, водною сумішшю) та органічною фазою (наприклад, органічною рідиною) у двофазовій системі при рівновазі. Коефіцієнт розподілу можна визначати як співвідношення концентрації молочної кислоти, розчиненої в органічній фазі ([молочна кислота]органічна) до концентрації молочної кислоти, розчиненої у воді ([молочна кислота]водна), за умови, що дві фази є в рівновазі: DR = [молочна кислота]органічна / [молочна кислота]водна (1) З формули (1) можна робити висновок, що при вищому співвідношенні розподілення більше молочної кислоти розчинено в органічній фазі. Коефіцієнт розподілу залежить від багатьох перемінних, охоплюючи температуру та конкретну композицію органічної та водної фази. Наприклад, концентрація розчиненого магній хлориду у водній суміші та тип застосованого розчинника впливає на співвідношення розподілення. Протягом попередньої екстракції молочній кислоті слід краще розчинятися в органічному розчиннику ніж у воді. Отже, коефіцієнт розподілу в попередній екстракції бав би якнайбільшим. Зокрема, високий коефіцієнт розподілу протягом попередньої екстракції є бажаним, оскільки будь-якій молочній кислоті, присутній у відпрацьованій рідині, слід безпосередньо призводити до зменшення загального виходу молочної кислоти, коли цю відпрацьовану рідину не можна переробити та/або рециклізувати знов до способу, або застосувати з іншою метою та видалити. Якщо коефіцієнт розподілу протягом попередньої екстракції є високим, відносно малу кількість молочної кислоти слід було б втрачати, бо найбільша кількість молочної кислоти була б розчиненою в органічній рідині. Краще щоб DR у попередній екстракції, також позначене як D FE, дорівнювало, принаймні, 0,1, конкретніше, принаймні, більше 0,4, зокрема, принаймні, ще більше 0,8. Протягом зворотної екстракції зберігається протилежне. Молочна кислота краще б розчинялася у водній фазі ніж в органічній рідині. Краще щоб DR у попередній екстракції, також позначене як DВE, дорівнювало не більше ніж 0,5, зокрема, не більше ніж 0,3, ще, зокрема, не більше ніж 0,1. Якщо коефіцієнт розподілу для попередньої екстракції є вищим ніж коефіцієнт розподілу для зворотної екстракції, це сприятиме ефекту концентрації, де водний розчин молочної кислоти, отриманий після зворотної екстракції, має вищу концентрацію молочної кислоти ніж водна суміш, застосована як вихідний матеріал у попередній екстракції. Краще співвідношення між DFE та DBE дорівнювало, принаймні, 1,1, ще краще, принаймні, 2. Співвідношенню між DFE та DBE звичайно не слід бути більшим 10. Діапазон 2 − 5 може бути кращим. 3 UA 113530 C2 5 10 15 20 25 30 35 40 45 50 55 Спосіб винаходу охоплює етап постачання водної суміші, яка містить молочну кислоту та розчинений магній хлорид. Водна суміш − суміш, екстрагована з органічної рідини. Водна суміш є кращим водним розчином, тому що екстракцію можна легше робити, коли відсутня тверда речовина. Такий розчин стосується розчину вихідної водної реакційної суміші. Однак, присутність твердої речовини у водній суміші є можливим до певного ступеню, залежного від застосованого обладнання, яке відоме спеціалісту. Отже, водна суміш також може бути суспензією. Прикладами твердої речовини, яка може бути присутньою в такій суспензії, є молочна кислота у твердій формі, нерозчинний магній хлорид та нерозчинні домішки. Кращим умістом молочної кислоти у водній суміші є можливо високий. Наприклад, водна суміш може містити, принаймні, 5 мас. %, краще, принаймні, 10 мас. %, ще краще, принаймні, 15 мас. % молочної кислоти, базованих на загальній масі водної суміші. Конкретно переважним можуть бути величини, принаймні, 20 мас. %, конкретніше, принаймні, більше 25 мас. %. Вода, присутня у водній суміші, може бути насичена молочною кислотою. В одному втіленні водна суміш має pH 2 або нижче, типово - pH нижче 1, наприклад, pH 0-1. Переважним є відносно низьке pH, щоб гарантувати присутність у суміші молочної кислоти в кислотній формі, що дозволяє екстракцію. Крім того, водна суміш може містити домішки, зокрема, домішки, які виникають зі способу ферментації. Такі домішки можуть бути розчинними або нерозчинними у водній суміші. Прикладами розчинних домішок є цукри, білки та солі. Нерозчинна біомаса (наприклад, мікроорганізми) та нерозчинні солі є прикладами нерозчинних домішок. Усі ці домішки типово можуть бути присутніми у ферментаційному бульйоні. Більше подробиць щодо отримання водної суміші надано нижче. Водна суміш містить, принаймні, 5 мас. % розчиненого магній хлориду. Присутність розчиненого магній хлориду у водній суміші має сприятливу дію на екстракцію, як описано вище. Розчинений магній хлорид, який тут застосовано, стосується магній хлориду в розчиненому стані, тобто у формі сольватованих іонів у воді. Водна суміш містить, принаймні, 5 мас. % розчиненого магній хлориду. Для підвищення результату винаходу - краще, щоб концентрація солі була відносно високою. Переважно, щоб концентрація солі розчиненого магній хлориду дорівнювала, принаймні, 10 мас. % ще краще, принаймні, 15 мас. %, навіть ще краще, принаймні, 20 мас. %, найкраще, принаймні, 25 мас. %. Залежно від розчинності солі, можливо застосовувати, принаймні, 30 мас. %, навіть ще краще, принаймні, 35 мас. % розчиненого магній хлориду, що базовано на загальній масі водної суміші. (тобто загальній масі водної суміші, за виключенням будь-якої твердої речовини). Максимальна величина звичайно обумовлена розчинністю магній хлориду, що дорівнює, приблизно, 45 мас. %. Краще, коли водна суміш є концентрованою до найбільш високої можливої концентрації розчиненого магній хлориду, тобто близької до розчинності магній хлориду, тобто близької до максимальної кількості маси магній хлориду, яка може бути розчиненою у водній суміші, виміряної при температурі, при якій проведено попередню екстракцію. Хоч нерозчинний магній хлорид може бути присутнім у водній суміші, це не є бажаним. Отже, краще щоб концентрація солі у водній суміші була не вище розчинності магній хлориду у водній суміші, щоб попереджати осадження. Відповідно, краще, коли водна суміш має концентрацію розчиненого магній хлориду у межах 10 мас. %, краще - у межах 5 мас. % розчинності магній хлориду у водній суміші. Розчинений магній хлорид може виникати з реакції підкислення, де солі лактатів реагують із хлоридною кислотою. Розчинений магній хлорид також може виникати при додаванні магній хлорид до водної суміші, щоб підвищити концентрацію розчиненого магній хлориду. Також можливі комбінації. Водну суміш краще отримувати підкислюванням магній лактату хлоридною кислотою, створюючи, таким чином, водну суміш, яка містить молочну кислоту та магній хлорид. Етап підкислювання типово проводили введенням солі лактату в контакт із кислотним розчином. Однак, у деяких випадках також можливий контакт солі лактату з газоподібною HCl. Сіль лактату може бути у твердій та/або в розчиненій формі. В одному втіленні сіль лактату постачено у твердій формі. У цьому випадку етап підкислювання проведено введенням солі лактату в контакт із кислотним розчином. Перевагою отримання водної суміш із сіллю лактату в твердій формі є отримання дуже високої концентрації молочної кислоти, як-то концентрація, принаймні, 15 мас. %, зокрема, принаймні, 25 мас. %, наприклад, упритул до 50 мас. %, або 40 мас. %. 4 UA 113530 C2 5 10 15 20 25 30 35 40 45 50 55 Сіль лактату також може бути в розчиненій формі, типово як частина водного розчину. У цьому випадку етап підкислювання можна супроводжувати введенням солі лактату в контакт із кислотним розчином або кислотним газом. Етап підкислювання також може супроводжуватися сумішшю молочної кислоти та солі лактату. Таку суміш, наприклад, можна отримувати при низькому pH ферментації. Суміш може бути, наприклад, водною суспензією. Кислота, застосована в етапі підкислювання, типово є сильною кислотою, як-то хлоридна кислота або сульфатна кислота. При потребі присутності, принаймні, 5 мас. % магній хлориду, переважним є застосування хлоридної кислоти. У такому випадку отримано водну суміш, яка містить молочну кислоту та хлоридну сіль. Підкислювання HCl, наприклад, можна робити введенням солі лактату в контакт із водним розчином HCl або введенням розчину або суспензії солі лактату в контакт із газом HCl. Коли підкислювання солі лактату проведено контактуванням із кислотним розчином, краще мати концентрацію кислоти можливо високою. Висока концентрація кислоти призведе до водної суміші з високою бажаною концентрацією молочної кислоти. Отже, кислотний розчин, містить, принаймні, 5 мас. %, ще краще, принаймні, 10 мас. % та найкраще, принаймні, 20 мас. % кислоти, що базовано на загальній масі кислотного розчину. Підкислювання типово роблять, застосовуючи надлишок кислоти. Надлишок переважно є малим за умови, щоб отримана водна суміш не мала високу кислотність, котра не може бути бажаною при подальшій обробці такої суміші. Наприклад, застосований надлишок кислоти може бути таким, щоб отримана водна суміш мала pH 2 або нижче, краще - pH 0 - 1. Якщо застосовано кислотний газ (наприклад, газ HCl), його можна вводити в контакт із розчином або суспензією лактату. Зокрема, газ HCl можна продувати через розчин або суспензію. При застосуванні газу HCl, HCl може виникати з етапу термічного розкладу, як описано вище. Краще проводити підкислювання при температурі 75 °C або менше. При вищих температурах це стає неекономічним для пристосування оснащення до жорстоких умов кислотного середовища при високих температурах. Після підкислювання твердий матеріал можна видаляти з водної суміші, наприклад, фільтруванням. Як описано вище, присутність твердого матеріалу у водній суміші протягом екстракція є небажаним. Водну суміш можна концентрувати після підкислювання перед екстракцією до концентрації упритул до розчинності магній хлориду, зокрема, до бажаної концентрації розчиненого магній хлориду. Конкретні величини для цієї концентрації описано вище. В одному втіленні застосовано магній лактат, котрий виникає зі способу ферментації. Відповідно, спосіб винаходу, крім того, може охоплювати етап ферментації для створення молочної кислоти, цей спосіб ферментації охоплює етапи бродіння джерела карбону, як-то вуглевод, способами мікроорганізму у ферментаційному бульйоні для створення молочної кислоти та нейтралізації, принаймні, частини молочної кислоти додаванням основи, зокрема, основи магнію, отримуючи, таким чином, сіль магній лактату. Способи ферментації для виробництва карбонових кислот відомі в рівні техніки та не потребують тут роз'яснення. Спеціалісту належить вибрати, застосовуючи його знання, придатний спосіб ферментації, залежно від отримання бажаної кислоти, джерела карбону та придатного мікроорганізму. Продуктом способу ферментації є ферментаційний бульйон, котрий є водною рідиною, яка містить магній карбоксилат, біомасу та необов'язково, крім того, компоненти, як-то домішки цукри, білки та солі. Якщо бажано, ферментаційний бульйон перед подальшою обробкою можна піддавати етапу видалення біомаси, наприклад, етапу фільтрування. Це звичайно є переважним для покращення якості продукту. Іншим проміжним етапом може бути відокремлення твердого продукту реакції, тобто магній лактату, з ферментаційного бульйону до, після, або одночасно з видаленням біомаси, та необов'язково піддавання магній лактату етапу промивання. Залежно від концентрації магній лактат може осаджуватися у ферментаційному середовищі. В одному втіленні твердий магній лактат відокремлено з ферментаційного середовища, наприклад, фільтруванням, та піддано етапу підкислення, який описано вище. Ще одним проміжним етапом може бути піддавання ферментаційного бульйону етапу концентрування для збільшення концентрації магній лактату в композиції до підкислення. Цей етап можна робити до, після, або одночасно з видаленням біомаси. 5 UA 113530 C2 5 10 15 20 25 30 35 40 45 50 55 Такий етап може бути привабливим для збільшення вмісту твердого магній лактату, котрий потім можна відокремлювати з ферментаційного бульйону, як описано вище, та обробляти як твердий магній лактат у способі згідно з винаходом. Інші проміжні етапи, наприклад, етапи очищення, можна робити як бажано, що відомо спеціалісту. У способі згідно з винаходом розглянуту вище водну суміш піддано етапу екстракції контактуванням з органічною рідиною, яка містить органічний розчинник, вибраний із групи кетонів C5+, діетилетеру та метил-третинний-бутил-етеру, таким чином, отримуючи органічний розчин молочної кислоти та водної відпрацьованої рідини, яка містить магній хлорид. У цій попередній екстракції молочну кислоту відокремлено з домішок, присутніх у водній суміші, розчиненням у першій органічній рідині. Домішки слід залишати у водній суміші. Краще, коли органічна рідина містить, принаймні, 90 мас. % органічного розчинника, краще, коли, принаймні, - 95 мас. %, ще краще, принаймні, - 99 мас. %. В одному втіленні органічна рідина є органічним розчинником. Типово, малі кількості води можуть бути присутніми в першій органічній рідині, зокрема, коли рідина (частково) містить рециклізований органічний розчинник із повторного циклу після екстракції. Органічний розчинник вибрано з наступної групи: кетони C5+, діетилетер та метилтретинний-бутил-етер. C5+ означає кетони, принаймні, з 5 атомами карбону. Знайдено, що конкретні розчинники сполук демонструють хороші властивості в способі згідно з винаходом, де вони виявляють хороший ефект концентрації. Вибір придатного органічного розчинника може сприяти створенню високого коефіцієнту розподілу протягом попередньої екстракції. У цьому випадку тільки відносно малу кількість молочної кислоти втрачено у водній непридатній рідині. Як ілюстровано в прикладі 10 наданої заявки, розчинники згідно з винаходом виявляють ефект концентрації в екстракції молочної кислоти. На відміну, інші розчинники, охоплюючи ізоаміловий спирт, діізопропіетер, та триоктиламін (Аламін 336), вказані як переважні в WO00/17378, не виявляють ефект концентрації. Те ж саме стосується суміші 48 % триоктиламіну, 20 % н-бутанолу та 32 % керосину, вказаних у прикладі 8 WO00/17378. У заявленому винаході переважним є застосування кетонів, зокрема, кетонів C5-C8. Також можна застосовувати суміші. Застосування кетонів C9+ є менш переважним, оскільки вважають, що ці сполуки демонструють нижчий ефект концентрації й можуть призводити до більших забруднень у кінцевому продукті. Знайдено, що застосування метил-ізобутил-кетону (MIBK) є дуже привабливим для отримання хорошої дії концентрації. Крім того, знайдено, що застосування кетонів має бути переважним, оскільки вони є стабільними в умовах способу, у якому вони не реагують або суттєво не розкладаються, отже, не надають зростання забруднень, та дозволяють стабільний спосіб операції. Як етери, можна застосовувати етилетер та метил-третинний-бутил-етер. Однак, знайдено, що вони є менш переважними, зокрема, оскільки застосування етерів призводить до більшої втрати розчинника та більших забруднень у кінцевому продукті. Спосіб винаходу не потребує застосування засобів екстрагування, як-то аміни. У дійсності, застосування засобів екстрагування в органічному розчиннику звичайно є небажаним. Засобом екстрагування є сполука, яка створює комплекс з екстрагованою сполукою (у цьому випадку − молочна кислота). Однак, формування (протягом попередньої екстракції) та розклад комплексу потребує відносно великої кількості енергії, за умови, щоб різниця температури між попередньою та зворотною екстракцією була б більшою ніж потрібно. Відповідно, краще, коли органічна рідина не містить або, по суті, не містить кількості засобів екстрагування, зокрема, не містить або, по суті, не містить кількості засобів екстрагування аміну. Отже, молочну кислоту в способі винаходу краще екстрагувати в нейтральній кислотній формі та не у формі солі або комплексу. Краще, коли органічна рідина по суті є вільною від амінів, етерів та спиртів, що означає, що ці сполуки, якщо присутні повністю, то кожна присутня в кількості, меншій 2 мас. %, краще меншій 1 мас. %, ще краще - меншій 0,5 мас. %, обчисленій щодо маси органічної рідини. Співвідношення органічної рідини до водної суміші, застосованої в попередній екстракції, визначено за наступними підставами. З одного боку, якщо кількість органічної рідини є відносно високою, ефективності екстракції, відображеної як процент кислоти у водній суміші, котру екстраговано в органічну рідину, слід бути високою. З іншого боку, слід застосовувати велику кількість органічної рідини, та ефект концентрації буде зменшено. Навпаки, якщо кількість органічної рідини є відносно низькою, ефект концентрації буде покращено, але ефективність екстракції буде зменшено. 6 UA 113530 C2 5 10 15 20 25 30 35 40 45 50 55 Коефіцієнт розподілу (DR), визначений вище, може надавати керівництво стосовно цього. В одному втіленні кількість органічної рідини, застосована в попередній екстракції, може бути в діапазоні 0,5/DR - 1,5/DR щодо кількості водної суміші. Застосування кількості органічної рідини в діапазоні 0,5/DR - 0,8/DR щодо кількості водної суміші для попередньої екстракції може бути бажаним для хорошого ефекту концентрації. Однак, вихід етапу екстракції в цьому випадку може бути меншим 99 %. Застосування кількості органічної рідини в діапазоні 1,3/DR - 1,5/DR щодо кількості водної суміші для попередньої екстракції може призводити до виходу екстракції вище 99 %, але типово має менший явний ефект концентрації. Застосування кількості органічної рідини в діапазоні 0,8/DR - 1,3/DR, та зокрема, у діапазоні 1,0/DR - 1,2/DR, щодо кількості водної суміші для попередньої екстракції є найбільш бажаним, оскільки можна отримати хороший ефект концентрації та вихід екстракції понад 99 %. Вихід екстракції, який тут застосовано, стосується проценту маси молочної кислоти, яку екстраговано в органічну рідину протягом попередньої екстракції. Попередню екстракцію типово супроводжено контактуванням водної суміші з першою органічною рідиною, отримуючи, таким чином, органічний розчин молочної кислоти та водної відпрацьованої рідини, який містить магній хлорид. Краще, коли екстракція є протиточною екстракцією, тобто водна суміш та органічна рідина контактують між собою при застосуванні протиточних потоків. У такому вигляді можна отримувати дуже ефективну екстракцію молочної кислоти в органічну рідину, зокрема, стосовно виходу. Екстракцію краще робити в екстракційній колонці. Якщо застосований органічний розчинник має нижчу густину ніж вода (наприклад, MIBK), органічний розчинник краще постачати до дна колонки, тоді як водну суміш краще постачати до верху колонки. Отже, дві фази слід формувати так: вища фаза, яка містить органічний розчинник, та нижча фаза, яка містить водну суміш. При поверхні розділу двох фаз буде акумулюватися будь-яка біомаса та/або інша тверда речовина, присутня у водній суміші. Як описано вище, біомаса не спричиняє емульгування, обумовленого присутністю солі у водній суміші. При постачанні органічного розчинника до дна колонки органічний розчинник буде рухатися догори через водну суміш, таким чином, екстрагуючи молочну кислоту та створюючи органічний розчин молочної кислоти. При дні колонки можна отримати водну відпрацьовану рідину, типово у формі водного розчину солі, котрий містить магній хлорид. Попередню екстракцію можна робити при температурі 20-100 °C, краще - при температурі 30-80 °C, наприклад, при температурі 40-60 °C. До кожної бажаної температури для попередньої екстракції, водну суміш та/або органічну рідину можна нагрівати до попередньої екстракції. Як описано вище, вищі температури в діапазоні 20-100 °C є сприятливими стосовно зменшення розчинності органічного розчинника у воді. Крім того, коефіцієнт розподілу може збільшуватися при підвищенні температури та/або може призводити до міцнішого ефекту концентрації. Через можливі умови корозії температура кислотної водної суміші вище 60 °C може бути несприятливою. Однак, корозії, наприклад, можна уникати застосуванням пластмасового або емальованого обладнання для екстракції. Відпрацьована водна рідина, створена в попередній екстракції, містить магній хлорид. Відпрацьовану водну рідину типово отримано у формі водного розчину солі, який містить розчин магній хлориду. Цей розчин є відносно чистим, оскільки нерозчинні домішки типово залишаються протягом екстракції при взаємодії води/органічного. Щоб попередити втрату кислоти із системи, переважним є можливо низька концентрація молочної кислоти у відпрацьованій рідині. В одному втіленні концентрація молочної кислоти у відпрацьованій рідині є нижчою 1 мас. %, зокрема, - нижчою 0,5 мас. %, конкретніше - нижчою 0,1 мас. %. Знайдено, що екстракція при застосуванні способу згідно з винаходом дозволяє отримувати дуже низькі втрати кислоти. Для попередження втрати розчинника із системи та для попередження, крім того, проблем в обробці, зокрема, коли застосовано етап термічного розкладу, переважним є можливо низька концентрація розчинника у відпрацьованій рідині. В одному втіленні концентрація розчинника у відпрацьованій рідині є нижчою 1 мас. %, зокрема, - нижчою 0,5 мас. %, конкретніше, - нижчою 0,2 мас. %, та краще - нижчою 0,1 мас. %. Знайдено, що екстракція при застосуванні способу згідно з винаходом дозволяє отримувати дуже низькі втрати розчинника. Переважним є присутність, принаймні, 80 % кислоти в органічній фазі системи після попередньої екстракції, зокрема, принаймні, 90 %, краще, принаймні, 95 %, ще краще, принаймні, 98 %, найкраще, принаймні, 99 %. Переважним є присутність, принаймні, 90 % магній хлориду у водній відпрацьованій рідині в системі після попередньої екстракції, краще, принаймні, 95 %, ще краще, принаймні, 98 %, зокрема, принаймні, 99 %. 7 UA 113530 C2 5 10 15 20 25 30 35 40 45 50 55 60 Органічний розчин молочної кислоти потім піддавали етапу зворотної екстракції, органічний розчин молочної кислоти, отриманий у попередній екстракції, необов'язково піддавали проміжному етапу промивання для видалення будь-яких домішок, присутніх у органічному розчині молочної кислоти. Такі домішки, наприклад, хлорид або іони металу, типово вилучають із водної суміші. На такому етапі промивання органічний розчин молочної кислоти контактує з рідиною для промивання. Такий етап може зменшити кількість домішок, як-то хлорид та/або іони металу в кінцевому продукті, тобто водному розчині молочної кислоти. Видалення цих іонів, крім того, може попереджати проблеми корозії. Рідиною для промивання типово є водна рідина. В одному втіленні частину водного розчину молочної кислоти, утвореного як продукт у зворотній екстракції, застосовано як рідину для промивання. У цьому втіленні, малу частина, наприклад, 0,5-5 мас. %, зокрема, 0,5-2 мас. %, продукту загального водного розчину молочної кислоти можна застосовувати для промивання. Рідину для промивання потім можна знов повертати до водної суміші, де знов піддавати попередній екстракції. Протягом промивання не слід видаляти занадто багато кислоти з органічної рідини, що збитково впливає на концентрацію карбонової кислоти в кінцевому продукті. У межах рішення спеціаліста є визначення умов придатного промивання. Органічний розчин карбонової кислоти, утворений у попередній екстракції, необов'язково є розчином після промивання, зворотно екстрагований у водну рідину, з отриманням, таким чином, водного розчину молочної кислоти та другої органічної рідини. Цей етап можна розглядати тут як другу екстракцію або зворотну екстракцію. Зворотна екстракція надає водний розчин карбонової кислоти, котрий має вищу чистоту та, зокрема, нижчу концентрацію солі ніж вихідна водна суміш. Як пояснено вище, продукт водного розчину молочної кислоти заявленого винаходу типово має вищу концентрацію молочної кислоти ніж водна суміш. Співвідношення водної рідини до розчину органічної кислоти, застосованої в зворотній екстракції, визначено за наступними підставами. З одного боку, якщо кількість водної рідини є відносно високою, ефективність екстракції, відображена як процент кислоти в розчині органічної кислоти, котру екстраговано у водну, буде високою. З іншого боку, слід застосовувати велику кількість водної рідини, та ефект концентрації буде зменшено. Навпаки, якщо кількість водної рідини є відносно низькою, ефект концентрації буде покращено, але ефективність екстракції буде зменшено. Придатну величину співвідношення водної рідини до розчину органічної кислоти, застосованої в цій зворотній екстракції, можна отримувати з коефіцієнту розподілу (DR), визначеного вище. В одному втіленні кількість водної рідини, застосованої в зворотній екстракції, є 0,5*DR - 1,5*DR разів кількості органічного розчину молочної кислоти. Ці співвідношення, зокрема, можуть бути значними стосовно ефекту концентрації заявленого способу. Застосування кількості водної рідини в діапазоні 0,5*DR - 0,8*DR разів кількості органічного розчину молочної кислоти для зворотної екстракції може бути бажаним для хорошого ефекту концентрації. Однак, вихід етапу зворотної екстракції в цьому випадку може бути меншим 99 %. Застосування кількості водної рідини в діапазоні 1,3*DR - 1,5*DR разів кількості органічного розчину молочної кислоти для зворотної екстракції може призводити до виходу в зворотній екстракції понад 99 %, але типово має менший явний ефект концентрації. Застосування кількості водної рідини в діапазоні 0,8*DR - 1,3*DR, та, зокрема, у діапазоні 1,0*DR - 1,2*DR разів кількості органічного розчину молочної кислоти є найбільш бажаним, оскільки можна отримувати хороший ефект концентрації та вихід зворотної екстракції понад 99 %. Вихід зворотної екстракції, який тут застосовано, стосується проценту маси молочної кислоти, яку екстраговано у водну рідину протягом зворотної екстракції. Зворотну екстракцію типово проведено контактуванням органічного розчину молочної кислоти з водною рідиною, отримуючи, таким чином, водний розчин молочної кислоти та другу органічну рідину. Водний розчин молочної кислоти є розчином продукту. Якщо так бажано, другу органічну рідину, цілком або частково, можна рециклізувати до попередньої екстракції як першу органічну рідину, необов'язково після піддавання етапу очищення. Краще, коли екстракція є протиточною екстракцією. У такому вигляді можна отримувати дуже ефективну екстракцію молочної кислоти в органічну рідину, зокрема, стосовно виходу. Екстракцію краще робити в екстракційній колонці. Якщо застосований органічний розчинник має нижчу густину ніж вода, водну рідину краще постачати до верху колонки, тоді як органічний розчин молочної кислоти постачали до дна колонки. Отже, дві фази слід формувати так: вища фаза, яка містить органічний розчинник, та нижча фаза, яка містить водну рідину. При постачанні водної рідини до верху колонки це буде рухатися донизу через органічний розчин молочної кислоти, таким чином, екстрагуючи молочну кислоту та формуючи органічний розчин молочної кислоти. Тоді водний розчин молочної кислоти можна отримувати на дні колонки. 8 UA 113530 C2 5 10 15 20 25 30 35 40 45 50 55 60 Відомо, що розглянуто можливість випаровувати органічний розчинник з органічного розчину молочної кислоти після попередньої екстракції, таким чином, безпосередньо отримуючи молочну кислоту. Однак, кращі результати отримували, коли застосовували зворотну екстракцію згідно із заявленим винаходом. Зворотна екстракція мала результатом менші домішки та більший енергоекономічний спосіб. Зворотну екстракцію можна проводити при температурі 20-100 °C, краще - при температурі 80 °C або нижче, ще краще - при температурі 60 °C або нижче. Зворотну екстракцію краще проводити при температурі вище 0 °C, краще - при температурі, принаймні, 10 °C, що обумовлено вартістю енергії, пов'язаної з охолодженням. Температури, рівні або близькі до температури в попередній екстракції, конкретно є переважними для зворотної екстракції. Це може зберігати енергію, оскільки потрібно менше нагрівання та/або охолодження між різними потоками в способі екстракції. Відповідно, в одному втіленні зворотну екстракцію проведено при температурі в межах 10 °C, наприклад, - у межах температури 5 °C, при якій проведено попередню екстракцію. Застосування подібної температури в попередній та зворотній екстракції стосується тут ізотермічних умов. Попередню екстракцію та зворотну екстракцію можна проводити, приблизно, при тій самій температурі, наприклад, застосовуючи різницю температур між попередньою та зворотною екстракцією менше 5 °C. В одному втіленні екстракцію в органічну рідину (попередню екстракцію) проведено при нижчій температурі ніж екстракцію у водну рідину (зворотну екстракцію). Такий спосіб екстракції також відомий як екстракція при регулярному коливанні температури. Температура протягом зворотної екстракції в цьому випадку є вищою на 5-45 °C, наприклад, на 10-20 °C ніж температура в попередній екстракції. У ще одному втіленні екстракцію в органічну рідину (попередню екстракцію) проведено при вищій температурі ніж екстракцію у водну рідину (зворотну екстракцію). Такий спосіб екстракції можна позначати як екстракцію при реверсному коливанні температури. В екстракції при реверсному коливанні температури етап зворотної екстракції в цьому випадку можна проводити при температурі, яка є на 10-50 °C або 20-30 °C нижчою ніж температура, при якій проведено попередню екстракцію. Знайдено, що екстракція в способі реверсного коливання температури може призводити до підвищеної концентрації кислоти в продукті. В одному втіленні в способі згідно з винаходом органічний розчин молочної кислоти приведено в контакт із другою органічною рідиною, застосовуючи теплообмінник. Е сприятливим, коли попередню та зворотну екстракцію проведено при різних температурах. Водний розчин молочної кислоти, отриманий після зворотної екстракції, як здійснено згідно із заявленим винаходом, має вищу концентрацію молочної кислоти ніж водна суміш, котру постачали до попередньої екстракції. Це також ілюстровано в прикладах нижче. Ступінь ефекту концентрації способу винаходу залежить, між іншим, від співвідношення органічної рідини та водної суміші, застосованої в попередній екстракції, співвідношення водної рідини та органічного розчину молочної кислоти, застосованого в зворотній екстракції, температури, при якій проведено етапи екстракції, типу застосованої органічної рідини та кількості розчиненого магній хлориду, присутнього у водній суміші. Крім того, переважним є так вибирати умови способу, щоб отримувати високий вихід екстракції. Стосовно цього, переважним є те, щоб кількість маси органічної рідини, застосованої в попередній екстракції, є 1,0/DR - 1,2/DR разів кількості маси водної суміші, тоді як кількість маси водної рідини, застосованої в зворотній екстракції, є 1,0*DR - 1,2*DR разів кількості маси розчину органічної молочної кислоти. Навіть ще кращим є, коли кількість маси органічної рідини, застосованої в попередній екстракції, є 1,1/DR - 1,2/DR разів кількості маси водної суміші, тоді як кількість маси водної рідини, застосованої в зворотній екстракції, є 1,1*DR - 1,2*DR разів кількості маси розчину органічної молочної кислоти. Такі співвідношення маси призводить до конкретно хорошого ефекту концентрації, коли це додатково комбіновано з температурою попередньої екстракції 50-60 °C та концентрацією розчиненого магній хлориду, принаймні, 10 мас. %, базованій на загальній кількості води та розчиненого матеріалу, присутнього у водній суміші. У цьому випадку кращою застосованою органічною рідиною є кетон, ще краще - MIBK. Зворотну екстракцію в цьому випадку краще проводити при 20-60 °C, ще краще - при 50-60 °C. Ще кращий ефект концентрації отримували, коли застосовували концентрацію магній хлориду, принаймні, 15 мас. % замість, принаймні, 10 мас. %, базованих на загальній кількості води та розчиненого матеріалу, присутнього у водній суміші. Отже, наступна комбінація параметрів може призводити, зокрема, до хорошого ефекту концентрації та може одночасно призводити до хорошого виходу екстракції: - концентрація магній хлориду, принаймні, 10 мас. %, базована на загальній кількості води та розчиненого матеріалу, присутнього у водній суміші; 9 UA 113530 C2 5 10 15 20 25 30 35 40 45 50 55 60 - температура попередньої екстракції дорівнює 30-60 °C, зокрема, 50-60 °C; - температура зворотної екстракції дорівнює 20-60 °C; - кількість маси органічної рідини, застосованої в попередній екстракції, яка дорівнює 1,1/DR - 1,2/DR разів кількості маси водної суміші; - кількість маси водної рідини, застосованої в зворотній екстракції, яка дорівнює 1,1*DR 1,2*DR разів кількості маси розчину органічної молочної кислоти; - органічна рідина − кетон C5+, краще - кетон C5-C8, конкретніше, - MIBK. Вища комбінація працює навіть краще, коли застосовують концентрацію магній хлориду, принаймні, 15 мас. %, базовану на загальній кількості води та розчиненого матеріалу, присутнього у водній суміші. Загальний вихід способу винаходу залежить від виходу екстракції в попередній екстракції та виходу екстракції в зворотній екстракції. Вихід попередньої екстракції можна підвищувати проведенням попередньої екстракції протиточними потоками (також дивись вище). Таку протиточну екстракцію можна проводити в одній або більше посудинах (наприклад, мішалці або сепараторі). Вихід етапу екстракції можна підвищувати збільшенням об'єму або числа посудин. Коли застосовують більше одної посудини, посудини поєднують послідовно одну із другою. У цьому випадку друга або подальша посудина далі екстрагує водну рідину, отриману після екстракції в попередній посудині. Однак, краще, коли попередню екстракцію проведено в одній посудині (наприклад, в екстракційній колонці), яка є достатньо великою для отримання бажаного високого виходу (типово вище 99 %). Наприклад, великі екстракційні колонки висотою 10-20 метрів відомі в рівні техніки. Спеціалісту слід визначати розмір та/або число посудин для отримання виходу 99 % або більше. Вихід зворотної екстракції можна підвищувати таким же шляхом, який описано вище для попередньої екстракції. Якщо застосовано більше одної посудини, друга або подальша посудина далі екстрагує органічну рідину, отриману після екстракції в попередній посудині. Спосіб винаходу, крім того, може охоплювати етап концентрування розчину продукту водного розчину молочної кислоти випаровуванням води. Випарену в цьому етапі воду можна рециклізувати повторним застосуванням її як водну рідину в зворотній екстракції. Розчин продукту водного розчину молочної кислоти може містити малу кількість органічного розчинника та осаду із етапу екстракції, якщо присутні, наприклад, приблизно, 0,1-3 мас. %, базовані на загальній кількості водного розчину молочної кислоти. Де зроблено етап випаровування, органічний розчинник також типово випаровували в етапі концентрування, часто підсиленому ефектом видалення води. Як показано вище, другу органічну рідину, отриману в зворотній екстракції, можна рециклізувати повторним її застосуванням як першу органічну рідину в попередній екстракції. В одному втіленні спосіб винаходу охоплює етап піддавання отриманого в попередній екстракції водної непридатної рідини, яка містить магній хлорид, етапу термічного розкладу при температурах, принаймні, 300 °C, утворюючи, таким чином, магній оксид та HCl. У цьому етапі сіль хлориду термічно гідролізовано під формування магній оксиду та HCl, ці сполуки можна рециклізувати в інших етапах способу для отримання молочної кислоти. Наприклад, магній оксид можна застосовувати в способі ферментації, наприклад, як засіб нейтралізації або як попередник цього. Із цією метою магній оксид можна вводити в контакт із водою для отримання кашки магній гідроксиду. Крім того, HCl можна застосовувати для підкислювання магній лактату, отриманого в способі ферментації. Типово HCl розчинювали у воді протягом або після термічного розкладу, отримуючи, таким чином, розчин HCl. Отже, етап термічного розкладу забезпечує спосіб, де відходи рециклізовано та, отже, де отримано відносно малі відходи. Спосіб винаходу переважно є подовженим процесом. Однак, його можна реалізувати як групову технологію. Далі винахід слід ілюструвати наступними прикладами, але без обмеження щодо цього. Приклад 1: Екстракція молочної кислоти у відсутність розчиненої порівняльної солі Розчин вихідної реакційної суміші молочної кислоти отримували додаванням 304 г кристалічної молочної кислоти до 745 г води та змішували до повного розчинення. Отже, отриманий розчин вихідної реакційної суміші містив 29 мас. % молочної кислоти. У попередній екстракції 101 г MIBK додавали до 1000 г розчину молочної кислоти вихідної реакційної суміші (базовано на співвідношенні маси 1:10). Отриману двофазову систему перемішували з достатньою швидкістю при 20 °C протягом 30 хвилин для забезпечення якісного диспергування обох фаз. Потім перемішування зупиняли, фазам дозволяли відокремлюватися та шар молочної кислоти, завантажений MIBK, відокремлювали від збідненого водного розчину молочної кислоти. 10 UA 113530 C2 5 10 15 20 25 30 35 40 45 50 55 60 У зворотній екстракції 5,2 г води додавали до 53 г цього шару молочної кислоти, завантаженого MIBK, (базовано на співвідношенні маси 1:10). Отриману двофазову систему перемішували при 20 °C протягом 30 хвилин із достатньою швидкістю для забезпечення якісного диспергування обох фаз. Потім перемішування зупиняли, фазам дозволяли відокремлюватися та відбирали зразок із водної донної фази. Концентрація молочної кислоти у цьому зразку дорівнювала 19,4 мас. % (визначено потенціометричним титруванням). У цьому прикладі показано, що екстракція, зроблена у відсутність розчиненого магній хлориду, як застосовано в способі згідно із заявленим винаходом, зменшує концентрацію молочної кислоти з 29 мас. % у розчині вихідної реакційної суміші до 19,4 мас. % у водному розчині продукту. Приклад 2: екстракція молочної кислоти в присутності розчиненої солі Розчин молочної кислоти вихідної реакційної суміші (водна суміш) отримували додаванням магній хлориду гексагідрату (790 г) до розчину 700 г кристалічної молочної кислоти в 924 г води та змішували до повного розчинення. Отже, отриманий розчин вихідної реакційної суміші містив 29 мас. % молочної кислоти та 15,3 мас. % магній хлориду. У попередній екстракції 100 г MIBK додавали до 1000 г розчину молочної кислоти вихідної реакційної суміші (базовано на співвідношенні маси 1:10). Отриману двофазову систему перемішували з достатньою швидкістю при 20 °C протягом 30 хвилин для забезпечення якісного диспергування обох фаз. Потім перемішування зупиняли, фазам дозволяли відокремлюватися та шар молочної кислоти, завантажений MIBK, відокремлювали від збідненого водного розчину молочної кислоти. У зворотній екстракції 4,7 г води додавали до 46,9 г цього шару молочної кислоти, завантаженого MIBK, (базовано на співвідношенні маси 1:10). Отриману двофазову систему перемішували з достатньою швидкістю при 20 °C протягом 30 хвилин для забезпечення гарного диспергування двох фаз. Потім перемішування зупиняли, фазам дозволяли відокремлюватися, та відбирали зразок із водної донної фази. Концентрація молочної кислоти у цьому зразку дорівнювала 34,8 мас. % (визначено потенціометричним титруванням). У цьому прикладі показано, що присутність розчиненої солі магній хлориду в попередній екстракції збільшує концентрацію молочної кислоти з 29 мас. % у розчині вихідної реакційної суміші до 34,8 мас. % у водному розчині після зворотної екстракції. Якщо розчин піддавали етапу випаровування після екстракції, отримували б підвищену концентрацію молочної кислоти у водному розчині зі зворотної екстракції, отже, це зменшувало б кількість води, яку потрібно випаровувати із продукту молочної кислоти в порівнянні з водним розчином, отриманим після зворотної екстракції з розчину вихідної реакційної суміші без розчиненого магній хлориду в прикладі 1 фактором 2. Приклад 3: Екстракція молочної кислоти при регульованому коливанні температури У попередній екстракції 100 г MIBK додавали до 1000 г розчину молочної кислоти вихідної реакційної суміші (базовано на співвідношенні маси 1:10), який отримано в прикладі 2, вище. Отриману двофазову систему перемішували при 20 °C протягом 30 хвилин із достатньою швидкістю для забезпечення якісного диспергування обох фаз. Потім перемішування зупиняли, фазам дозволяли відокремлюватися, та шар молочної кислоти, завантажений MIBK, відокремлювали від збідненого водного розчину молочної кислоти. У зворотній екстракції 6,9 г води додавали до 67,2 г цього шару молочної кислоти, завантаженого MIBK, (базовано на співвідношенні маси 1:10). Отриману двофазову систему перемішували при 60 °C протягом 30 хвилин із достатньою швидкістю для забезпечення гарного диспергування двох фаз. Потім перемішування зупиняли, фазам дозволяли відокремлюватися та відбирали зразок із водної донної фази. Концентрація молочної кислоти у цьому зразку дорівнювала 36,2 мас. % (визначено потенціометричним титруванням). У цьому прикладі показано, що застосування комбінації розчиненого магній хлориду та вищої температури у зворотній екстракції надає збільшену концентрацію молочної кислоти 36,2 мас. % у водному розчині після зворотної екстракції в порівнянні з ізотермічними умовами, застосованими в прикладі 2. Можна робити висновок, що застосування підвищеної температури в зворотній екстракції є, крім того, ефективними способами подальшого концентрування молочної кислоти протягом екстракції. Приклад 4: Екстракція молочної кислоти при реверсному коливанні температури У попередній екстракції 100 г MIBK додавали до 997 г розчину молочної кислоти вихідної реакційної суміші (базовано на співвідношенні маси 1:10), яку отримано в прикладі 2. Отриману двофазову систему перемішували при 60 °C протягом 30 хвилин із достатньою швидкістю для забезпечення якісного диспергування обох фаз. Потім перемішування зупиняли, фазам дозволяли відокремлюватися та шар молочної кислоти, завантажений MIBK, відокремлювали 11 UA 113530 C2 5 10 15 20 25 30 35 40 45 50 55 60 від збідненого водного розчину молочної кислоти. У зворотній екстракції 5,8 г води додавали до 58 г цього шару молочної кислоти, завантаженого MIBK, (базовано на співвідношенні маси 1:10). Отриману двофазову систему перемішували при 20 °C протягом 30 хвилин із достатньою швидкістю для забезпечення якісного диспергування обох фаз. Потім перемішування зупиняли, фазам дозволяли відокремлюватися та відбирали зразок із водної донної фази. Концентрація молочної кислоти у цьому зразку дорівнювала 37,1 мас. % (визначено потенціометричним титруванням). У цьому прикладі показано, що застосування комбінації розчиненого магній хлориду та вищої температури в попередній екстракції надає збільшену концентрацію молочної кислоти 37,1 мас. % у водному розчині після зворотної екстракції в порівнянні з ізотермічними умовами, застосованими в прикладі 2. Можна робити висновок, що застосування підвищеної температури в попередній екстракції є, крім того, ефективними способами подальшого концентрування молочної кислоти протягом екстракції. Приклад 5: Екстракція молочної кислоти при підвищеній температурі У попередній екстракції 100 г MIBK додавали до 996 г розчину молочної кислоти вихідної реакційної суміші (базовано на співвідношенні маси 1:10), яку отримано в прикладі 2. Отриману двофазову систему перемішували при 60 °C протягом 30 хвилин із достатньою швидкістю для забезпечення якісного диспергування обох фаз. Потім перемішування зупиняли, фазам дозволяли відокремлюватися, та шар молочної кислоти, завантажений MIBK, відокремлювали від збідненого водного розчину молочної кислоти. У зворотній екстракції 6,2 г води додавали до 63 г цього шару молочної кислоти, завантаженого MIBK, (базовано на співвідношенні маси 1:10). Отриману двофазову систему перемішували при 60 °C протягом 30 хвилин із достатньою швидкістю для забезпечення якісного диспергування обох фаз. Потім перемішування зупиняли, фазам дозволяли відокремлюватися, та відбирали зразок із водної донної фази. Концентрація молочної кислоти у цьому зразку дорівнювала 36,0 мас. % (визначено потенціометричним титруванням). У цьому прикладі показано, що застосування комбінації розчиненого магній хлориду та вищої температури у попередній а також у зворотній екстракції надає збільшену концентрацію молочної кислоти 36,0 мас. % у водному розчині після зворотної екстракції в порівнянні з ізотермічними умовами, застосованими в прикладі 2. Можна робити висновок, що ізотермічна операція при підвищеній температурі протягом попереднього та екстракції є ефективними способами подальшого концентрування молочної кислоти протягом екстракції. Приклад 6: співставлення MIBK та ізоамілового спирту Цей експеримент проводили для співставлення стабільності двох розчинників, MIBK та ізоамілового спирту в контакті з розчином молочної кислоти вихідної реакційної суміші, яку отримано в прикладі 1. Для кожного розчинника закритий скляний реактор наповнювали 20 г розчинника та 20 г розчину молочної кислоти вихідної реакційної суміші, розміщували в печі для тримання температури 60 °C та тривало струшували. Через 3 год., 24 год. (1 доба) та 168 год. (1 тиждень) струшування зупиняли на 1 годину, щоб дозволити фазам осаджуватися, зразок відбирали з верхнього шару розчинника, та верхній шар композиції розчинника аналізували газовою хроматографією. Результати показали, що навіть після 168 год. ніяких змін чистоти MIBK не визначено, тоді як у випадку ізоамілового спирту утворено після 3 год. 14,6 міри% ізоамілацетату. При 24 год. та 168 год. знайшли, що зразки концентрації ізоамілацетату далі підвищено до 22,5 міри%. У цьому прикладі показано, що естери молочної кислоти створено, коли спирти, як-то ізоаміловий спирт, застосовано як органічний розчинник екстракції, тоді як кетони, як-то MIBK, є стабільним органічними розчинниками. Можна робити висновок, що нестабільні органічні розчинники, як-то спирти, є нестабільними як розчинники екстракції, та що стабільні органічні розчинники, як-то кетони, є придатними розчинниками екстракції. Приклад 7: Дія концентрації розчиненої солі та температури на співвідношення розподілення 100 г органічного розчинника MIBK додавали до 100 г водного розчину з бажаним MgCl 2 та вихідною концентрацією молочної кислоти 20 мас. %. Отриману двофазову систему перемішували при 20 °C або 60 °C протягом 30 хвилин з достатньою швидкістю для забезпечення гарного диспергування двох фаз. Потім перемішування зупиняли, фазам дозволяли відокремлюватися, та зразки відбирали із двох фаз. Концентрацію молочної кислоти (мас. %) у цих зразках визначали потенціометричним титруванням. Потім обчислювали коефіцієнт розподілу як співвідношення концентрації молочної кислоти (мас. %) у фазі органічного розчинника MIBK до концентрації молочної кислоти (мас. %) у водній фазі. Результати показано в таблиці 1. 12 UA 113530 C2 Таблиця 1 MgCl2 (мас. %) 0 10,5 16,0 5 10 15 Коефіцієнт розподілу молочної кислоти (мас. %/мас. %) 20 °C 60 °C 0,16 0,19 0,33 0,37 0,49 0,56 У цьому прикладі показано, що з підвищенням концентрації солі молочної кислоти коефіцієнт розподілу значно збільшується. Крім того, у прикладі також показано, що коефіцієнт розподілу можна підвищувати зростанням температури. Можна робити висновок, що присутність солі та/або зростання температури значно підвищують ефективність екстракції карбонових кислот із водної потоку вихідної реакційної суміші в органічний розчинник. Приклад 8: Дії концентрації розчиненої солі та температури на розчинність у розчиннику 50 г органічного розчинника MIBK додавали до 100 г водного розчину з конкретною концентрацією MgCl2, та отриману двофазову систему перемішували при конкретній температурі протягом 30 хвилин із достатньою швидкістю для забезпечення гарного диспергування двох фаз. Потім перемішування зупиняли, фазам дозволяли відокремлюватися, та відбирали зразок із водної донної фази. Концентрацію MIBK у цьому зразку визначали газовою хроматографією. Експеримент проводили для трьох різних концентрацій MgCl 2 (0, 15 та 30 мас. %) при двох різних температурах (20 °C та 60 °C). Результати показано в таблиці 2. Таблиця 2 MgCl2 (мас. %) 0 15 30 20 25 30 35 40 45 Розчинність MIBK (мас. %) 20 °C 60 °C 1,8 1,4 0,48 0,20 0,17 0,11 У цьому прикладі показано, що додавання солі значно зменшує розчинність органічного розчинника MIBK у водній фазі. Можна робити висновок, що присутність солі значно зменшує втрату органічного розчинника у водній фазі після екстракція карбонової кислоти. Приклад 9: Пілотна екстракція молочної кислоти Експерименти пілотної екстракції проводили в системі пілотного пристрою Pulsed Disc та Donut Column (PDDC) pilot set-up, яка містить секцію активної колонки чотирьох термостатованих скляних сегментів, кожний довжиною 1,04 м та із внутрішнім діаметром 40 мм. Цю активну секцію оточували із двох боків сепаратори довжиною 42 см, які мали внутрішній діаметр 80 мм. Внутрішня частина колонки складалася з розміщених по черзі диску та тороїдальних перегородок із відстанню 8,4 мм, зроблених PVDF для забезпечення зволоження фазою органічного розчинника. Дно сепаратору приєднано до пульсатору поршневого типу для пульсації рідини в колонку з бажано частотою та амплітудою. Водні розчини вводили до верху та органічний розчинник MIBK до дна колонки. Колонка керувала органічним розчинником MIBK як суцільною фазою, а водними розчинами як диспергованою фазою. Рівень взаємодії на дні сепаратору спостерігали візуально та контролювали через клапан із ручним управлінням у водному потоці, який залишав дно колонки. Органічному розчиннику MIBK дозволяли залишати верхній сепаратор колонки через водозлив. В попередній екстракції розчин молочної кислоти вихідної реакційної суміші (7 кг/год.), отриманий шляхом, подібним тому як у прикладі 2, контактував як протипотік у пілотному пристрої PDDC pilot setup з MIBK (9,3 кг/год.) при температурі 60 °C. Пульсатор працював з -1 частотою 90 хвил. та амплітудою 11 мм. Молочну кислоту, завантажену органічним розчинником MIBK, збирали протягом кількох годин, щоб отримати достатню кількість для зворотної екстракції. У зворотній екстракції молочна кислота, завантажена органічним розчинником MIBK (10,4 кг/год.), контактувала як протипотік з водою (2,5 кг/год.) у пристрої -1 PDDC setup при температурі 20 °C. Пульсатор працював з частотою 67,5 хвил. та амплітудою 11 мм. Зразки відбирали з водної донної фази. Концентрація молочної кислоти у цьому зразку дорівнювала 34,5 мас. % (визначено потенціометричним титруванням). У цьому прикладі показано, що застосування розчиненого магній хлориду, поєднане з вищою температурою в попередній екстракції збільшує концентрацію молочної кислоти із 29 13 UA 113530 C2 5 10 15 мас. % у розчині вихідної реакційної суміші до 34,5 мас. % у водному розчині після зворотної екстракції. Можна робити висновок, що застосування розчиненого магній хлориду, зрештою, комбіноване з підвищеною температурою в попередній екстракції в екстракційній колонці є ефективними способами концентрування молочної кислоти протягом екстракції. Приклад 10: Зіставлення різних розчинників в екстракції молочної кислоти. Отримували вихідну реакційну суміш розчинів, яка містить 29 мас. % молочної кислоти та 15 мас. % магній хлориду. Розчини перемішували протягом ночі. Екстракцію робили як викладено нижче: 1000 г розчину вихідної реакційної суміші змішували, приблизно, з 100 г розчинника та перемішували при 20 °C протягом мінімум 15 хвилин. Суміш переносили до ділильної лійки, де фази відокремлювали. Зразки обох фаз брали для аналізу. Потім, приблизно, 100 г органічної фази змішували з 10 г чистої води та перемішували протягом мінімум 15 хвил. при 20 °C. Потім усю суміш знов переносили до ділильної лійки, фази відокремлювали та відбирали зразки обох фаз. Зразки аналізували на вміст кислоти. Результати надано в таблиці 3, де inv означає приклад згідно з винаходом, та comp означає порівняльний приклад. Таблиця 3 Розчинник 1 inv 2 inv 3 inv 4 inv 5 inv 6 inv 7 inv 8 inv 9 inv 10 comp 11 comp 12 comp 13 comp 14 comp 15 comp 16 comp 17 comp [молочна кислота] вихідна реакційна суміш (мас. %) 29 29 29 29 29 29 29 29 29 29 29 29 29 29 29 29 29 2-пентанон метил-ізобутил-кетон цикло-гексанон 2-гексанон ацетофенон 2-гептанон 2-октанон діетилетер метил-третинний-бутил-етер етил-пропіл-етер діізопропіловий етер метил-етил-кетон триоктиламін (TOA) н,н-діетил-м-толуамід толуол ізоаміловий спирт TOA-BuOH-Керосин ** [молочна кислота] продукт (мас. %) 30 35 32 35 34 34 30 38 37 25 21 -* 13 27 1 23 11 * не було відокремлення фази в попередній екстракції. Результати не отримано ** 48 мас. % триоктиламін, 20 мас. % н-бутанол та 32 мас. % керосин 20 25 Дані в таблиці 3 показують, що для кетонів C5+ отримано найкращі результати для метилізобутил-кетону. Щодо етерів, тільки діетилетер та метил-третинний-бутил-етер показали ефект концентрації. Однак, слід зазначити, що тоді, як ці сполуки дійсно показали хороші властивості екстракції, це пов'язано зі збитками, які стосуються більшої втрати розчинника та більшого вмісту забруднень у продукті. Приклад 11: Порівняння різних солей в екстракціях молочної кислоти Отримували розчини вихідної реакційної суміші, які містять 29 мас. % молочної кислоти та точно визначену кількість конкретної солі. Розчини перемішували протягом ночі. Експерименти щодо екстракції робили згідно процедури, описаної в прикладі 10, застосовуючи метил-ізобутилкетон як розчинник. Результати надано в таблиці 4, де inv означає приклад згідно з винаходом, та comp означає порівняльний приклад. 14 UA 113530 C2 Таблиця 4 сіль (концентрація) 1 inv 2 comp 3 comp 4 comp 5 comp 6 comp 7 comp 8 comp 5 MgCl2 (15 мас. %) CaCl2 (18 мас. %) NaCl (19 мас. %) KCl (24 мас. %) NaNO3 (27 мас. %) Na2SO4 (23 мас. %) Na3PO4 (18 мас. %) (NH4)2SO4 (23 мас. %) [молочна кислота] вихідна реакційна суміш (мас. %) 29 29 29 29 29 29 29 29 [молочна кислота] продукт (мас. %) 35 18 23 21 24 23 6,4 26 Як можна побачити з таблиці 4, тільки MgCl2 надає ефект концентрації. Усі інші солі надають послаблений ефект. Конкретно це - дивовижна дія, оскільки концентрація солей є вищою ніж концентрація MgCl2, а вища концентрація, як вважають, стимулює ефект концентрації. ФОРМУЛА ВИНАХОДУ 10 15 20 25 30 35 40 45 1. Спосіб регенерації молочної кислоти з водної суміші, який включає наступні етапи: - забезпечення водної суміші, яка містить молочну кислоту та принаймні 5 мас. % розчиненого магнію хлориду, базованого на загальній масі води, та розчинення матеріалу у водній суміші, - екстрагування молочної кислоти з водної суміші в першу органічну рідину, яка містить принаймні 90 мас. % органічного розчинника, вибраного із групи, яка складається з наступного: кетони С5+, діетилетер та метил-третинний-бутил-етер, отримуючи, таким чином, органічний розчин молочної кислоти та водну відпрацьовану рідину, яка містить магнію хлорид, та - екстрагування молочної кислоти з органічного розчину молочної кислоти у водну рідину, отримуючи, таким чином, водний розчин молочної кислоти та другу органічну рідину. 2. Спосіб за п. 1, де водна суміш містить принаймні 15 мас. % розчиненого магнію хлориду, базованого на загальній масі води та розчиненого матеріалу у водній суміші. 3. Спосіб за п. 1 або 2, де органічний розчинник - кетон С5-С8. 4. Спосіб за п. 3, де органічний розчинник є метил-ізобутил-кетоном. 5. Спосіб за будь-яким із попередніх пунктів, де перший етап екстракції здійснюють при температурі принаймні 30 °C. 6. Спосіб за будь-яким із пп. 1-5, де другий етап екстракції здійснюють при температурі, яка є нижчою, ніж температура, при якій здійснено першу екстракцію. 7. Спосіб за п. 6, де другий етап екстракції здійснено при температурі на 10-50 °C нижче, ніж температура, при якій здійснено першу екстракцію. 8. Спосіб за будь-яким із пп. 1-6, де другий етап екстракції здійснено в межах 10 °C температури, при якій здійснено першу екстракцію. 9. Спосіб за будь-яким із пп. 1-8, де органічна рідина не містить екстрагентів. 10. Спосіб за будь-яким із пп. 1-8, де органічна рідина не містить екстрагентів аміну. 11. Спосіб за будь-яким із пп. 1-10, де органічна рідина, по суті, є вільною від амінів, етерів та спиртів, що означає, що ці сполуки, якщо присутні повністю, кожна присутня в кількості, меншій 2 мас. %, обчисленій щодо маси органічної рідини. 12. Спосіб за будь-яким із пп. 1-11, де водна суміш має рН 2 або нижче. 13. Спосіб за будь-яким із пп. 1-12, який додатково включає: - піддавання розчину магнію хлориду етапу термічного розкладу при температурі принаймні 300 °C, розкладаючи, таким чином, сіль магнію хлориду до магнію оксиду та НСl, та - розчинення НСl, утвореної в етапі термічного розкладу у воді, отримуючи, таким чином, розчин НСl. 14. Спосіб за будь-яким із пп. 1-12, що додатково включає: - піддавання розчину магнію хлориду етапу термічного розкладу при температурі принаймні 300 °C, розкладаючи, таким чином, сіль магнію хлориду до магнію оксиду та НСl, та - розчинення НСl, утвореної в етапі термічного розкладу у воді, отримуючи, таким чином, розчин НСl, та - рециркуляція магнію оксиду в етапі ферментації як засобу нейтралізації або попередника цього. 15 UA 113530 C2 5 10 15. Спосіб за будь-яким із пп. 1-14, що додатково включає етап ферментації для створення молочної кислоти, причому етап ферментації включає етапи бродіння джерела карбону за допомогою мікроорганізму у ферментаційному бульйоні для створення молочної кислоти та нейтралізації принаймні частини молочної кислоти додаванням магнієвої основи, отримуючи, таким чином, відповідний лактат. 16. Спосіб за п. 15, який додатково включає етап отримання водної суміші підкислюванням солі лактату HCl, отримуючи, таким чином, водну суміш. 17. Спосіб за п. 16, який додатково включає етап концентрування цієї отриманої водної суміші до екстракції до концентрації розчиненої солі принаймні 5 мас. %, що базовано на загальній масі води та розчиненого матеріалу у водній суміші. Комп’ютерна верстка О. Гергіль Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 16
ДивитисяДодаткова інформація
Назва патенту англійськоюLactic acid extraction
Автори англійськоюde Haan, Andre, Banier, van Krieken, Jan, Dekic Zivkovic, Tanja
Автори російськоюдэ Хан Андрэ Банье, ван Крикен Ян, Дэкич Живкович Таня
МПК / Мітки
МПК: B01D 11/04, C07C 59/08, C07C 51/48, C12P 7/00
Мітки: екстракція, молочної, кислоти
Код посилання
<a href="https://ua.patents.su/18-113530-ekstrakciya-molochno-kisloti.html" target="_blank" rel="follow" title="База патентів України">Екстракція молочної кислоти</a>
Попередній патент: Мартенситні сталі з міцністю при розтягуванні 1700-2200 мпа
Наступний патент: Пристрій для фіксації ємності, призначеної, зокрема, для рідких продуктів
Випадковий патент: Горілка особлива "золото полуботка. ювілейна"