Спосіб одержання похідного піридину
Номер патенту: 74687
Опубліковано: 16.01.2006
Автори: Тохіама Йосітомо, Коморі Такасі, Санеміцу Юзуру
Формула / Реферат
1. Спосіб одержання похідного піридину формули [d]
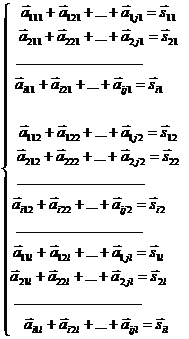 ,[d]
,[d]
де R1, R3 і R4 є такими, як вони визначені нижче, взаємодією похідного піридону формули [а]
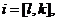 ,[a]
,[a]
де R3 є атомом галогену, ціаногрупою або нітрогрупою і R4 є атомом водню або атомом галогену з похідним α-діазоефіру формули [f]
N2CHCOR1 ,[f]
де R1 є С1-С6-алкоксигрупою у присутності кислоти.
2. Спосіб за п. 1, в якому кислота є апротонною кислотою.
3. Спосіб за п. 1, в якому кислота є сіллю родію (II).
4. Спосіб за п. 1, в якому кислота є трифторидом бору.
5. Спосіб за п. 1, в якому кислота є сульфоновою кислотою.
6. Похідне піридону формули [а]
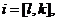 , [a]
, [a]
де R3 є атомом галогену, ціаногрупою або нітрогрупою і R4 є атомом водню або атомом галогену.
7. Похідне піридону за п. 6, де R3 є атомом галогену і R4 є атомом галогену.
8. Похідне піридону за п. 6, де R3 є атомом хлору і R4 є атомом фтору.
Текст
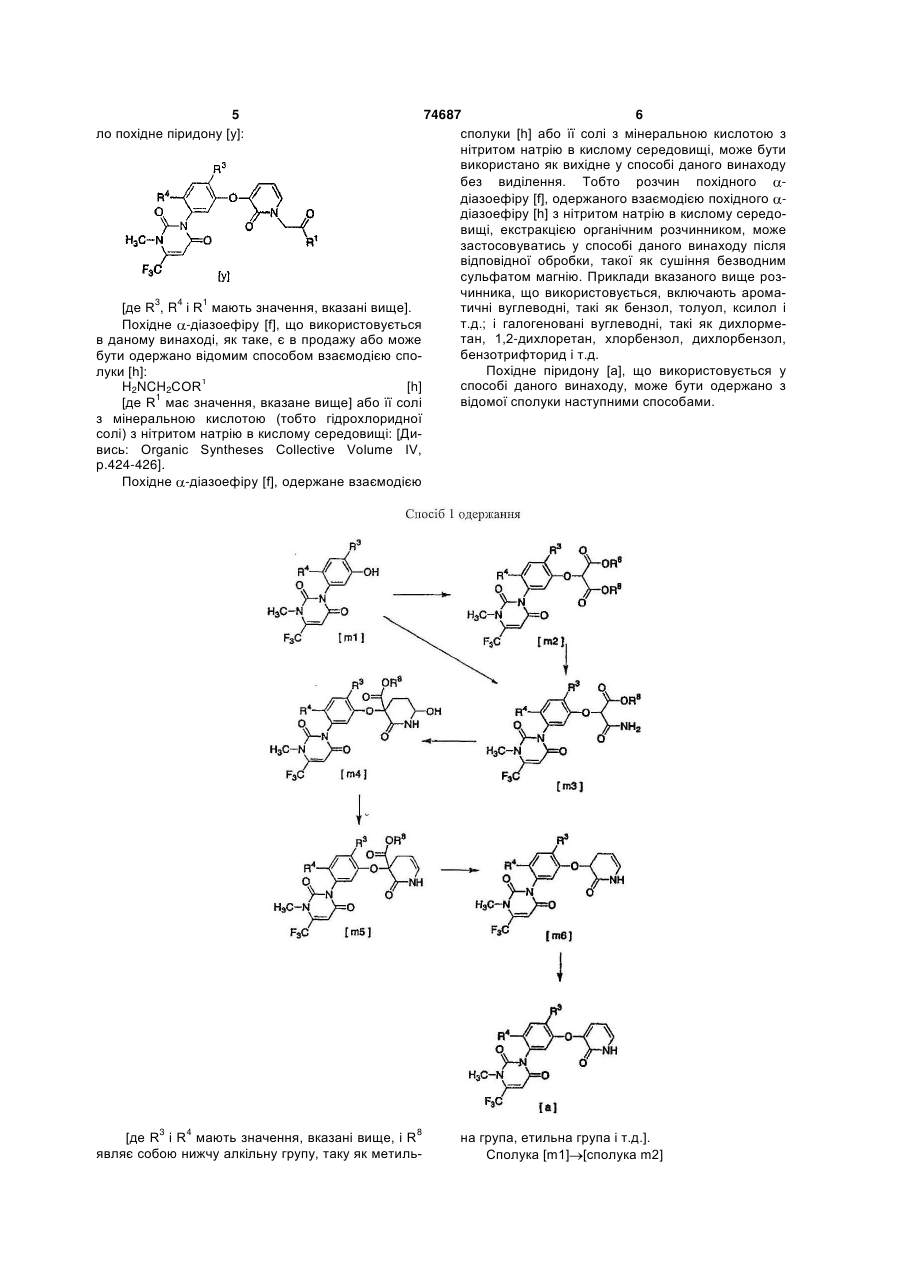
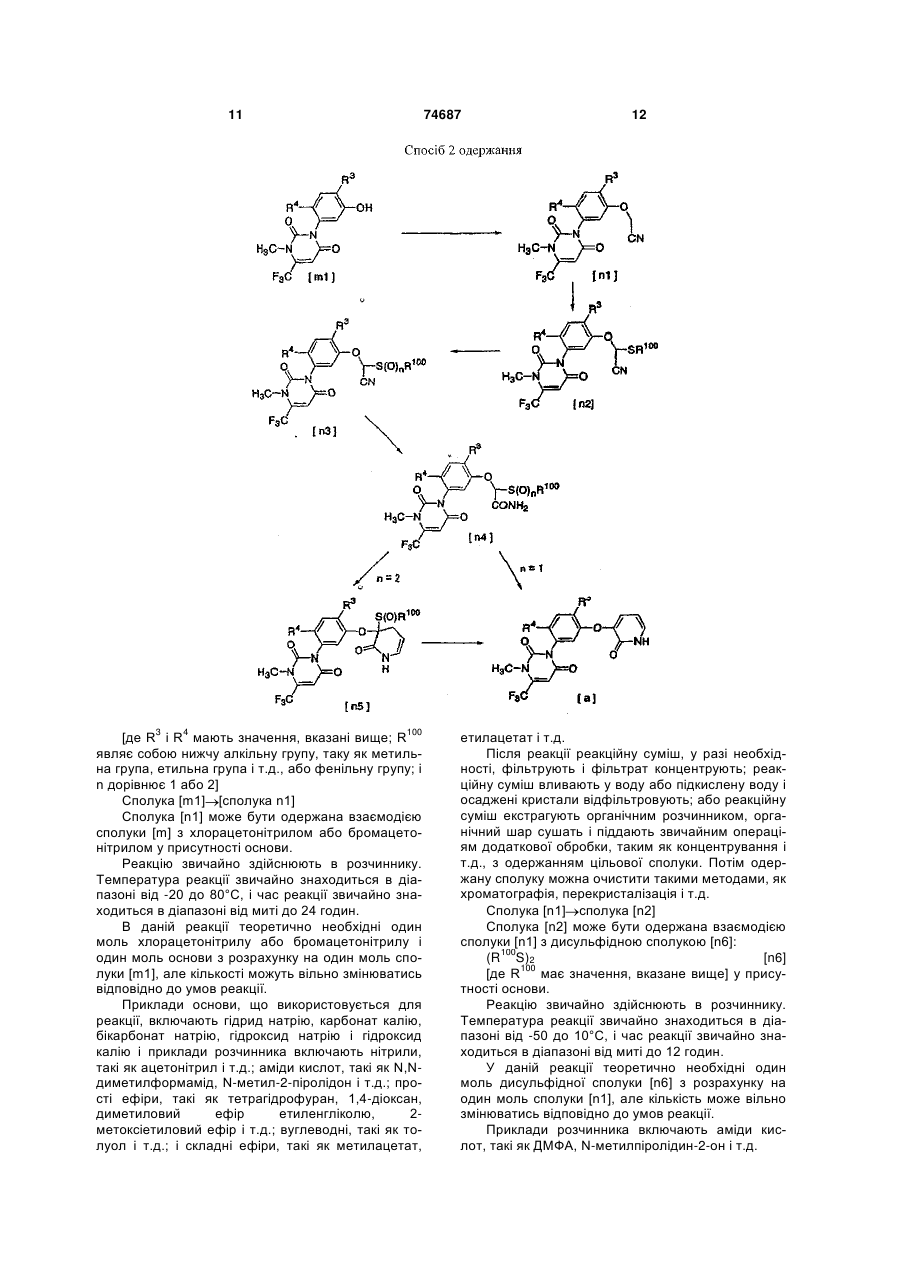
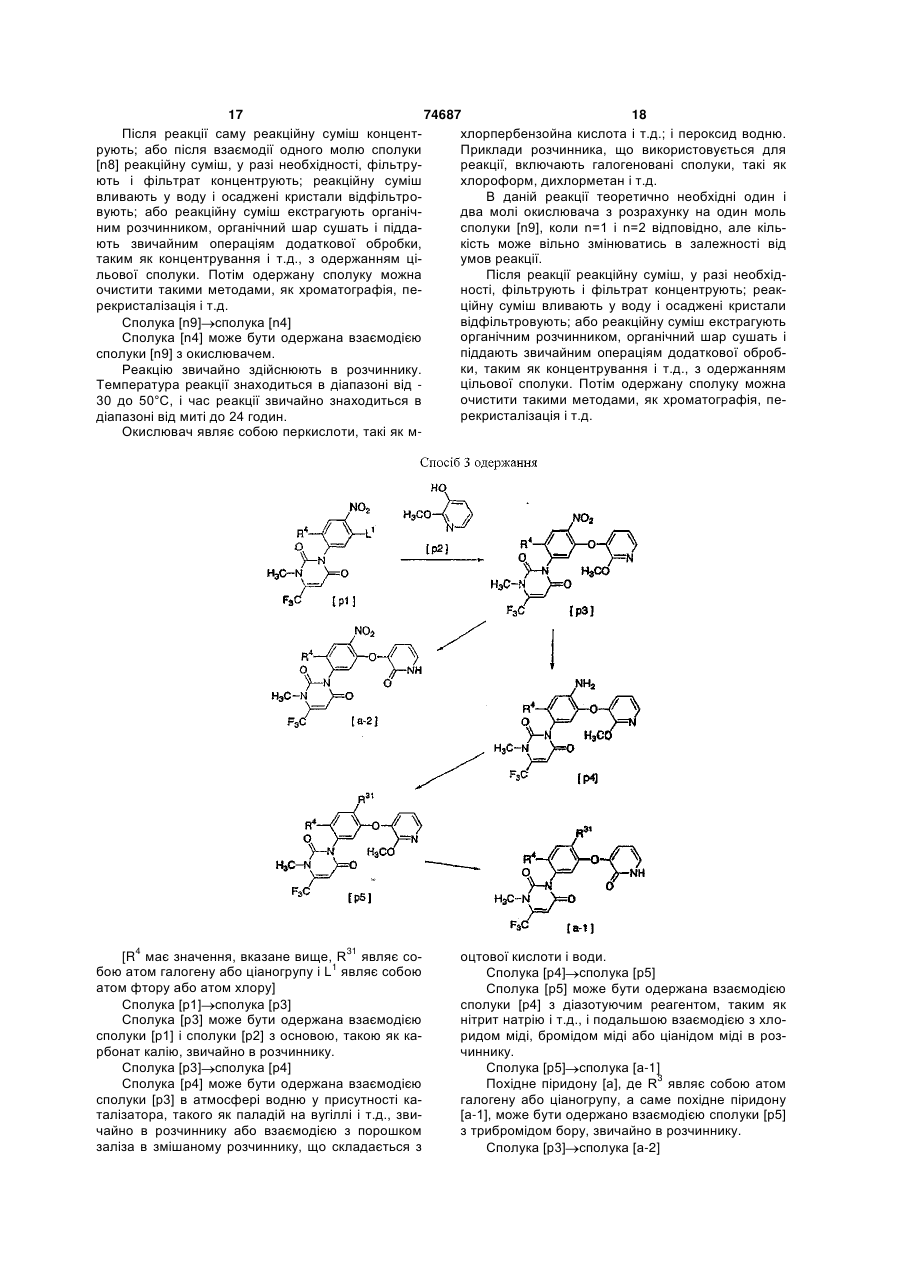
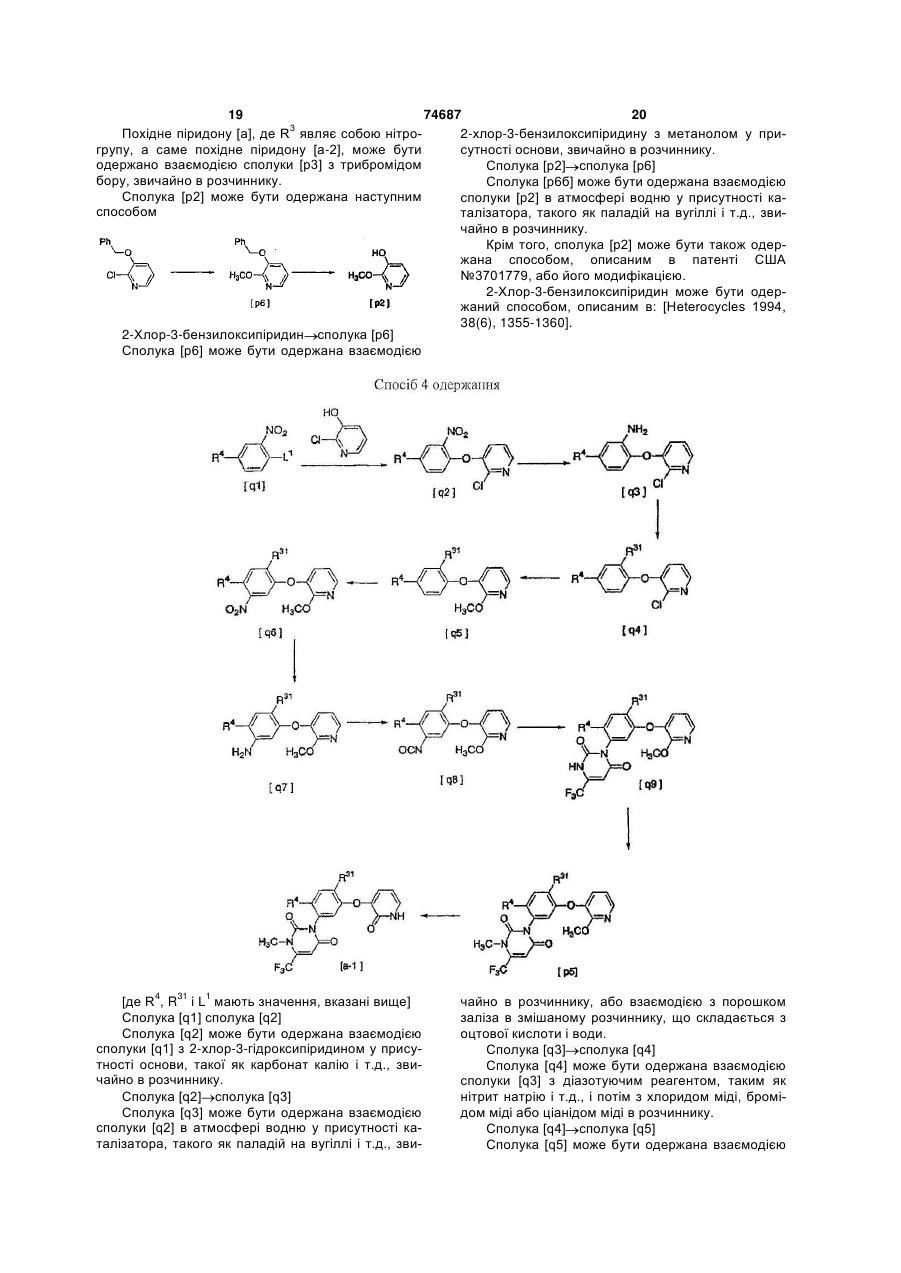
1. Спосіб одержання похідного піридину формули [d] 2 (19) Даний винахід відноситься до нового способу одержання похідних піридину, що володіють чудовою гербіцидною активністю, і до вихідних сполук, що використовуються для способу. Похідні піридину (d): [де R1 являє собою С1-С6-алкоксигрупу, R3 яв 3 74687 4 ляє собою атом галогену, ціаногрупу або нітрогручає катіон двовалентного родію і відповідний аніпу і R4 являє собою атом водню або атом галогеон, і, крім того, необов'язково відповідний ліганд і ну] володіють чудовою гербіцидною активністю. типові приклади являють собою димер трифтораПохідні піридину [d] містять два гетероциклічних цетату родію (II) ([CF3CO2)2Rh]2), димер ацетату кільця, які являють собою урацилове кільце і піриродію (II) ([CH3CO2)2Rh]2) і т.д. Як трифторид бору динове кільце, і є вельми бажаним вигідний спосіб може бути використаний сам BF3 або його комїх одержання. Задачею даного винаходу є вигідний плекс, і приклади комплексу включають діетилефіспосіб одержання похідних піридину [d], які волорний комплекс, диметилсульфідний комплекс, тетдіють специфічною системою замісників, і до вихірагідрофурановий комплекс і т.д. Беручи до уваги дних сполук, що використовуються в цьому спосошвидкість реакції, переважно використати як кисбі. лоту димер трифторацетату родію (II), комплекс Для створення вигідного способу одержання трифторид бору/діетиловий ефір, тетрахлорид похідних піридину [d] автори даного винаходу проолова або трифторметансульфонову кислоту. водили інтенсивні дослідження. В результаті вони В даній реакції теоретично необхідний один виявили, що похідне піридину [d] може бути одермоль похідного -діазоефіру [f] з розрахунку на жано взаємодією похідного піридону [а]: один моль похідного піридону [а], а практично використовуються від 1 до 2моль похідного діазоефіру. В даній реакції кислота має каталітичну активність і її використовують з урахуванням швидкості реакції в кількості, що знаходиться в діапазоні від 0,001 до 5моль, переважно в кількості 0,01моль або більше з розрахунку на моль похідного піридону [а]. Температура реакційної маси в даній реакції з урахуванням її швидкості звичайно складає від -50 до 120°С, переважно -20°С або більше. Час реакції звичайно знаходиться в діапа3 4 [де R і R мають значення, вказані вище] з позоні від миті до 72 годин. хідним -діазоефіру [f] Реагенти, що використовуються для даної ре1 NaCHCOR [f] акції, додають в реакційну посудину, наприклад в 1 [де R має значення, вказане вище] у присутнаступному порядку. ності кислоти для здійснення регіоселективного О1) Спосіб включає попереднє змішування похіалкілування, внаслідок чого був створений даний дного піридону [а], кислоти і розчинника і додаванвинахід. За рахунок вибору способу даного винаня в суміш краплями похідного -діазоефіру [f]. ходу може бути вигідно одержане похідне піридину 2) Спосіб включає попереднє змішування похі[d], що має специфічну систему замісників. дного піридону [а], похідного -діазоефіру [f ] і розСаме даний винахід відноситься до способу чинника і додавання в суміш краплями кислоти. одержання похідного піридину [d] взаємодією похі3) Спосіб включає попереднє змішування похідного піридону [а] з похідним -діазоефіру [f] у дного піридону [а] і розчинника і додавання в суприсутності кислоти (далі вказується як «спосіб міш краплями відповідно кислоти і похідного даного винаходу) і до похідного піридону [а], яке діазоефіру [f]. являє собою необхідну вихідну сполуку, що викоЗакінчення даної реакції може бути встановристовується в цьому способі. У даному винаході лене відбиранням частини реакційної суміші, ана1 приклади С1-Сб-алкоксильної групи, дані для R , лізом проби рідинною хроматографією, тонкошавключають метоксигрупу, етоксигрупу, пропоксигровою хроматографією і т.д. і вимірюванням 3 рупу і т.д. і приклади атома галогену, дані для R і кількості, що залишилась, похідного піридону [а] R4, включають атом фтору, атом хлору і атом або похідного -діазоефіру [f]. брому. Після реакції похідне піридину [d] може бути Спосіб даного винаходу здійснюється взаємоодержано, наприклад, наступними методами додією похідного піридону [а] з похідним даткової обробки реакційної суміші: діазоефіру [f] у присутності кислоти і реакцію зви1) Фільтрація реакційної суміші і концентручайно проводять в розчиннику. Приклади розчинвання фільтрату. ника включають ароматичні вуглеводні, такі як 2) Хроматографування реакційної суміші на бензол, толуол, ксилол і т.д.; галогеновані вуглесилікагелі і потім концентрування. водні, такі як 1,2-дихлоретан, хлорбензол, дихлор3) Вливання реакційної суміші у водний розчин бензол і т.д.; і їх суміші. бікарбонату натрію, екстракція органічним розчинВ даному способі кислота означає кислоту, виником, сушіння і концентрування органічного шару. значену Льюїсом, а саме речовину, яка може Одержане похідне піридину [d] може бути приймати електронну пару, і включає апротонну очищено таким методом, як хроматографія, перекислоту і протонну кислоту (кислота Бренстеда). кристалізація і т.д. Приклади апротонної кислоти включають солі роУ випадку взаємодії похідного піридону [а] зі дію (II), трифторид бору і тетрахлорид олова, і складноефірною сполукою [х]: приклади протонної кислоти включають сульфоX1CH2COR1 [х] нові кислоти, такі як трифторметансульфонова [де R1 має значення, вказане вище і X1 являє кислота, п-толуолсульфонова кислота і т.д.; трисобою атом хлору, атом брому, метансульфонілофтороцтову кислоту; і сірчану кислоту. Термін ксигрупу або п-толуолсульфонілоксигрупу] «солі родію (II)» означає металеву сіль, що вклюу присутності основи, основним продуктом бу 5 ло похідне піридону [у]: 74687 6 сполуки [h] або її солі з мінеральною кислотою з нітритом натрію в кислому середовищі, може бути використано як вихідне у способі даного винаходу без виділення. Тобто розчин похідного діазоефіру [f], одержаного взаємодією похідного діазоефіру [h] з нітритом натрію в кислому середовищі, екстракцією органічним розчинником, може застосовуватись у способі даного винаходу після відповідної обробки, такої як сушіння безводним сульфатом магнію. Приклади вказаного вище розчинника, що використовується, включають арома[де R3, R4 і R1 мають значення, вказані вище]. тичні вуглеводні, такі як бензол, толуол, ксилол і т.д.; і галогеновані вуглеводні, такі як дихлормеПохідне -діазоефіру [f], що використовується тан, 1,2-дихлоретан, хлорбензол, дихлорбензол, в даному винаході, як таке, є в продажу або може бензотрифторид і т.д. бути одержано відомим способом взаємодією споПохідне піридону [а], що використовується у луки [h]: способі даного винаходу, може бути одержано з H2NCH2СOR1 [h] відомої сполуки наступними способами. [де R1 має значення, вказане вище] або її солі з мінеральною кислотою (тобто гідрохлоридної солі) з нітритом натрію в кислому середовищі: [Дивись: Organic Syntheses Collective Volume IV, p.424-426]. Похідне -діазоефіру [f], одержане взаємодією [де R3 і R4 мають значення, вказані вище, і R8 являє собою нижчу алкільну групу, таку як метиль на група, етильна група і т.д.]. Сполука [m1] [сполука m2] 7 74687 Сполуку [m2] одержують взаємодією сполуки [m1] зі сполукою [m7]: [де R8 має значення, вказане вище, і X являє собою групу, що видаляється, таку як атом хлору, атом брому і т.д.] у присутності основи. Реакцію звичайно здійснюють в розчиннику. Температура реакції звичайно знаходиться в діапазоні від кімнатної температури до 80°С, і час реакції звичайно знаходиться в діапазоні від миті до 12 годин. В даній реакції теоретично необхідні один моль сполуки [m7] і один моль основи з розрахунку на один моль сполуки [m1], але кількості можуть вільно змінюватись відповідно до умов реакції. Приклади основи, що використовується для реакції, включають карбонат калію і приклади розчинника включають нітрили, такі як ацетонітрил і т.д.; і аміди кислот, такі як N,N-диметилформамід, N-метил-2-піролідон і т.д. Після реакції реакційну суміш, у разі необхідності, фільтрують і фільтрат концентрують; реакційну суміш вливають у воду або підкислену воду і осаджені кристали відфільтровують; або реакційну суміш екстрагують органічним розчинником, органічний шар сушать і піддають звичайним операціям додаткової обробки, таким як концентрування і т.д., з одержанням цільової сполуки. Потім одержану сполуку можна очистити такими методами, як хроматографія, перекристалізація і т.д. Сполука [m2] сполука [m3] Сполука [m3] одержується взаємодією сполуки [m2] з аміаком. Реакцію звичайно здійснюють в розчиннику. Температура реакції звичайно знаходиться в діапазоні від -20°С до 50°С, і час реакції звичайно знаходиться в діапазоні від миті до 12 годин. В даній реакції теоретично необхідний один моль аміаку з розрахунку на один моль сполуки [m2], але кількість може вільно змінюватись відповідно до умов реакції. Приклади розчинника, що використовується для реакції, включають спирти, такі як метанол, етанол і т.д. Після реакції реакційну суміш, у разі необхідності, фільтрують і фільтрат концентрують; реакційну суміш вливають у воду і осаджені кристали відфільтровують; або реакційну суміш екстрагують органічним розчинником, органічний шар сушать і піддають звичайним операціям додаткової обробки, таким як концентрування і т.д., з одержанням цільової сполуки. Потім одержану сполуку можна очистити такими методами, як хроматографія, перекристалізація і т.д. Сполука [m1] [сполука m3] Сполука [m3] одержується взаємодією сполуки [m1] зі сполукою [m8]: 8 [де R8 і X мають значення, вказані вище] у присутності основи. Реакцію звичайно здійснюють в розчиннику. Температура реакції звичайно знаходиться в діапазоні від кімнатної температури до 80°С, і час реакції звичайно знаходиться в діапазоні від миті до 12 годин. В даній реакції теоретично необхідні один моль сполуки [m8] і один моль основи з розрахунку на один моль сполуки [m1], але кількості можуть вільно змінюватись відповідно до умов реакції. Приклади основи, що використовується для реакції, включають карбонат калію і приклади розчинника включають нітрили, такі як ацетонітрил і т.д.; і аміди кислот, такі як Ν,Ν-диметилформамід, N-метил-2-піролідон і т.д. Після реакції реакційну суміш, у разі необхідності, фільтрують і фільтрат концентрують; реакційну суміш вливають у воду або підкислену воду і осаджені кристали відфільтровують; або реакційну суміш екстрагують органічним розчинником, органічний шар сушать і піддають звичайним операціям додаткової обробки, таким як концентрування і т.д., з одержанням цільової сполуки. Потім одержану сполуку можна очистити такими методами, як хроматографія, перекристалізація і т.д. Сполука [m3] сполука [m4] Сполука [m4] одержується взаємодією сполуки [m3] з акролеїном у присутності основи. Реакцію звичайно здійснюють в розчиннику. Температура реакції звичайно знаходиться в діапазоні від --30 до 50°С, переважно від -10°С до 20°С. Час реакції звичайно знаходиться в діапазоні від миті до 12 годин. В даній реакції теоретично необхідні один моль акролеїну і від 0,01 до 2моль основи з розрахунку на один моль сполуки [m3], але кількості можуть вільно змінюватись відповідно до умов реакції. Приклади основи, що використовується для реакції, включають алкоксиди металів, такі як третбутоксид калію і т.д.; і неорганічні основи, такі як карбонат калію і т.д. Приклади розчинника, що використовується для реакції, включають прості ефіри, такі як тетрагідрофуран і т.д.; і складні ефіри, такі як етилацетат і т.д. Після реакції реакційну суміш, у разі необхідності, фільтрують і фільтрат концентрують; реакційну суміш вливають у воду і осаджені кристали відфільтровують; або реакційну суміш екстрагують органічним розчинником, органічний шар сушать і піддають звичайним операціям додаткової обробки, таким як концентрування і т.д., з одержанням цільової сполуки. Потім одержану сполуку можна очистити такими методами, як хроматографія, перекристалізація і т.д. Сполука [m4] сполука [m5] Сполука [m5] одержується взаємодією сполуки [m4] у присутності кислоти. 9 74687 10 Реакцію звичайно здійснюють в розчиннику. ки, таким як концентрування і т.д., з одержанням Температура реакції звичайно знаходиться в діацільової сполуки. Потім одержану сполуку можна пазоні від кімнатної температури до 150°С, і час очистити такими методами, як хроматографія, переакції звичайно знаходиться в діапазоні від миті рекристалізація і т.д. до 24 годин. Сполука [m6] похідне піридону [а] В даній реакції використовується від 0,001 до Похідне піридону [а] одержується взаємодією 0,2моль кислоти з розрахунку на один моль сполусполуки [m6] з дегідруючим реагентом. ки [m4], але кількість може вільно змінюватись Реакцію звичайно здійснюють в розчиннику. відповідно до умов реакції. Температура реакції звичайно знаходиться в діаПриклади кислоти, що використовується для пазоні від 60 до 190°С, і час реакції звичайно знареакції, включають органічні кислоти, такі як оцтоходиться в діапазоні від миті до 48 годин. ва кислота, п-толуолсульфонова кислота і т.д.; і Дегідруючий реагент, що використовується неорганічні кислоти, такі як хлористоводнева кисдля даної реакції, означає хіноїдні окислювальні лота і т.д. Приклади розчинника включають прості реагенти, такі як хлораніл і т.д.; і гетерогенний меефіри, такі як тетрагідрофуран і т.д.; і складні ефіталевий каталізатор, такий як паладій на вугіллі і ри, такі як етилацетат і т.д. Після реакції реакційну т.д. суміш, у разі необхідності, фільтрують і фільтрат В даній реакції використовується від 1 до концентрують; реакційну суміш вливають у воду і 3моль хіноїдного окислювального реагенту, або осаджені кристали відфільтровують; або реакційну від 10 до 30мас.% гетерогенного металевого катасуміш екстрагують органічним розчинником, оргалізатора з розрахунку на один моль сполуки [m6], нічний шар сушать і піддають звичайним операціале кількість може вільно змінюватись в залежносям додаткової обробки, таким як концентрування і ті від умов реакції. т.д., з одержанням цільової сполуки. Потім одерПриклади розчинника включають ароматичні жану сполуку можна очистити такими методами, як вуглеводні, такі як толуол, ксилол і т.д.; галогенохроматографія, перекристалізація і т.д. вані ароматичні вуглеводні, такі як хлорбензол, Сполука [m5] сполука [m6] дихлорбензол, бензотрифторид і т.д.; прості ефіСполука [m6] одержується із сполуки [m5] у ри, такі як діоксан, тетрагідрофуран, диглим, диприсутності води і галогеніду лужного металу, звифеніловий ефір і т.д.; і їх суміші. чайно в розчиннику. Після реакції реакційну суміш, у разі необхідТемпература реакції звичайно знаходиться в ності, фільтрують і фільтрат концентрують; реакдіапазоні від 80 до 140°С, і час реакції звичайно ційну суміш розбавляють органічним розчинником, знаходиться в діапазоні від миті до 48 годин. потім вливають у водний розчин бікарбонату наВ даній реакції використовуються від 0,5 до трію, екстрагують органічним розчинником, органі2моль води і від 1 до 5моль галогеніду лужного чний шар сушать і піддають звичайним операціям металу з розрахунку на один моль сполуки [m5], додаткової обробки, таким як концентрування і але кількості можуть вільно змінюватись відповідт.д., з одержанням цільової сполуки. Потім одерно до умов реакції. жану сполуку можна очистити такими методами, як Приклади лужного металу, що використовухроматографія, перекристалізація і т.д. ється для реакції галогеніду, включають хлорид Сполука [m1] відома з патенту США №4859229 літію, хлорид натрію, йодид літію і йодид натрію і і може бути одержана відомим способом або подіприклади розчинника включають диметилсульфобними способами. ксид і піридин. Сполука [m7] як така є в продажу або може буПісля реакції реакційну суміш, у разі необхідти одержана відомим способом. ності, фільтрують і фільтрат концентрують; реакСполука [m8] може бути одержана взаємодією ційну суміш вливають у воду і осаджені кристали сполуки [m7] з аміаком при умовах реакції, предвідфільтровують; або реакційну суміш екстрагують ставлених вище для перетворення «Сполука [m2] органічним розчинником, органічний шар сушать і сполука [m3]». піддають звичайним операціям додаткової оброб 11 [де R3 і R4 мають значення, вказані вище; R100 являє собою нижчу алкільну групу, таку як метильна група, етильна група і т.д., або фенільну групу; і n дорівнює 1 або 2] Сполука [m1] [сполука n1] Сполука [n1] може бути одержана взаємодією сполуки [m] з хлорацетонітрилом або бромацетонітрилом у присутності основи. Реакцію звичайно здійснюють в розчиннику. Температура реакції звичайно знаходиться в діапазоні від -20 до 80°С, і час реакції звичайно знаходиться в діапазоні від миті до 24 годин. В даній реакції теоретично необхідні один моль хлорацетонітрилу або бромацетонітрилу і один моль основи з розрахунку на один моль сполуки [m1], але кількості можуть вільно змінюватись відповідно до умов реакції. Приклади основи, що використовується для реакції, включають гідрид натрію, карбонат калію, бікарбонат натрію, гідроксид натрію і гідроксид калію і приклади розчинника включають нітрили, такі як ацетонітрил і т.д.; аміди кислот, такі як Ν,Νдиметилформамід, N-метил-2-піролідон і т.д.; прості ефіри, такі як тетрагідрофуран, 1,4-діоксан, диметиловий ефір етиленгліколю, 2метоксіетиловий ефір і т.д.; вуглеводні, такі як толуол і т.д.; і складні ефіри, такі як метилацетат, 74687 12 етилацетат і т.д. Після реакції реакційну суміш, у разі необхідності, фільтрують і фільтрат концентрують; реакційну суміш вливають у воду або підкислену воду і осаджені кристали відфільтровують; або реакційну суміш екстрагують органічним розчинником, органічний шар сушать і піддають звичайним операціям додаткової обробки, таким як концентрування і т.д., з одержанням цільової сполуки. Потім одержану сполуку можна очистити такими методами, як хроматографія, перекристалізація і т.д. Сполука [n1] сполука [n2] Сполука [n2] може бути одержана взаємодією сполуки [n1] з дисульфідною сполукою [n6]: (R100S)2 [n6] [де R100 має значення, вказане вище] у присутності основи. Реакцію звичайно здійснюють в розчиннику. Температура реакції звичайно знаходиться в діапазоні від -50 до 10°С, і час реакції звичайно знаходиться в діапазоні від миті до 12 годин. У даній реакції теоретично необхідні один моль дисульфідної сполуки [n6] з розрахунку на один моль сполуки [n1], але кількість може вільно змінюватись відповідно до умов реакції. Приклади розчинника включають аміди кислот, такі як ДМФА, N-метилпіролідин-2-он і т.д. 13 74687 14 Після реакції реакційну суміш, у разі необхідтрію. ності, фільтрують і фільтрат концентрують; реакСполука [n4] похідне піридону [а] ційну суміш вливають у воду і осаджені кристали Похідне піридону [а] може бути одержано взавідфільтровують; або реакційну суміш екстрагують ємодією сполуки [n4], де n дорівнює 1, з акролеїорганічним розчинником, органічний шар сушать ρ ном у присутності основи і подальшим перетвопіддають звичайним операціям додаткової обробренням у присутності кислоти. ки, таким як концентрування і т.д., з одержанням Реакцію звичайно здійснюють в розчиннику. цільової сполуки. Потім одержану сполуку можна Температура реакції на першій стадії знаходиться очистити такими методами, як хроматографія, пев діапазоні від -20 до 50°С, і температура реакції рекристалізація і т.д. на другій стадії знаходиться в діапазоні від кімнатСполука [n2] сполука [n3] ної температури до 80°С. Час реакції звичайно Сполука [n3] може бути одержана взаємодією знаходиться в діапазоні від миті до 48 годин. сполуки [n2] з окислювачем. Приклади основи, що використовується для Реакцію звичайно здійснюють в розчиннику. реакції, включають гідрид натрію, трет-бутоксид Температура реакції звичайно знаходиться в діакалію, гідроксид натрію, карбонат калію, фторид пазоні від -20 до 50°С, і час реакції звичайно знакалію і т.д. і приклади кислоти включають оцтову ходиться в діапазоні від миті до 24 годин. кислоту, трифтороцтову кислоту, метансульфоноОкислювач являє собою перкислоти, такі як мву кислоту, п-толуолсульфонову кислоту, трифтохлорпербензойна кислота і т.д.; і пероксид водню. рид бору і його комплекс (наприклад, комплекс Приклади розчинника, що використовується для трифторид бору-метанол). Приклади розчинника реакції, включають галогеновані сполуки, такі як включають прості ефіри, такі як діетиловий ефір, хлороформ, дихлорметан і т.д. метил трет-бутиловий ефір, диметоксіетан, тетраВ даній реакції теоретично необхідні один і гідрофуран, 1,4-діоксан і т.д.; галогеновані сполудва молі окислювача з розрахунку на один моль ки, такі як хлороформ, дихлорметан і т.д.; і вуглесполуки [т2], коли т=1 і т=2 відповідно, але кільводні, такі як толуол і т.д. кість може вільно змінюватись відповідно до умов В даній реакції теоретично необхідні кількості реакції. основи і кислоти, які дорівнюють відповідно від Після реакції реакційну суміш, у разі необхідкаталітичної кількості до одного еквівалента і від ності, фільтрують і фільтрат концентрують; реаккаталітичної кількості до надлишку, і один моль ційну суміш вливають у воду і осаджені кристали акролеїну з розрахунку на один моль сполуки [n4], відфільтровують; або реакційну суміш екстрагують але кількості можуть вільно змінюватись відповідорганічним розчинником, органічний шар сушать і но до умов реакції. піддають звичайним операціям додаткової обробПісля реакції реакційну суміш, у разі необхідки, таким як концентрування і т.д., з одержанням ності, фільтрують і фільтрат концентрують; реакцільової сполуки. Потім одержану сполуку можна ційну суміш вливають у воду і осаджені кристали очистити такими методами, як хроматографія, певідфільтровують; або реакційну суміш екстрагують рекристалізація і т.д. органічним розчинником, органічний шар сушать і піддають звичайним операціям додаткової обробСполука [n3] сполука [n4] ки, таким як концентрування і т.д., з одержанням Сполука [n4] може бути одержана взаємодією цільової сполуки. Потім одержану сполуку можна сполуки [n3] у присутності води і діоксиду марганочистити такими методами, як хроматографія, пецю. рекристалізація і т.д. Реакцію звичайно здійснюють в розчиннику. Температура реакції звичайно знаходиться в діаСполука [n4] сполука [n5] пазоні від 50 до 120°С, і час реакції звичайно знаСполука [n5] може бути одержана взаємодією ходиться в діапазоні від миті до 24 годин. сполуки [п4], де n дорівнює 2, з акролеїном у приДіоксид марганцю в даній реакції використовусутності основи і подальшим перетворенням у ється в кількості від каталітичної кількості до надприсутності кислоти. лишку. Реакцію звичайно здійснюють в розчиннику. Приклади розчинника, що використовується Температура реакції першої стадії знаходиться в для реакції, включають воду і суміші води з органідіапазоні від -20 до 50°С, і температура реакції чним розчинником (спирти, такі як метанол, етадругої стадії знаходиться в діапазоні від кімнатної нол, ізопропанол і т.д.; кетони, такі як ацетон, метемператури до 50°С. Час реакції звичайно знахотилетилкетон, метилізобутилкетон і т.д.; і прості диться в діапазоні від миті до 48 годин. ефіри, такі як тетрагідрофуран, 1,4-діоксан і т.д.). Приклади основи, що використовується для Після реакції реакційну суміш, у разі необхідреакції включають гідрид натрію, трет-бутоксид ності, фільтрують і фільтрат концентрують; реаккалію, гідроксид натрію, карбонат калію, фторид ційну суміш вливають у воду і осаджені кристали калію і т.д. і приклади кислоти включають оцтову відфільтровують; або реакційну суміш екстрагують кислоту, трифтороцтову кислоту, метансульфоноорганічним розчинником, органічний шар сушать і ву кислоту, п-толуолсульфонову кислоту, трифтопіддають звичайним операціям додаткової обробрид бору і його комплекс (наприклад, комплекс ки, таким як концентрування і т.д., з одержанням трифторид бору-метанол). Приклади розчинника цільової сполуки. Потім одержану сполуку можна включають прості ефіри, такі як діетиловий ефір, очистити такими методами, як хроматографія, пеметилтрет-бутиловий ефір, диметоксіетан, тетрарекристалізація і т.д. гідрофуран, 1,4-діоксан і т.д.; галогеновані сполуСполука [n4] одержується також взаємодією ки, такі як хлороформ, дихлорметан і т.д.; і вуглесполуки [n3] у присутності води і тетраборату наводні, такі як толуол і т.д. 15 74687 16 В даній реакції теоретично необхідні кількості моль сполуки [n10] з розрахунку на один моль 2основи і кислоти, які дорівнюють відповідно від хлорацетаміду, але кількість може вільно змінювакаталітичної кількості до одного еквівалента і від тись відповідно до умов реакції. каталітичної кількості до надлишку, і один моль Після реакції саму реакційну суміш концентакролеїну з розрахунку на один моль сполуки [n4], рують; або після взаємодії одного молю 2але кількості можуть вільно змінюватись відповідхлорацетаміду реакційну суміш, у разі необхідносно до умов реакції. ті, фільтрують і фільтрат концентрують; реакційну суміш вливають у воду і осаджені кристали відфіСполука [n5] похідне піридону [а] льтровують; або реакційну суміш екстрагують орПохідне піридону [а] може бути одержано взаганічним розчинником, органічний шар сушать i ємодією сполуки [n5] у присутності кислоти. піддають звичайним операціям додаткової обробРеакцію звичайно здійснюють в розчиннику. ки, таким як концентрування і т.д., з одержанням Температура реакції знаходиться в діапазоні від цільової сполуки. Потім одержану сполуку можна 50 до 130°С, і час реакції звичайно знаходиться в очистити такими методами, як хроматографія, педіапазоні від миті до 48 годин. рекристалізація і т.д. Приклади кислоти включають оцтову кислоту, трифтороцтову кислоту, метансульфонову кислоСполука [n7] сполука [n8] ту, п-толуолсульфонову кислоту, трифторид бору і Сполука [n8] може бути одержана взаємодією його комплекс (наприклад, комплекс трифторид сполуки [n7] з хлоруючим реагентом. бору-метанол). Приклади розчинника включають Реакцію звичайно здійснюють в розчиннику. сполуки сірки, такі як диметилсульфоксид і т.д.; Температура реакції знаходиться в діапазоні від похідні простих ефірів, такі як диметоксіетан, тет10 до 30°С і час реакції звичайно знаходиться в рагідрофуран, 1,4-діоксан і т.д.; і вуглеводні, такі діапазоні від миті до 48 годин. як толуол і т.д. Приклади розчинника включають галогеновані У даній реакції кислота використовується в кісполуки, такі як хлороформ, дихлорметан і приклькості від каталітичної кількості до надлишку. лади хлоруючого реагенту включають сульфурилПісля реакції реакційну суміш, у разі необхідхлорид. ності, фільтрують і фільтрат концентрують; реакВ даній реакції теоретично необхідний один ційну суміш вливають у воду і осаджені кристали моль хлоруючого реагенту з розрахунку на один відфільтровують; або реакційну суміш екстрагують моль сполуки [n7], але кількість може вільно зміорганічним розчинником, органічний шар сушать і нюватись в залежності від умов реакції. піддають звичайним операціям додаткової обробПісля реакції саму реакційну суміш концентки, таким як концентрування і т.д. з одержанням рують; або після взаємодії одного молю хлоруючоцільової сполуки. Потім одержану сполуку можна го реагенту реакційну суміш, у разі необхідності, очистити такими методами, як хроматографія, пефільтрують і фільтрат концентрують; реакційну рекристалізація і т.д. суміш вливають у воду і осаджені кристали відфіКрім того, сполуку [n4] одержують також нальтровують; або реакційну суміш екстрагують орступним способом: ганічним розчинником, органічний шар сушать і піддають звичайним операціям додаткової обробки, таким як концентрування і т.д., з одержанням цільової сполуки. Потім одержану сполуку можна очистити такими методами, як хроматографія, перекристалізація і т.д. Сполука [n8] сполука [n9] Сполука [n9] може бути одержана взаємодією сполуки [n8] зі сполукою[m1] у присутності основи і необов'язково додатково йодидної солі. Реакцію звичайно здійснюють в розчиннику. Температура реакції знаходиться в діапазоні від 10 до 80°С, і час реакції звичайно знаходиться в діапазоні від миті до 48 годин. Приклади розчинника включають кетони, такі [де R3, R4 і R100 мають значення, вказані вище]. як ацетон, метилетилкетон, метилізобутилкетон і 2-Хлорацетамід сполука [n7] т.д.; сполуки сірки, такі як диметилсульфоксид і Сполука [n7] може бути одержана взаємодією т.д.; прості ефіри, такі як діетиловий ефір, метилтсполуки [n10] рет-бутиловий ефір, диметоксіетан, тетрагідрофуNaSR100 [n10] 100 ран, 1,4-діоксан і т.д.; і вуглеводні, такі як толуол. [де R має значення, вказані вище] з 2Приклади основи включають гідрид натрію, карбохлорацетамідом. нат калію, бікарбонат натрію, гідроксид натрію і Реакцію звичайно здійснюють в розчиннику. трет-бутоксид калію і приклади йодидної солі Температура реакції знаходиться в діапазоні від включають йодид натрію і йодид калію. кімнатної температури до 50°С, і час реакції звиВ даній реакції теоретично необхідний один чайно знаходиться в діапазоні від миті до 48 гомоль сполуки [m1] з розрахунку на один моль сподин. луки [n8] і теоретично необхідний один моль осноПриклади розчинника включають спирти, такі ви з розрахунку на один моль сполуки [m1], але як метанол, етанол, ізопропанол і т.д.; воду і їх кількості можуть вільно змінюватись в залежності суміші. від умов реакції. В даній реакції теоретично необхідний один 17 74687 18 Після реакції саму реакційну суміш концентхлорпербензойна кислота і т.д.; і пероксид водню. рують; або після взаємодії одного молю сполуки Приклади розчинника, що використовується для [n8] реакційну суміш, у разі необхідності, фільтруреакції, включають галогеновані сполуки, такі як ють і фільтрат концентрують; реакційну суміш хлороформ, дихлорметан і т.д. вливають у воду і осаджені кристали відфільтроВ даній реакції теоретично необхідні один і вують; або реакційну суміш екстрагують органічдва молі окислювача з розрахунку на один моль ним розчинником, органічний шар сушать і піддасполуки [n9], коли n=1 і n=2 відповідно, але кільють звичайним операціям додаткової обробки, кість може вільно змінюватись в залежності від таким як концентрування і т.д., з одержанням ціумов реакції. льової сполуки. Потім одержану сполуку можна Після реакції реакційну суміш, у разі необхідочистити такими методами, як хроматографія, пеності, фільтрують і фільтрат концентрують; реакрекристалізація і т.д. ційну суміш вливають у воду і осаджені кристали відфільтровують; або реакційну суміш екстрагують Сполука [n9] сполука [n4] органічним розчинником, органічний шар сушать і Сполука [n4] може бути одержана взаємодією піддають звичайним операціям додаткової обробсполуки [n9] з окислювачем. ки, таким як концентрування і т.д., з одержанням Реакцію звичайно здійснюють в розчиннику. цільової сполуки. Потім одержану сполуку можна Температура реакції знаходиться в діапазоні від очистити такими методами, як хроматографія, пе30 до 50°С, і час реакції звичайно знаходиться в рекристалізація і т.д. діапазоні від миті до 24 годин. Окислювач являє собою перкислоти, такі як м [R4 має значення, вказане вище, R31 являє собою атом галогену або ціаногрупу і L1 являє собою атом фтору або атом хлору] Сполука [р1] сполука [р3] Сполука [р3] може бути одержана взаємодією сполуки [р1] і сполуки [р2] з основою, такою як карбонат калію, звичайно в розчиннику. Сполука [р3] сполука [р4] Сполука [р4] може бути одержана взаємодією сполуки [р3] в атмосфері водню у присутності каталізатора, такого як паладій на вугіллі і т.д., звичайно в розчиннику або взаємодією з порошком заліза в змішаному розчиннику, що складається з оцтової кислоти і води. Сполука [р4] сполука [р5] Сполука [р5] може бути одержана взаємодією сполуки [р4] з діазотуючим реагентом, таким як нітрит натрію і т.д., і подальшою взаємодією з хлоридом міді, бромідом міді або ціанідом міді в розчиннику. Сполука [р5] сполука [а-1] Похідне піридону [а], де R3 являє собою атом галогену або ціаногрупу, а саме похідне піридону [а-1], може бути одержано взаємодією сполуки [р5] з трибромідом бору, звичайно в розчиннику. Сполука [р3] сполука [а-2] 19 74687 20 Похідне піридону [а], де R3 являє собою нітро2-хлор-3-бензилоксипіридину з метанолом у пригрупу, а саме похідне піридону [а-2], може бути сутності основи, звичайно в розчиннику. одержано взаємодією сполуки [р3] з трибромідом Сполука [р2] сполука [р6] бору, звичайно в розчиннику. Сполука [р6б] може бути одержана взаємодією Сполука [р2] може бути одержана наступним сполуки [р2] в атмосфері водню у присутності каспособом талізатора, такого як паладій на вугіллі і т.д., звичайно в розчиннику. Крім того, сполука [р2] може бути також одержана способом, описаним в патенті США №3701779, або його модифікацією. 2-Хлор-3-бензилоксипіридин може бути одержаний способом, описаним в: [Heterocycles 1994, 38(6), 1355-1360]. 2-Хлор-3-бензилоксипіридин сполука [р6] Сполука [р6] може бути одержана взаємодією [де R4, R31 і L1 мають значення, вказані вище] Сполука [q1] сполука [q2] Сполука [q2] може бути одержана взаємодією сполуки [q1] з 2-хлор-3-гідроксипіридином у присутності основи, такої як карбонат калію і т.д., звичайно в розчиннику. Сполука [q2] сполука [q3] Сполука [q3] може бути одержана взаємодією сполуки [q2] в атмосфері водню у присутності каталізатора, такого як паладій на вугіллі і т.д., зви чайно в розчиннику, або взаємодією з порошком заліза в змішаному розчиннику, що складається з оцтової кислоти і води. Сполука [q3] сполука [q4] Сполука [q4] може бути одержана взаємодією сполуки [q3] з діазотуючим реагентом, таким як нітрит натрію і т.д., і потім з хлоридом міді, бромідом міді або ціанідом міді в розчиннику. Сполука [q4] сполука [q5] Сполука [q5] може бути одержана взаємодією 21 74687 22 сполуки [q4] з метанолом у присутності основи, ну феніл С1-С4-алкіламіногрупу], яке легко одерзвичайно в розчиннику. жується з похідного піридину [d], являє собою сполуку, що володіє чудовою гербіцидною активністю, Сполука [q5] сполука [q6] також як і похідне піридину [d]. Похідне піридину Сполука [q6] може бути одержана взаємодією [е] може бути одержане: 1) реакцією похідного сполуки [q5] з азотною кислотою в сірчаній кислоті. піридину [d] зі сполукою [z] Сполука [q6] сполука [q7] H-R6 [z] Сполука [q7] може бути одержана взаємодією [де R6 має значення, вказане вище] або 2) гідсполуки [q6] в атмосфері водню у присутності каролізом похідного піридину [d], перетворенням в талізатора, такого як паладій на вугіллі і т.д., звийого галогенідкислотну сполуку з використанням чайно в розчиннику, або взаємодією з порошком галогенуючого реагенту і подальшою взаємодією заліза в змішаному розчиннику, що складається з продукту зі сполукою [z]. оцтової кислоти і води. З точки зору гербіцидної активності в похідноСполука [q7] сполука [q8] му піридину [d] і похідному піридину [e] для групи, Сполука [q8] може бути одержана взаємодією позначеної R3, переважним є атом галогену, особсполуки [q7] з фосгеном, звичайно в розчиннику. ливо атом хлору, і для групи, позначеної R4, переСполука [q8] сполука [q9] важним є атом галогену, особливо атом фтору. Сполука [q9] може бути одержана взаємодією Похідне піридину [d], похідне піридину [e] і посполуки [q8] з етил 4,4,4-трифтор-3хідне піридону [а] володіють чудовою гербіцидиою амінокротонатом у присутності основи, такої як активністю і деякі з них виявляють високу вибіркогідрид натрію і т.д., звичайно в розчиннику. вість відносно сільськогосподарських культур і Сполука [q9] сполука [q5] бур'янистих рослин. Похідне піридину [d], похідне Сполука [q5] може бути одержана взаємодією піридину [e] і похідне піридону [а] володіють гербісполуки [q9] з метилуючим реагентом, таким як цидною активністю проти різних перерахованих диметилсульфат, метилйодид і т.д., у присутності нижче бур'янистих рослин, які заподіюють шкоду основи, такої як гідрид натрію і т.д., звичайно в як при обприскуванні листя, так і при обробці ґрунрозчиннику. ту на нагірному полі. Сполука [р5] сполука [а-1] Бур'яни сімейства Onagraceae (енотери): Похідне піридону [а-1], яке являє собою похідOenothera erythrosepala і Oenothera laciniata; не піридону [а], де R являє собою атом галогену Бур'яни сімейства Ranunculaceae (жовтні): або ціаногрупу, може бути одержано взаємодією Ranunculus muricatus і Ranunculus sardous; сполуки [р5] з трибромідом бору, звичайно у приБур'яни сімейства Polygonaceae (гречка): сутності розчинника. Polygonum convolvulus (спориш в'юнкий), Похідне піридону [а] є, крім того, сполукою, що Polygonum lapathifolium (спориш перцевий), володіє гербіцидною активністю, і тому є застосоPolygonum pensylvanlcum (спориш пенсільвансьвним як активний інгредієнт гербіциду. кий), Polygonum persicaria (дзвоники), Rumex Похідне піридину [e]: crispus (щавель кучерявий), Rumex obtusifolius і Polygonum cuspidatum (спориш японський); Бур'яни сімейства Portulacaceae (портулак): Portulaca oleracea (портулак городній); Бур'яни сімейства Caryophyllaceae (гвоздики): Stellaria media (зірочник середній) і Cerastium glomeratum (роговик скупченоквітковий); Бур'яни сімейства Chenopodiaceae (лободи): Chenopodium album (лобода біла) і Kochia scoparia (кохія вінцева); [де R3 і R4 мають значення, вказані вище; R6 Бур'яни сімейства Amaranthaceae (щириці): являє собою С1-С6-галогеналкоксильну групу, С3Amaranthus retroflexus (щириця колосиста) і Сб-алкенілоксигрупу, С3-С6Amaranthus hybridus (щириця гібридна); галогеналкенілоксигрупу, С3-Сб-алкінілоксигрупу, Бур'яни сімейства Crusiferae (хрестоцвіті): С3-С6-галогеналкінілоксигрупу, С3-С6Raphanus raphanistrum (редька дика), Sinapis циклоалкоксильну групу, С3-С8arvensis (гірчиця польова), Capsella bursa-pastoris галогенциклоалкоксильну групу, C3-C8(грицики звичайні) і Lepidum virginicum; циклоалкенілоксигрупу, С3-С8Бур'яни сімейства Leguminosae (боби): циклоалкінілоксигрупу, C3-C8Sesbania exaltata (сесбанія екзалтата), Cassia галогенциклоалкенілоксигрупу, С1-С6obtusifolia (гусимець канадський), Desmodium алкоксикарбоніл, С1-С6-алкоксильну групу, С1-С6tortuosum (флоридська конюшина), Trifolium repens алкіліденамінооксигрупу, С1-С6(конюшина повзуча), Vicia sativa (горошок посівалкіламінооксигрупу, (С1-С6-алкіл)(С1-С3ний) і Medicago lupulina (люцерна хмелевидна); алкіл)амінооксигрупу, необов'язково заміщену феБур'яни сімейства Malvaceae (представники ноксигрупу, необов'язково заміщену феніл С1-С4сімейства мальвових): Abutilin theophrasti (лімноалкоксильну групу, аміногрупу, С1-С6харіс) і Sida spinosa (грудинка колюча); алкоксіаміногрупу, (С1-С6-алкокси)(С1-С3Бур'яни сімейства Violaceae (фіалки): Viola алкіл)аміногрупу, С1-С6-алкіламіногрупу, (С1-С6arvensis (фіалка польова) і Viola tricolor (фіалка алкіл)С1-С6-алкіламіногрупу, необов'язково замітриколірна); щену феніламіногрупу або необов'язково заміщеБур'яни сімейства Rubiaceae (підмаренники): 23 74687 24 Galium aparine (підмаренники чіпкі); ячмінь (Hordeum vulgare), рис (Oryza sativa), сорго Бур'яни сімейства Convolvulaceae (іпомеї): (Sorghum bicolor), сою культурну (Glycine max), Ipomoea hederacea (плющолиста іпомея), Ipomoea бавовник (Gossypium spp.), буряк цукровий (Beta purpurea (іпомея пурпурна), Ipomoea hederacea var vulgaris), земляний горіх (Arachis hypogaea), соняintegriuscula, Ipomoea lacunose і Convolvulus шник (Helianthus annuus), капусту і т.д.; і садових arvensis (берізка польова); рослин, що включають квіти, овочі і т.д. Крім того, Бур'яни сімейства Labiatae (м'яти): Lamium похідне піридину [d], похідне піридину [e] і похідне purpureum (глуха кропива пурпурова) і Lamium піридону [а] ефективно використовуються для боamplexicavle (глуха кропива стеблообгортна); ротьби з різними бур'янистими рослинами, які заБур'яни сімейства Solanaceae (пасльони): подіюють шкоду, при неорному вирощуванні сої Datura stramonium (дурман смердючий) і Solanum культурної, кукурудзи, пшениці і т.д. і деякі з похідnigram (паслін чорний); них піридину [d], похідних піридину [e] і похідних Бур'яни сімейства Scrophulariaceae (ранники піридону [а] не виявляють токсичність відносно шишкуваті): Veronica persica (вероніка персидсьсільськогосподарських культур. ка), Veronica arvensis і Veronica hederaefolia (вероПохідне піридину [d], похідне піридину [e] і поніка плющолиста); хідне піридону [а] володіють також гербіцидною Бур'яни сімейства Compositae (гібриди): активністю проти різних перерахованих нижче буXanthium pensylvanicum (нетреба звичайна), р'янистих рослин, які заподіюють шкоду, при оброHelianthus annuus (соняшник однорічний), бці затопленням рисового поля. Matricaria chamomilla, Matricaria perforate orinodora Бур'яни сімейства Gramineae (злакові трави): (ромашка), Chrysanthemum segetum (хризантема Echinochloa oryzicola (просо півняче), посівна), Matricaria matricarioides (ромашка ромашScrophulariaceae (ранник шишкуватий): Lindernia ковидна), Ambrosia artemisiifolia (амброзія звичайprocumbens (ліндернія лежача); Lythraceae (плана), Ambrosia trifida (амброзія тринадрізана), кун): Rotala indica (ротала гілляста) і Ammannia Erigeron canadensis, Artemisia princeps (полин multiflora; японський), Selidago altissima і Taraxacum Сімейство Elatinaceae (руслиці): Elatine triandra officinala; (руслиця); Бур'яни сімейства Boraginaceae (огірочники): Сімейство Cyperaceae (осоки): Cyperus Myosotis arvensis (незабудка польова); difformis (зонтиколиста осока), Scripus juncoides Бур'яни сімейства Acslepiadaceae (частухи): (очерет твердостебловий), Eleocharis acicularis Asclepias syriaca (ваточник сірійський): (голчатий ситняг), Cyperus serotinus і Eleocharis Бур'яни сімейства Euphorbiaceae (молочаї): kuroguwai (водяний каштан); Euphorbia helioscopia (молочай сонцегляд) і Сімейство Pontederiaceae (водяні гіацинти): Euphorbia maculate (молочай плямистий); Monochoria vaginalis; Бур'яни сімейства Geraniaceae (герані): Сімейство Alismataceae (частухи звичайні): Geranium carolinianum (герань каролінська); Sagittaria pygmaea (стрілолист), Sagittariatrifolia і Бур'яни сімейства Oxalidaceae (кислиці): Oxalis Alisma canaliculatum (частуха водяна); corymbosa (кислиця повзуча); Сімейство Potamogetonaceae (рдесники): Бур'яни сімейства Cucurbitaceae (гарбузи): Potamogeton distinctus (крупнолистий рдесник); і Sicyos angulatus; Сімейство Umbelliferae (зонтичні): Oenanthe Бур'яни сімейства Gramineae (злакові трави): javanica (селера водяна). Echinochloa crus-galli (куряче просо), Setaria viridis Деякі сполуки з похідних піридину [d], похідних (мишій зелений), Setaria faberi (багатомишій), піридину [e] і похідних піридону [а] також не виявDigitaris sanguinalis (куряча лапка кров'яна), ляють значну фітотоксичність відносно пересаEleusine indica (елеузина індійська), Poa annua дженої культури рису. (тонконіг однолітній), Alopecurus myosuroides (лиКрім того, з використанням похідного піридину сохвіст мишехвостовидний), Avena fatua (овес пус[d], похідного піридину [e] і похідного піридону [а] тий), Sorghum halepense (сорго алепське), можна боротись з бур'янами, які проростають або Agropyron repens (свинорий), Bromus tectorum будуть проростати на некультивованих землях, (стоколос покрівельний), Cynodone dactylon (бертаких як дамби (насипи), берегові укоси рік, доромудська трава), Panicum dichotomiflorum (просо жні узбіччя, залізничні шляхи, зелені смуги парків, вильчатоквіткове), Panicum texanum (просо техаземельні ділянки, місця стоянок; аеропорти, проське), Sorghum vulgare (сорго африканське зерномислові об'єкти, що включають заводи (фабрики), ве) і Alopecurus geniculatus (водяний лисохвіст); товарні склади і т.д., невикористані земельні надіБур'яни сімейства Commelinaceae (традесканли і невикористані землі в місті; і у фруктових сації віргінські): Commelina communis (комеліна звидах, на лугах (пасовищах), газонах і в лісах. Похідчайна); не піридину [d], похідне піридину [e] і похідне Бур'яни сімейства Equisetaceae (хвощі): піридону [а] володіють також гербіцидною активніEquisetum arvense (хвощ польовий); і бур'яни сістю проти водяних бур'янистих трав, таких як мейства Суреrсеае (осоки): Cyperus iria (смикаEichhornia crassipes (водяний гіацинт) і т.д., які вець віяловидний), Cyperus rotundus (смикавець виростають або будуть виростати в ріках, водних круглий), Cyperus esculentus (осока лускоплідна). шляхах, каналах, ставках і т.д. Крім того, деякі з похідних піридину [d] і похідПохідне піридину [d], похідне піридину [e] і поних піридину [а] не є токсичними для основних хідне піридону [а] мають такі ж властивості, як і сільськогосподарських культур, що включають гербицидні сполуки, описані в опублікованому мікукурудзу (Zea mays), пшеницю (Triticum aestivvm), жнародному патенті WO 95/34659. У випадку куль 25 74687 26 тур, що обробляються, де толерантність передакування листя або обробки затопленням до або ється культурам за рахунок введення гена толерапісля появи бур'янів. Обробка ґрунту може вклюнтності до гербіцидів, представленого в описі вкачати поверхневу обробку ґрунту і внесення в товзаного патенту, похідне піридину [d], похідне щу ґрунту. Крім того, обприскування листя може піридину [e] і похідне піридону [а] можуть бути вивключати нанесення на рослини і безпосереднє користані в більших кількостях, ніж ті кількості, які нанесення, коли воно здійснюється тільки на бувикористовуються при вирощуванні звичайних р'янисті рослини для того, щоб виключити попакультур без толерантності, що забезпечує можлидання на культурні рослини. вість більш ефективної боротьби з іншими несприКрім того, є ситуації, коли при введенні в суміш ятливими бур'янистими рослинами. інших гербіцидів підвищена гербіцидна активність Коли похідне піридину [d], похідне піридину [e] підтверджується. або похідне піридону [а] використовується як актиУ випадку, коли похідне піридину [d], похідне вний інгредієнт гербіциду, його звичайно змішують піридину [e] або похідне піридону [а] використовуз твердими або рідкими носіями, поверхневоється як активний інгредієнт гербіциду, доза внеактивними речовинами та іншими допоміжними сення може змінюватись в залежності від погодних домішками з одержанням при цьому емульгованих умов, виду препаратів, часу внесення, способів концентратів, змочувальних порошків, концентравнесення, стану ґрунту, цільових культур і цільотів, які утворюють суспензію, гранул, концентровавих бур'янистих рослин, але звичайно вона скланих емульсій, диспергованих у воді гранул і т.д. дає від 0,01г до 20000г, переважно від 1г до Вказані препарати можуть включати похідне 12000г на один гектар. Коли вносять емульговані піридину [d], похідне піридину [e] і похідне піридону концентрати, змочувальні порошки, концентрати, [а] як активний інгредієнт, взятий в кількості від які утворюють суспензію, концентровані емульсії, 0,001 до 80%, переважно від 0,005 до 70мас.%. дисперговані у воді гранули і т.д., їх вносять звиТвердий носій може включати, наприклад, мічайно при розбавленні водою, взятою в кількості неральні тонкоподрібнені порошки, такі як каоліновід 10 літрів до 1000 літрів (якщо необхідно, вода ва глина, атапульгіт, бентоніт, кисла глина, пірофіможе включати допоміжну домішку, таку як речоліт, тальк, діатомова земля, кальцит і т.д.; вина, що підвищує змочувальну здатність), для органічні тонкоподрібнені порошки, такі як порошок того, щоб вказану кількість можна було внести на горіхової шкаралупи і т.д.; водорозчинні тонкопокожний гектар. Гранули і деякі види поточних предрібнені порошки органічних сполук, таких як сепаратів звичайно вносять без розбавлення. Крім човина і т.д.; тонкоподрібнені порошки неорганічвищезгаданих поверхнево-активних речовин доних солей, таких як сульфат амонію і т.д. і поміжна домішка, яка може бути використана в тонкоподрібнені порошки синтетичного гідратоваданому винаході, у разі необхідності, може вклюного оксиду кремнію. Рідкий носій може включати, чати складні ефіри поліоксіетилену і жирних киснаприклад, ароматичні вуглеводні, такі як метиллот, солі лігнінсульфонової кислоти, солі абіетинафталін, фенілксилілетан, алкілбензол (напринової кислоти, солі динафтилметандісульфонової клад, ксилол) і т.д.; спирти, такі як ізопропанол, кислоти, концентрована олія сільськогосподарсьетиленгліколь, 2-етоксіетанол і т.д. складні ефіри, кої культури, олії, такі як соєва олія, кукурудзяна такі як діалкілфталат і т.д., кетони, такі як ацетон, олія, бавовняна олія, соняшникова олія і т.д. циклогексанон, ізофорон і т.д.; мінеральні масла, Далі даний винахід більш детально пояснений такі як машинне масло і т.д.; олії, такі як соєва прикладами і посилальними прикладами, але вкаолія, бавовняна олія і т.д.; диметилсульфоксид; зані приклади в жодній мірі не обмежують даний Ν,Ν-диметилформамід; ацетонітрил; Nвинахід. метилпіролідон; вода; і т.д. Приклад 1 Як поверхнево-активна речовина для емульгуДо суміші 0,5г 3-[2-хлор-4-фтор-5-(3-метил-2,6вання, диспергування або підвищення змочувальдіоксо-4-трифторметил-1,2,3,6ної здатності можуть бути використані аніоногенні тетрагідропіримідин-1-іл)фенокси]-1Н-піридин-2поверхнево-активні речовини, такі як алкілсульфаону тні солі, алкілсульфонатні солі, алкіларилсульфонатні солі, діалкілсульфосукцинатні солі, фосфатні солі простого поліоксіетиленалкіларилового ефіру і т.д.; і неіоногенні поверхнево-активні речовини, такі як прості поліоксіетиленалкілові ефіри, прості поліоксіетиленалкіларилові ефіри, блокспівполімери поліоксіетилену і поліоксипропілену, складні ефіри жирних кислот і сорбітану, складні ефіри поліоксіетиленсорбітану і жирних кислот і т.д. і 8мг димеру трифторацетату родію (II) і 15мл Як інші допоміжні домішки можуть бути вказані дихлоретану при 80°С протягом 3 годин додавали солі лігнінсульфонової кислоти, солі альгінової краплями 0,15г метилдіазоацетату. Після додакислоти, полівініловий спирт, аравійська камедь, вання краплями реакційну суміш додатково переКМІД (карбоксиметилцелюлоза), кислий ІПФ (кисмішували протягом однієї години при 80°С і потім лий ізопропілфосфат) і т.д. концентрували. Залишок піддавали хроматографії З похідного піридину [d], похідного піридину [e] на колонці з силікагелем (елюент:суміш гекабо похідного піридону [а] одержують препарат і сан/етилацетат = від 3/1 до 0/1) з одержанням потім використовують для обробки ґрунту, обприс0,18г витягнутого 3-[2-хлор-4-фтор-5-(3-метил-2,6 27 74687 28 діоксо-4-трифторметил-1,2,3,6Приклад 3 тетрагідропіримідин-1-іл)фенокси]-1Н-піридин-2Перша стадія ону і 0,34г 3-[2-хлор-4-фтор-5-(3-метил-2,6-діоксоУ суміш 1,01г гідрохлориду етилгліцинату, 4-трифторметил-1,2,3,6-тетрагідропіримідин-11,83г води і 5,15г 1,2-дихлоретану приблизно при іл)фенокси]-2-(метоксикарбонілметокси)піридину. 5°С додавали краплями розчин 0,60г нітриту натрію в 1,82г води. Після додавання краплями реакційну суміш додатково перемішували протягом 1,5 годин при такій же температурі, в неї додавали краплями 0,67г 5% сірчаної кислоти і потім знову перемішували протягом 10 хвилин. Потім відділений органічний шар промивали 5% водним розчином бікарбонату натрію і сушили над безводним сульфатом магнію з одержанням 1,2дихлоретанового розчину етилдіазоацетату. Друга стадія Т.пл. 52,2°С. 1 У суміш 1,8г 3-[2-хлор-4-фтор-5-(3-метил-2,6Н ЯМР (300МГц, CDCІ3, TMS (ч/млн)): 3,50 діоксо-4-трифторметил-1,2,3,6(3Н, кв, J=1,0Гц), 3,70 (3Н, с), 4,90 (1Н, д, тетрагідропіримідин-1-іл)фенокси]-1Н-піридин-2J=15,8Гц), 4,97 (1Н, д, J=15,8Гц), 6,29 (1Н, с), 6,90ону, 0,026г комплексу трифторид бору-діетиловий 6,95 (2Н, м), 7,32 (1Н, дд, J=1,9Гц, 7,7Гц), 7,37 (1Н, ефір і 6мл 1,2-дихлоретану при кімнатній темперад, 1=8,7Гц), 7,92 (1Н, дд, J=1,9Гц, 4,9Гц). турі протягом 30 хвилин додавали краплями 1,2Приклад 2 дихлоретановий розчин етилдіазоацетату, одерУ суміш 1,0г 3-[2-хлор-4-фтор-5-(3-метил-2,6жаний на першій стадії. Після додавання краплями діоксо-4-трифторметил-1,2,3,6реакційну суміш додатково перемішували протятетрагідропіримідин-1-іл)фенокси]-1Н-піридин-2гом 1,5 годин, в неї додавали краплями 2мл 15% ону, 42мкл комплексу трифторид бору-діетиловий сірчаної кислоти і потім знову перемішували проефір і 40мл 1,2-дихлоретану протягом 2 годин при тягом 30 хвилин. До реакційної суміші додавали 20 кімнатній температурі додавали краплями 0,4мл мілілітрів (20мл) водного насиченого розчину бікаетилдіазоацетату (міру чистоти: 90%). Після додарбонату натрію і відділений органічний шар сушивання краплями реакційну суміш додатково перели над безводним сульфатом магнію і концентрумішували протягом двох годин і потім піддавали вали. Залишок піддавали хроматографії на хроматографії на колонці з силікагелем (елюколонці з силікагелем (елюент:суміш гекент:суміш гексан/етилацетат = 2:1) з одержанням сан/етилацетат = 2/1) з одержанням 1,94г 3-[21,10г 3-[2-хлор-4-фтор-5-(3-метил-2,6-діоксо-4хлор-4-фтор-5-(3-метил-2,6-діоксо-4трифторметил-1,2,3,6-тетрагідропіримідин-1трифторметил-1,2,3,6-тетрагідропіримідин-1-іл)іл)фенокси]-2-(етоксикарбонілметокси)піридину. фенокси]-2-(етоксикарбонілметокси)піридину. Приклад 4 У суміш 1,0г 3-[2-хлор-4-фтор-5-(3-метил-2,6діоксо-4-трифторметил-1,2,3,6тетрагідропіримідин-1-іл)фенокси]-1Н-піридин-2ону, 121мг тетрахлориду олова і 40мл 1,2дихлоретану при кімнатній температурі протягом 2 годин додавали краплями 0,4мл етилдіазоацетату (міра чистоти 90%). Після додавання краплями реакційну суміш додатково перемішували протя1 Н ЯМР (300МГц, CDCІ3, TMS (ч/млн)): 1,25 гом 2 годин і піддавали хроматографії на колонці з (3Н, т, J=7,1Гц), 3,50 (3Н, кв, J=1,2Гц), 4,16 (2Н, кв, силікагелем (елюент:суміш гексан/етилацетат = J=7,2Гц), 4,88 (1Н, д, J=15,9Гц), 4,96 (1Н, д, 2/1) з одержанням 3-[2-хлор-4-фтор-5-(3-метилJ=15,9Гц), 6,29 (1Н, с), 6,9-7,0 (2Н, м), 7,3-7,4 (2Н, 2,6-діоксо-4-трифторметил-1,2,3,6м), 7,9-8,0 (1Н, м). тетрагідропіримідин-1-іл)фенокси]-2N-алкіловану сполуку 3-[2-хлор-4-фтор-5-(3(етоксикарбонілметокси)піридину. метил-2,6-діоксо-4-трифторметил-1,2,3,6Приклад 5 тетрагідропіримідин-1-іл)фенокси]-1У суміш 1,0г 3-[2-хлор-4-фтор-5-(3-метил-2,6(етоксикарбонілметокси)-1Н-піридин-2-он не виявдіоксо-4-трифторметил-1,2,3,6ляли. тетрагідропіримідин-1-іл)фенокси]-1Н-піридин-2Умови аналізу: ону, 70мг трифторметансульфонової кислоти і Високоефективна рідинна хроматографія 40мл 1,2-дихлоретану при кімнатній температурі Рідинний хроматограф LC-10AS (виробництво протягом 2 годин додавали краплями 0,4мл етилфірми Shimadzu Corp.) діазоацетату (міра чистоти 90%). Після додавання Детектор: детектор УФ-Vis SPD-10A (виробникраплями реакційну суміш додатково перемішувацтво фірми Shimadzu Corp.) ли протягом 2 годин і піддавали хроматографії на Аналітична довжина хвилі: 254нм колонці з силікагелем (елюент:суміш гекКолонка: SUMIPAX ODS А-212 (виробництво сан/етилацетат = 2/1) з одержанням 3-[2-хлор-4фірми Sumika Chemical Analysis Service) фтор-5-(3-метил-2,6-діоксо-4-трифторметилТемпература колонки: кімнатна температура 1,2,3,6-тетрагідропіримідин-1-іл)фенокси]-2Рухома фаза: ацетонітрил/вода = 1/1 (етоксикарбонілметокси)піридину. 29 74687 30 Далі описані посилальні приклади для одертетрагідропіримідин-1-іл)фенокси]-3жання вихідних сполук і т.д. метоксикарбоніл-3,4-дигідро-1Н-піридин-2-ону, Посилальний приклад 1 52мг хлориду літію, 2мл диметилсульфоксиду і Перша стадія 10мкл води перемішували при 120°С протягом До суміші 20,0г 2-хлор-4-фтор-5-(3-метил-2,6однієї години. Реакційну суміш охолоджували до діоксо-4-трифторметил-1,2,3,6кімнатної температури, потім в неї вливали воду і тетрагідропіримідин-1-іл)фенолу, 10,8г диметилхсуміш екстрагували етилацетатом. Органічний лормалонату і 120мл Ν,Ν-диметилформаміду дошар промивали насиченим сольовим розчином, давали 9,79г карбонату калію і перемішували при сушили над безводним сульфатом магнію і конце70°С протягом 1,5 годин. Після охолоджування нтрували. Залишок піддавали хроматографії на реакційної суміші до кімнатної температури її вликолонці з силікагелем з одержанням 70мг 3-[2вали в суміш хлористоводневої кислоти і льоду і хлор-4-фтор-5-(3-метил-2,6-діоксо-4екстрагували етилацетатом. Органічний шар пострифторметил-1,2,3,6-тетрагідропіримідин-1лідовно промивали 10% водним розчином карбоіл)фенокси]-3,4-дигідро-1Н-піридин-2-ону. нату калію і насиченим сольовим розчином, сушиТ.пл. 91,0°С. 1 ли над безводним сульфатом магнію і Н ЯМР (300МГц, CDCІ3, TMS (ч/млн)): 2,7концентрували. Залишок промивали метанолом і 2,8 (м, 2Н), 3,53 (с, 3Н), 4,6-4,8 (м, 1Н), 5,0-5,2 (м, діізопропіловим ефіром з одержанням 21,6г диме1Н), 6,0-6,1 (м, 1Н), 6,33 (с, 1Н), 7,1-7,2 (м, 1Н), тил [2-хлор-4-фтор-5-(3-метил-2,6-діоксо-47,28 (д, 1Н, J=9,0Гц), 7,7-8,1(м,1Н). трифторметил-1,2,3,6-тетрагідропіримідин-1П'ята стадія іл)фенокси]малонату. Суміш 144мг 3-[2-хлор-4-фтор-5-(3-метил-2,6Т.пл. 141,1°С. діоксо-4-трифторметил-1,2,3,61 Н ЯМР (300МГц, CDCІ3, TMS (ч/млн)): 3,55 тетрагідропіримідин-1-іл)фенокси]-3,4-дигідро-1Н(д, 3Н, J=1,1Гц), 3,86 (с, 6Н), 5,15 (с, 1Н), 6,35 (с, піридин-2-ону, 0,66мл тетрагідрофурану і 163мг о1Н), 6,99 (д, 1Н, J=6,5Гц), 7,3-7,4 (м, 1Н). хлоранілу кип'ятили зі зворотним холодильником Друга стадія протягом однієї години при перемішуванні. РеакУ суміш 21,6г диметил [2-хлор-4-фтор-5-(3ційну суміш охолоджували до кімнатної темпераметил-2,6-діоксо-4-трифторметил-1,2,3,6тури, потім в неї вливали воду і суміш екстрагуватетрагідропіримідин-1-іл)фенокси]малонату, 80мл ли етилацетатом. Органічний шар сушили над хлороформу і 80мл метанолу при 0°С додавали безводним сульфатом магнію і концентрували. краплями 26,3мл 7н розчину аміак/метанол. Після Залишок піддавали хроматографії на колонці з додавання краплями реакційну суміш перемішувасилікагелем з одержанням 72мг 3-[2-хлор-4-фторли протягом 20 хвилин і потім при кімнатній тем5-(3-метил-2,6-діоксо-4-трифторметил-1,2,3,6пературі протягом 7 годин. Реакційну суміш фільттетрагідропіримідин-1-іл)фенокси]-1Н-піридин-2рували і концентрували з одержанням 6,91г метил ону. 1 2-[2-хлор-4-фтор-5-(3-метил-2,6-діоксо-4Н ЯМР (300МГц, CDCІ3, TMS (ч/млн)): 3,52 трифторметил-1,2,3,6-тетрагідропіримідин-1(с, 3Н), 6,22 (дд, 1Н, J=7,0, 7,0Гц), 6,32 (с, 1Н), 6,95 іл)фенокси]-2-карбоксамідацетату. (д, 1Н, J=6,6Гц), 7,00 (дд, 1Н, J=7,0, 1,6Гц), 7,2-7,3, Т.пл. 196,4°С (розкл.) (м, 1Н), 7,39 (д, 1Н, J=8,9Гц). 1 Н ЯМР (250МГц, CDCІ3, TMS (ч/млн)): 3,56 Посилальний приклад 2 (с, 3Н), 3,84 (с, 3Н), 5,06 (с, 1Н), 5,76 (в.с, 1Н), 6,36 Перша стадія (с, 1Н), 6,8-7,0 (м, 2Н), 7,37 (д, 1Н, J=8,7Гц). До суміші 1,3г гідриду натрію і 100мл диметокТретя стадія сіетану при кімнатній температурі додавали 10г 2До суміші 363мг метил 2-[2-хлор-4-фтор-5-(3хлор-4-фтор-5-(3-метил-2,6-діоксо-4метил-2,6-діоксо-4-трифторметил-1,2,3,6трифторметил-1,2,3,6-тетрагідропіримідин-1тетрагідропіримідин-1-іл)фенокси]-2іл)фенолу і перемішували протягом 30 хвилин. карбоксіамідацетату, 6,0мл тетрагідрофурану і Потім в неї додавали 2,2г йодиду натрію і 6,7г не50мг акролеїну при 0°С додавали 9мг треточищеного 2-хлор-2-(метилтіо)ацетаміду, перемібутоксиду калію і перемішували протягом 30 хвишували при кімнатній температурі протягом 3 голин. Потім після додавання до реакційної суміші дин і в реакційну суміш вливали воду. Реакційну 17мг моногідрату п-толуолсульфонової кислоти суміш екстрагували етилацетатом. Органічний суміш кип'ятили зі зворотним холодильником прошар промивали водним розчином бікарбонату натягом однієї години при перемішуванні. трію, сушили над безводним сульфатом магнію і Реакційну суміш охолоджували до кімнатної концентрували. Залишок піддавали хроматографії температури, потім в неї вливали воду і суміш ексна колонці з силікагелем (елюент:етилацетат) з трагували етилацетатом. Органічний шар сушили одержанням 10,2г 2-[2-хлор-4-фтор-5-(3-метил-2,6над безводним сульфатом магнію і концентрували. діоксо-4-трифторметил-1,2,3,6Залишок піддавали хроматографії на колонці з тетрагідропіримідин-1-іл)фенокси]-2силікагелем з одержанням 202мг 3-[2-хлор-4-фтор(метилтіо)ацетаміду. 1 5-(3-метил-2,6-діоксо-4-трифторметил-1,2,3,6Н ЯМР (300МГц, CDCІ3, TMS (ч/млн)): 2,18 тетрагідропіримідин-1-іл)фенокси]-3(3Н, с), 3,56 (3Н, кв, J=1,3Гц), 5,54 (1Н, д, 3=3,4Гц), метоксикарбоніл]-3,4-дигідро-Ш-піридин-2-ону. 5,94 (1Н, шир), 6,37 (1Н, д, 3=2,9Гц), 6,80 (1Н, Т.пл. 82,4°С. шир.), 7,06-7,11 (1Н, м), 7,36 (1Н, д, J=9,0Гц). Четверта стадія Друга стадія Суміш 202мг 3-[2-хлор-4-фтор-5-(3-метил-2,6До суміші 2-[2-хлор-4-фтор-5-(3-метил-2,6діоксо-4-трифторметил-1,2,3,6діоксо-4-трифторметил-1,2,3,6 31 74687 32 тетрагідропіримідин-1-іл)фенокси]-2Т.пл. 79,5°С. 1 (метилтіо)ацетаміду і 50мл хлороформу при кімнаН ЯМР (300МГц, CDCІ3, TMS (ч/млн)): 3,86 тній температурі протягом 3 днів додавали 3,7г м(с, 3Н), 4,79 (с, 1Н), 5,8-6,0 (шир.с, 1Н), 6,5-6,7 хлорпербензойної кислоти. До реакційної суміші (шир.с, 1Н). додавали водний розчин бікарбонату натрію і водДруга стадія ний розчин тіосульфату натрію. Реакційну суміш До суміші 0,50г 2-хлор-4-фтор-5-(3-метил-2,6екстрагували етилацетатом. Органічний шар продіоксо-4-трифтормєтил-1,2,3,6мивали насиченим сольовим розчином, сушили тетрагідропіримідии-1-іл)фенолу, 0,22г метил-2над безводним сульфатом магнію і концентрували. хлор-2-карбоксамідацетату і 0,75мл Ν,ΝЗалишок піддавали хроматографії на колонці з диметилформаміду додавали 0,24г карбонату касилікагелем (елюент:етилацетат) з одержанням лію і перемішували при 50-60°С протягом 0,5 го3,3г 2-[2-хлор-4-фтор-5-(3-метил-2,6-діоксо-4дини. До суміші додавали 0,75мл Ν,Νтрифторметил-1,2,3,6-тетрагідропіримідин-1диметилформаміду і потім перемішували при 50іл)фенокси]-2-(метилсульфоніл)ацетаміду. 60°С протягом 2 годин. Реакційну суміш охоло1 Н ЯМР (300МГц, CDCІ3, TMS (ч/млн)): 3,11 джували до кімнатної температури і вливали на (3Н, с), 3,46 (1,5Н, с), 3,49 (1,5 Н, с), 5,44 (1Н, с), лід. Осаджені кристали відфільтровували і послі6,26 (0,5 Н, с), 6,30 (0,5 Н, с), 6,55 (1Н, шир.), 7,03 довно промивали водою і гексаном з одержанням (1Н, шир.), J, 27-7,34 (2Н, м). 0,42г метил 2-[2-хлор-4-фтор-5-(3 -метил-2,6Третя стадія діоксо-4-трифторметил-1,2,3,6До суміші 1,3г 2-[2-хлор-4-фтор-5-(3-метил-2,6тетрагідропіримідин-1-іл)фенокси]-2діоксо-4-трифторметил-1,2,3,6(карбоксамід)ацетату. тетрагідропіримідин-1-іл)фенокси]-2Посилальний приклад 4 (метилсульфоніл)ацетаміду, 0,21г акролеїну і 20мл Перша стадія ТГФ при кімнатній температурі додавали 0,03г До суміші 10г 3-(2,5-дифтор-4-нітрофеніл)-1трет-бутоксиду калію і перемішували протягом 3,5 метил-6-трифторметил-1Н-піримідин-2,4-діону, годин. Потім додавали 0,1г п-толуолсульфонової 5,0г 3-гідрокси-2-метоксипіридину і 100мл Ν,Νкислоти і реакційну суміш кип'ятили зі зворотним диметилформаміду додавали 7,8г карбонату калію холодильником протягом 4 годин при перемішуі кип'ятили зі зворотним холодильником протягом ванні. Реакційну рідину концентрували при зниже6 годин при перемішуванні. Потім реакційну суміш ному тиску і залишок піддавали хроматографії на вливали у воду і екстрагували етилацетатом. Орколонці з силікагелем (елюент:суміш гекганічний шар послідовно промивали водним розсан/етилацетат = 1/1) з одержанням 0,55г 3-[2чином бікарбонату натрію і насиченим сольовим хлор-4-фтор-5-(3-метил-2,6-діоксо-4розчином, сушили над сульфатом магнію і концентрифторметил-1,2,3,6-тетрагідропіримідин-1трували з одержанням 12,8г 3-[4-фтор-5-(3-метиліл)фенокси]-3-(метилсульфоніл)-3,4-дигідро-1Н2,6-діоксо-4-трифторметил-2-нітро-1,2,3,6піридин-2-ону. тетрагідропіримідин-1-іл)фенокси]-21 метоксипіримідину. Н ЯМР (300МГц, CDCІ3, TMS (ч/млн)): 2,751 2,88 (1Н, м), 3,19-3,31 (1H, м), 3,30 (1H, с), 3,54 Н ЯМР (300МГц, CDC13, TMS (ч/млн)): 3,52 (3Н, с), 4,97-5,05 (1Н, м), 6,00-6,05 (1Н, м), 7,27(3Н, кв, J=1,2Гц), 3,93 (3Н, с), 6,32 (1Н, с), 6,76 (1Н, 7,36 (2Н, м), 8,04 (1Н, д, J=4,1Гц). д, J=5,8Гц), 6,93 (1Н, дд, J=5,0Гц, 7,8Гц), 7,40 (1Н, Четверта стадія дд, J=1,4Гц, 7,8Гц), 7,90 (1Н, д, J=8,6Гц), 8,04 (1Н, Суміш одного еквівалента 3-[2-хлор-4-фтор-5дд, J=1,4Гц, 5,0Гц). (3-метил-2,6-діоксо-4-трифторметил-1,2,3,6Друга стадія тетрагідропіримідин-1-іл)фенокси]-3У суміш 6,3г порошку заліза, 50мл оцтової ки(метилсульфоніл)-3,4-дигідро-1Н-піридин-2-ону, слоти і 50мл води при 80°С додавали краплями 0,1 еквівалента п-толуолсульфонової кислоти і 60мл етилацетатного розчину 3-[4-фтор-5-(3толуолу кип'ятили зі зворотним холодильником метил-2,6-діоксо-4-трифторметил-2-нітро-1,2,3,6при перемішуванні. Після реакції реакційну рідину тетрагідропіримідин-1-іл)фeнокси]-2концентрували і залишок піддавали хроматографії метоксипіримідину. Після додавання краплями на колонці з силікагелем з одержанням 3-[2-хлорреакційну суміш перемішували протягом 15 хвилин 4-фтор-5-(3-метил-2,6-діоксо-4-трифторметилпри цій же температурі і охолоджували до кімнат1,2,3,6-тетрагідропіримідин-1-іл)фенокси]-1Нної температури. Реакційну суміш вливали у воду і піридин-2-ону. екстрагували етилацетатом. Органічний шар посПосилальний приклад 3 лідовно промивали водою, водним розчином бікаПерша стадія рбонату натрію і насиченим сольовим розчином і До 8,33г диметилхлормалонату при 0°С додаконцентрували з одержанням 12,1г 3-[2-аміновали краплями 7н розчин аміак/метанол і потім 4~фтор-5-(3-метил-2,6-діоксо-4-трифторметилперемішували протягом 10 хвилин. Після цього 1,2,3,6-тетрагідропіримідин-1-іл)фенокси]-2реакційну суміш перемішували при кімнатній темметоксипіридину. 1 пературі протягом 2 годин, фільтрували і концентН ЯМР (300МГц, CDCІ3, TMS (ч/млн): 3,51 рували. Залишок розчиняли в змішаному розчин(3Н, кв, J=1,0Гц), 4,00 (3Н, с), 4,20 (1Н, шир.), 6,30 нику, що складається з хлороформу і метанолу. (1Н, с), 6,62 (1Н, д, J=10,6Гц), 6,63 (1Н, д, J=7,1Гц), Розчин фільтрували і потім концентрували. Зали6,82 (1H, дд, J=5,0Гц, 7,8Гц), 7,18 (1Н, дд, J=1,4Гц, шок піддавали хроматографії на колонці з силіка7,8Гц), 7,90 (1Н, дд, J=1,4Гц, 5,0Гц). гелем з одержанням 4,4г метил 2-хлор-2Третя стадія карбоксамідацетату. У суміш 12г 3-[2-аміно-4-фтор-5-(3-метил-2,6 33 74687 діоксо-4-трифторметил-1,2,3,6тетрагідропіримідин-1-іл)фенокси]-2метоксипіридину, 2,8г хлориду міді (І), 5,7г хлориду міді (II) і 100мл ацетонітрилу додавали краплями 4,6г ізоамілнітриту. Після додавання краплями реакційну суміш перемішували протягом 2 годин і залишали на 2 дні. Потім в неї додавали водний розчин аміаку і суміш екстрагували етилацетатом. Органічний шар послідовно промивали водою і насиченим сольовим розчином, сушили над безводним сульфатом магнію і концентрували. Залишок піддавали хроматографії на колонці з силікагелем (елюент:cуміш гексан/етилацетат = 2/1) з одержанням 8,6г 3-[2-хлор-4-фтор-5-(3-метил-2,6діоксо-4-трифторметил-1,2,3,6тетрагідропіримідин-1-іл)фенокси]-2метоксипіридину. Т.пл. 179,5°С. Четверта стадія До суміші 0,5г 3-[2-хлор-4-фтор-5-(3-метил-2,6діоксо-4-трифторметил-1,2,3,6тетрагідропіримідин-1-іл)фенокси]-2метоксипіридину і 10мл хлороформу додавали 0,5г триброміду бору і перемішували при кімнатній температурі протягом 3 годин. Потім реакційну суміш концентрували. Залишок вливали у воду і екстрагували етилацетатом. Органічний шар сушили над безводним сульфатом магнію і концентрували. Залишок піддавали хроматографії на колонці з силікагелем (елюент: етил ацетат) з одержанням 0,31г 3-[2-хлор-4-фтор-5-(3-мeтил-2,6діоксо-4-трифторметил-1,2,3,6тетрагідропіримідин-1-іл)фенокси]-1Н-піридин-2ону. Т.пл. 180,8°С. Нижче перераховані деякі з похідних піридину [d] і похідних піридину [e] з номерами їх сполук. Дані сполуки мають наступну формулу: Таблиця 1 Сполука № 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 R3 СІ СІ СІ СІ СІ СІ СІ СІ СІ СІ СІ СІ СІ СІ СІ R7 ОН ОМе OEt Оі·Рr ОСН2СН=СН2 ОСН2СН2СН3 ОСН2СН2СН2СН3 ОСН2СН2СН2СН2СН3 ОС(СН3)3 ОСН2СбН5 ОСбН5 NHOCH3 NHOCH2CH3 N(CH3)OCH3 ON=C(CH3)2 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 СІ СІ СІ СІ Вr Вr Вr Вr Вr Вr Br Br Br Br Br Br Br Br Br Br Br Br Br CN CN CN CN CN CN CN CN CN CN CN CN CN CN CN CN CN CN CN NO2 NO2 NO2 NO2 NO2 NO2 NO2 NO2 NO2 NO2 NO2 NO2 NO2 NO2 NO2 NO2 NO2 NO2 34 ОСН2СО2СН3 ОСН(СН3)СО2СН2СН3 ОС(СН3)2СО2СН3 Ос·С5Н9 ОН ОМе OEt Оі·Рr ОСН2СН=СН2 ОСН2СН2СН3 OCH2CH2CH2CH3 OCH2CH2CH2CH2CH3 ОС(СН3)3 OCH2C6H5 OC6H5 NHOCH3 NHOCH2CH3 N(CH3)OCH3 ON=C(CH3)2 OCH2CO2CH3 OCH(CH3)CO2CH2CH3 OC(CH3)2CO2CH3 Oc·C5H9 OH OMe OEt Oi·Pr OCH2CH=CH2 OCH2CH2CH3 OCH2CH2CH2CH3 OCH2CH2CH2CH2CH3 ОС(СН3)3 ОСН2СбН5 ОС6Н5 NHOCH3 NHOCH2CH3 N(CH3)OCH3 ON=C(CH3)2 OCH2CO2CH3 OCH(CH3)CO2CH2CH3 OC(CH3)2CO2CH3 Oc·C5H9 OH OMe OEt Oi·Pr OCH2CH=CH2 OCH2CH2CH3 OCH2CH2CH2CH3 OCH2CH2CH2CH2CH3 ОС(СН3)3 OCH2C6H5 OC6H5 NHOCH3 NHOCH2CH3 N(CH3)OCH3 ON=C(CH3)2 OCH2CO2CH3 OCH(CH3)CO2CH2CH3 OC(CH3)2CO2CH3 Потім нижче перераховані деякі з похідних пі 35 ридону [а] з номерами їх сполук. Дані сполуки мають наступну формулу: 74687 36 сягнення середнього розміру частинок 5мкм або менше з одержанням суспендованого концентрату кожної сполуки. Посилальний приклад 5 препарату П'ять частин кожної зі сполук 1-84 додавали до 40 частин 10% водного розчину полівінілового спирту і суміш емульгували диспергуванням з використанням гомогенізатора до досягнення середнього розміру частинок 10мкм або менше, потім додавали 55 частин води, при цьому одержували концентровану емульсію кожної сполуки. Далі показано, що похідне піридину [d] і похідТаблиця 2 не піридону [а] застосовні як гербицидні активні інгредієнти. Сполука № R3 R4 Посилальний приклад 1 випробувань 76 СІ F Циліндричні пластикові горщечки, кожний з 77 СІ Η яких має діаметр 10см і глибину 10см, наповнюва78 Вr F ли ґрунтом і потім засівали плющолистою іпомеєю 79 CN F і лімнохарісом. Піддослідні рослини вирощували в 80 CN Η теплиці протягом 10 днів. Потім з кожної зі сполук 81 NO2 F 1, 2, 3, 6, 8, 12, 15, 16, 19, 21, 40, 59 і 76 одержу82 NO2 Η вали емульгований концентрат відповідно до по83 СІ СІ силального прикладу 2 препарату і розбавляли 84 CN СІ водою, що містить речовину, яка підвищує змочувальну здатність. Одержаний розбавлений препаДалі йдуть приклади препаратів, де як гербірат однорідно розбризкували на листя піддослідцидні активні інгредієнти використовуються похідних рослин з використанням обприскувача при не піридину [d] і похідне піридону [а], в даних принормі витрати 1000 літрів на гектар. Після розбрикладах частина(и) являє(ють) собою частину(и) за зкування піддослідні рослини вирощували в тепмасою. лиці протягом 12 днів і визначали гербіцидну актиПосилальний приклад 1 препарату вність. В результаті було знайдено, що кожна зі П'ятдесят частин кожної зі сполук 1-84, 3 чассполук 1, 2, 3, 6, 8, 12, 15, 16, 19, 21, 40, 59 і 76 тини лігнінсульфонату кальцію, 2 частини лаурилповністю придушувала зростання плющолистої сульфату натрію і 45 частин синтетичного гідратоіпомеї і лімнохарісу при нормі витрати 125г/га. ваного оксиду кремнію ретельно подрібнювали і Посилальний приклад 2 випробувань змішували з одержанням змочуваного порошку Циліндричні пластикові горщечки, кожний з кожної сполуки. яких має діаметр 10см і глибину 10см, наповнюваПосилальний приклад 2 препарату ли ґрунтом і потім засівали плющолистою іпомеєю Десять частин кожної зі сполук 1-84, 14 частин і лімнохарісом. З кожної зі сполук 1, 2, 3, 6, 8, 12, простого поліоксіетиленстирилфенілового ефіру, 6 15, 16, 19, 21, 40, 59 і 76 одержували емульговачастин додецилбензолсульфонату кальцію, 35 ний концентрат відповідно до посилального прикчастин ксилолу і 35 частин циклогексанону ретеладу 2 препарату і розбавляли водою. Одержаний льно змішували з одержанням емульгованого конрозбавлений препарат однорідно розбризкували центрату кожної сполуки. на поверхню ґрунту з використанням обприскувача Посилальний приклад 3 препарату при нормі витрати 1000 літрів на гектар. Після роДві частини кожної зі сполук 1-84, 2 частини збризкування піддослідні рослини вирощували в синтетичного гідратованого оксиду кремнію, 2 частеплиці протягом 19 днів і визначали гербіцидну тини лігнінсульфонату кальцію, 30 частин бентоніактивність. В результаті було знайдено, що кожна ту і 64 частини каолінової глини ретельно подрібзі сполук 1, 2, 3, 6, 8, 12, 15, 16, 19, 21, 40, 59 і 76 нювали і змішували і суміш ретельно повністю придушувала зростання плющолистої перемішували з водою, потім гранулювали і сушиіпомеї і лімнохарісу при нормі витрати 500г/га. ли з одержанням гранул кожної сполуки. Промислова застосовність Посилальний приклад 4 препарату Згідно зі способом даного винаходу може бути Двадцять п'ять частин кожної зі сполук 1-84, 50 вигідно одержане нове похідне піридину [d], що частин 10% водного розчину полівінілового спирту володіє чудовою гербіцидною активністю. і 25 частин води змішували і подрібнювали до до Комп’ютерна верстка О. Гапоненко Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюA process for producing a pyridine derivative
Назва патенту російськоюСпособ получения производного пиридина
МПК / Мітки
МПК: C07D 401/12
Мітки: похідного, одержання, піридину, спосіб
Код посилання
<a href="https://ua.patents.su/18-74687-sposib-oderzhannya-pokhidnogo-piridinu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання похідного піридину</a>
Попередній патент: Фазовий гідролокатор бокового огляду
Наступний патент: Спосіб одержання композиційного матеріалу на основі спученого графіту і двооксиду титану
Випадковий патент: Вертикально-осьове вітроколесо