Три(цикло)заміщені аміди, фармацевтична композиція, способи лікування та профілактики, спосіб одержання сполуки
Формула / Реферат
1. Сполука формули (І):
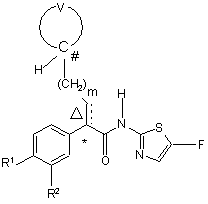 , (I)
, (I)
або її фармацевтично прийнятна сіль, де:
V - (СН2)k, де одна група СН2 може, як варіант, бути заміненою групами СН(ОН), C=O, C=NOH, C=NOCH3, СНХ, СХХ1, СН(ОСН3), СН(ОСОСН3), СН(С1-4алкіл) або С(ОН)(С1-4алкіл);
X та X1 незалежно один від одного вибрані з-посеред атомів флуору та хлору;
кожний з R1 та R2 незалежно один від одного вибрані з групи яку складають водень, галоген, гідроксил, аміно-, ціано-, нітрогрупа, SR3, SOR3, SO2R3, SO2NR4R5, NHSO2R3, С1-4алкіл, С2-4алкеніл, С2-4алкініл, С1-4алкоксигрупа та гетероарильна група, де будь-яка група факультативно заміщена 1-5 замісниками, незалежно один від одного вибраними з групи, яку складають галоген, ціано-, нітрогрупа, гідроксил, С1-2алкоксигрупа, -N(С0-2алкіл)(С0-2алкіл), С1-2алкіл, CFnH3-n, арил, гетероарил, -CON(C0-2алкіл)(C0-2алкіл), SCH3, SOCH3, SO2CH3 тa -SО2N(С0-2алкіл)(С0-2алкіл);
R3 - С1-4алкільна група, С3-7циклоалкільна група, арильна група, гетероарильна група або 4-7-членна гетероциклічна група, де будь-яка група, факультативно заміщена 1-5 замісниками, незалежно один від одного вибраними з групи, яку складають галоген, ціано-, нітрогрупа, гідроксил, С1-2алкоксигрупа, -N(C0-2алкіл)(C0-2алкіл), C1-2алкіл, C3-7циклоалкіл, 4-7-членна гетероциклічна група, CFnH3-n, арил, гетероарил, СОС1-2алкіл, -CON(C0-2алкіл)(C0-2алкіл), SOCH3, SO2CH3 та -SO2N(C0-2алкіл)(С0-2алкіл);
кожний з R4 та R5 незалежно один від одного є водень або С1-4алкільна група, C3-7циклоалкільна група, арильна група, гетероарильна група або 4-7-членна гетероциклічна група, де будь-яка група факультативно заміщена 1-5 замісниками, незалежно один від одного вибраними з групи, яку складають галоген, ціано-, нітрогрупа, гідроксил, С1-2алкоксигрупа, -N(C0-2алкіл)(C0-2алкіл), С1-2алкіл, C3-7циклоалкіл, 4-7-членна гетероциклічна група, CFnH3-n, арил, гетероарил, -СОN(C0-2алкіл)(C0-2алкіл), SOCH3, SO2CH3 та -SO2N(C0-2алкіл)(C0-2алкіл);
або R4 та R5 спільно утворюють 4-8-членну гетероциклічну групу, факультативно заміщену 1 або 2 замісниками, незалежно один від одного вибраними з групи яку складають С1-2алкіл та гідроксил;
k - ціле число від 2 до 7;
m = 0 або 1;
n = 1, 2 або 3; а
пунктирна лінія спільно із суцільною лінією означають факультативний подвійний зв’язок; та
![]() означає, що подвійний зв'язок має (Е)-конфігурацію.
означає, що подвійний зв'язок має (Е)-конфігурацію.
2. Сполука за п. 1, або фармацевтично прийнятна сіль цієї сполуки, де пунктирна лінія спільно із суцільною лінією означає подвійний зв'язок.
3. Сполука за п. 1, або фармацевтично прийнятна сіль цієї сполуки, де пунктирна лінія спільно із суцільною лінією означає одинарний зв'язок.
4. Сполука за п. 3, або фармацевтично прийнятна сіль цієї сполуки, де пунктирна лінія спільно із суцільною лінією означає одинарний зв'язок, та абсолютна конфігурація при асиметричному центрі в ![]() -положенні до атома вуглецю амідокарбонільної групи є (R).
-положенні до атома вуглецю амідокарбонільної групи є (R).
5. Сполука за будь-яким з попередніх пунктів, або фармацевтично прийнятна сіль, де m - 0.
6. Сполука за будь-яким з попередніх пунктів, або фармацевтично прийнятна сіль цієї сполуки, де k - 4 або 5.
7. Сполука за п. 6, або фармацевтично прийнятна сіль цієї сполуки, де група, утворена -НС< та >V представляє 3-оксоциклопентил, 4-оксоциклогексил або 3-гідроксициклопентил.
8. Сполука за будь-яким з попередніх пунктів, або фармацевтично прийнятна сіль цієї сполуки, де R1 та R2 не є одночасно атомами водню.
9. Сполука за будь-яким з попередніх пунктів, або фармацевтично прийнятна сіль цієї сполуки, де R1 - SOR3, SO2R3 або SO2NR4R5.
10. Сполука за будь-яким з попередніх пунктів, або фармацевтично прийнятна сіль цієї сполуки, де R3 - С1-4алкіл або C3-7циклоалкіл.
11. Сполука за будь-яким з попередніх пунктів, або фармацевтично прийнятна сіль цієї сполуки, де R1 - SО2C3-4циклоалкіл.
12. Сполука за будь-яким з попередніх пунктів, або фармацевтично прийнятна сіль цієї сполуки, де R2 - водень, хлор, фтор або трифторметил.
13. Сполука, вибрана з групи яку складають:
2(R)-2-(3-хлор-4-метансульфонілфеніл)-N-(5-фтортіазол-2-іл)-3-((R)-3-оксоциклопентил)пропіонамід;
2(R)-2-(3-хлор-4-метансульфонілфеніл)-N-(5-фтортіазол-2-іл)-3-(4-оксоциклогексил)пропіонамід;
2(R)-2-(3-хлор-4-метансульфонілфеніл)-N-(5-фтортіазол-2-іл)-3-(3-гідроксициклопентил)пропіонамід;
(Е)-N-(5-флуортіазол-2-іл)-2-(4-метансульфонілфеніл)-3-((S)-3-оксоциклопентил)акриламід;
(Е)-N-(5-флуортіазол-2-іл)-2-(4-метансульфонілфеніл)-3-(4-оксоциклогексил)акриламід;
(Е)-N-(5-флуортіазол-2-іл)-3-(3-гідроксициклопентил)-2-{4-метансульфонілфеніл)акриламід;
2(R)-2-(4-циклопропансульфонілфеніл)-N-(5-фтортіазол-2-іл)-3-((R)-3-оксоциклопентил)пропіонамід;
2(R)-2-(4-циклопропансульфонілфеніл)-N-(5-фтортіазол-2-іл)-3-(4-оксоциклогексил)пропіонамід;
2(R)-2-(4-циклопропансульфонілфеніл)-N-(5-фтортіазол-2-іл)-3-(3-гідроксициклопентил)пропіонамід;
2(R)-2-(4-циклобутансульфонілфеніл)-N-(5-фтортіазол-2-іл)-3-(3-оксоциклопентил)пропіонамід;
2(R)-2-(4-циклобутансульфонілфеніл)-N-(5-фтортіазол-2-іл)-3-(4-оксоциклогексил)пропіонамід;
2(R)-2-(4-циклобутансульфонілфеніл)-N-(5-фтортіазол-2-іл)-3-(3-гідроксициклопентил)пропіонамід;
2(R)-2-{3-фтор-4-метансульфонілфеніл)-N-(5-фтортіазол-2-іл)-3-((R)-3-оксоциклопентил)пропіонамід;
2(R)-2-(3-фтор-4-метансульфонілфеніл)-N-(5-фтортіазол-2-іл)-3-(4-оксоциклогексил)пропіонамід та
2(R)-2-(3-фтор-4-метансульфонілфеніл)-N-(5-фтортіазол-2-іл)-3-(3-гідроксициклопентил)пропіонамід;
або фармацевтично прийнятні солі будь-якої з цих сполук.
14. Фармацевтична композиція, яка містить сполуку за будь-яким із пп. 1-13, або фармацевтично прийнятну сіль цієї сполуки, та фармацевтично прийнятний носій.
15. Спосіб профілактики або терапії стану, при якому бажаним є активування глюкокінази, який включає стадію введення в організм пацієнта ефективної кількості сполуки за будь-яким з пп. 1-13, або фармацевтично прийнятної солі цієї сполуки.
16. Спосіб профілактики або терапії гіперглікемії або діабету, який включає стадію введення в організм пацієнта ефективної кількості сполуки за будь-яким з пп. 1-13, або фармацевтично прийнятної солі цієї сполуки.
17. Спосіб за п. 16, де сполуку за будь-яким з пп. 1-13 вводять в організм пацієнта у комбінації з одним або декількома іншими антигіперглікемічними засобами або протидіабетичними засобами.
18. Спосіб запобігання діабету у людини, яка виявляє переддіабетичну гіперглікемію або погіршену толерантність до глюкози, який включає стадію введення в організм пацієнта ефективної профілактичної кількості сполуки за будь-яким із пп. 1-13, або фармацевтично прийнятної солі такої сполуки.
19. Спосіб одержання сполуки формули (Іа):
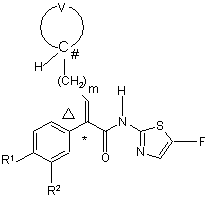 , (Іа)
, (Іа)
або фармацевтично прийнятної солі цієї сполуки, який включає стадію конденсування сполуки формули (IV):
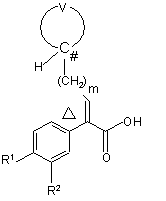 (IV)
(IV)
зі сполукою формули (V):
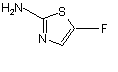 , (V)
, (V)
або сіллю такої сполуки, де:
V - (СН2)k, де одна з груп СН2 може бути факультативно замінена групами СН(ОН), С=О, C=NOH, C=NOCH3, СНХ, СХХ1, СН(ОСН3), СН(ОСОСН3), СН(С1-4алкіл) або С(ОН)(C1-4алкіл);
кожний з R1 та R2 незалежно один від одного вибрані з групи, яку складають водень, галоген, гідроксил, аміно-, ціано-, нітрогрупа, SR3, SOR3, SO2R3, SO2NR4R5, NHSO2R3, С1-4алкіл, С2-4алкеніл, С2-4алкініл, С1-4алкоксигрупа та гетероарильна група, де будь-яка група факультативно заміщена 1-5 замісниками, незалежно один від одного вибраними з групи, яку складають галоген, ціано-, нітрогрупа, гідроксил, С1-2алкоксигрупа, -N(С0-2алкіл)(С0-2алкіл), С1-2алкіл, CFnH3-n, арил, гетероарил, -СОN(С0-2алкіл)(С0-2алкіл), SCH3, SOCH3, SO2CH3 та -SO2N(С0-2алкіл)(С0-2алкіл);
m - 0 або 1;
![]() означає, що подвійний зв'язок має (E)-конфігурацію.
означає, що подвійний зв'язок має (E)-конфігурацію.
20. Спосіб одержання сполуки формули (Іb):
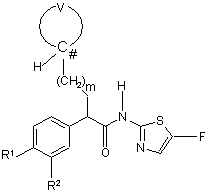 , (Іb)
, (Іb)
який включає стадію конденсування сполуки формули (VIII):
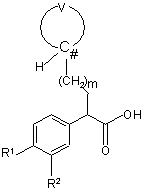 (VIII)
(VIII)
зі сполукою формули (V):
 , (V)
, (V)
або сіллю такої сполуки, де:
V - (СН2)k, де одна з груп СН2 може бути факультативно замінена групами СН(ОН), С=О, C=NOH, C=NOCH3, СНХ, СХХ1, СН(ОСН3), СН(ОСОСНз), СН(С1-4алкіл) або С(ОН)(С1-4алкіл);
кожний з R1 та R2 незалежно один від одного вибрані з групи, яку складають водень, галоген, гідроксил, аміно-, ціано-, нітрогрупа, SR3, SOR3, SO2R3, SO2NR4R5, NHSO2R3, С1-4алкіл, С2-4алкеніл, С2-4алкініл, С1-4алкоксигрупа та гетероарильна група, де будь-яка група факультативно заміщена 1-5 замісниками, незалежно один від одного вибраними з групи, яку складають галоген, ціано-, нітрогрупа, гідроксил, С1-2алкоксигрупа, N(С0-2алкіл)(С0-2алкіл), С1-2алкіл, CFnH3-n, арил, гетероарил, -СОN(С0-2алкіл)(С0-2алкіл), SCH3, SOCH3, SO2CH3 та -SO2N(С0-2алкіл)(С0-2алкіл);
m - 0 або 1.
21. Сполука формули IV за п. 19, де група, утворена -НС< та >V, означає оксоциклоалкіл або гідроксициклоалкіл;
R1 - SO2R3 або SO2NR4R5 ;
R2 - водень;
R3 - С1-3алкільна група, С3-7циклоалкільна група або 4-6-членна гетероциклічна група;
R4 та R5 незалежно один від одного - водень або С1-4алкіл, за умови, що R4 та R5 не є одночасно атомами водню;
m - 0; та
![]() означає, що подвійний зв'язок має (E)-конфігурацію.
означає, що подвійний зв'язок має (E)-конфігурацію.
22. Сполука формули VIII за п. 20, де група, утворена -НС< та >V, означає оксоциклоалкіл або гідроксициклоалкіл;
R1 - SO2R3 або SO2NR4R5; R2 - водень;
R3 - С3-7циклоалкільна група або 4-6-членна гетероциклічна група;
R4 та R5 незалежно один від одного - водень або С1-4алкіл,
за умови, що R4 та R5 не є одночасно атомами водню; та m - 0.
Текст
УКРАЇНА (19) UA (11) 90264 (13) C2 (51) МПК (2009) C07D 277/46 (2006.01) A61K 31/427 A61P 3/10 (2006.01) МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ ДЕРЖАВНИЙ ДЕПАРТАМЕНТ ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ ОПИС ДО ПАТЕНТУ НА ВИНАХІД (54) ТРИ(ЦИКЛО)ЗАМІЩЕНІ АМІДИ, ФАРМАЦЕВТИЧНА КОМПОЗИЦІЯ, СПОСОБИ ЛІКУВАННЯ ТА ПРОФІЛАКТИКИ, СПОСІБ ОДЕРЖАННЯ СПОЛУКИ # (CH2) m H N S * O R1 2 N F R , (I) або її фармацевтично прийнятна сіль, де: V - (СН2)k, де одна група СН2 може, як варіант, бути заміненою групами СН(ОН), C=O, C=NOH, C=NOCH3, СНХ, СХХ1, СН(ОСН3), СН(ОСОСН3), СН(С1-4алкіл) або С(ОН)(С1-4алкіл); X та X1 незалежно один від одного вибрані зпосеред атомів флуору та хлору; кожний з R1 та R2 незалежно один від одного вибрані з групи яку складають водень, галоген, гідроксил, аміно-, ціано-, нітрогрупа, SR3, SOR3, SO2R3, SO2NR4R5, NHSO2R3, С1-4алкіл, С2-4алкеніл, С24алкініл, С1-4алкоксигрупа та гетероарильна група, C2 (13) 90264 C H (11) V де будь-яка група факультативно заміщена 1-5 замісниками, незалежно один від одного вибраними з групи, яку складають галоген, ціано-, нітрогрупа, гідроксил, С1-2алкоксигрупа, -N(С0-2алкіл)(С02алкіл), С1-2алкіл, CFnH3-n, арил, гетероарил, CON(C0-2алкіл)(C0-2алкіл), SCH3, SOCH3, SO2CH3 тa -SО2N(С0-2алкіл)(С0-2алкіл); R3 - С1-4алкільна група, С3-7циклоалкільна група, арильна група, гетероарильна група або 4-7членна гетероциклічна група, де будь-яка група, факультативно заміщена 1-5 замісниками, незалежно один від одного вибраними з групи, яку складають галоген, ціано-, нітрогрупа, гідроксил, С1-2алкоксигрупа, -N(C0-2алкіл)(C0-2алкіл), C1-2алкіл, C3-7циклоалкіл, 4-7-членна гетероциклічна група, CFnH3-n, арил, гетероарил, СОС1-2алкіл, -CON(C02алкіл)(C0-2алкіл), SOCH3, SO2CH3 та -SO2N(C02алкіл)(С0-2алкіл); кожний з R4 та R5 незалежно один від одного є водень або С1-4алкільна група, C3-7циклоалкільна група, арильна група, гетероарильна група або 47-членна гетероциклічна група, де будь-яка група факультативно заміщена 1-5 замісниками, незалежно один від одного вибраними з групи, яку складають галоген, ціано-, нітрогрупа, гідроксил, С1-2алкоксигрупа, -N(C0-2алкіл)(C0-2алкіл), С1-2алкіл, C3-7циклоалкіл, 4-7-членна гетероциклічна група, CFnH3-n, арил, гетероарил, -СОN(C0-2алкіл)(C02алкіл), SOCH3, SO2CH3 та -SO2N(C0-2алкіл)(C02алкіл); або R4 та R5 спільно утворюють 4-8-членну гетероциклічну групу, факультативно заміщену 1 або 2 замісниками, незалежно один від одного вибраними з групи яку складають С1-2алкіл та гідроксил; k - ціле число від 2 до 7; m = 0 або 1; n = 1, 2 або 3; а пунктирна лінія спільно із суцільною лінією означають факультативний подвійний зв’язок; та означає, що подвійний зв'язок має (Е)конфігурацію. 2. Сполука за п.1, або фармацевтично прийнятна сіль цієї сполуки, де пунктирна лінія спільно із суцільною лінією означає подвійний зв'язок. UA (21) a200610724 (22) 19.04.2005 (24) 26.04.2010 (86) PCT/GB2005/050053, 19.04.2005 (31) 60/564,171 (32) 21.04.2004 (33) US (31) 60/601,077 (32) 12.08.2004 (33) US (46) 26.04.2010, Бюл.№ 8, 2010 р. (72) ФАЙФ МЕТТ'Ю, GB (73) ПРОЗІДІОН ЛТД., GB (56) WO 03/095438 A, 20.11.2003 WO 02/08209 A, 31.01.2002 WO 2004/072031 A, 26.08.2004 WO 01/85706 A, 15.11.2001 WO 01/44216 A, 21.06.2001 WO 02/46173 A, 13.06.2002 US 6610846 B1, 26.08.2003 WO 00/58293 A, 05.10.2000 (57) 1. Сполука формули (І): 2 (19) 1 3 3. Сполука за п.1, або фармацевтично прийнятна сіль цієї сполуки, де пунктирна лінія спільно із суцільною лінією означає одинарний зв'язок. 4. Сполука за п.3, або фармацевтично прийнятна сіль цієї сполуки, де пунктирна лінія спільно із суцільною лінією означає одинарний зв'язок, та абсолютна конфігурація при асиметричному центрі в -положенні до атома вуглецю амідокарбонільної групи є (R). 5. Сполука за будь-яким з попередніх пунктів, або фармацевтично прийнятна сіль, де m - 0. 6. Сполука за будь-яким з попередніх пунктів, або фармацевтично прийнятна сіль цієї сполуки, де k 4 або 5. 7. Сполука за п.6, або фармацевтично прийнятна сіль цієї сполуки, де група, утворена -НСV представляє 3-оксоциклопентил, 4оксоциклогексил або 3-гідроксициклопентил. 8. Сполука за будь-яким з попередніх пунктів, або фармацевтично прийнятна сіль цієї сполуки, де R1 та R2 не є одночасно атомами водню. 9. Сполука за будь-яким з попередніх пунктів, або фармацевтично прийнятна сіль цієї сполуки, де R1 - SOR3, SO2R3 або SO2NR4R5. 10. Сполука за будь-яким з попередніх пунктів, або фармацевтично прийнятна сіль цієї сполуки, де R3 - С1-4алкіл або C3-7циклоалкіл. 11. Сполука за будь-яким з попередніх пунктів, або фармацевтично прийнятна сіль цієї сполуки, де R1 - SО2C3-4циклоалкіл. 12. Сполука за будь-яким з попередніх пунктів, або 2 фармацевтично прийнятна сіль цієї сполуки, де R - водень, хлор, фтор або трифторметил. 13. Сполука, вибрана з групи яку складають: 2(R)-2-(3-хлор-4-метансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-((R)-3оксоциклопентил)пропіонамід; 2(R)-2-(3-хлор-4-метансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(4оксоциклогексил)пропіонамід; 2(R)-2-(3-хлор-4-метансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(3гідроксициклопентил)пропіонамід; (Е)-N-(5-флуортіазол-2-іл)-2-(4метансульфонілфеніл)-3-((S)-3оксоциклопентил)акриламід; (Е)-N-(5-флуортіазол-2-іл)-2-(4метансульфонілфеніл)-3-(4оксоциклогексил)акриламід; (Е)-N-(5-флуортіазол-2-іл)-3-(3гідроксициклопентил)-2-{4метансульфонілфеніл)акриламід; 2(R)-2-(4-циклопропансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-((R)-3оксоциклопентил)пропіонамід; 2(R)-2-(4-циклопропансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(4оксоциклогексил)пропіонамід; 2(R)-2-(4-циклопропансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(3гідроксициклопентил)пропіонамід; 2(R)-2-(4-циклобутансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(3оксоциклопентил)пропіонамід; 90264 4 2(R)-2-(4-циклобутансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(4оксоциклогексил)пропіонамід; 2(R)-2-(4-циклобутансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(3гідроксициклопентил)пропіонамід; 2(R)-2-{3-фтор-4-метансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-((R)-3оксоциклопентил)пропіонамід; 2(R)-2-(3-фтор-4-метансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(4-оксоциклогексил)пропіонамід та 2(R)-2-(3-фтор-4-метансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(3гідроксициклопентил)пропіонамід; або фармацевтично прийнятні солі будь-якої з цих сполук. 14. Фармацевтична композиція, яка містить сполуку за будь-яким із пп.1-13, або фармацевтично прийнятну сіль цієї сполуки, та фармацевтично прийнятний носій. 15. Спосіб профілактики або терапії стану, при якому бажаним є активування глюкокінази, який включає стадію введення в організм пацієнта ефективної кількості сполуки за будь-яким з пп.1-13, або фармацевтично прийнятної солі цієї сполуки. 16. Спосіб профілактики або терапії гіперглікемії або діабету, який включає стадію введення в організм пацієнта ефективної кількості сполуки за будь-яким з пп.1-13, або фармацевтично прийнятної солі цієї сполуки. 17. Спосіб за п.16, де сполуку за будь-яким з пп.113 вводять в організм пацієнта у комбінації з одним або декількома іншими антигіперглікемічними засобами або протидіабетичними засобами. 18. Спосіб запобігання діабету у людини, яка виявляє переддіабетичну гіперглікемію або погіршену толерантність до глюкози, який включає стадію введення в організм пацієнта ефективної профілактичної кількості сполуки за будь-яким із пп.1-13, або фармацевтично прийнятної солі такої сполуки. 19. Спосіб одержання сполуки формули (Іа): V C# H (CH2) m H N S * O R1 F N (Ia) R ,, (Іа) або фармацевтично прийнятної солі цієї сполуки, який включає стадію конденсування сполуки формули (IV): 2 V C H # (CH2) m OH O R1 R2 , (IV) (IV) 5 90264 6 зі сполукою формули (V): зі сполукою формули (V): H2 N H2 N S S F N N ,, (V) (V) або сіллю такої сполуки, де: V - (СН2)k, де одна з груп СН2 може бути факультативно замінена групами СН(ОН), С=О, C=NOH, C=NOCH3, СНХ, СХХ1, СН(ОСН3), СН(ОСОСН3), СН(С1-4алкіл) або С(ОН)(C1-4алкіл); кожний з R1 та R2 незалежно один від одного вибрані з групи, яку складають водень, галоген, гідроксил, аміно-, ціано-, нітрогрупа, SR3, SOR3, SO2R3, SO2NR4R5, NHSO2R3, С1-4алкіл, С2-4алкеніл, С24алкініл, С1-4алкоксигрупа та гетероарильна група, де будь-яка група факультативно заміщена 1-5 замісниками, незалежно один від одного вибраними з групи, яку складають галоген, ціано-, нітрогрупа, гідроксил, С1-2алкоксигрупа, -N(С0-2алкіл)(С02алкіл), С1-2алкіл, CFnH3-n, арил, гетероарил, СОN(С0-2алкіл)(С0-2алкіл), SCH3, SOCH3, SO2CH3 та -SO2N(С0-2алкіл)(С0-2алкіл); m - 0 або 1; означає, що подвійний зв'язок має (E)конфігурацію. 20. Спосіб одержання сполуки формули (Іb): V C# H (CH2) m H N O R1 S N F (Ib) , , (Іb) який включає стадію конденсування сполуки формули (VIII): R2 V C# H (CH2)m OH F , (V) , (V) або сіллю такої сполуки, де: V - (СН2)k, де одна з груп СН2 може бути факультативно замінена групами СН(ОН), С=О, C=NOH, C=NOCH3, СНХ, СХХ1, СН(ОСН3), СН(ОСОСНз), СН(С1-4алкіл) або С(ОН)(С1-4алкіл); кожний з R1 та R2 незалежно один від одного вибрані з групи, яку складають водень, галоген, гідроксил, аміно-, ціано-, нітрогрупа, SR3, SOR3, SO2R3, SO2NR4R5, NHSO2R3, С1-4алкіл, С2-4алкеніл, С24алкініл, С1-4алкоксигрупа та гетероарильна група, де будь-яка група факультативно заміщена 1-5 замісниками, незалежно один від одного вибраними з групи, яку складають галоген, ціано-, нітрогрупа, гідроксил, С1-2алкоксигрупа, N(С0-2алкіл)(С02алкіл), С1-2алкіл, CFnH3-n, арил, гетероарил, СОN(С0-2алкіл)(С0-2алкіл), SCH3, SOCH3, SO2CH3 та -SO2N(С0-2алкіл)(С0-2алкіл); m - 0 або 1. 21. Сполука формули IV за п.19, де група, утворена -НСV, означає оксоциклоалкіл або гідроксициклоалкіл; R1 - SO2R3 або SO2NR4R5 ; R2 - водень; R3 - С1-3алкільна група, С3-7циклоалкільна група або 4-6-членна гетероциклічна група; R4 та R5 незалежно один від одного - водень або С1-4алкіл, за умови, що R4 та R5 не є одночасно атомами водню; m - 0; та означає, що подвійний зв'язок має (E)конфігурацію. 22. Сполука формули VIII за п.20, де група, утворена -НСV, означає оксоциклоалкіл або гідроксициклоалкіл; R1 - SO2R3 або SO2NR4R5; R2 - водень; R3 - С3-7циклоалкільна група або 4-6-членна гетероциклічна група; R4 та R5 незалежно один від одного - водень або С1-4алкіл, за умови, що R4 та R5 не є одночасно атомами водню; та m - 0. O R1 R2 , (VIII) (VIII) Предметом цього винаходу є три(цикло)заміщені аміди. Зокрема, предметом цього винаходу є аміди, заміщені і) при карбонільному атомі вуглецю етилом або етенілом, приєднаним до феніл ьного циклу та карбоциклу, та іі) при аміногрупі фторзаміщеним тіазольним циклом, які є модуляторами глюкокінази та корисні при профілактиці або терапії гіперглікемії та діабету, зокрема, діабету типу II. Вважається, що глюкокіназа ("GK") відіграє важливу роль у процесах регулювання організмом рівня глюкози у плазмі. Глюкокіназа, яка знахо диться, головним чином, у печінці та підшлунковій залозі, є однією із чотирьох гексокіназ, які є каталізаторами початкового метаболізму глюкози. Глюкокіназний шлях насичується при вищих рівнях глюкози, ніж інші гексокіназні шляхи (дивись Принц та ін. - R.L. Printz et al., Annu. Rev. Nutr., 13:463-496 (1993)). Глюкокіназа відіграє вирішальну роль у підтриманні балансу глюкози в організмах ссавців. Тварини, які не експресують глюкокіназу, вмирають від діабету невдовзі після народження, в той час як тварини з надлишковою експресією глюкокінази мають підвищену стійкість до глюкози. Ак 7 тивування глюкокінази може спричиняти гіперінсулінемічну гіпоглікемію (дивись, наприклад, Крістесен та ін. - Н.В.Т. Christesen et al., Diabetes, 51:1240-1246 (2002)). Крім того, ювенільний діабет типу II, що починається у період зрілості, спричиняється втратою функціональних мутацій у гені глюкокінази, з чого випливає, що глюкокіназа в людському організмі діє як сенсор глюкози (Лянь та ін. - Y. Liang et al., Biochem. J. 30^:167-173 (1995)). Таким чином, сполуки, які активують глюкокіназу, підвищують чутливість сенсорної системи глюкокінази та можуть бути корисними при лікуванні гіперглікемії, зокрема, гіперглікемії, пов'язаної з діабетом типу II. Тому бажаним є віднайдення нових сполук, які активують глюкокіназу, з метою лікування діабету. У публікації міжнародної заявки на патент № WO2001/044216 та у патенті США №6,353,111 описані (Е)-2,3-двозаміщені-Nгетероарилакриламіди як активатори глюкокінази. У публікації міжнародної заявки на патент № WO2002/014312 та у патентах США №6,369,232, №6,388,088 та №6,441,180 описані тетразолілфенілацетамідні активатори глюкокінази. У публікації міжнародної заявки на патент № WO2000/058293, Заявці на європейський патент ЕР 1169312 та у патенті США №6,320,050 описані арилциклоалкілпропіонаміди як активатори глюкокінази. У публікації міжнародної заявки на патент № WO2002/008209 та у патенті США №6,486,184 описані бензолацетамідні активатори глюкокінази, заміщені в ос-положенні ацилу та гетероатома, як протидіабетичні засоби. У публікації міжнародної заявки на патент № WO2001/083478 описані гідантоїновмісні активатори глюкокінази. У публікації міжнародної заявки на патент № WO2001/083465 та у патенті США №6,388,071 описані алкінілфенільні гетероароматичні активатори глюкокінази. У публікації міжнародної заявки на патент № WO2001/085707 та у патенті США №6,489,485 описані пара-амінозаміщені феніламідні активатори глюкокінази. У публікації міжнародної заявки на патент № WO2002/046173 та у патентах США №6,433,188, № 6,441,184 та №6,448,399 описані конденсовані гетероароматичні активатори глюкокінази. У публікації міжнародної заявки на патент № WO2002/048106 та у патенті США №6,482,951 описані активатори глюкокінази - похідні ізоіндолін1-ону. У публікації міжнародної заявки на патент № WO2001/085706 описані активатори глюкокінази на основі заміщеного фенілацетаміду для лікування діабету типу II. У патенті США №6,384,220 описані активатори глюкокінази - пара-арил- або гетероарилзаміщені похідні фенілу. У патенті Франції №2,834,295 описані способи очищення та кристалічна структура людської глюкокінази. У публікації міжнародної заявки на патент № WO2003/095438 описані Nгетероарилфенілацетаміди та аналогічні сполуки як активатори глюкокінази для лікування діабету типу II. У патенті США №6,610,846 описано одержання циклоалкілгетероарилпропіонамідів як активаторів глюкокінази. У публікації міжнародної заявки на патент № WO2003/000262 описані вінілфенільні активатори глюкокінази. У публікації 90264 8 міжнародної заявки на патент № WO2003/000267 описані похідні амінонікотинатів як модулятори глюкокінази. У публікації міжнародної заявки на патент № WO2003/015774 описані сполукимодулятори глюкокінази. У публікації міжнародної заявки на патент № WO2003/047626 описано застосування активатора глюкокінази у комбінації з антагоністом глюкагону для лікування діабету типу II. У публікації міжнародної заявки на патент № WO2003/055482 описані похідні амідів як активатори глюкокінази. У публікації міжнародної заявки на патент № WO2003/080585 описані похідні амінобензаміду, активні щодо глюкокінази для лікування діабету та ожиріння. У публікації міжнародної заявки на патент № WO2003/097824 описано кристали глюкокінази з людської печінки та їх застосування для проектування лікарських засобів на основі структури. У публікації міжнародної заявки на патент № WO2004/002481 описані арилкарбонільні похідні як активатори глюкокінази. У публікаціях міжнародних заявок на патенти № WO2004/072031 та № WO2004/072066 (опублікованих пізніше дати пріоритету цієї заявки) описані різноманітні три(цикло)заміщені аміди, які є модуляторами глюкокінази. Сполуки, представлені формулою (І): , або фармацевтично прийнятні солі цих сполук, корисні при профілактиці або терапії гіперглікемії та діабету, зокрема, діабету типу II. Цей винахід пропонує сполуку формули (І): , або фармацевтично прийнятну сіль цієї сполуки, де: V-(СН2)k, де одна з груп СН2 може бути факультативно замінена групами СН(ОН), С=О, C=NOH, C=NOCH3, СНХ, СХХ1, СН(ОСН3), СН(ОСОСН3), СН(С1-4-алкіл) або С(ОН)(С1-4-алкіл); 1 X та X незалежно один від одного вибрані зпосеред атомів фтору та хлору; кожний з R1 та R2 незалежно один від одного вибрані з групи, яку складають водень, галоген, гідроксил, аміно-, ціано-, нітрогрупа, SR3, SOR3, SO2R3, SO2NR4R5, NHSO2R3, С1-4-алкіл, С2-4алкеніл, С2-4-алкініл, С1-4-алкоксигрупа та гетероа 9 рильна група, де будь-яка група факультативно заміщена 1-5 замісниками, незалежно один від одного вибраними з групи, яку складають галоген, ціано-, нітрогрупа, гідроксил, С1-2-алкоксигрупа, N(С0-2-алкіл)(С0-2-алкіл), С1-2-алкіл, CFnH3-n, арил, гетероарил, -СОN(С0-2-алкіл)(С0-2-алкіл), SCH3, SOCH3, SO2CH3 та -SO2N(С0-2-алкіл)(С0-2-алкіл); R3 – С1-4-алкільна група, С3-7-циклоалкільна група, арильна група, гетероарильна група або 47-членна гетероциклічна група, де будь-яка група факультативно заміщена 1-5 замісниками, незалежно один від одного вибраними з групи, яку складають галоген, ціано-, нітрогрупа, гідроксил, С1-2-алкоксигрупа, -N(С0-2-алкіл)(С0-2-алкіл), С1-2алкіл, С3-7-циклоалкіл, 4-7-членна гетероциклічна група, CFnH3-n, арил, гетероарил, СОС1-2-алкіл, СОN(С0-2-алкіл)(С0-2-алкіл), SOCH3, SO2CH3 та SO2N(C0-2-алкіл)(C0-2-алкіл); кожний з R4 та R5 незалежно один від одного є водень або С1-4-алкільна група, С3-7-циклоалкільна група, арильна група, гетероарильна група або 47-членна гетероциклічна група, де будь-яка група факультативно заміщена 1-5 замісниками, незалежно один від одного вибраними з групи, яку складають галоген, ціано-, нітрогрупа, гідроксил, С1-2-алкоксигрупа, -N(C0-2-aлкіл)(C0-2-алкіл), С1-2алкіл, С3-7-циклоалкіл, 4-7-членна гетероциклічна група, CFnH3-n, арил, гетероарил, -СОN(С0-2алкіл)(С0-2-алкіл), SOCH3,SО2СН3 та -SO2N(С0-2алкіл)(С0-2-алкіл); або R4 та R5 спільно утворюють 4-8-членну гетероциклічну групу, факультативно заміщену 1 або 2 замісниками, незалежно один від одного вибраними з групи, яку складають С1-2-алкіл та гідроксил; k - ціле число від 2 до 7; m - 0 або 1; n - 1, 2 або 3; та пунктирна лінія спільно із суцільною лінією означають факультативний подвійний зв'язок, та А означає, що подвійний зв'язок має (Е)конфігурацію. Якщо пунктирна лінія спільно із суцільною лінією означає одинарний зв'язок, то атом вуглецю, який приєднує арильний цикл та -HC V-вмісний бічний ланцюг до вуглецю амідокарбонільної групи, тобто атом вуглецю, позначений "*", є хіральним центром. Відповідно, відносно цього центра сполука може бути як рацематом, так і окремим енантіомером у (R)- або (S)-конфігурації. Перевага віддається (R)-енантіомерам. Атом вуглецю, позначений "#", також може бути хіральним. Відповідно, відносно цього центра сполука може бути як рацематом, так і окремим енантіомером у (R)- або (S)-конфігурації. Перевага віддається (R)енантіомерам, якщо пунктирна лінія спільно із суцільною лінією означають одинарний зв'язок. Якщо пунктирна лінія спільно із суцільною лінією означають подвійний зв'язок, перевага віддається (S)-енантіомерам. За іншим аспектом, цей винахід пропонує сполуку, представлену формулою (Іа): 90264 10 , або фармацевтично прийнятну сіль цієї сполуки, де V, R1, R2, m та відповідають вищенаведеним визначенням для формули (І). За іншим варіантом здійснення цей винахід пропонує сполуку, представлену формулою (Іа), або фармацевтично прийнятну сіль цієї сполуки, де група, утворена -НСV, означає оксоциклоалкіл або гідроксициклоалкіл, наприклад, 3оксоциклопентил, зокрема, (R)-3-оксоциклопентил, 4-оксоциклогексил або 3-гідроксициклопентил, особливо (R)-3-оксоциклопентил. За іншим аспектом, якому віддається перевага, цей винахід пропонує сполуку, представлену формулою (Іb): , або фармацевтично прийнятну сіль цієї сполуки, де V, R1, R2 та m відповідають вищенаведеним визначенням для формули (І). За одним із варіантів здійснення цього аспекту, якому віддається перевага, цей винахід пропонує сполуку, представлену формулою (Іb), або фармацевтично прийнятну сіль цієї сполуки, де група, утворена -НСV, означає оксоциклоалкіл або гідроксициклоалкіл, наприклад, 3оксоциклопентил, зокрема, (R)-3-оксоциклопентил, 4-оксоциклогексил або 3-гідроксициклопентил, особливо (R)-3-оксоциклопентил. Молекулярна маса сполуки формули (І) за варіантом, якому віддається перевага, становить менш ніж 800, за варіантом, якому віддається більша перевага, становить менш ніж 600, за варіантом, якому віддається найбільша перевага, становить менш ніж 500. Згідно із цим винаходом R1 та R2 відповідно до варіанта, якому віддається перевага, не є одночасно атомами водню. Згідно із цим винаходом R1 за варіантом, якому віддається перевага, -CF3, SOR3, SO2R3, SO2NR4R5, NHSO2R3 або триазоліл; за варіантом, якому віддається більша перевага, -SOR3, SO2R3 або SO2NR4R5; за варіантом, якому віддається найбільша перевага, -SO2R3 або SO2NR4R5, особливо -SO2R3. 11 Зокрема, R1 - SО2С3-4-циклоалкіл, особливо SO2-циклопропіл. Згідно із цим винаходом R2 за варіантом, якому віддається перевага, - водень, хлор, фтор або трифторметил; за варіантом, якому віддається більша перевага, - водень або хлор. Згідно із цим винаходом R3 за варіантом, якому віддається перевага, - С1-3-алкіл або С3-4Циклоалкіл, за варіантом, якому віддається більша перевага, - С3-4-циклоалкіл, особливо - циклопропіл. Згідно із цим винаходом R4 та R5 відповідно до варіанта, якому віддається перевага, незалежно один від одного є водень або С1-4-алкіл? наприклад, один із R4 та R5 - водень, а інший - етил, або спільно утворюють 4-8-членну гетероциклічну групу. Відповідно до варіанта, якому віддається перевага, R4 та R5 не є одночасно атомами водню. Згідно із цим винаходом m за варіантом, якому віддається перевага, - 0. Згідно із цим винаходом V за варіантом, якому віддається перевага, -(СН2)k, де одна з груп СН2 заміщена групою СН(ОН) або С=О. Згідно із цим винаходом k за варіантом, якому віддається перевага, - 4 або 5. Серед сполук за цим винаходом особлива перевага віддається таким сполукам: 2(R)-2-(3-хлор-4-метансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-((ІІ)-3оксоциклопентил)пропіонамід; 2(R)-2-(3-хлор-4-метансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(4оксоциклогексил)пропіонамід; 2(R)-2-(3-хлор-4-метансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(3гідроксициклопентил)пропіонамід; (Е)-N-(5-фтортіазол-2-іл)-2-(4метансульфонілфеніл)-3-((S)-3оксоциклопентил)акриламід; (Е)-N-(5-фтортіазол-2-іл)-2-(4метансульфонілфеніл)-3-(4оксоциклогексил)акриламід; (Е)-N-(5-фтортіазол-2-іл)-3-(3гідроксициклопентил)-2-(4метансульфонілфеніл)акриламід; 2(R)-2-(4-циклопропансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-((К)-3оксоциклопентил)пропіонамід; 2(R)-2-(4-циклопропансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(4оксоциклогексил)пропіонамід; 2(R)-2-(4-циклопропансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(3гідроксициклопентил)пропіонамід; 2(R)-2-(4-циклобутансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(3оксоциклопентил)пропіонамід; 2(R)-2-(4-циклобутансульфонілфеніл)-ЇЧ-(5фтортіазол-2-іл)-3-(4оксоциклогексил)пропіонамід; 2(R)-2-(4-циклобутансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(3гідроксициклопентил)пропіонамід; 90264 12 2(R)-2-(3-фтор-4-метансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-((R)-3оксоциклопентил)пропіонамід; 2(R-2-(3-фтор-4-метансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(4-оксоциклогексил)пропіонамід та 2(R)-2-(3-фтор-4-метансульфонілфеніл)-N-(5фтортіазол-2-іл)-3-(3гідроксициклопентил)пропіонамід, або фармацевтично прийнятним солям цих сполук. Групи, яким віддається перевага для кожної змінної, у загальному вигляді перелічені вище окремо для кожної змінної; однак сполуки за цим винаходом, яким віддається перевага, включають сполуки, де кілька змінних або кожна змінна у Формулі (І) вибрана з груп, яким віддається перевага, більша перевага, найбільша перевага, спеціально або конкретно перелічених стосовно до кожної змінної. Таким чином, мається на увазі, що цей винахід охоплює усі комбінації груп, яким віддається перевага, більша перевага, найбільша перевага, спеціально або конкретно перелічених груп. У значенні, вживаному у цьому описі, якщо не зазначено інше, "алкіл", а також інші групи, які мають префікс "алк", такі як, наприклад, алкоксигрупа, алкеніл, алкініл тощо, означають вуглецеві ланцюги, які можуть бути лінійними або розгалуженими, або їх комбінації. До прикладів алкільних груп належать метил, етил, пропіл, ізопропіл, бутил, втор- та трет-бутил, пентил, гексил, гептил тощо. "Алкеніл", "алкініл" та інші подібні терміни охоплюють вуглецеві ланцюги, які мають щонайменше один ненасичений вуглець-вуглецевий зв'язок. У значенні, вживаному у цьому описі, наприклад, термін "С0-4-алкіл" вживається для позначення алкілу, який має 0-4 атоми вуглецю, тобто 0, 1, 2, З або 4 атоми вуглецю в нормальній або розгалуженій конфігурації. Алкіл, який не має атомів вуглецю, є воднем, якщо згаданий алкіл є кінцевою групою. Алкіл, який не має атомів вуглецю, є простим зв'язком, якщо згаданий алкіл є місточковою (з'єднувальною) групою. Терміни "циклоалкіл" та "карбоциклічна група" означає карбоцикли, які не містять гетероатомів, та охоплює моноциклічні насичені С3-7-карбоцикли. До прикладів циклоалкілів та карбоциклічних груп належить циклопропіл, циклобутил, циклопентил та циклогексил тощо. Термін "галоген" охоплює атоми фтору, хлору, брому та йоду. Термін "арил" охоплює, наприклад, феніл та нафтил, за варіантом, якому віддається перевага, феніл. Якщо не обумовлено інше, термін "гетероциклічна група" охоплює 4-8-членні насичені цикли, які містять один або два гетероатоми, вибрані зпосеред атомів кисню, сірки та азоту. Гетероатоми не з'єднані безпосередньо один з одним. До прикладів гетероциклічних груп належать оксетан, тетрагідрофуран, тетрагідропіран, оксепан, оксокан, тієтан, тетрагідротіофен, тетрагідротіопіран, тієпан, тіокан, азетидин, піролідин, піперидин, азепан, азокан, [1,3]діоксан, оксазолідин, піперазин 13 тощо. До інших прикладів гетероциклічних груп належать окиснені форми сірковмісних циклів. Отже, тетрагідротіофен-1-оксид, тетрагідротіофен1,1-діоксид, тетрагідротіопіран-1-оксид та тетрагідротіопіран-1,1-діоксид також належать до гетероциклічних груп. Якщо не обумовлено інше, термін "гетероарил" охоплює 5- або 6-членні гетероарильні цикли, які містять 1-4 гетероатоми, вибрані з-посеред атомів кисню, сірки та азоту. До прикладів таких гетероарильних циклів належать фурил, тієніл, піроліл, піразоліл, імідазоліл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, триазоліл, оксадіазоліл, тіадіазоліл, тетразоліл, піридиніл, піридазиніл, піримідиніл, піразиніл та триазиніл. Вказані вище формули зображені без визначених стереохімічних конфігурацій у певних положеннях. Цей винахід охоплює усі стереоізомери (наприклад, геометричні ізомери, оптичні ізомери, діастереоізомери тощо) та фармацевтично прийнятні солі цієї сполуки, за виключенням конкретно вказаних або визначених іншим чином. Крім того, суміші стереоізомерів а також виділені конкретні стереоізомери також охоплюються винаходом, за виключенням конкретно зображених або визначених іншим чином. Під час виконання операцій синтезу, застосовуваних для одержання таких сполук, або операцій рацемізації або епімеризації, відомих фахівцям в цій галузі, можуть утворюватися продукти, які являють собою суміш стереоізомерів. Якщо існують таутомери сполук вищезгаданих формул, цей винахід охоплює будь-які можливі таутомери та їх фармацевтично прийнятні солі, та їх суміші, за виключенням конкретно зображених або визначених іншим чином. Якщо сполуки вищезгаданих формул та фармацевтично прийнятні солі цих сполук існують у формі сольватів або поліморфних формах, цей винахід охоплює будь-які можливі сольвати та поліморфні форми. Тип розчинника, який утворює сольват, конкретно не обмежується за умови, що розчинник є фармакологічно прийнятним. Можуть бути застосовані, наприклад, вода, етанол, пропанол, ацетон тощо. Оскільки сполуки формули (І) призначені для фармацевтичного застосування, вони відповідно до варіанта, якому віддається перевага, пропонуються у практично чистій формі, наприклад, із чистотою щонайменше 60%, за варіантом, якому віддається більша перевага, із чистотою щонайменше 75%, із чистотою щонайменше 95% та за варіантом, якому віддається особлива перевага, із чистотою щонайменше 98% (відсотки визначаються за масою). Цей винахід також охоплює фармацевтичну композицію, яка містить сполуку формули (І) або фармацевтично прийнятну сіль цієї сполуки у комбінації із фармацевтично прийнятним носієм. За варіантом, якому віддається перевага, композиція містить фармацевтично прийнятний носій та нетоксичну терапевтично ефективну кількість сполуки формули (І) або фармацевтично прийнятної солі цієї сполуки. Крім того, в межах цього варіанта здійснення, цей винахід охоплює фармацевтичну композицію для профілактики або лікування гіперглікемії та 90264 14 діабету, зокрема, діабету типу II, шляхом активування глюкокінази, яка містить фармацевтично прийнятний носій та нетоксичну терапевтично ефективну кількість сполуки формули (І) або фармацевтично прийнятної солі цієї сполуки. Цей винахід також пропонує застосування сполуки формули (І) або фармацевтично прийнятної солі цієї сполуки як фармацевтичний засіб. Сполуки та композиції за цим винаходом ефективні для лікування гіперглікемії та діабету, зокрема, діабету типу II, у ссавців, наприклад, у людей. Цей винахід також пропонує спосіб профілактики або терапії стану, при якому бажаним є активування глюкокінази, який включає стадію введення в організм хворого ефективної кількості сполуки формули (І) або фармацевтично прийнятної солі цієї сполуки. Цей винахід також пропонує спосіб профілактики або терапії гіперглікемії або діабету, зокрема, діабету типу II, який включає стадію введення в організм хворого ефективної кількості сполуки формули (І) або фармацевтично прийнятної солі цієї сполуки. Цей винахід також пропонує спосіб запобігання діабету, зокрема, діабету типу II, у людини, яка виявляє переддіабетичну гіперглікемію або погіршену толерантність до глюкози, який включає стадію введення в організм хворого ефективної профілактичної кількості сполуки формули (І) або фармацевтично прийнятної солі цієї сполуки. Цей винахід також пропонує застосування сполуки формули (І) або фармацевтично прийнятної солі цієї сполуки як активатора глюкокінази. Цей винахід також пропонує застосування сполуки формули (І) або фармацевтично прийнятної солі цієї сполуки для профілактики або терапії гіперглікемії або діабету, зокрема, діабету типу II. Цей винахід також пропонує застосування сполуки формули (І) або фармацевтично прийнятної солі цієї сполуки для попередження діабету, зокрема, діабету типу II, у людини, яка виявляє переддіабетичну гіперглікемію або погіршену толерантність до глюкози. Цей винахід також пропонує застосування сполуки формули (І) або фармацевтично прийнятної солі цієї сполуки при виготовленні лікарського засобу для активування глюкокінази. Цей винахід також пропонує застосування сполуки формули (І) або фармацевтично прийнятної солі цієї сполуки при виготовленні лікарського засобу для профілактики або терапії гіперглікемії або діабету, зокрема, діабету типу II. Цей винахід також пропонує застосування сполуки формули (І) або фармацевтично прийнятної солі цієї сполуки при виготовленні лікарського засобу для попередження діабету, зокрема, діабету типу II, у людини, яка виявляє переддіабетичну гіперглікемію або погіршену толерантність до глюкози. Сполуки та композиції за цим винаходом можуть бути факультативно застосовані у комбінації з одним або декількома іншими протидіабетичними або антигіперглікемічними засобами, до яких належать, наприклад, сульфонілсечовини (напри 15 клад, глібурид, глімепірид, гліпірид, гліпізид, хлорпропамід, гліклазид, глісоксепід, ацетогексамід, гліборнурид, толбутамід, толазамід, карбутамід, гліквідон, глігексамід, фенбутамід, толцикламід тощо), бігуаніди (наприклад, метформін, фенформін, буформін тощо), антагоністи глюкагону (наприклад, пептидні або непептидні антагоністи глюкагону), інгібітори глюкозидази (наприклад, акарбоз, міглітол тощо), засоби, що підвищують секрецію інсуліну, сенсибілізатори до інсуліну (наприклад, троглітазон, розиглітазон, піоглітазон тощо) і т.ін.; або засоби проти ожиріння (наприклад, сибутрамін, орлістат тощо) і т.ін. Сполуки та композиції за цим винаходом та інші протидіабетичні засоби або антигіперглікемічні засоби можуть бути введені в організм одночасно, послідовно або окремо. Термін "фармацевтично прийнятні солі" означає солі, виготовлені із фармацевтично прийнятних нетоксичних основ або кислот. Якщо сполука за цим винаходом має кислотний характер, її відповідна сіль може бути без утруднень одержана із фармацевтично прийнятних нетоксичних основ, в тому числі з неорганічних основ та органічних основ. До солей, одержаних із таких неорганічних основ, належать солі алюмінію, амонію, кальцію, двовалентної міді, одновалентної міді, тривалентного заліза, двовалентного заліза, літію, магнію, тривалентного марганцю, двовалентного марганцю, калію, натрію, цинку тощо. Особлива перевага віддається солям амонію, кальцію, магнію, калію та натрію. До солей, похідних із фармацевтично прийнятних органічних нетоксичних основ, належать солі первинних, вторинних та третинних амінів, а також циклічних амінів та заміщених амінів, наприклад, природних та штучних амінів. До інших фармацевтично прийнятних органічних нетоксичних основ, з яких можуть бути утворені солі, належать, наприклад, аргінін, бетаїн, кофеїн, холін, N',N'-дибензилетилендіамін, діетиламін, 2діетиламіноетанол, 2-диметиламіноетанол, етаноламін, етилендіамін, N-етилморфолін, Nетилпіперидин, глюкамін, глюкозамін, гістидин, ізопропіламін, лізин, метилглюкамін, морфолін, піперазин, піперидин, поліамінні смоли, прокаїн, пурини, теобром, триетиламін, триметиламін, трипропіламін, трометамін тощо. Якщо сполука за цим винаходом має основний характер, її відповідні солі можуть бути без утруднень одержані із фармацевтично прийнятних нетоксичних кислот, в тому числі неорганічних та органічних кислот. До таких кислот належать, наприклад, оцтова, бензолсульфонова, бензойна, камфорсульфонова, лимонна, етансульфонова, фумарова, глкжонова, глутамінова, бромистоводнева, хлористоводнева, ізетіонова, молочна, малеїнова, яблучна, мигдальна, метансульфонова, слизова, азотна, памова, пантотенова, фосфорна, бурштинова, сірчана, винна, яяратолуолсульфонова кислота тощо. До кислот, яким віддається особлива перевага, належать лимонна, бромистоводнева, хлористоводнева, малеїнова, фосфорна, сірчана, метансульфонова та винна кислоти. 90264 16 Фармацевтичні композиції за цим винаходом містять сполуку формули (І) або фармацевтично прийнятну сіль цієї сполуки як активний інгредієнт, фармацевтично прийнятний носій та факультативно інші терапевтичні інгредієнти або допоміжні речовини. Згадані композиції охоплюють композиції, прийнятні для перорального, ректального, місцевого та парентерального (в тому числі підшкірного, внутрішньом'язового та внутрішньовенного) введення, а також введення шляхом інгаляції, однак найбільш прийнятний шлях у будь-якому випадку буде залежати від конкретного реципієнта, та природи й тяжкості станів, для лікування яких має вводитися активний інгредієнт. Фармацевтичні композиції без утруднень можуть бути представлені у формі дозованих одиниць та виготовлені будь-яким зі способів, відомих у фармацевтичній галузі. Фармацевтичні композиції за цим винаходом відповідно до варіанта, якому віддається перевага, придатні для перорального введення. На практиці сполуки формули (І) або фармацевтично прийнятні солі цих сполук можуть поєднуватися як активний інгредієнт у складі однорідної суміші із фармацевтичним носієм відповідно до звичайних фармацевтичних способів приготування лікарських засобів. Носій може мати різноманітні форми, залежно від форми лікарського засобу, бажаного для введення, наприклад, перорального або парентерального (в тому числі внутрішньовенного). Таким чином, фармацевтичні композиції за цим винаходом можуть бути представлені у вигляді дискретних одиниць, прийнятних для перорального введення, наприклад, капсул, облаток або таблеток, які містять заздалегідь визначену кількість активного інгредієнта. Крім того, композиції можуть бути представлені у вигляді порошку, у вигляді гранул, у вигляді розчину, у вигляді суспензії у водній рідині, у вигляді неводної рідини, у вигляді емульсії типу "масло у воді" або у вигляді емульсії типу "вода у маслі". Окрім вищезгаданих звичайних дозованих лікарських форм, сполуки, представлені формулою (І), або фармацевтично прийнятні солі цих сполук можуть вводитися в організм у вигляді лікарських форм із модифікованим вивільненням та/або депо. Композиції можуть бути виготовлені будь-яким способом, відомим у фармацевтичній галузі. Загалом, такі способи включають стадію поєднання активного інгредієнта з носієм, який утворює один або кілька необхідних інгредієнтів. Як правило, композиції виготовляють шляхом рівномірного та ретельного перемішування активного інгредієнта з рідкими носіями, тонкоподрібненими твердими носіями або обома видами носіїв. Потім продукту можна надати форму, зручну для бажаного способу застосування. Отже, фармацевтичні композиції за цим винаходом можуть містити фармацевтично прийнятний носій та сполуку формули (І) або фармацевтично прийнятну сіль цієї сполуки. Сполуки формули (І) або фармацевтично прийнятні солі цих сполук можуть також міститися у фармацевтичній композиції у комбінації з одним або декількома іншими терапевтично активними сполуками. 17 Фармацевтичні композиції за цим винаходом охоплюють фармацевтично прийнятні ліпосоми, які містять сполуку формули (І) або фармацевтично прийнятну сіль цієї сполуки. Застосовуваним фармацевтичним носієм може бути, наприклад, тверда речовина, рідина або газ. Прикладами твердих носіїв є лактоза, подрібнений гіпс, сахароза, тальк, желатин, агар, пектин, аравійська камедь, стеарат магнію та стеаринова кислота. Прикладами рідких носіїв є цукровий сироп, арахісова олія, оливкова олія та вода. Прикладами газоподібних носіїв є діоксид вуглецю та азот. При виготовленні композицій для пероральних лікарських форм можуть бути застосовані будь-які прийнятні для цього фармацевтичні середовища та засоби. Наприклад, для виготовлення рідких препаратів для перорального вживання, наприклад, суспензій, еліксирів та розчинів, можна застосовувати воду, гліколі, олії, спирти, смакоароматичні домішки, консерванти, барвники тощо; такі носії, як крохмалі, цукри, мікрокристалічна целюлоза, розріджувачі, гранулювальні засоби, змащувальні засоби, в'яжучі, розпушувальні засоби тощо, можуть бути застосовані при виготовленні твердих препаратів для перорального вживання, таких як порошки, капсули та таблетки. Таблеткам та капсулам віддається перевага як дозованим лікарським формам для перорального застосування внаслідок простоти їх вживання; при їх виготовленні застосовуються тверді фармацевтичні носії. Факультативно на таблетки можуть бути нанесені покриття стандартними способами із застосуванням водних або неводних середовищ. Таблетки, які містять композиції за цим винаходом, можна виготовляти шляхом пресування або формування, факультативно із застосуванням одного або кількох додаткових інгредієнтів або допоміжних речовин. Пресовані таблетки можна виготовляти шляхом пресування на відповідних машинах активного інгредієнта у сипкій формі, такій як порошок або гранули, факультативно змішаного з в'яжучим, змащувальним засобом, інертним розріджувачем, поверхнево-активним або розпушувальним засобом або з іншим допоміжним засобом. Такими засобами можуть бути, наприклад, інертні розріджувачі, такі як карбонат кальцію, карбонат натрію, лактоза, фосфат кальцію або фосфат натрію; гранулювальні та розпушувальні засоби, наприклад, кукурудзяний крохмаль або альгінова кислота; в'яжучі засоби, наприклад, крохмаль, желатин або аравійська камедь; та змащувальні засоби, наприклад, стеарат магнію, стеаринова кислота або тальк. Таблетки можуть бути непокритими або мати покриття, нанесене відомими способами, з метою уповільнення розпаду та поглинання у шлунково-кишковому тракті та забезпечення таким чином пролонгованої дії протягом довшого часу. Наприклад, можуть бути застосовані такі уповільнювачі, як гліцерилмоностеарат або гліцериндистеарат. У твердих желатинових капсулах активний інгредієнт змішаний з інертним твердим розріджувачем, наприклад, карбонатом кальцію, фосфатом кальцію або каоліном. У м'яких желатинових кап 90264 18 сулах активний інгредієнт змішаний з водним або олійним середовищем, наприклад, з арахісовою олією, рідким парафіном або оливковою олією. Формовані таблетки можуть виготовлятися шляхом формування у відповідному устаткуванні суміші порошкоподібної сполуки, зволоженої інертним рідким розріджувачем. Кожна таблетка за варіантом, якому віддається перевага, містить від приблизно 0,05мг до приблизно 5г активного інгредієнта, а кожна облатка або капсула за варіантом, якому віддається перевага, містить від приблизно 0,05мг до приблизно 5г активного інгредієнта. Наприклад, лікарська форма, призначена для перорального введення людині, може містити від приблизно 0,5мг до приблизно 5г активного засобу, змішаного з відповідною та прийнятною кількістю носія, яка може становити від приблизно 5% до приблизно 95% загальної кількості композиції. Дозовані одиниці, як правило, містять від приблизно 1 мг до приблизно 2г активного інгредієнта, у типових випадках 25мг, 50мг, 100мг, 200мг, 300мг, 400мг, 500мг, 600мг, 800мг або 1000мг. Фармацевтичні композиції за цим винаходом, придатні для парентерального введення, можуть бути виготовлені у формах розчинів або суспензій активної сполуки у воді. До композицій може бути додана відповідна поверхнево-активна речовина, така як гідроксипропілцелюлоза. Можуть бути виготовлені також дисперсії у гліцерині, рідких поліетиленгліколях та їх сумішах із рослинними оліями. Крім того, до композицій можна додавати консервант для попередження шкідливого розвитку мікроорганізмів. До фармацевтичних композицій за цим винаходом, придатних для ін'єкційного застосування, належать стерильні водні розчини або дисперсії. Крім того, композиції можуть мати форму стерильних порошків для виготовлення на місці таких стерильних ін'єкційних розчинів або дисперсій для негайного застосування. У всіх випадках кінцева ін'єкційна лікарська форма має бути стерильною та матидостатню плинність для полегшення введення за допомогою шприца. Фармацевтичні композиції мають бути стабільними в умовах виготовлення та зберігання; отже, за варіантом, якому віддається перевага, мають бути захищені від забруднювального впливу мікроорганізмів, таких як бактерії та грибки. Носієм може бути розчинник або дисперсійне середовище, які містять, наприклад, воду, етанол, багатоатомні спирти (наприклад, гліцерин, пропіленгліколь та рідкий поліетиленгліколь), рослині олії та прийнятні суміші таких носіїв. Фармацевтичні композиції за цим винаходом можуть мати форму, придатну для місцевого застосування, наприклад, аерозолю, крему, мазі, лосьйону, пудри тощо. Крім того, композиції можуть мати форму, придатну для застосування у пристроях для черезшкірного введення. Такі лікарські форми можна виготовляти, використовуючи сполуку формули (І) або фармацевтично прийнятну сіль такої сполуки, із застосуванням звичайних способів оброблення. Наприклад, крем або мазь виготовляють шляхом змішування гідрофільного 19 90264 20 матеріалу та води з приблизно 5-10% (мас.) сполуки для одержання крему або мазі бажаної консистенції. Фармацевтичні композиції за цим винаходом можуть мати форму, придатну для ректального введення, де носієм є тверда речовина. Відповідно до варіанта, якому віддається перевага, суміш формують у одиничні дозовані супозиторії. До придатних носіїв належить какаова олія та інші матеріали, звичайно застосовувані в галузі. Супозиторії зручно формувати шляхом попереднього змішування композиції з розм'якшеним або розплавленим носієм (носіями) з подальшим охолодженням та формуванням у формах для відливання. Фармацевтичні композиції за цим винаходом можуть мати форму, придатну для введення інгаляційним способом. Такі лікарські препарати можуть бути виготовлені у формах та із застосуванням носіїв, описаних, наприклад, у: 1) Particulate Interactions in Dry Powder Formulations for Inhalation, Xian Zeng et al., 2000, Taylor and Francis, 2) Pharmaceutical Inhalation Aerosol Technology, Anthony Hickey, 1992, Marcel Dekker, 3) Respiratory Drug Delivery, 1990, Editor: P.R. Byron, CRC Press. Крім вищезгаданих інгредієнтів носіїв, описані вище фармацевтичні композиції можуть містити, за потребою, один або кілька додаткових компонентів носіїв, таких як розріджувачі, буфери, ароматизатори, в'яжучі, поверхнево-активні речовини, загусники, змащувальні засоби, консерванти (в тому числі антиоксиданти) тощо. Крім того, можуть додаватися інші допоміжні речовини для забезпечення ізотонічності композиції з кров'ю очікуваного реципієнта. Композиції, які містять сполуку формули (І) або фармацевтично прийнятні солі цієї сполуки, можуть виготовлятися також у формах порошкоподібних або рідких концентратів. Як правило, при лікуванні вищевказаних станів корисними є рівні дозування порядку від приблизно 0,01мг/кг до приблизно 150мг/кг маси тіла на добу, або за альтернативним варіантом від приблизно 0,5мг до приблизно 10г на добу для одного пацієнта. Наприклад, діабет можна ефективно лікувати шляхом введення від приблизно 0,01мг до 100мг сполуки на кілограм маси тіла на добу або, за альтернативним варіантом, від приблизно 0,5мг до приблизно 7г на добу для одного пацієнта. Мається на увазі, однак, що конкретний рівень дозування для кожного конкретного пацієнта залежить від різноманітних чинників, в тому числі від віку, маси тіла, загального стану здоров'я, статі, режиму харчування, часу вживання, шляху введення, швидкості виділення, комбінації з іншими лікарськими засобами та тяжкості захворювання конкретного хворого на діабет, який підлягає лікуванню. Крім того, мається на увазі, що сполуки та солі за цим винаходом можуть вживатися профілактично у субтерапевтичних дозах у випадках очікування гіперглікемічного стану. Сполуки формули (І) можуть мати більш сприятливі властивості у порівнянні з відомими активаторами глюкокінази, як показують, наприклад, випробування, описані в цьому документі. Зокрема, сполуки за цим винаходом можуть виявляти сприятливіші значення Km, Vmax, EC50, максимальної активації (концентрація глюкози 5мМ) та/або максимального ступеня зниження глюкози до основного рівня глюкози в крові (наприклад, у мишей лінії C57BL/6J), або інші більш сприятливі фармакологічні властивості у порівнянні з відомими активаторами глюкокінази. Згідно із цим винаходом, сполуки формули (Іа) можна одержати за методикою, ілюстрованою нижченаведеною Схемою 1: Де V, R1, R2, m та відповідають вищенаведеним визначенням, та R11 – С1-4-алкіл. Альдегіди II та складні ефіри фенілоцтової кислоти III є наявними на ринку або можуть бути легко одержані з використанням відомих способів, карбаніон складного ефіру фенілоцтової кислоти III (R11=С1-4-алкіл), утворений при -78°С, наприклад, у тетрагідрофурані, дією сильної основи, наприклад, діізопропіламіду літію, можна конденсувати зі сполукою II, одержуючи , -ненасичений складний ефір (Т. Severin et al. Chem. Ber. 1985, 118, 4760-4773), який можна омилити використовуючи, наприклад, гідроксид натрію (W.L. Corbett et al., WO2001/44216), і одержати сполуку IV. В разі необхідності, будь-які функціональні групи в проміжних сполуках, наприклад, оксо- або гідроксильні групи у сполуках формули II, можуть бути захищені, а групи захисту відщеплені із застосуванням відомих способів. Наприклад, оксогрупи можуть бути захищені у формі кеталів, а гідроксильні групи — у формі простих ефірів, наприклад, метоксиметилових (MOM) простих ефірів. 21 90264 22 , -ненасичені карбонові кислоти IV можна конденсувати з 2-аміно-5-фтортіазолом V, або його сіллю, наприклад, гідрохлоридом, який можна одержати, як описано у прикладах, застосовуючи різноманітні умови сполучення, наприклад, карбодіімід-1-гідроксибензотриазол, прищеплений до полімеру, у N,N-диметилформаміді при 20°С (типові способи дивись http://www.argotech.com/PDF/resins/ps_carbodiimide .pdf та способи, розроблені Argonaut Technologies, Inc., Foster City, Каліфорнія), одержуючи сполуку (Іа). Згідно із цим винаходом сполуки формули (Іb) можуть бути виготовлені способом, показаним на нижченаведеній Схемі 2: де V, R1, R2 та m відповідають вищенаведеним визначенням, Y - CO2R12, де R12 - водень, С1-4алкіл або бензил; та X - хлор, бром, йод або OSO2R13, де R13 - С1-4-алкіл, факультативно заміщений одним або декількома атомами фтору, або факультативно заміщений арил. Галогеніди та складні ефіри сульфокислоти VI, а також феніл оцтові кислоти та складні ефіри VII є наявними на ринку або можуть бути легко одержані з використанням відомих способів, наприклад як описано у міжнародних патентних публікаціях № WO2000/058293, № WO2001/044216 та № WO2003/095438. Ці алкілувальні реагенти можна ввести в реакцію з діаніонами фенілоцтової кислоти VII, одержаними при -78°С у тетрагідрофурані з 2екв. сильної основи, такої як діізопропіламід літію, одержуючи сполуку VIII безпосередньо (F.T. Bizzarro et al., WO2000/58293). За альтернативним варіантом -карбаніон складного ефіру фенілоцтової кислоти VII, одержаний при -78°С у тетрагідрофурані дією сильної основи, такої як біс(триметилсиліл)амід літію (L. Snyder et al., J. Org. Chem. 1994, 59, 7033-7037), можна алкілувати сполукою VI, одержуючи -заміщені складні ефіри. Омиленням цих складних ефірів, із застосуванням, наприклад, гідроксиду натрію у водному розчині метанолу при температурі від 20°С до кипіння, одержують карбонові кислоти VIII. В разі необхідності, будь-які функціональні групи в проміжних сполуках, наприклад, оксо- або гідроксильні групи у сполуках формули VI, можуть бути захищені, а групи захисту відщеплені із застосуванням відомих способів. Наприклад, оксогрупи можуть бути захищені у формі кеталів, а гідроксильні групи - у формі простих ефірів, наприклад, метоксиметилових (MOM) простих ефірів. Карбонові кислоти VIII можна конденсувати з 2-аміно-5-фтортіазолом V або його сіллю, наприклад, гідрохлоридом, який можна одержати, як описано у прикладах, застосовуючи різноманітні умови сполучення, наприклад, карбодіімід-1гідроксибензотриазол, прищеплений до полімеру, у N,N-диметилформаміді при 20°С (типові методики дивись http://www.argotech.com/PDF/resins/ps_carbodiimide .pdf та методики, розроблені Argonaut Technologies, Inc., Foster City, Каліфорнія), одержуючи аміди (Ib). Сполука формули (Ib) має асиметричний атом вуглецю, який зв'язує карбонільний вуглець аміду, арил та -HC V-вмісний бічний ланцюг. Згідно із цим винаходом, перевага віддається стереохімічній конфігурації (R) при асиметричному центрі. При бажанні виділити чисті (R)- або (S)стереоізомери сполуки формули (Ib), можна розділити рацемічну суміш попередників хіральних карбонових кислот VIII будь-яким зручним хімічним способом, після чого конденсувати енантіомерно чисті карбонові кислоти з 2-аміно-5-фтортіазолом V або його сіллю, застосовуючи реагент, який викликає лише незначну рацемізацію. Як ілюстративний приклад, рацемічну сполуку VIII можна конденсувати із хіральним похідним оксазолідинону (дивись, наприклад, F.T. Bizzarro et al. WO2000/58293), одержуючи суміш діастереомерних імідів, яку можна розділити будь-яким відомим способом, наприклад, хроматографією на колонці. Шляхом гідролізу чистих імідів одержують стереохімічно чисті (R)- та (S)-карбонові кислоти, які потім можна конденсувати з 2-аміно-5-фтортіазолом V або його сіллю, застосовуючи реагент, який забезпечує мінімальну рацемізацію хірального центру, наприклад, гексафторфосфат бензотриазол-1-ілокситрис(піролідино)фосфонію (J. Coste et al. Tetrahedron Lett. 1990, 31, 205-208), одержуючи енантіомерно чисті (R)- або (S)-аміди формули (Ib). За альтернативним варіантом рацемічну суміш амідів формули (Ib) можна розділити за допомогою рідинної хроматографії високої ефективності, застосовуючи хіральну стаціонарну фазу, яку можна придбати, наприклад, у фірми Daicel Chemical Industries, Ltd, Токіо, Японія. Різноманітні функціональні групи, наявні у сполуках формули (І) та проміжних сполуках, за 23 стосовуваних при їх виготовленні, можуть бути одержані шляхом перетворення функціональних груп способами, відомими фахівцям в цій галузі. Наприклад, у сполуках формули VIII сульфонільні групи можуть бути одержані шляхом окиснення відповідної сульфанільної групи, із застосуванням, наприклад, mСРВА. Інші подробиці одержання сполук формули (І) описані у прикладах. Сполуки формули (І) можна одержати поодинці або у формі серій сполук, які охоплюють щонайменше 2, наприклад, від 5 до 1000, сполук та за варіантом, якому віддається більша перевага, від 10 до 100 сполук формули (І). Серії сполук можуть бути виготовлені із застосуванням комбінаторного принципу "розщеплення та змішування" або шляхом множинних паралельних синтезів із застосуванням рідкофазового або твердофазового синтезу, з використаням методик, відомих фахівцям в цій галузі. Під час синтезу сполуки формули (І), лабільні функціональні групи проміжних сполук, наприклад, гідроксильні, оксо-, карбоксильні та аміногрупи, можуть бути захищені. Групи захисту можуть бути видалені на будь-якій стадії синтезу сполуки формули (І) або можуть бути присутні у кінцевій сполуці формули (І). Детальний розгляд можливих шляхів захисту різних лабільних функціональних груп та способів розщеплення одержаних захищених похідних дано, наприклад, у Protective Groups in Organic Chemistry, T.W. Greene and P.G.M. Wuts, nd (1991) Wiley-Interscience, New York, 2 edition. Будь-які нові проміжні сполуки, які відповідають вищенаведеним визначенням, також охоплюються обсягом цього винаходу. Отже, цей винахід також пропонує: a) сполуку формули IV, яка відповідає вищенаведеному визначенню, де R1 - SO2R3 або SO2NR4R5; R2 - водень; 3 R - С1-3-алкільна група, С3-7-циклоалкільна група або 4-6-членна гетероциклічна група; R4 та R5 незалежно один від одного - водень або С1-4-алкіл, за умови, що R4 та R5 не є одночасно атомами водню; m - 0; та означає, що подвійний зв'язок має (Е)конфігурацію; та b) сполуку формули VIII, яка відповідає вищенаведеному визначенню, де R1 - SO2R3 або SO2NR4R5; R2 - водень; R3 – С3-7-циклоалкільна група або 4-6-членна гетероциклічна група; R4 та R5 незалежно один від одного - водень або С1-4-алкіл, за умови, що R4 та R5 не є одночасно атомами водню; та m-0. Усі публікації, в тому числі (але не тільки) патенти та заявки на патенти, на які в цьому документі дано посилання, включено до цього документу шляхом посилання, так, як би щодо кожної окремої публікації була дана вказівка про її включення шляхом посилання у повному обсязі. Матеріали та способи 90264 24 Хроматографія на колонці, якщо не вказано інше, виконувалася на SiO2 (40-63 меш - 0,250,40мм). Дані LCMS (рідинна хроматографія з масспектроскопічним детектуванням) можуть бути одержані із застосуванням одного з двох способів: Методика А: колонка Waters Symmetry 3,5мкм C18 (2,1 30,0мм, швидкість потоку = 0,8мл/хв), елюювання розчином (5% MeCN в H2O)-MeCN, який містить 0,1% НСО2Н, протягом 6хв та УФ детектування на довжині хвилі 220нм. Дані про градієнт: 0,0-1,2хв: 100% (5% MeCN в Н2О); 1,2-3,8хв: лінійний градієнт до 10% (5% MeCN в Н2О)-90% MeCN; 3,8-4,4хв: ізократичне елюювання 10% (5% MeCN в Н2О)-90% MeCN; 4,4-5,5хв: лінійний градієнт до 100% MeCN; 5,5-6,0хв: повернення до 100% (5% MeCN в Н2О). Методика В: колонка Phenomenex Mercury Luna 3мкм Qg (2,0 10,0мм, швидкість потоку = 1,5мл/хв), елюювання розчином (5% MeCN в Н2О)-MeCN (градієнт від 4:1 до 1:4), який містить 0,1% НСО2Н, протягом 2,95хв, детектування за допомогою діодної лінійки. Мас-спектри для обох методик А та В можуть бути одержані із застосуванням джерела іонізації електророзпиленням в режимі позитивних (ES+) або негативних (ES-) іонів. Спектри з хімічною іонізацією під атмосферним тиском (АРСІ) можна одержати на приладі FinniganMat SSQ 7000C. Раніше були описані синтези таких сполук: 7(S)-йодмєтил-2(S), 3(S)-дифеніл-1,4діоксаспіро[4,4]нонан: WO2003/095438. Абревіатури та акроніми: Ас: ацетил; АТР: аденозин-5'-трифосфат; n-Вu: н-бутил; DMF: N,Nдиметилформамід; DMPU: 1,3-диметил-3,4,5,6тетрагідро-2(1H)-піримідинон; DMSO: диметилсульфоксид; EDCI: гідрохлорид 1-(3диметиламінопропіл)-3-етилкарбодііміду; Et: етил; FA: активація згортання; GK: глкжокіназа; Glc: глюкоза; G6P: глюкоза-6-фосфат; G6PDH: глюкоза-6фосфатдегідрогеназа; GST-GK: складний білок глутатіон-5-трансфераза-глюкокіназа; ІН: ізогексан; LHMDS: біс(триметилсиліл)амід літію; Me: метил; NADP(H): нікотинамідаденівдинуклеотидфосфат (відновлений); NBS: N-бромсукцинімід; Ph: феніл; к.т.: кімнатна температура; RT: час затримання; TFAA: трифтороцтовий ангідрид; THF: тетрагідрофуран. Підготовчий синтез 1: гідрохлорид 5фтортіазол-2-іламіну NEt3 (63,4мл, 455ммоль) додавали при перемішуванні до суспензії гідроброміду 5-бромтіазол2-іламіну (102,7г, 379ммоль) у СН2СІ2 (1,5л). Через 1год додавали краплями TFAA (64,2мл, 455ммоль) при 0°С протягом 15хв. Суміші дозволяли нагрітися до 20°С протягом 1 год, після чого перемішували протягом ще 2 год. Додавали Н2О (600мл), та відділяли одержаний осад. Водний шар фільтрату відділяли та екстрагували СНСІ3 (3 300мл). Об'єднані органічні екстракти промивали розсолом, сушили (Na2SO4), фільтрували та концентрували. Відділений осад та залишкову тверду речовину об'єднували та розтирали з ЕtOAc-н-С6Н14, одержуючи N-(5-бромтіазол-2-іл)-2,2,2 25 трифторацетамід: Н (CDCl3): 7,45 (1Н, s), 13,05 (1Н, br). Додавали краплями n-BuLi (253мл 1,58М розчину у гексані, 403ммоль) протягом 50хв при перемішуванні до розчину вищезгаданого аміду (50,0г, 183ммоль) у безводному THF (1,3л) при 78°С. Через 1,5год додавали краплями розчин TVфторбензолсульфоніміду (86,0г, 275ммоль) у безводному THF (250мл) протягом 30хв. Суміш перемішували протягом 3 год, після чого нагрівали до 30°С. Додавали Н2О (300мл), та суміш фільтрували через шар целіту. Тверду речовину відділяли, та целіт промивали Et2O (400мл) та Н2О (400мл). Органічний шар фільтрату відділяли та екстрагували водою (2 400мл). Об'єднані водні шари промивали Et2O (400мл), після чого підкислювали 2М розчином НСl до рН 6,5 та екстрагували EtOAc (2 400мл). Об'єднані органічні екстракти промивали водою (2 400мл) та розсолом, після чого сушили (MgSO4), фільтрували, та концентрували. Після хроматографії на колонці (ЕtOАс-n-С6Н14, градієнт від 1:3 до 1:2) одержали N-(5-фтортіазол-2-іл)2,2,2-трифторацетамід: H (CDCI3): 7,13 (1Н, d). Додавали краплями АсСІ (12,6мл, 175ммоль) при перемішуванні до розчину цього аміду (15,7г, 73ммоль) у МеОН (300мл) при 0°С. Суміш перемішували при 20°С протягом 30хв., нагрівали зі зворотним холодильником протягом 1год, після чого концентрували у вакуумі. Залишкову тверду речовину розтирали з THF, одержуючи вказану в заголовку сполуку: H (D2O):7,00 (1H, d). Вільну основу вказаної в заголовку сполуки одержували шляхом суспендування гідрохлориду в діетиловому ефірі, промивання насиченим водним розчином NaHCO3, сушіння ефірного шару та випарювання, одержуючи вільну основу, яку одразу ж використовували. Підготовчий синтез 2: Етил-(4метансульфонілфеніл)ацетат SOCl2 (8,2мл, 112,0ммоль) додавали при перемішуванні до суспензії (4метансульфонілфеніл)оцтової кислоти (20,00г, 93,3ммоль) у EtOH (80мл) при -10°С. Одержаній суміші дозволяли нагрітися до 20°С протягом 16 год, після чого розчинники видаляли під зниженим тиском. Залишок розчиняли у EtOAc, після чого одержаний розчин промивали Н2О, доки водна фаза не ставала нейтральною. EtOAc розчин промивали додатковою кількістю насиченого водного розчину N2СО3, після чого сушили (MgSO4). Після фільтрування та випарювання розчинника одержали вказану в заголовку сполуку: m/z(ES+)=284,1 [M+MeCN+H]+. Підготовчі синтези 3-14: 2(R)-2-(3-хлор-4метансульфонілфеніл)-3-((R)-3оксоциклопентил)пропіонову кислоту, 2(R)-2-(3хлор-4-метансульфоніл-феніл)-3-(4оксоциклогексил)пропіонову кислоту та 2(R)-2-(3хлор-4-метан-сульфонілфеніл)-3-(3гідроксициклопентил)пропіонову кислоту можна одержати, як описано у WO2003/095438. Проміжні продукти карбонової кислоти формули VIII, необ 90264 26 хідні для синтезу сполук Прикладів 7-15, можуть бути одержані за певною загальною методикою, яка включає алкілування відповідного складного ефіру сполукою 4-йодметил-НСУ з подальшим гідролізом цього продукту. Проміжну карбонову кислоту формули VIII, необхідну для синтезу сполуки Прикладу 7, одержували, як описано нижче: Підготовчий синтез 6а: (4циклопропілсульфанілфеніл)оксооцтова кислота 2М водний розчин NaOH (163мл) додавали до розчину етил-(4циклопропілсульфанілфеніл)оксоацетату (40,62г, 162,5ммоль) у EtOH (200мл), та суміш при перемішуванні нагрівали при 60°С протягом 2год. Після охолодження суміш концентрували до об'єму 150мл та промивали діетиловим ефіром (2 100мл). Потім додавали концентровану НСl в кількості, достатній для досягнення рН 1, та одержаний осад екстрагували EtOAc (2 300мл). Об'єднані органічні фази промивали водою (3 100мл), розсолом (200мл) та сушили (MgSO4). Після видалення розчинника одержали вказану в заголовку сполуку: m/z (ES-)=221,0 [M-H+]-. Підготовчий синтез 6b: (4циклопропілсульфанілфеніл)оцтова кислота Гідразингідрат (14,19г, 283,5ммоль) охолоджували до -50°С, та додавали однією порцією (4циклопропілсульфанілфеніл)оксооцтову кислоту (Підготовчий синтез 6а, 12,6г, 56,7ммоль). Одержану суспензію при інтенсивному перемішуванні нагрівали спочатку до кімнатної температури, а потім при 80°С протягом 5хв. Додавали твердий КОН (8,76г, 156,5ммоль) чотирма рівними частинами, та одержаний розчин нагрівали при 100°С протягом 20год. Після охолодження до кімнатної температури додавали воду (25мл), та водну фазу промивали Et2O (20мл). Ефірну фазу промивали водою (2 5мл), та додавали до об'єднаних водних фаз достатню кількість НСl до досягнення рН 1. Потім одержаний осад екстрагували у EtOAc (2 300мл), та об'єднані органічні фази промивали водою (3 100мл), розсолом (200мл), після чого сушили (MgSO4). Після випарювання розчинника одержали вказану в заголовку сполуку: m/z (ES)=207,1 [M-H+]Підготовчий синтез 6с: 2-(4циклопропілсульфанілфеніл)-N-(2(R)-гідрокси1(R)-метил-2-фенілетил)-N-метилацетамід Безводний ацетон (148мл) додавали до (4циклопропілсульфанілфеніл)-оцтової кислоти (Підготовчий синтез 6b, 16,41г, 78,8ммоль) та К2СО3 27 (32,67г, 236,4ммоль) до утворення суспензії, яку охолоджували до -10°С при перемішуванні. Додавали краплями нерозведений триметилацетилхлорид (10,2мл, 82,74ммоль), підтримуючи протягом додавання температуру не вище -10°С. Реакційну суміш перемішували при -10°С протягом 20хв., нагрівали до 0°С протягом 20хв., після чого охолоджували до -15°С, та додавали однією порцією твердий (1(R),2(R))-(-)-псевдоефедрин (19,53г, 118,2ммоль). Через 10хв. реакційну суміш доводили до кімнатної температури, після чого продовжували перемішування протягом 1,5год. Додавали воду (100мл), та суміш екстрагували EtOAc (500мл). Органічну фазу промивали водою (2 100мл), та об'єднані водні шари піддавали зворотному екстрагуванню EtOAc (2 250мл). Потім об'єднані органічні шари промивали розсолом (100мл), та сушили (MgSO4. Розчинник видаляли, та одержаний твердий жовтий залишок перекристалізовували з EtOAc-IH, одержуючи вказану в заголовку сполуку: m/z (ES+)=356,1 [M+H]+. Підготовчий синтез 6d: 2(R)-(4циклопропілсульфанілфеніл)-3(3(R)оксоциклопентил)пропіонова кислота LHMDS (162мл 1М розчину у THF, 162ммоль) розводили безводним THF (161мл) та охолоджували до -20°С при перемішуванні. Розчин 2-(4циклопропілсульфанілфеніл)-N-(2(R)-гідрокси-1R)метил-2-фенілетил)-N-метилацетаміду (Підготовчий синтез 6с, 30г, 84,4ммоль) у безводному THF (245мл) додавали через канюлю протягом 10хв., підтримуючи протягом додавання температуру нижче -15°С. Реакційній суміші дозволяли нагрітися до -7°С протягом 30хв., після чого охолоджували до -12°С, та додавали розчин 7(S)-йодметил2(S), 3(R)-дифеніл-1,4-діоксаспіро[4,4]нонану (27г, 64,2ммоль) у суміші безводного THF (111 мл) та DMPU (18,9 мл) через канюлю протягом 10хв., підтримуючи протягом додання температуру нижче -7°С. Реакційну суміш нагрівали до 2°С та перемішували протягом 4,5год., після чого виливали у суміш толуолу (770мл) та 20% водного розчину NH4CI (550мл). Після інтенсивного перемішування органічний шар відділяли та промивали 20% водним розчином NH4Cl (550мл) та розсолом (100мл). Водні фази об'єднували та екстрагували EtOAc (500мл), який, після відділення, промивали розсолом (100мл). Об'єднані органічні фази сушили (MgSO4, фільтрували, випарювали, та одержане масло очищали флеш-хроматографією (IH-EtOAc, ступінчастий градієнт від 9:1 до 1:1,), одержуючи 2(R)-(4-циклопропілсульфанілфеніл)-3-(2(S), 3(S)дифеніл-1,4-діоксаспіро[4,4]нон-7(R)-іл)-N-(2(R)гідрокси-1(R)-метил-2-фенілетил)-Nметилпропіонамід: m/z (ES+)=648,3 [М+Н]+. Розчин цього аміду (30,7г, 47,38ммоль) у 1,4-діоксані (62мл) при перемішуванні розводили 4,5М водним розчином H2SO4 (61,5мл), та одержану суміш ви 90264 28 тримували при спокійному кипінні зі зворотним холодильником протягом 18год. Після охолодження на льоді, додавали воду (162мл), та суміш екстрагували ЕЮ Ас (250мл). Водний шар відділяли та екстрагували додатковою кількістю EtOAc (2 150мл), та об'єднані органічні фази промивали водою (3 200мл), до гарантованого нейтрального рН кінцевої промивної води, та розсолом (100мл). Після висушування (MgSO4) та фільтрування розчинник видаляли, та залишок очищали флешхроматографією (СН2СІ2, після чого CH2Cl2-THF, змінювання від 5:1 до 3:1), одержуючи вказану в заголовку сполуку: m/z (ES+)=305,1 [M+H]+. Підготовчий синтез 6е: 2(R)-(4циклопропансульфонілфеніл)-3(3(R)оксоциклопентил)пропіонова кислота Розчин 2(R) - (4-циклопропілсульфанілфеніл)3-(3(R)оксоциклопентил)-пропіонової кислоти (Підготовчий синтез 6d, 5,0г, 16,43ммоль) у СН2Сl2 (250мл) при перемішуванні охолоджували до 1°С на льоді, та додавали порціями 70% mСРВА (8,099г, 32,85ммоль), підтримуючи температуру нижче 3°С. Через 6 год розчинник видаляли, та залишок очищали флеш-хроматографією (1% АсОН у СН2Сl2, після чого THF), одержуючи вказану в заголовку сполуку: m/z (ES+)=337,1 [M+H]+. Підготовчі синтези 15-17: Проміжні продукти формули IV, необхідні для синтезу сполук Прикладів 4-6 можуть бути одержані за описаними нижче загальними методиками. Якщо необхідно, будь-які функціональні групи в проміжних сполуках, наприклад оксо- або гідроксигрупи у сполуках формули II, можуть бути захищені, а групи захисту відщеплені із застосуванням відомих способів: Методика A: LDA (24мл 1,8M розчину в hC7H16-THF-PhEt, 43,3ммоль) додають краплями при перемішуванні до розчину DMPU (19мл, 153,0ммоль) у безводному THF (100мл) при -78°С. Через 30хв. додають краплями розчин відповідного складного ефіру фенілоцтової кислоти III (20,6ммоль) у безводному THF (42мл). Суміш перемішують протягом ще 1год., після чого додають краплями розчин альдегіду II або його захищеного похідного (20,6ммоль) у безводному THF (25мл). Дозволяють суміші нагрітися до 20°С протягом 16год., після чого реакцію гасять насиченим водним розчином NH4CI (210мл). THF видаляють під зниженим тиском, після чого залишок екстрагують EtOAc (3 250мл). Об'єднані екстракти EtOAc сушать (MgSO4), фільтрують, та концентрують. Після хроматографії на колонці одержують складний ефір - етилакрилат. Цей складний ефір омилюють, наприклад, шляхом нагрівання розчину цього складного ефіру (19,1ммоль) у МеОН (30мл) та 1М розчині NaOH (40мл, 40,0ммоль) зі зворотним холодильником протягом 1год. Після охолодження 29 суміш промивають EtOAc. Водну фазу підкислюють 1М розчином НСl, після чого екстрагують EtOAc. Об'єднані органічні екстракти сушать (MgSO4). Після фільтрування та випарювання розчинника одержують бажану (E)-акрилову кислоту. Методика В: До розчину складного ефіру фенілоцтової кислоти III (3,16 ммоль) та альдегіду II або його захищеного похідного (3,47 ммоль) у безводному DMSO (3мл) додають краплями NaOEt (0,63мл 0,5М розчину в EtOH, 0,32ммоль) при перемішуванні. Суміш нагрівають при 80°С протягом 16год., після чого обробляють АсОН до досягнен 90264 30 ня рН 7. Додають EtOAc (30мл), потім розчин промивають водою (2 10мл) та розсолом (10мл), після чого сушать (MgSO4). Після фільтрування, випарювання розчинника та хроматографії на колонці одержують складний ефір - етилакрилат. Цей складний ефір омилюють, як описано вище у Методиці А, одержуючи бажану (E)-акрилову кислоту. Перелічені нижче сполуки можуть бути виготовлені із застосуванням загальних методик, описаних нижче: 31 Методика С: До розчину РРh3 (3,53г, 13,4ммоль) у СН2СІ2 (70мл) при перемішуванні додають NBS (882мг, 10,6ммоль) при 0°С. Через 10хв додають відповідну сполуку формули IV або VIII (9,0ммоль), після чого суміш перемішують при 0°С протягом 20хв., а потім при 20°С протягом 90264 32 30хв. Додають гідрохлорид 5-фтортіазол-2-іламіну (933мг, 9,3ммоль) та піридин (2,2мл, 18,8ммоль) при 0°С, після чого суміш перемішують при 20°С протягом 20год. Після випарювання розчинника залишок розподіляють між 5% водним розчином лимонної кислоти (100мл) та EtOAc (500мл). Вод 33 ний шар додатково екстрагують ЕtOАс (200мл), після чого об'єднані органічні шари промивають Н2О та розсолом, а потім сушать (Na2SO4), фільтрують, та концентрують у вакуумі. Після очищення залишку хроматографією (СНСl3-МеОН, 99:1) на колонці Chromatorex® NH-DM1020 (Fuji Silysia Chemical, Ltd., Aichi-ken, Японія; дивись також http://www.fuji-sirysia.co.jp/e-fl 100dx.htm) одержують бажану сполуку. Методика D: EDCI (80мг, 420мкмоль) та HOBt (56мг, 420мкмоль) додають при перемішуванні до розчину відповідної сполуки формули IV або VIII (320мкмоль) у безводному DMF (6мл). Через 15хв. розчин обробляють гідрохлоридом 5-фтортіазол-2іламіну (38 мг, 380 мкмоль) та піридином (61мкл, 760мкмоль). Суміш перемішують при 20°С протягом 16 год, після чого концентрують під зниженим тиском. Залишок розподіляють між СН2Сl2 та насиченим водним розчином Na2CO3. Органічний шар промивають 1М розчином НСl та сушать (MgSO4). Після фільтрування та випарювання розчинника одержують бажану сполуку, яку, якщо була одержана рацемічна суміш, можна виділити РХВЕ на хіральній стаціонарній фазі. Методика: CHIRAL CEL OJ® (Daicel Chemical Industries, Ltd., Токіо, Японія), 10см 25см, МеОН (100%), 189мл/хв, УФ 285нм, 25°С. Методика Е: Оксалілхлорид (0,23мл, 0,47ммоль) додають при перемішуванні до розчину прийнятної сполуки формули IV або VIII (0,42ммоль) у безводному СН2СІ2 (6мл) при 0°С. Додають безводний DMF (50мкл), після чого суміш перемішують при 0°С протягом 2год. Додають 5фтортіазол-2-іламін (151мг, 1,28ммоль; одержаний шляхом розподілення гідрохлориду між Et2O та насиченим водним розчином Na2CO3, відділення шару Et2O, сушіння (MgSO4), та випарювання розчинника) та піридин (69 мкл, 0,85ммоль), після чого суміш перемішують при 0-5°С протягом 16год., а потім дозволяють нагрітися до 20°С та розводять ЕtOАс (45мл). Розчин промивають 1М розчином НСl (2 20мл) та насиченим водним розчином Na2CO3 (2 20мл), після чого сушать (MgSO4), фільтрують, та концентрують. Після хроматографічного очищення одержують бажану сполуку. Сполуку Прикладу 7, 2(R)-2-(4циклопропансульфонілфеніл)-N-(5-фтортіазол-2іл)-3-((R)-3-оксоциклопентил)пропіонамід, одержували, як описано нижче. Розчин 2(R)-(4-циклопропансульфонілфеніл)3-3(R)оксоциклопентил)-пропіонової кислоти (Підготовчий синтез 6е, 893мг, 2,65ммоль) у безводному СН2СІ2 (38мл) охолоджували до 0°С, та додавали краплями розчин оксалілхлориду (0,408г, 3,21ммоль) у безводному СН2СІ2 (2мл), підтримуючи протягом додавання температуру на рівні 0°С. Додавали безводний DMF (0,08мл), та реакційну суміш перемішували 2,5год. Повільно додавали розчин 2-аміно-5-фтортіазолу (Підготовчий синтез 1, 345мг, 2,92ммоль) у безводному СН2СІ2 (6мл), а потім піридин (0,53мл, 5,31ммоль), та перемішували суміш при 0°С протягом 2год., після чого при кімнатній температурі протягом ночі. 90264 34 Розчин розводили СН2СІ2 (150мл), та промивали 5% (маса/об'єм) водним розчином лимонної кислоти (2 30мл), насиченим водним розчином NaHCO3 (2 30мл), водою (50мл) та розсолом (50мл). Органічну фазу сушили (MgSO4), випарювали, залишок очищали флеш-хроматографією (IH-EtOAc, 3:2), та одержували вказану в заголовку сполуку: RT=3,47хв.; m/z (ES+)=437,1 [М+Н]+. ВИПРОБУВАННЯ Активність глюкокінази in vitro Застосовуючи методику, аналогічну описаній у WO2000/58293, активність глюкокінази можна випробувати шляхом поєднання продукування G6P під впливом GST-GK з генеруванням NADPH із застосуванням G6PDH як приєднувального ензиму. Випробування активності глюкокінази виконують при 30°С у випробувальному 96-лунковому планшеті фірми Costar при кінцевому інкубаційному об'ємі 100мкл. Випробувальний буфер містить: 25мМ буфер Hepes (рН 7,4), 12,5мМ КСl, 5мМ DGlc, 5мМ АТР, 6,25мМ NADP, 25мМ MgCl2, 1мМ дитіотреїзол, випробовувану сполуку або 5% DMSO, 3,0од/мл G6PDH та 0,4мкл/мл GST-GK одержаної з людської печінки глюкокінази. ATP, G6PDH та NADP можуть бути придбані у фірми Roche Diagnostics. Інші реагенти мають ступінь чистоти >98% та можуть бути придбані у фірми Kanto Chemicals. Випробовувані сполуки розчиняють у DMSO, після чого додають до випробувального буфера без АТР. Цю суміш попередньо інкубують у камері з регулюванням температури спектрофотометра SPECTRAmax 250 (Molecular Devices Corporation, Sunnyvale, CA) протягом 10хв, після чого ініціюють реакцію шляхом додання 10 мкл розчину АТР. Після ініціювання реакції безперервно контролюють зростання оптичної густини (OD) на довжингі хвилі 340нм протягом 10хв. інкубаційного періоду як кількісну характеристику активності глюкокінази. Додають GST-GK у кількості, достатній для підвищення OD340 на протязі 10хв. інкубаційного періоду у лунках, які містять 5% DMSO, але не містять випробовуваної сполуки. При попередніх експериментах з'ясовано, що реакція глюкокінази на протязі цього періоду часу є лінійною, навіть у присутності активаторів, які спричиняють 8-разове підвищення активності глюкокінази. Активність глюкокінази у контрольних лунках порівнюють з активністю у лунках, які містять випробовувані активатори глюкокінази. Обчислюють концентрації сполук, які спричиняють 50% зростання активності глюкокінази (тобто FA1,5). FA1,5 досягається при концентрації активаторів глюкокінази
ДивитисяДодаткова інформація
Назва патенту англійськоюTri(cyclo) substituted amide compounds, pharmaceutical composition, methods for the treatment and prophylactic, process for the preparation of compound
Автори англійськоюFYFE, Matthew
Назва патенту російськоюТри(цикло)замещенные амиды, фармацевтическая композиция, способы лечения и профилактики, способ получения соединения
Автори російськоюФайф Меттью
МПК / Мітки
МПК: C07D 277/46, A61P 3/10, A61K 31/427
Мітки: профілактики, аміди, спосіб, одержання, композиція, способи, лікування, три(цикло)заміщені, фармацевтична, сполуки
Код посилання
<a href="https://ua.patents.su/18-90264-triciklozamishheni-amidi-farmacevtichna-kompoziciya-sposobi-likuvannya-ta-profilaktiki-sposib-oderzhannya-spoluki.html" target="_blank" rel="follow" title="База патентів України">Три(цикло)заміщені аміди, фармацевтична композиція, способи лікування та профілактики, спосіб одержання сполуки</a>
Попередній патент: Композиція, що містить молекулярно диспергований дроспіренон
Наступний патент: Дельта-кристалічна форма гідрохлориду івабрадину, спосіб її одержання і фармацевтична композиція, яка її містить
Випадковий патент: Фармацевтична композиція, яка об'єднує піперидиноалканол з протинабряковим агентом












