Кристалічна форма сполуки трициклічного бензопірану і спосіб її отримання (варіанти)
Номер патенту: 105385
Опубліковано: 12.05.2014
Автори: Такада Ясутака, Камон Міяко, Кавахара Сіро, Умеда Ясухіро
Формула / Реферат
1. Кристалічна форма А (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу Формули (1):
 , (1)
, (1)
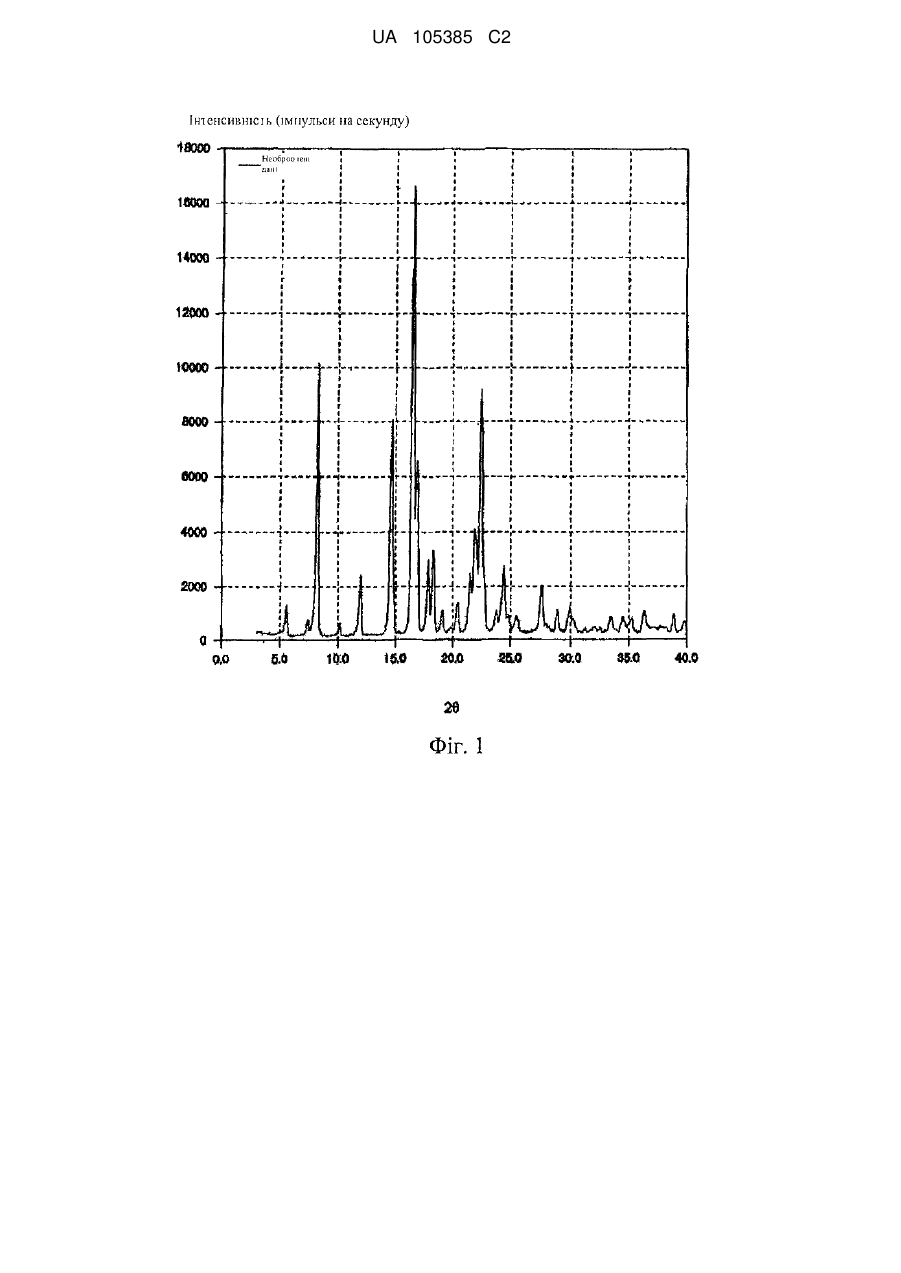
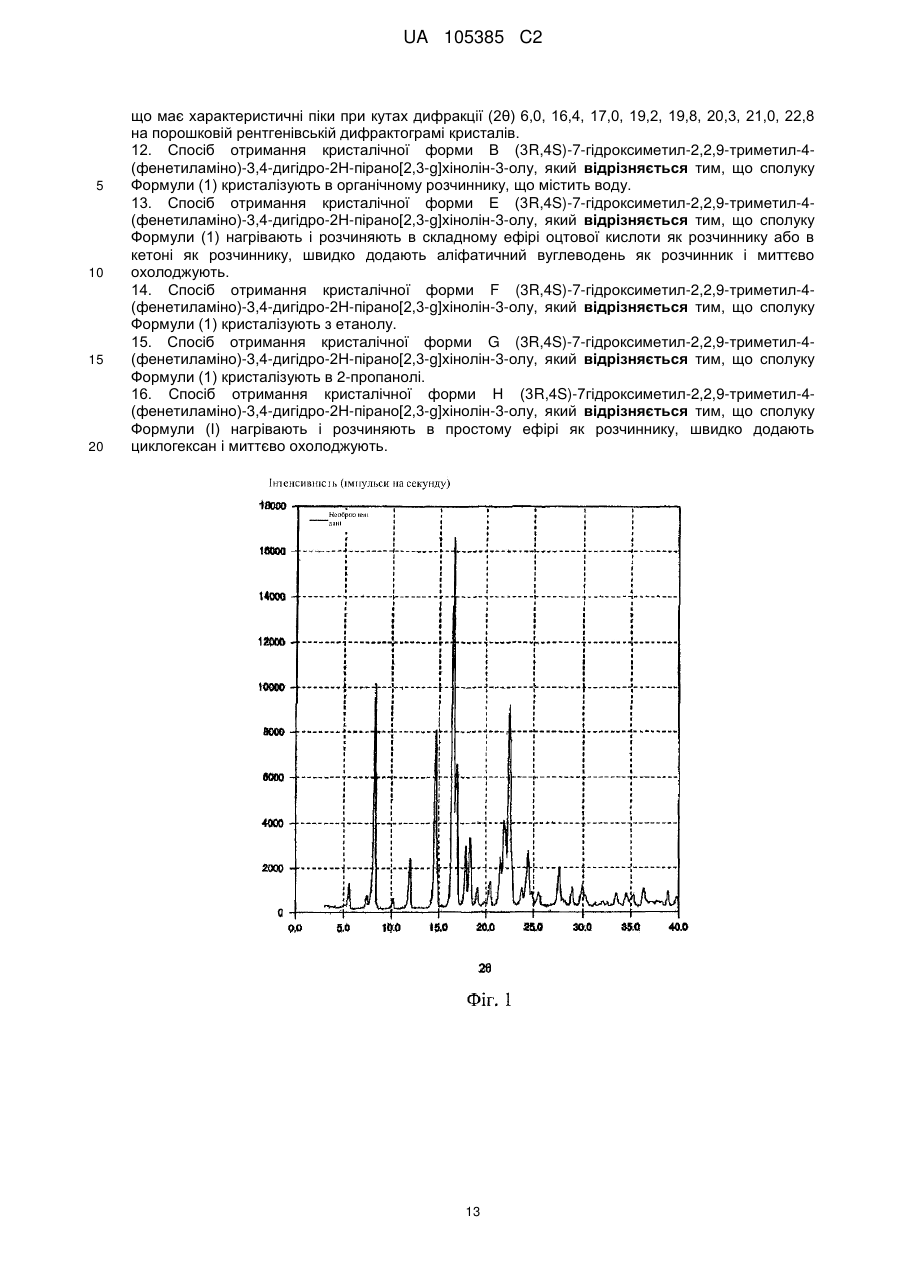
що має характеристичні піки при кутах дифракції (2θ) 5,6, 8,2, 12,0, 14,7, 16,6, 16,9, 17,9, 18,4, 22,5, 24,5, 27,6 на порошковій рентгенівській дифрактограмі кристалів.
2. Спосіб отримання кристалічної форми А (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (1) кристалізують в складному ефірі як розчиннику.
3. Спосіб отримання кристалічної форми А (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (1) кристалізують в аліфатичному вуглеводні як розчиннику.
4. Спосіб отримання кристалічної форми А (3R,4S)-7-гідроксиметил-2,2,9-тpимeтил-4-(фeнeтилaмiнo)-3,4-дигiдpo-2H-пірано[2,3-g]хінолін-3-oлy, який відрізняється тим, що сполуку Формули (1) кристалізують в нітрилі як розчиннику.
5. Спосіб отримання кристалічної форми А (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (1) кристалізують в ароматичному вуглеводні як розчиннику.
6. Спосіб отримання кристалічної форми А (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (1) кристалізують в кетоні як розчиннику.
7. Кристалічна форма В (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу Формули (1):
 , (1)
, (1)
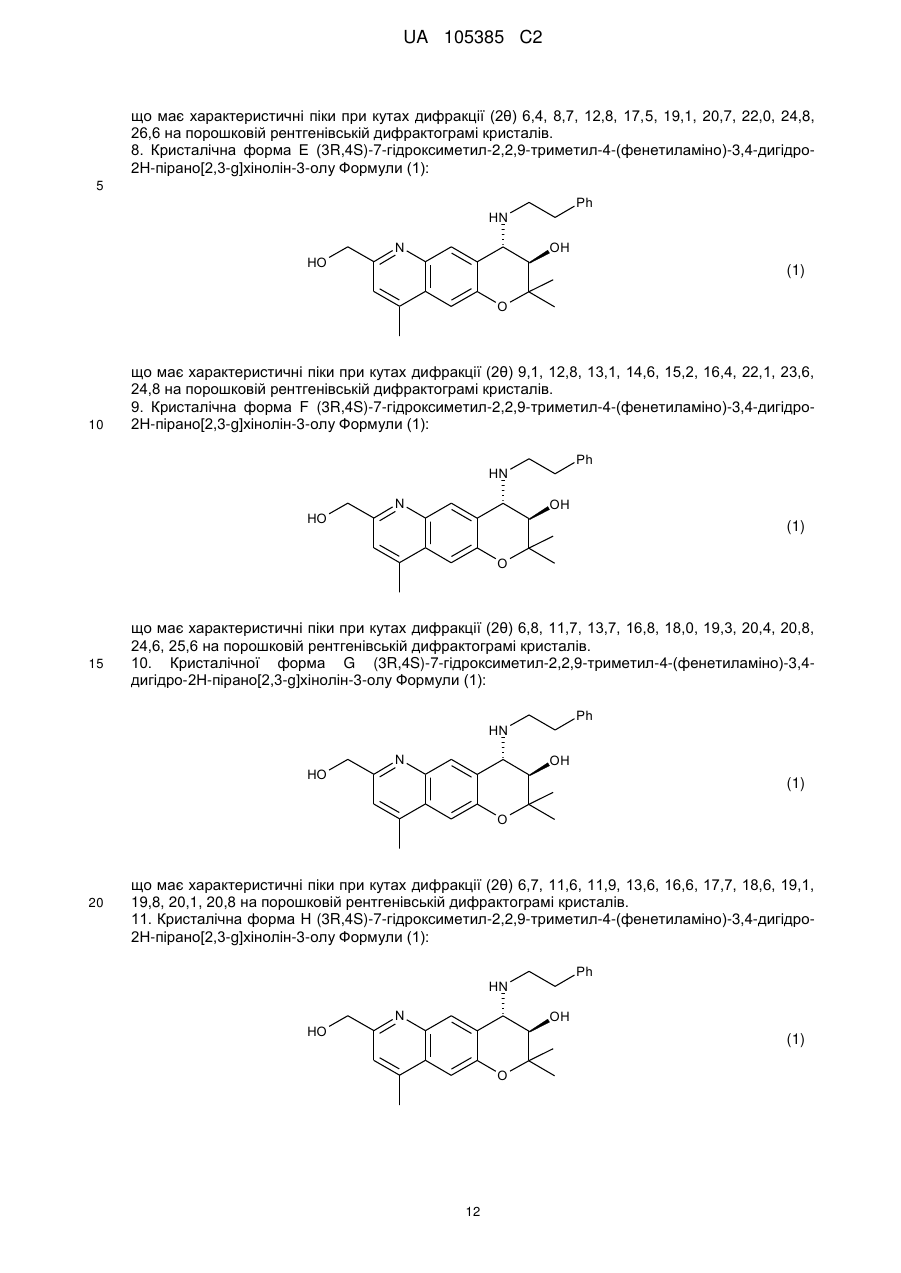
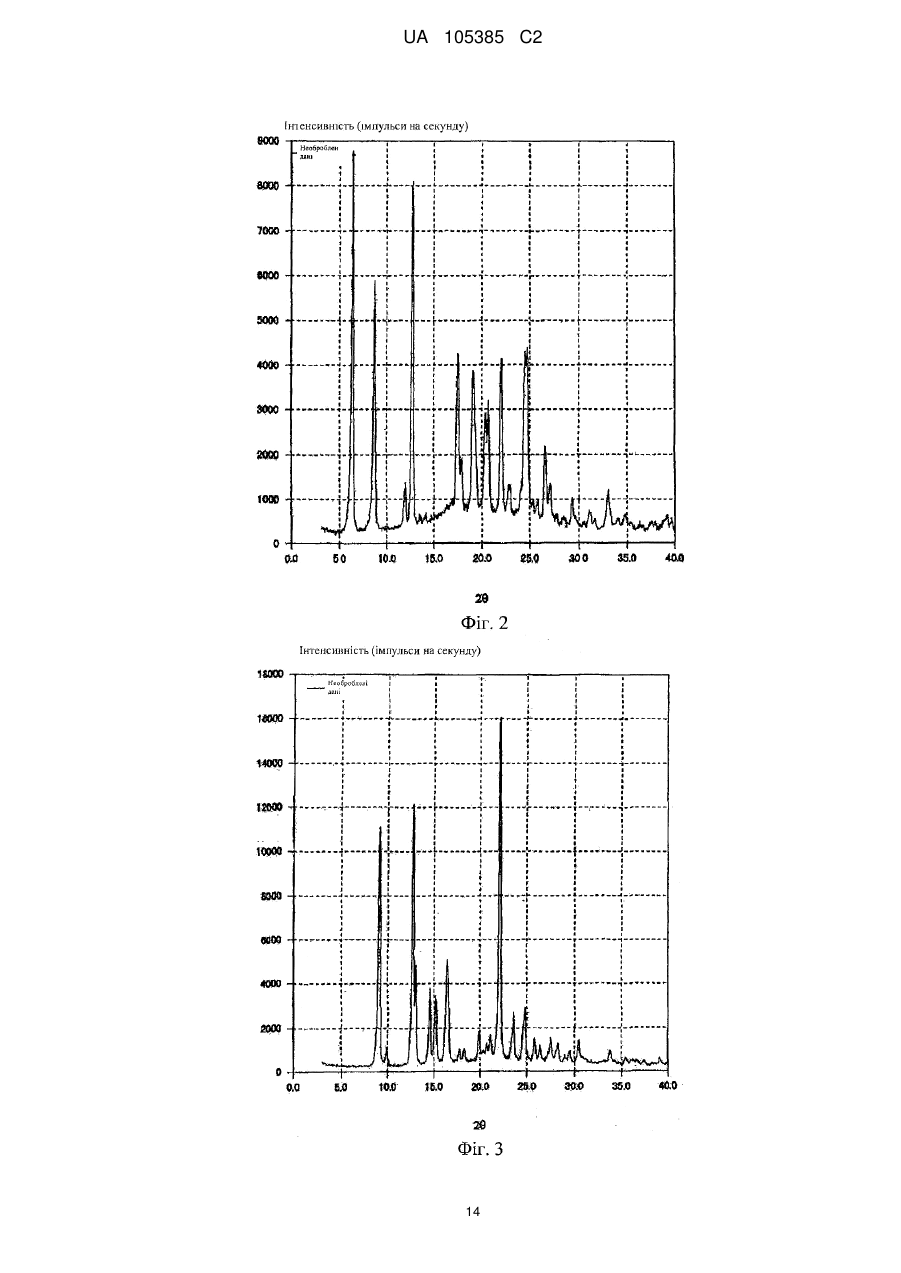
що має характеристичні піки при кутах дифракції (2θ) 6,4, 8,7, 12,8, 17,5, 19,1, 20,7, 22,0, 24,8, 26,6 на порошковій рентгенівській дифрактограмі кристалів.
8. Кристалічна форма Е (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу Формули (1):
 , (1)
, (1)
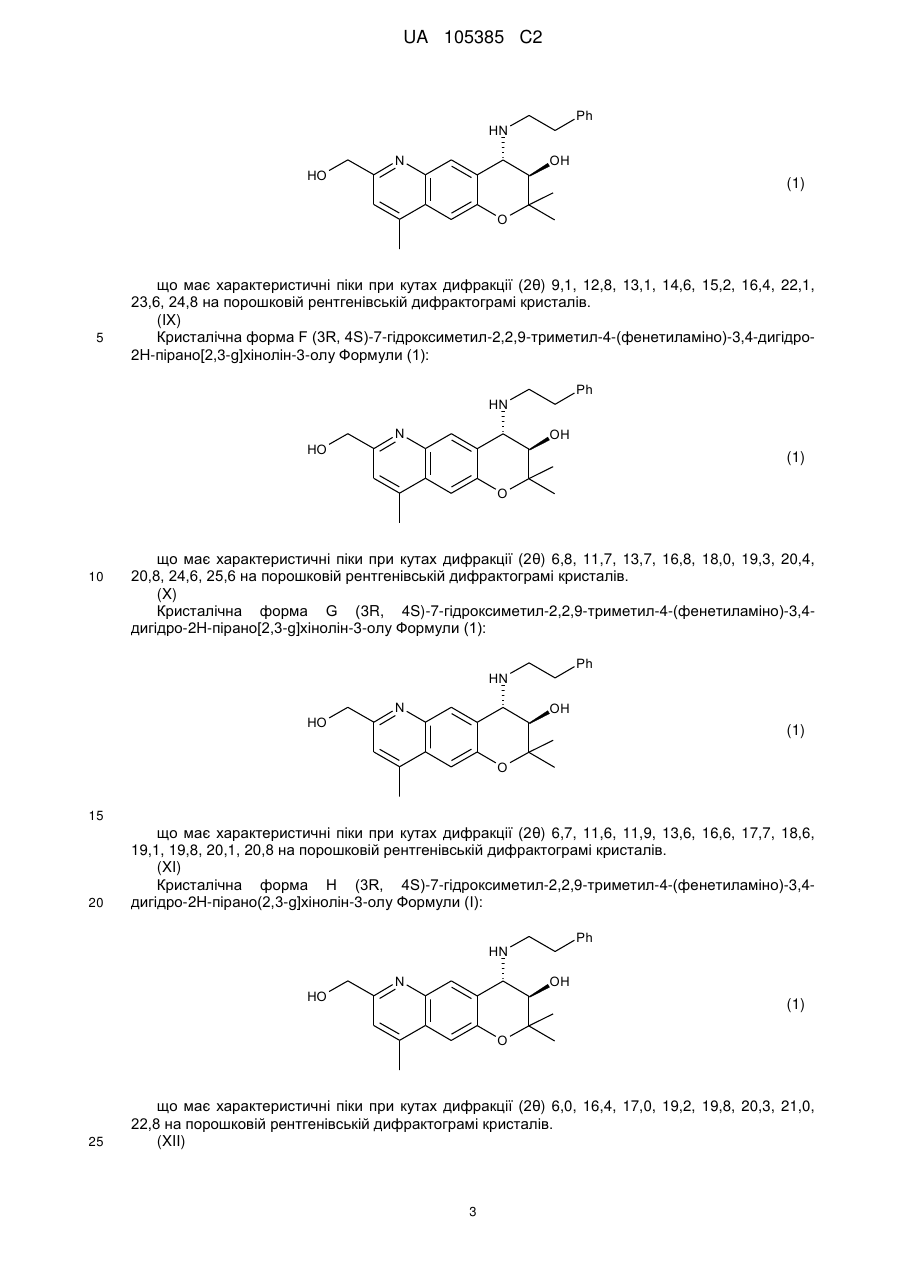
що має характеристичні піки при кутах дифракції (2θ) 9,1, 12,8, 13,1, 14,6, 15,2, 16,4, 22,1, 23,6, 24,8 на порошковій рентгенівській дифрактограмі кристалів.
9. Кристалічна форма F (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу Формули (1):
 , (1)
, (1)
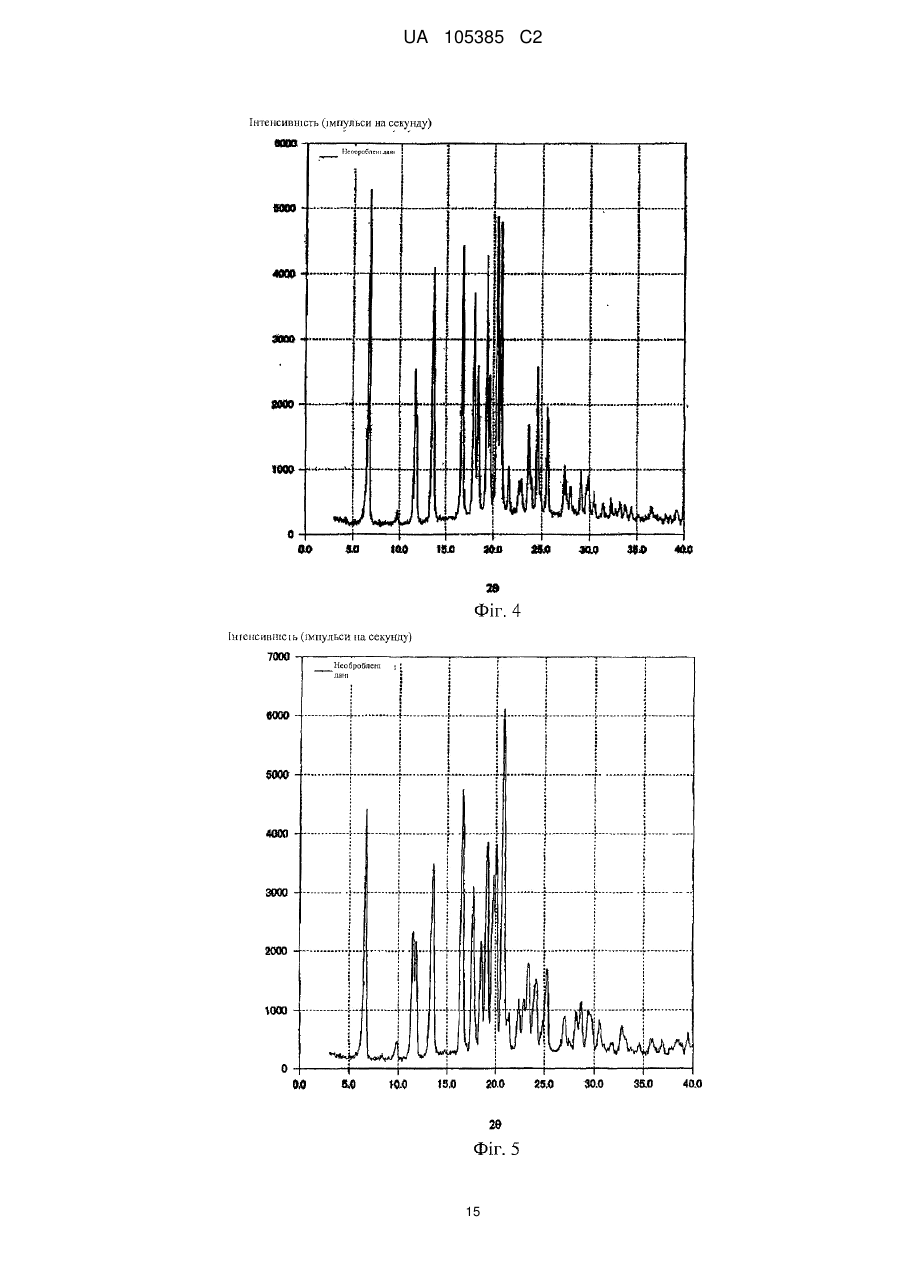
що має характеристичні піки при кутах дифракції (2θ) 6,8, 11,7, 13,7, 16,8, 18,0, 19,3, 20,4, 20,8, 24,6, 25,6 на порошковій рентгенівській дифрактограмі кристалів.
10. Кристалічної форма G (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу Формули (1):
 , (1)
, (1)
що має характеристичні піки при кутах дифракції (2θ) 6,7, 11,6, 11,9, 13,6, 16,6, 17,7, 18,6, 19,1, 19,8, 20,1, 20,8 на порошковій рентгенівській дифрактограмі кристалів.
11. Кристалічна форма H (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу Формули (1):
 , (1)
, (1)
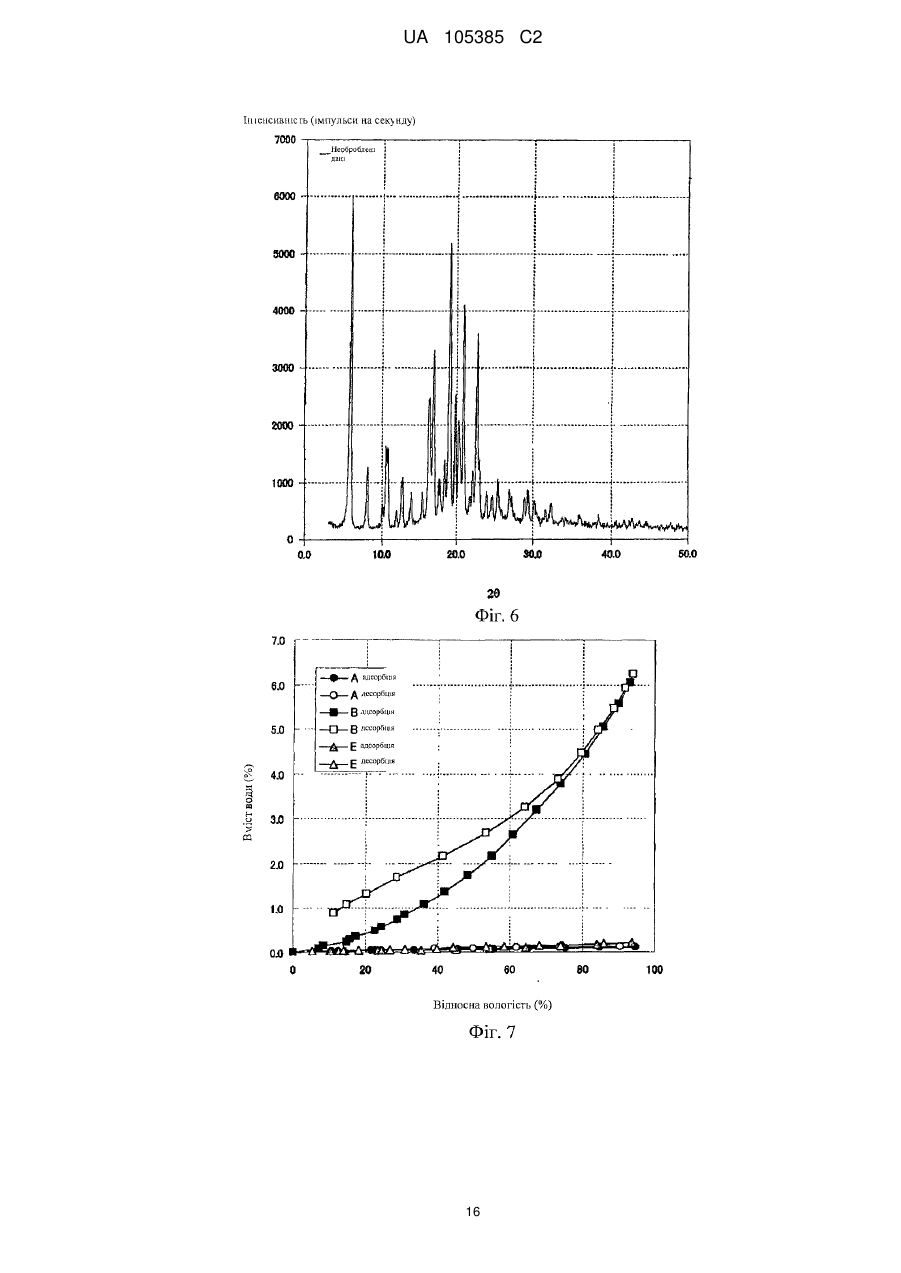
що має характеристичні піки при кутах дифракції (2θ) 6,0, 16,4, 17,0, 19,2, 19,8, 20,3, 21,0, 22,8 на порошковій рентгенівській дифрактограмі кристалів.
12. Спосіб отримання кристалічної форми В (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (1) кристалізують в органічному розчиннику, що містить воду.
13. Спосіб отримання кристалічної форми Е (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (1) нагрівають і розчиняють в складному ефірі оцтової кислоти як розчиннику або в кетоні як розчиннику, швидко додають аліфатичний вуглеводень як розчинник і миттєво охолоджують.
14. Спосіб отримання кристалічної форми F (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (1) кристалізують з етанолу.
15. Спосіб отримання кристалічної форми G (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (1) кристалізують в 2-пропанолі.
16. Спосіб отримання кристалічної форми Н (3R,4S)-7гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (І) нагрівають і розчиняють в простому ефірі як розчиннику, швидко додають циклогексан і миттєво охолоджують.
Текст
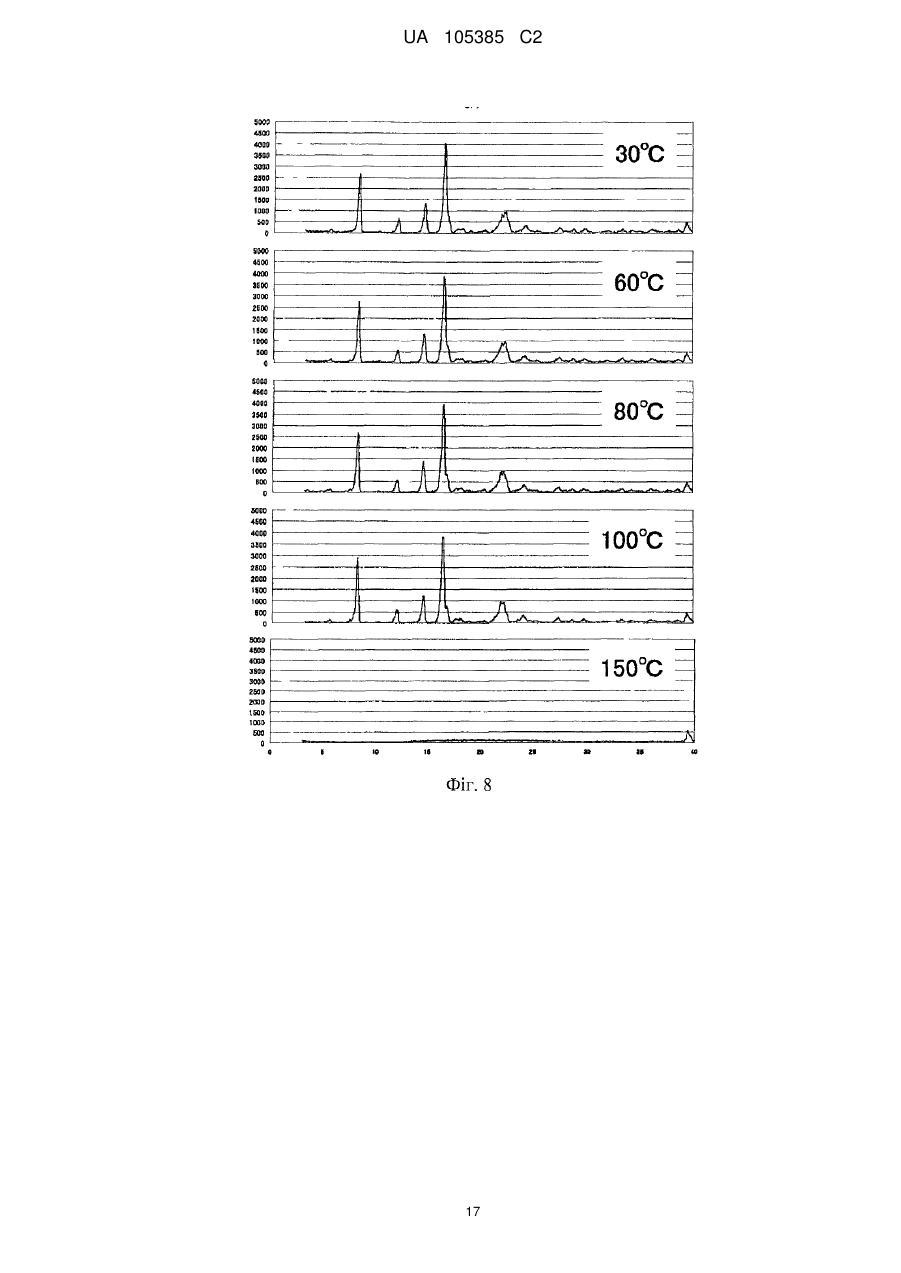
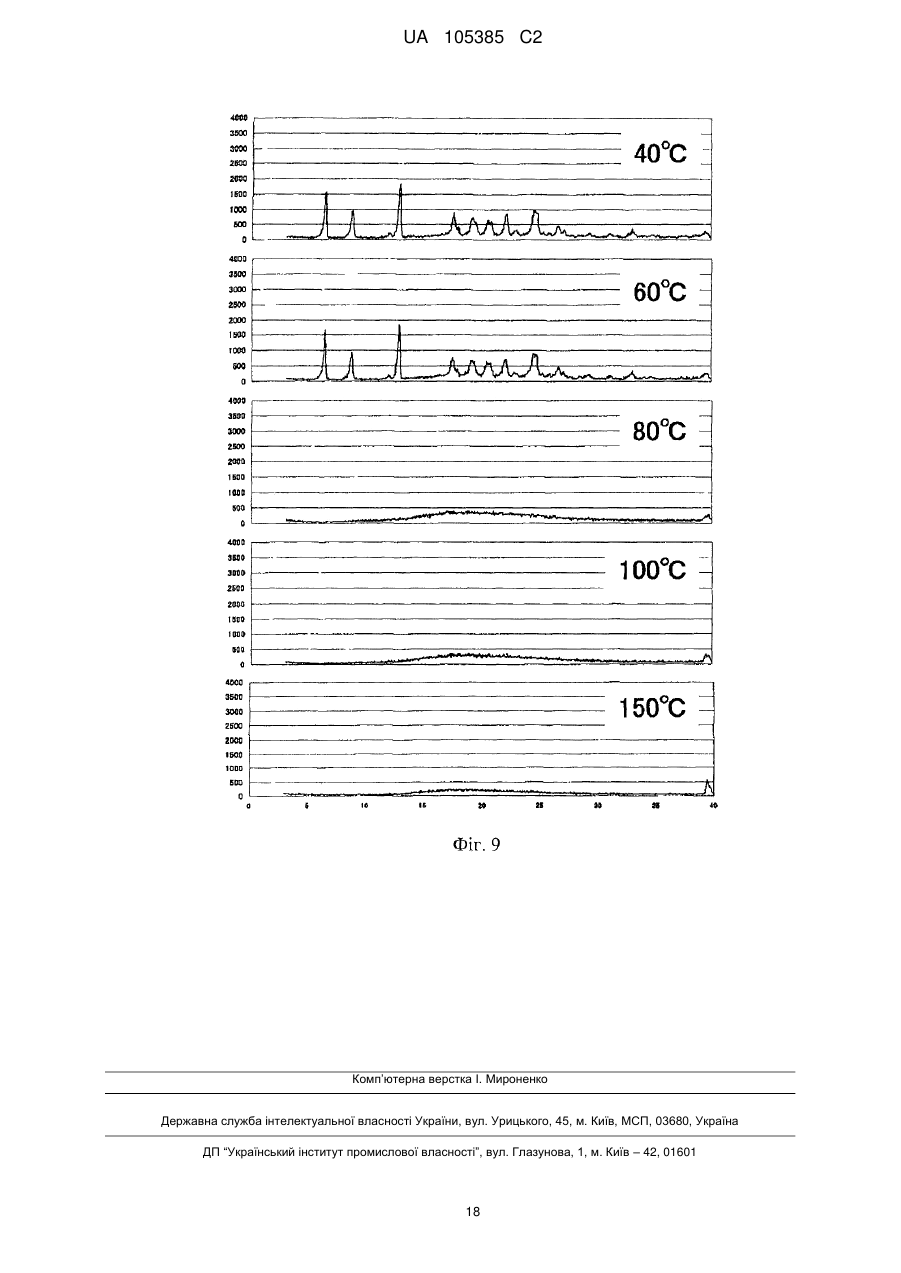
Реферат: Надання кристалічних форм (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)3,4дигідро-2Н-пірано[2,3-g]хінолін-3-олу, що являють собою чудовий лікарський засіб, і способи їх отримання. Способи отримання, що включають в себе кристалізацію (3R,4S)-7-гідроксиметил-2,2,9триметил-4-(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу зі складного ефіру оцтової кислоти, аліфатичного вуглеводню, нітрилу, ароматичного вуглеводню, кетону або простого ефіру, що застосовуються як розчинники, і кристалічні форми, отримані цими способами. UA 105385 C2 (12) UA 105385 C2 UA 105385 C2 5 Галузь техніки, до якої належить винахід Даний винахід стосується кристалічних форм (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу і способів його виробництва. Передумови створення винаходу (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2H-пірано[2,3g]хінолін-3-ол (що далі в цьому документі називається Сполукою (1)) Формули (1): Ph HN N OH HO (1) O 10 15 20 25 30 35 40 45 50 проявляє антиаритмічну дію, і, як відомо, його можна застосовувати як лікарський засіб. Як лікарські засоби потрібні сполуки, що мають постійні властивості, завдяки яким завжди можна чекати, що вони будуть виявляти постійну ефективність, і тому їх, як правило, кристалізують. Крім того, кристалізація сполуки дає можливість отримувати таку перевагу, як підвищення її хімічної стабільності (див., наприклад, непатентний документ 1). Тим часом відомо, що твердий матеріал має здатність набувати двох або більше різних кристалічних структур. Ці дві або більше кристалічні структури, як описано вище, називають кристалічним поліморфізмом. Крім того, відомо, що в тих випадках, коли сполуку кристалізують в органічному розчиннику або у воді, органічний розчинник або вода, що використовується для кристалізації, іноді включаються в сполуку, так що сполука стає кристалічним сольватом (кристалосольватом) (сольватом) або кристалогідратом (гідратом). У даному описі для кристалічного поліморфізму, кристалічних сольватів (кристалосольватів) і кристалогідратів прийняте найменування "кристалічні форми". Ці кристалічні форми звичайно мають різну розчинність, швидкість розчинення, стабільність, гігроскопічність, точки плавлення, здатність зазнавати обробки і т. п., тому при розробці лікарського засобу у вигляді кристалічної форми деякої сполуки необхідно всебічно оцінювати ці характеристики і відбирати таку кристалічну форму, яка підходить для створення лікарського засобу (див., наприклад, непатентний документ 2). Однак відносно Сполуки (1) до цього часу є тільки повідомлення про те, що ця сполука отримана за допомогою очищення із застосуванням колонкової хроматографії, а кристалічна форма Сполуки (1) невідома (див., наприклад, Патентний документ 1). Необхідно було з'ясувати, чи здатна дана сполука кристалізуватися і мати кристалічні форми. Потім, якщо кристалічні форми існують, необхідно було знайти способи отримання хімічно стабільних кристалічних форм, що відтворюються, і виявити нові кристалічні форми даної сполуки. Документи по споріднених галузях техніки Патентні документи [Патентний документ 1] Публікація міжнародної заявки № WO 2005/090357. Непатентні документи [Непатентний документ 1] "Iyakuhin no kesshoutakei to shouseki no kagaku (Science of crystal polymorphism and crystallization of drugs)" edited and written by Kazuhide Ashizawa, р. 392, published by Maruzen Planet Co., Ltd. [Непатентний документ 2] "Farumashia" vol. 45, No. 4, р. 327 (2009). Суть винаходу Задачі, що вирішуються винаходом Для розробки (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2Hпірано[2,3-g]хінолін-3-олу як лікарського засобу необхідно підтвердити можливість кристалізації даної сполуки і існування його кристалічних форм; при наявності кристалічних форм потрібно знайти способи отримання хімічно стабільних кристалічних форм, що відтворюються, і виявити нові кристалічні форми даної сполуки. Засоби вирішення поставлених задач Внаслідок ретельного дослідження, зробленого для вирішення цих задач, автори даного винаходу виявили, що (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро 1 UA 105385 C2 5 2H-пірано[2,3-g]хінолін-3-ол можна кристалізувати і, крім того, було встановлено, що існує не менше шести типів кристалічних форм цієї сполуки. Конкретно, даний винахід полягає в наступному. (I) Кристалічна форма А (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4дигідро-2H-пірано[2,3-g]хінолін-3-олу Формули (I): Ph HN N OH HO (1) O 10 15 20 25 30 що має характеристичні піки при кутах дифракції (2θ) 5,6, 8,2, 12,0, 14,7, 16,6, 16,9, 17,9, 18,4, 22,5, 24,5, 27,6 на порошковій рентгенівській дифрактограмі кристалів. (II) Спосіб отримання кристалічної форми А (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу, що характеризується тим, що включає кристалізацію сполуки Формули (1) в складному ефірі як розчиннику. (III) Спосіб отримання кристалічної форми А (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу, що характеризується тим, що включає кристалізацію сполуки Формули (1) в аліфатичному вуглеводні як розчиннику. (IV) Спосіб отримання кристалічної форми А (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу, що характеризується тим, що включає кристалізацію сполуки Формули (1) в нітрилі як розчиннику. (V) Спосіб отримання кристалічної форми А (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу, що характеризується тим, що включає кристалізацію сполуки Формули (1) в ароматичному вуглеводні як розчиннику. (VI) Спосіб отримання кристалічної форми А (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу, що характеризується тим, що включає кристалізацію сполуки Формули (1) в кетоні як розчиннику. (VII) Кристалічна форма В (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4дигідро-2H-пірано[2,3-g]хінолін-3-олу Формули (1): Ph HN N OH HO (1) O 35 40 що має характеристичні піки при кутах дифракції (2θ) 6,4, 8,7, 12,8, 17,5, 19,1, 20,7, 22,0, 24,8, 26,6 на порошковій рентгенівській дифрактограмі кристалів. (VIII) Кристалічна форма Е (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4дигідро-2H-пірано[2,3-g]хінолін-3-олу Формули (1): 2 UA 105385 C2 Ph HN N OH HO (1) O 5 що має характеристичні піки при кутах дифракції (2θ) 9,1, 12,8, 13,1, 14,6, 15,2, 16,4, 22,1, 23,6, 24,8 на порошковій рентгенівській дифрактограмі кристалів. (IX) Кристалічна форма F (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро2H-пірано[2,3-g]хінолін-3-олу Формули (1): Ph HN N OH HO (1) O 10 що має характеристичні піки при кутах дифракції (2θ) 6,8, 11,7, 13,7, 16,8, 18,0, 19,3, 20,4, 20,8, 24,6, 25,6 на порошковій рентгенівській дифрактограмі кристалів. (X) Кристалічна форма G (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4дигідро-2H-пірано[2,3-g]хінолін-3-олу Формули (1): Ph HN N OH HO (1) O 15 20 що має характеристичні піки при кутах дифракції (2θ) 6,7, 11,6, 11,9, 13,6, 16,6, 17,7, 18,6, 19,1, 19,8, 20,1, 20,8 на порошковій рентгенівській дифрактограмі кристалів. (XI) Кристалічна форма Н (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4дигідро-2H-пірано(2,3-g]хінолін-3-олу Формули (I): Ph HN N OH HO (1) O 25 що має характеристичні піки при кутах дифракції (2θ) 6,0, 16,4, 17,0, 19,2, 19,8, 20,3, 21,0, 22,8 на порошковій рентгенівській дифрактограмі кристалів. (XII) 3 UA 105385 C2 5 10 15 20 25 30 35 40 45 50 55 60 Спосіб отримання кристалічної форми В (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу, що характеризується тим, що включає кристалізацію сполуки Формули (1) з органічного розчинника, що містить воду. (XIII) Спосіб отримання кристалічної форми Е (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу, що характеризується тим, що включає нагрівання і розчинення сполуки Формули (1) в складному ефірі оцтової кислоти як розчиннику або в кетоні як розчиннику і одне швидке додавання аліфатичного вуглеводню як розчинника і миттєве охолоджування. (XIV) Спосіб отримання кристалічної форми F (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу, що характеризується тим, що включає кристалізацію сполуки Формули (1) з етанолу. (XV) Спосіб отримання кристалічної форми G (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу, що характеризується тим, що включає кристалізацію сполуки Формули (1) з 2-пропанолу. (XVI) Спосіб отримання кристалічної форми Н (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу, що характеризується тим, що включає нагрівання і розчинення сполуки Формули (1) в простому ефірі як розчиннику і швидке додавання аліфатичного вуглеводню як розчинника і миттєве охолоджування. Найкращий спосіб здійснення винаходу Першим описаний спосіб отримання кристалічної форми А. Приклади складних ефірів, що застосовуються як розчинники, включають в себе: складний ефір мурашиної кислоти, що має C1-3-алкоксильну групу, такий як метилформіат, етилформіат і н-пропілформіат; і складний ефір оцтової кислоти, що має C 1-4-алкоксильну групу, такий як метилацетат, етилацетат, н-пропілацетат, ізопропілацетат, н-бутилацетат, ізобутилацетат і трет-бутилацетат; серед них переважні етилацетат, н-пропілацетат і ізопропілацетат. Приклади аліфатичних вуглеводнів, що застосовуються як розчинник, включають в себе C 57-аліфатичні вуглеводні, такі як пентан, н-гексан, циклогексан, н-гептан і метилциклогексан; серед них переважний н-гептан. Приклади нітрилів, що застосовуються як розчинники, включають в себе C 2-4-нітрили, такі як ацетонітрил, пропіонітрил і бутиронітрил; серед них переважний ацетонітрил. Приклади ароматичних вуглеводнів, що застосовуються як розчинники, включають в себе C6-8-ароматичні вуглеводні, такі як бензол, толуол і ксилол; серед них переважні толуол і ксилол. Приклади кетонів, що застосовуються як розчинники, включають в себе C 3-6-кетони, такі як ацетон, метилетилкетон, метилізопропілкетон і метилізобутилкетон; серед них переважні ацетон і метилізобутилкетон. Крім того, можна застосовувати тільки один з цих розчинників або суміш цих розчинників і можна додавати інші розчинники. Кількість розчинника, що застосовується, становить від 1- до 50-кратної кількості по масі, переважно, від 2- до 20-кратної кількості по масі, більш переважно, від 5- до 10-кратної кількості по масі відносно одиниці маси Сполуки (1). Якщо кристалізацію проводять, охолоджуючи розчин Сполуки (1), то температурою для цього охолоджування може бути певна температура від 0 °C до температури, при якій розчинник кипить із зворотним холодильником; однак переважно кристалізацію провести, охолоджуючи розчин до 0-5 °C. Якщо кристалізацію проводять, концентруючи розчин Сполуки (1), то кристалізацію можна провести, залишаючи будь-яку кількість розчинника або видаляючи розчинник повністю. Крім того, кристалізацію можна провести, комбінуючи обидві операції охолоджування і концентрування. Для кристалізації можна застосовувати кристали-затравки. Кристали для затравки можна отримувати добре відомими способами, наприклад, тертям шпателем внутрішньої стінки колби, що містить розчин, який кристалізується. Наступним описаний спосіб отримання кристалічної форми В, яка являє собою гідрат Сполуки (1). Застосовуваний органічний розчинник ніяк не обмежують, при умові, що цей розчинник може змішуватися з водою; приклади застосовних органічних розчинників, включають в себе спирт, 4 UA 105385 C2 5 10 15 20 25 30 35 40 45 50 55 що застосовується як розчинник, нітрил, що застосовується як розчинник, простий ефір, що застосовується як розчинник, кетон, що застосовується як розчинник, амід, що застосовується як розчинник, і сульфоксид, що застосовується як розчинник. Переважні приклади таких розчинників включають в себе: метанол, етанол, 1-пропанол і 2-пропанол, що застосовуються як спиртові розчинники; ацетонітрил і пропіонітрил, що застосовуються як нітрильні розчинники; тетрагідрофуран, 1,2-диметоксіетан і 1,4-діоксан, що застосовуються як ефірні розчинники; ацетон і метилетилкетон, що застосовуються як кетонові розчинники; N, N-диметилформамід і N, N-диметилацетамід, що застосовуються як амідні розчинники; і диметилсульфоксид, що застосовується як сульфоксидний розчинник. Крім того, переважні приклади органічних розчинників включають в себе метанол, етанол, 2-пропанол, ацетонітрил і ацетон. Якщо в складі водовмісного органічного розчинника використовують деяку кількість води, то вміст такої води можна вибирати на будь-якому рівні, здатному тимчасово забезпечувати розчинення Сполуки (1). Враховуючи баланс між ефективністю кристалізації і ефективністю очищення, співвідношення органічного розчинника і води, переважно, знаходяться в діапазоні від 1:4 до 10:1, більш переважно, від 1:2 до 3:1. Кристалізацію можна провести або способом, що включає в себе первинне приготування водовмісного органічного розчинника і подальше нагрівання і розчинення Сполуки (1) в підготовленому органічному розчиннику для охолоджування отриманого розчину, або способом, що включає в себе розчинення Сполуки (1) в органічному розчиннику і подальше додавання води в отриманий розчин. В обох способах кристалізацію можна провести, застосовуючи охолоджування, концентрування або поєднання охолоджування і концентрування. Відносно кількості органічного розчинника, що застосовується, допустима будь-яка кількість, достатня для розчинення Сполуки (1). Однак переважна кількість, що складає від 1- до 100кратної кількості по масі, більш переважно, від 2- до 50-кратної кількості по масі, ще більш переважно, від 5- до 20-кратної кількості по масі відносно одиниці маси Сполуки (1). Наступним описаний спосіб отримання кристалічної форми Е. Приклади складного ефіру оцтової кислоти, що застосовується як розчинник, включають в себе складний ефір оцтової кислоти, що має C1-4-алкоксильну групу, такий як метилацетат, етилацетат, н-пропілацетат, ізопропілацетат, н-бутилацетат, ізобутилацетат і трет-бутилацетат. Серед них переважні етилацетат, н-пропілацетат і ізопропілацетат; особливо переважний етилацетат. Відносно кількості складного ефіру оцтової кислоти, що застосовується як розчинник, допустима будь-яка кількість, достатня для розчинення Сполуки (1); однак переважна кількість, що складає від 4- до 20-кратної кількості по об'єму, особливо переважно, від 5- до 10-кратної кількості по об'єму відносно одиниці маси Сполуки (1). Приклади кетонів, що застосовуються як розчинники, включають в себе C 3-6-кетони, такі як ацетон, метилетилкетон, метилізопропілкетон і метилізобутилкетон. Серед них переважні ацетон і метилізобутилкетон і особливо переважний метилізобутилкетон. Відносно кількості кетону, що застосовується як розчинник, допустима будь-яка кількість, достатня для розчинення Сполуки (1). Однак переважна кількість, що складає від 5- до 50кратної кількості по об'єму, найбільш переважно, від 10- до 30-кратної кількості по об'єму відносно одиниці маси Сполуки (1). Приклади аліфатичних вуглеводнів, що застосовуються як розчинники, включають в себе C 5-аліфатичні вуглеводні, такі як пентан, н-гексан, циклогексан, н-гептан і метилциклогексан. 7 Серед них переважні н-гексан і н-гептан і особливо переважний н-гептан. Кількість аліфатичного вуглеводню, що застосовується як розчинник, складає від 1- до 100кратної кількості по об'єму, більш переважно, від 5- до 50 кратної кількості по об'єму, найбільш переважно, від 10- до 30-кратної кількості по об'єму відносно одиниці маси Сполуки (1). Кристалізацію Сполуки (1) можна провести при певній температурі в діапазоні від 0 °C до температури, при якій розчинник кипить із зворотним холодильником. Однак переважний спосіб, що включає в себе розчинення Сполуки (1) в складному ефірі оцтової кислоти, що застосовується як розчинник, або в кетоні, що застосовується як розчинник, при 60-70 °C і швидке додавання аліфатичного вуглеводню, що застосовується як розчинник, до отриманого розчину і миттєве охолоджування розчину, що кристалізується, до кімнатної температури. У цьому випадку "швидко" означає "в межах 30 секунд". Далі описаний спосіб отримання кристалічної форми F, яка являє собою сольват (3R, 4S)-7гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу з етанолом. Як розчинник застосовують етанол. 5 UA 105385 C2 5 10 15 20 25 30 35 40 45 50 55 Кількість етанолу, що застосовується, складає від 1- до 50-кратної кількості по масі, переважно, від 2- до 20-кратної кількості по масі, більш переважно, від 3- до 10-кратної кількості по масі відносно одиниці маси Сполуки (1). Кристалізацію Сполуки (1) можна провести при певній температурі в діапазоні від 0 °C до температури, при якій розчинник кипить із зворотним холодильником. Однак переважно кристалізацію провести, застосовуючи спосіб, що включає в себе нагрівання і розчинення Сполуки (1) в етанолі, взятому в як можна меншій кількості, і охолоджування отриманого розчину; застосовуючи спосіб, що включає в себе розчинення Сполуки (1) в етанолі і концентрування отриманого розчину; або застосовуючи спосіб, в якому поєднують два вищезгаданих способи. Наступним описаний спосіб отримання кристалічної форми G, яка представляє сольват (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу з 2-пропанолом. Як розчинник застосовують 2-пропанол. Кількість 2-пропанолу, що застосовується, складає, переважно, від 2- до 20-кратної кількості по масі, більш переважно, від 3- до 10-кратної кількості по масі відносно одиниці маси Сполуки (1). Кристалізацію Сполуки (1) можна провести при певній температурі в діапазоні від 0 °C до температури, при якій розчинник кипить із зворотним холодильником. Однак переважно кристалізацію провести, застосовуючи спосіб, що включає в себе нагрівання і розчинення Сполуки (1) в 2-пропанолі, взятому в як можна меншій кількості, і охолоджування отриманого розчину; застосовуючи спосіб, що включає в себе розчинення Сполуки (1) в 2-пропанолі і концентрування отриманого розчину; або застосовуючи спосіб, в якому поєднують два вищезгаданих способи. Наступним описаний спосіб отримання кристалічної форми Н, яка являє собою сольват (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу з циклогексаном. Як розчинник застосовують розчинник на основі простого ефіру, переважно, діоксан. Кількість діоксану, що застосовується, складає від 1- до 5-кратної кількості по масі, переважно, від 2- до 20-кратної кількості по масі, більш переважно, від 3- до 10-кратної кількості по масі відносно одиниці маси Сполуки (1). Як розчинник застосовують циклогексан. Кількість циклогексану, що застосовується, складає від 1- до 50-кратної кількості по масі, переважно, від 2- до 20-кратної кількості по масі відносно одиниці маси Сполуки (1). Кристалізацію Сполуки (1), переважно, проводять, застосовуючи спосіб, що включає в себе розчинення Сполуки (1) в розчиннику на основі простого ефіру, взятому в як можна меншій кількості, при 60-70 °C, швидке додавання циклогексану до отриманого розчину і миттєве охолоджування розчину, що кристалізується, до кімнатної температури. У цьому випадку "швидко" означає "в межах 30 секунд". Короткий опис креслень [Фіг. 1] Фіг. 1 являє собою порошкову рентгенівську дифрактограму кристалічної форми А (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3олу, отриманої згідно з даним винаходом. [Фіг. 2] Фіг. 2 являє собою фігуру, що показує порошкову рентгенівську дифрактограму кристалічної форми В (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро2H-пірано[2,3-g]хінолін-3-олу, отриманої згідно з даним винаходом. [Фіг. 3] Фіг. 3 являє собою фігуру, що показує порошкову рентгенівську дифрактограму кристалічної форми Е (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро2H-пірано[2,3-g]хінолін-3-олу, отриманої згідно з даним винаходом. [Фіг. 4] Фіг. 4 являє собою фігуру, що показує порошкову рентгенівську дифрактограму кристалічної форми F (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро2H-пірано[2,3-g]хінолін-3-олу, отриманої згідно з даним винаходом. [Фіг. 5] Фіг. 5 являє собою фігуру, що показує порошкову рентгенівську дифрактограму кристалічної форми G (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро2H-пірано[2,3-g]хінолін-3-олу, отриманої згідно з даним винаходом. [Фіг. 6] Фіг. 6 являє собою фігуру, що показує порошкову рентгенівську дифрактограму кристалічної форми Н (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро2H-пірано[2,3-g]хінолін-3-олу, отриманої згідно з даним винаходом. 6 UA 105385 C2 5 10 15 20 25 30 35 40 45 50 55 60 [Фіг. 7] Фіг. 7 являє собою фігуру, що показує ізотерми адсорбції води на кристалах форм А, В і Е (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2H-пірано[2,3g]хінолін-3-олу, отриманих згідно з даним винаходом. [Фіг. 8] Фіг. 8 являє собою фігуру, що показує високотемпературну рентгенівську дифрактограму кристалічної форми А (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу, отриманої згідно з даним винаходом. [Фіг. 9] Фіг. 9 являє собою фігуру, що показує високотемпературну рентгенівську дифрактограму кристалічної форми В (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу, отриманої згідно з даним винаходом. Приклади Нижче в цьому документі даний винахід буде описаний більш детально з посиланнями на Приклади, які не треба тлумачити як такі, що обмежують об'єм даного винаходу. У Прикладах вимірювання точки плавлення проводили капілярним способом, застосовуючи прилад В-545 (виготовлений Shibata Scientific Technology Ltd.) (швидкість підвищення температури: 1 °C/хв.); диференціальну скануючу калориметрію (DSC) проводили на приладі DSC 8230 (виготовленому Rigaku Corporation) (швидкість підвищення температури: 5 °C/хв.); а вимірювання порошкової рентгенівської дифракції проводили на приладі MXLabo (виготовленому Mac Science Co., Ltd.; -10 джерело випромінювання: Cu∙Kα, довжина хвилі: 1,54056 (10 м)). Неочищений продукт (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро2H-пірано[2,3-g]хінолін-3-олу (Сполуки (1)) можна отримувати способом (Способом синтезу А), описаним в публікації міжнародної заявки № WO 2005/090357. Крім того, Сполуку (1) можна також синтезувати нижченаведеним способом (Способом синтезу В). Посилальний приклад синтезу 1 Синтез (Спосіб синтезу В) (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4дигідро-2H-пірано[2,3-g]хінолін-3-олу 10,05 г (32,1 ммоль) (3R, 4S)-(3,4-епокси-2,2,9-триметил-3,4-дигідро-2H-пірано[2,3-g]хінолін7-іл)метилацетату (синтезованого згідно зі способом, описаним в публікації міжнародної заявки № WO 2005/090357) розчиняли в 99,79 г метанолу і в розчин, отриманий в результаті цього, додавали по краплях 40 мл (40 ммоль) 1 М водного розчину гідроксиду натрію, після чого отриману суміш перемішували при кімнатній температурі протягом 30 хвилин. До реакційної суміші, отриманої таким чином, додавали 60,06 г хлороформу і 60,30 г H 2О і розділяли шари, після чого реакційну суміш два рази екстрагували хлороформом. Органічний шар концентрували, отримуючи 9,53 г ясно-коричневої твердої речовини. До цієї твердоїречовини додавали 49,85 г толуолу і отриману суспензію перемішували при 60 °C протягом 10 хвилин і охолоджували до 5 °C або нижче, відфільтровували кристалічну речовину. Кристали промивали 10,0 г толуолу і сушили при 50 °C при зниженому тиску, отримуючи 7,98 г (вихід: 91,7 %) (3R, 4S)-3,4-епокси-7-гідроксиметил-2,2,9-триметил-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу у вигляді білої твердої речовини. Зовнішній вигляд: біла тверда речовина 1 1H-ЯМР (CDCl3, TMS) δ м. ч.: 1,31 (3H, с, Me), 1,65 (3H, с, Me), 2,59 (3H, с, Me), 3,60 (1Н, д, J=4,3 Гц, C3), 4,15 (1Н, д, J=4,3 Гц, C4), 4,42 (1Н, т, J=4,0 Гц, CH2ОH), 4,83 (2H, д, J=4,0 Гц, CH2ОH), 7,07 (1Н, с, Ar), 7,31 (1Н, с, Ar), 8,08 (1Н, с, Ar). Точка плавлення: 143-144 °C До рідкої суміші 7,98 г (29,4 ммоль) отриманого (3R, 4S)-3,4-епокси-7-гідроксиметил-2,2,9триметил-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу і 16,07 г 1-пропанолу додавали 4,30 г (35,5 ммоль, 1,2 еквіваленти) 2-фенілетиламіну і суміш, отриману таким чином, нагрівали і кип'ятили із зворотним холодильником протягом 5 годин. Відігнавши розчинник, отримували 14,52 г (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу у вигляді коричневої маслянистої речовини. Приклад 1 Виробництво кристалічної форми А (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу До 14,52 г неочищеного продукту (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу, отриманого в Посилальному прикладі синтезу 1, додавали 12,02 г етилацетату і суміш, отриману таким чином, для розчинення нагрівали до 50 °C, після чого в отриманий розчин по краплях додавали 59,94 г н-гептану при 49-58 °C для кристалізації. Суміш, отриману таким чином, безперервно охолоджували до 3 °C і потім відфільтровували кристали, після чого кристали промивали сумішшю 1,5 г етилацетату і 7 UA 105385 C2 5 10 15 20 25 30 35 40 45 50 55 60 7,5 г н-гептану, а потім 8,0 г н-гептану, отримуючи 10,02 г кристалічної форми А Сполуки (1) у вигляді білої кристалічної речовини. Точка плавлення отриманої кристалічної речовини знаходилася при 124-125 °C. Отриману кристалічну речовину піддавали аналізу DSC, результат якого підтвердив наявність ендотермічного піку при 130 °C. На порошковій рентгенівській дифрактограмі кристалічної речовини спостерігали характеристичні піки при кутах дифракції (2θ) 5,6, 8,2, 12,0, 14,7, 16,6, 16,9, 17,9, 18,4, 22,5, 24,5, 27,6. Результат показаний на Фіг. 1. Приклад 2 Виробництво кристалічної форми В (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу 62,23 г кристалічної форми А (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4дигідро-2H-пірано[2,3-g]хінолін-3-олу розчиняли в 247,73 г етанолу, нагріваючи суміш до 62 °C. До розчину, отриманого внаслідок цього, по краплях додавали 275,19 г води при температурі від 55 до 67 °C протягом 20 хвилин і отриману суміш охолоджували до 5 °C протягом 3 годин, після чого суміш перемішували при тій же температурі протягом 30 хвилин і відфільтровували кристалічну речовину. Кристали сушили при 50 °C при зниженому тиску доти, доки маса кристалів не переставала зменшуватись при подальшому висушуванні, внаслідок чого було вироблено 59,22 г білої твердої речовини. Отриману кристалічну речовину піддавали аналізу DSC, результат якого підтвердив наявність ендотермічного піку при 91 °C. На порошковій рентгенівській дифрактограмі кристалічної речовини спостерігали характеристичні піки при кутах дифракції (2θ) 6,4, 8,7, 12,8, 17,5, 19,1, 20,7, 22,0, 24,8, 26,6. Результат показаний на Фіг. 2. Крім того, в кристалічній речовині вимірювали вміст води із застосуванням вологоміру Карла Фішера (об'ємний аналіз), в результаті чого було виявлено, що вміст води становив 3,2 % по масі. Приклад 3 Виробництво кристалічної форми Е (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу 14,99 г кристалічної форми А (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4дигідро-2H-пірано[2,3-g]хінолін-3-олу розчиняли в 75 мл етилацетату, нагріваючи суміш до 63 °C. Після цього нагрівання припиняли і при кімнатній температурі до отриманого розчину однією порцією додавали 300 мл н-гептану, після чого отриману суміш охолоджували до 26 °C. У такому стані отриману суміш перемішували протягом 1 години і відфільтровували кристали. Ці кристали сушили при 40 °C при зниженому тиску, отримуючи 12,67 г зернистої твердої речовини жовтого кольору. Отриману кристалічну речовину піддавали аналізу DSC, результат якого підтвердив наявність ендотермічного піку при 119 °C. На порошковій рентгенівській дифрактограмі кристалічної речовини спостерігали характеристичні піки при кутах дифракції (2θ) 9,1, 12,8, 13,1, 14,6, 15,2, 16,4, 22,1, 23,6, 24,8. Результат показаний на Фіг. 3. Приклад 4 Виробництво кристалічної форми F (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу 10,01 г кристалічної форми А (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4дигідро-2H-пірано[2,3-g]хінолін-3-олу розчиняли в 60,20 г етанолу, нагріваючи суміш до 76 °C. Розчин, отриманий внаслідок цього, охолоджували до 5 °C протягом 1 години і 45 хвилин і перемішували при 5 °C протягом 1 години, відфільтровували кристали. Ці кристали сушили при 50 °C при зниженому тиску доти, доки маса кристалів не переставала зменшуватись при подальшому висушуванні, внаслідок чого було вироблено 10,96 г білої твердої речовини. Отриману кристалічну речовину піддавали аналізу DSC, результат якого підтвердив наявність ендотермічного піку при 99 °C. Крім того, на порошковій рентгенівській дифрактограмі кристалічної речовини спостерігали характеристичні піки при кутах дифракції (2θ) 6,8, 11,7, 13,7, 16,8, 18,0, 19,3, 20,4, 20,8, 24,6, 25,6. Результат показаний на Фіг. 4. У доповнення до цього, розчин кристалів в CDCl3 з тетраметилсиланом як внутрішній 1 стандарт досліджували методом H-ЯМР-спектроскопії. Відношення інтегральної величини двох протонів етанолу, детектованої при δ 3,7 м. ч., до відповідної величини одного протона в положенні 4 Сполуки (1) становило 2,4 до 1, що свідчило про існування кристалічної речовини у вигляді сольвату з 1,2 екв. етанолу. Приклад 5 Виробництво кристалічної форми G (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу 1,00 г кристалічної форми А (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4дигідро-2H-пірано[2,3-g]хінолін-3-олу суспендували в 5 мл 2-пропанолу і перемішували при 21 °C протягом 19,7 годин. Кристали відфільтровували і сушили при 40 °C протягом 6 годин при 8 UA 105385 C2 5 10 15 20 25 30 35 40 45 зниженому тиску доти, доки маса кристалів не переставала зменшуватись при подальшому висушуванні, внаслідок чого було вироблено 0,97 г білої кристалічної речовини. Отриману кристалічну речовину піддавали аналізу DSC, результат якого підтвердив наявність ендотермічного піка при 75,9 °C. На порошковій рентгенівській дифрактограмі кристалічної речовини спостерігали характеристичні піки при кутах дифракції (2θ) 6,7, 11,6, 11,9, 13,6, 16,6, 17,7, 18,6, 19,1, 19,8, 20,1, 20,8. Результат показаний на Фіг. 5. У доповнення до цього, розчин кристалів в CDCl3 з тетраметилсиланом як внутрішній 1 стандарт досліджували методом H-ЯМР-спектроскопії. Відношення інтегральної величини одного протона 2-пропанолу, детектованої при δ 4,0 м. ч., до відповідної величини одного протона в положенні 4 Сполуки (1) становило 0,83 до 1, що свідчило про існування кристалічної речовини у вигляді сольвату з 0,83 екв. 2-пропанолу. Приклад 6 Виробництво кристалічної форми Н (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу 19,95 г кристалічної форми А (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4дигідро-2H-пірано[2,3-g]хінолін-3-олу розчиняли в 140 мл діоксану. Нерозчинний матеріал відфільтровували і промивали 60 мл діоксану. Розчинник відганяли при зниженому тиску, отримуючи 50 г залишкового розчину. Залишковий розчин нагрівали до 60 °C, потім однією порцією додавали 600 мл циклогексану і розчин піддавали миттєвому охолоджуванню від 60 °C до 28 °C. Розчин перемішували при 25-28 °C протягом 5,1 години і відфільтровували кристали. Кристали сушили при 50 °C протягом 2 годин при зниженому тиску доти, доки маса кристалів не переставала зменшуватись при подальшому висушуванні, внаслідок чого було вироблено 21,96 г білої кристалічної речовини. Отриману кристалічну речовину піддавали аналізу DSC, результат якого підтвердив наявність ендотермічногой піку при 80,1 °C і 86,1 °C. Крім того, на порошковій рентгенівській дифрактограмі кристалічної речовини спостерігали характеристичні піки при кутах дифракції (2θ) 6,0, 16,4, 17,0, 19,2, 19,8, 20,3, 21,0, 22,8. Результат показаний на Фіг. 6. У доповнення до цього, розчин кристалів в CDCl3 з тетраметилсиланом як внутрішній 1 стандарт досліджували методом H-ЯМР-спектроскопії. Відношення інтегральної величини 12 протонів циклогексану, детектованій при δ 51,4 м. ч., до відповідної величини трьох протонів метилу в Сполуці (1) становило 2,69 до 1, що свідчило про існування кристалічної речовини у вигляді сольвату з 0,67 екв. циклогексану. Приклади випробувань Нижче в цьому документі описані Приклади випробувань, проведених з кристалічними формами А, В, Е і F, отриманими способами, вказаними вище в Прикладах 1-4. Приклад випробувань 1 Випробовували термостійкість, вологостійкість і світлостійкість кристалічних форм А, В і F Сполуки (1). Умови проведення кожного випробування були наступними. Випробування на термостійкість: 60 °C, вологість не регулювали, 2 тижні, у повітронепроникному контейнері. Випробування на вологостійкість: 25 °C, відносна вологість 90 %, 2 тижні, у відкритому контейнері. 2 Випробування на світлостійкість: 200 Вт/м •год., 25 °C, відносна вологість 60 %, 57 годин, у відкритому контейнері. Крім того, стабільність кристалів оцінювали по мірі збільшення загальної кількості забруднень за допомогою ВЕРХ-аналізу. Результат показаний в Таблиці 1. Таблиця 1 Початкове значення Термостійкість Вологостійкість Світлостійкість 50 Кристалічна форма А Кристалічна форма В 0,84 % 0,55 % 0,83 % 1,70 % 0,83 % 0,53 % 0,85 % 0,72 % Кристалічна форма F 0,25 % 0,37 % 0,35 % 0,74 % В умовах проведення випробувань збільшення вмісту забруднень в кожній кристалічній формі складало не більше за 1,5 %. Підтверджено, що серед перевірених кристалічних форм кристали форми А є найбільш стабільними, оскільки в умовах випробувань ця форма не показала ніякого збільшення вмісту забруднень. 9 UA 105385 C2 5 Приклад випробувань 2 Кристалічні форми А, В і Е Сполуки (1) піддалися випробуванню в умовах прискореного старіння. Умови випробування були наступними. Випробування в умовах прискореного старіння: 40 °C, відносна вологість 75 %, 6 місяців, у повітронепроникному контейнері. [Умови вимірювань] Крім того, стабільність кристалів оцінювали по мірі збільшення загальної кількості забруднень за допомогою ВЕРХ-аналізу. Результат показаний в Таблиці 2. Таблиця 2 0,70 % Кристалічна форма В 0,42 % Кристалічна форма Е 0,64 % 0,80 % 1,15 % 0,64 % Кристалічна форма А Початкове значення Значення, виміряне після випробування 10 15 20 25 30 35 При проведенні випробувань в умовах прискореного старіння збільшення вмісту забруднень в кожній кристалічній формі складало не більше за 1,5 %. Підтверджено, що найбільш стабільними є кристалічні форми А і Е, оскільки в них не спостерігали ніякого збільшення вмісту забруднень. Приклад випробувань 3 Кристалічні форми А, В і Е Сполуки (1) оцінювали за допомогою аналізу адсорбції води. [Умови вимірювань] кількість зразка: 0,2 г; попередня обробка: 60 °C, 20 годин; температура 25 °C, застосовували волюмометричний апарат дослідження адсорбції (торгове найменування: BELSORP 18, виготовлений BEL Japan, Inc.). У кристалах форми В спостерігали зворотну адсорбцію води. У кристалах форм А і Е не спостерігали ніякої адсорбції води. Спостерігали, що адсорбція води на кристалах форми А була меншою, ніж адсорбція води на кристалах форми Е. Результат показаний на Фіг. 7. Приклад випробувань 4 Визначали розчинність і питому поверхню кристалів форми А, форми В, форми Е і форми F Сполуки (1). Розчинність [Умови вимірювань] JP2, pH 6,8 (3,40 г однозаміщеного фосфату калію і 3,55 г безводного двозаміщеного фосфату натрію розчиняли у воді, отримуючи 1 літр розчину. Один об'єм розчину змішували з одним об'ємом води, отримуючи розчин згідно JP2, рН 6,8), 60 хвилин. Згідно з п'ятнадцятим виданням Фармакопеї Японії, випробування на розчинність (Протокол випробування на розчинність; кількість зразка: 10 мг, випробувальний розчин: згідно JP2, pH 6,8, 500 мл, час відбору зразків: 5, 15, 30, 60 хв., швидкість обертання лопатевої мішалки: 100 об./хв., температура бані: 37 °C). Питома поверхня [Умови вимірювань] температура адсорбції: 77K, час встановлення адсорбційної рівноваги: 300 секунд. [Одиниця вимірювання] квадратні метри на грам. Вимірювання проводили методом БЕТ, використовуючи адсорбцію азоту в рідкому азоті після попередньої обробки в умовах рефлюксу рідкого азоту. Результат показаний в Таблиці 3. 40 Таблиця 3 Розчинність Питома поверхня Кристалічна форма А 36 % 0,7 Кристалічна форма В 27 % 0,3 Кристалічна форма Е 23 % 0,3 Кристалічна форма F 30 % («-» в Таблиці 3 означає "вимірювання не проводили".) Кожна кристалічна форма проявляла здатність розчинятися в розчині, приготованому згідно JP2. Конкретно, високу розчинність мала кристалічна форма А. Крім того, кристалічна форма А демонструвала також і високе значення питомої поверхні. 10 UA 105385 C2 5 10 15 Виявилося несподіваним, що кристалічна форма А мала чудову стабільність і високу розчинність. Крім того, можна вказати, що кристалічна форма А мала чудові характеристики як лікарський засіб. Приклад випробувань 5 З кристалічними формами А і В Сполуки (I) були проведені вимірювання методом високотемпературної XRD. Як показано на Фіг. 8 і Фіг. 9, нижче 100 °C ніяких змін на порошковій рентгенівській дифрактограмі кристалічної форми А не спостерігали, так само як і на порошковій рентгенівській дифрактограмі кристалічної форми В при температурі нижчій за 60 °C. Зокрема, кристалічна форма А демонструвала задовільну стабільність як лікарський засіб. Застосовність у виробничих умовах Згідно з даним винаходом, можна надати спосіб, за допомогою якого можна виробляти хімічно стабільну сполуку, застосовну як лікарський засіб, що має таку ж якість і таку ж кристалічну форму, як і (3R, 4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро2H-пірано[2,3-g]хінолін-3-ол, і його нові кристалічні форми. ФОРМУЛА ВИНАХОДУ 20 1. Кристалічна форма А (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро2Н-пірано[2,3-g]хінолін-3-олу Формули (1): Ph HN N OH HO (1) O 25 30 35 40 що має характеристичні піки при кутах дифракції (2θ) 5,6, 8,2, 12,0, 14,7, 16,6, 16,9, 17,9, 18,4, 22,5, 24,5, 27,6 на порошковій рентгенівській дифрактограмі кристалів. 2. Спосіб отримання кристалічної форми А (3R,4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (1) кристалізують в складному ефірі як розчиннику. 3. Спосіб отримання кристалічної форми А (3R,4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2H-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (1) кристалізують в аліфатичному вуглеводні як розчиннику. 4. Спосіб отримання кристалічної форми А (3R,4S)-7-гідроксиметил-2,2,9-тpимeтил-4(фeнeтилaмiнo)-3,4-дигiдpo-2H-пірано[2,3-g]хінолін-3-oлy, який відрізняється тим, що сполуку Формули (1) кристалізують в нітрилі як розчиннику. 5. Спосіб отримання кристалічної форми А (3R,4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (1) кристалізують в ароматичному вуглеводні як розчиннику. 6. Спосіб отримання кристалічної форми А (3R,4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (1) кристалізують в кетоні як розчиннику. 7. Кристалічна форма В (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро2Н-пірано[2,3-g]хінолін-3-олу Формули (1): Ph HN N OH HO (1) O 11 UA 105385 C2 що має характеристичні піки при кутах дифракції (2θ) 6,4, 8,7, 12,8, 17,5, 19,1, 20,7, 22,0, 24,8, 26,6 на порошковій рентгенівській дифрактограмі кристалів. 8. Кристалічна форма Е (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро2H-пірано[2,3-g]хінолін-3-олу Формули (1): 5 Ph HN N OH HO (1) O 10 що має характеристичні піки при кутах дифракції (2θ) 9,1, 12,8, 13,1, 14,6, 15,2, 16,4, 22,1, 23,6, 24,8 на порошковій рентгенівській дифрактограмі кристалів. 9. Кристалічна форма F (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро2Н-пірано[2,3-g]хінолін-3-олу Формули (1): Ph HN N OH HO (1) O 15 що має характеристичні піки при кутах дифракції (2θ) 6,8, 11,7, 13,7, 16,8, 18,0, 19,3, 20,4, 20,8, 24,6, 25,6 на порошковій рентгенівській дифрактограмі кристалів. 10. Кристалічної форма G (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4дигідро-2Н-пірано[2,3-g]хінолін-3-олу Формули (1): Ph HN N OH HO (1) O 20 що має характеристичні піки при кутах дифракції (2θ) 6,7, 11,6, 11,9, 13,6, 16,6, 17,7, 18,6, 19,1, 19,8, 20,1, 20,8 на порошковій рентгенівській дифрактограмі кристалів. 11. Кристалічна форма H (3R,4S)-7-гідроксиметил-2,2,9-триметил-4-(фенетиламіно)-3,4-дигідро2Н-пірано[2,3-g]хінолін-3-олу Формули (1): Ph HN N OH HO (1) O 12 UA 105385 C2 5 10 15 20 що має характеристичні піки при кутах дифракції (2θ) 6,0, 16,4, 17,0, 19,2, 19,8, 20,3, 21,0, 22,8 на порошковій рентгенівській дифрактограмі кристалів. 12. Спосіб отримання кристалічної форми В (3R,4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (1) кристалізують в органічному розчиннику, що містить воду. 13. Спосіб отримання кристалічної форми Е (3R,4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (1) нагрівають і розчиняють в складному ефірі оцтової кислоти як розчиннику або в кетоні як розчиннику, швидко додають аліфатичний вуглеводень як розчинник і миттєво охолоджують. 14. Спосіб отримання кристалічної форми F (3R,4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (1) кристалізують з етанолу. 15. Спосіб отримання кристалічної форми G (3R,4S)-7-гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (1) кристалізують в 2-пропанолі. 16. Спосіб отримання кристалічної форми Н (3R,4S)-7гідроксиметил-2,2,9-триметил-4(фенетиламіно)-3,4-дигідро-2Н-пірано[2,3-g]хінолін-3-олу, який відрізняється тим, що сполуку Формули (І) нагрівають і розчиняють в простому ефірі як розчиннику, швидко додають циклогексан і миттєво охолоджують. 13 UA 105385 C2 14 UA 105385 C2 15 UA 105385 C2 16 UA 105385 C2 17 UA 105385 C2 Комп’ютерна верстка І. Мироненко Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 18
ДивитисяДодаткова інформація
Назва патенту англійськоюNovel crystal forms of tricyclic benzopyran compound and processes for producing same
Автори англійськоюTakada, Yasutaka, Kamon, Miyako, Kawahara, Shiro, Umeda, Yasuhiro
Автори російськоюТакада Ясутака, Камон Мияко, Кавахара Сиро, Умеда Ясухиро
МПК / Мітки
МПК: C07D 491/052
Мітки: кристалічна, сполуки, трициклічного, спосіб, бензопірану, форма, варіанти, отримання
Код посилання
<a href="https://ua.patents.su/20-105385-kristalichna-forma-spoluki-triciklichnogo-benzopiranu-i-sposib-otrimannya-varianti.html" target="_blank" rel="follow" title="База патентів України">Кристалічна форма сполуки трициклічного бензопірану і спосіб її отримання (варіанти)</a>
Попередній патент: Лікування порушень, пов’язаних з інсулінорезистентністю
Наступний патент: Гуманізовані анти-egfl7-антитіла і способи їх застосування
Випадковий патент: Телекомунікаційна система широкополосного радіодоступу з інтеграцією засобів радіо- і проводового доступу "мітріс-е"