Спосіб паралельного синтезу аліфатичних оксамідів
Формула / Реферат
1. Спосіб паралельного синтезу аліфатичних оксамідів загальної формули (І):
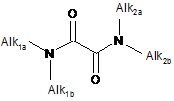 ,
,
де
Аlk1ата Аlk1b кожен незалежно являє собою Н або С1-С6 алкіл, який необов'язково заміщений одним або більшою кількістю замісників, незалежно вибраних з С1-С6алкілу, С1-С6алкокси, С3-С10циклоалкілу, С6-С10арилу, С2-С9гетероарилу, галогену, -CN, NO2, NH2, -SC1-С6алкілу, -SOC1-C6алкілу, -SO2C1-C6алкілу, -NSO2C1-C6алкілу, -NHC1-C6алкілу, -N(C1-C6алкіл)2, -NHCOOC1-C6алкілу, -NHCONHC1-C6алкілу, -CONHC1-C6алкілу, -СОС1-С6алкілу, -СООС1-С6алкілу, -SC1-С6алкілу, -SOC1-С6алкілу або -SO2C1-C6алкілу, де згадані С1-С6алкільні, С3-С10циклоалкільні, С6-С10арильні або С2-С9гетероарильні частини згаданих вище замісників можуть бути також заміщені одним або більшою кількістю додаткових замісників, незалежно вибраних з С1-С6алкілу, С1-С6алкокси, С3-С10циклоалкілу, С6-С10арилу, C2-C9гетероарилу, галогену, ОН, -CN, NO2 або NH2;
або Аlk1а та Аlk1b можуть бути об'єднані разом, утворюючи 5- або 6-членну циклічну систему, що містить як елемент кільця атом N, до якого вони приєднані, і необов'язково містить в кільці ще один додатковий гетероатом, такий як N, О або S, де утворене кільце необов'язково заміщене одним або більшою кількістю замісників, незалежно вибраних з =O, С1-С6алкілу, С6-С10арилу, де С1-С6алкільний та С6-С10арильний фрагменти необов'язково заміщені одним або більшою кількістю замісників, незалежно вибраних з галогену, ОН, С1-С6алкілу, С1-С6алкокси, С3-С10циклоалкілу, С6-С10арилу, -СООС1-С6алкілу;
Аlk2а та Аlk2b кожен незалежно являє собою Н або С1-С6алкіл, який необов'язково заміщений одним або більшою кількість замісників, незалежно вибраних з С1-С6алкілу, С1-С6алкокси, С3-С10циклоалкілу, С6-С10арилу, С2-С9гетероарилу, галогену, -CN, NO2, NH2, -SC1-C6алкілу, -SOC1-C6алкілу, -SO2C1-C6алкілу, -NSO2C1-C6алкілу, -NHC1-C6алкілу, -N(C1-C6алкілу)2, -NHCOOC1-C6алкілу, -NHCONHC1-C6алкілу, -CONHC1-C6алкілу, -СОС1-С6алкілу, -СООС1-С6 алкілу, -SC1-C6алкілу, -SOC1-С6алкілу або -SO2C1-C6алкілу, де згадані С1-С6алкільні, С3-С10 циклоалкільні, С6-С10 арильні або С2-С9 гетероарильні частини згаданих вище замісників можуть бути також заміщені одним або більшою кількістю додаткових замісників, незалежно вибраних з С1-С6 алкілу, С1-С6 алкокси, С3-С10 циклоалкілу, С6-С10 арилу, С2-С9 гетероарилу, галогену, ОН, -CN, NO2 або NH2;
або Alk2a та Аlk2b можуть бути об'єднані разом, утворюючи 5- або 6-членну циклічну систему, що містить як елемент кільця атом N, до якого вони приєднані, і необов'язково містить в кільці ще один додатковий гетероатом, такий як N, О або S, де утворене кільце необов'язково заміщене одним або більшою кількістю замісників, незалежно вибраних з =O, С1-С6алкілу, С6-С10арилу, де С1-С6алкільний та С6-С10арильний фрагмент, необов'язково заміщені одним або більшою кількістю замісників, незалежно вибраних з галогену, ОН, С1-С6алкілу, С1-С6алкокси, С3-С10циклоалкілу, С6-С10арилу, -СООС1-С6алкілу;
що включає приведення в контакт оксалату формули (II):
 ,
,
де R являє собою Н, Me або CF3;
спочатку з аміном формули (III):
![]() ,
,
де Alk1a тa Аlk1b є такими як визначено вище;
а потім з аміном формули (IV):
![]() ,
,
де Аlk2a та Аlk2b є такими як визначено вище;
з одержанням N1,N2-заміщених оксамідів загальної формули (І).
2. Спосіб за пунктом 1, який відрізняється тим, що реакції оксалату (II) з амінами (III) та (IV), необов'язково, проводять при нагріванні.
Текст
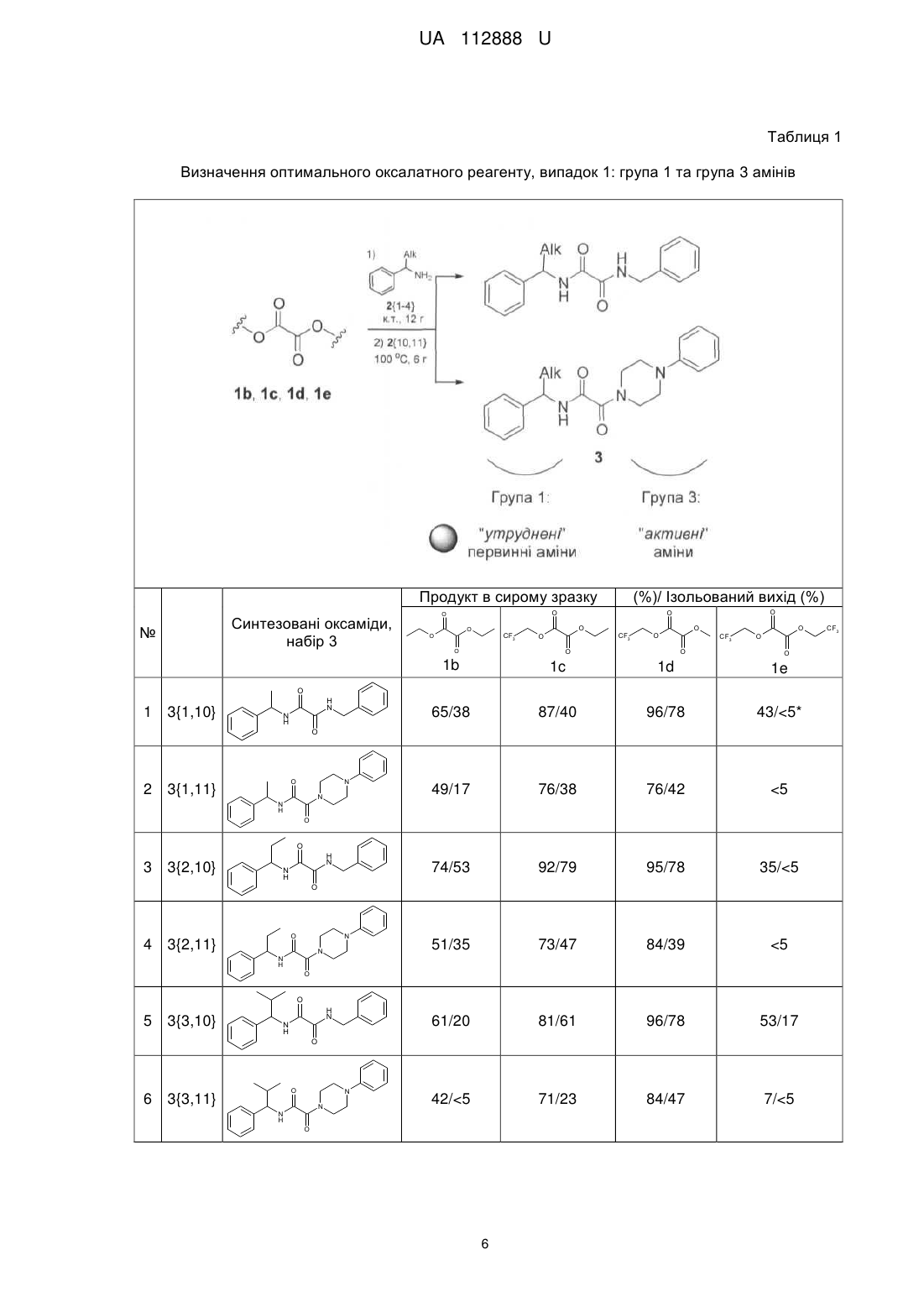
Реферат: Спосіб паралельного синтезу аліфатичних оксамідів загальної формули (І): Alk2a O Alk1a N N Alk1b Alk2b O , де Аlk1ата Аlk1b кожен незалежно являє собою Н або С1-С6алкіл, який необов'язково заміщений одним або більшою кількістю замісників, незалежно вибраних з С1-С6алкілу, С1-С6алкокси, С3С10циклоалкілу, С6-С10арилу, С2-С9гетероарилу, галогену, -CN, NO2, NH2, -SC1-С6алкілу, -SOC1C6алкілу, -SO2C1-C6алкілу, -NSO2C1-C6алкілу, -NHC1-C6алкілу, -N(C1-C6алкіл)2, -NHCOOC1C6алкілу, -NHCONHC1-C6алкілу, -CONHC1-C6алкілу, -СОС1-С6алкілу, -СООС1-С6алкілу, -SC1С6алкілу, -SOC1-С6алкілу або -SO2C1-C6алкілу, де згадані С1-С6алкільні, С3-С10циклоалкільні, С6С10арильні або С2-С9гетероарильні частини згаданих вище замісників можуть бути також заміщені одним або більшою кількістю додаткових замісників, незалежно вибраних з С 1С6алкілу, С1-С6алкокси, С3-С10циклоалкілу, С6-С10арилу, C2-C9гетероарилу, галогену, ОН, -CN, NO2 або NH2. UA 112888 U (54) СПОСІБ ПАРАЛЕЛЬНОГО СИНТЕЗУ АЛІФАТИЧНИХ ОКСАМІДІВ UA 112888 U UA 112888 U 5 10 15 20 25 30 Корисна модель стосується галузі органічної хімії, а саме способу одержання аліфатичних оксамідів, що можуть знайти застосування як біологічно активних сполук. Концепція "Escape the Flatland" ("Відход від пласких") є важливою частиною сучасного процесу розробки ліків: як зазначається в недавніх публікаціях, складність і об'ємність молекулкандидатів при пошуку ліків - серед основних характеристик. Концепція полягає у заміні плоских 3 ароматичних частин в молекулі на зр -збагачений фрагмент, який матиме позитивний вплив на важливі властивості ліків: він зменшує ліпофільність і токсичність, підвищує розчинність, проникність і поліпшує доступність при пероральному прийомі. Важливим аспектом цього є розробка відповідних методів для складання молекул з "насичених" фрагментів. Задачею 1 2 останнього проекту було знайти спосіб синтезу різноманітних несиметричних N ,N -заміщених аліфатичних оксамідів. Такий фрагмент можна знайти у медичній і синтетичній органічній хімії, 1 2 але простий синтетичний шлях до бібліотек N ,N -заміщених аліфатичних оксамідів залишався невідомим. Типова стратегія отримання бібліотек сполук основана на паралельному синтезі. Критерії паралельного синтезу: 1) використання простих реакцій та процедур; 2) використання доступних субстратів, які забезпечують різноманітність бібліотек; 3) застосованість методів до різних субстратів. 1 2 Поширений синтетичний підхід до несиметричних N ,N -заміщених аліфатичних оксамідів поступовий аміноліз етилхлорооксоацетату (1a) [V.G. Albano, M. Bandini, M. Моnаrі, Е. Marcucci, F. Piccinelli, A. Umani-Ronchi, J. Org. Chem. 2006, 71, 6451-6458) чи діетилоксалату (1b) (J. В. Hynes, G. R. Gale, L. M. Atkins, D. M. Cline, K. F. Hill, J. Med. Chem. 1973, 16, 576-578.; X. Luo, С Li, Y. Liang, Chem. Commun. 2000, 2091-2092]. Ha перший погляд, процедура задовольняє нашим критеріям, але ретельніше дослідження показало, що реагенти 1а і 1b були несумісні з паралельним синтезом. Аміноліз 1а енергійно відбувався з аліфатичними амінами і вимагав повільного додавання реагентів за низької температури для одержання чистого моноаміду. Аміноліз 1b з активними амінами був успішно досягнутий, але він зазнав невдачі зі стерично ускладненим аміно-субстратом. Вирішення дилеми "занадто активний - занадто інертний" може бути у введенні менш активного реагенту. а) Відомий підхід - "колба" двостадійний синтез 1 UA 112888 U 5 10 Наш попередній досвід з несиметричними аліфатичними сечовинами показав, що заміна етилхлорформіату та діетилкарбонату на біс-2,2,2-трифторетильний аналог призводить до високої хемоселективності амінолізу. Таким чином, цей підхід уможливив паралельний синтез. Дійсно, помірно реактивний біс(2,2,2-трифторетил)карбонат довів свою ефективність з різними аліфатичними амінами при одержанні сечовин з виходами чистого продукту 30-90 %. Винахідник розширив цю стратегію на аліфатичні оксаміди, впровадивши 2,2,2трифторетилоксалатні похідні як альтернативу відомих реагентів. Відповідно, об'єктом даної корисної моделі став однореакторний спосіб паралельного синтезу ускладнених аліфатичних оксамідів загальної формули (І): Alk2a O Alk1a Alk1b 15 20 25 30 35 N N Alk2b O , де Аlk1a та Аlk1b кожен незалежно являє собою Н або С1-С6алкіл, який необов'язково заміщений одним або більшою кількістю замісників незалежно вибраних з С 1-С6 алкілу, С1-С6алкокси, С3С10циклоалкілу, С6-С10арилу, С2-С9гетероарилу, галогену, -CN, NO2, NH2, -SC1-C6алкілу, -SOC1C6алкілу, -SO2C1-C6алкілу, -NSO2C1-C6алкілу, -NHC1-C алкілу, -N(C1-C6 алкілу)2, -NHCOOC1C6алкілу, -NHCONHC1-C6алкілу, -CONHC1-C6алкілу, -СОС1-С6алкілу, -СООС1-С6алкілу, -SC1С6алкілу, -SOC1-С6алкілу або –SО2С1-С6алкілу, де згадані С1-С6алкільні, С3-С10циклоалкільні, С6С10арильні або С2-С9гетероарильні частини згаданих вище замісників можуть бути також заміщені одним або більшою кількістю додаткових замісників незалежно вибраних з С 1-С6алкілу, С1-С6алкокси, С3-С10циклоалкілу, С6-С10 арилу, С2-С9гетероарилу, галогену, ОН, -CN, NO2 або NH2; або Alk1a та Аlk1b можуть бути об'єднані разом утворюючи 5- або 6-членну циклічну систему, що містить як елемент кільця атом N до якого вони приєднані, і необов'язково містить в кільці ще один додатковий гетероатом, такий як N, О або S, де утворене кільце необов'язково заміщене одним або більшою кількістю замісників незалежно вибраних з =O, С1-С6алкілу, С6С10арилу, де С1-С6алкільний та С6-С10арильний фрагмент необов'язково заміщені одним або більшою кількістю замісників, незалежно вибраних з галогену, ОН, С1-С6алкілу, С1-С6алкокси, С3-С10циклоалкілу, С6-С10арилу, -СООС1-С6алкілу; Alk2a тa Аlk2b кожен незалежно являє собою Н або С1-С6 алкіл, який необов'язково заміщений одним або більшою кількістю замісників, незалежно вибраних з С 1-С6алкілу, С1С6алкокси, С3-С10циклоалкілу, С6-С10арилу, С2-С9гетероарилу, галогену, -CN, NO2, NH2, -SC1С6алкілу, -SOC1-C6алкілу, -SO2C1-C6алкілу, -NSO2C1-C6алкілу, -NHC1-C6алкілу, -N(C1-C6 алкіл)2, NHCOOC1-C6алкілу, -NHCONHC1-C6алкілу, -CONHC1-C6алкілу, -СОС1-С6алкілу, -СООС1С6алкілу, -SC1-С6алкілу, -SOC1-С6алкілу або -SO2C1-C6алкілу, де згадані C1-C6алкільні, С3С10циклоалкільні, С6-С10арильні або С2-С9гетероарильні частини згаданих вище замісників можуть бути також заміщені одним або більшою кількістю додаткових замісників, незалежно 2 UA 112888 U 5 10 вибраних з С1-С6алкілу, С1-С6алкокси, С3-С10циклоалкілу, С6-С10арилу, С2-С9гетероарилу, галогену, ОН, -CN, NO2 або NH2; або Alk2a та Аlk2b можуть бути об'єднані разом утворюючи 5- або 6-членну циклічну систему, що містить як елемент кільця атом N, до якого вони приєднані, і необов'язково містить в кільці ще один додатковий гетероатом, такий як N, О або S, де утворене кільце необов'язково заміщене одним або більшою кількістю замісників, незалежно вибраних з =O, С 1-С6алкілу, С6С10арилу, де С1-С6алкільний та С6-С10арильний фрагмент необов'язково заміщені одним або більшою кількістю замісників, незалежно вибраних з галогену, ОН, C1-С6алкілу, С1-С6алкокси, С3-С10циклоалкілу, С6-С10арилу, -СООС1-С6алкілу; що включає приведення в контакт оксалату формули (II): O CF3 O O O R , де R являє собою Н, Me або CF3; спочатку з аміном формули (III): Alk1a Alk1bHN 15 , де Alk1a тa Аlk2b є такими як визначено вище; а потім з аміном формули (IV): Alk2a Alk2bHN 20 25 30 35 40 45 50 55 , де Аlk2a та Аlk2b є такими як визначено вище; 1 2 з одержанням N ,N -заміщених оксамідів загальної формули (І). Вказані вище реакції оксалату (II) з амінами (III) та (IV), необов'язково проводять при нагріванні. Термін "С1-С6 алкіл" стосується алкільного радикала, що має від одного до шести атомів вуглецю, і має нерозгалужену або розгалужену будову. Прикладами алкільних груп є, але не обмежується, метил, етил, пропіл, ізопропіл, бутил, ізобутил, втор-бутил, тpeт-бутил, пентил, 2пентил, 3-пентил, ізопентил, неопентил, (R)-2-метилбутил, (S)-2-метилбутил, 3-метилбутил, 2,3диметилпропіл, 2,3-диметилбутил, гексил і т.і. Термін "С1-С6алкокси", стосується алкокси радикала, що має від одного до шести атомів вуглецю, що мають нерозгалужену або розгалужену будову. Алкокси групами є, але не обмежується, метокси, етокси, пропокси, ізопропокси, бутокси, гексилокси і т.і. Термін "С3-С10циклоалкіл", як тут використовується, стосується моно, конденсованих або місткованих біциклічних або трициклічних карбоциклічних кілець, що містять, в деяких втіленнях, від трьох до десяти атомів вуглецю. Як тут використовується, циклоалкільні кільця можуть необов'язково містити один або два подвійні зв'язки. Термін "циклоалкіл" також включає спіроциклоалкільні групи, включаючи поліциклічні системи, зв'язані через один атом. Циклоалкільними групами є, але не обмежується, циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил, циклопентеніл, циклогексеніл, біцикло[2.2.1]гептаніл, біцикло[3.2.1]октаніл, біцикло[5.2.0]нонаніл, адамантил і т.і. Термін "С6-С10 арил", як тут використовується, стосується групи, що походить від ароматичного вуглеводню, що містить від шести до десяти атомів вуглецю. Прикладами таких груп є, але не обмежується, феніл і нафтил. Термін "арил" також включає конденсовані поліциклічні ароматичні системи, в яких ароматичне кільце є конденсованим з одним або більше кілець. Прикладами є, але не обмежується, 1-нафтил, 2-нафтил, 1-антрацил і 2антрацил. Також включеними в межі рамок терміну "арил", як тут використовується, є група, в якій ароматичне кільце є конденсованим з одним або більше неароматичних кілець, таким як інданіл, фенантридиніл або тетрагідронафтил, де радикал або точка приєднання знаходиться на ароматичному кільці. Термін "С2-С9 гетероарил, як тут використовується, стосується ароматичної моноциклічної або біциклічної гетероциклічної групи, що має загалом від 5 до 9 атомів в кільці, і що містить від 2 до 9 атомів вуглецю і від одного до чотирьох гетероатомів, що незалежно вибирають з азоту, кисню і сірки, за умови, що кільце згаданої групи не містить два сусідні атоми кисню або два сусідні атоми сірки. Гетероарильні групи є бензо-конденсованими циклічними системами. Прикладами гетероарильних груп є, але не обмежується, піроліл, фурил, тієніл, імідазоліл, піразоліл, оксазоліл, ізоксазоліл, ізотіазоліл, триазоліл, оксадіазоліл, фуразаніл, тіадіазоліл, тіазоліл, тетразоліл, піридиніл, піразиніл, піримідил, піридазиніл, триазиніл, індоліл, ізоіндоліл, індолізиніл, бензофураніл, бензотіофеніл, індазоліл, бензімідазоліл, бензоксазоліл, фуро[3,2 3 UA 112888 U 5 10 15 20 b]піридиніл, бензотіазоліл, бензофуразаніл, пуриніл, хінолініл, ізохінолініл, хіназолініл, хіноксалініл, нафтиридиніл, цинолініл, фталазиніл, піридо[3,4-b]піримідил, піридиніл і т.і. Розроблений однореакторний спосіб включає два типи реагентів: аміни і оксалати, і перша частина дослідження полягала у визначенні оптимального оксалатного реагенту, а друга частина мала визначити обмеження способу. Для отримання оксалатних реагентів, ми вибрали три відомі похідні 2,2,2-трифторетилу: етил (2,2,2-трифторетил)оксалат (1с), метил (2,2,2трифторетил)оксалат (1d) і біс(2,2,2-трифторетил)оксалат (1е), і 1b як еталон. Ефективність амінолізу зростає зі зменшенням величини рКа спирту, якому відповідає вибраний естер (значення рКа для етанолу, метанолу та 2,2,2-трифторетанолу є 16, 15,5 та 12,5, відповідно). Реакційна здатність цих реагентів, таким чином, збільшиться від 1b до 1е. Як амінні субстрати були вибрані 36 аліфатичних амінів з нашого складу, 11 з яких - для оптимізації умов реакції (набір 2). Увагу було зосереджено на оптимізації реакцій просторово-ускладнених амінів, тому що вони були основними причинами невдач у реакціях амінолізу. Аміносубстрати було розділено на групи за ускладненими первинними (групи 1, 2{1-4}) і ускладненими вторинними амінами (група 2, 2{5-9}), але також були включені два неутруднені або активні аміни (група 3, 2{ 10-11}), щоб дослідити більше комбінацій. Фенілвмісні аміни були вибрані для легкої ідентифікації за допомогою РХ-МС. Оксалат-реагенти мають підтримувати а) Хемоселективне утворення естеру моноаміду, але не побічних продуктів - симетричних бісамідів при першому амінолізі і b) ефективне перетворення естеру моноаміду в продукт при другому амінолізі. Для того, щоб визначити оптимальну похідну оксалату, ми провели 72 реакції (по 18 на оксалат) на мілімолярній шкалі при введенні ускладнених амінів 2 {1-9}, групи 1, 2, в першому амінолізі і активних амінів 2 {10 4 UA 112888 U 5 10 15 20 25 30 35 11}, група 3, - в другому амінолізі (таблиця 1). Було використано одностадійну процедуру, схожу з процедурою для несиметричних аліфатичних сечовин. Віалу з розчином першого аміну 2 (1 екв) і оксалату (1 екв) у ацетонітрилі (1 мл) витримували при кімнатній температурі протягом 12 год. при періодичному струшуванні. Потім додавали 1 екв 2 {10} або 2 {11} (1 екв) і реакційну суміш нагрівали при 100° С протягом 6 годин. Застосували дві різні процедури обробки в залежності від характеру реакційних сумішей. Якщо продукт випадав в осад, його фільтрували і сушили в сушильній шафі. В інших випадках, проводили екстракцію СНСl3. Вміст продукту в 1 сирих сумішах визначали за допомогою РХ-МС або Н ЯМР. Зразки з чистотою нижче 90 %, піддавали флеш-хроматографії. Всі синтезовані сполуки були охарактеризовані з 1 13 використанням ЯМР Н і С і РХ-МС, щоб підтвердити їх ідентичність і чистоту. Комбінаторний підхід часто означає низькі виходи для чистих продуктів, незважаючи на високий вміст продукту в сирих сумішах після реакції. Низькі виходи часто є результатом застосування єдиного методу очищення, що є оптимальним для більшості сполук, але не для всього набору. Аналіз, оснований на ізольованих виходах може призвести до неправильних висновків про ефективність досліджуваної реакції. Тому ми використовували вміст продукту в сирому зразку як основний параметр при аналізі отриманих даних. Експерименти виявили два випадки з урахуванням типів амінів. Реакції, де використовуються ускладнені первинні аліфатичні аміни (Таблиця 1), були успішними з несиметричними реагентами 1с і Id, вміст продукту в неочищеній суміші був 70-96 %. Реагент 1b був менш ефективний, ніж 1с і 1d при тих же умовах, в той час як експерименти з 1е не вдалися, і дали в основному симетричні побічні продукти. Ізольовані виходи для оксамідів 3 {1-4, 10-11} були вище в реакції з реагентами 1с і 1d, ніж в реакціях з 1b. Ми були не в змозі ізолювати сполуки 3 {1,10-11}, 3 {2,10-11}, і 3 {3,11} в експериментах з 1e. Утворення естеру моноаміду вимагає збалансованої активності аміну і оксалату, щоб забезпечити повне завершення реакції, але уникнути симетричних побічних продуктів. Акцепторні 2,2,2-трифторетил-групи могли б модулювати активність досліджуваних оксалатів. Цей ефект підтримує хемоселективне утворення складних естерів моноамідів з реагентів 1c-d і ускладенних первинних аліфатичних амінів 2 {1-4} в той час як 1е пройшли повний аміноліз, що дало симетричні бісаміди. Аналіз неочищених сумішей для експериментів 3 {1-4, 10-11} чітко довів висновок, наведений вище. Крім того, ці експерименти підтримали нашу концепцію: заміщення етильної групи на 2,2,2-трифлуоретильну позитивно впливає на перший аміноліз, що приводить до більших виходів чистого продукту в реакціях з 1с і 1d, ніж ті, що з 1b. Об'єднані дані, таким чином, дозволяють визначити оксалати 1с або 1d як оптимальні реагенти в паралельному 1 2 синтезі N N -заміщених аліфатичних оксамідів (процедура А, в експериментальній частині). Реакції, де викоритовується стерично ускладений вторинний аліфатичний амін (Таблиці 2), були успішними з реагентом 1е, в той час як з 1b, 1c, 1d реакції не відбувались. Аналіз РХ-МС показав вміст продукту 54-97 % в дослідах з 1е - щонайменше в 2,5 разу більший, ніж з іншими оксалатними реагентами. 40 5 UA 112888 U Таблиця 1 Визначення оптимального оксалатного реагенту, випадок 1: група 1 та група 3 амінів Продукт в сирому зразку № Синтезовані оксаміди, набір 3 (%)/ Ізольований вихід (%) O O O O CF3 O O O O O CF3 O O O O CF3 O O O 1b 1c 1d 1e 65/38 87/40 96/78 43/
ДивитисяДодаткова інформація
МПК / Мітки
МПК: C07C 233/56
Мітки: паралельного, синтезу, аліфатичних, спосіб, оксамідів
Код посилання
<a href="https://ua.patents.su/20-112888-sposib-paralelnogo-sintezu-alifatichnikh-oksamidiv.html" target="_blank" rel="follow" title="База патентів України">Спосіб паралельного синтезу аліфатичних оксамідів</a>
Попередній патент: Спосіб одержання 3,5-дизаміщених 1,2,4-оксадіазолів
Наступний патент: Спосіб о-дифлуорометилування функціоналізованих аліфатичних спиртів
Випадковий патент: Місцевий склад для попередження ампутації інфікованих кінцівок та спосіб його отримання, місцевий ранозагоювальний склад та його спосіб отримання і застосування