Спосіб одержання 4-нітро та/або 4-нітрозодифеніламіну або їх похідних, спосіб одержання 4-амінодифеніламіну або його заміщених похідних та спосіб одержання алкілованих р-фенілендіамінів або їх заміщених похідних
Номер патенту: 26851
Опубліковано: 29.12.1999
Автори: ШТЕРН Майкл Кейт, ЕЛЛМАН Джеймс Малькольм, БЕШКІН Джеймс Кін, РЕЙНС Роджер Керанен
Текст
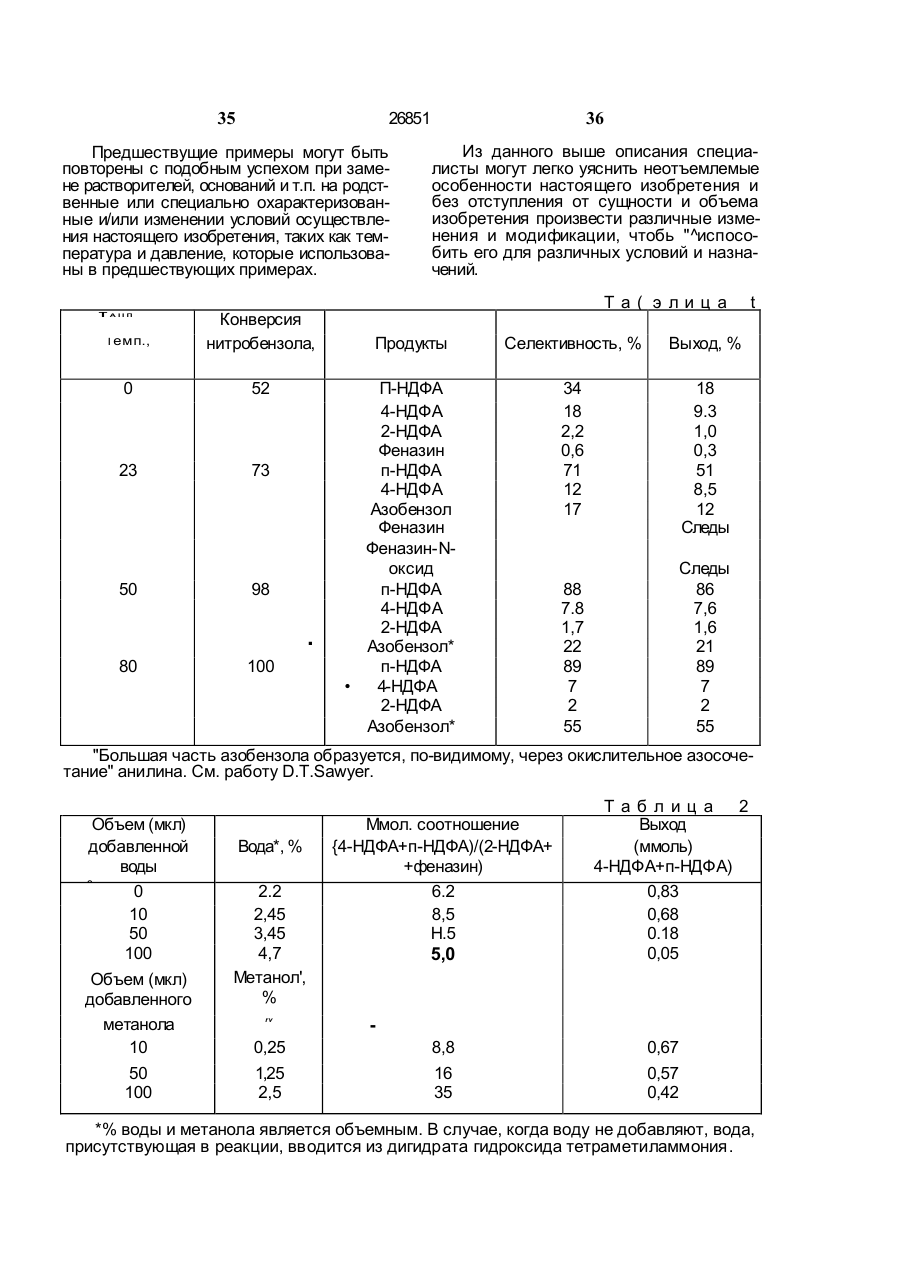
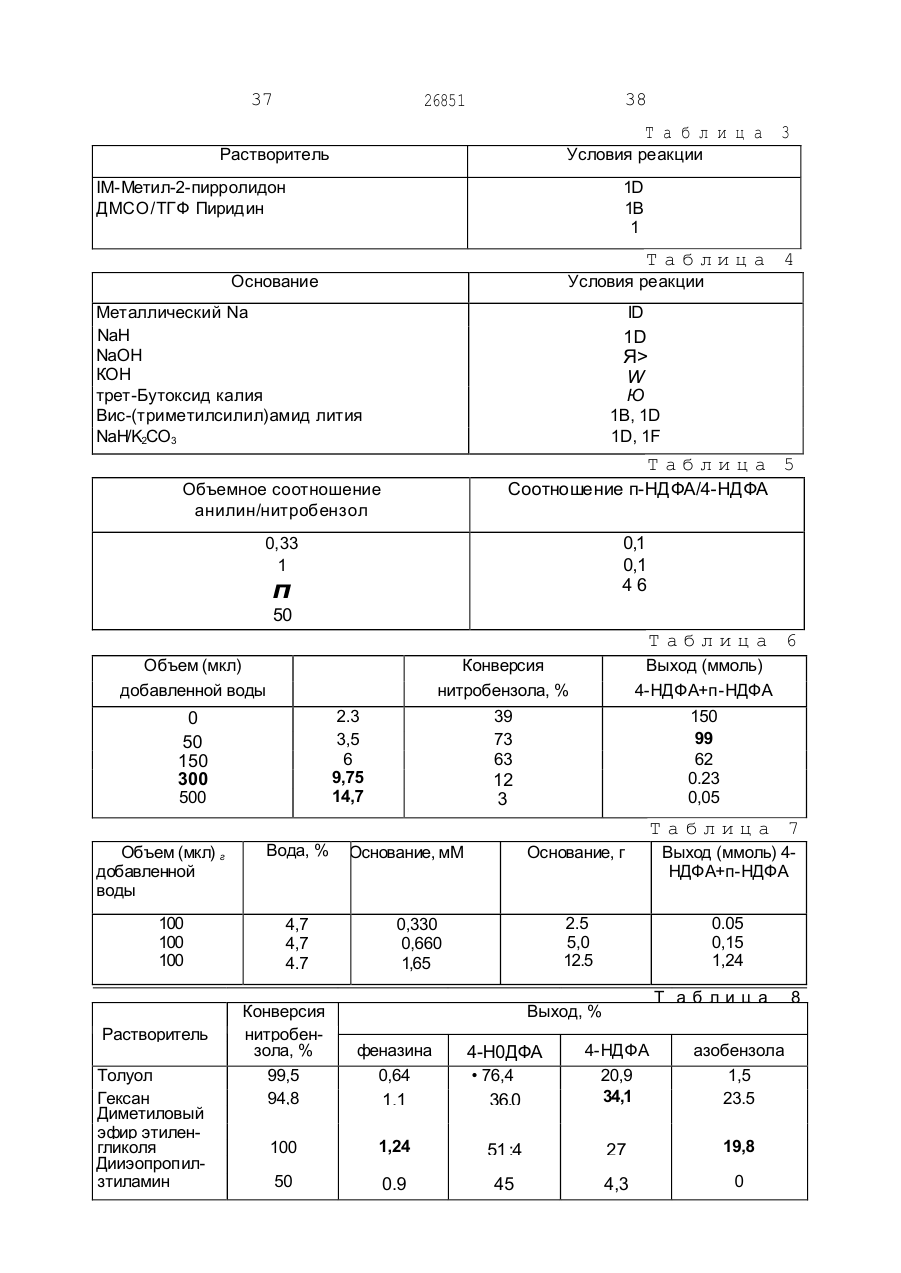
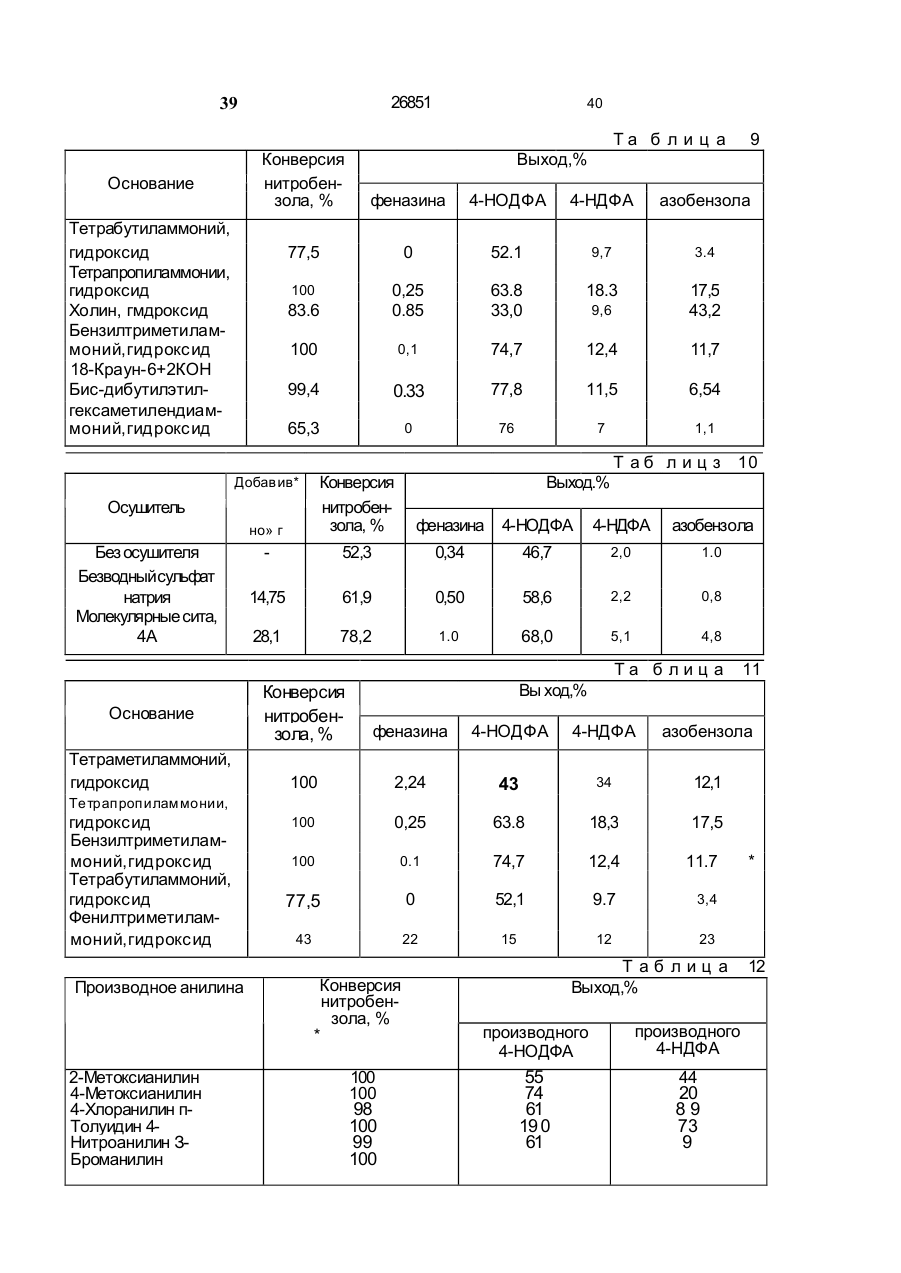
УКРАЇНА (19) UA ( 11) _2685I С 07 С 209/36, С 07 С 209/38, С 07 С 211/55, С 07 С 211/56 ДЕРЖАВНЕ ПАТЕНТНЕ ВІДОМСТВО С1 _«_ у* (П) ОПИС ДО ПАТЕНТУ НА ВИНАХІД (54) СПОСІБ ОДЕРЖАННЯ 4-НІТРО ТА/АБО 4-НІТРОЗОДИФЕНІЛАМІНУ АБО ЇХ ПОХІДНИХ, СПОСІБ ОДЕРЖАННЯ 4-АМІНОДИФЕНІЛАМІНУ АБО ЙОГО ЗАМІЩЕНИХ ПОХІДНИХ ТА СПОСІБ ОДЕРЖАННЯ АЛКІЛОВАНИХ Р-ФЕНІЛЕНДІАМІНІВ АБО ЇХ ЗАМІЩЕНИХ ПОХІДНИХ 1 (21) 93003978 (22) 27.03.92 (24) 29.12.99 (31) 07/719.876 (32) 21.06.91 (33) US (86) PCT/US92/02232 (27.03.92) ' (46) 29.12.99. Бюл. № 8 (56) Патент DE № 3501698, кл. С 07 С 87/60, 1986. Патент ЕР № 0107336, кл. С 07 С 87/58, 1984. (72) Еллман Джеймс Малькольм (US), БешКІН Джеймс Кін (US), Рейне Роджер Керанен (US), Штерн Майкл Кейт (US) (73) Монсанто к омпані (US) (57) 1. Способ получения 4-нитро и/или 4-нитрозодифениламина или их производ ных путем взаимодействия анилина или его производного с нитробензолом в при сутствии основания в растворителе, о тл и ч а ю щ и й с я тем, что указанную реакцию проводят в присутствии необхо димого количества вещества, являющего ся донором протонов. 2. Способ по п. 1, о т л и ч а ю щи й с я тем, что включает стадии: а) приведения в реакционный контакт анилина или замещенного одним или бо лее заместителями в ароматическом коль це анилина и нитробензола в системе растворителей; б) взаимодействия анилина или заме щенных производных анилина и нитро бензола в ограниченной зоне при темпе ратуре от -10 до 150"С в присутствии органического или неорганического осно вания и необходимого количества вещест ва, являющегося донором протонов, для получения 4-нитро и/или 4-нитрозодифе ниламина или их производных. 3. Способ по любому из пп. 1,2, от л и ч а ю щ и й с я тем, что упомянутая система растворителей включает раство ритель, выбираемый из анилина, нитро бензола, диметилсульфоксида, диметилформамида, N-метилпирролидона, пири дина, толуола, гексана, диметилового эфира этиленгликоля, диизопропилэтиламина и их смесей. 4. Способ по п. 3, о т л и ч а ю щ и й с я тем, что растворитель выби рают из анилина, диметилсульфоксида, диметилформамида и толуола. 5. Способ по п. 3, о т л и ч а ю щ и й с я тем, что подходящая система растворителей включает в себя протон ный растворитель. 6. Способ по п. 5, о т л и ч а ю щ и й с я тем, что упомянутый протонный растворитель выбирают из метанола, во ды и их смесей. 7. Способ по любому из пп. 1,2, от л и ч а ю щ и й с я тем, что упомянутая система растворителей включает анилин и до 4 об. % воды относительно об щего объема реакционной смеси. 8. Способ по любому из пп. 1,2, от л и ч а ю щ и й с я тем, что упомянутая система растворителей включает диметилсульфоксид и до 8 об. % воды относитель но общего объема реакционной смеси. 9. Способ по любому из пп. 1,2, от л и ч а ю щ и й с я тем, что упомянутая система растворителей включает в себя анилин и до 3 об. % метанола относитель но общего объема реакционной смеси. 10. Способ по любому из пп. 1, 2, о тл и ч а ю щ и й с я тем, что упомянутые органические и неорганические основа ния включают щелочные металлы, гидри ды щелочных металлов, гидроксиды ще лочных металлов, алкоксиды щелочных ме с > о со аО 26851 таллов, межфазные катализаторы в сочетании с источником основания, амины, краун-эфиры в сочетании с источником основания и их смеси. 11. Способ по любому из пп. 1,2, от л и ч а ю щ и й с я тем, что упомянутое основание выбирают из солей ариламмония, алкиламмония, арилалкиламмония и алкилдиаммония в сочетании с источни ком основания. 12. Способ по п. 1, о т л и ч а ю щ и й с я тем, что упомянутое основание смешивают с анилином или замещенным производным анилина с образованием смеси, которую затем приводят в контакт для реакции с нитробензолом. 13. Способ по п. 1, о т л и ч а ю щ и й с я тем, что упомянутый анилин или замещенное производное анилина и нитробензол смешивают, чтобы получить смесь, в которую добавляют основание. 14. Способ по п. 1, о т л и ч а ю щ и й с я тем, что упомянутый раство ритель представляет собой анилин, упо мянутое основание представляет собой гидроксид тетраалкиламмония или гидрокоид алкилзамещенного диаммония. 15. Способ по п. 1, о т л и ч а ю щ и й с я тем, что упомянутые анилин или замещенное производное анилина и нитробензол реагируют в аэробных усло виях. 16. Способ по п. 1, о т л и ч а ю щийс я тем, что упомянутые анилин или замещенное производное анилина и нитробензол реагируют в анаэробных ус ловиях. 17. Способ по л. 2, о т л и ч а ю щ и й с я тем, что на стадии (б) при сутствует осушитель, связывающий опре деленное количество воды, присутствую щей во время реакции анилина или заме щенного производного анилина и нитро бензола. 18. Способ по п. 17, о т л и ч а ю щ и й с я тем, что упомянутый осушитель выбирают из группы, сосіиящей из б езводного сульфата натрия, молекулярных сит, хлорида кальция, дигидрата гидроксида тетраметиламмония, безводного гидроксида калия, безводного гидроксида нат рия и активированного оксида алюминия. 19. Способ по п. 2, о т л и ч а ю щ и й с я тем, что количество вещества, являющегося донором протонов, на ста дии (б) регулируют посредством непре рывной отгонки вышеупомянутого вещест ва, являющегося донором протонов, 20. Способ по п. 19, о т л и ч а ю щ к й с я тем, что упомянутое вещество, являющееся донором прогонов, представляет собой воду, упомянутую воду удаляют непрерывной азеотропной отгонкой, утилизируя азеотроп вода/анилин. 21. Способ по любому из пп. 1, 2, о т л и ч а ю щ и й с я тем, что заместитель в упомянутых выше замещен ных производных анилина выбирают из группы, состоящей из атомов F, CI, Вг, групп -NO2, -NHZ , -SO3H, -СООН, алкильных групп, алкоксигрупп и арильных, алкарильных, аралкильных групп, содержа щих по крайней мере одну NHa-rpynny. 22. Способ по п. 21, о т л и ч а ю щ и й с я тем, что упомянутые замещен ные производные анилина выбирают из группы, состоящей из 2-метоксианилина, 4-метоксианилича, 4-хлоранилина, п-толуидина, 4-нитроаиилина, 3-броманилина, З-бром-4-амиі ;отолуола. п-аминобензойной кислоты, 2,4-диаминотолуола, 2,5-дихлоранилина, 1,4-фенилендиамина, 4,4'-мечилендианилина, и 1,3,5-триаминобензола. 23. Способ получения 4-аминодифениламина (4-АДФА) или его замещенных производный восстановлением соот ветствующего промежуточного соедине ния, о т л и ч а ю щ и й с я тем, что включает стадию получения промежу точных 4-нитро и/или 4-нитрозодифениламина и/или их производных реакцией анилина или его производных с нитро бензолом в растворителе в присутствии основания и необходимого количества ве щества, являющегося донором протонов и стадию их восстановления. 24. Способ получения 4-аминодифениламина или его замещенных производ ных по п. 23, о т л и ч а ю щ и й с я тем, что включает стадииа) приведения в реакционный контакт анилина, или его замещенных одним мли более заместителями в ароматическом кольце производных, и нитробензола в сис теме растворителей; б) взаимодействия анилина или его упомянутых замещенных производных и нитробензола в ограниченной зоне при температуре от -10 до 150'С в присутст вии органического или неорганического основания и необходимого количества ве щества, являющегося донором протонов, с получением 4-нитро и/или 4-нитрозодифениламина или их производных; в) восстановления 4-нитро и/или 4нитрозодифениламина или их производ ных. 25. Способ по п 24, о т л и ч а ю щ и й с я тем, что упомянутая система 26851 растворителей включает растворитея-.., выбираемый из анилина, нитробензола, циметилсульфоксида, ди метил формам и да, Nметилпирролидона, пиридина, тглуола, гексана, циметилового эфира этилен? ликоля, диизопропилэтиламина и их смзсей. 26. Способ по п. 25, о т л и ч а ю щ и й с я тем, что упомянутый раство ритель выбирают из анилина, диметилсульфоксида, диметилформамида, толуо ла и их смесей. 27. Способ по п. 25, о т л и ч а гащи й с я тем, что упомянутая подходя щая система растворителей включает протонный растворитель. 28. Способ по п. 27, о т л и ч а ю щ и й с я тем, что упомянутый протонный растворитель выбирают из метанола, во ды и их смесей. 29. Способ по п. 24, о т л и ч а ю щ и й с я тем, что упомянутая система растворителей включает анилин и до 4 об.% воды относительно общего объема реакционной смеси. 30. Способ по п. 24 о т л и ч а ю щ и й с я тем, что упомянутая система растворителей включает диметилсульфоксид и до 8 об.% воды относительно объ ема реакционной смеси. 31. Способ по п. 24, о т л и ч а ю щ и й с я тем, что упомянутая система растворителей включает анилин и до 3 об.% метанола относительно объема реак ционной смеси. 32. Способ по п. 24, о т л и ч а ющ и й с я тем, что упомянутые орга нические и неорганические основания включают щелочные металлы, гидриды щелочных металлов, гидроксиды щелоч ных металлов, межфазные катализаторы в сочетании с источником основания, ами ны, краун-эфир в сочетании с источником основания и их смеси. 33. Способ по п. 24, о т л и ч а ю щ и й с я тем, что упомянутое основание выбирают среди солей ариламмония, алкиламмония, арилалкиламмония и алкилдиаммония в сочетании с источником ос нования. 34. Способ по п. 23, о т л и ч а ю щ и й с я тем, что упомянутое основание смгшивают с анилином или замещенным производным анилина, чтобы образовать смесь, которую затем приводят а реак ционный контакт с нитробензолом. 35. Способ по п. 24, о т л и ч а ю щ и й с я тем, что упомянутый анилин или замещенное производное анилина и нитробензол смешивают, чтобы образо вать смесь, к которой добавляют основание. 36. Способ по п. 24, о т л и ч а ю щ и й с я тем, что упомянутый раство ритель представляет собой анилин, упо мянутое основание представляет с обой гидроксид тетраалкиламмония или гидроксид алкилзамещенного диаммония. 37. Способ по п. 24, о т л и ч а ю щ и й с я тем, что упомянутый анилин или замещенное производное анилина и нитробензол вводят в реакцию в аэроб ных условиях. 38. Способ по п. 24, о т л и ч а ю щ и й с я тем, что упомянутый анилин или замещенное производное анилина и нитробензот вводят во взаимодействие в анаэробных условиях. 39. Способ по п. 24, о т л и ч а ю щ и й с я тем, что упомянутые 4-нитро и/или 4-нитрозодифениламин и/или их производные восстанавливают, используя водород, в присутствии подходящего ка тализатора. 40. Способ по п. 24, о т л и ч а ю щ и й с я тем, что упомянутый катали затор представляет собой платину на уг ле, палладий на угле или никель, 41. Способ по п. 24, о т л и ч а ю щи й с я тем, что на стадии (б) при сутствует осушитель, связывающий опре деленное количество вещества, являюще гося донором протонов, присутствующего во время реакции анилина или замещен ного производного анилина и нитробензо ла. 42. Способ по п, 41, о т л и ч а ю щ и й с я тем, что упомянутый осушитель выбирают из группы, состоящей из без водного сульфата натрия, молекулярных сит, хлорида кальция, дигидрата гидроксида тетраметиламмонияг безводного гидроксида калия, безводного гидроксида нат рия и активированного оксида алюминия. 43. Способ по п. 24, о т л и ч а ю щ и й с я тем, что количество вещества, являющегося донором протонов, на ста дии (б) регулируют посредством непре рывной отгонки упомянутого вещества, яв ляющегося донором протонов. 44. Способ по п. 43, о т л и ч а ю щ и й с я тем, что упомянутое вещество, являющееся донором протонов, представ ляет собой воду, и упомянутую воду уда ляют непрерывной азеотропнои отгонкой утилизируя азеотроп вода/анилин. 45. Способ по п. 24, о т л и ч а ю щ и й с я тем, что заместитель в упо мянутых выше замещенных производных анилина выбирают из группы, состоящей 26851 из атомов F, СІ, Вг, групп -NO2, -NH2, SO3H, -COOH, алкильных групп, алкоксигрупп и арильных, алкарильных, аралкильных групп, содержащих по крайней мере одну NH -группу. 46. Способ по п. 45, о т л и ч а ю щ и й с я тем, что упомянутые замещен ные производные анилина выбирают из группы, состоящей из 2-метоксианилина, 4-метоксианилина, 4-хлоранилина, п-толуидина, 4-нитроанилина, 3-броманилина, 3бром-4-аминотолуола, п-аминобензойной кислоты, 2,4-диаминотолуола, 2,5-дихлоранилина, 1,4-фени лен диамина, 4,4'-мети~ лендианилина и 1,3,5-триаминобензола. 47. Способ получения алкилированных п - фен иле н диаминов или их замещен ных производных восстановительным ал кил и ров а ни ем 4-аминодифениламина или его замещенных производных, о тл и ч а ю щ и й с я тем, что включает стадии получения 4-нитро и/или 4-нитрозодифениламина реакцией анилина или его производных с нитробензолом в раст ворителе в присутствии основания и необ ходимого количества вещества, являюще гося донором протонов, восстановления полученного продукта с получением 4аминодифениламина или его замещенных производных и восстановительного алкилирования. 48. Способ получения алкилированных п-фенилендиаминов или их замещен ных производных по п. 47, о т л и ч аю щ и й с я тем, что включает стадии: а) приведения в реакционный контакт анилина или замещенных производных анилина и нитробензола в системе раст ворителей; б) взаимодействия анилина или его замещенных производных и нитробензола в ограниченной зоне при температуре от -10 до 150*С и в присутствии органичес кого или неорганического основания и необходимого количества вещества, яв ляющегося донором протонов; в) восстановления полученных проме жуточных соединений с получением 4-ами нодифениламина или его замещенных производных; г) восстановительного алкилирования 4аминодифениламина или его замещенных производных, полученных на стадии (в). 49. Способ по п. 48, о т л и ч а ющ и й с я тем, что упомянутая система растворителей включает растворитель, вы бираемый из анилина, нитробензола, димэтилсульфоксида, диметилформамида, Nметилпирролидона, пиридина, толуола, гексана, диметилового эфира этиленгли 8 коля, диизопропилэтиламина и их с месей. 50. Способ по п. 49, о т л и ч а ю щ и й с я тем, что упомянутый раство ритель выбирают среди анилина, диметилсульфоксида, диметилформамида, то луола и их смесей. 51. Способ по п. 49, о т л и ч а ю щ и й с я тем, что упомянутая система растворителей включает протонный раст воритель. 52. Способ по п. 51, о т л и ч а ю щ и й с я тем, что упомянутый протонный растворитель выбирают из метанола, во ды и их смес ей. 53. Способ по п. 49, о т л и ч а ю щ и й с я тем, что упомянутая система растворителей включает анилин и до 4 об.% воды относительно объема реаги рующей смеси, 54. Способ по п. 49, о т л и ч а ю щ и й с я тем, нто упомянутая система растворителей включает диметшюульфоксид и до 8 об.% воды относительно объ ема реакционной смес и. 55. Способ по п. 49, о т л и ч а ю щ и й с я тем, что упомянутая система растворителей включаат анилин и до 3 об.% метанола относительно объема реак ционной смеси. 56. Способ по п. 48, о т л и ч а ю щ и й с я тем, что упомянутые орга нические и неорганические основания включают щелочные металлы, гидриды щелочных металлов, гидроксиды щелоч ных металлов, алкоксиды щелочных ме таллов, межфазные катализаторы в соче тании с источником основания, амины, краун-эфиры в сочетании с источником основания и их смеси. 57. Способ0 по п. 49, о т л и ч а ю щ и й с я тем, что упомянутое основание выбирают среди солэй ариламмония, алкиламмония, арилалкиламмония и алкилдиаммония в сочетании с источником ос нования. 58. Способ по п. 47, о т л и ч а ю щ и й с я тем, что упомянутое основание соединяют с анилином или замещенным производными анилина с образованием смеси, которую затем приводят в реак ционный контакт с нитробензолом. 59. Способ по п. 49, о т л и ч а ю щ и й с я тем, что упомянутый анилин или замещенные производные анилина и нитробензол смешивают, чтобы образо вать смесь, к которой добавляют основа ние. 60. Способ по п. 49, с т л м ч а ющ и Й с я тем, что упомянутый растьо 26851 ритель представляет собой анилин, упомянутое основание представляет собой гидроксид тетраал кил аммония или гидроксид алкилзамещенного диаммония. 61. Способ по п. 49, о т л и ч а ю щ и й с я тем, что упомянутые анилин или замещенные производные анилина и нитробензол вводят в реакцию в аэроб ных условиях. 62. Способ по п. 49, о т л и ч а ю щ и й с я тем, что упомянутые анилин или замещенные производные анилина и нит робензол вводят в реакцию в анаэробных условиях. 63. Способ по п. 48, о т л и ч а ю щ и й с я тем, что упомянутый 4-аминодифениламин или его замещенные производные подвергают восстановитель ному алкилированию с использованием кетона, выбираемого из группы, состоя щей из ацетона, мети л изобутил кетона, ме тил изоам ил кетона и 2-октанона. 64. Способ по п. 40, о т л и ч а ю щ и й с я тем, что на стадии (б) при сутствует осушитель, связывающий опре деленное количество вещества, являюще гося донором протонов, присутствующего во время реакции анилина или замещен ного производного анилина и нитробензо ла. 65. Способ по п. 64, о т л и ч а ю щ и й с я тем, что упомянутый осушитель выбирают из группы, состоящей из без водного сульфата натрия, молекулярных сит, хлорида кальция, дигидрата гидрок 10 сида тетраметиламмония, безводного гидроксида калия, безводного гидроксида натрия и активированного оксида алюминия 66. Способ по п. 48, о т л и ч а ю щ и й с я тем, что количество вещества, являющегося донором протонов на ста дии (б) регулируют непрерывной отгонкой упомянутого вещества, являющегося до нором протонов. 67. Способ по п. 66, о т л и ч а ю щ и й с я тем, что упомянутое вещество, являющееся донором протонов, представ ляет собой воду, и упомянутую воду уда ляют непрерывной азеотропнои отгонкой, утилизируя азеотроп вода/анилин. 68. Способ по п. 48, о т л и ч а ю щ и й с я тем, что заместитель в упо мянутых выше замещенных производных анилина выбирают из группы, состоящей из атомов F, CI, Вг, групп -NO 2, -NH2 , SO3H, -COOH, алкильных групп, алкоксигрупп и арильных, алкарильных, аралкильных групп, содержащих по крайней мере одну NH.-rpynny. 69. Способ по п.68, о т л и ч а ю щ и й с я тем, что упомянутые замещен ные производные анилина выбирают из группы, состоящей из 2-метоксианилина, 4-метоксианилина, 4-хлоранилина, п-толуидина, 4-нитроанилина, 3-броманилина, З-бром-4-аминотолуола, п-аминобензойной кислоты, 2,4-диаминотолуола, 2,5-дихлоранилина, 1,4-фенилендиамина, 4,4'-метилендианилина и 1 3,5-триаминобензола. Изобретение относится к способу по4-НДФА получают путем взаимодействия лучения алкилированных п-фенилендиамип-хлорнитробензола с производным анинов, применяемых в качестве антиоксилина, таким как форманилид или его дов. Изобретение также относится к спосоль щелочного металла, в присутствии собам получения 4-нитро и/или 4-нитро- с акцептора кислоты или нейтрализующего зодифениламина и 4-аминодифенилаагента, такого как карбонат калия, и, мина (4-АДФА), которые являются пронеобязательно, с применением катализамежуточными соединениями в способе потора. См., например, Патенты США № лучения алкилированных п-фенилендиами4187248; 4683332; 4155936; 4670595; нов. 10 4122118; 4614817; 4209463, 4196146; Известный способ получения 4-АДФА 4187249, 4140716. Этот способ имеет по механизму нуклеофильного замещетот недостаток, что галогенид, который ния в ароматическом ядре, когда произзамещается, является коррозионным по водное анилина заменяет галогєнид. Этот отношению к реакторам и появляется в способ включает в себя получение про15 стРУ е отходов и, следовательно, должен межуточного соединения, а именно 4-нитбыть извлечен оттуда, что обходится дородифениламина (4-НДФА) с последуювольно дорого. Кроме того, применение щим восстановлением нитрофрагмента такого производного анилина, как форма 11 26851 нилид, и применение п-хлорнитробензола требуют дополнительного производственного оборудования и возможностей для производства таких исходных материалов из анилина и нитробензола соответственно. Также известно, что 4-АДФА получают при реакции сочетания анилина "голова к хвосту". См., например, Патент Великобритании 1440767 и Патент США 4760186. Этот способ имеет тот недостаток, что выход 4-АДФА неприемлем для производственного процесса. Также известно, что 4-АДФА получают декарбоксилироаанием уретана. См. Патент США 3847990. Однако такой способ коммерчески непрактичен с точки зрения стоимости и выхода. Известно о получении 4-АДФА гидрированием п-нитрозодифенилгидроксиламина, который может быть получен каталитической димеризацией нитрозобензола при использовании в качестве восстановителя алифатических соединений, бензола, нафталина или этиленненасыщенных соединений. См., например, Патенты США 4178315 и 4404401. Так же известно о получении 4-нитрозодифениламина из дифениламина и алкилнитрата в присутствии избытка хлористого водорода. См., например, Патенты США 4518803 и 4479008. Также известно о получении 4-нитрозедифенилаюина при взаимодействии ацетанилида и нитробензола з ДМСО в присутствии гидроксида натрип и карбоната калия при 80'С в течение 5 ч. См. Ayyangar et al. Tetrahedron Letters, vol. 31, № 22, pp. 3217-3220 (1990). См. также W oh', Chemische Berichte, 36, p. 4135 (1903) и Chemische Berichte, 34, p. 242 (1901). Однако выход 4-нитрозодифениламина является низким и, следовательно, коммерчески нецелесообразен. Кроме того, такой способ требует утилизации производного анилина, а именно ацетанилида, и, следовательно, возрастает стоимость исходных материалов. Способ настоящего изобретения не включает галогенидный источник и, следовательно, избегает дорогостоящего удаления галогенида из потока отходов. Кроме того, способ настоящего изобретения значительно дешевле с точки зрения стоимости произзодстза, так же, как и с точки зрения стоимости сырья, поскольку вместо производных анилина и нитробензола настоящее изобретение использует непосредственно анилин и нитробензол. 12 Изобретение относится к способу получения промежуточных соединений для 4-АДФА или его замещенных производных, например, 4-нитродифениламина (45 НДФА) и его солей и/или 4-нитрозодифениламина (п-НДФА или 4-НОДФА) и/или его солей, когда анилин или замещенные производные анилина и нитробензол приводят в реакционный контакт в подходя10 щей системе растворителей и затем осуществляют реакцию в присутствии основания и при условии, когда количество протонного материала, такого как вода, регулируют. Полученная в результате реакцион15 ная смесь насыщена промежуточными соединениями для 4-АДФЛ или их замещенными производными, включая соли 4-нитродифениламина и/или 4-нитрозодифениламина. Способ может быть использован, 20 в соответствии с указаниями настоящего изобретения, для получения с высоким выходом 4-нифОзопродукта (4-нитрозодифениламина и его соли) с малым количеством или при отсутствии 4-нитропродукта. 25 Реакционная смесь 4-нитрозопродукта затем может быть гидрирована непосредственно или 4-нитрозопродукт может быть выделен и потом гидрирован для того, чтобы получить 4-АДФА с высоким выходом. 30 Подобным образом, 4-нитропродукт (4-нитродифениламин и его соль) может быть получен с высоким выходом и с малым количеством или при отсутствии 4-нитрозрпродукта, и 4-нитропродукт или выде35 ленный 4-нитропродукт может быть гидрирован с образованием 4-АДФА с высоким выходом С другой стоооны, и 4-нитро-, и 4-нитрозопродукты получают и не выделяют, но гидрируют непосредственно реак40 ционную смесь, чтобы получить 4-АДФА. Полученный в результате 4-АДФА может быть использован для получения злкилированных продуктов п-феиилендиамина, которые используют в качестве антиокси45 дантов и антиозонантов. С другой стороны, промежуточные соединения 4-АДФА могут быть восстановлены, и восстановленные вещества алкилируют в том же реакционном сосуде, используя кетон в 50 качестве растворителя. При осуществлении изобретения количество протонного материала, присутствующего в процессе реакции анилина или замещенных производных анилина, и нит55 ообензола регулируют за счет присутствия во время реакции осушителя. При другом варианте осуществления изобретения количество протонного материала, присутствующего в ходе реакции анилина или замещенных производных анилина, и нит 13 26851 робензола регулируют путем непрерывного удаления протонного вещества отгонкой. Настоящее изобретение направлено также на тетразамещенные соли аммония или алкилзамещенные диаммониевыв соли 4-нитродифениламина, 4-нитрозодифениламина и их замещенных производных, где каждый заместитель тетразамещенной аммониевой соли выбирают независимо из группы, состоящей из алкильных, арильных и арилалкильных групп, и каждый заместитель алкилзамещенной диаммониевой соли выбирают независимо. Составляющий предмет изобретения способ получения промежуточных соединений для 4-АДФА включает следующие стадии: a) приведение анилина или замещен ных производных анилина и нитробензола в контакт для реакции в подходящей сис теме растворителей; b) взаимодействие анилина, или за мещенных производных анилина, и нит робензола в ограниченной зоне, такой как реактор, при подходящей температуре и в присутствии подходящего основания и контролируемого количества протонного вещества, такого как вода, с целью полу чения 4-нитродифениламина или его за мещенных производных и его соли и/или 4-нитрозодифениламина или его 'заме щенных производных и его с оли. Для получения 4-АДФА или его замещенных производных составляющий предмет изобретения способ включает в себя следующую стадию: c) восстановление 4-нитрозодифени ламина или его замещенных производных и его соли и/или 4-нитродифениламина или его замещенных производных и его соли, чтобы получить 4-АДФА. Для получения алкилированных п-фенилендинаминов или их замещенных производных составляющий предмет изобретения способ включает стадию: d) восстановительного алкилирования 4-ДДФА или его замещенных производ ных со стадии (с). Используемый здесь термин "промежуточные соединения (для) 4-АДФА" означает 4-нитродифениламин, 4-нитрозодифениламин (называемый также п-нитрозодифениламин), их замещенные производные и их соли. Таким образом, ссылка на "одно или большее число промежуточных соединений 4-АДФА" относится к одному или к обоим нейтральным соединениям, т.е. к соединениям, которые не находятся в форме соли и/или соли одного 14 или обоих таких соединений. Соль образуется в реакционной смеси при реакции 4-нитро и/или 4-нитрозопродуктов с основанием. Таким образом, реакционная 5 смесь, полученная по способу настоящего изобретения, может включать одно из соединений или одну из солей, или их любое сочетание в зависимости от выбранных специфических условий реакции. 10 Молярное соотношение анилина или замещенных производных анилина и нитробензола может изменяться от большого избытка нитробензола до большого избытка анилина, или замещенных произ15 водных анилина. Предпочтительно проводить реакцию при использовании избытка анилина или замещенного производного анилина. Соотношение 4-нитро- и 4-нкггрозопродуктов, образовавшихся при реакции ?0 настоящего изобретения, можно регулировать путем изменения соотношения анилина и нитробензола. Например, чем выше отношение анилина к нитробензолу, тем выше отношение 4-нитрозо- к 4-нитропро25 дуктам. Наоборот, чем выше отношение нитробензола к анилину, тем выше отношение 4-нитро- к 4-ниі'.>озопродуктам. Использованный здесь термин "замещенные производные анилина" означает 30 анилин, содержащий один или большее число заместителей в ароматическом кольце, которые оттягивают или высвобождают электроны. Подходящие заместители включают, но не ограничиваются, галогениды, 35 - NO2, - N1H2, алкильные группы, алкоксигруппы, - SO3, -СООН и арильные, аралкильные или алкарильные группы, содержащие, по крайней мере, одну группу NH2, Галогениды выбирают из группы, сос40 тоящей из хлорида, бромида и фторида. Предпочтительные арильные, аралкильные и алкарильные группы содержат от 6 до 18 атомов углерода. Предпочтительные алкильные и алкоксигруппы содержат от 1 45 до 6 атомов углерода. Примеры замещенных производных анилина включают, но не ограничиваются, 2-метоксианилин, 4метоксианилин, 4-хлоранилин, п-толуилин, 4-нитроанилин, 3-броманилин, З-бром-450 аминотолуол, n-амимобензойную кислоту, 2,4-диаминотолуол, 2,5-Дихлоранилин, 1,4фенилендиамин, 4,4'- метилендианилин, 1,3,5-триаминобензол и их смеси. Анилин или замещенные производные 55 анилина могут быть добавлены непосредственно или могут быть образованы In situ при добавлении соединения, которое будет образовывать анилин или соответствующее производное анилина в условиях, t .шествующих в реакционной системе. 15 26851 Азобензол также получают в этой реакции в различных количествах в зависимости от условий реакции. Один из путей регулирования получения азобензола проходит'через соотношение анилин/нит- 5 робензол. Так, когда это соотношение возрастает, количество азобензола, как правило, снижается. Как обсуждается ниже и как объясняется далее в примерах, другие переменные, такие как количество ос- 10 нования и"кислорода, также могут влиять на количество образовавшегося азобензола. Таким образом, используя указания настоящего изобретения, специалист может провести реакцию настоящего изоб- 15 ретения с регулированием количества азобензола, которое образуется при реакции. Подходящие системы растворителей включают, но не ограничиваются ими, та- 20 кие растворители, как, нэпримрр, диметилсульфоксид, N-метилпирролицон, диметил формам ид, анилин, пиридин, нитробензол, неполярные углеводородные растворители, такие как толуол и гексан, ди- 25 метиловый эфир этил єн гликоля, диизопропилэтиламин, и т.п., так же, как и их смеси. Предпочтительно использовать в реакции избыток анилина или замещенного производного анилина, как упомина- 30 лось выше, и избыточное молярное количество анилина или замещенного производного анилина по отношению к нитробензолу выступает в качестве растворителя. Как подробнее описано ниже, смеси 35 растворителей могут использоваться при сочетании одного или большего числа подходящих растворителей с еще одним растворителем, таким как протонный растворитель, например метанол, в регулируе- 40 мом количестве. Подходящие основания включают, но не ограничиваются этим перечнем, органические и неорганические основания, такие как, например, щелочные металлы, 45 такие как металлический натрий, гидриды щелочных металлов, гидроксиды и алкоксиды щелочных металлов, такие как гидрид натрия, гидроксид лития, гидроксид натрия, гидроксид цезия, гидроксид ка- 50 дия, третбугоксид калия и т.п., включая их смеси. Другие приемлемые основные вещества включают, но не ограничиваются ими, межфазные катализаторы в сочетании с подходящим источником основа- 55 ния, таким как гидроксиды тетрззамещен-ного аммония, в которых каждый замес титель независимо выбирают среди ал-кильных, арильных или арилалкильных групп, когда алкильные, арильныв и ари 16 лалкильные группы предпочтительно содержат от 1 до 18 атомов углерода, включая гидроксиды тетраалкиламмония, например, гидроксид тетраметиламмония, гидроксиды арилтриалкиламмония, например, гидроксид фенилтриметчламмония, гидроксиды арилалкилтриалкиламмония, например гидроксид бензилтриметиламмония, гидроксиды алкилзамещенного диаммония, например гидроксид бисдибутилэтилгексаметидендиаммония, и другие сочетания межфазных катализаторов и подходящих оснований, такие как подходящие основания в сочетании с солями ариламмония, краун-эфирами и т.п., и аминооснования, такие как бис-(триметилсилил)-амид лития и т.п., включая их смеси. Предпочтительными веществами (основаниями) для применения в качестве оснований являются гидроксиды тетраалкиламония, такие как гідроксид тетраметиламмония. Предпочтительно добавлять основание к анилину или к замещенному производному анилина, чтобы получить смесь, которую затем соединяют с нитробензолом. Альтернативно основание может быть добавлено после того, как соединены анилин или замещенное производное анилина с нитробензолом. Введение материалов может осуществляться выше или ниже поверхности введения. Количество основания, используемого в настоящем способе, может изменяться в широких пределах. Например, реакция кгожет быть осуществлена таким образом, чтобы ограничивалось основание или резкция может проводиться с ограничением нитробензола или анилина или замещенного производного анилина в зависимости, среди других факторов, от желаемой степени сведения к минимуму количества азобензола. Реакцию осуществляют при соответствующей температуре, которая может изменяться в широких пределах. Например, температура может лежать з области от КУС до 15СГС, 0°С - 100'С, предпочтительно от WC до 90°С. Наиболее предпочтительная температура для проведения реакции настоящего изобретения составляет от 60'С до 80°С, например 75*С. Когда анилин используют в качестве растворителя при аэробных условиях реакции, тогда при возрастании температуры реакции возрастает количество полученного азобензола. Однако, когда реакцию проводят в анилине в анаэробных условиях, более высокие температуры не обязательно увеличивают количество азобензола. Когда образование азобензола не являет 17 26851 ся проблемой, подходящими будут более высокие температуры. Однако, когда желательно свести к минимуму количество азобензола, более подходящими являются более низкие температуры или анаэробные условия реакций. Альтернативно, чтобы свести к минимуму количество азобензола, когда реакцию проводят при более высоких температурах, может быть использован иной, чем анилин, растворитель, и может быть отрегулировано соотношение анилина или замещенного производного анилина и нитробензола. Регулирование количества протонного вещества, присутствующего в реакции, является важным. Обычно, когда реакцию проводят в анилине, вода, присутствующая в реакции в количестве, превышающем 4% HJD {по отношению к объему реакционной смеси), ингибирует взаимодействие анилина с нитробензолом до такой степени, что реакция по существу не продолжается. Снижение количества воды ниже 4% уровня вызывает существенное протекание реакции. Когда гидроксид тетраметиламмония используют в качестве основания с анилином в качестве растворителя, тогда количество воды еще уменьшают, например, до 0,5% по отношению к объему реакционной смеси, общее количество 4-нитродифениламина и 4-нитрозодифениламина и/или их солей возрастает при некоторой потере селективности, так что получается больше 2нитродифениламина, но еще в малых количествах. Так им образом, настоящая реакция может быть проведена в безводных условиях. "Регулируемое количество" протонного вещества представляет собой такое количество, которое лежит ниже количества, вызывающего ингибирование реакции анилина с нитробензолом, например, до 4% Н2О по отношению к объему реакционной смеси, когда анилин используют в качестве растворителя. Верхний предел количества протонного вещества, присутствующего в реакции, изменяется в зависимости от растворителя. Например, когда в качестве растворителя используют ДМСО, и гидроксид тетраметиламмония используют в качестве основания, верхний предел протонного вещества, присутствующего в реакции, составляет 8% по отношению к объему реакционной смеси. Кода в качестве растворителя используют анилин с тем же самым основанием, верхний предел составляет 4% НгО по отношению к объему реакционной смеси. Кроме того, допустимое количество протонного вещества будет ме 18 няться в зависимости от типа основания, количества основания и основного катиона, используемых в системах различных растворителей. Однако, дело специалис5 та, использующего указания настоящего изобретения, - установить специфический верхний предел количества протонного вещества для определенного растворителя, типа и количества основания, катиона ос10 нования и т.п. Минимальное количество протонного вещества, необходимое для поддержания селективности нужных продуктов, также будет зависеть от растворителя, типа и количества основания, катио15 на основания и т.п., которые используются, и также может быть определено специалистом. Так как количество протонного материала, присутствующего в реакции, яв20 ляется важным, можно уменьшить количество присутствующего протонного вещества насколько возможно и затем снова добавить в реакцию нужное количество, например, 0,5 об,% в случае исполь25 зования анилина в качестве растворителя. Протонные вещества, которые могут быть использованы для повторного добавления в реакцию, известны специалистам и вклю-чают, но не ограничиваются, воду, ме30 танол и т. п. Методы измерения количества протонного вещества и снижения количества протонного вещества до возможного предела хорошо известны специалистам. Например, количество воды, при35 сутствующей в некоторых реагентах, может быть определено с помощью аппаратуры Карла Фишера и количество воды может быть уменьшено отгонкой и/или сушкой при пониженном давлении, сушкой в 40 присутствии Р2О5 или других агентов, азеотропной отгонкой, используя, например, анилин и т.п., вк лючая их сочетание. В одном из вариантов осуществления изобретения для регулирования количест45 ва протонного вещества в ходе реакции анилина или замещенных производных анилина и нитробензола добавляют осушитель в таком количестве, чтобы он присутствовал во время реакции анилина или 50 замещенного производного анилина и нитробензола. Например, когда протонное вещество представляет собой воду, осушитель удаляет воду, присутствующую во время реакции анилина или" замещенных 55 производных анилина и нитробензола, и результат проявляется в более высоком превращении нитробензола и в более высоких выходах 4-нитродифениламина и 4нитрозодифениламина или их замещенных производных. Как используется здесь, 19 26851 осушитель представляет собой соединение, присутствующее в ходе реакции анилина или замещенных производных анилина и нитробензола в дополнение к соответствующему используемому основанию. Примеры подходящих осушителей включают, но не ограничиваются, безводный сульфат натрия, молекулярные сита, такие как сита типа 4А, 5А и 13Х, поступающие от Vion Carbide Corporation, хлорид кальция, дигидрат гидроксида тетраметиламмония, безводные основания, такие как КОН, NaOH, и активированный оксид алюминия. В другом варианте осуществления изобретения для регулирования количества протонного вещества в ходе реакции анилина или замещенных производных анилина и нитробензола протонное вещество непрерывно удаляют из реакционной смеси отгонкой: Когда протонное вещество представляет собой воду, предпочтительный способ включает непрерывную азеотропную отгонку воды, используя азеотроп вода/анилин. Непрерывна» отгонка протонного вещества является общепринятым предпочтительным методом регулирования количества протонного вещества, присутствующего во время реакции анилина или замещенных производных аналина и нитробензола. Непрерывное удаление протонного вещества позволяет использовать меньшие количества основания в реакции анилина или замещенных производных анилина и нитробензола, хотя достигается очень высокая конверсия нитробензола и отличные выходы 4-нитродифениламина и 4-нитрозодифениламина и/или их солей или их замещенных производных. Реакцию можно проводить в аэробных и анаэробных условиях. В аэробных условиях реакцию проводят, по существу, так, как описано выше, в реакционной зоне, которую подвергают действию кислорода обычно посредством выдержки на воздухе. В аэробных условиях давление, при котором проводят реакцию, может меняться и оптимальное давление, так же, как и оптимальное сочетание давления и условий температура/давление, легко устанавливается специалистом. Например, реакция может проводиться при комнатной температуре и при давлении в области от 7* 103 Па до 175* 103 Па, таком как от 9,8-103 Па до 105,5 • 103 Па. При анаэробных условиях реакция может проводиться при атмосферном давлении, или при уменьшенном или повышенном давлении в присутствии нейтрального газа, 20 такого как, например, азот или аргон. Оптимальные условия при конкретном наборе параметров реакции, такие как температура, основание, растворитель и т.п., 5 легко определит специалист, используя указания настоящего изобретения. Замечено, что меньшее количество азобензола образуется при проведении реакции в анаэробных условиях с анилином в ка10 честве растворителя. Также замечено, что меньшее количество азобензола образуется тогда, когда реакцию проводят в аэробных условиях с ДМСО и другими подобными растворителями. 15 4-Нитродифениламин или его замещенные производные и/или 4-нитроэодифениламин, или его замещенные производные и/или их соли могут быть восстановлены до 4-АДФА или его замещенных 20 производных. Нейтральные соединения могут быть генерированы из солей с использованием воды и/или кислоты. См., например, пример ID. С другой стороны, соли могут быть восстановлены так, как описа25 но в примере 1А. Это восстановление может быть выполнено любым из многих известных способов восстановления, таких, какие используют источник гидрида, например, борогидрид натрия в сочетании с 30 катализатором палладий на угле или с катализатором платина на угле. Предпочтительно проводить восстановление методом каталитического восстановления, когда гидрирование осуществляют при давлении {в 35 атмосфере) водорода в присутствии платина или палладий на угле, никеля и т. п. Это процесс гидрирования подробно описан в "Catalytic Hydrogenation in Organic Synthesis, P.N. Rylander, Academic Press, 40 N,Y,, p.299 (1979). Гидрирование может быть проведено во многих растворителях, включая, но не ограничиваясь, толуол, ксилол, анилин, 4-АДФА, воду и их смеси. Предпочтительно проводить гидрирование, ис45 пользуя катализатор платина на угле или палладий на угле, в подходящем растворителе, таком как, например, толуол, 4АДФА, ксилол или анилин, их смеси или смеси, которые включают воду в качестве 50 растворителя, и при давлении водорода от 70 і 103 Па до 240* 103 Па и температуре около 80'С.Восстановительное алкилирование 4-55 АДФА для получения антиозонантов гложет быть проведено одним или несколькими хорошо известными способами. См., например, Патент США № 4900868. Предпочтительно, когда 4-АДФА и соответствующий кетон или альдегид взаимодейст 26851 21 22 гие реагенты, такие как другие растворители или другие основания, путем обычной модификации условий реакции и т.п., либо другие реакции, раскрытые здесь, или обусловленные иным образом, будут подходящими для способа настоящего изобретения. Во всех препаративных методах все исходные вещества являются известными или могут быть легко получены из известных исходных веществ. Без дальнейших уточнений предполагается, что специалист, пользуясь предшествующим описанием, может использовать настоящее изобретение в самой полной мере. Следовательно, предполагаемые далее конкретные варианты осуществления изобретения следует рассматривать только как пояснительные и никоим образом не ограничивающие остальное раскрытие изобретения. Все используемые реагенты получают, за исключением оснований и растворителей, и сушат так, как описано здесь далее. Если нет иных указаний, выход во всех случаях определяют при помощи высокоэффективной жидкостной хроматографии (ВЖХ) в соответствии с изложенным далее методом. Материалы и методы. Анилин или замещенные производные анилина и нитробензол являются чистыми реагентами и используются без дальнейшей очистки. Растворители закупают у Aldrier Chemical и обезвоживают Гидроксид тетраметиламмония закупают в виде пентагидрата. Твердое вещество сушат в эксикаторе над Р2О5 при пониженном давлении в течение нескольких дней перед использованием. Титрование полученного в результате твердого вещества показывает, что высушенное вещество представляет собой дигидрат. Оценка ВЖХ. Для анализа реакционных смесей используют ВЖХ с обращенной фазой. Используют колонку (4,6x150 мм) с 5 мкм Beckman / Altex ultrasphereODS, и насосную систему с тройным градиентом (ternary gradient pump system). элюирования АСЫ МеОН вуют в присутствии водорода и платины на угле в качестве катализатора. Подходящие кетоны включают метилизобутилкетон (МИБК), ацетон, метилизоамилкетон и 2-октанон. Следует отметить, что восстановление промежуточных соединений 4-АДФА и алкилирование восстановленного вещества может быть проведено в одном и том же реакционном сосуде с использованием кетона в качестве раст- 10 ворителя. См., например, Патент США № 4463191 и Banerjee et al. J. Chem. Soc. Chem. Comm. 18," 1275-76 (1988). Предполагаемые эквиваленты реагентов и реагенты, рекомендованные выше, 15 представляют собой реагенты, к тому же соответствующие в других отношениях, и имеющие одинакоэые основые свойства, когда одна или большее число разных групп, например NO2, представляют собой 20 простые варианты. Кроме того, когда заместитель определен как , или может представлять собой водород, точная химическая природа заместителя в этой позиции, который представляет собой за- 25 меститель иной, чем водород, не является критической до тех пор, пока она не оказывает вредного влияния на общую активность и/или процедуру синтеза. Химические реакции, описанные вы- 30 ше, вообще раскрываются с точки зрения их самого широкого применения в способе настоящего изобретения. Специфически описанные условия реакции изредка могут являться не подходящими для каж- 35 дого реагента, который раскрыт в объеме изобретения. Например, некоторые соответствующие основания могут не растворяться в одном растворителе так, как они растворяются в других растворителях. Реа- 40 генты, в случае которых это имеет место, легко распознают специалисты. Во всех таких случаях либо условия реакции могут быть успешно выполнены путем обычных модификаций, известных специалис- 45 там, например, соответствующими поправками для температуры, давления и т.п., путем замены реагентов на обычные друГрадиент Время, мин Скорость потока, мл/мин % воды 0 1,5 1,5 1.5 90 63 60 60 10 10 90 90 12,0 12,1 15 35 40 41 50 1.5 W ш 1* 1.5 10 30 20 20 45 45 10 10 0 8 20 20 45 45 0 0 23 26851 П р и м е р 1. А) Этот пример иллюстрирует чистую реакцию анилина и нитробензола в аэробных условиях при комнатной температуре для генерирования продуктов 4-НДФА и п-нитрозодифениламина {п-НДФА). Реакционную смесь затем непосредственно гидрируют, чтобы получить 4-АДФА. Трехгорлую 500 мл круглодонную колбу снабжают магнитной мешалкой с брусочками. В реакционный сосуд загружают 195 мл анилина и нитробензол (4,3 мл, 42 ммоль). В реакционную смесь при перемешивании добавляют дигидрат гидроксида тетраметиламмония (17,7 г, 140 ммолей) в виде твердого вещества. Показано, что почти весь нитробензол в реакции расходуется через 2 часа, однако реакционную смесь перемешивают в течение 18 часов. По окончании этого времени расходуется > 99 % нитробензола. ВЖХанализ реакционной смеси показывает следующий выход продуктов относительно нитробензола: 4-НДФА (6,4 ммоль, 1,37 г, 15 %); п-НДФА (30,6 ммоль, 6,1 г, 73 %); 2-НДФА (0,3 ммоль, 0,064 г, 0,7 %); азобензол (3,6 ммоль, 0,65 г, 8,5 %); феназин (0,8 ммоль, 0,14 г, 1,9 %); феназин-Ы-оксид (0,3 ммоль, 0,05 г, 0,7 %). К смеси добавляют воду (16 мл) и затем всю реакционную смесь загружают в автоклав, емкостью 300 см3 для гидрирования. В автоклав добавляют катализатор - 1 % Ptj на угле (0,5 г сухого веса). Реакционную смесь нагревают до 80°С при давлении Н2 10,5 10э Па. Поглощение водорода завершается в течение 30 минут. ВЖХ-анализ показывает, что образовалось 35,9 ммоль 4-АДФА, что соответствует выходу а 97% по отношению к молярному количеству 4-НДФА и п-НДФА. B) Этот пример является примером реакции анилина и нитробензола при ком натной температуре в дим етил сульфокси де при анаэробных условиях. В 25-мл круглодонную колбу в атмосфере аргона загружают 4 мл ДМСО, анилин (200 мкл, 1,9 ммоль) и дигидрат гидроксида тетраметиламмония (330 мг, 2,5 ммоль). Реакцию оставляют на 4 часа при комнатной температуре. Конверсия нитробензола составляет 68%. ВЖХ-анализ показывает следующий выход по отношению к нитробензолу: 4-НДФА - 30,5%; пНДФА - 33,6%; азобензол - 2,6%; азоксибензол (следы). C) Этот пример является примером чистой реакции между анилином и нитро бензолом при комнатной температуре в анаэробных условиях. 24 В круглодонную колбу емкостью 25 мл в снабженном перчатками боксе, в контролируемой атмос фере аргона, загружают анилин (1,8 мл) и нитробензол 5 (0,02 мл, 0,19 ммоль). К этому раствору добавляют дагидрат гидрокси "тоаметиламмония (330 мг, 2,5 ммоль). Ье нитробензол расходуется через несколько ов. ВЖХ-анализ показывает следующий выход 10 по отношению к нитробензолу: 4-НДФА10%, п-НДФА - 76, азобензол - 7% и феназин - 5%. D) Этот пример является примером реакции между анилином и нитробензо15 лом при комнатной температуре в ДМСО в аэробных условиях. ?тот пример также иллюстрирует генерирование 4-НДФА и п-НДФА из их солей при использовании воды и кислоты. 20 Реакционная смесь содержит анилин (200 мкл, 2,1 ммоль) и нитробензол (200 мкл, 1,9 ммоль) в 4 мл ДМСО. Добавляют в один прием дигидрат гидроксида тетраметиламмония (330 мг, 2,5 ммоль). Реакционную 25 смесь перемешивают в течение 18 часов, по окончании которых реагирует 80% нитробензола. Реакционную смесь сливают в 200 мл воды, что вызывает немедленное осаждение 4-НДФА. Раствор охлаждают 30 льдом в течение нескольких часов и продукт отфильтровывают и сушат при 100'С, Фильтрат обрабатывают ледяной уксусной кислотой до тех пор, пока рН не станет нейтральным, что вызывает осаж35 дение п-НДФА. Осадок отфильтровывают и сушат при 100'С. Окончательный выход выделенных веществ по отношению к нитробензолу составляет 66% для 4-НДФА и 29% для п-НДФА. 40 Е) Этот пример является примером реакции анилина и нитробензола s ДМСО при 80'С в аэ робных условиях. В круглодонную колбу емкостью 250 мл'загружают анилин (0,05 моль, 4,6 г), 45 нитробензол (0,05 ммоль, 6,1 г) и 75 мл ДМСО. К раствору в один прием добавляют дигидрат гидроксида тетраметиламмония (0,2 ммоль, 25,44 г). Реакционную смесь нагревают до 80*С на масляной 50 бане и поддерживают при этой температуре в течение 5 часов. Реакционную смесь анализируют ВЖХ. Выход по отношению к нитробензолу составляет 35% 4-НДФА, 51% п-НДФА и 3,1% азобензола. 55 F) Этот пример является примером реакции анилина и нитробензола в ДМФА в аэробных условиях. Анилин (200 мкл, 2,1 ммоль) и нитробензол (200 мкл, 1,9 ммоль) растворяют в 5 мл ДМФА. К реакционной смеси до 25 26351 бавляют дигидрат гидроксида тетраметиламмония (1,0 г, 7,8 ммоль). Реакционную смесь перемешивают в течение 2 часов, в течение которых расходуется 39% нитробензола. Выход по отношению к израсходованному нитробензолу составляет 99% 4-НДФА и следовое количество пНДФА. П р и м е р 2. Этот пример иллюстрирует, что реакция настоящего изобретения может проводится в некотором интервале температур. Готовят четыре идентичные реакционные смеси указанным далее с пособом и работают при 0; 23; 50 и 80*С на воздухе. В круглодонную колбу емкостью 50 мл загружают 49 мл анилина и нитробензол (1,0 мл, 9,5 ммоль). В реакцию вводят дигидрат гидроксида тетраметиламмония (4,40 г, 34,6 ммоль), и реакционную смесь оставляют на 5 часов. Выход продуктов определяют ВЖХ-анализом и считают по отношению к израсходованному нитробензолу (в молях). Селективность предостзвляет собой молярное соотношение полученного продукта и израсходованного нитробензола. Выход зависит от конверсии и селективности (табл. 1). П р и м е р 3. Этот пример показывает, насколько важным является регулирование количества протонного вещества, присутствующего в реакции. Осуществляют четыре реакции, которые идентичны во всем, за исключением количества воды, которое добавляют в смесь и которое составляет 0; 10; 50 и 100 мкл. Итак, в круглсдонную колбу емкостью 25 мл загру> хают анилин (2 мл) и нитробензол (2 мл) и добавляют различное количество воды. Дигидрат гидроксида тетраметиламмония (330 мг, 2,5 ммоль) добавляют в один прием. Реакции оставляют протекать на воздухе при комнатной температуре и отбирают образцы через 16 ч. Проводят также идентичную серию реакций, в которых вместо аоды добавляют метанол (табл. 2). П р и м е р 4. Этот пример показывает, что при практическом осуществлении способа настоящего изобретения для получения продуктов 4-НДФА и/или п-НДФА могут быть использованы различные растворители. Реакции, указанные в табл. 3, проводят так же, как указано в примере 1, за исключением того, что растворитель примера 1 заменяют на растворитель, указанный в табл. 3. П р и м е р 5. Этот пример иллюстрирует возможность использования различных оснований в способе настоящего изобретения для получения продуктов 4НДФА и/или п-НДФА. Реакции, представ 26 ленные в табл. 4, проводят так, как указано в примере 1, за исключением того, что основание примера 1 заменяют на основание, указанное в табл. 4. 5 П р и м е р 6. Этот пример иллюстрирует неожиданное возрастание селективности и конверсии нитробензола при использовании способа настоящего изобретения по сравнению со способом, раск10 рытым Ayyangar et al. Осуществляют реакцию ацетанилида, нитробензола, NaOH и tC,C03 в ДМСО в соответствии с методикой, описанной Ayyangar et al. Tetrahedron Letters, vol. 31, 15 N 22, p. 3217-3220 (1990). Анализ этой реакции с помощью ВЖХ показывает, что конвертируется 37% нитробензола и достигаются следующие выходы по отношению к нитробензолу. 420 НДФА- 6%, п-НДФА- 4,5%, азобензол 0,7%. Когда для сравнения реакцию проводят в соответствии с указаниями настоящего изобретения, конверсия нитробензо25 ла и селективность для нужных продуктов существенно возрастают. Например, при проведении реакции в соответствии с описанием в примере 1D анилин (0,05 моль), нитробензол (0,05 моль) и дигидрат гид30 роксида тетраметиламмония (0,2 моль) смешивают в 75 мл ДМСО. Реакционную смесь перемешивают при комнатной температуре в течение 5 часов, после чего реакционную смесь анализируют ВЖХ, и 35 получают следующие результаты: конверсия нитробензола составляет 85%; выход Относительно нитробензола для 4-НДФА составляет 18%, для рп-НДФА- 51%, для азобензола - 3%. 40 Взаимодействие ацетанилида и нитробензола также осуществляют при комнатной температуре. Итак, ацетанилид (0,05 ммоль), нитробензол (0,05 ммоль), NaOH (0,5 ммоль) и К гСО3 растворяют в 45 75 мл ДМСО. Реакционную смесь перемешивают в течение 5 часов при комнатной температуре (23"С). Анализ реакционной смеси показывает отсутствие конверсии нитробензола и не обнаруживает про 50 дуктов. П р и м е р 7. Этот пример иллюстрирует возможность регулирования соотношения п-НДФА и 4-НДФА с помощью соотношений анилина и нитробензола. 55 Анилин и нитробензол вводят в реакцию при различных соотношениях, хотя общий реакционный объем и количество дигидрата гидроксида тетраметиламмония держат постоянными. Так, для иллюстрации типичной реакции при объемном соот 27 26851 ношении анилина и нитробензола равном 1, анилин (2 мл) и нитробензол (2 мл) загружают в круглодонную колбу емкостью 25 мл. Добавляют дигидрат гидроксида тетраметиламмония {330 мг, 2,5 моль), и реакции предоставляют протекать при комнатной температуре на воздухе в течение 14 часов. Анализ проводят методом ВЖХ (табл. 5). П р и м е р 8. Этот пример иллюстрирует действие, которое оказывает количество протонного вещества, присутствующего или добавленного в реакцию на степень конверсии и выход 4-НДФА и п-НДФА. Количество воды, которую добавляют в реакцию анилина, нитробензола и дигидрата гидроксида тетраметиламмония в ДМСО, изменяют от О до 500 мкл/0; 50; 150; 300; 500 мкл), хотя общий объем реакционной смеси поддерживают постоянным. Так , типичная реакционная смесь содержит анилин (200 мкл, 2,1 ммоль), нитробензол (200 мкл, 1,9 ммоль), дигидрат гидроксида тетраметиламмония (330 мг, 2,5 ммоль) и воду (50 мкл) в 3,55 мл безводного ДМСО. Реакцию проводят в аэробных условиях при комнатной температуре в течение 24 часов, после чего отбирают образцы, и подвергают их ВЖХ-аиализу (табл. 6). П р и м е р 9. Этот пример иллюстрирует действие, которое оказывает увеличение количества основания на выход 4-НДФА и п-НДФА при условии, когда количество протонного вещества, вводимого в реакцию, остается постоянным. Проводят три идентичных реакции, за исключением того, что изменяют в каждой количество дигидрата гидроксида тетраметиламмония. В типичной реакции смешивают анилин (2 мл), нитробензол (2 мл), воду (100 мкл) и дигидрат гидроксида тетраметиламмония (330 мг, 2,5 ммоль) и оставляют реагировать в течение 24 часов на воздухе при комнатной температуре. В тех случаях, когда в растворах образуется большое количество осадка, добавляют дополнительно 10 мл анилина, чтобы солюбилизировать реакционную смесь перед отбором образцов. Все реакционные смеси анализируют методом ВЖХ (табл. 7). П р и м е р 10. Этот пример иллюстрирует взаимодействие анилина, нитробензола и дигидрата гидроксида тетраметиламмония в анаэробных условиях при 50"С. В четырехгорлую круглодонную колбу емкостью 500 мл, снабженную механической мешалкой, капельной воронкой, термометром и трубкой для подачи азота. 28 загружают 90 мл анилина. Анилин продувают азотом и добавляют в один прием дигидрат гидроксида тетраметиламмония (54 г, 0,42 моль). Реакционную смесь в 5 атмос фере азота при перемешивании нагревают до 50*С. Как толь "температура реакционной смеси в реакционном сосуде достигнет 50*С, добавляют по каплям нитробензол (10 мл, 95 ммоль) при 10 энергичном перемешивании смеси анилина и основания. Нитробензол добавляют с такой скоростью, чтобы закончить добавление через 30 минут. Во время добавления нитробензола температура 15 реакции поднимается до 65*С. Реакционную смесь перемешивают еще в течение 90 минут, после чего анализируют ВЖХ. Конверсия нитробензола - 100%. Выход относительно нитробензола: п-НДФА 20 88,5%, 4-НДФА - 4,3%, феназин - 2,6%, азобензол - 3,6%. П р и м е р 11. Этот пример показывает, как можно получить соль 4-НДФА 25 и п-НДФА с ионом тетраметиламмония по способу настоящего изобретения. Анилин (3,0 мл) смешивают с дигидратом гидроксида тетраметиламмония (330 мг, 2,5 ммоль) в сухом боксе с 30 контролируемой атмосферой аргона. Смесь анилина и основания фильтруют таким образом, чтобы анилин поступал прямо 8 1 мл нитробензола. После добавления раствора анилина и основания 35 реакционная смесь сразу становится красной, и начинает образовываться осадок. Смесь перемешивают в течение 5 минут, после чего реакционную смесь фильтруют. Красный осадок промывают 40 несколькими объемами сухого эфира и оставляют сушиться. Часть твердого вещества анализируют 'Н-ЯМР -спектроскопией (ДМСО) 5 3,1 (с), 6,1 (д.,1), 6,5 (т.,1), 6,6 (д.,1), 6,76 (д.,1), 6,8 (т.,1), 7,04 45 (т.,1), 7,5 (д., 1). В ЯМР-трубку добавляют каплю уксусной кислоты-с! 4, что вызывает немедленное изменение цвета с красного на желтый, и снова подвергают ЯМР-спектроскопии, Полученный в резуль50 тате спектр идентичен аутентичному 4~ НДФА. Часть красного твердого вещества растворяют во влажном ацетонитриле и подвергают ВЖХ-анализу, который показывает, что 4-НДФА является основ55 ным компонентом. П р и м е р 12. Этот пример иллюстрирует конверсию 4-АДФА в Ы*(1,3-диметилбутил-М'-фемил-п-фенилендиамин, пригодный для применения в качестве антиозонанта для защиты резины. 29 ЗО 56851 Полученный при взаимодействии ачилина и нитробензола (по методике примера 1D) 4-АДФА (52 г), 100 г метилизобутилкетона (МИБК) и 0,3 г катализатора 3% платины на угле загружают в автоклав Парра (Parr ) емкостью 1 л. После продувания азотом реакционную смесь нагревают до 170-175'С и при давлении водорода в 5,6* 10 5 Па. Смесь реагирует в течение 95 минут, после чего отбирают 10 образец, ГХ-анализ показывает присутствие 0,4% непрореагировавшего 4-АДФА. Реакционную смесь охлаждают и фильтруют, чтобы удалить катализатор, и отгоняют легкие компоненты - воду и избыток 15 Время, мин 0 35 ' 40 45 46 55 МБИК. При охлаждении кристаллизуется твердое вещество пурпурного цвета - 71 г. Оценка ГХ-методом внутреннего стандарта показывает 95,9% чистоты. Подобные реакции с подобными результатам проводят, используя метилизоамилкетон и ацетон. Следующие далее примеры используют улучшенный метод анализа с помощью ВЖХ. Для анализа продуктов реакции азосочетания ВЖХ используют метод внешнего стандарта. A Waters 600 series ВЖХ. снабженные колонкой Vygac 201HS54 (4,6x250 мм) и УФ-детектором для 254 нм, используют для контроля всех реакций. Градиент элюирования Растворитель А (вода) 75 20 0 25 80 100 100 25 25 0 , 75 75 Внешние стандарты готовят, раство- зо ряя N-метиланилин (5,7 мг), нитробензол (13,0 мг), феназин (4,5 мг), 4-нитрозодифениламин (68,1 мг), 4-нитродифениламин (7,2 мг), азобензол (4,7 мг) и 25% водный раствор тетраметиламмонийгидрок- 35 сида (130 мюі) в 50 мл ацетонитрила. В случаях с производными анилина готовят подобные стандартные растворы. П р и м е р 13. Этот пример иллюстрирует непрерывную отгонку воды при 40 реакции анилина, нитробензола и гидроксида тетрзметиламмония (ТМА (Г)) путем отгонки при пониженном давлении азеотропа анилина с водой. В круглодонную колбу емкостью 22 л, 45 снабженную механической мешалкой, насадкой Дина-Старка, термопарой, линией подачи нитробензола и тефлоновым дефлектором, загружают 6,85 кг 25% раствора ТМА(Г) (6,70 л, 18,8 молей ТМА (Г)). 5 0 Воду удаляют отгонкой при пониженном давлении (55 торр) до точки, когда концентрация основания составляет 35%. На этой стадии температуру поднимают равномерно до значения 50-55"С. В реактор 55 загружают анилин (10,1 кг, 9,88 л, 108 ммоль) и продолжают вакуумную отгонку при 55 тор. Воду и анилин непрерывно удаляют в виде азеотропа до молярного соотношения воды и ТМА (Г) 4:1. Во вре Растворитель В (метанол в ACN) мя этого процесса температура реакции поднимается до 75*С. Как только будет достигнуто соответствующее молярное соотношение воды и основания, добавляют нитробензол (2,19 кг, 1,79 л, 17,82 ммоль) непрерывно в течение трех часов. Во время этого добавления воду и анилин продолжают удалять из реакции вакуумной отгонкой при 55 тор. Хорошая скорость удаления воды с анилином является такой скоростью, при которой вес удаленного конденсата равен весу добавленного нитрозобензола за все время добавления. Точка окончания реакции может быть определена ВЖХ-анализом путем контроля конверсии нитробензола. Типичный выход, определенный ВЖХ-анализатором при 100% конверсии нитробензола, составляет 92,1% для 4-нитрозодифениламина, 3,4% для 4-нитродифениламина, 3,4% для азобензола и 0,9% для феназина. П р и м е р 14. Этот пример иллюстрирует применение различных растворителей при реакции анилина, нитробензола и основания при получении промежуточных соединений 4-АДФА. К раствору, содержащему 0,5 г (5,3 ммоль) анилина и 0,95 г {6,5 ммоль) дигидрата гидроксида тетраметиламмония в 8 мл растворителя при 70'С в атмосфере азота добавляют с помощью шприца 0,65 г 31 26851 (5,3 ммоль) нитробензола. После перемешивания раствора при 70'С в атмосфере азота в течение 12 часов реакционную смесь анализируют ВЖХ, результаты которой суммированы в табл. 8. П р и м е р 15. Этот пример иллюстрирует, каким образом могут быть использованы различные межфазные катализаторы в реакции анилина, нитробензола и основания при получении промежуточных соединений 4-АДФА, В типичной реакции в трехгорлую круглодонную колбу, снабженную холодильником Дина-Старка, загружают 59 г (0,091 моль основания) водного гидроксида тетрабутиламония и 55 г (0,59 ммоль) анилина. Воду удаляют посредством азеотропиой отгонки с анилином (35 мл) при 20 мм рт.ст. при 70"С. Нитробензол (11,2 г, 0,091 ммоль) вводят через капельную воронку при 70*С в течение 5 минут. Реакционную смесь перемешивают при 20 мм рт.ст. и 70'С в течение 4 часов. Реакционную смесь анализируют ВЖХ и результаты суммированы в табл. 9. В случае, когда в качестве основания используют гидроксид бис-дибутилэтилгексаметилендиаминаммония, условия реакции несколько отличаются. В таком случае 50 мл водного раствора гидроксида четвертичного аммония (0,0575 ммоль гидроксида) смешивают с 200 мл анилина. Воду удаляют вакуумной отгонкой при 67*С до тех пор, пок а не отгонят 28 мл воды. В реакцию в атмос фере азота при 50*С добавляют по каплям нитробензол (23,2 ммоль, 2,85 г). Реакционную смесь перемешивают в течение 2 ч, после чего отбирают образцы для анализа. 32 ммоль). В процессе добавления поддерживают температуру 70*С. Реакцию продолжают после завершения добавления нитробензола в течение одного часа. Ре5 зультаты этих экспериментов представлены в табл.10. П р и м е р 17. Этот пример иллюстрирует, каким образом может быть уменьшено количество феназина, обра10 зующегося в реакции, путем увеличения пространственного объема иона тетраалкиламмония, используемого в качестве межфазного катализатора. Экспериментальная методика идентична методике, 15 описанной в примере 15. Результаты суммированы в табл. 11. П р и м е р 18, Этот пример иллюстрирует, каким образом могут быть использованы в этой реакции различные за20 мещенные производные анилина. Реакцию анализируют методом ВЖХ, и результаты суммированы в табл. 12. A) З-Броманилин. Раствор 10 мл (0,09 ммоль) 3-брома-25 нилина и 1,5 г (0,01 ммоль) дигидрата гидроксида тетраметиламмония перемешивают при 70'С в атмосфере азота. С помощью шприца добавляют по каплям нитробензол (0,9 мл, 8,78 ммоль) и раст-30 вор перемешивают при 70'С в атмосфере азота в течение 12 часов. B) 4-Нитроанилин. Раствор 4-нитроанилина (1,38 г, 0,01 ммоль) и дигидрата гидроксида тетраме35 тиламмония (1,81 г, 0,012 моль) в 3 мл диметилсульфоксида перемешивают при 7СГС в атмосфере азота. С помощыо шприца добавляют по каплям нитробензол (1 мл, 0,01 ммоль), и раствор перемешивают при 40 70'С в атмос фере азота в течение 12 часов. C) п-Толуидин. Раствор п-толуидина (3 г, 28 ммоль) и дигидрата гидроксида тетраметиламмо45 ния (0,9 г, 6 ммоль) перемешивают при 70"С в атмосфере азота. С помощью шприца добавляют по каплям нитробензол (0,5 мл, 5 ммоль), и раствор перемешивают при 70'С в атмосфере азота в течение 12 П р и м е р 16. Этот пример иллюстрирует, каким образом в этой реакции добавление внешнего осушителя может быть использовано для поглощения воды вместо азеотропной отгонки, описанной в примере 13. В трехгорлую круглодонную колбу емкостью 500 мл, снабженную механической мешалкой и холодильником Дина-Старка, загружают 59,01 г (0,162 молей осно- 50 часов. 1) ) 4-Хлоранилин. вания) 25% водного раствора гидроксида Раствор 4-хлоранилина (4,8 г, 0,03 тетраметиламмония. Воду (17 мл) удаляют ммоль) и дигидрата гидрооксида тетравакуумной отгонкой при 50 тор. Добавметиламмония (0,9 г, 6 ммоль) в 2 мл диляют анилин (88,05 г) и удаляют вакуумной отгонкой 18 мл, что дает в результате 55 метилсульфоксида перемешивают при 70*С в атмосфере азота. С помощью шприца молярное соотношение воды и основания добавляют по каплям нитробензол (0,71 r, 3:1. Отгонку прекращают и добавляют 5,6 ммоль) и раствор перемешивают при соответствующий осушитель. Затем в те70"С в атмос фере азота в течение 12 чение одного часа в атмосфере азота часов. добавляют нитробензол (19,18 г, 0,155 26851 E) 4-Метоксианилин. Раствор 4-метоксианилина (3 г, 0,03 ммоль) и дигидрата гидроксида тетраметиламмония (0,95 г, 6 ммоль) в 2 мл диметилсульфоксида перемешивают при 70'С в атмосфере азота. С помощью шприца добавляют по каплям нитробензол (0,6 г, 5 ммоль) и раствор перемешивают при 70*С в атмосфере азота в течение 12 часоя. F) 2-Метоксианилим. Раствор 2-метоксианилина (4,9 г, 0,03 ммоль) и дигидрата гидроксида тетраметиламмония (1,1 г, 7,58 ммоль) перемешивают при 70'С в атмос фере азота. С помощью шприца добавляют по каплям нитробензол (0,75 г, 6,09 ммоль) и раствор перемешивают при 70'С в атмосфере азота в течение 12 часов (табл.12). П р и м е р 19. Этот пример иллюстрирует, каким образом различные диаминокуклеофилы будут вступать в реакцию азосочетания в пара-положение нитробензола. К перемешиваемому раствору, содержащему 1,08 г (0,01 ммоль) 1,4-фенилендиамина, 3,6 г (0,02 моль) пентагидрата гидроксида тетраметиламмония в 2 мл диметилсульфоксида, в атмосфере азота при 70*С с помощью шприца добавляют нитробензол (2 мл, 0,02 моль). Раствор перемешивают при этих условиях в течение 4 часов. Отбирают аликвоту для ЖХ, МС и ЖХ-МС анализов. Обнаружизают N, N1нитрозофенил)-1, 4-фэнилендиамин, N-(4ни1рэфенил)-М'-(4-нитрозофенил)-1,4-фенилендиамин и Ы,М'-(4-нитрофенил) -1,4фенилендиамин. Другие диаминонуклеофилы, такие как4,4'-метилендианилин и 2,4-диамииотолуол, дают подобные результаты при идентичных условиях реакции. П р и м е р 20. Этот пример иллюстрирует гидрирование соли тетраметиламмония (ГМА) 4-НОДФА и соли ТМА 4НДФА до 4-АДФА в различных растворителях. Реакции гидрирования выполняют в автоклаве из нержавеющей стали емкостью 300 см3, снабженном механической мешалкой и регулятором температуры. А) Загружают з автоклав ТМА соль 4НОДФА (12,4 г, 0,0464 ммоль) со 150 мл толуола. В автоклав добавляют катализатор -1% И иа угле {300 мг сухого веса). Реактор продувают азотом и затем дают давление водорода 14'105 Па, которое поддерживают постоянным в течение гидрирования. Реагенты перемешивают при 1500 об/мин, и позволяют температуре достигнуть ЗО'С. По окончании поглоще 34 ния водорода полагают, что реакция завершена. Содержимое извлекают и фильтруют, чтобы удалить катализатор. Отбирают образец из органического слоя и 5 анализируют ВЖХ с обращенной фазой, которая показывает 100% конверсию субстрата и 97% выход 4-АДФА. B) Смесь соли ТМА 4-НОДФА (71 г, 262 ммоль) и ТМА соли 4-НДФА (7 г, 24 10 ммоль) загружают в автоклав со 150 г анилина. Добавляют катализатор -1% Pt на угле (300 мг сухого веса). Реактор продувают азотом и затем создают давление водорода 14-10 5 Па, которое поддержи15 вают постоянным в течение реакции. Реагенты перемешивают при 1500 об/мин и позволяют температуре подниматься до 80'С. По окончании поглощения водорода полагают, что реакция завершена. Мате20 риалы извлекают и фильтруют, чтобы удалить катализатор. Отбирают образец органического слоя и анализируют ВЖХ с обращенной фазой, которая показывает 100% конверсию субстрата и 98% выход 25 4-АДФА. C) Смесь ТМА соли 4-НОДФА (36,5 г, 135 ммоль) и ТМА соли 4-НДФА (3,4 г, 12 ммоль) загружаю7" в автоклаа с 51 г 4-АДФА, Добавляют катализатор - 1% Pt на угле 30 (300 мг сухого веса). Реактор продувают азотом, и затем создают давление водорода 14* 105 Па, которое поддерживают постоянным в течение реакции. Реагенты перзмешивают при 1500 об/мин, и позволяют 35 температуре достигать 80°С. По окончании поглощения водорода полагают, что реакция завершена. Материалы извлекают и фильтруют, чтобы удалить катализатор. Отбирают образец органического слоя, и 40 анализируют ВЖХ с обращенной фазой, которая показывает 100% конверсию субстрата, причем только 4-АДФА определяется как основной продукт. П р и м е р 21. Этот пример иллюст45 рирует гидрирование 4-НОДФА до 4-АДФА в анилине с применением никелевого катализатора на носителе. В автоклаз емкостью один литр заг-50 ружают 50 г 4-НОДФА, 200 г анилина и 2,0 г никеля на носителе (диоксид кремния) (оксид алюминия). После продувания с целью удаления кислорода, смесь нагревают до 80*С и подают водород в 55 количестве 200 мл/мин. Подачу ограничивают таким образом, чтобы максимальное давление составляло 19,7* 105 Па. Через 120 мин поток водорода показывает, что остается непрорєагировавшим 0,1% 4-НОДФА. Продукт представляет собой 4АДФА. 35 Предшествущие примеры могут быть повторены с подобным успехом при замене растворителей, оснований и т.п. на родственные или специально охарактеризованные и/или изменении условий осуществления настоящего изобретения, таких как температура и давление, которые использованы в предшествующих примерах. І емп., Конверсия нитробензола, 0 52 23 73 50 98 ТАІІ П 80 36 26851 100 Из данного выше описания специалисты могут легко уяснить неотъемлемые особенности настоящего изобретения и без отступления от сущности и объема изобретения произвести различные изменения и модификации, чтобь "^испособить его для различных условий и назначений. Та( э лиц a Продукты Селективность, % Выход, % 34 18 2,2 0,6 71 12 17 t 18 9.3 1,0 0,3 51 8,5 12 Следы П-НДФА 4-НДФА 2-НДФА Феназин п-НДФА 4-НДФА Азобензол Феназин Феназин-Nоксид п-НДФА 4-НДФА 2-НДФА Азобензол* п-НДФА • 4-НДФА 2-НДФА Азобензол* 88 7.8 1,7 22 89 7 2 55 Следы 86 7,6 1,6 21 89 7 2 55 "Большая часть азобензола образуется, по-видимому, через окислительное азосочетание" анилина. См. работу D.T.Sawyer. Объем (мкл) добавленной воды о 0 10 50 100 Объем (мкл) добавленного метанола 10 50 100 Вода*, % 2.2 2,45 3,45 4,7 Метанол', % rv Ммол. соотношение {4-НДФА+п-НДФА)/(2-НДФА+ +феназин) 6.2 8,5 Н.5 5,0 Таб л иц а 2 Выход (ммоль) 4-НДФА+п-НДФА) 0,83 0,68 0.18 0,05 0,25 8,8 0,67 1,25 2,5 16 35 0,57 0,42 *% воды и метанола является объемным. В случае, когда воду не добавляют, вода, присутствующая в реакции, вводится из дигидрата гидроксида тетраметиламмония. 37 38 26851 Т а б л и ц а 3 Растворитель Условия реакции ІМ-Метил-2-пирролидон ДМСО/ТГФ Пиридин 1D 1В 1 Таблица 4 Основание Условия реакции Металлический Na NaH NaOH КОН трет-Бутоксид калия Вис-(триметилсилил)амид лития NaH/K2CO3 ID 1D Я> W Ю 1В, 1D 1D, 1F Таблица 5 Объемное соотношение анилин/нитробензол Соотношение п-НДФА/4-НДФА 0,33 1 0,1 0,1 46 п 50 Таблица 6 Объем (мкл) добавленной воды Конверсия нитробензола, % Выход (ммоль) 4-НДФА+п-НДФА 39 73 63 150 99 62 0.23 0,05 2.3 3,5 6 9,75 14,7 0 50 150 300 500 12 3 Таблица 7 Объем (мкл) г добавленной воды 100 100 100 Растворитель Толуол Гексан Диметиловый эфир этиленгликоля Дииэопропилзтиламин Вода, % 4,7 4,7 4.7 Основание, мМ Основание, г Выход (ммоль) 4НДФА+п-НДФА 2.5 5,0 12.5 0.05 0,15 1,24 0,330 0,660 1,65 Конверсия нитробензола, % 99,5 94,8 феназина 0,64 4-Н0ДФА 1.1 100 50 Т аб лиц а Выход, % 36,0 4-НДФА 20,9 34,1 азобензола 1,5 23.5 1,24 51 ;4 27 19,8 0.9 45 4,3 0 • 76,4 8 26851 39 40 Та б л и ц а 9 Конверсия нитробензола, % феназина 4-НОДФА 4-НДФА азобензола 77,5 0 52.1 9,7 3.4 100 0,25 0.85 63.8 33,0 18.3 83.6 9,6 17,5 43,2 100 0,1 74,7 12,4 11,7 99,4 0.33 77,8 11,5 6,54 65,3 Основание 0 76 7 1,1 Тетрабутиламмоний, гидроксид Тетрапропиламмонии, гидроксид Холин, гмдроксид Бензилтриметиламмоний,гидроксид 18-Краун-6+2КОН Бис-дибутилэтилгексаметилендиаммоний,гидроксид Выход,% Т аб л иц з 10 но» г Конверсия нитробензола, % феназина 4-НОДФА 4-НДФА азобензола 52,3 0,34 46,7 2,0 1.0 14,75 61,9 0,50 58,6 2,2 0,8 28,1 78,2 1.0 68,0 5,1 4,8 Добавив* Осушитель Без осушителя Безводный сульфат натрия Молекулярные сита, 4А Выход.% Та б лиц а Основание Тетраметиламмоний, гидроксид 11 Вы ход,% Конверсия нитробензола, % феназина 4-НОДФА 4-НДФА азобензола 100 2,24 43 34 12,1 100 0,25 63.8 18,3 17,5 100 0.1 74,7 12,4 11.7 77,5 0 52,1 9.7 3,4 43 22 15 12 23 Тетрапропиламмонии, гидроксид Бензилтриметиламмоний,гидроксид Тетрабутиламмоний, гидроксид Фенилтриметиламмоний,гидроксид Производное анилина 2-Метоксианилин 4-Метоксианилин 4-Хлоранилин пТолуидин 4Нитроанилин ЗБроманилин Конверсия нитробензола, % * 100 100 98 100 99 100 Таб лиц а Выход,% производного 4-НОДФА производного 4-НДФА 55 74 61 19 0 61 44 20 89 73 9 * 12 26851 Упорядник Замовлення 536 Техред М. Келемеш Коректор Л.Пчолинська Тираж Підписне Державне патентне відомство України, 254655, ГСП, Київ-53, Львівська пл., 8 Відкрите акціонерне товариство "Патент", м. Ужгород, вул. Гагаріна, 101
ДивитисяДодаткова інформація
МПК / Мітки
МПК: C07C 213/00, C07C 211/54, C07C 217/92, C07C 211/56, C07C 209/36, C07C 209/60, C07B 61/00, C07C 209/26, C07C 229/54, C07C 209/38, C07C 211/64, C07C 307/00, C07C 209/02
Мітки: заміщених, похідних, одержання, 4-нітрозодифеніламіну, алкілованих, спосіб, р-фенілендіамінів, 4-амінодифеніламіну, 4-нітро
Код посилання
<a href="https://ua.patents.su/22-26851-sposib-oderzhannya-4-nitro-ta-abo-4-nitrozodifenilaminu-abo-kh-pokhidnikh-sposib-oderzhannya-4-aminodifenilaminu-abo-jjogo-zamishhenikh-pokhidnikh-ta-sposib-oderzhannya-alkilovanik.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 4-нітро та/або 4-нітрозодифеніламіну або їх похідних, спосіб одержання 4-амінодифеніламіну або його заміщених похідних та спосіб одержання алкілованих р-фенілендіамінів або їх заміщених похідних</a>
Попередній патент: Спосіб одержання стабільного соматотропіну, стабільний соматотропін і композиція стабільного соматотропіну
Наступний патент: Спосіб одержання оцтової кислоти
Випадковий патент: Спосіб визначення поточної продуктивності преса-гранулятора комбікормів