Складні ефіри кватернізованого хінуклідину
Номер патенту: 88634
Опубліковано: 10.11.2009
Автори: Буіл Альберо Марія Антонія, Прат Кіньонес Марія, Фернандес Форнер Марія Долорс
Формула / Реферат
1. Сполука формули (І):
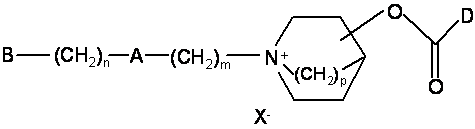 , (І)
, (І)
де В означає атом водню або групу, яку вибирають із групи, яка включає -R1, -OR1, гідрокси, -O(CO)R1, ціано й необов'язково заміщений неароматичний гетероцикліл, який містить один або більше гетероатомів, де R1 вибирають із групи, яка включає атоми водню, необов'язково заміщений С1-С8алкіл, необов'язково заміщений С2-С8алкеніл і необов'язково заміщений С3-С8циклоалкіл,
n дорівнює цілому числу від 0 до 4,
А вибирають із групи, яка включає -СН2-, -CH=CR3-, -CR3=CH-, -CR3R4-, -O-, -CO-, -О-(СН2)2-О-, де R3 і R4 кожний незалежно означає атом водню або С1-С8алкіл,
m дорівнює цілому числу від 0 до 8,
р дорівнює цілому числу від 1 до 2,
біциклічне кільце азонію містить замісники в положеннях 2, 3 або 4, включаючи всі можливі конфігурації асиметричних центрів,
D вибирають із групи, яка включає:
 або
або  ,
,
де R5 вибирають із групи, яка включає феніл, 2-тієніл, 3-тієніл, 2-фураніл, 3-фураніл, причому вказані групи необов'язково заміщені одним або більше замісниками Ra,
R6 вибирають із групи, яка включає 2-тієніл, 3-тієніл, 2-фураніл, 3-фураніл, С3-С8циклоалкіл, С3-С8циклоалкеніл, С1-С8алкіл, С2-С8алкеніл, С2-С8алкініл, бензил і фенетил, причому вказані групи необов'язково заміщені одним або більше замісниками Rb,
R7 означає атом водню або групу, яку вибирають із групи, яка включає гідроксил, гідроксиметил і метил,
Q означає простий зв'язок або групу, яку вибирають із групи, яка включає -СН2-, -СН2СН2-, -О-, -О-СН2-, -S-, -S-CH2- і -СН=СН-,
Ra і Rb незалежно вибирають із групи, яка включає атоми галогену, необов'язково заміщений С1-С8алкіл, необов'язково заміщений С1-С8алкокси, гідрокси, трифторметил, нітро, ціано, -COOR8, -NR8R9, де R8 і R9 незалежно означають атом водню або С1-С8алкіл,
у дорівнює цілому числу від 0 до 3,
X- означає фармацевтично прийнятний аніон моно- або поліосновної кислоти,
за умови, що група B-(CH2)n-A-(CH2)m- не означає прямий С1-С4алкіл, а також що виключені наступні сполуки:
1-алілоксикарбонілметил-3-(2-гідрокси-2,2-дитіофен-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октан і
1-карбоксиметил-3-(2-гідрокси-2,2-дитіофен-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октан.
2. Сполука за п. 1, у якій В вибирають із групи, яка включає атоми водню, гідрокси, необов'язково заміщений С1-С8алкіл, необов'язково заміщений С2-С8алкеніл, необов'язково заміщений С3-С8циклоалкіл і неароматичний гетероцикліл, заміщений принаймні гідроксигрупою.
3. Сполука за п. 1, де група азонійбіцикло заміщена за атомом азоту групою, яку вибирають із групи, яка включає аліл, 4-метилпент-3-еніл, ізопропіл, циклопропілметил, ізобутил, гептил, циклогексилметил, 3-циклогексилпропіл, 3,7-диметилокта-(Е)-2,6-дієніл, 2-гідроксіетил, 3-гідроксипропіл, 4-гідроксибутил, 5-гідроксипентил, 6-гідроксигексил, 2-етоксіетил, 2-(2-гідроксіетоксі)етил, 2-(2-метоксіетоксі)етил, оксиранілметил, 2-[1,3]діоксолан-2-ілетил, 2-[2-(2-гідроксіетоксі)етоксі]етил, 3-[1,3]діоксолан-2-ілпропіл, 2-етоксикарбонілетил, 3-етоксикарбонілпропіл, 4-етоксикарбонілбутил, 4-ацетоксибутил, 2-ціаноетил, 3-ціанопропіл, 4-ціанобутил, 6-ціаногексил, 4,4,4-трифторбутил, 3-(4-гідроксипіперидин-1-іл)пропіл і 4-(4-гідроксипіперидин-1-іл)бутил.
4. Сполука за п. 3, у якій група азонійбіцикло заміщена за атомом азоту групою, яку вибирають із групи, яка включає аліл, 4-метилпент-3-еніл, ізопропіл, циклопропілметил, ізобутил, гептил, 2-гідроксіетил, 3-гідроксипропіл, 4-гідроксибутил, 5-гідроксипентил, 6-гідроксигексил, 2-(2-метоксіетоксі)етил, 2-(2-гідроксіетоксі)етил, 4-етоксикарбонілбутил, 4-ацетоксибутил, 3-ціанопропіл і 4-ціанобутил.
5. Сполука за будь-яким з попередніх пунктів, у якій р дорівнює 2.
6. Сполука за будь-яким з попередніх пунктів, у якій біциклічне кільце азонію містить замісники в положенні 3, включаючи всі можливі конфігурації асиметричного атома вуглецю.
7. Сполука за п. 6, у якій атом вуглецю в азонійбіциклічному кільці в положенні 3 знаходиться в R-конфігурації.
8. Сполука за п. 6, у якій атом вуглецю в азонійбіциклічному кільці в положенні 3 знаходиться в S-конфігурації.
9. Сполука за будь-яким з попередніх пунктів, у якій D означає групу формули (і), a R5 означає незаміщений феніл, 2-тієніл, 3-тієніл, 2-фурил або 3-фурил.
10. Сполука за будь-яким з попередніх пунктів, у якій D означає групу формули (і), a R6 означає 2-тієніл, 3-тієніл, 2-фурил, 3-фурил або циклопентил.
11. Сполука за будь-яким з попередніх пунктів, у якій D означає групу формули (і), а групу формули -O-CO-C(R5)(R6)(R7) вибирають із групи, яка включає 2,2-дитієн-2-ілацетокси, 2,2-дитієн-2-ілпропіонілокси, 2-гідрокси-2,2-дитієн-2-ілацетокси, 2-гідрокси-2-феніл-2-тієн-2-ілацетокси, 2-фур-2-ил-2-гідрокси-2-фенілацетокси, 2-фур-2-ил-2-гідрокси-2-тієн-2-ілацетокси, (2*)-2-гідрокси-2,3-дифенілпропіонілокси, 2-гідрокси-2-тієн-2-ілпент-4-еноїлокси, (2S)-2-циклопентил-2-гідрокси-2-тієн-2-ілацетокси й (2R)-2-циклопентил-2-гідрокси-2-тієн-2-ілацетокси.
12. Сполука за п. 11, у якій групу -O-CO-C(R5)(R6)(R7) вибирають із групи, яка включає 2-циклопентил-2-гідрокси-2-тієн-2-ілацетокси, 2,2-дитієн-2-ілацетокси, 2-гідрокси-2,2-дитієн-2-ілацетокси, 2,2-дитієн-2-ілпропіонілокси, 2-гідрокси-2-феніл-2-тієн-2-ілацетокси, 2-фур-2-ил-2-гідрокси-2-тієн-2-ілацетокси й 2-фур-2-ил-2-гідрокси-2-фенілацетокси.
13. Сполука за будь-яким з попередніх пунктів, у якій D означає групу формули (іі), а групу формули D-COO- вибирають із групи, яка включає 9-метил-9Н-флуорен-9-карбонілокси, 9-гідрокси-9Н-флуорен-9-карбонілокси, 9Н-ксантен-9-карбонілокси, 9-метил-9Н-ксантен-9-карбонілокси, 9-гідрокси-9Н-ксантен-9-карбонілокси, 9,10-дигідроантрацен-9-карбонілокси й 10,11-дигідро-5Н-дибензо[а,d]циклогептен-5-карбонілокси.
14. Сполука за п. 13, у якій групу формули D-COO- вибирають із групи, яка включає 9-метил-9Н-флуорен-9-карбонілокси, 9-гідрокси-9Н-флуорен-9-карбонілокси, 9Н-ксантен-9-карбонілокси, 9-метил-9Н-ксантен-9-карбонілокси й 9-гідрокси-9Н-ксантен-9-карбонілокси.
15. Сполука за будь-яким з попередніх пунктів, у якій атом вуглецю, заміщений групами R5, R6 і R7, знаходиться в R-конфігурації.
16. Сполука за будь-яким з попередніх пунктів, у якій атом вуглецю, заміщений групами R5, R6 і R7, знаходиться в S-конфігурації.
17. Сполука за п. 1, яка означає:
бромід (3R)-1-аліл-3-(2,2-дитієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-(2,2-дитієн-2-ілацетокси)-1-(4-метилпент-3-еніл)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-аліл-3-(2,2-дитієн-2-ілпропіонілоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-(4-метилпент-3-еніл)-3-(2,2-дитієн-2-ілпропіонілоксі)-1-азонійбіцикло[2.2.2]октану,
тpифтopaцeтaт (3R)-3-(2-гiдpoкcи-2,2-дитiєн-2-iлaцeтoкcі)-1-iзoпpoпiл-1-азонійбіцикло[2.2.2]октану,
тpифтopaцeтaт (3R)-1-циклoпpoпiлмeтил-3-(2-гiдpoкcи-2,2-дитiєн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
тpифтopaцeтaт (3R)-3-(2-гiдpoкcи-2,2-дитiєн-2-iлaцeтoкcі)-1-iзoбyтил-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-гептил-3-(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
тpифтopaцeтaт (3R)-1-циклoгeкcилмeтил-3-(2-гiдpoкcи-2,2-дитiєн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
тpифтopaцeтaт (3R)-1-(3-циклoгeкcилпpoпiл)-3-(2-гiдpoкcи-2,2-дитiєн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-аліл-3-(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-(2-гiдpoкcи-2,2-дитiєн-2-iлaцeтoкcи)-l-(4-мeтилпeнт-3-eнiл)-1-азонійбіцикло[2.2.2]октану,
тpифтopaцeтaт (3R)-1-(3,7-димeтилoктa-(E)-2,6-дiєнiл)-3-(2-гiдpoкcи-2,2-дитієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
тpифтopaцeтaт (3R)-3-(2-гiдpoкcи-2,2-дитiєн-2-iлaцeтoкcи)-l-(2-гідроксіетил)-1-азонійбіцикло[2.2.2]октану,
трифторацетат (3R)-3-(2-гідрокси-2,2-дитієн-2-ілацетокси)-1-(3-гідроксипропіл)-1-азонійбіцикло[2.2.2]октану,
трифторацетат (3R)-1-(4-гідроксибутил)-3-(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-(2-етоксіетил)-3-(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
гідрохлорид (3R)-3-(2-гідрокси-2,2-дитієн-2-ілацетокси)-1-[2-(2-гідроксіетоксі)етил]-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-(2-гідрокси-2,2-дитієн-2-ілацетокси)-1-[2-(2-метоксіетоксі)етил]-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1-оксиранілметил-1-азонійбіцикло[2.2.2]октану,
трифторацетат (3R)-1-(2-[1,3]діоксолан-2-ілетил)-3-(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
трифторацетат (3R)-3-(2-гідрокси-2,2-дитієн-2-ілацетокси)-1-{2-[2-(2-гідроксіетоксі)етоксі]етил}-1-азонійбіцикло[2.2.2]октану,
трифторацетат (3R)-1-(3-[1,3]діоксолан-2-ілпропіл)-3-(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
трифторацетат (3R)-1-(3-етоксикарбонілпропіл)-3-(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
трифторацетат (3R)-1-(4-етоксикарбонілбутил)-3-(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
трифторацетат (3R)-1-(4-ацетоксибутил)-3-(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
трифторацетат (3R)-1-(3-ціанопропіл)-3-(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
трифторацетат (3R)-1-(4-ціанобутил)-3-(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
трифторацетат (3R)-1-(6-ціаногексил)-3-(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
трифторацетат (3R)-3-(2-гідрокси-2,2-дитієн-2-ілацетокси)-1-(4,4,4-трифторбутил)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-аліл-3-(2-гідрокси-2-феніл-2-тієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-аліл-3-(2-фур-2-ил-2-гідрокси-2-фенілацетоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-аліл-3-(2-фур-2-ил-2-гідрокси-2-тієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-аліл-3-(9-метил-9Н-флуорен-9-карбонілоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-аліл-3-(9-гідрокси-9Н-флуорен-9-карбонілоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-(9-гідрокси-9H-флуорен-9-карбонілокси)-1-(4-метилпент-3-еніл)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-гептил-3-(9-гідрокси-9Н-флуорен-9-карбонілоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-(9-гідрокси-9Н-флуорен-9-карбонілокси)-1-оксиранілметил-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-(9-гідрокси-9Н-флуорен-9-карбонілокси)-1-[2-(2-метоксіетоксі)етил]-1-азонійбіцикло[2.2.2] октану,
бромід (3R)-1-(2-[1,3]дioкcoлaн-2-iлeтил)-3-(9-гiдpoкcи-9H-флyopeн-9-карбонілоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-аліл-3-(9Н-ксантен-9-карбонілоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-(4-метилпент-3-eніл)-3-(9H-ксантен-9-карбонілоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-аліл-3-(9-метил-9Н-ксантен-9-карбонілоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-аліл-3-(9-гідрокси-9Н-ксантен-9-карбонілоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-(3-гідроксипропіл)-3-(9-гідрокси-9H-кcaнтен-9-карбонілоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-аліл-3-(10,11-дигідро-5Н-дибензо[а,d]циклогептен-5-карбонілоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-(4-метилпент-3-еніл)-3-(10,11-дигідро-5Н-дибензо[а,d]циклогептен-5-карбонілоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-аліл-3-[(2*)-2-гідрокси-2,3-дифенілпропіонілоксі]-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-[(2*)-2-гідрокси-2,3-дифенілпропіонілокси)]-1-(4-метилпент-3-еніл)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-аліл-3-(2-гідрокси-2-тієн-2-ілпент-4-еноїлоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-(4-метилпент-3-еніл)-3-(2-гідрокси-2-тієн-2-ілпент-4-еноїлоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-аліл-3-[(2S)-2-циклопентил-2-гідрокси-2-тієн-2-ілацетоксі]-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-(4-метилпент-3-еніл)-3-[(2S)-2-циклопентил-2-гідрокси-2-тієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-аліл-3-[(2R)-2-циклопентил-2-гідрокси-2-тієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси-2-тієн-2-ілацетокси]-1-(2-гідроксіетил)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси-2-тієн-2-ілацетокси]-1-(3-гідроксипропіл)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси-2-тієн-2-ілацетокси]-1-(4-гідроксибутил)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси-2-тієн-2-ілацетокси]-1-[2-(2-гідроксіетоксі)етил]-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси-2-тієн-2-ілацетокси]-1-(6-гідроксигексил)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси-2-тієн-2-ілацетокси]-1-(5-гідроксипентил)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси-2-тієн-2-ілацетокси]-1-[3-(4-гідроксипіперидин-1-іл)пропіл]-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси-2-тієн-2-ілацетокси]-1-[4-(4-гідроксипіперидин-1-іл)бутил]-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-3-(9,10-дигідроантрацен-9-карбонілокси)-1-(2-гідроксіетил)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-(2-гідроксіетил)-3-(9Н-ксантен-9-карбонілоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-(2-гідроксіетил)-3-(9-гідрокси-9Н-ксантен-9-карбонілоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-(2-гідроксіетил)-3-(9-гідрокси-9Н-флуорен-9-карбонілоксі)-1-азонійбіцикло[2.2.2]октану,
бромід (3R)-1-(2-гідроксіетил)-3-(9-метил-9Н-флуорен-9-карбонілоксі)-1-азонійбіцикло[2.2.2]октану.
18. Спосіб одержання сполук формули (І)
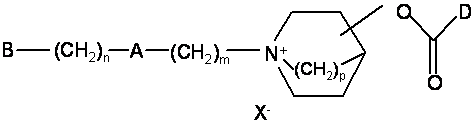 , (I)
, (I)
де В, n, A, m, p і D визначені в пп. 1-17, причому вказаний спосіб включає кватернізацію атома азоту азабіциклічного кільця в сполуці формули (III):
 , (III)
, (III)
де р і D визначені вище, алкілувальним агентом формули (II):
![]() , (II)
, (II)
де В, n, А і m визначені вище, a W означає групу, яка вилучається.
19. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-17 у суміші з фармацевтично прийнятним носієм або розріджувачем.
20. Сполука за будь-яким з пп. 1-17 або фармацевтична композиція за п. 19 для застосування при лікуванні людини або тварини.
21. Застосування сполуки за будь-яким з пп. 1-17 або фармацевтичної композиції за п. 19 для одержання лікарського засобу, призначеного для лікування респіраторних, урологічних захворювань або захворювань шлунково-кишкового тракту.
22. Спосіб лікування респіраторних, урологічних захворювань або захворювань шлунково-кишкового тракту, причому вказаний спосіб лікування включає введення людині або тварині, яка потребує такого лікування ефективної нетоксичної кількості сполуки за будь-яким з пп. 1-17 або фармацевтичної композиції за п. 19.
23. Комбінація продуктів, яка включає (і) сполуку за будь-яким з пп. 1-17, і (іі) іншу сполуку, ефективну при лікуванні респіраторних, урологічних захворювань або захворювань шлунково-кишкового тракту, причому вказану комбінацію використовують для одночасного, окремого або послідовного застосування.
24. Комбінація продуктів за п. 23, яка включає (і) сполуку за будь-яким з пп. 1-17, і (іі) агоніст ![]() , стероїд, антиалергічний лікарський засіб, інгібітор фосфодіестерази IV і/або антагоніст лейкотриєну D4 (LTD4), причому вказану комбінацію використовують для одночасного, окремого або послідовного застосування при лікуванні респіраторних захворювань.
, стероїд, антиалергічний лікарський засіб, інгібітор фосфодіестерази IV і/або антагоніст лейкотриєну D4 (LTD4), причому вказану комбінацію використовують для одночасного, окремого або послідовного застосування при лікуванні респіраторних захворювань.
Текст
1. Сполука формули (І): O D (19) 1 3 С8циклоалкіл і неароматичний гетероцикліл, заміщений принаймні гідроксигрупою. 3. Сполука за п. 1, де група азонійбіцикло заміщена за атомом азоту групою, яку вибирають із групи, яка включає аліл, 4-метилпент-3-еніл, ізопропіл, циклопропілметил, ізобутил, гептил, циклогексилметил, 3-циклогексилпропіл, 3,7диметилокта-(Е)-2,6-дієніл, 2-гідроксіетил, 3гідроксипропіл, 4-гідроксибутил, 5-гідроксипентил, 6-гідроксигексил, 2-етоксіетил, 2-(2гідроксіетоксі)етил, 2-(2-метоксіетоксі)етил, оксиранілметил, 2-[1,3]діоксолан-2-ілетил, 2-[2-(2гідроксіетоксі)етоксі]етил, 3-[1,3]діоксолан-2ілпропіл, 2-етоксикарбонілетил, 3етоксикарбонілпропіл, 4-етоксикарбонілбутил, 4ацетоксибутил, 2-ціаноетил, 3-ціанопропіл, 4ціанобутил, 6-ціаногексил, 4,4,4-трифторбутил, 3(4-гідроксипіперидин-1-іл)пропіл і 4-(4гідроксипіперидин-1-іл)бутил. 4. Сполука за п. 3, у якій група азонійбіцикло заміщена за атомом азоту групою, яку вибирають із групи, яка включає аліл, 4-метилпент-3-еніл, ізопропіл, циклопропілметил, ізобутил, гептил, 2гідроксіетил, 3-гідроксипропіл, 4-гідроксибутил, 5гідроксипентил, 6-гідроксигексил, 2-(2метоксіетоксі)етил, 2-(2-гідроксіетоксі)етил, 4етоксикарбонілбутил, 4-ацетоксибутил, 3ціанопропіл і 4-ціанобутил. 5. Сполука за будь-яким з попередніх пунктів, у якій р дорівнює 2. 6. Сполука за будь-яким з попередніх пунктів, у якій біциклічне кільце азонію містить замісники в положенні 3, включаючи всі можливі конфігурації асиметричного атома вуглецю. 7. Сполука за п. 6, у якій атом вуглецю в азонійбіциклічному кільці в положенні 3 знаходиться в Rконфігурації. 8. Сполука за п. 6, у якій атом вуглецю в азонійбіциклічному кільці в положенні 3 знаходиться в Sконфігурації. 9. Сполука за будь-яким з попередніх пунктів, у 5 якій D означає групу формули (і), a R означає незаміщений феніл, 2-тієніл, 3-тієніл, 2-фурил або 3-фурил. 10. Сполука за будь-яким з попередніх пунктів, у 6 якій D означає групу формули (і), a R означає 2тієніл, 3-тієніл, 2-фурил, 3-фурил або циклопентил. 11. Сполука за будь-яким з попередніх пунктів, у якій D означає групу формули (і), а групу формули 5 6 7 -O-CO-C(R )(R )(R ) вибирають із групи, яка включає 2,2-дитієн-2-ілацетокси, 2,2-дитієн-2ілпропіонілокси, 2-гідрокси-2,2-дитієн-2-ілацетокси, 2-гідрокси-2-феніл-2-тієн-2-ілацетокси, 2-фур-2-ил2-гідрокси-2-фенілацетокси, 2-фур-2-ил-2-гідрокси2-тієн-2-ілацетокси, (2*)-2-гідрокси-2,3дифенілпропіонілокси, 2-гідрокси-2-тієн-2-ілпент-4еноїлокси, (2S)-2-циклопентил-2-гідрокси-2-тієн-2ілацетокси й (2R)-2-циклопентил-2-гідрокси-2-тієн2-ілацетокси. 12. Сполука за п. 11, у якій групу -O-CO5 6 7 C(R )(R )(R ) вибирають із групи, яка включає 2циклопентил-2-гідрокси-2-тієн-2-ілацетокси, 2,2дитієн-2-ілацетокси, 2-гідрокси-2,2-дитієн-2ілацетокси, 2,2-дитієн-2-ілпропіонілокси, 2 88634 4 гідрокси-2-феніл-2-тієн-2-ілацетокси, 2-фур-2-ил-2гідрокси-2-тієн-2-ілацетокси й 2-фур-2-ил-2гідрокси-2-фенілацетокси. 13. Сполука за будь-яким з попередніх пунктів, у якій D означає групу формули (іі), а групу формули D-COO- вибирають із групи, яка включає 9-метил9Н-флуорен-9-карбонілокси, 9-гідрокси-9Нфлуорен-9-карбонілокси, 9Н-ксантен-9карбонілокси, 9-метил-9Н-ксантен-9-карбонілокси, 9-гідрокси-9Н-ксантен-9-карбонілокси, 9,10дигідроантрацен-9-карбонілокси й 10,11-дигідро5Н-дибензо[а,d]циклогептен-5-карбонілокси. 14. Сполука за п. 13, у якій групу формули D-COOвибирають із групи, яка включає 9-метил-9Нфлуорен-9-карбонілокси, 9-гідрокси-9Н-флуорен9-карбонілокси, 9Н-ксантен-9-карбонілокси, 9метил-9Н-ксантен-9-карбонілокси й 9-гідрокси-9Нксантен-9-карбонілокси. 15. Сполука за будь-яким з попередніх пунктів, у 5 6 7 якій атом вуглецю, заміщений групами R , R і R , знаходиться в R-конфігурації. 16. Сполука за будь-яким з попередніх пунктів, у 5 6 7 якій атом вуглецю, заміщений групами R , R і R , знаходиться в S-конфігурації. 17. Сполука за п. 1, яка означає: бромід (3R)-1-аліл-3-(2,2-дитієн-2-ілацетоксі)-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-(2,2-дитієн-2-ілацетокси)-1-(4метилпент-3-еніл)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(2,2-дитієн-2-ілпропіонілоксі)1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-(4-метилпент-3-еніл)-3-(2,2-дитієн-2ілпропіонілоксі)-1-азонійбіцикло[2.2.2]октану, тpифтopaцeтaт (3R)-3-(2-гiдpoкcи-2,2-дитiєн-2iлaцeтoкcі)-1-iзoпpoпiл-1азонійбіцикло[2.2.2]октану, тpифтopaцeтaт (3R)-1-циклoпpoпiлмeтил-3-(2гiдpoкcи-2,2-дитiєн-2-ілацетоксі)-1азонійбіцикло[2.2.2]октану, тpифтopaцeтaт (3R)-3-(2-гiдpoкcи-2,2-дитiєн-2iлaцeтoкcі)-1-iзoбyтил-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-гептил-3-(2-гідрокси-2,2-дитієн-2ілацетоксі)-1-азонійбіцикло[2.2.2]октану, тpифтopaцeтaт (3R)-1-циклoгeкcилмeтил-3-(2гiдpoкcи-2,2-дитiєн-2-ілацетоксі)-1азонійбіцикло[2.2.2]октану, тpифтopaцeтaт (3R)-1-(3-циклoгeкcилпpoпiл)-3-(2гiдpoкcи-2,2-дитiєн-2-ілацетоксі)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(2-гідрокси-2,2-дитієн-2ілацетоксі)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-3-(2-гiдpoкcи-2,2-дитiєн-2-iлaцeтoкcи)1-(4-мeтилпeнт-3-eнiл)-1азонійбіцикло[2.2.2]октану, тpифтopaцeтaт (3R)-1-(3,7-димeтилoктa-(E)-2,6дiєнiл)-3-(2-гiдpoкcи-2,2-дитієн-2-ілацетоксі)-1азонійбіцикло[2.2.2]октану, тpифтopaцeтaт (3R)-3-(2-гiдpoкcи-2,2-дитiєн-2iлaцeтoкcи)-l-(2-гідроксіетил)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-(3-гідроксипропіл)-1азонійбіцикло[2.2.2]октану, 5 трифторацетат (3R)-1-(4-гідроксибутил)-3-(2гідрокси-2,2-дитієн-2-ілацетоксі)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-(2-етоксіетил)-3-(2-гідрокси-2,2дитієн-2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану, гідрохлорид (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-[2-(2-гідроксіетоксі)етил]-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-(2-гідрокси-2,2-дитієн-2-ілацетокси)1-[2-(2-метоксіетоксі)етил]-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-(2-гідрокси-2,2-дитієн-2-ілацетоксі)1-оксиранілметил-1-азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-(2-[1,3]діоксолан-2-ілетил)3-(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-{2-[2-(2-гідроксіетоксі)етоксі]етил}-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-(3-[1,3]діоксолан-2ілпропіл)-3-(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-(3-етоксикарбонілпропіл)-3(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-(4-етоксикарбонілбутил)-3(2-гідрокси-2,2-дитієн-2-ілацетоксі)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-(4-ацетоксибутил)-3-(2гідрокси-2,2-дитієн-2-ілацетоксі)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-(3-ціанопропіл)-3-(2гідрокси-2,2-дитієн-2-ілацетоксі)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-(4-ціанобутил)-3-(2-гідрокси2,2-дитієн-2-ілацетоксі)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-(6-ціаногексил)-3-(2гідрокси-2,2-дитієн-2-ілацетоксі)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-(4,4,4-трифторбутил)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(2-гідрокси-2-феніл-2-тієн-2ілацетоксі)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(2-фур-2-ил-2-гідрокси-2фенілацетоксі)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(2-фур-2-ил-2-гідрокси-2-тієн2-ілацетоксі)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(9-метил-9Н-флуорен-9карбонілоксі)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(9-гідрокси-9Н-флуорен-9карбонілоксі)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-3-(9-гідрокси-9H-флуорен-9карбонілокси)-1-(4-метилпент-3-еніл)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-гептил-3-(9-гідрокси-9Н-флуорен-9карбонілоксі)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-3-(9-гідрокси-9Н-флуорен-9карбонілокси)-1-оксиранілметил-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-(9-гідрокси-9Н-флуорен-9карбонілокси)-1-[2-(2-метоксіетоксі)етил]-1азонійбіцикло[2.2.2]октану, 88634 6 бромід (3R)-1-(2-[1,3]дioкcoлaн-2-iлeтил)-3-(9гiдpoкcи-9H-флyopeн-9-карбонілоксі)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(9Н-ксантен-9-карбонілоксі)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-(4-метилпент-3-eніл)-3-(9H-ксантен9-карбонілоксі)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(9-метил-9Н-ксантен-9карбонілоксі)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(9-гідрокси-9Н-ксантен-9карбонілоксі)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-(3-гідроксипропіл)-3-(9-гідрокси-9Hкcaнтен-9-карбонілоксі)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(10,11-дигідро-5Ндибензо[а,d]циклогептен-5-карбонілоксі)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-(4-метилпент-3-еніл)-3-(10,11дигідро-5Н-дибензо[а,d]циклогептен-5карбонілоксі)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-[(2*)-2-гідрокси-2,3дифенілпропіонілоксі]-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-[(2*)-2-гідрокси-2,3дифенілпропіонілокси)]-1-(4-метилпент-3-еніл)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(2-гідрокси-2-тієн-2-ілпент-4еноїлоксі)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-(4-метилпент-3-еніл)-3-(2-гідрокси-2тієн-2-ілпент-4-еноїлоксі)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-[(2S)-2-циклопентил-2гідрокси-2-тієн-2-ілацетоксі]-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-(4-метилпент-3-еніл)-3-[(2S)-2циклопентил-2-гідрокси-2-тієн-2-ілацетоксі)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-[(2R)-2-циклопентил-2гідрокси-2-тієн-2-ілацетоксі)-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси-2тієн-2-ілацетокси]-1-(2-гідроксіетил)-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси-2тієн-2-ілацетокси]-1-(3-гідроксипропіл)-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси-2тієн-2-ілацетокси]-1-(4-гідроксибутил)-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси-2тієн-2-ілацетокси]-1-[2-(2-гідроксіетоксі)етил]-1азонійбіцикло[2.2.2]октану, (3R)-3-[(2S)-2-циклопентил-2-гідрокси-2бромід тієн-2-ілацетокси]-1-(6-гідроксигексил)-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси-2тієн-2-ілацетокси]-1-(5-гідроксипентил)-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси-2тієн-2-ілацетокси]-1-[3-(4-гідроксипіперидин-1іл)пропіл]-1-азонійбіцикло[2.2.2]октану, бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси-2тієн-2-ілацетокси]-1-[4-(4-гідроксипіперидин-1іл)бутил]-1-азонійбіцикло[2.2.2]октану, 7 88634 бромід (3R)-3-(9,10-дигідроантрацен-9карбонілокси)-1-(2-гідроксіетил)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-(2-гідроксіетил)-3-(9Н-ксантен-9карбонілоксі)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-(2-гідроксіетил)-3-(9-гідрокси-9Нксантен-9-карбонілоксі)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-(2-гідроксіетил)-3-(9-гідрокси-9Нфлуорен-9-карбонілоксі)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-(2-гідроксіетил)-3-(9-метил-9Нфлуорен-9-карбонілоксі)-1азонійбіцикло[2.2.2]октану. 18. Спосіб одержання сполук формули (І) D O B (CH2)n A (CH2)m N+ (CH2)p O X , (I) де В, n, A, m, p і D визначені в пп. 1-17, причому вказаний спосіб включає кватернізацію атома азоту азабіциклічного кільця в сполуці формули (III): D O N (CH2)p O , (III) де р і D визначені вище, алкілувальним агентом формули (II): B (CH2)n A (CH2)m W , (II) де В, n, А і m визначені вище, a W означає групу, яка вилучається. Даний винахід стосується нових терапевтично придатних похідних хінуклідину, деяких способів їх одержання й фармацевтичних композицій, які їх містять. Нові сполуки за даним винаходом є антимускариновими агентами, які мають високоефективну й довгострокову дію. Насамперед, такі сполуки характеризуються високою спорідненістю у відношенні мускаринових рецепторів М3. Мускаринові рецептори даного підвиду розташовані в залозах і гладенькій мускулатурі й опосередковують стимулюючий ефект у парасимпатичній системі на секрецію залози й скорочення гладенької мускулатури внутрішніх органів (див. книгу Cholinergic Transmission, Н.Р. Rang і ін., Pharmacology, Churchill Livingstone, гл. 6, New York (1995)). Відомо, що антагоністи рецепторів М3 використовують для лікування захворювань, які характеризуються підвищеним парасимпатичним тонусом, надлишковою залозистою секрецією або скороченням гладенької мускулатури (R.M. Eglen і S.S. Hegde, Drug News Perspect, 10(8), стор. 462-469 (1997)). Приклади захворювань такого роду включають респіраторні захворювання, такі як хронічне об 8 19. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-17 у суміші з фармацевтично прийнятним носієм або розріджувачем. 20. Сполука за будь-яким з пп. 1-17 або фармацевтична композиція за п. 19 для застосування при лікуванні людини або тварини. 21. Застосування сполуки за будь-яким з пп. 1-17 або фармацевтичної композиції за п. 19 для одержання лікарського засобу, призначеного для лікування респіраторних, урологічних захворювань або захворювань шлунково-кишкового тракту. 22. Спосіб лікування респіраторних, урологічних захворювань або захворювань шлунковокишкового тракту, причому вказаний спосіб лікування включає введення людині або тварині, яка потребує такого лікування ефективної нетоксичної кількості сполуки за будь-яким з пп. 1-17 або фармацевтичної композиції за п. 19. 23. Комбінація продуктів, яка включає (і) сполуку за будь-яким з пп. 1-17, і (іі) іншу сполуку, ефективну при лікуванні респіраторних, урологічних захворювань або захворювань шлунково-кишкового тракту, причому вказану комбінацію використовують для одночасного, окремого або послідовного застосування. 24. Комбінація продуктів за п. 23, яка включає (і) сполуку за будь-яким з пп. 1-17, і (іі) агоніст β2 , стероїд, антиалергічний лікарський засіб, інгібітор фосфодіестерази IV і/або антагоніст лейкотриєну D4 (LTD4), причому вказану комбінацію використовують для одночасного, окремого або послідовного застосування при лікуванні респіраторних захворювань. структивне захворювання легень (COPD), бронхіт, підвищена бронхіальна реактивність, астма, кашель і риніт; урологічні захворювання, такі як нетримання сечі, полакіурія, нейрогенний або нестабільний сечовий міхур, цистоспазм і хронічний цистит; захворювання шлунково-кишкового тракту, такі як синдром подразненого кишечнику, спастичний коліт, дивертикуліт і пептична виразка; а також серцево-судинні захворювання, такі як синусова брадикардія, індукована блукаючим нервом (див. книгу Muscarinic Receptor Agonists and Antagonists, Goodman і Gilman, The Pharmacological Basis of Therapeutics, 10-e вид., McGraw Hill, гл.7, New York (2001)). Сполуки за даним винаходом можна використовувати окремо або в комбінації з іншими лікарськими засобами, ефективними при лікуванні таких захворювань. Такі сполуки вводять, наприклад, у комбінації з β2-агоністами, стероїдами, протиалергічними лікарськими засобами, інгібіторами фосфодіестерази IV і/або антагоністами лейкотриєну D4 (LTD4) для одночасного, окремого або послідовного використання при лікуванні респіраторних захворювань. Сполуки за даним винаходом можна використовувати для лікування рес 9 піраторних захворювань, описаних вище, у комбінації з β2-агоністами, стероїдами, протиалергічними лікарськими засобами або інгібіторами фосфодіестерази IV. Сполуки з подібною структурою описані в ряді патентів як антихолінергічні агенти і/або спазмолітики. Наприклад, у патенті FR 2012964 описані похідні хінуклідину формули де R означаєН, OH або алкільну групу, яка мі1 стить від 1 до 4 атомів вуглецю, R означає феніл 2 або тієніл, a R означає циклогексил, циклопентил або тієніл, або якщо R означаєН, то R1 і R2 разом з атомом вуглецю, до якого вони приєднані, утворюють трициклічну групу формули 88634 10 де X означаєН, галоген, (нижч.)алкіл, (нижч.)алкокси, гідрокси, a R означає морфолініл, тіоморфолініл, піперидиніл, 1,4-діокса-8азаспіро[4,5]деканіл, 4-(2,6-диметилморфолініл), 4-кетопіперидиніл, 4-гідроксипіперидиніл, 4заміщений піперазиніл. У даний винахід включені також четвертинні солі (нижч.)алкілгалогенідів і фармацевтично прийнятні кислотно-адитивні солі. У патенті США №4644003 описані складні ефіри 3-хінуклідинолу й α-дизаміщених гліколевих кислот і їх фармацевтично прийнятні солі, де R означає феніл, незаміщений або заміщений не більше 3 замісниками, які включають алкокси, галоген, нітро, аміно, алкіламіно, діалкіламіно, 1 ациламіно й трифторметил, a R означає водень, алкіл, циклоалкіл, алкеніл, циклоалкеніл, алкініл, алкілоксіалкіл, циклоалкілоксіалкіл, галогеналкіл або галогеналкеніл. У заявці WO 92/04346 описані сполуки формули де X означає -O-, -S- або -CH2-, або кислотно-адитивні або солі четвертинного амонію вказаних вище сполук. У патенті США №4465834 описаний клас антихолінергічних лікарських препаратів формули 1 де R означає карбоциклічну або розгалужену аліфатичну групу, яка містить від 3 до 8 атомів вуглецю (таку як феніл, циклогексил, циклопентил, 2 циклопропіл, циклогептил і ізопропіл), R означає розгалужену або пряму аліфатичну групу, яка містить від 3 до 10 атомів вуглецю й 1 або 2 олефінові або ацетиленові зв'язки, або фенілетиніл, сти3 рил або етиніл, a R означає алкільну або циклічну групу, яка містить від 4 до 12 атомів вуглецю й атом азоту третинного аміну. Сполуки за даним винаходом включають також вільні основи або їх кислотно-адитивні солі, а також солі четвертинного амонію вказаних сполук. У патенті США №4843074 описані продукти формули і їх фармацевтично прийнятні солі, де X означає феніл (необов'язково заміщений) або тієніл, a "Het" означає (а) п'яти-членний азот-вмісний гетероцикл, (б) оксадіазоліл або тіадіазоліл або (в) шести-членну азот-вмісну гетероциклічну групу, m дорівнює 1 або 2 (більш докладний опис наведений у вказані вище публікаціях). У заявках WO 01/04118 і WO 02/053564 описані біциклічні сполуки азонію, загальна формула яких аналогічна до формули сполук за даним винаходом. У заявці WO 2004/096800 описані складні ефіри кватернізованих 3-хінуклідинолів формули 4 де кватернізуюча група (R ) означає C1С8алкіл, заміщений, наприклад, групами -OR11, 13 14 11 OCO-R або -COO-R , де R означає водень, С1С8алкіл, C1-С8алкіл-C1-С8алкокси або C1-С8алкіл13 С3-С15карбоцикліл, R означає C1-С8алкіл або С3С15карбоцикліл, a R14 означає водень, С3С15карбоциклічну групу, С1-С8алкеніл або C1С8алкіл, необов'язково заміщений С3С15карбоциклічною групою, причому насамперед вказані сполуки включають, наприклад, сполуки 1 11 алілоксикарбонілметил-3-(2-гідрокси-2,2-дитіофен2-ілацетокси)-1-азоній біцикло[2.2.2]октан і 1карбоксиметил-3-(2-гідрокси-2,2-дитіофен-2ілацетокси)-1-азоній біцикло[2.2.2]октан. У даному винаході пропонуються нові похідні складних ефірів хінуклідину формули (І), які мають високу антагоністичну активність у відношенні мускаринових рецепторів М3: де В означає атом водню або групу, яка виби1 1 рають із групи, яка включає -R , -OR , гідрокси, 1 O(CO)R , ціано й необов'язково заміщений неароматичний гетероцикліл, який містить один або бі1 льше гетероатомів, де R вибирають із групи, яка включає атоми водню, необов'язково заміщений C1-С8алкіл, необов'язково заміщений С2-С8алкеніл і необов'язково заміщений C3-С8циклоалкіл, п дорівнює цілому числу від 0 до 4, А вибирають із групи, яка включає -CH2-, CH=CR3-, -CR3=CH-, -CR3R4-, -О-, -СО-, -O-(СН2)23 4 O-, де R і R кожний незалежно означає атом водню або С1-С8алкіл, m дорівнює цілому числу від 0 до 8, р дорівнює цілому числу від 1 до 2, біциклічне кільце азонію містить замісники в положеннях 2, 3 або 4, включаючи всі можливі конфігурації асиметричних центрів, D вибирають із групи, яка включає: 5 де R вибирають із групи, яка включає феніл, 2-тієніл, 3-тієніл, 2-фураніл, 3-фураніл, причому вказані групи необов'язково заміщені одним або більше замісниками Ra, 6 R вибирають із групи, яка включає 2-тієніл, 3тієніл, 2-фураніл, 3-фураніл, С3-С8циклоалкіл, С3С8циклоалкеніл, С1-С8алкіл, С2-С8алкеніл, С2С8алкініл, бензил і фенетил, причому вказані групи необов'язково заміщені одним або більше замісниками Rb, 7 R означає атом водню або групу, яка вибирають із групи, яка включає гідроксил, гідроксиметил і метил, Q означає простий зв'язок або групу, яка вибирають із групи, яка включає -CH2-, -CH2CH2-, -О-, -O-CH2-, -S-, -S-CH2- і -CH=CH-, Ra і Rb незалежно вибирають із групи, яка включає атоми галогену, необов'язково заміщений необов'язково заміщений С1C1-С8алкіл, С8алкокси, гідрокси, трифторметил, нітро, ціано, 8 8 9 8 9 COOR , -NR R , де R і R незалежно означають атом водню або С1-С8алкіл, у означає ціле число від 0 до 3, X означає фармацевтично прийнятний аніон моно- або поліосновної кислоти, 88634 12 за умови, що група B-(CH2)n-A-(CH2)m- не означає прямий С1-4алкіл, а також що виключені наступні сполуки: 1-алілоксикарбонілметил-3-(2-гідрокси-2,2дитіофен-2-ілацетокси)-1-азоній біцикло[2.2.2]октан і 1-карбоксиметил-3-(2-гідрокси-2,2-дитіофен-2ілацетокси)-1-азоній біцикло [2.2.2] октан. Інші об'єкти даного винаходу включають: а) спосіб одержання сполук формули (І), б) фармацевтичні композиції, які включають ефективну кількість вказаних сполук, в) застосування вказаних сполук для одержання лікарських засобів, призначених для лікування респіраторних захворювань, захворювань сечової системи та/або захворювань шлунково-кишкового тракту й г) способи лікування респіраторних захворювань, захворювань сечової системи та/або шлунково-кишкового тракту, причому вказані способи включають введення сполук за даним винаходом суб'єктові, який потребує такого лікування. Використаний у даному контексті термін «(нижч.)алкіл» означає необов'язково заміщені, прямі або розгалужені радикали, які містять від 1 до 8, переважно від 1 до 6 і більш переважно від 1 до 4 атомів вуглецю. Приклади включають радикали метил, етил, нпропіл, ізопропіл, н-бутил, втор-бутил і трет-бутил, н-пентил, 1-метилбутил, 2-метилбутил, ізопентил, 1-етилпропіл, 1,1-диметилпропіл, 1,2диметилпропіл, н-гексил або 1-етилбутил, 2етилбутил, 1,1-диметилбутил, 1,2-диметилбутил, 1,3-диметилбутил, 2,2-диметилбутил, 2,3диметилбутил, 2-метилпентил, 3-метилпентил, трифторметил і ізогексил. Використаний у даному контексті термін «(нижч.)алкеніл» означає необов'язково заміщені, прямі або розгалужені моно- або поліненасичені радикали, які містять від 2 до 8, переважно від 2 до 6 і більш переважно від 2 до 4 атомів вуглецю. Насамперед переважні алкенільні радикали є моно- або диненасиченими. Приклади включають радикали вініл, аліл, 1пропеніл, ізопропеніл, 1-бутеніл, 2-бутеніл, 3бутеніл, 1-пентеніл, 2-пентеніл, 3-пентеніл і 4пентеніл. Використаний у даному контексті термін «(нижч.)алкініл» означає необов'язково заміщені, прямі або розгалужені моно- або поліненасичені радикали, які містять від 2 до 8, переважно від 2 до 6 і більш переважно від 2 до 4 атомів вуглецю. Насамперед переважні алкінільні радикали є моно- або диненасиченими. Приклади включають радикали 1-пропініл, 2пропініл, 1-бутиніл, 2-бутиніл і 3-бутиніл. Використаний у даному контексті термін «(нижч.)алкокси» означає необов'язково заміщені прямі або розгалужені кисень-вмісні радикали, які містять в алкільному фрагменті від 1 до 8, переважно від 1 до 6 і більш переважно від 1 до 4 атомів вуглецю. Переважні алкоксирадикали включають метокси, етокси, н-пропокси, ізопропокси, н-бутокси, втор-бутокси, трет-бутокси, трифторметокси, диф 13 торметокси, гідроксиметокси, 2-гідроксіетокси або 2-гідроксипропокси. Використаний у даному контексті термін «циклоалкіл» означає насичені карбоциклічні радикали й, якщо не вказане інше, циклоалкільний радикал у більшості випадків містить від 3 до 7 атомів вуглецю. Циклоалкільний радикал у більшості випадків є незаміщеним або заміщеним 1, 2 або 3 замісниками, які є однаковими або різними. Якщо циклоалкільний радикал містить 2 або більше замісників, то замісники є однаковими або різними. Приклади включають циклопропіл, циклобутил, циклопентил, циклогексил і циклогептил. Переважними є радикали циклопропіл, циклопентил або циклогексил. Використаний у даному контексті термін «циклоалкеніл» означає частково ненасичені карбоциклічні радикали й, якщо не вказане інше, циклоалкенільний радикал у більшості випадків містить від 3 до 7 атомів вуглецю. Циклоалкенільний радикал у більшості випадків є незаміщеним або заміщеним 1, 2 або 3 замісниками, які є однаковими або різними. Якщо циклоалкенільний радикал містить 2 або більше замісників, то замісники є однаковими або різними. Приклади включають циклобутеніл, циклопентеніл, циклогексеніл і циклогептеніл. Переважними є циклопентеніл або циклогексеніл. Використаний у даному контексті термін «гетероциклічний радикал» у більшості випадків означає неароматичне, насичене або ненасичене C3-С10карбоциклічне кільце, таке як 5-, 6- або 7членний радикал, у якому один або більше, наприклад, 1, 2, 3 або 4 атоми вуглецю, переважно 1 або 2 атомів вуглецю замінені на гетероатом, який вибирають із групи, яка включає N, O і S, за винятком групи бензо[1,3]діоксоліл. Переважними є насичені гетероциклічні радикали. Гетероциклічний радикал включає одне кільце, два або більше конденсовані кільця, причому принаймні одне кільце містить гетероатом. Якщо гетероциклічний радикал містить 2 або більше замісників, то замісники є однаковими або різними. Гетероциклічний радикал у більшості випадків є незаміщеними або заміщені 1, 2 або 3 замісниками, які є однаковими або різними. Замісники переважно вибирають із групи, яка включає атоми галогену, переважно атоми фтору, гідрокси, оксо, алкіл, який містить від 1 до 4 атомів вуглецю, і алкокси, який містить від 1 до 4 атомів вуглецю. Якщо гетероциклічний радикал містить 2 або більше замісників, то замісники є однаковими або різними. Приклади неароматичних гетероциклічних радикалів включають піперидил, піролідиніл, піролініл, піперазиніл, морфолініл, тіоморфолініл, піразолініл, піразолідиніл, хінуклідиніл, імідазолідиніл, оксираніл і азаридиніл. Використаний у даному контексті термін «атом галогену» означає атоми хлору, фтору, брому або йоду, у більшості випадків атоми фтору, хлору або брому, найбільш переважно атоми хлору або фтору. Використаний у даному контексті термін «необов'язково заміщена група або радикал» означає, 88634 14 що деякі атоми водню в даній групі або радикалі замінені не більше, ніж на 3 замісники, які вибирають із групи, яка включає атоми галогену, гідрокси, алкіл, який містить від 1 до 4 атомів вуглецю, і алкокси, який містить від 1 до 4 атомів вуглецю. Якщо група містить більше 1 замісника, переважними є замісники, пов'язані з різними атомами в вказаній групі. Використаний у даному контексті термін «моно- або поліосновна кислота» означає фармацевтично прийнятні кислоти, які включають як неорганічні кислоти, наприклад, хлористоводневу, сірчану, фосфорну, дифосфорну, бромистоводневу, йодистоводневу й азотну кислоти, і органічні кислоти, наприклад, лимонну, фумарову, малеїнову, яблучну, мигдалеву, аскорбінову, щавлеву, янтарну, винну, бензойну, мурашину, оцтову, трифтороцтову, метансульфонову, етансульфонову, бензолсульфонову або пара-толуолсульфонову кислоту. Якщо сполуки за даним винаходом містять один або більше хіральних центрів, то в даний винахід включені всі конфігурації хірального центра й, насамперед, енантіомери або діастереомери з різними конфігураціями. Приклади хіральних центрів, які присутні в сполуках за даним винаходом, включають, без обмеження перерахованим, четвертинний атом азоту в біциклічному азонієвому кільці, атом вуглецю в біциклічному азонієвому кільці, до якого приєднана група D-COO-, і атом вуглецю, через який група D приєднана до складноефірної групи. У переважному варіанті здійснення даного винаходу сполуки формули (І) є сполуками, у яких В означає атом водню або групу, яка вибирають із 1 1 1 групи, яка включає -R , -OR , гідрокси, -O(CO)R , ціано й необов'язково заміщений неароматичний гетероцикліл, який містить один або більше гетероатомів, де 1 R вибирають із групи, яка включає атом водню, необов'язково заміщений C1-С8алкіл, необов'язково заміщений С2-С8алкеніл і необов'язково заміщений C3-С8циклоалкіл, n дорівнює цілому числу від 0 до 4, А вибирають із групи, яка включає -CH2-, CH=CR3-, -CR3=CH-, -CR3R4-, -О-, -СO-, -O-(СН2)23 4 O-, де R і R кожний незалежно означає атом водню або С1-С8алкіл, m дорівнює цілому числу від 0 до 8, р дорівнює цілому числу від 1 до 2, біциклічне кільце азонію містить замісники в положеннях 2, 3 або 4, включаючи всі можливі конфігурації асиметричних центрів, D вибирають із групи, яка включає: 5 де R вибирають із групи, яка включає феніл, 2-тієніл, 3-тієніл, 2-фураніл, 3-фураніл, причому вказані групи необов'язково заміщені одним або більше замісниками Ra, 15 R6 вибирають із групи, яка включає 2-тієніл, 3тієніл, 2-фураніл, 3-фураніл, С3-С8циклоалкіл, С3С8циклоалкеніл, С1-С8алкіл, С2-С8алкеніл, С2С8алкініл, бензил і фенетил, причому вказані групи необов'язково заміщені одним або більше замісниками Rb, R7 означаєатом водню або групу, яка вибирають із групи, яка включає гідроксил, гідроксиметил і метил, Q означає простий зв'язок або групу, яка вибирають із групи, яка включає -CH2-, -CH2CH2-, -О-, -O-CH2-, -S-, -S-CH2- і -CH=CH-, Ra і Rb незалежно вибирають із групи, яка включає атоми галогену, необов'язково заміщений необов'язково заміщений C1C1-С8алкіл, С8алкокси, гідрокси, трифторметил, нітро, ціано, COOR8, -NR8R9, де R8 і R9 незалежно означають атом водню або C1-С8алкіл, у дорівнює цілому числу від 0 до 3, X означає фармацевтично прийнятний аніон моно- або поліосновної кислоти, за умови, що група B-(CH2)n-A-(CH2)m- не означає прямий С1-С4алкіл і C1-С8алкіл, заміщений групами -OR11, -OCO-R13 або -COO-R14, де R11 C1-С8алкіл-C1означає водень, C1-С8алкіл, С8алкокси або С1-С8алкіл-O-С3-С15карбоцикліл, R13 14 означає C1-С8алкіл або С3-С15карбоцикліл, a R означає водень, C3-С15карбоцикліл, С1-С8алкеніл або С1-С8алкіл, необов'язково заміщений C3С15карбоциклічною групою. В одному варіанті здійснення даного винаходу сполуки формули (І) переважно є сполуками, у яких А вибирають із групи, яка включає -CH2-, CH=CR3-, -CR3=CH-, -CR3R4-, -O-, -O-(СН2)2-O-, де 3 4 R і R кожний незалежно означає атом водню або C1-С8алкіл. В іншому варіанті здійснення даного винаходу сполуки формули (І) переважно є сполуками, у яких В вибирають із групи, яка включає атоми водню, гідрокси, необов'язково заміщений C1С8алкіл, необов'язково заміщений C2-С8алкеніл, необов'язково заміщений С3-С8циклоалкіл і неароматичний гетероцикліл, заміщений принаймні гідроксигрупою. В ще одному варіанті група азонійбіцикло заміщена за атомом азоту групою, яку вибирають із групи, яка включає аліл, 4-метилпент-3-еніл, ізопропіл, циклопропілметил, ізобутил, гептил, циклогексилметил, 3-циклогексилпропіл, 3,7диметилокта-(Е)-2,6-дієніл, 2-гідроксіетил, 3гідроксипропіл, A-гідроксибутил, 5-гідроксипентил, 6-гідроксигексил, 2-етоксіетил, 2-(2гідроксіетокси)етил, 2-(2-метоксіетокси)етил, оксиранілметил, 2-[1,3]діоксолан-2-ілетил, 2-[2-(2гідроксіетокси)етокси]етил, 3-[1,3]діоксолан-2ілпропіл, 2-етоксикарбонілетил, 3етоксикарбонілпропіл, 4-етоксикарбонілбутил, Aацетоксибутил, 2-ціаноетил, 3-ціанопропіл, 4ціанобутил, 6-ціаногексил, 4,4,4-трифторбутил, 3(4-гідроксипіперидин-1-іл)пропіл і 4-(4гідроксипіперидин-1-іл)бутил. Більш переважно, група азонійбіцикло заміщена за атомом азоту групою, яку вибирають із групи, яка включає аліл, 4-метилпент-3-еніл, ізопропіл, циклопропілметил, ізобутил, гептил, 2-гідроксіетил, 3-гідроксипропіл, 88634 16 A-гідроксибутил, 5-гідроксипентил, 6гідроксигексил, 2-(2-гідроксіетокси)етил, 2-(2метоксіетокси)етил, 4-етоксикарбонілбутил, 4ацетоксибутил, 3-ціанопропіл і 4-ціанобутил. Ще більш переважно, група азонійбіцикло заміщена за атомом азоту групою, яку вибирають із групи, яка включає аліл, 4-метилпент-3-еніл і н-гептил, найбільш переважно групою, яку вибирають із групи, яка включає аліл і н-гептил, і ще більш переважно аліл. В одному варіанті р дорівнює 2. В іншому варіанті біциклічне кільце азонію містить замісники в положенні 3, включаючи всі можливі конфігурації асиметричного вуглецю. Більш переважно третій атом вуглецю в азонійбіциклічному кільці знаходиться в R конфігурації. 5 У ще одному варіанті R означає незаміщений феніл, 2-тієніл, 3-тієніл, 2-фурил або 3-фурил. 6 В одному варіанті R означає 2-тієніл, 3-тієніл, 2-фурил, 3-фурил або циклопентил. В іншому варіанті групу формули -O-CO5 6 7 C(R )(R )(R ) вибирають із групи, яка включає 2,2дитієн-2-ілацетокси, 2,2-дитієн-2-ілпропіонілокси, 2-гідрокси-2,2-дитієн-2-ілацетокси, 2-гідрокси-2феніл-2-тієн-2-ілацетокси, 2-фур-2-ил-2-гідрокси-2фенілацетокси, 2-фур-2-ил-2-гідрокси-2-тієн-2ілацетокси, (2*)-2-гідрокси-2,3дифенілпропіонілокси, 2-гідрокси-2-тієн-2-ілпент-4еноїлокси, (2S)-2-циклопентил-2-гідрокси-2-тієн-2ілацетокси й (2R)-2-циклопентил-2-гідрокси-2-тієн2-ілацетокси. Більш переважно групу -O-CO5 6 7 C(R )(R )(R ) вибирають із групи, яка включає 2циклопентил-2-гідрокси-2-тієн-2-ілацетокси, 2,2дитієн-2-ілацетокси, 2-гідрокси-2,2-дитієн-2ілацетокси, 2,2-дитієн-2-ілпропіонілокси, 2гідрокси-2-феніл-2-тієн-2-ілацетокси, 2-фур-2-ил-2гідрокси-2-тієн-2-ілацетокси й 2-фур-2-ил-2гідрокси-2-фенілацетокси. Ще більш переважно 5 6 7 групу -O-СО-C(R )(R )(R ) вибирають із групи, яка включає 2-гідрокси-2,2-дитієн-2-ілацетокси й (2S)2-циклопентил-2-гідрокси-2-тієн-2-ілацетокси й найбільш переважно 2-гідрокси-2,2-дитієн-2ілацетокси. У ще одному варіанті групу формули D-COOвибирають із групи, яка включає 9-метил-9Нфлуорен-9-карбонілокси, 9-гідрокси-9Н-флуорен9-карбонілокси, 9Н-ксантен-9-карбонілокси, 9метил-9Н-ксантен-9-карбонілокси, 9-гідрокси-9Нксантен-9-карбонілокси, 9,10-дигідроантрацен-9карбонілокси й 10,11-дигідро-5НБільш дибензо[а,d]циклогептен-5-карбонілокси. переважно групу формули D-COO- вибирають із групи, яка включає 9-метил-9Н-флуорен-9карбонілокси, 9-гідрокси-9Н-флуорен-9карбонілокси, 9Н-ксантен-9-карбонілокси, 9-метил9Н-ксантен-9-карбонілокси й 9-гідрокси-9Нксантен-9-карбонілокси, і найбільш переважно 9метил-9Н-ксантен-9-карбонілокси й 9-гідрокси-9Нксантен-9-карбонілокси. В одному варіанті атом вуглецю, заміщений 5 6 7 групами R , R і R , знаходиться в R-конфігурації. В іншому варіанті атом вуглецю, заміщений 5 6 7 групами R , R і R , знаходиться в S-конфігурації. Наступні сполуки призначені для ілюстрації даного винаходу без обмеження його обсягу: 17 бромід (3R)-1-аліл-3-(2,2-дитієн-2-ілацетокси)1-азонійбіцикло[2.2.2]октану, бромід (3R)-3-(2,2-дитієн-2-ілацетокси)-1 -(4метилпент-3-еніл)-1-азонійбіцикло [2.2.2] октану, бромід (3R)-1 -аліл-3-(2,2-дитієн-2ілпропіонілокси)-1 -азонійбіцикло[2.2.2]октану, бромід (3R)-1-(4-метилпент-3-еніл)-3-(2,2дитієн-2-ілпропіонілокси)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-ізопропіл-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-циклопропілметил-3-(2гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану, трифторацетат (ЗR)-3-(2-гiдpoкcи-2,2-дитiєн-2iлaцeтoкcи)-1-ізобутил-1-азонійбіцикло [2.2.2]октану, бромід (3R)-1-гептил-3-(2-гідрокси-2,2-дитієн2-ілацетокси)-1-азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-циклогексилметил-3-(2гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-(3-циклoгeкcилпpoпiл)3-(2-гiдpoкcи-2,2-дитiєн-2-ілацетокси)-1азонійбіцикло[2.2.2] октану, бромід (3R)-1-аліл-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-3-(2-гiдpoкcи-2,2-дитiєн-2iлaцeтoкcи)-1-(4-мeтилпeнт-3-eнiл)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-(3,7-диметилокта-(E)2,6-дієніл)-3-(2-гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-(2-гідроксіетил)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-(3-гідроксипропіл)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-(4-гідроксибутил)-3-(2гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-(2-етоксіетил)-3 -(2-гідрокси-2,2дитієн-2-ілацетокси)-1-азонійбіцикло[2.2.2]октану, гідрохлорид (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-[2-(2-гідроксіетокси)етил]-1азонійбіцикло [2.2.2] октану, бромід (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-[2-(2-метоксіетокси)етил]-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-оксиранілметил-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-(2-[1,3]діоксолан-2ілетил)-3-(2-гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло [2.2.2] октану, трифторацетат (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-(2-[2-(2-гідроксіетокси)етокси] етил)1-азонійбіцикло[2.2.2] октану, трифторацетат (3R)-1-(3-[1,3]дioкcoлaн-2iлпpoпiл)-3-(2-гiдpoкcи-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану, 88634 18 трифторацетат (3R)-1-(3етоксикарбонілпропіл)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-(4етоксикарбонілпропіл)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-(4-ацетоксибутил)-3-(2гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-(3-ціанопропіл)-3-(2гідрокси-2,2-дитієн-2-ілацетокси)-1-азонійбіцикло [2.2.2]октану, трифторацетат (3R)-1-(4-ціанобутил)-3-(2гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану, трифторацетат (3R)-1-(6-ціаногексил)-3-(2гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2] октану, трифторацетат (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-(4,4,4-трифторбутил)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(2-гідрокси-2-феніл-2тієн-2-ілацетокси)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(2-фур-2-ил-2-гідрокси-2фенілацетокси)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(2-фур-2-ил-2-гідрокси-2тієн-2-ілацетокси)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(9-метил-9Н-флуорен-9карбонілокси)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(9-гідрокси-9Н-флуорен9-карбонілокси)-1-азонійбіцикло[2.2.2] октану, бромід (3R)-3-(9-гiдpoкcи-9H-флyopeн-9кapбoнiлoкcи)-1-(4-мeтилпeнт-3-еніл)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-гептил-3 -(9-гідрокси-9Нфлуорен-9-карбонілокси)-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-(9-гiдpoкcи-9H-флyopeн-9кapбoнiлoкcи)-1-oкcиpaнiлмeтил-1-азонійбіцикло [2.2.2] октану, бромід (3R)-3-(9-гiдpoкcи-9H-флyopeн-9кapбoнiлoкcи)-1-[2-(2-метоксіетокси)етил]-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-(2-[1,3] діоксолан-2-ілетил)-3-(9гідрокси-9Н-флуорен-9-карбонілокси)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(9Н-ксантен-9карбонілокси)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-(4-метилпент-3-еніл)-3-(9Нксантен-9-карбонілокси)-1-азонійбіцикло [2.2.2] октану, бромід (3R)-1-аліл-3-(9-метил-9Н-ксантен-9карбонілокси)-1-азонійбіцикло [2.2.2] октану, бромід (3R)-1-аліл-3-(9-гідрокси-9Н-ксантен-9карбонілокси)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-(3-гідроксипропіл)-3-(9-гідрокси9H-ксантен-9-карбонілокси)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-aлiл-3-(10,11-дигiдpo-5Hдибeнзo[a,d]циклoгeптeн-5-карбонілокси)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-(4-метилпент-3-еніл)-3-(10,11дигідро-5Н-дибензо[а,d]циклогептен-5карбонілокси)-1-азонійбіцикло[2.2.2]октану, 19 бромід (3R)-1-аліл-3-[(2*)-2-гідрокси-2,3дифенілпропіонілокси]-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-[(2*)-2-гідрокси-2,3дифенілпропіонілокси)]-1-(4-метилпент-3-еніл)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-(2-гідрокси-2-тієн-2ілпент-4-еноїлокси)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-(4-метилпент-3-еніл)-3-(2гідрокси-2-тієн-2-ілпент-4-еноїлокси)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-аліл-3-[(2S)-2-циклопентил-2гідрокси-2-тієн-2-ілацетокси]-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-(4-метилпент-3-еніл)-3-[(2S)-2циклопентил-2-гідрокси-2-тієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-aлiл-3-[(2R)-2-циклoпeнтил-2гiдpoкcи-2-тiєн-2-iлaцeтoкcи)-1-азонійбіцикло [2.2.2] октану, бромід (3R)-3-[(2S)-2-циклoпeнтил-2-гiдpoкcи2-тiєн-2-iлaцeтoкcи]-1-(2-гідроксіетил)-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-[(2S)-2-циклoпeнтил-2-гiдpoкcи2-тiєн-2-iлaцeтoкcи]-1-(3-гідроксипропіл)-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-[(2S)-2-циклoпeнтил-2-гiдpoкcи2-тiєн-2-iлaцeтoкcи]-1-(4-гідроксибутил)-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-[(2S)-2-циклoпeнтил-2-гiдpoкcи2-тiєн-2-iлaцeтoкcи]-1-[2-(2-гідроксіетокси)етил]-1азонійбіцикло[2.2.2]октану, бромід (3R)-3-[(2S)-2-циклoпeнтил-2-гiдpoкcи2-тiєн-2-iлaцeтoкcи]-1-(6-гідроксигексил)-1азонійбіцикло [2.2.2] октану, бромід (3R)-3-[(2S)-2-4HraoneHTM-2-riflpoKCH2-TieH-2-maneTOKCH]-1 -(5-гідроксипентил)-1азонійбіцикло[2.2.2]октану, бромід (ЗR)-3-[(2S)-2-циклoпeнтил-2-гiдpoкcи2-тiєн-2-iлaцeтoкcи]-1-[3-(4-гідроксипіперидин-1іл)пропіл]-1-азонійбіцикло[2.2.2]октану, бромід (3R)-3-[(2S)-2-циклoпeнтил-2-гiдpoкcи2-тiєн-2-iлaцeтoкcи]-1-[4-(4-гідроксипіперидин-1іл)бутил]-1-азонійбіцикло[2.2.2]октану, бромід (3R)-3-(9,10-дигідроантрацен-9карбонілокси)-1-(2-гідроксіетил)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-(2-гідроксіетил)-3-(9Н-ксантен-9карбонілокси)-1-азонійбіцикло[2.2.2]октану, бромід (3R)-1-(2-гідроксіетил)-3-(9-гідрокси-9Нксантен-9-карбонілокси)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-(2-гідроксіетил)-3-(9-гідрокси-9Нфлуорен-9-карбонілокси)-1азонійбіцикло[2.2.2]октану, бромід (3R)-1-(2-гідроксіетил)-3-(9-метил-9Нфлуорен-9-карбонілокси)-1-азонійбіцикло [2.2.2] октану. (* - конфігурація не визначена) Найбільший інтерес представляють сполуки: бромід 1-гептил-(3R)-3-(2-гідрокси-2,2-дитієн2-ілацетокси)-1-азонійбіцикло[2.2.2]октану, бромід 1-аліл-(3R)-3-(9-метил-9H-ксантен-9карбонілокси)-1-азонійбіцикло [2.2.2]октану, 88634 20 бромід 1-аліл-(3R)-3-(9-гідрокси-9H-ксантен-9карбонілокси)-1-азонійбіцикло [2.2.2] октану. У ще одному варіанті здійснення даного винаходу пропонуються способи одержання сполук формули (І). Нові похідні четвертинного амонію загальної формули (І) одержують, як показано на наведеній нижче схемі, при взаємодії алкілувального агента формули (II) зі сполуками загальної формули (III) з використанням двох можливих способів а) або b), докладно описаних в експериментальній частині. Методика b) включає використання твердофазної екстракції, що дозволяє одночасно одержати декілька сполук. У формулі (II), W означає будь-яку придатну групу, яка вилучається, переважно групу X , як описано вище для сполук загальної формули (І). Якщо W означає групу, яка вилучається, відмінну від X , то четвертинну амонійну сіль формули (І) одержують із продукту, отриманого за способом (а) або (b) з використанням реакції заміщення за стандартною методикою заміщення аніона W- на необхідний аніон X . Сполуки загальної формули (II), які не є комерційними продуктами, одержують за стандартними методиками. Наприклад, деякі сполуки формули 3 (II), де А означає -О-, -S-, -NR -, одержують за реакцією відповідного спирту, тіолу або похідного аміну або їх натрієвої або калієвої солі з алкілувальним агентом загальної формули Y-(CH2)m-W, де W має значення, визначене вище, більш переважно W означає атом галогену, a Y означає атом галогену або складний ефір сульфонату. В іншому варіанті сполуки загальної формули (II) одержують із відповідних похідних спиртів загальної формули (IV) за стандартними методиками. Сполуки формул (І) і (III) містять один або більше асиметричних атомів вуглецю. В обсяг даного винаходу включені всі можливі стереоізомери, індивідуальні ізомери й суміші ізомерів. Діастереомери сполук розділяють за стандартними методиками, наприклад, хроматографією або кристалізацією. Сполуки формули (III) одержують трьома різними способами (с), (d) і (е), як показано на наведеній нижче схемі й докладно описано в експериментальній частині. 21 88634 22 У сполуках формули (VI), описаних у способі 10 (с), R означає (нижч.)алкіл. Наступні сполуки формули (V) описані в літературі: 4-гідрокси-1-азабіцикло[2.2.1]гептан, описаний у заявці WO 93/15080, 4-гідрокси-1-азабіцикло[2.2.2]октан, описаний у статті Grob С.А. і ін., Helv.Chim.Acta, т. 41, стор 1184-1190 (1958), або (3R)-3-гідрокси-1-азабіцикло[2.2.2]октан (3S)-3-гідрокси-1-азабіцикло[2.2.2]октан, описаний у статті Ringdahl R., Acta Pharm Suec, т. 16, стор. 281-283 (1979) і є комерційним продуктом фірми CU Chemie Uetikon GmbH. Деякі сполуки загальної формули (III), де D означає групу формули і), R5 і R6 мають значення, описані вище, a R7 означає гідроксигрупу, одержують також зі складних ефірів гліоксалевої кислоти загальної формули (VII) за реакцією з відповідними металоорганічними похідними, як показано на наведеній нижче схемі й докладно описано в експериментальній частині (спосіб (f)). Сполуки формули (VII) одержують із відповідних гліоксилових кислот з використанням стандартних способів (с), (d) і (е) або як описано в заявках WO 01/04118 і WO 92/04346. Як показано на наведеній нижче схемі, сполуки формули (III), де R7 означає групу -CH2OH, оде ржують також з відповідної сполуки формули (III), 7 де R означає атомН, за реакцією з формальдегідом в основних умовах (див. методику (g), заявки WO 93/06098 і WO 02/053564). Структуру отриманих сполук визначали мето1 дами R-HMP і MC Спектри ЯМР реєстрували на приладі Varian 300МГц, причому величини хімічних зсувів вказані в част./млн. (δ) відносно величини внутрішнього стандарту тетраметилсилану. Чистоту сполук визначали методом PXBP із використанням хроматографії із оберненою фазою на приладі фірми Waters. Сполуки аналізували масспектрометрією (метод іонізації електроспреєм) на приладі фірми Hewlett Packard. Величини оптичного обертання вимірювали на поляриметрі PERKIN-ELMER 241 MC. Наведені нижче приклади призначені для ілюстрації й не обмежують обсягу винаходу. 23 Спосіб (а) Приклад 37 Бромід (3R)-1-гептил-3-(9-гідрокси-9Нфлуорен-9-карбонілокси)-1-азонійбіцикло [2.2.2] октану 250мг (0,75 ммоля) (3R)-1-азабіцикло[2.2.2]окт3-илового ефіру 9-гідрокси-9Н-флуорен-9карбонової кислоти (проміжна сполука 1-3) розчиняли в 4мл ацетонітрилу й 6мл CHCl3. В отриманий розчин додавали 0,59мл (0,67г, 3,75 ммоля) 1бромгептану. Після перемішування в атмосфері N2 протягом 72 год при кімнатній температурі розчинники упарювали, додавали ефір і суміш перемішували. Отриману тверду речовину декілька разів промивали ефіром і відфільтровували. Вихід вказаної в заголовку сполуки становив 330мг (85,5%). tпл. 214,9-216,6°C + MC: 434 [M-Br] . 1 Н-ЯМР (300МГц, ДМСО-d6) δ част./млн: 0,88 (t, 3Н), 1,12-1,70 (m, 12Н), 1,70-1,93 (m, 2Н), 2,04 (m, 1Н), 2,78 (m, 1Н), 2,96-3,18 (m, 3Н), 3,18-3,48 (m, 3Н), 3,77 (m, 1Н), 5,01 (m, 1Н), 6,84 (s, 1Н, ОН), 7,34 (m, 2Н), 7,45 (m, 2Н), 7,61 (m, 2Н), 7,84 (d, 2Н). Приклад 39 Бромід (3R)-3-(9-гідрокси-9Н-флуорен-9карбонілокси)-1-[2-(2-метоксіетокси)етил]-1азонійбіцикло[2.2.2]октану 0,5г (0,0015 моля) (3R)-1-азабіцикло[2.2.2]окт3-илового ефіру 9-гідрокси-9Н-флуорен-9карбонової кислоти (проміжна сполука 1-3) розчиняли в 10мл ацетонітрилу й 15мл CHCl3. В отриманий розчин додавали 1,02мл (1,37г, 0,0075 моля) 1-бром-2-(2-метоксіетокси)етану й суміш перемішували при кімнатній температурі протягом 96 год. Потім додавали ще одну порцію (0,2мл, 0,27г, 0,0015 моля) 1-бром-2-(2метоксіетокси)етану й суміш перемішували при кімнатній температурі протягом ще 24 год. Потім розчинники упарювали, додавали ефір і суміш перемішували, при цьому одержували тверду речовину, розчинник екстрагували й додавали ще одну порцію ефіру. Дану процедуру повторювали декілька разів з метою видалення залишкового алкілувального агента. Потім суспензію відфільтровували й отриману тверду речовину промивали ефіром і сушили. Вихід вказаної в заголовку сполуки становив 610мг (78,2%). tпл. 194°C. MC: 438 [M-Br]+. 1 H - Я М Р (300МГц, ДМСО-d6) δ част./млн: 1,44 (m, 1Н), 1,64 (m, 1Н), 1,85 (m, 2Н), 2,09 (m, 1Н), 2,93 (m, 1Н), 3,18-3,28 (m, 1Н), 3,26 (s, 3Н), 3,303,60 (m, 9Н), 3,73 (m, 2Н), 3,88 (m, 1Н), 5,00 (m, 1Н), 6,83 (s, 1Н, ОН), 7,35 (m, 2Н), 7,45 (m, 2Н), 7,61 (m, 2Н), 7,83 (d, 2Н). Приклад 43 Бромід (3R)-1-аліл-3-(9-метил-9Н-ксантен-9карбонілокси)-1-азонійбіцикло [2.2.2] октану 1,05г (3 ммоля) (3R)-1-азабіцикло[2.2.2]окт-3илового ефіру 9-метил-9Н-ксантен-9-карбонової кислоти розчиняли в 15мл ТГФ і додавали 0,544г (4,5 ммоля) 3-бромпроп-1-ену (алілброміду). Суміш кип'ятили зі зворотним холодильником протягом 4 год і перемішували при кімнатній температурі протягом 15 год. Потім розчинник 88634 24 1 концентрували до /4 вихідного об'єму, додавали ефір і суміш перемішували протягом 20хв, при цьому одержували тверду речовину, розчинник екстрагували й додавали ще одну порцію ефіру. Дану процедуру повторювали декілька разів з метою видалення залишкового алкілувального агента. Потім суспензію відфільтровували й отриману тверду речовину промивали ефіром і сушили. Вихід вказаної в заголовку речовини становив 1,04г (73,8%). tпл. 64,3-67,8°C. + MC: 390 [M-Br] . 1 H-ЯМР (300МГц, ДМСО-d6) δ част./млн: 1,35 (m, 1Н), 1,65 (m, 1Н), 1,73-1,91 (m, 2Н), 1,89 (s, 3Н), 2,11 (m, 1Н), 2,75 (m, 1Н), 3,00 (m, 1Н), 3,15-3,45 (m, 3Н), 3,70-3,90 (m, 3Н), 5,03 (m, 1Н), 5,50-5,65 (m, 2Н), 5,86 (m, 1Н), 7,12-7,19 (m, 4Н), 7,35 (m, 2Н), 7,42 (m, 2 Н). Спосіб (b) Приклад 29 Трифторацетат (3R)-1-(6-ціаногексил)-3-(2гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану 60мг (0,17 ммоля) (3R)-1-азабіцикло[2.2.2]окт3-илового ефіру 2-гідрокси-2,2-дитієн-2-ілоцтової кислоти розчиняли в 0,7мл ДМСО. В отриманий розчин додавали 161мг (0,128мл, 0,85 ммоля) 7бромгептаннітрилу, розчиненого в 0,3мл ДМСО. Після перемішування при кімнатній температурі протягом ночі суміш очищали твердофазної екстракцією на картриджі, що містить катіоно-обмінну смолу фірми Mega Bond Elut, попередньо промиту буферним розчином 0,1M Na2PO4, рН 7,5. Реакційну суміш наносили на картридж і промивали 1 раз 2мл ДМСО й потім 3 рази по 5мл CH3CN, при цьому всі вихідні матеріали втримувалися в промивних фракціях. Похідне амонію елюювали 5мл 0,03M розчину ТФО в суміші CH3CN/CHCl3, 2:1. Отриманий розчин нейтралізували додаванням 300мг полі(4-вінілпіридину), фільтрували й упарювали досуха. Вихід вказаної в заголовку сполуки становив 19,1мг (19,6%). MC: 459 [M-CF3COO]+. Спосіб (c) Похідні метилового ефіру загальної формули (VI) одержували за стандартними методиками етерифікації з відповідних карбонових кислот або за методиками, описаними у літературі: патент FR 2012964; статті Larsson L. і ін., Acta Pharm. Suec, 11 (3), 304-308 (1974); Nyberg К. і ін., Acta Chem. Scand., 24, 1590-1596 (1970); Cohen V.I. і ін, J. Pharm. Sciences, 81, 326-329 (1992); заявки WO 01/04118, WO 02/053564 і цитовані в них роботи. Проміжна сполука 1-1 Одержання (3R)-1-азабіцикло[2.2.2]окт-3илового ефіру 2,2-дитієн-2-ілоцтової кислоти 1,67г (0,007 моля) метилового ефіру 2,2дитієн-2-ілоцтової кислоти розчиняли в 40мл толуолу. В отриманий розчин додавали 1,04г (0,0082 моля) (3R)-3-гідрокси-1-азабіцикло[2.2.2]октану й 0,14г (0,0035 моля) HNa (60% дисперсія в мінеральному маслі). Суміш кип'ятили зі зворотним холодильником протягом 10хв, потім кип'ятили при безперервному видаленні дистиляту й заміні при необхідності на свіжий толуол протягом 2 год. 25 Охолоджену суміш екстрагували 2н. HCl, водний шар промивали етилацетатом, підлуговували K2CO3 і екстрагували CHCl3. Органічний шар промивали невеликою кількістю води, сушили над Na2SO4 і упарювали. Отриману речовину у вигляді масла (2г) очищали хроматографією на силікагелі (елюент CHCl3/MeOH/NH4OH, 95:5:0,5). Відповідні фракції об'єднували й упарювали, при цьому одержували вказаний у заголовку продукт у вигляді масла (0,82г, 35%). Вказаний продукт одержували у вигляді фумарату. Порцію отриманого масла 0,43г (0,00128 моля, у вигляді вільної основи) обробляли фумаровою кислотою в суміші ацетон/діетиловий ефір, при цьому одержували тверду речовину, яку відфільтровували й промивали ефіром. Вихід фумарату становив 0,44 г. Фумарат (3R)-1-азабіцикло[2.2.2]окт-3-илового ефіру 2,2-дитієн-2-ілоцтової кислоти tпл. 122°C. MC: 334 [M вільної основи + 1]+. 1 Н-ЯМР (300МГц, ДМСО-d6) δ част./млн: 1,44 (m, 1Н), 1,64 (m, 3Н), 2,03 (m, 1Н), 2,62-2,98 (m, 5Н), 3,30 (m, 1Н), 4,89 (m, 1Н), 5,84 (s, 1Н), 6,54 (s, 2Н), 7,01 (m, 2Н), 7,09 (m, 2Н), 7,48 (m, 2Н). Метиловий ефір 2,2-дитієн-2-ілоцтової кислоти одержували відновленням метилового ефіру 2гідрокси-2,2-дитієн-2-ілоцтової кислоти з наступною обробкою за методикою, описаною в статті F. Leonard, I. Ehranthal, J. Am. Chem. Soc, т. 73, стор. 2216-2218 (1951). Проміжна сполука 1-2 Одержання (3R)-1-азабіцикло[2.2.2]окт-3илового ефіру 2,2-дитієн-2-ілпропіонової кислоти 0,86г (0,0034 моля) метилового ефіру 2,2дитієн-2-ілпропіонової кислоти розчиняли в 25мл толуолу. В отриманий розчин додавали 0,51г (0,004 моля) (3R)-3-гідрокси-1азабіцикло[2.2.2]октану й 0,055г (0,0014 моля) HNa (60% дисперсія в мінеральному маслі). Отриману суміш кип'ятили зі зворотним холодильником протягом 10хв, а потім кип'ятили при безперервному видаленні дистиляту при необхідності із заміною на свіжий толуол протягом 1,5 год. Охолоджену суміш екстрагували 2н. HCl, водний шар промивали етилацетатом, підлуговували K2CO3 і екстрагували CHCl3. Органічний шар промивали невеликим об'ємом води, сушили над Na2SO4 і упарювали. Вихід вказаного в заголовку продукту у вигляді масла становив 1,11г (94,07%). ГХ-МС: 347 [M]+ Вказаний продукт одержували у вигляді оксалату. 0,25г вільної основи (0,00072 моля) обробляли щавлевою кислотою (0,065г, 0,00072 моля) у суміші ацетон/діетиловий ефір. При цьому одержували тверду речовину, яку відфільтровували й промивали ефіром. Вихід становив 0,25г (79,4%). Оксалат (3R)-1-азабіцикло[2.2.2]окт-3-илового ефіру 2,2-дитієн-2-ілпропіонової кислоти tпл. 126,7-128,6°C. 1 Н-ЯМР (300МГц, ДМСО-d6) част/млн: 1,61 (m, 2Н), 1,83 (m, 2Н), 2,08 (s, 3Н), 2,19 (m, 1Н), 2,88 (m, 1Н), 2,95-3,28 (m, 4Н), 3,61 (m, 1Н), 5,09 (m, 1Н), 7,01 (m, 2Н), 7,07 (m, 2Н), 7,51 (m, 2Н), 9,15 (ушир, s, 2Н). 88634 26 Метиловий ефір 2,2-дитієн-2-ілпропіонової кислоти одержували за стандартною методикою етерифікації з 2,2-дитієн-2-ілпропіонової кислоти, отриманої, як описано в статті М. Sy і ін. Bull. Soc. Chim. Fr, т. 7, стор. 2609-2611 (1957). Проміжна сполука I-3 Одержання (3R)-1-азабіцикло[2.2.2]окт-3илового ефіру 9-гідрокси-9Н-флуорен-9карбонової кислоти 1,0г (0,0042 моля) метилового ефіру 9гідрокси-9Н-флуорен-9-карбонової кислоти розчиняли в 25мл толуолу. В отриманий розчин додавали 0,67г (0,0053 моля) (3R)-3-гідрокси-1азабіцикло[2.2.2]октану й 0,064г (0,0016 моля) HNa (60% дисперсія в мінеральному маслі). Отриману суміш кип'ятили зі зворотним холодильником протягом 15хв, а потім кип'ятили при безперервному видаленні дистиляту із заміною при необхідності на свіжий толуол протягом 1,5 год. Охолоджену суміш екстрагували 2н. HCl, водний шар промивали діетиловим ефіром, підлуговували K2CO3 і екстрагували CHCl3. Органічний шар промивали водою, сушили над Na2SO4 і упарювали. Отриману тверду речовину обробляли діетиловим ефіром і фільтрували. Отриманий продукт перекристалізовували із суміші СНСl3/діізопропіловий ефір, фільтрували й промивали діізопропіловим ефіром. Вихід вказаного в заголовку продукту становив 0,75г (53,2%). tпл. 217°C. MC: 336 [М+1]+. 1 Н-ЯМР (300МГц, ДМСО-d6) δ част/млн: 1,00 (m, 2Н), 1,25-1,50 (m, 2Н), 1,60 (m, 1Н), 2,0-2,16 (m, 2Н), 2,37-2,56 (m, 3Н), 2,91 (m, 1Н), 4,57 (m, 1Н), 6,74 (ушир, s, 1Н, ОН), 7,31 (m, 2H), 7,42 (m, 2Н), 7,51 (m, 2Н), 7,81 (m, 2 Н). Метиловий ефір 9-гідрокси-9Н-флуорен-9карбонової кислоти одержували з 9-гідрокси-9Нфлуорен-9-карбонової кислоти (комерційний продукт) за стандартною методикою етерифікації. Наведені нижче сполуки формули (III) також одержували за способом (с): (3R)-1-азабіцикло[2.2.2]окт-3-иловий ефір 2гідрокси-2,2-дитієн-2-ілоцтової кислоти, (3R)-1-азабіцикло[2.2.2]окт-3-иловий ефір 2фур-2-ил-2-гідрокси-2-фенілоцтової кислоти, (3R)-1-азабіцикло[2.2.2]окт-3-иловий ефір 2фур-2-ил-2-гідрокси-2-тієн-2-ілоцтової кислоти, (3R)-1-азабіцикло[2.2.2]окт-3-иловий ефір 9метил-9Н-флуорен-9-карбонової кислоти, (3R)-1-азабіцикло[2.2.2]окт-3-иловий ефір 9метил-9Н-ксантен-9-карбонової кислоти, (3R)-1-азабіцикло[2.2.2]окт-3-иловий ефір 9гідрокси-9Н-ксантен-9-карбонової кислоти, (3R)-1-азабіцикло[2.2.2]окт-3-иловий ефір 2гідрокси-2-тієн-2-ілпент-4-енової кислоти, (3R)-1-азабіцикло[2.2.2]окт-3-иловий ефір (2S)2-циклопентил-2-гідрокси-2-тієн-2-ілоцтової кислоти й (3R)-1-азабіцикло[2.2.2]окт-3-иловий ефір (2R)2-циклопентил-2-гідрокси-2-тієн-2-ілоцтової кислоти, (2 останні сполуки одержували також за способом (f)). Спосіб (d) 27 Одержання (3R)-1-азабіцикло[2.2.2]окт-3илового ефіру 10,11-дигідро-5Ндибензо[а,d]циклогептен-5-карбонової кислоти 2,15г 10,11-дигідро-5Ндибензо[а,d]циклогептен-5-карбонової кислоти (9,0 ммоля) розчиняли в 40мл CHCl3 (що не містить етанолу). Розчин охолоджували до 0°C і додавали 0,86мл оксалілхлориду (9,9 ммоля) і краплю ДМФА. Суміш перемішували й нагрівали до кімнатної температури. Після витримування суміші при даній температурі протягом 1 год розчинники упарювали, залишок розчиняли в CHCl3 і розчинники знову упарювали. Дану процедуру повторювали 2 рази. Отримане масло розчиняли в 20мл толуолу й додавали в розчин 1,26г (9,9 ммоля) (3R)-3гідрокси-1-азабіцикло[2.2.2]октану в 40мл гарячого толуолу. Реакційну суміш кип'ятили зі зворотним холодильником протягом 2 год. Після охолодження суміш екстрагували 2н. HCl. Водний шар підлуговували K2CO3 і екстрагували CHCl3. Органічний шар сушили над Na2SO4 і упарювали досуха. Залишок очищали хроматографією на колонці (силікагель, елюент: CHCl3/MeOH/NH4OH, 95:5:0,5). Вихід вказаного в заголовку продукту становив 1,5г (48%). tпл. 112-113°C. ГХ-МС: 347 [M]+ 1 H-ЯМР (300МГц, CDCl3) δ част/млн: 1,10-1,35 (m, 2Н), 1,40-1,52 (m, 1Н), 1,52-1,68 (m, 1Н), 1,90 (m, 1Н), 2,40-2,60 (m, 2Н), 2,60-2,77 (m, 3Н), 2,832,96 (m, 2Н), 3,07-3,19 (m, 1Н), 3,25-3,40 (m, 2Н), 4,80 (m, 2Н), 7,10-7,30 (m, 8 Н). 10,11-дигідро-5Н-дибензо[а,d]циклогептен-5карбонову кислоту одержували, як описано в статті Kumazawa Т. і ін, J. Med. Chem, т. 37, стор. 804810 (1994). Наведену нижчу сполуку формули (III) також одержували за способом (d) з відповідної карбонової кислоти: (3R)-1-азабіцикло[2.2.2]окт-3-иловий ефір 9Нксантен-9-карбонової кислоти Спосіб (е) Проміжна сполука 1-5 Одержання 1-азабіцикло[2.2.2]окт-4-илового ефіру (2R)-2-циклогексил-2-гідрокси-2фенілоцтової кислоти 660мг (0,00282 моля) (2R)-2-циклогексил-2гідрокси-2-фенілоцтової кислоти (отриманої, як описано в заявці WO 02/053564) розчиняли в 9мл ДМФА. Розчин перемішували при кімнатній температурі й у нього додавали 548мг (0,00338 моля) 1,1'-карбонілдіімідазолу. Здійснення реакції контролювали ТШХ (елюент: СНСl3/МеОН/АсОН, 70:30:2) за утворенням імідазоліду. Через 1 год реакція завершена. Реакційну суміш охолоджували до 0°C і в неї додавали 394мг (0,0031 моля) 4гідрокси-1-азабіцикло[2.2.2]октану й 104мг (0,00259 моля) HNa (60% дисперсія в мінеральному маслі). Після перемішування протягом 44 год при кімнатній температурі реакційну суміш обробляли водою й 3 рази екстрагували діетиловим ефіром. Органічні шари об'єднували, промивали сольовим розчином і сушили над безводним сульфатом магнію. Розчинник упарювали й залишок очищали хроматографією на силікагелі (елюент: 88634 28 від CHCl3 до CHCl3/MeOH, 15:1). Вихід вказаного в заголовку продукту становив 300мг (31%). [α]22D=-27,6°(с 1,CHCl3) MC: 344 [М+1]+ 1 Н-ЯМР (300МГц, CDCl3) δ част/млн: 1,0-1,55 (m, 7Н), 1,55-1,75 (m, 2Н), 1,75-1,85 (m, 1Н), 1,852,05 (m, 6Н), 2,10-2,22 (m, 1Н), 2,90-3,10 (m, 6Н), 3,60-3,80 (ушир.s, 1Н, ОН), 7,20-7,40 (m, 3Н), 7,577,67 (m, 2Н). Спосіб (f) Проміжна сполука 1-6 Одержання (3R)-1-азабіцикло[2.2.2]окт-3илового ефіру 2-гідрокси-2,3-дифенілпропіонової кислоти 0,00386 моля хлориду бензилмагнію (1,93мл 2М розчину в ТГФ) додавали в розчин 1г (0,00385 моля) (3R)-1-азабіцикло[2.2.2]окт-3-илового ефіру 2-оксо-2-фенілоцтової кислоти, розчиненого в 8мл ТГФ при -70°C в атмосфері N2. Суміш перемішували при вказаній температурі протягом 10хв, потім нагрівали до кімнатної температури й розбавляли 4мл ТГФ. Через 1 год реакційну суміш обробляли 10% розчином K2CO3 і 2 рази екстрагували етилацетатом. Органічні фази об'єднували й сушили над Na2SO4. Після видалення розчинника отриману маслоподібну речовину розподіляли між 2н. HCl і діетиловим ефіром. Водну фазу підлуговували K2CO3 і екстрагували CHCl3. Органічний розчин промивали водою, сушили над Na2SO4 і розчинник упарювали, при цьому одержували 1,2г речовини у вигляді масла. Вказану реакцію повторювали з використанням як вихідні речовини 2г (0,0077 моля) (3R)-1азабіцикло[2.2.2]окт-3-илового ефіру 2-оксо-2фенілоцтової кислоти й 0,0077 моля хлориду бензилмагнію (3,85мл 2М розчину в ТГФ), при цьому одержували 2,91г кінцевого продукту у вигляді масла. Загальна кількість продукту (4,11г) очищали хроматографією на колонці (силікагель, елюент: градієнт CHCl3/MeOH/NH4OH, від 99:1:0,1 до 95:5:0,5). Відповідні фракції об'єднували, при цьому одержували 1,86г чистого продукту у вигляді твердої суміші діастереомерів І-6а і І-6b, яку розділяли мацерацією з використанням суміші діетиловий ефір/діізопропіловий ефір. Проміжна сполука І-6а Одержання (3R)-1-азабіцикло[2.2.2]окт-3илового ефіру (2*)-2-гідрокси-2,3дифенілпропіонової кислоти (діастереомер 1, перший отриманий діастереомер) 1,86г суміші діастереомерів (1-6) обробляли сумішшю діетиловий ефір/діізопропіловий ефір і фільтрували, при цьому одержували тверду речовину, охарактеризовану як чистий діастереомер. Вихід становив 0,87г (42,6% при розрахунку на індивідуальний ізомер). tпл. 132°C MC: 352 [М+1]+. 1 H - Я М Р (300МГц, CDCl3) δ част/млн: 1,301,60 (m, 2Н), 1,60-1,90 (m, 2Н), 2,05 (m, 1Н), 2,202,35 (m, 1Н), 2,50-2,90 (m, 4Н), 3,0-3,15 (m, 1Н), 3,25 і 3,60 (dd, 2Н), 3,70 (ушир.s, 1Н, ОН), 4,70-4,80 (m, 1Н), 7,15-7,45 (m, 8Н), 7,65-7,75 (m, 2Н). 29 Проміжна сполука І-6b Одержання (3R)-1-азабіцикло[2.2.2]окт-3илового ефіру (2*)-2-гідрокси-2,3дифенілпропіонової кислоти (діастереомер 2, другий отриманий діастереомер) Маточні розчини після фільтрування першого діастереомеру використовували для одержання другого діастереомеру. Після упарювання розчинників 0,55г залишку обробляли діетиловим ефіром і фільтрували, при цьому одержували тверду речовину, охарактеризовану як чистий другий діастереомер. Вихід становив 0,23г (11,2% при розрахунку на індивідуальний ізомер). tпл. 107°С. MC: 352 [М+1]+. 1 H-ЯMP (300МГц, CDCl3) δ част./млн: 1,20-1,35 (m, 1Н), 1,35-1,55 (m, 2Н), 1,55-1,70 (m, 1Н), 1,801,95 (m, 1Н), 2,55-2,90 (m, 5Н), 3,10-3,20 (m, 1Н), 3,25 і 3,60 (dd, 2Н), 3,80 (ушир.s, 1Н, ОН), 4,65-4,80 (m, 1Н), 7,20-7,50 (m, 8Н), 7,65-7,75 (m, 2Н). (*) - конфігурація не визначена, у цьому випадку можна одержати (2R)- або (2S)- ізомери описаних вище сполук. (3R)-1-азабіцикло[2.2.2]окт-3-иловий ефір 2оксо-2-фенілоцтової кислоти одержували, як описано в заявці WO 92/04346. Наведені нижче сполуки формули (III) також одержували за способом (f): (3R)-1-азабіцикло[2.2.2]окт-3-иловий ефір (2S)2-циклопентил-2-гідрокси-2-тієн-2-ілоцтової кислоти, (3R)-1-азабіцикло[2.2.2]окт-3-иловий ефір (2R)2-циклопентил-2-гідрокси-2-тієн-2-ілоцтової кислоти (сполуки одержували також за способом (с)) і ефір 2(3R)-1-азабіцикло[2.2.2]окт-3-иловий гідрокси-2-феніл-2-тієн-2-ілуксуной кислоти. Інші карбонові кислоти формули D-C(O)OH, одержання яких (або синтез їх метилових ефірів, гідрохлориду або імідазоліду) не описано в способах (с), (d), (е), і які не є комерційними продуктами, можна одержати за методиками, описаними у наступних роботах: FR 2012964, М.А. Davis і ін, J. Med. Chem, т. 6, стор. 513516 (1963), Т. Kumazawa і ін, J.Med. Chem, т. 37(6), стор. 804-810 (1994), М.А. Davis і ін, J. Med. Chem, т. 7, стор. 88-94 (1964), Sestanj K., Can. J. Chem, т. 49, стор. 664-665 (1971), Burtner R, J. Am. Chem. Soc, т. 65, стор. 15821585 (1943), Heacock R.A. і ін, Ann. Appl. Biol, т. 46(3), стор. 352-365 (1958), Rigaudy J. і ін., Bull. Soc. Chim. France, стор. 638-643 (1959), Ueda I. і ін., Bull. Chem. Soc. Jpn, т. 48 (8), стор. 2306-2309 (1975), E.L. May і ін, J. Am. Chem. Soc, т. 70, стор. 1077-1079 (1948), G.W. Moersch і ін. Synthesis, стор. 647-648 (1971), A. Waldemar і ін, J.Org. Chem, т. 42 (1), стор. 38-40 (1977), WO 01/04118 і WO 02/053564. 88634 30 В обсяг даного винаходу включені також фармацевтичні композиції, які як активний інгредієнт включають принаймні одне похідне хінуклідину загальної формули (І) у комбінації з фармацевтично прийнятним носієм або розріджувачем. Переважну композицію одержують у формі, призначеній для перорального введення. Для одержання композиції за даним винаходом використовують відомі фармацевтично прийнятні носії або розріджувачі, змішані з активною сполукою або сполуками, причому вибір конкретних ексципієнтів залежить, крім інших факторів, від способу введення композиції. Композиції за даним винаходом переважно одержують у формі для перорального введення. У цьому випадку композиції для перорального введення одержують у вигляді таблеток, таблеток із плівковим покриттям, рідких препаратів для інгаляції, порошкоподібних препаратів для інгаляції й аерозолів для інгаляції, причому всі вказані препарати містять одну або більше сполук за даним винаходом. Вказані препарати одержують відомими способами. Розріджувачі, використовувані при одержанні композицій, включають такі рідкі або тверді розріджувачі, які є сумісними з активним інгредієнтом, а також при необхідності з барвниками або ароматизаторами. Таблетки або таблетки із плівковим покриттям містять від 1 до 500мг, переважно від 5 до 300мг активного інгредієнта. Композиції для інгаляції містять від 1мкг до 1000мкг, переважно від 10мкг до 800мкг активного інгредієнта. При лікуванні людини доза сполуки загальної формули (І) залежить від необхідного ефекту й тривалості лікування, дози для дорослих у більшості випадків становлять від 3мг до 300мг на добу у вигляді таблеток і від 10мкг до 800мкг на добу у вигляді композиції для інгаляції. Фармакологічні властивості Оцінку зв'язування мускаринових рецепторів людини зі сполуками за винаходом й випробування на моделі бронхоспазмів у морських свинок проводили, як описано нижче. Зв'язування сполук з мускариновими рецепторами людини Зв'язування [3H]-NMS з мускариновими рецепторами людини проводили за методикою, описаною в статті Waelbroek і ін. Моl. Pharmacol, т. 38, стор. 267-273 (1990). Аналіз проводили при 25°C і використовували мембранну фракцію стабільно трансфектованих клітин яєчників китайського хом'яка K1 (СНО), які експресують гени мускаринових рецепторів людини М3. Для визначення величин IC50 мембранну фракцію суспендували в буферному розчині DPBS до кінцевої концентрації 89мкг/мл для рецепторів підтипу М3. Суспензію мембранної фракції інкубували в присутності сполуки, міченого тритієм, протягом 60хв. Після інкубування мембранну фракцію відокремлювали фільтруванням і вимірювали зв'язану радіоактивність. Неспецифічне зв'язування визна-4 чали при додаванні 10 M розчину атропіну. Для побудови кривих заміщення використовували принаймні 6 різних концентрацій у двох повторах. 31 Результати випробувань показали, що сполуки за даним винаходом характеризуються високою афінністю до мускаринових рецепторів М3, переважно мускаринових рецепторів людини. Переважні сполуки за даним винаходом характеризуються величиною IC50 (нМ) відносно рецепторів М3 менше 50, переважно менше 25, більш переважно менше 15 і найбільш переважно менше 10, 8 або 5. Випробування на моделі бронхоспазму в морських свинок Випробування проводили за методикою, описаною в статті Н. Konzett і F. Rossler, Arch. Exp. Path. Pharmacol, т. 195, стор. 71-74 (1940). Водні розчини досліджуваних агентів розпилювали й вводили самцям морських свинок (Dunkin-Hartley) при вдиханні після анестезії із штучною вентиляцію легень. Відповідну реакцію бронхів на внутрішньовенне введення ударної дози ацетилхоліну визначали перед введенням лікарського засобу й після нього за зміною опору легень через певні періоди часу, а інгібування бронхоспазму у відсотках визначали з використанням вказаної зміни опору. Сполуки за даним винаходом проявляють високу й довгострокову ефективність при інгібуванні відповідної реакції бронхоспазму на ацетилхолін. На основі описаних вище даних фахівцям у даній галузі представляється очевидним, що сполуки за даним винаходом характеризуються високою антимускариновою активністю (М3) і, отже, їх можна застосовувати при лікуванні захворювань, зв'язаних з мукариновим рецептором МЗ, включаючи респіраторні захворювання, такі як хронічне обструктивне захворювання легень (COPD), бронхіт, підвищена реактивність бронхів, астма, кашель і риніт; урологічні захворювання, такі як нетримання сечі, полакіурія, синдром нейрогенного або нестабільного сечового міхура, цистоспазм і хронічний цистит; захворювання шлунковокишкового тракту, такі як синдром подразненого кишки, спастичний коліт, дивертикуліт і пептична виразка, а також серцево-судинні захворювання, такі як синусова брадикардія, індукована блукаючим нервом. У даному винаході пропонується також сполука формули (І) або фармацевтично прийнятна композиція, яка включає сполуку формули (І), для застосування при лікуванні людини або тварин, насамперед для лікування респіраторних, урологічних захворювань або захворювань шлунковокишкового тракту. У даному винаході пропонується також застосування сполуки формули (І) або фармацевтично прийнятної композиції, які включає сполуку формули (І), для одержання лікарських засобів, призначених для лікування респіраторних, урологічних захворювань або захворювань шлунковокишкового тракту. В іншому варіанті сполуки формули (І) і фармацевтично прийнятні композиції, які включають сполуки формули (І), використовуються для лікування респіраторних, урологічних захворювань або захворювань шлунково-кишкового тракту, причому вказаний спосіб лікування включає вве 88634 32 дення людині або тварині, яка потребує такого лікування ефективної нетоксичної кількості сполуки формули (І) або фармацевтичної композиції, які включає сполуку формули (І). У ще одному варіанті сполуки формули (І) і фармацевтично прийнятні композиції, які включають сполуки формули (І), використовуються в комбінації з іншими лікарськими засобами, ефективними при лікуванні вказаних захворювань. Сполуки формули І використовують, наприклад, у комбінації з агоністами β2, стероїдами, протиалергічними лікарськими засобами, інгібіторами фосфодіестерази IV і/або лейкотриєну D4 (LTD4), для одночасного, окремого або послідовного введення при лікуванні респіраторного захворювання. Приклади сполук формули І Приклад 1 Бромід (3R)-1-аліл-3-(2,2-дитіен-2-ілацетокси)1-азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та а із проміжної сполуки 1-1. Вихід на кінцевій стадії становив 310мг, 90,9%. MC: 374 [M-Br]+. 1 Н-ЯМР (300МГц, ДМСО-d6) δ част./млн: 1,722,07 (m, 4Н), 2,28 (m, 1Н), 3,07-3,56 (m, 5Н), 3,783,99 (m, 3Н), 5,19 (m, 1Н), 5,52-5,68 (m, 2Н), 5,89 (s, 1Н), 5,98 (m, 1Н), 7,01 (m, 2Н), 7,12 (m, 2Н), 7,50 (m, 2Н). Приклад 2 Бромід (3R)-3-(2,2-дитієн-2-ілацетокси)-1-(4метилпент-3-еніл)-1-азонійбіцикло [2.2.2] октану Вказану в заголовку сполуку одержували за способами с та а із проміжної сполуки 1-1. Вихід на кінцевій стадії становив 270мг, 72,9%. tпл. 163,5-165,1°C. MC: 416 [M-Br]+. 1 Н-ЯМР (300МГц, ДМСО-d6) δ част./млн: 1,62 (s, 3Н), 1,67 (s, 3Н), 1,73-2,03 (m, 4Н), 2,20-2,43 (m, 3Н), 3,05-3,46 (m, 6Н), 3,52 (m, 1Н), 3,92 (m, 1Н), 4,98 (m, 1Н), 5,18 (m, 1Н), 5,89 (s, 1Н), 7,01 (m, 2Н), 7,13 (m, 2Н), 7,50 (m, 2Н). Приклад 3 Бромід (3R)-1-аліл-3-(2,2-дитієн-2ілпропіонілокси)-1-азонійбіцикло [2.2.2] октану Вказану в заголовку сполуку одержували за способами с та а із проміжної сполуки 1-2. Вихід на кінцевій стадії становив 260мг, 11,2%. tпл. 156-158°C. + MC: 388 [M-Br] . 1 Н-ЯMP (300МГц, ДМСО-d6) δ част./млн: 1,65 (m, 1Н), 1,80 (m, 1Н), 1,95 (m, 2Н), 2,08 (s, 3Н), 2,28 (m, 1Н), 3,06 (m, 1Н), 3,25-3,52 (m, 4Н), 3,82-4,05 (m, 3Н), 5,20 (m, 1Н), 5,53-5,67 (m, 2Н), 5,97 (m, 1Н), 7,01 (m, 2Н), 7,10 (m, 2Н), 7,51 (m, 2Н). Приклад 4 Бромід (3R)-1-(4-метилпент-3-еніл)-3-(2,2дитіен-2-ілпропіонілокси)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та а із проміжної сполуки 1-2. Вихід на кінцевій стадії становив 380мг, 100%. tпл. 130-131°C. MC: 430 [M-Br]+. 1 Н-ЯМР (300МГц, DMCO-d6) δ част./млн: 1,571,82 (m, 2Н), 1,62 (s, 3Н), 1,67 (s, 3Н), 1,91 (m, 2Н), 33 2,07 (s, 3Н), 2,22-2,42 (m, 3Н), 3,10 (m, 1Н), 3,17 (m, 2Н), 3,25-3,42 (m, 3Н), 3,48 (m, 1Н), 3,92 (m, 1Н), 4,98 (m, 1Н), 5,19 (m, 1Н), 7,02 (m, 2Н), 7,09 (m, 2Н), 7,50 (m, 2Н). Приклад 5 Трифторацетат (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-ізопропіл-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 21,6мг, 25,2%. + MC: 392 [M-CF3COO] . Приклад 6 Трифторацетат (3R)-1-циклопропілметил-3-(2гідрокси-2,2-дитієн-2-ілацетокси)-1-азонійбіцикло [2.2.2]октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 5,5мг, 6,2%. + MC: 404 [M-CF3COO] . Приклад 7 Трифторацетат (3R)-3-(2-гідрокси-2.2-дитієн-2ілацетокси)-1-ізобутил-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 25,0мг, 28,3%. + MC: 406 [M-CF3COO] . Приклад 8 Бромід (3R)-1-гептил-3-(2-гідрокси-2,2-дитієн2-ілацетокси)-1-азонійбіцикло [2.2.2] октану Вказану в заголовку сполуку одержували за способами с та а. Вихід на кінцевій стадії становив 490мг, 66,6%. tпл. 134°C. MC: 448 [M-Br]+. 1H-ЯМР (300МГц, CDCl3) δ част./млн: 0,86 (t, 3Н), 1,16-1,32 (m, 8Н), 1,60 (m, 2Н), 1,91 (m, 2Н), 2,05 (m, 2Н), 2,42 (m, 1Н), 3,32-3,48 (m, 2Н), 3,483,80 (m, 5Н), 4,24 (m, 1Н), 5,28 (m, 1Н), 5,98 (s, 1Н, ОН), 6,95 (m, 2Н), 7,17 (m, 1Н), 7,22-7,28 (m, 3Н). Приклад 9 Трифторацетат (3R)-1-циклогексилметил-3-(2гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 23,4мг, 24,6%. + MC: 446 [M-CF3COO] . Приклад 10 Трифторацетат (3R)-1-(3-циклогексилпропіл)3-(2-гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло [2.2.2] октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 12,6мг, 12,6%. + MC: 474 [M-CF3COO] . Приклад 11 Бромід (3R)-1-аліл-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та а. Вихід на кінцевій стадії становив 400мг, 70,0%. tпл. 176°C. MC: 390 [M-Br]+. 88634 34 1 H - Я М Р (300МГц, ДМСО-d6) δ част./млн: 1,77 (m, 2Н), 1,92 (m, 2Н), 2,31 (m, 1Н), 3,15 (m, 1Н), 3,20-3,52 (m, 4Н), 3,81-4,01 (m, 3Н), 5,24 (m, 1Н), 5,53-5,68 (m, 2Н), 5,96 (m, 1Н), 7,02 (m, 2Н), 7,16 (m, 2Н), 7,48 (s, 1Н, ОН), 7,53 (m, 2Н). Приклад 12 Бромід (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-(4-метилпент-3-еніл)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та а. Вихід на кінцевій стадії становив 260мг, 36,0%. tпл. 199°C. MC: 432 [M-Br]+. 1 H-ЯМР (300МГц, CDCl3) δ част./млн: 1,58 (s, 3Н), 1,64 (m, 3Н), 1,87 (m, 2Н), 2,03 (m, 2Н), 2,262,47 (m, 3Н), 3,22-3,45 (m, 2Н), 3,45-3,82 (m, 5Н), 4,23 (m, 1Н), 4,92 (m, 1Н), 5,27 (m, 1Н), 6,07 (s, 1Н, ОН), 6,93 (m, 2Н), 7,15 (m, 1Н), 7,24 (m, 3Н). Приклад 13 Трифторацетат (3R)-1-(3,7-диметилокта-(E)2,6-дієніл)-3-(2-гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 14,5мг, 14,2%. + MC: 486 [M-CF3COO] . Приклад 14 Трифторацетат (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-(2-гідроксіетил)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 16,6мг, 19,3%. + MC: 394 [M-CF3COO] . Приклад 15 Трифторацетат (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-(3-гідроксипропіл)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 16,0мг, 18,0%. + MC: 408 [M-CF3COO] . Приклад 16 Трифторацетат (3R)-1-(4-гідроксибутил)-3-(2гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 6,5мг, 7,1%. + MC: 422 [M-CF3COO] . Приклад 17 Бромід (3R)-1-(2-етоксіетил)-3-(2-гідрокси-2,2дитієн-2-ілацетокси)-1-азонійбіцикло [2.2.2] октану Вказану в заголовку сполуку одержували за способами с та а. Вихід на кінцевій стадії становив 220мг, 31,0%. tпл. 155°C. MC: 422 [M-Br]+. 1 Н-ЯМР (300МГц, CDCl3) δ част./млн: 1,15 (t, 3Н), 1,88 (m, 2Н), 2,03 (m, 2Н), 2,46 (m, 1H), 3,49 (q, 2Н), 3,54-3,96 (m, 8Н), 4,06 (m, 1Н), 4,31 (m, 1Н), 5,27 (m, 1Н), 5,73 (s, 1Н, ОН), 6,97 (m, 2Н), 7,20 (m, 1Н), 7,22-7,33 (m, 3Н). 35 Приклад 18 Гідрохлорид (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-[2-(2-гідроксіетокси)етил]-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та а. Вихід на кінцевій стадії становив 580мг, 14,0%. tпл. 156°C. MC: 438 [M-Cl]+. 1 Н-ЯМР (300МГц, ДМСО-dб) δ част./млн: 1,72 (m, 2Н), 1,92 (m, 2Н), 2,27 (m, 1Н), 3,10-3,70 (m, 11Н), 3,79 (m, 2Н), 3,96 (m, 1Н), 4,72 (m, 1Н), 5,21 (m, 1Н), 6,97 (m, 2Н), 7,15 (m, 2Н), 7,51 (m, 3Н). Приклад 19 Бромід (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-[2-(2-метоксіетокси)етил]-1азонійбіцикло [2.2.2] октану Вказану в заголовку сполуку одержували за способами с та а. Вихід на кінцевій стадії становив 260мг, 35,0%. MC: 452 [M-Br]+. 1 H-ЯMP (300МГц, CDCl3) δ част./млн: 1,87 (m, 2Н), 2,04 (m, 2Н), 2,44 (m, 1Н), 3,32 (s, 3Н), 3,48 (m, 2Н), 3,54-3,96 (m, 10Н), 3,98-4,08 (m, 1Н), 4,30 (m, 1Н), 5,26 (m, 1Н), 6,0 (ушир.s, 1Н, ОН), 6,97 (m, 2Н), 7,20 (m, 1Н), 7,23-7,32 (m, 3Н). Приклад 20 Бромід (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-оксиранілметил-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та а. Вихід на кінцевій стадії становив 240мг, 35,0%. + MC: 406 [M-Br] . Приклад 21 Трифторацетат (3R)-1-(2-[1,3]-діоксолан-2ілетил)-3-(2-гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 15,7мг, 16,4%. + MC: 450 [M-CF3COO] . Приклад 22 Трифторацетат (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-{2-[2-(2-гідроксіетокси)етокси]етил}1-азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 7,9мг, 7,8%. + MC: 482 [M-CF3COO] . Приклад 23 Трифторацетат (3R)-1-(3-[1,3]-діоксолан-2ілпропіл)-3-(2-гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 17,1мг, 17,4%. + MC: 464 [M-CF3COO] . Приклад 24 Трифторацетат (3R)-1-(3етоксикарбонілпропіл)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-азонійбіцикло [2.2.2]октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 15,1мг, 15,4%. 88634 36 MC: 464 [M-CF3COO]+. Приклад 25 Трифторацетат (3R)-1-(4етоксикарбонілбутил)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-азонійбіцикло [2.2.2] октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 15,0мг, 14,9%. + MC: 478 [M-CF3COO] . Приклад 26 Трифторацетат (3R)-1-(4-ацетоксибутил)-3-(2гідрокси-2.2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 10,7мг, 10,9%. MC: 464 [M-CF3COO]+. Приклад 27 Трифторацетат (3R)-1-(3-ціанопропіл)-3-(2гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 14,0мг, 15,5%. + MC: 417 [M-CF3COO] . Приклад 28 Трифторацетат (3R)-1-(4-ціанобутил)-3-(2гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 16,2мг, 17,5%. + MC: 431 [M-CF3COO] . Приклад 29 Трифторацетат (3R)-1-(6-ціаногексил)-3-(2гідрокси-2,2-дитієн-2-ілацетокси)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 19,1мг, 19,6%. + MC: 459 [M-CF3COO] . Приклад 30 Трифторацетат (3R)-3-(2-гідрокси-2,2-дитієн-2ілацетокси)-1-(4,4,4-трифторбутил)-1азонійбіцикло [2.2.2] октану Вказану в заголовку сполуку одержували за способами с та b. Вихід на кінцевій стадії становив 18,4мг, 18,8%. + MC: 460 [M-CF3COO] . Приклад 31 Бромід (3R)-1-аліл-3-(2-гідрокси-2-феніл-2тієн-2-ілацетокси)-1-азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували у вигляді суміші діастереомерів за способами f та а. Вихід на кінцевій стадії становив 350мг, 50,0%. tпл. 170°C. MC: 384 [M-Br]+. 1 Н-ЯМР (300МГц, ДМСО-d6) δ част./млн: (суміш діастереомерів) 1,46-1,79 (m, 2Н), 1,81-2,02 (m, 2Н), 2,28 (m, 1Н), 3,07 (m, 1Н), 3,17-3,46 (m, 4Н), 3,80-4,0 (m, 3Н), 5,23 (m, 1Н), 5,53-5,67 (m, 2Н), 5,96 (m, 1Н), 7,03 (m, 1Н), 7,12 (m, 1Н), 7,20 (s, 1Н, ОН), 7,29-7,42 (m, 3Н), 7,42-7,49 (m, 2Н), 7,53 (m, 1Н). 37 Приклад 32 Бромід (3R)-1-аліл-3-(2-фур-2-ил-2-гідрокси-2фенілацетокси)-1-азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували у вигляді суміші діастереомерів за способами с та а. Вихід на кінцевій стадії становив 120мг, 88,8%. MC: 368 [M-Br]+. 1 H-ЯMP (300МГц, ДМСО-d6) δ част./млн: (суміш діастереомерів) 1,45-1,80 (m, 2Н), 1,80-2,03 (m, 2Н), 2,26 (m, 1Н), 2,95-3,24 (m, 2Н), 3,24-3,47 (m, 3Н), 3,75-3,98 (m, 3Н), 5,20 (m, 1Н), 5,52-5,67 (m, 2Н), 5,96 (m, 1Н), 6,28 (dd, 1Н), 6,46 (m, 1Н), 6,95 (d, 1Н, ОН), 7,31-7,45 (m, 3Н), 7,48 (m, 2Н), 7,68 (m, 1Н). Приклад 33 Бромід (3R)-1-аліл-3 -(2-фур-2-ил-2-гідрокси-2тієн-2-ілацетокси)-1-азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували у вигляді суміші діастереомерів за способами с та а. Вихід на кінцевій стадії становив 170мг, 62,9%. MC: 374 [M-Br]+. 1 H-ЯMP (300МГц, ДМСО-d6) δ част./млн: (суміш діастереомерів) 1,58-1,83 (m, 2Н), 1,83-2,06 (m, 2Н), 2,28 (m, 1Н), 3,06 (m, 1Н), 3,18 (m, 1Н), 3,25-3,54 (m, 3Н), 3,78-4,02 (m, 3Н), 5,22 (m, 1Н), 5,52-5,68 (m, 2Н), 5,97 (m, 1Н), 6,33 (dd, 1Н), 6,46 (m, 1Н), 7,04 (m, 1Н), 7,15 (m, 1Н), 7,29 (d, 1Н), 7,55 (m, 1Н), 7,69 (m, 1 Н). Приклад 34 Бромід (3R)-1-аліл-3-(9-метил-9Н-флуорен-9карбонілокси)-1-азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та а. Вихід на кінцевій стадії становив 180мг, 88,2%. tпл. 75,2-76,8°C. MC: 374 [M-Br]+. 1 H-ЯМР (300МГц, ДМСО-d6) δ част./млн: 1,54 (m, 1Н), 1,69 (m, 1Н), 1,76 (s, 3Н), 1,87 (m, 2H), 2,11 (m, 1Н), 3,00 (m, 1Н), 3,16-3,47 (m, 4Н), 3,79 (m, 1Н), 3,91 (m, 2Н), 4,99 (m, 1Н), 5,52-5,66 (m, 2Н), 5,93 (m, 1Н), 7,30-7,50 (m, 4Н), 7,64 (d, 1Н), 7,72 (d, 1Н), 7,90 (d, 2Н). Приклад 35 Бромід (3R)-1-аліл-3-(9-гідрокси-9Н-флуорен9-карбонілокси)-1-азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та а із проміжної сполуки 1-3. Вихід на кінцевій стадії становив 550мг, 80,3%. tпл. 260°C. MC: 376 [M-Br]+. 1 H-ЯMP (300МГц, ДМСО-d6) δ част./млн: 1,40 (m, 1Н), 1,64 (m, 1Н), 1,85 (m, 2Н), 2,08 (m, 1Н), 2,77 (m, 1Н), 3,03 (m, 1Н), 3,17-3,41 (m, 3Н), 3,703,94 (m, 3Н), 5,03 (m, 1Н), 5,50-5,68 (m, 2Н), 5,90 (m, 1Н), 6,85 (s, 1Н, ОН), 7,35 (m, 2Н), 7,46 (m, 2Н), 7,60 (m, 2Н), 7,83 (d, 2Н). Приклад 36 Бромід (3R)-3-(9-гідрокси-9Н-флуорен-9карбонілокси)-1-(4-метилпент-3-еніл)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та а із проміжної сполуки 1-3. Вихід на кінцевій стадії становив 490мг, 65,5%. tпл. 192,4-193,1°C. MC: 418 [M-Br]+. 88634 38 1 H-ЯМР (300МГц, ДМСО-d6) δ част./млн: 1,40 (m, 1Н), 1,55-1,72 (m, 1Н), 1,61 (s, 3Н), 1,66 (s, 3Н), 1,84 (m, 2Н), 2,04 (m, 1Н), 2,26 (m, 2Н), 2,76 (m, 1Н), 2,98-3,16 (m, 3Н), 3,18-3,45 (m, 3Н), 3,79 (m, 1Н), 4,95 (m, 1Н), 5,01 (m, 1Н), 6,82 (s, 1Н, ОН), 7,33 (m, 2Н), 7,44 (m, 2Н), 7,59 (m, 2Н), 7,82 (d, 2Н). Приклад 37 Бромід (3R)-1-гептил-3-(9-гідрокси-9Нфлуорен-9-карбонілокси)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та а із проміжної сполуки 1-3. Вихід на кінцевій стадії становив 330мг, 85,5%. тпл. 214,9-216,6°C. MC: 434 [M-Br]+. 1 Н-ЯМР (300МГц, ДМСО-d6) δ част./млн: 0,88 (t, 3Н), 1,12-1.70 (m, 12Н), 1,70-1,93 (m, 2Н), 2,04 (m, 1Н), 2,78 (m, 1Н), 2,96-3,18 (m, 3Н), 3,18-3,48 (m, 3Н), 3,77 (m, 1Н), 5,01 (m, 1Н), 6,84 (s, 1Н, ОН), 7,34 (m, 2Н), 7,45 (m, 2Н), 7,61 (m, 2Н), 7,84 (d, 2Н). Приклад 38 Бромід (3R)-3-(9-гідрокси-9Н-флуорен-9карбонілокси)-1-оксиранілметил-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та а із проміжної сполуки 1-3. Вихід на кінцевій стадії становив 270мг, 38,0%. MC: 392 + [M-Br] . Приклад 39 Бромід (3R)-3-(9-гідрокси-9Н-флуорен-9карбонілокси)-1-[2-(2-метоксіетокси)етил]-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та а із проміжної сполуки 1-3. Вихід на кінцевій стадії становив 610мг, 78,2%. tпл. 194°C. + MC: 438 [M-Br] . 1 Н-ЯMP (300МГц, ДМСО-d6) δ част./млн: 1,44 (m, 1Н), 1,64 (m, 1Н), 1,85 (m, 2Н), 2,09 (m, 1Н), 2,93 (m, 1Н), 3,18-3,28 (m, 1Н), 3,26 (s, 3Н), 3,303,60 (m, 9Н), 3,73 (m, 2Н), 3,88 (m, 1Н), 5,00 (m, 1Н), 6,83 (s, 1Н, ОН), 7,35 (m, 2Н), 7,45 (m, 2Н), 7,61 (m, 2Н), 7,83 (d, 2Н). Приклад 40 Бромід (3R)-1-(2-[1,3]-діоксолан-2-ілетил)-3-(9гідрокси-9Н-флуорен-9-карбонілокси)-1азонійбіцикло [2.2.2] октану Вказану в заголовку сполуку одержували за способами с та а із проміжної сполуки 1-3. Вихід на кінцевій стадії становив 660мг, 85,7%. tпл. 62°C. MC: 436 [M-Br]+. 1 H-ЯMP (300МГц, ДМСО-d6) δ част./млн: 1,43 (m, 1Н), 1,64 (m, 1Н), 1,71-2,15 (m, 5Н), 2,86 (m, 1Н), 3,0-3,64 (m, 8Н), 3,74-3,97 (m, 3Н), 4,89 (m, 1Н), 5,00 (s, 1Н), 7,34 (m, 2Н), 7,45 (m, 2Н), 7,63 (m, 2Н), 7,82 (d, 2Н). Приклад 41 Бромід (3R)-1-аліл-3-(9Н-ксантен-9карбонілокси)-1-азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами d і а. Вихід на кінцевій стадії становив 170мг, 51,5%. tпл. 57°C. MC: 376 [M-Br]+. 39 1 Н-ЯMP (300МГц, ДМСО-d6) δ част./млн: 1,632,00 (m, 4Н), 2,17 (m, 1Н), 3,06-3,56 (m, 5Н), 3,77 (m, 1Н), 3,92 (m, 2Н), 5,03 (m, 1Н), 5,30 (s, 1Н), 5,50-5,70 (m, 2Н), 5,94 (m, 1Н), 7,20 (m, 4Н), 7,38 (m, 2Н), 7,50 (m, 2Н). Приклад 42 Бромід (3R)-1-(4-метилпент-3-еніл)-3-(9Нксантен-9-карбонілокси)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами d і а. Вихід на кінцевій стадії становив 270мг, 72,9%. tпл. 225°C. MC: 418 [M-Br]+. 1 H-ЯMP (300МГц, ДМСО-d6) δ част./млн: 1,602,0 (m, 4Н), 1,64 (s, 3Н), 1,69 (s, 3Н), 2,16 (m, 1Н), 2,32 (m, 2Н), 3,10-3,46 (m, 6Н), 3,53 (m, 1Н), 3,85 (m, 1Н), 4,93-5,08 (m, 2Н), 5,32 (s, 1Н), 7,19 (m, 4Н), 7,38 (m, 2Н), 7,52 (m, 2Н). Приклад 43 Бромід (3R)-1-аліл-3-(9-метил-9Н-ксантен-9карбонілокси)-1-азонійбіцикло [2.2.2] октану Вказану в заголовку сполуку одержували за способами с та а. Вихід на кінцевій стадії становив 1,04г, 73,8%. tпл. 64,3-67,8°C. MC: 390 [M-Br]+. 1 H-ЯMP (300МГц, ДМСO-d6) δ част./млн: 1,35 (m, 1Н), 1,65 (m, 1Н), 1,73-1,91 (m, 2Н), 1,89 (s, 3Н), 2,11 (m, 1Н), 2,75 (m, 1Н), 3,00 (m, 1Н), 3,15-3,45 (m, 3Н), 3,70-3,90 (m, 3Н), 5,03 (m, 1Н), 5,50-5,65 (m, 2Н), 5,86 (m, 1Н), 7,12-7,19 (m, 4Н), 7,35 (m, 2Н), 7,42 (m, 2Н). Приклад 44 Бромід (3R)-1-аліл-3-(9-гідрокси-9Н-ксантен-9карбонілокси)-1-азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та а. Вихід на кінцевій стадії становив 270мг, 67,5%. tпл. 232°C. MC: 392 [M-Br]+. 1 H-ЯMP (300МГц, ДМСО-d6) δ част./млн: 1,29 (m, 1Н), 1,62 (m, 1Н), 1,70-1,94 (m, 2Н), 2,06 (m, 1Н), 2,62 (m, 1Н), 2,79 (m, 1Н), 3,13-3,42 (m, 3Н), 3,64-3,87 (m, 3Н), 5,02 (m, 1Н), 5,47-5,65 (m, 2Н), 5,81 (m, 1Н), 7,18 (s, 1Н, ОН), 7,25 (m, 4Н), 7,44 (m, 2Н), 7,65 (m, 2Н). Приклад 45 Бромід (3R)-1-(3-гідроксипропіл)-3-(9-гідрокси9Н-ксантен-9-карбонілокси)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами с та а. Вихід на кінцевій стадії становив 315мг, 90,5%. tпл. 87,6-89,1°C. MC: 410 [M-Br]+. 1 Н-ЯМР (300МГц, ДМСО-d6) δ част./млн: 1,28 (m, 1Н), 1,50-1,95 (m, 5Н), 2,05 (m, 1Н), 2,63 (m, 1Н), 2,83 (m, 1Н), 3,10-3,50 (m, 7Н), 3,73 (m, 1Н), 4,76 (t, 1Н, ОН), 5,0 (m, 1Н), 7,18 (s, 1Н, ОН), 7,187,30 (m, 4Н), 7,40-7,50 (m, 2Н), 7,60-7,70 (m, 2Н). Приклад 46 Бромід (3R)-1-аліл-3-(10,11-дигідро-5Ндибензо[а,d]циклогептен-5-карбонілокси)-1азонійбіцикло[2.2.2]октану 88634 40 Вказану в заголовку сполуку одержували за способами d і а із проміжної сполуки 1-4. Вихід на кінцевій стадії становив 260мг, 95,6%. tпл. 219,5-220,3°C. MC: 388 [M-Br]+. 1 Н-ЯМР (300МГц, CDCl3) δ част./млн: 1,52 (m, 1Н), 1,71 (m, 1Н), 1,93 (m, 2Н), 2,20 (m, 1Н), 2,792,94 (m, 2Н), 3,02 (m, 1Н), 3,11-3,31 (m, 2Н), 3,403,52 (m, 1Н), 3,52-3,75 (m, 3Н), 4,06-4,39 (m, 3Н), 5,10 (m, 1Н), 5,21 (s, 1Н), 5,57-5,87 (m, 3Н), 7,16 (m, 6Н), 7,39 (m, 2Н). Приклад 47 Бромід (3R)-1-(4-метилпент-3-еніл)-3-(10,11дигідро-5Н-дибензо[а,d]циклогептен-5карбонілокси)-1-азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами d і а із проміжної сполуки 1-4. Вихід на кінцевій стадії становив 290мг, 97,9%. tпл. 216°C. MC: 430 [M-Br]+. 1 H-ЯMP (300МГц, CDCl3) δ част./млн: 1,53 (m, 1Н), 1,62 (s, 3Н), 1,67 (s, 3Н), 1,81 (m, 1Н), 1,98 (m, 2Н), 2,18-2,35 (m, 3Н), 2,75-2,98 (m, 3Н), 3,11-3,46 (m, 5Н), 3,54-3,76 (m, 3Н), 4,20 (m, 1Н), 4,95 (m, 1Н), 5,14 (s, 1Н), 5,10-5,20 (m, 1Н), 7,19 (m, 6Н), 7,36 (m, 2Н). Приклад 48 Бромід (3R)-1-аліл-3-[(2*)-2-гідрокси-2,3дифенілпропіонілокси]-1азонійбіцикло[2.2.2]октану (діастереомер 1) Вказану в заголовку сполуку одержували за способами f та а із проміжної сполуки І-6а. Вихід на кінцевій стадії становив 250мг, 75,7%. tпл. 180°C. MC: 392 [M-Br]+. 1 H-ЯMP (300МГц, ДМСО-d6) δ част./млн: 1,72 (m, 2Н), 1,92 (m, 2Н), 2,21 (m, 1Н), 3,02 (m, 1Н), 3,11 (m, 1Н), 3,18-3,52 (m, 5Н), 3,74 (m, 1Н), 3,84 (m, 2Н), 5,04 (m, 1Н), 5,49-5,64 (m, 2Н), 5,90 (m, 1Н), 6,15 (s, 1Н, ОН), 7,14 (m, 5Н), 7,23-7,40 (m, 3Н), 7,53 (m, 2Н). (*) - конфігурація не визначена. Приклад 49 Бромід (3R)-3-[(2*)-2-гідрокси-2,3дифенілпропіонілокси]-1-(4-метилпент-3-еніл)-1азонійбіцикло[2.2.2]октану (діастереомер 1) Вказану в заголовку сполуку одержували за способами f та а із проміжної сполуки І-6а. Вихід на кінцевій стадії становив 280мг, 77,7%. tпл. 224°C. MC: 434 [M-Br]+. 1 H-ЯМР (300МГц, ДМСО-d6) δ част./млн: 1,61 (s, 3Н), 1,67 (s, 3H), 1,63-1,75 (m, 2Н), 1,75-2,00 (m, 2Н), 2,21 (m, 1Н), 2,28 (m, 2Н), 2,99-3,20 (m, 4Н), 3,20-3,50 (m, 5Н), 3,77 (m, 1Н), 4,97 (m, 1Н), 5,04 (m, 1Н), 6,14 (s, 1Н, ОН), 7,14 (m, 5Н), 7,23-7,39 (m, 3Н), 7,54 (m, 2Н). (*) - конфігурація не визначена. Приклад 50 Бромід (3R)-1-аліл-3-(2-гідрокси-2-тієн-2ілпент-4-еноїлокси)-1-азонійбіцикло [2.2.2] октану Вказану в заголовку сполуку одержували у вигляді суміші діастереомерів за способами с та а. Вихід на кінцевій стадії становив 210мг, 61,8%. tпл. 62,6-63,9°C. 41 MC: 348 [M-Br]+. 1 H-ЯMP (300МГц, ДМСО-d6) δ част./млн: (суміш діастереомерів) 1,68-2,05 (m, 4Н), 2,26 (m, 1Н), 2,76 (m, 1Н), 2,95 (m, 1Н), 3,08-3,53 (m, 5Н), 3,744,00 (m, 3Н), 5,02-5,21 (m, 3Н), 5,51-5,67 (m, 2Н), 5,78 (m, 1Н), 5,97 (m, 1Н), 6,49 (d, 1Н, ОН), 7,01 (m, 1Н), 7,15 (m, 1Н), 7,48 (m, 1Н). Приклад 51 Бромід (3R)-1-(4-метилпент-3-еніл)-3-(2гідрокси-2-тієн-2-ілпент-4-еноїлокси)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували у вигляді суміші діастереомерів за способами с та а. Вихід на кінцевій стадії становив 290мг, 78,4%. tпл. 56,2-57,9°C. MC: 390 [M-Br]+. 1 H-ЯMP (300МГц, ДМСО-d6) δ част./млн: (суміш діастереомерів) 1,52-2,06 (m, 4Н), 1,63 (d, 3Н), 1,69 (s, 3Н), 2,16-2,43 (m, 3Н), 2,78 (dd, 1Н), 2,96 (m, 1Н), 3,07-3,59 (m, 7Н), 3,88 (m, 1Н), 4,92-5,23 (m, 4Н), 5,78 (m, 1Н), 6,48 (d, 1Н, ОН), 7,01 (m, 1Н), 7,15 (m, 1Н), 7,46 (m, 1Н). Приклад 52 Бромід (3R)-1-аліл-3-[(2S)-2-циклопентил-2гідрокси-2-тієн-2-ілацетокси]-1-азонійбіцикло [2.2.2] октану Вказану в заголовку сполуку одержували за способами f та а. Вихід на кінцевій стадії становив 180мг, 78,3%. tпл. 68,2-70,1°C. + MC: 376 [M-Br] . 1 Н-ЯМР (300МГц, ДМСО-d6) δ част./млн: 1,261,66 (m, 8Н), 1,78-2,08 (m, 4Н), 2,30 (m, 1Н), 2,81 (m, 1Н), 3,14 (m, 1Н), 3,20-3,58 (m, 4Н), 3,78-4,03 (m, 3Н), 5,15 (m, 1Н), 5,52-5,68 (m, 2Н), 5,97 (m, 1Н), 6,18 (s, 1Н, ОН), 7,01 (m, 1Н), 7,16 (d, 1Н), 7,45 (d, 1Н). Приклад 53 Бромід (3R)-1-(4-метилпент-3-еніл)-3-[(2S)-2циклопентил-2-гідрокси-2-тієн-2-ілацетокси]-1азонійбіцикло [2.2.2]октану Вказану в заголовку сполуку одержували за способами f та а. Вихід на кінцевій стадії становив 290мг, 71,7%. tпл. 84°C. + MC: 418 [M-Br] . 1 Н-ЯМР (300МГц, ДМСO-d6) δ част./млн: 1,191,76 (m, 8Н), 1,63 (s, 3Н), 1,68 (s, 3Н), 1,77-2,05 (m, 4Н), 2,20-2,42 (m, 3Н), 2,81 (m, 1Н), 3,11-3,24 (m, 3Н), 3,24-3,61 (m, 4Н), 3,89 (m, 1Н), 5,01 (m, 1Н), 5,14 (m, 1Н), 6,19 (s, 1Н, ОН), 7,00 (m, 1Н), 7,16 (d, 1Н), 7,44 (d, 1Н). Приклад 54 Бромід (3R)-1-аліл-3-[(2R)-2-циклопентил-2гідрокси-2-тієн-2-ілацетокси]-1-азонійбіцикло [2.2.2] октану Вказану в заголовку сполуку одержували за способами с та а. Вихід на кінцевій стадії становив 230мг, 85,2%. tпл. 65,3-66,0°C. MC: 376 [M-Br]+. 1 Н-ЯМР (300МГц, ДМСO-d6) δ част./млн: (суміш діастереомерів (3R,2R):(3R,2S), 72:28) 1,301,66 (m, 8Н), 1,67-2,05 (m, 4Н), 2,23 і 2,30 (m, 1Н), 2,83 (m, 1Н), 3,06-3,55 (m, 5Н), 3,74-4,03 (m, 3Н), 88634 42 5,14 (m, 1Н), 5,53-5,68 (m, 2Н), 5,99 (m, 1Н), 6,18 і 6,19 (s, 1Н, ОН), 7,00 (m, 1Н), 7,16 (m, 1Н), 7,44 (m, 1Н). Приклад 55 Бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси2-тієн-2-ілацетокси]-1-(2-гідроксиетил)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами f та а. Неочищену суміш очищали хроматографією із оберненою фазою (елюент: вода). Вихід на кінцевій стадії становив 148мг, 66%. + MC: 380 [M-Br] . 1 H-ЯMP (300МГц, ДМСО-d6) δ част./млн: 1,251,99 (m, 12Н), 2,29 (m, 1Н), 2,75-2,85 (m, 1Н), 3,303,60 (m, 7Н), 5,13 (m, 1Н), 5,29-5,32 (t, 1Н), 6,21 (s, 1Н), 6,98-7,01 (dd, 1Н), 7,13-7,15 (dd, 1Н), 7,42-7,44 (dd, 1Н). Приклад 56 Бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси2-тієн-2-ілацетокси]-1-(3-гідроксипропіл)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами f та а. Неочищену суміш очищали хроматографією із оберненою фазою (елюент: вода). Вихід на кінцевій стадії становив 145мг, 53%. + MC: 394 [M-Br] . Приклад 57 Бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси2-тієн-2-ілацетокси]-1-(4-гідроксибутил)-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами f та а. Неочищену суміш очищали хроматографією із оберненою фазою (елюент: вода). Вихід на кінцевій стадії становив 40мг, 20%. MC: 408 [M-Br]+. 1 Н-ЯМР (300МГц, ДМСО-d6) δ част./млн: 1,251,93 (m, 18Н), 2,29 (m, 1Н), 2,81 (m, 1Н), 3,08-3,48 (m, 5Н), 3,75-3,90 (m, 1Н), 4,61-4,64 (tm, 1Н), 5,105,20 (m, 1Н), 6,23 (s, 1Н), 6,99-7,02 (t, 1Н), 7,147,16 (m, 1Н), 7,43-7,45 (d, 1Н). Приклад 58 Бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси2-тієн-2-ілацетокси]-1-[2-(2-гідроксіетокси)етил]-1азонійбіцикло[2.2.2]октану Вказану в заголовку сполуку одержували за способами f та а. Неочищену суміш очищали хроматографією із оберненою фазою (елюент: вода). Вихід на кінцевій стадії становив 110мг, 37%. MC: 424 [M-Br]+. 1 Н-ЯМР (300МГц, ДМСО-d6) δ част./млн: 1,101,53 (m, 14Н), 1,82-2,04 (m, 3Н), 2,17-2,37 (m, 1Н), 2,76-2,87 (m, 1Н), 3,23-3,51 (m, 5Н), 3,79-3,95 (m, 2Н), 4,67-4,71 (t, 1Н), 5,09-5,19 (m, 1Н), 6,20 (s, 1Н), 6,99-7,01 (dd, 1Н), 7,14-7,16 (m, 1Н), 7,42-7,44 (dd, 1Н). Приклад 59 Бромід (3R)-3-[(2S)-2-циклопентил-2-гідрокси2-тієн-2-ілацетокси]-1-(6-гідроксигексил)-1азонійбіцикло [2.2.2] октану Вказану в заголовку сполуку одержували за способами f та а. Неочищену суміш очищали хроматографією із оберненою фазою (елюент: вода). Вихід на кінцевій стадії становив 90мг, 35%. + MC: 436 [M-Br] . 43 88634 1 H-ЯМР (300МГц, DMCO-d6) δ част./млн: 1,202,00 (m, 20Н), 2,28 (m, 1Н), 2,81 (m, 1Н), 3,10-3,50 (m, 9Н), 3,81 (m, 1Н), 4,38-4,41 (t, 1Н), 5,12 (m, 1Н), 6,20 (s, 1Н), 6,69-7,02 (t, 1Н), 7,14-7,15 (m, 1Н), 7,43-7,46 (m, 1Н). Наведені нижче приклади призначені для ілюстрації фармацевтичних композицій за даним винаходом й способів їх одержання. Приклад 60 Одержання фармацевтичної композиції: таблетки Композиція: Сполука за даним винаходом 5,0мг Лактоза 113,6мг Мікрокристалічна целюлоза 28,4мг 1,5мг Ангідрид кремнієвої кислоти Стеарат магнію 1,5мг 15г Сполуки за даним винаходом змішували з 340,8г лактози й 85,2г мікрокристалічної целюлози з використанням змішувача. Суміш формували під тиском з використанням роликового ущільнювача, при цьому одержували пластівчастий спресований матеріал. Пластівчастий компактний матеріал подрібнювали за допомогою молоткового млина й подрібнений матеріал просіювали через сито з розміром комірок 20 меш. У просіяний матеріал додавали 4,5г ангідриду кремнієвої кислоти й 4,5г стеарату магнію, потім перемішували. З отриманої суміші пресували таблетки на машині для таблетування, обладнаною системою матриця/пуансон діаметром 7,5мм, при цьому одержували 3000 таблеток масою 150мг кожна. Приклад 61 Одержання фармацевтичної композиції: таблетки з покриттям Композиція: 5,0мг Сполука за даним винаходом Лактоза 95,2мг Кукурудзяний крохмаль 40,8мг Полівінілпіролідон ДO25 7,5мг Стеарат магнію 1,5мг Гідроксипропілцелюлоза 2,3мг Поліетиленгліколь 6000 0,4мг Діоксид титану 1,1мг Очищений тальк 0,7мг 15г Сполуки за даним винаходом змішували з 285,6г лактози й 122,4г кукурудзяні крохмалі на пристрої для гранулювання із псевдозрідженим шаром. В окремій посудині 22,5г полівінілпіролідону розчиняли в 127,5г води, при цьому одержували сполучний розчин. Сполучний розчин розпилювали у вказаній вище суміші на пристрої для гранулювання із псевдозрідженим шаром, при цьому одержували гранули, до яких додавали 4,5г стеарату магнію й змішували. З отриманої суміші одержували таблетки на машині для таблетування, обладнаною двоввігнутою системою матри Комп’ютерна верстка А. Крулевський 44 ця/пуансон діаметром 6,5мм, при цьому одержували 3000 таблеток масою 150мг кожна. Розчин для одержання покриття одержували в окремій посудині при суспендуванні 6,9г гідроксипропілметилцелюлози 2910, 1,2г поліетиленгліколю 6000, 3,3г діоксиду титану й 2,1г очищеного тальку в 72,6г води. На машині для нанесення покриттів High Coated 3000 отриманих таблеток покривали розчином для одержання покриття, при цьому одержували таблетки із плівковим покриттям масою 154,4мг кожна. Приклад 62 Одержання фармацевтичної композиції: рідкий препарат для інгаляції Композиція: Сполука за даним винаходом 400мкг Фізіологічний сольовий розчин 1мл 40мг Сполуки за даним винаходом розчиняли в 90мл фізіологічного сольового розчину й об'єм розчину доводили до 100мл вказаним фізіологічним розчином, розливали по 1мл в ампули об'ємом 1мл і потім стерилізували при 115°C. протягом 30хв, при цьому одержували рідкий препарат для інгаляції. Приклад 63 Одержання фармацевтичної композиції: порошок для інгаляції Композиція: Сполука за даним винаходом 200мкг Лактоза 4000мкг 20г Сполуки за даним винаходом перемішували з 400г лактози до гомогенного стану й порції по 200мг упаковували в порошкоподібні інгалятори, що видають при використанні порошкоподібну дозу для інгаляції. Приклад 64 Одержання фармацевтичної композиції: аерозоль для інгаляції Композиція: Сполука за даним винаходом 200мкг Безводний (абсолютований) етиловий спирт USP 8400мкг 1,1,1,2-тетрафторетан (HFC134A) 46810мкг Концентрат активного інгредієнта одержували при розчиненні 0,0480г сполуки за даним винаходом в 2,0160г етилового спирту. Концентрат поміщали у відповідний пристрій для наповнення. Концентратом заповнювали контейнери для аерозолів, верхню частину контейнера продували азотом або парами HFC-134А (інгредієнти для продування не повинні містити більше 1 част./млн кисню) і закривали клапаном. Закритий контейнер заповнювали пропелентом HFC-134А (11,2344г) під тиском. Підписне Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюQuaternized quinuclidine esters
Автори англійськоюFernandez Forner Maria Dolors, Prat Quinones Maria, Buil Albero Maria Antonia
Назва патенту російськоюСложные эфиры кватернизированного хинуклидина
Автори російськоюФернандес Форнер Мария Долорс, Прат Киньонес Мария, Буил Альберо Мария Антония
МПК / Мітки
МПК: A61P 13/00, C07D 453/00, A61P 11/00, A61K 31/439
Мітки: кватернізованого, хінуклідину, складні, ефіри
Код посилання
<a href="https://ua.patents.su/22-88634-skladni-efiri-kvaternizovanogo-khinuklidinu.html" target="_blank" rel="follow" title="База патентів України">Складні ефіри кватернізованого хінуклідину</a>
Попередній патент: Структурована композиція на основі ліпідів, спосіб її виготовлення та спосіб зниження атерогенного ризику людини
Наступний патент: Суспензійний концентрат на масляній основі та спосіб його одержання
Випадковий патент: Піримідини, які інгібують cdk-кінази, спосіб їх одержання і їх застосування як лікарських засобів












