Кристалічні гідрати 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2н)-піримідиніл]-4-фтор-n-[[метил-(1-метилетил)аміно]сульфоніл]бензаміду, способи одержання гідрату, гербіцид, що містить гідрат,
Номер патенту: 99114
Опубліковано: 25.07.2012
Автори: Міхель Альфред, Зайтц Вернер, Кайл Міхаель, Ерк Петер, Шмідт Томас, Кокс Герхард, Цагар Сірілл, Веверс Ян Хендрік, Закселль Хайді Емілія, Гебхардт Йоахім, Майєр Гуідо, Зіверніх Бернд, Хампрехт Герхард, Льор Сандра, Райнхард Роберт, Вольф Бернд
Формула / Реферат
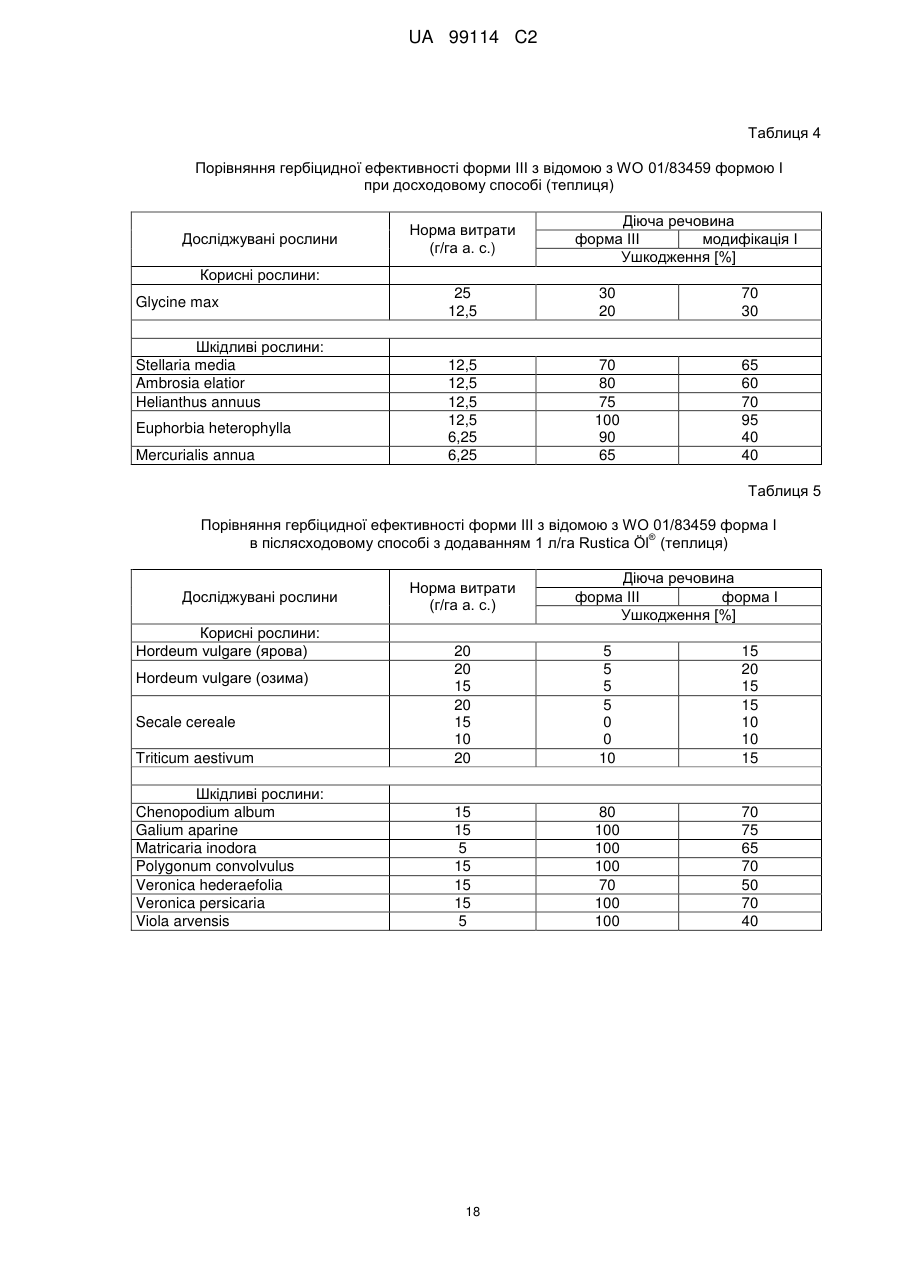
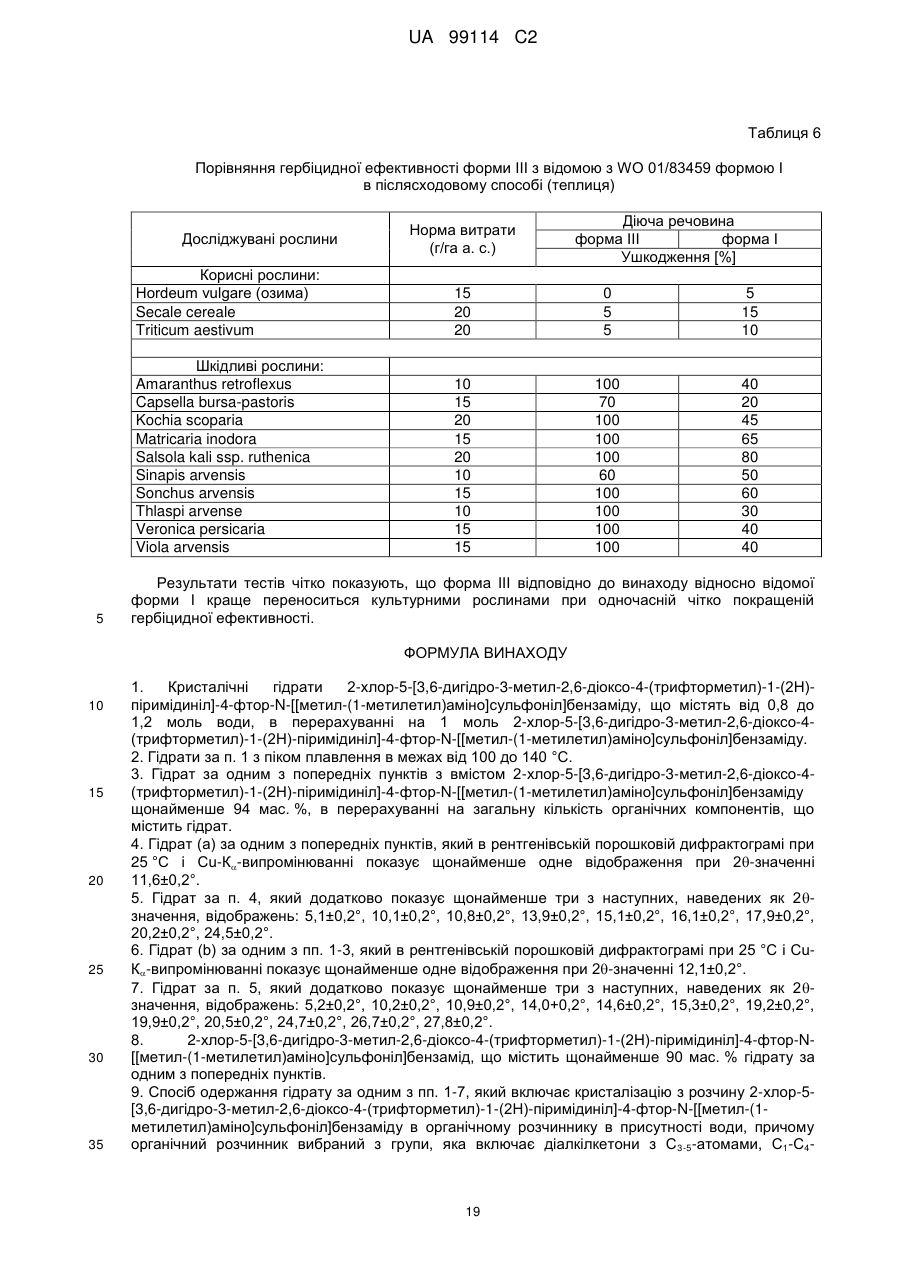
1. Кристалічні гідрати 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2Н)-піримідиніл]-4-фтор-N-[[метил-(1-метилетил)аміно]сульфоніл]бензаміду, що містять від 0,8 до 1,2 моль води, в перерахуванні на 1 моль 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2Н)-піримідиніл]-4-фтор-N-[[метил-(1-метилетил)аміно]сульфоніл]бензаміду.
2. Гідрати за п. 1 з піком плавлення в межах від 100 до 140 °C.
3. Гідрат за одним з попередніх пунктів з вмістом 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2Н)-піримідиніл]-4-фтор-N-[[метил-(1-метилетил)аміно]сульфоніл]бензаміду щонайменше 94 мас. %, в перерахуванні на загальну кількість органічних компонентів, що містить гідрат.
4. Гідрат (а) за одним з попередніх пунктів, який в рентгенівській порошковій дифрактограмі при 25 °C і Сu-Кa-випромінюванні показує щонайменше одне відображення при 2q-значенні 11,6±0,2°.
5. Гідрат за п. 4, який додатково показує щонайменше три з наступних, наведених як 2q-значення, відображень: 5,1±0,2°, 10,1±0,2°, 10,8±0,2°, 13,9±0,2°, 15,1±0,2°, 16,1±0,2°, 17,9±0,2°, 20,2±0,2°, 24,5±0,2°.
6. Гідрат (b) за одним з пп. 1-3, який в рентгенівській порошковій дифрактограмі при 25 °C і Сu-Кa-випромінюванні показує щонайменше одне відображення при 2q-значенні 12,1±0,2°.
7. Гідрат за п. 5, який додатково показує щонайменше три з наступних, наведених як 2q-значення, відображень: 5,2±0,2°, 10,2±0,2°, 10,9±0,2°, 14,0+0,2°, 14,6±0,2°, 15,3±0,2°, 19,2±0,2°, 19,9±0,2°, 20,5±0,2°, 24,7±0,2°, 26,7±0,2°, 27,8±0,2°.
8. 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2Н)-піримідиніл]-4-фтор-N-[[метил-(1-метилетил)аміно]сульфоніл]бензамід, що містить щонайменше 90 мас. % гідрату за одним з попередніх пунктів.
9. Спосіб одержання гідрату за одним з пп. 1-7, який включає кристалізацію з розчину 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2Н)-піримідиніл]-4-фтор-N-[[метил-(1-метилетил)аміно]сульфоніл]бензаміду в органічному розчиннику в присутності води, причому органічний розчинник вибраний з групи, яка включає діалкілкетони з С3-5-атомами, С1-С4-алканоли, С2-С3алкіленглікольмоно-С1-С4-алкілові ефіри, ді-(С2-С3-алкіленгліколь-моно-С1-С4-алкілові ефіри, тетрагідрофуран і суміші цих розчинників.
10. Спосіб одержання гідрату за одним з пп. 1-7, який включає суспендування аморфного 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2Н)-піримідиніл]-4-фтор-N-[[метил-(1-метилетил)-аміно]сульфоніл]бензаміду у воді або водомісткому органічному розчиннику, причому органічний розчинник вибраний з групи, яка включає діалкілкетони з С3-5-атомами, С1-С4-алканоли, С2-С3-алкіленглікольмоно-С1-С4-алкілові ефіри, ді-(С2-С3-алкіленгліколь-моно-С1-С4-алкілові ефіри, тетрагідрофуран і суміші цих розчинників.
11. Гербіцид, що містить гідрат за одним з пп. 1-7 і звичайні допоміжні засоби для приготування засобів для захисту рослин.
12. Гербіцид за п. 11 у вигляді водного суспензійного концентрату.
13. Гербіцид за п. 11 у вигляді неводного суспензійного концентрату.
14. Гербіцид за п. 11 у вигляді здатного до диспергування в воді порошку або грануляту.
15. Спосіб боротьби з небажаним ростом рослин, який відрізняється тим, що гідратом 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2Н)-піримідиніл]-4-фтор-N-[[метил-(1-метилетил)аміно]сульфоніл]бензаміду за одним з пп. 1-7 впливають на рослини, їх життєвий простір і/або насіння.
Текст
Реферат: Кристалічні гідрати 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2Н)піримідиніл]-4-фтор-N-[[метил-(1-метилетил)аміно]сульфоніл]бензаміду, що містять від 0,8 до 1,2 моль води, в перерахуванні на 1 моль 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4(трифторметил)-1-(2Н)-піримідиніл]-4-фтор-N-[[метил-(1-метилетил)аміно]сульфоніл]бензаміду. Способи одержання гідрату; гербіцид, що містить гідрат, та спосіб боротьби з небажаним ростом рослин. UA 99114 C2 (12) UA 99114 C2 UA 99114 C2 5 Даний винахід належить до гідратів 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4(трифторметил)-1-(2H)-піримідиніл]-4-фтор-N-[[метил-(1-метилетил)аміно]сульфоніл]бензаміду, який надалі також зазначається як фенілурацил I. Винахід також відноситься до способу одержання цих гідратів, а також до композицій для захисту рослин, які містять гідрати фенілурацилу I. Фенілурацил I, який відповідає наступній формулі, CH3 F3C N O O N O 10 15 20 25 30 35 40 45 50 F O N Cl H O S N CH(CH3)2 I, CH3 представляє собою гербіцидно діючу речовину, яка відома з WO 01/083459. Інші способи його одержання відомі з WO 03/097589, WO 05/054208 і WO 06/097589, а також з більш ранньої міжнародної заявки PCT/EP 2006/062414. Всі відомі способи одержання фенілурацилу I, надають його як аморфну речовину. Власні дослідження заявника показали, що аморфний фенілурацил I для одержання композицій, які містять речовину у вигляді твердої речовини, є придатним тільки умовно. Зокрема в багатофазних композиціях можуть існувати проблеми зі стабільністю. Тепер несподівано було винайдено, що завдяки придатним способам одержують гідрати фенілурацилу I, які не мають подібного недоліку. До того ж несподівано було виявлено, що ці гідрати володіють кращою гербіцидною дією і кращою сумісністю технічних рослин в цілому ряді культур, ніж відома до цього часу аморфна форма фенілурацилу I. Гідрати фенілурацилу I представляють собою кристалічні субстанції, які є більш густими, ніж відома до цього часу аморфна форма. І тому з гідратами легше поводитися, ніж з відомою до сих пір аморфною формою фенілурацилу I. Відповідно до цього даний винахід відноситься до гідратів 2-хлор-5-[3,6-дигідро-3-метил-2,6діоксо-4-(трифторметил)-1-(2H)-піримідиніл]-4-фтор-N-[[метил-(1метилетил)аміно]сульфоніл]бензаміду. Гідрати фенілурацилу I представляють собою кристалічні субстанції, які залежно від формування кристаліту, містять приблизно від 0,8 до 1,2 моль води, зокрема від 0,9 до 1,1 моль і особливо від 0,95 до 1,05 моль на моль фенілурацилу і які тому розглядаються як моногідрати. Склад можна визначити шляхом аналізу води відповідно до Карла-Фішера. Гідрати плавляться, залежно від швидкості нагріву і виду пробовідбірних посудин, в температурному інтервалі від 100 до 150 °C. У відкритих пробовідбірних посудинах і при низьких швидкостях нагріву в до 2 K/хв. Гідрати розплавляються в межах від 100 до 130 °C, в той час як область плавлення при більш високих швидкостях нагріву і/або при застосуванні закритих пробовідбірних посудин зрушується до більш високих значень. В закритих пробовідбірних посудинах і швидкостях нагріву в 5 K/хв. область плавлення звичайно знаходиться в межах від 120 до 150 °C, з піковим максимумом в межах від 130 до 140 °C. Наведені тут точки плавлення відносяться до значень, визначених за допомогою диференційної калориметрії (Differential Scanning Calorimetry: ДСК, тигельний матеріал алюміній). Більш ретельне дослідження гідратів показало, що вони можуть бути одержані в двох різних формах, надалі також зазначаються як гідрат (a) і гідрат (b), однак які мають ідентичний склад і порівняні точки плавлення. Для розрізнення від відомої аморфної форми, надалі також зазначається як форма I, гідрат (a) відповідно до винаходу надалі також зазначений як форма III і гідрат (b) відповідно до винаходу надалі також зазначений як форма IV. Відповідно до винаходу форма III може бути ідентифікована за допомогою рентгенівської порошкової дифрактометрії за допомогою її дифракційної діаграми. Таким чином, при 25 °C з застосуванням Cu-K-випромінювання (1,54178 Å) одержана рентгенівська порошкова дифрактограма форми III показує, щонайменше, одне характеристичне відображення при 2 (= 11,6±0,2°, тоді як форма IV показує, щонайменше, одне характеристичне відображення при 2 (= 12,1±0,2°. Зокрема рентгенівська порошкова дифрактограма форми III при цих умовах показує додатково до відображення при 2 (= 11,6±0,2° щонайменше 3, часто щонайменше 5, зокрема щонайменше 7 інших і особливо всі з наведених відображень в наведеній нижче таблиці 1 як 2-значення, відповідно як міжплощинні відстані d: 1 UA 99114 C2 Таблиця 1: 2 5,1±0,2° 10,1±0,2° 10,8±0,2° 11,6±0,2° 13,9±0,2° 15,1±0,2° 16,1±0,2° 17,9±0,2° 20,2±0,2° 24,5±0,2° 5 d [Å] 17,37±0,02 8,76±0,02 8,15±0,02 7,62±0,02 6,35±0,02 5,86±0,02 5,49±0,02 4,95±0,02 4,40±0,02 3,63±0,02 Дослідження монокристалів форми III показують, що кристалічна структура, яка лежить в основі, є моноклінною. Елементарна комірка має просторову групу P2(1)/c. Характеристичні данні кристалічної структури форми III (визначено при -170 °C) наведені в таблиці 2. Таблиця 2: Кристалографічні властивості форми III Параметри Клас Просторова група a b c Об'єм Z Густина (підрахована) R1; wR2 Довжина хвилі Форма III моноклінна P2(1)/c 17,624(2) Å 9,012(1) Å 13,624(1) Å 90° 92,223(4)° 90° 2162,3(3) Å 3 4 1,594 мг/м 3 0,096; 0,278 1,54178 Å a, b,c = контурна довжина елементарної комірки , , = кут елементарної комірки Z = кількість молекул в елементарній комірці 10 При 25 °C з застосуванням Cu-K-випромінювання (1,54178 Å) одержана рентгенівська порошкова дифрактограма форми IV знову показує додатково до відображення при 2 = 12,03±0,2°, як правило, щонайменше 3, часто щонайменше 5, зокрема щонайменше 7 інших і особливо всі з наведених відображень в наведеній нижче таблиці 3 як 2-значення, відповідно як міжплощинні відстані d: 2 UA 99114 C2 Таблиця 3: 2 5,2±0,2° 10,2±0,2° 10,9±0,2° 12,1±0,2° 14,0±0,2° 14,6±0,2° 15,4±0,2° 19,2±0,2° 19,9±0,2° 20,5±0,2° 24,7±0,2° 26,7±0,2° 27,8±0,2° 5 10 15 20 25 30 35 40 d [Å] 17,21±0,02 8,63±0,02 8,11±0,02 7,32±0,02 6,31±0,02 6,08±0,02 5,77±0,02 4,61±0,02 4,44±0,02 4,33±0,02 3,60±0,02 3,34±0,02 3,21±0,02 Одержання гідратів фенілурацилу I вдається, наприклад, за допомогою описаних надалі способів, які як головну стадію включають кристалізацію з розчину фенілурацилу I в органічному розчиннику в присутності води. Органічні розчинники можуть представляти собою як ті органічні розчинники, які змішуються з водою, так і ті, які мають тільки умовну змішуваність з водою. Прикладами переважних органічних розчинників, які надалі також зазначаються як розчинники L1, є - прості ациклічні ефіри з від 4 до 6 C-атомами, такі як метил-трет.-бутиловий ефір, - прості ациклічні ефіри з від 4 до 6 C-атомами, такі як тетрагідрофуран, - діалкілкетони з від 3 до 5 C-атомами, зокрема ацетон, - C1-C4-алканоли, такі як метанол, етанол, n-пропанол, ізопропанол, трет.-бутанол, - C2-C3-алкіленгліколь-моно-C1-C4-алкілові ефіри, такі як метиловий ефір етиленгліколю і nпропіловий ефір етиленгліколю, - ді-(C2-C3-алкіленгліколь-моно-C1-C4-алкілові ефіри, - складні C1-C4-алкілові ефіри аліфатичних C1-C4-карбонових кислот, зокрема складні C1-C4алкілові ефіри оцтової кислоти, такі як етилацетат і бутилацетат, - аліфатичні і ароматичні вуглеводні, зокрема моно- і ді-C1-C4-алкілбензоли, такі як толуол і ксилол, а також C5-C8-алкани, такі як пентан, гептан і гексан, - аліфатичні і ароматичні хлорвуглеводні, такі як дихлорметан і хлорбензол, і - суміші цих розчинників. Особливо переважними органічними розчинами є метанол, а також моно- і ді-C1-C4алкілбензоли, зокрема толуол, а також суміші моно- і ді-C1-C4-алкілбензолів, зокрема толуол, з зазначеними вище розчинами L1, зокрема з тетрагідрофураном і/або з метанолом. В цих сумішах моно- відповідно ді-C1-C4-алкілбензол складає щонайменше 50 об'ємн.-% і зокрема щонайменше 80 об'ємн.-%, в перерахуванні на загальну кількість органічного розчинника L1. Поряд з зазначеними вище розчинами L1 використовуваний для кристалізації органічний розчинник може також містити інші, що відрізняються від них органічні розчинники (надалі розчинники L2). Доля розчинника L2, як правило, складає не більш ніж 50 об'ємн.-%, зокрема не більш ніж 20 об'ємн.-%, в перерахуванні на загальну кількість використовуваного для кристалізації органічного розчинника. Кристалізацію гідратів відповідно до винаходу проводять в присутності води. Її, як правило, додають до розчину фенілурацилу в органічному розчиннику. У випадку розчинників, які здатні розчиняти воду, щонайменше, частково, завдяки додаванню води знижується розчинність фенілурацилу в органічному розчиннику і починається кристалізація гідрату. У випадку розчинників, які з доданою кількістю води утворюють багатофазну систему, кристалізація, як правило, досягається шляхом охолодження. Кількість води звичайно знаходиться в межах від 5 до 300 об'ємних частин, зокрема в межах від 5 до 200 об'ємних частин, в перерахуванні на 100 об'ємних частин органічного розчинника. Часто для кристалізації гідратів роблять так, що підготовляють розчин фенілурацилу I в одному з названих вище органічних розчинників і до нього додають бажану кількість води. Додавання води може відбуватися при кімнатній температурі або при підвищеній температурі і звичайно відбувається при температурах від 20 °C до температури кипіння 3 UA 99114 C2 5 10 15 20 25 30 35 40 45 50 55 60 використовуваного органічного розчинника, однак переважно при температурах максимально до 90 °C. Бажана кількість води може додаватися однією або декількома порціями протягом короткого проміжку часу, тобто до 10 хв., або повільно, наприклад, протягом проміжку часу в, щонайменше, 30 хв. або, щонайменше, 60 хв., наприклад, від 30 до 300 хв. або від 60 до 300 хв. або від 120 до 300 хв. Якщо додавання води відбувається при підвищеній температурі, то, як правило, слідом за додаванням води температуру знижують. Наприклад, можна зробити так, що до гарячого розчину додають воду, поки не починається кристалізація, потім охолоджують і при необхідності додають ще воду для доповнення кристалізації. Рівним чином є можливим розчинити фенілурацил I, переважно аморфну форму, в придатній суміші з органічного розчинника і води, при необхідності при нагріванні, наприклад, до температур в межах від 40 до 90 °C, і досягти кристалізації шляхом додавання додаткової води і/або шляхом охолодження. Для кристалізації форми III придатні, наприклад, ті способи, які сприяють повільній кристалізації, наприклад, коли додавання води проводять протягом тривалих відрізків часу і/або які повільно охолоджують суміш з розчинника і води, що містить розчинений фенілурацил I. Утворенню форми IV можна знову сприяти завдяки тим мірам, при яких досягається швидка кристалізація, наприклад, швидке додавання води або здійснення кристалізації при температурах нижче 40 °C. Кристалізацію форми III або IV можна регулювати або прискорювати за допомогою затравлювання затравлювальними кристалами відповідної форми, наприклад, тим, що перед або під час кристалізації додають затравлювальні кристали відповідної форми. Якщо при кристалізації додають затравлювальні кристали, то їх кількість звичайно складає від 0,001 до 10 мас.-%, часто від 0,005 до 5 мас.-%, зокрема від 0,01 до 1 мас.-% і особливо від 0,05 до 0,5 мас.-%, в перерахуванні на розчинений фенілурацил I. Оскільки кристалізацію проводять в присутності затравлювальних кристалів, то спочатку їх переважно додають при температурі, при якій досягається концентрація насичення фенілурацилу I у відповідному розчиннику, тобто при або нижче тієї температури, при якій розчинена кількість фенілурацилу I у відповідному розчиннику утворює насичений розчин. Температурна залежність концентрації насичення в розчиннику може бути встановлена спеціалістом в даній галузі техніки в ході звичайних експериментів. Часто додавання затравлювальних кристалів здійснюється, якщо температура розчину складає не більш ніж 60 °C. Переважно після додавання затравлювальних кристалів склад залишають охолоджуватися до температур нижче 30 °C, зокрема в 25 °C або нижче, наприклад, до температур в межах від 0 °C до 25 °C, перш ніж для виділення гідратів фенілурацилу I відокремлюють одержаний кристалічний матеріал з маточного розчину. Охолодження при відсутності затравлювальних кристалів можна контролювати зі швидкістю охолодження, як правило, не більш ніж в 30 K/ч, наприклад, від 1 до 30 K/ч, часто від 2 до 20 K/ч і зокрема від 3 до 15 K/ч або не здійснювати контролювання. Може бути вигідним, слідом за додаванням води або після закінчення охолодження одержаного осаду, ще протягом деякого періоду часу суспендування в маточному розчині, наприклад, протягом проміжку часу від 30 хв. до 3 дн., перш ніж продукт кристалізації виділять з маточного розчину. Альтернативно можна також фенілурацил I, переважно аморфну форму, суспендувати у воді або суміші з води і органічного розчинника, причому через деякий час утворюється гідрат фенілурацилу I відповідно до винаходу. Спосіб, названий останнім є особливо придатним для одержання форми IV. Що стосується органічних розчинників, то аналогічним чином відноситься зазначене вище. Виділення гідратів з кристалізаційної суміші, тобто відділення гідратів від маточного розчину, вдається завдяки звичайним методам розділення твердих компонентів від рідин, наприклад, шляхом фільтрації, центрифугування або за допомогою декантації. Як правило, виділену тверду речовину промивають, наприклад, застосовним для кристалізації розчинником, водою або сумішшю з застосовного для кристалізації органічного розчинника з водою. Промивання може здійснюватися за одну або декілька стадій, причому часто на останній промивальній стадії промивають водою. Промивання звичайно здійснюють при температурах нижче 30 °C, часто нижче 25 °C і зокрема нижче 20 °C, щоб утримати як можна меншу втрату цінного продукту. Потім можна одержаний гідрат піддати сушінню, що щадить, щоб уникнути втрати гідратної води, і потім провести наступну обробку. Однак часто одержану після промивання вологу активну речовину, зокрема зволожену водою активну речовину, безпосередньо піддають подальшій обробці. 4 UA 99114 C2 5 10 15 20 25 30 35 40 45 50 55 За допомогою кристалізації відповідно до винаходу одержують фенілурацил I, який по суті складається з гідрату відповідно до винаходу, тобто доля гідрату, в перерахуванні на загальну кількість фенілурацилу I в кристалізаційній суміші звичайно знаходиться при, щонайменше, 90 %, часто, щонайменше, 95 % і зокрема, щонайменше, 98 %. Чистота фенілурацилу в одержаних гідратах, тобто доля фенілурацилу I, в перерахуванні на загальну кількість органічних компонентів, що містяться в гідраті, як правило, складає, щонайменше, 94 мас.-%, зокрема, щонайменше, 96 мас.-%. Використовуваний для кристалізації фенілурацилу I розчин може бути одержаний, наприклад, шляхом наступних методів: (1) розчинення фенілурацилу I, переважно в формі, що відрізняється від гідратів, в органічному розчиннику або суміші розчинника і води; або (2) одержання фенілурацилу I шляхом хімічної взаємодії і переведення реакційної суміші, при необхідності після відділення реагентів і/або побічних продуктів, в придатний відповідно до винаходу органічний розчинник. Для одержання розчину шляхом розчинення фенілурацилу I в принципі може бути використана кожна відома форма фенілурацилу I. Звичайно вибирають форму фенілурацилу I, яка відрізняється від гідратних форм. Сюди відносяться зокрема твердий або рідкий розплав фенілурацилу або аморфний фенілурацил I, такий як відомий з рівня техніки. Поряд з аморфною формою I фенілурацилу також придатна кристалічна ангідратна форма II фенілурацилу. Ангідратна форма II є об'єктом паралельної патентної заявки, на яку тут робиться посилання у повному обсязі. Застосовний для розчинення фенілурацилу I розчинник звичайно представляє собою один їх названих вище органічних розчинників L1 або суміш різних розчинників L1 або суміш розчинників, яка містить, щонайменше, 70 мас.-% і особливо, щонайменше, 90 мас.-% розчинника L1, в перерахуванні на загальну кількість використовуваного для розчинення розчинника. Для розчинення форми фенілурацилу I, що відрізняється від гідратних форм III і IV, звичайно фенілурацил I вводять в розчинник у вигляді тонкодисперсної твердої речовини або у вигляді розплаву при перемішуванні при температурі, при якій розчинник відповідно суміш розчинників здатні розчинити фенілурацил I повністю. Розчинення фенілурацилу I відбувається звичайно при температурах в межах від 20 до 160 °C. В переважній формі здійснення винаходу розчинення фенілурацилу I здійснюється при підвищеній температурі, зокрема, щонайменше, при 50 °C, особливо, щонайменше, при 80 °C, причому застосовна для розчинення температура, звичайно, не перевищує точку кипіння розчинника. Часто розчинення відбувається при температурах в межах від 50 до 140 °C, зокрема в межах від 80 до 120 °C і особливо переважно в межах від 95 до 115 °C. Кількість фенілурацилу I, яка розчиняється в розчиннику, звичайно залежить від виду розчинника L1 і температури розчинення і часто знаходиться в межах від 50 до 800 г/л. Сприятливі умови можуть бути визначені спеціалістом в даній галузі техніки в ході звичайних експериментів. Розчин фенілурацилу I може також бути приготовлений завдяки тому, що одержану за допомогою хімічної взаємодії реакційну суміш, яка містить фенілурацил I, при необхідності після відділення реагентів і/або побічних продуктів, переводять в придатний відповідно до винаходу органічний розчинник або суміш з розчинника і води. При цьому можна зробити так, що взаємодію здійснюють в органічному розчиннику або суміші розчинників, яка, щонайменше, частково, переважно, щонайменше, до 50 мас.-%, складається з придатного для кристалізації розчинника і, якщо необхідно, проводять переробку, причому видаляють надлишкові реагенти і при необхідності наявні каталізатори і при необхідності наявний, не придатний розчинник. Одержання розчину фенілурацилу I шляхом хімічної взаємодії придатного попередника фенілурацилу I, може відбуватися по аналогії з методами, описаними в процитованому на початку рівні техніки, на що тут робиться посилання у повному обсязі. Одержання гідратів III і IV може також здійснюватися виходячи з аморфного 2-хлор-5-[3,6дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2H)-піримідиніл]-4-фтор-N-[[метил-(1метилетил)аміно]сульфоніл]бензаміду, при якому суспендують аморфний фенілурацил у воді або органічному розчиннику, що містить воду. Як органічні розчинники для цього зокрема придатні ті розчинники L1, які при 298 K і 1 бар можуть розчиняти, щонайменше, 100 г/л води. До них відносяться зокрема діалкілкетони з від 3 до 5 C-атомами, C1-C4-алканоли, C2-C3алкіленглікольмоно-C1-C4-алкілові ефіри, ді-(C2-C3-алкіленгліколь-моно-C1-C4-алкілові ефіри, тетрагідрофуран і суміші цих розчинників. Якщо використовується суміш з води і органічного 5 UA 99114 C2 5 10 15 20 25 30 35 40 45 розчинника, то кількість води складає звичайно від 50 до 2000 об'ємних частин, в перерахуванні на 100 об'ємних частин органічного розчинника. Одержання застосовного як вихідний матеріал для одержання гідратів 2-хлор-5-[3,6-дигідро2,6-діоксо-4-(трифторметил)-1(2H)-піримідиніл]-4-фтор-N-[[метил(1-метилетил)аміно]сульфоніл]-бензаміду може здійснюватися відповідно до способів, описаних в WO 01/083459, WO 03/097589, WO 05/054208, WO 06/097589 і PCT/EP 2006/062414, на які тим самим робиться посилання у повному обсязі. Особливо переважно фенілурацил I одержують наступними способами: 1) перетворення 2-хлор-5-[3,6-дигідро-2,6-діоксо-4-(трифторметил)-1(2H)-піримідиніл]-4фтор-бензойної кислоти в її кислотний хлорид або відповідний ангідрид і наступної взаємодії відповідного активованого кислотного похідного з N-метил-N-(1-метилетил)сульфамоїламідом, наприклад: Ця взаємодія звичайно відбувається при температурах від 20 °C до точки кипіння реакційної суміші в органічному розчиннику в присутності основи, а також при необхідності каталізатора [порівн. наприклад, WO 01/083459, WO 03/097589 і також WO 04/039768]. Придатними розчинами є аліфатичні вуглеводні, такі як пентан, гексан, циклогексан і суміші C5-C8-алканів, ароматичні вуглеводні, такі як толуол, o-, m- і p-ксилол, галогеновані вуглеводні, такі як метиленхлорид, хлороформ і хлорбензол, прості ефіри, такі як діетиловий ефір, діізопропіловий ефір, трет.-бутилметиловий ефір, діоксан, анізол і тетрагідрофуран, нітрили, такі як ацетонітрил і пропіонітрил, кетони, такі як ацетон, метилетилкетон, діетилкетон і трет.-бутилметилкетон, спирти, такі як метанол, етанол, n-пропанол, ізопропанол, n-бутанол і трет.-бутанол, а також диметилсульфоксид, диметилформамід і диметилацетамід. Також можуть застосовуватися суміші названих розчинників. Як основи, загалом, придатні неорганічні основи, такі як гідроксиди лужних і лужноземельних металів, такі як гідроксид літію, гідроксид натрію, гідроксид калію і гідроксид кальцію, оксиди лужних і лужноземельних металів, такі як оксид літію, оксид натрію, оксид кальцію і оксид магнію, гідриди лужних і лужноземельних металів, такі як гідрид літію, гідрид натрію, гідрид калію і гідрид кальцію, аміди лужних металів, такі як амід літію, амід натрію і амід калію, карбонати лужних і лужноземельних металів, такі як карбонат літію, карбонат калію і карбонат кальцію, а також гідрокарбонати лужних металів, такі як гідрокарбонат натрію, металоорганічні сполуки, зокрема алкіли лужних металів, такі як метиллітій, бутиллітій і феніллітій, галогеніди алкілмагнію, такі як хлорид метилмагнію, а також алкоголяти лужних і лужноземельних металів, такі як метанолат натрію, етанолат натрію, етанолат калію, трет.бутанолат калію, трет.-пентанолат калію і диметоксимагній, крім того, органічні основи, наприклад, третинні аміни, такі як триметиламін, триетиламін, діізопропілетиламін і Nметилпіперидин, піридин, заміщені піридини, такі як колідин, лутидин і 4-диметиламінопіридин, а також біциклічні аміни. Основи, загалом, використовують в каталітичних або еквімолярних кількостях, однак вони також можуть застосовуватися в надлишку або при необхідності як розчинник. Вихідні продукти, загалом, взаємодіють один з іншим в еквімолярних кількостях. Може бути вигідним використання одного з вихідних продуктів в надлишку. 2) метилування 2-хлор-5-[3,6-дигідро-2,6-діоксо-4-(трифторметил)-1(2H)-піримідиніл]-4фтор-N-[[метил(1-метилетил)аміно]сульфоніл]-бензаміду (надалі "NH-урацил") з метилуючим агентом C: H F3C N O O N O F N Cl O CH3 O H S CH3 N CH3 6 H3C-L1 I C UA 99114 C2 1 5 10 15 20 25 30 35 40 45 50 55 60 Група L означає нуклеофільну відхідну групу, переважно галоген, такий як хлор, бром або йод, C1-C6-алкілсульфат, такий як метилсульфат, C1-C6-алкілсульфонілокси, такий як метилсульфонілокси, C1-C6-галогеналкілсульфонілокси, такий як трифторметилсульфонілокси або фенілсульфонілокси; дуже переважно означає C1-C6-алкілсульфат. Придатними метилуючими агентами C є метилгалогеніди, такі як метилйодид, метилбромід, метилхлорид, диметилсульфат, складний метиловий ефір C 1-C6-галогеналкілсульфокислоти або складний метиловий ефір фенілсульфокислоти, особливо переважні метилгалогеніди і диметилсульфат; виключно переважний диметилсульфат. Метилуючий агент C може використовуватися як в еквімолярній кількості, в перерахуванні на NH-урацил, так і в достехіометричній кількості або надстехіометричній кількості. Звичайно спосіб (2) здійснюють в присутності основи, причому придатними є всі звичайні органічні і неорганічні основи, наприклад, основи, названі для способу (1). Переважно основи вибрані з гідроксидів лужних і лужноземельних металів, таких як гідроксид літію, гідроксид натрію, гідроксид калію і гідроксид кальцію, оксидів лужних і лужноземельних металів, таких як оксид літію, оксид натрію, оксид кальцію і оксид магнію, карбонатів лужних і лужноземельних металів, таких як карбонат літію, карбонат натрію, карбонат калію і карбонат кальцію, а також гідрокарбонатів лужних металів, таких як гідрокарбонат натрію. В особливо переважній формі здійснення використовують як основу гідроксид натрію або гідроксид калію. Основи, загалом, використовують в еквімолярних кількостях в перерахуванні на NH-урацил, однак вони також можуть застосовуватися каталітично, в надлишку або при необхідності як розчинники. В дуже переважному варіанті способу (2) значення pH під час загальної взаємодії утримують в межах від 1 до 6 шляхом безперервного або порційного додавання основи. "Порційне додавання основи" означає, що додавання основи під час взаємодії відбувається окремими порціями, тобто щонайменше, 2 порціями, або від декількох до багатьох порцій, або безперервно. Для взаємодії NH-урацил, метилуючий агент C і при необхідності основа можуть вноситися в реакційну посудину окремо, одночасно або один за іншим і приводитися в реакцію. Відповідно до першої форми здійснення способу (2) взаємодія NH-урацилу з метилуючим агентом C відбувається в органічному розчиннику. Як розчинники для цих взаємодій придатні, залежно від температурного інтервалу, аліфатичні, циклоаліфатичні або ароматичні вуглеводні, такі як пентан, гексан, циклопентан, циклогексан, толуол, ксилол, хлоровані аліфатичні і ароматичні вуглеводні такі як дихлорметан, трихлорметан, 1,2-дихлоретан, 1,1,2,2-тетрахлоретан, хлорбензол, 1,2-, 1,3- або 1,4дихлорбензол, хлортолуоли, дихлортолуоли, прості діалкілові ефіри з відкритим ланцюгом, такі як діетиловий ефір, ді-n-пропіловий ефір, ді-n-ізопропіловий ефір, метил-трет-бутиловий ефір, циклічні прості ефіри, такі як тетрагідрофуран, 1,4-діоксан, анізол, прості ефіри гліколей, такі як диметилгліколевий ефір, діетилгліколевий ефір, диметиловий ефір діетиленгліколю, діетиловий ефір діетиленгліколю, C1-C4-спирти, такі як метанол, етанол, n-пропанол, ізо-пропанол, nбутанол, аліфатичні C1-C6-складні алкілові ефіри карбонової кислоти, такі як метилацетат, етилацетат або n-бутилацетат; кетони, такі як ацетон, метилетилкетон, метилізопропілкетон, метилізобутилкетон, бутанон, карбонати, такі як діетилкарбонат і етиленкарбонат, N, Nдіалкіламіди, такі як N, N-диметилформамід або N, N-диметилацетамід, N-алкіллактами, такі як N-метилпіролідон, сульфоксиди, такі як диметилсульфоксид, тетраалкілсечовини, такі як тетраметилсечовина, тетраетилсечовина, тетрабутилсечовини, диметилетиленсечовина, диметилпропіленсечовина або суміші цих розчинників. Як розчинники переважні N, N-діалкіламіди, такі як N, N-диметилформамід, N-алкіллактами, такі як N-метилпіролідон, кетони, такі як ацетон, ароматичні вуглеводні, такі як толуол, хлоровані аліфатичні і ароматичні вуглеводні, такі як дихлорметан або хлорбензол, циклічні прості ефіри, такі як тетрагідрофуран, аліфатичні C1-C6-складні алкілові ефіри карбонової кислоти, такі як етилацетат, бутилацетат або суміші цих розчинників. Переважно метилування NH-урацилу проводять при температурах між -5 °C і 100 °C. Тривалість реакції може бути визначена звичайним для спеціаліста в даній галузі техніки чином за допомогою стандартних методів, таких як тонкошарова хроматографія або ВЕРХ. В іншому варіанті способу (2a) взаємодію можна здійснювати також в багатофазній системі. Цей варіант є переважним. Сказане раніше відноситься і до алкілуючого агента С, pH-значення, основи, температури і тиску. Відповідно до другої переважної форми здійснення способу (2) взаємодія NH-урацилу з метилуючим агентом C відбувається в водно-органічній багатофазній системі в присутності одного або декількох міжфазних каталізаторів. 7 UA 99114 C2 5 10 15 20 25 30 35 40 45 50 55 60 Прикладами міжфазних каталізаторів є четвертинні амонієві солі, солі фосфонію, краунефіри або полігліколі. Переважні придатні четвертинні амонієві солі включають, наприклад, галогеніди тетра-(C1-C18)-алкіламонію і галогеніди N-бензилтри-(C1-C18)-алкіламонію. Переважні придатні солі фосфонію включають, наприклад, хлориди, броміди, ацетати C 1-C18алкілтрифенілфосфонію, хлориди або броміди тетра-(C1-C18)-алкілфосфонію хлорид або бромід тетрафенілфосфонію, хлорид або бромід бензилтрифенілфосфонію. Переважні придатні краунефіри включають, наприклад, 18-краун-6, дибензо-18-краун-6. Переважні придатні полігліколі включають, наприклад, дибутиловий ефір діетиленгліколю (=бутилдігліми), диметиловий ефір тетраетиленгліколю (= тетрагліми), диметиловий ефір триетиленгліколю (= тригліми), диметиловий ефір полігліколю. Як правило, межфазний каталізатор використовують в кількості до 20 моль-%, в перерахуванні на NH-урацил. Багатофазна система включає одну водну фазу і щонайменше одну органічну рідку фазу. Поряд з цим можуть також зустрічатися тверді фази. Водна фаза переважно є розчином, який містить основу, зокрема водним розчином гідроксидів лужних і лужноземельних металів (таких як гідроксид літію, гідроксид натрію, гідроксид калію і гідроксид кальцію), карбонатів лужних і лужноземельних металів (таких як карбонат літію, карбонат натрію, карбонат калію і карбонат кальцію) або гідрокарбонатів лужних металів (такі як гідрокарбонат натрію) у воді. Особливо переважно застосовують гідроксиди лужних і лужноземельних металів, дуже переважно гідроксид натрію. Основу(и) загалом, застосовують в еквімолярних кількостях в перерахуванні на NH-урацил, однак вони також можуть застосовуватися каталітично, в надлишку або при необхідності як розчинники. Переважно використовують, щонайменше, одну еквимолярну кількість основи, в перерахуванні на NH-урацил. Для органічної фази як розчинники залежно від температурного інтервалу переважно придатні аліфатичні, циклоаліфатичні або ароматичні вуглеводні, такі як пентан, гексан, циклопентан, циклогексан, толуол, ксилол, хлоровані аліфатичні і ароматичні вуглеводні такі як дихлорметан, трихлорметан, 1,2-дихлоретан, 1,1,2,2-тетрахлоретан, хлорбензол, 1,2-, 1,3- або 1,4-дихлорбензол, хлортолуоли, дихлортолуоли, прості діалкілові ефіри з відкритим ланцюгом, такі як діетиловий ефір, ді-n-пропіловий ефір, ді-n-ізопропіловий ефір, метил-трет-бутиловий ефір, циклічні прості ефіри, такі як тетрагідрофуран (ТГФ) і анізол, аліфатичні карбонової кислоти-C1-C6-складні алкілові ефіри, такі як метилацетат, етилацетат або n-бутилацетат або суміші цих розчинників. Для органічної фази як розчинники переважно придатні етилацетат, nбутилацетат, хлорбензол, ТГФ, толуол або суміші цих розчинників; дуже переважні етилацетат, n-бутилацетат, хлорбензол і ТГФ-суміші, а також толуол і ТГФ-суміші. Під час взаємодії можуть зустрічатися тверді фази, коли наприклад, NH-урацил, метилуючий агент C, основа і/або межфазний каталізатор не розчинені повністю. В переважній формі здійснення багатофазна система як водна фаза складається з водного розчину гідроксиду натрію, і як органічна фаза з толуолу і тетрагідрофурану, або дихлорметану і тетрагідрофурану, хлорбензолу і тетрагідрофурану, або з етилацетату або n-бутилацетату. Для взаємодії NH-урацил, метилуючі засоби C, основа і при необхідності межфазний каталізатор можуть вноситися в реакційну посудину окремо, одночасно або один за іншим і приводитися в реакцію. Як правило, при застосуванні двофазної системи перед кристалізацією форми III відповідно IV фази розділяють. Особливо переважно одержаний таким шляхом продукт перед кристалізацією висушують за допомогою відомих для спеціаліста в даній галузі техніки способів сушіння, наприклад, шляхом азеотропного відгону води разом з частиною органічного розчинника. Наведені нижче зображення і приклади служать для пояснення винаходу і не повинні розумітися як такі, що обмежують його. Зображення 1 показує рентгенівську порошкову дифрактограму форми III. Рентгенівська дифрактограма форми III була одержана за допомогою дифрактометра D-5000 фірми BrukerAXS в відбивній геометрії в межах від 2 = 4° – 35° з величиною кроку в 0,02° при застосуванні Cu-K-випромінювання при 25 °C. З визначених 2-значень були розраховані зазначені міжплощинні відстані d. Зображення 2 показує рентгенівську порошкову дифрактограму форми IV. Сказане раніше відноситься і до умов вимірювання. Зображення 3 показує ІЧ-спектр форми III і зображення 4 спектр форми IV. ІЧ-спектри були одержані за допомогою FTIR-спектрометрів "Nicolet Magna 550" і "Nicolet Magna 750" фірми -1 -1 Thermo Electron Corp./США в області хвильового числа від 400-4000 см при дозволі в 4 см (32 Scans). Як пробні зразки служили KBr-прес-вироби. 8 UA 99114 C2 5 10 15 20 25 30 35 40 45 50 55 60 Визначення точок плавлення і теплоти плавлення відбувалось за допомогою ДСК з Метлер Толедо ДСК 25 фірми Mettler зішвидкістю нагріву в 5 K/хв. в межах від -5° до +180 °C. Кількість проби склала 5 до 10 мг. Визначення кристалографічних даних форми III (Таблиця 2) здійснювалось на монокристалічному дифрактометрі фірми Bruker ("Bruker P4") з застосуванням Cu-Kαвипромінювання. Вимірювання було проведено при -170 °C. Приклад 1: Одержання форми III фенілурацилу I шляхом кристалізації аморфної форми I з тетрагідрофуран/води Метод a: 20 г аморфного фенілурацилу I розчиняли в 300 мл ТГФ. До розчину при кімнатній температурі додавали порцію 300 мл води і через 48 год. знову додаткові 300 мл води. Одержану суспензію ще 3 дні піддавали руху при кімнатній температурі. Потім одержану тверду речовину відфільтровували від маточного розчину. Одержаний таким чином кристалічний матеріал аналізували за допомогою ДСК і за допомогою рентгенівської порошкової дифрактометрії. Була одержана форма III. Метод b: 20 г аморфного фенілурацилу I розчиняли в 300 мл ТГФ. Нагрівали до 40 °C і до розчину додавали порцію в 300 мл води. Потім охолоджували до кімнатної температури, і одержану тверду речовину відфільтровували від маточного розчину. Одержаний таким чином кристалічний матеріал аналізували за допомогою ДСК і за допомогою рентгенівської порошкової дифрактометрії. Була одержана форма III. Приклад 2: Одержання форми III фенілурацилу I шляхом кристалізації аморфної форми I з ацетон/води 2 г аморфного фенілурацилу I розчиняли в 20 мл ацетону. Розчин нагрівали до 40 °C і до нього, зберігаючи температуру, додавали протягом проміжку часу в 2 год. 5 порцій води по 5 мл. При цьому почав викристалізовуватися осад. Повільно охолоджували до кімнатної температури (прибл. 4 год.) і потім одержаний осад відфільтровували. Рентгенівська порошкова дифрактограма підтверджувала наявність форми III. Приклад 3: Одержання форми III фенілурацилу I шляхом кристалізації аморфної форми I з монопропілового ефіру етиленгліколю/води 2 г аморфного фенілурацилу I розчиняли при 80 °C в 20 мл монопропілового ефіру етиленгліколю. До нього, зберігаючи температуру, додавали протягом проміжку часу в 1 год. 25 мл води. При цьому почав викристалізовуватися осад. Повільно охолоджували і потім одержаний осад відфільтровували. Рентгенівська порошкова дифрактограма підтверджувала наявність форми III. Приклад 4: Одержання форми IV фенілурацилу I шляхом кристалізації аморфної форми I з ізопропанол/вода 5 г аморфного фенілурацилу I розчиняли в 60 мл ізопропанолу при нагріванні зі зворотнім холодильником. До нього, зберігаючи температуру, додавали 50 мл води. При цьому почав викристалізовуватися осад. Охолоджували до від 50 до 60 °C, температуру утримували 2 дні, потім охолоджували до кімнатної температури і 2 дні утримували температуру. Потім нагрівали до від 50 до 60 °C, утримували температуру 2 дні, потім охолоджували до кімнатної температури і потім одержаний осад відфільтровували. Одержаний таким чином кристалічний матеріал аналізували за допомогою ДСК і за допомогою рентгенівської порошкової дифрактометрії. Була одержана форма IV. Приклад 5: Одержання форми IV фенілурацилу I за допомогою переосадження аморфної форми I у воді 2 г аморфного фенілурацилу I 2 дні перемішували при кімнатній температурі в 20 мл води. Потім тверду речовину відокремлювали за допомогою центрифугування. Рентгенівська порошкова дифрактограма підтверджувала наявність форми IV. Приклад 6: Одержання форми IV фенілурацилу I шляхом кристалізації аморфної форми I з тетрагідрофуран/води Метод a: 20 г аморфного фенілурацилу I розчиняли в 300 мл ТГФ. До розчину додавали при кімнатній температурі в порцію 600 мл води. Одержану суспензію збовтували ще 2 дні при кімнатній температурі. Потім одержану тверду речовину відфільтровували від маточного розчину. Рентгенівська порошкова дифрактограма підтверджувала наявність форми IV. Приклад 7: Одержання форми III шляхом взаємодії N-(2-хлор-4-фтор-5-ізоціанатобензоїл)N’-метил-(1-метилетил)сульфамід зі складним етиловим ефіром 3-метиламіно-4,4,4трифторкротонової кислоти і осадження з метанол/води Під азотом перемішували 0,99 г (5,021 ммоль) складного етилового ефіру 3-метиламіно4,4,4-трифторкротонової кислоти в 25 мл N,N-диметилформаміду і 50 мл n-пентану 45 хвилин в водовіддільнику нагрівали зі зворотнім холодильником. Потім дистилювали n-пентан до 9 UA 99114 C2 5 10 15 20 25 30 35 40 45 50 55 60 внутрішньої температури 70 °C. Залишали охолоджуватися до 40 °C і після цього додавали протягом 15 хвилин при температурі до 45 °C 1,13 г (10,043 ммоль) трет-бутилату калію за 3 порції при перемішуванні, причому утворювався червоно-бурий розчин. Після 20-хвилинного перемішування при 40 °C залишали охолоджуватися і потім при від -15 °C до -10 °C додавали 1,55 г (4,419 ммоль) N-(2-хлор-4-фтор-5-ізоціанатобензоїл)-N’-метил-(1-метилетил)сульфаміду протягом 2 хвилин, причому починалось негайне розчинення. Перемішували 30 хвилин при 10 °C, після цього залишали реакційну суміш нагріватися до 22 °C і перемішували ще 30 хвилин при цій температурі. При незначному охолодженні при 20-22 °C одержану реакційну суміш підкисляли за допомогою 0,46 г (12,553 ммоль) 4 n соляної кислоти в 3,1 мл діоксану, причому випадав осад, і концентрували в вакуумі. Одержаний залишок розподіляли в суміші розчинників з 100 мл метилтрет.-бутилового ефіру і 100 мл води. Органічну фазу відокремлювали і після цього концентрували в вакуумі до сухості. Склоподібну смолу ресуспендировали в холодній як лід суміші з метанолу:води = 7:3 при перемішуванні, причому протягом 30 хв. Почалося утворення осаду. Відсмоктаний залишок перемішували 0 °C 0,5 год. в метил-трет.-бутиловому ефірі, відсмоктували, промивали метил-трет.-бутиловим ефіром і висушували в вакуумі, причому одержували 1,00 г (43,6 % теорії) сполуки, зазначеної в заголовку, у вигляді безбарвного 1 порошку з H-ЯМР-чистотою в 95 % і точкою плавлення в 107-122 °C. Рентгенівська порошкова дифрактограма підтверджувала наявність форми III. Приклад 8: Одержання форми III шляхом осадження одержаного при метилуванні сирого продукту з метил-трет.-бутилового ефіру і води До суміші розчинників з 155 г толуолу і 31 г тетрагідрофурану при 25 °C додавали 14,18 г (0,0274 моль) 2-хлор-5-3,6-дигідро-2,6-діоксо-4-(трифторметил)-1(2H)-піримідиніл(-4-фтор-N((метил(1-метилетил)аміно(сульфоніл(бензаміду (93,9 %ий) і після цього суміш розбавляли з розчином з 2,55 г (0,0319 моль) гідроксиду натрію (50 % ig) в 61,2 г води. До реакційної суміші додавали 0,88 г (0,0027 моль) броміду тетрабутиламонію і 4,08 г (0,0329 моль) диметилсульфату. Двофазну реакційну суміш інтенсивно перемішували 23 години при 25 °C. Після чого водну фазу відокремлювали і органічну фазу промивали два рази за допомогою 100 мл води в кожному випадку. Після висушування об'єднаної органічної фази розчинник дистилювали при нормальному тиску, причому одержували 15,4 г сирого продукту, який відповідно до кількісної ВЕРХ містив сполуку, зазначену в заголовку до 77,6 % (відповідає виходу в 87,2 %). Слідом за цим додавали до нагрітої до 40 °C суміші розчинників з 60 мл метил-третбутилового ефіру і 6 мл води при перемішуванні 14 г одержаного сирого продукту. Залишали повільно охолоджуватися до 0 °C, причому випадав осад. Тверду речовину, що випала в осад, відсмоктували і висушували її. В цій стадії осадження одержували 11,3 г сполуки, зазначеної в заголовку (чистота відповідно до кількісної ВЕРХ визначена як моногідрат: 93,3 %; загальний вихід після осадження: 81,5 %). Рентгенівська порошкова дифрактограма підтверджувала наявність форми III. Приклад 9: одержання кристалічного гідрату форми III шляхом кристалізації з толуол/води Розчин 0,92 моль 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4-трифторметил-1-(2H)піримідиніл]-4-фтор-N-[(метил-ізопропіл-аміно)сульфоніл]-бензаміду в 95 % толуолі з 5 % ТГФ змішували з 180 г (10 моль) води при 75 °C і протягом 3 год. охолоджували до 20 °C. Перемішували 15 год. і тверду речовину, що випала в осад, при 20 °C відфільтровували. Тверду речовину промивали на фільтрі з 150 г толуолу і висушували в вакуумі при температурах < 50 °C. Вихід: 0,82 моль. Рентгенівська порошкова дифрактограма підтверджувала наявність форми III. Приклад 10: одержання кристалічного гідрату 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4трифторметил-1-(2H)-піримідиніл]-4-фтор-N-[(метил-ізопропіл-аміно)сульфоніл]-бензаміду (= форма III) з реакційного розчину 50,0 г (0,098 моль) 2-хлор-5-[3,6-дигідро-2,6-діоксо-4-(трифторметил)-1(2H)-піримідиніл]-4фтор-N-{[метил-(1-метилетил)аміно]сульфоніл}-бензаміду, 3,2 г (0,0089 моль) броміду тетрабутиламонію (= TBAB) і 15,1 г (0,12 моль) диметилсульфату при 25 °C поміщали в суміш з толуолу, води і ТГФ і склад нагрівали до 40 °C. Потім шляхом додавання водного 10 %-ого розчину NaOH в реакційній суміші встановлювали значення pH в 5,3-5,5. Під час всієї тривалості реакції далі додавали водний 10 %-ий розчин NaOH, так що значення pH протягом всього перебігу реакції було постійним на рівні раніше встановленого значення pH. Після завершеної реакції реакційну суміш перемішували ще 3,5 год. при 40 °C. Метод a): Фази розділяли при 40 °C. До органічної фази додавали 250 г води і толуол і ТГФ повністю відганяли азеотропно. Одержану суміш при 65 °C змішували з метанолом і протягом 3 10 UA 99114 C2 5 10 15 20 25 30 35 40 45 50 55 60 год. охолоджували до 20 °C. Одержували 45.6 г (82 % теорії; чистота 91,4 %) фенілурацилу у вигляді форми III, яка була встановлена виходячи з її рентгенівської порошкової дифрактограми. Метод b): Фази розділяли і від 65 до 70 % використовуваного розчинника відганяли. Розчин охолоджували до 75 °C і потім додавали 18 г води. Розчин протягом 3 год. лінійно охолоджували до 20 °C і перемішували 3 год. при 20 °C. Тверду речовину, що випала в осад відсмоктували і висушували. Одержували 44,8 г (83 % теорії; чистота 94,1 %) форми III, яка була встановлена виходячи з її рентгенівської порошкової дифрактограми. Форми III і IV в такому ж ступені, як і форма I придатні як гербіциди, однак перевершують її у відношенні ефективності. Тому винахід також відноситься до засобу для захисту рослин, який містить кристалічну форму III відповідно форму IV і звичайні допоміжні засоби для приготування засобів для захисту рослин, зокрема засобів для захисту рослин у вигляді водних або неводних суспензійних концентратів. Винахід також відноситься до способу боротьби з небажаним ростом рослин, який відрізняється тим, що формою III відповідно формою IV фенілурацилу, переважно у вигляді придатного препарату діючої речовини впливають на рослини, їх життєвий простір і/або насіння. Гербіцидні засоби, що містять форму III відповідно форму IV дуже гарно борються з ростом рослин на площах, не відведених під певну культуру, особливо при високих нормах витрати. В культурах, таких як пшениця, рис, кукурудза, соя і бавовник вони діють проти бур'янів і шкідливих трав, не наносячи суттєвої шкоди культурним рослинам. Цей ефект, перш за все, проявляється при низьких нормах витрати. Залежно від відповідного методу нанесення форма III відповідно форма IV або засоби, що їх містять можуть використовуватися також на цілому ряді інших культурних рослин для знищення небажаної рослинності. Придатними є, наприклад, наступні культури: Allium cepa, Ananas comosus, Arachis hypogaea, Asparagus officinalis, Beta vulgaris spec. altissima, Beta vulgaris spec. rapa, Brassica napus var. napus, Brassica napus var. napobrassica, Brassica rapa var. silvestris, Camellia sinensis, Carthamus tinctorius, Carya illinoinensis, Citrus limon, Citrus sinensis, Coffea arabica (Coffea canephora, Coffea liberica), Cucumis sativus, Cynodon dactylon, Daucus carota, Elaeis guineensis, Fragaria vesca, Glycine max, Gossypium hirsutum, (Gossypium arboreum, Gossypium herbaceum, Gossypium vitifolium), Helianthus annuus, Hevea brasiliensis, Hordeum vulgare, Humulus lupulus, Ipomoea batatas, Juglans regia, Lens culinaris, Linum usitatissimum, Lycopersicon lycopersicum, Malus spec., Manihot esculenta, Medicago sativa, Musa spec., Nicotiana tabacum (N.rustica), Olea europaea, Oryza sativa, Phaseolus lunatus, Phaseolus vulgaris, Picea abies, Pinus spec., Pisum sativum, Prunus armeniaca, Prunus avium, Prunus cerasus, Prunus dulcis, Prunus domesticua, Prunus persica, Pyrus communis, Ribes sylvestre, Ricinus communis, Saccharum officinarum, Secale cereale, Solanum tuberosum, Sorghum bicolor (s. vulgare), Theobroma cacao, Trifolium pratense, Triticum aestivum, Triticum durum, Vicia faba, Vitis vinifera і Zea mays. На додаток до цього форма III відповідно форма IV або гербіцидні засоби, що їх містять, можуть також застосовуватися для культур, які завдяки вирощуванню, включаючи методи генної інженерії, є стійкими до дії гербіцидів. Далі форма III відповідно форма IV або гербіцидні засоби, що їх містять, можуть також застосовуватися для культур, які завдяки вирощуванню, включаючи методи генної інженерії, є стійкими до комах або ураження грибами. Крім того, було винайдено, що форми III і IV також придатні для дефоліації і/або десікації частин рослин, для чого придатні культурні рослини, такі як бавовник, картопля, рапс, соняшник, соєві боби або боби польові, особливо бавовник. В зв'язку з цим були розроблені засоби для десікації і/або дефоліації рослин, спосіб одержання цих засобів і спосіб десікації і/або дефоліації рослин за допомогою форми III відповідно форми IV. Як десіканти придатні форми III і IV, зокрема для висушування надземних частин культурних рослин, таких як картопля, рапс, соняшник і соєві боби. Що дає можливість здійснювати повністю механічний збір врожаю цих важливих культур. В інтересах сільського господарства є важливим подальше полегшення збирання врожаю, яке роблять можливим за допомогою сконцентрованого у часі обпадання або зниження зчеплення з деревом у цитрусових плодів, оливок і інших видів і сортів зерняткових, кісточкових плодів і горіхоплідних. Той же самий механізм, тобто, сприяння утворенню розділювальної тканини між плодовою або листяною і стебловою частиною рослин є також важливим для добре контрольованого видалення листя технічних культур, особливо бавовнику. Крім того, скорочення часового інтервалу, за який дозрівають окремі рослини бавовнику, приводить до підвищеної якості волокна після збирання врожаю. 11 UA 99114 C2 5 10 15 20 25 30 35 40 45 50 55 Крім того, було винайдено, що форми III і IV також придатні для боротьби з хвойними, зокрема з дикоростучими сіянцями хвойних, особливо для боротьби з дикоростучими сіянцями сосни. Далі форми III і IV також придатні для боротьби з бур'янистими травами в культурних рослинах, таких як, наприклад, соєвібоби, бавовник, рапс, льон, сочевиця, рис, цукровий буряк, соняшник, тютюн і зернові культури, такі як, наприклад, кукурудза або пшениця. Форма III відповідно IV відповідно гербіцидні засоби, що їх містять, можуть застосовуватися, наприклад, в формі водних розчинів для безпосереднього обприскування, порошків, суспензій, також високопроцентних водних, олійних або інших суспензій, олійних суспензій, паст, препаратів для обпилювання, препаратів для опудрювання або гранулятів, шляхом обприскування, дрібнокрапельного обприскування, обпилювання, опудрювання або поливу. Форми застосування залежать від цілей використання; в будь-якому випадку вони повинні забезпечувати тонкий і рівномірний розподіл діючих речовин відповідно до винаходу. Гербіцидні засоби містять гербіцидно активну кількість форми III відповідно IV і звичайні для приготування засобів для захисту рослин допоміжні речовини і носії. Як тверді носії в принципі придатні всі тверді речовини, які звичайно використовуються в засобах для захисту рослин, зокрема в гербіцидах. Твердими носіями є мінеральні землі, такі як силікагелі, силікати, тальк, каолін, вапняк, вапно, крейда, болюс, лес, глина, доломіт, діатомова земля, сульфат кальцію, сульфат магнію, оксид магнію, розмелені пластмаси, добрива, такі як сульфат амонію, фосфат амонію, нітрат амонію, сечовини й рослинні продукти, такі, як наприклад борошно зернових культур, борошно деревної кори, деревне борошно й борошно горіхової шкарлупи, целюлозний порошок або інші тверді носії. У випадку рідких композицій форми III відповідно IV склади мають рідку фазу. Як рідка фаза в принципі придатні вода, а також ті органічні розчинники, в яких форма III відповідно IV мають тільки незначну розчинність або не мають, наприклад, ті в яких розчинність форм III відповідно IV фенілурацилу I при 25 °C і 1013 мбар складає не більш ніж 1 мас.-%, зокрема не більш ніж 0,1 мас.-% і особливо не більш ніж 0,01 мас.-%. Переважними рідкими фазами є зокрема вода і водні розчинники, тобто суміші розчинників, які поряд з водою ще містять до 30 мас.-%, однак переважно не більш ніж 10 мас.-%, в перерахуванні на загальну кількість води і розчинника, одного або декількох, змішуваних з водою органічних розчинників, наприклад, змішуваних з водою простих ефірів, таких як тетрагідрофуран, метилгліколь, метилдигліколь, алканоли, такі як метанол, етанол, ізопропанол або поліоли, такі як гліколь, гліцерин, діетиленгліколь, пропіленгліколь тощо. Далі переважними рідкими фазами є неводні органічні розчинники, в яких розчинність форми III відповідно IV фенілурацилу I при 25 °C і 1013 мбар складає не більш ніж 1 мас.-%, зокрема не більш ніж 0,1 мас.-% і особливо не більш ніж 0,01 мас.-%. До них відносяться зокрема аліфатичні і циклоаліфатичні вуглеводні, а також олії, зокрема рослинного походження, далі C1-C4-алкілові ефіри насичених або ненасичених кислот жирного ряду або суміші кислот жирного ряду, зокрема складні метилові ефіри, наприклад, метиловий ефір олеїнової кислоти, метиловий ефір стеаринової кислоти, метиловий ефір рапсової олії, а також парафінові мінеральні олії тощо. Типові допоміжні засоби включають поверхнево-активні речовини, зокрема, звичайно використовувані в засобах захисту рослин змочувальні агенти і диспергувальні (допоміжні) засоби, крім того, добавки, що змінюють в'язкість, (загущувачі, згущувачі), антиспінювачі, антифризи, засоби для регулювання значення pH, стабілізатори, засоби, що перешкоджають спіканню і біоциди (консерванти). Особливо винахід відноситься до засобів для захисту рослин в формі водного суспензійного концентрату (СК). Подібні суспензійні концентрати містять форму III відповідно IV фенілурацилу I в тонкодисперсній окремій формі, причому частинки форми III відповідно IV в водній фазі знаходяться в суспендованому стані. Розмір частинок діючої речовини, тобто розмір, який не перевищують 90 мас. % частинок діючої речовини, є звичайно менше 30 мкм, зокрема менше 20 мкм. Переважно, щонайменше, 40 мас. % і зокрема, щонайменше, 60 мас. % частинок в СК відповідно до винаходу мають діаметри менше 2 мкм. Поряд з діючою речовиною водні суспензійні концентрати звичайно містять поверхневоактивні речовини, а також, при необхідності, антиспінювачі, загущувачі (=згущувачі), антифризи, стабілізатори (біоциди), засоби для регулювання значення pH і засоби, що перешкоджають спіканню. В СК подібного роду, кількість діючої речовини, тобто загальна кількість фенілурацилу форм III і/або IV, а також, при необхідності, інших діючих речовин знаходиться звичайно в межах від 12 UA 99114 C2 5 10 15 20 25 30 35 40 45 50 55 60 10 до 70 мас. %, зокрема в межах від 20 до 50 мас. %, в перерахуванні на загальну вагу суспензійного концентрату. Як переважні поверхнево-активні речовини придатні аніонні і неіоногенні поверхнево-активні речовини. Придатними поверхнево-активними речовинами також є захисні колоїди. Кількість ПАР, як правило, складає від 0,5 до 30 мас.-%, зокрема від 1 до 20 мас.-%, в перерахуванні на загальну вагу водного СК відповідно до винаходу. Переважно поверхнево-активні речовини включають, щонайменше, одну аніонну поверхнево-активну речовину і, щонайменше, одну неіоногенну поверхнево-активну речовину, причому кількісне співвідношення аніонних до неіоногенних поверхнево-активних речовин, звичайно знаходиться в межах від 10:1 до 1:10. До прикладів аніонних поверхнево-активних речовин (ПАР) відносяться алкіларилсульфонати, фенілсульфонати, алкілсульфати, алкілсульфонати, алкілові ефіри сульфатів, алкіларильні ефіри сульфатів, алкілполігліколеві ефіри фосфатів, поліарилфенілові ефіри фосфатів, алкілсульфосукцинати, олефінсульфонати, парафінсульфонати, нафтові сульфонати, тауриди, саркозиди, жирні кислоти, алкілнафталінсульфокислоти, нафталінсульфокислоти, лігнінсульфонові кислоти, продукти конденсації сульфонованих нафталінів з формальдегідом або з формальдегідом і фенолом і, при необхідності, сечовиною, і також продукти конденсації з фенолсульфонової кислоти, формальдегіду і сечовини, лігнінсульфітні відпрацьовані луги і лігносульфонати, алкілфосфати, алкіларилфосфати, наприклад, тристирилфосфати, а також полікарбоксилати, такі як, наприклад, поліакрилати, співполімери ангідриду малеїнової кислоти/олефіну (наприклад, Sokalan CP9, BASF), включаючи солі лужних, лужноземельних металів, амонієві і амінові солі наведених вище речовин. Переважними аніонними поверхнево-активними речовинами є ті, які мають, щонайменше, одну сульфонатну групу, і зокрема їх солі лужних металів і їх амонієві солі. Приклади неіоногенних поверхнево-активних речовин включають алкілфенолалкоксилати, алкоксилати спиртів, алкоксилати жирних амінів, ефіри поліоксіетиленгліцерину і кислот жирного ряду, алкоксилати рицинової олії, алкоксилати кислот жирного ряду, алкоксилати жирних амідів, полідіетаноламіди кислот жирного ряду, етоксилати ланоліну, складні полігліколеві ефіри кислот жирного ряду, ізотридециловий спирт, аміди жирних кислот, метилцелюлоза, складні ефіри жирних кислот, алкілполіглікозиди і складні ефіри гліцерину і жирної кислоти, поліетиленгліколь, поліпропіленгліколь, поліетиленгліколь/поліпропіленгліколеві блокспівполімери, алкіловий ефір поліетиленгліколю, алкіловий ефір поліпропіленгліколю, блокспівполімери поліетиленгліколь/поліпропіленгліколевих ефірів (блокспівполімери поліетиленоксиду /поліпропіленоксиду) і їх суміші. Переважними неіоногенними поверхнево-активними речовинами є етоксилати жирних спиртів, алкілполіглікозиди, складні ефіри гліцерину і жирної кислоти, алкоксилати рицинової олії, алкоксилати кислот жирного ряду, алкоксилати жирних амідів, етоксилати ланоліну, полігліколеві ефіри кислот жирного ряду і блокспівполімери етиленоксиду/пропіленоксиду і їх суміші. Захисні колоїди звичайно представляють собою розчинні у воді амфіфільні полімери. Прикладами цих колоїдів є білки і денатуровані білки, такі як казеїн, полісахариди, такі як розчинні у воді похідні крохмалю, і похідні целюлози, зокрема гідрофобно модифіковані крохмалі і целюлози, крім того, полікарбоксилати, такі як поліакрилові кислоти і співполімери акрилових кислот, полівініловий спирт, полівінілпіролідон, співполімери вінілпіролідону, полівініламіни, поліетиленіміни і прості поліалкіленові ефіри. Для водних СК відповідно до винаходу добавками, що змінюють в'язкість, (загущувачами) придатні зокрема сполуки, які надають складові псевдопластичну плинність, тобто високу в'язкість в стані спокою і низьку в'язкість в рухомому стані. В принципі, придатні всі сполуки, використовувані для цієї цілі в суспензійних концентратах. Серед них слід назвати, наприклад, неорганічні речовини, такі як бентоніти або атапульгіти (наприклад, Attaclay фірми Engelhardt), і органічні речовини, такі як полісахариди і гетерополісахариди, такі як Xanthan Gum (Kelzan фірми Kelco), Rhodopol 23 (Rhone Poulenc) або Veegum (фірми R.T. Vanderbilt), причому переважно застосовують Xanthan Gum. Часто, кількість добавок, що змінюють в'язкість складає від 0,1 до 5 мас. %, в перерахуванні на загальну вагу СК. Як антиспінювачі для водних СК відповідно до винаходу придатні, наприклад, відомі для цієї цілі силіконові емульсії, (SilikonSRE, фірми Wacker, або Rhodorsil фірми Rhodia), довголанцюгові спирти, жирні кислоти і їх солі, піногасники типу водних воскових дисперсій, тверді піногасники (так звані компаунди), фторорганічні сполуки і їх суміші. Кількість антиспінювача складає звичайно від 0,1 до 1 мас. %, в перерахуванні на загальну вагу СК. Також для стабілізації до суспензійних концентратів відповідно до винаходу можна додати консерванти. Придатними консервантами є консерванти на основі ізотіазолонів, наприклад, 13 UA 99114 C2 5 10 15 20 25 30 35 40 45 50 55 60 Proxel фірми ICI або Acticide РТС фірми Thor Chemie або Kathon MK фірми Rohm & Haas. Кількість консервантів складає звичайно від 0,05 до 0,5 мас. %, в перерахуванні на загальну вагу СК. Придатними антифризами є рідкі поліоли, наприклад етиленгліколь, пропіленгліколь або гліцерин, а також сечовина. Кількість антифризу складає, як правило, від 1 до 20 мас. %, зокрема від 5 до 10 мас. %, в перерахуванні на загальну вагу суспензійного концентрату. При необхідності СК відповідно до винаходу можуть містити буфер для регулювання значення pH. Прикладами буферів є солі лужних металів і слабких неорганічних або органічних кислот, таких як, наприклад, фосфорна кислота, борна кислота, оцтова кислота, пропіонова кислота, лимонна кислота, фумарова кислота, винна кислота, щавлева кислота і бурштинова кислота. Оскільки препарати форми III відповідно IV використовуються для обробки посівного матеріалу, то вони можуть містити інші звичайні компоненти, такі як використовують для обробки посівного матеріалу, наприклад, для протравляння або покриття. Поряд з вказаними вище компонентами, до них зокрема відносяться барвники, клейкі речовини, наповнювачі і пластифікатори. Як барвники придатні всі для подібних цілей звичайні барвні речовини і пігменти. При цьому застосовують як малорозчинні у воді пігменти і розчинні у воді барвні речовини. Як приклади слід назвати барвні речовини і пігменти, відомі під назвами Rhodamin B, C. I. Пігмент червоний 112 і C.I. Сольвент червоний 1, Пігмент синій 15:4, Пігмент синій 15:3, Пігмент синій 15:2, Пігмент синій 15:1, Пігмент синій 80, Пігмент жовтий 1, Пігмент жовтий 13, Пігмент червоний 48:2, Пігмент червоний 48:1, Пігмент червоний 57:1, Пігмент червоний 53:1, Пігмент оранжевий 43, Пігмент оранжевий 34, Пігмент оранжевий 5, Пігмент зелений 36, Пігмент зелений 7, Пігмент білий 6, Пігмент коричневий 25, Основний фіолетовий 10, Основний фіолетовий 49, Кислотний червоний 51, Кислотний червоний 52, Кислотний червоний 14, Кислотний синій 9, Кислотний жовтий 23, Основний червоний 10, Основний червоний 108. Кількість барвника звичайно складає не більше ніж 20 мас. % композиції і переважно в межах від 0,1 до 15 мас. %, в перерахуванні на загальну вагу композиції. Як клейкі речовини придатні всі звичайно використовувані в протравлювальних засобах сполучні засоби. Приклади придатних сполучних засобів включають термопластичні полімери, такі як полівінілпіролідон, полівінілацетат, полівініловий спирт і тилез, крім того, поліакрилати, поліметакрилати, полібутени, поліізобутени, полістирол, поліетиленаміни, поліетиленаміди, захисні колоїди, наведені вище, поліестери, поліетерестери, поліангідриди, поліестеруретани, поліестераміди, термопластичні полісахариди, наприклад похідні целюлози, такі як складні ефіри целюлози, прості ефіри целюлози, етерестери целюлози, включаючи метилцелюлозу, етилцелюлозу, гідроксиметилцелюлозу, карбоксиметилцелюлозу, гідроксипропілцелюлозу і похідні крохмалю і модифіковані крохмалі, декстрини, мальтодекстрини, альгинати і хитозани, крім того жири, олії, білки, включаючи казеїн, желатин і зеїн, гуміарабік, шелак. Переважно клейкі речовини є сумісними з рослинами, тобто вони не мають ніякої ябо ніякої суттєвої фітотоксичної дії. Клейкі речовини переважно розкладаються біологічним шляхом. Переважно клейку речовину вибирають таким чином, що вона діє як матриця для активних компонентів композиції. Кількість клейкої речовини звичайно складає не більше ніж 40 мас. % композиції і переважно в межах від 1 до 40 мас. % і зокрема в межах від 5 до 30 мас. %, в перерахуванні на загальну вагу композиції. Поряд з клейкою речовиною препарат для обробки посівного матеріалу також може містити інертні наповнювачі. Прикладами наповнювачів є наведені вище тверді носії, зокрема тонкодисперсні неорганічні матеріали, такі як глина, крейда, бентоніт, каолін, тальк, перліт, слюда, силікагель, діатомова земля, кварцовий порошок, монтморилоніт, а також тонкодисперсні органічні матеріали, такі як деревне борошно, борошно зернових культур, активоване вугілля тощо. Кількість наповнювача переважно вибирають таким чином, що загальна кількість наповнювача не перевищує 75 мас. %, в перерахуванні на загальну вагу всіх нелетких компонентів композиції. Часто, кількість наповнювача знаходиться в межах від 1 до 50 мас. %, в перерахуванні на загальну вагу всіх нелетких компонентів композиції. Крім того, композиція для обробки посівного матеріалу може містити ще пластифікатор, який підвищує гнучкість покриття. Прикладами пластифікаторів є олігомерні поліалкіленгліколі, гліцерин, діалкілфталати, алкілбензилфталати, глікольбензоати і подібні сполуки. Кількість пластифікатора в покритті знаходиться часто в межах від 0,1 до 20 мас. %, в перерахуванні на загальну вагу всіх нелетких компонентів композиції. Винахід також особливо відноситься до засобу для захисту рослин у вигляді неводного суспензійного концентрату. Подібні суспензійні концентрати містять форму III відповідно форму 14 UA 99114 C2 5 10 15 20 25 30 35 40 45 50 55 60 IV фенілурацилу I в тонкодисперсній окремій формі, причому частинки форми III відповідно IV в неводній фазі знаходяться в суспендованому стані. Розмір частинок діючої речовини, тобто розмір, який не перевищують 90 мас. % частинок діючої речовини, є при цьому менше 30 мкм, зокрема менше 20 мкм. Переважно, щонайменше, 40 мас. % і зокрема, щонайменше, 60 мас. % частинок в неводних СК відповідно до винаходу мають діаметри менше 2 мкм. Неводні суспензійні концентрати поряд з діючою речовиною звичайно містять поверхневоактивні речовини, а також при необхідності антиспінювачі, загущувачі (= згущувачі), антифризи, стабілізатори (біоциди), засоби для регулювання значення pH і засоби, що запобігають спіканню. Кількість діючої речовини, тобто загальна кількість фенілурацилу I в формі III відповідно IV, а також при необхідності інших діючих речовин, в неводних СК звичайно знаходиться в межах від 10 до 70 мас.-%, зокрема в межах від 20 до 50 мас.-%, в перерахуванні на загальну вагу неводного суспензійного концентрату. Як поверхнево-активних речовини переважно придатні названі раніше аніонні і неіоногенні ПАР. Кількість поверхнево-активних речовин, як правило, складає від 1 до 30 мас.-%, зокрема від 2 до 20 мас.-%, в перерахуванні на загальну вагу неводного СК відповідно до винаходу. Переважно поверхнево-активні речовини включають щонайменше одну аніонну поверхневоактивну речовину і щонайменше одну неіоногенну поверхнево-активну речовину, причому кількісне співвідношення аніонної до неіоногенної поверхнево-активної речовини звичайно знаходиться в межах від 10: 1 до 1: 10. Відповідно до винаходу форми III і IV можуть також бути приготовлені у вигляді порошків, засобів для обпилювання і опудрювання. Подібні композиції можуть бути одержані шляхом змішування або спільного розмелу форми III відповідно IV з твердим носієм і при необхідності іншими допоміжними засобами. Відповідно до винаходу форма III і IV можуть також бути приготовлені у вигляді гранулятів, наприклад, покритих, просочених і гомогенних гранулятів. Подібні композиції можуть бути одержані шляхом зв'язування діючих речовин з твердими носіями. Твердими носіями є мінеральні землі, такі як кремнієві кислоти, силікагелі, силікати, тальк, каолін, вапняк, вапно, крейда, болюс, лес, глина, доломіт, діатомова земля, сульфат кальцію, сульфат магнію, оксид магнію, розмелені пластмаси, добрива, такі як сульфат амонію, фосфат амонію, нітрат амонію, сечовини і рослинні продукти, такі, як наприклад, борошно зернових культур, борошно деревної кори, деревне борошно і борошно горіхової шкарлупи, целюлозний порошок або інші тверді носії. Концентрації форми III відповідно IV в готових для застосування препаративних формах можуть варіюватися в широких межах. Загалом, препарати містять приблизно від 11 до 98 мас.%, переважно від 10 до 95 мас.-%, в перерахуванні на загальну вагу діючих речовин. Наведені нижче приклади препаративних форм пояснюють одержання таких композицій: I. 20 вагових частин форми III відповідно IV змішують з 3 ваговими частинами натрієвої солі діізобутилнафталінсульфонової кислоти, 17 ваговими частинами натрієвої солі лігнінсульфонової кислоти з сульфітного відпрацьованого лугу і 60 ваговими частинами порошкоподібного силікагелю і перемелюють в молотковому млині. Таким чином, одержують водно-дисперсійний порошок, який містить форму III відповідно IV. Тонким розподілом суміші в 20000 вагових частин води одержують розчин для обприскування, який містить 0,1 мас. % форми III відповідно IV. II. 3 вагові частини форми III відповідно IV змішують з 97 ваговими частинами тонкого каоліну. Таким чином, одержують засіб для розпилення, який містить 3 мас. % форми III відповідно IV. III. 20 вагових частин форми III відповідно IV ретельно перемішують з 2 ваговими частинами кальцієвої солі додецилбензолсульфонової кислоти, 8 ваговими частинами простого полігліколевого ефіру спиртів жирного ряду, 2 ваговими частинами натрієвої солі конденсату фенолу, сечовини і формальдегіду і 68 ваговими частинами парафінової мінеральної олії. Одержують стабільний неводний суспензійний концентрат форми III відповідно IV. IV. 10 вагових частин форми III відповідно IV приготовляли в розчині з 17 вагових частин блокспівполімеру полі(етиленгліколю)(пропіленгліколю), 2 вагових частин конденсату фенолсульфокислоти, формальдегіду і приблизно 1 вагової частини інших допоміжних засобів (загущувачі, піногасники) в суміші з 7 вагових частин пропіленгліколю і 63 вагових частин води у вигляді суспензійного концентрату. V. 30,5 вагових частин форми III відповідно IV приготовляли в розчині з 1 вагової частини блокспівполімеру полі(етиленгліколю)(пропіленгліколю), 1 вагової частини конденсату фенолсульфокислоти, формальдегіду і приблизно 1 вагової частини інших допоміжних засобів 15 UA 99114 C2 5 10 15 20 25 30 35 40 45 50 55 (загущувачі, піногасники) в суміші з 6 вагових частин пропіленгліколю і 61 вагової частини води у вигляді суспензійного концентрату. Нанесення форми III відповідно IV відповідно гербіцидних засобів, що їх містять відбувається, оскільки препаративна форма не є майже готовою до застосування, у вигляді водних рідин для обприскування. Їх приготовляють шляхом розведення з водою зазначених вище препаративних форм, що містять форму III відповідно IV фенілурацилу I. Рідини для обприскування можуть також містити інші компоненти в розчиненому, емульгованому або суспендованому вигляді, наприклад, добрива, діючі речовини інших груп гербіцидних або регулюючих ріст діючих речовин, інші діючі речовини, наприклад, діючі речовини для боротьби з тваринними шкідниками або фітопатогенними грибами відповідно бактеріями, далі мінеральні солі, які використовуються для усунення нестачі поживних речовин і мікроелементів, а також нефітотоксичні олії і олійні концентрати. Як правило, ці компоненти додають перед, під час або після розведення водою препаратів рідини для обприскування відповідно до винаходу. Нанесення форми III відповідно IV відповідно гербіцидних засобів, що їх містять може здійснюватися досходовим або післясходовим способом. Оскільки фенілурацил I є менш стерпним певними культурними рослинами, то можуть застосовуватися техніки нанесення, при яких гербіцидний засіб розприскується за допомогою розприскувальних пристроїв таким чином, що листя чутливих культурних рослин по можливості не піддаються обприскуванню, у той час, як діючі речовини попадають на листя зростаючих під ними небажаних рослин або на непокритий ґрунт, (метод спрямованого обприскування, відповідно, метод стрічкового обприскування). Норми витрати форми III відповідно IV залежно від цілі обробки, пори року та стадії росту складають від 0,001 до 3,0, переважно, від 0,01 до 1,0 кг/га активної субстанції (а. с.). Для розширення спектру дії і одержання синергічного ефекту або для підвищення селективності форми III і IV можуть змішуватися і спільно вноситися з численними представниками інших гербіцидних і регулюючих ріст груп діючих речовин або з сафенерами. Форми III і IV можуть, наприклад, по аналогії з в WO2003/024221, WO 2004/080183, WO 2006/097509 і WO 2007/042447 описаними сумішами фенілурацилів I застосовуватися відповідно, наноситися з гербіцидами, регуляторами росту і/або сафенерами. Наприклад, як реагенти суміші придатні 1,2,4-тіадіазоли, 1,3,4-тіадіазоли, аміди, амінофосфорна кислота і її похідні, амінотріазоли, аніліди, арилокси-гетероарилоксиалканові кислоти і їх похідні, бензойна кислота і її похідні, бензотіадіазинони, 2-(гетароїл/ароїл)-1,3– циклогександіони, гетероарил-арил-кетони, бензилізоксазолідинони, похідні мета-CF3-фенілу, карбамати, хінолінкарбонова кислота і її похідні, хлорацетаніліди, похідні циклогексеноноксимового ефіру, діазини, дихлорпропіонова кислота і її похідні, дигідробензофурани, дигідрофуран-3-они, динітроаніліни, динітрофеноли, дифенілові ефіри, дипіриділи, галогенкарбонові кислоти і їх похідні, сечовини, 3-фенілурацили, імідазоли, імідазолінони, N-феніл-3,4,5,6-тетрагідрофталіміди, оксадіазоли, оксирани, феноли, складні ефіри арилокси- і гетероарилоксифеноксипропіонової кислоти, фенілоцтова кислота і її похідні, 2-фенілпропіонова кислота і її похідні, піразоли, фенілпіразоли, піридазини, піридинкарбонова кислота і її похідні, піримідилові ефіри, сульфаміди, сульфонілсечовини, тріазини, тріазинони, тріазолінони, тріазолкарбоксаміди і урацили. Придатними сафенерами є, наприклад, (хінолін-8окси)оцтові кислоти, 1-феніл-5-галоалкіл-1H-1,2,4-тріазол-3-карбонові кислоти, 1-феніл-4,5дигідро-5-алкіл-1H-піразол-3,5-дикарбонові кислоти, 4,5-дигідро-5,5-діарил-3-ізоксазолкарбонові кислоти, дихлорацетаміди, альфа-оксімінофенілацетонітрили, ацетофеноноксими, 4,6-дигало-2фенілпіримідини, аміди N-[[4-(амінокарбоніл)феніл]сульфоніл]-2-бензойної кислоти, ангідрид 1,8-нафталевої кислоти, 2-гало-4-(галоалкіл)-5-тіазолкарбонові кислоти, фосфортиолати і Nалкіл-O-фенілкарбамати, а також їх застосовні в сільському господарстві солі, і при умові, що вони мають кислотну функцію, їх застосовні в сільському господарстві похідні, такі як аміди, складні ефіри і складні тіоефіри. Крім того, може бути корисним, змішувати форму III відповідно IV окремо або в комбінації з іншими гербіцидами і/або сафенерами, а також ще з іншими засобами для захисту рослин, спільно вносити, наприклад, з засобами для боротьби зі шкідливими грибами або фітопатогенними грибами відповідно бактеріями. Далі представляє інтерес здатність змішуватися з мінеральними розчинами, які використовуються для усунення нестачі поживних речовин і мікроелементів. Також можуть бути додані нефітотоксичні олії і олійні концентрати. Гербіцидну дію форм III і IV можна показати за допомогою наступних експериментів у теплиці: 16 UA 99114 C2 5 10 15 20 25 Як ємності для вирощування використовували пластикові горщики з глинистим піском із прибл. 3,0 % гумусу як субстрату. Насіння рослин, які тестують, висівали розділеними за видами. При досходовій обробці концентрати діючої речовини, розведені водою до бажаної концентрації застосування, були внесені одразу після висівання за допомогою тонко розподілювальних розпилювачів. Ємності злегка зросили, щоб сприяти проростанню і росту, і потім накрили прозорими пластиковими ковпаками, до тих пір, поки рослини не виросли. Це покриття сприяло рівномірному проростанню досліджуваних рослин, якщо вони не були ушкоджені діючими речовинами. Для цілей післясходової обробки досліджувані рослини залежно від форми росту спочатку підростали до висоти від 3 до 15 см і тільки потім обробляли суспендованими у воді діючими речовинами. Досліджувані рослини або безпосередньо висаджували і вирощували у тих же ємностях, або спочатку вони виростали окремо як паростки і за декілька днів до обробки їх пересаджували в ємності для дослідів. Рослини витримували відповідно до видів при температурі від 10-25 °C або 20-35 °C. Період експерименту складав від 2 до 4 тижнів. Протягом цього часу рослини доглядали, і відзначали їх реакцію на окремі обробки. Оцінювання проводилось за шкалою від 0 до 100. При цьому 100 означає, що рослина не зійшла або повне знищення, щонайменше, надземних частин і 0 означає відсутність ушкодження або нормальну динаміку росту. Відповідно до зазначених вище методів в тепличному тесті порівнювали форми III і IV відповідно до винаходу і як порівняльну сполуку відому з заявки WO 01/83459 форму I, в кожному випадку приготовлені у вигляді водного суспензійного концентрату (СК; 100 г/л), при ® необхідності з додаванням 1 л/га Rustica Öl . Суспензійні концентрати мали наступний склад: Фенілурацил I 100 г/л 1,2-пропіленгліколь 70 г/л Диспергатор I 167 г/л Диспергатор II 20 г/л Xanthan Gum 3 г/л Біоцид 1,8 г/л Вода до 1 л Диспергатор I: ЕО/ПО-блокспівполімер Диспергатор II: продукт конденсації фенолсульфокислоти-формальдегіду Використовувані в тепличних дослідах рослини складались з наступних видів: Латинська назва Amaranthus retroflexus Ambrosia elatior Capsella bursa-pastoris Chenopodium album Euphorbia heterophylla Galium aparine Glycine max Helianthus annuus Hordeum vulgare Kochia scoparia Matricaria inodora Mercurialis annua Polygonum convolvulus Salsola kali ssp. ruthenica Secale cereale Sinapis arvensis Sonchus arvensis Stellaria media Thlaspi arvense Triticum aestivum Veronica hederaefolia Veronica persicaria Viola arvensis Загальна назва Щириця запрокинута Амброзія полинолиста Грицики звичайні Лобода біла Молочай різнолистяний Підмаренник чіпкий Соя звичайна Соняшник однорічний Ячмінь яровий або ячмінь озимий Віниччя справжнє Ромашка непахуча Переліска однорічна Гірчак березкоподібний Солянка російська Жито посівне Гірчиця польова Осот жовтий польовий Зірочник середній Талабан польовий Пшениця м'яка Вероніка плющолиста Вероніка перська Фіалка польова 17 UA 99114 C2 Таблиця 4 Порівняння гербіцидної ефективності форми III з відомою з WO 01/83459 формою I при досходовому способі (теплиця) Досліджувані рослини Норма витрати (г/га а. с.) Діюча речовина форма III модифікація I Ушкодження [%] Корисні рослини: Glycine max Шкідливі рослини: Stellaria media Ambrosia elatior Helianthus annuus Euphorbia heterophylla Mercurialis annua 25 12,5 30 20 70 30 12,5 12,5 12,5 12,5 6,25 6,25 70 80 75 100 90 65 65 60 70 95 40 40 Таблиця 5 Порівняння гербіцидної ефективності форми III з відомою з WO 01/83459 форма I ® в післясходовому способі з додаванням 1 л/га Rustica Öl (теплиця) Досліджувані рослини Корисні рослини: Hordeum vulgare (ярова) Норма витрати (г/га а. с.) Діюча речовина форма III форма I Ушкодження [%] Triticum aestivum 20 20 15 20 15 10 20 5 5 5 5 0 0 10 15 20 15 15 10 10 15 Шкідливі рослини: Chenopodium album Galium aparine Matricaria inodora Polygonum convolvulus Veronica hederaefolia Veronica persicaria Viola arvensis 15 15 5 15 15 15 5 80 100 100 100 70 100 100 70 75 65 70 50 70 40 Hordeum vulgare (озима) Secale cereale 18 UA 99114 C2 Таблиця 6 Порівняння гербіцидної ефективності форми III з відомою з WO 01/83459 формою I в післясходовому способі (теплиця) Досліджувані рослини Норма витрати (г/га а. с.) Діюча речовина форма III форма I Ушкодження [%] Корисні рослини: Hordeum vulgare (озима) Secale cereale Triticum aestivum 0 5 5 5 15 10 Шкідливі рослини: Amaranthus retroflexus Capsella bursa-pastoris Kochia scoparia Matricaria inodora Salsola kali ssp. ruthenica Sinapis arvensis Sonchus arvensis Thlaspi arvense Veronica persicaria Viola arvensis 5 15 20 20 10 15 20 15 20 10 15 10 15 15 100 70 100 100 100 60 100 100 100 100 40 20 45 65 80 50 60 30 40 40 Результати тестів чітко показують, що форма III відповідно до винаходу відносно відомої форми I краще переноситься культурними рослинами при одночасній чітко покращеній гербіцидної ефективності. ФОРМУЛА ВИНАХОДУ 10 15 20 25 30 35 1. Кристалічні гідрати 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2Н)піримідиніл]-4-фтор-N-[[метил-(1-метилетил)аміно]сульфоніл]бензаміду, що містять від 0,8 до 1,2 моль води, в перерахуванні на 1 моль 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4(трифторметил)-1-(2Н)-піримідиніл]-4-фтор-N-[[метил-(1-метилетил)аміно]сульфоніл]бензаміду. 2. Гідрати за п. 1 з піком плавлення в межах від 100 до 140 °C. 3. Гідрат за одним з попередніх пунктів з вмістом 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4(трифторметил)-1-(2Н)-піримідиніл]-4-фтор-N-[[метил-(1-метилетил)аміно]сульфоніл]бензаміду щонайменше 94 мас. %, в перерахуванні на загальну кількість органічних компонентів, що містить гідрат. 4. Гідрат (а) за одним з попередніх пунктів, який в рентгенівській порошковій дифрактограмі при 25 °C і Сu-К-випромінюванні показує щонайменше одне відображення при 2-значенні 11,6±0,2°. 5. Гідрат за п. 4, який додатково показує щонайменше три з наступних, наведених як 2значення, відображень: 5,1±0,2°, 10,1±0,2°, 10,8±0,2°, 13,9±0,2°, 15,1±0,2°, 16,1±0,2°, 17,9±0,2°, 20,2±0,2°, 24,5±0,2°. 6. Гідрат (b) за одним з пп. 1-3, який в рентгенівській порошковій дифрактограмі при 25 °C і СuК-випромінюванні показує щонайменше одне відображення при 2-значенні 12,1±0,2°. 7. Гідрат за п. 5, який додатково показує щонайменше три з наступних, наведених як 2значення, відображень: 5,2±0,2°, 10,2±0,2°, 10,9±0,2°, 14,0+0,2°, 14,6±0,2°, 15,3±0,2°, 19,2±0,2°, 19,9±0,2°, 20,5±0,2°, 24,7±0,2°, 26,7±0,2°, 27,8±0,2°. 8. 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2Н)-піримідиніл]-4-фтор-N[[метил-(1-метилетил)аміно]сульфоніл]бензамід, що містить щонайменше 90 мас. % гідрату за одним з попередніх пунктів. 9. Спосіб одержання гідрату за одним з пп. 1-7, який включає кристалізацію з розчину 2-хлор-5[3,6-дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2Н)-піримідиніл]-4-фтор-N-[[метил-(1метилетил)аміно]сульфоніл]бензаміду в органічному розчиннику в присутності води, причому органічний розчинник вибраний з групи, яка включає діалкілкетони з С 3-5-атомами, С1-С4 19 UA 99114 C2 5 10 15 алканоли, С2-С3алкіленглікольмоно-С1-С4-алкілові ефіри, ді-(С2-С3-алкіленгліколь-моно-С1-С4алкілові ефіри, тетрагідрофуран і суміші цих розчинників. 10. Спосіб одержання гідрату за одним з пп. 1-7, який включає суспендування аморфного 2хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2Н)-піримідиніл]-4-фтор-N-[[метил(1-метилетил)-аміно]сульфоніл]бензаміду у воді або водомісткому органічному розчиннику, причому органічний розчинник вибраний з групи, яка включає діалкілкетони з С 3-5-атомами, С1С4-алканоли, С2-С3-алкіленглікольмоно-С1-С4-алкілові ефіри, ді-(С2-С3-алкіленгліколь-моно-С1С4-алкілові ефіри, тетрагідрофуран і суміші цих розчинників. 11. Гербіцид, що містить гідрат за одним з пп. 1-7 і звичайні допоміжні засоби для приготування засобів для захисту рослин. 12. Гербіцид за п. 11 у вигляді водного суспензійного концентрату. 13. Гербіцид за п. 11 у вигляді неводного суспензійного концентрату. 14. Гербіцид за п. 11 у вигляді здатного до диспергування в воді порошку або грануляту. 15. Спосіб боротьби з небажаним ростом рослин, який відрізняється тим, що гідратом 2-хлор5-[3,6-дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2Н)-піримідиніл]-4-фтор-N-[[метил-(1метилетил)аміно]сульфоніл]бензаміду за одним з пп. 1-7 впливають на рослини, їх життєвий простір і/або насіння. Комп’ютерна верстка М. Ломалова Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 20
ДивитисяДодаткова інформація
Назва патенту англійськоюCrystalline hydrates of 2-chloro-5-[3,6-dihydro-3-methyl-2,6-dioxo-4-(trifluoro-methyl)-1-(2h)-pyrimidinyl]-4-fluoro-n-[[methyl-(1-methylethyl)-amino]sulphonyl]benzamide, processes for the preparation thereof, herbicide comprising thereof and method for control of undesired plant growth
Автори англійськоюSchmidt Thomas, Gebhardt Joachim, Loehr Sandra, Keil Michael, Wevers Jan Hendrik, Erk, Peter, Saxell, Heidi, Emilia, Hamprecht, Gerhard, Seitz Werner, Mayer, Guido, Wolf, Bernd, Cox, Gerhard, Michel, Alfred, Zagar Cyrill, Reinhard Robert, Sievernich Bernd
Назва патенту російськоюКристаллические гидраты 2-хлор-5-[3,6-дигидро-3-метил-2,6-диоксо-4-(трифторметил)-1-(2н)-пиримидинил]-4-фтор-n-[[метил-(1-метилетил)амино]сульфонил]бензамида, способы получения гидрата, гербицид, содержащий гидрат, и способ борьбы с нежелательным ростом растений
Автори російськоюШмидт Томас, Гебхардт Йоахим, Льор Сандра, Кайль Михаэль, Веверс Ян Хендрик, Эрк Петер, Закселль Хайди Эмилия, Хампрехт Герхард, Зайтц Вернер, Майер Гуидо, Вольф Бернд, Кокс Герхард, Михель Альфред, Цагар Сирилл, Райнхард Роберт, Зиверних Бернд
МПК / Мітки
МПК: C07D 239/54, A01P 13/00, A01N 43/48
Мітки: гідрати, способи, 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2н)-піримідиніл]-4-фтор-n-[[метил-(1-метилетил)аміно]сульфоніл]бензаміду, містить, гідрат, гідрату, одержання, гербіцид, кристалічні
Код посилання
<a href="https://ua.patents.su/22-99114-kristalichni-gidrati-2-khlor-5-36-digidro-3-metil-26-diokso-4-triftormetil-1-2n-pirimidinil-4-ftor-n-metil-1-metiletilaminosulfonilbenzamidu-sposobi-oderzhannya-gidratu-gerbicid-sh.html" target="_blank" rel="follow" title="База патентів України">Кристалічні гідрати 2-хлор-5-[3,6-дигідро-3-метил-2,6-діоксо-4-(трифторметил)-1-(2н)-піримідиніл]-4-фтор-n-[[метил-(1-метилетил)аміно]сульфоніл]бензаміду, способи одержання гідрату, гербіцид, що містить гідрат,</a>
Попередній патент: Рідка пестицидна композиція, що містить n-фенілсемікарбазонові пестицидні сполуки
Наступний патент: Водна композиція, що твердне, спосіб її одержання, спосіб скріплення нетканих волокон, скріплений зв’язуючим нетканий виріб та теплоізоляція будівель
Випадковий патент: Спосіб та проміжні сполуки для одержання похідних заміщеного хроманолу