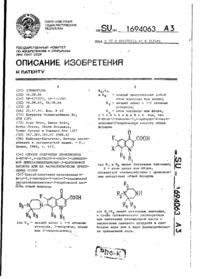
Гідрати 7-[7-(s)-аміно-5-азаспіро[2,4]гептан-5-іл]-8-хлор-6-фтор-1-[(1r,2s)-2-фторциклопропіл]-4-оксо-1,4-дигідрохінолін-3-карбонової кислоти, спосіб їх одержання і фармацевтична композиція
Номер патенту: 41312
Опубліковано: 17.09.2001
Автори: Міката Норімаса, Утіяма Кейдзі, Уємура Тазуо, Юкімото Юзуке, Кімура Іуіті, Кавакамі Кацухіро
Формула / Реферат
1. Способ селективного получения 3/2 гидрата 7-[7-(S)амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты, который включает обработку 7-[7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1 R, 2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-З-карбоновой кислоты в водном растворителе, где минимальное содержание воды в данном водном растворителе составляет, по крайней мере, 40% при 25°С и, по крайней мере, 90% при 60°С, или перекристаллизацию 7-[7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты из водного растворителя, где содержание воды в упомянутом водном растворителе составляет от 50% до 100%, предпочтительно от 50% до 75%.
2. Способ по п. 1 селективного получения 3/2 гидрата 7-[7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты, который включает обработку 7-[7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1 -[(1R,2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты в водном растворителе, где минимальное содержание воды в данном водном растворителе составляет, по крайней мере, 40% при 25 °С и, по крайней мере, 90% при 60°С.
3. Способ по п. 1 селективного получения 3/2 гидрата 7-[7-(S)- амино - 5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R, 2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-З-карбоновой кислоты, который включает перекристаллизацию 7-[7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты из водного растворителя, где содержание воды в упомянутом водном растворителе составляет от 50% до 100%, предпочтительно от 50% до 75%.
4. Способ по п.п. 1, 2 или 3, отличающийся тем, что указанный водный растворитель является этанолом, содержащим водный аммиак.
5. Безводная 7-[7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1 -[(1R,2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-З-карбоновая кислота.
6. 3/2 гидрат 7-[7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1 - [(1R,2S)-2-фторциклопропил] -4-оксо-1,4-дигидрохинолин-З - карбоновой кислоты в кристаллической форме, которая, по существу, имеет следующие характеристики дифракции рентгеновских лучей:
Значение d (постоянные решетки) Относительная интенсивность .
(А)
11,47
Слабая
10,49
Сильная
9,69
Слабая
7,12
Исключительно слабая
6,87
Сильная
6,23
Сильная
5,68
Слабая
5,25
Сильная
4,90
Исключительно сильная
4,71
Исключительно слабая
4,61
Слабая
4,25
Слабая
4,15
Исключительно слабая
4,01
Сильная
3,85
Исключительно слабая
3,80
Исключительно слабая
3,74
Исключительно слабая
3,69
Слабая
3,58
Слабая
3,50
Слабая
3,46
Слабая
3,39
Слабая
3,34
Слабая
3,29
Слабая
3,17
Слабая
7. Фармацевтическая композиция, включающая в качестве активного ингредиента терапевтически эффективное количество безводной 7-[7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1 -[(1 R, 2S)-2-фторциклопропил] -4-оксо-1,4-дигидрохинолин-З-карбоновой кислоты.
8. Безводная 7-[7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1 -[(1R, 2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-З -карбоновая кислота по п. 5 полезная для получения фармацевтической композиции для лечения бактериальных инфекций.
Текст
1. Способ селективного получения 3/2 гидрата 7-[7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор6-фтор-1-[(1R,2S)-2-фторциклопропил]-4-оксо-1,4дигидрохинолин-3-карбоновой кислоты, который включает обработку 7-[7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2фторциклопропил]-4-оксо-1,4-дигидрохинолин-3карбоновой кислоты в водном растворителе, где минимальное содержание воды в данном водном растворителе составляет, по крайней мере, 40% при 25°С и, по крайней мере, 90% при 60°С, или перекристаллизацию 7-[7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2фторциклопропил]-4-оксо-1,4-дигидрохинолин-3карбоновой кислоты из водного растворителя, где содержание воды в упомянутом водном растворителе составляет от 50% до 100%, предпочтительно от 50% до 75%. 2. Способ по п. 1 селективного получения 3/2 гидрата 7-[7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8хлор-6-фтор-1-[(1R,2S)-2-фторциклопропил]-4оксо-1,4-дигидрохинолин-3-карбоновой кислоты, который включает обработку 7-[7-(S)-амино-5азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R, 2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты в водном растворителе, где минимальное содержание воды в данном водном растворителе составляет, по крайней мере, 40% при 25°С и, по крайней мере, 90% при 60°С. 3. Способ по п. 1 селективного получения 3/2 гидрата 7-[7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8хлор-6-фтор-1-[(1R,2S)-2-фторциклопропил]-4оксо-1,4-дигидрохинолин-3-карбоновой кислоты, который включает перекристаллизацию 7-[7-(S)амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор 41312 7. Фармацевтическая композиция, включающая в качестве активного ингредиента терапевтически эффективное количество безводной 7-[7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1[(1R,2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты. 8. Безводная 7-[7-(S)-амино-5-азаспиро[2,4]гептан5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота по п. 5, полезная для получения фармацевтической композиции для лечения бактериальных инфекций. Это изобретение относится к кристаллам, содержащим кристаллизационную воду (далее упоминается как гидратная форма или просто гидрат), и к кристаллам без кристаллизационной воды (далее упоминаемым как безводная форма или просто безводные), к способу селективного получения этих кристаллов, и, кроме того, к фармацевтическим препаратам, содержащим такую кристаллическую форму. Производное хинолина, представленное формулой (І): Соответственно, данное изобретение относится к способу селективного получения 3/2 гидрата соединения (І), который включает обработку 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор6-фтор-1-[(1R,2S)-2-фторциклопропил]-4-оксо-1,4дигидрохинолин-3-карбоновой кислоты в водном растворителе или в воде, или перекристаллизацию соединения (І) из водного растворителя или воды. Данное изобретение относится к способу селективного получения 3/2 гидрата соединения (І), который включает обработку 7-[(7-(S)-амино-5азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R, 2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты в водном растворе или в воде. Данное изобретение относится к способу селективного получения 3/2 гидрата соединения (I), который включает перекристаллизацию 7-[(7-(S)амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор1-[(1R,2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты из водного растворителя или воды. Данное изобретение относится также к указанным выше способам, где водным растворителем является водный раствор этанола, содержащий аммиак. Данное изобретение относится также к 3/2 гидрату 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5ил]-8-хлор-6-фтор-1-[(1R,2S)-2-фторциклопропил]4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты. Данное изобретение относится также к безводной 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5ил]-8-хлор-6-фтор-1-[(1R,2S)-2-фторциклопропил]4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты. Данное изобретение относится также к кристаллическому 3/2 гидрату 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2фторциклопропил]-4-оксо-1,4-дигидрохинолин-3карбоновой кислоты, который, в основном, имеет следующие характеристики дифракции рентгеновских лучей: O F COOH (I) N N Cl H2N F то есть, 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор6-фтор-1-[(1R,2S)-2-фторциклопропил]-4-оксо-1,4дигидрохинолин-3-карбоновая кислота (далее упоминаемая как соединение (І)), имеет высокую антимикробную активность, с превосходной безопасностью (EP-A-0341493 или JP-A-2-231475; где термин JP-A, в том виде, как он используется, означает ("не прошедшая экспертизу опубликованная заявка на патент Японии") и, как ожидается, должно быть превосходным синтетическим антимикробным агентом. Обнаружено, что соединение (І) может существовать в форме нескольких видов гидратных форм, иных чем 1/4 (0,25) гидрат, таких как 1/2 (0,5) гидрат (т.е. полугидрат), 1 гидрат (т.е., моногидрат) и 3/2 (1,5) гидрат (т.е. сесквигидрат). Обнаружено также, что в дополнение к этим гидратам, существует также безводная форма. Гидратная форма соединения (І) включает различные типы кристаллов, имеющих различное число молекул кристаллизационной воды. В зависимости от условий кристаллизации или перекристаллизации в целевых кристаллах образуются, различные типы гидратов, и такие кристаллы являются непригодными в качестве основного материала для твердых фармацевтических препаратов. В результате широких исследований, авторы данного изобретения обнаружили, что возможно селективное получение кристаллов, как гидратов, так и безводных, соединения (І) путем контроля условий кристаллизации или перекристаллизации. Данное изобретение полностью основывается на этом обнаруженном факте. Значение d (постоянные решетки) (А) 11,47 10,49 9,69 7,12 6,87 6,23 5,68 5,25 4,90 4,71 4,61 4,25 2 Относительная интенсивность Слабая Сильная Слабая Исключительно слабая Сильная Сильная Слабая Сильная Исключительно сильная Исключительно слабая Слабая Слабая 41312 Значение d (постоянные решетки) (А) 4,15 4,01 3,85 3,74 3,69 3,58 3,50 3,46 3,39 3,34 3,29 3,17 состоит во введении терапевтически эффективного количества 3/2 гидрата 7-[(7-(S)-амино-5азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S) -2-фторциклопропил]-4-оксо-1,4-дигидрохинолин3-карбоновой кислоты. Данное изобретение относится также к способу лечения бактериальных инфекций, который состоит во введении терапевтически эффективного количества 3/2 гидрата 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R, 2S)-2фторциклопропил]-4-оксо-1,4-дигидрохинолин-3карбоновой кислоты, который имеет следующие характеристики дифракции рентгеновских лучей: Относительная интенсивность Исключительно слабая Сильная Исключительно слабая Исключительно слабая Слабая Слабая Слабая Слабая Слабая Слабая Слабая Слабая Значение d (постоянОтносительная ные решетки) (А) интенсивность 11,47 Слабая 10,49 Сильная 9,69 Слабая 7,12 Исключительно слабая 6,87 Сильная 6,23 Сильная 5,68 Слабая 5,25 Сильная 4,90 Исключительно сильная 4,71 Исключительно слабая 4,61 Слабая 4,25 Слабая 4,15 Исключительно слабая 4,01 Сильная 3,85 Исключительно слабая 3,80 Исключительно слабая 3,74 Исключительно слабая 3,69 Слабая 3,58 Слабая 3,50 Слабая 3,46 Слабая 3,39 Слабая 3,34 Слабая 3,29 Слабая 3,17 Слабая Данное изобретение относится, далее, к фармацевтическим композициям, содержащим моногидрат или безводное соединение, указанное выше. Данное изобретение относится к антибактериальному агенту, содержащему в качестве активного ингредиента терапевтически эффективное количество 3/2 гидрата 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2фторциклопропил]-4-оксо-1,4-дигидрохинолин-3карбоновой кислоты. Данное изобретение также относится к антибактериальному агенту, содержащему в качестве активного ингредиента терапевтически эффективное количество 3/2 гидрата 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2фторциклопропил]-4-оксо-1,4-дигидрохинолин-3карбоновой кислоты, который имеет следующие характеристики дифракции рентгеновских лучей: Значение d (постоянОтносительная ные решетки) (А) интенсивность 11,47 Слабая 10,49 Сильная 9,69 Слабая 7,12 Исключительно слабая 6,87 Сильная 6,23 Сильная 5,68 Слабая 5,25 Сильная 4,90 Исключительно сильная 4,71 Исключительно слабая 4,61 Слабая 4,25 Слабая 4,15 Исключительно слабая 4,01 Сильная 3,85 Исключительно слабая 3,80 Исключительно слабая 3,74 Исключительно слабая 3,69 Слабая 3,58 Слабая 3,50 Слабая 3.46 Слабая 3,39 Слабая 3,34 Слабая 3,29 Слабая 3,17 Слабая Краткое описание иллюстраций Фиг. 1 представляет пример спектра дифракции рентгеновских лучей 3/2 гидрата соединения (І). Фиг. 2 представляет пример спектра дифракции рентгеновских лучей 1/2 гидрата соединения (І). Фиг. 3 представляет пример спектра дифракции рентгеновских лучей безводного соединения (І). Фиг. 4 представляет пример спектра дифракции рентгеновских лучей моногидрата соединения (І). Прежде всего, авторы изучили кристаллы соединения (І) и, как результат, обнаружили, что они существуют как в безводной так и гидратных формах, включая 1/2 гидраты, 1 гидраты и 3/2 гидраты, в дополнение к 1/4 гидрату. С точки зрения промышленного производства кристаллов, 3/2 гидрат является предпочтительным, как из-за его физико-химической стабильности, так и из-за выхода продукта и легкости подбора условий производства при производстве основного материала для фармацевтических применений. С другой стороны, безводная форма подходит из-за скорости растворения сама по себе и в таблетках. Каждый из гидратов и безводная форма соединения (І) данного изобретения дает структуру Далее, данное изобретение относится к способу лечения бактериальных инфекций, который 3 41312 спектра, показанную на фигурах, и имеет достаточно характерную структуру спектра дифракции рентгеновских лучей порошков, представленную в последующих примерах. Термин "достаточно характерная" означает, что структура спектра каждого из кристаллов не ограничивается той, которая представлена на прилагаемых фигурах и таблицах, но включает ошибки в определении постоянной решетки (значения d) и интенсивности, обычно приемлемые в этой области. Обнаружено, что может образовываться более, чем один кристаллический гидрат при различных условиях получения гидрата. В частности, 1/2 гидрат получается, как загрязнение при получении 3/2 гидрата. Такая смесь гидратов является непригодной в качестве основного материала для фармацевтических препаратов. Таким образом, авторы изучили способ селективного получения кристаллов соединения (І), содержащих исключительно единственный гидрат или единственную безводную форму. Авторы исследовали стабильность кристаллов соединения (І) в водном растворителе или в воде следующим образом. Эквивалентные количества 1/2 гидрата и 3/2 гидрата смешивают и добавляют к смеси водный растворитель. Смесь перемешивают при различных температурах и, после заданного периода времени, анализируют пропорцию гидратов в общем количестве кристаллов. Во время перемешивания смесь находится в суспендированном состоянии, а именно, в состоянии мутной взвеси. В качестве водного растворителя используют водный раствор этанола, имеющий содержание воды (определяемое ниже) между 0% и 100%. Обнаружено также, что водный раствор этанола, содержащий, кроме того, от 1% до 28% водного раствора аммиака, повышает растворимость кристаллов и ускоряет превращения одной формы гидрата в другую. Растворитель используют в количестве от 15 мл до 30 мл на 1 г кристаллов. Содержание воды в используемом растворителе выражают в терминах объемного отношения до смешивания. Например, водный раствор этанола, имеющий содержание воды 60%, означает смесь этанола и воды с объемным соотношением 4:6, и водный раствор этанола, имеющий содержание воды 60%, содержащий 1% водного раствора аммиака, является смесью, содержащей этанол, воду и 28% водный раствор аммиака в объёмном отношении 40:59:1. Перемешивание продолжают в течение 3 дней при температуре 25°С или 45°С. Период времени в 3 дня не является обязательным для превращения кристаллов, и показано, что превращение завершается в течение примерно одного дня. Результаты этих экспериментов показывают, что виды кристаллов, существующих в смеси, могут изменяться в зависимости от температуры, содержания воды в растворителе, и от времени. Более подробно, (і) 14-часовая обработка при температуре кипения растворителя дает только безводную форму при содержании воды 5% или менее, только 1/2 гидрат при содержании воды 50%, и смесь 1/2 гидрата 3/2 гидрата при содержании воды 75% или более; (іі) 3-х дневная обработка при 45°С дает только 3/2 гидрат при содер жании воды 50% или более, и смесь 1/2 гидрата и 3/2 гидрата при содержании воды 45% или менее; и (і іі) 3-х дневная обработка при 25°С дает только 3/2 гидрат при содержании воды 40% или более и смесь 1/2 гидрата и 3/2 гидрата при содержании воды в 25% или менее. Эти результаты показывают, что 3/2 гидрат может быть получен в виде единственного вещества путем обработки в растворителе, имеющем содержание воды 50% или более, когда температура составляет 45°С; или в растворителе, имеющем содержание воды 40% или более, когда температура составляет 25°С. Термин "обработка", как он здесь используется, означает непрерывнoe перемешивание смеси кристаллов и растворителя в виде мутной взвеси при указанной выше температуре в течение указанного выше периода. Взвесь кристаллов может быть получена либо путем только одного растворения кристаллов с последующей кристаллизацией, либо простым смешиванием кристаллов и растворителя. Растворитель, который может быть использован в данном изобретении, не является специально ограниченным, до тех пор, пока кристаллы могут растворяться в растворителе и растворитель является смешиваемым с водой. Иллюстративные примеры растворителя включают низкоатомные спирты, такие как метанол, этанол и пропанол, и ацетон, среди которых этанол является предпочтительным. В дополнение, вода сама по себе может быть использована в качестве растворителя. Авторы обнаружили также, что кристаллы, состоящие только из 3/2 гидрата, могут быть селективно получены путем перекристаллизации, которая служит в качестве условий при начале кристаллизации в описанных выше условиях, которые дают возможность только 3/2 гидрату существовать в виде взвеси. Термин "при начале кристаллизации" используют здесь для обозначения точки, до которой вся предварительная обработка перед образованием кристаллов, например, растворение исходных кристаллов в растворителе и, если желательно, воздействие на раствор путем обработки активированным углем, концентрирование и тому подобное, является законченной. Авторы также достигли цели в установлении способа получения 1/2 гидрата, безводной формы или 1 гидрата в виде монокристаллов путем перекристаллизации или обработки растворителя подобным способом. Например, 1 гидрат соединения (І) может быть получен путем обработки при примерно 25°С в водном растворе метанола, имеющего содержание воды 1% или менее, и безводная форма может быть получена путем обработки в этаноле, содержащем 15% (вес/вес) аммиака. Следующие методики являются примерами селективного получения гидратов и безводной формы соединения (І). А) Способ получения безводной формы: Смесь неочищенных кристаллов соединения (І), которые могут быть получены по способу патента EP-A-0341493, и водный раствор этанола или водный раствор метанола нагревают с обратным холодильником при перемешивании в состоянии мутной взвеси в течение от 0,5 часа до 8 4 41312 часов. Содержание воды в водном растворе метанола или этанола составляет менее, чем 5% (объем-объем). Количество растворителя находится в отношении от 10 мл до 30 мл на 1 г исходного соединения (І). Увеличение содержания воды в растворителе вызывает тенденцию к уменьшению времени завершения обработки. Когда используют безводный этанол в качестве растворителя, превращение завершается при температуре 70°С и за 8 часов. Безводная форма может быть получена с помощью способа перекристаллизации. Одной из наилучших методик является представленная в примере 3, изложенном ниже. В этой методике водный растворитель, содержащий менее, чем 5% (объем/объем) воды, может быть использован в качестве растворителя. Б) Способ получения 1/2 гидрата: Смесь исходных кристаллов соединения (І) и водный раствор этанола, имеющий содержание воды в 50%, нагревают с обратным холодильником при перемешивании в состоянии мутной взвеси в течение от 1 часа до 20 часов. Количество растворителя берется в соотношении от 10 мл до 30 мл на 1 г исходного соединения (І). Известно, что, когда используют растворитель, содержащий аммиак, скорость образования 1/2 гидрата увеличивается. 1/2 Гидрат может быть получен с помощью способа перекристаллизации. Одной из наилучших методик является представленная в примере 2, изложенном ниже. С) Способ получения 1 гидрата: Одной из наилучших методик для селективного получения 1 гидрата является представленная в примере 4, изложенном ниже. Д) Способ получения 3/2 гидрата: 3/2 Гидрат получают из смеси в виде мутной взвеси, перемешиваемой при условиях, изложенных ранее, при которых образуется преимущественно 3/2 гидрат. Условия, в которых преимущественно образуется 3/2 гидрат, определяются, в основном, содержанием воды в растворителе и температурой, и зависимость представлена в следующей таблице: дится в отношении от 5 мл до 50 мл на 1 г исходного соединения (I), и предпочтительно, от 10 мл до 20 мл. Содержание воды находится в пределах от 50% до 100%, и предпочтительно, от 50% до 75%. Если содержание аммиака возрастает, количество используемого растворителя может быть уменьшено. Количество аммиака находится в отношении от 0,5 до 2,0 г, предпочтительно, от 0,7 до 1,0 г на 1 г исходного соединения (І). Растворитель, содержащий аммиак, может быть получен путем добавления аммиачной воды или введения газообразного аммиака в растворитель. Когда используют аммиачную воду, необходимо рассчитывать ее ингредиенты для получения растворителя с заданным содержанием воды. Температура для кристаллизации может быть определена с помощью таблицы, приведенной выше. Кристаллы данного изобретения могут быть включены в антимикробные препараты в соответствующей твердой лекарственной форме с помощью обычных способов приготовления. Твердые лекарственные формы для перорального приема включают таблетки, порошки, гранулы и капсулы. При приготовлении твердых форм, активный ингредиент может быть смешан с соответственно подобранными фармацевтически приемлемыми наполнителями, такими как вкусовые и цветовые наполнители, связующие, увлажняющие агенты и смазывающие вещества. Кристаллы изобретения могут быть включены в препараты для животных, такие как порошки, мелкие гранулы и растворимые порошки, с помощью широко используемых способов приготовления. Данное изобретение ниже будет иллюстрировано более подробно с помощью примеров, но не ограничено ими. Данные спектров дифракции рентгеновских лучей, представленные в примерах, определяются при следующих условиях с использованием установки Geider Flex производства Rigaku-Denki: Мишень Си-Ка Фильтр Ni Напряжение 40 кв Ток 20 ма Пример 1 3/2 Гидрат 7-[(7-(S)-амино-6-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты Исходные кристаллы 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2фторциклопропил]-4-оксо-1,4-дигидрохинолин-3карбоновой кислоты добавляют к смеси 5500 мл водного раствора этанола, имеющего содержание воды 75% , и 45 мл 28% аммиачной воды, и смесь перемешивают на водяной бане при 45°С в течение 30 минут. После растворения кристаллов добавляют 7,5 г активированного угля с последующей фильтрацией. Фильтрат концентрируют при пониженном давлении, при температуре снаружи 45°С для удаления примерно 3000 мл растворителя путём выпаривания. Концентрат охлаждают до комнатной температуры и собирают путем фильтрации выпавшие в осадок кристаллы, и сушат при 40°С, при пониженном давлении, получая 143 г целевого соединения. Таблица Преимущественная область взвеси 3/2 гидрата Температура (°С) 45 50 55 60 Содержание воды более, чем 50% более, чем 60% более, чем 70% более, чем 90% Количество растворителя находится в отношении от 10 мл до 30 мл на 1 г исходного соединения (І). 3/2 Гидрат может быть получен с помощью способа перекристаллизации. Преимущественная методика представлена в примерах 1 и 5, изложенных ниже. Обычно, для способа перекристаллизации является предпочтительным использование растворителя, содержащего аммиак, поскольку требуемое количество растворителя может быть уменьшено. Количество растворителя нахо 5 41312 Температура плавления: 225°С (разложение). Порошковая рентгеновская дифрактометрия (характерные пики): 9,19 8,42 7,80 7,60 6,82 6,15 5,55 5,40 4,60 4,23 Значение d (постоянОтносительная ные решетки) (А) интенсивность 11,47 Слабая 10,49 Сильная 9,69 Слабая 7,12 Исключительно слабая 6,87 Сильная 6,23 Сильная 5,68 Слабая 5,25 Сильная 4,90 Исключительно сильная 4,71 Исключительно слабая 4,61 Слабая 4,25 Слабая 4,15 Исключительно слабая 4,01 Сильная 3,85 Исключительно слабая 3,80 Исключительно слабая 3,74 Исключительно слабая 3,69 Слабая 3,58 Слабая 3,50 Слабая 3,46 Слабая 3,39 Слабая 3,34 Слабая 3,29 Слабая 3,17 Слабая ИК; nах (KB r) см-1: 3420, 3000, 2860, 1620. Элементный анализ, для С19Н18F2ClN3O3 1/2 H2O: Вычисл. (%) С 54,49; Н 4,57; N 10,03. Обнаруж. (%) С 54,59; Н 4,29; N 9,88. Содержание воды (способ Karl Fisher): Вычисл.: 2,15%; Обнаруж.: 2,1%. Пример 3 Безводная 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота Исходные кристаллы 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2фторциклопропил]-4-оксо-1,4-дигидрохинолин-3карбоновой кислоты добавляют к 360 мл 15% раствора аммиака в этаноле (по весу этанола; получают путем продувки газообразного аммиака через абсолютный этиловый спирт), и смесь перемешивают в течение 30 минут. После растворения кристаллов к раствору добавляют 0,2 г активированного угля с последующим фильтрованием. Фильтрат концентрируют при атмосферном давлении, удаляя примерно 260 мл растворителя. Концентрат охлаждают до комнатной температуры и собирают выпавшие в осадок кристаллы путем фильтрования и сушат при 40°С при пониженном давлении, получая 3,5 г целевого соединения. Температура плавления 231°С (разложение). Порошковая рентгеновская дифрактометрия (характерные пики): ИК; nах (KB r) см-1: 3450, 3000, 2880, 1620. Элементный анализ, для С19Н18F2ClN3O3 3/2 H2O: Вычисл. (%) С 52,24; Н 4,85; N 9,62. Обнаруж. (%) С 52,07; Н 4,68; Н 9,47. Содержание воды (способ Karl Fisher): Вычисл: 6,18%; Обнаруж.; 6,5%. Пример 2 1/2 Гидрат 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты Иcходные кристаллы 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2фторциклопропил]-4-оксо-1,4-дигидрохинолин-3карбоновой кислоты добавляют к смеси 160 мл водного раствора этанола, имеющего содержание воды в 50%, и 6 мл 28% аммиачной воды, и смесь перемешивают при 60°С в течение 30 минут. После растворения кристаллов добавляют к раствору 0,2 г активированного угля с последующей фильтрацией. Фильтрат концентрируют при атмосферном давлении для удаления примерно 80 мл растворителя. Концентрат охлаждают до комнатной температуры и собирают путем фильтрации выпавшие в осадок кристаллы, и сушат при 40°С при пониженном давлении, получая 3,6 г целевого соединения. Температура плавления: 195°С (разложение). Порошковая рентгеновская дифрактометрия (характерные пики): Значение d (постоянные решетки) (А) 15,66 Слабая Слабая Исключительно сильная Слабая Исключительно слабая Слабая Слабая Слабая Слабая Слабая Значение d (постоянные решетки) (А) 11,35 10,72 9,07 6,94 5,63 5,42 4,99 4,54 4,45 4,32 3,83 3,70 3,56 3,47 3,42 3,35 3,19 Относительная интенсивность Слабая Сильная Исключительно сильная Исключительно слабая Исключительно сильная Сильная Слабая Сильная Слабая Сильная Сильная Исключительно слабая Сильная Слабая Исключительно слабая Слабая Сильная ИК; nах (KB r) см-1: 3430, 2950, 2800, 1630, 1610. Элементный анализ, для С19Н18F2ClN3O3: Вычисл. (%) С 55,69; Н 4,43; N 10,25. Обнаруж. (%) С 55,78; Н 4,23; N 10,26. Относительная интенсивность Слабая 6 41312 Обнаруж. (%) С 53,31; Н 4,55; N 9,93. Содержание воды (способ Karl Fisher): Вычисл: 4,2%; Обнаруж.: 4,1%. Пример 5 3/2 Гидрат 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты Исходные кристаллы 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2фторциклопропил]-4-оксо-1,4-дигидрохинолин-3карбоновой кислоты добавляют к смеси 45 мл этанола, 37 мл воды и 25 мл 28% аммиачной воды, и всю смесь перемешивают на бане при 45°С в течение 10 минут. После растворения кристаллов удаляют около 50 мл растворителя при пониженном давлении и целевые кристаллы собирают путем фильтрования, затем сушат при 40°С в вакууме, получая 7,32 г (94,8%) целевого соединения. Пример приготовления 1 Капсула: Соединение формулы (I) (3/2 гидрат) 100,0 мг Пшеничный крахмал 23,0 мг Кальцикарбоксиметилцеллюлоза 22,5 мг Гидроксипропилцеллюлоза 3,0 мг Стеарат магния 1,5 мг Итого: 150,0 мг Пример приготовления 2: Порошок для примешивания в корм: Соединение по примеру 1 от 1 до 10 г (3/2 гидрат) Пшеничный крахмал от 89,5 до 98,5 г Легкая безводная кремниевая кислота 0,5 г Итого: 100 г Хотя изобретение описано подробно с упоминанием конкретных примеров, для специалистов понятно, что различные изменения и модификации могут быть осуществлены без выхода за его рамки. Содержание воды (способ Karl Fisher): Вычисл.: 0%; Обнаруж.: 0,2%. Пример 4 Моногидрат 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2фторциклопропил]-4-оксо-1,4-дигидрохинолин-3карбоновой кислоты Исходные кристаллы 7-[(7-(S)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1R,2S)-2фторциклопропил]-4-оксо-1,4-дигидрохинолин-3карбоновой кислоты добавляют к 150 мл водного раствора метанола, имеющего содержание воды в 1% или менее, для образования мутной взвеси. Взвесь перемешивают при 25°С в течение 3 дней. Кристаллы собирают путем фильтрования и сушат при комнатной температуре при пониженном давлении до тех пор, пока не подтвердится, что вес стал постоянным, получая 4,5 г целевого соединения. Порошковая рентгеновская дифрактометрия (характерные пики): Значение d (постоянОтносительная ные решетки) (А) интенсивность 13,22 Сильная 7,74 Исключительно сильная 6,94 Исключительно слабая 6,68 Слабая 5,77 Слабая 5,60 Сильная 5,16 Исключительно слабая 4,71 Средняя 4,09 Сильная 3,91 Слабая 3,72 Слабая 3,60 Сильная ИК; nах (KB r) см-1: 3620, 3410, 3080, 2870, 1630, 1610, 1540. Элементный анализ, для С19Н18F2ClN3O3 H2O: Вычисл. (%) С 53,34; Н 4,71; N 9,82. 7 41312 Фиг. 1 Фиг. 2 8 41312 Фиг. 3 Фиг. 4 __________________________________________________________ ДП "Український інститут промислової власності" (Укрпатент) Україна, 01133, Київ-133, бульв. Лесі Українки, 26 (044) 295-81-42, 295-61-97 __________________________________________________________ Підписано до друку ________ 2002 р. Формат 60х84 1/8. Обсяг ______ обл.-вид. арк. Тираж 50 прим. Зам._______ ___________________________________________________________ УкрІНТЕІ, 03680, Київ-39 МСП, вул. Горького, 180. (044) 268-25-22 ___________________________________________________________ 9
ДивитисяДодаткова інформація
Назва патенту англійськоюHydrates of 7-[7-(s)amino-5-azaspiro[2,4]heptane-5-yl]-8-chloro-6-fluoro-1-[(1r,2s)-2-fluoricyclopropyl]-4-oxo-1,4-dihydroquinoline-3-carboxylic acid, a process for the preparation thereof and a pharmaceutical composition
Автори англійськоюKimura Iuiti, Kawakama Katsuhiro, Mikata Norimasa, Utiiama Keidzi, Uemura Tazuo, Yukimoto Yuzuke
Назва патенту російськоюГидраты 7-[7-(s)-амино-5-азаспиро[2,4]гептан-5-ил]-8-хлор-6-фтор-1-[(1r,2s)-2-фторциклопропил]-4-оксо-1,4-дигидрохинолин-3-карбоновой кислоты, способ их получения и фармацевтическая композиция
Автори російськоюКимура Иуити, Каваками Кацухиро, Миката Норимаса, Утияма Кейдзи, Уемура Тазуо, Юкимото Юзуке
МПК / Мітки
МПК: C07D 401/04
Мітки: гідрати, спосіб, кислоти, одержання, 7-[7-(s)-аміно-5-азаспіро[2,4]гептан-5-іл]-8-хлор-6-фтор-1-[(1r,2s)-2-фторциклопропіл]-4-оксо-1,4-дигідрохінолін-3-карбонової, фармацевтична, композиція
Код посилання
<a href="https://ua.patents.su/9-41312-gidrati-7-7-s-amino-5-azaspiro24geptan-5-il-8-khlor-6-ftor-1-1r2s-2-ftorciklopropil-4-okso-14-digidrokhinolin-3-karbonovo-kisloti-sposib-kh-oderzhannya-i-farmacevtichna-kompoziciya.html" target="_blank" rel="follow" title="База патентів України">Гідрати 7-[7-(s)-аміно-5-азаспіро[2,4]гептан-5-іл]-8-хлор-6-фтор-1-[(1r,2s)-2-фторциклопропіл]-4-оксо-1,4-дигідрохінолін-3-карбонової кислоти, спосіб їх одержання і фармацевтична композиція</a>
Попередній патент: Конденсовані індольні похідні як антагоністи 5нт4 рецептора, фармацевтична композиція
Наступний патент: Спосіб визначення каналів зв’язку в транспортній мережі та транспортна мережа
Випадковий патент: Спосіб вибору тактики лікування гострих запальних захворювань орбіти