Заміщені індоли, спосіб їх отримання, їх застосування
Формула / Реферат
1. Спосіб лікування хвороби, опосередкованої простагландином D2, в якому пацієнту вводять терапевтично ефективну кількість сполуки формули (І)
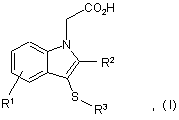
в якій:
R1 представляє один або більше замісників, незалежно вибраних з групи: NR4COR6, NHSO2R5, NHCOR6, NHCONR4, NHSO2NR5R6, або гетероарил, останній може бути, як варіант, заміщений С1-3-алкілом;
R2 - гідроген або С1-3-алкіл;
R3 - арил, який, як варіант, заміщений одним або більше замісниками, незалежно вибраними з групи: галоген, CN, SO2R4, OR8 або С1-3-алкіл, останній, як варіант, може бути заміщений одним або кількома атомами галогену;
R4 - С1-6-алкіл;
R5 - C1-6-aлкіл;
R6 - С1-6-алкіл, циклоалкіл або бензоїл;
R8 - С1-6-алкіл,
або її фармацевтично прийнятної солі або сольвату.
2. Спосіб за п. 1, в якому у формулі І R1 означає NHSO2R5, NH(CO)R6 або гетероарил (останній, як варіант, заміщений С1-3алкілом).
3. Спосіб за п. 1 або 2, в якому у формулі І R2 означає С1-3-алкіл.
4. Спосіб за п. 3, в якому R3 означає феніл, як варіант, заміщений галогеном або метилсульфоном.
5. Спосіб за п. 1, в якому сполука вибрана з групи, яку складають:
4-(ацетиламіно)-3-[(4-хлорфеніл)тіо]-2-метил-1Н-індол-1-оцтова кислота;
3-[(4-хлорфеніл)тіо]-2-метил-4-[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота;
3-[(4-хлорфеніл)тіо]-2-метил-4-(5-піримідиніл)-1Н-індол-1-оцтова кислота;
3-[(4-хлорфеніл)тіо]-2-метил-4-піразиніл-1Н-індол-1-оцтова кислота;
3-[(2-хлорфеніл)тіо]-2-метил-5-[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота;
3-[(3-хлорфеніл)тіо]-2-метил-4-[(метилсульфоніл)аміно]-1Н-індолол-1-оцтова кислота;
3-[(4-хлорфеніл)тіо]-2-метил-4-[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота;
3-[(3-метоксифеніл)тіо]-2-метил-4-[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота;
3-[(4-метоксифеніл)тіо]-2-метил-4-[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота;
3-[(2-трифлуорметилфеніл)тіо]-2-метил-4-[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота;
3-[(8-хінолініл)тіо]-2-метил-4-[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота;
3-[(2-(метилетил)феніл)тіо]-2-метил-4-[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота;
5-(ацетиламіно)-3-[(4-хлорфеніл)тіо]-2-метил-1Н-індол-1-оцтова кислота;
4-(ацетилетиламіно)-3-[(4-хлорфеніл)тіо]-2-метил-1Н-індол-1-оцтова кислота;
3-[(4-хлорфеніл)тіо]-4-[(циклопропілкарбоніл)аміно]-2-метил-1Н-індол-1-оцтова кислота;
4-(бензоїламіно)-3-[(4-хлорфеніл)тіо]-2-метил-1Н-індол-1-оцтова кислота;
4-(ацетиламіно)-3-[(3-хлорфеніл)тіо]-2-метил-1Н-індол-1-оцтова кислота;
3-[(4-хлорфеніл)тіо]-4-[[(диметиламіно)сульфоніл]аміно]-2-метил-1Н-індол-1-оцтова кислота;
3-[(4-хлорфеніл)тіо]-2-[(метил-4-1Н-імідазол-4-іл)сульфоніл]аміно-1Н-індол-1-оцтова кислота;
3-[(4-хлорфеніл)тіо]-4-[[(диметиламіно)ацетил]аміно]-2-метил-1Н-індол-1-оцтова кислота;
4-(ацетиламіно)-2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота;
4-(ацетиламіно)-3-[(2-хлорфеніл)тіо]-2-метил-1Н-індол-1-оцтова кислота;
4-(ацетиламіно)-2-метил-3-[[4-(етилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота;
3-[(4-хлорфеніл)тіо]-4-[[(етиламіно)карбоніл]аміно]-2-метил-1Н-індол-1-оцтова кислота;
3-[[4-(метилсульфоніл)феніл]тіо]-4-(5-піримідиніл)-1Н-індол-1-оцтова кислота;
2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-4-(2-тіофеніл)-1Н-індол-1-оцтова кислота;
4-(3,5-диметил-4-ізоксазоліл)-2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота;
4-(3-фураніл)-2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота;
2-метил-4-[(метилсульфоніл)аміно]-3-[[4-(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота;
2-метил-5-[(метилсульфоніл)аміно]-3-[[3-(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота;
2-метил-5-[(метилсульфоніл)аміно]-3-[[2-(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота;
2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-5-(5-піримідиніл)-1Н-індол-1-оцтова кислота;
2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-5-(3-тіофеніл)-1Н-індол-1-оцтова кислота;
5-(3,5-диметил-4-ізоксазоліл)-2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота;
2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-5-(3-піридиніл)-1Н-індол-1-оцтова кислота;
2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-5-(1Н-піразол-4-іл)-1Н-індол-1-оцтова кислота;
4-(ацетиламіно)-3-[(4-ціанофеніл)тіо]-2-метил-1Н-індол-1-оцтова кислота та
їх фармацевтично прийнятні солі та сольвати.
6. Спосіб лікування за будь-яким з пп. 1-5, де хворобою є астма або риніт.
7. Застосування сполуки формули (І) або її фармацевтично прийнятної солі або сольвату, що визначені вище, у виробництві медикаменту для лікування хвороби, опосередкованої CRTh2.
8. Застосування за п. 7, де хворобою є астма.
9. Спосіб отримання сполуки формули (І) або її фармацевтично прийнятної солі або сольвату, в якому здійснюють реакцію сполуки формули (II):
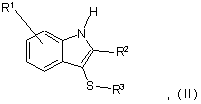
у котрій R1, R2 та R3 визначені у формулі (І) або є їх захищеними похідними,
зі сполукою формули (НА):
L-CH2CO2R17, (НА)
де R17 - алкіл, a L - відщеплювана група, як-то атом галогену,
у присутності основи, та, як варіант, після цього у будь-якому порядку:
видалення будь-якої захисної групи,
гідроліз естерної групи R17 до відповідної кислотної,
утворення фармацевтично прийнятної солі чи сольвату.
10. Сполука формули (І) або її фармацевтично прийнятна сіль або сольват

в якій
R1 представляє один або більше замісників, незалежно вибраних з групи: NR4COR6, NHSO2R5, NHCOR6, NHSO2NR5R6, або гетероарил;
R2 - гідроген або С1-7-алкіл;
R3 - арил, який, як варіант, заміщений одним або більше замісниками, незалежно вибраними з групи: галоген, CN, SO2R4, OR4, SR4, SOR4 або С1-3-алкіл, останній, як варіант, може бути заміщений одним або кількома атомами галогену;
R4 - С1-6-алкіл;
R5 і R6 - С1-6-алкіл.
11. Сполука за п. 10, в якій R1 означає NHSO2R5 або NH(CO)R6, або гетероарил.
12. Сполука за п. 10 або 11, в якій R2 означає С1-7-алкіл.
13. Сполука за п. 12, в якій R3 означає феніл, необов'язково заміщений галогеном.
14. Сполука за п. 10, вибрана з групи, яку складають:
4-(ацетиламіно)-3-[(4-хлорфеніл)тіо]-2-метил-1Н-індол-1-оцтова кислота;
3-[(4-хлорфеніл)тіо]-2-метил-4-[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота;
2-метил-3-(фенілтіо)-4-(4-піримідиніл)-1Н-індол-1-оцтова кислота
та їх фармацевтично прийнятні солі.
15. Сполука формули (І) за будь-яким з пп. 10-14 для застосування в терапії.
16. Спосіб лікування хвороби, опосередкованої простагландином D2, в якому пацієнту вводять терапевтично ефективну кількість сполуки формули (І) або її фармацевтично прийнятної солі, як визначено в пп. 10-15.
17. Спосіб лікування за п. 16, в якому хворобою є астма або риніт.
Текст
1. Спосіб лікування хвороби, опосередкованої простагландином D2, в якому пацієнту вводять терапевтично ефективну кількість сполуки формули (І) CO2H 2 (19) 1 3 3-[(3-хлорфеніл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індолол-1-оцтова кислота; 3-[(4-хлорфеніл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота; 3-[(3-метоксифеніл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота; 3-[(4-метоксифеніл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота; 3-[(2-трифлуорметилфеніл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота; 3-[(8-хінолініл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота; 3-[(2-(метилетил)феніл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота; 5-(ацетиламіно)-3-[(4-хлорфеніл)тіо]-2-метил-1Ніндол-1-оцтова кислота; 4-(ацетилетиламіно)-3-[(4-хлорфеніл)тіо]-2-метил1Н-індол-1-оцтова кислота; 3-[(4-хлорфеніл)тіо]-4[(циклопропілкарбоніл)аміно]-2-метил-1Н-індол-1оцтова кислота; 4-(бензоїламіно)-3-[(4-хлорфеніл)тіо]-2-метил-1Ніндол-1-оцтова кислота; 4-(ацетиламіно)-3-[(3-хлорфеніл)тіо]-2-метил-1Ніндол-1-оцтова кислота; 3-[(4-хлорфеніл)тіо]-4[[(диметиламіно)сульфоніл]аміно]-2-метил-1Ніндол-1-оцтова кислота; 3-[(4-хлорфеніл)тіо]-2-[(метил-4-1Н-імідазол-4іл)сульфоніл]аміно-1Н-індол-1-оцтова кислота; 3-[(4-хлорфеніл)тіо]-4[[(диметиламіно)ацетил]аміно]-2-метил-1Н-індол-1оцтова кислота; 4-(ацетиламіно)-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота; 4-(ацетиламіно)-3-[(2-хлорфеніл)тіо]-2-метил-1Ніндол-1-оцтова кислота; 4-(ацетиламіно)-2-метил-3-[[4(етилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота; 3-[(4-хлорфеніл)тіо]-4-[[(етиламіно)карбоніл]аміно]2-метил-1Н-індол-1-оцтова кислота; 3-[[4-(метилсульфоніл)феніл]тіо]-4-(5-піримідиніл)1Н-індол-1-оцтова кислота; 2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-4-(2тіофеніл)-1Н-індол-1-оцтова кислота; 4-(3,5-диметил-4-ізоксазоліл)-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота; 4-(3-фураніл)-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота; 2-метил-4-[(метилсульфоніл)аміно]-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота; 84701 4 2-метил-5-[(метилсульфоніл)аміно]-3-[[3(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота; 2-метил-5-[(метилсульфоніл)аміно]-3-[[2(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота; 2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-5-(5піримідиніл)-1Н-індол-1-оцтова кислота; 2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-5-(3тіофеніл)-1Н-індол-1-оцтова кислота; 5-(3,5-диметил-4-ізоксазоліл)-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота; 2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-5-(3піридиніл)-1Н-індол-1-оцтова кислота; 2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-5-(1Нпіразол-4-іл)-1Н-індол-1-оцтова кислота; 4-(ацетиламіно)-3-[(4-ціанофеніл)тіо]-2-метил-1Ніндол-1-оцтова кислота та їх фармацевтично прийнятні солі та сольвати. 6. Спосіб лікування за будь-яким з пп. 1-5, де хворобою є астма або риніт. 7. Застосування сполуки формули (І) або її фармацевтично прийнятної солі або сольвату, що визначені вище, у виробництві медикаменту для лікування хвороби, опосередкованої CRTh2. 8. Застосування за п. 7, де хворобою є астма. 9. Спосіб отримання сполуки формули (І) або її фармацевтично прийнятної солі або сольвату, в якому здійснюють реакцію сполуки формули (II): R1 H N R2 S R3 , ( II ) у котрій R , R та R визначені у формулі (І) або є їх захищеними похідними, зі сполукою формули (НА): L-CH2CO2R17, (Н А) де R17 - алкіл, a L - відщеплювана група, як-то атом галогену, у присутності основи, та, як варіант, після цього у будь-якому порядку: видалення будь-якої захисної групи, гідроліз естерної групи R17 до відповідної кислотної, утворення фармацевтично прийнятної солі чи сольвату. 10. Сполука формули (І) або її фармацевтично прийнятна сіль або сольват CO2H 1 2 3 N R2 R1 S R3 , ( I) в якій R1 представляє один або більше замісників, незалежно вибраних з групи: NR4COR6, NHSO2R5, NHCOR6, NHSO2NR5R6, або гетероарил; 5 84701 6 R2 - гідроген або С1-7-алкіл; R3 - арил, який, як варіант, заміщений одним або більше замісниками, незалежно вибраними з групи: галоген, CN, SO2R4, OR4, SR4, SOR4 або С1-3алкіл, останній, як варіант, може бути заміщений одним або кількома атомами галогену; R4 - С1-6-алкіл; R5 і R6 - С1-6-алкіл. 11. Сполука за п. 10, в якій R1 означає NHSO2R5 або NH(CO)R6, або гетероарил. 12. Сполука за п. 10 або 11, в якій R2 означає С1-7алкіл. 13. Сполука за п. 12, в якій R3 означає феніл, необов'язково заміщений галогеном. 14. Сполука за п. 10, вибрана з групи, яку складають: 4-(ацетиламіно)-3-[(4-хлорфеніл)тіо]-2-метил-1Ніндол-1-оцтова кислота; 3-[(4-хлорфеніл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота; 2-метил-3-(фенілтіо)-4-(4-піримідиніл)-1Н-індол-1оцтова кислота та їх фармацевтично прийнятні солі. 15. Сполука формули (І) за будь-яким з пп. 10-14для застосування в терапії. 16. Спосіб лікування хвороби, опосередкованої простагландином D2, в якому пацієнту вводять терапевтично ефективну кількість сполуки формули (І) або її фармацевтично прийнятної солі, як визначено в пп. 10-15. 17. Спосіб лікування за п. 16, в якому хворобою є астма або риніт. Представлений винахід стосується заміщених індолів, корисних як фармацевтичні сполуки для лікування респіраторних розладів, фармацевтичних композицій, що їх містять, та способів їх отримання. [ЕРА 1 170 594] розкриває способи ідентифікації сполук, корисних для лікування хвороб, опосередкованих простагландином D2, лігандом для орфанового рецептору CRTh2. [US 5486525] розкриває серії індолів, що виявляють PAFантагоністичну активність. Зараз несподівано виявлено, що деякі індолоцтові кислоти є активними стосовно рецептору GRTh2, та як наслідок, очікувано, є потенційно корисними для лікування різних респіраторних хвороб, охоплюючи астму та хронічну обстр уктивну хворобу легенів (COPD). У першому аспекті винахід тому стосується сполуки формули (І) або фармацевтично прийнятної солі та її сольватів: С6-алкініл, С1-6-апкіл, останні три групи, як варіант, заміщені одним або більше замісниками, незалежно вибраними з групи: атоми галогену, OR8 та NR5R6, S(O) xR7, де х дорівнює 0, 1 або 2; R4 репрезентує арил, гетероарил, або С1-6алкіл, усі які можуть бути, як варіант, заміщеними одним або більше замісниками, незалежно вибраними з групи: атоми галогену, арил, гетероарил, OR10, OH, NR11R12, S(O) xR13 (де х дорівнює 0, 1 або 2), CONR14R15, NR14COR15 SO2NR14R 15, NR14SO2R15, CN, нітро; R5 та R6 незалежно репрезентують атом гідрогену, С1-6-алкіл, арил, або гетероарил, останні три з яких можуть бути, як варіант, заміщеними одним або більше замісниками, незалежно вибраними з групи: атоми галогену, арил, OR8 та NR14R 15, CONR14R15, NR14COR15 , SO 2NR14R15, NR14SO2R 15; CN, нітро, С1-3-алкіл (котрий може бути, як варіант, заміщеним атомами галогену; або R5 та R6 разом з атомом нітрогену, до котрого вони приєднані можуть утворювати 3-8-членне насичене гетероциклічне кільце, що містить, як варіант, один або більше атомів, вибраних з групи: O, S(O) x, де х дорівнює 0, 1 або 2, NR16, та саме, як варіант, заміщене С 1-3-алкілом; R7 та R13 незалежно репрезентують C1-С6алкіл, арил або гетероарил, усі які можуть бути, як варіант, заміщеними атомами галогену; R8 репрезентує атом гідрогену, C(O)R9, С1-С6алкіл (як варіант, заміщений атомами галогену або арил ом) арил або гетероарил (як варіант, заміщений галогеном); кожне з R9 R10, R11, R12, R14, R15 незалежно репрезентує атом гідрогену, C1-C6-SnKm, арил або гетероарил (усі які можуть бути, як варіант, заміщеними атомами галогену); а R16 - гідроген, C1-4-алкіл, СОС1-С4-алкіл або СОУС1-С4-алкіл, де Y - O або NR7. У контексті представленого опису, якщо не встановлено інше, алкіл чи алкеніл або алкіл чи алкеніл у заміснику можуть бути лінійними, розгалуженими або циклічними. Aрилами можуть бути феніл або нафтил. Гетероарил визначено як 5-7-членне ароматичне кільце, або він може бути 6,6-або 6,5 (I) у котрій: R1 представляє один або більше замісників, незалежно вибраних з групи: NR4SO2R5, NR4CO2R5, NR4COR6, NR4SO 2NR5R6, NHSO2R5, NHCO2R6, NHCOR6, NHCONR4, NHSO2NR5R6 або гетероарил, останній може бути, як варіант, заміщеним галогеном, CN, OR7, C1-3-алкіл (котрий може бути, як варіант, заміщеним атомами галогену); R2 - гідроген, галоген, CN, SO2R4 або CONR5R6, CH2OH, CH2OR4 або C1-7-алкіл, останній, як варіант, заміщений одним або більше замісниками, незалежно вибраними з групи: атоми галогену, OR8 та NR5R6, S(O)xR7, де х дорівнює 0, 1 або 2; R3 - арил або гетероарил, кожний з яких, як варіант, заміщений одним або більше замісниками, незалежно вибраними з групи: гідроген, галоген, CN, OH, SO 2R4,-OR4, SR 4, SOR4, SQ2NR5R6, CONR5R6, NR5R6S NHSO2R4, NHCOR4, NHCO2R4, NR7SO2R4, NR7CO 2R4, NR7COR4, С2-С 6-алкеніл. С2 7 84701 конденсованим дициклічним кільцем, що містить один або більше гетероатомів, вибраних з групи: N, S та O. Приклади охоплюють піридин, піримідин, тіазол, оксазол, піразол, імідазол, фуран, ізоксазол, пірол, ізотіазол та азулен, нафтил, інден, хінолін, ізохінолін, індол, індолізин, бензо[b]фуран, бензо[b]тіофен, 1Н-індазол, бензімідазол, бензтіазол, бензоксазол, пурин, 4Н-хінолізин, цинолін, фталазин, хіназолін, хіноксалін, 1,8-нафтиридин, птеридин, хінолон. Коли R5 та R6 разом з атомом нітрогену, до котрого вони приєднані, утворюють 3-8-членне насичене гетероциклічне кільце, приклади охоплюють морфолін, тіоморфолін, азетидин, імідазолідин, піролідин, піперидин та піперазин. Замісники можуть бути на атомах карбону або прийнятних атомах нітрогену таких кілець. Придатний R1 представляє один або більше замісників, незалежно вибраних з групи: NR4SO2R5, NR4CO2R6, NR4COR6, NR4SO2NH5R6, NHSO2R5, NHCO2R6, NHCOR6, NHCONR4, 5 6 NHSO2NR R або гетероарил, останній може бути, як варіант, заміщеним галогеном, CN чи OR7. Придатний R1 представляє один або більше замісників, незалежно вибраних з групи: NR4SO2R5, NR4CO2R6, NR4COR6, NR4SO2NR5R6, NHSO2R5, NBCO2R6, NHCOR6, NHSO2NR5R6, або гетероарил, останній може бути, як варіант, заміщеним галогеном, CN або OR7. Переважно R1 - NR 4COR64, NHSO2R4 , NHCOR 6 або гетероарил. Більш переважно R1 - NHSO2Me або NR4COMe, NHCONHaлкiл, NR4COциклопропіл, NHSO2гетероарил, NHSO2NMe2, NHCONR4, 5-6членна гетероароматична група, що містить 1-2 гетероатоми. Найпереважніше R1 - NHSO2Me або NR4COMe, NHCONHaлкiл, диметіоксазол, піримідин або піразин. Ще краще, коли R1-NHCOMe. R1 може бути у будь-якій придатній позиці на індольному кільці. Переважно R1 є у 5-позиції та/або 4-позиції. Переважно R2 - С1-6-алкіл або гідроген, більш переважно С1-6-алкіл або гідроген, ще краще метил або гідроген. Найкраще, коли R2 - метил. Переважно R3 - хіноліл або феніл, останній, як варіант, заміщено галогеном, алко-кси, SO2R4, більш переважно феніл заміщено хлором, метокси, метилсульфоном або етилсульфоном. Замісники можуть бути представлені у будьякій придатній позиції R3. Переважно, якщо R3 феніл, замісники представлені у 2, 3 та 4-позиціях. Найкраще, коли одиничний замісник представлено у 4-позиції. Кращі сполуки винаходу охоплюють: 4(ацетиламіно)-3-[(4-хлорфеніл)тіо]-2-метил-1Ніндол-1-оцтова кислота; 3-[(4-хлорфеніл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота; 3-[(4-хлорфеніл)тіо]-2-метил-4-(5-піримідиніл)1Н-індол-1-оцтова кислота; 3-[(4-хлорфеніл)тіо]-2-метил-4-піразиніл-1Ніндол-1-оцтова кислота; 3-[(2-хлорфеніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кисло 8 та; 3-[(3-хлорфеніл)тіо]-2-метил[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота; 3-[(4-хлорфеніл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота; 3-[(3-метоксифеніл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індолол-1-оцтова кислота; 3-[(4-метоксифеніл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота; 3-[(2-трифлуорметилфеніл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота: 3-[(8-хінолініл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота; 3-[(2-(метилетил)феніл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота; 5-(ацетиламіно)-3-[(4-хлорфеніл)тіо]-2-метил1Н-індол-1-оцтова кислота; 4-(ацетиламіно)-3-[(4-хлорфеніл)тіо]-2-метил1Н-індол-1-оцтова кислота; 3-[(4-хлорфеніл)тіо]-4[циклопропілкарбоніл)аміно]-2-метил-1Н-індол-1оцтова кислота; 4-(бензоїламіно)-3-[(4-хлорфеніл)тіо]-2-метил1Н-індол-1-оцтова кислота; 4-(ацетиламіно)-3-[(3-хлорфеніл)тіо]-2-метил1Н-індол-1-оцтова кислота; 3-[(4-хлорфеніл)тіо]-4[[(диметиламіно)сульфоніл]аміно]-2-метил-1Ніндол-1-оцтова кислота; 3-[(4-хлорфеніл)тіо]-2-метил-4-1Н-імідазол-4іл)сульфоніл]аміно-1Н-індол-1-оцтова кислота; 3-[(4-хлорфеніл)тіо]-4[[(диметиламіно)ацетил]аміно]-2-метил-1Н-індол-1оцтова кислота; 4-(ацетиламіно)-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота; 4-(ацетиламіно)-3-[(2-хлорфеніл)тіо]-2-метил1Н-індол-1-оцтова кислота; 4-(ацетиламіно)-2-метил-3-[[4(етилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота; 3-[(4-хлорфеніл)тіо]-4[[(етиламіно)карбоніл]аміно]-2-метил-1Н-індол-1оцтова кислота; 3-[[4-(метилсульфоніл)феніл]тіо]-4-(5піримідиніл)-1Н-індол-1-оцтова кислота; 2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-4-(2тіофеніл)-1Н-індол-1-оцтова кислота; 4-(3,5-диметил-4-ізоксазоліл)-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота; 4-(3-фураніл)-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота; 2-метил-4-[(метилсульфоніл)аміно]-3-[[4{метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота; 9 84701 2-метил-5-[(метилсульфоніл)аміно]-3-[[3(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота 2-метил-5-[(метилсульфоніл)аміно]-3-[[2(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота; 2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-5-(5піримідиніл)-1Н-індол-1-оцтова кислота; 2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-5-(3тіофеніл)-1Н-індол-1-оцтова кислота 5-(3,5-диметил-4-ізоксазоліл)-2-метил-3-[[4метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота; 2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-5-(3піридиніл)-1Н-індол-1-оцтова кислота 2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-5(1Н-піразол-4-іл)-1Н-індол-1-оцтова кислота; 4-(ацетиламіно)-3-[(4-ціанофеніл)тіо]-2-метил1Н-індол-1-оцтова кислота та їх фармацевтично прийнятні солі та сольвати. Деякі сполуки формули (І) можуть існувати у стереоізомерних формах. Зрозуміло, що винахід охоплює усі геометричні та оптичні ізомери сполук формули (І) та їх суміші, о хоплюючи рацемати. Таутомери та їх суміші також утворюють аспект представленого винаходу. Сполуку формули (І) вище можна перетворити у її фармацевтично прийнятну сіль або сольват, переважно основно-адитивну сіль, як-то амінонію, натрію, калію, кальцію, алюмінію, літію, магнію, цинку, бензатину, хлорпрокаїну, холіну, діетаноламіну, етаноламіну, етилдіаміну, меглуміну, трометаміну або прокаїну, або кислотно-адитивну сіль, як-то хлорид, гідробромід, фосфат, ацетат, фумарат, малеат, тартрат, цитрат, оксалат, метансульфонат або п-толуолсульфонат. Кращі солі охоплюють солі натрію та амінонію. Фахівцям буде ясно, що при здійсненні способів представленого винаходу деякі функціональні групи у вихідних реагентах або інтермедіатах можуть потребувати захисту захисними групами. Відтак, отримання сполуки формули (І) може охоплювати на прийнятному етапі видалення одної або більше захисних груп. Захист та зняття захисту функціональних груп повністю описано у ['Protective Groups in Organic Chemistry', вид. J. W. F. McOmie, Plenum Press (1973), та 'Protective Groups in Organic Synthesis', III вид., Т. W. Greene & P. G. M. Wilts, Wiley-interscience (1999)]. Згідно з наступним аспектом винахід стосується способу отримання сполуки формули (І) або її фармацевтично прийнятної солі або сольвату, який полягає у реакції сполуки формули (II): (II) у котрій R1, R2 та R3 визначені у формулі (І) або є їх захищеними похідними, зі сполукою формули (IIА): L-CH2CO2R17 (IIА) де R17 - алкіл та L - відщеплювана група, як-то атом галогену, у присутності основи, та, як варіант, після цього у будь-якому порядку: 10 - видалення будь-якої захисної групи - гідроліз естерної групи R17 до відповідної кислоти - утворення фармацевтично прийнятної солі чи сольвату. Реакцію можна проводити у придатному розчиннику, як-то ТГФ, застосовуючи основу, як-то натрій гідрид. Придатні групи R17 охоплюють С 1-6алкіли, як-то метил, етил або трет-бутил. Придатне L - відщеплювана група, як-то галоген, зокрема бром. Переважно сполукою формули (MA) є етил-, метил- або трет-бутилбромацетат. Гідроліз естерної групи R17 можна проводити, застосовуючи звичайні способи, наприклад, перемішуванням з водним натрій гідроксидом або трифлуороцтовою кислотою. Ясно, що деякі функціональні групи можуть потребувати захисту, застосовуючи стандартні захисні групи. Захист та зняття захисту функціональних груп, наприклад, описано у ['Protecti ve Groups in Organic Chemistry', вид. J, W. F. McOtoie, Plenum Press (1973), та 'Protective Groups in Organic Synthesis'; 3rd edition, T. W. Greene & P. G. M. Wuts, Wiley-lnterscience (1999)]. Сполуки формули (II), у котрій R1 - NRSO2R або NRC(O)R, можна отримувати зі сполук формули (III), реакцією з ацилувальним реагентом, як-то ацетилхлорид або суль-фонілхлорид Сполуки формули (III) можна отримувати зі сполук формули (IV) відновленням, застосовуючи водень та придатний каталізатор, переважно каталізатор є паладієм чи платиною на активованому вугіллі, у присутності полярного розчиннику, якто етанол. Сполуки формули (IV) можна отримувати зі сполук формули (V) та (Vl) у де R1 , R2 та R3 визначені у формулі (І). Переважно реакцію проводять у придатному розчиннику, як-то дихлорметан або тетрагідрофуран, застосовуючи хлорувальний засіб, як-то сульфонілхлорид або трет-бутил гіпохлорит, 1. Сполуки формул (V) та (Vl) є комерційно доступними або їх можна отримувати, застосовуючи стандартні способи, добре відомі у рівні те хніки. Деякі сполуки формули (І) можна отримувати зі сполук формули (VII), де X=галоген, переважно бром або йод, реакцією з органостананами (сполучення Стилла) або бороновими кислотами (сполучення Сузукі), застосовуючи каталіз паладієм. 11 84701 Переважно каталізаторами є тетракістрифенілфосфінпаладій(0), або паладій(ІІ)ацетат у присутності фосфінового ліганду, як-то три-орто-толілфосфін, у придатному розчиннику, як-то толуол або метанол при 8O0C. Групу R17 потім гідролізують як показано вище. Сполуки формули (VII) отримують зі сполук формули (II) зі сполуками формули (IIА) як показано вище: Сполуки формули (II), де X - галоген, отримують реакцією сполуки формули (VIII) зі сполукою формули (Vl): де R1, R2 та R3 визначені у формулі (І). Сполуки формули (II) можна отримувати реакцією сполуки формули (IX) зі сполукою формули (X), з наступним гідролізом естеру, як показано вище у синтезі сполуки формули (І): де R1, R2 та R3 або їх захищені похідні визначені у формулі (І). Реакцію проводять у придатному розчиннику у присутності галогену, переважно йоду, при кімнатній температурі, у полярному апротонному розчиннику, наприклад, диметилформаміді. Сполуки формул (IX) та (X) є комерційно доступними або їх можна отримувати способами, добре відомими у рівні техніки. Сполуки формули (І) мають активність як фармацевтичні засоби, зокрема, як модулятори активності рецептору CRTh2, та можуть бути застосовуваними у лікуванні (терапевтичному або профілактичному) станів/хвороб у людини та тварини, котрі загострені або викликані надлишковим або нерегульованим продукуванням PGD2 та його метаболітів. Сполуку винаходу, або її фармацевтично прийнятну сіль, можна застосовувати у лікуванні хвороб: (1) (респіраторний тракт) обструктивні хвороби 12 дихальних шляхів, о хоплюючи астму, охоплюючи бронхіальну, алергічну, інфекційно-алергічну, набуту, індуковану фізичним навантаженням, індуковану ліками (охоплюючи індуковану аспірином та NSAID) та індуковану пилом астму періодичної та постійної тяжкості, та інші випадки гіперчутливо-сті дихальних шляхів; хронічну обстр уктивну хворобу легенів (COPD); бронхіт, охоплюючи інфекційний та еозинофільний бронхіт; емфізему; бронхоекстазію; муковісцидоз, фіброзно-кістозну дегенерацію; саркоїдоз; легені фермера та асоційцовані хвороби; пневмоніт з гіперчутливістю; фіброз легенів, охоплюючи ендогенний фіброзний альве-оліт, ідіопатичні інтерстиціальні пневмонії, фіброзне ускладнення антинеопластичної терапії та хронічну інфекцію, охоплюючи туберкулез та аспергілез, та інші грибкові інфекції; ускладнення при трансплантації легенів; васкулітичні та тромботичні розлади судинної мережі легенів, та легеневу гіпертензію; активність проти кашлю, охоплюючи лікування хронічного кашлю, асоційцовані з запальними та секреторними станами дихальних шляхів, та ятрогенного кашлю; гострий та хронічний риніт, охоплюючи медикаментозний риніт, та вазомоторний риніт: багаторічний та сезонний алергічний риніт, охоплюючи нервову нежить (сінну лихоманку); назальний поліпоз; гостру вірусну інфекцію, охоплюючи звичайну застуду, та інфекцію респіраторним синтиціальним вірусом, грип, коронавірус (охоплюючи SARS) та аденовірус. (2) (кістки та суглоби) артритиди, асоційцовані з хворобами, або що охоплюють остеоартрит/остеоартроз, первинні та вторинні стосовно, наприклад, природженої дисплазії степна; цервікальний та поперековий спондиліт, та біль нижньої частини спини та шиї; ревматоїдний артрит та хвороба Стилла; серонегативні артропатії, охоплюючи анкілоз-ний спондиліт, псоріазний артрит, реактивний артрит та недиференційовану спондарт-ропатію; септичний артрит та інші асоційцовані з інфекцією артропатії та розлади кісток, як-то туберкулез, охоплюючи хворобу Потта та синдром Понсета; гострий та хронічний кристаліндукований синовіт, охоплюючи уратну подагру, хворобу відкладення кальцій пірофосфату, та сухожилля з кальцій апатитом, запалення синовіальної сумки; хвороба Бекхета; первинний та вторинний синдром Сьоргена; системний склероз та. обмежена склеродерма: системний червоний вовчак, змішана хвороба сполучної тканини, та хвороба недиференційованої сполучної тканини; запальні міопатії, охоплюючи дерматоміозитит та поліміозит; ревматична поліміалгія; юнацький артрит, охоплюючи ідіопатичні запальні артритиди будь-яких суглобів та асоційцовані синдроми, та ревматичну лихоманку та її системні ускладнення; васкулітиди, охоплюючи артерит велетенських клітин, артерит Такаясу, синдром Чарга-Штрауса, вузлуватий поліартерит, мікроскопічний поліартерит, та васкулітиди, асоційцовані з вірусною інфекцією, реакції гіпер-чутливості, кріоглобуліни, та парапротеїни; біль нижньої частини спини; родинна среди-земноморська лихоманка, синдром Мукле-Велса, та родинна ірландська лихоманка, хвороба Кікуші; індуковані ліками артралгії, 13 84701 тендонітитиди, та міопатії. (3) (шкіра) псоріаз, атопічний дерматит, контактий дерматит або інші екзематозні дерматози, та реакції гіперчутливості затяжного типу; фіто- та фотодерматит; себорейний дерматит, герпетиформний дерматит, червоний плоский лишай, склерозно-атрофічний лишай, піодерма гангренозна, саркоїд шкіри, дисковидний червоний вовчак, пемфігус, пемфігоїд, булезний епідермоліз, кропивниця, ангіоводянка, васкулітиди, токсичні еритеми, шкірні еозинофілії, осередкове облисіння, чоловіча плішивість, синдром Світа, синдром ВебераКристіана, багатоформна еритема; целюліт, інфекційний та не-інфекційний; гіподерміт; шкірна лімфома, немеланомний рак шкіри та інші диспластичні ураження; індуковані ліками розлади, охоплюючи сип на шкірі від ліків. (4) (очі) блефарит; кон'юнктивіт, охоплюючи багаторічний та весняний алергічний кон'юнктивіт;, ірит; передній та задній увеїт; хороїдит; автоімунний; вражаючі сітчатку дегенеративні або запальні розлади; офтальміт, охоплюючи симпатичний офтальміт; саркоїдоз; інфекції, охоплюючи вірусні, грибкові, та бактеріальні. (5) (шлунково-кишковий тракт) глоссит, гінгівіт, періоддонтит; езофагіт, охоплюючи рефлюкс; еозинофільний гастроентерит, мастоцитоз, хвороба Крона, коліт, охоплюючи виразковий коліт, проктит, з уд; хвороба черевної порожнини, синдром подразненої товстої кишки, та асоційцовані з їжею алергії, котрі можуть діяти поза кишечником (наприклад мігрень, риніт або екзема). (6) (абдомінальні) гепатит, охоплюючи автоімунний, алкогольний та вірусний; фіброз та цироз печінки; холецистит; панкреатит, гострий та хронічний. (7) (сечостатевий тракт) нефрит, охоплюючи інтерстиціальний та гломерулонефрит; нефротичний синдром; цистит, охоплюючи гострий та хронічний (інтерстиціальний) цистит та виразка Ханнера; гострий та хронічний уретрит, простатит, епідиміт, запалення придатків та сальпінгіт; вульвовагініт; хвороба Пейрона; еректильна дисфункція (самців та самиць). (8) (Відторгнення алотрансплантату) гостре та хронічне після, наприклад, трансплантації нирок, серця, печінки, легенів, кісткового мозку, шкіри або роговиці або після переливання крові; або хронічна хвороба трансплантат проти хазяїна; (9) (ЦНС) хвороба Альцгеіймера та інші дементні розлади, охоплюючи хворобу КрейцфельдаЯкоба; амілоїдоз; розсіяний склероз та інші синдроми демієлінізації; церебральний атеросклероз та васкуліт; скроневий артерит; важку міастенію; гострий та хронічний біль (гострий, періодичний або постійний, чи центрального або периферійного походження), охоплюючи вісцеральний біль, головний біль, мігрень, тригемінальну невралгію, атиповий лицьовий біль, біль суглобів та кісток, біль від інвазії раку та пухлин, синдроми невропатичного болю, охоплюючи діабетичні, післягерпетичні та ВІЛ-асоційовані невропатії; нейросаркоїдоз; злоякісні ускладнення центральної та периферійної нервової системи, інфекційні або автоімунні процеси. 14 (10) Інші автоімунні та алергічні розлади, охоплюючи тироїдит Хашимото, хворобу Граве, хворобу Аддісона, цукровий діабет, ідіопатичну тромбоцитопенічну пурпуру, еозинофільний фасцит, синдром гіпер-lgE, антифосфоліпідний синдром. (11) Інші розлади з запальним або імунологічним компонентом, охоплюючи синдром набутого імунодефіциту (СНІД), проказу, синдром Цезарі, та паранеопластичний синдроми. (12) (серцево-судинні); атеросклероз, вражаючий коронарний та периферійний кругообіг; перикардит; міокардит, запальні та автоімунні кардіоміопатії, охоплюючи міо-кардіальнмй саркоїд; ішемічні реперфузійні пошкодження; ендокардит, вальвуліт, та аортит, охоплюючи інфекційний (наприклад, сифілітичний); васкулітиди; розлади проксимальних та периферійних вен, охоплюючи флебіт та тромбоз, охоплюючи глибокий тромбоз вен та ускладнення варикозних вен. (13) (Онкологія) лікування звичайних типів раку, о хоплюючи пухлини простати, молочної залози, легенів, яєчнику, підшлункової залози, товстої кишки та ободової кишки, шлунку, шкіри та мозку та злоякісності кісткового мозку (охоплюючи лейкемії) та лімфо-проліферативної системи, як-то лімфома Ходжкінса та неХоджкінса, охоплюючи попередження та лікування метастазних хвороб та повторну появу пухлин, та паранеопластичні синдроми. (14) Хвороби, асоційцовані з підвищеними рівнями PGD2 або його метаболітів. Відтак, представлений винахід стосується сполуки формули (І), або її фармацевтично прийнятної солі або сольвату, що визначено вище, для застосування у терапії. Переважно сполуки винаходу застосовують для лікування хвороб, у котрих рецептор хемокіну належить до підсімейства рецепторів CRTh2. Конкретними станами, котрі можна лікувати сполуки винаходу є астма, риніт та інші хвороби, у котрих підвищені рівні PGD2 або його метаболітів. Переважно сполуки винаходу застосовують для лікування астми. Згідно з наступним аспектом, представлений винахід стосується застосування сполуки формули (І), або її фармацевтично прийнятної солі або сольвату, що визначено вище, у виробництві медикаменту для застосування у терапії, зокрема для лікування хвороби, опосередкованої CRTh2, як-то астма або риніт. Відтак, представлений винахід стосується сполуки формули (І), або її фармацевтично прийнятної солі або сольвату, що визначено вище, для застосування у терапії. Переважно сполуки винаходу застосовують для лікування хвороб, у котрих рецептор хемокіну належить до підсімейства рецептору CRTh2. Конкретними станами, котрі можна лікувати сполуками винаходу є астма, риніт та інші хвороби, у котрих підвищені рівні PGD2, або сполуки формули (І), або її фармацевтично-прийнятної солі або сольвату. Переважно, сполуки винаходу застосовують для лікування астми. Винахід також стосується комбінованих терапій, де сполуку формули (1) або її фармацевтично 15 84701 прийнятні солі, сольват або здатний до гідролізу in vi vo естер, або фармацевтичну композицію, що містить сполуку формули (1), застосовують одночасно або послідовно з терапією та/або засобом для лікування будь-чого одного з групи: астма, алергічний риніт, рак, COPD, ревматоїдний артрит, псоріаз, запальні хвороби товстої кишки, остеоартрит або остеопороз. Зокрема, для лікування запальних хвороб: ревматоїдний артрит, псоріаз, запальна хвороба товстої кишки, COPD, астма та алергічний риніт, сполуки винаходу можна комбінувати із засобами, як-то інгібітори TNF-α, як-то анти-TNF моноклональні антитіла (як-то ремікад, CDP-87G та D2E7.) та молекули імуноглобуліну рецептору TNF (як-то ЕнбреЛрег.), неселективні інгібітори СОХ-1/СОХ-2 (як-то піроксикам, диклофенак, пропіонові кислоти, як-то напроксен, флубіпрофен, фенопрофен, кетопрофен та ібупрофен, фенамати, як-то мефенамінова кислота, індометацин, суліндак, апазон, піразолони, як-то фенілбутазон, саліцилати, як-то аспірин), інгібітори СОХ-2 (як-то мелоксикам, целекоксиб, рофекоксиб, вальдекоксиб та еторикоксиб), нижня доза метотрексат, лефуномід; циклезонід, гідроксихлорохін, d-пеніциламін, ауранофін або парентеральне або пероральне золото. Представлений винахід також стосується комбінації сполуки винаходу з інгібітором біосинтезу лейкотриєну, інгібітором 5-ліпоксигенази (5-LO) або антагоністом активу-вального білку (FLAP) 5ліпоксигенази, як-то зилейтон; ABT- 761; фенлейтон; тепоксалін; Abbott-79175; Abbott-85761; N-(5заміщені)-тіофен-2-алкілсульфонаміди; 2,6-дітрет-бутилфенол гідразони; метокситетрагідропірани, як-то Zeneca ZD-2138; сполука SB-210661; піридиніл-заміщені 2-ціанонафталінові сполуки, якто L-739,010; 2-ціанохінолінові сполуки, як-то L746,530; сполуки індолу та хіноліну, як-то МК-591, MK- . 886, та BAY х 1005. Представлений винахід також стосується комбінації сполуки винаходу з рецептором антагоністу лейкотриєнів LTB4., LTC4., LTD4 ., та LTE4, вибраним з групи: фенотіазин-3-они, як-то L-651,392; амідино-сполуки, як-то CGS-25019c; бензоксаламіни, як-то онтазоласт; бензолкарбохімідаміди, якто BUL 284/260; та сполуки, як-то зафірлукаст, аблукаст, монтелукаст, пранлукаст, верлукаст (МК-679), RG-12525, Ro-245913, іралукаст (CGP 45715A), та BAY x 7195. Представлений винахід також стосується комбінації сполуки винаходу з інгібітором PDE4, охоплюючи інгібітори ізоформи PDE4D. Представлений винахід також стосується комбінації сполуки винаходу з антагоністами антигістамінового рецептору H1, як-то цетиризин, лоратадин, дезлоратадин, фекзофенадин, астемізол, азеластин, та хлорфенірамін. Представлений винахід також стосується комбінації сполуки винаходу з антагоністом гастропротективного, рецептору H2. Представлений винахід також стосується комбінації сполуки винаходу з судинозвужувальним симпатоміметичним засобом агоністом α1- та α2адреноцептору, як-то пропілгекседрин, фенілефрин, фенілпропаноламін, псевдоефедрин, нафа 16 золін хлорид, оксиметазолін хлорид, тетрагідрозолін хлорид, ксилометазолін хлорид, та етилнорепінефрин хлорид. Представлений винахід також стосується комбінації сполуки винаходу з антихолінергічними засобами, як-то іпратропіум бромід; тіотропіум бромід; окситропіум бромід; пірензепін та телензепін. Представлений винахід також стосується комбінації сполуки винаходу з агоністами β1- - β2адреноцептору, як-то метапротеренол, ізопротеренол, ізопреналін, альбутерол, сальбутамол, формотерол, салметерол, тербуталін, орсипреналін, бітолтерол мезилат, та пірбутерол; або метилксантаніни, охоплюючи теофілін та амінофілін; натрій хромоглікат; або антагоніст мускаринового рецептору (М1, М2 та М3). Представлений винахід також стосується комбінації сполуки винаходу з міметиком інсуліноподібного фактору росту типу І (IGF-1). Представлений винахід також стосується комбінації сполуки винаходу з інгаляційним глюкокортикоїдом зі зменшеною системнною побічною дією, як-то преднізон, преднізолон, флунізолід, триамцинолон ацетонід, беклометазон дипропіонат, будезонід, флутиказон пропіонат та мометазон фуроат. Представлений винахід також стосується комбінації сполуки винаходу з інгібітором матричних металопротеаз (MMP), тобто, стромелізини, колагенази та желатинази, а також анреканази; особливо колагенази-1 (ММР-1), колагенази-2 (ММР-8), колагенази-3 (ММР-13), стромелізину-1 (ММР-3), стромелізину-2 (ММР-10), та стромелізину-3 (ММР-11) та ММР-12. Представлений винахід також стосується комбінації сполуки винаходу з іншими модуляторами функції рецептор хемокіну, як-то CCR1, CCR2, CCR2A, CCR2B, CCR3, CCR4 CCR5, CCR6, CCR7, CCR8, CCR9, CCR10 та CCR11 (для сімейства CC); CXCR1, CXCR2, CXCR3, CXCR4 та CXCR5 (для сімейства C-X-C) та CX3CR1 для сімейства C-Х3-С. Представлений винахід також стосується комбінації сполуки винаходу з антивірус-ними засобами, як-то Viracept, AZT, ацикловір та фамцикловір, та антисептичними сполуками, як-то Valant. Представлений винахід також стосується комбінації сполуки винаходу з серцево-судинними засобами, як-то блокатори каналу кальцію, засоби зниження ліпідів, як-то ста-тини, фібрати, бетаблокатори, інгібітори Асе, антагоністи рецептору ангіотензину-2 та інгібітори агрегації тромбоцитів. Представлений винахід також стосується комбінації сполуки винаходу з засобами ЦНС, як-то антидепресанти (як-то сертралін), антипаркінсонові ліки (як-то депреніл, L-допа, Requip, Mirapex, інгібітори MAOB, як-то селегін та разагілін, інгібітори соmР, як-то Tasmar, інгібітори А-2, інгібітори ресорбції допаміну, антагоністи NMDA, агоністи нікотину, агоністи допаміну та інгібітори нейронної синтази нітроген оксиду), та ліки проти хвороби Альцгеймера, як-то донепезил, такрин, інгібітори СОХ-2, пропентофілін або метрифонат. Представлений винахід також стосується ком 17 84701 бінації сполуки винаходу з (і) інгібіторами тритптази; (іі) антагоністами фактору активуваня тромбоцитів (PAF): (ііі) інгібіторами ферменту перетворення інтерлейкіну (ICE); (iv) інгібіторами IMPDH; (v) інгібіторами адгезійних молекул, охоплюючи антагоністи VLA-4; (vi) катепсинами; (vii) інгібіторами МАР-кінази; (viii) інгібіторами глюкоза-6фосфа т-дегідрогенази; (іх) антагоністами рецепторів кініну B.sub1 та B.sub2; (x) засобами проти подагри, наприклад, колхіцином; (xi) інгібіторами ксантин-оксидази, наприклад, алопуринолом; (хіі) урикозуричними засобами, як-то, пробенецид, сульфінпіразон, та бензбромарон; (хііі) засобами посилення секреції гормону росту; (xi v) трансформувальним фактором росту (TGFP); (xv) похідним від тромбоцитів фактором росту (PDGF); (xvi) фактором росту фібробластів, наприклад, основним фактором росту фібробластів (bFGF); (xvii) гранулоцитом, фактором стимулювання колоній макрофагів (GM-CSF); (xviii) капсациновим кремом; (хіх) антагоністами рецептору тахікініну NK1 та NK3, вибраними з групи: NKP-6G8C; SB-233412 (талнентант); та D-4418; (хх) eiastase інгібіторами вибран з групи: UT-77 та ZD-0892; (ххі) інгібіторами ферменту перетворення TNFα (TACE); (ххіі) інгібіторами індукування синтази нітроген оксиду (iNOS) або (ххііі) хемоатрактантою рецептор-гомологічною молекулою, експресованою на клітинах TH2 . Сполуки представленого винаходу можна також застосовувати у комбінації з остеопорозними засобами, як-то ролоксифен, дролоксифен, лазофоксифен або фосомакс та імуносупресорами, якто FK-506, рапаміцин, циклоспорин, азатіоприн та метотрексат. Сполуки винаходу можна також застосовувати у комбінації з існуючими терапевтичними засобами для лікування остеоартриту. Придатні для застосування у комбінації засоби охоплюють стандартний нестероїдний антизапальний засіб (далі NSAID), як-то піроксикам, диклофенак, пропіонові кислоти, як-то напроксен, флубіпрофен, фенопрофен, кетопрофен та ібупрофен, фенамати, як-то мефенамінова кислота, індометацин, суліндак, апазон, піразолони, як-то фенілбутазон, саліцилати, як-то аспірин, інгібітори СОХ-2, як-то целекоксиб, вальдекоксиб, рофекоксиб та еторикоксиб, аналгетики та внутрішньосуглобовими терапіями, як-то кортикостероїди та гіалуронові кислоти, як-то гіалган та синвіск та антагоністи рецептору Р2Х7. Сполуки винаходу можна також застосовувати у комбінації з існуючими терапевтичними засобами для лікування раку. Придатні для застосування у комбінації засоби охоплюють: (і) антипроліферативні/антинеопластичні ліки та їх комбінації, що застосовують у медичній онкології, як-то полегшуючі засоби (наприклад цис-платина, карбоплатина, циклофосфамід, нітроген-гірчиця, мелфалан, хлорамбуцил, бусульфан та нітрозосечовини); антиметаболіти (наприклад анфолати, як-то флуорпіримідини типу 5-флуор урацилу та тегафур у, ралтитрексед, метотрексат, цитозин арабінозид, гідрокси-сечовина, гемцитабін та паклітаксел (Таксол®); антипухлинні антибіотики (наприклад антрацикліни типу адріаміцину, блеоміцину, доксорубіцину, дауноміцину, епірубіцину, ідарабіцину, 18 мітоміцину-С, дактиноміцину та мітраміцину); антимітотичні засоби (наприклад алкалоїди вінка типу вінкристину, вінбластину, віндезину та вінорелбіну, та таксоїди типу таксолу та таксотеру); та інгібітори топоізомерази (наприклад епіподофілотоксини типу етопозиду та теніпозиду, амсакрину, топотекану та камптотецину); (іі) цитотоксичні засоби, як-то антіестрогени (наприклад, ралоксифен, дролоксифен та йодоксифен), даун-регулятори рецептору естрогену (наприклад фулвестрант), антіандрогени (наприклад бікалутамід, флутамід, нілутамід та ципротерон ацетат), антагоністи LHRH або агоністи LHRH (наприклад госерелін, лейпрорелін та бусерелін), прогестогени (наприклад мегестрол ацетат), інгібітори ароматази (наприклад, анастрозол, летрозол, іоразол та екземістан) та інгібітори 5а-редукгази, як-то фінастерид; (ііі) Засоби, котрі інгібують інвазію ракових клітин (наприклад інгібітори металопротеїнази типу маримістату та інгібітори функції рецептору активатору плазміногену урокінази); (iv) інгібітори функції фактору росту, наприклад, такі інгібітори охоплюють антитіла фактору росту, антитіла рецептору фактору росту (наприклад антитіло antierbb2 трас-тубумаб [Herceptin™] та антитіло antierbbi цетуксимаб [С225]), інгібітори фарнезилтрансферази, інгібітори тирозин-кінази та інгібітори серин/треонін-кінази, наприклад, інгібітори сімейства епідермального фактору росту (наприклад сімейства інгібіторів EGER тирозинкінази, як-то N-(3-хлор-4-флуорфеніл)-7-метокси-6(3-морфолінопропокси)-хіназолін-4-аміну (гефі тиніб, A2D1839), N-(3-етинілфеніл)-6,7-біс(2метоксіетокси)-хіназолін-4-аміну (ерлотиніб, OSI774) та 6-акриламідо-N-(3-хлор-4-флуорфеніл)-7(3-морфолінопропокси)-хіназолін-4-аміну (Cl1033)), наприклад, інгібітори сімейства похідного від сімейства фактору росту тромбоцитів та, наприклад, інгібітори фактору росту гепатоцитів; (v) антиангіогенні засоби, як-то ті, котрі інгібують дію судинного ендотеліального фактору росту, (наприклад антитіло проти судинного ендотеліального фактору росту клітин бевацизумаб [Avastin™], сполуки, як-то розкриті [у міжнародних патентних заявках WO 97/22596, WO 97/30035, WO 97/32856 та WO 98/13354]), та сполуки, що діють за іншими механізми (наприклад ліномід, інгібітори інтегрину αvβ3 функції та ангіостатин); (vi) засоби судинної пошкоджуваності, як-то комбретастатин А4 та сполуки, розкриті [у міжнародних патентних заявках WO 99/02166, WO 00/40529, WO 00/41669, WO 01/92224, WO 02/04434 та WO 02/08213]; (vii) антисенсові терапії, наприклад, ті, котрі спрямовані на вищезазначені цілі, як-то ISIS 2503, антирас антисенс; (viii) підходи генної терапії, охоплюючи, наприклад, підходи для заміщення аберантних генів, якто підходи аберантного р53 або аберантного BRCA1 або BRCA2, GDEPT (ген-спрямована фермент терапія проліками), як-то застосовуючи цитозин-деаміназу, тимідин-кіназу або фермент бактеріальної нітроредуктази, та підходи для підвищення толерантності пацієнта до хемотерапі 19 84701 або радіотерапі, як-то генної терапії мультирезистеності до ліків; та (іх) підходи імунотерапії, охоплюючи, наприклад, підходи ex-vi vo та in vi vo для підвищення імуногенності клітин пухлини пацієнта, як-то трансфекція цитокінами, як-то інтерлейкіном 2, інтерлейкіном 4 або фактором стимулювання колоній гранулоцитів-макрофагів, підходи для зниження анергії Т-клітин, підходи, застосовуючи трансфектовані імунні клітини, як-то цитокінтрансфектовані дендритні клітини, підходи, застосовуючи лінії цитокін-трансфектованих клітин пухлин та підходи, застосовуючи антиідіотипові антитіла. У наступному аспекті представлений винахід стосується застосування сполуки формули (І), або її фармацевтично прийнятної солі або сольвату, що визначено вище, у виробництві у медикаменту для лікування хвороб або станів людини, у котрих модуляція активності рецептору CRTh2 є корисною. У контексті представленого опису, термін "терапія" також охоплює "профілактику" якщо не встановлено інше. Терміни "терапевтичний" та "терапевтично" слід застосовувати відповідно. Винахід також стосується способу лікування хвороби, опосередкованої PGD2 або його метаболітами, де простаноїд приєднується до свого рецептору (особливо рецептору CRTh2), котрий полягає у застосуванні до пацієнта терапевтично ефективної кількості сполуки формули (І), або її фармацевтично прийнятної солі, сольвату або проліків, що визначено вище. Винахід також стосується способу лікування запальних хвороб, особливо псоріазу, у пацієнта, що потерпає від вказаної хвороби або має її ризик, що полягає у застосуванні до пацієнта терапевтично ефективної кількості сполуки формули (І), або її фармацевтично прийнятної солі або сольвату, що визначено вище. Для вищезгаданих терапевтичних застосувань застосовувана доза, безумовно, залежить від застосовуваної сполуки, режиму застосування, потрібного лікування та вказаного розладу. Для вищезгаданих терапевтичних застосувань застосовувана доза, безумовно, залежить від застосовуваної сполуки, режиму застосування, потрібного лікування та вказаного розладу. Сполуку формули (І), її проліки та фармацевтично прийнятні солі та сольвати можна застосовувати як такі, але слід звичайно застосовувати у формі фармацевтичної композиції, у котрій сполука/сіль/сольват формули (І) (активний інгредієнт) є в асоціаціїз фармацевтично прийнятним ад'ювантом, розріджувачем або носієм. Залежно від режиму застосування, фармацевтична композиція переважно містить від 0,05 до 99мас.%, більш переважно від 0,05 до 80мас.%, ще краще від 0,10 до 70мас.%, та ще краще від 0,10 до 50мас.%, активного інгредієнту, усі мас.%% надано на основі загальної композиції. Представлений винахід також стосується фармацевтичної композиції, що містить сполуку формули (І), або її фармацевтично прийнятну сіль або сольват, як визначено вище, в асоціації з фа 20 рмацевтично прийнятним ад'ювантом, розріджувачем або носієм. Представлений винахід також стосується фармацевтичної композиції, що містить сполуку формули (І), або її фармацевтично прийнятну сіль або сольват, як визначено вище, в асоціації з фармацевтично прийнятним ад'ювантом, розріджувачем або носієм. Винахід далі ілюстровано необмежувальними прикладами, у котрих, якщо не встановлено інше: (і) заголовні та підзаголовні сполуки прикладів та способів були названі, застосовуючи програму ACD labs/name (версія 6,0) від Advanced Chemical Development lnc, Canada; (ii) якщо не встановлено інше, зворотнофазову препаративну ВЕРХ проводили, застосовуючи зворотно-фазову колонку з діоксидом силіцію Symmetry, NovaPak або Ex-Terra; (ііі) колонка для флеш-хроматографії стосується нормально-фазової хроматографії на діоксиді силіцію; (iv) розчинники сушили магній сульфатом чи натрій сульфатом; (v) випарювання проводили роторним випарюванням у вакуумі та обробку проводили після видалення залишків твердого продукту, як-то сушильні засоби, фільтруванням; (vi) якщо не встановлено інше, операції проводили при зовнішній температурі, що є у межах 1825°С, та в атмосфері інертного газу, як-то аргон чи азот; (vii) ви ходи надані тільки для ілюстрації та не є обов'язково максимально досяжними; (viii) структури кінцевих продуктів формули (1) підтверджували ядерним (звичайно протонним) магнітним резонансом (ЯМР) та масспектроскопією; значення хімічного зсуву протонного магнітного резонансу вимірювали на дельта шкалі, а мультиплетності піка показані так: s, синглет; d, дублет; t, триплет; т, мультиплет; br, широкий; q, квартет, quin, квінтет; (іх) інтермедіати звичайно не повністю охарактеризовано, а частот визначали тонко-шаровою хроматографією (ТШХ), високоефективною рідинною хроматографією (ВЕРХ), мас-спектрометрією (MC), ін фрачервоним (N) або ЯМР-аналізом; (х) мас-спектри (MC): описано звичайно тільки іони, котрі вказують вихідну масу, коли надано. Дані 1H ЯМР представлено у формі дельтазначень для головних діагностичних протонів і надано у частках на мільйон (чнм -1) відносно тетраметилсилану (TMC) як внутрішнього стандарту; (хі) застосовують наступні скорочення: Темп.пл.= точка плавлення ТГФ= тетрагідрофуран EtOAc= етилацетат MCPB А= мета-хлорпербензойна кислота ДМФ= N,N-диметилформамід MgSO4= магній сульфат Na2SO4= натрій сульфат NaHCO3= натрій гідрогенкарбонат Приклад 1 21 84701 4-(Ацетиламіно)-3-[(4-хлорфеніл)тіо]-2-метил1Н-індол-1-оцтова кислота і) 3-[{4-хлорфеніл)тіо]2-метил-4-нітро-1Н-індол При перемішуванні до розчину 3-нітроаніліну у ТГФ (700мл), що охолоджували до -78°С, додавали трет-бутил гіпохлорит (6,3г) краплями протягом 5 хвилин. Реакційній суміші давали нагрітися до 65°C протягом 20 хвилин перед тим, як додавали 1-[4-хлор феніл)тіо]-2-пропанон (11,6г) як розчин у ТГФ (20мл). Після 2 годин додавали триети-ламін (8,1мл) та реакційній суміші давали нагрітися до кімнатної температури. 2M HCI (водн) додавали до реакційної суміші перед концентруванням у вакуумі. Залишок суспендували у метанолі та твердий продукт, котрий осаджувався, виділяли фільтруванням, отримуючи підзаголовну сполуку (5,8г). 1 H ЯМР (ДМСО-d6) δ 12,55 (s, 1Н), 7,76 (dd, 1H), 7,63 (dd, 1H), 7,31-7,22 (m, 3H), 6,91 (dd, 2H), 2,47 (s, 3H) іі) 3-[(4-хлорфеніл)тіо]-2-метил-4-нітро-1Ніндол-оцтова кислота, етиловий естер При перемішуванні до суспензії натрій гідриду, 60% дисперсія у мінеральному маслі, (0,85г) у ТГФ (100мл) додавали продукт з етапу (і) (5,6г) як розчин у ТГФ (50мл). Після перемішування при кімнатній температурі протягом 30 хвилин додавали краплями етил бромацетат (2,3мл) протягом 10 хвилин. Після 2 годин реакційну суміш концентрували у вакуумі, залишок розчиняли в етилацетаті, промивали водою, розсолом, сушили магній сульфатом та концентрували у вакуумі. Перекристалізація з етанолу дала підзаголовну сполуку (5г). 1 H ЯМР (ДМСО-d6) δ 7,97 (dd, 1 H), 7,65 (dd, 1 H), 7,35 (t, 1 H), 7,26 (dt, 2H)1 6,92 (dt, 2Н), 5,40 (s, 2Н), 4,19 (q, 2H), 2,45 (s, 3H), 1,22 (t, 3H). ііі) 4-аміно-3-[(4-хлорфеніл)тіо]-2-метил-1Ніндол-оцтова кислота, етиловий естер Суспензію продукту з етапу (іі) (2,25г) в етанолі (170мл) перемішували у присутності 5% Pt/C (0,5г) під тиском водню 2бар. Після перемішування протягом ночі каталізатор видаляли фільтруванням та фільтрати концентрували у вакуумі. Очистка колонкою для флеш-хроматографії (14% ЕtOАс/гексан як елюент), дала підзаголовну сполуку (1,4г). 1 H ЯМР (ДMCO-d6) δ 7,30 (dd, 2H), 7,00 (dt, 2H), 6,85 (t, 1H), 6,68 (dd, 1H), 6,23 (dd, 1Н), 5,33 (s, 2Н), 5,09 (s, 2H), 4,16 (q, 2H), 2,33 (s, 3H), 1,21 (t, 3H). 3-[(4-хлорфеніл)тіо]-4-(етиламіно)-2-метил-1Ніндол-1-оцтова кислота, етиловий естер також виділяли як побічний продукт реакції (0,33г). 1 H ЯМР (ДMCO-d6) δ 7,32 (dd, 2H), 7,01 (dd, 2H), 6,95 (t, 1H), 6,73 (d, 1H), 6,16 (d, 1Н), 5,70 (t, 1H), 5,11 (s, 2Н), 4,16 (q, 2H), 3,05 (dt, 2H), 2,34 (s, 3H), 1,21 (t, 3H), 1,02 (t, 3H). iv) 4-(ацетиламіно)-3-[(4-хлорфеніл)тіо]-2метил-1Н-індол-оцтова кислота, етиловий естер 22 До розчину продукту з етапу (ііі) (0,5г) у дихлорметані (10мл) додавали триетиламін (0,18мл) та ацетилхлорид (0,1мл), реакційну суміш перемішували при кімнатній температурі протягом 30 хвилин. Суміш тоді абсорбували на силікагелі та очищали хроматографією на колонці (33% ЕtOАс/гексан як елюент), отримуючи підзаголовну сполуку (0,52г). 1 H ЯМР (ДМСO-d6) δ 9,51 (s, 1H), 7,46 (d, 1H), 7,34-7,27 (m, 3H), 7,11 (t, 1H), 6,97 (d, 2H), 5,24 (s, 2Н), 4,18 (q, 2H), 2,39 (s, 3H), 1,86 (s, 3H), 1,21 (t, 3H). v) 4-(ацетиламіно)-3-[(4-хлорфеніл)тіо]-2метил-1Н-індол-оцтова кислота До розчину продукту з етапу (iv) (0,31г) у ТГФ (10мл) додавали 1M розчин NaOH (водн) (0,75мл). Реакційну суміш перемішували протягом ночі при кімнатній температурі. Реакційну суміш концентрували у вакуумі та залишок розчиняли/суспендували у воді. рН доводили до 2, застосовуючи розбавлену HCI (водн) та твердий продукт, котрий осаджувався, виділяли фільтруванням. Перекристалізація з ацетонітрилу дала заголовну сполуку (0,16г). 1 H ЯМР (ДМСО-d6) δ 13,21 (s, 1Н), 9,51 (s, 1Н), 7,46 (d, 1H), 7,33 - 7,27 (m, 3H), 7,11 (t, 1H), 6,98 (d, 2H), 5,12 (s, 2H), 2,39 (s, 3H), 1,85 (s, 3H). ХІАТ+ [М+Н] 389 Темп.пл. розкл. >266°С Приклад 2 3-[(4-хлорфеніл)тіо]-2-метил-4[(метилсульфоніл)аміно1-1Н-індол-1 оцтова кислота іі) 3-[(4-хлорфеніл)тіо]-2-метил-4[(метилсульфоніл)аміно1-1Н-індол-1 оцтова кислота, етиловий естер До розчину продукту з прикладу 1, етап (ііі) (0,5г) у ди хлорметані (10мл) додавали триетиламін (0,18мл) та метансульфонілхлорид (0,1мл), та реакційну суміш перемішували при кімнатній температурі протягом 2 годин перед нагріванням при кипінні під зворотним холодильником протягом ночі. Дихлорметан видаляли у вакуумі, ацетонітрил додавали (10мл) та реакційну суміш гріли до 60°С протягом 5 годин. Суміш абсорбували на силікагелі та очищали хроматографією на колонці (33% ЕtOАс/гексан як елюент), отримуючи підзаголовну сполуку (0,44г). 1 H ЯМР (ДМСО-d6) δ 8,80 (s, 1H), 7,39 (d, 1H), 7,32 (d, 2H), 7,20-7,07 (m, 2H), 6,97 (d, 2H), 5,27 (s, 2Н), 4,18 (q, 2H), 2,74 (s, 3H), 2,38 (s, 3H), 1,22 (t, 3H). іі) 3-[(4-хлорфеніл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 1, етап (v), застосовуючи продукт з етапу (і). 23 84701 1 H ЯМР (ДМСО-d6) δ 13,25 (s, 1H), 8,80 (s, 1H), 7,39 (d, 1H), 7,32 (m, 2H), 7,16 (t, 1H), 7,09 (d, 1H), 6,98 (dt, 2H), 5,15 (s, 2H), 2,73 (s, 3H), 2,38 (s, 3H). XIAT- [M-H] 423 Темп.пл. розкл. >243°С Приклад 3 3-[(4-хлорфеніл)тіо]-2-метил-4-(5-піримідиніл)1Н-індол-оцтова кислота і) 4-бром3-[4(-хлорфеніл)тіо]-2-метил-1Н-індол 3-бромфеніл гідразин хлорид (15,34г) у воді (80мл) додавали до суспензії 1-[(4хлорфеніл)тіо]ацетону (13,77г) в ацетонітрилі (200мл) та перемішували протягом ночі при кімнатній температурі і тоді концентрували у вакуумі. Залишок розподіляли між водним натрій гідрогенкарбонатом та дихлорметаном. Органічну фазу промивали розсолом, сушили магній сульфатом та концентрували у вакуумі. Залишкове масло обробляли оцтовою кислотою (70мл) та гріли при 80°С протягом ночі. Реакційну суміш виливали у воду, підлужували водним натрій гідроксидом та екстрагували EtOAc (двічі). Комбіновані органічні продукти промивали (розсолом), сушили магній сульфатом та концентрували у вакуумі. Суміш очищали колонкою для флешхроматографії (40% ЕtOАс/гексан як елюент), отримуючи підзаголовну сполуку (4,43г). 1 H ЯМР (ДMCO-d6) δ 7,31 (s, 1Н),7,30 (d, 2H), 7,13 (dt, 2H),7,02(t, 1H), 6,94 (dt, 2H), 2,52 (s, 3H). ii) 4-бром3-[(4-хлорфеніл)тіо]-2-метил-1Ніндол-1-оцтова кислота, 1,1-диметилетиловий естер Підзаголовну сполуку отримували способом прикладу 1, етап (іі), застосовуючи продукт етапу (і) та трет-бутил бромацетат. Продукт очищали, застосовуючи хроматографію на колонці (10% ЕtOАс/гексан як елюент). 1 H ЯМР (CDCI3) δ 7,31 (dd, 1H), 7,21 (dd, 1H)1 7,14-7,10 (m, 2H), 7,05 (t, 1H), 6,94-6,91 (m, 2Н), 4,77 (s,2H), 2,49 (s, 3H), 1,43 (s, 9Н). ііі) 3-[(4-хлорфеніл)тіо]-2-метил)-4-(5піримідиніл)-1Н-індол-1-оцтова кислота, 1,1диметилетиловий естер До розчину/суспензії продукту з етапу (іі) (500мг) у толуолі (4мл) додавали етанол (1мл), 5піримідиніл-боронову кислоту (133мг), 2 M натрій карбонат (1,5мл) та кінцево тетракіс(трифенілфосфін)паладій(0), (125мг). Суміш гріли при 1000C протягом 3 діб. Очистка хроматографією на колонці (елюент 2: 1 гексан: EtOAc) дала підзаголовну сполуку як оранжевий твердий продукт (140мг). 1 H ЯМР (ДМСО-d6) δ 8,99 (s, 1H), 8,57 (s, 2H), 7,68 (d, 1H), 7,10 (dd, 2H), 6,99 (d,1Н), 7,30 (dt, 1H), 6,46 (dd, 2H), 5,21 (s, 2H), 2,42 (s, 3H), 1,45 (s, 9H). ііі) 3-[(4-хлорфеніл)тіо]-2-метил-4-(5піримідиніл)-1Н-індол-оцтова кислота 24 Заголовну сполуку отримували способом прикладу 1, етап (v), застосовуючи продукт з етапу (ііі), з очисткою зворотно-фазовою ВЕРХ (МеСN/NН3 (водн) як елюент). 1 H ЯМР (ДMCO-d6) δ 8,99 (s, 1H), 8,57 (s, 2Н), 7,69 (d, 1H), 7,29 (t, 1H), 7,10 (m, 2Н), 6,98 (d, 1H), 6,47 (m, 2H), 5,19 (s, 2Н), 2,43 (s, 3H). XIAT- [M-H] 408 Приклад 4 3-[(4-Хлорфеніл)тіо]-2-метил-4-піразиніл-1Ніндол-1-оцтова кислота і) 3-[(4-хлорфеніл)тіо]-2-метил-4-піразиніл-1Ніндол-1-оцтова кислота, 1,1-диметилетиловий естер До розчину продукту з прикладу 3, етап (іі) (0,4г) у толуолі (4мл) додавали 2трибутилстанілпіразин (0,32г) та тетракіс(трифенілфосфін)паладій(0) (0,1г). Реакційну суміш гріли до 80°С протягом 18 годин. Суміш абсорбували на оксиді силіцію та очищали, застосовуючи хроматографію на колонці (33% ЕtOАс/гексан як елюент), отримуючи підзаголовну сполуку (160мг). 1 H ЯМР (ДMCO-d6) δ 8,52 (d, 1H), 8,47 (d, 1H), 8,41 (t, 1H), 7,68 (d, 1H), 7,30 (t, 1Н), 7,13-7,09 (m, 3H), 6,55 (m, 2H), 5,21 (s, 2Н), 2,40 (s, 3H), 1,44 (s, 9H). іі) 3-[(4-хлорфеніл)тіо]-2-метил-4-піразиніл-1Ніндол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 1, етап (v), з очисткою препаративною ВЕРХ (MeCN/NH3 (водн) як елюент). Х Н ЯМР (ДMCО-d6) δ 5,50 (d, 1H), 8,45 (4 1H), 8,41 (dd, 1H), 756 (dd, 1H), 7,22 (dd, 1H), 7,13-7,09 (m, 2H), 7,04 (dd, 1H), 6,58 (dt, 2H), 4,68 (s, 2H), 2,38 (s, 3H). XIAT- [M-H] 408 Приклад 5 3-[(2-Xлopфeнiл)тio]-2-мeтил-5(мeтилcyльфoнiл)aмiнo]-1H-iндoл-1-оцтова кислота і) 2-метил-5-нітро-1Н-індол-1-оцтова кислота, етиловий естер 2-Метил-5-нітро-1Н-індол (5,3г) розчиняли у диметилформаміді (20мл) та додавали натрій гідрид (1,2г), суміш перемішували протягом 1 години. Етил бромацетат (6,8г) додавали та почав утворюватися осад. Суміш гасили 1% водною оцтовою кислотою та осад збирали фільтруванням та добре промивали водою, розтирали з діетиловим етером та сушили у вакуумі, отримуючи чистий підза 25 84701 головний продукт (6,2г). 2 H ЯМР (ДМСO-d6) δ 8,45 (d, 1H), 7,96 (dd, 1H), 7,59 (d, 1H), 6,56 (s, 1H), 5,21 (s, 2Н), 4,16 (q, 2H), 2,37 (s, 3H), 1,19 (t, 3H). XIAT- [M-H] 263 іі) 5-аміно-2-метил-1Н-індол-1-оцтова кислота, етиловий естер Суспензію 2-метил-5-нітро-1Н-індол-1-оцтової кислоти, етилового естеру (6,2г) в етанолі (600мл) у присутності 10% паладію на активованому вугіллі (0,6г) перемішували в атмосфері водню при 3 бар протягом 4 годин. Суміш фільтрували через броунмілерит та фільтрат випарювали, отримуючи підзаголовну сполуку як в'язке рожеве масло (5,3г). XIAT- [M-H] 233 ііі) 2-метил-3-[(метилсульфоніл)аміно]-1Ніндол-1-оцтова кислота, етиловий естер Метансуль фонілхлорид (1,15г) додавали до розчину 5-аміно-2-метил-1Н-індол-1-оцтової кислоти, етилового естеру (2,3г) у триетиламіні (1,7мл) та дихлорметані (20мл) при 0°С рожеве в'язке масло для рожевого в'язкого масла для та перемішували при 20°С протягом 1 години. Воду додавали та суміш екстрагували ди хлорметан, сушили натрій сульфатом та випарювали, отримуючи сирий твердий продукт. Це очищали хроматографією, застосовуючи оксид силіцію (40: 1 дихлорметан/етилацетат як елюент), отримуючи підзаголовну сполуку як рожевий твердий продукт (1,4г) 1 Н ЯМР (ДМСО-d6) δ 9,23 (s, 1Н), 7,30 (m, 2H), 6,94 (dd, 1Н), 6,23 (s, 1H), 5,03 (s, 2Н), 4,14 (q, 2H), 2,85 (s, 3H), 2,31 (s, 3H), 1,19 (t, 3H). XIAT- [M-H] 311 iv) 3-[(2-хлорфеніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота, етиловий естер 2-метил-5-[(метилсульфоніл)аміно]-1Н-індол1-оцтову кислоту, етиловий естер (0,31г) та 2хлорбензолтіол (0,27г) розчиняли у диметилформамід (3мл) та після додавання йоду 0,30г) перемішували при кімнатній температурі протягом ночі. Суміш виливали у водний натрій тіосульфат (50мл) та утворений білий осад збирали фільтруванням та промивали водою, сушили у вакуумі для перекристалізації з етанолу. Кристали збирали та промивали ізогексаном та сушили у вакуумі, отримуючи підзаголовну сполуку (0,20г) 1 H ЯМР (ДМСО-d6) δ 9,34 (s, 1H), 7,55 (d, 1H), 7,45 (m, H), 7,21 (d, 1H), 7,23-7,06 (m, 3H), 6,44 (m, 1Н), 5,26 (s, 2H), 4,18 (q, 2H), 2,83 (s, 3H), 2,38 (s, 3H), 1,22 (t, 3H). XIAT- [M-H] 453/455 v) 3-[(2-хлорфеніл)тіо]-2-метил-4[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 1, етап (v), за винятком того, що перекристалізація не була потрібною. (0,10г) 1 H ЯМР (ДMCO-d6) δ 13,25 (s, 1Н), 9,33 (s, 1H), 7,54 (d, 1H), 7,45 (dd, 1H), 7,21 (d, 1H), 7,08 (m, 3H), 26 6,45 (d, 1H), 5,13 (s, 2H), 2,83 (s, 3H), 2,38 (s, 3H). XIAT-[M-H] 425/427 Темп.пл. 212°С Приклад 6 3-[(3-хлорфеніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота і) 3-[(3-хлорфеніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота Підзаголовну сполуку отримували способом прикладу 5, етап (Iv), застосовуючи продукт прикладу 5, етап (iv) та 3-хлорбензолтіол (0,34г). XIAT- [M-H] 453/455 іі) 3-[(3-хлорфеніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 5, етап (v), застосовуючи продукт з прикладу 6, етап (і). 1 H ЯМР (ДМСО-d6) δ 13,25 (s, 1Н), 9,33 (s, 1H), 7,46 (d, 1H), 7,21 (m, 2H), 7,11 (dd, 1Н), 7,07 (dd, 1H), 6,95 (m, 2Н), 4,88 (s, 2H), 2,82 (s, 3H), 2,39 (s, 3H). XIAT+ [М+Н] 425/427 Темп.пл. 224°C Приклад 7 3-[(4-хлорфеніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота і) 3-[(4-хлорфеніл)тіо]-2-меттил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 5, етап (iv), застосовуючи продукт прикладу 5, етап (iv) та 4-хлорбензолтіол. XIAT- [M-H] 453/455 іі) 3-[(4-хлорфеніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 5, етап (v), застосовуючи продукт з етапу (і). 1H ЯМР (ДМСО-d6) δ 13,25 (s, 1H), 9,37 (s, 1H), 7,57 (d, 1H), 7,23 (d, 2H), 7,22 (d, 1H), 7,07 (dd, 1H), 6,96 (d, 2H), 5,11 (s, 2H), 2,82 (s, 3H), 2,39 (s, 3H). XIAT+ [M+H] 425/427 Темп.пл. 214°С. 27 84701 Приклад 8 3-[(3-Метоксифеніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота і) 3-[(3-Метоксифеніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 5, етап (iv), застосовуючи продукт прикладу 5, етап (iv) та 3-метоксибензолтіол XIAT- [M-H] 449 іі) 3-[(3-метоксифеніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 5, етап (v), застосовуючи продукт з етапу (і). 1 H ЯМР (ДMCO-d6) δ 13,25 (s, 1Н), 9,34 (s, 1H), 7,50 (d, 1H), 7,26 (d, 1Н, 7,08 (t, 1H), 7,06 (dd, 1H), 6,64 (dd, 1H), 6,55 (d, 1H), 6,47 (d, 1H), 5,11 (s, 2H), 3,62 (s, 3H), 2,82 (s, 3H), 2,40 (s, 3Н). XIAT- [M-H] 421 Темп.пл. 292°С Приклад 9 3-[(4-метоксифеніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота і) 3-[(4-метоксифеніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 5, етап (iv), застосовуючи продукт прикладу 5, етап (iv) та 4-метоксибензолтіол. XIAT- [M-H] 449 ii) 3-[(4-метоксифеніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 5, етап (v), застосовуючи продукт з етапу (і). 1 H ЯМР (ДМСО-d6) δ 13,25 (s, 1 H), 9,33 (s, 1 H), 7,46 (d, 1 H), 7,03 (d, 1 H), 7,04 (dd, 1Н), 7,00 (d, 2H), 6,81 (d, 2H), 5,07 (s, 2H), 3,67 (s, 3H), 2,83 (s, 3H), 2,42 (s, 3H). XIAT+ [М+Н] 421 Темп.пл. 215°C Приклад 10 28 3-[(2-трифлуорметилфеніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота і) 3-[(2-трифлуорметилфеніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 5, етап (iv), застосовуючи продукт прикладу 5, етап (iv) та 2-трифлуорметилбензолтіол. 1 H ЯМР (ДМСO-d6) δ 13,25 (s, 1Н), 9,35 (s, 1H), 7,72 (d, 1H), 7,54 (d, 1H), 7,36 (t, 1Н), 7,24 (t, 1H), 7,22 (s, 1H), 7,11 (dd, 1H), 6,73 (d, 1H), 5,12 (s, 2H), 2,82 (s, 3H), 2,40 (s, 3H). XIAT- [М+Н] 459 Темп.пл. 207°C Приклад 11 3-[(2-(8-хінолініл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота і) 3-[(2-(8-хінолініл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 5, етап (iv), застосовуючи продукт прикладу 5, етап (iv) та 8-хінолінтіол. іі) 3-[(2-(8-хінолініл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 5, етап (v), застосовуючи продукт з етапу (і). 1 H ЯМР (ДМСО-d6) δ 13,25 (s, 1Н), 9,29 (s, 1Н), 8,99 (dd, 1H), 8,38 (d, 1H), 7,65 (m, 2Н), 7,54 (d, 1H), 7,30 (t, 1H), 7,20 (s, 1H), 7,11 (dd, III), 6,68 (d, 1H), 5,14 (s, 2H), 2,80 (s, 3H), 2,40 (s, 3H). XIAT- [М+Н] 442 Темп.пл. 257°С Приклад 12. 3-[(2-(Метилетил)феніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота і) 3-[(2-(2-метилетил)феніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 5, етап (iv), застосовуючи продукт прикладу 5, етап (iv) та 2-(2-метилетил)бензолтіол. XIAT- [M-H] 461. іі) 3-[(-2-(2-метилетил)феніл)тіо]-2-метил-5[(метилсульфоніл)аміно]-1Н-індол-1-оцтова кислота 29 84701 Заголовну сполуку отримували способом прикладу 5, етап (v), застосовуючи продукт з етапу (і). 1 H ЯМР (ДМСО-d6) δ 13,25 (s, 1H)1 9,33 (s, 1H), 7,49 (d, 1H), 7,27 (d, 1H), 7,22 (d, 1Н), 7,06 (m, 2H), 6,89 (t, 1H), 6,50 (dd, 1H), 5,10 (s, 2H), 3,50 (m, 1Н), 2,81 (s, 3H), 2,39 (s, 3H), 1,33 (s,3H), 1,31 (s, 3H). XIAT+ [М+Н] 433 Темп.пл. 160°С Приклад 13 5-(Ацетиламіно)-3-[(4-хлорфеніл)тіо]-2-метил1Н-індолол-1-оцтова кислота і) 5-(ацетиламіно)-2-метил-1Н-індол-оцтова кислота, етиловий естер Ацетилхлорид (0,10г) додавали до розчину продукту з прикладу 5 частини іі) (0,28г) у ди хлорметані (10мл) та триетиламіні (0,2мл) при 0°C та залишали перемішуватися при 20°С протягом 1 години. Воду додавали та суміш екстрагували дихлорметаном, сушили натрій сульфатом та очищали хроматографією на колонці (елюючи 1:1 ізогексан/етилацетат), отримуючи підзаголовну сполуку як рожевий порошок (0,19г). 1 H ЯМР (ДMCO-d6) δ 9,69 (s, 1Н), 7,73 (d, 1H), 7,22 (d, 1H), 7,12 (dd, 1H), 6,18(s, 1H), 5,00 (s, 2Н), 4,13 (q, 2H), 2,30 (s, 3H), 2,02 (s, 3H), 1,20 (t, 3H). XIAT- [M-H] 275 іі) 5-(ацетиламіно)-3-[(4-хлорфеніл)тіо]-2метил-1Н-індол-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 5, етап (iv), застосовуючи продукт з етапу (і) (0,19г) та 4-хлорбензолтіол (0,20г). Суміш виливали у водний натрій тіосульфат, екстрагували етилацетатом, промивали водою, сушили натрій сульфатом та випарювали. Залишок перекристалізовували з етанолу, отримуючи підзаголовну сполуку як рожевий твердий продукт (0,13г). 1 H ЯМР (ДМСО-d6) δ 9,80 (s, 1H), 7,67 (d, 1H), 7,43 (d, 1H), 7,36 (dd, 1H), 7,27 (d, 2H), 6,94 (d, 2H), 5,20 (s, 2H), 4,16 (q, 2H), 2,39 (s, 3H), 1,98 (s, 3H), 1,21 (t, 3H). XIAT- [M-H] 417/419 iiі) 5-(ацетиламіно)-3-[(4-хлорфеніл)тю]-2метил-1Н-індол-оцтова кислота Заголовну сполуку отримували способом прикладу 5 етапу (v), застосовуючи продукт з етапу (іі). 1 H ЯМР (ДMCO-d6) δ 13,25 (s, 1H), 9,79 (s, 1H), 7,67 (d, 1H), 7,42 (d, 1H), 7,34 (dd, 1Н), 7,27 (d, 2H), 6,96 (d, 2H), 5,07 (s, 2H), 2,39 (s, 3H), 1,98 (s, 3H). ХІАТ+ [М+Н] 389/391 Темп.пл. 247°С Приклад 14 30 І 4-(Ацетилетиламіно)-3-[(4-хлорфеніл)тіо]-2метил-1Н-індол-1-оцтова кислота і) 4-(Ацетилетиламіно)-3-[(4-хлорфеніл)тіо]-2метил-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 1, етап (iv), застосовуючи побічний продукт з прикладу 1, етап (ііі). 1 H ЯМР (ДMCO-d6) δ 7,53 (d, 1H), 7,22-7,18 (m, 3H), 6,91-6,87 (m, 3Н), 5,21 (s, 2Н), 4,19 (q, 2H), 4,01 (m, 1H), 2,92-2,81 (m, 1H), 2,41 (s, 3H), 1,31 (s, 3H), 1,21 (t, 3H), 0,91 (t, 3H). іі) 4-(Ацетилетиламіно)-3-[(4-хлорфеніл)тіо]-2метил~1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 1, етап (v) та продукту з етапу (i). 1 H ЯМР (ДMCO-d6) δ 7,55 (d, 1H), 7,22 (dt, 2H), 7,18 (t, 1H), 6,89-6,86 (m, 3H), 4,99 (s, 2Н), 2,77 (m, 1Н), 4,02 (m, 1Н), 2,39 (s, 3H), 1,28 (s, 3H), 0,91 (t, 3H). ХІАТ+ [М+Н]417 Приклад 15 3-[(4-хлорфеніл)тіо]-4[цикпопропілкарбоніл)аміно]-2-метил-1Н-індол-1оцтова кислота і) 3-[(4-хлорфеніл)тіо]-4[циклопропілкарбоніл]аміно]-2-метил-1Н-індол-1оцтова кислота, етиловий естер. Підзаголовну сполуку отримували способом прикладу 1, етап (iv), застосовуючи продукт з прикладу 1, етап (ііі) та циклопропілкарбонілхлорид. 1 H ЯМР (ДМСО-d6) δ 9,74 (s, 1H), 7,49 (d, 1H), 7,43-7,26 (m, 3H), 7,10 (t, 1H), 6,98 (m, 2H), 5,24 (s, 2H), 4,18 (q, 2H), 2,40 (s, 3H), 1,53 (m, 1Н), 1,18 (t, 3H), 0,64 (m, 4Н). іі) 3-[(4-хлорфеніл)тіо]-4гциклопропілкарбоніл)аміно]-2-метил-1Н-індол-1оцтова кислота Підзаголовну сполуку отримували, застосовуючи спосіб прикладу 1, етап (v) та продукт з етапу (і). 1 H ЯМР (ДМСО-d6) δ 9,58 (s, 1Н), 7,60 (d, 1H), 7,28 - 7,22 (m, 3H), 7,09 (t, 1H), 7,02 (m, 2Н), 5,03 (s, 2Н), 2,41 (s, 3H), 1,50 (m, 1H), 0,68 (m, 4Н). XIAT- [M-H] 413 Темп.пл. 183-185°С. Приклад 16 31 84701 32 6,97 - 6,95 (m, 2H), 4,96 (s, 2H), 2,38 (s, 3H), 1,86 (s, 3H). XIAT- [M-H] 387 Приклад 18 4-(Бензоїламіно)-3-[(4-хлорфеніл)тіо]-2-метил1Н-індол-1-оцтова кислота і) 4-(Бензоїламіно)-3-[(4-хлорфеніл)тіо]-2метил-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 1, етап (iv), застосовуючи продукт з прикладу 1, етап (ііі) та бензоїлхлорид. 1 H ЯМР (ДМСO-d6) δ 10,25 (s, 1H), 7,84 (d, 1H), 7,75 (m, 2H), 7,59 (m, 1H), 7,50 (m, 2H), 7,40 (d, 1H), 7,21 (m, 3H), 6,88 (m, 2H), 5,28 (s, 2H), 4,19 (q, 2H), 2,40 (s, 3H), 1,17 (t, 3H). ii) 4-(бензоїламіно)-3-[(4-хлорфеніл)тіо]- 2метил-1Н-індол-1-оцтова кислота Заголовну сполук у отримували, застосовуючи спосіб прикладу 1, етап (v) та продукт з етапу (і). 1 H ЯМР (ДМСО-d6) δ 10,26 (s, 1Н), 7,86 (d, 1H), 7,75 (dt, 2H), 7,58 (m, 1H), 7,50 (m, 2Н), 7,36 (dd, 1H), 7,21 (dt, 2H)1 7,17 (t, 1H), 6,90 (dt, 2H), 5,03 (s, 2H), 2,40 (s, 3H). XIAT- [M-H] 449. Темп.пл. 213-215°С Приклад 17 4-(Ацетиламіно)-3-[(3-хлорфеніл)тіо]-2-метил1Н-індол-1-оцтова кислота і) 4-(ацетиламіно)-2-метил-1Н-індол-1-оцтова кислота, етиловий естер Тіосаліцилову кислоту додавали до розчину продукту з прикладу 1, етап (iv) (474мг) у трифлуороцтовій кислоті (10мл) додавали тіосаліцилову кислоту (351мг) та утворену суспензію гріли до 60°C протягом 4 годин. Суміш концентрували у вакуумі та залишок розчиняли в EtOAc та промивали NaHCO3 (водн), розсолом, сушили магній сульфатом та випарювали, отримуючи сирий матеріал. Очистка хроматографією на колонці (50% ЕtOАс/гексан як елюент) дала підзаголовну сполуку (0,13г). 1 H ЯМР (ДMCO-d6) δ 9,51 (s, 1Н), 7,54 (d, 1H), 7,07 (d, 1H), 6,96 (t, 1H), 6,50 (s, 1H), 5,02 (s, 2Н), 4,14 (q, 2H), 2,33 (d, 3H), 2,12 (s, 3H), 1,20 (t, 3H). ii) 4-(ацетиламіно)-3-[(3-хлорфеніл)тіо]-2метил-1Н-індол-1-оцтова кислота Підзаголовну сполуку отримували способом прикладу 5, етап (iv), застосовуючи продукт з етапу (і) (0,11г) та 3-хлорбензолтіол (0,048г), тоді очищали препаративною ВЕРХ (елюент MeCN/NH3 (водн)), отримуючи заголовну сполуку (70мг). 1 H ЯМР (ДMCO-d6) δ 9,49 (s, 1Н), 7,43 (d, 1H), 7,29 (d, 1H), 7,24 (t, 1H), 7,14 (dd, 1 H), 7,08 (t, 1H), 3-[(4-хлорфеніл)тіо]-4(диметиламіно)сульфонілІаміно]-2-метил-1Ніндол-1-оцтова кислота і) 3-[(4-хлорфеніл)тіо]-4(диметиламіно)сульфонілІаміно]-2-метил-1Ніндол-1-оцтова кислота, етиловий естер Триетиламін (55мл) та диметилсульфамоїлхлорид (43мл) додавали до розчину продукту з прикладу 1, етап (iv) (150мг) в ацетонітрилі (5мл). Суміш гріли при кипінні під зворотним холодильником протягом 24 годин, абсорбували на оксиді силіцію та очищали, застосовуючи хроматографію на колонці (33% ЕtOАс/гексан як елюент), отримуючи підзаголовну сполуку (95мг). 1 H ЯМР (ДМСО-d6) δ 8,80 (s, 1H), 7,35-7,29 (m, 3H), 7,13 (t, 1H), 7,07 (dd, 1H), 6,99 (dt, 2H), 5,25 (s, 2H), 4,18 (q, 2H), 2,56 (s, 6Н), 2,37 (s, 3H), 1,21 (t, 3H). іі) 3-[(4-хлорфеніл)тіо]-4(диметиламіно)сульфонілІаміно]-2-метил-1Ніндол-1-оцтова кислота Заголовну сполук у отримували, застосовуючи спосіб прикладу 1, етап(v) та продукт з етапу (і). 1 H ЯМР (ДMCO-d6) δ 8,79 (s, 1Н), 7,31 (m, 2H), 7,14 (dd, 1H), 7,04 - 6,99 (m, 4Н), 4,51 (s, 2Н), 2,54 (s, 6H), 2,34 (s, 3H). XIAT- [M-H] 452 Приклад 19 3-[(4-хлорфеніл)тіо]-2-метил-4-{[(1-метил-1Німідазол-4-іл)сульфоніл]аміно]-1H-індол-1-оцтова кислота і) 3-[(4-хлорфеніл)тіо]-2-метил-4-{[(1-метил-1Німідазол-4-іл)сульфоніл]аміно]-1H-індол-1-оцтова кислота, етиловий естер Триетиламін (75мл) та 1-метил-1Н-імідазол-4сульфонілхлорид (96мг) додавали до розчину продукту з прикладу 1, етап (ііі) (0,2г) в ацетонітрилі (20мл) та суміш гріли при кипінні під зворотним холодильником протягом ночі, охолоджували, абсорбували на оксиді силіцію та очищали, застосовуючи хроматографію на колонці (70% ЕtOАс/гексан як елюент), отримуючи підзаголовну сполуку як масло (245мг). 33 84701 1 H ЯМР (ДМСО-d6) δ 9,17 (s, 1Н), 7,73 (d, 1H), 7,63 (d, 1H), 7,32 (dt, 2H), 7,24 (dd, 1Н), 7,08-7,02 (m, 2H), 6,98 (dt, 2H), 5,20 (s, 2H), 4,15 (q, 2H), 3,60 (s, 3H), 2,33 (s, 3H),1,17 (t, 3H). іі) 3-[(4-хлорфеніл)тіо]-2-метил-4-{[(1-метил1Н-імідазол-4-іл)сульфоніл]аміно]-1Н-індол-1оцтова кислота. Заголовну сполук у отримували, застосовуючи спосіб прикладу 1, етап (v) та продукт з етапу (і). 1 H ЯМР (ДМСО-d6) δ 9,16 (s, 1Н), 7,73 (d, 1H), 7,62 (d, 1H), 7,31 (dt, 2H), 7,22 (dd, 1Н), 7,08 - 7,02 (m, 2H), 6,99 (dt, 2H), 5,01 (s, 2Н), 3,59 (s, 3H), 2,32 (s, 3H). XIAT- [M-H] 489 Приклад 20 3-[(4-хлорфеніл)тіо]-4[[(диметиламіно)ацетил]аміно]-2-метил-1Н-індол-1оцтова кислота і) 3-[(4-хлорфеніл)тіо]-4[[(диметиламіно)ацетил]аміно]-2-метил-1Н-індол-1оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 1, етап (iv), застосовуючи продукт з прикладу 1, етап (ііі) та (диметиламіно)-ацетилхлорид, хлорид. Продукт очищали, застосовуючи хроматографію на колонці (33% ЕtOАс/гексан як елюент). 1 H ЯМР (ДМСО-d6) δ 10,77 (s, 1H), 8,15 (d, 1H), 7,35-7,27 (m, 3H), 7,13 (t, 1H), 6,97 (d, 2H), 5,25 (s, 2H), 4,17 (q, 2H), 2,94 (s, 2H), 2,38 (s, 3H), 2,10 (s, 6H), 1,21 (t, 3H). ii) 3-[(4-хлорфеніл)тіо]-4[[(диметиламіно)ацетил]аміно]-2-метил-1Н-індол-1оцтова кислота; Заголовну сполук у отримували, застосовуючи спосіб прикладу 1, етап (v) та продукт з етапу (і). 1 H ЯМР (ДМСО-d6) δ 10,76 (s, 1Н), 8,10 (d, 1H), 7,30 (dt, 2H), 7,17 (d, 1H), 7,05 (t, 1Н), 6,98 (dd, 2H), 4,66 (s, 2H), 2,93 (s, 2Н),2,35 (s, 3H), 2,09 (s, 6H). XIAT- [M-H] 430 Приклад 21 4-(Ацетиламіно)-2-метил-3-[[4(метилсульфоруІ)феніл]тіо]-1Н-індол-1-оцтова кислота і) 4-(метилсульфоніл)бензолтіол 1-флуор-4-(метилсульфоніл)бензол та натрій дисульфід (10г) гріли у NMP (10мл) при 80°C протягом 2 годин. Суміш виливали у воду, промивали EtOAc, підкислювали концентрованою хлоридною 34 кислотою та екстрагували EtOAc. Органічні продукти промивали водою, сушили магній сульфатом та випарювали, отримуючи підзаголовну сполуку, котру застосовували у наступному етапі без охарактеризування. іі) 4-(ацетиламіно)-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота, етиловий естер. Підзаголовну сполуку отримували способом прикладу 5, етап (iv), застосовуючи продукт з етапу (і) та продукт з прикладу 17, етап (і), та очищали хроматографією (50% ЕtOАс/гексан підвищуючи до 66% ЕtOАс/гексан як елюент), отримуючи підзаголовну сполук. 1 H ЯМР (ДMCO-d6) δ 9,45 (s, 1H), 7,72 (dt, 2H), 7,38 (d, 1H), 7,32 (d, 1H), 7,16 - 7,11 (m, 3H), 5,27 (s, 2Н), 4,19 (q, 2H), 3,14 (s, 3H), 2,38 (s, 3H), 1,82 (s, 3H), 1,22 (t, 3H). iv) 4-(ацетиламіно)-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота Заголовну сполук у отримували, застосовуючи спосіб прикладу 1, етап (v) та продукт з етапу (іі). 1 H ЯМР (ДМСО-d6) δ 9,44 (s, 1H), 7,72 (dd, 2H), 7,38 (d, 1H), 7,31 (d, 1H), 7,17-7,10 (m, 3H), 5,14 (s, 2Н), 3,14 (s, H), 2,38 (s, 3H), 1,82 (s, 3H). XIAT- [M-H] 431 Приклад 22 4-(Ацетиламіно)-3-[(2-[(2-хлорфеніл)тіо]-2метил-1Н-індол-1-оцтова кислота 4-(Ацетиламіно)-3-[(2-хлорфеніл)тіо]-2-метил1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 5, етап (iv) та, застосовуючи продукт з прикладу 17, етап (і) та 2-хлортіофенол, та очищали хроматографією на колонці (33% ЕtOАс/гексан як елюент). Утворений продукт обробляли, як показано у приклад 1, етап (v), отримуючи заголовну сполуку. 1 H ЯМР (ДMCO-d6) δ 9,43 (s, 1 H), 7,46 (dd, 1H), 7,37 (dd, 2H), 7,14-7,05 (m, 3H), 6,42 (dd, 1H), 5,14 (s, 2Н), 2,37 (s, 3H), 1,81 (s, 3H). XIAT+ [М+Н] 389 Приклад 23 4-(ацетиламіно)-2-метил-3-[[4(етилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота і) 4-(ацетиламіно)-2-метил-3-[[4(етилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кис 35 84701 лота Заголовну сполуку отримували способом прикладу 5, етап (iv), застосовуючи продукт з прикладу 17, етап (і) та 4-(етилсульфоніл)бензолтіол. Продукт очищали препаративною ВЕРХ (елюент MeCN/NH3 (водн)). 1 H ЯМР (ДМСО-d6) δ 9,41 (s, 1Н), 7,66 (d, 2H), 7,30 (d, 2H), 7,17 (d, 2H), 7,08 (t, 1H), 4,85 (s, 2Н), 3,20 (q, 2H), 2,37 (s, 3H), 1,78 (s, 3H), 1,05 (t, 3H). ХІАТ- [M-H] 445. Приклад 24 3-[(4-хлорфеніл)тіо]-4[((етиламіно)карбоніл]аміно]-2-метил-1Н-індол-1оцтова кислота і) 3-[(4-хлорфеніл)тіо]-4[((етиламіно)карбоніл]аміно]-2-метил-1Н-індол-1оцтова кислота, етиловий естер Етил ізоціанат (32мл) додавали до розчину продукту з прикладу 1, етап (ііі) (150мг) у дихлорметані (10мл). Реакційну суміш перемішували при кімнатній температурі протягом 4 діб перед нагріванням при кипінні під зворотним холодильником протягом 24 годин. Суміш абсорбували на оксиді силіцію та очищали, застосовуючи хроматографію на колонці (33% ЕtOАс/гексан підвищуючи до 50% ЕtOАс/гексан як елюент), отримуючи підзаголовну сполуку (150мг). 1 H ЯМР (ДMCO-d6) δ 8,37 (s, 1Н), 7,57 (d, 1H), 7,28 (dt, 2H), 7,12 (dd, 1H), 7,06-6,98 (m, 3H), 6,81 (t, 1H), 5,19 (s, 2Н), 4,17 (q, 2H), 2,98 (dt, 2H), 2,37 (s, 3H), 1,21 (t, 3H), 0,96 (t, 3H). ii) 3-[(4-хлорфеніл)тю]-4{[(етиламіно)карбоніл]аміно]-2-метил-1Н-індол-1оцтова кислота Заголовну сполук у отримували, застосовуючи спосіб прикладу 1, етап (v) та продукт з етапу (і). 1 H ЯМР (ДMCO-d6) δ 8,39 (s, 1Н), 7,53 (dd, 1H), 7,26 (dt, 2H), 7,04 - 6,94 (m, 4H), 6,76 (t, 1H), 4,56 (s, 2Н), 2,98 (dt, 2H), 2,34 (s, 3H), 0,95 (t, 3H). XIAT+ [М+В] 418 Приклад 25 3-[[4-(Метилсульфоніл)феніл]тіо]-4-(5піримідиніл)-1Н-індол-1-оцтова кислота і) 4-бром-3-[[4-(Метилсульфоніл)феніл]тю]-4(5-піримідиніл)-1Н-індол Підзаголовну сполуку отримували способом прикладу 5, етап (iv), застосовуючи продукт з прикладу 21, етап (і) (0,89г) та 4-броміндол (0,96г). 36 Залишок очищали хроматографією (50% ЕtOАс/гексан як елюент), отримуючи підзаголовну сполуку (1,3г). 1 H ЯМР (ДМСО-d6) δ 12,18 (s, 1Н), 7,93 (s, 1H), 7,73 (d, 2H), 7,56 (d, 1H), 7,29 (d, 1Н), 7,17 (d, 2H), 7,12 (t, 1H), 3,14 (s, 3H). іі) 4-бром-3-[[4-(метилсульфоніл)феніл]тіо]-1Ніндол-1-оцтова кислота Натрій трет-бутоксид (1,37г) додавали до розчину продукту з етапу (і) (2,4г) у ДМФ (20мл) та суміш перемішували протягом 15 хвилин. Етил бромацетат (0,86мл) додавали та суміш перемішували протягом ще 30 хвилин, 1M натрій гідроксид (10мл) тоді додавали та суміш перемішували протягом 2 годин. Суміш розбавляли водою (200мл), промивали EtOAc (50мл), підкислювали 2M хлоридною кислотою та утворений твердий продукт відфільтровували та сушили, отримуючи підзаголовну сполуку (2,5г). 1 H ЯМР (ДMCO-d6) δ 7,86 (s, 1Н), 7,73 (d, 2H), 7,50 (d, 1H), 7,28 (d, 1H), 7,19 (d, 2Н), 7,11 (t, 1H), 4,73 (s, 2H), 3,14 (s, 3H) ііі) 3-{[4-(метилсульфоніл)феніл]тіо]-4-(5піримідиніл]-1Н-індол-1-оцтова кислота Продукт з етапу (іі) (0,4г), фенілборонову кислоту (0,17г), тетракіс(трифенілфосфін)паладій (100мг) та 2M водний натрій гідрогенкарбонат (2мл) розчиняли в етанолі (10мл) та гріли при кипінні під зворотним холодильником протягом 8 годин. Суміш охолоджували до кімнатної температури, розбавляли EtOAc (100мл), промивали водою та розсолом. Органічний розчин сушили магній сульфатом, фільтрували та випарювали у вакуумі та залишок очищали ВЕРХ, отримуючи заголовну сполуку (190мг). 1 H ЯМР (ДMCO-d6) δ 8,93 (s, 1H), 8,58 (s, 1H), 7,93 (s, 1H), 7,70 (а, 1Н); 7,52 (а, 2Н), 7,37 (t, 1H), 7,03 (d, 1H), 6,70 (d, 2H), 5,15 (s, 2Н), 3,12 (s, 3H). XIAT- [M-H] 438 Приклад 26 2-Метил-3-[[4-(метилсульфоніл)феніл]тіо]-4-(2тіофеніл)-1Н-індол-1-оцтова кислота і) 1-[(4-(метилсульфоніл)феніл]тіо]ацетон Продукт з прикладу 21, етап (і) (3,4г) розчиняли в ацетоні (100мл), додавали калій карбонат (3,0г), додавали краплями хлорацетон (1,5мл). Суміш перемішували при кімнатній температурі протягом 20 годин, концентрували, розподіляли між EtOAc та водою, сушили магній сульфатом та випарювали. Залишок очищали хроматографією (50% ЕtOАс/гексан як елюент), отримуючи підзаголовну сполуку (2,6г). 1 H ЯМР (400МГц, CDCI3) δ 7,84 (d, 2H), 7,43 (d, 2H), 3,81 (s, 2H), 3,06 (s, 3H), 2,34 (s, 3H). XIAT- [M-H] 243 Темп.пл. 95-7°C. іі) 4-бром-2-метил-3-[[4 37 84701 (метилсульфоніл)феніл]тіо]-1Н-індол Підзаголовну сполуку отримували способом прикладу 3, етап (і), застосовуючи продукт з етапу (і) (1,6г) та 3-бромфенілгідразин гідрохлорид (1,47г). Продукт очищали, застосовуючи хроматографію (30% ЕtOАс/гексан як елюент), отримуючи підзаголовну сполуку (0,5г). 1 H ЯМР (CDCI3) δ 8,41 (s, 1Н), 7,68 (d, 2H), 7,54 (s, 1H), 7,32 (d, 1H), 7,25 (d, 1H), 7,10 (d, 2H), 3,00 (s, 3H), 2,50 (s, 3H). XIAT- [M-H] 394 ііі) 4-бром-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота, 1,1-диметилетиловий естер Підзаголовну сполуку отримували способом прикладу 1, етап (іі), застосовуючи продукт етапу (і) та трет-бутилбромацетат. Продукт очищали, застосовуючи хроматографію (50% ЕtOАс/гексан як елюент), отримуючи підзаголовну сполуку (0,5г). XIAT+ [М+Н] 510 iv) 2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-4(2-тіофеніл)-1Н-індол-1-оцтова кислота, 1,1диметилетиловий естер Суміш паладій ацетату (24мг), три-ортотолілфосфін (64мг) та метанол (6мл) перемішували під азотом протягом 10 хвилин. Продукт етапу (іі) у метанолі (10мл) додавали, а потім натрій карбонат (1,12г) та тіофен-2-боронову кислоту (0,68г). Після перемішування протягом 45 хвилин при 80°C додавали ще паладій ацетат (24мг) та триорто-толілфосфін (64мг) у метанолі (1мл), а потім тіофен-2-боронову кислоту (0,2г) та толуол (5мл), реакційну суміш перемішували при 80°C протягом 1 години. Реакційну суміш концентрували у вакуумі, додавали воду та суміш екстрагували дихлорметаном. Органічний шар сушили магній сульфатом та концентрували у вакуумі. Залишок розчиняли у метанолі та обробляли натрій гідроксидом (5мл). Через 1 годину реакційну суміш концентрували у вакуумі, тоді очищали зворотнофазовою ВЕРХ, отримуючи заголовну сполуку (160мг). 1 H ЯМР (ДМСО-d6) δ 7,58 (m, 3H), 7,38 (d, 1H), 7,18 (t, 1H), 6,99 (d, 1H), 6,87 (m, 3H), 6,78 (s, 1H), 4,98 (s, 2Н), 3,11 (s, 3H), 2,38 (s, 3H). XIAT- [M-H] 456 Приклад 27 4-(3,5-диметил-4-ізоксазоліл)-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота Отримано способом прикладу 26, етап (iv), застосовуючи продукт прикладу 26, етап (іі) та 3,5диметтилізоксазоліл-4-боронову кислоту. Продукт очищали, застосовуючи зворотно-фазову препаративну хроматографію (елюент MeCN/NH3 (водн)), отримуючи заголовну сполуку (6мг). 1 H ЯМР (ДМСО-d6) δ 7,61 (d, 1H), 7,46 (d, 2H), 7,17 (t, 1H), 6,82 (d, 2H), 6,75 (d, 1H), . 4,57 (s, 2Н), 38 3,32 (s, 3H), 1,9 (s, 3H), 1,11 (s, 6H). XIAT- [М-Н] 469 Приклад 28 4-(3-Фураніл)-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота і) 4-(3-Фураніл)-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 26, етап (iv), застосовуючи продукт прикладу 27, етап (і) та фуран-3-боронову кислоту. Продукт застосовували без охарактеризування у етапі (іі). іі) 4-(3-Фураніл)-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 1, етап (v), застосовуючи продукт з етапу (і). Продукт очищали, застосовуючи ВЕРХ (елюент MeCN/NH3 (водн)), отримуючи заголовну сполуку(60мг). 1 H ЯМР (ДМСО-d6) δ 7,41-7,63 (m, 5H)1 7,17 (t, 1H), 6,9-6,96 (m, 3H), 6,36 (s, 1H), 5,18 (s, 2Н), 3,18 є, 3H), 2,4 (s, 3H). XIAT- [M-H] 440 Приклад 29 2-Метил-4-[(метилсульфоніл)аміно]-3-F-[4(метилсульфоніл)феніл]тю]-1Н-індол-1-оцтова кислота і) 2-метил-4-[(метилсульфоніл)аміно]-1Н-індол1-оцтова кислота Тіосаліцилову кислоту (0,35г) додавали до розчину продукту з прикладу 2, етап (і) (0,47г) у ТФОК (10мл). Суміш перемішували при кімнатній температурі протягом 1 години та тоді гріли протягом 60°C протягом 4 годин. ТФОК випарювали та залишок розчиняли у EtOAc. Ор ганічні продукти промивали водним натрій гідрогенкарбонатом та розсолом, сушили магній сульфатом та випарювали. Залишок очищали, застосовуючи хроматографію (50% EtOAc/гексан як елюент), отримуючи підзаголовну сполуку (0,16г). 1 H ЯМР (ДМСО-d6) δ 9,4 (s, 1Н), 7,19 (d, 1H), 6,95-7,04 (m, 2H), 6,53 (d, 1H), 5,04 (s, 2Н), 4,15 (q, 2H), 2,91 (s, 3H), 2,32 (d, 3H), 1,21 (t, 3H). іі) 2-метил-4-[(метилсульфоніл)аміно]-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 5, етап (iv), застосовуючи продукт з ета 39 84701 пу (і) та продукт з прикладу 21, етап (і). 1 H ЯМР (ДMCO-d6) δ 8,76 (s, 1H), 7,74 (dd, 2H), 7,44 (d, 1H), 7,07-7,21 (m, 4H), 5,29 (s, 2Н), 4,19 (q, 2H), 3,14 (s, 3H), 2,76 (s, 3H), 2,36 (s, 3H), 1,22 (t, 3H) ііі) 2-метил-4-[(метилсульфоніл)аміно]-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 1, етап (v), застосовуючи продукт з етапу (іі) та перекристалізовували з етанолу, отримуючи заголовну сполуку як блідо-рожевий твердий продукт (75мг). 1 H ЯМР (ДMCO-d6) δ 8,73 (s, 1H), 7,74 (d, 2H), 7,44 (d, 1H), 7,13-7,2 (m, 3H), 7,08 (d, 1H) 5,15 (s, 2Н), 3,14 (s, 3H), 2,76 (s, 3H), 2,36 (s, 3H). ХІАТ+ [М+Н] 469 Приклад 30 2-Метил-5-[(метилсульфоніл)аміно]-3-[[3(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота і) 2-Метил-5[(метилсульфоніл)феніл]карбамотіонова кислота, диметиловий естер Натрій гідрид (0,33г) додавали до розчину of 3(метилсульфоніл)фенол у ДМФ (10мл) та перемішували протягом 30 хвилин. Диметилкарбамотіоновий хлорид (1,1г) додавали та реакційну суміш гріли при 80°C протягом 4 годин. Суміш виливали у водний аміноній хлорид, екстрагували EtOAc, промивали водою, сушили магній сульфатом та випарювали у вакуумі. Залишок очищали, застосовуючи хроматографію (30-50% етер/гексан як елюент), отримуючи підзаголовну сполуку (1,3г). 1 H ЯМР (ДМСO-d6) δ 7,82 (dd, 1H), 7,69 (t, 1H), 7,59 (t, 1H), 7,39 (dd, 1H), 3,47 (s, 3H), 3,37 (s, 3H), 3,08 (s, 3H). XIAT+ [М+Н] 260. іі) S-[3-(метилсульфоніл)феніл]карбамотіонова кислота, диметиловий естер Продукт з етапу (і) (1,1г) розчиняли у N.Nдиметиланілін (3мл) та гріли при 220°C протягом 8 годин. Суміш охолоджували, виливали у 2M хлоридну кислоту та екстрагували EtOAc. Органічні продукти промивали 2M хлоридноюкислотою та водою, сушили магній сульфатом та випарювали у вакуумі. Масляний залишок обробляли етером, отримуючи підзаголовну сполуку як білий твердий продукт (0,9г). 1 H ЯМР (ДMCO-d6) δ 8,07 (d, 1H), 7,94 (dd, 1H), 7,79 (dd, 1H), 7,59 (t, 1H), 3,04-3,12 (m, 6H), 3,07 (s, 3H). XIAT [М+Н] 260 ііі) 3-(метилсульфоніл)бензолтіол Продукт з етапу (іі) (0,9г) суспендували у 2M натрій гідроксиді (70мл) та гріли при кипінні під зворотним холодильником протягом 1,5 годин, отримуючи коричневий розчин. The розчин охолоджували, екстрагували EtOAc, сушили магній су 40 льфатом та випарювали, отримуючи підзаголовну сполуку (0,45г). 1 H ЯМР (ДMCO-d6) δ 7,84 (m, 1H), 7,7 (m, 1H), 7,52 (m, 1H), 7,44 (t 1H), 3,67 (s, 1Н), 3,06 (s, 3H) XIAT- [M-H] 187 іv) 2-метил-5-[(метилсульфоніл)аміно]-3-[[3(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 5, етап (iv), застосовуючи продукт з етапу (ііі) (0,22г) та продукт з прикладу 5, етап (ііі) та перекристалізовували з етанол. 1 H ЯМР (ДMCO-d6) δ 7,58 (m, 2H), 7,34 (m, 2H), 7,18 (t, 2H), 6,28 (s, 1H), 4,89 (s, 2H), 4,25 (q, 2H), 3,06 (s, 3H), 2,96 (s, 3H), 2,49 (s, 3H), 1,28 (t, 3H). XIAT+ [M+NH4] 514 Темп.пл. 176-8°С, v) 2-метил-5-[(метилсульфоніл)аміно]-3-[[3(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 1, етап (v), застосовуючи продукт з етапу (iv). Основний розчин доводили до рН 5М хлоридною кислотою та утворений осад відфільтровували та сушили, отримуючи заголовну сполуку (0,19г). 1 H ЯМР (ДМСО-d6) δ 9,35 (s, 1H), 7,61 (m, 1H), 7,57 (d, 1H), 7,53 (d, 1H), 7,46 (t, 1H), 7,24 (d, 1H), 7,18 (m, 1Н), 7,08 (dd, 1H), 5,05 (s, 2H), 3,17 (s, 3H), 2,82 (s, 3H), 2,41 (s, 3H) XIAT+ [M+NH 4 ] 469 Темп.пл. 233-6°С. Приклад 31 2-метил-5-[(метилсульфоніл)аміно]-3-[[2(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота і) 1-флуор-2-(метилсульфоніл)бензол Розчин оксону (17г) у воді (85мл) додавали до розчину 2-флуортіоанізолу в ацетонітрилі (85мл) та суміш перемішували при кімнатній температурі протягом 20 годин. Суміш концентрували, екстрагували EtOAc, промивали водою, сушили магній сульфатом та випарювали, отримуючи підзаголовну сполуку (5,9г). 1 H ЯМР (ДMCO-d6) δ 7,98 (t, 1H), 7,66 (m, 1H), 7,35 (t, 1H), 7,26 (t, 1H), 3,23 (s, 3H) іі) 2-(метилсульфоніл)бензолтіол Підзаголовну сполуку отримували способом прикладу 26, етап (і), застосовуючи продукт з етапу (і) (5,4г). 1 H ЯМР (ДMCO-d6) δ 8,05 (d, 1H), 7,46 (m, 2H), 7,35 (m, 1H), 4,84 (s, 1H), 3,21 (s, 3H). XIAT- [M-H] 187 ііі)2-метил-5-[(метилсульфоніл)аміно]-3-[[2(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота, етиловий естер 41 84701 Підзаголовну сполуку отримували способом прикладу 5, етап (iv), застосовуючи продукт з етапу (іі) (1,3г) та продукт з прикладу 5, етап (ііі) (0,6г). Продукт очищали, застосовуючи хроматографію (50-67% ЕtOАс/гексан як елюент), отримуючи підзаголовну сполуку (0,18г). 1 H ЯМР (ДМСО-d6) δ 8,05 (d, 1H), 7,16-7,27 (m, 4H), 6,77 (dd, 1H), 6,33 (s, 1H), 4,9 (s, 2Н), 4,26 (q, 2H), 3,44 (s, 3H), 2,88 (s, 3H), 2,5 (s, 3H), 1,21 (t, 3H). XIAT+ [M+NH4] 514 Темп.пл. 174-7°С. v) 2-метил-5-[(метилсульфоніл)анізол-3-[[2(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота Отримано способом прикладу 1, етап (v), застосовуючи продукт з етапу (ііі). Основний розчин доводили до рН 5 0,5 M хлоридною кислотою та утворений осад фільтрували та сушили, отримуючи заголовну сполуку. 1 H ЯМР (ДMCO-d6) δ 9,38 (s, 1Н), 7,92 (dd, 1H), 7,53 (d, 1H), 7,39 (m, 1H), 7,31 (m, 1Н), 716 (d, 1H), 7,10 (dd, 1H), 6,75 (dd, 1H), 5,11 (s, 2H), 3,51 (s, 3H), 2,81 (а, 3Н), 2,41 (s, 3H). XIAT- [M+NH4] 486 Темп.пл. 227-30°С. Приклад 32 2-метил-5-[(метилсульфоніл)аміно]-3-[[2(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота і) 1-флуор-2-(метилсульфоніл)бензол Розчин оксону (17г) у воді (85мл) додавали до розчину 2-флуортіоанізолу в ацетонітрилі (85мл) та суміш перемішували при кімнатній температурі протягом 20 годин. Суміш концентрували, екстрагували EtOAc, промивали водою, сушили магній сульфатом та випарювали, отримуючи підзаголовну сполуку (5,9г). 1 H ЯМР (ДМСО-d6) δ 7,98 (t, 1H), 7,66 (m, 1H), 7,35 (t, 1H), 7,26 (t, 1H), 3,23 (s, 3Н). іі) 2-(метилсульфоніл)бензолтіол Підзаголовну сполуку отримували способом прикладу 26, етап (і), застосовуючи продукт з етапу (і) (5,4г). 1 H ЯМР (ДМСО-d6) δ 8,05 (d, 1H), 7,46 (m, 2H), 7,35 (m, 1Н), 4,84 (s, 1H), 3,21 (s, 3H). XIAT- [M-H] 187 ііі) 2-метил-5-[(метилсульфоніл)аміно]-3-[[2(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 5, етап (iv), застосовуючи продукт з етапу (іі) (1,3г) та продукт з прикладу 5, етап (ііі) (0,6г). Продукт очищали, застосовуючи хроматографію (50-67% ЕtOАс/гексан як елюент), отримуючи підзаголовну сполуку (0,18г). 1 H ЯМР (ДМСО-d6) δ 8,05 (d, 1H), 7,16-7,27 (m, 4H), 6,77 (dd, 1H), 6,33 (s, 1H), 4,9 (s, 2Н), 4,26 (q, 2H), 3,44 (s, 3H), 2,88 (s, 3H), 2,5 (s, 3H), 1,21 (t, 42 3H). XIAT+ [M+NH 4 ] 514 Темп.пл. 174-7°С. v) 2-метил-5-[(метилсульфоніл)анізол-3-[[2(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота Отримано способом прикладу 1, етап (v), застосовуючи продукт з етапу (ііі). Основний розчин доводили до рН5 0,5M хлоридною кислотою та утворений осад фільтрували та сушили, отримуючи заголовну сполуку. 1 H ЯМР (ДMCO-d6) δ 9,38 (s, 1Н), 7,92 (dd, 1H), 7,53 (d, 1H), 7,39 (m, 1H), 7,31 (m, 1H), 716 (d, 1H), 7,10 (dd, 1H), 6,75 (dd, 1H), 5,11 (s, 2H), 3,51 (s, 3H), 2,81 (а, 3Н), 2,41 (s, 3H). XIAT- [M+NH4] 486 Темп.пл. 227-30°С. Приклад 22 2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-5-(5піриміданіл)-1Н-індол-1-оцтова кислота 5-бром-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол і) Підзаголовну сполуку отримували способом прикладу 3, етап (і), застосовуючи продукт з прикладу 26, етап (і) (2,5г) та 4-бромфеніл гідразин хлорид (2,3г). Реакційну суміш випарювали до половини об'єму та утворений осад відфільтровували, промивали етер та сушили, одержуючи підзаголовну сполук у (2,2г). 1 H ЯМР (ДМСО-d6) δ 12,04 (s, 1Н), 7,73 (d, 2H), 7,4 (до, 2Н), 7,27 (dd, 1H), 7,14 (d, 2Н), 3,14 (s, 3H), 2,45 (s, 3H). XIAT- [M-H] 394 іі) 5-бром-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 1, етап (іі), застосовуючи продукт етапу (і), та продукт очи щали, застосовуючи хроматографію (33-50% EtOAc/гексан як елюент). 1 H ЯМР(ДMCO-d6) δ 7,71 (d, 2H), 7,64 (d, 1H), 7,34 (dd, 1H)1 7,16 (d, 1H), 7,1 (d, 2Н), 4,88 (s, 2Н), 4,24 (q, 2H), 3,0 (s, 3H), 2,47 (s, 3H) 1,29 (t, 3H). XIAT+ [М+Н] 482 ііі) 2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-5{5-піримідиніл)-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 3, етап (ііі), застосовуючи продукт етапу (іі) та піримідин-5-боронову кислоту. Проводили етап (ііі) без охарактеризування. iv) 2-метил-3-І[4-(метилсульфоніл)феніл]тіо]-5(5-піримідиніл)-1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 1, етап (v), застосовуючи продукт з етапу (ііі). Основний розчин доводили до рН5 0,5M хлоридною кислотою та утворений осад відфільтровували та сушили, отримуючи заголовну сполук у (21мг). 1 H ЯМР (ДMCO-d6) δ 9,38 (s, 1H), 9,09 (s, 2H), 43 84701 7,71-7,79 (m, 4H), 7,64 (dd, 1H), 7,17 (d, 2H), 5,23 (s, 2Н), 3,12 (s, 3H) 2,45 (s, 3H). ХІАТ+ [М+Н] 454 Темп.пл. >290°С. Приклад 33 2-Метил-3-[[4-(метилсульфоніл)феніл]тіо]-5-(2тіофеніл)-1Н-індол-1-оцтова кислота і) 2-Метил-3-[[4-(метилсульфоніл)феніл]тіо]-5(2-тіофеніл)-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 3, етап (ііі), застосовуючи продукт етапу (її) та тіофен-2-боронову кислоту. Застосовували без подальшого охарактеризування. її) 2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-5(2-тіофеніл)-1Н-індол-1-оцтова кислота. Заголовну сполуку отримували способом прикладу 1, етап (v), застосовуючи продукт з етапу (іі). Основний розчин доводили до рН5 0,5M хлоридною кислотою та утворений осад відфільтровували та сушили та перекристалізовували з ацетонітрилу, отримуючи заголовну сполуку. 1 H ЯМР (ДМСО-d6) δ 7,72 (d, 2H), 7,63 (d, 1H), 7,53 (m, 2H), 7,42 (d, 1H), 7,39 (t, 1Н), 7,18 (d, 2H), 7,08 (m, 1Н), 5,15 (s, 2H), 3,13 (s, 3H) 2,42 (s, 3H). ХІАТ+[М+Н] 458 Приклад 34 5-(3,5-диметил-4-ізоксазоліл-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол1-оцтова кислота і) 5-(3,5-диметил-4-ізоксазоліл-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1H-індол-1-оцтова кислота, етилов естер Підзаголовну сполуку отримували способом прикладу 3, етап (ііі), застосовуючи продукт етапу (іі) та 3,5-диметилізоксазоліл-4-боронову кислоту. Застосовували у наступному етапі без охарактеризування. іі) 5-(3,5-диметил-4-ізоксазоліл-2-метил-3-[[4(метилсульфоніл)феніл]тіо]-1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 1, етап (v), застосовуючи продукт з етапу (іі). Основний розчин доводили до рН5 0,5M хлоридною кислотою та утворений осад фільтрували, сушили та перекристалізовували з суміші циклогексан/етанол, отримуючи заголовну сполуку. 1 H ЯМР (ДМСО-d6) δ 7,73 (d, 2H), 7,66 (d, 1H), 7,24 (d, 1H), 7,19 (m, 3H), 5,19 (s, 2Н), 3,13 (s, 3H) 2,44 (s, 3BD, 2,31 (s, 3H), 2,13 (s, 3H). 44 XIAT+ [М+Н] 471 Приклад 35 2-Метил-3-[[4-(метилсульфоніл)феніл]тіо]-5-(3піридніл)-1Н-індол-1-оцтова кислота і) 2-метил-3-[[4-(метилсульфоніл)феніл]тіо]-5(3-піридніл)-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 3, етап (ііі), застосовуючи продукт етапу (іі) та піридин-3-боронову кислоту. 1 H ЯМР (CDCI3) δ 8,85 (s, 1Н), 8,54 (s, 1H)1 7,87 (m, 1H), 7,73-7,69 (m, 3Н}, 7,49 (d, 1Н), 7,39 (d, 1H), 7,33 (t, 1H), 7,14 (d, 2H), 4,95 (s, 2Н), 4,26 (q, 2H), 2,98 (s, 3Н), 2,51 (s, 3H),1,29 (t, 3H). іі) 2-Метил-3-[[4-(метилсульфоніл)феніл]тіо]-5(3-піридніл)-1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 1, етап (v), застосовуючи продукт з етапу (іі). Основний розчин доводили до рН5 0,5M хлоридною кислотою та утворений осад відфільтровували та сушили, отримуючи заголовну сполуку (20мг). 1 H ЯМР (ДMCO-d6) δ 8,84 (d, 1H), 8,5 (dd, 1H), 8,1 (m, 1H), 7,73-7,69 (d, 3H), 7,63 (d, 1H), 7,53 (dd, 1H), 7,43 (dd, 1H), 7,18 (d, 2H), 5,22 (s, 2H), 3,12 (s, 3H) 2,44 (s, 3H). ХІАТ+ [М+Н] 453 Приклад 36 2-Метил-3-[[4-(метилсул ьфоніл)феніл]тіо]-5(1Н-піразол-4-іл)-1Н-індол-1-оцтова кислота і) 2-Метил-3-[[4-(метилсульфоніл)феніл]тіо]-5(1Н-піразол-4-іл)-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку отримували способом прикладу 3, етап (ііі), застосовуючи продукт етапу (іі) та (1Н-піразол-4-іл)-боронову кислоту та застосовували у наступному етапі без охарактеризування. іі) 2-Метил-3-[[4-(метилсульфоніл)феніл]тіо]-5(1Н-піразол-4-іл)-1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 1, етап (v), застосовуючи продукт з етапу (іі). Основний розчин доводили до рН5 0,5M хлоридною кислотою та утворений осад відфільтровували та сушили, отримуючи заголовну сполуку. 1 H ЯМР (ДМСО-d6) δ 7,97 (s, 2H), 7,71 (d, 2H), 7,56 (d, 1H), 7,53 (s, 1Н), 7,45 (dd, 1Н), 7,15 (d, 2H), 5,14 (s, 2Н), 3,12 (s, 3H) 2,4 (s, 3H). ХІАТ-[М+Н] 442 45 84701 Приклад 37 4-(Ацетиламіно)-3-[(4-ціанофеніл)тіо]-2-метил1Н-індол-1-оцтова кислота і) 4-(ацетиламіно)-3-[(4-ціанофеніл)тіо]-2метил-1Н-індол-1-оцтова кислота, етиловий естер Підзаголовну сполуку було отримано способом прикладу 5, етап (iv), застосовуючи • продукт з прикладу 13, етап (і) (330мг) та 4меркаптобензонітрил (330мг). Очищали, застосовуючи хроматографією на колонці (3% EtOAc/ди хлорметан як елюент), отримуючи підзаголовну сполук у (300мг). 1 H ЯМР (ДМСО-d6) δ 9,33 (s, 1H), 8,07 (d, 1H), 7,47 (d, 2H), 7,23 (t, 1H), 7,09 (d, 2H), 7,02 (d, 1H), 4,88 (s, 2H), 4,23 (q, 2H), 2,44 (s, 3H), 1,93 (s, 3H), 1,28 (t, 3H). XIAT+ [M+H] 408 Темп.пл. 263-5°С. ii) 4-(ацетиламіно)-3-[(4-ціанофеніл)тіо]-2метил-1Н-індол-1-оцтова кислота Заголовну сполуку отримували способом прикладу 1, етап (v), застосовуючи продукт з етапу (іі). Основний розчин доводили до рН5 0,5M хлоридною кислотою та утворений осад фільтрували, сушили, отримуючи заголовну сполук у. 1 H ЯМР (ДМСО-d6) δ 7,63 (d, 2H), 7,37 (d, 1H), 7,27 (d, 1H), 7,13 (t, III), 7,07 (d, 2H), 5,13 (s, 2Н), 2,37 (s, 3H) 1,79 (s, 3H). ХІАТ+ [М+Н] 380 Фармакологічні дані Аналіз зв'язування ліганду [3H]PGD2 отримували від Perkin Elmer Life Sciences зі специфічною активністю 100210Кі/ммоль. Усі інші хімікати були аналітичного ґатунку. НЕК-клітини, що експресують rhCRTh2/GaI 6 звичайним чином тримали у DMEM, що містить 10% сироватки зародка теляти (НуСІоnе), 1мг/мл генетицину, 2мМ L-глутаміну та 1% замінних амінокислот. Для отримання мембран, липкі трансфектовані НЕК-клітини вирощували до конфлюєнтності у дво шарових установках культивування тканин (Fisher, номер по каталогу ТКТ-170-070Е). Максимальні рівні експресії рецептору були індуковані додаванням 500мМ натрій бутирату протягом останніх 18 годин культивації. Липкі клітини промивали буферованим фосфатом фізіологічним розчином (PBS, 50мл на установку культивування Комп’ютерна в ерстка Т. Чепелев а 46 тканин та відділяли додаванням 50мл на установку льодяного мембранного гомогенізаційного буферу [20мМ ГЕПЕС (рН7,4), 0,1мМ дитіотреїтолу, 1мМ ЕДТА, 0,1мМ фенілметилсульфонілфлуориду та 100мкг/мл бацитрацину]. Клітини гранулювали центрифугуванням при 220хg протягом 10 хвилин при 4°С, ресуспендували у половині початкового об'єму свіжого мембранного гомогенізаційного буферу та руйнували, застосовуючи гомогенізатор Politron протягом 2´20с, тримаючи туби у льоді у кожному разі. Незруйновані клітини видаляли центрифугуванням при 220хg протягом 10 хвилин при 4°C та фракцію мембран гранулювали центрифугуванням при 90000хg протягом 30 хвилин при 4°С. Кінцеву гранулу ресуспендували у 4мл на установку мембранного гомогенізаційного буферу та визначали вміст білку. Мембрани зберігали при -80°C у придатних аліквотах. Усі дослідження проводили у білих 96коміркових планшетах NBS з прозорим дном (Fisher). Перед дослідженням НЕК-клітин мембрани, що містять CRTh2, наносили на бісеринки SPA PVT WGA (Amersham). Для покриття мембрани інкубували з бісеринками звичайно при 25мкг мембранного білку на мг бісеринок при 4°C з постійним перемішуванням протягом ночі (оптимум концентрації покриття визначали для кожної партії мембран). Бісеринки гранулювали центрифугуванням (800хg протягом 7 хвилин при 4°С), промивали буфером для дослідження (50мM HEPES рH7,4, що містить 5мМ магній хлориду) та кінцево ресуспендували у буфері для дослідження при концентрації бісеринок 10мг/мл. Кожне дослідження містило 20мкл 6,25нМ [3H]PGD2 , 20мкл насичених мембранами бісеринок SPA у буфері для дослідження та 10мкл розчину сполуки або 13,14-дигідро-іб-кето-прсстагландину D2 (DK-PGD25 для визначення неспецифічного зв'язування, Cayman chemical company). Сполуки та DK-PGD2 розчиняли у ДМСО та розбавляли тим же розчинником до 100х потрібну кінцеву концентрацію. Буфер для дослідження додавали, отримуючи кінцеву концентрацію 10% ДМСО (сполуки мали при цьому 10 х потрібну кінцеву концентрацію) та це було розчином, що додавали до планшету для дослідження. Планшет для дослідження інкубували при кімнатній температурі протягом 2 годин та підраховували на рідинному сцинтиляційному лічильнику Waliac Microbeta (1 хвилина на комірку). Сполуки формули (l) мають значення IK50 менше 10мкМ. Конкретно, приклад 14 має plK50=6,65, приклад 26 має рІK50=8,35, а приклад 34 має рІK50=9,4. Підписне Тираж 28 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted indoles, methods for their production and their use
Автори англійськоюBonnert Roger, Rasul Rukhsana
Назва патенту російськоюЗамещенные индолы, способ их получения, их использования
Автори російськоюБоннерт Роджер, Расул Рухсана
МПК / Мітки
МПК: C07D 403/04, C07D 401/04, A61P 11/00, C07D 401/12, C07D 403/12, C07D 209/30, C07D 409/04, C07D 405/04, C07D 413/04
Мітки: отримання, застосування, спосіб, заміщені, індоли
Код посилання
<a href="https://ua.patents.su/23-84701-zamishheni-indoli-sposib-kh-otrimannya-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Заміщені індоли, спосіб їх отримання, їх застосування</a>
Попередній патент: Спосіб визначення часу роботи в захисному модулі
Наступний патент: Транспортний засіб високої прохідності з крокуючими ланками
Випадковий патент: Спосіб одержання оксалату заліза з відходів збагачення залізної руди












