Спосіб одержання сульфонамідів та проміжних сполук
Номер патенту: 96281
Опубліковано: 25.10.2011
Автори: Рак Міхаель, Льор Сандра, Кайл Міхаель, Плешке Аксель, Майєр Гуідо, Гебхардт Йоахім, Веверс Ян Хендрік, Шмідт Томас
Формула / Реферат
1. Спосіб одержання фторованих хлорангідридів м-нітробензойної кислоти формули IIА
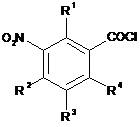 ІІA,
ІІA,
де замісники мають такі значення:
R1, R2, R3 та R4 - водень, галоген, ціано, нітро, С1-С6-алкіл, С1-С6-галогеналкіл, С1-С6-алкоксі або С1-С6-галогеналкоксі,
де щонайменше один з залишків R1 - R4 означає фтор,
шляхом взаємодії фторованих м-нітробензойних кислот формули VIIA
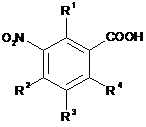 , VIIA,
, VIIA,
де замісники мають такі значення:
R1, R2, R3, R4 - водень, галоген, ціано, нітро, С1-С6-алкіл, С1-С6-галогеналкіл, С1-С6-алкоксі або С1-С6-галогеналкоксі,
де щонайменше один з залишків R1 - R4 означає фтор,
з хлоруючими сполуками VIII,
який відрізняється тим, що взаємодію проводять у присутності каталітичної кількості похідних фосфіну формули IX
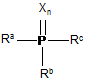 , IX
, IX
де замісники мають такі значення:
Ra, Rb, Rc - С1-С6-алкіл або феніл, що можуть бути при необхідності заміщені С1-С4-алкілом;
X - кисень чи зв'язані простим зв'язком два атоми хлору;
n - 0 або 1
2. Спосіб за п. 1, який відрізняється тим, що
R1 означає водень;
R2 - водень або галоген;
R3 - водень; та
R4 - водень або галоген,
де щонайменше один з залишків R2 - R4 означає фтор.
3. Спосіб за п. 1 або 2, який відрізняється тим, що хлоруючі сполуки VIII вибирають з групи, що складається з оксалілхлориду, трихлориду фосфору, пентахлориду фосфору, тіонілхлориду та фосфорилхлориду.
4. Спосіб за будь-яким з пп. 1-3, який відрізняється тим, що співвідношення хлоруючих сполук VIII до фторованих м-нітробензойних кислот формули VIIА становить 1,5-1.
5. Спосіб за будь-яким з пп. 1-4, який відрізняється тим, що похідні фосфіну формули IX вибирають з групи, що складається з трифенілфосфіну, трифенілфосфіноксиду та три-(С1-С6-алкіл)фосфіноксиду.
6. Спосіб за будь-яким з пп. 1-5, який відрізняється тим, що реакцію проводять додатково у присутності кислот Льюїса.
7. Спосіб за будь-яким з пп. 1-6, який відрізняється тим, що кислоту Льюїса вибирають з групи, що складається з борної кислоти, С1-С4-алкілового ефіру борної кислоти або циклічних ефірів борної кислоти.
8. Спосіб одержання сульфонамідів формули І
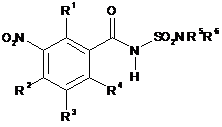 , І
, І
де замісники мають такі значення:
R1, R2, R3 та R4 - водень, галоген, ціано, нітро, С1-С6-алкіл, С1-С6-галогеналкіл, С1-С6-алкоксі або С1-С6-галогеналкоксі,
де щонайменше один з залишків R1 - R4 означає фтор,
R5 та R6 - водень, С1-С6-алкіл, С3-С6-алкеніл, С3-С6-алкініл, С3-С7-циклоалкіл, С3-С7-циклоалкеніл, С1-С6-алкоксі, феніл або бензил,
який відрізняється тим, що одержують фторовані хлорангідриди м-нітробензойної кислоти формули ІІА відповідно до будь-якого з пп. 1-7, та вводять їх у взаємодію з аміносульфонами формули III
H2N-SO2NR5R6, III
де замісники мають такі значення:
R5 та R6 - водень, С1-С6-алкіл, С3-С6-алкеніл, С3-С6-алкініл, С3-С7-циклоалкіл, С3-С7-циклоалкеніл, С1-С6-алкоксі, феніл або бензил.
9. Спосіб за п. 8, який відрізняється тим, що
R1 означає водень;
R2 - водень або галоген;
R3 - водень;
R4 - водень або галоген,
де щонайменше один з залишків R2 - R4 означає фтор;
та R5 та R6 означають С1-С6-алкіл.
Текст
1. Спосіб одержання фторованих хлорангідридів м-нітробензойної кислоти формули IIА 1 R 2 3 96281 фору, пентахлориду фосфору, тіонілхлориду та фосфорилхлориду. 4. Спосіб за будь-яким з пп. 1-3, який відрізняється тим, що співвідношення хлоруючих сполук VIII до фторованих м-нітробензойних кислот формули VIIА становить 1,5-1. 5. Спосіб за будь-яким з пп. 1-4, який відрізняється тим, що похідні фосфіну формули IX вибирають з групи, що складається з трифенілфосфіну, трифенілфосфіноксиду та три-(С1-С6алкіл)фосфіноксиду. 6. Спосіб за будь-яким з пп. 1-5, який відрізняється тим, що реакцію проводять додатково у присутності кислоти Льюїса. 7. Спосіб за будь-яким з пп. 1-6, який відрізняється тим, що кислоту Льюїса вибирають з групи, що складається з борної кислоти, С1-С4-алкілового ефіру борної кислоти або циклічних ефірів борної кислоти. 8. Спосіб одержання сульфонамідів формули І 1 O R 5 O2 N R N 2 R R 4 SO2N R R 6 H 4 де замісники мають такі значення: 1 2 3 4 R , R , R та R - водень, галоген, ціано, нітро, С1С6-алкіл, С1-С6-галогеналкіл, С1-С6-алкоксі або С1С6-галогеналкоксі, 1 4 де щонайменше один з залишків R - R означає фтор, 5 6 R та R - водень, С1-С6-алкіл, С3-С6-алкеніл, С3С6-алкініл, С3-С7-циклоалкіл, С3-С7-циклоалкеніл, С1-С6-алкоксі, феніл або бензил, який відрізняється тим, що одержують фторовані хлорангідриди м-нітробензойної кислоти формули ІІА відповідно до будь-якого з пп. 1-7, та вводять їх у взаємодію з аміносульфонами формули III 5 6 H2N-SO2NR R , III де замісники мають такі значення: 5 6 R та R - водень, С1-С6-алкіл, С3-С6-алкеніл, С3С6-алкініл, С3-С7-циклоалкіл, С3-С7-циклоалкеніл, С1-С6-алкоксі, феніл або бензил. 9. Спосіб за п. 8, який відрізняється тим, що 1 R означає водень; 2 R - водень або галоген; 3 R - водень; 4 R - водень або галоген, 2 4 де щонайменше один з залишків R - R означає фтор; 5 6 та R та R означають С1-С6-алкіл. 3 ,І Даний винахід стосується способу одержання сульфонамідів формули І де замісники мають наступні значення: 1 2 3 4 R ,R ,R та R водень, галоген, ціано, нітро, С1-С6-алкіл, С1-С6-галогеналкіл, С1-С6-алкоксі або С1-С6-галогеналкоксі; 5 6 R та R водень, С1-С6-алкіл, С3-С6-алкеніл, С3С6-алкініл, С3-С7-циклоалкіл, С3-С7-циклоалкеніл, С1-С6-алкоксі, феніл або бензил. У рівні техніки, наприклад у WO 01/83459, описано спосіб одержання гетероциклілзаміщених фенілсульфамоїлкарбоксамідів шляхом реакції похідних бензойної кислоти з сульфамідами у присутності агентів сполучення. Крім того, відомо, наприклад з WO04/39768, що N-ароїлсульфонаміди можуть бути одержані шляхом реакції відповідних похідних бензойної кислоти з діамідами сульфокислот у присутності основ, коли діаміди сульфокислот та основи піддають взаємодії з похідними бензойної кислоти. Задачею даного винаходу є розробка простого, економічного та ефективного способу одержання сульфонамідів формули І, де, з одного боку, значно зменшено утворення побічних продуктів, а з іншого - досягається високий вихід та чистота цільового продукту. Несподівано було знайдено, що ця задача вирішується за допомогою способу, за яким хлориди м-нітробенозойної кислоти формули II взаємодіють з аміносульфонами формули III у присутності 1,5-3 еквівалентів основ формули IV у перерахунку на аміносульфони формули III, вказані вище, що включає стадію а) у якій аміносульфони формули III взаємодіють з 0,1-1,3 еквівалентами основи формули IV, та стадію b) у якій реакційна суміш, утворена у стадії а), взаємодіє з хлоридами мнітро-бензойної кислоти формули II та залишковою кількістю основи формули IV, у розчині. Відповідно до зазначеного вище, даний винахід стосується способу одержання сульфонамідів формули І де замісники мають наступні значення: 1 2 3 4 R ,R ,R та R водень, галоген, ціано, нітро, С1-С6-алкіл, С1-С6-галогеналкіл, С1-С6-алкоксі або С1-С6-галогеналкоксі; 5 5 96281 6 R та R водень, С1-С6-алкіл, С3-С6-алкеніл, С3С6-алкініл, С3-С7-циклоалкіл, С3-С7-циклоалкеніл, С1-С6-алкоксі, феніл або бензил; реакцією хлоридів м-нітро-бензойної кислоти формули II 1 2 3 4 де замісники R ,R ,R та R мають вказані вище значення; з аміносульфонами формули III 5 6 H2N-SO2NR R III, 5 6 де замісники R та R мають вказані вище значення; у присутності В еквівалентів основи формули IV, визначеної вище, де на стадії а) аміносульфон формули III взаємодіє з В1 еквівалентів основи формули IV, та на стадії b) реакційна суміш зі стадії а) взаємодіє з хлоридом м-нітро-бензойної кислоти формули II та В2 еквівалентів основи формули IV; де В являє собою 1,5-3 еквівалентів основ формули IV у перерахунку на аміносульфон формули III; В1 являє собою частину від В та знаходиться у межах 0,1-1,3 еквівалентів основи формули IV у перерахунку на аміносульфон III; та В2 являє собою частину В та є різницею між В та В1. Сульфонаміди формули І, одержані способом за даним винаходом, можуть містити, в залежності від типу заміщення, декілька хіральних центрів, та існувати у вигляді суміші енантіо- або діастереомерів. Об'єктом винаходу є, таким чином, спосіб одержання як чистих енантіо- або діастереомерів, так і їхніх сумішей. 1 6 a b c Для замісників R -R , а також R , R та R , вказані органічні частини молекул означають збірні поняття для індивідуальних переліків окремих групових членів. Усі вуглецеві ланцюги, а також усі алкіл-, галогеналкіл-, алкоксі- та галогеналкоксіланцюги можуть бути як розгалуджені, так і нерозгалуджені. Якщо не вказано інше, то галогенові замісники означають, переважно, від одного до 5 однакових чи різних атомів галогенів. Галоген означає відповідно фтор, хлор, бром або йод. Надалі, наприклад: С1-С4-алкіл означає: наприклад метил, етил, нпропіл, 1-метилетил, н-бутил, 1-метилпропіл, 2метилпропіл та 1,1-диметилетил; С1-С6-алкіл означає: С1-С4-алкіл, як вказано вище, а також наприклад н-пентил, 1-метилбутил, 2-метилбутил, 3-метилбутил, 2,2-диметилпропіл, 1-етилпропіл, н-гексіл, 1,1-диметилпропіл, 1,2диметилпропіл, 1-метилпентил, 2-метилпентил, 3метилпентил, 4-метилпентил, 1,1-диметилбутил, 1,2-диметилбутил, 1,3-диметилбутил, 2,2диметилбутил, 2,3-диметилбутил, 3,3 6 диметилбутил, 1-етилбутил, 2-етилбутил, 1,1,2триметилпропіл, 1-етил-1-метилпропіл та 1-етил-3метилпропіл; С1-С4-галогеналкіл означає: С1-С4-алкільний залишок, як вказано вище, частково чи повністю заміщений фтором, хлором, бромом та/або йодом, а також, наприклад хлорметил, дихлорметил, трихлорметил, фторметил, дифторметил, трифторметил, хлорфторметил, дихлорфторметил, хлордифторметил, 2-фторетил, 2-хлоретил, 2брометил, 2-йодетил, 2,2-дифторетил, 2,2,2трифторетил, 2-хлор-2-фторетил, 2-хлор-2,2дифторетил, 2,2-дихлор-2-фторетил, 2,2,2трихлоретил, пентафторетил, 2-фторпропіл, 3фторпропіл, 2,2-дифторпропіл, 2,3-дифторпропіл, 2-хлорпропіл, 3-хлорпропіл, 2,3-дихлорпропіл, 2бромпропіл, 3-бромпропіл, 3,3,3-трифторпропіл, 3,3,3-трихлорпропіл, 2,2,3,3,3-пентафторпропіл, гептафторпропіл, 1-(фторметил)-2-фторетил, 1(хлорметил)-2-хлоретил, 1-(бромметил)-2брометил, 4-фторбутил, 4-хлорбутил, 4-бромбутил та нона-фторбутил; С1-С6-галогеналкіл означає: С1-С4галогеналкіл як вказано вище, а також, наприклад, 5-фторпентил, 5-хлорпентил, 5-бромпентил, 5йодпентил, ундекафторпентил, 6-фторгексіл, 6хлоргексіл, 6-бромгексіл, 6-йодгексіл та тридекафторгексіл; С2-С6-алкенілозначає: наприклад етеніл, 1пропеніл, 2-пропеніл, 1-метилетеніл, 1-бутеніл, 2бутеніл, 3-бутеніл, 1-метил-1-пропенил, 2-метил-1пропенил, 1-метил-2-пропенил, 2-метил-2пропенил, 1-пентеніл, 2-пентеніл, 3-пентеніл, 4пентеніл, 1-метил-1-бутеніл, 2-метил-1-бутеніл, 3метил-1-бутеніл, 1-метил-2-бутеніл, 2-метил-2бутеніл, 3-метил-2-бутеніл, 1-метил-3-бутеніл, 2метил-3-бутеніл, 3-метил-3-бутеніл, 1,1-диметил2-пропенил, 1,2-диметил-1-пропенил, 1,2-диметил2-пропенил, 1-етил-і-пропенил, 1-етил-2-пропенил, 1-гексеніл, 2-гексеніл, 3-гексеніл, 4-гексеніл, 5гексеніл, 1-метил-1-пентеніл, 2-метил-1-пентеніл, 3-метил-1-пентеніл, 4-метил-1-пентеніл, 1-метил2-пентеніл, 2-метил-2-пентеніл, 3-метил-2пентеніл, 4-метил-2-пентеніл, 1-метил-3-пентеніл, 2-метил-3пентеніл, 3-метил-3-пентеніл, 4-метил-3пентеніл, 1-метил-4-пентеніл, 2-метил-4-пентеніл, 3-метил-4-пентеніл, 4-метил-4-пентеніл, 1,1диметил-2-бутеніл, 1,1-диметил-3-бутеніл, 1,2диметил-1-бутеніл, 1,2-диметил-2-бутеніл, 1,2диметил-3-бутеніл, 1,3-диметил-1-бутеніл, 1,3диметил-2-бутеніл, 1,3-диметил-3-бутеніл, 2,2диметил-3-бутеніл, 2,3-диметил-1-бутеніл, 2,3диметил-2-бутеніл, 2,3-диметил-3-бутеніл, 3,3диметил-1-бутеніл, 3,3-диметил-2-бутеніл, 1-етил1-бутеніл, 1-етил-2-бутеніл, 1-етил-3-бутеніл, 2етил-1-бутеніл, 2-етил-2-бутеніл, 2-етил-3-бутеніл, 1,1,2-триметил-2-пропенил, 1-етил-1-метил-2пропенил, 1-етил-2-метил-1-пропенил та 1-етил-2метил-2-пропенил; С2-С6-алкініл означає: наприклад етініл, 1пропініл, 2-пропініл, 1-бутиніл, 2-бутиніл, 3бутиніл, 1-метил-2-пропініл, 1-пентиніл, 2пентиніл, 3-пентиніл, 4-пентиніл, 1-метил-2бутинил, 1-метил-3-бутинил, 2-метил-3-бутинил, 3метил-1-бутинил, 1,1-диметил-2-пропініл, 1-етил 7 2-пропініл, 1-гексиніл, 2-гексиніл, 3-гексиніл, 4гексиніл, 5-гексиніл, і-метил-2-пентинил, 1-метил3-пентинил, 1-метил-4-пентинил, 2-метил-3пентинил, 2-метил-4-пентинил, 3-метил-1пентинил, 3-метил-4-пентинил, 4-метил-1пентинил, 4-метил-2-пентинил, 1,1-диметил-2бутинил, 1,1-диметил-3-бутинил, 1,2-диметил-3бутинил, 2,2-диметил-3-бутинил, 3,3-диметил-1бутинил, 1-етил-2-бутинил, 1-етил-3-бутинил, 2етил-3-бутинил та 1-етил-1-метил-2-пропініл; С3-С8-циклоалкіл означає: наприклад циклопропіл, циклобутил, циклопентил, циклогексіл та циклогептіл; С3-С7-циклоалкеніл означає: наприклад 1циклопропенил, 2-циклопропенил, 1-циклобутеніл, 2-циклобутеніл, 1-циклопентеніл, 2-циклопентеніл, 1,3-циклопентадієніл, 1,4-циклопентадієніл, 2,4циклопентадієніл, 1-циклогексеніл, 2циклогексеніл, 3-циклогексеніл, 1,3циклогексадієніл, 1,4-циклогексадієніл, 2,5циклогексадієніл; 1-циклогептеніл, 3циклогептеніл, 4-циклогептеніл, 3,5циклогептідаєніл, 2,4-циклогептідаєніл, 1,3циклогептідаєніл, 1,3,5-циклогептатрієніл, 2,4,6циклогептатрієніл; С1-С4-алкоксі означає: наприклад метоксі, етоксі, пропоксі, 1-метилетоксі, Бутоксі, 1метилпропоксі, 2-метилпропоксі та 1,1диметилетоксі; С1-С6-алкоксі означає: С1-С4-алкоксі як вказано вище, а також наприклад пентоксі, 1-метил бутоксі, 2-метилбутоксі, 3-метоксилбутоксі, 1,1-диметилпропоксі, 1,2-диметилпропоксі, 2,2диметилпропоксі, 1-етилпропоксі, гексоксі, 1метилпентоксі, 2-метилпентоксі, 3-метилпентоксі, 4-метилпентоксі, 1,1-ди-метилбутоксі, 1,2диметилбутоксі, 1,3-диметилбутоксі, 2,2диметилбутоксі, 2,3-диметилбутоксі, 3,3диметилбутоксі, 1-етилбутоксі, 2-етилбутоксі, 1,1,2-три-метилпропоксі, 1,2,2-триметилпропоксі, 1-етил-1-метилпропоксі та 1-етил-2-метилпропоксі; С1-С4-галогеналкоксі означає: С1-С4алкоксильний залишок, як вказано вище, частково чи повністю заміщений фтором, хлором, бромом та /або йодом, а також, наприклад, фторметоксі, дифторметоксі, трифторметоксі, хлордифторметоксі, бромдифторметоксі, 2-фторетоксі, 2хлоретоксі, 2-бромметоксі, 2-йодетоксі, 2,2дифторетоксі, 2,2,2-трифторетоксі, 2-хлор-2фторетоксі, 2-хлор-2,2-дифторетоксі, 2,2-дихлор-2фторетоксі, 2,2,2-трихлоретоксі, пентафторетоксі, 2-фторпропоксі, 3-фторпропоксі, 2-хлорпропоксі, 3-хлорпропоксі, 2-бромпропоксі, 3-бромпропоксі, 2,2-дифторпропоксі, 2,3-дифторпропоксі, 2,3дихлорпропоксі, 3,3,3-трифторпропоксі, 3,3,3трихлорпропоксі, 2,2,3,3,3-пентафторпропоксі, гептафторпропоксі, 1-(фторметил)-2-фторетоксі, 1(хлорметил)-2-хлор-етоксі, 1-(бромметил)-2брометоксі, 4-фторбутоксі, 4-хлорбутоксі, 4бромбутоксі та нонафторбутоксі; С1-С6-галогеналкоксі означає: С1-С4галогеналкоксі, як вказано вище, а також, наприклад 5-фторпентоксі, 5-хлорпентоксі, 5бромпентоксі, 5-йодпентоксі, ундекафторпентоксі, 96281 8 6-фторгексоксі, 6-хлоргексоксі, 6-бромгексоксі, 6йодгексоксі та тридекафторгексоксі; У найбільш переважних втіленнях способу за 1 2 3 4 5 6 даним винаходом замісники R , R , R , R , R та R мають такі значення, де ці замісники окремо чи у комбінації являють найбільш переважне втілення способу за даним винаходом: Переважними є такі втілення способу за даним винаходом, де 1 R означає водень, галоген або С1-С6-алкіл; переважно, водень або галоген; більш переважно, водень, фтор або хлор; особливо переважно, водень; Також переважними є такі втілення способу за даним винаходом, де 2 R означає водень, галоген, ціано, С1-С6-алкіл або С1-С6-галогеналкіл; переважно, водень або галоген; більш переважно, водень, фтор або хлор; особливо переважно, водень або фтор, найбільш переважно, водень; аналогічно, найбільш переважно, фтор. Також переважними є такі втілення способу за даним винаходом, де 2 R означає водень або галоген; переважно, галоген; більш переважно, фтор або хлор; особливо переважно, фтор. Також переважними є такі втілення способу за даним винаходом, де 3 R означає водень, галоген або С1-С6-алкіл; переважно, водень або галоген; більш переважно, водень, фтор або хлор; особливо переважно, водень. Також переважними є такі втілення способу за даним винаходом, де 4 R означає водень, галоген, ціано, С1-С6-алкіл або С1-С6-галогеналкіл; переважно, водень, галоген або ціано; більш переважно, водень, фтор, хлор або ціано; особливо переважно, водень, хлор або ціано, найбільш переважно, водень; аналогічно, найбільш переважно, хлор або ціано; ще найбільш переважно, хлор. Також переважними є такі втілення способу за даним винаходом, де 4 R означає галоген або ціано; переважно, галоген; більш переважно, фтор або хлор; особливо переважно, хлор. Також переважними є такі втілення способу за даним винаходом, де 4 R означає водень, галоген або ціано; переважно, водень або галоген; більш переважно, водень, фтор або хлор; особливо переважно, водень або хлор. Також переважними є такі втілення способу за даним винаходом, де 5 6 R та R незалежно означають водень, С1-С6-алкіл або С2-С6-алкеніл; переважно, водень або С1-С6-алкіл; більш переважно, С1-С6-алкіл; особливо переважно, С1-С4-алкіл. 9 Також переважними є такі втілення способу за даним винаходом, де 5 R означає водень або С1-С6-алкіл; переважно, водень або С1-С4-алкіл; більш переважно, С1-С4-алкіл; особливо переважно, метил. Також переважними є такі втілення способу за даним винаходом, де 6 R означає водень або С1-С6-алкіл; переважно, водень або С1-С4-алкіл; більш переважно, С1-С4-алкіл. Ще в одному переважному втіленні способу за 1 2 3 4 даним винаходом замісники R ,R ,R ,R мають значення, вказані вище, зокрема, як переважні значення, вказані вище, де, щонайменше, один із 1 4 залишків R -R означає фтор. Ще в одному переважному втіленні способу за 1 2 3 4 даним винаходом, замісники R ,R ,R та R мають такі значення: 1 R водень; 2 R водень або галоген; переважно, галоген; більш переважно, фтор; 3 R водень; та 4 R водень, хлор або ціано, переважно, хлор або ціано; більш переважно, хлор. Ще в одному переважному втіленні способу за 1 2 3 4 даним винаходом, замісники R ,R ,R та R мають такі значення: 1 R водень; 2 R водень або галоген; переважно, галоген; більш переважно, фтор; 3 R водень; 4 та R водень або галоген, переважно, водень або хлор; більш переважно, хлор, аналогічно, більш переважно, водень. Ще в одному переважному втіленні способу за 1 2 3 4 даним винаходом, замісники R ,R ,R та R мають такі значення: 1 R водень; 2 R фтор; 3 R водень; та 4 R галоген, переважно, хлор. Ще в одному переважному втіленні способу за 1 2 3 4 5 даним винаходом, замісники R ,R ,R ,R та R мають такі значення: 1 R водень; 2 R водень або галоген; переважно, галоген; більш переважно, фтор; 3 R водень; та 4 R водень або галоген, переважно, водень або хлор; більш переважно, хлор, аналогічно, більш переважно, водень; 5 6 R та R водень, С1-С6-алкіл або С2-С6-алкеніл; переважно, водень або С1-С6-алкіл; більш переважно, С1-С6-алкіл; особливо переважно, С1-С4-алкіл. У переважному втіленні способу за даним винаходом одержують сульфонаміди формули ІА 96281 10 де замісники мають наступні значення: 1 2 3 4 R ,R ,R та R водень, галоген, ціано, нітро, С1-С66-алкіл, С1-С6-галогеналкіл, С1-С6-алкоксі або С1-С6-галогеналкоксі; та 1 4 де, щонайменше, один з залишків R -R означає фтор, а 5 6 R та R - водень, С1-С6-алкіл, С3-С6-алкеніл, С3-С6-алкініл, С3-С7-циклоалкіл, С3-С7циклоалкеніл, С1-С6-алкоксі, феніл або бензил. Ще в одному переважному втіленні способу за даним винаходом одержують сульфонаміди формули І.а 2 3 4 5 6 1 3 4 5 6 1 2 4 5 6 де замісники R ,R ,R ,R та R є такими, як визначено вище, зокрема, як вказано вище для переважних втілень. Ще в одному переважному втіленні способу за даним винаходом одержують сульфонаміди формули І.b де замісники R ,R ,R ,R та R є такими, як визначено вище, зокрема, як вказано вище для переважних втілень. Ще в одному переважному втіленні способу за даним винаходом можна одержати сульфонаміди формули І.с де замісники R ,R ,R ,R та R є такими, як визначено вище, зокрема, як вказано вище для переважних втілень. Ще в одному переважному втіленні способу за даним винаходом можна одержати сульфонаміди формули I.d 11 96281 1 2 3 2 4 5 5 6 де замісники R ,R .R ,R та R є такими, як визначено вище, зокрема, як вказано вище для переважних втілень. Ще в одному переважному втіленні способу за даним винаходом можна одержати сульфонаміди формули l.e 6 де замісники R ,R ,R та R є такими, як визначено вище, зокрема, як вказано вище для переважних втілень, та де, щонайменше, один із залишків 2 4 R та R означає фтор. Ще в одному переважному втіленні способу за даним винаходом, положення замісників по відношенню один до одного, являють собою незалежно від комбінації, у якій вони наведені, найбільш переважне втілення способу за даним винаходом. Хлориди м-нітро-бензойної кислоти формули II та аміносульфони формули III можуть реагувати в еквімолярних кількостях. Придатними є молярні кількості, де хлориди мнітро-бензойної кислоти формули II, переважно, фторовані хлориди м-нітро-бензойної кислоти формули llА та аміносульфони формули III реагують між собою у співвідношеннях, 1:0.9-1,8; переважно 1:0,9-1,5; більш переважно 1:0,9-1,2; особливо переважно 1:0,95-1,2; найбільш переважно 1:0,951,1 у перерахунку на II, переважно llА, з утворенням III. Реакцію за даним винаходом - взаємодію хлориді м-нітро-бензойної кислоти формули II з аміносульфонами формули III, здійснюють, зазвичай, при температурах від - 30 °C до 120 °C, переважно, від - 10 °C до 100 °C, особливо переважно, від 0 °C до 80 °C, в інертному органічному розчиннику у присутності 1,5-3 еквівалентів основи формули IV у перерахунку на аміносульфони формули III, у присутності каталізатору, якщо необхідно. Придатними розчинниками є аліфатичні вуглеводні, такі, як пентан, гексан, гептан, циклогексан та суміші С5-С8-алканів, ароматичні вуглеводні, такі, як толуол, о-, м- та п-ксилол, галогензаміщені вуглеводні, такі, як метиленхлорид, хлор-форм, дихлоретан та хлорбензол, ефіри, такі, як діетиловий ефір, диізопропіловий ефір, трет-бутилметиловий ефір, діоксан, анізол та тетрагідрофуран, такі ефіри, як етилацетат, пропілацетат, н-бутилацетат, метилізобутират, ізобутилацетат; а також диметилсульфоксид, диметилформамід та диметилацетамід; особливо переважно, ароматичні вуглеводні та галогензаміщені вуглеводні. 12 Також можна використовувати суміші вказаних розчинників та суміші вказаних розчинників з водою. Реакцію за даним винаходом хлоридів м-нітробензойної кислоти формули II з аміносульфонами формули III з утворенням сульфонамідів формули І здійснюють у присутності 1,5-3 еквівалентів основи формули IV у перерахунку на аміносульфони формули III. Ці 1,5-3 еквівалентів основи формули IV являють собою повну кількість основи "В", що використовують у способі за даним винаходом. На стадії а) спосіб за даним винаходом включає взаємодію аміносульфонів формули III з 0,11,3 еквівалентами основи у перерахунку на аміносульфони формули III. Ці 0,1-1,3 еквівалентів основи IV являють собою частину від усієї кількості основи В, та можуть бути також позначені як кількість основи "В1". У стадії b) спосіб за даним винаходом включає взаємодію реакційної суміші, що була утворена на стадії а), з хлоридами м-нітробензойної кислоти формули II та остаточне випаровування усієї кількості основи В до кількості В1. Остаточне випаровування основи В проводять також до кількості основи "В2". Таким чином, використовують таке співвідношення між В, В1 та В2: В1+В2=В. Як основи формули IV можна використовувати такі неорганічні сполуки, як гідроксиди лужних та лужноземельних металів, такі, як гідроксид літію, гідроксид натрію, гідроксид калію та гідроксид кальцію, такі оксиди лужних та лужноземельних металів, як оксид літію, оксид натрію, оксид кальцію та оксид магнію, такі гідриди лужних та лужноземельних металів, як гідрид літію, гідрид натрію, гідрид калію та гідрид кальцію, такі аміди лужних та лужноземельних металів, як амід літію, амід натрію та амід калію, такі карбонати лужних та лужноземельних металів, як карбонат літію, карбонат калію та карбонат кальцію, а також такі гідрокарбонати лужних металів, як гідрокарбонат натрію, такі алкоголяти лужних та лужноземельних металів, як метанолят натрію, метанолят калію, трет-бутанолят калію, трет-пентанолят калію та диметоксимагній, а також такі органічні основи, як, наприклад, третинні аміни, такі, як триметиламін, триетиламін, діізопропілетиламін та Nметилпіперидин, піридин, такі заміщені піридини, як коллідін, лутидин та 4-диметиламінопіридин, а також такі біциклічні аміни, як, наприклад, 1,8діазабіциклоцикло[5.4.0]ундек-7-ен (DBU) та 1,5діазабіцикло[4.3.0]нон-5-ен (DBN). Особливо переважними є гідроксиди лужних та лужноземельних металів та третинні аміни. Особливо переважними є гідроксиди лужних та лужноземельних металів, найбільш переважними є гідроксиди лужних металів. Використовують 1,5-3 еквівалентів основи IV (повна кількість основи В) у перерахунку на аміносульфони формули III. Більш переважно, В становить 1,8-2,5 еквівалентів у перерахунку на аміносульфон формули III. Особливо переважними є 1,8-2,5 еквівалентів у перерахунку на хлориди м-нітро-бензойної кис 13 лоти формули II, особливо переважно, у перерахунку на фторовані хлориди м-нітро-бензойної кислоти формули llА, де замісники мають наступні значення: 1 2 3 4 R ,R ,R та R водень, галоген, ціано, нітро, С1-С6-алкіл, С1-С6-галогеналкіл, С1-С6-алкоксі або С1-С6-галогеналкоксі; 1 4 де, щонайменше, один із залишків R -R означає фтор; Переважно, на стадії а) способу за даним винаходом, розчиняють аміносульфони формули III в інертному розчиннику. Після цього, додають В1 еквівалентів основи формули IV, тобто, від 0,1 до 1,3 еквівалентів, переважно, 0,1-1 еквівалентів, більш переважно, від 0,2 до 0,95 еквівалентів формули IV. Особливо переважним є додавання основи формули IV протягом деякого періоду часу. Більш переважно, В1 еквівалентів основи формули IV додають безперервно, особливо переважно, безперервно з постійною швидкістю протягом певного періоду часу. Цей період додавання В1 еквівалентів основи IV у стадії с) може становити від 1 хвилини аж до 20 годин. Загалом, цей період становить від 1 хвилини до 6 годин, переважно, від 1 хвилини до 3 годин. Можна також, переважно, у варіантах, що були описані вище, додавати аміносульфони формули III до заданої кількості основи В1, зокрема, до переважної заданої кількості основи В1. Переважно, на стадії b) способу за даним винаходом хлориди м-нітро-бензойної кислоти формули II, переважно, фторовані хлориди м-нітробензойної кислоти формули llА, переважно, розводять в інертному розчиннику, а також В2 еквівалентів основи формули IV з реакційною сумішшю, що одержали на стадії а), переважно також розводять в інертному розчиннику. Переважно, на стадії b) додають хлориди мнітро-бензойної кислоти формули II, а також В2 еквівалентів основи формули IV у той самий час (= паралельне додавання), більш переважно, у той самий час протягом деякого періоду часу, особливо переважно, у той самий час безперервно протягом деякого періоду часу, найбільш переважно, у той самий час безперервно рівномірно протягом деякого часу до реакційної суміші, утвореній на стадії а). Цей період додавання хлоридів м-нітробензойної кислоти формули II, а також В2 еквівалентів основи IV у стадії b) може становити від 1 хвилини аж до 20 годин. Загалом, цей період становить від 1 хвилини до 6 годин, переважно, від 1 хвилини до 3 годин. Можна також, переважно, в описаних вище варіантах, реакційну суміш, що утворилась у стадії а), а також кількість В2 основи, у той самий час, 96281 14 переважно, протягом деякого періоду часу, додавати до хлоридів м-нітро-бензойної кислоти II, переважно, розведеному в інертному розчиннику. Далі, можна хлориди м-нітро-бензойної кислоти II, переважно фторовані хлориди м-нітробензойної кислоти формули llА, піддавати реакції також у вигляді речовин, тобто, наприклад, у вигляді їх розплавів, з аміносульфоном формули III, де III, переважно, розчинено в інертному розчиннику, у присутності основи, переважно, як описано вище. Ще в одному варіанті втілення способу за даним винаходом, можна також проводити реакцію у багатофазній водній системі. Цей варіант є переважним. Ще в одному варіанті втілення способу за даним винаходом можна також проводити реакцію у багатофазній водній системі з каталізатором фазового переносу (РТС) та без нього. Переважно, реакцію здійснюють у багатофазній водній системі з каталізатором фазового переносу. Переважними є реакції у водній багатофазній системі у присутності каталізаторів фазового переносу, таких, як четвертинні солі амонію, солі фосфору, полігліколі та краунефіри. Придатним є використання четвертинних солей амонію - тетра (С1-С18)алкіл-аммоній-фториду, -хлориду, -броміду, -йодиду, -гідросульфату, гідроксиду, -перхлорату, борату, -диборату або тетрафторборату, таких, як тетраметиламонійфторид-тетра гідрат, тетраметиламоній-хлорид, тетраметиламоній-бромід, тетраметиламоніййодид, тетраметиламоній-гідроксид, метилтрибутиламоній хлорид (наприклад ALIQUAT® 175), метилтриоктиламоній-хлорид, метилтрикаприліламоній-хлорид (наприклад ALIQUAT® 336, ALIQUAT® HTA1), тетраетиламоній-хлорид, тетраетиламоній-хлорид-гідрат, тетраетиламонійбромід, бетраетиламоній-гідроксид, тетрабутиламоній-фторид, тетрабутиламоній-фторидтригідрат, тетрабутиламоній-хлорид, тетрабутиламоній-бромід, тетрабутиламоній-йодид, тетрабутиламоній-гідросульфат, тетрабутиламонійгідроксид, тетрабутиламоній-перхлорат, тетрабутиламоній-тетрафтороборат, тетрапропіламоній хлорид, тетрапропіламоній-бромід, тетрапропіламоній-гідроксид, тетрагексіламоній-бромід, тетрагексіламоній-йодид, тетраоктиламоній-бромід, цетилтриметиламоній-бромід, додецилтриметиламоній-бромід, додецилтриметиламоній-хлорид, С12-С14-алкілтриметиламонійборат, С12-С14-алкілтриметиламоній-диборат; Nфeнiл(С1-С18)тpиaлкiлaмoнiй-фтopид, -хлорид або -бромід, такий, як фенілтриметиламоній-хлорид; N-бензил(С1-С18)триалкіламоній-фторид, -хлорид або -бромід, такий, як бензилтриметиламонійхлорид, бензилтриетиламоній-хлорид, бензилтриетиламоній-бромід, бензилтрибутиламоній-бромід; піридин- фторид, -хлорид або -бромід, такий, як 1-цетил-піридин-хлорид-моногідрат, цетилпіридин-бромід. Придатними солями фосфору є, наприклад, тетрафенілфосфонійхлорид або -бромід, бензилтрифенілфосфоній-хлорид, бензилтрифенілфос 15 фоній-бромід; алкіл-феніл-фосфоній-хлорид, бромід, -йодид, -ацетат, такі, як метилтрифенілфосфоній-бромід, етилтрифенілфосфоній-бромід, етилтрифенілфосфоній-йодид, етилтрифенілфосфоній-ацетат, бутилтрифеніл фосфоній-хлорид, бутилтрифенілфосфоній-бромід; тетраалкіл-(С1С18)-фосфонійхлорид або -бромід, такий, як тетрабутилфосфонійбромід. Придатними полігліколями та краунефірами є, наприклад діетиленгліколь дибутиловий ефір ("бутил диглім"), 18-краун-6 та дибензо-18-краун-6. Переважними є тетра-(С1-С18)-алкіламонійгідросульфат та тетра-(С1-С18)-алкіламонійхлорид, більш переважно тетра-(С1-С6)алкіламоній-гідросульфат та тетра-(С1-С6)алкіламоній-хлорид. Особливо переважними є тетра-(С1-С18)алкіламоній-хлорид, найбільш переважним є тетра-(С1-С6)-алкіламоній-хлорид. Поряд з цим переважним є використання тетрабутиламоній-фториду, тетрабутиламонійгідросульфату, метилтрибутиламоній-хлориду, тетрапропіламоній-хлориду, тетрапропіламонійброміду, бензилтрифенілфосфоній-хлориду, бензилтрифенілфосфоній-броміду або дибензо-18кроун-6. Зазвичай, використовують каталізатор фазового переносу у кількості аж до 20 мол %, переважно, від 0,5 до 5 мол %, та, зокрема, від 0,3 до 2 мол. - %, у перерахунку на хлориди м-нітробензойної кислоти формули II, переважно, фторовані хлориди м-нітро-бензойної кислоти формули llА. Більш переважно кількість каталізатору фазового переносу становить 0,01-20 мол%, особливо переважно, 0,05-5 мол%, ще більш переважно 0,1-2 мол%, у перерахунку на хлориди м-нітробензойної кислоти формули II, переважно, фторовані хлориди м-нітро-бензойної кислоти формули llА. Багатофазова система містить одну водну фазу та, щонайменше, одну органічну рідку фазу. Разом з цим можна проводити реакцію у твердій фазі. Водна фаза являє собою, переважно, розчин гідроксидів чи карбонатів лужних або лужноземельних металів у воді. Відносно придатним є використання гідроксидів чи карбонатів лужних або лужноземельних металів, вказаних вище. Особливо переважними є гідроксиди лужних або лужноземельних металів, особливо гідроксид натрію або гідроксид калію. Переважними для використання як органічної фази є аліфатичні, циклоаліфатичні, або ароматичні, за необхідності, галогензаміщені вуглеводні, циклічні або аліфатичні ефіри або їх суміші, де використовують аліфатичні, циклоаліфатичні або ароматичні, за необхідності, галогензаміщені вуглеводні, циклічний або аліфатичний ефір, як вказано вище. Якщо як органічну фазу використовують розчинник, що змішується з водою, то реакцію можна проводити без каталізатору фазового переносу. Ще в одному переважному втіленні способу за даним винаходом, багатофазна система складається з водного розчину гідроксиду калію чи на 96281 16 трію, як водної фази та з толуолу, хлорбензолу, діоксану, дихлоретану, дихлорметану, тетрагідрофурану або метилтетрагідрофурану, наприклад, з сумішей цих органічних розчинників як органічної фази. В особливо переважному втіленні способу за даним винаходом, багатофазна система складається з водного розчину гідроксиду калію чи натрію, як водної фази та, за необхідності, галогензаміщених ароматичних вуглеводнів, таких, як, наприклад толуол, ксилол або хлорбензол, найбільш переважно, з галогензаміщених ароматичних вуглеводнів, таких, як, наприклад хлорбензол, наприклад, з сумішей цих органічних розчинників як органічної фази. Придатна багатофазна система може містити, наприклад, хлориди м-нітро-бензойної кислоти формули II, переважно, фторовані хлориди мнітро-бензойної кислоти формули llА, та каталізатор фазового переносу без додаткового розчиннику або в одному органічному розчиннику чи суміші розчинників. Потім водний розчин кількості В2 основи, та реакційну суміш, що утворилася на стадій а) змішують та після змішування, або під час змішування доводять до вказаної температури та проводять реакцію до кінця. Переважно корисним є використання багатофазових систем у стадії а) способу за даним винаходом для одержання аміносульфону формули lll в інертному розчиннику. Також, додають В1 еквівалентів основи формули IV, тобто, 0,1-1,3 еквівалентів, переважно 0,1-1 еквівалентів, більш переважно 0,2-0,7 еквівалентів основи формули IV, що є сприятливим для переносу протягом деякого часу. Також, корисним є використання багатофазових систем у стадії b), де, переважно, спочатку додають каталізатор фазового переносу до реакційної суміші, що утворилася на стадії а). Потім додають хлорид м-нітро-бензойної кислоти формули II, а також кількість В2 основи. Особливо переважно, паралельно додають хлорид м-нітробензойної кислоти формули ll та кількість В2 основи, більш переважно - паралельно та через деякий час повертають у реакційну суміш, що утворилася на стадії а). Переважно корисним є використання багатофазових систем у стадії b) способу за даним винаходом, де спочатку хлорид м-нітро-бензойної кислоти формули II, а також кількість В2 основи додають до реакційної суміші, що утворилася на стадії а), а потім додають каталізатор фазового переносу. Реакцію можна проводити під нормальним тиском, зменшеним чи збільшеним тиском, за необхідності при безперервному або періодичному пропусканні інертного газу. Закінчення реакції може бути визначено фахівцем у цій галузі за відомими методами. Реакційні суміші обробляють відомими способами. Зазвичай, розчинник видаляють стандартними способами, наприклад, випаровуванням. Можна також розчиняти продукт у воді, та органічному розчиннику, що не змішується з водою, екст 17 рагувати усі домішки водою, за необхідності підкисленою, сушити та видаляти розчинник під зменшеним тиском. Подальша очистка відома фахівцю у цій галузі, це, наприклад, перекристалізація, осадження (наприклад, шляхом додавання неполярних розчинників, таких, як пентан, циклогексан, гептан або толуол, або суміші вказаних розчинників) або хроматографічне розділення. У разі використання багатофазової системи, зазвичай, застосовують екстракцію. Цільовий продукт можна виділяти шляхом осадження (наприклад, шляхом додавання таких неполярних розчинників, як пентан, циклогексан, гептан або толуол, або суміші вказаних розчинників). У переважному варіанті втілення способу за даним винаходом після закінчення реакції с) реакційну суміш розводять шляхом додавання води та/або водних розчинів мінеральних кислот, де значення рН водної фази становить 7. Особливо переважні значення рН у водній фазі становить рН=2-6,5, особливо - рН=3-5,0. Для цього придатними водними мінеральними кислотами будуть водні мінеральні кислоти, відомі фахівцю у цій галузі, такі, як, наприклад соляна кислота, сірчана кислота, азотна кислота або фосфорна кислота. Потім реакційну суміш обробляють стандартними способами. Зазвичай, фази розділюють, а розчинник видаляють стандартними способами, наприклад, випаровують. Для подальшої очистки можна використовувати такі стандартні процедури, як перекристалізація, (наприклад, також шляхом додавання неполярних розчинників, таких, як пентан, циклогексан, гептан або толуол, або суміші вказаних розчинників). У разі використання багатофазових систем, зазвичай, застосовують екстракцію. Ще в одному переважному варіанті реакції за даним винаходом розведену реакційну суміш, одержану на стадії с) нагрівають на стадії d) та при цій температурі відбувається розділення фаз. Цей варіант способу за даним винаходом відбувається, переважно, у випадках, коли на стадії с) не утворюється прозорий розчин. Переважно, на стадії с) одержана розведена реакційна суміш швидко нагрівається до температури кипіння, при якій відбувається розділення фаз. Потім, цільовий продукт може бути виділений стандартними способами, як, наприклад, видалення розчинника, та, за необхідності, наступна перекристалізація. Далі органічну фазу, одержану на стадії d), за необхідності, знов використовують на стадії с) та, за необхідності, у стадії d), та повторюють стадії с) та d) довільну кількість разів, переважно, стільки разів, скільки потрібно. Для одержання сульфонамідів формули І використовували вказані аміносульфони формули lll, що відомі з літератури (Houben-Weyl, Methoden der organischen Chemie Vol.E11, 1985, S. 1019; Hamprecht et al., Angew.Chem.93, 151, 1981) або можуть бути одержані способами, відомими з літератури. Для одержання сульфонамідів формули І використовують вказані хлориди м-нітро-бензойної 96281 18 кислоти II, відомі з літератури, що можуть бути одержані з м-нітро-бензойної кислот формули Vll де замісники мають наступні значення: 1 2 3 4 R ,R ,R ,R водень, галоген, ціано, нітро, С1С6-алкіл, С1-С6-галогеналкіл, С1-С6-алкоксі або С1С6-галогеналкоксі; з одержанням проміжних хлорзаміщених сполук формули VIII. Відповідно до даного винаходу, існує додатковий спосіб одержання сульфонамідів формули І, вказаних у цій заявці, за яким хлориди м-нітробензойної кислоти II одержують з м-нітробензойних кислот формули VII та хлорзаміщених проміжних сполук формули VIII. У найбільш переважних втіленнях способу за 1 2 3 4 даним винаходом замісники R ,R ,R та R хлоридів м-нітро-бензойної кислоти II мають для сульфонамідів формули І вказані значення, зокрема, переважні значення, де незалежно від комбінації замісників, їх розташування являє собою найбільш перевалене втілення способу за даним винаходом. Переважні втілення реакції м-нітро-бензойних кислот формули VII з хлорзаміщеними проміжними сполуками формули VIII в умовах реакції для вказаних фторованих м-нітро-бензойних кислот формули VIIA з хлорзаміщеними проміжними сполуками формули VIII у присутності каталітичних кількостей похідних фосфінів формули IX, мають наступні значення, зокрема, вказані для переважних втілень. Зокрема, у рівні техніки (наприклад WO89/02891, WO04/106324, WO04/035545 та US 6,251,829) описані способи одержання фторованих хлоридів бензойної кислоти або фторованих хлоридів бензойних кислот. Тим не менш, в описаних у рівні техніки способах існує проблема розділення фторзаміщених сполук, v.a. коли каталізаторами є, наприклад, N,N-диметиламінопіридин (DMAP) або азотисті основи, такі, як піридин, піколін чи лутидин. Фториди, що виділяються, мають пошкоджуючу дію наприклад, на устаткування ("фторидна корозія"), тому необхідно ізолювати матеріали від приладів. Крім того, виділення фторидів призводить до утворення домішок, наприклад, побічних продуктів, у цільовому продукті. Проте, якщо спосіб здійснюють без каталізатора, то виходи є зниженими, через це, наприклад, необхідно підвищувати температуру. Таким чином, задача даного винаходу також полягає у розробці економічного та ефективного способу одержання фторованих хлоридів м-нітробензойної кислоти формули IIА, в якому, з одного боку, зменшено забруднення фторидами, та одночасно одержують цільовий продукт з високим виходом та високим ступенем очищення. 19 96281 Несподівано було знайдено, що ця задача вирішується способом, за яким фторовані м-нітробензойні кислоти формули VII взаємодіють з проміжними хлорзаміщеними сполуками формули VIII, так, як описано у цій заявці, та реакція проходить у присутності каталітичних кількостей похідних фосфінів формули IX, а також, за необхідності, у присутності кислот Льюіса, у розчині. Даний винахід стосується способу одержання фторованих хлоридів м-нітро-бензойної кислоти IIА де замісники мають наступні значення: 1 2 3 4 R ,R ,R та R водень, галоген, ціано, нітро, С1-С6-алкіл, С1-С6-галогеналкіл, С1-С6-алкоксі або С1-С6-галогеналкоксі; 1 4 де, щонайменше, один із залишків R -R означає фтор, шляхом взаємодії фторованих м-нітробензойних кислот формули VIIA де замісники мають наступні значення: 1 2 3 4 R ,R ,R ,R водень, галоген, ціано, нітро, С1С6-алкіл, С1-С6-галогеналкіл, С1-С6-алкоксі або С1С6-галогеналкоксі; 20 1 4 де, щонайменше, один із залишків R -R означає фтор; з хлорзаміщеними проміжними сполуками формули VIII, що описані у цій заявці, де реакція відбувається у присутності каталітичних кількостей похідних фосфінів формули IX де замісники мають наступні значення: a b c R ,R ,R С1-С6-алкіл або феніл, що можуть бути заміщені, за необхідності, С1-С4-алкілом; X кисень чи зв'язані простим зв'язком два атоми хлору; n 0 або 1 Додатково даний винахід стосується способу одержання фторованих сульфонамідів формули ІА (= сульфонамід І, де, щонайменше, один з залиш1 4 ків R -R означає фтор), що відрізняється тим, що фторовані хлориди м-нітробензойної кислоти формули IIА, необхідні для цього, одержують способом, вказаним вище, зі фторованих м-нітробензойних кислот формули VII. Наступні переважні втілення реакції фторованих м-нітро-бензойних кислот формули VIIA з проміжними хлорзаміщеними сполуками формули VIII у присутності каталітичних кількостей похідних фосфінів формули IX, де вони, незалежно від комбінації, являють собою найбільш переважне втілення способу за даним винаходом. Цей спосіб за даним винаходом одержання фторованих хлоридів м-нітро-бензойних кислот IIА включає реакцію фторованих м-нітро-бензойних кислот формули VIIA з проміжними хлорзаміщеними сполуками формули VIII у присутності каталітичних кількостей похідних фосфіну формули IX: хлорзаміщена сполука формули VIII де замісники у випадку одержання фторованих хлоридів м-нітро-бензойних кислоти формули IIА мають вказані значення. Ця реакція, зазвичай, відбувається при температурах від 20 °C до 160 °C, переважно від 20 °C до 120 °C, особливо переважно від 70 °C до 120 °C, в інертному розчиннику. Тиск реакції у способі за даним винаходом може знаходитись, наприклад, у діапазоні від 500 мБар до 10 Бар. Переважно, реакцію проводять у діапазоні нормального тиску, тобто, у діапазоні від 0,9 до 1,2 Бар. Період часу, необхідний для проведення реакції, зазвичай, знаходиться у діапазоні від 1 години до 24 годин, зокрема у діапазоні від 2 годин 8 годин. Спосіб за даним винаходом може бути здійснений, в принципі, у твердому стані. Переважно, проте, спосіб за даним винаходом здійснюють в інертному органічному розчиннику. В принципі, можна використовувати усі розчинники, що здатні, щонайменше, частково розчиняти фторовані м-нітро-бензойні кислоти формули VIIA, хлорзаміщені проміжні сполуки та похідну фосфіну III, переважно, повністю розчиняти за умов проведення реакції. Придатними розчинниками є, наприклад, аліфатичні вуглеводні, такі, як пентан, гексан, цикло 21 гексан та суміш С5-С8-алканів, такі ароматичні вуглеводні, як толуол, о-, м- та п-ксилол, галогензаміщені вуглеводні, такі, як метиленхлорид, хлорформ та хлорбензол, такий ефір, як діетиловий ефір, діізопропіловий ефір, трет-бутилметиловий ефір, діоксан, анізол та тетрагідрофуран, особливо переважно, ароматичні вуглеводні або галогензаміщені вуглеводні. Можна також використовувати суміші вказаних розчинників. Як проміжні хлорзаміщені сполуки формули VIII, зазвичай використовують хлорзаміщену проміжну сполуку, таку, як оксалілхлорид, фосфотрихлорид, фосфопентахлорид, тіонілхлорид, фосфорилхлорид (РОСl3). Крім того, використовують також відомі газоподібні чи рідкі фосген, відповідний димер (трихлорметиловий ефір хлормурашиної кислоти, "дифосген") або відповідний тример (біс(трихлорметиловий ефір карбонової кислоти), "трифосген") (порівн. R.Beckert et al., Organikum, 22. Auflage 2004, S. 496-499). Переважно, проміжною хлорзаміщеною сполукою VIII є оксалілхлорид, фосфотрихлорид, фосфопентапентахлорид, тіонілхлорид та фосфорилхлорид (РОСl3); більш переважно - тіонілхлорид. Фторовані м-нітро-бензойні кислоти формули VIIA та проміжні хлорзаміщені сполуки формули VIII взаємодіють, зазвичай, в еквімолярній кількості. Сприятливим буде використання проміжної хлорзаміщеної сполуки формули VIII у надлишку у перерахунку на м-нітро-бензойну кислоту формули VIIA. Переважно, використовують проміжну хлорзаміщену сполуку формули VIII та фторовану мнітро-бензойну кислоту формули VIIА у співвідношенні 2:1, особливо переважно, 1,5:1. Як каталізатори використовують похідні фосфіну формули IX де замісники мають наступні значення: a b c R ,R ,R С1-С6-алкіл або феніл, що можуть бути, за необхідністю, заміщені С1-С4-алкілом; X кисень чи зв'язані простим зв'язком два атоми хлору; n 0 або 1. Переважно використовують трифенілфосфін, трифенілфосфіноксид (ТРРО), трифенілдіхлорфосфан, три-(С1-С6-алкіл)фосфін, три-(С1-С6алкіл)фосфіноксид, а також три-(С1-С6алкіл)дихлорфосфан; особливо переважно, трифенілфосфін, трифенілфосфіноксид та три-(С1-С6алкіл)фосфіноксид; найбільш переважно, трифенілфосфіноксид; Похідні фосфіну формули IX зазвичай використовують у кількостях від 0,01 до 5 мол%, переважно, від 0,1 до 1 мол %, особливо переважно, від 0,1 до 0,5 мол% у перерахунку на визначену кількість фторованої м-нітро-бензойної кислоти формули VII. Крім того, спосіб за даним винаходом може бути здійснений у присутності кислот Льюїса. Як кислоти Льюїса використовують звичайні кислоти 96281 22 Льюїса (порівн. наприклад Lewis Acids in Organic Synthesis, ed.H. Yamamoto, Vol.1 та 2, Weinheim 2000). Як кислоти Льюїса використовують, зокрема, сполуки бору, такі, як боргалогеніди (наприклад BF3, BCl3, ВF3-ефірат), борну кислоту (Н3ВО3), ангідрид борної кислоти, ефір борної кислоти (наприклад три-С1-С4-алкільний ефір борної кислоти), борат (наприклад борат натрію/боракс), боронові кислоти (наприклад С1-С6-алкілборонові кислоти, арилборонові кислоти, зокрема, фенілборонову кислоту), С1-С4-алкіловий ефір боронової кислоти (наприклад С1-С4-алкіловий ефір С1-С6алкілборонової кислоти, -С1-С4-алкіловий ефір арилборонової кислоти), циклічні ефіри борної кислоти (наприклад трис(С1-С4-алкоксі)бороксін, зокрема триметоксібороксін, та тріетаноламінборат). Особливо переважними є борна кислота, триС1-С4-алкіловий ефір борної кислоти або циклічні ефіри борної кислоти. Кислоти Льюїса зазвичай використовують у кількостях від 0,01 до 5 мол%, переважно, від 0,1 до 1 мол%, у перерахунку на визначену кількість мнітро-бензойної кислоти формули II. Спосіб може бути здійснений як безперервно, так і постадійно (через напівстадії). У способі за даним винаходом змішують сполуки та реагенти, у принципі, у довільному порядку, тобто, реагенти та похідні фосфіну формули IX, а також, за необхідності, кислоту Льюїса, вони можуть бути окремо, одночасно або послідовно поміщені у реакційну судину для проведення реакції. Сприятливою є взаємодія фторованих м-нітробензойних кислот формули VIIA та похідних фосфіну формули IX, а також, за необхідності, кислоти Льюїса в інертному розчиннику, та змішування, наприклад, при інтенсивному перемішуванні, із проміжною хлорзаміщеною сполукою формули VIII. Крім того, можна змішувати проміжну хлорзаміщену сполуку формули VIII разом із похідним фосфіну формули IX, а також, за необхідності, з кислотою Льюїса, а потім із фторованою м-нітробензойною кислотою формули VIIA, переважно, розчиненою в інертному розчиннику. Реакційні суміші можуть бути очищені звичайними способами, наприклад, шляхом відгонки розчинника та видалення надлишку хлорованих реагентів. Проміжні або кінцеві продукти знаходяться, наприклад, у вигляді в'язких масел, які при зниженому тиску та при помірно високій температурі вивільняють від летких компонентів або очищають. Якщо проміжні та кінцеві продукти одержують у вигляді твердих речовин, очищення можна здійснювати перекристалізацією або дигеруванням. Переважно, після закінчення реакції подальша очистка не потрібна. Для одержання фторованих хлоридів м-нітробензойної кислоти формули IIА потребуються фторовані м-нітро-бензойні кислоти формули VIIA, відомі з літератури, або такі, що можуть бути одержані шляхом нітрування відповідних бензойних кислот або нітрування відповідних метилових ефірів бензойних кислот з наступним омиленням (на 23 приклад R.Beckert et al., Organikum, 22. Auflage 2004, S. 358-361). Відповідно до даного винаходу, фторовані хлориди м-нітро-бензойної кислоти формули IIА, що застосовують у способі, можуть бути використані також як вихідні речовини для одержання сульфонамідів формули ІА, що є цінним проміжним продуктом для синтезу фармацевтично активних сполук або засобів захисту рослин. Тому додатковою задачею даного винаходу є забезпечення способу одержання сульфонамідів формули ІА, виходячи з фторованих хлоридів мнітро-бензойних кислот формули ІА. Фторовані хлориди м-нітро-бензойної кислоти формули IIА можуть мати, в залежності від типу зміщення, один чи декілька центрів хіральності та являє собою суміш енантіо- та діастереомерів. Тому об'єктом винаходу є спосіб одержання чистих енантіо- або діастереомерів та їх сумішей. 1 6 a b c Для замісників R -R , а також R , R та R вказані частини органічних молекул являють собою усі значення номерів членів окремих груп, відповідно до значень, вказаних вище. Усі вуглеводні, а також усі алкіл, галогеналкіл, алкоксі та галогеналкоксі групи можуть бути розгалуженими чи нерозгалуженими. Якщо не вказано інше, то галогеновані замісники мають не більш, ніж п'ять, переважно, однакових, чи різних атомів галогенів. Галоген у кожному разі означає фтор, хлор, бром або йод. Для фторованих хлоридів м-нітро-бензойних 1 2 3 4 кислот формули IIА, замісники R ,R ,R та R мають значення, вказані вище, особливо переважні 1 значення, де комбінація усіх чотирьох залишків R 4 R , більш переважно, щонайменше, один із залиш1 4 ків R -R означає фтор, де ці значення, вказані вище, окремо чи у комбінації, є найкращими втіленнями способу за даним винаходом. Переважними є втілення способу за даним винаходом, де 1 R означає водень, галоген або С1-С6-алкіл; переважно, водень або галоген; більш переважно, водень, фтор або хлор; особливо переважно, водень; Також переважними є такі втілення способу за даним винаходом, де 2 R означає водень, галоген, ціано, С1-С6-алкіл або С1-С6-галогеналкіл; переважно, водень або галоген; більш переважно, водень, фтор або хлор; особливо переважно, водень або фтор, найбільш переважно, водень; аналогічно, найбільш переважно, фтор. Крім того, переважними є такі втілення способу за даним винаходом, де 2 R означає водень або галоген; переважно, галоген; більш переважно, фтор або хлор; особливо переважно, фтор. Також переважними є такі втілення способу за даним винаходом, де 3 R означає водень, галоген або С1-С6-алкіл; переважно, водень або галоген; більш переважно, водень, фтор або хлор; особливо переважно, водень. 96281 24 Також переважними є такі втілення способу за даним винаходом, де 4 R означає водень, галоген, ціано, С1-С6-алкіл або С1-С6-галогеналкіл; переважно, водень, галоген або ціано; більш переважно, водень, фтор, хлор або ціано; особливо переважно, водень, хлор або ціано, найбільш переважно, водень; аналогічно, найбільш переважно, хлор або ціано; та ще найбільш переважно хлор; Крім того, переважними є такі втілення способу за даним винаходом, де 4 R означає галоген або ціано; переважно, галоген; більш переважно, фтор або хлор; особливо переважно, хлор; Крім того, переважними є такі втілення способу за даним винаходом, де 4 R означає водень, галоген або ціано; переважно, водень або галоген; більш переважно, водень, фтор або хлор; особливо переважно, водень або хлор; Ще в одному переважному втіленні способу за даним винаходом замісники 1 2 3 R ,R , R та R мають такі значення: 1 R водень; 2 R водень або галоген; переважно, галоген; більш переважно фтор; 3 R водень; та 4 R водень, хлор або ціано, переважно, хлор або ціано; більш переважно, хлор. Ще в одному більш переважному втіленні спо1 2 3 4 собу за даним винаходом замісники R ,R ,R та R мають такі значення: 1 R водень; 2 R водень або галоген; переважно, галоген; більш переважно, фтор; 3 R водень; та 4 R водень або галоген, переважно, водень або хлор; більш переважно, хлор, аналогічно більш переважно, водень. Ще в одному більш переважному втіленні спо1 2 3 4 собу за даним винаходом замісники R ,R ,R та R мають такі значення: 1 R водень; 2 R фтор; 3 R водень; та 4 R галоген, переважно, хлор. Ще в одному найбільш переважному втіленні способу за даним винаходом одержання фторованих хлоридів м-нітро-бензойної кислоти формули 1 IIА.а (відповідає формулі IIА, де R = фтор) 25 96281 26 1 3 4 1 2 3 R ,R та R мають, переважно, значення, вказані вище. Ще в одному найбільш переважному втіленні способу за даним винаходом одержання фторованих хлоридів м-нітро-бензойної кислоти формули 4 IIA.d (відповідає формулі IIА, де R = фтор) 2 3 4 де R ,R та R мають, переважно, значення, вказані вище. Ще в одному найбільш переважному втіленні способу за даним винаходом одержання фторованих хлориду м-нітро-бензойної кислоти формули 2 IIА.b (відповідає формулі IIА, де R = фтор) R ,R та R мають, переважно, значення, вказані вище. Ще в одному найбільш переважному втіленні способу за даним винаходом одержання фторованих хлоридів м-нітро-бензойної кислоти формули 1 3 IIА.e (відпові-дає формулі ІА, де R та R = Н) 1 3 4 R ,R та R мають, переважно, значення, вказані вище. Ще в одному найбільш переважному втіленні способу за даним винаходом одержання фторованих хлоридів м-нітро-бензойної кислоти формули 3 IIА.с (відповідає формулі IIА, де R = фтор) 2 4 Замісники R та R мають значення, вказані вище, зокрема, вказані як переважні значення, та, 2 4 щонайменше, один із залишки R та R означає фтор. Крім того, хлориди м-нітро бензойної кислоти формули II можуть бути одержані шляхом гідролізу відповідних бензотрихлоридів формули X у присутності каталізатору або у слабко-кислому середовищі. гідроліз де замісники мають наступні значення: 1 2 3 4 R ,R ,R та R водень, галоген, ціано, нітро, С1-С6-алкіл, С1-С6-галогеналкіл, С1-С6-алкоксі або С1-С6-галогеналкоксі. Відповідно, даний винахід також стосуються способу одержання сульфонамідів формули І, що відрізняється тим, що хлориди м-нітро бензойної кислоти формули II, потрібний для цього, одержують шляхом гідролізу бензотрихлоридів формули X у присутності каталізатору або у слабко-кислому середовищі. У найбільш кращих втіленнях способу за да1 2 3 4 ним винаходом замісники R ,R ,R та R хлоридів м-нітро-бензойної кислоти II мають значення, вказані вище для сульфонамідів формули І, зокрема, переважні вказані значення, де положення замісників окремо по відношенню один до одного, являють собою незалежно від комбінації, у якій вони наведені, найбільш переважне втілення способу за даним винаходом. У переважному втіленні гідролізу відповідного бензотрихлоридів формули X застосовують умови гідролізу, вказані для фторованих м-нітробензотрихлориду формули ХА, зокрема, ті, що вказані для переважного втілення. У рівні техніки (наприклад О. Scherer et al., Liebigs Ann.Chem. 1964, 677, 83-95; WO 06/090210) описано способи одержання хлоридів ароматичних кислот з від-похідних бензойних кислот. Проте, у рівні техніки описано проблему видалення фторованих замісників при умовах проведення реакцій з ароматичними сполуками, описаних у рівні техніки. Недоліки виділення вказаних вільних фторидів є такими, як вказано вище для одержання хлори 27 96281 дів бензойної кислоти з відповідних бензойних кислот. Додатковою задачею даного винаходу, відповідно, є розробка способу одержання фторованих хлоридів м-нітро-бензойної кислоти формули IIА шляхом гідролізу відповідних фторованих м-нітробензотрихлоридів формули ХА, за яким відбувається повне видалення фторидів, та у той же час цільовий продукт одержують з високими виходами та високого ступеню чистоти. Несподівано було знайдено, що ця задача вирішується способом, за яким фторовані м-нітробензотрихлориди формули ХА у присутності каталізатору або у слабко-кислому середовищі гідролізує у розчині при температурах, нижчих за 80 °C. Даний винахід, відповідно, додатково стосується способу одержання фторованих хлоридів мнітро-бензойної кислоти формули IIА де замісники мають наступні значення: 1 3 4 R ,R, R та R водень, галоген, ціано, нітро, С1С6-алкіл, С1-С6-галогеналкіл, С1-С6-алкоксі або С1С6-галогеналкоксі; 1 4 де, щонайменше, один із залишків R -R означає фтор, шляхом гідролізу фторованих м-нітробензотрихлоридів формули ХА 1 2 3 4 де замісники R ,R ,R та R мають вказані вище значення, що відрізняється тим, що реакція відбувається у присутності каталізатору або у слабко-кислому середовищі, а також при температурах нижчих за 80 °C. Додатково даний винахід стосується способу одержання фторованих сульфонамідів формули ІА, що відрізняється тим, що фторовані хлориди мнітро бензойної кислоти формули IIА, потрібний для цього, одержують способом, вказаним вище для фторованих м-нітро-бензотрихлоридів формули ХА. 1 2 3 4 Замісники R ,R ,R та R мають значення, вказані вище для фторованих хлоридів м-нітробензойної кислоти формули IIА, зокрема, вказані як переважні значення, де у комбінації усі чотири 1 4 залишки R -R , та, щонайменше, один з залишків 1 4 R -R означає фтор, та де ці вказані вище значення незалежно від комбінації замісників та їх розташування являють собою найбільш переважне втілення способу за даним винаходом. Ще в одному переважному втіленні описано гідроліз фторованих м-нітро-бензотрихлоридів формулиХА до фторованих хлоридів м-нітро 28 бензойної кислоти формули IIА, де ці вказані вище значення незалежно від комбінації замісників та їх розташування являють собою найбільш переважне втілення способу за даним винаходом. Гідроліз фторованих м-нітро-бензотрихлоридів формули ХА до фторованих хлоридів м-нітробензойної кислоти формули IIА відбувається при температурах, нижчих за 80 °C (
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for producing sulfonamides and intermediates
Автори англійськоюSchmidt Thomas, Gebhardt, Joachim, Gebhardt Joachim, Lohr Sandra, Keil Michael, Wevers Jan Hendrik, Rack Michael, Mayer Guido, Pleschke Axel
Назва патенту російськоюСпособ получения сульфонамидов и промежуточных соединений
Автори російськоюШмидт Томас, Гебхардт Йоахим, Льор Сандра, Кайль Михаэль, Веверс Ян Хендрик, Рак, Михаэль, Майер Гуидо, Плешке Аксель
МПК / Мітки
МПК: C07C 303/40, C07C 205/06, C07C 205/58, C07C 201/00
Мітки: проміжних, сульфонамідів, одержання, сполук, спосіб
Код посилання
<a href="https://ua.patents.su/23-96281-sposib-oderzhannya-sulfonamidiv-ta-promizhnikh-spoluk.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання сульфонамідів та проміжних сполук</a>
Попередній патент: Похідні бензамідазолу та їх застосування для модуляції рецепторного комплексу гамкa
Наступний патент: 3,5-заміщені піперидини як інгібітори реніну
Випадковий патент: Спосіб низькотемпературної сепарації газу (варіанти)