Рентгенівська діагностична композиція з низькими концентраціями контрастної речовини та спосіб рентгологічного дослідження з низькою дозою опромінення
Формула / Реферат
1. Рентгенівська діагностична композиція, що містить йодовмісний рентгенівський контрастний агент та фармацевтично прийнятний носій або наповнювач, в якій композиція має концентрацію йоду від 10 до менше ніж 100 мг І/мл, йодовмісний рентгенівський контрастний агент являє собою сполуку формули ІІ
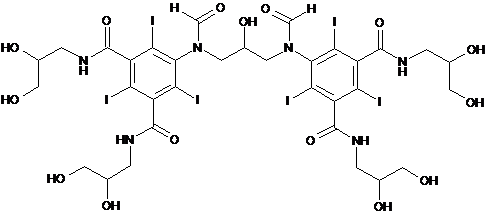 , формула II.
, формула II.
2. Спосіб рентгенологічного дослідження, за яким
в організм вводять композицію за п. 1,
застосовують дозу рентгенівського випромінювання до організму, що передбачає енергію напруги на трубці в діапазоні 70-140 кВ пікової напруги,
обстежують організм з використанням діагностичного обладнання,
збирають дані з обстеження,
і який додатково включає зниження шуму за рахунок сучасного способу реконструкції зображення.
3. Спосіб за п. 2, який підвищує контрастний ефект контрастного агента, де контрастний агент є йодовмісним, та де зазначена доза опромінення має середній спектр енергії, який в основному відповідає К-смузі йоду.
4. Спосіб за п. 2, в якому дозу рентгенівського випромінювання забезпечують за рахунок сили струму трубки в діапазоні 5-1000 мА.
5. Спосіб за п. 2, в якому зниження шуму вибирають з ітераційних способів реконструкції зображення ASiR або MBIR.
6. Спосіб за п. 2, який включає КТ з подвійною енергією.
7. Спосіб за будь-яким з пунктів 2-6, в якому об'єм композиції, що містить йодовмісний рентгенівський контрастний агент, становить від 1 до 50 мл.
8. Спосіб за п. 2, в якому рентгенівський контрастний агент містить наночастинки з атомним числом 53 або вище.
Текст
Реферат: Представлений винахід стосується рентгенологічних досліджень та покращення безпеки пацієнтів під час такого дослідження. Більш конкретно винахід стосується композицій для рентгенологічної діагностики, що мають ультранизькі концентрації йоду. Крім того, винахід стосується способів рентгенологічних досліджень, в яких в організм вводять композицію для рентгенологічної діагностики та опромінюють зниженою дозою опромінення. UA 108758 C2 (12) UA 108758 C2 UA 108758 C2 5 10 15 20 25 Представлений винахід стосується рентгенологічних досліджень та покращення безпеки пацієнтів під час такого дослідження. Більш конкретно винахід стосується рентгенівських діагностичних композицій, що мають ультра-низькі концентрації йоду. Крім того, винахід стосується способів рентгенологічних досліджень, в якому в організм вводять рентгенівську діагностичну композицію та опромінюють зниженою дозою випромінення. У конкретному варіанті здійснення винахід стосується рентгенівських діагностичних композицій, що мають ультра-низькі концентрації йоду та способів рентгенологічних досліджень із використанням таких, в яких організм з введеною композицією опромінюють зниженою дозою рентгенівського випромінювання. Все створення діагностичного зображення ґрунтується на досягненні різних рівнів сигналів від різних структур всередині тіла, таким чином, що дані структури можуть бути побаченими. Таким чином, в рентгенівських зображеннях, наприклад, для даної будови тіла, що є видимою на зображенні, рентгенівські промені ослабленні, тим самим будова повинна відрізнятися від будови навколишніх тканин. Різниця в сигналі між будовою тіла та його периферією часто називають контрастом, та багато зусиль було присвячено способам підвищення контрасту при створенні діагностичного зображення з більшим контрастом або чіткістю між будовою тіла або областю інтересу та його периферіями, вищій видимості або якості зображень та велике їх значення для лікаря, що виконує діагностування. Крім того, чим більший контраст, тим менші структури тіла, які можуть бути візуалізовані в процесах створення зображення, тобто збільшена контрастність може призвести до збільшеної видимої просторової роздільної здатності та видимості. Для рентгенографії, комп'ютерна томографія (КТ) передбачає 3-вимірну просторову роздільну здатність та контрастну роздільну здатність, що не забезпечує планарне рентгенівське зображення. Доза опромінення значно варіює в радіологічних процедурах. Середня ефективна доза для деяких процедур становить нижче, ніж 0,01 мЗв (таблиця 1), в той час як більш високі дози випромінювання є стандартними для процедур КТ, таких як коронарна ангіографія, де дози 16 мЗв або більше не є рідкістю, дивись (таблиця 2) Mettler et al, Radiology, vol 248: 254-263 (2008). Ефективні дози для дорослих для різних діагностичних радіологічних процедур Дослідження Череп Шийний відділ хребта Грудний відділ хребта Поперерековий відділ хребта Задньопереднє та бокове дослідження грудної клітини Задньопереднє дослідження грудної клітини Мамографія Черевна порожнина Таз Бедро Плече Коліно Інші кінцівки Подвійне вимірювання поглинання рентгенівського випромінення (без КТ) Подвійне вимірювання поглинання рентгенівського випромінення (з КТ) Внутрішньовенна урографія Верхні відділи шлунково-кишкового тракту Відділи тонкоко кишечника Барієва клізма Ендоскопічна ретроградна холангіопанкреатографія *Включає флуороскопію 30 1 Середня ефективна Значення наведені в доза (мЗв) літературі (мЗв) 0,1 0,03-0,222 0,2 0,07-0,3 1,0 0,6-1,4 1,5 0,5-1,8 0,1 0,05-0,24 0,02 0,4 0,7 0,6 0,7 0,01 0,005 0,001 0,007-0,050 0,10-0,60 0,04-1,1 0,2-1,2 0,18-2,71 … … 0,0002-0,1 0,001 0,001-0,035 0,04 0,003-0,06 3 6* 5 8* 4,0 0,7-3,7 1,5-12 3,0-7,8 2,0-18,0 … UA 108758 C2 Таблиця 1 показує ефективні дози для різних радіологічних процедур, Mettler et al, Radiology, vol 248: 254-263 (2008). Ефективні дози для дорослих для різних КТ процедур Середня ефективна доза (мЗв) 2 3 7 15 8 6 15 6 16 3 10 Дослідження Голова Шия Грудна клітина Грудна клітина для емболії сндин легень Черевна порожнина Ниркова лоханка Трифазне дослідження печінки Хребет Коронарна ангіографія Кальцієві выдкладення Фактична колоноскопія 5 10 15 20 25 30 35 40 Значення наведені в літературі (мЗв) 0,9-4,0 … 4,0-18,0 13-40 3,5-25 3,3-10 … 1,5-10 5,0-32 1,0-12 4,0-13,2 Таблиця 2 показує ефективні дози для різних КТ процедур Mettler et al, Radiology, vol 248: 254-263 (2008). Діагностична якість зображень сильно залежить від рівню власного внутрішнього шуму в процесі створення образу, та співвідношення рівня контрасту до рівня шуму або розділова здатність між контрастом та шумом може, таким чином, бути побачена, для того щоб представити ефективний діагностичний чинник якості діагностичних зображень. Досягнення покращення в такому діагностичному чиннику якості вже давно існує та до цих пір залишається важливим завданням наряду з цим збереження безпеки пацієнта, особливо від надмірного випромінювання. В методиках, таких як рентгенографія, існує один підхід до покращення діагностичного чинника якості, за яким вводять речовини, що підсилюють контрастність, сформульовані, як контрастне середовище в області тіла, зображення якого створюється. Таким чином, раніше в рентгенівських знімках прикладами контрастних агентів були нерозчинні неорганічні солі барію, які підсилювали поглинання рентгенівських променів в ділянках тіла, в яких вони розподілені. Протягом останніх 50 років в галузі рентгенівських контрастних агентів домінують розчинні сполуки, що містять йод. Комерційно доступні контрастні засоби, що містять йодвмісні контрастні агенти, як правило, класифікуються як іонні мономери, такі як діатрізоат (на ринку, наприклад, під торговою маркою Gastrografen™), іонні димери, такі як іоксаглат (на ринку, наприклад, під торговою маркою Hexabrix™), неіонні мономери, такі як іогексол (на ринку, наприклад, під торговою маркою Omnipaque™), іопамідол (на ринку, наприклад, під торговою маркою Isovue™), іомепрол (на ринку, наприклад, під торговою маркою Iomeron™) та неіонний димер іодіксанол (на ринку під торговою маркою Visipaque™). Найбільш широко використовувані комерційні неіонні рентгенівські контрастні агенти, такі як згадані вище, вважають безпечними для клінічного застосування. Контрастний засіб, що містить йодвмісні контрастні агенти, застосовують в більш ніж 20 мільйонах рентгенологічних досліджень щорічно в США, та число побічних реакцій вважається прийнятним. Однак, все ще існує необхідність вдосконалення методів створення рентгенівських та КТ зображень, забезпечуючи високу якість зображення. Дана необхідність є більш вираженою у хворих/пацієнтів з вже існуючими захворюваннями та станами або недорозвинутими/з низькою функцією нирками. Це існує тому, що деякі захворювання та низька функція нирок збільшують вірогідність розвитку побічних реакцій від ін'єкцій йодвмісних контрастних речовин. Ускладнення від раніше існуючих захворювань включають захворювання легень, захворювання нирок, захворювання серця, захворювання печінки, запальні захворювання, аутоімунні захворювання та інші супутні захворювання, наприклад, порушення обміну речовин (цукровий діабет, гіперліпідемія, гіперінсулінемія, гіперхолистеринемія, гіпертригліцеридемія та гіпертензія), серцево-судинні захворювання, захворювання периферичних судин, атеросклероз, інсульт та застійна серцева недостатність. Крім того, важливим є вік суб'єкта, оскільки більше число побічних ефектів зазначені в літньому віці, в той час як незріла функція нирок, як така може бути виявлена в маленьких дітей та немовлят, також може призвести до тривалої циркуляції контрастної речовини та більшої кількості та інтенсивності побічних реакцій. 2 UA 108758 C2 5 10 15 20 25 30 35 40 45 50 55 Ризик побічних ефектів не обмежується ефектами від контрастної речовини. Радіація, пов'язана з КТ, становить близько 70-75 % від загального іонізуючого випромінювання від діагностичної візуалізації. Разом з тим дані рівні випромінювання є значно нижчими за ті, які викликають детерміновані ефекти (наприклад, загибель клітин), існують побоювання, що вони можуть бути пов'язані з ризиком розвитку стохастичних ефектів (таких як рак, катаракти та генетичні ефекти). Тими, хто піддається найбільшому ризику розвитку раку, пов'язаного з радіаційним опроміненням, пізніше протягом життя є діти та жінки у віці від 20 років. Близько 33 % всіх КТ обстежень дітей проводяться у дітей в перші десять років життя, 17 % у дітей у віці 5 або до 5 років. Дія випромінювання в ранньому віці несе в собі ризик, тому що органи та тканини у дітей є більш чутливими до дії випромінення, ніж у дорослих, та вони мають довшу очикувану тривалість життя, що залишилася, протягом якої рак потенційно може утворитися. Крім того, сучасна поширеність КТ дає більшу імовірність, що діти отримають більш високу сумарну дозу випромінення, пов'язаного з медичними процедурами, протягом життя, ніж ті, хто в даний момент є дорослими. Оскільки такі контрастні речовини традиційно використовують для діагностичних цілей, а не для досягнення прямої терапевтичної дії, вони, як правило, є переважними для забезпечення контрастного середовища, яке має якомога менший вплив на різні біологічні механізми клітини або організму, так як це призведе до зниження токсичності та більш низького побічного клінічного ефекту. Токсичність та побічні біологічні ефекти йодвмісної контрастної речовини роблять внесок в компоненти при формуляції середовища, наприклад, розчинник або носій, а також сам контрастний агент та його компоненти, такі як іони для іонних контрастних агентів, та також його метаболітів. Основні чинники, що роблять внесок у токсичність контрастної речовини, визначають як хіміотоксичність структури йодвмісного контрастного агенту та його фізикохімічні властивості, зокрема осмоляльність контрастного середовища та іонної композиції, або їх відсутність в складі контрастної речовини. Розглядається, що бажаними характеристиками йодвмісного контрастного агенту є низька токсичність самої сполуки (хіміотоксичність), низька осмоляльність контрастної речовини, висока гідрофільність (розчинність) та високий вміст йоду, який часто вимірюють в мг йоду на мл сформульованого контрастного середовища для введення. Йодвмісний контрастний агент, до того ж, повинен бути повністю розчинним у середовищі формуляції, як правило, у водному середовищі, та залишатися в розчині під час зберігання та введення. Осмоляльність комерційних продуктів, та, зокрема, неіонних сполук, є прийнятною для більшості середовищ, що містять димери та неіонні мономери, хоча існують ще можливості для вдосконалення. В коронарній ангіографії, наприклад, ін'єкція дози болюса контрастної речовини в кровоносну систему може призвести до серйозних побічних ефектів. У цій процедурі, відразу після введення контрастної речовини, швидше ніж кров протікає через систему протягом короткого періоду часу, та відмінності в хімічній та фізико-хімічній природі контрастного середовища, та кров, яку вона замінює може викликати небажані побічні ефекти, такі як аритмія, продовження QT, зниження серцевої стискаючої сили, зниження кисневої пропускної здатності клітин крові та тканинна ішемія органу, в якому присутній високий рівень КЗ. Такі ефекти проявляються, зокрема, з іонними контрастними агентами, де хіміотоксичні та осмотоксичні ефекти є пов'язаними з підвищеним осмотичним тиском введеної контрастної речовини. Контрастні речовини, які є ізотонічними або злегка гіпотонічними з рідинами організму є особливо бажаними. Гіпоосмотичні контрастні речовини мають низьку нефротоксичність, що є особливо бажаним. У пацієнтів з гострою нирковою недостатністю, нефропатія, викликана контрастною речовиною, залишається одним з найбільш клінічно значущих ускладнень при застосуванні йодвмісної контрастної речовини. Aspelin, P et al, The New England Journal of Medicine, Vol. 348:491-499 (2003) прийшли до висновку, що нефропатія, викликана контрастною речовиною, може бути менш вірогідною для розвитку у пацієнтів високого ризику, коли іодіксанол, гіпоосмотичний агент, який ставав ізотонічним з кров'ю завдяки додаванню електролітів плазми, використовують швидше ніж низькоосмолярну, неіонну контрастну речовину. Ці одержані результати пізніше були підкріплені іншими, які показують, що осмоляльність йодовмісної контрастної речовини є ключовим чинником нефротоксичності, викликаної контрастною речовиною (CIN), та контрастна речовина викликала гостре пошкодження нирок. Частина контингенту пацієнтів, яка розглядається як пацієнти високого ризику, збільшується. Для задоволення потреби постійного вдосконалення in vivo рентгенівських діагностичних агентів для всього контингенту пацієнтів, існує постійна потреба в пошуку рентгенівських контрастних 3 UA 108758 C2 5 10 15 20 25 30 35 40 45 50 55 60 агентів та способів створення рентгенівського зображення, за яких безпека пацієнтів є оптимізованою. Для збереження низького об'єму ін'єкції контрастної речовини переважним є сформулювати контрастний засіб з високою концентрацією йоду/мл, та ще підтримувати осмоляльність засобів на низькому рівні, переважно нижче або близько до ізотонічності. Дана думка добре узгоджується із загальним правилом, що більш висока концентрація йоду, як вважається, забезпечує більш високе підсилення контрастності. Розвиток неіонних мономерних контрастних агентів та, зокрема неіонних біс(трийодфеніл)ьних димерів, таких як іодіксанол (EP 108638) забезпечує контрастні засоби зі зниженою осмотоксичністю. Це дає контрастне зображення з ефективної концентрації йоду при досягненні гіпотонічного розчину, та навіть дозволяє корекцію іонного дисбалансу шляхом включення іонів плазми, в той же час підтримуючиконтрастний засіб з необхідною осмоляльністю (наприклад, Visipaque™). Однак, для зменшення ризику побічних ефектів, особливо у чутливих суб'єктів, для покращення безпеки пацієнтів та зниження вартості, на даний момент існує необхідність зменшити кількість рентгенівського контрастного засобу, який вводять пацієнтам, яких піддають рентгенологічним дослідженням. Yoshiharu Nakayama et al Radiology, 237: 945–951, 2005 є спрямованим на способи КТ черевної порожнини з низькою напругою трубки, та приходить до висновку, що зменшення напруги на трубці, кількість контрастної речовини може бути зменшена щонайменше на 20 % без погіршення якості зображення. Крім того, він повідомив, що з низькою напругою трубки, доза опромінення може бути зменшений на 57 %. Yoshiharu Nakayama et al AJR: 187, листопад 2006 р. є спрямованим на способи КТангіографії аорти, які виконують при низькій напрузі трубки та зменшенній загальній дозі контрастної речовини. В першій групі пацієнтам вводять 100 мл іопамірону 300 мг I/мл, в той час як в другій групі вводять 40 мл того ж самого контрастного засобу. Для другої групи застосовуються зниження дози опромінення на 30 %. В публікації робиться висновок, що низька контрастність та низька напруга сканування є прийнятною для пацієнтів з меншою вагою ( 70 кг) з нирковою дисфункцією. Kristina T. Flicek et al AJR, 195: 126-131, липень 2010 є спрямованою на зниження доз опромінення для КТ колонографіі (КТК) з використанням адаптивної статистичної ітераційної реконструкції (ASIR) та припускає, що доза опромінення під час КТК може бути зменшена на 50 % без істотного впливу на якість зображення, коли застосовують ASIR. Крім того, існує, однак, бажання покращити безпеку пацієнта, який проходить рентгенологічні обстеження, і, зокрема обстеження КТ, щоб зменшити витрати на лікування та зробити контрастно підсилений рентген/КТ доступним для пацієнтів, які зазначені раніше, не контрастно підсилені зображення. Представлений винахід передбачає композицію та спосіб створення рентгенівського зображення, в якому для покращення безпеки пацієнтів застосовують поєднання зниженої концентрації контрастного засобу та зниження дози рентгенівського випромінювання. Існує спосіб оптимізації безпеки пацієнта, такої як безпеки дорослого пацієнтів, дитини та немовляти, під час процедури рентгенівського/КТ сканування. Існує п'ять основних змінних, які враховують при оптимізації зображень: доза опромінення, концентрація контрастного засобу, доза контрастного засобу, швидкість (темп) ін'єкційного введення контрастного засобу (ставка), якість зображення та, до сих пір, три основних змінних, які необхідно враховувати при оптимізації безпеки пацієнта та мінімізації ризику пацієнта. Існують: доза опромінення, доза контрастного засобу та якість зображення. Заявник досліджував та несподівано виявив, що концентрація контрастного засобу може бути зменшена до несподівано низьких рівнів без шкоди контрастності до шуму та/або якості отриманого рентгенівського зображення. Щодо композицій та способів винаходу, існує декілька цілей, що досягаються. Значна економія коштів може бути досягнена шляхом зниження вартості за рахунок зменшення застосування контрастних засобів з більш високими концентраціями таким чином, щоб досягти економії вартості товару та економії вихідної речовини. Крім того, існує непряма економія витрат, пов'язана зі зниженням випромінювання, таким чином, в сукупності може бути знижена вартість лікування. Найбільш важливо, що існують переваги безпеки пацієнта за рахунок поєднання зниженої концентрації йоду, та сумарної дози контрастного засобу, та зниженого радіаційного опромінення. Нижча доза опромінення рентгенологічних/КТ процедур є особливо корисною для педіатричних (дітей та немовлят) рентгенологічних/КТ досліджень та для пацієнтів високого ризику з вже існуючими захворюваннями, при яких одноразове або повторні контрастно підсилене рентгенологічне дослідження та КТ є необхідними для діагностики стану, розвитку або навіть зниження захворювання у відповідь на втручання лікаря. Експозиція з більш 4 UA 108758 C2 5 10 15 20 25 30 35 40 45 50 55 60 низькими концентраціями йоду є особливо корисною для пацієнтів з вже існуючими захворюваннями, такими як знижена функція серця та нирок. Таким чином, досягають фіксовану або більш високу якість зображення, та побічні ефекти можуть зводити до мінімуму. Зображення достатньо високої якості можуть бути одержані при низьких дозах опромінення для більшої кількості пацієнтів, як правило, для тих, які раніше не були направлені на контрастно підсилене сканування, пацієнтів, яким необхідні повторні сканування, наприклад, для допоміжного терапевтичного моніторингу або лікування хвороби, або пацієнтів з факторами ризику, наприклад, в результаті впливу радіаційного опромінення, або пацієнта факторів ризику. Використовуючи композицію та спосіб відповідно до винаходу, оптимальний баланс щодо якості зображення, радіаційного опромінення та концентрації йоду до окремого пацієнта може бути досягнутий шляхом, або зниження концентрації йоду, та/або за рахунок зниження дози опромінення. Таким чином, у першому аспекті винахід передбачає композицію для рентгенологічної діагностики, що містить йодвмісний рентгенівський контрастний агент разом з фармацевтично прийнятним носієм або наповнювачем, де композиція має ультра-низькою концентрацією йоду. В одному варіанті здійснення винаходу композиція містить суміш двох або більше йодвмісних рентгенівських контрастних агентів. "Контрастні агенти", є агентами, які містять речовину, яка може значно послаблювати характерне рентгенівське випромінювання, яке викликає зменшення випромінювання, що передається за рахунок об'єму зони, що цікавить. Після проведення реконструкції КТ зображення та типової пост-обробки, дане збільшене рентгенівське послаблення інтерпретується як збільшення щільності об'єму або області, що викликає зацікавленність, яка створює підсилення контрастності або покращує визначення об'єму, що містить контрастний агент відповідно до фонової тканини на зображенні. Терміни композиція, композиція для рентгенологічної діагностики та контрастний засіб будуть використовувати взаємозамінно в даному документі, та мають однаковий зміст. Під терміном "ультра-низька концентрація" (ULC) йоду ми визначаємо концентрацію, яка становить 10-170 мг I/мл, або більш переважно 10-150 мг I/мл, ще більш переважно 10-100 мг I/мл, та найбільш переважно 10-75 мг I/мл. В особливо переважному втіленні концентрація йоду становить менше, ніж 100 мг I/мл. Знайдено, що концентрація рентгенівської композиції є важливою, так як композиція, при введенні в організм, замінює кров. При зниженні дози опромінення рентгенівської трубки, тобто за рахунок зниження напруги на трубці (максимум кіловольт або кВ), тобто різниці потенціалів між катодом і анодом, та вводячи ультра-низькі концентрації йоду, якість зображення, тобто ефект контрасту, фактично зберігається або покращується. Це відбувається тому, що значення послаблення йодованого приросту збільшується на більш низькій напрузі трубки, так як доза випромінювання має середній енергетичний спектр, який в основному відповідає К-смузі йоду, що в результаті призводить до більшого зростання. HU значення йоду (одиниці Хаунсфілда) у зображенні КТ є більшими, тобто якість зображення підвищується, при більш низьких пікових напругах в кВ, тому що середня енергія спектру є ближче до К-смуги йоду (33,2 кеВ (кілоелектрон-вольт)), таким чином, збільшення коефіцієнта ослаблення йоду при нижчих рентгенівських енергіях в результаті призводить до більш високих значень HU зображення КТ. Щоб прояснити, це є фактичною концентрацією речовини, переважно йоду, яка послаблює відбиття рентгенівського випромінювання, що знижується, і не тільки від дози йодовмісного контрастного засобу (об'єму). Як наслідок, якщо об'єми введеного йодвмісного контрастного агенту залишаються тими самими та концентрація йоду на основі контрастного агенту зменшується, то загальна кількість йодвмісного контрастного агенту, яку вводять в організм, може бути зменшена. Застосування композиції за винаходом, що містить ультра-низькі концентрації йоду, або використовуючи спосіб за другим аспектом, має переваги над безпосереднім зниженням загальної стандартної дози діагностичної композиції або зменшенням швидкості її введення. Виявлено, що концентрація йоду є більш важливою, ніж доза, для можливості створення зображення після того, як контрастний засіб відштовхує кров в бік та тобто витісняє або замінює кров, так що він один "створює зображення". Оскільки загальна доза контрастного засобу зменшується, так як зменшується концентрація контрастного засобу, доза контрастного агенту має важливе значення для безпеки пацієнта. Контрастний агент заявленої композиції стосується одного втілення йодвмісної рентгенівської сполуки. Переважно, композиція за винаходом є контрастним засобом з нізкою осмоляльністю (LOCM). Переважно, контрастний агент є неіонною йодвмісною мономерною сполукою або неіонною йодвмісною димерною сполукою, тобто сполукою, що містить одиничні трийодфенільні групи або сполукою, що містить дві з'єднані трийодфенільні групи. Однак, 5 UA 108758 C2 5 10 15 20 25 30 тримерні, тетрамерні та пентамерні сполуки також є включеними. Це відбувається, тому що, коли кількість мультімерів збільшується, осмоляльність зменшується. Це є важливим, тому що це означає, що більше сироваткових електролітів можуть бути доданими до розчину, щоб зробити його ізотонічним. Таким чином, те, що вводять, є в основному електролітами плазми. Крім того, до сих пір відомо, що в'язкість зростає зі збільшенням числа мультімеров, ULC підхід може означати, що мультімерні агенти на даний час є прийнятними для застосування при низькій концентрації, що є необхідним для створення зображення, що знизило б загальну в'язкість, що робить можливим практичне застосування даних сполук. Прийнятні мономерні та димерні сполуки є передбаченими в заявці WO2010/079201 заявника. Особливо прийнятні мономерні сполуки є описаними в WO97/00240 та, зокрема сполуки BP257 прикладу 2, та додатково комерційно доступні сполуки іопамідол, іомепрол, йоверсол, йопромід, йоверсол, йобітридол, йопентол та йогексол. Найбільш особливо переважними є сполуки йопамідол та йогексол. Особливо прийнятні димерні сполуки є сполуками формули (I) з двох з'єднаних трийодфенільних груп, що означають неіонні димерні сполуки, 6 R─N(CHO) ─X─N(R )─R формула (I) та солі або їх оптично активні ізомери, де X означає від C3 до C8 лінійний або розгалужений алкіленовий залишок, необов'язково з 4 однією або двома CH2 залишками, заміщеними на атоми оксигену, атоми сульфуру або NR 4 групи, та де алкіленовий залишок є необов'язково заміщеним на аж до шести –OR групи; 4 R означає атом гідрогену або від C1 до C4 лінійну або розгалужену алкільну групу; 6 R означає атом гідрогену або ацильну функціональну групу, таку як формільна група; та кожна R незалежно є однаковими або різними та означає трийодфенільну групу, переважно 5 5 2,4,6-трийодфенільну групу, крім того, заміщеною двома групами R , де кожна R є однаковими або різними та означає атом гідрогену або неіонний гідрофільний залишок за умови, що 5 щонайменше одна R група в сполуці формули (II) є гідрофільним залишком. Переважні групи та сполуки є описаними в заявках WO2010/079201 та WO2009/008734, які є включеними в даний документ як посилання. Особливо переважними димерними контрастними агентами, які можуть бути застосовані в композиції або способі за винаходом, є сполуки йодіксанол (Візипак) та сполука формули (II): O HO I H OH O H N I HN O I O N I N H HO O I I O OH OH 40 45 50 OH NH HO 35 OH N H OH формула (II) Сполуці формули (II) була надана міжнародна невласна назва йоформінол. Таким чином, в перважному втіленні винахід передбачає композицію, що містить йодіксанол або йоформінол, або обидва, де композиція має ультра-низьку концентрацію йоду. Композиція для рентгенологічної діагностики за винаходом може бути в готовій до застосування концентрації, або може бути в концентрованій формі для розбавлення перед введенням, або вона може бути аморфним порошком, який може бути змішаний з електролітами плазми перед введенням. Може бути бажаним компенсувати тонічність розчину шляхом додавання катіонів плазми таким чином, щоб зменшити внесок токсичності, який походить від дисбалансу ефектів після ін'єкції ударної дози речовини. Зокрема, додавання іонів натрію, кальцію та магнію, щоб забезпечити ізотонічність контрастного зособу з кров'ю для всіх концентрації йоду, є бажаним та досяжним. Катіони плазми можуть бути представлені у вигляді солей з фізіологічно прийнятними протиіонами, наприклад, хлоридами, сульфатами, фосфатами, гідрокарбонатами, тощо, які переважно використовуються з аніонами плазми. Для зниження серцево-судинних ефектів існує можливість додавати електроліти до контрастного засобу. В одному втіленні винахід передбачає дозу композиції, таку як доза для рентгенологічної діагностики для введення, де композиція містить ультра-низьку концентрацію йоду, та де загальний об'єм композиції становить від 1 до 50 мл. Для рентгенівських діагностичних композицій, які вводять шляхом ін'єкції або інфузії, бажана верхня межа в'язкості розчину при температурі навколишнього середовища (20 °C) становить 6 UA 108758 C2 . 5 10 15 20 25 30 35 40 45 50 55 . . близько 30 мПа с, однак в'язкість аж до 50 до 60 мПа с та навіть більший, ніж 60 мПа с може бути прийнятним. Для рентгенівських діагностичних композицій, які вводяться шляхом ін'єкції ударної дози речовини, наприклад, в ангіографічних процедурах, повинні бути розглянуті осмотоксичні ефекти та, переважно, осмоляльність повинна бути нижче 1 осмоль/кг H 2O, переважно нижче 850 мосмоль/кг H2O та більш переважно близько 300 мосмоль/кг H 2O. З композицією за винаходом така мета щодо в'язкості, осмоляльності та концентрації йоду може бути досягнута. Дійсно, ефективні концентрації йоду можуть бути досягнуті в гіпотонічних розчинах, тобто з меншою ніж 200 мосмоль/кг H2O. Композицію для рентгенологічної діагностики можуть вводити шляхом ін'єкції або інфузії, наприклад, шляхом внутрішньосудинного введення. В одному втіленні, композицію для рентгенологічної діагностики вводять як швидку внутрішньосудинну ін'єкцію, в іншому втіленні її вводять як рівнгомірну інфузію. Альтернативно, композицію для рентгенологічної діагностики можуть також вводити перорально. Для перорального введення композиція може бути у формі капсули, таблетки або як рідкий розчин. У другому аспекті винахід передбачає спосіб рентгенологічного обстеження, який включає введення в організм композиції для рентгенологічної діагностики, що містить рентгенівський контрастний агент, застосування зниженої дози опромінення до організму, дослідження організму за допомогою діагностичного приладу та збір даних з дослідження. В одному з втілень єдина мета способу за винаходом полягає в одержанні інформації. Спосіб може включати аналіз даних. В іншому втіленні спосіб додатково включає стадію порівняння одержаної інформації з іншою інформацією таким чином, щоб міг бути поставлений діагноз. В одному втіленні спосіб дослідження є способом діагностики або є допоміжним засобом для діагностики. Зменшену дозу опромінення застосовують до організму, наприклад, для конкретної області тіла, що представляє інтерес. На даний момент алгоритми рентгенівського/КТ обладнання розглядають тільки якість зображення та дозу опромінення як параметри оптимізації (тобто зниження) дози опромінення та/або покращення якості зображення. Як правило, доза опромінення, яка є необхідною для одержання зображення певної якості в рентгенівському/КТ скануванні, може бути зменшена, використовуючи передові алгоритми для зменшення шумів на зображенні, пов'язаних з нижчим радіаційним опроміненням при одержанні зображень. Крім того, заявником на даний момент встановлено, що при зниженні напруги на трубці, кількість контрастної речовини може бути зменшена до несподівано низьких рівнів за рахунок зниження концентрації без погіршення якості зображення. У випадках, коли рентгенівське/КТ сканування вимагає покращених оптимальних зображень вводять контрастний агент, який містить речовину, що послаблює опромінення, з високим атомним числом, наприклад, йодовмісний контрастний засіб, для покращення контрастності та одержання зображення необхідної якості. Чинники, що впливають на рішення про застосування композиції для рентгенологічної діагностики, є або не пацієнти групи ризику, такі як з надлишковою масою тіла (ожиріння), низькою функцією нирок, низькою функцією печінки, вік (немовляти, діти, та похилого віку) та/або з супутніми захворюваннями, наприклад, порушення обміну речовин (цукровий діабет, гіперліпідемія, гіперінсулінемія, гіперхолестеринемія, гіпертригліцеридемія та гіпертензія), серцево-судинні захворювання, захворювання периферичних судин, атеросклероз, інсульт, застійна серцева недостатність, або тип процедури, наприклад, внутрішньовенний, внутрішньоартеріальний, периферичний, серцевий, ангіографія та КТ. Хоча було показано, що низькі дози контрастного засобу та низькі напруги сканування є прийнятними для пацієнтів з невеликою масою тіла (маса тіла 0,99) як функція концентрації йоду при 120, 100 та 80 кВ пікової напруги збору даних. Дивись фігуру 6. 45 50 55 - Використовуючи стандартний FBP, CNRD збільшився на 24 % при зборі даних при низькій піковій напрузі 80 кВ у порівнянні зі 120 кВ пікової напруги. - Для всіх трьох комплектувань – при 120, 100 та 80 кВ пікової напруги, CNRD збільшилися в середньому на 47 % (в межах 44-50 %), використовуючи ASIR (60 %) ітераційна реконструкція в порівнянні з FBP. Дивись фігуру 6. - Не існувало значної різниці в отриманих CNRD між рівнями високої та низької дози опромінення (CTDIvol), використовуючи ASIR. На відміну від цього, результати Veo безперечно знаходилися в залежності від рівня дози опромінення: - При стандартному рівні дози опромінення (10,8 мГр), CNRD збільшився в середньому на 60 % (в межах 56-64 %) у порівнянні з FPB, в той час як при низькому рівні дози опромінення (2,7 мГр), CNRD збільшився на 103 % (в межах 96-110 %). - Для рівних CNRD, використовуючи 80 кВ пікової напруги дає зниження концентрації йоду приблизно на29 % у порівнянні зі стандартними 120 кВ пікової напруги сканування. 13 UA 108758 C2 5 10 15 20 25 30 35 40 45 50 55 60 - З ASIR та Veo надане зниження концентрації йоду збільшилося аж до 53 % та 61 %, відповідно. При низькому рівні дози, Veo дає зниження концентрації йоду на 68 %. У порівнянні зі стандартними FBP, обидва типи ітераційної реконструкції, ASIR та Veo, значно покращили CNRD в дослідженнях з йодвмісним контрастом. Відносна користь ASIR не залежить від дози опромінення. З Veo, однак, відносний CNRD збільшився при нижчих дозах опромінення. Дані результати ілюструють потенціал для зменшення концентрації йоду та/або зниження дози опромінення пацієнтів при застосуванні ітераційної реконструкції при низькій піковій напрузі сканувань в кВ. Екстраполяція до клінічних умов: Хоча CNRD є однаковими при 80 кВ пікової напруги, це дозволяє зниження концентрації йоду приблизно на 29 % у порівнянні зі стандартними 120 кВ пікової напруги сканування. Ці дані припускають, що, встановлений взаємозв'язок між концентрацією ін'єкційно введеного йодвмісного контрастного агенту та концентрації, яка виявляється в кровоносних судинах під час клінічних ангіографічних КТ процедур, ін'єкційно введена (концентрація у флаконі) концентрація може бути зменшена зі стандартної концентрації, наприклад, з 320 мг I/мл до 227,2 мг I/мл (тобто 71 % з 320 мг I/мл). Звідси випливає, що, якщо об'єми ін'єкційно введеного йодвмісного контрастного агенту залишаються тими самими та концентрація йоду на основі контрастного агенту зменшується, загальна кількість ін'єкційно введеного йодвмісного контрастного агенту в організмі, буде зменшена. Це зниження загальної кількості йодвмісного контрастного агенту спричиняло б менше побічних ефектів (особливо для нирок) для пацієнта та надавало б значні переваги в безпеці пацієнтів. Показано, що завдяки алгоритмічним реконструкціям цих даних за допомогою ASIR та Veo концентрація йоду може бути додатково зменшена, аж до 53 % та 61 %, відповідно. Ці дані показують, що концентрація у флаконі може бути додатково зниженою від стандартних концентрацій (наприклад, 320 мг I/мл) до 150,4 мг I/мл та 124,8 мг I/мл, відповідно, шляхом застосування ітераційних способів реконструкції. Крім того, оскільки при низькому рівні дози опромінення (2,7 мГр) модель на основі ітераційного реконструкції з використанням Veo передбачає, що концентрація йоду може бути зменшена на 68 %, це передбачає, що концентрація в флаконі може бути додатково зменшена до 102,4 мг I/мл. Таким чином, випливає, що, якщо об'єми ін'єкційно введеного йодвмісного контрастного агенту залишаються тими ж самими та концентрація йоду на основі контрастного агенту є ще більше зниженою, то загальна кількість ін'єкційно введеного йодвмісного контрастного агенту в організмі може бути радикально зниженою з Veo, наприклад, до концентрації нижче 100 мг I/мл. Це додаткове зниження загальної кількості йодвмісного контрастного агенту призведе до ще менших побічних ефектів для пацієнта та надасть значні переваги для безпеки пацієнта, особливо тих суб'єктів, які були б чутливими до потенційно несприятливих подій, таких як порушення функції нирок, викликане йодвмісним контрастним агентом, або гостре пошкодження нирок, викликане контрастним засобом. Приклад 6: Комп'ютерна томографія з подвійною енергією (DECT) та ітераційні методи реконструкції сприяє зниженій концентрації йоду з покращеним співвідношенням контрастності до шуму (CNR): Сканування з використанням КТ з подвійною енергією (DECT) та застосування обробки спектральних зображень Gemstone (GSI) адаптує спектральну інформацію, яку одержують шляхом реконструкції синтетичних монохроматичних зображень від 40 до 140 кеВ. Зображення з вибором низької енергії ( 0,99), як функція від концентрації йодвмісного контрастного агента для всіх досліджуваних протоколів випробування. Для всіх випробуваних концентрацій 14 UA 108758 C2 5 10 15 20 25 30 35 40 45 йоду, обидва DECT сканування показують покращення максимальних CNR близько до 36 % у порівнянні зі стандартними 120 кВ пікової напруги сканування в тій самій дозі випромінювання (21,8 мГр). Без сучасних прийомів послаблення шуму максимальний CNR пік спостерігався при 68 кеВ зі швидким падінням при більш низьких енергіях у зв'язку з переважанням шуму. Дане CNR падіння запобігають, використовуючи передові прийоми послаблення шуму, так, що CNR залишається фіксованим в більшому каналі реєстрації випромінювання (40-70 кеВ). На обох рівнях дози опромінення, обидві GSI версії (з та без послаблення шуму) дозволяють знизити концентрацію йодвмісного контрастного агенту приблизно на 25 %у порівнянні зі стандартними 120 кВ пікової напруги сканування для однакових CNR. Даний фантом дослідження показує, що CNR з йодом може бути суттєво покращений шляхом застосування DECT, та, що залучення сучасних прийомів послаблення шуму збільшує прийнятний канал реєстрації випромінення без шкоди для якості зображення. Результати показують потенціал або для зниження концентрації йоду та/або для зниження дози опромінення пацієнта при застосуванні ітераційної реконструкції на DECT. Екстраполяція в клінічних умовах: GSI версії дозволяють знизити концентрацію йодвмісного контрастного агенту приблизно на 25 % у порівнянні зі стандартними 120 кВ пікової напруги сканування для однакових CNR. Ці дані передбачають, що, враховуючи взаємозв'язок між концентрацією ін'єкційно введеного йодвмісного контрастного агенту та концентрацією присутнього в кровоносних судинах під час клінічних ангіографічних КТ процедур, ін'єкційно введена (концентрація у флаконі) концентрація може бути зниженою по відношенню до стандартної концентрації, наприклад, з 320 мг I/мл до 240 мг I/мл. Звідси випливає, що, якщо об'єми ін'єкційно введеного йодвмісного контрастного агенту залишаються тими ж самими та концентрація йоду на основі контрастного агенту зменшується, то загальна кількість ін'єкційно введеного йодвмісного контрастного агенту в організм, буде зменшена. Дане зниження загальної кількості йодвмісного контрастного агенту буде мати менше побічних ефектів (особливо для нирок) для пацієнта та надасть значні переваги для безпеки пацієнтів. Приклад 7: Поєднання зниженої концентрації йоду, зниженої дози опромінення та сучасних методик реконструкції зберігає співвідношення сигналу-до-шуму (SNR) контрастних підсилених КТ зображень черевної порожнини у свині: Отримували зображення анестезованої карликової свинки (максимальний та мінімальний черевні діаметри 36 см та 20 см, відповідно) 3 рази (протоколи зображення 1, 2 та 3 таблиці 3 та 4) на Discovery CT 750 HD. Візипак (60 мл) вводили зі швидкістю 2 мл/с в яремну вену, після чого промивали 20 мл сольового розчину з тією ж швидкістю ін'єкційного введення. Щонайменше було 2 дні періоду виведення між кожною сесією сканування. Протокол 1 з концентрацією візипаку 320 мг I/мл та 120 кВ піковової напруги на трубці представляє собою сучасний стандарт клінічної практики (SoC) отримання зображення для людей. Автоматизовану модуляцію сили струму трубки (≤ 500 мА) використовували з рівнем індексу шуму 30 та часом обертання трубки 0,7 с. Пост-контрастні КТ зображення були одержані під час артеріальної фази, фази портальної вени, венозної фази та пізнішої фази. Реконструкцію зображення виконували, використовуючи (1) FBP, (2) ASiR 60 % та (3) Veo. Розмір пікселя становив 0,703 мм х 0,703 мм х 0,625 мм. Підвищення контрастності йоду оцінювали шляхом вимірювання співвідношення сигналу-дошуму (SNR) кругових областей, що викликають зацікавленість (ROI), дивись таблиці 3 та 4. SNR розраховують як співвідношення середньої ROI інтенсивності в HU та стандартного відхилення (SD). ROI були розташовані в аорті та м'язі (квадратний м'яз попереку) в зображеннях артеріальної фази та в печінці в зображеннях венозної фази. Номер протоколу 1 2 3 Концентрація Візипаку [мг I/мл] 320 170 120 Пікова напруга на трубці [кВ] 120 80 80 Доза CTDIvol [мГр] 6,7 3,2 6,4 50 15 FBP [SNR] ASiR 60 % [SNR] Veo [SNR] 7,4 8,5 12,8 14,2 8,3 Фіг. 7 8A, 9A 8B, 9B UA 108758 C2 Таблиця 3: Одержання зображення та аналіз даних зображень артеріальної фази, що охоплює аорту та м'яз. CTDIvol: об'єм дози індексу КТ 1 Концентрація Візипаку [мг I/мл] 320 Пікова напруга на трубці [кВ] 120 Доза CTDIvol [мГр] 6,7 2 170 80 3,2 3,5 8,1 3 120 80 6,4 4,7 8,1 Номер протоколу 5 10 15 20 25 30 35 40 45 FBP [SNR] ASiR 60 % [SNR] Veo [SNR] 4,3 Фіг. 10 11A, 12A 11B, 12B Таблиця 4: Одержання зображення та аналіз даних зображень венозної фази, що охоплюють печінку. CTDIvol: об'єм дози індексу КТ Той самий SNR (в межах 15 %) спостерігається з протоколом 1 та FBP реконструкцією, протоколом 2 та ASIR 60 % реконструкцією та протоколом 3 і ASIR 60 % реконструкцією. SNR з протоколами 2 і 3 та Veo реконструкцією є приблизно в два рази більшим. Висновки: така ж сама якість зображення у відповідності з SNR спостерігається зі зменшенням сили струму трубки на 80 кВ пікової напруги (в порівнянні з SoC установкою 120 кВ пікової напруги) та ASiR 60 % (у порівнянні зі стандартним методом FBP SoC), при одночасному (а) зменшенні концентрації йод-контрасту до 170 мг I/мл та вдвічі дози опромінення, або (б) зниженні концентрації йод-контрасту далі до 120 мг I/мл та підтриманні дози опромінення на тому ж рівні, що і в умовах SoC. Екстраполяція до клінічних умов: Ці дані несподівано показали, що SNR є подібним до артеріальної фази, тобто 7,4 та 8,5, коли концентрація йоду знижується до 170 мг I/мл та 120 мг I/мл тобто на ~ 47 % та ~ 62 % нижче, ніж при 320 мг I/мл, коли дані є реконструйованими з використанням ASIR. Ще більш дивно, SNR є ще вищим в артеріальній фазі, тобто 12,8 та 14,2, коли дані є реконструйованими з використанням Veo. Крім того, в венозній фазі SNR є подібними, тобто 3,5 та 4,7, коли концентрація йоду знижується до 170 мг I/мл та 120 мг I/мл, тобто на ~ 47 % та ~ 62 % нижче, ніж при 320 мг I/мл, коли дані є реконструйованими з використанням ASIR. І на цей раз, та дивно SNR є ще вищим, у венозній фазі, тобто 8,1 та 8,1, коли дані є реконструйованими з використанням Veo. Ці дані передбачають, що, враховуючи взаємозв'язок між концентрацією ін'кційно введеного йодвмісного контрастного агенту та концентрацією присутню в кровоносних судинах під час клінічних ангіографічних КТ процедур, ін'кційно введена (концентрація у флаконі) концентрація може бути зменшена по відношенню до стандартної концентрації, наприклад, з 320 мг I/мл до від 170 мг I/мл до 120 мг I/мл. Звідси випливає, що, якщо об'єми ін'кційно введеного йодвмісного контрастного агенту залишаються тими самими та концентрація йоду на основі контрастного агенту зменшується, то загальна кількість ін'кційно введеного йодвмісного контрастного агенту в організм буде зменшена. Дане зменшення загальної кількості йодвмісного контрастного агенту дало б менше побічних ефектів для немовлят, дітей та дорослих пацієнтів, та надало б значні переваги для безпеки пацієнтів, особливо тих суб'єктів, в кого недорозвинуті нирки, або тих, хто був би чутливим до потенційних несприятливих наслідків, таких як викликане йодвмісним контрастним агентом порушення функції нирок або викликане контрастним засобом гостре ураження нирок. Крім того, також пердбачається відповідне зниження рівнів дози опромінення до 6,4 таі 3,2 мГр після 120 мг I/мл / 80 кВ пікової напруги та 170 мг I/мл / 80 кВ пікової напруги в порівнянні з 6,7 мГр (320 мг I/мл та 120 кВ пікової напруги), та одночасно є можливими більш низькі рівні опромінення. Оскільки опромінення в ранньому віці несе ризик для органів та тканин, нижче радіаційне опромінення було б значною додатковою перевагою у даних суб'єктів. Підписи до фігур: Фігури 7-9: In vivo КТ зображення карликової свині, одержані під час артеріальної фази після введення Візипаку. Суцільна стрілка вказує на аорту, пунктирна стрілка – на м'яз (квадратний м'яз попереку). Відповідні КТ параметри наведені в таблиці 3. Реконструкцію виконували з використанням FBP (фігура 7), ASiR 60 % (фігури 8А, 8Б) та Veo (фігури 9А, 9В). 16 UA 108758 C2 Фігури 10-12: In vivo КТ зображення карликової свині, одержані під час венозної фази після введення Візипаку. Суцільна стрілка вказує на печінку. Відповідні КТ параметри наведені в таблиці 4. Реконструкцію виконували з використанням FBP (фігура 10), ASiR 60 % (фігури 11А, 11В) та Veo (фігури 12А, 12В). 5 ФОРМУЛА ВИНАХОДУ 10 1. Рентгенівська діагностична композиція, що містить йодовмісний рентгенівський контрастний агент та фармацевтично прийнятний носій або наповнювач, в якій композиція має концентрацію йоду від 10 до менше ніж 100 мг І/мл, йодовмісний рентгенівський контрастний агент являє собою сполуку формули ІІ O HO I H OH N N H O H I O N I HN O I I O OH OH 20 25 30 OH NH HO 15 OH N H I HO O OH , формула II. 2. Спосіб рентгенологічного дослідження, за яким в організм вводять композицію за п. 1, застосовують дозу рентгенівського випромінювання до організму, що передбачає енергію напруги на трубці в діапазоні 70-140 кВ пікової напруги, обстежують організм з використанням діагностичного обладнання, збирають дані з обстеження, і який додатково включає зниження шуму за рахунок сучасного способу реконструкції зображення. 3. Спосіб за п. 2, який підвищує контрастний ефект контрастного агента, де контрастний агент є йодовмісним, та де зазначена доза опромінення має середній спектр енергії, який в основному відповідає К-смузі йоду. 4. Спосіб за п. 2, в якому дозу рентгенівського випромінювання забезпечують за рахунок сили струму трубки в діапазоні 5-1000 мА. 5. Спосіб за п. 2, в якому зниження шуму вибирають з ітераційних способів реконструкції зображення ASiR або MBIR. 6. Спосіб за п. 2, який включає КТ з подвійною енергією. 7. Спосіб за будь-яким з пунктів 2-6, в якому об'єм композиції, що містить йодовмісний рентгенівський контрастний агент, становить від 1 до 50 мл. 8. Спосіб за п. 2, в якому рентгенівський контрастний агент містить наночастинки з атомним числом 53 або вище. 17 UA 108758 C2 18 UA 108758 C2 19 UA 108758 C2 20 UA 108758 C2 21 UA 108758 C2 Комп’ютерна верстка Л. Бурлак Державна служба інтелектуальної власності України,вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 22
ДивитисяДодаткова інформація
Назва патенту англійськоюX-ray imaging at low contrast agent concentrations and/or low dose radiation
Автори англійськоюKaiser, Clemens, Newton, Ben
Автори російськоюКайзер Клеменс, Ньютон Бен
МПК / Мітки
МПК: A61K 49/04
Мітки: дозою, низькою, контрастної, рентгенівська, спосіб, діагностична, концентраціями, композиція, дослідження, речовини, рентгологічного, опромінення, низькими
Код посилання
<a href="https://ua.patents.su/24-108758-rentgenivska-diagnostichna-kompoziciya-z-nizkimi-koncentraciyami-kontrastno-rechovini-ta-sposib-rentgologichnogo-doslidzhennya-z-nizkoyu-dozoyu-oprominennya.html" target="_blank" rel="follow" title="База патентів України">Рентгенівська діагностична композиція з низькими концентраціями контрастної речовини та спосіб рентгологічного дослідження з низькою дозою опромінення</a>
Попередній патент: Зносостійкий сплав
Наступний патент: Похідні 6,7-дигідро-5н-бензо[7]анулену, спосіб їх одержання, фармацевтичний препарат, що їх містить, та їх застосування для одержання лікарських засобів
Випадковий патент: Пристрій захищеного голосового радіоуправління функціями безпілотного літального апарата












