Похідні хіноліну для застосування як мікобактеріальних інгібіторів
Номер патенту: 83875
Опубліковано: 26.08.2008
Автори: Жільмон Жером Еміль Жорж, Ланкуа Давід Франсіс Ален, Паск'є Елізабет Тереза Жанна
Формула / Реферат
1. Сполука формули (І)
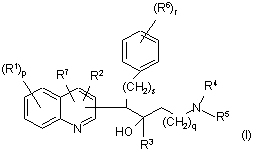 ,
,
її фармацевтично прийнятні кислотно- або основно-адитивні солі, її четвертинні аміни, її стереохімічно ізомерні форми, її таутомерні та N-оксидні форми, де
R1 являє собою водень, галоген, галогеналкіл, ціано, гідрокси, Аr, Het, алкіл, алкілокси, алкілтіо, алкілоксіалкіл, алкілтіоалкіл, Аr-алкіл або ді(Аr)алкіл;
р означає ціле число, рівне 1, 2 або 3;
s означає ціле число, рівне нулю, 1, 2, 3 або 4;
R являє собою водень; галоген; алкіл; гідрокси; меркапто; алкілоксигрупу, необов'язково заміщену аміно або моно- або ді(алкіл)аміно, або радикалом формули
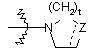 , де Z являє собою СН2, CH-R8, О, S, N-R8, a t означає ціле число, рівне 1 або 2, а пунктирна лінія означає необов'язковий зв'язок; алкілоксіалкілокси; алкілтіо; моно- або ді(алкіл)аміно, де алкіл може бути необов'язково заміщений одним або двома замісниками, кожен незалежно вибраний з алкілокси або Аr, або Het, або морфолінілу, або 2-оксопіролідинілу; Аr, Неt або радикал формули
, де Z являє собою СН2, CH-R8, О, S, N-R8, a t означає ціле число, рівне 1 або 2, а пунктирна лінія означає необов'язковий зв'язок; алкілоксіалкілокси; алкілтіо; моно- або ді(алкіл)аміно, де алкіл може бути необов'язково заміщений одним або двома замісниками, кожен незалежно вибраний з алкілокси або Аr, або Het, або морфолінілу, або 2-оксопіролідинілу; Аr, Неt або радикал формули 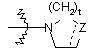 , де Z являє собою СН2, CH-R8, О, S, N-R8; t означає ціле число, рівне 1 або 2; а пунктирна лінія означає необов'язковий зв'язок;
, де Z являє собою СН2, CH-R8, О, S, N-R8; t означає ціле число, рівне 1 або 2; а пунктирна лінія означає необов'язковий зв'язок;
R3 являє собою алкіл, Аr, Аr-алкіл, Het або Het-алкіл;
q означає ціле число, рівне нулю, 1, 2, 3 або 4;
R4 та R5, кожен, незалежно являє собою водень, алкіл або бензил; або
R4 та R5, разом та включаючи N, до якого вони приєднані, можуть утворювати радикал, вибраний із групи, що включає піролідиніл, 2Н-піроліл, 2-піролініл, 3-піролініл, піроліл, імідазолідиніл, піразолідиніл, 2-імідазолініл, 2-піразолініл, імідазоліл, піразоліл, триазоліл, піперидиніл, піридиніл, піперазиніл, імідазолідиніл, піридазиніл, піримідиніл, піразиніл, триазиніл, морфолініл та тіоморфолініл, кожен з зазначених циклів необов'язково заміщений алкілом, галогеном, галогеналкілом, гідрокси, алкілокси, аміном, моно- або діалкіламіном, алкілтіо, алкілоксіалкілом, алкілтіоалкілом та піримідинілом;
R6 являє собою водень, галоген, галогеналкіл, гідрокси, Аr, алкіл, алкілокси, алкілтіо, алкілоксіалкіл, алкілтіоалкіл, Аr-алкіл або ді(Аr)алкіл; або
два сусідніх радикали R6 можуть разом з фенільним кільцем, до якого вони приєднані, утворювати нафтил;
r означає ціле число, рівне 1, 2, 3, 4 або 5; та
R7 являє собою водень, алкіл, Аr або Het;
R8 являє собою водень, алкіл, гідроксил, амінокарбоніл, моно- або ді(алкіл)амінокарбоніл, Аr, Het, алкіл, заміщений одним або двома Het, алкіл, заміщений одним або двома Аr, Het-C(=O)- або Аr-С(=O)-;
алкіл являє собою нерозгалужений або розгалужений насичений вуглеводневий радикал, що містить від 1 до 6 атомів вуглецю; або являє собою циклічний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю; або являє собою циклічний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю, приєднаний до нерозгалуженого або розгалуженого насиченого вуглеводневого радикала, що містить від 1 до 6 атомів вуглецю; де кожен атом вуглецю може бути необов'язково заміщений галогеном, гідрокси, алкілокси або оксо;
Аr означає гомоцикл, вибраний з групи, що включає феніл, нафтил, аценафтил, тетрагідронафтил, кожен необов'язково заміщений 1, 2 або 3 замісниками, кожен замісник незалежно вибраний із групи: гідрокси, галоген, ціано, нітро, аміно, моно- або діалкіламіно, алкіл, галогеналкіл, алкілокси, галогеналкілокси, карбоксил, алкілоксикарбоніл, алкілкарбоніл, амінокарбоніл, морфолініл та моно- або діалкіламінокарбоніл;
Het означає моноциклічний гетероцикл, вибраний із групи, що включає N-феноксипіперидиніл, піроліл, піразоліл, імідазоліл, фураніл, тієніл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, триазоліл, піридиніл, піримідиніл, піразиніл та піридазиніл; або біциклічний гетероцикл, вибраний із групи, що включає хінолініл, ізохінолініл, 1,2,3,4-тетрагідроізохінолініл, хіноксолініл, індоліл, індазоліл, бензимідазоліл, бензоксазоліл, бензізоксазоліл, бензотіазоліл, бензізотіазоліл, бензофураніл, бензотієніл, 2,3-дигідробензо[1,4]діоксиніл або бензо[1,3]діоксоліл;
атом вуглецю кожного моноциклічного та біциклічного гетероциклу може бути необов'язково заміщений 1, 2 або 3 замісниками, вибраними з групи: галоген, гідрокси, алкіл або алкілокси;
галоген являє собою замісник, вибраний із групи: фтор, хлор, бром та йод, а галогеналкіл являє собою нерозгалужений або розгалужений насичений вуглеводневий радикал, що містить від 1 до 6 атомів вуглецю або циклічний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю, де один або декілька атомів вуглецю заміщені одним або декількома атомами галогену;
за умови, що коли радикал 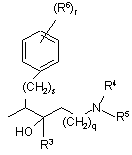 розташований в положенні 3 хінолінового фрагмента; R7 розташований в положенні 4 хінолінового фрагмента, а R2 розташований в положенні 2 хінолінового фрагмента та являє собою водень, гідрокси, меркапто, алкілокси, алкілоксіалкілокси, алкілтіо, моно- або ді(алкіл)аміно або радикал формули
розташований в положенні 3 хінолінового фрагмента; R7 розташований в положенні 4 хінолінового фрагмента, а R2 розташований в положенні 2 хінолінового фрагмента та являє собою водень, гідрокси, меркапто, алкілокси, алкілоксіалкілокси, алкілтіо, моно- або ді(алкіл)аміно або радикал формули 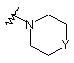 , де Y являє собою СН2, О, S, NH або N-алкіл;
, де Y являє собою СН2, О, S, NH або N-алкіл;
тоді s означає 1, 2, 3 або 4.
2. Сполука за п. 1, де
R2 являє собою водень; галоген; алкіл; гідрокси; меркапто; алкілокси, необов'язково заміщений аміно або моно- або ді(алкіл)аміно, або радикалом формули 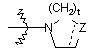 , де Z являє собою СН2, CH-R8, О, S, N-R8, a t означає ціле число, рівне 1 або 2, а пунктирна лінія означає необов'язковий зв'язок: алкілоксіалкілокси; алкілтіо; моно- або ді(алкіл)аміно, де алкіл може бути необов'язково заміщений одним або двома замісниками, кожен незалежно вибраний з алкілокси або Аr, або Het, або морфолінілу, або 2-оксопіролідинілу; Het або радикал формули
, де Z являє собою СН2, CH-R8, О, S, N-R8, a t означає ціле число, рівне 1 або 2, а пунктирна лінія означає необов'язковий зв'язок: алкілоксіалкілокси; алкілтіо; моно- або ді(алкіл)аміно, де алкіл може бути необов'язково заміщений одним або двома замісниками, кожен незалежно вибраний з алкілокси або Аr, або Het, або морфолінілу, або 2-оксопіролідинілу; Het або радикал формули 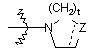 , де Z являє собою CH2, CH-R8, О, S, N-R8; t означає ціле число, рівне 1 або 2; а пунктирна лінія означає необов'язковий зв'язок;
, де Z являє собою CH2, CH-R8, О, S, N-R8; t означає ціле число, рівне 1 або 2; а пунктирна лінія означає необов'язковий зв'язок;
R4 та R5, кожен, незалежно являють собою водень, алкіл або бензил;
або R4 та R5, разом та включаючи N, до якого вони приєднані, можуть утворювати радикал, вибраний із групи, що включає піролідиніл, 2Н-піроліл, 2-піролініл, 3-піролініл, піроліл, імідазолідиніл, піразолідиніл, 2-імідазолініл, 2-піразолініл, імідазоліл, піразоліл, триазоліл, піперидиніл, піридиніл, піперазиніл, імідазолідиніл, піридазиніл, піримідиніл, піразиніл, триазиніл, морфолініл та тіоморфолініл, необов'язково заміщені алкілом, галогеном, галогеналкілом, гідрокси, алкілокси, аміном, моно- або діалкіламіном, алкілтіо, алкілоксіалкілом, алкілтіоалкілом та піримідинілом;
R8 являє собою водень, алкіл, амінокарбоніл, моно- або ді(алкіл)аміно карбоніл, Аr, Het, алкіл, заміщений одним або двома Het, алкіл, заміщений одним або двома Аr, Het-C(=O)-; Het означає моноциклічний гетероцикл, вибраний із групи, що включає N-феноксипіперидиніл, піроліл, піразоліл, імідазоліл, фураніл, тієніл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, триазоліл, піридиніл, піримідиніл, піразиніл та піридазиніл; або біциклічний гетероцикл, вибраний із групи, що включає хінолініл, хіноксалініл, індоліл, індазоліл, бензимідазоліл, бензоксазоліл, бензізоксазоліл, бензотіазоліл, бензізотіазоліл, бензофураніл, бензотієніл, 2,3-дигідробензо[1,4]діоксиніл або бензо[1,3]діоксоліл; атом вуглецю кожного моноциклічного та біциклічного гетероциклу може бути необов'язково заміщений 1, 2 або 3 замісниками, вибраними з групи: галоген, гідрокси, алкіл або алкілокси;
3. Сполука за пп. 1 або 2, за умови, що коли радикал
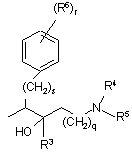 розташований в положенні 3 хінолінового фрагмента; R7 розташований в положенні 4 хінолінового фрагмента, a R2 розташований в положенні 2 хінолінового фрагмента, тоді s означає 1, 2, 3 або 4.
розташований в положенні 3 хінолінового фрагмента; R7 розташований в положенні 4 хінолінового фрагмента, a R2 розташований в положенні 2 хінолінового фрагмента, тоді s означає 1, 2, 3 або 4.
4. Сполука за будь-яким з попередніх пунктів, де сполука являє собою сполуку формули (I-а)
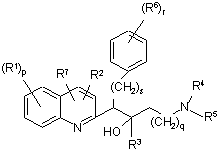 (I-а),
(I-а),
де R1-R7, p, s, r та q є такими, як визначено в будь-якому з пп. 1-3.
5. Сполука за будь-яким з пп. 1-3, де сполука являє собою сполуку формули (І-b)
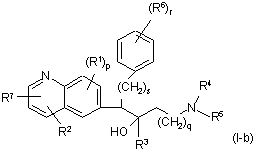 ,
,
де R1-R7, p, s, r та q є такими, як визначено в будь-якому з пп. 1-3.
6. Сполука за будь-яким з пп. 1-3, де сполука являє собою сполуку формули (I-c)
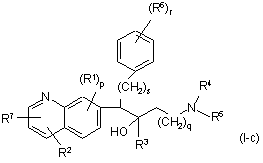 ,
,
де R1-R7, p, s, r та q є такими, як визначено в будь-якому з пп. 1-3.
7. Сполука за будь-яким з попередніх пунктів, де R1 являє собою галоген.
8. Сполука за будь-яким з попередніх пунктів, де р дорівнює 1.
9. Сполука за будь-яким з попередніх пунктів, де R2 являє собою водень, галоген або С1-6-алкіл.
10. Сполука за будь-яким з попередніх пунктів, де R3 являє собою нафтил або феніл, причому кожен необов'язково заміщений 1 або 2 замісниками, переважно такий замісник являє собою галоген.
11. Сполука за будь-яким з попередніх пунктів, де q означає число, рівне 1.
12. Сполука за будь-яким з попередніх пунктів, де R4 та R5, кожен, незалежно являє собою водень або С1-6-алкіл.
13. Сполука за будь-яким з попередніх пунктів, де R6 являє собою водень, алкіл або галоген.
14. Сполука за будь-яким з попередніх пунктів, де R7 являє собою водень або Аr.
15. Сполука за будь-яким з попередніх пунктів, де s означає ціле число, рівне 0 або 1.
16. Сполука за будь-яким з попередніх пунктів для застосування як лікарського засобу.
17. Композиція, що містить фармацевтично прийнятний носій та як активний інгредієнт терапевтично ефективну кількість сполуки, яку визначено в будь-якому з пп. 1-15.
18. Застосування сполуки за будь-яким з пп. 1-15 або композиції за п. 17 для виробництва лікарського засобу для лікування мікобактеріальних захворювань.
19. Спосіб одержання сполуки за п. 1, який відрізняється тим, що проміжну сполуку формули (II) піддають взаємодії з проміжною сполукою формули (III), в присутності придатного агента сполучення та в присутності придатного розчинника та, необов'язково, в присутності придатної основи
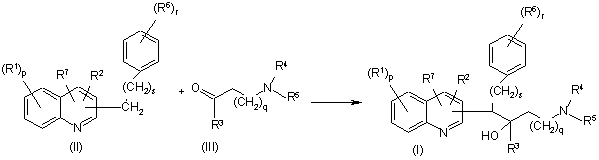 ,
,
де R1-R7, р, s, r та q є такими, як визначено в п. 1;
або, при бажанні, сполуки формули (Іа) або (Іb) переводять одна в одну шляхом відомих у даній галузі реакцій перетворень та потім, при бажанні, переводять сполуки формули (Іа) або (Іb) у терапевтично активну нетоксичну кислотно-адитивну сіль шляхом обробки кислотою або в терапевтично активну нетоксичну основно-адитивну сіль шляхом обробки основою, або навпаки, переводять кислотно-адитивну сольову форму в вільну основу шляхом обробки лугом, або переводять основно-адитивну сіль у вільну кислоту шляхом обробки кислотою, та, при бажанні, одержують їх стереохімічнo ізомерні форми, четвертинні аміни, таутомерні форми або N-оксидні форми.
Текст
1. Сполука формули (І) (19) 1 3 83875 тить від 1 до 6 атомів вуглецю; або являє собою циклічний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю; або являє собою циклічний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю, приєднаний до нерозгалуженого або розгалуженого насиченого вуглеводневого радикала, що містить від 1 до 6 атомів вуглецю; де кожен атом вуглецю може бути необов'язково заміщений галогеном, гідрокси, алкілокси або оксо; Аr означає гомоцикл, вибраний з групи, що включає феніл, нафтил, аценафтил, тетрагідронафтил, кожен необов'язково заміщений 1, 2 або 3 замісниками, кожен замісник незалежно вибраний із групи: гідрокси, галоген, ціано, нітро, аміно, моно- або діалкіламіно, алкіл, галогеналкіл, алкілокси, галогеналкілокси, карбоксил, алкілоксикарбоніл, алкілкарбоніл, амінокарбоніл, морфолініл та моно- або діалкіламінокарбоніл; Het означає моноциклічний гетероцикл, вибраний із групи, що включає N-феноксипіперидиніл, піроліл, піразоліл, імідазоліл, фураніл, тієніл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, триазоліл, піридиніл, піримідиніл, піразиніл та піридазиніл; або біциклічний гетероцикл, вибраний із групи, що включає хінолініл, ізохінолініл, 1,2,3,4тетрагідроізохінолініл, хіноксолініл, індоліл, індазоліл, бензимідазоліл, бензоксазоліл, бензізоксазоліл, бензотіазоліл, бензізотіазоліл, бензофураніл, бензотієніл, 2,3-дигідробензо[1,4]діоксиніл або бензо[1,3]діоксоліл; атом вуглецю кожного моноциклічного та біциклічного гетероциклу може бути необов'язково заміщений 1, 2 або 3 замісниками, вибраними з групи: галоген, гідрокси, алкіл або алкілокси; галоген являє собою замісник, вибраний із групи: фтор, хлор, бром та йод, а галогеналкіл являє собою нерозгалужений або розгалужений насичений вуглеводневий радикал, що містить від 1 до 6 атомів вуглецю або циклічний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю, де один або декілька атомів вуглецю заміщені одним або декількома атомами галогену; (R6)r (CH2) s HO R4 N (CH2)q R5 R за умови, що коли радикал розташований в положенні 3 хінолінового фрагмента; R7 розташований в положенні 4 хінолінового фрагмента, а R2 розташований в положенні 2 хінолінового фрагмента та являє собою водень, гідрокси, меркапто, алкілокси, алкілоксіалкілокси, алкілтіо, моно- або ді(алкіл)аміно або радикал фо3 N Y рмули NH або N-алкіл; , де Y являє собою СН2, О, S, 4 тоді s означає 1, 2, 3 або 4. 2. Сполука за п. 1, де R2 являє собою водень; галоген; алкіл; гідрокси; меркапто; алкілокси, необов'язково заміщений аміно або моно- або ді(алкіл)аміно, або радикалом (CH 2)t N Z формули , де Z являє собою СН2, CH-R8, О, S, N-R 8, a t означає ціле число, рівне 1 або 2, а пунктирна лінія означає необов'язковий зв'язок: алкілоксіалкілокси; алкілтіо; моно- або ді(алкіл)аміно, де алкіл може бути необов'язково заміщений одним або двома замісниками, кожен незалежно вибраний з алкілокси або Аr, або Het, або морфолінілу, або 2-оксопіролідинілу; Het або (CH 2)t N Z радикал формули , де Z являє собою CH2, CH-R8, О, S, N-R 8; t означає ціле число, рівне 1 або 2; а пунктирна лінія означає необов'язковий зв'язок; R4 та R5, кожен, незалежно являють собою водень, алкіл або бензил; або R4 та R5, разом та включаючи N, до якого вони приєднані, можуть утворювати радикал, вибраний із групи, що включає піролідиніл, 2Н-піроліл, 2піролініл, 3-піролініл, піроліл, імідазолідиніл, піразолідиніл, 2-імідазолініл, 2-піразолініл, імідазоліл, піразоліл, триазоліл, піперидиніл, піридиніл, піперазиніл, імідазолідиніл, піридазиніл, піримідиніл, піразиніл, триазиніл, морфолініл та тіоморфолініл, необов'язково заміщені алкілом, галогеном, галогеналкілом, гідрокси, алкілокси, аміном, моно- або діалкіламіном, алкілтіо, алкілоксіалкілом, алкілтіоалкілом та піримідинілом; R8 являє собою водень, алкіл, амінокарбоніл, моно- або ді(алкіл)аміно карбоніл, Аr, Het, алкіл, заміщений одним або двома Het, алкіл, заміщений одним або двома Аr, Het-C(=O)-; Het означає моноциклічний гетероцикл, вибраний із групи, що включає N-феноксипіперидиніл, піроліл, піразоліл, імідазоліл, фураніл, тієніл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, триазоліл, піридиніл, піримідиніл, піразиніл та піридазиніл; або біциклічний гетероцикл, вибраний із групи, що включає хінолініл, хіноксалініл, індоліл, індазоліл, бензимідазоліл, бензоксазоліл, бензізоксазоліл, бензотіазоліл, бензізотіазоліл, бензофураніл, бензотієніл, 2,3дигідробензо[1,4]діоксиніл або бензо[1,3]діоксоліл; атом вуглецю кожного моноциклічного та біциклічного гетероциклу може бути необов'язково заміщений 1, 2 або 3 замісниками, вибраними з групи: галоген, гідрокси, алкіл або алкілокси; 3. Сполука за пп. 1 або 2, за умови, що коли радикал 5 83875 6 (R6) r (R6 )r HO (R1)p R4 (CH2) s N (CH2) q N R5 HO розташований в положенні 3 хінолінового фрагмента; R7 розташований в положенні 4 хінолінового фрагмента, a R2 розташований в положенні 2 хінолінового фрагмента, тоді s означає 1, 2, 3 або 4. 4. Сполука за будь-яким з попередніх пунктів, де сполука являє собою сполуку формули (I-а) R2 R7 R2 N R4 (CH2)s HO N (CH2)q R5 R3 (I-а), де R -R , p, s, r та q є такими, як визначено в будьякому з пп. 1-3. 5. Сполука за будь-яким з пп. 1-3, де сполука являє собою сполуку формули (І-b) 1 7 (R6)r (R1)p N R4 (CH2)s R7 R2 HO N (CH2 )q R5 (I-b) R3 , де R1-R7, p, s, r та q є такими, як визначено в будьякому з пп. 1-3. 6. Сполука за будь-яким з пп. 1-3, де сполука являє собою сполуку формули (I-c) (R6) r (R1 )p R7 R2 + O N (CH2) q CH2 N (II) (I-c) R3 (R6) r R4 (CH2) s R5 , де R1-R7, p, s, r та q є такими, як визначено в будьякому з пп. 1-3. 7. Сполука за будь-яким з попередніх пунктів, де R1 являє собою галоген. 8. Сполука за будь-яким з попередніх пунктів, де р дорівнює 1. 9. Сполука за будь-яким з попередніх пунктів, де R2 являє собою водень, галоген або С1-6-алкіл. 10. Сполука за будь-яким з попередніх пунктів, де R3 являє собою нафтил або феніл, причому кожен необов'язково заміщений 1 або 2 замісниками, переважно такий замісник являє собою галоген. 11. Сполука за будь-яким з попередніх пунктів, де q означає число, рівне 1. 12. Сполука за будь-яким з попередніх пунктів, де R4 та R5, кожен, незалежно являє собою водень або С1-6-алкіл. 13. Сполука за будь-яким з попередніх пунктів, де R6 являє собою водень, алкіл або галоген. 14. Сполука за будь-яким з попередніх пунктів, де R7 являє собою водень або Аr. 15. Сполука за будь-яким з попередніх пунктів, де s означає ціле число, рівне 0 або 1. 16. Сполука за будь-яким з попередніх пунктів для застосування як лікарського засобу. 17. Композиція, що містить фармацевтично прийнятний носій та як активний інгредієнт терапевтично ефективну кількість сполуки, яку визначено в будьякому з пп. 1-15. 18. Застосування сполуки за будь-яким з пп. 1-15 або композиції за п. 17 для виробництва лікарського засобу для лікування мікобактеріальних захворювань. 19. Спосіб одержання сполуки за п. 1, який відрізняється тим, що проміжну сполуку формули (II) піддають взаємодії з проміжною сполукою формули (III), в присутності придатного агента сполучення та в присутності придатного розчинника та, необов'язково, в присутності придатної основи (R6 )r (R1)p N (CH2)q R7 R3 R4 (CH2) s (R1 )p R7 де R1-R7, р, s, r та q є такими, як визначено в п. 1; або, при бажанні, сполуки формули (Іа) або (Іb) переводять одна в одну шляхом відомих у даній галузі реакцій перетворень та потім, при бажанні, переводять сполуки формули (Іа) або (Іb) у тера R4 (CH2) s N R3 (III) R2 R5 N (I) HO (CH2 )q R3 R5 , певтично активну нетоксичну кислотно-адитивну сіль шляхом обробки кислотою або в терапевтично активну нетоксичну основно-адитивну сіль шляхом обробки основою, або навпаки, переводять кислотно-адитивну сольову форму в вільну 7 83875 8 основу шляхом обробки лугом, або переводять основно-адитивну сіль у вільну кислоту шляхом обробки кислотою, та, при бажанні, одержують їх стереохімічнo ізомерні форми, четвертинні аміни, таутомерні форми або N-оксидні форми. Даний винахід відноситься до нових заміщених похідних хіноліну, придатних для лікування мікобактеріальних захворювань, зокрема, таких захворювань, які викликані патогенними мікобактеріями, такими як Mycobacterium tuberculosis, M. bovis, Μ. a vium та Μ. marinum. Mycobacterium tuberculosis є збудником туберкульозу (ТБ), важкого та потенційно смертельного інфекційного захворювання, розповсюдженого в усьому світі. За даними Всесвітньої організації охорони здоров'я щорічно туберкульозом занедужують більше 8 мільйонів чоловік та щороку від туберкульозу вмирають 2 мільйони чоловік. За останнє десятиліття захворюваність туберкульозом виросла в усьому світі на 20%, причому особливо важка ситуація спостерігається в країнах з найбільш низьким рівнем життя. Якщо дана тенденція збережеться, захворюваність туберкульозом збільшиться на 41% протягом наступних двадцяти років. Через п'ятдесятьох років після введення ефективної хіміотерапії ТБ залишається після СНІДу в числі лідируючих інфекцій, що викликають смертність серед дорослого населення у світі. Боротьба з епідемією туберкульозу ускладнюється появою лікарсько стійких штамів та виникненням смертельного симбіозу з ВІЛ. У ВІЛ-позитивних пацієнтів, інфікованих туберкульозом, імовірність виникнення активної форми туберкульозу в 30 разів вище, ніж у ВІЛ-негативних пацієнтів, при цьому у світі від туберкульозу вмирає кожна третя людина, що страждає від ВІЛ/СНІД. Існуючі методи лікування туберкульозу включають комбіновану терапію із застосуванням багатьох лікарських засобів. Наприклад, схема лікування, рекомендована Службою суспільної охорони здоров'я США, включає комбіноване введення ізоніазиду, рифампіцину та піразинаміду протягом двох місяців, з наступним введенням тільки ізоніазиду та рифампіцину протягом наступних чотирьох місяців. ВІЛ-інфіковані пацієнти продовжують приймати зазначені лікарські засоби протягом ще семи місяців. При лікуванні пацієнтів, інфікованих лікарсько стійкими штамами М.tuberculosis, комбінована терапія вищевказаними лікарськими засобами доповнюється такими засобами, як етамбутол, стрептоміцин, канаміцин, амікацин, капреоміцин, етіонамід, циклосерин, ципрофоксацин та офлоксацин. Не існує такого лікарського засобу, який забезпечував би ефективне клінічне лікування туберкульозу, або будь-якої комбінації лікарських засобів, що дозволила б скоротити шестимісячний курс лікування. В медицині існує насущна потреба в нових лікарських засобах, що дозволили б поліпшити застосовувані в даний час методи лікування завдяки створенню схем лікування, що полегшують дотримання режиму лікування як хворим, так і лікуючим лікарем. Менш тривалі схеми лікування, що не потребують строгого нагляду, найкраще відпові дають досягненню поставленої мети. Найбільш сприятливий вплив лікування здійснює в перші 2 місяці, протягом інтенсивної або бактерицидної фази, коли пацієнт приймає чотири лікарських засоби; у даний період значно зменшується бактеріальне навантаження, та пацієнти перестають бути заразними. Наступне лікування протягом 4-6 місяців, або так названа фаза стерилізації, необхідна для знищення бацил, що залишилися, та мінімізації імовірності рецидиву. Надзвичайно корисним був б сильнодіючий стерилізуючий лікарський засіб, що дозволило б скоротити курс лікування до 2 місяців або менше. Крім того, необхідні лікарські засоби, що полегшують режим лікування завдяки здійсненню менш строгого нагляду. Зовсім очевидно, що сполука, що дозволила б скоротити тривалість лікування та частоту введення лікарського засобу, була б особливо корисною. Епідемічне поширення туберкульозу ускладнюється усе більш частою появою лікарсько стійких штамів або MDR-ТБ. До чотирьох відсотків усіх випадків захворювання туберкульозом у світі обумовлене MDR-ТБ, тобто штамами, стійкими до найбільш ефективних лікарських засобів, що призначаються під час основного курсу лікування, здійснюваного чотирма лікарськими засобами, а саме до ізоніазиду та рифампіну. При відсутності лікування MDR-ТБ є смертельним захворюванням, при цьому дане захворювання не можна ефективне лікувати стандартними методами, тому лікування проводять "допоміжними" лікарськими засобами протягом періоду часу до 2 років. Такі лікарські засоби часто є токсичними, дорогими та малоефективними. За відсутності ефективного лікування пацієнти, інфіковані MDR-ТБ, залишаються переносниками захворювання, заражаючи інших людей штамами MDR-ТБ. У медицині існує насущна потреба в новому лікарському засобі з новим механізмом дії, що мав би активність проти штамів MDR. Метою даного винаходу є одержання нових сполук, зокрема, заміщених похідних хіноліну, що мають здатність інгібувати ріст мікобактерій та, отже, є корисними при лікуванні мікобактеріальних захворювань, особливо захворювань, викликаних патогенними мікобактеріями, такими як Mycobacterium tuberculosis, M. bovis, Μ. a vium, Μ. smegmatis та Μ. marinum. Заміщені хіноліни описані в [патенті США №5965572] (Сполучені Штати Америки) для лікування інфекцій, стійких до антибіотиків, та в [WO 00/34265] для інгібування росту бактеріальних мікроорганізмів. У [публікації WO 2004/011436] описані похідні хіноліну як антимікобактеріальні засоби. Даний винахід відноситься до нових заміщених похідних хіноліну формули (І) 9 83875 їх фармацевтично прийнятних кислотно- або основно-адитивних солей, їх че твертинних амінів, їх стереохімічно ізомерних форм, їх таутомерних форм та N-оксидних форм, де: R1 являє собою водень, галоген, галогеналкіл, ціано, гідрокси, Ar, Het, алкіл, алкілокси, алкілтіо, алкілоксіалкіл, алкілтіоалкіл, Ar-алкіл або ді(Аr)алкіл; p означає ціле число, рівне 1, 2 або 3; s означає ціле число, рівне нулю, 1, 2, 3 або 4; R2 являє собою водень; галоген; алкіл; гідрокси; меркапто; алкілокси, необов'язково заміщений аміногрупою або моно- або ді(алкіл)аміногрупою, або радикалом формули , де Ζ являє собою СН 2, CH-R8, О, S, N-R 8, a t означає ціле число, рівне 1 або 2, та пунктирна лінія означає необов'язковий зв'язок; алкілоксіалкілокси; алкілтіо; моно- або ді(алкіл)аміно, де алкіл може бути необов'язково заміщений одним або двома замісниками, кожен незалежно вибраний з алкілокси, або Аr, або Het, або морфолінілу, або 2оксопіролідинілу; Ar; Het або радикал формули , де Ζ являє собою СН2, CH-R8, О, S, N-R ; t означає ціле число, рівне 1 або 2; а пунктирна лінія означає необов'язковий зв'язок; R3 являє собою алкіл, Аr, Ar-алкіл, Het або Hetалкіл; q являє собою ціле число, рівне нулю, 1, 2, 3 або 4; R4 та R5, кожен, незалежно являє собою водень, алкіл або бензил; або R4 та R5 разом та включаючи N, до якого вони приєднані, можуть утворювати радикал, вибраний із групи, що включає піролідиніл, 2Н-піроліл, 2піролініл, 3-піролініл, піроліл, імідазолідиніл, піразолідиніл, 2-імідазолініл, 2-піразолініл, імідазоліл, піразоліл, триазоліл, піперидиніл, піридиніл, піперазиніл, імідазолідиніл, піридазиніл, піримідиніл, піразиніл, триазиніл, морфолініл та тіоморфолініл, кожен з зазначених циклів необов'язково заміщений алкілом, галогеном, галогеналкілом, гідрокси, алкілокси, аміном, моно- або діалкіламіном, алкілтіо, алкілоксіалкілом, алкілтіоалкілом та піримідинілом; R6 являє собою водень, галоген, галогеналкіл, гідрокси, Аr, алкіл, алкілокси, алкілтіо, алкілоксіалкіл, алкілтіоалкіл, Ar-алкіл або ді(Аr)алкіл; або два сусідніх радикали R6 разом з фенільним кільцем, до якого вони приєднані, можуть утворювати нафтил; 8 10 r означає ціле число, рівне 1, 2, 3, 4 або 5; та R7 являє собою водень, алкіл. Аr або Het; R8 являє собою водень, алкіл, гідроксил, амінокарбоніл, моно- або ді(алкіл)амінокарбоніл, Ar, Het, алкіл, заміщений одним або двома Het, алкіл, заміщений одним або двома Ar, Het-C(=O)- або АrС(=О)-; алкіл являє собою нерозгалужений або розгалужений насичений вуглеводневий радикал, що містить від 1 до 6 атомів вуглецю; або являє собою циклічний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю; або являє собою циклічний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю, приєднаний до нерозгалуженого або розгалуженого насиченого вуглеводневого радикалу, що містить від 1 до 6 атомів вуглецю; де кожен атом вуглецю може бути необов'язково заміщений галогеном, гідрокси, алкілокси або оксо; Аr означає гомоцикл, вибраний з групи, що включає феніл, нафтил, аценафтил, тетрагідронафтил, кожен необов'язково заміщений 1, 2 або 3 замісниками, кожен замісник незалежно вибраний із групи, що включає гідрокси, галоген, ціано, нітро, аміно, моно- або діалкіламіно, алкіл, галогеналкіл, алкілокси, галогеналкілокси, карбоксил, алкілоксикарбоніл, алкілкарбоніл, амінокарбоніл, морфолініл та моно- або діалкіламінокарбоніл; Het означає моноциклічний гетероцикл, вибраний із групи, що включає N-феноксипіперидиніл, піроліл, піразоліл, імідазоліл, фураніл, тієніл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, триазоліл, піридиніл, піримідиніл, піразиніл та піридазиніл; або біциклічний гетероцикл, вибраний із групи, що включає хінолініл, ізохінолініл, 1,2,3,4тетрагідроізохінолініл, хіноксолініл, індоліл, індазоліл, бензимідазоліл, бензоксазоліл, бензизоксазоліл, бензотіазоліл, бензізотіазоліл, бензофураніл, бензотієніл, 2,3-дигідробензо[1,4]діоксиніл або бензо[1,3]діоксоліл; атом вуглецю кожного моноциклічного та біциклічного гетероциклу може бути необов'язково заміщений 1, 2 або 3 замісниками, вибраними з групи: галоген, гідрокси, алкіл або алкілокси; галоген являє собою замісник, вибраний із групи: фтор, хлор, бром та йод, а галогеналкіл являє собою нерозгалужений або розгалужений насичений вуглеводневий радикал, що містить від 1 до 6 атомів вуглецю або циклічний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю, де один або декілька атомів вуглецю заміщені одним або декількома атомами галогену; за умови, що коли радикал розташований в положенні 3 хінолінового фрагменту, R7 розташований в положенні 4 хінолінового фрагменту, a R2 розташований в положенні 2 хінолінового фрагменту та являє собою водень, гідрокси, меркапто, алкілок 11 си, алкілоксіалкілокси, 83875 алкілтіо, моно або ді(алкіл)аміно або радикал формули , де Υ являє собою СН 2, О, S, NH або N-алкіл; тоді s означає 1, 2, 3 або 4. В рамках даної заявки алкіл являє собою нерозгалужений або розгалужений насичений вуглеводневий радикал, що містить від 1 до 6 атомів вуглецю; або являє собою циклічний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю; або являє собою циклічний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю, приєднаний до нерозгалуженого або розгалуженого насиченого вуглеводневого радикалу, що містить від1 до 6 атомів вуглецю; де кожен атом вуглецю може бути необов'язково заміщений галогеном, гідрокси, алкілокси або оксо. Переважно алкіл являє собою метил, етил або циклогексилметил. Більш переважно алкіл являє собою С 1-6-алкіл, що як група або частина групи включає нерозгалужені та розгалужені насичені вуглеводневі радикали, що містять від 1 до 6 атомів вуглецю, такі як метил, етил, бутил, пентил, гексил, 2-метилбутил та т.п. В рамках даної заявки, Аr являє собою гомоцикл, вибраний з групи, що включає феніл, нафтил, аценафтил, тетрагідронафтил, кожен необов'язково заміщений 1, 2 або 3 замісниками, кожен замісник незалежно вибраний із групи, що включає гідрокси, галоген, ціано, нітро, аміно, моно- або діалкіламіно, алкіл, галогеналкіл, алкілокси, галогеналкілокси, карбоксил, алкілоксикарбоніл, амінокарбоніл, морфолініл та моно- або діалкіламінокарбоніл. Переважно Аr означає нафтил або феніл, кожен необов'язково заміщений 1 або 2 галогеновими замісниками. В рамках даної заявки, Het означає моноциклічний гетероцикл, вибраний із групи, що включає Nфеноксипіперидиніл, піроліл, піразоліл, імідазоліл, фураніл, тієніл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, триазоліл, піридиніл, піримідиніл, піразиніл та піридазиніл; або біциклічний гетероцикл, вибраний із групи, що включає хінолініл, ізохінолініл, 1,2,3,4-тетрагідроізохінолініл, хіноксалініл, індоліл, індазоліл, бензимідазоліл, бензоксазоліл, бензизоксазоліл, бензотіазоліл, бензізотіазоліл, бензофураніл, бензотієніл, 2,3дигідробензо[1,4]діоксиніл або бензо[1,3]діоксоліл; атом вуглецю кожного моноциклічного та біциклічного гетероциклу може бути необов'язково заміщений 1, 2 або 3 замісниками, вибраними з групи: галоген, гідрокси, алкіл або алкілокси. Переважно Het означає тієніл. В рамках даної заявки, галоген являє собою замісник, вибраний із групи: фтор, хлор, бром та йод, а галогеналкіл являє собою нерозгалужений або розгалужений насичений вуглеводневий радикал, що містить від 1 до 6 атомів вуглецю або циклічний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю, де один або декілька атомів вуглецю заміщені одним або декількома атомами галогену. Переважно, галоген являє собою бром, фтор або хлор, та переважно галогеналкіл являє собою трифторметил. 12 В рамках даної заявки, хіноліновий фрагмент нумерують, як зазначено нижче: Радикал , R2, R7 та R1 можуть знаходитися в будь-якому підходящому положенні хінолінового фрагменту. Мається на увазі, що в рамках даної заявки термін "сполуки формули (І)" або будь-яка їх підгрупа також включає їх N-оксидні форми, солі, четвертинні аміни, їх таутомерні форми та стереохімічно ізомерні форми. Особливий інтерес представляють стереохімічно чисті сполуки формули (І). Цікавий варіант здійснення даного винаходу відноситься до сполук формули (І), до їх фармацевтично прийнятних кислотно- або основноадитивних солей, їх стереохімічно ізомерних форм, їх та утомерних та N-оксидних форм, де R1 являє собою водень, галоген, галогеналкіл, ціано, гідрокси, Ar, Het, алкіл, алкілокси, алкілтіо, алкілоксіалкіл, алкілтіоалкіл, Ar-алкіл або ді(Аr)алкіл; p означає ціле число, рівне 1, 2 або 3; s означає ціле число, рівне нулю, 1, 2, 3 або 4; R2 являє собою водень, галоген, алкіл, гідрокси, меркапто, алкілокси, необов'язково заміщений аміно або моно- або ді(алкіл)аміно, або радикалом формули , де Ζ являє собою СН 2, CH-R8, О, S, N-R 8, a t означає ціле число, рівне 1 або 2, а пунктирна лінія означає необов'язковий зв'язок; алкілоксіалкілокси; алкілтіо; моно- або ді(алкіл)аміно, де алкіл може бути необов'язково заміщений одним або двома замісниками, кожен незалежно вибраний з алкілокси, або Аr, або Het, або морфолінілу, або 2-оксопіролідинілу; Het або радикал формули , де Ζ являє собою СН2, CH-R , О, S, N-R8; t означає ціле число, рівне 1 або 2; а пунктирна лінія означає необов'язковий зв'язок; R3 являє собою алкіл, Аr, Ar-алкіл, Het або Hetалкіл; q означає ціле число, рівне нулю, 1, 2, 3 або 4; R4 та R5 кожен, незалежно являє собою водень, алкіл або бензил; або 13 83875 R4 та R5, разом та включаючи N, до якого вони приєднані, можуть утворювати радикал, вибраний із групи, що включає піролідиніл, 2Н-піроліл, 2піролініл, 3-піролініл, піроліл, імідазолідиніл, піразолідиніл, 2-імідазолініл, 2-піразолініл, імідазоліл, піразоліл, триазоліл, піперидиніл, піридиніл, піперазиніл, імідазолідиніл, піридазиніл, піримідиніл, піразиніл, триазиніл, морфолініл та тіоморфолініл, необов'язково заміщений алкілом, галогеном, галогеналкілом, гідрокси, алкілокси, аміно, моно- або діалкіламіно, алкілтіо, алкілоксіалкілом, алкілтіоалкілом та піримідинілом; R6 являє собою водень, галоген, галогеналкіл, гідрокси, Аr, алкіл, алкілокси, алкілтіо, алкілоксіалкіл, алкілтіоалкіл, Ar-алкіл або ді(Аr)алкіл; або два сусідніх радикали R6 можуть разом з фенільним кільцем, до якого вони приєднані, утворювати нафтил; r означає ціле число, рівне 1, 2, 3, 4 або 5; та R7 являє собою водень, алкіл, Аr або Het; R8 являє собою водень, алкіл, амінокарбоніл, моно- або ді(алкіл)амінокарбоніл, Ar, Het, алкіл, заміщений одним або двома Het, алкіл, заміщений одним або двома Аr, Het-C(=O)-; алкіл являє собою нерозгалужений або розгалужений насичений вуглеводневий радикал, що містить від 1 до 6 атомів вуглецю; або являє собою циклічний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю; або являє собою циклічний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю, приєднаний до нерозгалуженого або розгалуженого насиченого вуглеводневого радикалу, що містить від 1 до 6 атомів вуглецю; де кожен атом вуглецю може бути необов'язково заміщений галогеном, гідрокси, алкілокси або оксо; Аr означає гомоцикл, вибраний з групи, що включає феніл, нафтил, аценафтил, тетрагідронафтил, кожен необов'язково заміщений 1, 2 або 3 замісниками, кожен замісник незалежно вибраний із групи: гідрокси, галоген, ціано, нітро, аміно, моно- або діалкіламіно, алкіл, галогеналкіл, алкілокси, галогеналкілокси, карбоксил, алкілоксикарбоніл, алкілкарбоніл, амінокарбоніл, морфолініл та моно- або діалкіламінокарбоніл; Het означає моноциклічний гетероцикл, вибраний із групи, що включає N-феноксипіперидиніл, піроліл, піразоліл, імідазоліл, фураніл, тієніл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, триазоліл, піридиніл, піримідиніл, піразиніл та піридазиніл; або біциклічний гетероцикл, вибраний із групи, що включає хінолініл, хіноксолініл, індоліл, індазоліл, бензимідазоліл, бензоксазоліл, бензизоксазоліл, бензотіазоліл, бензізотіазоліл, бензофураніл, бензотієніл, 2,3-дигідробензо[1,4]діоксиніл або бензо[1,3]діоксоліл; атом вуглецю кожного моноциклічного та біциклічного гетероциклу може бути необов'язково заміщений 1, 2 або 3 замісниками, вибраними з групи: галоген, гідрокси, алкіл або алкілокси; галоген являє собою замісник, вибраний із групи: фтор, хлор, бром та йод, а галогеналкіл являє собою нерозгалужений або розгалужений насичений вуглеводневий радикал, що містить від 1 до 6 атомів вуглецю, або цикліч 14 ний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю, де один або декілька атомів вуглецю заміщені одним або декількома атомами галогену; за умови, що коли радикал розташований в положенні 3 хінолінового фрагменту, R7 розташований в положенні 4 хінолінового фрагменту, а R2 розташований в положенні 2 хінолінового фрагменту та являє собою водень, гідрокси, меркапто, алкілокси, алкілоксіалкілокси, алкілтіо, моно- або ді(алкіл)аміно або радикал формули , де Υ являє собою СН2, О, S, NH або Nалкіл; тоді s означає 1, 2, 3 або 4. Переважно, винахід відноситься до сполук формули (І) або будь-якої їх підгрупи, як описано вище, за умови, що коли радикал розташований в положенні 3 хінолінового фрагменту, R7 розташований в положенні 4 хінолінового фрагменту та R2 розташований в положенні 2 хінолінового фрагменту, тоді s означає 1,2, 3 або 4. Переважно, винахід відноситься до сполук формули (І) або будь-якої їх підгрупи, як описано вище, за умови, що коли радикал розташований в положенні 3 хінолінового фрагменту; тоді s означає 1, 2, 3 або 4. Переважно, винахід відноситься до сполук формули (І) або будь-якої їх підгрупи, як описано 15 83875 вище, за умови, що радикал не розташований в положенні 3 хінолінового фрагменту. Переважно, винахід відноситься до сполук формули (І) або будь-якої їх підгрупи, як описано вище, де сполуки мають наступну формулу їх фармацевтично прийнятних кислотно- або основно-адитивних солей, їх че твертинних амінів, їх стереохімічно ізомерних форм, їх таутомерних форм та Ν-оксидних форм. Переважно, винахід відноситься до сполук формули (І-а-1) або будь-якої їх підгр упи, як описано вище Переважно, винахід відноситься до сполук формули (І-а-1-1) або будь-якої їх підгрупи, як описано вище їх фармацевтично прийнятних кислотно- або основно-адитивних солей, їх че твертинних амінів, їх стереохімічно ізомерних форм, їх таутомерних форм та N-оксидних форм. Переважно, винахід відноситься до сполук формули (І) або будь-якої їх підгрупи, як описано вище, де сполуки мають наступну формулу 16 їх фармацевтично прийнятних кислотно- або основно-адитивних солей, їх че твертинних амінів, їх стереохімічно ізомерних форм, їх таутомерних форм та N-оксидних форм. Переважно, винахід відноситься до сполук формули (І) або будь-якої їх підгрупи, як описано вище, де сполуки мають наступну формулу їх фармацевтично прийнятних кислотно- або основно-адитивних солей, їх че твертинних амінів, їх стереохімічно ізомерних форм, їх таутомерних форм та N-оксидних форм. Переважно, винахід відноситься до сполук формули (І) або будь-якої їх підгрупи, як описано вище, де R1 являє собою водень, галоген, ціано, Ar, Het, алкіл та алкілокси; p означає ціле число, рівне 1, 2, 3 або 4; зокрема 1 або 2; більш конкретно 1; s означає ціле число 0 або 1; R2 являє собою водень, алкіл, гідрокси, алкілокси, необов'язково заміщений аміно або моноабо ді(алкіл)аміно, або радикалом формули , де Ζ являє собою СН2, CH-R10, О, S, N-R10, a t означає ціле число, рівне 1 або 2; а пунктирна лінія означає необов'язковий зв'язок; алкілоксіалкілокси; алкілтіо; моно- або ді(алкіл)аміно; Аr, Het або радикал формули , де Ζ являє собою СН2, CH-R10, О, S, N-R 10; t означає ціле число, рівне 1 або 2; а пунктирна лінія означає необов'язковий зв'язок; зокрема R2 являє собою водень, гідрокси, алкілокси, алкілоксіалкіло кси, алкілтіо або радикал формули , де Υ являє собою О; більш конкретно R2 являє собою водень, галоген або алкіл, ще більш конкретно R 2 являє собою водень або алкіл; R3 являє собою алкіл, Аr, Ar-алкіл або Het; зокрема Аr; 17 83875 q означає ціле число, рівне нулю, 1, 2 або 3; зокрема 1; R4 та R5, кожен, незалежно являє собою водень, алкіл або бензил; або R4 та R5, разом та включаючи N, до якого вони приєднані, можуть утворювати радикал, вибраний із групи, що включає піролідиніл, імідазоліл, триазоліл, піперидиніл, піперазиніл, піразиніл, морфолініл та тіоморфолініл, необов'язково заміщений алкілом та піримідинілом; зокрема R4 та R5 являють собою алкіл; більш конкретно R4 та R5 являють собою C1-6алкіл, переважно метил; R6 являє собою водень, галоген або алкіл; або два сусідніх радикали R6 можуть разом з фенільним кільцем, до якого вони приєднані, утворювати нафтил; r означає ціле число, рівне 1; та R7 являє собою водень або Аr; зокрема водень або феніл; алкіл являє собою нерозгалужений або розгалужений насичений вуглеводневий радикал, що містить від 1 до 6 атомів вуглецю; або являє собою циклічний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю; або являє собою циклічний насичений вуглеводневий радикал, що містить від 3 до 6 атомів вуглецю, приєднаний до нерозгалуженого або розгалуженого насиченого вуглеводневого радикалу, що містить від 1 до 6 атомів вуглецю; де кожен атом вуглецю може бути необов'язково заміщений галогеном або гідрокси; Аr означає гомоцикл, вибраний з групи, що включає феніл, нафтил, аценафтил, тетрагідронафтил, кожен необов'язково заміщений 1, 2 або 3 замісниками, кожен замісник незалежно вибраний із групи, що включає галоген, галогеналкіл, ціано, алкілокси та морфолініл; Het означає моноциклічний гетероцикл, вибраний із групи, що включає N-феноксипіперидиніл, фураніл, тієніл, піридиніл, піримідиніл; або біциклічний гетероцикл, вибраний із групи, що включає бензотієніл, 2,3-дигідробензо[1,4]діоксиніл або бензо[1,3]діоксоліл; атом вуглецю кожного моноциклічного та біциклічного гетероциклу може бути необов'язково заміщений 1, 2 або 3 алкільними замісниками; та галоген являє собою замісник, вибраний із групи: фтор, хлор та бром. Для сполук формули (І) або будь-якої їх підгрупи, як описано вище, переважно R1 являє собою водень, галоген, Ar, Het, алкіл або алкілокси. Більш переважно R1 являє собою водень, галоген, Аr, алкіл або алкілокси; ще більш переважно R1 являє собою галоген. Найбільш переважно, R1 являє собою бром або хлор. Для сполук формули (І) або будь-якої їх підгрупи, як описано вище, переважно, p дорівнює 1 або 2. Більш переважно, p дорівнює 1. Для сполук формули (І) або будь-якої їх підгрупи, як описано вище, переважно R2 являє собою водень; галоген; алкіл; гідрокси; меркапто; алкілокси, необов'язково заміщений аміно або моно- або ді(алкіл)аміно, або радикалом формули 18 , де Ζ являє собою СН2, CH-R8, О, S, N-R , a t означає ціле число, рівне 1 або 2; а пунктирна лінія означає необов'язковий зв'язок; алкілоксіалкілокси; алкілтіо; моно- або ді(алкіл)аміно, де алкіл може бути необов'язково заміщений одним або двома замісниками, кожен незалежно вибраний з алкілокси, або Аr або Het, або морфолінілу або 2-оксопіролідинілу; Het або радикал формули 8 , де Ζ являє собою СН2, CH-R8, О, S, N-R , a t означає ціле число, рівне 1 або 2; а пунктирна лінія означає необов'язковий зв'язок. Крім того, цікавою групою сполук формули (І) або будь-якою їх підгр упою, як описано вище, є такі сполуки, де R2 являє собою водень; алкіл; алкілокси, необов'язково заміщений аміно або моно- або ді(алкіл)аміно, або радикалом формули 8 , де Ζ являє собою СН2, CH-R10, О, S, N-R ; t означає ціле число, рівне 1 або 2; а пунктирна лінія означає необов'язковий зв'язок; моноабо ді(алкіл)аміно, Аr, Het або радикал формули 10 , де Ζ являє собою СН2, CH-R10, О, S, N-R ; t означає ціле число, рівне 1 або 2; а пунктирна лінія означає необов'язковий зв'язок. Більш переважно, R2 являє собою водень, галоген, алкіл, алкілокси або алкілтіо. Ще більш переважно, R2 являє собою водень, галоген або С1-6алкіл (наприклад, етил). Найбільш переважно, R2 являє собою водень або С1-6алкіл (наприклад, етил). 10 Для сполук формули (І) або будь-якої їх підгрупи, як описано вище, переважно R3 являє собою нафтил, феніл або Het, кожен необов'язково заміщений 1 або 2 замісниками, такий замісник переважно являє собою галоген або галогеналкіл, найбільш переважно являє собою галоген. Більш переважно, R3 являє собою необов'язково заміщений нафтил або необов'язково заміщений феніл. Найбільш переважно, R3 являє собою нафтил або необов'язково заміщений феніл (наприклад, 3галогенфеніл або 3,5-дигалогенфеніл). Для сполук формули (І) або будь-якої їх підгрупи, як описано вище, q дорівнює нулю, 1 або 2. Більш переважно, q дорівнює 1. Для сполук формули (І) або будь-якої їх підгрупи, як описано вище, R4 та R5, кожен, незалежно являє собою водень або алкіл, більш переважно водень або С 1-6алкіл, наприклад, метил або етил, найбільш переважно метил. Для сполук формули (І) або будь-якої їх підгрупи, як описано вище, R4 та R5 разом з N, до якого вони приєднані, можуть утворювати радикал, вибраний із групи, що включає імідазоліл, триазоліл, піперидиніл, піперазиніл та тіоморфолініл. необов'язково заміщений алкілом, галогеном, га 19 83875 логеналкілом, гідрокси, алкілокси, алкілтіо, алкілоксіалкілом або алкілтіоалкілом, переважно заміщений алкілом, найбільше переважно заміщений метилом або етилом. Для сполук формули (І) або будь-якої їх підгрупи, як описано вище, R6 являє собою водень, галоген, галогеналкіл, гідрокси, Аr, алкіл, алкілокси, алкілтіо, алкілоксіалкіл, алкілтіоалкіл, Ar-алкіл або ді(Аr)алкіл. Більш переважно R6 являє собою водень, алкіл або галоген. Найбільш переважно R6 являє собою водень. Переважно r означає 1 або 2. Більш переважно r означає 1. Для сполук формули (І) або будь-якої їх підгрупи, як описано вище, переважно R7 являє собою водень, метил або Аr, більш переважно водень або Аr, наприклад, феніл. Для сполук формули (І) або будь-якої їх підгрупи, як описано вище, переважно R8 являє собою водень, алкіл, амінокарбоніл, моно- або ді(алкіл)амінокарбоніл, Аr, Het, алкіл, заміщений одним або двома Het, алкіл, заміщений одним або двома Аr, Het-C(=O)-. Для сполук формули (І) або будь-якої їх підгрупи, як описано вище, переважно s означає ціле число, рівне 0 або 1. Цікавою групою сполук формули (І) або будьякою їх підгрупою, як описано вище, є такі сполуки, в яких R1 являє собою галоген, зокрема бром; p дорівнює 1; s дорівнює 0 або 1; R2 являє собою водень, галоген або алкіл; зокрема водень або алкіл; R3 необов'язково заміщений феніл або необов'язково заміщений нафтил, зокрема 3галогенфеніл, 3,5-дигалогенфеніл або нафтил; R4 та R5 являють собою С 1-6алкіл, конкретно метил. R6 являє собою водень, а r означає 1. R7 являє собою водень або Аr, зокрема водень або феніл. Проміжні сполуки, що представляють інтерес, за даним винаходом являють собою проміжні сполуки формули (II) де R1, R2, R6, R7, p та s є такими, як описано вище, зокрема проміжні сполуки, що представляють інтерес, являють собою проміжні сполуки формули (ll-а) 20 де R1, R2, R6, R7, p та s є такими, як описано вище. Фармацевтично прийнятні кислотно-адитивні солі включають терапевтично активні нетоксичні кислотно-адитивні сольові форми, які здатні утворювати сполуки формули (І) або будь-яка їх підгрупа, як описано вище. Зазначені кислотноадитивні солі можна одержати за допомогою обробки основної форми сполук формули (І) або будь-якої їх підгрупи, як описано вище, відповідними кислотами, наприклад, неорганічними кислотами, наприклад, галогенводневою кислотою, зокрема соляною кислотою, бромистоводневою кислотою, сірчаною кислотою, азотною кислотою та фосфорною кислотою; органічними кислотами, наприклад, оцтовою кислотою, гідроксіоцтовою кислотою, пропановою кислотою, молочною кислотою, піровиноградною кислотою, щавлевою кислотою, малоновою кислотою, бурштиновою кислотою, малеїновою кислотою, фумаровою кислотою, яблучною кислотою, винною кислотою, лимонною кислотою, метансульфоновою кислотою, етансульфоновою кислотою, бензолсульфоновою кислотою, п-толуолсуль фоновою кислотою, цикламовою кислотою, саліциловою кислотою, паміносаліциловою кислотою та памовою кислотою. Сполуки формули (І) або будь-яка їх підгрупа, як описано вище, що містять кислотні протони, також можна перетворити на їх терапевтично активні нетоксичні основно-адитивні сольові форми за допомогою обробки відповідними органічними та неорганічними основами. Відповідні основні сольові форми включають, наприклад, амонієві солі, солі лужних та лужноземельних металів, зокрема солі літію, натрію, калію, магнію та кальцію, солі з органічними основами, наприклад, солі бензатину, Ν-метил-D-глюкаміну, гідраміну, та солі з амінокислотами, наприклад, аргініном та лізином. Навпаки, зазначені кислотно- або основноадитивні сольові форми можна перетворити на вільні форми за допомогою обробки відповідною кислотою або основою. Термін "адитивна сіль", як використовується в даній заявці, також включає сольвати, які здатні утворювати сполуки формули (І) або будь-яка їх підгрупа, як описано вище, а також їх солі. Такими сольватами є, наприклад, гідрати та алкоголяти. Термін "четвертинний амін", як використовується в даній заявці, включає четвертинні амонієві солі, що здатні утворювати сполуки формули (І) або будь-яка їх підгрупа, як описано вище, за допомогою реакції між основним азотом сполуки формули (І) або будь-якої її підгрупи, як описано вище, та відповідним кватернізуючим агентом, таким як, наприклад, необов'язково заміщений алкілгалогенід, арилгалогенід, арилалкілгалогенід, наприклад, метилйодид або бензилйодид. Можуть бути також використані інші реагенти з групами, що легко відходять, такі як алкілтрифторметансульфонати, алкілметансульфонати та алкіл-птолуолсульфонати. Четвертинний амін містить позитивно заряджений атом азоту. Фармацевтично прийнятні протиіони включають хлор, бром, йод, трифторацетат та ацетат. Вибраний протиіон 21 83875 може бути введений за допомогою іонообмінних смол. Термін "стереохімічно ізомерні форми", як використовується в даній заявці, включає всі можливі ізомерні форми, які можуть мати сполуки формули (І) або будь-яка їх підгрупа, як описано вище. Якщо не згадано або не зазначено інше, хімічне позначення сполук включає суміш всіх можливих стереохімічно ізомерних форм, при цьому зазначені суміші містять всі діастереомери та енантіомери основної молекулярної структури. Більш конкретно, стереогенний центр може мати R- або Sконфігурацію; замісники двовалентних циклічних (частково) насичених радикалів можуть мати або цис-, або транс-конфігурацію. Зрозуміло, що стереохімічно ізомерні форми сполук формули (І) або будь-якої їх підгрупи, як описано вище, включені в межі даного винаходу. Відповідно до правил номенклатури CAS, при наявності в молекулі двох стереогенних центрів відомої абсолютної конфігурації, позначення R або S привласнюється (на основі правила послідовності Кана-Інгольда-Прелога) хіральному центру з найменшим номером, що є базовим центром. Конфігурацію другого стереогенного центру позначають, використовуючи відносні позначення [R*.R*] або [R*,S*], де R* завжди є базовим центром, [R*,R*] позначає центри з однакової хіральністю та [R*, S*] позначає центри з різною хіральністю. Наприклад, якщо хіральний центр із найменшим номером в молекулі має S-конфігурацію та др угий центр має R-конфігурацію, стерео позначення повинне бути позначене як S-[R*,S*]. При використанні символів "a" та "b": положення замісника з найвищим пріоритетом у асиметричного атома вуглецю в кільцевій системі з найменшим номером у кільці завжди умовно вважається "a" положенням середньої площини, обумовленою кільцевою системою. Положення замісника з найвищим пріоритетом у іншого асиметричного атома вуглецю в кільцевій системі щодо положення замісника з найвищим пріоритетом у базового атома позначається символом "a", якщо воно знаходиться з тієї ж сторони середньої площини, обумовленою кільцевою системою, або символом "b", якщо воно знаходиться з іншої сторони середньої площини, обумовленою кільцевою системою. Сполуки формули (І) або будь-яка їх підгрупа, як описано вище, та деякі з проміжних сполук постійно мають, щонайменше, один стереогенний центр в своїй структурі, що дозволяє одержати, щонайменше, 2 стереохімічно різні структури. Сполуки формули (І) або будь-яка їх підгрупа, як описано вище, одержані за допомогою описаних нижче способів, можуть бути синтезовані у формі рацемічних сумішей енантіомерів, що можуть бути відділені один від одного наступними методами розділення, відомими в даній галузі техніки. Рацемічні сполуки формули (І) або будь-яка їхня підгрупа, як описано вище, можуть бути перетворені у відповідні діастереомерні сольові форми шляхом взаємодії з підходящою хіральною кислотою. Зазначені діастереомерні сольові форми потім розділяють, наприклад, шляхом селективної або фракційної кристалізації та за допомогою лугу 22 виділяють з них енантіомери. Альтернативний метод розділення енантіомерних форм сполук формули (І) або будь-якої їх підгрупи, як описано вище, включає рідинну хроматографію з використанням хіральної фази. Зазначені чисті стереохімічно ізомерні форми можуть бути також отримані з відповідних чистих стереохімічно ізомерних форм відповідних вихідних речовин, за умови, що реакція відбувається стереоспецифічно Переважно, якщо бажаним є визначений стереоізомер, зазначену сполуку синтезують стереоспецифічними способами одержання. У подібних способах переважно будуть використовуватися енантіомерно чисті ви хідні речовини. Як описано вище, мається на увазі, що таутомерні форми сполук формули (І) або будь-якої їх підгрупи, включають такі сполуки формули (І) або будь-яку їх підгрупу, як описано вище, де, наприклад, єнольна група перетворена на кетогрупу (кето-єнольна таутомерія). Мається на увазі, що N-оксидні форми даних сполук включають сполуки формули (І) або будьяку їх підгрупу, як описано вище, де один або декілька третинних атомів азоту окиснені в так названий N-оксид. Даний винахід відноситься також до похідних сполук (звичайно названих "проліками") фармакологічно активних сполук за даним винаходом, що розщеплюються in vivo з утворенням сполук за даним винаходом. Проліки звичайно (але не завжди) менш ефективні відносно цільового рецептора, ніж сполуки, в які вони перетворюються в результаті розщеплення. Проліки є особливо корисними в тих випадках, коли необхідна сполука має хімічні або фізичні властивості, що утр уднюють її введення або роблять таке введення неефективним. Наприклад, необхідна сполука може бути погано розчинною, може погано проникати через епітелій слизової оболонки або може характеризуватися небажано коротким періодом напіввиведення з плазми. Проліки описані в [публікаціях Stella, V.J. et al., "Prodrugs", Drug Delivery Systems, 1985, pp.112-176, та Drugs, 1985, 29, pp.455-473]. Пролікарські форми фармакологічно активних сполук за винаходом, як правило, є сполуками формули (І) або будь-якою їх підгрупою, як описано вище, їх фармацевтично прийнятними кислотно- або основно-адитивними сольовими формами, їх стереохімічно ізомерними формами, їх таутомерними та N-оксидними формами, що містять етерифіковану або амідовану кислотну групу. Такими етерифікованими кислотними групами є групи формули –COOR x, де R x означає С 1-6алкіл, феніл, бензил або одну з нижченаведених гр уп: Амідованими групами є групи формули CONRyRx, де Ry означає Н, С1-6алкіл, феніл або бензил та Rx означає -ОН, Н, С1-6алкіл, феніл або бензил. Зі сполук за даним винаходом, що містять аміногрупу, можуть бути отримані похідні сполуки з 23 83875 використанням кетону або альдегіду, такого як формальдегід, з утворенням основи Маніха. Дана основа гідролізує у водному розчині відповідно до кінетики першого порядку. Зненацька, було виявлено, що сполуки відповідно до даного винаходу, придатні для лікування мікобактеріальних захворювань, зокрема, мікобактеріальних захворювань, викликаних патогенними мікобактеріями, включаючи лікарсько стійкі та стійкі до дії численних лікарських засобів, такими, як Mycobacterium tuberculosis, Μ. bovis, Μ. a vium, Μ. smegmatis та Μ. marinum. Таким чином, даний винахід відноситься до сполук формули (І) або будьякої їх підгрупи, як описано вище, їх фармацевтично прийнятних кислотно- або основно-адитивних солей, їх стереохімічно ізомерних форм, їх та утомерних форм та N-оксидних форм для застосування як лікарського засобу. Даний винахід відноситься також до композиції, що містить фармацевтично прийнятний носій та терапевтично ефективну кількість сполуки за даним винаходом, як активний інгредієнт. Сполуки за даним винаходом можуть входити до складу різних фармацевтичних форм, призначених для введення. Як підходящі композиції можна привести всі композиції, що звичайно використовуються для системного введення лікарських засобів. Для одержання фармацевтичних композицій за даним винаходом ефективну кількість визначеної сполуки, необов'язково у формі адитивної солі, як активний інгредієнт, ретельно змішують з фармацевтично прийнятним носієм, що може бути використаний в різних формах в залежності від форми, призначеного для введення препарату. Зазначені фармацевтичні композиції бажано використовувати у вигляді стандартної лікарської форми, придатної, зокрема, для перорального введення або у вигляді парентеральної ін'єкції. Наприклад, при одержанні композицій у вигляді лікарської форми для перорального введення можна використовувати будь-які звичайно застосовувані фармацевтичні середовища, такі як, наприклад, вода, гліколі, олії, спирти тощо, у випадку рідких препаратів для перорального введення, таких як суспензії, сиропи, еліксири, емульсії та розчини; або тверді носії, такі як крохмалі, цукри, каолін, розріджувачі, змазуючі речовини, зв'язуючі речовини, розпушуючі агенти, тощо, у випадку порошків, пігулок, капсул та таблеток. Завдяки легкості введення таблетки та капсули є найбільш підходящими стандартними лікарськими формами для перорального введення, при виготовленні яких звичайно використовують тверді фармацевтичні носії. Для парентеральних композицій носій звичайно включає стерильну воду, принаймні, здебільшого, хоча в нього можуть входити інші інгредієнти, наприклад, для поліпшення розчинності. Наприклад, можуть бути отримані ін'єкційні розчини, в яких носієм є фізіологічний розчин, розчин глюкози або суміш фізіологічного розчину та розчину глюкози. Крім того, можуть бути отримані ін'єкційні суспензії, що можуть містити відповідні рідкі носії, суспендуючі агенти тощо. В межі даного винаходу входять також тверді форми препаратів, 24 призначені для перетворення в рідкі форми препаратів незадовго до використання. В залежності від способу введення, фармацевтична композиція переважно містить від 0,05 до 99мас.%, більш переважно від 0,1 до 70мас.% активного інгредієнта формули (І) або будь-якої його підгрупи, як описано вище, та від 1 до 99,95мас.%, більш переважно від 30 до 99,9мас.% фармацевтично прийнятного носія; всі відсотки зазначені з розрахунку на загальну масу композиції. Фармацевтична композиція може додатково містити різні інші інгредієнти, відомі в даній галузі техніки, наприклад, змазуючу речовину, стабілізатор, буфер, емульгатор, речовину, що регулює в'язкість, поверхнево-активну речовину, консервант, ароматизатор або барвник. Вищевказані фармацевтичні композиції особливо бажано використовувати для одержання стандартної лікарської форми, що характеризується легкістю введення та однорідністю дози. Термін "стандартна лікарська форма", як використовується в даній заявці, означає фізично роздільні форми, придатні для застосування як стандартні дози, оскільки кожна форма містить заздалегідь визначену кількість активного інгредієнта, розраховану на досягнення бажаної терапевтичної дії, у сполученні з необхідним фармацевтичним носієм. Прикладами таких стандартних лікарських форм є таблетки (включаючи таблетки з насічкою або з покриттям), капсули, пігулки, пакетики з порошком, облатки, супозиторії, ін'єкційні розчини або суспензії тощо, а також зазначені препарати, розділені на декілька частин. Добова доза сполуки за даним винаходом є різною в залежності від використовуваної сполуки, способу введення, необхідного лікування та конкретного мікобактеріального захворювання. Однак, як правило, задовільні результати досягаються при введенні сполуки за даним винаходом у вигляді добової дози, що не перевищує 1 грам, наприклад, в межах від 10 до 50мг/кг маси тіла. Додатково даний винахід також відноситься до застосування сполуки формули (І) або будь-якої її підгрупи, як описано вище, їх фармацевтично прийнятних кислотно- або основно-адитивних солей, їх стереохімічно ізомерних форм, їх таутомерних форм та N-оксидних форм, а також будь-яких вищевказаних фармацевтичних композицій для виготовлення лікарського засобу для профілактики або лікування мікобактеріальних захворювань. Відповідно, в іншому аспекті, винахід забезпечує спосіб лікування пацієнта, що страждає або піддається ризику виникнення мікобактеріального захворювання, що включає введення зазначеному пацієнту терапевтично ефективної кількості сполуки або фармацевтичної композиції за даним винаходом. Сполуки за даним винаходом можуть бути також об'єднані з одним або декількома іншими антимікобактеріальними засобами. Таким чином, даний винахід також відноситься до комбінації (а) сполуки формули (І) або будь-якої її підгрупи, як описано вище, та (b) одного або декількох інших антимікобактеріальних засобів. 25 83875 26 Даний винахід також відноситься до комбінації (а) сполуки формули (І) або будь-якої її підгрупи, як описано вище, та (b) одного або декількох інших антимікобактеріальних засобів для застосування як лікарського засобу. Також даний винахід відноситься до фармацевтичної композиції, що містить фармацевтично прийнятний носій, та, як активний інгредієнт, терапевтично ефективну кількість (а) сполуки формули (І) або будь-якої її підгрупи, як описано вище, та (b) один або декілька інших антимікобактеріальних засобів. Інші мікобактеріальні засоби, які можна комбінувати зі сполуками формули (І) або будь-якою їх підгрупою, як описано вище, являють собою, наприклад, рифампіцин (=рифампін), ізоніазид, пиразинамід, амікацин, етіонамід, моксифлоксацин, етамбутол, стрептоміцин, пара-аміносаліцилову кислоту, циклосерин, капреоміцин, канаміцин, тіоацетазон, РА-824, хінолони/фторхінолони, такі як, наприклад, офлоксацин, ципрофлоксацин, спарф локсацин, макроліди, такі як, наприклад, кларитроміцин, клофазимін, амоксицилін із клавулановою кислотою, рифаміцини, рифабутин, рифапентин. Переважно дані сполуки формули (І) або будьяку їх підгрупу, як описано вище, комбінують з рифапентином та моксифлоксацином. Сполуки за даним винаходом, як правило, можна одержати за допомогою послідовності стадій, кожна з яких відома фахівцю в даній галузі техніки. Сполуки формули (І) можна одержати за допомогою взаємодії проміжної сполуки формули (II) із проміжною сполукою формули (III) в присутності придатного агента сполучення, такого як, наприклад, н-бутил літію, втор-BuLi, та в присутності придатного розчинника, такого як, наприклад, тетрагідрофуран, та необов'язково в присутності придатної основи, такої як, наприклад, 2,2,6,6тетраметилпіперидин, NH(CH2CH2CH3)2, N,Nдіізопропіламін або триметилетилендіамін. В зазначеній вище реакції отриману сполуку формули (І) можна виділити та, якщо необхідно, очистити за допомогою способів, як правило, відомих в даній галузі, таких як, наприклад, екстракція, кристалізація, перегонка, розтирання в порошок та хроматографія. У випадку, коли сполука формули (І) кристалізується, її можна виділити за допомогою фільтрування. В протилежному випадку, кристалізацію викликають за допомогою додавання відповідного розчинника, такого як, наприклад, вода, ацетонітрил, спирт, такий як, наприклад, метанол, етанол, та комбінації зазначених розчинників. Альтернативно, реакційну суміш можна також випарити насухо, з наступним очищенням залишку хроматографією (наприклад, ВЕРХ з оберненою фазою, флеш-хроматографія тощо). Реакційна суміш може бути також очищена хроматографією без попереднього випарювання розчинника. Сполуку формули (І) також можна виділити за допомогою випарювання розчинника з наступною перекристалізацією у відповідному розчиннику, такому як, наприклад, вода, ацетонітрил, спирт, такий як, наприклад, метанол, та комбінації зазначених розчинників. Фахівцю в даній галузі повинно бути відомо, який спосіб варто використовува ти, який розчинник є найбільш підходящим, або необхідно вдатися до звичайного експериментування для визначення найбільш підходящого методу виділення. Сполуки формули (І) можуть бути також отримані шляхом перетворення сполук формули (І) одна в одну за допомогою відомих у даній галузі реакцій перетворення груп. Сполуки формули (І) можуть бути перетворені у відповідні N-оксиди за допомогою відомих у даній галузі методів перетворення тривалентного азоту на його N-оксид. Зазначену реакцію Nокиснення можна виконати, здійснюючи взаємодію вихідної сполуки формули (І) з відповідним органічним або неорганічним пероксидом. Відповідні неорганічні пероксиди включають, наприклад, пероксид водню, пероксиди лужних металів або лужноземельних металів, наприклад, пероксид натрію, пероксид калію; відповідні органічні пероксиди можуть включати пероксикислоти, такі як надбензойна кислота або галогензаміщена надбензойна кислота, наприклад, 3-хлорнадбензойна кислота, пероксоалканові кислоти, наприклад, пероксооцтова кислота, алкілгідропероксиди, наприклад, гідропероксид трет-бутилу. Підходя щими розчинниками є, наприклад, вода, нижчі спирти, такі як етанол тощо, вуглеводні, наприклад, толуол, кетони, наприклад, 2-бутанон, галогеновані вуглеводні, наприклад, дихлорметан, та суміші таких розчинників. Сполуки формули (І), де R1 являє собою галоген, можуть бути перетворені на сполуку формули (І), де R1 являє собою Het, наприклад, піридил, за допомогою реакції з в присутності придатного каталізатора, такого як, наприклад, Рd(РРh3)4, придатного розчинника, такого як, наприклад, диметиловий ефір або спирт, наприклад, 27 83875 28 метанол та т.п., та придатної основи, такої як, наприклад, карбонат динатрію або карбонат дикалію. Сполуки формули (І), де R1 являє собою галоген, також можуть бути перетворені на сполуку формули (І), де R1 являє собою метил, за допомогою реакції з Sn(CH3)4 в присутності придатного каталізатора, такого як, наприклад. Pd(PPh3)4, придатного розчинника, такого як, наприклад, толуол. Деякі зі сполук формули (І) та деякі з проміжних сполук за даним винаходом можуть являти собою суміш стереохімічно ізомерних форм. Чисті стереохімічно ізомерні форми зазначених сполук та зазначених проміжних сполук можуть бути отримані методами, відомими в даній галузі. Наприклад, діастереоізомери можуть бути розділені фізичними методами, такими як селективна кристалізація, або хроматографічними методами, такими як протиточній розподіл, рідинна хроматографія тощо. Енантіомери можуть бути отримані з рацемічних сумішей спочатку шляхом перетворення зазначених рацемічних сумішей з використанням підходящих розчинників, таких як, наприклад, хіральні кислоти, у суміші діастереомерних солей або сполук; фізичного розділення зазначених сумішей діастереомерних солей або сполук, наприклад, селективною кристалізацією або хроматографічними методами, зокрема, рідинною хроматографією, та подібними методами; та наступного перетворення зазначених розділених діастереомерних солей або сполук на відповідні енантіомери. Чисті стереохімічно ізомерні форми можуть бути також отримані з чистих стереохімічно ізомерних форм відповідних проміжних сполук та вихідних речовин, за умови, що проміжні реакції відбуваються стереоспецифічно. Альтернативний спосіб розділення енантіомерних форм сполук формули (І) та проміжних сполук включає рідинну хроматографію, зокрема рідинну хроматографію із застосуванням хіральної нерухомої фази. Необхідно розуміти, що в приведених вище або наступних одержаннях, продукти реакції можуть бути виділені з реакційного середовища та, при необхідності, очищені далі за допомогою загальновідомих у даній галузі те хніки методів, наприклад, таких, як екстракція, кристалізація, перегонка, розтирання в порошок та хроматографія. Деякі проміжні сполуки та вихідні речовини є відомими сполуками та можуть бути комерційно доступними або можуть бути отримані методами, відомими в даній галузі. Проміжні сполуки формули (II), де радикал Проміжні сполуки формули (IV), де R2 та R7 являють собою водень, зазначені проміжні сполуки представлені формулою (IV-a), можуть бути одержані за допомогою проведення реакції промі жної сполуки формули (V) із проміжною сполукою формули (VI) в присутності придатної основи, такої як, наприклад, гідроксид натрію. розташований в положенні 2 хінолінового кільця, s означає ціле число, рівне 1, а положення 4 хінолінового кільця є незаміщеним, зазначені проміжні сполуки представлені формулою (ІІа), можуть бути одержані за допомогою проведення реакції проміжної сполуки формули (IV) з фенілоксибензолом в присутності етилацетату. 29 83875 Проміжні сполуки формули (II), де радикал розташований в положенні 2 хінолінового кільця, та s дорівнює 0, зазначені проміжні сполуки представлені формулою (ΙΙ-b), можуть бути одержані за допомогою проведення реакції 30 проміжної сполуки формули (VII), де W1 являє собою придатну гр уп у, що відходить, таку як, наприклад, галоген, наприклад, хлор та т.п., із проміжною сполукою формули (VIII), де W2 являє собою придатну групу, що відходить, таку як, наприклад, галоген, наприклад, хлор, бром та т.п., в присутності Zn, хлортриметилсилану, 1,2-диброметану та Pd(PPh3)4, та придатного розчиннику, такого як, наприклад, тетрагідрофуран. Проміжні сполуки формули (VII), де W1 являє собою хлор, зазначені проміжні сполуки представлені формулою (VII-a), можуть бути одержані за допомогою проведення реакції проміжної сполуки формули (IX) з РОСІ 3. Проміжні сполуки формули (IX) можуть бути одержані за допомогою проведення реакції проміжної сполуки формули (X) з 4метилбензолсульфонілхлоридом в присутності придатного розчинника, такого як, наприклад, метиленхлорид, та придатної основи, такої як, наприклад, карбонат калію. Проміжні сполуки формули (X) можуть бути одержані за допомогою проведення реакції проміжної сполуки формули (XI) із придатним окисни ком, таким як, наприклад, 3-хлорнадбензойна кислота, в присутності придатного розчинника, такого як, наприклад, метиленхлорид. 31 83875 32 Проміжні сполуки формули (II), де s дорівнює 0, зазначені проміжні сполуки представлені формулою (ll-с), можуть бути одержані за допомогою проведення реакції проміжної сполуки формули (XII) з Et3SiH в присутності придатної кислоти, такої як, наприклад, трифтороцтова кислота, та придатного розчинника, такого як,наприклад, метиленхлорид. Проміжні сполуки формули (XII) можуть бути одержані за допомогою проведення реакції проміжної сполуки формули (XIII), де W3 являє собою придатну груп у, що відходить, таку як галоген, наприклад, хлор або бром та т.п. із проміжною сполукою формули (XIV) в присутності придатного агента сполучення, такого як, наприклад, н-бутил літію, втор-BuLi, та в присутності придатного розчинника, такого як, наприклад, тетрагідрофуран, та необов'язково в присутності придатної основи, такої як, наприклад, 2,2,6,6-тетраметилпіперидин, NH(CH2CH2CH3)2, Ν,Ν-діізопропіламін або триметилетилендіамін. Проміжні сполуки формули (XII), де радикал розташований в положенні 8 хінолінового кільця, R2 розташований в положенні 2, R7 розташований в положенні 4 та R1 розташований в положенні 6 хінолінового кільця, зазначені проміжні сполуки представлені формулою (Хll-а), можуть бути одержані за допомогою проведення реакції проміжної сполуки формули (XV) із проміжною сполукою фо рмули (XIV) в присутності придатного агента сполучення, такого як, наприклад, н-бутил літію, вторBuLi, та в присутності придатного розчинника, такого як, наприклад, тетрагідрофуран, та необов'язково в присутності придатної основи, такої як, наприклад, 2,2,6,6-тетраметилпіперидин, NН(СН2СН2СН3)2, N,N-діізопропіламін або триметилетилендіамін. Проміжні сполуки формули (III) являють собою сполуки, що є комерційно доступними, або можуть бути отримані відповідно до стандартних методик реакцій, як правило, відомих в даній галузі. Напри клад, проміжні сполуки формули (III), де q дорівнює 1, зазначені проміжні сполуки, представлені формулою (lll-а), можуть бути отримані відповідно до наступної схеми реакцій (1): 33 83875 34 Схема реакцій (1) включає стадію (а), на якій відповідний R3 взаємодіє за допомогою реакції Фріделя-Крафтса з відповідним хлорангідридом, таким як 3-хлорпропіонілхлорид або 4хлорбутирилхлорид, в присутності придатної кислоти Льюїса, такої як АlСl3, FeCl3, SnCl 4, ТіСl4 або ZnCl2, та придатного реакційно-інертного розчиннику, такого як метиленхлорид або етилендихлорид. Відповідно реакцію можна проводити при температурі в діапазоні від кімнатної температури до температури кипіння зі зворотним холодильником. На наступній стадії (b) аміногрупу (наприклад, NR4R5) вводять за допомогою взаємодії проміжної сполуки, отриманої на стадії (а), з відповідним аміном. Проміжні сполуки формули (III) також можуть бути одержані за допомогою проведення реакції проміжної сполуки формули (XVI) та проміжної сполуки формули (XVII) з формальдегідом в присутності придатного розчинника, такого як, наприклад, спирт, наприклад, етанол, та придатної кислоти, наприклад, НСl. Очевидно, що в згаданих ви ще та в наступних реакціях продукти реакції можна виділити з реакційного середовища та, при необхідності, очистити далі відповідно до методів, загальновідомих в даній галузі, наприклад, такими як екстракція, кристалізація та хроматографія. Крім того, мабуть, що продукти реакції, що існують більш, ніж в одній енантіомерній формі, можна виділити з їх суміші відомими методами, зокрема, препаративною хроматографією, такою, як ВЕРХ. Як правило, сполуки формули (І) можна розділити на їх ізомерні форми. Нижченаведені приклади ілюструють даний винахід, не обмежуючи його обсяг. Для деяких сполук абсолютну конфігурацію стереогенного атома(атомів) вуглецю експеримен тально не визначали. В цих випадках стереохімічно ізомерну форму, виділену першою, позначали «А», а другу «В», без додаткового посилання на конкретну стереохімічну конфігурацію. Однак фахівець у даній галузі може однозначно охарактеризувати зазначені ізомерні форми «А» та «В» за допомогою відомих у даній галузі методів, наприклад, таких, як дифракція рентгенівських променів. Спосіб виділення докладно описаний нижче. Для деяких кінцевих сполук стереохімічні конфігурації зазначені в структурах. Дані конфігурації є відносними конфігураціями, що вказують, що розглянуті групи розташовані в одній і тій же або в протилежних площинах молекули Далі "DIPE" означає діізопропіловий ефір, "ТГФ" означає тетрагідрофуран, "НОАс" означає оцтову кислоту, "EtOAc" означає етилацетат. А. Одержання проміжних сполук Приклад A1 Одержання проміжної сполуки 1 та проміжної сполуки 2 Суміш 5-бром-1Н-індол-2,3-діону (0,221моль) в 3N NaOH (500мл) перемішували при 80°С протягом 30 хвилин та потім охолоджували до кімнатної 35 83875 температури. Додавали 4-феніл-2-бутанон (0,221моль). Суміш перемішували та кип'ятили зі зворотним холодильником протягом 90 хвилин, охолоджували до кімнатної температури та підкисляли HOAc до рН=5. Осад відфільтровували, промивали Н2О та сушили. Ви хід: 75г (95%) суміші проміжної сполуки 1 та проміжної сполуки 2. Приклад А2 Одержання проміжної сполуки 3 Суміш проміжної сполуки 1 та проміжної сполуки 2 (0,21моль) в 1,1`-оксибіс[бензолі] (600мл) перемішували при 30°С протягом 12 годин. Додавали EtOAc. С уміш екстрагували три рази 6N НСl, підлужували твердим К2СО3 та екстрагували СН2Сl2. Органічний шар відокремлювали, сушили (MgSO4), фільтрували та випарювали розчинник. Осад (36г) очищали за допомогою колоночної хроматографії на силікагелі (елюент: СН2Сl2/СН3ОН 99/1; 15-40мкм). Чисті фракції збирали та випарювали розчинник. Вихід: 11г (16%) проміжної сполуки 3. Приклад A3 Одержання проміжної сполуки 4 Суміш 1-(3-фторфеніл)етанону (0,195моль), формальдегіду (0,235моль) та NH(CH3)2×HCl (0,235моль) в етанолі (300мл) та концентрованої НСl (1мл) перемішували та кип'ятили зі зворотним холодильником протягом ночі, потім доводили до кімнатної температури. Осад фільтрували, промивали етанолом та сушили. Матковий шар випарювали. Осад поміщали в діетиловий ефір. Осад фільтрували, промивали діетиловим ефіром та сушили. Цю фракцію поміщали в К2СО3 10%. Осад промивали СН 2Сl2 та сушили. Ви хід: 18,84г (49%) проміжної сполуки 4. Приклад A4 a. Одержання проміжної сполуки 5 Суміш 6-бром-2-(1Н)-хінолінону (0,089моль) в РОСl3 (55мл) перемішували при 60°С протягом ночі, потім при 100°С протягом 3 годин, та випарювали розчинник. Осад поміщали в СН2Сl2, виливали в крижану воду, підлужували концентрованим NH4OH, фільтрували через целіт та екстрагували СН 2Сl2. Органічний шар відокремлювали, сушили (MgSO 4), фільтрували та розчинник випарювали. Вихід: 14,5г проміжної сполуки 5 (67%). b. Одержання проміжної сполуки 6 36 Суміш Zn (0,029моль) та 1,2-диброметану (0,001моль) в ТГФ (6мл) перемішували та кип'ятили зі зворотним холодильником протягом 10 хвилин, потім охолоджували до кімнатної температури. Додавали хлортриметилсилан (0,001моль). Суміш перемішували при кімнатній температурі протягом 30 хвилин. Додавали по краплям розчин бромметилбензолу (0,025моль) в ТГФ (25мл) при 5°С протягом 90 хвилин. Суміш перемішували при 0°С протягом 2 годин. Додавали розчин проміжної сполуки 5 (отриманої відповідно до A4.а) (0,021моль) в ТГФ (75мл). Додавали Pd(PPh3)4 (0,0008моль). Суміш перемішували та кип'ятили зі зворотним холодильником протягом 2 годин, потім охолоджували до кімнатної температури, виливали в NH4Cl 10% та екстрагували EtOAc. Органічний шар промивали Н 2О, потім насиченим NaCl, сушили (MgSO 4), фільтрували та випарювали розчинник. Осад (12г) очищали за допомогою колоночної хроматографії на силікагелі (елюент: циклогексан/СН 2Сl2 50/50; 20-45мкм). Збирали дві фракції та випарювали розчинник. Вихід другої фракції: 2,5г проміжної сполуки 6. Приклад А5 a. Одержання проміжної сполуки 7 При -50°С до суміші 6-бром-2-хлор-3етилхіноліну (0,055моль) в ТГФ (150мл) додавали по краплям н-BuLi (1,6М) (0,066моль). Суміш перемішували при -50°С протягом 1 години. Додавали розчин бензальдегіду (0,066моль) в ТГФ (70мл) при -70°С. Суміш перемішували при -70°С протягом 1 години, виливали в Н2О при 0°С та екстрагували EtOAc. Органічний шар відокремлювали, сушили (MgSO4), фільтрували та випарювали розчинник. Осад (15г) кристалізували з DIPE/iPrOH. Осад відфільтровували та сушили. Вихід: 7,6г проміжної сполуки 7 (46%). b. Одержання проміжної сполуки 8 Суміш проміжної сполуки 7 (отриманої відповідно до А5.а) (0,021моль), Et3SiH (0,21моль) та CF3COOH (0,21моль) в СН2Сl2 (100мл) перемішували при кімнатній температурі протягом 3 діб. Додавали Н2О. Суміш екстрагували СН 2Сl2. Органічний шар відокремлювали, промивали К2СО3 10%, сушили сульфатом магнію, фільтрували та випарювали розчинник. Осад (8г) очищали за допомогою колоночної хроматографії на силікагелі (елюент: циклогексан/AcOEt 95/5; 15-40мкм). Чисті фракції збирали та випарювали розчинник. Вихід: 3,8г (64%, т.п.: 66°С). Приклад А6 37 83875 а. Одержання проміжної сполуки 9 До суміші 7-бром-2-хлор-3-етилхіноліну (0,037моль) в ТГФ (100мл) повільно додавали нбутил лі тію (0,055моль) при -70°С в потоці N2. Суміш перемішували протягом 2 годин, потім додавали розчин бензальдегіду (0,055моль) в ТГФ (55мл). Суміш перемішували протягом 3 годин, додавали воду при -20°С та екстрагували суміш EtOAc. Органічний шар відокремлювали, сушили сульфатом магнію, фільтрували та випарювали розчинник. Осад (12,2г) очищали за допомогою колоночної хроматографії на силікагелі (елюент: циклогексан/AcOEt 80/20; 15-40мкм). Чисті фракції збирали та випарювали розчинник. Вихід: 6,1г проміжної сполуки 9 (56%). b. Одержання проміжної сполуки 10 Суміш проміжної сполуки 9 (отриманої відповідно до А6.а) (0,0205моль), Et3SiH (0,205моль) та CF3COOH (0,205моль) в СН2Сl2 (300мл) перемішували при кімнатній температурі протягом 7 діб. Додавали Н2О. Суміш екстрагували СН 2Сl2. Органічний шар відокремлювали, промивали К2СО3 10%, сушили над сульфатом магнію, фільтрували та випарювали розчинник. Осад (7,1г) очищали за допомогою колоночної хроматографії на силікагелі (елюент: циклогексан/AcOEt 95/5; 15-40мкм). Чисті фракції збирали та випарювали розчинник. Вихід: 4,8г проміжної сполуки 10 (83%). Приклад А7 а. Одержання проміжної сполуки 11 До суміші 2,2,6,6-тетраметилпіперидину (0,0090моль) в ТГФ (15мл) повільно додавали нбутил літій (0,0090моль) при -20°С в потоці N 2. Суміш перемішували протягом 20 хвилин, потім охолоджували до -70°С. Додавали розчин 6-бром2-хлор-4-фенілхіноліну (0,0060моль) в ТГФ (40мл). Суміш перемішували протягом 1 години. Додавали розчин бензальдегіду (0,0090моль) в ТГФ (15мл). Суміш перемішували протягом 1 години при -70°С, потім 3 години при кімнатній температурі. Додавали Н2О. Суміш екстрагували EtOAc. Органічний шар відокремлювали, сушили сульфа том магнію, фільтрували та випарювали розчинник. Осад (3,0г) очищали за допомогою колоночної хроматографії на силікагелі (елюент: циклогек 38 сан/АсОЕt: 95/5; 15-40мкм). Чисті фракції збирали та випарювали розчинник. Вихід: 1,8г проміжної сполуки 11 (71%). b. Одержання проміжної сполуки 12 Суміш проміжної сполуки 11 (отриманої відповідно до А7.а) (0,0042моль), Et3SiH (0,0424моль) та CF3COOH (0,0424моль) в СН2Сl2 (100мл) перемішували при кімнатній температурі протягом 24 годин. Додавали Н2О. Суміш екстрагували СН 2Сl2. Органічний шар відокремлювали, промивали К2СО3 10%, сушили сульфа том магнію, фільтрували та випарювали розчинник. Осад (1,3г) кристалізували з DIPE. Осад відфільтровували та сушили. Вихід: 0,66г (38%, т.п.: 121°С). В. Одержання кінцевих сполук Приклад В1 Одержання сполуки 1 та сполуки 4 До суміші N-(1-метилетил)-2пропанаміну:гідрохлориду (1:1) (0,0071моль) в ТГФ (25мл) додавали н-BuLi 1,6Μ (0,0072моль) при 20°С в потоці азоту. С уміш перемішували протягом 20 хвилин, потім охолоджували до -70°С. Додавали розчин проміжної сполуки 3 (0,0061моль) в ТГФ (5мл). Суміш перемішували протягом 2 годин. Додавали розчин проміжної сполуки 4 (0,0061моль) в ТГФ (5мл) при -70°С. Суміш перемішували при -70°С протягом 3 годин. Додавали NH4Cl 10%. Суміш екстрагували EtOAc. Органічний шар відокремлювали, сушили (MgSO 4), фільтрували та випарювали розчинник. Осад (3,4г) очищали за допомогою колон очної хроматографії на силікагелі (елюент: CH2CI2/CH3OH/NH4OH 97/3/0,1; 15-40мкм). Збирали дві фракції та випарювали розчинник. Перший осад (0,9г) кристалізували з діізопропілового ефіру. Осад відфільтровували та сушили. Вихід: 0,49г сполуки 1 (діастереоізомер А) (т.п.: 136°С). Другий осад (0,79г) кристалізували з діізопропілового ефіру. Осад відфільтровували та сушили. Вихід: 0,105г сполуки 4 (діастереоізомер В) (т.п.: 179°С). Приклад В2 Одержання сполуки 2 та сполуки 3 39 83875 До розчину N-(1-метилетил)-2пропанаміну:гідрохлориду (1:1) (0,0071моль) в ТГФ (25мл) додавали по краплям н-BuLi 1,6М (0,0072моль) при -20°С в потоці азоту. Суміш перемішували протягом 20 хвилин. Потім охолоджували до -70°С. Додавали розчин проміжної сполуки 3 (0,0061моль) в ТГФ (5мл). Суміш перемішували протягом 2 годин. Додавали розчин 3-(диметиламіно)-1-(1-нафталініл)-1-пропанону (0,0062моль) в ТГФ (5мл) при -70°С. Суміш перемішували при -70°С протягом 3 годин. Додавали NH4Cl 10%. Суміш екстрагували EtOAc. Органічний шар відокремлювали, сушили (MgSO 4), фільтрували та випарювали розчинник. Осад (4г) очищали за допомогою колоночної хроматографії на силікагелі (елюент: CH2CI2/CH3OH/NH4OH 97/3/0,1; 1540мкм). Збирали фракції та випарювали розчинник. Перший осад (0,61г) кристалізували з DIPE. Осад відфільтровували та сушили. Вихід: 0,303г сполуки 2 (діастереоізомер А) (т.п.: 143°С). Другий осад (0,56г) очищали за допомогою колоночної хроматографії на силікагелі (елюент: СН2Сl2/СН3ОН 98/2). Збирали чисті фракції та випарювали розчинник. Вихід: 0,104г сполуки 3 (діастереоізомер В) (т.п.: 69°С). Приклад В3 Одержання сполук 5 та 6 До суміші N-(1-метилетил)-2-пропанаміну (0,0049моль) в ТГФ (15мл) додавали н-BuLi 1,6Μ (0,0048моль) при -70°С. Суміш перемішували при 20°С протягом 20 хвилин. Додавали розчин проміжної сполуки 6 (отриманої відповідно до А4.b) (0,004моль) в ТГФ (5мл) при -70°С. Суміш перемішували при -70°С протягом 2 годин. Додавали розчин проміжної сполуки 4 (отриманої відповідно до A3) (0,004моль) в ТГФ (5мл) при -70°С. Суміш перемішували при -70°С протягом 3 годин. Додавали NH4CI 10%. Суміш екстрагували EtOAc. Органічний шар відокремлювали, сушили (MgSO4), фільтрували та випарювали розчинник. Вихід: 2,1г. 40 Цю фракцію очищали за допомогою колоночної хроматографії на силікагелі (елюент: CH2CI2/CH3OH/NH4OH 96,5/3,5/0,1; 15-40мкм). Збирали дві фракції та випарювали розчинник. Вихід: 0,123г фракції А та 0,122г фракції В. Фракцію А очищали за допомогою колоночної хроматографії на силікагелі (елюент: СН2Сl2/СН3ОН 98/2; 15 -40мкм). Збирали чисті фракції та випарювали розчинник. Вихід: 0,119г. Цю фракцію поміщали в іРr2О/пентан. Суміш випарювали. Вихід: 0,077г сполуки 5 (т.п.: 58°С). Фракцію В кристалізували з DIPE. Осад відфільтровували та сушили. Вихід: 0,039г сполуки 6 (т.п.: 134°С). Приклад В4 Одержання сполук 13 та 14 До суміші N-(1-метилетил)-2-пропанаміну (0,013моль) в ТГФ (25мл) додавали н-BuLi 1,6Μ (0,013моль) при -20°С в потоці Ν 2. Суміш перемішували при -20°С протягом 20 хвилин, потім охолоджували до -70°С. Додавали розчин проміжної сполуки 8 (отриманої відповідно до А5.b) (0,0106моль) в ТГФ (25мл). Суміш перемішували при -70°С протягом 45 хвилин. Додавали розчин 3(диметиламіно)-1-(і-нафталініл)-1-пропанону (0,013моль) в ТГФ (20мл). Суміш перемішували при -70°С протягом 2 годин, виливали в Н2О при 30°С та екстрагували EtOAc. Органічний шар відокремлювали, сушили (MgSO4), фільтр ували та випарювали розчинник. Осад (5,5г) очищали за допомогою колоночної хроматографії на силікагелі (елюент: CH2CI2/CH3OH/NH4OH 99/1/0,1; 1540мкм). Збирали дві фракції та випарювали розчинник. Вихід: 0,33г сполуки 13 (діастереоізомер А) (3%) та 0,11г сполуки 14 (діастереоізомер В) (1%). Наступні сполуки одержували відповідно до зазначеної вище методики. Очищення осаду (*) вказує на відмінність від описаного вище очищення. 41 83875 42 Приклад В5 Одержання сполук 7 та 8 До суміші діізопропіламіну (0,0043моль) в ТГФ (10мл) повільно додавали н-бутил літію (0,0043моль) при -20°С в потоці N2. Суміш перемішували протягом 20 хвилин, потім охолоджували до -70°С. Додавали розчин проміжної сполуки 10 (отриманої відповідно до А6.b) (0,0036моль) в ТГФ (10мл). Суміш перемішували протягом 2 годин. Додавали розчин 3-(диметиламіно)-1-(1нафталініл)-1-пропанону (0,0043моль) в ТГФ (10мл). Суміш перемішували протягом 2 годин. Додавали Н2О. Суміш екстрагували EtOAc. Органічний шар відокремлювали, сушили сульфатом магнію, фільтрували та випарювали розчинник. Осад (*) (1,8г) очищали за допомогою колоночної хроматографії на силікагелі (елюент: CH2Cl2/MeOH/NH 4OH 98/2/0,2; 15-40мкм). Збирали дві фракції та випарювали розчинник. Вихід: 0,17г фракції 1 та 0,15г фракції 2. Фракцію 1 кристалізували з МеОН. Осад відфільтровували та сушили. Вихід: 0,082г сполуки 7 (5%, діастереоізомер А). Фракцію 2 очищали за допомогою колоночної хроматографії на силікагелі (елюент: СН2Сl2/МеOН: 98/2; 15-40мкм). Збирали чисті фракції та випарювали розчинник. Вихід: 0,13г сполуки 8 (7%, діастереоізомер В). Наступні сполуки одержували відповідно до зазначеної вище методики. Очищення осаду (*) вказує на відмінність від описаного вище очищення. 43 83875 44 Приклад В6 Одержання сполук 11 та 12 До суміші діізопропіламіну (0,002моль) в ТГФ (5мл) повільно додавали н-бутил літію (0,002моль) при -20°С в потоці N2. Суміш перемішували протягом 20 хвилин, потім охолоджували до -70°С. Додавали розчин проміжної сполуки 12 (отриманої відповідно до А7.b) (0,0017моль) в ТГФ (7мл). Суміш перемішували протягом 2 годин. Додавали розчин 1-(3,5-дифторфеніл)-3-диметиламіно-1пропанону (0,002моль) в ТГФ (4мл). Суміш перемішували протягом 2 годин. Додавали Н2О. Суміш екстрагували EtOAc. Органічний шар відокремлювали, сушили сульфатом магнію, фільтрували та випарювали розчинник. Осад (1,1г) очищали за допомогою колоночної хроматографії на силікагелі (елюент: СН2Сl2/МеOН: 99/1; 15-40мкм). Збирали дві фракції та випарювали розчинник. Вихід: 0,061г фракції 1 та 0,070г фракції 2. Фракцію 1 кристалізували з Ме ОН. Осад відфільтровували та сушили. Вихід: 0,046г сполуки 11 (5%, т.п.: 220°С, діастереоізомер А). Фракцію 2 кристалізували з МеОН. Осад відфільтровували та сушили. Вихід: 0,053г (5%, т.п.: 216°С, діастереоізомер В). С. Аналітичні способи Масу сполук визначали за допомогою LCMS (рідинна хроматографія з мас-спектрометрією). Були використані три нижчеописаних методи. Дані підсумовані в приведеній нижче таблиці 1. LCMS-метод 1 Аналіз методом LCMS (іонізація електророзпиленням в позитивному режимі, режим сканування від 100 до 900 атомних одиниць маси) виконували на колонці Kromasil С18 (Interchim, Montlucon, FR; 5мкм, 4,6´150мм) зі швидкістю потоку 1мл/хвилину. Були використані дві рухливі фази (рухлива фаза А: 30% 6,5мМ ацетату амонію + 40% ацетонітрилу + 30% мурашиної кислоти (2мл/л); рухлива фаза В: 100% ацетонітрилу) для створення градієнта від 100% А протягом 1 хвилини до 100% В протягом 4 хвилин, від 100% В протягом 5 хвилин до 100% А протягом 3 хвилин та повторного встановлення рівноваги при 100% А протягом 2 хвилин. Метод LC MS 2 Аналіз методом LCMS (іонізація електророзпиленням в позитивному та негативному (імпульсному) режимі, сканування від 100 до 1000 атомних одиниць маси) виконували на колонці Kromasil C18 (Interchim, Montlucon, FR; 3,5мкм, 4,6´100мм) зі швидкістю потоку 0,8мл/хвилину. Були використані дві рухливі фази (рухлива фаза А: 35;% 6,5мМ 45 83875ацетату амонію + 30% ацетонітрилу + 5% мурашиної кислоти (2мл/л); рухлива фаза В: 100% ацетонітрилу) для створення градієнта від 100% А протягом 1 хвилини до 100% В протягом 4 хвилин, від 100% В зі швидкістю потоку 1,2мл/хвилину протягом 4 хвилин до 100% А зі швидкістю потоку 0,8мл/хвилину протягом 3 хвилин та повторного встановлення рівноваги при 100% А протягом 1,5 хвилин. Таблиця 1 Вихідний пік LCMS № МН+ Сполука 7 Сполука 9 Сполука 15 Сполука 13 Сполука 14 509 495 495 509 509 LCMSметод 1 2 1 1 1 D. Фармакологічні приклади D.1. In vitro спосіб тестування сполук проти М. tuberculosis. Плоскодонні стерильні 96-лункові пластикові мікротитрувальні планшети заповнювали 100мкл бульйонним середовищем Middlebrook (1х). Після цього додавали основні розчини (10х кінцева тестова концентрація) сполук в об'ємі 25мкл до ряду парних лунок в колонці 2 для того, щоб оцінити їх вплив на бактеріальний ріст. Послідовні п'ятикратні розведення проводили безпосередньо в мікротитрувальних планшетах з колонки 2 по 11 за допомогою виконаного за замовленням робототехнічного комплексу (Zymark Corp,. Hopkinton, MA). Наконечники піпеток змінювали після кожних трьох розведень, щоб звести до мінімуму помилки піпеток з високогідрофобними сполуками. Неопрацьовані контрольні зразки, що містять (колонка 1) та не містять (колонка 12) інокулят, входили в кожен мікротитрувальний планшет. До рядів з А по Н, за винятком колонки 12, додавали приблизно 5000 CFU на лунку Mycobacterium tuberculosis (штам H37RV) в об'ємі 100мкл в бульйонному середовищі Middlebrook (1х). Такий же об'єм бульйонного середовища без інокулята додавали в колонку 12 в ряд з А по Н. Культури інкубували при 37°С протягом 7 днів у зволоженій атмосфері (інкубатор з відкритим повітряним клапаном та безперервною вентиляцією). За день до закінчення інкубації, через 6 днів після інокуляції в усі лунки додавали Resazurin (1:5) в об'ємі 20мкл та інкубували планшети ще протягом 24 годин при 37°С. На 7 день проводили кількісну оцінку бактеріального росту методом флуоресценції. Флуоресценцію вимірювали на керованому комп'ютером флуориметрі (Spectramax Gemini EM, Molecular Devices) при довжині хвилі збудження 530нм та довжині хвилі емісії 590нм. Процентний ріст інгібування, досягнутий сполуками, розраховували стандартними методами та розраховували дані МІС (що представляють величини ІС90, виражені в мікрограмах/мл). 46 D.2. Спосіб тестування сполук на антибактеріальну активність проти штаму М. Smegmatis ATCC607 in vitro. Плоскодонні стерильні 96-лункові пластикові мікротитрувальні планшети заповнювали 180мкл стерильної деіонізованої води з добавкою 0,25% BSA. Після цього додавали основні розчини (7,8х кінцева тестова концентрація) сполук в об'ємі 45мкл до ряду парних лунок в колонці 2 для того, щоб оцінити їх вплив на бактеріальний ріст. Послідовні п'ятикратні розведення (45мкл в 180мкл) проводили безпосередньо в мікротитрувальних планшетах з колонки 2 по 11 за допомогою виконаного за замовленням робототехнічного комплексу (Zymark Corp,. Hopkinton, ΜΑ). Наконечники піпеток змінювали після кожних трьох розведень, щоб звести до мінімуму помилки піпеток з високогідрофобними сполуками. Неопрацьовані контрольні зразки, що містять (колонка 1) та не містять (колонка 12) інокулят, входили в кожен мікротитрувальний планшет. В ряди з А по Н, за винятком колонки 12, додавали приблизно 250 CFU на лунку бактеріального інокулята, в об'ємі 100мкл в 2,8х бульйонного середовища Mueller-Hinton. Той же об'єм бульйонного середовища без прищеплювального матеріалу додавали в колонку 12 в ряд з А по Η. Культури інкубували при 37°С протягом 48 годин в зволоженій атмосфері, що містить 5% СО2 (інкубатор з відкритим повітряним клапаном та безперервною вентиляцією). Наприкінці інкубації, через два дні після інокуляції, проводили кількісну оцінку бактеріального росту методом флуоресценції. Тому в усі лунки додавали Alamar Blue (10х) в об'ємі 20мкл та інкубували планшети ще 2 години при 50°С. Флуоресценцію вимірювали на керованому комп'ютером флуориметрі (Cytofluor, Biosearch) при довжині хвилі збудження 530нм та довжині хвилі емісії 590нм (збільшення 30). Процентний ріст інгібування, досягнутий сполуками, розраховували стандартними методами. pIC50 визначали, як 50% концентрації, що інгібує ріст бактерій. Результати представлені в таблиці 2. Таблиця 2 Результати in vitro-скринінгу сполук за даним винаходом для M.smegmatis і М. tuberculosis (рІС50) Сполука № 1 2 3 6 15 10 14 13 9 8 11 Μ. smegmatis РІС50 6,2 6,5 5,7 4,9 6,4 5,9 5,9 5,8 5,8 5,8 5,7 Μ. tuberculosis pIC50 5 5,1 47 Комп’ютерна в ерстка Л.Литв иненко 83875 Підписне 48 Тираж 28 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюQuinoline derivatives for use as mycobacterial inhibitors
Автори англійськоюGuillemont Jerome Emile Georges, Pasquier Elisabeth Therese Jeanne, Lancois David Francis Alain
Назва патенту російськоюПроизводные хинолина для применения в качестве микобактериальных ингибиторов
Автори російськоюЖильмон Жером Эмиль Жорж, Паскье Элизабет Тереза Жанна, Ланкуа Давид Франсис Ален
МПК / Мітки
МПК: A61K 31/47, A61P 31/06, C07D 215/18
Мітки: мікобактеріальних, хіноліну, похідні, інгібіторів, застосування
Код посилання
<a href="https://ua.patents.su/24-83875-pokhidni-khinolinu-dlya-zastosuvannya-yak-mikobakterialnikh-ingibitoriv.html" target="_blank" rel="follow" title="База патентів України">Похідні хіноліну для застосування як мікобактеріальних інгібіторів</a>
Попередній патент: Матеріал для інтерференційних покриттів та інтерференційне просвітлювальне широкосмугове покриття (варіанти)
Наступний патент: Магніторідинне ущільнення та спосіб виготовлення магніторідинного ущільнення
Випадковий патент: Електрофорезна устілка












