Похідні 1,3-пропандіолу як біологічно активні сполуки
Номер патенту: 61884
Опубліковано: 15.12.2003
Автори: Уекфілд Пол, Макморді Остін, Бредлі Пол, Пит Ендре, Менку Мехар, Реден Пітер, Ноулз Філіп, Горобін Девід Фредерік
Формула / Реферат
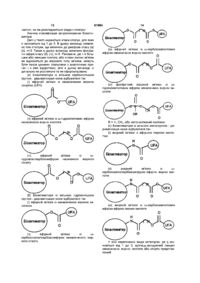
1. Сполуки, що мають зв'язану за допомогою 1,3-пропандіолу хімічну структуру:
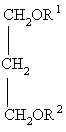 ,
,
де R1 включає ацильну групу або групу жирного спирту, що є похідною жирної кислоти з 12-30 атомами вуглецю, переважно з 16-30 атомами вуглецю, з двома чи більше цис- або транс-подвійними зв'язками, a R2 є воднем або включає ацильну групу або групу жирного спирту, таку саму як у R1 або іншу, або є будь-якою іншою поживною речовиною, лікарською речовиною чи іншою біологічно активною речовиною, окрім залишку ніацину.
2. Сполука за п. 1, де між R1 та/або R2 та 1,3-пропандіоловим залишком включена фосфатна, сукцинатна або інша дифункціональна кислотна група, особливо коли R2 є поживною речовиною, лікарською речовиною чи іншою біологічно активною речовиною, що включає функціональну гідрокси- або аміногрупу.
3. Сполука за будь-яким з пп. 1 або 2, де жирною кислотою є ефірна жирна кислота серії n-6 чи n-3 або олеїнова кислота, або колумбінова кислота, або паринарова кислота, або спряжена лінолева кислота.
4. Сполука за п. 3, де жирною кислотою є гамма-ліноленова кислота, дигомо-гамма-ліноленова кислота, арахідонова кислота, адренова кислота, стеаридонова кислота, ейкозапентаєнова кислота, докозапентаєнова кислота серії n-3, докозагексаєнова кислота або спряжена лінолева кислота.
5. Сполука за будь-яким з пп. 1, 2, 3 або 4, де R2 є лікарською речовиною або іншою активною речовиною, що має проникати крізь ліпідні мембрани в організмі для того, щоб проявляти свою активність чи то при вході в ту клітину, чи то під час руху усередині тієї клітини, де вона має діяти, або при проникненні крізь шкірний, гематоенцефалічний чи інший бар'єр.
6. Сполука за будь-яким з п. 1, 2, 3 або 4, де незалежно від типу проникнення крізь ліпідні мембрани R2 є лікарською речовиною, вітаміном, амінокислотою, антиоксидантом чи іншою активною речовиною, що має забезпечувати дію, адитивну, доповнюючу або синергетичну до дії R1.
7. Сполука за п. 1, яка включає дві жирні кислоти, одною з яких є гамма-ліноленова (GLA) або дигомо-гамма-ліноленова (DGLA) кислота, а другою - гамма-ліноленова (GLA), дигомо-гамма-ліноленова (DGLA), стеаридонова (SA), ейкозапентаєнова (ЕРА), докозагексаєнова (DHA), спряжена лінолева (cLA) або колумбінова (СА) кислота.
8. Сполука за п. 1, яка включає дві жирні кислоти, одною з яких є арахідонова кислота (АА), а другою - арахідонова (АА), гамма-ліноленова (GLA), докозагексаєнова (DHA), дигомо-гамма-ліноленова (DGLA) або ейкозапентаєнова (ЕРА) кислота.
9. Сполука за п. 1, яка включає дві жирні кислоти, одною з яких є ейкозапентаєнова кислота (ЕРА), а другою - ейкозапентаєнова (ЕРА) або докозагексаєнова (DHA) кислота.
10. Сполука за п. 1, де одне положення зайняте жирною кислотою з ряду GLA, DGLA, АА, SA, cLA, ЕРА або DHA, а друге положення зайняте речовиною, вибраною з наведеного нижче переліку, хімічна структура якої є такою, що вона може бути зв'язана із 1,3-пропандіолом через вільну карбоксильну, спиртову або аміногрупу:
(а) триптофан;
(б) фенілаланін;
(в) аргінін;
(г) карнітин або його похідні;
(д) будь-яка інша амінокислота або її похідні, або амінолевулінова кислота чи її похідні;
(е) аденілосукцинат або його похідні;
(є) аспірин, саліцилова кислота, індометацин, ібупрофен або будь-яка інша нестероїдна протизапальна лікарська речовина;
(ж) будь-який антибіотик, особливо тетрациклін, кліндаміцин, міноциклін, хлортетрациклін та еритроміцин;
(з) будь-яка протималярійна або антипротозоальна лікарська речовина, особливо хлороквін, мепакрин, квинакрин та мефлоквін;
(и) будь-яка протигрибкова лікарська речовина, особливо метронідазол та протигрибкові імідазоли, нітроімідазоли та амфотерицин;
(і) будь-який протизапальний стероїд, особливо гідрокортизон, бетаметазон, беклометазон та будезонід;
(й) будь-який гонадальний стероїд, особливо естрогени, прогестрогени та андрогени;
(к) будь-який адреностероїд, особливо дегідроепіандростерон;
(л) будь-який ретиноїд, особливо третиноїн та ізотретиноїн;
(м) будь-яка протиракова лікарська речовина;
(н) будь-яка протипсихотична лікарська речовина;
(о) будь-який антидепресант;
(п) будь-яка лікарська речовина для лікування тривожних станів;
(р) будь-який імунодепресант, особливо циклоспорин та такролімус;
(с) будь-який інгібітор протонного насосу або антагоніст Н2;
(т) будь-яка сечогінна лікарська речовина;
(у) будь-який антагоніст кальцію;
(ф) будь-який ферментний інгібітор, що перетворює ангіотензин, або антагоніст анпотензину;
(х) будь-який бета-блокатор;
(ц) будь-яка протиепілептична лікарська речовина, особливо фенітоїн, карбамазепін, вальпроат, етосуксимід, вігабатрин або ламотригін;
(ч) будь-який гіполіпідемічний агент, особливо фібрати та статини;
(ш) будь-які гіпоглікемічні або інсулінсенсибілізуючі лікарські речовини для перорального застосування;
(щ) будь-які біфосфонати;
(ь) будь-які контрастні агенти, що використовуються в радіології, зокрема, сполуки діатризоату, іодипамід, іогліцамати, іопаноати, іофендилат, іоталамат, іоксаглат, метризамід та їхні похідні;
ю) будь-який пептид або протеїн, включаючи інсулін, кальцітомін, еритропоетин;
(я) будь-який вітамін;
(аа) будь-який антиоксидант;
(бб) будь-який порфірин, хлорин, або лікарські речовини на основі бактеріохлорину, особливо тетракіс (гідроксифеніл) та його похідні.
11. Композиція для догляду за шкірою або волоссям або для лікування шкірних захворювань, яка містить сполуку за будь-яким з пп. 1-10.
12. Харчовий продукт, який містить сполуку за будь-яким з пп. 1-10.
13. Харчовий продукт за п. 12, який містить сполуку за п. 10, причому згаданою речовиною є вітамін або антиоксидант.
14. Харчова добавка, яка містить сполуку за будь-яким з пп. 1-10.
15. Харчова добавка за п. 14, яка містить сполуку за п. 10, причому згаданою речовиною є вітамін або антиоксидант.
16. Поживна добавка, яка містить сполуку за будь-яким з пп. 1-10.
17. Поживна добавка за п. 16, яка містить сполуку за п. 10, причому згаданою речовиною є вітамін або антиоксидант.
18. Лікарський засіб, який містить сполуку за будь-яким з пп. 1-10.
Текст
1 Сполуки, що мають зв'язану за допомогою 1,3-пропандюлу хімічну структуру CILOR сн, CH2OR l де R1 включає ацильну групу або групу жирного спирту, що є похідною жирної кислоти з 12-30 атомами вуглецю, переважно з 16-30 атомами вуглецю, з двома чи більше цис- або транс-подвійними зв'язками, a R2 є воднем або включає ацильну групу або групу жирного спирту, таку саму як у R або іншу, або є будь-якою іншою поживною речовиною, лікарською речовиною чи іншою біологічно активною речовиною, окрім залишку ніацину 2 Сполука за п 1, де між R1 та/або R2 та 1,3пропандюловим залишком включена фосфатна, сукцинатна або інша дифункцюнальна кислотна група, особливо коли R2 є поживною речовиною, лікарською речовиною чи іншою біологічно активною речовиною, що включає функціональну гідрокси- або аміногрупу 3 Сполука за будь-яким з пп 1 або 2, де жирною кислотою є ефірна жирна кислота серії п-6 чи п-3 або олеїнова кислота, або колумбінова кислота, або паринарова кислота, або спряжена лінолева кислота 4 Сполука за п 3, де жирною кислотою є гаммаліноленова кислота, дигомо-гамма-ліноленова кислота, арахідонова кислота, адренова кислота, стеаридонова кислота, ейкозапентаєнова кислота, докозапентаєнова кислота серії n-З, докозагексаєнова кислота або спряжена лінолева кислота 5 Сполука за будь-яким з пп 1, 2, 3 або 4, де R2 є лікарською речовиною або іншою активною речовиною, що має проникати крізь ЛІПІДНІ мембрани в організмі для того, щоб проявляти свою активність чи то при вході в ту клітину, чи то під час руху усередині тієї клітини, де вона має діяти, або при проникненні крізь шкірний, гематоенцефалічний чи інший бар'єр 6 Сполука за будь-яким з п 1, 2, 3 або 4, де незалежно від типу проникнення крізь ЛІПІДНІ мембрани R2 є лікарською речовиною, вітаміном, амінокислотою, антиоксидантом чи іншою активною речовиною, що має забезпечувати дію, адитивну, доповнюючу або синергетичну до дії R1 О 00 00 (О 61884 7 Сполука за п 1, яка включає дві жирні кислоти, одною з яких є гамма-ліноленова (GLA) або дигомо-гамма-ліноленова (DGLA) кислота, а другою гамма-ліноленова (GLA), дигомо-гаммаліноленова (DGLA), стеаридонова (SA), ейкозапентаєнова (ЕРА), докозагексаєнова (DHA), спряжена лінолева (сІ_А) або колумбінова (СА) кислота 8 Сполука за п 1, яка включає дві жирні кислоти, одною з яких є арахідонова кислота (АА), а другою - арахідонова (АА), гамма-ліноленова (GLA), докозагексаєнова (DHA), дигомо-гамма-ліноленова (DGLA) або ейкозапентаєнова (ЕРА) кислота 9 Сполука за п 1, яка включає дві жирні кислоти, одною з яких є ейкозапентаєнова кислота (ЕРА), а другою - ейкозапентаєнова (ЕРА) або докозагексаєнова (DHA) кислота 10 Сполука за п 1, де одне положення зайняте жирною кислотою з ряду GLA, DGLA, АА, SA, cLA, ЕРА або DHA, а друге положення зайняте речовиною, вибраною з наведеного нижче переліку, хімічна структура якої є такою, що вона може бути зв'язана із 1,3-пропандюлом через вільну карбоксильну, спиртову або аміногрупу (а) триптофан, (б) фенілаланін, (в) аргінін, (г) карнітин або його ПОХІДНІ, (д) будь-яка інша амінокислота або и ПОХІДНІ, або амінолевулінова кислота чи и ПОХІДНІ, (є) аденілосукцинат або його ПОХІДНІ, (є) аспірин, саліцилова кислота, індометацин, ібупрофен або будь-яка інша нестероідна протизапальна лікарська речовина, (ж) будь-який антибіотик, особливо тетрациклін, кліндаміцин, міноциклін, хлортетрациклін та еритроміцин, (з) будь-яка протималярійна або антипротозоальна лікарська речовина, особливо хлороквін, мепакрин, квинакринта мефлоквін, (и) будь-яка протигрибкова лікарська речовина, особливо метронідазол та протигрибкові імідазоли, нітроімідазоли та амфотерицин, (і) будь-який протизапальний стероїд, особливо гідрокортизон, бетаметазон, беклометазон та будезонід, (й) будь-який гонадальний стероїд, особливо естрогени, прогестрогени та андрогени, (к) будь-який адреностероїд, особливо депдроепіандростерон, (л) будь-який ретиноїд, особливо третинош та ізотретинош, (м) будь-яка протиракова лікарська речовина, (н) будь-яка протипсихотична лікарська речовина, (о) будь-який антидепресант, (п) будь-яка лікарська речовина для лікування тривожних станів, (р) будь-який імунодепресант, особливо циклоспорин татакролімус, (с) будь-який інгібітор протонного насосу або антагоніст Н2, (т) будь-яка сечогінна лікарська речовина, (у) будь-який антагоніст кальцію, (ф) будь-який ферментний інгібітор, що перетворює анпотензин, або антагоніст анпотензину, (х) будь-який бета-блокатор, (ц) будь-яка протиепілептична лікарська речовина, особливо фенітош, карбамазепін, вальпроат, етосуксимід, вігабатрин або ламотрипн, (ч) будь-який пполіпідемічний агент, особливо фібрати та статини, (ш) будь-які гіпоглікемічні або інсулінсенсибілізуючі лікарські речовини для перорального застосування, (щ) будь-які біфосфонати, (ь) будь-які контрастні агенти, що використовуються в радіологи, зокрема, сполуки діатризоату, юдипамід, югліцамати, юпаноати, юфендилат, юталамат, юксаглат, метризамідта їхні ПОХІДНІ, ю) будь-який пептид або протеїн, включаючи інсулін, кальцітомш, еритропоетин, (я) будь-який вітамін, (аа) будь-який антиоксидант, (бб) будь-який порфірин, хлорин, або лікарські речовини на основі бактерюхлорину, особливо тетракіс (пдроксифеніл) та його ПОХІДНІ 11 Композиція ДЛЯ догляду за шкірою або волоссям або для лікування шкірних захворювань, яка містить сполуку за будь-яким з пп 1-10 12 Харчовий продукт, який містить сполуку за будь-яким з пп 1-10 13 Харчовий продукт за п 12, який містить сполуку за п 10, причому згаданою речовиною є вітамін або антиоксидант 14 Харчова добавка, яка містить сполуку за будьяким з пп 1-10 15 Харчова добавка за п 14, яка містить сполуку за п 10, причому згаданою речовиною є вітамін або антиоксидант 16 Поживна добавка, яка містить сполуку за будьяким з пп 1-10 17 Поживна добавка за п 16, яка містить сполуку за п 10, причому згаданою речовиною є вітамін або антиоксидант 18 Лікарський засіб, який містить сполуку за будьяким з пп 1-10 Ця специфікація стосується форми реалізації бюактиваторів, під цим терміном автори розуміють лікарський засіб, ефірну живильну речовину та будь-яку іншу сполуку, котру може бути введено в організм людини або тварини з метою терапевтичного втручання або здійснення профілактичних заходів В більш вузькому розумінні ця специфікація стосується реалізації згаданих бюактиваторів у тій формі, в котрій вони є ліпофільними, що дозволяє їм легко проходити крізь ЛІПІДНІ бар'єри різних тканин організму, або реалізації двох бюактиваторів в одній і тій же молекулі (де принаймні один з них являє собою жирну кислоту або жирний спирт), або реалізації речовин бюактиваторів у формі, котра може служити для досягнення двох вищезгаданих цілей та/або для полегшення синте 61884 зу подібних сполук без хірального центра 3 точки зору стабільності лікарських засобів великою перевагою є те, що два бюактиватори можуть представляти спільну одинарну молекулу, у порівнянні з існуванням їх у формі двох окремих ХІМІЧНИХ одиниць Також з'являється можливість реалізувати вже ВІДОМІ бюактиватори в нових варіантах До переваг віднесено підвищену ліпофільність, додаткові присадочні ефекти двох бюактиваторів, які в звичайних формулах не виявляються разом, а також спорадичні синергетичні ефекти таких речовин Цей винахід стосується ХІМІЧНОГО сполучення бюактиваторів через певні молекулярні зв'язки, детальний опис яких подається нижче у тексті документу, а також синтезу ряду сполук, деякі з цих сполук є самі по собі цілком новими сполуками, в той час як новизна інших розглядається з точки зору їх корисності в терапевтичному лікуванні та/або для збереження здоров'я Але виникає спірне питання з приводу сполук, в яких використовуються ІНШІ зв'язуючи молекули, що їх на даний час не заявлено, а також сполук із прямим ХІМІЧНИМ зв'язком, описаних, наприклад, в ЕРА-0 393 920, стосовно жирних кислот та антивірусних засобів, і в спільно заявленому ЕР-95301315 8 (опубліковано як ЕРА-0 675 103), стосовно жирних кислот та нестероідних протизапальних лікарських засобів Концепціям, що розглянуті вище, не надавалося великої уваги в опублікованій патентній та загальнонауковій літературі, але є дані про деякі описані ПОХІДНІ натуральних дюлів і про застосування деяких специфічних діольних ефірів в живильних та фармацевтичних цілях Першоджерельним виданням в загальнонауковій літературі можна вважати статтю Bergelson et al (Biochim , Biophys Acta 116 (1966) 511-520), де, зокрема, дано опис довголанцюгових диефірів 1,3пропанового дюлу В тій праці було дано зовсім мало інформації про кислотні складові сполук, але визначене саме поняття про ПОХІДНІ ДЮЛІВ В патентній літературі дані щодо ХІМІЧНИХ імітаторів споживних жирів, наприклад, було запропоновано Nabisco в ERA-0 405 873 і ЕРА-0 405 874, в цій праці до таких сполук було віднесено ефіри ліноленової кислоти (під ЦІЄЮ назвою, коли не наводиться інше специфічне визначення, слід розуміти "альфа"-ізомер) та ефіри арахідонової кислоти, очевидно, 1,4-бутановий дюл В загальній британській специфікації 2 161 477 (що відповідає ЕРА-0 161 114) підкреслюється зростання КІЛЬКОСТІ та економічне значення фармацевтичних підприємств, які, зокрема, використовують 1,3-пропандюлові ефіри лінолевої кислоти та ліноленової кислоти (знову, без сумніву, альфа-ізомер) Противиразкові препарати на базі 2,3-бутандюлових ефірів описано у ЕРА-0 056 189 компанії SS Pharmaceutical Co Різноманітні фармацевтичні впливи пропан-1,3-дюлових ефірів коротколанцюгових жирних кислот показано в ЕРА-0 018 342 фірми Sanofi Більш далеким від теми є ХІМІЧНИЙ ЗВ'ЯЗОК 5-фторо-урацилу із альфа-ліноленовою кислотою, дигомо-гама-ліноленовою кислотою, або із ейкозапентаеновою кислотою через групу -CH(R)-O-, де R = метил тощо, ці модифікації дають, зокрема, протираковий лікувальний ефект ЛІПІДНІ бар'єри Багато препаратів впливають на поверхню мембрани клітин шляхом безпосереднього з'єднання із клітинними реагентами-рецепторами, або, навпаки, проникають у клітину за допомогою специфічних транспортуючих систем 3 другого боку, існує ціла низка препаратів, котрі не можуть ефективно проникати в клітину і обробляти и через те, що вони діють усередині клітини шляхом змінений лише однієї з багатьох різних функцій, зокрема функцій нуклеїнових кислот, внутрішньоклітинних ферментів, або шляхом змінення властивостей таких систем, як лізосоми чи мікротубули Очевидно, не існує таких реагентів-рецепторів або транспортуючих систем, з якими подібні препарати мали б змогу ХІМІЧНО зв'язуватися, або ж ці системи здатні транспортувати препарати в клітину надто повільно Тобто, хоча такі препарати і можуть проникати через більш глибокі внутрішньоклітинні мембрани, такі, як мембрани мітохондрій та ядер, але це відбувається надто повільно Існують ІНШІ бар'єри, що заважають пересуванню препаратів, які визнаються важливими Одним з них є гемато-енцефаловий бар'єр, який має низку аналогічних характеристик в порівнянні з клітинною мембраною Для багатьох препаратів неможливо досягти потрібної їх концентрації в тканинах мозку саме через наявність згаданого бар'єру Інша справа - вплив препарату на організм через шкіряні покрови до останніх років препарати вживали таким шляхом лише у тих випадках, коли об'єктом лікування була сама шкіра Але зараз визнається, що шкіра може бути цілком прийнятним "шляхом доставки" в організм препаратів систематичного характеру дії, і, внаслідок цього, все більше і більше сполук виготовляється таким чином, щоб їх можна було призначати способом накладки пластирутощо Усі три типи бар'єрів - клітинна та внутрішньоклітинні мембрани, гемато-енцефаловий бар'єр і шкіряні покрови - мають ту характерну спільну рису, що вони складаються в значній мірі з ЛІПІДІВ Це означає, що вони є ХІМІЧНО непроникними для препаратів, створених на базі водних розчинів, якщо не знайдеться ВІДПОВІДНИЙ реагент-рецептор або транспортуюча система, здатні супроводжувати ці препарати крізь згадані мембрани Напроти, ліпофільні речовини здатні проходити через бар'єри досить легко і не потребують будь-яких специфічних реагентів-рецепторів або транспортуючих систем Класи бюактивних сполук, що потребують ХІМІЧНОГО супроводження в процесі проникнення в клітини крізь ЛІПІДНІ бар'єри Препарати, що їх фармакокшетичні властивості може бути поліпшено шляхом підвищення ліпофільності, перелічено за принципом шляху доставки в тканини організму 1 Клітинний ВХІД найбільшу перевагу мають препарати внутрішньоклітинного впливу До них відносяться а Усі протизапальні препарати, стероїдні чи нестероідні, б Усі ЦИТОТОКСИЧНІ препарати, що використовуються при контролюванні канцерогенних проце 61884 сів, в Усі противірусні препарати, г Усі ІНШІ препарати, що їх може бути введено до клітин з метою досягнення оптимальних результатів, зокрема, препарати, які впливають на ДНК або РНК, або на внутрішньоклітинні ферменти, або на системи вторинного транспортування, або на мікротубули, мітохондрм, лізосоми та будьякі ІНШІ внутрішньоклітинні елементи д Стероїдні гормони та ІНШІ гормони внутрішньоклітинного впливу, такі як ЖІНОЧІ статеві гормони, прогестини, ЧОЛОВІЧІ статеві гормони та депдроепіандростерон 2 Гемато-енцефаловий бар'єр запропонована технологія допоможе поліпшити транспортування в організмі усіх препаратів, що впливають на центральну нервову систему До переліку таких препаратів входять всі ті, що застосовуються в психіатри, всі препарати, що їх використовують при лікуванні церебральних інфекцій в будь-якому організмі, або при лікуванні ракових захворювань мозку, в цей перелік також входять усі ІНШІ препарати, що впливають на нервові клітини, зокрема протиепілептичні засоби та ІНШІ препарати, що лікують від неврологічних розладів, зокрема складних склерозів, амютропних латеральних склерозів, хореї Хантінгтонатощо 3 Шкіряні покрови як і у випадку гематоенцефалового бар'єра, усі препарати, які потрібно вводити через шкіру для досягнення систематичного ефекту, бажано перетворити у ПОХІДНІ жирних кислот Як приклад можна навести амінокислоти Найбільш цікавими серед них є, очевидно, ті, що відіграють суттєву роль в регулюванні функцій клітини, а також ті, що діють як компоненти протеїнів До таких відносяться триптофан (попередній продукт 5-пдрокситриптаміну [5-НТ], ключовий регулятор нервової та м'язової функції), фенілаланін (попередній продукт катехоламшів) та аргінін (регулятор синтезу окису азоту, який також відіграє значну роль в керуванні клітинними процесами) Загальне порівняння властивостей Взагалі сполуки, що пропонуються згідно з цим винаходом, мають цілу низку переваг додатково до їх підвищеної ліпофільності Дві складові частини жирної кислоти або навіть одну з складових може бути введено в організм у зручній формі як оральним, так і парентеральним чи поверхневим шляхом, сполука, згідно з цим винаходом, є цілком толерантною (без жодних побічних ефектів) із вільними жирними кислотами, сполука, згідно з цим винаходом, не є занадто стійкою, для того, щоб бути повністю утилізованою, сполука, згідно з цим винаходом, не потребує наявності хірального центра, також сполука, згідно з цим винаходом, набагато легше синтезується, ніж ВІДПОВІДНИЙ тригліцерид із трьома складовими частинами тієї ж приєднаної жирної кислоти Незважаючи нате, що тригліцериди є високотолерантними сполуками та добре утилізуються, їх застосування є менш практично вигідним, ніж застосування запропонованих в цьому винаході сполук справа в тому, що їх синтезування проходить більш складно, і вони повинні мати хіральний центр із кількома потенціальними ізомерами Крім того, з тригліцеридами жирні кис 8 лоти можуть відносно легко мігрувати з одного положення в інше, створюючи нові молекули, які не присутні в оригінальному препараті Це, що очевидно, породжує зайві проблеми, особливо у контексті стабільності препарату у тих випадках, коли нестабільність не може бути допустимою Коли необхідно ввести в організм дві різні жирні кислоти, переваги сполук цього винаходу є очевидними, плюс можливість одночасного призначення двох активаторів із різними біологічними властивостями у вигляді одномолекулярної сполуки Це дозволяє уникнути проблем регулятивного характеру, котрі виникають під час призначення двох речовин як окремих сполук, а також позбутися проблем, які з'являються там, де потрібні хіральні центри хімічної молекули Коли іде мова про поставки двох препаратів у вигляді різних сполук, кожна із своєю молекулою, представники місцевих офіційних фармацевтичних установ звичайно вимагають окремого вивчення як кожної сполуки, так і їх спільної дії Якщо ці дві сполуки ХІМІЧНО об'єднані під єдиною молекулою, виникає потреба [продиктована вимогами офіційних установ - перекл ] у вивченні лише тієї єдиної молекули, що значно зменшує вартість впровадження препарату Аналогічні переваги спостерігаються і в тому випадку, коли активатори не є жирними кислотами Застосування сполук цього винаходу дає можливість призначати препарати або ІНШІ суміші у формі нехіральних відносно-ліпофільних сполук (якщо ті препарати чи ІНШІ сполуки є самі по собі хіральними) Завдяки цьому активні складові частини можуть бути порівняно легко вивільнені, а також може бути покращено толерантність орального, поверхневого чи парентерального призначення Ліпофільність дозволяє таким препаратам частково адсорбуватися через лімфатичні вузли, обминаючи печінку, застосування сполук згідно з цим винаходом обумовлює також менший ризик виникнення шлунково-кишкових подразнень, ніж при застосуванні багатьох інших сполук, крім того застосування сполук згідно з цим винаходом полегшує та прискорює транспортування препаратів та інших агентів через такі ліпофільні бар'єри, як шкіра, клітинна мембрана та гемато-енцефаловий бар'єр Очевидно, що для багатьох живильних та фармацевтичних препаратів у випадку збільшення їхньої ліпофільності може бути виявлено чимало цікавих специфічних властивостей, додатково до більш легкого проникнення крізь ЛІПІДНІ бар'єри До таких властивостей може бути віднесено пролонгованість дії, зменшення побічних ефектів, особливо з боку шлунково-кишкового тракту, виключення первинного біохімічного метаболізму в печінці і, в перспективі, врахування особливостей локальної доставки різних речовин ПОХІДНІ жирних кислот, ефекти впливу жирних кислот Транспортування активних сполук крізь ЛІПІДНІ мембрани може бути поліпшене шляхом їх безпосереднього зв'язування або зв'язування через проміжні ланки (кільця), зокрема із гамаліноленовою кислотою (GLA) або дигомо-гамалінолевої кислотою (DGLA), тобто двома кислотами, які самі по собі характеризуються кількома корисними ефектами Подібні зв'язки також дозво ляють вводити ІНШІ бюаісгивні сполуки в формі єдиної молекули із жирними кислотами, що вже самі по собі є здатними давати сприятливі ефекти відносно впливу на організм незалежно від будьяких переваг, пов'язаних із переносом речовини Також може бути використано ІНШІ жирні кислоти, наприклад, будь-яку з ефірних жирних кислот (EFA) та, зокрема, дванадцять природних кислот EFA серій п-6 та n-З (Фіг) 3 цих дванадцяти найбільш цікавими є арахідонова, адренова, стеаридонова, ейкозапентаенова та докозагексаенова кислоти через те, що вони самі по собі мають бажані ефекти Крім того, може бути використано будь-яку жирну кислоту, що відповідає КІЛЬКОСТІ атомів вуглецю С12-С30 або Сіє-Сзо бажано із двома чи більше цис або транс-вуглець-вуглець подвійним зв'язком Практичне застосування може бути прийнятним у формі жирної кислоти або ВІДПОВІДНОГО жирного спирту Сполучені лінолева та колумбинова кислоти є прикладом жирних кислот, що самі по собі мають ЦІННІ властивості, та, очевидно, особливо цікаві з точки зору їх практичного застосування Посилання на жирні кислоти в тексті цього винаходу повинні стосуватися обох форм, за виключенням тих випадків, коли хімічна структура тієї чи іншої форми має власну специфіку та підлягає додатковому обговоренню Слід відзначити, що практично корисні властивості GLA та DGLA роблять їх особливо привабливими для досягнення поставленої цим винаходом мети 61884 10 Отже, сполуки на основі жирних кислот можуть бути двобічно-(при прямому зв'язку) або трибічно(при існуванні проміжного зв'язку) взаємозамінюючими препаратами До інших жирних кислот, які мають особливу ЦІННІСТЬ в цьому контексті, можна віднести арахідонову та докозогексаенову кислоти, що є головними складовими компонентами усіх клітинних мембран, адренову кислоту, стеаридонову та ейкозапентаенову кислоти, що мають цілу низку практично цінних властивостей, аналогічних GLA та DGLA До переліку найбільш цікавих жирних кислот, що їх не було включено до Фіг, можна віднести сполучену лінолеву кислоту (cLA) та колумбинову кислоту (СА) Кислота cLA має певні цікаві властивості при лікуванні та запобіганні ракової хвороби, зокрема активізує збільшення об'єму протеш-вміщуючих тканин, допомагає при лікуванні та запобіганні серцево-судинних захворювань та відіграє важливу роль як проти окислювач СА також має більшість корисних властивостей ефірних жирних кислот Ефірним жирним кислотам, які в природних умовах можуть бути представлені усіма цисконфігураціями, систематично призначені найменування похідних ВІДПОВІДНО октадеканової, ейкозанової або докозанової кислот, наприклад, z.z-октадека9,12-діенова кислота або z,z,z,z,z,z-flOKO3a4,7,10,13,16,19-гексаенова кислота, але числова нумерація базується на КІЛЬКОСТІ атомів вуглецю, на КІЛЬКОСТІ центрів ненасиченості та на КІЛЬКОСТІ атомів вуглецю на тому КІНЦІ ХІМІЧНОГО ланцюга, де починається ненасичення, наприклад, 18 2п-6 або 22 6п-3 Для звичних ХІМІЧНИХ назв у деяких випадках використовуються абревіатури, наприклад, ЕРА, та скорочені форми напису, наприклад, ейкозапентаенова кислота GLATaDGLA Самі по собі GLA та DGLA ВІДОМІ ЯК сполуки, які мають протизапальні властивості, знижують тиск, шпбірують накопичення дрібних пластинчастих бляшок шкідливих речовин, понижують рівень холестерину, шпбірують процес розвитку ракових клітин, зменшують вплив дискінетичних (некоординованих) рухів, заспокоюють болі у грудях, покращують абсорбцію кальцію та полегшують його відкладення у тканини кісток, зменшують шкідливий вплив юнизуючої радіації, лікують різноманітні ПСИХІЧНІ розлади, сприяють кращому розтягненню стінок кровоносних судин, поліпшують функцію нирок, лікують ускладнення в процесі захворювання на діабет, в цілому сприяють розширенню кровоносних судин тощо Таким чином, активні реагенти, сполучені з GLA та DGLA, стають не лише більш ліпофільними, покращуючи властивості проникнення крізь мембрани, шкіряний та гематоенцефаловий бар'єри, але, додатково до цього, набувають нових терапевтичних властивостей Класи активних речовин, що ефективно взаємодіють із бюактивними жирними кислотами До активних лікарських речовин, які можуть утворювати сполуки із запропонованими в цьому винаході речовинами, відноситься широке коло медичних препаратів а) Препарати, що вміщують антибіотики, антипротозоали (засоби проти найпростіших), антипсихотики, антидепресанти, NSAID (нестероідні протизапальні сполуки) та сполуки, які застосовуються при лікуванні серцево-судинних, дерматологічних, психічних, неврологічних, ниркових, м'язових, шлунково-кишкових, ракових захворювань, а також захворювань органів дихання та репродукції тощо б) Гормони в) Амінокислоти г) Вітаміни, особливо групи В, а також ІНШІ ЖИВИЛЬНІ ефірні речовини д) Цитокши та пептиди є) Нейропередавачі та ХІМІЧНІ попередники нейропередавачів ж) Фосфоліпідні головні групи, такі як шоситол, холін, серин та етаноламш, які можуть бути з'єднані безпосередньо одна з одною, або через проміжну фосфатну складову з) Ароматичні жирні кислоти, такі як фенілоцтова кислота, фенілбутирова кислота та корична кислота, котрі мають особливе значення при лікуванні від ракових захворювань Ефективність Комбінація терапевтичного ефекту лікарського препарату та терапевтичного ефекту жирної кислоти можна проілюструвати такими прикладами а) Психотропні препарати можуть бути приєднані до жирних кислот, таких, як GLA, DGLA, арахідонової, ейкозапентаенової або докозагексаеновоі кислоти, що відіграють суттєву роль в регулюванні функції мозку, таким чином забезпечується подвійний терапевтичний ефект б) Препарати, що використовуються для лікування серцево-судинних захворювань, можуть бути приєднані до жирної кислоти, яка сама по собі також має лікувальне значення, до таких кис 11 лот відносяться ейкозапентаенова кислота, що понижує рівні вмісту тригліцериду та шпбірує накопичення дрібних бляшок шкідливих речовин, а також GLA або DGLA, які знижують рівень вмісту холестерину та сприяють розширенню судин, сюди ж відносяться арахідонова кислота, яка є потужним холестерин-знижуючим агентом, а також DHA, що має властивості, які сприяють зникненню аритмії серця в) Препарати, що використовуються при лікуванні запальних процесів у будь-якій формі, можуть бути приєднані до таких жирних кислот гамаліноленової, дигомо-гамаліноленової, ейкозапентаенової, або до докозагексаенової кислоти, яка також діє як протизапальний засіб г) Препарати, що використовуються для контролю над розвитком остеопорозу, можуть бути приєднані до GLA або DGLA, які підвищують вміст кальцію в КІСТКОВІЙ тканині, ці препарати також можуть бути приєднаними до ЕРА або DHA, які знижують виділення кальцію з сечею д) Препарати, що використовуються при захворюваннях шкіри, можуть бути приєднані до GLA або DGLA, які мають протизапальний вплив на шкіру є) Препарати, що використовуються в онкологи, можуть бути приєднані до GLA, DGLA, арахідонової кислоти, ЕРА або DHA, які самі по собі мають властивості протиракових засобів і, до того ж, здатні скасувати опірність до інших протиканцерогенних препаратів Концепція щодо застосування ефірних жирних кислот як бюактиваторів Ефірні жирні кислоти (EFA), як вже було згадано у тексті цього винаходу та є добре відомим для фахівців, утворюють серію з дванадцяти сполук Хоча лінолева кислота, первісна (материнська) сполука сери п-6, і альфа-ліноленова кислота, первісна кислота сери n-З, є головними харчовими кислотами, вони, як самостійні речовини, мають порівняно невелике значення в організмі Для більш повного їх використання в тканинах тіла, головні сполуки повинні бути метаболізованими в сполуки з довголанцюговими молекулами та мати більший ступінь ненасиченості Якщо це оцінювати КІЛЬКІСНО, звертаючи увагу на реальну участь речовини в ХІМІЗМІ клітинних мембран та в інших ЛІПІДНИХ реакціях, то слід відзначити, що головними метаболітами EFA сери п-6 є дигомогамаліноленова (DGLA) та арахідонова (АК) кислоти, а головними метаболітами EFA сери п-3 є ейкозапентаенова (ЕРА) та докозагексаенова (DHA) кислоти DGLA, АК, ЕРА та DHA є найважливішими компонентами більшості ЛІПІДІВ в організмі Крім того, що вони самі по собі відіграють суттєву роль в біохімічних процесах, вони також є основою для створення широкого діапазону окислених похідних сполук, ейкозаноідів, включаючи простагландини, лейкотриени тощо Очевидно, що особливу роль в терапії відіграють згадані DGLA, АК, ЕРА та DHA, разом із GLA - попередником DGLA, стеаридоновою кислотою (SK) - попередником ЕРА, і DPA (докозапентаеновою кислотою) (22 5п-3) - попередником DHA, а також із адреновою кислотою Крім того, в терапії успішно використовуються олеїнова кислота, паринарова кислота та нюбино 61884 12 ва кислота, які не відносяться до EFA, але відіграють суттєву роль у ХІМІЧНИХ процесах в організмі Однією З найцікавіших поміж них є сполучена олеїнова кислота, котра, як було відзначено раніше, має цілу низку корисних властивостей Існувала думка про те, що, як з метою підживлення організму, так і при терапевтичному лікуванні, головним моментом є введення первинних лінолевої та альфа-ліноленової кислот, а вже власний метаболізм живого організму, мовляв, завершить решту справи Зараз більшість фахівців погоджуються з думкою, що це не так РІЗНІ захворювання можуть супроводжуватися різними аномальними характеристиками EFA, і через складні проблеми щодо самого метаболізму, ці аномалії не можуть бути скоригованими лише шляхом введення лінолевої чи альфа-ліноленової кислоти Отже, у багатьох ситуаціях виникає потреба призначати більші об'єми тієї чи іншої EFA, або вводити дві чи більше EFA одночасно Оскільки EFA можуть бути введеними в різних формах і в різних сумішах, як з метою підживлення організму, так і в терапевтичних цілях, зручно мати можливість вводити жирні кислоти як речовини із окремими молекулами Також, в різних ситуаціях, бажано вводити EFA чи іншу жирну кислоту в організм разом із амінокислотою, вітаміном, будь-яким препаратом та речовинами, що мають самі по собі корисні властивості До останнього часу пропозиції щодо призначення двох жирних кислот одночасно стосувалися переважно тригліцеридїв, враховуючи природну форму існування ефірних жирних кіслот саме у вигляді тригліцеридів Однак, якщо не зважати на модифікації із симетрією відносно 2вуглецю, тригліцериди є сполуками із хіральними центрами, і це, в сукупності з міграцією кислотного залишку (ацила) між альфа- і бета позиціями, робить синтез специфічних тригліцеридів тяжким завданням Згадана міграція може створити після здійснення синтезу певні проблеми з погляду на регулятивний аспект застосування препарату Брак специфіки впливу, коли дві жирних кислоти є присутніми в одній молекулі тригліцериду, спричиняє чимало труднощів з точки зору синтезу, фармакологи, розробки та збереження стабільності сполуки До того ж, власне синтезування тригліцеридів може відбуватися поволі і важко За однаковими стартовими умовами ПОХІДНІ пропанового дюлу можуть бути виготовлені значно швидше З метою зручності одночасного призначення різних жирних кислот або призначення справжньої одинарної жирної кислоти в великих дозах та у добре толерантній формі автори рекомендують віддавати перевагу використанню ефірів дюлів (етиленгліколі в) Хімічна природа бюактиваторів, ПОХІДНІ ЯКИХ пропонуються згідно з цим винаходом Ця специфікація охоплює ПОХІДНІ жирної кислоти (або жирного спирту), які стосуються речовин з карбоксильною, спиртовою або аміно- групою, що представляють собою ХІМІЧНІ ОДИНИЦІ З ЄДИНОЮ, добре визначеною формулою ХІМІЧНИЙ ЗВ'ЯЗОК може бути здійснено шляхом прямого з'єднання рухливих груп двоскладових сполук або через відповідну проміжну зв'язуючу групу, у випадку трискладових сполук, в залежності від числа складових 61884 13 частин, на які розкладаються згадані сполуки Хімічна класифікація запропонованих бюактиваторів Далі у тексті надаються класи сполук, для яких п змінюється від 1 до З В цьому винаході заявлено такі сполуки, що включені до диефірів класу (а) (їм) ефірний зв'язок із ш-карбоксиалкіловим (м), п=3 Також в цьому винаході заявлено фосфаефіром ненасиченої жирної кислоти тні ефіри класу (б) (iv), n=3 Речовини, де п є більшим або меншим числом, або в яких ХІМІЧНІ ЗВ'ЯЗКИ не відносяться до ефірного типу зв'язків, можуть бути також цінними сполуками з аналогічних причин і є вже відкритими, але в цьому винаході їх детально не розглянуто та не сформульовано (а) Бюактиватори із вільною карбоксильною групою - дериватизація може відбуватися так (і) ефірний зв'язок із ненасиченим жирним (iv) фосфатний ефірний зв'язок із шспиртом (UFA) пдроксиалкіловим ефіром ненасиченої жирної кислоти О о-р—о П" І OR (м) ефірний зв'язок із ш-пдроалкіловим ефіром ненасиченої жирної кислоти О О (їм) ефірний зв'язок із шпдроалкілкарбоксиефіром насиченого жирного спирту R = Н, СНз, або катюнактивний протиюн (с) Бюактиватори із вільною аміногрупою - дериватизація може відбуватися так (і) амідний зв'язок із ефірною жирною кислотою О (м) амідний зв'язок із шкарбоксиалкілкарбоксиефіром ефірної жирної кислоти UFA (б) Бюактиватори із вільною гідроксильною групою - дериватизація може відбуватися так (і) ефірний зв'язок із ненасиченою жирною кислотою (м) ефірний зв'язок із шкарбоксиалкілкарбоксиефіром ненасиченого жирного спирту (їм) амідний зв'язок із ш-карбоксиалкіловим ефіром ефірної жирної кислоти У всіх перелічених вище категоріях, де п змінюється від 1 до 3, вуглець-вміщуючий ланцюг ненасиченої жирної кислоти або спирту представлений 15 61884 В усіх перелічених вище категоріях "ненасичена жирна кислота" (і похідна "ненасиченого жирного спирту" - UFA) представляє собою член групи, що містить в собі олеїнову кислоту (і олеоіловий спирт) та будь-яку жирну кислоту (або ВІДПОВІДНИЙ жирний спирт) з двома чи більше цис або транс подвійними зв'язками Але слід відзначити, що ефірні жирні кислоти, яким надається перевага у контексті цього винаходу, є саме ті кислоти, що їх показано на фіг, особливо GLA, DGLA, АК, ЕРА та DHA В окремих випадках може виникати зацікавленість у застосуванні сполученої лінолевої та колумбинової кислот Загальний опис синтезу Жирні кислоти в самостійному вигляді можуть бути виділені з природної тваринної, рослинної та мікробіологічної речовини або можуть бути ХІМІЧНО синтезовані за допомогою відомих фахівцям методів, або методів, що запропоновані далі в цьому документі Жирні спирти в самостійному вигляді можуть бути виготовлені шляхом ХІМІЧНОГО відновлення згаданих жирних кислот також за допомогою відомих фахівцям методів, або методів, що запропоновані далі в цьому документі Дериватизація (здобуття ХІМІЧНИХ ПОХІДНИХ) бюактивних сполук класів (а), (б) та (в) [субкласів (м) та (Ні)] вимагає формування одного чи більше ефірних зв'язків Такий ХІМІЗМ можна здійснити за допомогою будь-якого оптимального методу синтезування ефірів, зокрема (а) шляхом реакції спирту з кислотним хлоридом, кислотним ангідридом або ВІДПОВІДНО активізованим ефіром в присутності (або без неї) органічного третинного аміну (наприклад, піридину), у відповідному інертному розчиннику (наприклад, дихлорметані), при температурі від 0° до 120°С (б) шляхом реакції спирту з кислотою, або з коротко- чи середньоланцюговим алкіловим ефіром кислоти, в присутності ВІДПОВІДНОГО кислотного каталізатора (наприклад, 4-толуоловоі сульфокислоти), із ВІДПОВІДНИМ інертним розчинником, наприклад, толуолом (або без нього), при температурі від 50° до 180°С, з умовою повного видалення води, що утворюється під час проходження реакції, наприклад, під вакуумом (в) шляхом реакції спирту з кислотою в присутності конденсуючого агента, наприклад, 1,3дициклогексилкарбодмміду, в присутності (або без неї) ВІДПОВІДНОГО органічного третинного аміну, наприклад, 4-(г\І,г\І-диметіламінопіридину), в інертному розчиннику, наприклад, дихлоро метані, при температурі від 0°до 50°С (г) шляхом реакції спирту з кислотою або з коротко- чи середньоланцюговим алкіловим ефіром кислоти або активізованим ефіром кислоти, наприклад, вінилом, в присутності пдролазового ферменту, наприклад, етерази, взятої з печінки однолітньої копитної тварини, в присутності (або без неї) ВІДПОВІДНОГО розчинника, наприклад, гексану, при температурі від 20° до 80°С з умовою повного видалення біпродуктів реакції, таких як вода, вто 16 ринний спирт та альдегід, наприклад, під вакуумом (д) шляхом реакції кислоти із ВІДПОВІДНОЮ ПОХІДНОЮ спирту, наприклад, юдидом, в присутності (або без неї) відповідної основи, наприклад, карбонату калію, у відповідному розчиннику, наприклад, диметилформаміді, при температурі від 0° до 180°С (є) шляхом реакції спирту із коротко- або середньоланцюговим алкиловим ефіром кислоти, в присутності каталізного об'єму алкоксиду типу + M OY~, де М є лужним або лужноземельним металом, наприклад, натрієм, a Y є алкіловою групою, яка містить в собі 1-4 атоми вуглецю і може бути розгалуженою, нерозгалуженою, насиченою чи ненасиченою, в присутності (або без неї) ВІДПОВІДНОГО розчинника, наприклад, толуолу, при температурах від 50° до 180°С, з умовою, що нижчий спирт із загальною формулою HOY буде повністю видалено з суміші реакції, наприклад, під вакуумом Дериватизація бюактивних сполук класу (в) вимагає формування амідного зв'язку Такий ХІМІЗМ може бути реалізовано за допомогою оптимальної методики синтезування амідів, зокрема (ж) шляхом реакції аміну із кислотним хлоридом, кислотним ангідридом або ВІДПОВІДНИМ ЧИНОМ активізованим ефіром в присутності (або без неї) органічного третинного аміну, наприклад, піридину, у відповідному інертному розчиннику, наприклад, дихлорометані, при температурі від 0° до 120°С (з) шляхом реакції аміну із кислотою в присутності кондесуючого агента, наприклад, 1,3дициклогексилкарбодмміду, в присутності (або без неї) ВІДПОВІДНОГО третинного аміну, наприклад, 4(г\І,г\І-диметиламінопіридину), у відповідному розчиннику, наприклад, дихлорометані, при температурі від 0° до 50°С (і) ШЛЯХОМ реакції аміну із кислотою або кислотним коротко- або середньоланцюговим ефіром, або із кислотою, активізованою ефіром, наприклад, вінилом, у присутності пдролазового ферменту, наприклад, ефірази, взятої з печінки однолітньої копитної тварини, у відповідному розчиннику (або без нього), наприклад, у гексані, при температурах від 20° до 80° С з умовою повного видалення біпродуктів реакції, таких як вода, спирт чи альдегід, наприклад, під вакуумом Дериватизація бюактивних сполук класу (б) (iv) потребує формування складних фосфатноефірних зв'язків Такий ХІМІЗМ можна здійснити за допомогою будь-якого оптимального методу синтезування складних фосфатних ефірів, зокрема (к) шляхом реакції спирту (наприклад, UFA, 3пдроксипропілового ефіру) із ВІДПОВІДНО активізованою фосфатною похідною (наприклад, РОСІз), із третинним аміном (наприклад, EtsN) у відповідному розчиннику (наприклад, THF), при температурі, меншій ніж 10°С, з виходом сирого фосфородихлоридату Наступним кроком має бути реакція спирту (наприклад, а-токоферолу) із сирим фосфородихлоридатом, із третинним аміном (наприклад, EtsN) у відповідному розчиннику (наприклад, у тетрапдро-2,5-фурандиметанолі) при температурі оточуючого середовища, з виходом сирого 18 17 61884 фосфородихлоридату Його має бути пдролізоваляна кислота), GLA-амшолевулшова кислота та в но (наприклад, шляхом додавання води та Ет.зІЧ), з цілому будь-яка кислота поміж GLA, DGLA, AK, SK, виходом складного фосфодиефіру Як варіант, ЕРА або DHA з будь-якою природною амінокислододавання метанолу призводить до виходу складтою або ХІМІЧНО спорідненою сполукою, наприклад, ного фосфотриефіру, котрий має бути позбавлено таурином та карнітином метилової групи за допомогою відповідної нуклеАроматичні кислоти офільної речовини (наприклад, броміду ЛІТІЮ), у GLA-фенілбутирова кислота, GLAвідповідному розчиннику (наприклад, метил етил фенілоцтова кислота, GLA-транс-корична кислота кетоні), з виходом складного фосфодиефіру та в цілому будь-яка з кислот GLA, DGLA, AK, SK, ЕРА або DHA із будь-якою кислотою арилалкано(л) шляхом реакції фосфомоноефіру (напривоі та арилалкенової групи клад, фосфату UFA, 3-пдроксипропілового ефіру) із спиртом (наприклад, холіном), в присутності Стероїди конденсуючого агенту (наприклад, 1,3GLA-пдрокортизон, GLA-естрадюл, GLA- та дициклогексилкарбодмміду) у відповідному розDHA-депдроепіандростерон і в цілому будь-яка з чиннику при ВІДПОВІДНІЙ температурі GLA, DGLA, AK, SK, ЕРА або DHA із будь-яким природним та синтетичним стероїдом, наприклад, (м) шляхом реакції трансфосфатидиляцм деоестогеном, будь-якими прогестином, адреналстексі-2-лізофосфатидилхолшу із первинним або второїдом та будь-яким протизапальним стероїдом, ринним спиртом, каталізованим фосфоліпазою D зокрема бетаметазоном, преднізоном, преднізоВ цілому ХІМІЗМ циклу виготовлення препаратів лоном, триамцинолоном, будезонідом, клобетазозалежить від природи сполук, які необхідно ХІМІЧНО лом, беклометазоном та іншими спорідненими з'єднати, а також від того, чи є ці зв'язки прямими стероїдами або опосередкованими Наприклад, пари жирних кислот можуть бути безпосередньо з'єднаними у Антиоксиданти формі ефірів тандему жирної кислоти-жирного GLA-ліпоідна кислота, DHA-ліпоідна кислота, спирту, або як ангідриди, і, якщо використовуються GLA-токоферол, fli-GLA-3,3'-TioflHnponioHOBa кисдюлові зв'язувачі, ефірні зв'язки із жирними спирлота та в цілому будь-яка з кислот GLA, DGLA, AK, тами є альтернативою більш традиційним (звичSK, ЕРА або DHA із будь-яким природним чи синним) ефірним зв'язкам із жирними кислотами, у тетичним антиоксидантом, з яким є можливим ХІвсіх випадках зв'язування може здійснюватися за МІЧНИЙ зв'язок вказаних кислот До переліку таких допомогою відомих ХІМІЧНИХ реакцій речовин входять фенолові антиоксиданти (наприклад, евгенол, карнозова кислота, кофеїнова (каПриклади пар активних сполук, які можуть бувова) кислота, ВНТ, галова кислота, токофероли, ти ХІМІЧНО зв'язаними безпосередньо або через токотриеноли та флавоноїдні (ароматичні) антиокпроміжні зв'язуючі елементи, зокрема через 1,3сиданти (наприклад, мірецитин, фізетин), поліени Пропан-дюловий зв'язувач (наприклад, ретинова кислота), ненасичені стероВ тій мірі, як це відомо авторам винаходу, пали (наприклад, Д5-авеностерол), органосірчані ри сполук, що даються нижче у тексті, а також респолуки (наприклад, аліцин), терпени (наприклад, зультативні сполуки є принципово новими препагераніол, абіетова кислота) та амінокислотні антиратами Тому їх слід розглядати, згідно з одним з оксиданти (наприклад, цистеїн, карнозин) аспектів цього винаходу, як нові ХІМІЧНІ структури, які роблять свій внесок в нові методи лікування та Препарати запобігання захворювань, незалежно від того, чи GLA і індометацин, ібупрофен, флюоксетин, було зроблено на них заявку як на ХІМІЧНІ сполуки ампіцилін, пеніцилін V, суліндак, саліцилова кисдо цього часу лота, метронідазол, флуфеназин, дапсон, транілципромш, ацетилкарнітин, галоперидол, мепакрин, Жирні кислоти хлороквін, пеніцилін, тетрацицилін, правастатин, GLA-OA (ОА = олеїнова кислота), GLA-GLA, бісфосфонати, наприклад, ефідронова кислота, ЕРА-ЕРА, GLA-EPA, GLA-DHA, AK-DHA, АК-ЕРА, памідронова кислота та хлордронова кислота та їх GLA-AK, GLA-SK, SK-DHA, AK-SK, DGLA-DGLA, натрієві солі, аденозилосукцинат і аденілосукцинат DGLA-GLA, DGLA-SK, DGLA-AK, DGLA-EPA, та споріднені сполуки і реагенти, що використовуDGLA-DHA, АК-АК, EPA-SK, EPA-DHA, DHA-DHA, ються як рентгенконтрастні речовини, а також взаcLA-cLA, cLA-GLA, cLA-DGLA, cLA-AK, cLA-SK, галі будь-які з кислот GLA, DGLA, AA, SK, ЕРА чи cLA-EPA, cLA-DHA, CA-CA, CA-GLA, CA-DGLA, DHA із будь-яким препаратом, зокрема з тих, що CA-AK, CA-EPA, CA-DHA використовуються при лікуванні інфекційних заВітаміни хворювань, запальних процесів, включаючи різноGLA-ніацин, GLA-ретинова кислота, GLAманітні форми артритів, ракових, серцеворетинол, GLA-піридоксал, Ди-СІ_А-піридоксин, дисудинних, респіраторних, дерматологічних, психічGLA-піридоксал і в цілому будь-яка з кислот GLA, них, неврологічних, м'язових, ниркових, шлунковоDGLA, АК, SK, ЕРА чи DHA із будь-яким вітаміном, кишкових захворювань, а також захворювань рещо містить в собі абсорбну кислоту, вітамін D та продуктивної системи тощо його ПОХІДНІ і аналоги, вітамін Е та його ПОХІДНІ І аналоги, вітамін К та його ПОХІДНІ І аналоги, вітамін Концепція NSAID-препаратів, аргументація Ві (тиамін), вітамін Вг (рібофлавін), фолієва кисефективності лота та споріднені з нею птерини, вітамін Ві2, біоЯк конкретний детальний приклад реалізації тин та пантотенова кислота авторської концепції запропоновано варіанти різних похідних нестероідних протизапальних препаАмінокислоти ратів (NSAID) та зокрема GLA-ефіру індометацину GLA-триптофан, GLA-пролш, GLA-арпнш, Індометацин як протизапальний препарат, очевиGLA- або DHA-фенілаланін, GLA-ГАБК (аміномас 19 61884 дно, має внутрішньомолекулярний характер впливу на організм за рахунок шпбірування ферментарної (ензимної) оксигенази, котра перетворює арахідонову кислоту на метаболіти простагландину, що спричиняють поширення запального процесу Відомо, ЩО індометацин проникає в клітину дуже слабо, і через це його потрібно призначати у порівняно великих дозах, що створює чимало побічних ефектів, для порівняння властивостей чистого індометацинута шдометацину-GLA проникати в клітину було вивчено нормальну спектральну клітинну ЛІНІЮ, ЛІНІЮ клітини раку грудної залози та ЛІНІЮ клітини злоякісної меланоми Результати було викладено в ЕРА 0 675 103, де показується, що у всіх вказаних клітинних ЛІНІЯХ внутрішньоклітинний рівень вмісту вільного індометацину після інкубації із ним є дуже низьким та переважно спостерігається у слідових концентраціях Напроти, якщо розглядати також усі перелічені КЛІТИННІ лінії, інкубація із зв'язаним індометацином-GLA призвела до накопичення у клітинах як шдометацину-GLA, так і вільного індометіцину у вельми значних концентраціях Ці результати безперечно свідчать про те, що GLA-ефір індометацину має властивість ефективно проникати в клітину організму, після чого в середині клітини проходить деефіразація цієї сполуки з виділенням вільного індометацину, а також проте, що, з точки зору наявності багатьох спільних рис між клітинномембранним, гемато-енцефаловим та шкіряним ЛІПІДНИМИ бар'єрами, застосування GLAіндометацину буде сприяти проникненню індометацину крізь бар'єри також двох останніх вказаних типів На аналогічне проникнення в клітину і подальший зворотний розклад на ВІЛЬНІ (не зв'язані) активні сполуки можна сподіватися щодо усіх сполук цього винаходу Аспекти цього винаходу викладено в розділі "Формула винаходу" далі у тексті Головний аспект стосується сполук, що використовуються в терапевтичних цілях, коли 1,3-пропан-дюловий залишок формує зв'язок між залишками R1, R2, R1 є групою ацилового або жирного спирту, яка є похідною жирної кислоти із КІЛЬКІСТЮ атомів вуглецю Сі2зо переважно Сієзо бажано з двома чи більше цис- або транс- подвійними зв'язками, a R2 є воднем, а також зв'язок між ациловою чи жирнокислотною групою, де R1 може бути аналогічною чи іншою групою, або іншою живильною речовиною, або препаратом, або іншим бюактивним залишком В цілому цісполуки є кислотнофункціональними речовинами, ефірізованими безпосередньо до дюлового залишку, але, наприклад, у варіанті із жирним спиртом або іншою гідроокисно-функціональною речовиною, між R1 та/або R2 і 1,3-пропан-дюловим залишком має бути вставлено проміжний фосфат, сукцинат чи іншу дифункцюнальну кислотну групу, особливо у тих випадках, коли R2 є живильною речовиною, препаратом або іншою бюактивною сполукою із гідрокси або аміно функціями Нижче у тексті цей винахід обговорюється у більш широкому аспекті, охоплюючи широке коло активних речовин, які мають властивість вивільнюватися у організмі 20 Оскільки раніше вже було обговорено прямі зв'язки бюактивних речовин і жирних кислот (класи (a)PL (б) [і] та (в)[і], цей винахід стосується перш за все класу (а)[іі], П = 3, за допомогою якого бюактиватори, що самі по собі є жирними кислотами, приєднуються до жирних кислот як диефіри 1,3пропан-дюлу, а також класу (6)(iv), n = 3, за допомогою якого бюактиватори, що самі по собі є жирними спиртами або 3-пдроксипропіловими ефірами, приєднуються до жирнокислотного моноефіру 1,3-пропан-дюлу через фосфатний зв'язок Цей дюл може бути розглянуто як 2-деоксигліцерол із ВІДПОВІДНИМИ диефірами, такими як 2-деокси-1,3дигліцеридами Сполуки класу (6)(iv), n=3 також базуються на 1,3-пропан-дюлі та їх можна розглядати як 2-диокси-2-лізофосфоліпіди Майже усі перелічені тут сполуки є новими ХІМІЧНИМИ структурними одиницями, або їх принаймні ніколи не було використано при лікуванні людей або тварин Як зв'язуюча ланка в ХІМІЧНИХ сполуках дюл, згідно з цим винаходом, досить часто згадується поміж інших дюлів у науковій літературі, але автори переконані, що його використання в терапії у формі диефіру ефірної жирної кислоти або у вигляді сполуки із ефірною жирною кислотою - з одного боку, і як бюактиватору (що не являє собою ефірну жирну кислоту) - з другого боку, ще не було досі відкрито і повинно мати особливе значення І дійсно, він створює сприятливі умови для введення одинарної жирної кислоти у формі складного моноефіру або диефіру, якщо ситуація вимагає призначення повністю визначеної сполуки, це стає можливим тому, що дюл, згідно з цим винаходом, по-перше, не має хірального центру, який, навпаки, є присутнім у складних гліцерин-1 (3)моноефірах і в дигліцеридах (а, [3 та 1,3, де жирна кислота в позиції 1 відрізняється від такої в позиції 3), а, по-друге, в ньому не існує так званих ізомерів положення Крім того, незалежно від введення окремих кислот, такі складні моно- та диефіри можуть мати значення у фармацевтичній формуліровці як емульсіфікатори 1,3-пропан-дюл структурно є дуже подібний до гліцерину природних тригліцеридів і представляє собою ефективну систему, яку легко та безпечно можна вводити в організм До того ж цей винахід дозволяє здійснювати доволі нескладне синтезування ВІДПОВІДНИХ сполук без проблем із міграцією ацилової групи, котрі, на відміну, існують для тригліцеридів, та без ускладнень, пов'язаних із оптичними ізомерами Автори, зокрема, показали, що внутрішньовенна інфузія та оральне призначення емульсії складного 1,3пропан-дюлового диефіру GLA/EPA призводять до дуже швидкого вивільнювання in vivo ХІМІЧНО не зв'язаних GLA та ЕРА і до подальшого метаболізму GLA в АА та ЕРА в DHA Аналогічно показано, що складні диефіри GLA-GLATa ЕРА-ЕРА і складні ефіри ніацин-GLA та шдометацин-GLA також можуть ефективно застосовуватися шляхом орального призначення із подальшим вивільненням з організму їх активних біохімічних складових На додаток до викладеної інформації, на думку авторів, всі ПОХІДНІ сполуки із 1,3-пропан-дюлом, згадані на сторінках 26, 27, 28 та 29, є новими сполуками, які ще ніколи не було описано Специфічні дюли жирних кислот з перелічених в тому 22 21 61884 списку, а також дюли, в яких - з одного боку - є льні положення про корисність складних 1,3присутньою жирна кислота з серії DGLA, GLA, АА, пропан-дюлів зведено у таких пунктах SK, EPA, DHA, сІ_А та СА, а з другого - вітамін, 1 Підвищення фармацевтичної толерантності амінокислота, ароматична кислота, стероїд, антижирних кислот Якщо не розглядати зараз тригліоксидант чи інший терапевтичний препарат - є цериди, більшість форм, в яких можуть бути приновими речовинами значені жирні кислоти, включаючи ВІЛЬНІ КИСЛОТИ, СОЛІ, складні етилові ефіри та ІНШІ гліцериди, Коло можливого застосування складних диеспричиняють деяку шлунково-кишкову штолерантфірів жирної кислоти є доволі широким, їх може ність (нудота, блювота, розладдя кишечнику) Вибути використано як фармацевтичні засоби для вчення складних пропан-дюлових диефірів на твалікування або запобігання захворювань, при яких ринах - щурах та мишах - дало виключно хороші було виявлено відхилення у ХІМІЗМІ жирних кислот результати щодо толерантності Наприклад, диеорганізму Ці сполуки може бути добавлено до фіри GLA-GLA і GLA-EPA було дано щурам та михарчових продуктів або використано як живильні шам у дозах до 10г/кг ваги, після чого ніяких ознак добавки для всіх пацієнтів, організм яких потребує розладдя шлунково-кишкового тракту виявлено не певних жирних кислот для лікування чи для запобібуло Це свідчить, що застосування диефірів є гання захворювань Вони також можуть бути викоцілком прийнятним методом доставки в живі ткаристані як харчові добавки та ліки для тварин Крім нини біологічно активних жирних кислот того, ці речовини є хорошим фармацевтичним засобом для збереження здорової шкіри Переваги 2 Зменшення токсичності препаратів Нестета різні конкретні сприятливі аспекти використання роїдні протизапальні препарати, наприклад, аспіпрепаратів згідно цього винаходу можна коротко рин та індометацин мають не зовсім добру репувикласти таким чином тацію через свою шлунково-кишкову токсичність і шкідливий вплив на стінки шлунку та кишечника та (і) Зручні та безпечні шляхи введення в оргачерез крововиливи у травний шлях Негодованим нізм (з метою терапевтичного лікування чи піджищурам давали дози індометацину, які були ВІДОМІ влення) таких препаратів, як одна чи дві складових як здатні спричиняти шлунково-кишкові пошконенасиченої жирної кислоти, або одна ненасичена дження (5-30мг/кг ваги), у формі вільного індомежирна кислота та одна бюактивна сполука, що не тацину, в той же час такий самий об'єм індометає жирною кислотою цину було дано в складному 1,3-пропан-дюловому (м) Наявність похідної бюактиватору, яку необдиефірі із GLA Через 24 години тварин було похідно ХІМІЧНО провести через ліпіднімембрани жизбавлено життя та розтято з метою вивчення цілових тканин для досягнення більш ефективного її го шлунково-кишкового тракту на предмет пошковпливу на організм, незалежно від типу ЛІПІДНОГО джень Якщо в тілах тваринок, яким давали лише бар'єру (клітинна мембрана, шкіряні покрови чи чистий індометацин, було виявлено інтенсивне гемато-енцефаловий бар'єр), ця похідна може пошкодження травного шляху, то у групи щурів, мати згадані корисні властивості завдяки присутяким давали GLA-шдометацин, пошкоджень пракності 1,3-пропан-дюлового приєднання до ефірної тично не було знайдено жирної кислоти з природних серій п-6 або п-3, особливо GLA чи DGLA, АА, SK, ЕРА чи DHA, або до 3 Ефективність доставки в тканини біологічно кон'югованих жирних кислот сІ_А чи С А активної форми жирної кислоти GLA призначалася у формі GLA-GLA або GLA-EPA, а ЕРА призна(їм) Похідна жирної кислоти в складі препарату, чалася у формі GLA-EPA або ЕРА-ЕРА Складні що дозволяє взаємодоповнювати ефективні власефіри давалися ПІДДОСЛІДНИМ тваринам або оративості згаданих препарату та жирної кислоти льним шляхом, або внутрішньовенно у формі 20% (iv) Методика поліпшення транспортування емульсії, використовуючи як емульсіфікатор вівсяпрепарату крізь ЛІПІДНІ бар'єри живих тканин, це ний галактоліпід в дозах від 0,1 до 2,0г/кг ваги поліпшення обумовлено згаданою вище зручністю ВІДПОВІДНО через 1, 2, 4, 8 і 24 години тваринок форм призначення препарату було позбавлено життя та зібрано плазму, червоні (v) Методика вироблення медикаментів підвикров'яні тільця та тканини печінки Наявність немещеної терапевтичної ЦІННОСТІ, яка полягає в кратаболізованих складних диефірів було визначено щому проходженні препарату через ЛІПІДНІ мемза допомогою рідинної хроматографії з запрограбрани живих тканин, мованим високим тиском Наявність жирних кислот ця методика характеризується впровадженням (як похідних цих складних ефірів) та метаболітів до складу медикаментів препарату цього винахоцих жирних кислот було встановлено шляхом ексДУ трагування ЛІПІДІВ печінкової тканини, плазми та (vi) Методика вироблення медикаментів, причервоних кров'яних тіл, подальшого сепарування значених для забезпечення живих тканин однією здобутої ліпідної фракції на тригліцериди, фосфоабо двома жирними кислотами зі списку по пункту ЛІПІДИ, складні ефіри холестерину та ВІЛЬНІ жирні (м), або для забезпечення живих тканин однією з кислоти за допомогою хроматографії тонких шарів, тих жирних кислот, які асоціюються із іншим актиметилацм жирних кислот, що є похідними згаданих вним агентом сепарованих фракцій, і подальшого аналізування Приклади назв конкретних сполук було дано здобутих жирних кислот за допомогою добре відовище у тексті цього винаходу, приклади процедур мих стандартних методів газової хроматографії Ці синтезування буде надано далі за текстом експерименти показали, що близько 10% орально Ефективність та застосування введеного складного диефіру було виявлено у Інформацію про конкретне застосування спеформі залишків складного диефіру Більшу частицифічних груп сполук може бути представлено в ну об'єму GLA та ЕРА було виявлено у формі вірізних частинах тексту цього винаходу, але зага 24 23 61884 льної жирної кислоти або фосфоліпіду і меншу - у 3 Імуномодуляторні функції, включаючи гасінвигляді хол есте рол о во го ефіру та фракцій тригліня надмірних імунних та алергічних реакцій в твацериду Більше того, саме у фосфоліпідних фракринних моделях, таких як експериментальні алерціях можна було побачити значну частину загальгічні енцефаломіеліт та увеїт, підвищену ного об'єму метаболітів GLA, DGLA та бронхіальну та шкіряну реактивність в штучно збуарахідонової кислоти, а також метаболітів ЕРА, джених до чутливого стану тваринних організмах, докозапентаенової кислоти та DHA Ці дослідження тваринні моделі породжують також концепцію вадовели, що складний диефір є джерелом досить жливості імуномодуляторних функцій при лікуванні легкого вивільнювання жирних кислот, які далі хворих людей, коли виникає надмірна імунна реаметаболізуються в біологічно активні речовини кція Аналогічні результати було одержано після внут4 Функція підтримки респіраторної системи, рішньовенного введення, за виключенням того, що включаючи процес поліпшення еластичності брончерез 1 годину близько 40% складного диефіру хів та інгібірування процесу стискання (стягування) залишалися в первинному вигляді, а чисті жирні бронхів кислоти вивільнювалися, метабол ізувалися та 5 Покращення кальцієвого балансу, тобто об'єднувалися в ІНШІ ЛІПІДНІ фракції протягом напідвищення здатності організму поглинати кальцій, ступних 24 годин Цілком ймовірно, що незмінені зменшення ефекту "вимивання" кальцію, сприяння диефірні форми є самі по собі біологічно активнибільш активному відкладенню кальцію в кістках, ми речовинами Виявлено, що лінолева кислота у зменшення локального ефекту відкладення кальформі 1,3-дигліцериду дає протираковий ефект, цію в таких тканинах, як артерії та нирки який цілеспрямовано впливає лише на ракові тка6 Протиракові ефекти трьох типів селективне нини, але не на нормальні здорові клітини Такий цитотоксичне пошкодження та внесення апоптозу ефект не спостерігався для інших форм лінолевої лише в ракові клітини, але не здорові, інгібіруванкислоти (A Matsuzaki et al, Cancer Res 1989, 49 ня зростання ракових клітин за рахунок гасіння 5702-7) Можна зробити припущення, що цей активності факторів зростання та подавляючої вплив, разом із можливими іншими ефектами, взаємодії із вторинною системою переносу, яка обумовлює необхідність введення двох молекул відповідає за розвиток злоякісних клітин, інгібіружирної кислоти, структурно розташованих у формі вання процесу поширення метастаз за допомогою 1,3-дигліцериду Таке молекулярне розташування механізму, що сприяє більш виразному впливові є можливим за допомогою додавання 1,3-пропанЕ-кадгеринів, та інгібірування протеолітових фердюлу, звідси можна припустити, що є особливий ментів (езимів), таких як урокінази, ліпоксигенази сенс у внутрішньовенному введенні деяких з прота матричні металопротеїнази, а також інгібіруванпан-дюлових похідних для того, щоб забезпечити ня спричиненого раком виснаження (кахексії} циркуляцію дюлових форм в крові протягом певно7 Вплив на нервові клітини, включаючи прого часу перед досягненням їх повного метаболізфілактику нормальної структури та функціонуванму ня мембрани нервових клітин, а також нормального пре- та постсинаптичного функціонування Жирні кислоти характеризуються цілою низкою нейропередатчиків біологічно та терапевтичне корисних властивостей, чий детальний опис викладено у численних Наведені практично важливі властивості ознапублікаціях, авторами яких є винахідники та ІНШІ чають, що цю групу жирних кислот можна викорисфахівці Найбільша частина загального спектру товувати при лікуванні різних захворювань, вклюкорисних ефектів належить чотирьом жирним кисчаючи серцево-судинні різних типів, запальних лотам GLA, DGLA, SK та ЕРА Такими ефектами процесів, зокрема ревматоїдного артриту, остеовважаються артриту, виразкового коліту та хвороби Крона, респіраторних захворювань, зокрема астми, психі1 Вплив на серцево-судинну систему, включних розладів, зокрема шизофренії, алкоголізму, чаючи розтягування (підвищення еластичності) розсіяної уваги, депресії та хвороби Альцгеймера, стінок судин, зниження кров'яного тиску, інгібірунейролопчних захворювань, зокрема розсіяного вання накопичення дрібних бляшок шкідливих ресклерозу та хореї Хантінгтона, захворювань нирчовин, зниження рівнів тригліцеридів та LDLкового та сечового тракту, зокрема різних типів холестерину, підвищення рівнів HDL-холестерину запальних процесів в нирках та відкладення кальта інгібірування зростання гладких м'язів за рахуцієвих каменів у сечовому тракті, розладдя у пронок новоутворень (тобто профілерації) цесах метаболізму, зокрема остеопорозу та над2 Протизапальні ефекти, включаючи зменмірного локального відкладення кальцію, запалень шення КІЛЬКОСТІ сприяючих запаленню медіаторів, та виразок у шлунково-кишковому тракті Не дивтаких як цитокіни, завдяки ейкозаноідам, що є полячись нате, що сполучену лінолеву кислоту (сІ_А) хідними арахідонової кислоти спостерігається не було в такій мірі протестовано, як, наприклад, ефект зменшення впливу нейтрофільної міграції GLA чи ЕРА, вона, очевидно, також характеризута імовірності спричиненого нейтрофільною міграється широким діапазоном корисних властивостей, цією респіраторного розриву, зменшення сили зокрема важливих при лікуванні раку, серцеволокальних запальних реакцій, інгібірування запасудинних захворювань та розладів у системі, що лень, що спостерігаються в різних тваринних мовідповідає за метаболізм GLA, DGLA, АА та нюбіделях, наприклад, запалень, спричинених видінова кислота мають корисні властивості щодо шкіленням сечової кислоти, та супровідних артритів, ри і можуть бути особливо потрібними при лікулікування різноманітних спричинених запаленням ванні таких захворювань шкіри, як атопічна розладь та ускладнень, таких як остеоартрит та екзема, псоріаз, кропів'янка та алергічні реакції ревматоїдний артрит 26 25 61884 АА досить часто вважають потенційно шкідлив Матригелі та буфері DMEM В ТІЛІ кожної тваринвою жирною кислотою Але вона є важливим комки розвивалася злоякісна пухлина, розміри якої понентом усіх нормальних типів мембран, і вияввизначалися за допомогою нутромірів, а об'єм її лено, що її концентрація помітно знижується під оцінювався за ЛІНІЙНИМИ розмірами Пухлини в час протікання таких захворювань, як атопічна кожній тваринці вимірювалося ДВІЧІ на тиждень екзема, шизофренія (Horrobm et al, Schizophrenia протягом п'яти тижнів Мишей було розділено на Res 1994,13 195-207) та захворювання серцевотри групи 5 тваринок було задіяно як контрольні, судиної системи (Horrobm, Prostaglandins Leukotr їм лише давалося по 10 г/кг ваги зернової олії щоEFAs-Іефірні жирні кислоти - EFA - перекл ] 1995, дня Іншим 5 тваринкам також давали по 10 г/кг 53 385-96) АА, очевидно, можна розглядати як ваги зернової олії, але у додаток робили дві ін'єкції важливу сполуку при лікуванні таких процесів, а на тиждень складного диефіру GLA-EPA, з розратакож інших психічних захворювань, наприклад, хунку 1,5 г/кг ваги на кожну ІН'ЄКЦІЮ Цей диефір алкоголізму та розсіяної уваги, при яких, в багавводився в формі 20% емульсії, де емульсіфікатотьох випадках, відмічено низьку концентрацію в ром був 2%-ий вівсяний галактоліпід, толеранторганізмі цієї речовини DHA поділяє деякі з вказаність внутрішньовенної емульсії була дуже добних властивостей EFA, але слід відзначити, що в рою, що повністю виключало можливість гемолізу, особливо великій концентрації DHA було виявлено тромбофлебіту або будь-якого подібного нездув клітинних мембранах і, зокрема, в мембранах жання у тварин 5 мишам третьої групи замість клітин серця, сітчастої оболонки (ока) та в мемзернової олії давали 10 г/кг ваги/день того ж диебранах клітин мозку DHA також є потужним протифіру GLA-EPA Таке експериментальне лікування запальним, і дає позитивний вплив на серцевотривало три тижні, після чого пухлини продовжусудинну систему Очевидно, що DHA є особливо вали розвиватися ще два тижні перед тим, як мицінним препаратом для лікування власне серцевошей було позбавлено життя, а пухлини витято та судинних захворювань, порушень у СІТКІВЦІ ока та зважено Вага витятої пухлинної тканини була тарозладів зору, зокрема змінення у пігментації СІТКІкою в контрольній групі - 1240 ± 290 мг, в групі ВКИ, старечої плямистої деградації та дислексм, а внутрішньовенної ін'єкції GLA-EPA - 820 ± 180 мг, в також психічних та неврологічних розладів, зокрегрупі орального введення GLA-EPA - 490 ± 160 мг ма шизофренії, розсіяної уваги, депресії, алкоголіЗвідси ВИДНО, ЩО ЯК оральне, так і внутрішньовензму, хвороби Альцгеймерата інших форм деменції не введення диефіру GLA-EPA призводять до знаі розсіяного склерозу чного шпбірування розвитку пухлини без жодного побічного ефекту або нездужання поміж ПІДДОСЛІОстанні дані свідчать про те, що протікання ДНИХ тварин Це доводить ефективність викорисінфекційних хвороб також залежить від наявності тання диефіру GLA-EPA при лікуванні раку, що і та вмісту в організмі жирних кислот, особливо інбуло зпрогнозовано по результатах ДОСЛІДІВ В лафекція чутлива до GLA, ЕРА та DHA Багато бакбораторних умовах, коли GLA та ЕРА було дослітерій гине через вплив цих жирних кислот, зокрема джено роздільно на предмет їх самостійної здатбактерій спадкових інфекцій, які відрізняються виності вбивати культивовані людські ракові клітини сокою опірністю до антибіотиків Результати доТаким чином, слід ВІДМІТИТИ, ЩО диефіри є біологісліджень у багатьох лабораторіях також свідчать чно активними агентами при призначенні різних про важливість цих жирних кислот для успішної жирних кислот Отже, можна сподіватися, що заборотьби із такими захворюваннями, як малярія та вдяки диефірам буде реалізовано багато практичпротозоальні хвороби них корисних властивостей жирних кислот, які було описано в численних публікаціях в науковій Таким чином, не викликає сумніву висновок, літературі (наприклад, Horrobm DF, ed , Omega-6 що різні специфічні жирні кислоти можна додавати Essential Fatty Acids Pathophysiology and Roles in з метою підвищення ефективності впливу до преClinical Medicine Wiley-Liss, New York, 1990 паратів і бюактивних речовин майже кожного з Simopoulos AP et al, Health Effects of Omega-3 Polyкласів, що використовуються як для лікування, так unsaturated Fatty Acids in Seafoods, Karger, Basel, і для запобігання захворювань, для збереження 1991 Fats and Oils in Human Nutnon, World Health шкіри та для підживлення організму, вони також Organization, Rome, 1994 Unsaturated Fatty Acids мають велике терапевтичне значення при введенNutnonal and Physiological Significance British Nuні у формі дюлів у вигляді як одинарної жирної tnon Foundation, Chapman and Hall, London, 1992) кислоти, так і двох різних жирних кислот в одній молекулярній структурі Величезне значення для терапії має те, що у більшості випадків жирні кисСпецифіка застосування окремих 1,3-пропанлоти є нетоксичними речовинами та їх можна придюлових сполук значати у великих дозах без жодного ризику появи 1 1,3-пропан-дюл як ПОХІДНІ, ЩО МІСТЯТЬ В собі суттєвих побічних ефектів дві жирних кислоти, з яких одна жирна кислота є Як конкретний приклад терапевтичної ефективності складних диефірів можна навести таке тестування 1,3 GLA-EPA пропан-дюл-диефір було апробовано для лікування раку підшлункової залози людини (ASPC-1), який було трансплантовано підшкірно оголеним мишам, здатним внаслідок втрачення функції зобної залози сприймати ЗОВНІШНІ транспланти без відторгнення Кожній з 15 мишей було введено підшкірно 5 МІЛЬЙОНІВ ASPC1-ракових клітин, підготовлених у вигляді суспензії GLA або DGLA, а інша є GLA, DGLA, SK, ЕРА, DHA, cLA (сполучена лінолева кислота) або СА (нюбінова кислота), застосовуються для лікування (а) ускладнень діабету, зокрема патолопй нервової системи та СІТКІВКИ, також для покращення реакції на інсулін при діабеті та в попередній період, (б) ракових захворювань, (в) остеоартриту, (г) ревматоїдного артриту, 27 (д) інших запальних процесів та захворювань аутоімунної системи, зокрема синдрому Сьогрена, хронічного туберкульозу шкіри (вовчанки), виразкового коліту, хвороби Крона та увеїту, (є) респіраторних захворювань, зокрема астми, (ж) нейролопчних розладів, зокрема розсіяного склерозу, хвороби Паркінсона та хореї Хантінгтона, (з) розладів нирок та сечового тракту, (і) серцево-судинних захворювань, (к) захворювань очних тканин, зокрема пігментози очної СІТКІВКИ та старечої плямової деградації, (л) психічних розладів, зокрема шизофренії, хвороби Альцгеймера, розсіяної уваги, алкоголізму та депресії, (м) гіпертрофії передміхурової залози та простатиту, (н) імпотенції та чоловічої безплідності, (о) масталгм, (п) чоловічої ПЛІШИВОСТІ (р) остеопорозу, (с) захворювань шкіри, зокрема атопічної екземи, екземи кистей рук, псоріазу, кропивниці та алергичних розладів, (т) дислексм та інших розладів слухових органів, (у) спричиненого раком виснаження 2 1,3-пропан-дюл як ПОХІДНІ, ЩО МІСТЯТЬ В собі дві жирні кислоти, де одна жирна кислота є АА, а інша є АА, GLA, DGLA або ЕРА, застосовуються для лікування по параграфу (1), зокрема по пунктах (а), (ж), (і), (К), (Л), (С) та (т) 3 1,3-пропан-дюл як ПОХІДНІ, ЩО МІСТЯТЬ В собі дві жирні кислоти, де одна жирна кислота є ЕРА, а інша є ЕРА або DHA, застосовуються для лікування по параграфу (1), зокрема по пунктах (б), (в), (г), (д), (є), (ж), (з),(і), (к), (л), (р), (т)та(у) 4 1,3-пропан-дюл як ПОХІДНІ, де одна позиція зайнята жирною кислотою з ряду GLA, DGLA, АА, SK, сІ_А, ЕРА або DHA, а інша позиція зайнята агентом, вибраним з переліку в наступних абзацах тексту цього винаходу, хімічна структура цього агенту може бути приєднаною до 1,3-пропан-дюлу за допомогою одного з описаних зв'язків (а) триптофан для лікування будь-якого захворювання, але переважно для психічних, поведінкових розладів, болю та інших недуг, особливо депресій, розладів сну та мігрені, (б) фенілаланін для лікування будь-якого захворювання, особливо депресії, розсіяного склерозу та синдрому хронічного перевтомлення, (в) арпнин для лікування будь-якого захворювання, особливо захворювань, при яких спотворюється механізм вироблення окису азоту, (г) карнітин або ПОХІДНІ карнітину для лікування будь-якого захворювання, особливо м'язової недостатності, серцевої недостатності, синдрому хронічного перевтомлення, хвороби Альцгеймера та періферійних невропатолопй, (д) будь-яка інша амінокислота або споріднена речовина для лікування будь-якого захворювання, або амінолевулинова кислота чи и ПОХІДНІ ДЛЯ лікування будь-яких захворювань, особливо ракових, (є) аденілосукцинат або споріднені речовини 61884 28 для лікування будь-якого захворювання, особливо м'язової дистрофії, серцевої недостатності, синдрому хронічного перевтомлення та хвороби Алцгеймерата ІНШІ форми недоумкуватості, (ж) аспірин, саліцилова кислота, індометацин, ібупрофен, або будь-який інший нестероідальний протизапальний препарат для лікування будьякого захворювання, особливо запалення, що спричиняє біль, хвороби Альцгеймера та інших форм недоумкуватості, а також будь-якого захворювання, при якому необхідно шпбірувати накопичення дрібних бляшок шкідливих речовин, (з) будь-який антібютик для лікування будьяких ВІДПОВІДНИХ інфекційних захворювань, особливо тетрациклін, кліндаміцин, міноциклін, хлортетрациклін та еритроміцин для лікування прищів (запалення сальної залози), (і) будь-який протималярійний або антипротозоальний препарат для лікування будь-якого захворювання, але особливо це стосується таких препаратів, як хлороквін, мепакрин, квінакрин та мефлоквін для лікування малярії, протозоальних розладів, запальних процесів та шизофренії, (к) будь-який протигрибковий препарат для лікування будь-якого захворювання, особливо це стосується таких препаратів, як метронідазол та протигрибкові імидазоли, а також нітроімидазоли та амфотеріцин для лікування грибкових інфекцій різних типів, (л) будь-який протизапальний стероїд для лікування будь-якого захворювання, особливо це стосується гідрокортизону та бетаметазону для лікування подразнень шкіри, а також беклометазону та будезониду для лікування астми, (м) будьякий гонадальний стероїд для лікування будьякого захворювання, особливо це стосується естрогенів та прогестогенів для лікування маткової недостатності та остеопорозу, а також андрогенів для лікування яєчкової недостатності, (н) будь-який адреностероїд для лікування будь-якого захворювання, особливо депдроепіандростерон для лікування розладів організму, пов'язаних із процесами старіння, (о) будь-який ретиноїд для лікування будьякого захворювання, особливо це стосується третиноіну та ізотретиношу для лікування подразнень шкіри, а також для догляду за шкірою, (п) будь-який протираковий агент для лікування раку, (р) будь-який агент для лікування шизофренії та інших форм психозу, (с) будь-який протидепресійний агент для лікування будь-якого захворювання, особливо для лікування власне депресії, (т) будь-який агент для лікування будь-якого захворювання, перш за все спричиненого тривожним синдромом та манією переслідування, (у) будь-який імуностримуючий агент для лікування будь-якого захворювання, але особливо циклоспорин та такролімус для підтримання контролю за станом імунної системи після трансплантування органів, а також для лікування розладів аутоімунного та запального характеру, зокрема псоріазу, екземи, астми, ревматоїдного артриту та запальних процесів у нутрощах, зокрема в шлунково-кишковому тракті, (ф) будь-який інгібітор нагнітання активних 29 протонів або Н2-антагоніст для лікування будьякого захворювання, особливо таких захворювань, які пов'язуються із надлишковим виділенням шлункової кислоти або із зниженою захисною реакцією проти надмірної шлункової кислотності, (х) будь-який сечогінний препарат для лікування будь-якої хвороби, перш за все для захворювань, пов'язаних із затримкою сечі та надмірним тиском унирково-сечовій системі, (ц) будь-який препарат - антагоніст кальцію для лікування будь-якого захворення, особливо захворювань, пов'язаних із серцево-судинною системою, (ч) будь-який ферментний інгібітор, що перетворює анпотензин, або антагоніст анпотензину, для використання в лікуванні будь-якого захворювання, особливо серцево-судинного, (ш) будь-який бета-пасиватор (бетаблокиратор) для лікування будь-яких захворювань, особливо серцево-судинних, (щ) будь-який протиепілептичний препарат для лікування будь-якої хвороби, особливо це стосується фенитошу, карбамазепину, вальпроату, етосукциміду, вігабатрину або ламотрипну для лікування епілепсії, (я) будь-який пполіпідемовий агент для лікування будь-якого захворювання, особливо це стосується фібратів і статинів, здатних знизити рівень холестерину та модифікувати його, (аа) будь-які ппогліцемові агенти, що вводяться оральним шляхом і підвищують чутливість до інсуліну, і які використовуються для контролю за протіканням діабету, (бб) будь-які біфосфонати, що використовуються для контролю за протіканням остеопорозу, хвороби Пагета та раку, (вв) будь-які контрастні агенти, що використовуються в радіологи, зокрема сполуки диатризоату, юдипамиду, югліцамати, юпаноати, юфендилат, юталамат, юксаглат, метризамід та споріднені сполуки, (гг) будь-який пептид або протеїн для такого лікування захворювань, коли використовуються власне пептид або протеїн, зокрема інсулін, кальцитонин, еритропоіетин та ІНШІ пептиди, (дд) будь-який вітамін, що використовується для лікування будь-якої хвороби, або додається до харчових продуктів, живильних або харчових добавок, завдяки застосуванню яких цей вітамін краще засвоюється, (ее) будь-який антиоксидант, що використовується для контролю за протіканням будь-яких захворювань, особливо таких, при яких антиоксиданти є життєво необхідними сполуками, зокрема серцево-судинні, ракові та запальні процеси, будьякий антиоксидант, що використовується як харчовий продукт, або як компонент продукту, живильна чи харчова добавка, (жж) будь-який порфіриновий хлорин або препарат на основі бактерюхлорину, особливо їх тетракіс(пдроксифеніл)-похідні, що використовуються в фотодинамічній терапії раку Легкість синтезування в порівнянні з тригліцеридами Синтез тригліцеридів Наступний розділ ілюструє переваги викорис 61884 30 тання 1,3-пропан-дюлу,зокрема у порівнянні з тригліцеридами Пропонується застосовувати 1,3-пропан-дюл замість гліцерину при етерифікації жирних кислот, особливо у випадку, коли до вуглецьтрьохатомного ланцюгового "хребта" молекули приєднується лише один тип жирної кислоти (наприклад, ліноленова кислота) Хоча складні диефіри та тригліцериди є дуже подібними ХІМІЧНО, виробництво диефірів може здійснюватись за дуже обумовлених технологічних вимог, і кінцевий результат може бути одержано за лічені години Виготовлення тригліцеридів вимагає більш складних технологічних умов, а також застосування хлоридів жирних кислот або бюкаталізаторів (реакція виготовлення у такому випадку триває кілька тижнів) СТИСЛО методику синтезування тригліцериду можна охарактеризувати так хімічна реакція з металами, хлоридами металів або органічними кислотами як каталізаторами, використання хлоридів жирних кислот, використання зафіксованих ферментів (ензимів) Всі процеси із використанням кислот, металів або хлоридів металів як каталізаторів дуже подібні і мають стандартний перелік переваг та недоліків Багато проблем спричинені специфічністю методики, наприклад, кислотними умовами та високими температурами (від 140°С до 180°С) протікання реакцій Застосування методики p-TSA можливо, зводить проблеми до мінімуму, оскільки вона передбачає найобмірковані для відомих технологій такого типу умови (140°С) Реакція гліцерину із хлоридами жирних кислот здійснюється в "холодному" стані, але під час м протікання виділяються токсичні гази, і крім того без ретельного нагляду можна утратити над такою реакцією контроль Ця методика передбачає, що по-перше мають бути виготовлені власне хлориди жирних кислот - додаткова процедура, яка негативно впливає на ефективність цілого процесу Для каталізу реакції за дуже м'яких умов (близько 60°С) може бути використано специфічний ряд ферментів, що їх названо ліпази, а при використанні поліненасичених жирних кислот є можливий вибір каталізаторів Але слід відзначити, що більшість ензимів найефективнішим чином взаємодіють із 1- та 3позиціями гліцерину Додавання жирної кислоти до 2-позицм відбувається повільно і часто залежить від "ацилової міграції", тобто жирна кислота поперше має бути приєднаною до 1- чи 3- позиції, після чого вона мігрує до 2-позицм, де і залишається ХІМІЧНО приєднаною до молекули Таким чином, як вже нотувалося раніше, реакція синтезу тригліцериду, каталізаторами якої є ензими (ферменти), може тривати до и остаточного завершення чимало днів Теоретично для етерифікації 1,3пропан-дюлу може бути застосовано ту ж саму методику, як і для гліцерину Однак, якщо звернути увагу на те, що ензими каталізують переважно приєднання жирних кислот до 1- та 3- позицій гліцерину, стає очевидним вийняткова ефективність цих ензимів при виготовленні складних диефірів І дійсно, реакція може бути повністю завершеною за лічені години при навіть ще нижчих температурах (від 45°С ДО 60°С), НІЖ ТІ, ЩО Є потрібними для синтезу тригліцериду По чотирьох годинах жирна 32 31 61884 кислота зникає з реакції, а після восьми годин виВода 100,00 хід диефіру може перевищувати 95%, решта об'Емульгатор-галактоліпід було було диспергоєму займає моноефір вано в диефірі та перемішано з вітаміном Е, АП та водою Масляну фазу додавали до фази водного Додаткові ускладнення при синтезуванні трирозчину за допомогою сильнодіючого механічного гліцериду обумовлені наявністю в молекулі гліцезмішувача (Ultraturrax) при швидкості 4 протягом рину як первинних, так і вторинних гідроксильних кількох хвилин Після ТОГО ЦЮ напів-емульсію було груп, а також прохірального центру (центральний гомогенізовано під тиском 80Мпа при температурі атом вуглецю) Такі проблеми можна вирішити 50°С за 6 циклів (міні-лаборатоторія 8 ЗО Н, APV шляхом використання старанно підібраних захиRanme AS, Данія) Середній розмір елементарних щуючих груп та синтезуванням хіральних центрів краплинок в здобутій емульсії становив близько Але це призводить до надмірної багатостадійності 230нм До цієї оральної емульсії також було добасинтезу, що значно зменшує ефективний вихід та влено сорбат калію та присмаки збільшує рівень вмісту зайвих ДОМІШКІВ за рахунок їх сумування на кожній стадії Навпаки, 1,3-пропан2 Виготовлення 20%-воі емульсії диефіру дюл містить лише одну первинну гідроксильну GLA та ЕРА із 1,3-пропан-дюлом для внутрішньогрупу та зовсім не має прохіральних центрів ВІДвенного введення в організм ПОВІДНО процес синтезування скорочується до Аналогічним способом було вигитовлено 200г двох стадій (максимум), при цьому підвищується масляно-водної емульсії, що містить такі компонеефективність корисного виходу та знижується рінти вень небажаних ДОМІШКІВ Компоненти % ПІДВОДЯЧИ підсумок, слід відзначити, що реакЕмульгатор 2,00 ція здобування складних диефірів з поліненасичеДиефір (GLA-EPA) 20,00 них жирних кислот та 1,3-пропану протікає скоріше Гліцерин 2,0 та за більш м'яких умов, ніж ті, що є необхідними Вода 100,00 для відповідної за масштабами реакції синтезу Ця емульсія, яку було гомогенізовано під висотригліцериду ким тиском протягом 6 хвилин, складалася з елементарних краплинок із середнім розміром 211нм, Фармацевтичний пропис цета-потенціалом - 40 мВ Здобуту емульсію було Фармацевтичний пропис сполук може бути або профільтровано через мембрану з розміром складено в будь-якій зручній формі, що є прийнятпори 0,22 мікрона, або оброблено в автоклаві із ною для фахівців з виготовлення лікарських засозміною розміру краплинок бів, препаратів для догляду за станом шкіри та харчових добавок, їх можна вводити оральним Дози активних речовин, що їх може бути ввешляхом, через тонкокишковий тракт, поверхнево, дено в організм, змінюються в широкому діапазоні парентерально (підшкірне, внутрішньом'язовим та від 1мг до 200г на добу, оптимально вони можуть внутрішньовенним шляхом), через пряму кишку, становити від 10 мг до 10 г (найбільш оптимальні вапнальним шляхом або будь-яким іншим прийнявід 10 мг до 3 г), у ВІДПОВІДНОСТІ до їх типу При тним способом лікуванні раку оптимальні дози можуть становити від 2 до 150 г на добу По ситуації ці емульсії моПодібно тригліцеридам, складні диефіри'.Зжуть використовуватися поверхнево-локально в пропан-дюлу, особливо ті, що містять в собі дві препаратах, де активних речовин локального прижирних кислоти, можуть бути без ускладнень емузначення міститься від 0,001% до 50%, оптимальльговані за допомогою фосфоліпідних або, ще но від 0,05 % до 20% і найбільш оптимально від краще, галактоліпідних емульгаторів Такі емульсії 0,1% до 10% є переважно зручними для введення в організм Приклади оральним, тонкокишковим та внутрішньовенним шляхами Синтез нестероідних протизапальних препаратів (NSAID), ХІМІЧНО приєднаних до жирних кисНаприклад, складні диефіри жирної кислоти лот, було висвітлено в опублікованому ЕРА-0 675 (НЖК) зустрічаються в практиці у вигляді вільної 103, на який автори цього винаходу вже посилалирозливної масляної речовини, отже, їх можна фася раніше Висвітлення синтезування ХІМІЧНОГО рмацевтичне прописати таким способом зв'язку жирних кислот через 1,3-пропан-дюловий 1 Виготовлення 20%-воі емульсії диефіру радикал-залишок пропонується нижче у тексті, GLA та ЕРА із 1,3 -пропан-дюдом Емульсії для разом із іншим загальним ілюстративним матеріапризначення оральним шляхом виготовляються за лом допомогою гомогенізації під високим тиском Розподіл розмірів частинок та цета-потенціал резульПриклад 1 тативних емульсій було визначено за допомогою 1,3-(flH-z,z,z-OKTafleKa-6,9,12методу динамічного розсіювання світла при кімнатриенойлокси)пропан тній температурі Вимірювання бляшок було вико(Диефір GLA із 1,3-пропан-дюлом) нано при кімнатній температурі (Zetasizer 4 MalРозчин 1,3-дициклогексилкарбодмміду (1,07г) vern Instruments Limited) Було виготовлено та 4-(г\І,г\І-диметиламшо) піридину (0,59 г) в метимасляно-водну емульсію (порція 200 г), що містить ленхлориді (5 мл) було добавлено до розчину 1,3в собі такі компоненти дипдроксипропану (0,152 мл) та г,г,г-октадека6,9,12-триеновоі кислоти (95%, 1,36 г) в метиленКомпоненти % хлориді (15 мл) Суміш реакції перемішували при Емульгатор (Галактоліпід)* 2,00 кімнатній температурі під штучно створеною азоДиефір (GLA-EPA) 20,00 тною атмосферою до повного розчинення, яке Аскорбил Пальмітат (АП) 0,02 було визначено за допомогою доданого до реакції Вітамін Е 0,5 34 33 61884 ХТШ [хроматографія тонких шарів]-гексану (80 мл) Приклад 5 Осад було видалено шляхом фільтрування та ре(±)-1 -(1,2-дитиолан-3-пентанойлокси)-3-(г,2,2тельно промито гексаном Комбіновані фільтрати октадека-6,9,12-триенойлокси)пропан було концентровано та очищено за допомогою (Диефір ЛІПОВОІКИСЛОТИ та GLA із 1,3-пропаноднократної (миттєвої) хроматографії, після чого дюлом) на виході отримано 1,3-(flH-z,z,z-OKTafleKa-6,9,12Суміш 1,3-дициклогексилкарбодмміду (720 мг, триенойлокси)пропан у вигляді блідо-жовтої вільно 3,45 ммол) та 4-(г\І,г\І-диметиламіно)піридину (480 розливної масляної речовини мг, 3,98 ммол) в ефірі трет-бутил-метилу (15 мл) було добавлено до суміші ліпової кислоти (645 мг, Приклад 2 3,12 ммол) та 1-(z,z,z-OKTafleKa-6,9,121-(г,г,г-октадека-6,9,12-триенойлокси)-3-(гтриенойлокси)-3-пдроксипропану (1 г, Зммол) в октадека-9-енойлокси)пропан, ефірі трет-бутил-метилу (ЗО мл) Суміш було ви(Диефір GLA та олеїнової кислоти із 1,3тримано при кімнатній температурі під азотною пропан-дюлом) атмосферою протягом 5 годин, розвиток реакції Частина 1 контролювалося за допомогою ХТШ (40% етилаРозчин г,г,г-октадека-6,9,12-триеновоі кислоцетат/гексан) По закінченні реакції суміш було ти (150 г) в метиленхлориді (500 мл) було по краппрофільтровано, концентровано та очищено за линах добавлено до суміші 1,3-дипдроксипропану допомогою однократної (миттєвої) хроматографії (205 г), 1,3-дициклогексилкарбодмміду (130 г) та 4(гексан, 2% етилацетат/гексан, 5% етилаце(г\І,г\І-диметиламіно)піридин (87 г) в метиленхлоритат/гексан і наприкінці 10% етилацетат/гексан), на ді (2500 мл) при кімнатній температурі під азотною виході здобуто (±)-1 -(1,2-дитиолан-Затмосферою Коли тонкошарова хроматографія показала, що реакція відбулася повністю, суміш пентанойлокси)-3-(г,2,2-октадека-6,9,12реакції було профільтровано Фільтрат промили триенойлокси)пропан у вигляді в'язкої жовтої масрозведеною соляною кислотою, водою насиченим ляної речовини розчином хлориду натрію Розчин було висушено, Приклад 6 концентровано та очищено за допомогою сухої 1 -([7]-5-фторо-2-метил-1 -[4колонкової хроматографії, на виході було отрима{метилсульфінил}бнзиліден]шден-3-ацетилокси)-3но 1-(г,г,гг-октадека-6,9,12-триенойлокси)-3(г,2,2-октадека-6,9,12-триенойлокси)пропан (Диепдроксипропан у вигляді блідо-жовтої масляної фір суліндакової кислоти та GLA із 1,3-пропанречовини дюлом) Розчин 1,3-дициклогексилкарбодмміду (720 мг, 3,45 ммол) в трет-бутилметиловому ефірі Частина 2 (ЗО мл) було добавлено до суміші суліндаку (1,12 Розчин 1,3-дициклогексилкарбодмміду (23,7г) г, 3,15 ммоло), 4-(г\І,г\І-диметиламшо)тридину (480 та 4-(г\І,г\І-диметиламіно)піридину (15,9 г) в метимг, 3,9 ммол) та 1-(z,z,z-OKTafleKa-6,9,12ленхлориді (200 мл) було добавлено до розчину 1триенойлокси)-3-пдроксипропану (1 г, 3 ммол) в (2,2,2-октадека-6,9,12-триенойлокси)-3трет-бутилметиловому ефірі (15 мл) Суміш було пдроксипропану (33,6 г) та г-октадека-9-еновоі перемішано та витримано при кімнатній темперакислоти (30г) в метиленхлориді (400 мл) під азотурі під азотом протягом 5 годин, розвиток реакції тною атмосферою при кімнатній температурі По контролювалося за допомогою ХТШ (40% етилазавершенні реакції, що було підтверджено ХТШцетату/гексан) По завершенні суміш було профіаналізом, здобутий розчин було розведено у гекльтровано, концентровано та очищено за допомосані, профільтровано, концентровано та очищено гою однократної (миттєвої) хроматографії (40% за допомогою сухої хроматографії, на виході етилацетат/гексан, далі 50% етил ацетат/гексан та отримано 1-(г,2,2-октадека-6,9,12-триенойлокси)наприкінці 60% етилацетат/гексан), на виході 3-(г-октадека-9-енойлокси)пропан у вигляді блідоотримано 1-([7]-5-фторо-2-метил-1-[4жовтої вільно розливної масляної речовини Приклад З 1,3-(ди-2,2,г-октадека-6,9,12-триенойлокси)-3(z,z,z,z,z^KO3a-5,8,11,14,17-neHTaeHOKCH)nponaH (Диефір GLA та ЕР А із 1,3-пропан-дюлом) Виготовлення є аналогічним прикладу 2, частина 2, але із заміною г-октадека-9-еновоі кислоти г,г,г,г,г-ейкоза-5,8,11,14,17-пентаеновою кислотою На виході хроматографія показала 1,3-(диейкоза-5,8,11,14,17-пентаенокси)пропан у вигляді блідо-жовтої масляної речовини Приклад 4 1,3-flH(z,z,z-OKTafleKa-6,9,12триенойлокси)пропан (Диефір GLA із 1,3-пропандюлом) Виготовлено як у прикладі 2, частина 2, але із заміною г-октадека-9-еновоі кислоти z,z,zоктадека-6,9,12-триеновою кислотою На виході хроматографія показала 1,3-ди(г,г,г-октадека6,9,12-триенойлокси) пропан у вигляді блідожовтої речовини {метилсульфінил} бензиліден]інден-3-ацетилокси)3-(z,z,z-OKTafleKa-6,9,12-триенойлокси) пропан у вигляді парафінистої (подібної до воску) жовтої твердої речовини Приклад 7 1-([ТЇ]-3-ацетокси-4[триметиламоню]бутиройлокси)-3-(г,г,г-октадека6,9,12-триенойлокси)пропан (Диефір ацетил карнитину та GLA із 1,3пропан-дюлом) Свіжодистильований тионілхлорид (1,5мл) повільно додавали до (Р)-ацетилкарнітину (лігроіру) в грушоподібній колбі Під час реакції уважно слідкували затим, щоб реагенти локалізувалися на дні колби, до моменту здобуття прозорого розчину Через 4 години після початку реакції при кімнатній температурі надлишковий тионілхлорид було видалено під зниженим тиском (зберігаючи температуру розчину в колбі не вище за 30°С) Таким чином, на виході було здобуто хлорангідрид у вигляді високопгроскопічної білої твердої речови 36 35 61884 ни, яку тут же було використано без додаткового зібрано після відстоювання та концентровано, на виході остаточно здобуто 1-(г,г,г-октадека-6,9,12ОЧИЩеННЯ ДО КОЛбИ буЛО ДОЛИТО 1-(flH-Z,Z,Zтриенойлокси)-3-(1-(4-хлоробензойл)-5-метокси-2октадека-6,9,12-триенойлокси)-3-пдроксипропан метил-шдол-3-ацетилокси)пропан у вигляді яскра(1,4 г, 4,17 ммол) та добавлено сухий тетрапдрово-жовтої в'язкої масляної речовини фуран (ТГФ) (4 мл) Суміш було залишено відстоюватися на ніч при кімнатній температурі ХромаПриклад 10 тографічний аналіз (40% етил ацетат/гексан) 1-(г,2,2-октадека-6,9,12-триенойлокси)-3-(2показав, що реакція відбулася повністю Суміш піролідин карбокси)пропан реакції по краплинах додавалося до гексану (250 (Диефір проліну та GLA із 1,3-пропан-дюлом) мл) при енергійному перемішуванні Утворився Частина 1 тонкозернистий осад, який було зібрано за допо1,3-дициклогексилкарбодмміду (674 мг, 3,3 могою центрифугування По видаленні шару, що ммол) та 4,4-(г\І,г\І-диметиламіно)піридин (472 мг, виявився зверху після відстоювання, здобуту тве3,9 ммол) в метилен хлориді (20 мл) було додано рду фракцію було знов перетворено на суспензію при помішуванні до розчину 1-(z,z,z-OKTafleKaв гексані та центрифуговано Після цього ще раз 6,9,12-триенойлокси)-3-пдроксипропану (1 г, 2,97 було виконано процедуру промивки гексаном та на ммол) та N-tBOC-пролшу (671 мг, 3,12 ммол) в виході остаточно здобуто 1-([Р]-3-ацетокси-4метиленхлориді (20 мл) при кімнатній температурі [триметиламоню]бутиройлокси)-3-(г,г,г-октадекапід азотом Помішування тривало 7 годин, після 6,9,12-триенойлокси)пропан чого суміш було залишено на ніч при температурі 0°С Суміш було профільтровано та очищено за Приклад 8 допомогою колонкової хроматографії (мета1-(3,3-диметил-7-оксо-6нол/метиленхлорид), на виході здобуто 1-(z,z,z([феноксиацетил)амшо]-4-тиа-1октадека-6,9,12-триенойлокси)-3-(г\І-1ВОСазабіцикло[3 2 0]гептан-2-ойлокси)-3-(г,2,2піролідин карбокси)пропан у вигляді жовтої масляоктадека-6,9,12-триенойлокси)пропан ної речовини (Диефір пеніциліну V ma GLA із 1,3-пропандюлом) Суміш пеніциліну V (1г, 2,9 ммол), 1-(z,z,zоктадека-6,9,12-триенойлокси)-3-пдроксипропану (860 мг, 2,6 ммол), 1,3-дициклогексилкарбодмміду (620 мг, 3 ммол) та 4-(г\І,г\І-диметиламіно)піридину (в об'ємі каталізатора) в дихлорометані (ЗО мл) перемішувалося та було залишено на ніч при кімнатній температурі Суміш реакції було після цього розведено із гексаном (50 мл), профільтровано та концентровано до сухості Залишок було промито гексаном (3 х 50 мл) для видалення решти 1 -(z,z,zоктадека-6,9,12-триенойлокси)-3-пдроксипропану, що не вступило в реакцію Напівтвердий залишок було розчинено в диетилефірі (150 мл), промито водою (100 мл) та висушено Ефірний розчин розводили в гексані (125 мл), після чого розчин було профільтровано через кремнієвий шар (4 см х 4 см) Фільтрат було концентровано, і на виході здобуто 1-(3,3-диметил-7-оксо-6([феноксиацетил)амшо]-4-тиа-1азабіцикло[3 2 0]гептан-2-ойлокси)-3-(г,г,гоктадека-6,9,12-триенойлокси)пропан у вигляді в'язкої рідини, що не має кольору Приклад 9 1 -(z,z,z-OKTafleKa-6,9,12-триенойлокси)-3-(1 -(4хлоробензойл)-5-метокси-2-метил-шдол-3ацетилокси)пропан (Диефіріндометацину та GLA із 1,3-пропандюлом) Розчин 1,3-дициклогексилкарбодмміду (58 г, 0,28 мол) та 4-(г\І,г\І-диметиламіно)піридину (37,9 г, 0,31 мол) в метиленхлориді (800 мл) було добавлено при помішуванні до розчину 1-(z,z,zоктадека-6,9,12-триенойлокси)-3-пдроксипропану (79,5 г, 0,24 мол) та індометацину (93,2 г, 0,26 мол) в метиленхлориді (400 мл) при кімнатній температурі під штучно створеною азотною атмосферою Помішування тривало 3 годин Суміш було профільтровано, концентровано та очищено за допомогою сухої колонкової хроматографії (етиацетат/гексан) Фракції здобутого продукту було Частина 2 ХІМІЧНО захищений продукт першої частини реакції було розчинено в 10% анизол^рифторооцтовій кислоті (10 мл) і залишено при кімнатній температурі під азотом на ЗО хвилин Після проведення аналізу ХШТ, яке показало, що депротекція відбулася повністю, суміш було очищено за допомогою колонкової хроматографії (8% метанол/42 %метиленхлорид/50% етилацетат), на виході здобуто 1-(г,г,г-октадека-6,9,12триенойлокси)-3-(2-піролідин карбокси)пропан у вигляді в'язкої речовини жовтогарячого кольору Приклад 11 1-(г,2,2-октадека-6,9,12-триенойлокси)-3-(2амшо-3-шдолілпропанойлокси)пропан (Диефір триптофану та GLA із 1,3-пропандюлом) Частина 1 Розчин 1,3-дициклогексилкарбодмміду (674 мг, 3,3 ммол) та 4-(г\І,г\І-диметиламіно)піридину (472 мг, 3,9 ммол) в метиленхлориді (20 мл) було добавлено при помішуванні до розчину 1-(z,z,zоктадека-6,9,12-триенойлокси)-3-пдроксипропану (1 г, 2,97 ммол) та N-tBOC-триптофану в метиленхлориді (20 мл) при кімнатній температурі під азотом Помішування тривало 7 год, після чого суміш було залишено на ніч при температурі 0°С Суміш було профільтровано та очищено за допомогою колонкової хроматографії (метанол/метиленхлорид), на виході здобуто 1-(z,z,zоктадека-6,9,12-триенойлокси)-3-(г\І-1ВОС-2-амшо3-шдолілпропанойлокси) пропан у вигляді жовтої масляної речовини Частина 2 ХІМІЧНО захищений продукт було розчинено в 10% анізолл'рифторооцтовій кислоті (6,1 мл) та залишено при кімнатній температурі під азотом на 15 хвилин Після хроматографічного аналізу, котрий виявив, що депротекція відбулася повністю, суміш було очищено за допомогою колонкової хроматографії (8% метанол/42% метиленхлори 37 61884 ду/50% етилацетату), на виході здобуто 1-(z,z,zоктадека-6,9,12-триенойлокси)-3-(2-амшо-3індолілпропанойлокси) пропану у вигляді в'язкої парафінистої речовини червоного кольору Приклад 12 1-(2,2,2-октадека-6,9,12-триенойлокси)-3-(аамшо-р-феніл-пропюнилокси)пропан (Диефір фенілаланіну та GLA із 1,3-пропандюлом) Частина 1 Розчин 1,3-дициклогексилкарбодмміду (1,77 г, 8,57 ммол) та 4-(г\І,г\І-диметиламіно)піридину (1,24 г,10,13 ммол) в метиленхлориді (ЗО мл) було добавлено при помішуванні до розчину 1-(z,z,zоктадека-6,9,12-триенойлокси)-3-пдроксипропану (2,62 г, 7,79 ммол) та N-tBOC-фенілаланшу (2,17 г, 8,18 ммол) в метиленхлориді (ЗО мл) при кімнатній температурі під азотом Помішування тривало 7 год, після чого суміш було залишено на ніч при температурі 0° С Далі суміш було профільтровано та очищено за допомогою колонкової хроматографії, на виході здобуто 1-(г,г,г-октадека-6,9,12триенойлокси)-3-(г\І-1ВОС-а-амшо-р-фенілпропюнілокси) пропан у вигляді жовтої масляної речовини Частина 2 ХІМІЧНО захищений продукт було розчинено в 10% анизолл'рифторооцтовій кислоті (17 мл) та залишено при кімнатній температурі під азотом на ЗО хвилин Після хроматографічного аналізу, який виявив, що депротекція відбулася повністю, суміш було очищено також за допомогою колонкової хроматографії (8% метанол/42%метиленхлорид/50% етилацетат), на виході здобуто 1-(z,z,z-OKTafleKa-6,9,12триенойлокси)-3-(а-амшо-р-фенілпропюнілокси)пропан у вигляді в'язкої масляної речовини жовтого кольору Приклад 13 1-(г,г,г-октадека-6,9,12-триенойлокси)-3-(4аміно бутанойлокси)пропан (Диефір аміномасляної кислоти (GABA) та GLA із 1,3-пропан-дюлом) Частина 1 Розчин 1,3-дициклогексилкарбодмміду (0,84 г, 4,06 ммол) та 4-(г\І,г\І-диметиламіно)піридину (0,59 г, 4,79 ммол) в метиленхлориді (10 мл) було добавлено при помішуванні до розчину 1-(z,z,zоктадека-6,9,12-триенойлокси)-3-пдроксипропану (1,24 г, 3,69 ммол) та N-tBOC-GABA (0,75 г, 3,69 ммол)в метиленхлориді (15 мл) при кімнатній температурі під азотом Помішування тривало 7 год, після чого суміш було залишено на ніч при температурі 0°С Далі суміш було профільтровано та очищено за допомогою колонкової хроматографії (етилацетат/гексан), на виході було здобуто 1(г,г,г-октадека-6,9,12-триенойлокси)-3-г\І-1ВОС-4амшобутанойлокси)пропан у вигляді безбарвної масляної речовини Частина 2 ХІМІЧНО захищений продукт було розчинено в 10% анизолл'рифторооцтовій кислоті (10,5 мл) та залишено при кімнатній температурі під азотом на ЗО хвилин Після проведення хроматографічного аналізу, котрий виявив, що депротекція відбулася повністю, суміш було очищено за допомогою ко 38 лонкової хроматографії (8% метанол, 42% метиленхлорид/50% етилацетат), на виході було здобуто 1-(г,2,2-октадека-6,9,12-триенойлокси)-3-(4аміно бутанойлокси)пропан у вигляді масляної речовини жовтого кольору Приклад 14 3,3'-тио-ди-(1-пропіонилокси-(3-(2,2,2-октадека6,9,12-триенилокси)-пропан)) (Подвійний складний ефір GLA та 1,3-пропандюл із 3,3'-тиодипропюновою кислотою) Розчин 1,3-дициклогексилкарбодмміду (660 мг, 3,22 ммол) та 4-(І\І,г\І-диметиламіно)піридину (445 мг, 3,64 ммол) в метиленхлориді (10 мл) було добавлено при помішуванні до розчину 1-(z,z,zоктадека-6,9,12-триенилокси)-3-пдроксипропану (940 мг, 2,8 ммол) та 3,3'-тюдипропюновоі кислоти (250 мг, 1,4 ммол) в метиленхлориді (ЗОмл) при кімнатній температурі під азотом Помішування тривало 4 год Суміш було розбавлено гексаном (50 мл), профільтровано, концентровано та очищено за допомогою однократної хроматографії (етилацетат/гексан) Фракції продукту було після цього виділено та концентровано, на виході здобуто 3,3'-тио-ди-(1-пропюншюкси-(3-(г,г,г-октадека6,9,12-триенилокси)-пропан)) у вигляді безбарвної масляної речовини Приклад15 1 -(1 -(z,z,z-OKTafleKa-6,9,12-триенойлокси)-3пропіл)-4-(г,г,г-октадека-6,9,12-триенил)бутан-1,4диоат (Диефір (моноефіру GLA із 1,3-пропан-дюлом) та спирту GLA із янтарною кислотою) Частина 1 Суміш 1-(г,2,2-октадека-6,9,12-триенойлокси)3-пдроксипропану (10 г, ЗОммол) та ангідрид янтарної кислоти (3 г, ЗОммол) в сухому тетрапдрофурані (THF) (100 мл) помішувалося при кімнатній температурі доти, поки розчин не став прозорим Цей розчин було охолоджено до 0°С, після чого до нього по краплинах добавляли розчин 1,8диазабіцикло[5,4 0]ундек-7-ену (4,5 мл, ЗО ммол) в сухому THF (50 мл) Через три години хроматографічний аналіз показав, що більша частина моноефіру вже прореагувала До суміші було додано ще декілька кристалів ангідриду янтарної кислоти, після чого наступні ЗО хвил розчин помішували Суміш реакції було розбавлено диетиловим ефіром (250 мл) і промито 2М хлороводневою (соляною) кислотою (2 х 250 мл), водою (250 мл) та соляним розчином (250 мл) Після ЦЬОГО продукт було висушено (сульфат натрію) та концентровано до сухості Далі матеріал використовували без жодного додаткового очищення Частина 2 Оксалілхлорид (3,9 мл, 45 ммол) було додано до розчину продукту першої частини реакції (13 г, ЗО ммол) в метиленхлориді (75 мл) Суміш помішували при кімнатній температурі під азотом протягом 2 год , після чого її було концентровано до сухості Далі додавали гексан (75 мл) і знову концентрували продукт до сухості Цю процедуру було повторено ДВІЧІ, з додаванням кожний раз також по 75 мл гексану Далі матеріал використовували без жодного додаткового очищення 39 61884 Частина З Розчин здобутого в другій частині реакції хлорангідриду (1 г, 2,2 ммол) в метиленхлориді (10 мл) по краплинах додавали до розчину z,z,zоктадека-6,9,12-триенолу (635 мг, 2,4 ммол), триетиламшу (1 мл, 7,2 ммол) та 4-(N,Nдиметиламшо)піридину (в об'ємі каталізатора) в метиленхлориді (20 мл) при кімнатній температурі По закінченні реакції суміш було концентровано та очищено за допомогою однократної хроматографії (етилацетат/гексан), на виході здобуто 1-(1-(z,z,zоктадека-6,9,12-триенойлокси)-3-пропіл)-4-(г,г,гоктадека-6,9,12-триенил)бутан-1,4-диоат у вигляді безбарвної масляної речовини Приклад 16 1-(2,3,5-триіодобензойлокси)-3-(2,2,г-октадека6,9,12-триенойлокси)пропан (Диефір 2,3,5-триюдобензойноікислоти та GLA із 1,3-пропан-дюлом) 2,3,5-Триюдобензойлхлорид (1,54 г, 3,08 ммол) було добавлено до суміші 1(г,2,2-октадека-6,9,12-триенойлокси)-3пдроксипропану (1 г, 2,97 ммол) та триетиламшу (1 мл) в метиленхлориді (80 мл), після чого результативну суміш помішували при кімнатній температурі під азотом протягом ночі Далі суміш було концентровано та очищено за допомогою однократної хроматографії (етилацетат/гексан), на виході здобуто 1-(2,3,5-триіодобензойлокси)-3-(г,2,2октадека-6,9,12-триенойлокси)пропан Приклад 17 (±)-1 -(1,2-дитиолан-3-пентанойлокси)-3(z,z,z,z,z,z-flOKO3a-4,7,10,13,16,19гексаенойлокси)пропан (Диефір GLA таліпоідноікислоти із 1,3-пропандюлом) Частина 1 Розчин z,z,z,z,z,z-flOKO3a-4,7,10,13,16,19гексаенова кислота (6,4 г, 19,5 ммол) в метиленхлориді (225 мл) по краплинах додавали до розчину 1,3-пропан-дюлу (7,5 г, 99 ммол), 1,3дициклогексилкарбодмміду (4,65 г, 20 ммол) та 4(г\І,г\І-диметиламіно)піридину (2,1 г, 17 ммол) в метиленхлориді (225 мл) при температурі -10°С Суміш реакції помішували протягом ночі, поступово підвищуючи температуру до кімнатної Продукт реакції було профільтровано, концентровано та очищено за допомогою однократної хроматографії (етилацетат/гексан), на виході здобуто 1(г,г,г,г,г,г-докоза-4,7,10,13,16,19-гексаенойлокси)3-пдроксипропан у вигляді блідо-жовтої масляної речовини Частина 2 Розчин 1,3-дициклогексилкарбодмміду (720 мг, 3,45 ммол) та 4-(г\І,г\І-диметиламіно)піридину (480 мг, 3,9 ммол) в метиленхлориді (ЗО мл) було добавлено до суміші 1-(z,z,z,z,z,z-flOKO3a-4, 7, 10, 13, 16, 19-гексаенойлокси)-3-пдроксипропану (1,16 г, З ммол) із ЛІПОІДНОЮ кислотою (645 мг, 3,12 ммол) та метиленхлориду (15 мл) За 2,5 год після цього суміш було профільтровано при кімнатній температурі під азотом, концентровано та очищено за допомогою однократної хроматографії (етилацетат/гексан), на виході здобуто (±)-1-(1,2-дитиолан3-пентанойлокси)-3-(г,г,г,г,г,г-докоза4,7,10,13,16,19-гексаенойлокси) пропан у вигляді масляної речовини жовтого кольору 40 Приклад 18 MeTHn-flH(z,z,z-OKTafleKa-6,9,12триенойлоксипропіл)-фосфат (Фосфотриефір 2 молекул складного 3пдроксипропіл-ефіру GLA та 1 молекули метанолу) Частина 1 Триетиламш (3,74 мл, 26,8 ммол) додавали по краплинах до охолодженого (0°С) розчину свіжодистильованого оксихлориду фосфору (2,74 г, 17,9 ммол) є безводному тетрапдрофурані (15 мл) До цієї суміші по краплинах було добавлене розчин 1(г,2,2-октадека-6,9,12-триенойлокси)-3пдроксипропану в безводном} тетрапдрофурані (15 мл) Температура реакції не перевищувала 10°С, і сама реакція відбувалася під штучною азотною атмосферою Хроматографічний аналіз, що йоге було проведено через 15 хвилин після цього, показав повне зникнення початкового матеріалу Суміш було профільтровано та концентровано Далі добавляли толуол (50мл), і суміш знову піддавали концентруванню Процедуру із толуолом (також по 50 мл) повторювали ДВІЧІ Частина 2 Розчин 1-(г,2,2-октадека-6,9,12-триенойлокси)3-пдроксипропану (3 г, 9 ммол) в безводному тетрапдрофурані (10 мл) додавали по краплинах до розчину сирого фосфохл ори дату (7,5 ммол) (половина порції, виготовленої в першій частині реакції") та триетиламшу (3,2 мл, 22,5 ммол) в безводному тетрапдрофурані (20 мл) при кімнатній температурі в азоті Реакція тривала 3 доби при температурі, що не перевищувала 10°С Після того було добавлено метанол (15 мл), і реакцію було продовжено при кімнатній температурі доти, поки хроматографічний аналіз не показав, що згаданий фосфохлоридат повністю прореагував і утворив необхідний складний фосфотриефір Шляхом виділення на хроматографічній колоні (етилацетат/гексан) було здобуто здобуто метилди(2,2,г-октадека-6,9,12-триенойлоксипропіл)фосфат у вигляді безбарвної масляної речовини Приклад 19 Ди(2,2,г-октадека-6,9,12-триенойлоксипропіл)фосфат (Фосфодиефір 2 молекул 3-пдроксипропілефіру GLA) Бромид ЛІТІЮ (104 мг, 1,13 ммол) в метил етил кетоні (1 мл) було добавлено до рочину метилди(2,2,г-октадека-6,9,12-триенойлоксипропіл)фосфату (0,85 г, 1,13 ммол) (виготовлення, аналогічне прикладу 18) в метил етил кетоні (1 мл), після чого суміш нагрівали із зворотним охолодженням протягом 1 год Після остаточного охолодження суміш розчинили в диетилефірі (З мл) та екстрагували у воді (3 мл) Емульсії, що утворилися, було розшаровано шляхом додавання кількох краплин метанолу Органічний шар було сепаровано, висушено (сульфат натрію), концентровано та виділено за допомогою хроматографії (метанол/хлороформ), на виході здобуто fln(z,z,zоктадека-6,9,12-триенойлоксипропіл)-фосфат у вигляді твердої парафіноподібної речовини білого кольору Приклад 20 (2-aMiHoeTHn)-(z,z,z-OKTafleKa-6,9,12 42 41 61884 триенойлоксипропіл)фосфат Приклад 22 (Фосфодиефір етаноламіну та 3(г,г,г-октадека-6,9,12пдроксипропіл-ефіру GLA) триенойлоксипропіл)фосфат Частина 1 (Фосфомоноефір 3-пдроксипропіп-ефгр GLA) Суміш етаноламіну (0,5 мл, 8,25 ммол) та триРозчин 1-(г,2,2-октадека-6,9,12-триенойлокси)етиламшу (4,2 мл, ЗО ммол) в безводному тетрап3-пдроксипропану (1,95 г, 5,8 ммол), піридину (1,41 дрофурані (20 мл) було добавлено до розчину мл,17,3 ммол) та безводного тетрапдрофурану (15 сирого фосфохл ори дату (7,5 ммол) (половина мл) було при помішуванні по краплинах добавлено порції, що її було виготовлено в прикладі 18, часдо охолодженого (0°С) розчину оксихлориду фостині 1) також в безводному тетрапдрофурані (20 фору (1,02 г, 6,6 ммол) в безводному тетрапдромл), із збереженням температури реакції не більш фурані (5 мл), і результативну суміш залишили на як 10°С Протікання реакції контролювалося за З год при температурі 0°С До суміші реакції додопомогою хроматографії Суміш було залишено давали водний розчин бікарбонату натрію (10% в на 3 доби при температурі, що не перевищувала о , 1 0 мл) По 20 хвилинах помішування суміш бу5°С Після ЦЬОГО ІІ профільтрували, концентрувало вилито в льодяну воду (ЗО мл), після чого рН ли, розбавили гексаном (50 мл) та концентрували розчину було доведено до 1 шляхом додавання по вдруге краплинах 2М хлористоводневої (соляної) кислоти Далі суміш екстрагували диетил-ефіром (2 х ЗО Частина 2 мл) Ефірні екстракти було об'єднано, висушено та Продукт, отриманий після першої частини реаконцетровано Результативну масляну речовину кції, було розчинено в ізопропанолі (100 мл), оцтобуло перетворено на азеотропну суміш із сухим вій кислоті (10 мл) та воді, після чого розчин залипіридином, на виході здобуто (г.г.г-октадекашили відстоюватися в азотній атмосфері при 6,9,12-триенойлоксипропіл) фосфат у вигляді в'язкімнатній температурі Коли хроматографія підкої масляної жовтої речовини твердила повне завершення реакції, суміш було концентровано та розподілено між ацетонітрилом (50 мл) та гексаном (50 мл) Шар гексану було сепаровано, концентровано та очищено за допомогою однократної хроматографії (метанол/хлороформ/вода) Очищені фракції було виділено та концентровано Додавання етилацетату призвело до бурхливого виділення (2aMiHoeTHn)-(z,z,z-OKTafleKa-6,9,12триенойлоксипропіл)фосфату у вигляді парафіноподібної твердої речовини кремового кольору, яку було зібрано за допомогою центрифугування Приклад 21 (2,2,г-октадека-6,9,12-триенойлоксипропіл)-(2(г\І,г\І,г\І-триметиламоній)етил)фосфат (Фосфодиефір коліну та 3-пдроксипропіл-ефір GLA) Частина 1 Розчин 2-хлоро-1,3,2-диоксафосфолан-2оксиду (430 мг, 3,4 ммол) в толуолі (5 мл) було добавлено до охолодженого (0°С) розчину 1-(z,z,zоктадека-6,9,12-триенойлокси)-3-пдроксипропан (1 г, 2,98 ммол) та триетиламш (0,57 мл, 4,1 ммол) в толуолі (4,5 мл) Суміш було залишено і перемішувалося до ранку, поступово вона прогрівалася до кімнатної температури Після цього хроматографія показала, що реакція повністю не відбулася Тоді було використано додаткові порції триетиламіну (0,3 мл) та 2-хлоро-1,3,2-диоксафосфолану (200 мг) (у формі розчину в толуолі (5 мл)), після чого реакцію було продовжено ще на одну ніч Після ЦЬОГО хроматографія показала, що реакція відбулася повністю, і суміш концентрували Частина 2 Сирий продукт першої частини реакції було розчинено в ацетонітрилі (60 мл) Чверть об'єму цього розчину (15 мл) та триметиламін (10 мл) нагрівали в запаяному тубусі при 60°С під тиском 5 атм (ОБЕРЕЖНОЇ) Суміш реакції було охолоджено та концентровано під струмом азоту, на виході здобуто (z,z,z-OKTafleKa-6,9,12триенойлоксипропіл)-(2-(г\І,г\І,г\Ітриметиламоній)етил)фосфат Приклад 23 MeTHn-(z,z,z-OKTafleKa-6,9,12триенойлоксипропіл)-(а-токоферил)фосфат (Фосфотриефір а-токоферолу, метанолу та 3пдроксипропіл-ефіру GLA) Частина 1 Триетиламш (7,5 мл) було добавлено до розчину свіжо дистильованого оксихлориду фосфору (1,26 г, 8,25 ммол) в безводному тетрапдрофурані (7,5 мл) при температурі 0°С Через 15 хвилин почали по краплинах добавляти розчин 1-(z,z,zоктадека-6,9,12-триенойлокси)-3-пдроксипропану (2,5 г, 7,5 ммол) в безводному тетрапдрофурані, і той процес тривав ЗО хвилин також при температурі 0°С Після додавання протягом наступних ЗО хвилин розчин помішували при тій же самій температурі Далі по краплинах при 10°С додавали атокоферол (3,23 г, 7,5 ммол) в безводному тетрапдрофурані, і результативну суміш після цього помішували також при 10°С протягом 1 години та залишили на ніч, поступово нагріваючи до кімнатної температури Частина 2 Чверть об'єму суміші, яку було виготовлено в першій частині реакції, триетиламш (0,8 мл, 6 ммол) та метанол (10 мл) перемішували протягом ночі в азотній атмосфері при кімнатній температурі Суміш реакції було концентровано та розподілено між етилацетатом (ЗО мл) та водою (20 мл), з додаванням хлориду натрію та метанолу для розкладання емульсії Етилацетатовий шар було висушено, концентровано та очищено за допомогою однократної хроматографії (хлороформ), на виході здобуто метил-(г,г,г-октадека-6,9,12триенойлоксипропіл)-(а-токоферил)фосфат Приклад 24 (2,2,г-октадека-6,9,12-триенойлоксипропіл)-(атокоферил)фосфат (Фосфодиефір а-токоферолу та 3пдроксипропіл-ефгру GLA) Триетиламш (2 мл) та воду було добавлено до четвертої частини суміші реакції, виготовленої по 43 прикладу 23, частина 1 Суміш було витримано в азотній атмосфері в льодяній бані протягом 1 години, підкислено до рН 1 2М-хлористоводневою кислотою та екстраговано етилацетатом (20 мл) та метанолом (5 мл) Екстракт було висушено, концентровано та очищено за допомогою однократної хроматографії (хлороформ), на виході здобуто (г,г,г-октадека-6,9,12-триенойлоксипропіл)-(атокоферил)фосфат Приклад 25 1-(г,г,г-октадека-6,9,12-триенойлокси)-5(z,z,z,z,z-eiiKO3a-5,8,11,14,17пентаенойлокси)пентан (Диефір GLA та ЕР А із 1,5-пентан-дюлом) Частина 1 г,г,г-Октадека-6,9,12-триенойлхлорид (2 г) було по краплинах добавлено до розчину 1,5дипдроксипентану (3,5 г), триетиламшу (0,94 мл) та 4-(г\І,г\І-диметиламіно)піридину (0,2 г) в метиленхлориді (50 мл) при помішуванні при 0°С в азоті По завершенні реакції, котре було встановлене за допомогою хроматографії, суміш реакції промили розбавленою хлористоводневою кислотою та водою, висушили та за допомогою колонкової хроматографії виділили 1-(г,г,г-октадека-6,9,12триенойлокси)-5-пдроксипентан у вигляді блідожовтої масляної речовини Частина 2 ПОСЛІДОВНІСТЬ процедур була аналогічною прикладу 2, частині 2, але замість 1-(z,z,zоктадека-6,9,12-триенойлокси)-3-пдроксипропану використано 1-(г,г,г-октадека-6,9,12триенойлокси)-5-пдроксипентан, а замість zоктадека-9-еновоі кислоти в реакцію введено г,г,г,г,г-ейкоза-5,8,11,14,17-пентаенова кислота На виході з колони здобуто 1-(г,г,г-октадека6,9,12-триенойлокси)-5-(г,г,г,г,г-ейкоза5,8,11,14,17-пентанойлокси)пентан 1-(г,г,г-октадека-6,9,12-триенойлокси)-5(г,г,г,г,2-ейкоза-5,8,11,14,17пентаенойлокси)пентан Приклад 26 1-(г,г,г-октадека-6,9,12-триенойлокси)-4(г,г,г,г,г-ейкоза-5,8,11,14,17пентаенойлокси)бензол (Диефір GLA та ЕРА із 1,4-дипдроксибензол) Процес виготовлення є аналогічним прикладу 25, частинам 1 і 2, але в першій частині власне цієї реакції замість 1,5-дипдроксипентану було введено 1,4-дипдроксибензол, а замість метиленхлориду як розчинника - тетрапдрофуран На виході з колони здобуто 1-(г,г,г-октадека-6,9,12триенойлокси)-4-(г,г,г,г,г-ейкоза-5,8,11,14,17пентаенойлокси)бензол Приклад 27 1,4-ди(г,г,г-октадека-6,9,12-триенил)-бутан1,4-диоат (Дпефір спирту GLA із янтарною кислотою) Розчин 1,8-диазабіцикло[5 4 0]ундек-7-ену (0,54 мл) в сухому тетрапдрофурані (10 мл) було по краплинах добавлено до охолодженого (0°С) розчину г,г,г-октадека-6,9,12-триенолу (1 г) та ангідриду янтарної кислоти (0,36 г) в сухому тетрапдрофурані (20 мл) По закінченні реакції, що було встановлено за допомогою хроматографії, суміш розвели із диетилефіром та промили розведеною 61884 44 хлористоводневою кислотою, водою та соляним розчином Органічний шар було висушено, концентровано та безпосередньо використано для другої частини реакції Частина 2 Розчин 1,3-дициклогексилкарбодмміду (0,83 г) та 4-(г\І,г\І-диметиламіно)піридину (0,55 г) в метиленхлориді (20 мл) було добавлено до розчину 1(г,г,г-октадека-6,9,12-триенил)-бутан-1,4-диоату (1,32 г) та г,г,г-октадека-6,9,12-триенолу (0,98 г) в метиленхлориді (40 мл) По закінченні реакції, підтвердженому хроматографією, суміш було розведено гексаном, профільтровано, концентровано та виділено 1,4-ди(г,г,г-октадека-6,9,12-триенил)бутан-1,4-диоат у вигляді блідо-жовтої масляної речовини Приклад 28 2-(2-метил-5-нітроімідазолил)етилг,г,гоктадека-6,9,12-триеноат (Складний ефір метронідазолу із GLA) Метод А До суспензії метронидазолу (206 г) в безводному ацетонітрилі (2300 мл) та безводному піридині (107 мл) при кімнатній температурі в азоті було при помішуванні добавлено г,г,г-октадека6,9,12-триенойлхлорид (373 г) на період ЗО хвилин Невдовзі після того, як було додано хлорангідрид, утворився прозорий розчин, і помішування продовжували наступні 2 години Суміш залишили відстоюватись протягом ночі, після чого розчинник було видалено in vacua (50°С/20 мм рт ст) До залишку (осаду) було добавлено етилацетат (1000 мл), далі усі тверді часточки, які були в осаді, відфільтрували Розчин етилацетату після цього промили соляним розчином, 2Мхлористоводневою кислотою, насиченим водним розчином бікарбонату натрію і остаточно ще раз соляним розчином Після просушки (сульфат натрію) розчинник було видалено з ХІМІЧНИМ ВИХОДОМ масляної речовини жовтогарячого кольору Цей матеріал було оброблено на сухій хроматографічній колоні із виходом 2-(2-метил-5нітроімідазолил)етил,г,г-октадека-6,9,12-триеноат у вигляді блідо-жовтого, нерозчинного масла Метод Метронідазол (1,9 г) було перетворено на суспензію в толуолі (ЗО мл), після цього суспензію при помішуванні нагрівали із зворотним охолодженням з використанням головки (Dean and Stark) протягом 20 хвилин з метою повного видалення води До киплячого розчину по краплинах, під азотною атмосферою, протягом 20 хвилин добавляли г,г,г-октадека-6,9,12-триенойлхлорид (2,96 г) Протягом наступних 2 год розчин при помішуванні нагрівали із зворотним охолодженням, що дало на вихід суміш темного кольору Після охолодження суміш знову було оброблено за допомогою сухої колонкової хроматографії, на виході остаточно було здобуто 2-(2-метил-5нітроімідазолил)етил-г,г,г-октадека-6,9,12триеноат у вигляді блідо-жовтої нерозчинної масляної речовини Приклад 29 2-(2-метил-5-нітроімідазолил)етил-г,гоктадека-9,12-диеноат (Складний ефір метронидазолу із ЛК) 46 45 61884 До суспензії метронидазолу (1,9г) в сухому дитоліл]пропіл-г,г,г-октадека-6,9,12-триенамід хлорметані (20 мл) послідовно добавляли 4-(N,N(Амід флюоксетину із GLA) диметиламшо)піридин, 1,3Аналогічним способом, але із заміщенням медициклогексилкарбодммід (2,2 г) та лшолеву кистронидазолу ВІДПОВІДНИМ об'ємом N-метил-Злоту (2,8 г) Суміш перемішували при кімнатній феніл-3[а,а,а-трифторо-п-толіл]пропіламшу температурі протягом ночі До суміші реакції було (флюоксетину), а лінолевої кислоти - ВІДПОВІДНИМ добавлено 2М-хлористоводневу кислоту (20 мл), і об'ємом GLA, виготовляється N-метил-З-фенілпомішування було продовжено Після фільтрації 3[а,а,а-трифторо-п-толіл]пропіл-2,2,2-октадекаорганічний шар було сепаровано, промито 50%-им 6,9,12-триенамід насиченим соляним розчином і остаточно промито Приклад 35 насиченим водним розчином бікарбонату натрію транс-1-(2,2,2-октадека-6,9,12-триенойламшо)Розчин дихлорометану було висушено (сульфат 2-феніл циклопропан натрію) та випарено in vacua (30° С/20 мм рт ст) (Амід транілципромшу із GLA) До результативного залишку було добавлено бенАналогічним способом, але із заміщенням мезин (темп кип 30-60°С, 20 мл), після чого суміш тронидазолу ВІДПОВІДНИМ об'ємом транс-1-амшо-2було залишено відстоюватись при кімнатній темфенілциклопропану (транилципромшу), а лінолепературі на 2 години, створюючи умови для осавої кислоти ВІДПОВІДНИМ об'ємом GLA, виготовлядження залишкової сечовини (карбаміду), и було ється TpaHC-1-(z,z,z-OKTafleKa-6,9,12видалено за допомогою фільтрації, після чого фітриенойламшо)-2-феніл циклопропан льтрат оброблено на сухій колоні, на виході здобуПриклад 36 то 2-(2-метил-5-нітроімідазолил)етил-2,г-октадека6-[(амшофенілацетил)амшо]-3,3-диметил-79,12-диеноат у вигляді блідо-жовтої нерозчинної оксо-4-тиа-1-азабіцикло[3 2 0]гептан-2-карбонова масляної речовини кислота-2,2,г-октадека-6,9,12-триенамід Приклад ЗО (Амід ампіциліну із GLA) 2-(2-метил-5-нітроімідазолойл)етил-2,2,гТриетиламш (0,3 мл) було добавлено до розейкоза-8,11,14-триеноат мішаної суспензії ампіциліну (0,7 г) в безводному (Складний ефір метронідазолу із DGLA) диметилформаміді (120 мл) в азоті До здобутого Аналогічним способом, але з заміщенням ліпісля цього прозорого розчину додавали складний нолевої кислоту ВІДПОВІДНИМ об'ємом г.г.г-ейкозаN-пдроксисукцинімід-ефір z,z,z-OKTafleKa-6,9,128,11,14-триеновоі кислоти, виготовляється 2-(2триенової кислоти (0,75 г), із збереженням темпеметил-5-нітроімідазолойл)етил-2,2,-ейкоза-8,11,14ратури реакції 0-10°С Суміш реакції помішували триеноат при цій температурі ще одну годину, після чого її було залишено відстоюватись при кімнатній темПриклад 31 пературі на ніч На цій стадії хроматографічний аналіз ЛТФ/гексан) показав, що в реакцію вступидокоза-4,7,10,13,16,19-гексаеноат ла більша частина ефіру сукциніміду В хімічну (Складний диефір метронидазолу із DHA) колбу було налито воду (40 мл), і речовини добре Аналогічним способом, але із заміщенням лірозмішали Після ТОГО сполуку було нейтралізованолевої кислоти ВІДПОВІДНИМ об'ємом z,z,z,z,z,zно та екстраговано етилацетатом Екстракт продокоза-4,7,10,13,16,19-гексаеновоі кислоти, вигомили водою, висушили (сульфат натрію) і довели товляється 2-(2-метил-5-нітроімідазолойл)етилдо повної сухості шляхом концентрування, внасліz,z,z,z,z,z-flOKO3a-4,7,10,13,16,19-reKcaeHoaT док чого здобули сиру скловидну тверду речовину Приклад 32 жовтого кольору Розтирання в гексані дало на 4-[3-[2-(трифторометил)1 ОН-фенотиазин-10виході 6-[(амшофенілацетил)амшо]-3,3-диметил-7ил]]-1-піперазинетил-г,г,г-октадека-6,9,12оксо-4-тиа-1-азабіцикло[3 2 0]гептан-2-карбонова триеноат кислота-2,2,г-октадека-6,9,12-триенаміду у вигляді (Складний диефір флюфеназину із GLA) жовтої порошковидної речовини Аналогічним способом, але із заміщенням метронидазолу ВІДПОВІДНИМ об'ємом вільної основи Приклад 37 4-[3-[2-(трифторометил)1 ОН-фенотиазин-10-ил]]-1 z,z,z-OKTafleKa-6,9,12-TpneHHn-z,z,z-OKTafleKaпіперазинетанолу (флюфеназину), а лінолевої 6,9,12-триеноат кислоти - ВІДПОВІДНИМ об'ємом GLA, виготовляєть(Складний ефір GLA зі спиртом GLA) ся 4-[3-[2-(трифторометил)1 ОН-фенотиазин-101,3-дициклогексилкарбодммід (0,82 г) та 4ил]]-1-піперазинетил-2,2,г-октадека-6,9,12(г\І,г\І-диметиламіно)піридин (0,48г) в метиленхлотриеноат риді (5 мл) було добавлено до розчину z,z,zПриклад 33 октадека-6,9,12-триенолу (0,95 г) та г,г,г-октадека4,4'-(біс z,z,z-OKTafleKa-6,9,126,9,12-триеновоі кислоти (1 г) в метиленхлориді триенойламшо)дифенілсульфон (10 мл) при помішуванні в азотній атмосфері при кімнатній температурі По закінченні реакції (після (Біс-амід дапсону із GLA) хроматографічного підтвердження) до суміші реаАналогічним способом, але із заміщенням мекції було добавлено гексан, після чого її було потронидазолу ВІДПОВІДНИМ об'ємом 4,4'слідовно профільтровано та очищено, на виході диамшодифенілсульфону (дапсону), а лінолевої після колонкової хроматографії здобуто z,z,zкислоти - ВІДПОВІДНИМ об'ємом GLA, виготовляєтьоктадека-6,9,12-триенил-г,г,г-октадека-6,9,12ся 4,4'-(біс z,z,z-OKTafleKa-6,9,12триеноат у вигляді блідо-жовтої масляної речовитриенойламшо)дифенілсульфон ни Приклад 34 |\|-метил-3-феніл-3[а,а,а-трифторо-пПриклад 38 48 47 61884 z,z,z-oicrafleKa-6,9,12-TpHei-mn-z,z,z,z,z-ei^KO3aоктадека-6,9,12-триенойлокси)метилпіридин у ви 5,8,11,14,17-пентаеноат (Складний ефір ЕРА зі спиртом GLA) Виготовлення є аналогічним прикладу 37, але із заміщенням г,г,г-октадека-6,9,12-триеновоі кислоти г,г,г,г,г-ейкоза-5,8,11,14,17-пентаеновою кислотою Приклад 39 2-Me™>3-(z,z,z,z,z-eHKO3a-5,8,11,14,17пентаенойлокси)-4-формил-5-(г,г,г,г,г-ейкоза5,8,11,14,17-пентаенойлокси)метил піридин (диЕРА- складний ефіртридоксалу) До суспензії хлористоводневого піридоксалу (1,0 г) в метиленхлориді (20 мл) додавали триетиламін (2,0 мл) Утворився прозорий розчин жовтого кольору Після охолодження в льодяній бані 2,2,2,2,г-ейкоза-5,8,11,14,17-пентаенойлхлорид (1,73 г) (суміш було виготовлено шляхом реакції ЕРА із оксалилхлоридом в метиленхлориді) Суміш було залишено відстоюватись на ніч в азотній температурі з поступовим нагріванням до кімнатної температури Після розведення в еквівалентному об'ємі метиленхлориду суміш екстрагували 2М-хлористоводневою кислотою (20 мл), промили водою (3 х 20 мл), висушили та концентрували Після очищення та виділення за допомогою однократної хроматографії (етилацетат/гексан) на виході було здобуто 2-MeTHn-3-z,z,z,z,z^KO3a5,8,11,14,17-пентаенойлокси-4-формил-5-(г,г,г,г,гейкоза-5,8,11,14,17 пентаенойлокси)метилпіридину у вигляді прозорої масляної речовини Приклад 40 2-метил-3-гідрокси-4-формил-5-(г,2,2октадека-6,9,12-триенойлокси)метил піридин (Складний GLA-ефір піридоксалу) Розчин (z,z,z-OKTafleKa-6,9,12триенойлхлориду (800 мг, 2,7 ммол) в метиленхлориді (10 мл) по краплинах додавали до суміші хлористоводневого піридоксалу (500 мг, 2,45 ммол), триетиламшу (1 мл, 7,2 ммол) та 4-(N,Nдиметиламшо)піридину (кілька мг, в об'ємі каталізатору) в метиленхлориді (20 мл) при 0°С в азоті По закінченні реакції, підтвердженому хроматографією, суміш було концентровано, очищено та за допомогою колонкової хроматографії (етилацетат/гексан) виділено 2-метил-3-пдрокси-4-формил5-(z,z,z-OKTafleKa-6,9,12триенойлокси)метилпіридин у вигляді безбарвної масляної речовини, яка пізніше поступово стужавіла Приклад 41 2-метил-3-пдрокси-4,5-ди(г,г,г-октадека6,9,12-триенойлокси)метил піридин (Біс GLA-ефір піридоксину) Розчин 2,2,г-октадека-6,9,12-триенойл хлориду (650 мг, 2,2 ммол) в метиленхлориді (10 мл) по краплинах повільно добавляли до суміші хлористоводневого піридоксину (206 мг, 1 ммол), триетиламшу (0,7 мл, 5 ммол) та 4-(N,Nдиметиламшо)піридину (кілька мг, в об'ємі каталізатору) в метиленхлориді (20 мл) при температурі 0°С в азотній атмосфері По закінченні, підтвердженому хроматографією (4п), суміш було концентровано, і за допомогою однократної хроматографії виділено 2-MeTHn-3-riflpoKCH-4,5-flH(z,z,z гляді безбарвної масляної речовини Приклад 42 1-(2-(2-метил-5-нітроімідазалойл)етил)-4(2,2,2-октадека-6,9,12-триенил)бутан-1,4-диоат (Складний диефір метронгдазолу та спирту GLA із янтарною кислотою) Розчин 1,3-дициклогексилкарбодмміду (780 г, 3,8 ммол) та 4-(г\І,г\І-диметиламіно)піридину (530 мг, 4,3 ммол) в метиленхлориді (15 мл) було добавлено при помішуванні до розчину складного ефіру сукцинату GLA-спирту (1,25 г, 3,3 ммол) (виготовлюється аналогічно прикладу 27, частина 1) та метронідазолу (620 мг, 3,6 ммол) в метиленхлориді (ЗО мл) при кімнатній температурі в азоті По закінченні реакції, підтвердженому хроматографією, суміш було розбавлено гексаном, профільтровано, концентровано та очищено за допомогою однократної хроматографії (етил ацетат/гексан) Фракції продукту було виділено та концентровано, на виході здобуто 1 - (2-(2-мети л-5нітроімідазалойл)етил)-4-(г,г,г-октадека-6,9,12триенил)-1,4-бутандиоат у вигляді безбарвної масляної речовини Приклад 43 Транс-1 -(z,z,z-OKTafleKa-6,9,12триенилоксикарбоніл бутилоксиамшо)-2-феніл циклопропан (янтарна кислота, складний спиртовий ефіріGLA, 4-транилципромш амід) Розчин 1,3-дициклогексилкарбодмміду (315 мг, 1,52 ммол) та 4-(І\І,г\І-диметиламіно)піридину (210 мг, 1,72 ммол) в метиленхлориді (10 мл) було добавлено при помішуванні до розчину складного ефіру сукцинату GLA-спирту (500 мг, 1,32 ммол) (виготовлено аналогічно прикладу 27, частина 1 та транилципрміну (225 мг, 1,32 ммол) в метиленхлориді (20 мл) при кімнатній температурі в азотній атмосфері По закінченні реакції, підтвердженому хроматографією, суміш було розбавлено гексаном, профільтровано, концентровано та очищено за допомогою однократної хроматографії (етилацетат/гексан) Фракції продукту було зібрано та концентровано, на виході здобуто транс-1 -(z,z,zоктадека-6,9,12-триенілоксикарбоніл бутилоксиамшо)-2-феніл циклопропан у вигляді безбарвної масляної речовини Приклад 44 (±)-2,5,7,8-тетраметил-2-(4',8',12'триметилдецил)-6-хроманил-г,г,г-октадека-6,9,12триеноат (Складний GLA-ефір а-токоферола) г,г,г-Октадека-6,9,12-триенойлхлорид (2,96, 10 ммол) по краплинах при помішуванні протягом 2-3 хвилини додавали до розчину (±)-атокоферолу (4,3г, 10 ммол) та піридину (0,885 мл, 11 ммол) в метиленхлориді (35 мл) в азоті при 5°С Після ТОГО суміш реакції залишили при помішуванні на ніч, із поступовим прогріванням до кімнатної температури Аналіз ХТШ показав, що реакція практично повністю закінчилася Суміш було промито водою (10 мл), 2М-хлористоводневою (соляною) кислотою (10 мл в 100 мл води) та вдруге водою (4 х 100 мл) Органічний шар було висушено (сульфат натрію) та концентровано При подальшій обробці за допомогою хроматографіч 49 61884 HOI колони (ефір/гексан) на виході здобуто (±)2,5,7,8-тетраметил-2-(4',8',12'-триметилдецил)-6хроманил-2,2,2-октадека-6,9,12-триеноат у вигляді блідо-жовтої масляної речовини Приклад 45 AHflpocT-5-eH-17-OH-3-(z,z,z,z,z,z-flOKO3a4,7,10,13,16,19-гексаеноат) (Складний DHA-ефір депдроепіандростерону) До охолодженої (0°С) суміші депдроепіандростерону (1 г)та триетиламшу (1 мл) в метиленхлориді (20 мл) було добавлено z,z,z,z,z,z-flOKO3a4,7,10,13,16,19-гексаенойлхлорид (1,33 г) (виготовлено шляхом реакції DHA із оксалилхлоридом в метиленхлориді) Суміш протягом ночі помішували, поступово нагріваючи до кімнатної температури Після ЦЬОГО її розбавили метиленхлоридом (20 мл), екстрагували 2М-хлористоводневою кислотою (20 мл), промили водою (2 х 20 мл), висушили та концентрували Після обробки на хроматографічній колоні (етилацетат/гексан) на виході здобуто fleriflpoemaHflpocT-5-eH-17-OH-3-(z,z,z,z,z,z-flOKO3a4,7,10,13,16,19-гексаеноат) у вигляді прозорої масляної речовини Приклад 46 г,г,г-октадека-6,9,12-триенил-(2(г,г,гоктадека-6,9,12-триенилокси)ацетат) (Складний ефір GLA та GLA-спирту із гліколевою кислотою) Частина 1 Розчин хлороацетилхлориду (0,4 мл, 5 ммол) в метиленхлориді (10 мл) по краплинах додавали до розчину z,z,z-OKTafleKa-6,9,12-триенолу (1 г, 3,8 ммол) та триетиламшу (1,4 мл, 10 ммол) в метиленхлориді (20 мл) при 0°С Протікання реакції контролювалося за допомогою ХТШ Через 3 години реакція відбулася для основного об'єму реагентів, але не остаточно Було добавлено кілька додаткових краплин хлороацетил хлориду Аналізування за допомогою ХТШ протягом 5 хвилин показало, що реакція відбулася вже повністю Здобуту суміш промили водою (2 х 50 мл) та соляним розчином (50 мл), висушили (сульфат натрію) та концентрували Після цього з метою азеотропічного видалення остаточних найменших домішок води добавили толуол (50 мл) Таким чином, було здобуто складний хлороацетил-ефір GLA у вигляді темно-коричневої масляної речовини, яку після цього використовували без жодного додаткового очищення Частина 2 Суміш г,г,г-октадека-6,9,12-триеновоі кислоти (700 мг, 2,5 ммол) та карбонату цезію (410 мг, 1,25 ммол) було енергійно розмішано в метанолі до перетворення суміші на прозорий розчин Далі цей розчин концентрували та витримали при 40°С під вакуумом протягом 1 год На виході було здобуто цезієву сіль GLA, котру далі використовували без додаткового очищення Частина З До колби із цезієвою сіллю GLA, виготовленою згідно частині 2, було влито складний хлороацетил-ефір спирту GLA (частина 1) (500 мг, 1,5 ммол) та сухий диметилформамід (15 мл) Суміш реакції розмішали в азотній атмосфері при кімнатній температурі По 90 хвилинах аналіз ХТШ показав, що реакція відбулася повністю Після цього здобуту 50 суміш було екстраговано гексаном (2 х 40 мл), і гексановий екстракт промито соляним розчином (2 х 50 мл) та водою (50 мл), висушено (сульфат натрію) та концентровано, на виході здобуто z,z,zоктадека-6,9,12-триенил-(2(г,г,г-окгадека-6,9,12триенилокси)ацетат) у вигляді безбарвної масляної речовини Приклад 47 Гідрокортизон-21-(2,2,2-октадека-6,9,12триеноат) (GLA-ефір гідрокортизону) Розчин г,г,г-октадека-6,9,12-триенойл хлориду (450 мг, 1,52 ммол) в метиленхлориді (10 мл) повільно по краплинах додавали до суміші гідрокортизону (500 мг, 1,38 ммол), триетиламшу (420 цл, 3 ммол) та 4-(г\І,г\І-диметиламшо)піридину (кілька мг, в об'ємі каталізатора) в метилен хлориді (20мл) при 0°С в азотній атмосфері Через 4 години аналіз ХТШ показав, що реакція відбулася повністю Суміш було концентровано, і після хроматографічної обробки (етилацетат/гексан) здобуто гідрокортизон-21-(2,2,2-октадека-6,9,12-триеноат) у вигляді безбарвної масляної речовини Приклад 48 г,г,г-октадека-6,9,12-триенил-(2-(1-(4хлоробензойл)-5-метокси-2-метил шдол-3ацетилокси)ацетат) Диефір індометацину та GLA-спирту із гліколєвою кислотою Частина 1 Суміш індометацину (895 мг, 2,5 ммол) та карбонату цезію (410 мг, 1,25 ммол) було енергійно розмішано в метанолі до утворення прозорого розчину Далі розчин концентрували та витримали при 40°С під високим вакуумом 1 годину На виході було здобуто цезієву сіль індометацину у вигляді яскраво-жовтої твердої речовини Частина 2 До колби із цезієвою сіллю індометацину, виготовленою згідно з частиною 1 цієї реакції, було влито складний хлороацетил-ефір GLA-спирту (виготовлений згідно прикладу 46, частина 1) (500 мг, 1,5 ммол) та добавлено сухий диметилформамід (15 мл) Суміш реакції розмішували під азотом при кімнатній температурі, протікання реакції контролювалося ХТШ Після відстоювання протягом ночі в холодильнику, хроматографічний аналіз підтвердив завершення реакції Далі суміш розподілили між водою (50 мл) та етилацетатом (50 мл) З метою розшарування емульсії було добавлено кілька мілілітрів соляного розчину Шар етилацетату було промито водою (3 х 50 мл), висушено (сульфат натрію), профільтровано через "подушку" з кремнієвого фільтруючого матеріалу та концентровано, на виході здобуто г.г.г-октадека6,9,12-триенил-(2-(1-(4-хлоробензойл)-5-метокси2-метил шдол-3-ацетилокси)ацетат) у вигляді яскраво-жовтої масляної речовини Приклад 49 1-(г,г,г-октадека-6,9,12-триенойлокси)-3-(4фенілбутанойлокси)пропан (Складний диефір 4-фенілбутановоі кислоти та GLA із 1,3-пропан дюлом) Розчин 1,3-дициклогексилкарбодмміду (710 мг, 3,45 ммол) та 4-(г\І,г\І-диметиламшо)піридину (475 мг, 3,9 ммол) в метилен хлориді (10 мл) було до 52 51 61884 бавлено до розчину 1-(г,г,г-октадека-6,9,12(430 мг, 3,15 ммол) було виготовлено 1-(z,z,zтриенойлокси)-3-пдроксипропану (1 г, 3 ммол) та октадека-6,9,12-триенойлокси)-34-фенілбутановоі кислоти (520 мг, 3,15 ммол) в (фенілацетокси)пропан метилен хлориді (15 мл) Результативну суміш Приклад 51 помішували при кімнатній температурі в азотній 1-(г,г,г-октадека-6,9,12-триенойлокси)-3атмосфері до остаточного завершення реакції, (транс-цинамойлокси)пропан підтвердженого ХТШ Далі суміш було профільт(Складний диефір транс-коричноі[цинамовоі ровано, концентровано, та за допомогою колонкопереклад] кислоти та GLA із 1,3-пропан-дюлом) вої хроматографії здобуто 1-(z,z,z-OKTafleKa-6,9,12Аналогічно прикладу 49, але із заміщенням 4триенойлокси)-3-(4-фенілбутанойлокси)пропан фенілбутанової кислоти транс-коричною кислотою (470 мг, 3,15 ммол) було виготовлено 1-(z,z,zПриклад 50 октадека-6,9,12-триенойлокси)-3-(транс1-(г,г,г-октадека-6,9,12-триенойлокси)-3цинамойлокси)пропан (фенілацетокси)пропан (Складний ефір фенілоцтової кислоти та GLA Пункти формули винаходу не стосуються споіз 1,3-пропан-дюлом) лук, що містять ніацин, що є об'єктом окремої заявки, яку було подано тим же числом Аналогічно прикладу 49, але із заміщенням 4фенілбутанової кислоти фенілоцтовою кислотою Комп'ютерна верстка М Клюкш Підписне Тираж39 прим Міністерство освіти і науки України Державний департамент інтелектуальної власності, Львівська площа, 8, м Київ, МСП, 04655, Україна ДП "Український інститут промислової власності", вул Сім'ї Хохлових, 15, м Київ, 04119
ДивитисяДодаткова інформація
Назва патенту англійською1,3-propane diol derivatives as biologically active compounds
Назва патенту російськоюПроизводные 1,3-пропандиола как биологически активные соединения
МПК / Мітки
МПК: C07D 213/66, A61P 27/14, A61K 38/28, A61P 1/00, C07D 279/00, C07J 5/00, A61P 25/24, A61K 31/23, C07D 339/00, C07F 9/09, A61P 11/00, A61K 38/23, A61P 25/26, A61P 13/02, C07D 209/28, A61K 31/70, C07C 229/08, A61K 38/22, A61P 25/28, A61P 25/30, A61P 9/10, C07D 321/00, C07J 1/00, C07C 69/602, A61P 9/08, A61P 43/00, A61P 37/08, A61P 3/02, A61P 35/00, A61K 31/40, C07C 69/007, A61P 25/18, A61K 31/54, A61K 31/405, C07D 207/16, C07D 209/40, C07C 323/52, C07C 69/587, A61K 31/44, C07D 477/00, A61P 37/00, A61P 17/00, A61P 27/02, A61P 15/00, A61K 31/404, A61K 31/397, C07C 317/34, A61K 31/415, A61P 29/00, C07D 233/94, C07F 9/655, A61P 3/08, C07D 499/00, A61K 31/5415, C07C 69/58, A61K 47/48, A61K 31/403, A61P 25/00, C07C 69/76, C07D 233/60, C07D 213/30
Мітки: активні, сполуки, 1,3-пропандіолу, біологічно, похідні
Код посилання
<a href="https://ua.patents.su/26-61884-pokhidni-13-propandiolu-yak-biologichno-aktivni-spoluki.html" target="_blank" rel="follow" title="База патентів України">Похідні 1,3-пропандіолу як біологічно активні сполуки</a>
Попередній патент: Вітроустановка “метелик-2″
Наступний патент: Спосіб зменшення вмісту no2 в топкових газах в колекторі та апарат для його здійснення
Випадковий патент: Спосіб виготовлення виробів з глини