Похідні тієно[3,2-c]піридину як інгібітори кіназ для застосування в лікуванні раку
Номер патенту: 103351
Опубліковано: 10.10.2013
Автори: Фрей Робін Р., Кертін Майкл Л., Мікаелідес Майкл Р.
Формула / Реферат
1. Сполука, яка має формулу І
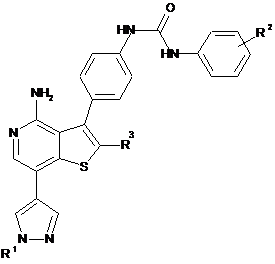 ,
,
або її терапевтично прийнятна сіль, де
R1 являє собою гідроксіалкіл;
R2 вибирають із групи, яка складається з алкокси, алкілу, галогену і галоалкокси; і
R3 являє собою водень або алкіл.
2. Сполука за п. 1, яка вибрана з групи:
N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл-N'-(3-фторфеніл)сечовина;
N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл-N'-[4-(дифторметокси)феніл]сечовина;
N-[4-(4-аміно-7-{1-[(2S)-2-гідроксипропіл]-1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл)феніл]-N'-(3-метилфеніл)сечовина;
N-(4-{4-аміно-7-[1-(2-гідрокси-2-метилпропіл)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-(4-метоксифеніл)сечовина та
N-[4-(4-аміно-7-{1-((2S)-2,3-дигідроксипропіл)-1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл)феніл]-N'-(4-метоксифеніл)сечовина.
3. Сполука за п. 1 або її фармацевтично прийнятна сіль, де вказана сполука не інгібує CYP3A4.
4. Композиція, яка містить допоміжну речовину і терапевтично ефективну кількість сполуки за п. 1.
5. Спосіб лікування раку в ссавця, що включає введення йому терапевтично прийнятної кількості сполуки за п. 1.
Текст
Реферат: Описані сполуки, які інгібують протеїнкінази, такі як Aurоrа-кінази і сімейства кіназ VEGFR і PDGFR, з поліпшеним профілем безпеки через низьке інгібування CYP3A4, композиції, що містять сполуки, і способи лікування захворювань з використанням сполук. UA 103351 C2 (12) UA 103351 C2 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 60 ГАЛУЗЬ ТЕХНІКИ, ДО ЯКОЇ НАЛЕЖИТЬ ВИНАХІД Даний винахід належить до сполук, які інгібують протеїнкінази, такі як Aurora-кінази і сімейства кіназ VEGFR і PDGFR, і які мають поліпшений профіль безпеки через низьке інгібування CYP3A4, композицій, що містять такі сполуки, і способів лікування захворювань з використанням сполук. СПИСОК ПОСЛІДОВНОСТЕЙ Дана заявка містить список послідовностей, який був представлений за допомогою EFSWeb і за допомогою чого включений у вигляді посилання повністю. Зазначена копія ASCII, створена 5 березня 2010 року, називається 9714WO01.txt і має розмір 943 байти. ПОПЕРЕДНІЙ РІВЕНЬ ТЕХНІКИ ВИНАХОДУ Мітоз являє собою процес, за допомогою якого повна копія дуплікованого геному розділяється за допомогою веретеноподібної структури мікротрубочок на дві дочірні клітини. Було виявлено, що Aurora-кінази, ключові регулятори мітозу, необхідні для стабільності геному, підвищено експресуються в людських пухлинах. Отже, існує дана необхідність в галузі терапії в сполуках, які інгібують Aurora-кінази, композиціях, які містять інгібітори, і способах лікування захворювань, протягом яких Aurora-кінази не регулюються або підвищено експресуються. Оборотне фосфорилування білків являє собою один з первинних біохімічних механізмів, які опосередковують передачу сигналу еукаріотичних клітин. Така реакція каталізується протеїнкіназами, що переносять g-фосфатну групу АТФ на гідрофільні групи цільових білків. 518 таких ферментів існують у людському геномі, з яких ~90 селективно каталізують фосфорилування гідроксильних груп тирозину. Цитозольні тирозинкінази розташовуються внутрішньоклітинно, тоді як рецептори тирозинкінази (RTK) мають і позаклітинні і внутрішньоклітинні домени і діють як мембранні рецептори поверхні клітин. Як такі RTK опосередковують клітинні відповіді на сигнали навколишнього середовища і полегшують широкий діапазон процесів у клітині, включаючи проліферацію, міграцію і виживаність. Шляхи сигналу RTK звичайно високо регульовані, однак було показано, що їхня надмірна активація запускає ріст, виживаність і метастазування ракових клітин. Дисрегуляція сигналу RTK виникає через підвищену експресію або мутації геному і корелює з прогресуванням різних видів людського раку. Сімейство рецепторів VEGF (VEGFR) складається з трьох RTK, KDR (рецептор, що містить кіназа-вставлений домен (kinase insert domain-containing receptor, VEGFR2), FLT-1 (Fms-подібна тирозинкіназа (Fms-like tyrosine kinase, VEGFR1)) і FLT4 (VEGFR3). Такі рецептори опосередковують біологічні функції судинних ендотеліальних факторів росту (VEGF-A, -B, -C, D, -E і плацентарного фактора росту (PlGF), сімейства гомодимерних глікопротеїнів, які зв'язують рецептори VEGF з різною афінністю. KDR являє собою основний медіатор мітогенних, ангіогенних і посилюючих проникність ефектів VEFD-A, який далі називається як VEGF. Множина різних типів клітин здатні продукувати VEGF, однак його біологічна активність обмежується переважно судинним руслом за допомогою експресії KDR, селективної для ендотеліальних клітин. Як і очікувало, вісь VEGF/KDR є основним регулятором ангіогенезу, процесу, за допомогою якого утворюються нові кровоносні судини з існуючих раніше судин. FLT1 зв'язує VEGF, VEGF-B і плацентарний фактор росту. FLT1 експресується на поверхні гладком’язових клітин, моноцитів і гематопоетичних стовбурових клітин на додачу до ендотеліальних клітин. Активація передачі сигналу FLT1 приводить до мобілізації ендотеліальних клітин-попередників з кісткового мозку, які захоплюються пухлинами, де вони беруть участь в утворенні нових кровоносних судин. FLT4 опосередковує передачу сигналу VEGF-C і VEGF-D, які опосередковують утворення лімфатичних судин, асоційованих з пухлиною (лімфоангіогенез). Лімфатичні судини є одним зі шляхів, за допомогою яких ракові клітини поширюються із солідних пухлин під час метастазування. Сімейство рецепторів PDGF (PDGFR) складається з п'яти RTK, PDGFR-a і -b, CSF1R, KIT і FLT3. a і b ізоформи рецепторів тромбоцитарного фактора росту (PDGF) існують як гомодимери або a/b гетеродимери і виявляються найбільш часто на поверхні фібробластів і гладком’язових клітин. PDGFR-b бере участь в ангіогенезі пухлини за допомогою проліферації і міграції перицитів, пери-ендотеліальних клітин, які асоціюються і стабілізують незрілі кровоносні судини. Угліомах аутокринна стимуляція PDGFR, здійснювана спільною експресією PDGF і рецепторів PDGF, опосередковує проліферацію і виживаність пухлинних клітин. CSF-1R кодується клітинним гомологом ретровірусного онкогену v-fms і є основним регулятором розвитку макрофагів. Макрофаги являють собою частий компонент строми 1 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 60 пухлини, і було показано, що вони модифікують позаклітинний матрикс чином, переважним для росту і метастазування пухлин. KIT експресується гематопоетичними клітинами попередниками, гладкими клітинами, зародковими клітинами і пейсмекерними клітинами в кишечнику (інтерстиціальні клітини Кайала). Він бере участь у прогресуванні пухлини за допомогою двох загальних механізмів, а саме аутокринної стимуляції його лігандом, фактором стовбурових клітин (SCF), і за допомогою мутацій, що приводять до ліганд-незалежної кіназної активності. FLT3 звичайно експресується на гематопоетичних стовбурових клітинах, де його взаємодія з лігандом FLT3 (FL) стимулює виживаність, проліферацію і диференціювання стовбурових клітин. На додачу до підвищеної експресії в різних лейкозних клітинах, FLT3 часто мутований у гематологічних злоякісних новоутвореннях, приблизно одна третина пацієнтів з гострим мієлолейкозом (AML) несе активуючі мутації. Отже, бажаною є ідентифікація невеликих ефективних сполук, які специфічно інгібують передачу сигналу і проліферацію клітин шляхом модуляції активності тирозинкіназ для регуляції і модуляції патологічної і невідповідної проліферації, диференціювання або метаболізму клітин. Зокрема корисною буде ідентифікація методів і сполук, які специфічно інгібують функцію тирозинкіназ, що необхідні для ангіогенних процесів або утворення підвищеної проникності судин, що приводить до набряків, асциту, випоту, ексудатів і екстравазації макромолекул і депонування матриксу, а також асоційованих розладів. Лікарські засоби, які вводяться, видаляються з організму або за допомогою екскреції або шляхом метаболізму до одного або більше метаболітів. Одним класом метаболізуючих ферментів, що є особливо важливими в метаболізмі лікарських засобів, є сімейство ферментів цитохрому Р450 (також відомого як CYP або Р450). Це велике сімейство ізоферментів, які розділені на 15 підродин. Підродина CYP3A, що включає CYP3A4, 3A5, 3A7 і 3А43, відповідає за метаболізм близько 60% відомих терапевтичних лікарських препаратів. CYP3A4 зокрема є найбільш поширеним ізоферментом CYP і в печінці й у кишечнику і втягнений в метаболізм більше ніж 50% клінічно використовуваних лікарських засобів (Mechanism-Based Inhibition of cytochrome P455 3A4 by therapeutic drugs. Clin. Pharmacokinet, 2005, 44, 279-304). Як всі інші CYP ферменти CYP3A4 підданий і оборотному і псевдо-необоротному або необоротному (на основі механізму) інгібування (Time-dependent CYP inhibition, Expert Opin. Drug Metab. Toxicol. 2007, 3, 51-66). Їх низька субстратна специфічність робить ферменти CYP підданими інгібуванню широкою розмаїтістю різних за структурою лікарських засобів. У результаті інгібування CYP можуть виникати різкі зміни відносно засобу, який спільно вводиться, в окремого індивіда, приводячи до істотного збільшення або зниження в крові і тканині концентрацій лікарського засобу або метаболіту. Такі типи змін можуть порушувати профіль безпеки й ефективності лікарського засобу істотно, особливо лікарських засобів з вузьким терапевтичним вікном. Як підкреслено в посібнику з виробництва FDA, докладна оцінка потенціалу інгібування CYP потрібна для всіх нових лікарських засобів-кандидатів (Guidance for industry. Drug Metabolism/Drug Interaction studies in the drug development process: Studies in vitro. US FDA April 1997). Така проблема взаємодій лікарських засобів один з одним є дуже важливою в лікуванні онкології, тому що звичайно пацієнти одержують множину лікарських засобів. Отже, зниження ризику такої взаємодії є важливим питанням у розробці нових терапевтичних засобів для лікування раку. Тоді як тієнопіридинові сполуки, описані в WO2005/010009, виявляють сильне інгібування Aurora і PDFR/VEGFR кіназ, вони також можуть бути інгібіторами CYP3A4. Даний винахід належить до нових тієнопіридинів по формулі I, що зберігають виражене інгібування і Auroraкіназ і сімейства кіназ, що охоплюють PDGFR і VEGFR, і також демонструють щонайменше 1030 кратне зменшення CYP3A4 інгібування. Тому що сполуки за даним винаходом мають істотно знижене інгібування CYP3A4, очікують, що вони будуть виявляти низьку схильність до міжлікарських взаємодій. На додачу до зменшення інгібування CYP сполуки за винаходом продемонстрували свою застосовність у додаткових аналізах, використовуваних для оцінки відповідності сполук як лікарських засобів-кандидатів. Наприклад, сполуки за винаходом демонструють ефективність у дослідженнях цільних клітин (наприклад, у дослідженнях людських ендотеліальних клітин пупкової вени (HUVEC) і дослідженні, що вимірює фосфорилування гістону D3 і індукцію поліплоїдії) і придатні фармакокінетичні властивості (наприклад, пероральний кліренс і пероральну біодоступність), ефективність in vivo (наприклад, модель набряку матки, моделі ортотопічної і бічної пухлини гризунів), серцево-судинну безпеку, дослідження ЦНС і дослідження шлунково-кишкового тракту. 2 UA 103351 C2 СУТЬ ВИНАХОДУ В одному варіанті здійснення даний винахід забезпечує сполуку за формулою (I) , 5 10 де 1 R являє собою гідроксіалкіл; 2 R вибирають із групи, яка складається з алкокси, алкілу, галогену, і галоалкокси; і 3 R являє собою водень або алкіл. Ще один варіант здійснення винаходу належить до способів лікування захворювань, що включають опосередкування, підвищену експресію або порушену регуляцію кіназ у ссавців, способи включають уведення їм терапевтично ефективної кількості сполуки, що має формулу I , 15 20 25 30 35 де 1 R являє собою гідроксіалкіл; 2 R вибирають із групи, яка складається з алкокси, алкілу, галогену, і галоалкокси; і 3 R являє собою водень або алкіл. Інший варіант здійснення винаходу належить до способів лікування акустичної невриноми, гострого лейкозу, гострого лімфоцитарного лейкозу, гострого мієлолейкозу (моноцитарного, мієлобластного, аденокарциноми, ангіосаркоми, астроцитоми, мієломоноцитарного і промієлоцитарного), гострого Т-клітинного лейкозу, базальноклітинної карциноми, карциноми жовчних проток, раку сечового міхура, раку головного мозку, раку молочної залози, бронхогенної карциноми, раку шийки матки, хондросаркоми, хордоми, хоріокарциноми, хронічного лейкозу, хронічного лімфолейкозу, хронічного мієлолейкозу (гранулоцитарного), хронічного мієлогенного лейкозу, раку товстої кишки, колоректального раку, краніофарингіоми, цистаденокарциноми, дифузійної велико В-клітинної лімфоми, диспроліферативних змін (дисплазій і метаплазій), ембріональної карциноми, раку ендометрія, ендотеліосаркоми, епендимоми, епітеліальної карциноми, еритролейкозу, раку стравоходу, раку молочної залози з позитивними рецепторами естрогенів, есенціальної тромбоцитемії, пухлини Евінга, фібросаркоми, фолікулярної лімфоми, раку зародкових клітин яєчок, гліоми, хвороби важких ланцюгів, гемангіобластоми, гепатоми, гепатоцелюлярного раку, гормон-нечутливого раку передміхурової залози, лейоміосаркоми, ліпосаркоми, раку легень, лімфангіоендотелиосаркоми, лімфангіосаркоми, лімфобластного лейкозу, лімфоми (ходжкінської і не-ходжкінської), злоякісних новоутворень і гіперпроліферативних захворювань сечового міхура, молочної залози, товстої кишки, легень, яєчників, підшлункової залози, передміхурової залози, шкіри і матки, лімфоїдних злоякісних новоутворень Т-клітинного і В 3 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 60 клітинного походження, лейкозу, лімфоми, медулярной карциноми, медулобластоми, меланоми, менінгіоми, мезотеліоми, множинної мієломи, мієлогенного лейкозу, мієломи, міксосаркоми, нейробластоми, недрібноклітинного раку легень, олігодендрогліоми, раку порожнини рота, остеогенної саркоми, раку яєчників, раку підшлункової залози, папілярних аденокарцином, папілярної карциноми, пінеаломи, істинної поліцитемії, раку передміхурової залози, раку прямої кишки, карциноми клітин нирки, ретинобластоми, рабдоміосаркоми, саркоми, карциноми сальних залоз, семіноми, раку шкіри, дрібноклітинного раку легень, солідних пухлин (карцином і сарком), дрібноклітинного раку легень, раку шлунка, лускатоклітинної карциноми, синовіоми, карциноми потових залоз, раку щитовидної залози, макроглобулінемії Вальденстрема, пухлин яєчок, раку матки і пухлини Вільмса в ссавців, способи, що включають ведення їм терапевтично ефективної кількості сполуки по формулі I окремо або в комбінації з променевою терапією. Інший варіант здійснення винаходу належить до способів лікування акустичної невриноми, гострого лейкозу, гострого лімфоцитарного лейкозу, гострого мієлолейкозу (моноцитарного, мієлобластного, аденокарциноми, ангіосаркоми, астроцитоми, мієломоноцитарного і промієлоцитарного), гострого Т-клітинного лейкозу, базальноклітинної карциноми, карциноми жовчних проток, раку сечового міхура, раку головного мозку, раку молочної залози, бронхогенної карциноми, раку шийки матки, хондросаркоми, хордоми, хоріокарциноми, хронічного лейкозу, хронічного лімфолейкозу, хронічного мієлолейкозу (гранулоцитарного), хронічного мієлогенного лейкозу, раку товстої кишки, колоректального раку, краниофарингіоми, цистаденокарциноми, дифузійної велико В-клітинної лімфоми, диспроліферативних змін (дисплазій і метаплазій), ембріональної карциноми, раку ендометрія, ендотеліосаркоми, епендимоми, епітеліальної карциноми, еритролейкозу, раку стравоходу, раку молочної залози з позитивними рецепторами естрогенів, есенціальної тромбоцитемії, пухлини Евінга, фібросаркоми, фолікулярної лімфоми, раку зародкових клітин яєчок, гліоми, хвороби важких ланцюгів, гемангіобластоми, гепатоми, гепатоцелюлярного раку, гормон-нечутливого раку передміхурової залози, лейоміосаркоми, ліпосаркоми, раку легень, лімфангіоендотеліосаркоми, лімфангіосаркоми, лімфобластного лейкозу, лімфоми (ходжкінської і не-ходжкінської), злоякісних новоутворень і гіперпроліферативних захворювань сечового міхура, молочної залози, товстої кишки, легень, яєчників, підшлункової залози, передміхурової залози, шкіри і матки, лімфоїдних злоякісних новоутворень Т-клітинного і В-клітинного походження, лейкозу, лімфоми, медулярной карциноми, медулобластоми, меланоми, менінгіоми, мезотеліоми, множинної мієломи, мієлогенного лейкозу, мієломи, міксосаркоми, нейробластоми, недрібноклітинного раку легень, олігодендрогліоми, раку порожнини рота, остеогенної саркоми, раку яєчників, раку підшлункової залози, папілярних аденокарцином, папілярної карциноми, пінеаломи, істинної поліцитемії, раку передміхурової залози, раку прямої кишки, карциноми клітин нирки, ретинобластоми, рабдоміосаркоми, саркоми, карциноми сальних залоз, семіноми, раку шкіри, дрібноклітинного раку легень, солідних пухлин (карцином і сарком), дрібноклітинного раку легень, раку шлунка, лускатоклітинної карциноми, синовіоми, карциноми потових залоз, раку щитовидної залози, макроглобулінемії Вальденстрема, пухлин яєчок, раку матки і пухлини Вільмса в ссавців, способи включають уведення їм терапевтично ефективної кількості N-(4-{4аміно-7-[1-(2-гідроксіетил)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-(3фторфеніл)сечовини окремо або в комбінації з променевою терапією. Інший варіант здійснення винаходу належить до способів лікування акустичної невриноми, гострого лейкозу, гострого лімфоцитарного лейкозу, гострого мієлолейкозу (моноцитарного, мієлобластного, аденокарциноми, ангіосаркоми, астроцитоми, мієломоноцитарного і промієлоцитарного), гострого Т-клітинного лейкозу, базальноклітинної карциноми, карциноми жовчних проток, раку сечового міхура, раку головного мозку, раку молочної залози, бронхогенної карциноми, раку шийки матки, хондросаркоми, хордоми, хоріокарциноми, хронічного лейкозу, хронічного лімфолейкозу, хронічного мієлолейкозу (гранулоцитарного), хронічного мієлогенного лейкозу, раку товстої кишки, колоректального раку, краніофарингіоми, цистаденокарциноми, дифузійної велико В-клітинної лімфоми, диспроліферативних змін (дисплазій і метаплазій), ембріональної карциноми, раку ендометрія, ендотеліосаркоми, епендимоми, епітеліальної карциноми, еритролейкозу, раку стравоходу, раку молочної залози з позитивними рецепторами естрогенів, есенціальної тромбоцитемії, пухлини Евінга, фібросаркоми, фолікулярної лімфоми, раку зародкових клітин яєчок, гліоми, хвороби важких ланцюгів, гемангіобластоми, гепатоми, гепатоцелюлярного раку, гормон-нечутливого раку передміхурової залози, лейоміосаркоми, ліпосаркоми, раку легень, лімфангіоендотеліосаркоми, лімфангіосаркоми, лімфобластного лейкозу, лімфоми (ходжкінської і не-ходжкінської), злоякісних новоутворень і гіперпроліферативних захворювань сечового міхура, молочної 4 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 60 залози, товстої кишки, легень, яєчників, підшлункової залози, передміхурової залози, шкіри і матки, лімфоїдних злоякісних новоутворень Т-клітинного і В-клітинного походження, лейкозу, лімфоми, медулярної карциноми, медулобластоми, меланоми, менінгіоми, мезотеліоми, множинної мієломи, мієлогенного лейкозу, мієломи, міксосаркоми, нейробластоми, недрібноклітинного раку легень, олігодендрогліоми, раку порожнини рота, остеогенної саркоми, раку яєчників, раку підшлункової залози, папілярних аденокарцином, папілярної карциноми, пінеаломи, істинної поліцитемії, раку передміхурової залози, раку прямої кишки, карциноми клітин нирки, ретинобластоми, рабдоміосаркоми, саркоми, карциноми сальних залоз, семіноми, раку шкіри, дрібноклітинного раку легень, солідних пухлин (карцином і сарком), дрібноклітинного раку легень, раку шлунка, лускатоклітинної карциноми, синовіоми, карциноми потових залоз, раку щитовидної залози, макроглобулінемії Вальденстрема, пухлин яєчок, раку матки і пухлини Вільмса в ссавців, спосіб включає введення їм терапевтично ефективної кількості N-(4-{4-аміно7-[1-(2-гідроксіетил)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-[4дифторметокси)феніл]сечовини окремо або в комбінації з променевою терапією. Інший варіант здійснення винаходу належить до способів лікування акустичної невриноми, гострого лейкозу, гострого лімфоцитарного лейкозу, гострого мієлолейкозу (моноцитарного, мієлобластного, аденокарциноми, ангіосаркоми, астроцитоми, мієломоноцитарного і промієлоцитарного), гострого Т-клітинного лейкозу, базальноклітинної карциноми, карциноми жовчних проток, раку сечового міхура, раку головного мозку, раку молочної залози, бронхогенної карциноми, раку шийки матки, хондросаркоми, хордоми, хоріокарциноми, хронічного лейкозу, хронічного лімфолейкозу, хронічного мієлолейкозу (гранулоцитарного), хронічного мієлогенного лейкозу, раку товстої кишки, колоректального раку, краніофарингіоми, цистаденокарциноми, дифузійної велико В-клітинної лімфоми, диспроліферативних змін (дисплазій і метаплазій), ембріональної карциноми, раку ендометрія, ендотеліосаркоми, епендимоми, епітеліальної карциноми, еритролейкозу, раку стравоходу, раку молочної залози з позитивними рецепторами естрогенів, есенціальної тромбоцитемії, пухлини Евінга, фібросаркоми, фолікулярної лімфоми, раку зародкових клітин яєчок, гліоми, хвороби важких ланцюгів, гемангіобластоми, гепатоми, гепатоцелюлярного раку, гормон-нечутливого раку передміхурової залози, лейоміосаркоми, ліпосаркоми, раку легень, лімфангіоендотеліосаркоми, лімфангіосаркоми, лімфобластного лейкозу, лімфоми (ходжкінської і не-ходжкінської), злоякісних новоутворень і гіперпроліферативних захворювань сечового міхура, молочної залози, товстої кишки, легень, яєчників, підшлункової залози, передміхурової залози, шкіри і матки, лімфоїдних злоякісних новоутворень Т-клітинного і В-клітинного походження, лейкозу, лімфоми, медулярної карциноми, медулобластоми, меланоми, менінгіоми, мезотеліоми, множинної мієломи, мієлогенного лейкозу, мієломи, міксосаркоми, нейробластоми, недрібноклітинного раку легень, олігодендрогліоми, раку порожнини рота, остеогенної саркоми, раку яєчників, раку підшлункової залози, папілярних аденокарцином, папілярної карциноми, пінеаломи, істинної поліцитемії, раку передміхурової залози, раку прямої кишки, карциноми клітин нирки, ретинобластоми, рабдоміосаркоми, саркоми, карциноми сальних залоз, семіноми, раку шкіри, дрібноклітинного раку легень, солідних пухлин (карцином і сарком), дрібноклітинного раку легень, раку шлунка, лускатоклітинної карциноми, синовіоми, карциноми потових залоз, раку щитовидної залози, макроглобулінемії Вальденстрема, пухлин яєчок, раку матки і пухлини Вільмса в ссавців, спосіб включає введення їм терапевтично ефективної кількості N-(4-(4-аміно7-{1-[(2S)-2-гідроксипропіл]-1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл}феніл)-N'-[3метилфеніл]сечовини окремо або в комбінації з променевою терапією. Інший варіант здійснення винаходу належить до способів лікування акустичної невриноми, гострого лейкозу, гострого лімфоцитарного лейкозу, гострого мієлолейкозу (моноцитарного, мієлобластного, аденокарциноми, ангіосаркоми, астроцитоми, мієломоноцитарного і промієлоцитарного), гострого Т-клітинного лейкозу, базальноклітинної карциноми, карциноми жовчних проток, раку сечового міхура, раку головного мозку, раку молочної залози, бронхогенної карциноми, раку шийки матки, хондросаркоми, хордоми, хоріокарциноми, хронічного лейкозу, хронічного лімфолейкозу, хронічного мієлолейкозу (гранулоцитарного), хронічного мієлогенного лейкозу, раку товстої кишки, колоректального раку, краніофарингіоми, цистаденокарциноми, дифузійної велико В-клітинної лімфоми, диспроліферативних змін (дисплазій і метаплазій), ембріональної карциноми, раку ендометрія, ендотеліосаркоми, епендимоми, епітеліальної карциноми, еритролейкозу, раку стравоходу, раку молочної залози з позитивними рецепторами естрогенів, есенціальної тромбоцитемії, пухлини Евінга, фібросаркоми, фолікулярної лімфоми, раку зародкових клітин яєчок, гліоми, хвороби важких ланцюгів, гемангіобластоми, гепатоми, гепатоцелюлярного раку, гормон-нечутливого раку передміхурової залози, лейоміосаркоми, ліпосаркоми, раку легень, лімфангіоендотеліосаркоми, 5 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 лімфангіосаркоми, лімфобластного лейкозу, лімфоми (ходжкінської і не-ходжкінської), злоякісних новоутворень і гіперпроліферативних захворювань сечового міхура, молочної залози, товстої кишки, легень, яєчників, підшлункової залози, передміхурової залози, шкіри і матки, лімфоїдних злоякісних новоутворень Т-клітинного і В-клітинного походження, лейкозу, лімфоми, медулярної карциноми, медулобластоми, меланоми, менінгіоми, мезотеліоми, множинної мієломи, мієлогенного лейкозу, мієломи, міксосаркоми, нейробластоми, недрібноклітинного раку легень, олігодендрогліоми, раку порожнини рота, остеогенної саркоми, раку яєчників, раку підшлункової залози, папілярних аденокарцином, папілярної карциноми, пінеаломи, істиною поліцитемії, раку передміхурової залози, раку прямої кишки, карциноми клітин нирки, ретинобластоми, рабдоміосаркоми, саркоми, карциноми сальних залоз, семіноми, раку шкіри, дрібноклітинного раку легень, солідних пухлин (карцином і сарком), дрібноклітинного раку легень, раку шлунка, лускатоклітинної карциноми, синовіоми, карциноми потових залоз, раку щитовидної залози, макроглобулінемії Вальденстрема, пухлин яєчок, раку матки і пухлини Вільмса в ссавців, спосіб включає введення їм терапевтично ефективної кількості N-(4-{4-аміно7-[1-(2-гідрокси-2-метилпропіл]-1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл}феніл)-N'-(4метоксифеніл)сечовини окремо або в комбінації з променевою терапією. Інший варіант здійснення винаходу належить до способів лікування акустичної невриноми, гострого лейкозу, гострого лімфоцитарного лейкозу, гострого мієлолейкозу (моноцитарного, мієлобластного, аденокарциноми, ангіосаркоми, астроцитоми, мієломоноцитарного і промієлоцитарного), гострого Т-клітинного лейкозу, базальноклітинної карциноми, карциноми жовчних проток, раку сечового міхура, раку головного мозку, раку молочної залози, бронхогенної карциноми, раку шийки матки, хондросаркоми, хордоми, хоріокарциноми, хронічного лейкозу, хронічного лімфолейкозу, хронічного мієлолейкозу (гранулоцитарного), хронічного мієлогенного лейкозу, раку товстої кишки, колоректального раку, краніофарингіоми, цистаденокарциноми, дифузійної велико В-клітинної лімфоми, диспроліферативних змін (дисплазій і метаплазій), ембріональної карциноми, раку ендометрія, ендотеліосаркоми, епендимоми, епітеліальної карциноми, еритролейкозу, раку стравоходу, раку молочної залози з позитивними рецепторами естрогенів, есенціальної тромбоцитемії, пухлини Евінга, фібросаркоми, фолікулярної лімфоми, раку зародкових клітин яєчок, гліоми, хвороби важких ланцюгів, гемангіобластоми, гепатоми, гепатоцелюлярного раку, гормон-нечутливого раку передміхурової залози, лейоміосаркоми, ліпосаркоми, раку легень, лімфангіоендотеліосаркоми, лімфангіосаркоми, лімфобластного лейкозу, лімфоми (ходжкінської і не-ходжкінської), злоякісних новоутворень і гіперпроліферативних захворювань сечового міхура, молочної залози, товстої кишки, легень, яєчників, підшлункової залози, передміхурової залози, шкіри і матки, лімфоїдних злоякісних новоутворень Т-клітинного і В-клітинного походження, лейкозу, лімфоми, медулярної карциноми, медулобластоми, меланоми, менінгіоми, мезотеліоми, множинної мієломи, мієлогенного лейкозу, мієломи, міксосаркоми, нейробластоми, недрібноклітинного раку легень, олігодендрогліоми, раку порожнини рота, остеогенної саркоми, раку яєчників, раку підшлункової залози, папілярних аденокарцином, папілярної карциноми, пінеаломи, істиною поліцитемії, раку передміхурової залози, раку прямої кишки, карциноми клітин нирки, ретинобластоми, рабдоміосаркоми, саркоми, карциноми сальних залоз, семіноми, раку шкіри, дрібноклітинного раку легень, солідних пухлин (карцином і сарком), дрібноклітинного раку легень, раку шлунка, лускатоклітинної карциноми, синовіоми, карциноми потових залоз, раку щитовидної залози, макроглобулінемії Вальденстрема, пухлин яєчок, раку матки і пухлини Вільмса в ссавців, спосіб включає введення їм терапевтично ефективної кількості N-[4-(4-аміно7-{1-[(2S)-2,3-дигідроксипропіл]-1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл}феніл]-N'-(4метоксифеніл)сечовини окремо або в комбінації з променевою терапією. Інший варіант здійснення винаходу належить до композицій, що включають допоміжну речовину і терапевтично ефективну кількість сполуки по формулі I і терапевтично ефективну кількість одного додаткового терапевтичного засобу або більше ніж одного додаткового терапевтичного засобу. Інший варіант здійснення винаходу належить до композицій, що включають допоміжну речовину і терапевтично ефективну кількість N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Н-піразол-4іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-(3-фторфеніл)сечовини і терапевтично ефективну кількість одного додаткового терапевтичного засобу або більше ніж одного додаткового терапевтичного засобу. Інший варіант здійснення винаходу належить до композицій, що включають допоміжну речовину і терапевтично ефективну кількість N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Н-піразол-4іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-[4-(дифторметокси)феніл]сечовини і терапевтично 6 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 60 ефективну кількість одного додаткового терапевтичного засобу або більше ніж одного додаткового терапевтичного засобу. Інший варіант здійснення винаходу належить до композицій, що включають допоміжну речовину і терапевтично ефективну кількість N-[4-(4-аміно-7-{1-[(2S)-2-гідроксипропіл]-1Нпіразол-4-іл}тієно[3,2-с]піридин-3-іл)феніл]-N'-(3-метилфеніл)сечовини і терапевтично ефективну кількість одного додаткового терапевтичного засобу або більше ніж одного додаткового терапевтичного засобу. Інший варіант здійснення винаходу належить до композицій, що включають допоміжну речовину і терапевтично ефективну кількість N-(4-{4-аміно-7-[1-(2-гідрокси-2-метилпропіл)-1Нпіразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-(4-метоксифеніл)сечовини і терапевтично ефективну кількість одного додаткового терапевтичного засобу або більше ніж одного додаткового терапевтичного засобу. Інший варіант здійснення винаходу належить до композицій, що включають допоміжний засіб і терапевтично ефективну кількість N-[4-(4-аміно-7-{1-[(2S)-2,3-дигідроксипропіл]-1Нпіразол-4-іл}тієно[3,2-с]піридин-3-іл)феніл]-N'-(4-метоксифеніл)сечовини і терапевтично ефективну кількість одного додаткового терапевтичного засобу або більше ніж одного додаткового терапевтичного засобу. Ще один варіант здійснення винаходу належить до способів лікування захворювань, що включають опосередкування, підвищену експресію або порушену регуляцію кіназ у ссавця, способи включають уведення їм терапевтично ефективної кількості сполуки по формулі I і терапевтично ефективної кількості одного додаткового терапевтичного засобу або більше ніж одного додаткового терапевтичного засобу окремо або в комбінації з променевою терапією. Ще один варіант здійснення винаходу належить до способів лікування захворювань, що включають опосередкування, підвищену експресію або порушену регуляцію кіназ у ссавця, способи включають уведення їм терапевтично ефективної кількості N-(4-{4-аміно-7-[1-(2гідроксіетил)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-(3-фторфеніл)сечовини і терапевтично ефективної кількості одного додаткового терапевтичного засобу або більше ніж одного додаткового терапевтичного засобу окремо або в комбінації з променевою терапією. Ще один варіант здійснення винаходу належить до способів лікування захворювань, що включають опосередкування, підвищену експресію або порушену регуляцію кіназ у ссавця, способи включають уведення їм терапевтично ефективної кількості N-(4-{4-аміно-7-[1-(2гідроксіетил)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-(4дифторметокси)феніл]сечовини і терапевтично ефективної кількості одного додаткового терапевтичного засобу або більше ніж одного додаткового терапевтичного засобу окремо або в комбінації з променевою терапією. Ще один варіант здійснення винаходу належить до способів лікування захворювань, що включають опосередкування, підвищену експресію або порушену регуляцію кіназ у ссавця, способи включають уведення їм терапевтично ефективної кількості N-[4-(4-аміно-7-{1-[(2S)-2гідроксипропіл]-1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл)феніл]-N'-(3-метилфеніл)сечовини і терапевтично ефективної кількості одного додаткового терапевтичного засобу або більше ніж одного додаткового терапевтичного засобу окремо або в комбінації з променевою терапією. Ще один варіант здійснення винаходу належить до способів лікування захворювань, що включають опосередкування, підвищену експресію або порушену регуляцію кіназ у ссавця, способи включають уведення їм терапевтично ефективної кількості N-(4-{4-аміно-7-[1-(2гідрокси-2-метилпропіл)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-(4метоксифеніл)сечовини і терапевтично ефективної кількості одного додаткового терапевтичного засобу або більше ніж одного додаткового терапевтичного засобу окремо або в комбінації з променевою терапією. Ще один варіант здійснення винаходу належить до способів лікування захворювань, що включають опосередкування, підвищену експресію або порушену регуляцію кіназ у ссавця, способи включають уведення їм терапевтично ефективної кількості N-[4-(4-аміно-7-{1-[(2S)-2,3дигідроксипропіл]-1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл)феніл]-N'-(4-метоксифеніл)сечовини і терапевтично ефективної кількості одного додаткового терапевтичного засобу або більше ніж одного додаткового терапевтичного засобу окремо або в комбінації з променевою терапією. Інший варіант здійснення винаходу належить до способів лікування дитячого раку або новоутворень, таких як ембріональна рабдоміосаркома, гострий лімфобластний лейкоз у дітей, гострий мієлогенний лейкоз у дітей, дитяча альвеолярна рабдоміосаркома, дитяча анапластична епендимома, дитяча анапластична великоклітинна лімфома, дитяча анапластична медулобластома, дитяча атипічна тератома/рабдоїдна пухлина центральної нервової системи, дитячий біфенотипічний гострий лейкоз, дитяча лімфома Беркітта, дитячий 7 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 60 рак сімейства пухлин Евінга, такий як примітивні нейроектодермальні пухлини, дитяча дифузійна анапластична пухлина Вільмса, дитяча гістологічно сприятлива пухлина Вільмса, дитяча гліобластома, дитяча медулобластома, дитяча нейробластома, дитячий мієлоцитоматоз, що походить з нейробластоми, дитячий пре-В-клітинний рак (такий як лейкоз), дитяча остеосаркома, дитяча рабдоїдна пухлина нирки, дитяча рабдоміосаркома і дитячий Тклітинний рак, такий як лімфома і рак шкіри, способи включають уведення їм терапевтично ефективної кількості сполуки по формулі I окремо або в комбінації з променевою терапією. Інший варіант здійснення винаходу належить до способів лікування дитячого раку або новоутворень, таких як ембріональна рабдоміосаркома, гострий лімфобластний лейкоз у дітей, гострий мієлогенний лейкоз у дітей, дитяча альвеолярна рабдоміосаркома, дитяча анапластична епендимома, дитяча анапластична великоклітинна лімфома, дитяча анапластична медулобластома, дитяча атипічна тератома/рабдоїдна пухлина центральної нервової системи, дитячий біфенотипічний гострий лейкоз, дитяча лімфома Беркітта, дитячий рак сімейства пухлин Евінга, такий як примітивні нейроектодермальні пухлини, дитяча дифузійна анапластична пухлина Вільмса, дитяча гістологічно сприятлива пухлина Вільмса, дитяча гліобластома, дитяча медулобластома, дитяча нейробластома, дитячий мієлоцитоматоз, що походить з нейробластоми, дитячий пре-В-клітинний рак (такий як лейкоз), дитяча остеосаркома, дитяча рабдоїдна пухлина нирки, дитяча рабдоміосаркома і дитячий Тклітинний рак, такий як лімфома і рак шкіри, способи включають уведення їм терапевтично ефективної кількості N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3іл}феніл)-N'-(3-фторфеніл)сечовини окремо або в комбінації з променевою терапією. Інший варіант здійснення винаходу належить до способів лікування дитячого раку або новоутворень, таких як ембріональна рабдоміосаркома, гострий лімфобластний лейкоз у дітей, гострий мієлогенний лейкоз у дітей, дитяча альвеолярна рабдоміосаркома, дитяча анапластична епендимома, дитяча анапластична великоклітинна лімфома, дитяча анапластична медулобластома, дитяча атипічна тератома/рабдоїдна пухлина центральної нервової системи, дитячий біфенотипічний гострий лейкоз, дитяча лімфома Беркітта, дитячий рак сімейства пухлин Евінга, такий як примітивні нейроектодермальні пухлини, дитяча дифузійна анапластична пухлина Вільмса, дитяча гістологічно сприятлива пухлина Вільмса, дитяча гліобластома, дитяча медулобластома, дитяча нейробластома, дитячий мієлоцитоматоз, що походить з нейробластоми, дитячий пре-В-клітинний рак (такий як лейкоз), дитяча остеосаркома, дитяча рабдоїдна пухлина нирки, дитяча рабдоміосаркома і дитячий Тклітинний рак, такий як лімфома і рак шкіри, способи включають уведення їм терапевтично ефективної кількості N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3іл}феніл)-N'-[4-дифторметокси)феніл]сечовини окремо або в комбінації з променевою терапією. Інший варіант здійснення винаходу належить до способів лікування дитячого раку або новоутворень, таких як ембріональна рабдоміосаркома, гострий лімфобластний лейкоз у дітей, гострий мієлогенний лейкоз у дітей, дитяча альвеолярна рабдоміосаркома, дитяча анапластична епендимома, дитяча анапластична великоклітинна лімфома, дитяча анапластична медулобластома, дитяча атипічна тератома/рабдоїдна пухлина центральної нервової системи, дитячий біфенотипічний гострий лейкоз, дитяча лімфома Беркітта, дитячий рак сімейства пухлин Евінга, такий як примітивні нейроектодермальні пухлини, дитяча дифузійна анапластична пухлина Вільмса, дитяча гістологічно сприятлива пухлина Вільмса, дитяча гліобластома, дитяча медулобластома, дитяча нейробластома, дитячий мієлоцитоматоз, що походить з нейробластоми, дитячий пре-В-клітинний рак (такий як лейкоз), дитяча остеосаркома, дитяча рабдоїдна пухлина нирки, дитяча рабдоміосаркома і дитячий Тклітинний рак, такий як лімфома і рак шкіри, способи включають уведення їм терапевтично ефективної кількості N-[4-(4-аміно-7-{1-[(2S)-2-гідроксипропіл]-1Н-піразол-4-іл}тієно[3,2с]піридин-3-іл)феніл]-N'-(3-метилфеніл)сечовини окремо або в комбінації з променевою терапією. Інший варіант здійснення винаходу належить до способів лікування дитячого раку або новоутворень, таких як ембріональна рабдоміосаркома, гострий лімфобластний лейкоз у дітей, гострий мієлогенний лейкоз у дітей, дитяча альвеолярна рабдоміосаркома, дитяча анапластична епендимома, дитяча анапластична великоклітинна лімфома, дитяча анапластична медулобластома, дитяча атипічна тератома/рабдоїдна пухлина центральної нервової системи, дитячий біфенотипічний гострий лейкоз, дитяча лімфома Беркітта, дитячий рак сімейства пухлин Евінга, такий як примітивні нейроектодермальні пухлини, дитяча дифузійна анапластична пухлина Вільмса, дитяча гістологічно сприятлива пухлина Вільмса, дитяча гліобластома, дитяча медулобластома, дитяча нейробластома, дитячий мієлоцитоматоз, що походить з нейробластоми, дитячий пре-В-клітинний рак (такий як лейкоз), 8 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 60 дитяча остеосаркома, дитяча рабдоїдна пухлина нирки, дитяча рабдоміосаркома і дитячий Тклітинний рак, такий як лімфома і рак шкіри, способи включають уведення їм терапевтично ефективної кількості N-(4-{4-аміно-7-[1-(2-гідрокси-2-метилпропіл)-1Н-піразол-4-іл]тієно[3,2с]піридин-3-іл}феніл)-N'-[4-метоксифеніл)сечовини окремо або в комбінації з променевою терапією. Інший варіант здійснення винаходу належить до способів лікування дитячого раку або новоутворень, таких як ембріональна рабдоміосаркома, гострий лімфобластний лейкоз у дітей, гострий мієлогенний лейкоз у дітей, дитяча альвеолярна рабдоміосаркома, дитяча анапластична епендимома, дитяча анапластична великоклітинна лімфома, дитяча анапластична медулобластома, дитяча атипічна тератома/рабдоїдна пухлина центральної нервової системи, дитячий біфенотипічний гострий лейкоз, дитяча лімфома Беркітта, дитячий рак сімейства пухлин Евінга, такий як примітивні нейроектодермальні пухлини, дитяча дифузійна анапластична пухлина Вільмса, дитяча гістологічно сприятлива пухлина Вільмса, дитяча гліобластома, дитяча медулобластома, дитяча нейробластома, дитячий мієлоцитоматоз, що походить з нейробластоми, дитячий пре-В-клітинний рак (такий як лейкоз), дитяча остеосаркома, дитяча рабдоїдна пухлина нирки, дитяча рабдоміосаркома і дитячий Тклітинний рак, такий як лімфома і рак шкіри, способи включають уведення їм терапевтично ефективної кількості N-[4-(4-аміно-7-{1-[(2S)-2,3-дигідроксипропіл]-1Н-піразол-4-іл}тієно[3,2с]піридин-3-іл)феніл]-N'-(4-метоксифеніл)сечовини окремо або в комбінації з променевою терапією. Ще один варіант здійснення винаходу належить до сполук: N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-(3фторфеніл)сечовина; N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-[4(дифторметокси)феніл)сечовина; N-[4-(4-аміно-7-{1-[(2S)-2-гідроксипропіл]-1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл)феніл]-N'(3-метилфеніл)сечовина; N-(4-{4-аміно-7-[1-(2-гідрокси-2-метилпропіл)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)N'-(4-метоксифеніл)сечовина; і N-[4-(4-аміно-7-{1-[(2S)-2,3-дигідроксипропіл]-1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл)феніл]N'-(4-метоксифеніл)сечовина і їх терапевтично прийнятні солі. Ще один варіант здійснення винаходу належить до N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Нпіразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-(3-фторфеніл)сечовини. Ще один варіант здійснення винаходу належить до N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Нпіразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-[4-(дифторметокси)феніл]сечовини. Ще один варіант здійснення винаходу належить до N-[4-(4-аміно-7-{1-[(2S)-2-гідроксипропіл]1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл)феніл]-N'-(3-метилфеніл)сечовини. Ще один варіант здійснення винаходу належить до N-(4-{4-аміно-7-[1-(2-гідрокси-2метилпропіл)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-(4-(метоксифеніл)сечовини. Ще один варіант здійснення винаходу належить до N-[4-(4-аміно-7-{1-[(2S)-2,3дигідроксипропіл]-1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл)феніл]-N'-(4-метоксифеніл)сечовини. Ще один варіант здійснення винаходу належить до сполуки по формулі I і її терапевтично прийнятних солей, проліків, складних ефірів, амідів, солей проліків, солей складних ефірів і солей амідів. Ще один варіант здійснення винаходу належить до N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Нпіразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-(3-фторфеніл)сечовини і її терапевтично прийнятних солей, проліків, складних ефірів, амідів, солей проліків, солей складних ефірів і солей амідів. Ще один варіант здійснення винаходу належить до N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Нпіразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-[4-дифторметокси)феніл]сечовини і її терапевтично прийнятних солей, проліків, складних ефірів, амідів, солей проліків, солей складних ефірів і солей амідів. Ще один варіант здійснення винаходу належить до N-[4-(4-аміно-7-{1-[(2S)-2-гідроксипропіл]1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл)феніл]-N'-(3-метилфеніл)сечовини і її терапевтично прийнятних солей, проліків, складних ефірів, амідів, солей проліків, солей складних ефірів і солей амідів. Ще один варіант здійснення винаходу належить до N-(4-{4-аміно-7-[1-(2-гідрокси-2метилпропіл)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-(4-метоксифеніл)сечовини і її терапевтично прийнятних солей, проліків, складних ефірів, амідів, солей проліків, солей складних ефірів і солей амідів. 9 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 Ще один варіант здійснення винаходу належить до N-[4-(4-аміно-7-{1-[(2S)-2,3дигідроксипропіл]-1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл)феніл]-N'-(4-метоксифеніл)сечовини і її терапевтично прийнятних солей, проліків, складних ефірів, амідів, солей проліків, солей складних ефірів і солей амідів. ДОКЛАДНИЙ ОПИС ВИНАХОДУ Різні компоненти сполук у даному описі представлені ідентифікаторами (великі букви з числовими і/або буквеними індексами) і можуть бути специфічно втілені. Передбачається, що розуміють, що для всіх компонентів і їхніх комбінацій підтримуються відповідні валентності, і що одновалентні компоненти, які мають більше ніж один атом, прикріплені за допомогою їхніх лівих кінців. Також розуміють, що специфічний варіант здійснення варіабельного компонента може бути таким же або відмінним від іншого специфічного варіанта здійснення, що має такий же ідентифікатор. Термін «алкокси», як використовується в даному описі, належить до алкільної групи, прикріпленої до батьківського молекулярного компонента через атом кисню. Термін «алкіл», як використовується в даному описі, належить до групи, отриманої з лінійного або розгалуженого ланцюга насиченого вуглеводню, що містить від одного до десяти атомів вуглецю. Терміни «гало» і «галоген», як використовується в даному описі, належать до F, Cl, Br або I. Термін «галоалкокси», як використовується в даному описі, належить до галоалкільної групи, прикріпленої до батьківського молекулярного компонента за допомогою атома кисню. Термін «галоалкіл», як використовується в даному описі, належить до алкільної групи, як визначено в даному описі, заміщеної щонайменше одним галогеном, як визначено в даному описі. Термін «гідрокси», як використовується в даному описі, належить до -ОН групи. Термін «гідроксіалкіл», як використовується в даному описі, належить до алкільної групи, заміщеної щонайменше однією гідроксигрупою. Термін «KDR» означає рецептор з кіназа-вставленим доменом (рецептор тирозин кіназу III типу) і також відомий як FLK1, VEGFR, VEGFR2 і CD309. Термін «VEGFR» означає рецептор судинного ендотеліального фактора росту. Термін «PDGFR» означає рецептор тромбоцитарного фактора росту. Сполуки за даним винаходом можуть містити асиметрично заміщені атоми вуглецю в R або S конфігурації, де терміни «R» і «S» визначені як у Pure Appl. Chem. (1976) 45, 13-10. Сполуки, що мають асиметрично заміщені атоми вуглецю з однаковими кількостями R і S конфігурацій є рацемічними по таких атомах. Атомам, що мають надлишок однієї конфігурації над іншою, приписана конфігурація в надлишку, переважно надлишок близько 85%-90%, більш переважно надлишок близько 95%-99% і ще більш переважно надлишок більше ніж близько 99%. Відповідно даний винахід охоплює рацемічні суміші і відносні й абсолютні діастереоізомери їхніх сполук. Сполуки за даним винаходом також можуть містити подвійні зв'язки вуглець-вуглець або подвійні зв'язки вуглець-азот в Е або Z конфігурації, де термін «Е» являє собою замісники більш високого порядку на протилежних сторонах подвійного зв'язку вуглець-вуглець або вуглець-азот і термін «Z» являє собою замісники більш високого порядку на одній стороні подвійного зв'язку вуглець-вуглець або вуглець-азот, що визначено Cahn-Ingold-Prelog priority Rules. Сполуки за даним винаходом також можуть існувати як суміш «Е» і «Z» ізомерів. Сполуки за даним винаходом також можуть існувати у вигляді таутомерів або їхніх рівноважних сумішей, де протон сполуки переходить з одного атома на іншій. Приклади таутомерів включають, але не обмежуються, кето-енол, фенол-кето, оксим-нітрозо, нітро-аци, імін-енамін і подібні. Сполуки за даним винаходом, що містять NH, C(O)OH, OH або SH компоненти, можуть мати прикріплені проліки-твірні компоненти. Проліки-твірні компоненти видаляються метаболічними процесами і вивільняють сполуки, що мають звільнені NH, C(O)OH, OH або SH in vivo. Проліки є застосовними для регуляції таких фармакокінетичних властивостей сполук, як розчинність і/або гідрофобність, абсорбція в шлунково-кишковому тракті, біодоступність, пенетрація в тканини і швидкість виведення. Метаболіти сполук за даним винаходом, які утворюються в метаболічних процесах in vitro або in vivo, також можуть мати властивості лікування захворювань, асоційованих з підвищеною експресією або порушеною регуляцією протеїнкіназ. 10 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 60 Визначені сполуки-попередники, які можуть метаболізуватися in vitro або in vivo з утворенням сполук за даним винаходом, також можуть мати властивості лікування захворювань, асоційованих з підвищеною експресією або порушеною регуляцією протеїнкіназ. Сполуки за даним винаходом можуть існувати у вигляді адитивних солей кислот, адитивних солей або основ цвітер-іонів. Солі сполук, що мають формулу I, одержують під час їхнього виділення або після їхнього очищення. Адитивні солі кислот являють собою такі, отримані з реакції сполуки за даним винаходом з кислотою. Відповідно, солі, що включають ацетат, адипат, альгінат, бікарбонат, цитрат, аспартат, бензоат, бензолсульфонат (безилат), бісульфат, бутират, камфорат, камфорсульфонат, диглюконат, формат, фумарат, гліцерифосфат, глютамат, гемісульфат, гептаноат, гексаноат, гідрохлорид, гідробромід, гідройодид, лактобіонат, лактат, малеат, мезитиленсульфонат, метансульфонат, нафтилсульфонат, нікотинат, оксалат, памоат, пектинат, персульфат, фосфат, пікрат, пропіонат, сукцинат, тартрат, тіоціанат, трихлороцтову, трифтороцтову, пара-толуолсульфонатну й ундеканоатну солі сполук за даним винаходом охоплюються даним винаходом. Адитивні солі основ сполук являють собою такі, отримані при реакції сполук за даним винаходом з бікарбонатом, карбонатом, гідроксидом або фосфатом катіонів, таких як літій, натрій, калій, кальцій і магній. Сполуки, які мають формулу I, можна вводити, наприклад, букально, в очі, перорально, осмотично, парентерально (внутрішньом’язово, інтраперитонеально, інтрастернально, внутрішньовенно, підшкірно), ректально, місцево, трансдермально, вагінально і інтраартеріально, а також шляхом внутрішньосуглобової ін'єкції, інфузії і вміщення в організм, наприклад, у судинне русло. Терапевтично ефективні кількості сполуки, що має формулу I, залежать від реципієнта лікування, захворювання, що піддається лікуванню і його тяжкості, композиції, що включає її, часу ведення, шляху введення, тривалості лікування, ефективності, швидкості виведення і вводиться або ні спільно інший лікарський засіб. Кількість сполуки, що має формулу I, використовувана для одержання композиції, що вводиться щодня пацієнту в разовій дозі або в розділених дозах, складає від близько 0,03 до близько 200 мг/кг маси тіла. Композиції разової дози містять такі кількості або комбінації їхніх підмножин. Сполуки, що мають формулу I, можна вводити з або без допоміжної речовини. Допоміжні речовини включають, але не обмежуються, інкапсулятори і добавки, такі як прискорювачі абсорбції, антиоксиданти, зв’язувальні засоби, буферні речовини, засоби для оболонки, барвники, розріджувачі, дезінтегруючі засобу, емульгатори, наповнювачі, заповнювачі, ароматизатори, зволожувачі, змащувальні засоби, віддушки, консерванти, пропеленти, вивільняючі засоби, стерилізуючі засоби, підсолоджувачі, розчинники, зволожувальні засоби, їхні суміші і подібні. Допоміжні речовини для одержання композицій, що включають сполуку, яка має формулу I, для введення перорально включають, але не обмежуються, агар, альгінову кислоту, гідроксид алюмінію, бензиловий спирт, бензилбензоат, 1,3-бутиленгліколь, карбомери, рициновук олію, целюлозу, ацетат целюлози, масло какао, кукурудзяний крохмаль, кукурудзяну олію, бавовняну олію, крос-повідон, дигліцериди, етанол, етилцелюлозу, етиллаурат, етилолеат, складні ефіри жирних кислот, желатин, олію зародків пшениці, глюкозу, гліцерин, арахісове масло, гідроксипропілметилцелюлозу, ізопропанол, ізотонічний сольовий розчин, лактозу, гідроксид магнію, стеарат магнію, солод, маніт, моногліцериди, маслинову олію, солі фосфату калію, картопляний крохмаль, повідон, пропіленгліколь, розчин Рінгера, сафлорову олію, кунжутну олію, карбоксиметилцелюлозу натрію, солі фосфату натрію, лаурилсульфат натрію, сорбіт натрію, соєву олію, стеаринові кислоти, стеарилфумарат, сахарозу, поверхнево-активні речовини, тальк, трагакант, тетрагідрофурфуриловий спирт, тригліцериди, воду, їхні суміші і подібні. Допоміжні речовини для одержання композицій, що включають сполуку, яка має формулу I, для введення офтальмологічно або перорально, включають, але не обмежуються, 1,3-бутиленгліколь, рицинову олію, кукурудзяну олію, бавовняну олію, етанол, складні ефіри сорбіту і жирних кислот, олію зародків пшениці, арахісове масло, гліцерин, ізопропанол, маслинову олію, поліетиленгліколі, пропіленгліколь, кунжутну олію, воду, їхні суміші і подібні. Допоміжні речовини для одержання композицій, що включають сполуку, яка має формулу I, для введення осмотично включають, але не обмежуються, хлорфторвуглеводні, етанол, воду, їхні суміші і подібні. Допоміжні речовини для одержання композицій, що включають сполуку, яка має формулу I, для введення парентерально включають, але не обмежуються, 1,3-бутандіол, рицинову олію, кукурудзяну олію, бавовняну олію, декстрозу, олію зародків пшениці, арахісове масло, ліпосоми, олеїнову кислоту, маслинову олію, арахісове масло, розчин Рінгера, сафлорову олію, кунжутну олію, соєву олію, U.S.P. або ізотонічний розчин хлориду натрію, воду, їхні суміші і подібні. Допоміжні речовини для одержання композицій, що включають сполуку, яка 11 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 має формулу I, для введення ректально або вагінально включають, але не обмежуються масло какао, поліетиленгліколь, віск, їхні суміші і подібне. Очікують, що сполуки, які мають формулу I, застосовні при використанні з алкілуючими засобами, інгібіторами ангіогенезу, антитілами, антиметаболітами, антимітотичними засобами, антипроліферативними засобами, інгібіторами Aurora-кінази, іншими інгібіторами промоторів апоптозу (наприклад, Bcl-xI, Bcl-w і Bfl-1), інгібіторами кінази Bcr-Abl, антитілами до BiTE (Biспецифічний Т-клітинний «поручитель»), модифікаторами біологічної відповіді, інгібіторами циклінзалежних кіназ, інгібіторами клітинного циклу, інгібіторами циклооксигенази-2, DVD, інгібіторами рецептора гомолога вірусного онкогену лейкемії (ErbB2), інгібіторами фактів росту, інгібіторами білків теплового шоку (HSP)-90, інгібіторами гістондеацетилази (HDAC), гормональним лікуванням, імунологічними препаратами, інгібіторами білків апоптозу (IAP), інтеркалюючими антибіотиками, інгібіторами кіназ, інгібіторами мети рапаміцину в ссавців, інгібіторами кінази, яка регулюється мікро РНК мітоген-активованого внутрішньоклітинного сигналу, полівалентними зв’язувальними білками, нестероїдними протизапальними засобами (НПЗЗ), інгібіторами полі АДФ (аденозиндифосфат)-рибозополімерази (PARP), хіміотерапевтичними препаратами платини, інгібіторами Polo-подібної кінази (Plk), інгібіторами протеосом, пуриновими аналогами, піримідиновими аналогами, інгібіторами рецепторів тирозинкіназ, ретиноїдними/дельтоїдними рослинними алкалоїдами, дрібними інгібуючими рибонуклеїновими кислотами (sіРНК), інгібіторами топоізомерази, їхніми комбінаціями і подібним. Антитіла до BiTE являють собою bi-специфічні антитіла, які направляють Т-клітини на прикріплення до ракових клітин шляхом одночасного зв'язування двох клітин. Потім Т-клітини атакують цільові ракові клітини. Зразкові антитіла до BiTE включають адекатумумаб (Micromet MT201), блінатумомаб (Micromet MT103) і подібні. SiРНК являють собою молекули, які мають ендогенні РНК основи або хімічно модифіковані нуклеотиди. Модифікації не повинні припиняти клітинну активність, але скоріше додавати підвищену стабільність і/або підвищену клітинну ефективність. Приклади хімічних модифікацій включають фосфоротіоатні групи, 2’-деоксинуклеотид, 2’-OCH3-вмісні рибонуклеотиди, 2’-Fрибонуклеотиди, 2’-метоксіетилрибонуклеотиди або їхні комбінації. sіРНК можуть мати довжину, що варіюється, (10-200 нп) і структури (шпильки, одинарні/подвійні ланцюги, опуклості, борозенки/петлі, розбіжності) і оброблятися в клітині з забезпеченням відключення активного гена. У визначених варіантах здійснення винаходу дволанцюжкова sіРНК (dsРНК) може мати однакову кількість нуклеотидів на кожному ланцюзі (тупі кінці) або асиметричні кінці (виступаючі частини). Виступаюча частина з 1-2 нуклеотидів може бути присутньою на смисловому і/або антисмисловому ланцюзі, а також бути присутньою на 5'- і/або 3'-кінцях заданого ланцюга. Полівалентні зв’язувальні білки являють собою зв’язувальні білки, які включають дві або більше ділянки зв'язування антигенів. Полівалентні зв’язувальні білки переважно створені як такі, що мають три або більше антигензв’язувальних ділянки і звичайно є штучними антитілами. Термін «мультиспецифічний зв’язувальний білок» означає зв’язувальний білок, здатний зв'язувати двох або більш зв'язаних або незв'язаних цілей. Білки, що зв'язують подвійний варіабельний домен (DVD), є тетравалентними або полівалентними зв’язувальними білками, що включають дві або більше антигензв’язувальні ділянки. Такі DVD можуть бути моноспецифічними, тобто здатними зв'язувати один антиген, або мультиспецифічними, тобто здатними зв'язувати два або більше антигени. DVD зв’язувальні білки, що включають два важких ланцюги DVD поліпептидів і два легкі ланцюги DVD поліпептидів називаються DVD Ig. Кожна половина DVD Ig включає важкий ланцюг DVD поліпептиду, легкий ланцюг DVD поліпептиду і дві антигензв’язувальні ділянки. Кожна зв’язувальна ділянка включає варіабельний домен важкого ланцюга і варіабельний домен легкого ланцюга з всього 6 CDR, втягнених у зв'язування антигену з антигензв’язувальною ділянкою. Алкілуючі засоби включають алтретамін, AMD-473, AP-5280, апазиквон, бендамустин, бросталіцин, бусульфан, карбоквон, кармустин (BCNU), хлорамбуцил, CLORETAZINE® (ЛАРОМУСТИН, VNP 40101M), циклофосфамід, декарбазин, естрамустин, фотемустин, глюфосфамід, іфосфамід, KW-2170, ломустин (CCNU), мафосфамід, мелфалан, мітобронітол, мітолактол, німустин, N-оксид азотистого іприту, ранімустин, темозоломід, тіотепа, TREANDA® (бендамустин), треосульфан, рофосфамід і подібні. Інгібітори ангіогенезу включають інгібітори ендотелій-специфічного рецептора тирозин кінази (Tie-2), інгібітори рецептора епідермального фактора росту (EGFR), інгібітори рецептора інсуліноподібного фактора росту-2 (IGFR-2), інгібітори матриксної металопротеїнази-2 (MMP-2), інгібітори матриксної металопротеїнази-9 (ММР-9), інгібітори тромбоцитарного фактора росту 12 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 60 (PDGFR), аналоги тромбоспондину, інгібітори рецептора тирозинкінази судинного ендотеліального фактора росту (VEGFR) і подібні. Антиметаболіти включають ALIMTA® (метрексед динатрію, LY231514, MTA), 5-азацитидин, XELODA® (капецитабін), кармофур, LEUSTAT® (кладрибін), клофарабін, цитарабін, цитарабін окфосфат, цитозин арабінозид, децитабін, дефероксамін, доксифлуридин, ефлорнітин, EICAR (5-етиніл-1-β-D-рибофуранозилімідазол-4-карбоксамід), еноцитабін, етнилцитидин, флударабін, 5-фторурацил окремо або в комбінації з лейковорином, GEMZAR® (гемцитабін), гідроксисечовина, ALKERAN® (мелфалан), меркаптопурин, 6-меркаптопурин рибозид, метотрексат, мікофенолова кислота, неларабін, нолатрексед, окфосфат, пелітрексол, пентостатин, ралтитрексед, рибавірин, триапін, триметрексат, S-1, тіазофурин, тегафур, TS-1, видарабін, UFT і подібні. Інгібітори Aurora-кінази включають AZD-1152, MLN-8054, VX-680 і подібні. Інгібітори Bcl-2 білків включають АТ-101 ((-)госипол), GENASENSE® (G3139 або облімерсен (антисмисловий олігонуклеотид, націлений на Bcl-2)), IPI-194, IPI-565, N-(4-(4-((4'-хлор(1,1'біфеніл)-2-ил)метил)піперазин-1-іл)бензоїл)-4-(((1R)-3-(диметиламіно)-1((фенілсульфаніл)метил)пропіл)аміно)-3-нітробензолсульфонамід (АВТ-737), N-(4-(4-((2-(4хлорфеніл)-5,5-диметил-1-циклогекс-1-ен-1-іл)метил)піперазин-1-іл)бензоїл)-4-(((1R)-3(морфолін-4-іл)-1-((фенілсульфаніл)метил)пропіл)аміно)-3((трифторметил)сульфоніл)бензолсульфонамід (АВТ-263), GX-070 (обатоклакс) і подібні. Інгібітори кінази Bcr-Abl включають DASATINIB® (BMS-354825), GLEEVEC® (іматиніб) і подібні. Інгібітори CDK включають AZD-5438, BMI-1040, BMS-032, BMS-387, CVT-2584, флавопіридол, GPC-286199, MCS-5A, PD0332991, PHA-690509, селицикліб (CYC-202, Rросковітин), ZK-304709 і подібні. Інгібітори COX-2 включають АВТ-963, ARCOXIA® (еторикоксиб), BEXTRA® (вальдекоксиб), BMS347070, CELEBREX® (целекоксиб), COX-189 (лумиракоксиб), СТ-3, DERAMAXX® (деракоксиб), JTE-522, 4-метил-2-(3,4-диметилфеніл)-1-(4-сульфамоїлфеніл-1Н-пірол), МК-663 (еторикоксиб), NS-398, парекоксиб, RS-57067, SC-58125, SD-8381, SVT-2016, S-2474, T-614, VIOXX® (рофекоксиб) і подібні. Інгібітори EGFR включають ABX-EGF, анти-EGFR імуноліпосоми, EGF-вакцину, EMD-7200, ERBITUX® (ектуксимаб), HR3, IgA антитіла, IRESSA® (гефитиніб), TARCEVA® (ерлотиніб або OSI-774), TP-38, EGFR зшитий білок, TYKERB® (лапатиніб) і подібні. Інгібітори рецептора ErbB2 включають СР-724-714, ССІ-1033 (канертиніб), HERCEPTIN® (трастузумаб), TYKERB® (лапатиніб), OMNITARG® (2С4, петузумаб), ТАК-165, GW-572016 (іонафарніб), GW-282974, EKB-569, PI-166, dHER2 (HER2 вакцина), АРС-8024 (HER-2 вакцина), анти-HER/2neu біспецифічні антитіла, B7.her2IgG3, AS HER2 трифункціональні біспецифичні антитіла, mAB AR-209, mAB 2B-1 і подібні. Інгібітори гістон-деацетилази включають депсипептид, LAQ-824, MS-275, трапоксин, субероїланілід гідроксамову кислоту (SAHA), TSA, вальпроеву кислоту і подібні. Інгібітори HSP-90 включають 17-AAG-nab, 17-AAG, CNF-101, CNF-1010, CNF-2024, 17DMAG, гелданаміцин, IPI-504, KOS-953, MTCOGRAB® (людське рекомбінантне антитіло до HSP-90), NCS-683664, PU24FCI, PU-3, радицикол, SNX-2112, STA-9090, VER49009 і подібні. Інгібітори білків апоптозу включають ApoMab (повністю людське афінно-зріле IgG1 моноклональне антитіло, антитіла, які націлені на TRAIL або рецептори смерті (наприклад, проапоптоїдні агоністи рецепторів DR4 і DR5), конатумумаб, ETR2-ST01, GDC0145 (лексатумумаб), HGS-1029, LBY-135, PRO-1762 і тратузумаб. Інгібітори МЕК включають ARRY-142886, ARRY-43162, PD-325901, PD-98059 і подібні. Інгібітори mTOR включають АР-23573, CCI-779, еверолімус, RAD-001, рапаміцин, темсиролімус і подібні. Нестероїдні протизапальні лікарські засоби включають AMIGESIC® (салсалат), DOLOBID® (дифлунізал), MOTRIN® (ібупрофен), ORUDIS® (кетопрофен), RELAFEN® (набуметон), FELDENE® (піроксикам), ібупрофеновий крем, ALEVE® (напроксен), і NAPROSYN® (напроксен), VOLTAREN® (диклофенак), INDOCIN® (індометацин), CLINORIL® (суліндак), TOLECTIN® (толметин), LODINE® (етодолак), TORADOL® (кеторолак), DAYPRO® (оксапрозин) і подібні. Інгібітори PDGFR включають З-451, СР-673, СР-868596 і подібні. Хіміотерапевтичні речовини на основі платини включають цисплатин, ELOXATIN® (оксаліплатин), ептаплатин, лобаплатин, нодаплатин, PARAPLATIN® (карбоплатин), сатраплатин і подібні. Інгібітори Polo-подібної кінази включають BI-2536 і подібні. Аналоги тромбоспондину включають АВТ-510, АВТ-567, TSP-1 і подібні. 13 UA 103351 C2 TM 5 10 15 20 25 30 35 40 45 50 55 Інгібітори VEGF включають AVASTIN® (бевасизумаб), АВТ-869, АЕЕ-788, ANGIOZYME (рибозим, який інгібує ангіогенез (Ribozyme Pharmaceuticals (Boulder CO.) і Chiron, (Emeryville CA)), акситиніб (AG-13736), AZD-2171, CP-547, 632, IM-862, MACUGEN (пегаптаміб), NEXAVAR® (сорафеніб, BAY43-9006), пазопаніб (GW-786034), ваталаніб (РТК-787, ZK-222584), TM SUTENT® (сунитиніб, SU-11248), VEGF пастка, ZACTIMA (вандетаніб, ZD-6474) і подібні. Антибіотики включають інтеркаловані антибіотики акларубіцин, актиноміцин D, амрубіцин, анаміцин, адріаміцин, BLENOXANE® (блеоміцин), даунорубіцин, CAELYX® або MYOCET® (ліпосомальний доксорубіцин), елсамітруцин, епірбуцин, глірбуїцин, ZAVEDOS® (ідарубіцин), мітоміцин С, неморубіцин, неокарзиностатин, пепломіцин, пірарубіцин, ребекаміцин, стималамер, стрептозоцин, VALSTAR® (вальрубіцин), зиностатин і подібні. Інгібітори топоізомерази включають акларубіцин, 9-амінокамптотецин, амонафід, амсакрин, бекатекарин, белотекан, BN-80915, CAMPTOSAR® (гідрохлорид іринотекану), камптотецин, CARDIOXANE® (дексразоксин), дифломотекан, едотекарин, ELLENCE® або PHARMORUBICIN® (епірубіцин), етопозид, ексатекан, 10-гідроксикамптотецин, гліматекан, луртотекан, мітоксантрон, оратецин, пірарбуцин, піксантрон, рубітекан, собузоксан, SN-38, тафлупозид, топотекан і подібні. Антитіла включають AVASTIN® (бевасиксумаб), CD40-специфічні антитіла, chTNT-1/B, деносумаб, ERBITUX® (цетуксимаб), HUMAX-CD4® (занолімумаб), IGF1R-специфічні антитіла, лінтузумаб, PANOREX® (едреколомаб), RENCAREX® (WX-G250), RITUXAN® (ритуксимаб), тицилімумаб, трастузимаб і подібні. Гормональні препарати включають ARIMIDEX® (анастрозол), AROMASTIN® (екземестан), арзоксифен, CASODEX® (бікалутамід), CETROTIDE® (цетрорелікс), дегарелікс, дезлорелін, DESOPAN® (трилостан), дексаметазон, DROGENIL® (флутамід), EVISTA® (ралоксифен), TM AFEMA (фадрозол), FARESTON® (тореміфен), FASLODEX® (фулвестрант), FEMARA® (летрозол), форместан, глюкокортикоїди, HECTOROL® (доксеркальциферол), RENAGEL® (севеламер карбонат), лазофоксифен, лейпроліду ацетат, MEGACE® (мегестрол), MIFEPREX® TM TM (міфепристон). NILANDRON (нілутамід), NOLVADEX® (тамоксифену цитрат), PLENAXIS (абарклікс), преднізон, PROPECIA® (фінастерид), рилостан, SUPREFACT® (бусерелін), TRELSTAR® (лютеїнізуючий гормон-рилізинг фактор (ЛГРФ)), VANTAS® (гістрелин імплант), VETORYL® (трилостан або модрастан), ZOLADEX® (фосрелін, госерелін) і подібні. Дельтоїди і ретиноїди включають сеокальцитол (ЕВ1089, СВ1093), лексакальцитрол (КН1060), фенретинід, PANRETIN® (аліретиноїн), ATRAGEN® (ліпосомальний ретиноїн), TARGRETIN® (бексаротен), LGD-1550 і подібні. Інгібітори PARP включають ABT-888, олапариб, KU-59436, AZD-2281, AG-014699, BSI-201, BGP-15, INO-1001, ONO-2231 і подібні. Рослинні алкалоїди включають, але не обмежуються, вінкристин, вінбластин, віндезин, вінореблін і подібні. Інгібітори протеасом включають VELCADE® (бортезоміб), MG132, NPI-0052, PR-171 і подібні. Приклади імунологічних засобів включають інтерферони й інші засоби, що підсилюють імунітет. Інтерферони включають інтерферон альфа, інтерферон альфа-2а, інтерферон альфа2b, інтерферон бета, інтерферон гама-1а, ACTIMMUNE® (інтерферон гама-1b) або інтерферон гама-n1, їхні комбінації і подібне. Інші засоби включають ALFAFERONE® (IFN-α), BAM-002 (окиснений глютатіон), BEROMUN® (тазонермін), BEXXAR® (тозитумомаб), CAMPATH® (алемтузумаб), CTLA4 (цитотоксичний лімфоцитарний антиген 4), декарбазин, денілейкін, епратузумаб, GRANOCYTE® (ленограстим), лентинан, лейкоцитарний альфа інтерферон, іміхімод, MDX-010 (анти-CTLA-4), вакцина від меланоми, мітумомаб, молграмостим, TM MYLOTARG (гемтузумаб озогаміцин), NEUPOGEN® (філграстим), Onco VAC-CL, OVAREX® (ореговомаб), пемтумомаб (Y-muIIMFG1), PROVENGE® (сипулейцел-Т), саргарамостим, сизофілан, тецелейкін, THERACYS® (Bacillus Calmette-Guerin), убенімекс, VIRULIZIN® (імунотерапевтичний засіб, Lorus Pharmaceuticals), Z-100 (специфічна субстанція Maruyama (SSM)), WF-10 (тетрахлордекаоксид (TCDO)), PROLEUKIN® (альдеслейкін), ZADAXIN® (тималфазин), ZENAPAX® (даклизумаб), ZEVALIN® (90Y-ібритумомаб тиуксетан) і подібні. Модифікатори біологічної відповіді являють собою засоби, які модифікують захисні механізми живих організмів або біологічні відповіді, такі як виживаність, ріст або диференціювання клітин тканин для спрямування їх на набуття протипухлинної активності і включають крестин, лентинан, сизофіран, піцибаніл PF-3512676 (CpG-8954), убенімекс і подібні. Піримідинові аналоги включають цитарабін (ara C або Арабінозид С), цитозин арабінозид, доксифлуридин, FLUDARA® (флударабін), 5-FU (5-фторурацил), флоксуридин, GEMZAR® 14 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 60 (гемцитабін), TOMUDEX® (ратитрексед), TROXATYL® (триацетилуридин троксацитабін) і подібні. Пуринові аналоги включають LANVIS® (тіогуанін) і PURI-NETHOL® (меркаптопурин). Антимітотичні засоби включають батабулін, епотилон D (KOS-862), N-(2-((4гідроксифеніл)аміно)піридин-3-іл)-4-метоксибензолсульфонамід, іксабепилон (BMS 247550), паклітаксел, TAXOTERE® (доцетаксел), PNU100940 (109881), патупілон, XRP-9881 (ларотаксел), вінфлунін, ZK-EPO (синтетичний епотилон) і подібні. Сполуки за даним винаходом також можуть бути використані як радіосенсибілізатори, що підсилюють ефективність променевої терапії. Приклади променевої терапії включають зовнішню променеву терапію, телетерапію, брахітерапію і герметичну, негерметичну витокову променеву терапію і подібне. Крім того сполуки, що мають формулу I, можуть бути скомбіновані з іншими TM хіміотерапевтичними засобами, такими як ABRAXANE (ABI-007), АВТ-100 (інгібітор фарнезилтрансферази), ADVEXIN® (Ad5CMV-p53 вакцина), ALTOCOR® або MEVACOR® (ловастатин), AMPLIGEN® (полі I:полі C12U, синтетична РНК), APTOSYN® (екзисулінд), AREDIA® (памідронова кислота), арглабін, L-аспарагіназа, атаместан (1-метил-3,17-діонандроста-1,4-дієн), AVAGE® (тазаротен), AVE-8062 (похідне комбреастатину), ВАГА2 (мітумомаб), кахектин або кахексин (фактор некрозу пухлин), канваксин (вакцина), CEAVAC® (ракова вакцина), CELEUK® (целмолейкін), CEPLENE® (дигідрохлорид гістаміну), CERVARIX® (вакцина від людського папіломавірусу), CHOP® (C: CYTOXAN® (циклофосфамід); H: TM ADRIAMYCIN® (гідроксидоксорубіцин); О: Вінкристин (ONCOVIN®); Р: преднізон), CYPAT (ципротерону ацетат), комбрестатин А4Р, DAB(389)EGF (каталітичний і транслокаційний домени токсини дифтерії, зшиті за допомогою лінкеру His-Ala з людським епідермальним фактором TM росту) або TransMID-107R (токсини дифтерії), дакарбазин, дактиноміцин, 5,6TM диметилксантенон-4-оцтова кислота (DMXAA), енилурацил, EVIZON (скваламіну лактат), DIMERICINE® (T4N5 ліпосомний лосьйон), дискодермолід, DX-8951f (ексатекану мезилат), ензастаурин, ЕРО906 (епітилон В), CARDASIL® (квадривалентна рекомбінантна вакцина для людського папіломавірусу (типи 6, 11, 16, 18), GASTRIMMUNE®, GENASENSE®, GMK (гангліозидна кон’югована вакцина), GVAX® (вакцина від раку передміхурової залози), галофугінон, гістерелін, гідроксикарбамід, ібандронова кислота, IGN-101, IL-13-PE38, IL-13PE38QQR (цинтредекіну бесудотокс), IL-13-токсин псевдомонади, інтерферон-α, інтерферон-γ, TM TM JUNOVAN або MEPACT (міфамуртид), лонафарніб, 5,10-метилентетрагідрофолат, мілтефозин (гексадецилфосфохолін), NEOVASTAT® (AE-941), NEUTREXIN® (триметрексату глюкуронат), NIPENT® (пентостатин), ONCONASE® (фермент рибонуклеаза), ONCOPHAGE® TM (лікування вакциною меланоми), ONCOVAX® (IL-2 вакцина), ORATHECIN (рубітекан), OSIDEM® (клітинний лікарський препарат на основі антитіл), OVAREX® MAb (мишаче TM моноклональне антитіло), паклітаксел, PANDIMEX (агліконові сапоніни з женьшенем, що включають 20(S)протопанаксадіол (aPPD) і 20(S)протопанаксатриол (aPPT)), панітумумаб, PANVAC®-VF (досліджувана вакцина від раку, пегаспаргаза, PEG інтерферон А, феноксодиол, прокарбазин, ребимастат, REMOVAB® (катумаксомаб), REVLIMID® (леналідомід), RSR13 (ефапроксирал), SOMATULINE® LA (ланреотид), SORIATANE® (ацитретин), стауроспорин (Streptomyces staurospores), талабослат (РТ100), TARGRETIN® (бексаротен), TAXOPREXIN® (DHA-паклітаксел), TELCYTA® (канфосфамід, TLK286), теміліфен, TEMODAR® (темозоломід), тезміліфен, талідомід, THERATOPE® (STn-KLH), тимітаг (2-аміно-3,4-дигідро-6-метил-4-оксо-5TM (4-піридилтіо)хіназоліну дигідрохлорид), TNFERADE (аденовектор: ДНК носій, що містить ген для фактора некрозу пухлин-α), TRACLEER® або ZAVESCA® (босентан), третиноїн (Ретин-А), тетрандрин, TRISENOX® (триоксид миш'яку), VIRULIZIN®, україн (похідне алкалоїдів з рослини великого чистотілу), вітаксин (анти-альфабета3 антитіло), XCYTRIN® (мотексафин гадолінію), TM TM XINLAY (атрасентан), XYOTAX (паклітаксел поліглюмекс), YONDELIS® (трабектедин), ZD6126, ZINECARD® (дексразоксан), ZOMETA® (золендронова кислота), зорубіцин і подібні. Для визначення активності відносно Aurora В характерних сполук за винаходом активний фермент Aurora В (рекомбінантні залишки 1-344) і INCENP (рекомбінантний GST зшитий білок (Upstate)) інкубували в ямках 384-ямкового планшета з біотинільованими гістон Н3-пептидними залишками 1-21 (Upstate), 1 мМ АТФ і різними концентраціями інгібіторів у буферній речовині HEPES, рН 7,4, що містить MgCl2, ортованадат натрію і Triton X-100. Через 1 годину реакцію зупиняли за допомогою ЕДТА й анти-фосфо-гістон Н3 Europium Cryptate (Cis-Bio) і SA-APC (Phycolink, Prozyme) додавали для визначення фосфопептиду. Ступінь фосфорилування визначали по співвідношенню сигналів флуоресценції з розрізненням у часі 665 нм і 615 нм. ІК 50 розраховували шляхом експонентного наближення значень інгібування з концентрацією інгібітору з використанням програмного забезпечення Assay Explorer. 15 UA 103351 C2 5 10 15 20 25 Для визначення Aurora А і С активності характерних сполук за винаходом, активні ферменти Aurora А або С інкубували в ямках 384-ямкового планшета з біотинільованим STK субстратом-2 (Upstate), 1 мМ АТФ і різними концентраціями інгібіторів у буферній речовині Hepes, рН 7,4, що містить MgCl2, ортованадат натрію і Triton X-100. Через 1 годину реакцію зупиняли за допомогою ЕДТА й анти-фосфо-STK антитілом Europium Cryptate (Upstate) і SA-XL665 (Upstate) додавали для визначення фосфопептиду. Ступінь фосфорилування визначали по співвідношенню сигналів флуоресценції з розрізненням у часі 665 нм і 615 нм. ІК 50 розраховували шляхом експонентного наближення значень інгібування з концентрацією інгібітору з використанням програмного забезпечення Assay Explorer. Для визначення активності різних кіназ, використовували аналіз кіназ in vitro флуоресценції з розрізненням у часі (HTRF) (Mathis, G., HTRF® Technology. J Biomol Screen, 1999, 4(6): p.309314; Alfred J. Kolb, Paul V. Kaplita, David J. Hayes, Young-Whan Park, Christine Pernell, John S. Major and Gerard Mathis, Drug Discovery Today, 1998, 3, 333-342. Наприклад для KDR, cKIT, FLT1, CSF1R і FLT3 очищені ферменти змішували з 0,5 мкМ Nбіотинільованого субстрату (біотин-Ahx-AEEEYFFLA-амід (SEQ. ID. 1)), різними концентраціями інгібітору в реакційному буфері (50 мМ HEPES, рН 7,1, 10 мМ MgCl2, 2 мМ MnCl2, 0,1% BSA і 1 мМ DTT, 40 мкл кінцевий об’єм), АТФ (1 мМ кінцева конц.) у чорному 384-ямковому планшеті. Через 60 хвилин інкубації при кімнатній температурі реакцію гасили додаванням буферного розчину ЕДТА (остаточні приблизні концентрації: 30 мМ ЕДТА, 0,1% BSA, 0,1% Triton X-100 і 0,24М KF) і до реакційної суміші додавали розчин засобів, що виявляють (для одержання 0,084 нг/ямку стрептавідину XL-665 (Cis-Bio) і 6,5 нг/ямку антифосфотирозину mAb PT66-K Europium kryptate). Гашеній реакційній суміші дозволяли стояти при кімнатній температурі протягом 3 годин і потім зчитували в детекторі флуоресценції з розрізненням у часі (InVision, Perkin-Elmer) при 620 нм і 665 нм послідовно зі збудженням. Співвідношення між сигналом при 620 нм і 665 нм використовували в розрахунку ІК50. Подробиці для різних кіназ показані в таблиці 1 (таблиця 1 описує «His6» і «His(6)», як SEQ ID NO: 2). Таблиця 1 Фермент KDR cKIT FLT1 CSF-1r FLT3 PDGFR-бета 30 Конструкт ММ (кДа) His6-KDR 789-1354 GST-зшивка His6-Tag M-His(6)-CSF-1R-Q547-C972 M-His(6)-FLT3 Q569-S993 GST-зшивка 63 70 65 50 50 100 HTRF аналізи Ферм. реакція, конц. (нг/ямку) 7 4 10 0,6 20 Таблиця 2 і таблиця 3 демонструють застосовність Прикладів 1-6, як інгібіторів множина кіназ. Таблиця 2 Сімейство VEGRF KDR FLT1 ІК50 (мкМ) ІК50 (мкМ) Приклад 1 2 3 4 5 6 0,00159 0,00265 0,0016 0,00501 0,00183 0,00218 CSF1R ІК50 (мкМ) 16 cKIT ІК50 (мкМ) 0,00342 0,00222 0,00562 0,00787 0,00134 0,00274 0,00125 0,0021 0,00204 0,00429 0,00145 0,0019 Сімейство PDGFR FLT3 ІК50 (мкМ) 0,0013 0,00113 0,00218 0,00193 0,00122 0,00181 0,01953 0,02727 0,02711 0,05305 0,01258 0,00428 UA 103351 C2 Таблиця 3 Aurora В ІК50 (мкМ) 0,00673 0,00787 0,01121 0,01484 0,02893 0,00844 Приклад 1 2 3 4 5 6 5 10 15 20 25 Aurora А ІК50 (мкМ) 0,67542 4,7431 0,24831 3,61985 0,57014 0,3572 АНАЛІЗ CYP3A4 Аналізи (200 мкл кінцевий об’єм) проводили в NUNC поліпропіленових планшетах із глибокими ямками в 50 мМ буфері калію фосфату, рН 7,4 з використанням струшувача планшетів мікротитратора в 37°С інкубаторі. Зібрані мікросоми людської печінки (BD Gentest, 50 мкг/мл) інкубували з 5 концентраціями тестованої сполуки (від 0,1 мкм до 10 мкм), 1 мм НАДФН (Sigma) і 2 мкм мідазоламу (Sigma). Постійну кількість диметилсульфоксиду (1%) додавали до інкубації з тестовними сполуками і кожен аналіз проводили в двох екземплярах. Для експериментів попередньої інкубації (Pre) мікросоми, тестовану сполуку і НАДФН змішували і інкубували 30 хвилин до додавання мідазоламу. Для експериментів спільної інкубації (Со) сполуки, мікросоми і мідазолам змішували, і реакцію починали шляхом додавання НАДФН в ямки. В обох протоколах повну реакцію зупиняли після 10 хвилин струшування шляхом додавання 100 мкл суміші 1/1 ацетонітрилу і метанолу, що містить 0,33 мкм 1гідрокситриазоламу. Для аналізу аліквоту кожної ямки переносили у флакон автоматичного пробовідбірника і 10 мкл вводили у ВЕРХ систему Shimadzu LC-10A, оснащену колонкою YMC-AQ (2,0×50 мм). Компоненти розділяли з використанням градієнта 10% ацетонітрилу - 0,1% оцтової кислоти до 70% ацетонітрилу - 0,1% оцтової кислоти зі швидкістю течії 0,4 мл/хвилину протягом 5 хвилин. Мідазолам, 1-гідрокситриазолам (внутрішній стандарт), 1-гідроксіміазолам і 4-гідроксімідазолам оцінювали кількісною РХ-МС/МС із використанням LCQ Duo (ThermoFinnigan). Співвідношення 1-гідроксимидазоламу (продукт CYP3A4) і внутрішнього стандарту в кожній концентрації сполуки використовували для розрахунку % інгібування активності щодо співвідношення, розрахованого для контрольної інкубації без інгібітору. Під час відсутності НАДФН не спостерігали гідроксилування мідазоламу. Кетоконазол використовували як стандартний інгібітор, що при 0,1 мкМ давав 70-80% інгібування CYP 3A4. ІК50 (концентрація, при якій інгібується 50% ферменту) розраховували для прикладів 1-5 і приклада 6 (описаного як ПРИКЛАД 703 у WO 2005/10009) і вона показана в таблиці 4 нижче. Таблиця 4 Умови інкубації ПРИКЛАД 1 ПРИКЛАД 2 ПРИКЛАД 3 ПРИКЛАД 4 ПРИКЛАД 5 ПРИКЛАД 6 Co Pre Co Pre Co Pre Co Pre Co Pre Co Pre ІК50 (мкМ) >10 >10 >10 >10 >10 >10 >10 >10 >10 >10 0,30 0,76 30 Дані в таблицях 2, 3 і 4 ілюструють здатність сполук за даним винаходом, як інгібіторів множини кіназ з додатковою перевагою зниженого інгібування CYP. 17 UA 103351 C2 5 Сполуки, описані як такі, що мають низьке інгібування СYP або як не інгібуючі CYP, являють собою сполуки з ІК50 >10 мкМ у вищевказаному аналізі. Про структурну гомологію між протеїнкіназами Aurora А, В і С повідомляють у Nature Reviews/Cancer, Vol.4 December 2004. Очікують, що оскільки сполука за даним винаходом інгібує активність кінази Aurora В, вона також може мати властивості інгібітору протеїнкіназ, що мають подібну з нею структурну гомологію, таких як, наприклад, кіназа Aurora А і кіназа Aurora С. Дані для приклада 1 показані в таблиці 5. Таблиця 5 Приклад 1 Aurora В HTRF ІК50 (мкМ) 0,007 Aurora A HTRF ІК50 (мкМ) 0,120 Aurora C HTRF ІК50 (мкМ) 0,001 10 15 20 25 30 35 40 45 50 Отримані дані демонструють застосовність приклада 1 як інгібітора кінази Aurora А і кінази Aurora В і кінази Aurora С. Відповідно очікують, що сполуки за даним винаходом мають застосовність у лікуванні захворювань, протягом яких експресується протеїнкінази, такі як будь-яка або усі з членів сімейства Aurora-кіназ. Про залучення Aurora-кінази в клітинах карциноми підшлункової залози повідомляють у Zhu, J., et al., AURKA Amplification, Chromosome Instability, and centrosome abnormality in human pancreatic carcinoma cells. Cancer Genet. Cytogenet., 2005. 159(1): p.10-17; і Li D., Zhu J., Firozi P.F. et al., Overexpression of oncogenic STK15/BTAK/Aurora A kinase in human pancreatic cancer. Clin. Cancer Re. 2003; 9:991-7. Про залучення Aurora-кінази в недрібноклітинну карциному легень повідомляють у Smith, S.L., et al., Overexpression of Aurora B kinase (AURKB) in primary non-small cell lung carcinoma in frequent, generally driven from one allele, and correlates with the level of genetic instability. Br.J. Cancer, 2005, 93(6): p.719-729. Про залучення Aurora-кінази в рак передміхурової залози повідомляють у Chieffi P., et al., Aurora B expression directly correlates with prostate cancer malignancy. Prostate, 2006. 66(3): p.32633; і Chieffi P., Cozzolino L., Kisslinger A., et al. Aurora B expression directly correlates with prostate cancer malignancy and influences prostate cell proliferation. Prostate 2006; 66:326-33. Про залучення Aurora-кінази в лускатоклітинну карциному голови і шиї повідомляють у Reiter, R., et al., Aurora kinase A messenger RNA overexpression is correlated with tumor progression and shortened survival in head and neck squamous cell carcinoma. Clin Cancer Res, 2006. 12(17): p.5136-41. Про залучення Aurora-кінази в гострий мієлолейкоз повідомляють у Walsby E., Walsh V., Pepper C., Burnett A., and Mills K. Haematologica. 2008 May; 93(5): 662-9. Про залучення Aurora-кінази в рак молочної залози повідомляють у Tanaka T., Kimura M., Matsunaga K., Fukada D., Mori H., Okano Y. Сеntrоsомаl kinase AIK1 is overexpressed in invasive ductal carcinoma of the breast. Cancer Res. 1999; 59:2041-4; Miyoshi Y., Iwao K., Egawa C., Noguchi S. Association of centrosomal kinase STK15/BTAK Mrna espression with chromosomal instability in human breast cancers. Int. J. Cancer 2001; 92:370-3; Hoque A., Carter J., Xia W., et al. loss of Aurora A/STK15/BTAK overexpression correlates with transition of in situ to invasive ductal carcinoma of the breast. Cancer Epidimiol. Biomarkers Prev, 2003; 12:1518-22; Royee M.E., Xia W., Sahin A.A., et al. STK15/Aurora-A expression in primary breast tumors is correlated with nuclear grade but not with prognosis. Cancer 2004; 100:12-9; Bodvarsdottir S.K., Hilmarsdottir H., Birgisdottir V., Steinarsdottir M., Jonasson J.G., Eyfjord J.E., Aurora-A amplification associated with BRCA2 mutation in breast tumours. Cancer Lett 2007; 248:96-102; Sen S., Zhou H., White R.A., A putative Serine/Threonine kinase encoding gene BTAK on chromosome 20q13 is amplified and overexpressed in human breast cancer cell lines. Oncogene 1997; 14:2195-200; Lo Y.L., Yu J.C., Chen S.T. et al, Breast cancer risk associated with genotypic polymorphism of the mitosisregulating gene AuroraA/STK15/BTAK. In. J. Cancer 2005; 115:276-83; Vidarsdottir L., Bodvarsdottir S.K., Hilmasdottir H., Tryggvadottir L., Eyfjord J.E., Breast cancer risk associated with AURKA 91T a polymorphismin relation to BRCA mutations. Cancer Lett 2007; 250:206-12; Cox D.G., Hankinson S.E., Hunter D.J., Polymorphisms of the Aurka (STK15/Aurora kinase) gene and breast cancer risk (United States). Cancer Causes Control 2006; 17:81-3; і Tehatchou S., Wirtenberger M., Hemminki K., et al. Aurora kinases A and B and familial breast cancer risk. Cancer Lett 2007; 247:266-72. 18 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 Про залучення Aurora-кінази в рак легень повідомляють у Smith S.L., Bowers N.L., Betticher D.C., et al. Overexpression of Aurora B kinase (AURBK) in primary non small cell lung carcinoma is frequent, generally driven from one allele and correlates with the level of genetic instability. Br. J. Cancer 2005; 93:719-29; Xu H.T., Ma L., Qi F.J. et al. Expression of Serine Threonine kinase15 is associated with poor differentiation in lung squamous cell carcinoma and adenocarcinoma. Pathol. Int. 2006; 56:375-80; Vischioni B., Oudejans J.J., Vos W., Rodriguez J.A., Giaccone G. Frequent overexpression of Aurora B kinase, a novel drug target, in non-small lung carcinoma patients. Mol. Cancer Ther. 2006; 5:2905-13 і Gu J., Gong Y., Huang M., Lu C., Spitz M.R., Wu X. polymorphisms of STK15 (Aurora-A) gene and lung cancer risk in Caucasians. Carcinogenesis 2007; 28:350-5. Про залучення Aurora-кінази в рак сечового міхура повідомляють у Comperat E., Camparo P., Haus R., et al. Aurora-A/STK-15 is predictive factor for recurrent behavior in non-invasive bladder carcinoma: a study of 128 cases of non-invasive neoplasms. Virchows Arch 2007; 450:419-24; Fraizer G.C., Diaz M.F., Lee L.L., Grossman H.B., Sen S. Aurora-A/STK15/BTAK enhances chromosomal instability in bladder cancer cells. Int. J. Oncol. 2004; 25:1631-9; і Sen S., Zhou H., Zhang R.D., et al. Amplification/overexpression of a mitotic kimase gene in human bladder cancer. J. Natl. Cancer Inst. 2002; 94:1320-9. Про залучення Aurora-кінази в рак стравоходу повідомляють у Tong T., Zhong Y., Kong J. Et al. Overexpression of Aurora-A contributes to malignant development of human esophageal squamous cell carcinoma. Clin. Cancer Res. 2004; 10:7304-10; Yang S.B., Zhou X.B., Zhu H.X., et al. Amplification and overexpression of Aurora-A in esophageal squamous call carcinoma. Oncol. Rep. 2007; 17:1083-8; і Kimura M.T., Mori T., Conroy J., et al. Two functional coding single nucleotide polymorphisms in STK15 (Aurora-A) coordinately increase esophageal cancer risk. Cancer Res. 2005; 65:3548-54. Про залучення Aurora-кінази в рак головного мозку повідомляють у Araki K., Nozaki K., Ueba T., Tatsuka M., Hashimoto N., High expression of Aurora-B/Aurora and IpII-like midbody-associated protein (AIM-1) in astrocytomas. J. Neurooncol. 2004; 67:53-64; Zheng W.F., Navaratne K., Prayson R.A., Weil R.J. Aurora B expression correlates with aggressive behavior in glioblastoma multiforme. J. Clin. Pathol. 2007; 60:218-21; Reichardt W., Jung V., Brunner C., et al. The putative Serine/Threonine kinase gene STK15 on chromosome 20q13.2 is amplified in human gliomas. Oncol. Rep. 2003; 10:1275-9; Klien A., Reichardt W., Jung V., Zang K.D., Meese E., Urbschat S. Overexpression and amplification of STK15 in human gliomas. Int. J. Oncol. 2004; 25:1789-94; і Neben K., korshunov A., Benner A., et al. Microarray based screening for molecular markers N medulloblastoma revealed STK15 as independent predictor for survival. Cancer Res. 2004; 64:3103-11. Про залучення Aurora-кінази в рак печінки повідомляють у Jeng Y.M., Peng S.Y., Lin C.Y., Hsu H.C. Overexpression and amplification of Aurora-A in hepatocellular carcinoma. Clin. Cancer Res. 2004; 10:2065-71. Про залучення Aurora-кінази в рак голови і шиї повідомляють у Zhao X., Li F.C., Li Y.H., et al. [Mutation of p53 and overexpression of STK15 in laryngeal squamous cell carcinoma]. Zhonghua Zhong Liu Za Zhi 2005; 27:134-7; Li F.C., Li Y.H., Zhao X., et al. [Detection of p15 and p16 genes and overexpression of STK15 gene in human laryngeal squamous cell carcinoma]. Zhonghua Yi Xue Za Zhi 2003; 83:316-9; Reiter R., Gais P., Jutting U., et al. Aurora kinase a messenger RNA overexpression is correlated with tumor progression and shortened survival in head and neck squamous cell carcinoma. Clin. Cancer Res. 2006; 12:5136-41; Qi G., Ogawa I., Kudo Y. et al. Aurora-B expression and its correlation with cell proliferation and metastasis in oral cancer. Virchows Arch 2007; 450:297-302; і Tatsuka M., Sato S., Kitajima S., et al. Overexpression of Aurora-A potentiates HRAS-mediated oncogenic transformation and is implicated in oral carcinogenesis. Oncogene 2005; 4:1122-7. Про залучення Aurora-кінази в рак щитовидної залози повідомляють у Sorrentino R., Libertini S., Pallante P.L. et al. Aurora B overexpression associates with the thyroid carcinoma undifferentiated phenotype and is required for thyroid carcinoma cell proliferation. J. Clin. Endocrinol. Metab. 2005; 90:928-35. Про залучення Aurora-кінази в рак яєчників повідомляють у Lassmann S., Shen Y., jutting U., et al. Predictive value of Aurora-A/STK15 expression for late stage epithelial ovarian cancer patients treated by adjuvant chemotherapy. Clin. Cancer Res. 2007; 13:4083-91; і Landen C.N., Jr., Lin Y.G., Immaneni A., et al. Overexpression of the centrosomal protein Aurora-A kinase is associated with poor prognosis in epithelial ovarian cancer patients. Clin. Cancer Res. 2007; 13:4098-104. Про залучення Aurora-кінази в рак нирки повідомляють у Kurahashi T., Miyake H., Hara I., Fujisawa M. Significance of Aurora-A expression in renal cell carcinoma. Urol. Oncol. 2007; 25:12833. 19 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 60 Про залучення Aurora-кінази в рак ендометрія повідомляють у Moreno-Bueno G., SanchezEstevez C., Cassia R., et al. Differential gene expression profile in endometrioid and nonendometrioid endometrial carcinoma: STK15 is frequently overexpression and amplified in nonendometrioid carcinomas. Cancer Res. 2003; 63:5697-702. Про залучення Aurora-кінази в рак шлунка повідомляють у Ju H., Cho H., Kim Y.S., et al. Functional polymorphism 57Val>Ile of Aurora kinase A associated with increased risk of gastric cancer progression. Cancer Lett. 2006; 242:273-9. Про залучення Aurora-кінази в рак товстої кишки повідомляють у Nishida N., Nagasaka T., Kashiwagi K., Boland C.R., Goel A. High copy amplification of the Aurora-A gene is associated with chromosomal instability phenotype in human colorectal cancers. Cancer Biol. Ther. 2007; 6:525-33; Bischoff J.R., Anderson L., Zhu Y., et al. A homologue of drosophila Aurora kinase is oncogenic and amplified in human colorectal cancers. EMBO J. 1998; 17:3052-65; Chen J., Sen S., Amos C.I., et al. Association between Aurora-A kinase polymorphisms and age of onset of hereditary nonpolyposis colorectal cancer in a Caucasian population. Mol. Carcinog. 2007; 46:249-56; Hienonen T., Salovaara R., Mecklin J.P., Jarvinen H., Karhu A., Aaltonen L.A. Preferential amplification of AURKA 91A (Ile31) in familial colorectal cancers. Int. J. Cancer 2006; 118-505-8; і Ewart-Toland A., Briassouli P., de Koning J.P., et al. Identification of Stk6/STK15 as a candidate low-penetrance tumor-susceptibility gene in mouse and human. Nat. Genet. 2003; 34:403-12. Про залучення Aurora-кінази в рак повідомляють у Lin Y.S., et al. Gene expression profiles of the Aurora family kinases. Gene Expr., 2006, 13(1):p.15-26; і Ewart-Toland A., Dai Q., Gao Y.T., et al. Aurora-A/STK15 T + 91A is a general low penetrance cancer susceptibility gene: a meta-analysis of multiple cancer types. Carcinogenesis 2005; 26:1368-73. Про залучення KDR (VEGFR2) у рак і дослідженнях з використанням VEGF-націленої терапії повідомляють у Ellis, Lee M., Hicklin, Daniel J. VEGF-targeted therapy: mechanisms of anti-tumor activity. Nature Reviews Cancer 2008; 8:579-591. Про залучення Aurora-кіназ у рак сечового міхура, рак молочної залози, рак шийки матки, рак товстої кишки, рак ендометрія, рак стравоходу, рак легень, рак яєчників, рак підшлункової залози, рак передміхурової залози, рак прямої кишки, рак шкіри, рак шлунка і рак щитовидної залози повідомляють у Nature Reviews/Cancer, Vol. 4 December, 2004. Сполуки за даним винаходом можуть бути отримані синтетичними хімічними процесами, приклади яких показані в даному описі. Розуміють, що порядок стадій у процесах може варіюватися, що реагенти, розчинники й умови реакції можуть бути замінені такими, специфічно згаданими, і що чутливі компоненти можуть бути захищені і депротектовані, якщо необхідно. Наприклад, 3-бромтієно[3,2-с]піридин-4-амін. Захисні групи для компонентів С(О)ОН включають, але не обмежуються, ацетоксиметил, аліл, бензоїлметил, бензил, бензилоксиметил, трет-бутил, трет-бутилдифенілсиліл, дифенілметил, циклобутил, циклогексил, циклопентил, циклопропіл, дифенілметилсиліл, етил, пара-метоксибензил, метоксиметил, метоксіетоксиметил, метил, метилтиометил, нафтил, паранітробензил, феніл, н-пропіл, 2,2,2-трихлоретил, триетилсиліл, 2-(триметилсиліл)етил, 2(триметилсиліл)етоксиметил, трифенілметил і подібні. Захисні групи для С(О) і С(О)Н компонентів включають, але не обмежуються, 1,3діоксикеталь, діетилкеталь, диметилкеталь, 1,3-дитіанілкеталь, О-метилоксим, О-фенілоксим і подібні. Захисні групи для NH компонентів включають, але не обмежуються, ацетил, аланіл, бензоїл, бензил(фенілметил), бензиліден, бензилоксикарбоніл (Cbz), трет-бутоксикарбоніл (Boc), 3,4диметоксибензилоксикарбоніл, дифенілметил, дифенілфосфорил, форміл, метансульфоніл, пара-метоксибензилоксикарбоніл, фенілацетил, фталоїл, сукциніл, трихлоретоксикарбоніл, триетилсиліл, трифторацетил, триметилсиліл, трифенілметил, трифенілсиліл, паратолуолсульфоніл і подібні. Захисні групи для ВІН і SH компонентів включають, але не обмежуються, ацетил, аліл, алілоксикарбоніл, бензилоксикарбоніл (Cbz), бензоїл, бензил, трет-бутил, третбутилдиметилсиліл, трет-бутилдифенілсиліл, 3,4-диметоксибензил, 3,4диметоксибензилоксикарбоніл, 1,1-диметил-2-пропеніл, дифенілметил, форміл, метансульфоніл, метоксіацетил, 4-метоксибензилоксикарбоніл, пара-метоксибензил, метоксикарбоніл, метил, пара-толуолсульфоніл, 2,2,2-трихлоретоксикарбоніл, 2,2,2трихлоретил, триетилсиліл, трифторацетил, 2-(триметилсиліл)етоксикарбоніл, 2триметилсилілетил, трифенілметил, 2-(трифенілфосфоніо)етоксикарбоніл і подібні. Наступні скорочення мають вказані значення. ADDP означає 1,1’(азодикарбоніл)дипіперидин; AD-mix-β означає суміш (DHQD)2PHAL, K3Fe(CN6), K2CO3 і K2SO4); AIBN означає 2,2’-азобіс(2-метилпропіонітрил); 9-BBN означає 9 20 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 60 борабіцикло(3.3.1)нонан; Ср означає циклопентадієн; (DHQD) 2PHAL означає 1,4-фталазиндіїл діетиловий ефір гідрохінідину; DBU означає 1,8-діазабіцикло(5.4.0)ундек-7-ен; DIBAL означає діізобутилалюмінію гідрид; DIEA означає діізопропілетиламін; DMAP означає N,Nдиметиламінопіридин; DME означає 1,2-диметоксіетан; DMF означає N,N-диметилформамід; dmpe означає 1,2-біс(диметилфосфіно)етан; DMSO означає диметилсульфоксид; dppa означає дифенілфосфорилазид; dppb означає 1,4-біс(дифенілфосфіно)бутан; dppe означає 1,2біс(дифенілфосфіно)етан; dppf означає 1,1’-біс(дифенілфосфіно)фероцен; dppm означає 1,1біс(дифенілфосфіно)метан; EDAC означає 1-(3-диметиламінопропіл)-3-етилкарбодіімід; Fmoc означає фторенілметоксикарбоніл; HATU означає О-(7-азабензотриазол-1-іл)-N,N,N’,N’тетраметилуроніюя гексафторфосфат; HMPA означає гексаметилфосфорамід; HOAT означає 1-гідроксі-7-азабензотриазол; IPA означає ізопропіловий спирт; LDA означає діізопропіламід літію; LHMDS означає біс(гексаметилдисиліламід) літію; MP-BH3 означає макропористий ціаноборогідрид метилполістиролу тіетиламонію; LAH означає алюмогідрид літію; NCS означає N-хлорсукцинімід; PyBOP означає гексафторфосфат бензотриазол-1ілокситрипіролідинофосфонію; TBTU означає тетрафторборат О-бензотриазол-1-іл-N,N,N’,N’тетраметилуронію; TDA-1 означає тріс(2-(2-метоксіетокси)етил)амін; ТЕА означає триетиламін; TFA означає трифтороцтову кислоту; THF означає тетрагідрофуран; NCS означає Nхлорсукцинімід; NMM означає N-метилморфолін; NMP означає N-метилпіролідин; PPh3 означає трифенілфосфін. ПРИКЛАД 1 N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-(3фторфеніл)сечовина ПРИКЛАД 1А 3-(4-амінофеніл)-7-йодтієно[3,2-с]піридин-4-амін Суспензію 3-бромтієно[3,2-с]піридину-4-аміну (13,7 г, 59,7 ммоль), трет-бутил 4-(4,4,5,5тетраметил-1,3,2-діоксаборолан-2-іл)фенілкарбамату (20 г, 62,7 ммоль), тетракіс(трифенілфосфін)паладію(0) (2,5 г, 2,1 ммоль) і Na2CO3 (13,3 г, 125 ммоль) у тетрагідрофурані (150 мл), метанолі (40 мл) і воді (80 мл) дегазували, потім перемішували при зворотному припливі протягом ночі. Реакційну суміш охолоджували до кімнатної температури, потім розподіляли між етилацетатом і водою. Водний шар екстрагували додатковим етилацетатом і комбіновані органічні фракції сушили (з використанням MgSO4), фільтрували і фільтрат концентрували. Залишок очищали за допомогою хроматографії на силікагелі, елюювали за допомогою 50-70% етилацетату-гексанів для одержання сирого трет-бутил 4-(4амінотієно[3,2-с]піридин-3-іл)фенілкарбамату. Розчин сирого продукту (59,7 ммоль на основі 100% виходу) у N,N-диметилформаміді (80 мл) обробляли N-йодсукцинімідом (13,5 г, 59,7 моль - доданим частинами) і отриманий темний розчин перемішували при кімнатній температурі протягом 2 годин, потім розподіляли між водою (500 мл) і етилацетатом (100 мл) з додаванням NaCl для полегшення розділення шарів. Водний шар екстрагували додатковим етилацетатом (275 мл) і комбіновані органічні фракції промивали тіосульфатом натрію (320 мл) і сольовим розчином (50 мл) і потім сушили з використанням MgSO 4, фільтрували і концентрували. Сирий матеріал обробляли TFA (20 мл) і CH2Cl2 (5 мл), перемішували при кімнатній температурі протягом 2 годин, концентрували під потоком азоту, потім концентрували у вакуумі. Тверді речовини розчиняли у воді (100 мл), ретельно обробляли твердим Na 2CO3 до припинення виділення газу і фільтрували, промиваючи додатковою водою. Зібрану тверду речовину сушили для одержання зазначеної в заголовку сполуки у вигляді твердої речовини (забрудненої на прибл. 10% моль PPh3). ПРИКЛАД 1В 2-(4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)-1Н-піразол-1-іл)етанол 4-(4,4,5,5,-тетраметил-1,3,2-діоксаборолан-2-іл)-1Н-піразол (9,66 г, 49,8 ммоль), 1,3діоксолан-2-он (21 г, 238 ммоль) і карбонат цезію (16 г, 49,1 ммоль) комбінували в 100 мл круглодонній колбі. Реакційну суміш нагрівали від кімнатної температури до 100°С в масляній бані, протягом зазначеного часу карбонат танув і служив як розчинник для реакційної суміші, що залишалася густою суспензією. Після нагрівання протягом 3,5 годин реакційну суміш охолоджували до кімнатної температури і розводили етилацетатом, потім фільтрували через целіт, повторно промиваючи етилацетатом. Фільтрат концентрували, потім очищали хроматографією на системі очищення Analogix® Intelliflash™ з використанням колонки SF60-200 g при швидкості струму 80 мл/хв, елююючи як зазначено далі: 5 хвилин у 20% етилацетаті/гексанах, потім піднімали з 40% до 90% етилацетату/гексанів протягом 35 хвилин, потім 100% етилацетату протягом ще 20 хвилин для одержання вказаної в заголовку сполуки. ПРИКЛАД 1С 21 UA 103351 C2 5 10 15 20 25 30 35 40 45 50 55 60 2-(4-(4-аміно-3-(4-амінофеніл)тієно[3,2-с]піридин-7-іл)-1Н-піразол-1-іл)етанол ПРИКЛАД 1А (6 г, 16,34 моль), ПРИКЛАД 1В (4,8 г, 20,16 ммоль), PdCl 2 (dppf) (1,2 г, 1,640 ммоль) і карбонат натрію (4,6 г, 43,4 ммоль) комбінували в тетрагідрофурані (400 мл, метанолі (80 мл) і воді (80 мл)), і реакційну суміш дегазували шляхом барботування N 2 через суміш протягом 1 години. Потім реакційну суміш нагрівали до 80°С протягом 2 годин, потім дозволяли охолонути і розводили 300 мл етилацетату. Суміш розподіляли між H 2O (500 мл) і водний шар екстрагували етилацетатом (2300 мл). Комбіновані органічні екстракти промивали сольовим розчином, сушили (Na2SO4), фільтрували через шар Целіту, концентрували до загального об’єму близько 200 мл, потім залишали стояти протягом ночі. Тверду речовину, що утвориться таким чином, збирали фільтрацією, одержуючи вказану в заголовку сполуку. ПРИКЛАД 1D N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'-(3фторфеніл)сечовина ПРИКЛАД 1С (2 г, 5,69 ммоль) розчиняли в N,N-диметилформаміді (80 мл) і колбу охолоджували в -20°С бані. 1-фтор-3-ізоціанатобензол (0,715 мл, 6,26 ммоль) додавали по краплях і реакційній суміші дозволяли повільно нагрітися до кімнатної температури і перемішували протягом ночі. Реакційну суміш розводили водою (500 мл) і етилацетатом (75 мл) і перемішували для переробки протягом 1 години. Потім суміш вміщували в сепараторну лійку. Після можливості шарам розділитися, нижній водний шар зливали. Біля інтерфази двох шарів знаходилася істотна кількість осаду. Цей матеріал і органічний шар фільтрували, одержуючи тверду речовину. Тверду речовину промивали етилацетатом і сушили для одержання вказаної в заголовку сполуки. 1 H ЯМР (ДМСО-d6) м. ч. 3,80 (кв, J=5,65 Гц, 2Н), 4,23 (т, J=5,59 Гц, 2Н), 4,96 (т, J=5,09 Гц, 1Н), 5,42 (с, 2Н), 6,80 (тд, J=8,31, 2,37 Гц, 1Н), 7,15 (дд, J=8,14, 1,02 Гц, 1Н), 7,32 (тд, J=8,22, 6,95 Гц, 1Н), 7,41 (д, J=8,81 Гц, 2Н), 7,51 (ддд, J=11,70, 2,37, 2,20 Гц, 1Н), 7,50 (с, 1Н), 7,61 (д, J=8,81 Гц, 2Н), 7,91 (д, J=1,02 Гц, 1Н), 8,05 (с, 1Н), 8,15 (д, J=0,68 Гц, 1Н), 8,96 (с, 1Н), 8,99 (с, + 1Н); МС (ESI(+)) m/z 489,1 (M+H) . ПРИКЛАД 2 N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл-N’-[4(дифторметокси)феніл]сечовина Вказану в заголовку сполуку одержували шляхом заміни 1-(дифторметокси)-4ізоціанатобензолу на 1-фтор-3-ізоціанатобензол у ПРИКЛАДІ 1D. 1 H ЯМР (300 МГц, ДМСО-d6) м. ч. 3,80 (кв, J=5,4 Гц, 2Н), 4,23 (т, J=5,6 Гц, 2Н), 4,95 (т, J=5,4 Гц, 1Н), 5,41 (уш.с, 2Н), 7,13 (т, J=74,4 Гц, 1Н), 7,13 (д, J=8,8 Гц, 2Н), 7,39 (д, J=8,5 Гц, 2Н), 7,487,55 (м, 3Н), 7,61 (д, J=8,5 Гц, 2Н), 7,90 (с, 1Н), 8,05 (с, 1Н), 8,15 (с, 1Н), 8,85 (с, 1Н), 8,91 (с, 1Н); + МС (ESI(+)) m/c 537 (M+H) . ПРИКЛАД 3 N-(4-(4-аміно-7-{1-[(2S)-2-гідроксипропіл)-1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл}феніл-N’-(3метилфеніл)сечовина Вказану в заголовку сполуку одержували, слідуючи методикам ПРИКЛАДІВ 1В-1D за винятком заміни (S)-4-метил-1,3-діоксолан-2-ону на 1,3-діоксолан-2-он і 1-ізоціанато-3метилбензолу на 1-фтор-3-ізоціанатобензол у ПРИКЛАДАХ 1В і 1D відповідно. 1 H ЯМР (300 МГц, ДМСО-d6) м. ч. 1,09 (д, J=6,10 Гц, 3Н), 2,29 (с, 3Н), 4,01-4,12 (м, 3Н), 4,96 (д, J=4,75 Гц, 1Н), 5,43 (с, 2Н), 6,81 (д, J=7,46 Гц, 1Н), 7,17 (т, J=7,80 Гц, 1Н), 7,26 (app д, J=9,15 Гц, 1Н), 7,32 (с, 1Н), 7,39 (д, J=8,48 Гц, 2Н), 7,50 (с, 1Н), 7,61 (д, J=8,81 Гц, 2Н), 7,90 (д, J=0,68 Гц, 1Н), 8,05 (с, 1Н), 8,13 (д, J=1,02 Гц, 1Н), 8,66 (с, 1Н), 8,86 (с, 1Н); МС (ESI(+)) m/z 499,2 + (M+H) . ПРИКЛАД 4 N-(4-{4-аміно-7-[1-(2-гідрокси-2-метилпропіл)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)N'-(4-метоксифеніл)сечовина ПРИКЛАД 4А 2-метил-1-(4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)-1Н-піразол-1-іл)пропан-2-ол Суміш 4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)-1Н-піразолу (500 мг, 2,57 ммоль), Cs2CO3 (840 мг, 2,57 ммоль) і 2,2-диметилоксирану (2 мл) нагрівали в герметичному флаконі при 120°С протягом 3 хвилин при перемішуванні в мікрохвильовій печі Smith Synthesizer (при 300 В), потім дозволяли охолонути і розводили CH2Cl2. Отриману суспензію фільтрували, і фільтрат концентрували для одержання вказаної в заголовку сполуки. ПРИКЛАД 4В N-(4-{4-аміно-7-[1-(2-гідрокси-2-метилпропіл)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)N’-(4-метоксифеніл)сечовина 22 UA 103351 C2 5 10 15 20 25 30 35 40 Вказану в заголовку сполуку одержували, слідуючи методикам ПРИКЛАДІВ 1С-1D за винятком заміни ПРИКЛАДА 4А на ПРИКЛАД 1В і 1-ізоціанато-4-метоксибензолу на 1-фтор-3ізоціанатобензол у ПРИКЛАДАХ 1С і ПРИКЛАДІ 1D, відповідно. 1 H ЯМР (300 МГц, ДМСО-d6) м. ч. 1,12 (с, 6Н), 3,72 (с, 3Н), 4,11 (с, 2Н), 4,76 (с, 1Н), 5,43 (с, 2Н), 6,88 (д, J=9,15 Гц, 2Н), 7,38 (д, J=8,81 Гц, 4Н), 7,49 (с, 1Н), 7,60 (д, J=8,81 Гц, 2Н), 7,89 (д, J=0,68 Гц, 1Н), 8,06 (с, 1Н), 8,11 (д, J=0,68 Гц, 1Н), 8,55 (с, 1Н), 8,80 (с, 1Н); МС (ESI(+)) m/z + 529,3 (M+H) . ПРИКЛАД 5 N-(4-(4-аміно-7-{1-[(2S)-2,3-дигідроксипропіл)-1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл)феніл]N'-(4-метоксифеніл)сечовина ПРИКЛАД 5А (S)-1-((2,2-диметил-1,3-діоксолан-4-іл)метил)-4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2іл)-1Н-піразол Суміш (R)-(2,2-диметил-1,3-діоксолан-4-іл)метилметансульфонату (1,08, 5,15 ммоль), 4(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)-1Н-піразолу (1 г, 5,15 ммоль) і NaH (262 мг, 10,9 ммоль) у N,N-диметилформаміді (25 мл) нагрівали при 90°С протягом 3 годин. Потім дозволяли охолонути до кімнатної температури, гасили водою й екстрагували етилацетатом (3х). Комбіновані органічні фракції промивали сольовим розчином, концентрували і залишок очищали хроматографією на системі очищення Analogix® Intelliflash™ з використанням колонки SF25-25g зі швидкістю потоку 80 мл/хвилину, елююючи за допомогою 0-30% етилацетату:гексанів протягом 30 хвилин для одержання вказаної в заголовку сполуки. ПРИКЛАД 5В (S)-1-(4-(4-аміно-7-(1-((2,2-диметил-1,3-діоксолан-4-іл)метил)-1Н-піразол-4-іл)тієно[3,2с]піридин-3-іл)феніл)-3-(4-метоксифеніл)сечовина Вказану в заголовку сполуку одержували, слідуючи методикам ПРИКЛАДІВ 1C-1D за винятком заміни ПРИКЛАДА 5А на 1В і 1-ізоціанато-4-метоксибензолу на 1-фтор-3ізоціанатобензол у ПРИКЛАДАХ 1В і 1D відповідно. ПРИКЛАД 5С N-[4-(4-аміно-7-{1-[(2S)-2,3-дигідроксипропіл)-1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл)феніл]N’-(4-метоксифеніл)сечовина Розчин ПРИКЛАДА 5В (44 мг, 0,077 мл) у тетрагідрофурані (2 мл) обробляли 2Н HCl (1 мл), потім перемішували при кімнатній температурі протягом 18 годин. Отриману суспензію фільтрували і тверду речовину збирали і сушили для одержання вказаної в заголовку сполуки. 1 H ЯМР (300 МГц, ДМСО-d6) м. ч. 3,72 (с, 3Н), 3,32-3,45 (м, 4Н), 3,84-3,91 (м, 1Н), 4,12 (дд, J=13,90 7,80 Гц, 1Н), 4,34 (дд, J=13,90, 3,73 Гц, 1Н), 6,89 (д, J=9,15 Гц, 2Н), 6,89-6,93 (м, 2Н), 7,38 (д, J=9,15 Гц, 2Н), 7,45 (д, J=8,81 Гц, 2Н), 7,65 (д, J=8,81 Гц, 2Н), 7,94 (с, 1Н), 7,99 (д, J=0,68 Гц, 1Н), 8,06 (с, 1Н), 8,28 (д, J=0,68 Гц, 1Н), 8,72 (с, 1Н), 9,05 (с, 1Н); МС (ESI(+)) m/z 531,2 + (M+H) . ПРИКЛАД 6 N-{4-[4-аміно-7-(1Н-піразол-4-іл)тієно[3,2-с]піридин-3-іл]феніл}-N'-(3-метилфеніл)сечовина Приклад 6 описаний як ПРИКЛАД 703 у WO 2005/10009. Вищевказане призначене для ілюстрації винаходу, але не для його обмеження. Варіанти і зміни, очевидні фахівцю в галузі техніки, знаходяться в рамках винаходу, що визначається формулою винаходу. 45 23 UA 103351 C2 ФОРМУЛА ВИНАХОДУ 5 1. Сполука, яка має формулу І 24 UA 103351 C2 O HN R 2 HN NH2 N 3 R S R 5 10 15 20 1 N N , або її терапевтично прийнятна сіль, де 1 R являє собою гідроксіалкіл; 2 R вибирають із групи, яка складається з алкокси, алкілу, галогену і галоалкокси; і 3 R являє собою водень або алкіл. 2. Сполука за п. 1, яка вибрана з групи: N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл-N'-(3фторфеніл)сечовина; N-(4-{4-аміно-7-[1-(2-гідроксіетил)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл-N'-[4(дифторметокси)феніл]сечовина; N-[4-(4-аміно-7-{1-[(2S)-2-гідроксипропіл]-1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл)феніл]-N'-(3метилфеніл)сечовина; N-(4-{4-аміно-7-[1-(2-гідрокси-2-метилпропіл)-1Н-піразол-4-іл]тієно[3,2-с]піридин-3-іл}феніл)-N'(4-метоксифеніл)сечовина та N-[4-(4-аміно-7-{1-((2S)-2,3-дигідроксипропіл)-1Н-піразол-4-іл}тієно[3,2-с]піридин-3-іл)феніл]-N'(4-метоксифеніл)сечовина. 3. Сполука за п. 1 або її фармацевтично прийнятна сіль, де вказана сполука не інгібує CYP3A4. 4. Композиція, яка містить допоміжну речовину і терапевтично ефективну кількість сполуки за п. 1. 5. Спосіб лікування раку в ссавця, що включає введення йому терапевтично прийнятної кількості сполуки за п. 1. Комп’ютерна верстка В. Мацело Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 25
ДивитисяДодаткова інформація
Автори російськоюMichaelides, Michael, R., Curtin, Michael, L., Frey, Robin, R.
МПК / Мітки
МПК: A61P 35/00, A61K 31/4365, C07D 495/04
Мітки: раку, лікуванні, кіназ, тієно[3,2-c]піридину, інгібітори, похідні, застосування
Код посилання
<a href="https://ua.patents.su/27-103351-pokhidni-tiehno32-cpiridinu-yak-ingibitori-kinaz-dlya-zastosuvannya-v-likuvanni-raku.html" target="_blank" rel="follow" title="База патентів України">Похідні тієно[3,2-c]піридину як інгібітори кіназ для застосування в лікуванні раку</a>
Попередній патент: Пачка
Наступний патент: Пристрій для маніпулювання рейкою, установка для термічної обробки рейок та спосіб маніпулювання рейкою
Випадковий патент: Спосіб вимірювання затухання












