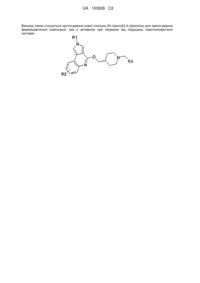
Сполука з серотонінергічною активністю, спосіб її одержання та фармацевтична композиція, яка її містить
Номер патенту: 103026
Опубліковано: 10.09.2013
Автори: Фурлотті Гвідо, Каццолла Нікола, Гугліелмотті Анджело, Алісі Марія Алессандра, Поленцані Лоренцо, Кості Роберта, Ді Санто Роберто
Формула / Реферат
1. Сполука формули (І):
 , (I)
, (I)
у якій:
R1 є атомом водню, лінійною або розгалуженою алкільною групою, яка в оптимальному варіанті містить 1-6 атомів вуглецю, або алкілалкоксигрупою, в оптимальному варіанті з 1-6 атомами вуглецю;
R2 є атомом водню, атомом галогену або лінійною або розгалуженою алкільною групою, яка в оптимальному варіанті містить 1-3 атоми вуглецю, -CF3, -OSO2CF3, -SO2CH3, -SO2NHCH3 або -NHSO2CH3;
R3 є (і) атомом водню; (іі) лінійною або розгалуженою алкільною групою, яка в оптимальному варіанті містить 1-6 атомів вуглецю; (ііі) алкілалкоксигрупою, яка в оптимальному варіанті містить 1-6 атомів вуглецю; (iv) арилалкільною групою або гетероарилалкільною групою, у якій алкільна група в оптимальному варіанті містить 1-3 атоми вуглецю, і арильна або гетероарильна група може бути заміщеною одним або двома замісниками, які можуть бути ідентичними або різними, вибраними з-поміж атома галогену, алкільної групи, яка містить 1-3 атоми вуглецю, алкоксигрупи, яка містить 1-3 атоми вуглецю, гідроксіалкільної групи, яка містить 1-3 атоми вуглецю, -ОН, -NR'R", -NO2, -CF3, -CO2R', R'CON(R")-, R'SO2N(R")- та R'R"NSO2-, де R' та R", які можуть бути ідентичними або різними, є атомом водню або алкільною групою, яка містить 1-3 атоми вуглецю; (v) RivRvNCO(CH2)n-, де n є цілим числом від 0 до 2, і Riv та Rv, які можуть бути ідентичними або різними, є атомом водню, алкільною групою, яка містить 1-3 атоми вуглецю, арильною групою або гетероарильною групою, необов'язково заміщеною одним або двома замісниками, які можуть бути ідентичними або різними, вибраними з-поміж атома галогену, алкільної групи, яка містить 1-3 атоми вуглецю, алкоксигрупи, яка містить 1-3 атоми вуглецю, гідроксіалкільної групи, яка містить 1-3 атоми вуглецю, -ОН, -NO2, -NH2, -CF3, -СО2Н, -СО2-С1-3алкіл, -SO2NH2 та -NHSO2-C1-3алкіл; і (vi) Cg-(CH2)m-, де m є цілим числом від 0 до 2, і Сg є аліциклічною групою з 3-7 атомів вуглецю або насиченою 5- або 6-членною гетероциклічною групою, яка включає принаймні один гетероатом, вибраний з-поміж N та О, необов'язково N-заміщений алкільною групою, яка містить від 1 до 3 атомів вуглецю,
її кислі адиційні солі з фармацевтично прийнятною органічною або мінеральною кислотою та її основні адиційні солі з фармацевтично прийнятною органічною або мінеральною основою.
2. Сполука за п. 1, де R1 є атомом водню або лінійною або розгалуженою алкільною групою, яка в оптимальному варіанті містить 1-6 атомів вуглецю, R2 є атомом водню, атомом галогену, -CF3, -OSO2CF3, -SO2CH3, -SO2NHCH3 або -NHSO2CH3, і R3 є (і) атомом водню; (іі) лінійною або розгалуженою алкільною групою, яка містить 1-6 атомів вуглецю; (ііі) арилалкільною групою або гетероарилалкільною групою, у якій арильна або гетероарильна група може бути заміщеною одним або двома замісниками, які можуть бути ідентичними або різними, вибраними з-поміж атома галогену, алкільної групи, яка містить 1-3 атоми вуглецю, алкоксигрупи, яка містить 1-3 атоми вуглецю, гідроксіалкільної групи, яка містить 1-3 атоми вуглецю, -ОН, -NR'R", -NO2, -CO2R', R'CON(R")-, R'SO2N(R")- та R'R"NSO2-, де R' та R", які можуть бути ідентичними або різними, є атомом водню або алкільною групою, яка містить 1-3 атоми вуглецю; (iv) RivRvNCO(CH2)n-, де n є цілим числом від 0 до 2, і Riv та Rv, які можуть бути ідентичними або різними, є атомом водню, арильною групою або гетероарильною групою; і (v) Cg-(CH2)m-, де m є цілим числом від 0 до 2, і Сg є насиченою гетероциклічною групою, вибраною з групи, яка включає морфолін, піперидин, N-метилпіперазин та піролідин.
3. Сполука за п. 1, де R1 є лінійною або розгалуженою алкільною групою, яка в оптимальному варіанті містить 1-6 атомів вуглецю, R2 є атомом водню, -CF3, -OSO2CF3, -SO2CH3, -SO2NHCH3 або -NHSO2CH3, і R3 є (і) лінійною або розгалуженою алкільною групою, яка містить 1-6 атомів вуглецю; (іі) арилалкільною групою, у якій арильна група може бути заміщеною замісником, вибраним з алкоксигрупи, яка містить 1-3 атоми вуглецю, гідроксіалкільної групи, яка містить 1-3 атоми вуглецю, -NR'R", -CO2R', R'CON(R")-, R'SO2N(R")- та R'R"NSO2-, де R' та R", які можуть бути ідентичними або різними, є атомом водню або алкільною групою, яка містить 1-3 атоми вуглецю; (ііі) RivRvNCO(CH2)n-, де n є цілим числом від 0 до 2, і Riv та Rv, які можуть бути ідентичними або різними, є атомом водню або арильною групою; і (iv) Cg-(CH2)m-, де m є цілим числом від 0 до 2, і Cg є морфоліновим або піперидиновим залишком.
4. Сполука за п. 1, де R1, R2 та R3 є представленими у наступній таблиці:
Сполука
R1
R2
R3
1
Н
Сl
СН3
2
C2H5
CH3
C2H5
3
CH3
H
СН2СН2СН3
4
CH3
Н
СН2-С6Н5
5
СН(СН3)2
Н
СН2-С6Н5
6
CH3
Н
CONH-C6H5
7
CH3
Н
C2H5
9
CH3
Н
СН2-N-морфолін
10
CH3
Н
CH2-C6H4-(4-NO2)
11
CH3
Н
CH2-C6H4-(4-NH2)
12
CH3
Н
СН2-С6Н4-(4-СООС2Н5)
12a
CH3
Н
СН2-С6Н4-(4-СООН)
13
CH3
Н
CH2-С6Н4-(4-NHCOCH3)
14
CH3
Н
CH2-С6Н4-(4-NHSO2CH3)
15
CH3
Н
СН2-С6Н4-(4-СН2ОН)
16
CH3
Н
СН2-С6Н4-(4-СН2СОСН3)
17
CH3
Н
СН2-С6Н4-(2-СООСН3)
17a
CH3
Н
СН2-С6Н4-(2-СООН)
18
CH3
Н
CH2-C6H4-(4-SO2NH2)
19
C2H5
Н
CH2-C6H4-(4-SO2NHCH3)
20
СН2ОСН3
Вr
СН2-N-піроло-(3-ОН)
21
CH3
Сl
CONH-C6H4-(4-NH2)
22
CH2OC2H5
C2H5
СН2-N-піперидин
23
CH3
Н
СН2-С6Н11
24
CH3
H
CH2-C5H9
5. Фармацевтична композиція, яка містить ефективну кількість сполуки формули (І) або її кислої адитивної або основної адитивної солі за будь-яким з попередніх пунктів та принаймні один фармацевтично прийнятний формоутворювач.
6. Фармацевтична композиція за п. 5, яка відрізняється тим, що вищезгадана фармацевтична композиція містить таку кількість сполуки формули (І) або її кислої адитивної або основної адитивної солі, щоб забезпечувався рівень введення від 0,001 до 100 мг/кг/день сполуки формули (І), вираженої у вільній формі.
7. Спосіб одержання сполуки формули (І)
 (I)
(I)
або її фармацевтично прийнятної кислої адитивної або основної адитивної солі, де R1, R2 та R3 мають значення, визначені в одному з пунктів з 1 по 4, який відрізняється тим, що здійснюють реакцію між сполукою формули (II)
 (II)
(II)
та сполукою формули (III)
![]() , (III)
, (III)
де R1, R2 та R3 мають описані вище значення, і X представляє атом галогену.
8. Спосіб одержання за п. 7, який відрізняється тим, що вищезгадану реакцію здійснюють в органічному розчиннику у присутності органічної або мінеральної основної сполуки.
9. Спосіб одержання за будь-яким з пунктів 7 або 8, який відрізняється тим, що вищезгадану реакцію здійснюють у присутності активуючого агента, вибраного з групи, яка включає йодид калію, йодид натрію, йодид цезію, йодид тетрабутиламонію та йодид триметилфеніламонію.
10. Спосіб одержання сполуки формули (І)
 (I)
(I)
або її фармацевтично прийнятної кислої адитивної або основної адитивної солі, де R1, R2 та R3 мають значення, визначені в одному з пунктів з 1 по 4, який відрізняється тим, що здійснюють реакцію між сполукою формули (IV)
 (IV)
(IV)
та сполукою формули (V)
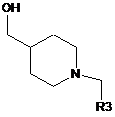 , (V)
, (V)
де R1, R2 та R3 мають описані вище значення.
11. Спосіб одержання за п. 10, який відрізняється тим, що вищезгадану реакцію здійснюють у диполярному апротонному органічному розчиннику у присутності основної сполуки.
12. Спосіб одержання сполуки формули (II):
 , (II)
, (II)
де R1, R2 та R3 мають значення, визначені в одному з пунктів з 1 по 4,
який відрізняється тим, що здійснюють:
(1) реакцію між сполукою формули (IV)
 (IV)
(IV)
та сполукою формули (VI)
 , (VI)
, (VI)
де R1 та R2 мають описані вище значення,
з одержанням сполуки формули (VII):
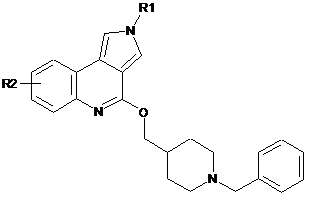 , (VII)
, (VII)
та
(2) реакцію дебензилування азоту піперидину сполуки формули (VII) з одержанням сполуки формули (II), причому вищезгадану реакцію здійснюють шляхом гідрогенізації.
13. Спосіб одержання за п. 12, який відрізняється тим, що вищезгадану реакцію (1) здійснюють у диполярному апротонному органічному розчиннику, вибраному з групи, яка включає кетони, тетрагідрофуран, диметилформамід, диметилсульфоксид, діоксан та ацетонітрил, у присутності основної сполуки, вибраної з групи, яка включає гідроксид натрію та гідрид натрію, і вищезгадану реакцію (2) здійснюють у спиртовому розчиннику в атмосфері водню у присутності паладію на вугіллі як каталізатора.
14. Сполука формули (II):
 , (II)
, (II)
де:
R1 є атомом водню, лінійною або розгалуженою алкільною групою, яка в оптимальному варіанті містить 1-6 атомів вуглецю, або алкілалкоксигрупою, яка в оптимальному варіанті містить 1-6 атомів вуглецю; і
R2 є атомом водню, атомом галогену або лінійною або розгалуженою алкільною групою, яка в оптимальному варіанті містить 1-3 атоми вуглецю.
15. Сполука формули (І)
 (I)
(I)
або її фармацевтично прийнятна кисла адитивна або основна адитивна сіль, де R1, R2 та R3 мають значення, визначені в одному з пунктів з 1 по 4, для фармацевтичного застосування.
16. Застосування сполуки формули (І)
 (I)
(I)
або її фармацевтично прийнятної кислої адитивної або основної адитивної солі, де R1, R2 та R3 мають значення, визначені вище у будь-якому з пунктів з 1 по 4,
для приготування фармацевтичної композиції для лікування порушень перистальтики кишечника та порушень центральної нервової системи, нетримання сечі та серцевої аритмії.
17. Застосування сполуки формули (І)
 (I)
(I)
або її фармацевтично прийнятної кислої адитивної або основної адитивної солі, де R1, R2 та R3 мають значення, визначені в одному з пунктів з 1 по 4,
для приготування фармацевтичної композиції для лікування хронічного болю.
18. Застосування сполуки за п. 17 для приготування фармацевтичної композиції для лікування невропатичного болю, викликаного діабетом, раком, імунодефіцитом, травмами, ішемією, розсіяним склерозом, ішіасом, тригемінальною невралгією та постгерпетичним синдромом.
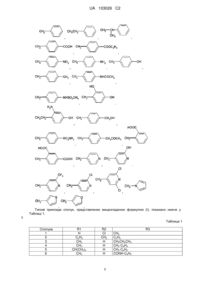
Текст
Реферат: Сполука формули (І) де R1, R2 та R3 є визначеними у представленому описі, та її фармацевтично прийнятні кислі адиційні або основні адиційні солі. Винахід також стосується способу та проміжної сполуки для її отримання, і фармацевтичної композиції, яка її містить. UA 103026 C2 (12) UA 103026 C2 Винахід також стосується застосування нової сполуки 2Н-піроло[3,4-с]хіноліну для приготування фармацевтичної композиції, яка є активною при лікуванні від порушень серотонінергічної системи. UA 103026 C2 5 10 15 20 25 30 35 40 45 50 55 Галузь винаходу Даний винахід стосується нової сполуки 2H-піроло[3,4-c]хіноліну, способу її одержання, її фармацевтичного застосування та фармацевтичної композиції, яка її включає. Винахід також стосується застосування нової сполуки 2H-піроло[3,4-c]хіноліну для приготування фармацевтичної композиції, яка є активною при лікуванні від порушень серотонінергічної системи. Рівень техніки Серед багатьох відомих класів серотонінових рецепторів рецептори 5HT4 було виявлено у сечовому міхурі, у шлунково-кишковій системі, у гладенькому м'язі та серцевому м'язі та у певних ділянках центральної нервової системи (Eglen RM et al., Central 5-HT4 receptors. Trends Pharmacol. Sci. 1995; 16(11): 391-8; Hedge SS and Eglen RM, Peripheral 5-HT4 receptors. FASEB J. 1996; 10(12): 1398-407). Сполуки з агоністичною, частковою агоністичною та антагоністичною активністю щодо рецепторів 5-HT4 мають потенційну перевагу у фармакологічному лікуванні порушень перистальтики кишечника та порушень центральної нервової системи, нетримання сечі та серцевої аритмії (Bockaert J. et al., 5-HT4 receptors. Curr. Drug Targets-CNS Neurol. Dізоrd. 2004, 3(1): 39-51; Gershon MD. Короткий виклад: серотонінові рецептори та транспортери – роль у нормальній та патологічній моториці шлунково-кишкового тракту. Aliment Pharmacol. Ther. 2004; 20 (Suppl.7):3-14). Також відомо, що певні медикаменти, які є активними у серотонінергічній системі, здатні тримати під контролем хронічний біль, зокрема, невропатичний біль. Хронічний біль являє собою низку патологій, від яких у середньому страждає приблизно 1020 % дорослого населення. Хронічний біль зазвичай є пов'язаним з клінічними станами, які характеризуються хронічними та/або дегенеративними ураженнями. Хронічний біль відрізняється від гострого болю, головним чином, тривалістю. Гострий біль триває кілька днів або тижнів у зв'язку з відновленням після випадку, яким було спричинено біль (травми, опіку, перенапруження, хірургічного або стоматологічного втручання і т. ін.). З іншого боку, хронічний біль триває протягом місяців і навіть років, викликаючи м'язове напруження, обмеження рухливості, стомлюваність, втрату апетиту та апатію. Хронічний біль також може виявлятися періодично, з тижневими, місячними або навіть річними інтервалами, або може бути пов'язаним з хронічними патологіями. Типовими прикладами патологій, які характеризуються хронічним болем, є ревматоїдний артрит, остеоартрит, фіброміалгія, невропатії і т. ін. [Ashburn MA, Staats PS. Management of chronic pain. Lancet 1999; 353: 1865-69]. Хронічний біль, зокрема, невропатичний біль, часто послаблює організм і буває причиною втрати працездатності та низької якості життя. Таким чином, внаслідок цього також можуть виникати економічні та соціальні проблеми. До анальгетичних медикаментів, які у даний час застосовують для лікування невропатичного болю, належать нестероїдні протизапальні медикаменти (NSAID), антидепресанти, опіоїдні анальгетики та протисудомні засоби [Woolf CJ, Mannion RJ, Neuropathic pain: aetiology, symptoms, mechanism, and management. Lancet 1999; 353: 19591964]. Однак, як відомо, хронічний біль, зокрема, невропатичний біль, важко піддається лікуванню з застосуванням наявних на даний час ліків. Отже, розробка нових медикаментів завжди є однією з головних цілей фармацевтичної промисловості. Крім того, незважаючи на численні дослідницькі зусилля, спрямовані на виявлення прийнятної анальгетичної сполуки, і досі існує значна кількість пацієнтів, які не знаходять належного лікування від больового стану [Scholz J, Woolf CJ. Can we conquer pain? Nat Neusci. 2002; 5: 1062-76]. Патентні заявки WO 2004/101 548 та WO 2005/013 989 стосуються застосування сполук індазолу для приготування фармацевтичної композиції, яка є активною при лікуванні невропатичного болю. Багато сполук, які діють на серотонінергічну систему, зокрема, як антагоністи рецептора 5HT4, розглядались як такі, що можуть мати анальгетичну активність. Сполуки, які діють на серотонінергічну систему, мають багато несприятливих ефектів та побічних ефектів через їхню низьку селективність щодо різних серотонінергічних рецепторів. Зокрема, відомо, що загальна категорія серотонінергічних рецепторів поділяється на різні підтипи, наприклад, 5HT 1(A-F), 5HT2(a-c), 5HT3, 5HT4, 5HT6 або 5HT7, які по-різному розташовуються у різних системах, наприклад, у центральній та/або периферичній нервовій системі, у травній системі і у серцево-судинній системі. Ефект від взаємодії активних сполук з серотонінергічними рецепторами буває різним, залежно від розташування цих рецепторів. 1 UA 103026 C2 5 10 15 20 25 30 35 40 Низька селективність часто змушує переривати лікування або уникати його у випадках певних типів пацієнтів, у яких, крім наявності хронічного болю, спостерігаються супутні патології у певних системах, таких, як серцево-судинна система. Зокрема, взаємодія з серотонінергічною системою, точніше, з конкретними субрецепторами, такими, як 5HT2a, може викликати небажані явища у серцево-судинній системі, включаючи вплив на серцевий ритм. Сполуки піролохіноліну є загальновідомими. Ці сполуки включають у хімічній формулі пірол, злитий з хіноліном для утворення трициклічної системи. Залежно від позиції злиття, розрізняють різні класи піролохінолінів. Сполуки 2H-піроло[3,4-b]хіноліну було описано у патентній заявці JP 2005/306 774 як фармацевтичні речовини з антибактеріальною активністю. Сполуки піроло[3,4-b]хіноліну було описано у патенті США US 6 335 346 як фармацевтичні речовини з седативним або снодійним ефектом. Сполуки піроло[3,2-c]хіноліну було описано у міжнародній патентній заявці WO 98/05660 як речовини, здатні діяти як інгібітори кінуренін-3-гідроксилази (KYN-OH), які є потенційно корисними для профілактики та/або лікування нейродегенеративних порушень, наприклад, церебральної ішемії та/або гіпоксії, хвороби Паркінсона, епілепсії, хореї Хантингтона, хвороби Альцгеймера і т. ін. Сполуки піроло[3,2-c]хіноліну також було описано у міжнародній патентній заявці WO 99/09029 як речовини, здатні інгібувати секрецію кислоти шлункового соку, які є потенційно корисними для лікування виразок шлунка. Сполуки гексагідро-2H-піроло[3,4-c]хіноліну було описано у патентах США US 4 268 513, US 4 350 814 та US 4 440 768 як фармацевтичні речовини з антипсихотичною, анальгетичною та антидепресантною активністю. Сполуки піроло[3,4-c]хінолін-1-ону було описано у патентах США US 6 323 216 та US 6 413 978 як фармацевтичні речовини з активністю антагоніста серотонінергічного рецептора 5HT 3, які є потенційно корисними як протиблювотні та протикашлеві засоби і при різних патологіях центральної нервової системи, таких, як, наприклад, страх, депресія, шизофренія, психоз, слабоумство Альцгеймера та старече слабоумство. Сполуки 5H-піроло[3,4-c]хіноліну було описано у патенті США US 5 908 932 як фармацевтичні речовини з агоністичною, антагоністичною та зворотно-агоністичною активністю на мозкових рецепторах GABA (γ-аміномасляна кислота) і потенційно корисні при лікуванні від порушень сну, страху та конвульсій, при лікуванні від передозування бензодіазепіну і для поліпшення уваги. Опис винаходу Заявником несподівано було виявлено, що нові сполуки 2H-піроло[3,4-c]хіноліну здатні взаємодіяти з серотонінергічною системою, з високою афінністю щодо серотонінергічного рецептора 5HT4. Крім того, Заявником також було несподівано виявлено, що ці нові сполуки не мають або майже не мають афінності щодо рецептора 5-HT2A, а отже, мінімальний несприятливий вплив на серцево-судинну систему. Таким чином, даний винахід стосується сполуки формули (I): (I) 45 у якій: R1 є атомом водню, лінійною або розгалуженою алкільною групою, яка в оптимальному варіанті містить 1-6 атомів вуглецю, необов'язково заміщеною 1-3 гідроксильними групами, або алкілалкокси-групою, в оптимальному варіанті - з 1-6 атомами вуглецю; 2 UA 103026 C2 5 10 15 20 25 30 35 40 R2 є атомом водню, атомом галогену або лінійною або розгалуженою алкільною групою, яка в оптимальному варіанті містить 1-3 атомів вуглецю, -CF3, -OSO2CF3, -SO2CH3, -SO2NHCH3 або NHSO2CH3; R3 є (i) атомом водню; (ii) лінійною або розгалуженою алкільною групою, яка в оптимальному варіанті містить 1-6 атомів вуглецю; (iii) алкілалкокси-групою, яка в оптимальному варіанті містить 1-6 атомів вуглецю; (iv) арилалкільною групою або гетероарилалкільною групою, у якій алкільна група в оптимальному варіанті містить 1- 3 атомів вуглецю, і арильна або гетероарильна група може бути заміщеною одним або двома замісниками, які можуть бути ідентичними або різними, вибраними з-поміж атома галогену, алкільної групи, яка містить 1-3 атомів вуглецю, алкокси-групи, яка містить 1- 3 атомів вуглецю, гідроксіалкільної групи, яка містить 1-3 атомів вуглецю, -OH, -NR'R", -NO2, -CF3, -CO2R', R'CON(R")-, R'SO2N(R")- та R'R'NSO2-, де R' та R", які можуть бути ідентичними або різними, є iv v атомом водню або алкільною групою, яка містить 1-3 атомів вуглецю; (v) R R NCO(CH2)n-, де n є iv v цілим числом від 0 до 2, і R та R , які можуть бути ідентичними або різними, є атомом водню, алкільною групою, яка містить 1-3 атомів вуглецю, арильною групою або гетероарильною групою, необов'язково заміщеною одним або двома замісниками, які можуть бути ідентичними або різними, вибраними з-поміж атома галогену, алкільної групи, яка містить 1-3 атомів вуглецю, алкокси-групи, яка містить 1-3 атомів вуглецю, гідроксіалкільної групи, яка містить 1-3 атомів вуглецю, -OH, -NO2, -NH2, -CF3, -CO2H, -CO2-C1-3алкілу, -SO2NH2 та -NHSO2-C1-3алкілу; і (vi) Cγ-(CH2)m-, де m є цілим числом від 0 до 2, і C γ є аліциклічною групою з 3- 7 атомів вуглецю або насиченою 5- або 6-членною гетероциклічною групою, яка включає принаймні один гетероатом, вибраний з-поміж N та O, необов'язково N-заміщений алкільною групою, яка містить від 1 до 3 атомів вуглецю, її кислих адиційних солей з фармацевтично прийнятною органічною або мінеральною кислотою та її основних адиційних солей з фармацевтично прийнятною органічною або мінеральною основою. Здатність до взаємодії з серотонінергічною системою, зокрема, з серотонінергічним рецептором 5HT4, робить ці сполуки особливо корисними для лікування від патологій, пов'язаних з цим рецептором, і дає їм потенційну перевагу у фармакологічному лікуванні порушень перистальтики кишечника та порушень центральної нервової системи, нетримання сечі та серцевої аритмії. Зокрема, Заявник спостерігав, що сполуки згідно з даним винаходом є особливо корисними для лікування від хронічного болю, зокрема, невропатичного болю. Висока селективність щодо інших серотонінергічних рецепторів, зокрема, рецепторів 5HT 2a, зменшує несприятливий вплив на серцево-судинну систему, який трапляється у разі застосування інших ліків, які діють на серотонінергічну систему. Таким чином, сполуки згідно з даним винаходом є корисними як фармацевтично активні складові, зокрема, при порушеннях перистальтики кишечника та порушеннях центральної нервової системи, при нетриманні сечі та серцевій аритмії, в оптимальному варіанті – при хронічному болі, у ще кращому варіанті – при невропатичному болі. Таким чином, у другому аспекті даний винахід стосується фармацевтичної композиції, яка включає ефективну кількість сполуки формули (I): (I) 45 де R1, R2 та R3 є такими, як описано вище, її кислих адиційних солей з фармацевтично прийнятною органічною або мінеральною кислотою та її основних адиційних солей з фармацевтично прийнятною органічною або мінеральною основою та принаймні одного фармацевтично прийнятного формоутворювача. Згідно з іншим аспектом, даний винахід стосується сполуки формули (I), як описано вище, та її фармацевтично прийнятних кислих адиційних або основних адиційних солей для фармацевтичного застосування. 3 UA 103026 C2 5 10 15 20 25 30 35 40 45 50 Згідно з ще одним аспектом, даний винахід стосується сполуки формули (I) як описано вище, та її фармацевтично прийнятних кислих адиційних або основних адиційних солей для приготування фармацевтичної композиції, яка є активною при лікуванні від порушень перистальтики кишечника та порушень центральної нервової системи, нетримання сечі та серцевої аритмії. У ще одному оптимальному аспекті даний винахід стосується застосування сполуки формули (I), як описано вище, та її фармацевтично прийнятних кислих адиційних або основних адиційних солей для приготування фармацевтичної композиції, яка є активною при лікуванні від хронічного болю, зокрема, невропатичного болю. Типовими прикладами патологій, які характеризуються невропатичним болем, є діабет, рак, імунодефіцит, травми, ішемія, розсіяний склероз, ішіас, тригемінальна невралгія та постгерпетичний синдром. В оптимальному варіанті, R1 є атомом водню або лінійною або розгалуженою алкільною групою, яка в оптимальному варіанті містить 1-6 атомів вуглецю. У ще кращому варіанті R1 є лінійною або розгалуженою алкільною групою, яка в оптимальному варіанті містить 1-6 атомів вуглецю. В оптимальному варіанті R1 є лінійною або розгалуженою алкільною групою, яка включає від 1 до 3 OH груп. В оптимальному варіанті R2 є атомом водню, атомом галогену, -CF3, -OSO2CF3, -SO2CH3, SO2NHCH3 або -NHSO2CH3. У ще кращому варіанті R2 є атомом водню, -CF3, -OSO2CF3, SO2CH3, -SO2NHCH3 або -NHSO2CH3. В оптимальному варіанті R3 є вибраним з групи, до якої належать (i) атом водню; (ii) лінійна або розгалужена алкільна група, яка в оптимальному варіанті містить 1-6 атомів вуглецю; (iii) арилалкільна група або гетероарилалкільна група, у якій арильна або гетероарильна група може бути заміщеною одним або двома замісниками, які можуть бути ідентичними або різними, вибраними з-поміж атома галогену, алкільної групи, яка містить 1-3 атомів вуглецю, алкоксигрупи, яка містить 1-3 атомів вуглецю, гідроксіалкільної групи, яка містить 1-3 атомів вуглецю, OH, -NR'R", -NO2, -CO2R', R'CON(R")-, R'SO2N(R")- та R'R'NSO2-, де R' та R", які можуть бути ідентичними або різними, є атомом водню або алкільною групою, яка містить 1-3 атомів iv v iv v вуглецю; (iv) R R NCO(CH2)n-, де n є цілим числом від 0 до 2, і R та R , які можуть бути ідентичними або різними, є атомом водню, арильною групою або гетероарильною групою; та (v) Cγ-(CH2)m-, де m є цілим числом від 0 до 2, і Cγ є насиченою гетероциклічною групою, вибраною з групи, яка включає морфолін, піперидин, N-метилпіперазин та піролідин. У ще кращому варіанті R3 є вибраним з групи, до якої належать (i) лінійна або розгалужена алкільна група, яка містить 1-6 атомів вуглецю; (ii) арилалкільна група, у якій арильна група може бути заміщена замісником, вибраним з алкокси-групи, яка містить 1-3 атомів вуглецю, гідроксіалкільної групи, яка містить 1-3 атомів вуглецю, -NR'R", -CO2R', R'CON(R")-, R'SO2N(R")та R'R'NSO2-, де R' та R", які можуть бути ідентичними або різними, є атомом водню або iv v алкільною групою, яка містить 1-3 атомів вуглецю; (iii) R R NCO(CH2)n-, де n є цілим числом від iv v 0 до 2, і R та R , які можуть бути ідентичними або різними, є атомом водню або арильною групою; і (iv) Cγ-(CH2)m-, де m є цілим числом від 0 до 2, і Cγ є морфоліновим або піперидиновим залишком. Арильна або гетероарильна група, яка складає частину арилалкільної або гетероарилалкільної групи, яка може бути представлена групою R3, як описано вище, може бути групою, яка походить від бензолу, нафталіну, піридину, хіноліну, ізохіноліну, піразину, хіноксаліну, піримідину, хіназоліну, піридазину, циноліну, фурану, бензофурану, ізобензофурану, піролу, індолу, ізоіндолу, тіофену, бензотіофену, ізобензотіофену, імідазолу, бензимідазолу, піразолу, індазолу, оксазолу, бензоксазолу, ізоксазол, бензізоксазолу, тіазолу та бензотіазолу; в оптимальному варіанті – бензолу, піридину, фурану, бензофурану та піролу. Типові приклади необов'язково заміщених арилалкільних або гетероарилалкільних груп, які можуть бути представлені описаною вище групою R3, показано нижче: 4 UA 103026 C2 Типові приклади сполук, представлених вищезгаданою формулою (I), показано нижче у Таблиці 1. 5 Таблиця 1 Сполука 1 2 3 4 5 6 R1 H C2H5 CH3 CH3 CH(CH3)2 CH3 R2 Cl CH3 H H H H 5 R3 CH3 C2H5 CH2CH2CH3 CH2-C6H5 CH2-C6H5 CONH-C6H5 UA 103026 C2 Продовження таблиці 1 7 9 10 11 12 12a 13 14 15 16 17 17a 18 19 20 21 22 23 24 5 10 15 20 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 C2H5 CH2OCH3 CH3 CH2OC2H5 CH3 CH3 H H H H H H H H H H H H H H Br Cl C2H5 H H C6H5 CH2-N-морфолін CH2-C6H4-(4-NO2) CH2-C6H4-(4-NH2) CH2-C6H4-(4-COOC2H5) CH2-C6H4-(4-COOH) CH2-C6H4-(4-NHCOCH3) CH2-C6H4-(4-NHSO2CH3) CH2-C6H4-(4-CH2OH) CH2-C6H4-(4-CH2COCH3) CH2-C6H4-(2-COOCH3) CH2-C6H4-(2-COOH) CH2-C6H4-(4-SO2NH2) CH2-C6H4-(4-SO2NHCH3) CH2-N-піроло-(3-OH) CONH-C6H4-(4-NH2) CH2-N-піперидин CH2-C6H11 CH2-C5H9 Типовими прикладами фармацевтично прийнятних мінеральних кислот є: хлористоводнева кислота, бромистоводнева кислота, фосфорна кислота, сірчана кислота та азотна кислота. Типовими прикладами фармацевтично прийнятних органічних кислот є: оцтова кислота, аскорбінова кислота, оксалатна кислота, бурштинова кислота, малеїнова кислота, фумарова кислота, винна кислота, метансульфонова кислота, пара-толуолсульфонова кислота, лимонна кислота, молочна кислота, дубильна кислота та бензойна кислота. Як органічні кислоти, також можуть застосовуватись амінокислоти, такі, як аспарагінова кислота та глутамінова кислота. Типовими прикладами фармацевтично прийнятних органічних та мінеральних основ є: моно-, ди- та триалкіламіни, наприклад метиламін, диметиламін, триметиламін, етиламін, діетиламін, триетиламін, пропіламін, дипропіламін, трипропіламін, етилендіамін, моно-, ди- та триалканоламіни, наприклад, моноетаноламін, діетаноламін та триетаноламін; гуанідин, морфолін, піперидин, піролідин, піперазин, 1-бутилпіперидин, 1-етил-2-метилпіперидин, Nметилпіперазин, 1,4-диметилпіперазин, N-бензилфенілетиламін, N-метилглюкозамін, трис(гідроксиметил)амінометан, аміак, гідроксид натрію, гідроксид кальцію, гідроксид калію, гідроксид алюмінію, гідроксид заліза, гідроксид магнію та гідроксид цинку. Як органічні основи, також можуть застосовуватись амінокислоти, такі, як аргінін та лізин. Описані вище сполуки формули (I) можуть бути одержані згідно з представленою нижче Схемою A, починаючи з нових проміжних сполук формули (II) шляхом реакції з відповідною гало-похідною (III): (Схема A) 25 де R1, R2 та R3 мають вищезазначене значення, і X представляє атом галогену, в оптимальному варіанті – хлору або брому. Реакцію за Схемою A в оптимальному варіанті здійснюють у присутності органічної або мінеральної основної сполуки і в органічному розчиннику. 6 UA 103026 C2 5 10 15 Прикладами корисних органічних основних речовин є аліфатичні або ароматичні аміни, такі, як моно-, ді- або триалкіламіни, моно-, ді- або триалканоламіни, бензиламін, N-метилбензиламін і т. ін. Прикладами корисних мінеральних основ є сильні основи, такі, як NaOH або KOH, або слабкі основи, такі, як NH4OH, Na2CO3, K2CO3, NaHCO3 і т. ін. Прикладами корисних органічних розчинників є диполярні протонні та апротонні органічні розчинники. Типовими прикладами диполярних протонних органічних розчинників є метанол, етанол, пропанол або бутанол. Типовими прикладами диполярних апротонних органічних розчинників є кетони (наприклад, ацетон або метилетилкетон), тетрагідрофуран, диметилформамід, диметилсульфоксид, діоксан, ацетонітрил і т. ін. В оптимальному варіанті реакцію здійснюють з нагріванням, в оптимальному варіанті – при температурі кипіння реакційного розчину. В оптимальному варіанті реакцію здійснюють у присутності активуючого агента, наприклад, йодиду калію, йодиду натрію, йодиду цезію, йодиду тетрабутиламонію або йодиду триметилфеніламонію. Нові проміжні сполуки формули (II) становлять ще один аспект даного винаходу. Нові проміжні сполуки формули (II) можуть бути одержані згідно з представленою нижче Схемою A1: (Схема A1) 20 25 30 Одержання нових проміжних сполук формули (II) спочатку включає реакцію між сполукою 4хлоро-2H-піроло[3,4-c]хіноліну (IV) та (1-бензилпіперид-4-ил)метанолом (VI), з наступною реакцією дебензилування азоту піперидину через гідрогенізацію. Реакцію 4-хлоро-2H-піроло[3,4-c]хіноліну (IV) в оптимальному варіанті здійснюють з натрієвою сіллю (1-бензилпіперид-4-ил)метанолу (VI), яку одержують шляхом реакції сполуки (VI) з сильною основою, наприклад, гідридом натрію. Реакція в оптимальному варіанті відбувається у присутності диполярного апротонного розчинника, вибраного з-поміж описаних вище, в оптимальному варіанті – диметилформаміду. Реакцію здійснюють з нагріванням, в оптимальному варіанті – з дефлегмацією. Реакцію дебензилування в оптимальному варіанті здійснюють шляхом каталітичної гідрогенізації в атмосфері водню, в оптимальному варіанті – з застосуванням як каталізатора паладію на вугіллі у спиртовому розчиннику. Типовим прикладом спиртового розчинника є метанол. Реакцію в оптимальному варіанті здійснюють при кімнатній температурі. В альтернативному варіанті описані вище сполуки формули (I) можуть бути одержані згідно з представленою нижче Схемою B: 7 UA 103026 C2 (Схема В) 5 10 15 20 25 30 35 40 45 50 Реакцію за Схемою B в оптимальному варіанті здійснюють у присутності органічного розчинника, застосовуючи натрієву сіль сполуки (V), яку одержують шляхом реакції сполуки (VI) з сильною основою, наприклад, гідридом натрію. Прикладами корисних органічних розчинників є диполярні апротонні органічні розчинники. Типовими прикладами диполярних апротонних органічних розчинників є ті, які було описано вище, в оптимальному варіанті – N, N-диметилформамід та метилетилкетон. Проміжні сполуки структури (IV) є відомими, і їх одержання описується у ARKIVOC (2004), номер V, 181-195. В оптимальному варіанті фармацевтичні композиції згідно з даним винаходом приготовляють у вигляді придатних дозованих форм, які включають ефективну дозу принаймні однієї сполуки формули (I) або її кислої адиційної солі з фармацевтично прийнятною органічною або мінеральною кислотою або її основної адиційної солі з фармацевтично прийнятною органічною або мінеральною основою та принаймні один фармацевтично прийнятний формоутворювач. Термін "фармацевтично прийнятний формоутворювач" означає, без будь-яких конкретних обмежень, матеріал, який є придатним для приготування фармацевтичної композиції, призначеної для введення людині. Цими матеріалами, які є відомими спеціалістам у даній галузі, є, наприклад, регулятори швидкості вивільнення, зв'язувальні речовини, дезінтегратори, наповнювачі, розріджувачі, барвники, флюїдизатори, суперпластифікатори, мастила, консерванти, стабілізатори, зволожувачі, поглиначі, поверхнево-активні речовини, буфери, солі для регулювання осмотичного тиску, емульгатори, ароматизатори та підсолоджувачі. Прикладами корисних фармацевтично прийнятних формоутворювачів є цукри, такі, як лактоза, глюкоза або цукроза, крохмалі, такі, як кукурудзяний крохмаль та картопляний крохмаль, целюлоза та її похідні, такі, як натрій карбоксиметилцелюлоза, етилцелюлоза та ацетат целюлози, трагакантова камедь, солод, желатин, тальк, масло какао, воски, олії, такі, як арахісова олія, бавовняна олія, сафлорова олія, кунжутна олія, оливкова олія, кукурудзяна олія та соєва олія, гліколі, такі, як пропіленгліколь, поліоли, такі, як гліцерин, сорбіт, маніт та поліетиленгліколь, естери, такі, як етилолеат та етиллаурат, агар-агар, буфери, такі, як гідроксид магнію та гідроксид алюмінію, альгінова кислота, вода, ізотонічні розчини, етанол, буферні розчини, поліестери, полікарбонати, поліангідриди, і т. ін. Прикладами прийнятних дозованих форм є таблетки, капсули, вкриті оболонкою таблетки, гранули, розчини та сиропи для перорального введення; антисептичні пластирі, розчини, пасти, креми та мазі для крізьшкірного введення; супозиторії для ректального введення та стерильні розчини для ін'єкційного або аерозольного введення. Іншими прийнятними формами є форми уповільненого вивільнення або форми на основі ліпосом для перорального або ін'єкційного шляху введення. Якщо цього вимагають конкретні засоби терапії, фармацевтична композиція згідно з даним винаходом може містити інші фармакологічно активні інгредієнти, які застосовуються з одночасним введенням. Кількість сполуки формули (I) або її кислої адиційної солі або основної адиційної солі у фармацевтичній композиції згідно з даним винаходом може коливатись у широких межах, залежно від відомих чинників, наприклад, типу патології, з якою пов'язаний невропатичний біль, що підлягає лікуванню, тяжкості хвороби, маси пацієнта, дозованої форми, вибраного шляху введення, кількості введень на день та ефективності вибраної сполуки формули (I). Однак оптимальна кількість може легко й звично визначатися спеціалістом у даній галузі. Як правило, кількість сполуки формули (I) або її кислої адиційної солі або основної адиційної солі у фармацевтичній композиції згідно з даним винаходом має бути такою, щоб забезпечувався рівень введення від 0,001 до 100 мг/кг/день сполуки формули (I) у перерахунку 8 UA 103026 C2 5 10 15 20 25 30 35 40 45 50 55 60 на вільну сполуку не у формі солі. В оптимальному варіанті рівень введення має становити від 0,05 до 50 мг/кг/день, і у ще кращому варіанті – від 0,1 до 10 мг/кг/день. Дозовані форми фармацевтичної композиції згідно з даним винаходом можуть виготовлятися згідно з технологіями, загальновідомими серед спеціалістів у галузі фармацевтики, включаючи змішування, гранулювання, пресування, розчинення, стерилізацію і т. ін. Активність сполук формули (I) у лікуванні від хронічного болю було продемонстровано за допомогою експериментальної моделі на щурах, яка представляла алодинію, викликану лігатурою сідничного нерва. Як відомо спеціалістам у даній галузі, вищезгадана експериментальна модель може розглядатись як прогностична модель активності у людському організмі. Експериментальна модель лігатури сідничного нерва у щурів представляє невропатію, яка відтворює низку реакцій, подібних до тих, що спостерігаються у людини при численних травматичних та патологічних станах, пов'язаних з невропатичним болем. Причиною цього є те, що лігатура сідничного нерва здатна викликати синдром, пов'язаний з активацією специфічних контурів, призначених для контролювання сприйняття болю, і характеризується виникненням алодинії, гіпералгезії та спонтанного болю. Відомо, що ця модель являє собою дієвий засіб для дослідження медикаментів, призначених для застосування у лікуванні від невропатичного болю у людини, зокрема, у контролюванні таких станів, як алодинія та гіпералгезія. Типовими прикладами людських патологій, які характеризуються дисфункціями, які описуються для вищезгаданої експериментальної моделі і характеризуються наявністю невропатичного болю, є діабет, рак, імунодефіцит, травма, ішемія, розсіяний склероз, ішіас, тригемінальна невралгія та постгерпетичний синдром. Підтвердження зв'язування з серотонінергічними рецепторами здійснювали за допомогою біохімічного випробування на очищених мембранах з рекомбінантних людських клітин, які стійко експресують специфічні рецептори, або з вибраних тваринних тканин, як описано, зокрема, у публікаціях Grossman C.J. et al. (1993), Br. J. Pharmacol. 109: 618-624, Bonhaus D.W. et al. (1995), Br. J. Pharmacol. 115(4): 622-628; та Saucier C. et al. (1997), J. Neurochem. 68(5): 1998-2011. Як відомо спеціалістам у даній галузі, це випробування являє собою прогностичну модель молекулярної взаємодії та селективності з вибраними рецепторами. Випробування 1. Алодинія, викликана лігатурою сідничного нерва у щурів Використовували самців щурів CD, які по надходженню важили 200-250 г. Алодинію викликали лігатурою сідничного нерва лівої задньої кінцівки під анестезією [Seltzer Z, Dubner R, Shir Y. A novel behavioral model of neuropathic pain disorders produced in rats by partial sciatic nerve injury. Pain 1990; 43: 205-218; Bennet GJ, Xie YK. A peripheral mononeuropathyin rat that produces disorders of pain sensation like those seen in man. Pain 1988; 33: 87-107]. Принаймні через два тижні після лігатури сідничного нерва щурів, у яких спостерігалося принаймні 50 % зниження порогу реакції, записували перед вибором втручання. Больовий поріг вимірювали за допомогою пристрою фон Фрея, який дозволяє при застосуванні поступового збільшення тиску на лапу лівої задньої кінцівки щура записувати ноцицептивну реакцію, виражену у грамах, яка відповідає моментові, у який тварина відсмикує кінцівку. Через 30 хвилин, 1, 2 та 4 години лікування больовий поріг, виміряний у контрольних тварин, порівнювали з виміряним у тварин, яких лікували випробуваним продуктом (сполукою 12a з Таблиці 1). Контрольні тварини отримували однаковий індиферентний носій (метилцелюлозу), який застосовували для введення випробуваного продукту. Результати показано на Фігурі 1. 2. Зв'язування з серотонінергічними рецепторами Підтвердження зв'язування з серотонінергічними рецепторами здійснювали з застосуванням очищених мембран з вибраних тваринних тканин або з рекомбінантних людських клітин, які стійко експресують специфічні рецептори. Зв'язування з серотоніновим рецептором 5-HT4 здійснювали з застосуванням стандартних способів, описаних у публікації: Grossman C.J., Kilpatrick G.J. and Bunce K.T. (1993) "Development of a radioligand binding assay for 5-HT4 receptors in guinea-pig and rat brain", Br. J. Pharmacol. 109: 618-624. Як вихідні матеріали застосовували гомогенат смугастого тіла морської свинки та RS23597190 як контрольну сполуку. Випробувані сполуки випробували у шести концентраціях для отримання значень pKi окремих сполук. Зв'язування з людським серотоніновим рецептором 5-HT2A здійснювали стандартним способом, описаним у публікаціях Bonhaus, D.W., Bach C, De Souza A., Salazar F.H., Matsuoka B.D., Zuppan P., Chan H.W., Eglen R.M. (1995): "The pharmacology and distribution of human 5 9 UA 103026 C2 5 hydroxytryptamine 2B (5-HT2B) receptor gene products: comparison with 5-HT2A and 5-HT2C receptors." Br. J. Pharmacol. 115(4): 622-628; та Saucier C, Albert P.R. (1997): "Identification of an endogenous 5-hydroxytryptamine 2A receptor in NIH-3T3 cells: agonist-induced down-regulation involves decreases in receptor RNA and number." J. Neurochem. 68(5): 1998-2011. Випробувані сполуки випробували у шести концентраціях для отримання значень pKi окремих сполук. Показники афінності щодо рецепторів 5-HT4 та 5-HT2A багатьох сполук формули (I) згідно з даним винаходом представлено, відповідно, у 2 та 3 і виражено як pKi, значення якого збільшується пропорційно збільшенню афінності сполуки щодо рецептора. Таблиця 2 Сполука 3 4 5 6 9a 11a 12a 13 15 16 5-HT4 (pKi) 7,83 8,73 6,86 6,88 8,64 8,34 8,65 8,73 8,00 7,72 10 Таблиця 3 Сполука 3 9a 11a 12a 13 15 20 25 30 35 5-HT2 (pKi)
ДивитисяДодаткова інформація
Назва патенту англійськоюCompound with serotoninergic activity, process for preparing it and pharmaceutical composition comprising it
Автори англійськоюAlisi, Maria Alessandra, Cazzolla, Nicola, Costi, Roberta, Di Santo, Roberto, Furlotti, Guido, Guglielmotti, Angelo, Polenzani, Lorenzo
Автори російськоюАлиси Мария Алессандра, Каццолла Никола, Фурлотти Гвидо, Гуглиелмотти Анджело, Гуглиэлмотти Анджело, Поленцани Лоренцо
МПК / Мітки
МПК: A61P 35/00, A61P 25/00, A61P 13/02, A61P 9/00, C07D 471/04, A61K 31/4745, A61P 1/00
Мітки: серотонінергічною, фармацевтична, сполука, містить, одержання, композиція, активністю, спосіб, яка
Код посилання
<a href="https://ua.patents.su/29-103026-spoluka-z-serotoninergichnoyu-aktivnistyu-sposib-oderzhannya-ta-farmacevtichna-kompoziciya-yaka-mistit.html" target="_blank" rel="follow" title="База патентів України">Сполука з серотонінергічною активністю, спосіб її одержання та фармацевтична композиція, яка її містить</a>
Попередній патент: Тверда композиція лікарського засобу уповільненого вивільнення
Наступний патент: Гідролого-гідрохімічний зонд для визначення профілю концентрації розчиненого сірководню (варіанти)
Випадковий патент: Спосіб стерилізації живильних середовищ