Окса- і тіадіазоли та їх застосування як інгібіторів металопротеїназ
Номер патенту: 78275
Опубліковано: 15.03.2007
Автори: Аскоу Ендру Пол, Пен Жіль, Дейвіс Стівен Джон, Жійон Жан-Ів
Формула / Реферат
1. Сполука формули (ІА) або (IВ)
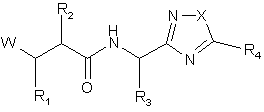 (ІА) ,
(ІА) ,
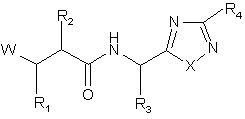 (IB),
(IB),
де
W є НО(С=O)-, HONH(C=O)- або H(C=O)N(OH)-;
X є -О- або -S-;
R1 є
водень;
-ОН або -SH;
фтор або хлор;
-СF3;
(С1-С6)алкіл;
(С1-С6)алкоксигрупа;
(С2-С6)алкеніл;
феніл або заміщений феніл;
феніл-(С1-С6)алкіл або заміщений феніл-(С1-С6)алкіл;
феніл-(С2-С6)алкеніл або заміщений феніл-(С2-С6)алкеніл;
гетероцикліл або заміщений гетероцикліл;
гетероцикліл-(C1-C6)алкіл або заміщений гетероцикліл-(С1-C6)алкіл;
група BSOnA-, де n є 0, 1 або 2, В є водень або (C1-C6)алкіл, феніл, заміщений феніл, гетероцикліл, заміщений гетероцикліл, (C1-C6)ацил, фенацил або заміщений фенацил і А є (C1-C6)алкілен;
-NH2, (C1-C6)алкіламіно або ді(C1-C6)алкіламіногрупа;
аміно-(C1-C6)алкіл, (C1-C6)алкіламіно-(C1-C6)алкіл, ді(C1-C6)алкіламіно-(C1-C6)алкіл, гідроксі-(C1-C6)алкіл, меркапто-(C1-C6)алкіл або карбоксі-(C1-C6) алкіл, де згадані аміно-, гідрокси-, меркаптогрупа або карбоксил факультативно захищені або згаданий карбоксил амідований; або
циклоалкіл, циклоалкеніл або неароматичний гетероцикл, що містить до 3 гетероатомів, кожен з яких може бути (і) заміщений одним або декількома замісниками, вибраними з групи, до якої входять (C1-C6)алкіл, (С2-C6)алкеніл, галоген, ціаногрупа (-CN),
-CO2H, -CO2R, -CONH2, -CONHR, -CON(R)2, -ОН, -OR, оксогрупа, -SH, -SR, -NHCOR та -NHCO2R, де R є (C1-C6)алкіл або бензил, та/або (іі) конденсований з циклоалкілом або гетероциклом;
R2 є група R10-(X)n-(ALK)m-, де
R10 є водень або (C1-C6)алкіл, (С2-C6)алкеніл, (С2-C6)алкініл, циклоалкіл, арил або гетероцикліл, кожен з яких може бути незаміщений або заміщений замісником, вибраним із групи, до якої входять (C1-C12)алкіл, (C1-C12)алкокси-, гідрокси-, меркапто-, (С1-C12)алкілтіо-, аміногрупа, галоген (в тому числі фтор, хлор, бром і йод), трифторметил, ціано-, нітро-, оксогрупа, -СООН, -CONH2, -COORA, –NHCORA, –CONHRA, –NHRA, -NRARB та –CONRARB де RA і RB незалежно один від одного є (C1-С12)алкіл, і
ALK є лінійний або розгалужений двовалентний радикал, вибраний з групи, до якої входять (C1-C6)алкілен, (С2-C6)алкенілен та (С2-C6)алкінілен, і може бути перерваний одним або декількома несуміжними містками -NH-, -О- або -S-, Х є -NH-, -О- або -S-, -NRC або –NCORC, де RC є (C1-C12)алкіл, і m і n незалежно один від одного є 0 або 1;
R3 є бічний ланцюг природної або синтетичної ![]() -амінокислоти;
-амінокислоти;
R4 є факультативно заміщений
(C1-C6)алкіл,
(С2-C6)алкеніл,
(С2-C6)алкініл,
(C1-С3)перфторалкіл,
циклоалкіл,
циклоалкіл(С1-C6-алкіл) -,
циклоалкеніл,
циклоалкеніл(C1-C6-алкіл)-,
феніл,
феніл(С1-C6-алкіл)-,
нафтил,
неароматичний гетероцикліл,
неароматичний гетероцикліл(C1-C6-алкіл)-,
гетероарил або
гетероарил(C1-C6-алкіл)-;
або її фармацевтично прийнятна сіль, гідрат або сольват.
2. Сполука за п. 1, яка відрізняється тим, що має формулу (ІА).
3. Сполука за п. 1, яка відрізняється тим, що має формулу (ІВ).
4. Сполука за будь-яким попереднім пунктом, яка відрізняється тим, що W є HONH(C=O)-.
5. Сполука за будь-яким попереднім пунктом, яка відрізняється тим, що Х є -O-.
6. Сполука за будь-яким попереднім пунктом, яка відрізняється тим, що R1 є
водень, гідроксил, фтор, хлор, метил, метоксигрупа, трифторметил, етил, н-пропіл, аліл, фенілпропіл, циклопропілметил, фенілпроп-2-еніл, тієнілсульфанілметил, тієнілсульфінілметил або тієнілсульфонілметил; або
(C1-С4)алкіл, наприклад, метил, етил, н-пропіл або н-бутил, заміщений замісником, вибраним із групи, до якої входять фталімідогрупа, 1,2-диметил-3,5-діоксо-1,2,4-триазолідин-4-іл, 3-метил-2,5-діоксо-1-імідазолідиніл, 3,4,4-триметил-2,5-діоксо-1-імідазолідиніл, 2-метил-3,5-діоксо-1,2,4-оксадіазол-4-іл, 3-метил-2,4,5-триоксо-1-імідазолідиніл, 2,5-діоксо-3-феніл-1-імідазолідиніл, 2-оксо-1-піролідиніл, 2,5-діоксо-1-піролідиніл або 2,6-діоксопіперидиніл, 5,5-диметил-2,4-діоксо-3-оксазолідиніл, гексагідро-1,3-діоксопіразоло-[1,2,а][1,2,4]-триазол-2-іл, нафталімідогрупа (тобто 1,3-дигідро-1,3-діоксо-2Н-бенз[f]ізоіндол-2-іл), 1,3-дигідро-1-оксо-2Н-бенз[f]ізоіндол-2-іл, 1,3-дигідро-1,3-діоксо-2Н-піроло[3,4-b]хінолін-2-іл та 2,3-дигідро-1,3-діоксо-1Н-бенз[d,е]ізохінолін-2-іл; або
циклогексил, циклооктил, циклогептил, циклопентил, циклобутил, циклопропіл, тетрагідропіраніл або морфолініл.
7. Сполука за будь-яким із пп. 1-5, яка відрізняється тим, що R1 є водень, гідроксил, (С2-С4)алкеніл або (C1-С4)алкоксигрупа.
8. Сполука за будь-яким із пп. 1-5, яка відрізняється тим, що R1 є водень, гідроксил, фтор, метоксигрупа, циклопентил, н-пропіл або аліл.
9. Сполука за будь-яким із пп. 1-8, яка відрізняється тим, що R2 є (C1-С12)алкіл, (С3-C6)алкеніл або (С3-C6)алкініл;
циклоалкіл(C1-C6-алкіл)-;
феніл(С1-C6-алкіл)-, феніл(С3-C6-алкеніл)- або феніл(С3-C6-алкініл)-, факультативно заміщений при згаданому фенільному циклі;
гетероарил(C1-C6-алкіл)-, гетероарил(С3-C6-алкеніл)- або гетероарил(С3-C6-алкініл)-, факультативно заміщений при згаданому гетероарильному циклі;
4-фенілфеніл(С1-C6-алкіл)-, 4-фенілфеніл(С3-C6-алкеніл)-, 4-фенілфеніл(С3-C6-алкініл)-, 4-гетероарилфеніл(C1-C6-алкіл)-, 4-гетероарилфеніл(С3-C6-алкеніл)-, 4-гетероарилфеніл(С3-C6-алкініл)-, факультативно заміщений при кінцевому фенільному або гетероарильному циклі; або
феноксі(C1-C6-алкіл)- або гетероарилоксі(C1-C6-алкіл)-, факультативно заміщений при згаданому фенільному або гетероарильному циклі.
10. Сполука за будь-яким із пп. 1-8, яка відрізняється тим, що R2 є метил, етил, н- або ізопропіл, н-, ізо- або трет-бутил, н-пентил, н-гексил, н-гептил, н-ноніл, н-децил, проп-2-ін-1-іл, циклогексилетил, циклопентилметил, 3-фенілпроп-2-ін-1-іл, 3-(2-хлорфеніл)проп-2-ін-1-іл, бензилфенілпропіл, 4-хлорфенілпропіл, 4-метилфенілпропіл, 4-метоксифенілпропіл, феноксибутил, 3-(4-піридилфеніл)пропіл-, 3-(4-(4-піридил)феніл)проп-2-ін-1-іл, 3-((4-феніл)феніл)пропіл-, 3-((4-феніл)феніл)проп-2-ін-1-іл та 3-[(4-хлорфеніл)-феніл]пропіл-.
11. Сполука за будь-яким із пп. 1-8, яка відрізняється тим, що R2 є (C1-С4)алкіл, 3-8-членний циклоалкіл-(С1-С4)алкіл-, який факультативно містить у згаданому циклі 1-3 гетероатоми, вибрані із групи, до якої входять N, О і S або арил-(C1-С4)алкіл.
12. Сполука за будь-яким із пп. 1-8, яка відрізняється тим, що R2 є бензил, н-бутил, ізобутил, н-гексил, циклопентилметил, 4-етоксифенілпропіл або фенілпропіл.
13. Сполука за будь-яким з попередніх пунктів, яка відрізняється тим, що R3 є (C1-C6)алкіл, феніл, 2-, 3- або 4-піридил, 2- або 3-тієніл, 2-, 3- або 4-гідроксифеніл, 2-, 3- або 4-метоксифеніл, 2-, 3- або 4-піридилметил, бензил, 2-, 3- або 4-гідроксибензил, 2-, 3- або 4-бензилоксибензил, 2-, 3- або 4-C1-C6-алкоксибензил або бензилоксі(C1-C6алкіл)-; або
характеристична група природної ![]() -амінокислоти, в якій будь-яка функціональна група може бути захищеною, будь-яка аміногрупа може бути ацилованою і будь-яка карбоксильна група може бути амідованою; або
-амінокислоти, в якій будь-яка функціональна група може бути захищеною, будь-яка аміногрупа може бути ацилованою і будь-яка карбоксильна група може бути амідованою; або
група -[Аlk]nR6, де Alk є (C1-C6)алкіл або (С2-C6)алкеніл, факультативно перерваний одним або декількома атомами -О- чи -S- або групами -N(R7)- [де R7 є атом водню або (C1-C6)алкіл], n є 0 або 1, і R6 є факультативно заміщена циклоалкільна або циклоалкенільна група; або
бензильна група, заміщена при фенільному циклі групою формули -OCH2COR8, де R8 є гідроксил, аміно-, (С1-C6)алкокси-, феніл-(C1-C6)алкокси-, (C1-C6)алкіламіно-, ді((C1-C6)алкіл)аміно-, феніл-(C1-C6)алкіламіногрупа, залишок амінокислоти або галогенангідриду амінокислоти, її складного ефіру або аміду, причому згаданий залишок приєднаний через амідний зв'язок, згадана амінокислота вибрана з групи, до якої входять гліцин, ![]() - або
- або ![]() -аланін, валін, лейцин, ізолейцин, фенілаланін, тирозин, триптофан, серин, треонін, цистеїн, метіонін, аспарагін, глутамін, лізин, гістидин, аргінін, глутамінова кислота та аспарагінова кислота; або
-аланін, валін, лейцин, ізолейцин, фенілаланін, тирозин, триптофан, серин, треонін, цистеїн, метіонін, аспарагін, глутамін, лізин, гістидин, аргінін, глутамінова кислота та аспарагінова кислота; або
гетероцикл-(C1-C6)алкіл, незаміщений або заміщений при згаданому гетероциклі одним або двома замісниками, вибраними з групи, до якої входять галоген, нітро-, карбокси-, (C1-C6)алкокси-, ціаногрупа, (C1-C6)алканоїл, трифторметил(C1-C6)алкіл, гідроксил, форміл, аміно-, (C1-C6)алкіламіно-, ді-(C1-C6)алкіламіно-, меркапто-, (C1-C6)алкілтіогрупа, гідроксі(C1-C6)алкіл, меркапто(C1-C6)алкіл або (C1-C6)алкілфенілметил; або
група –CRaRbRc, в якій:
кожний з Ra, Rb і Rc незалежно від інших є водень, (C1-C6)алкіл, (С2-C6)алкеніл, (С2-C6)алкініл, феніл(C1-C6)алкіл, (С3-С8)циклоалкіл;
або
Rc є водень і Ra і Rb незалежно один від одного є феніл або гетероарил, наприклад піридил; або
Rc є водень, (C1-C6)алкіл, (С2-C6)алкеніл, (С2-C6)алкініл, феніл(C1-C6)алкіл або (С3-С8)циклоалкіл, і Ra і Rb разом з атомом вуглецю, до якого вони приєднані, утворюють 3-8-членний циклоалкіл або 5-6-членний гетероцикл; або
Ra, Rb і Rc разом з атомом вуглецю, до якого вони приєднані, утворюють трициклічну групу (наприклад адамантил); або
кожний з Ra і Rb незалежно від іншого є (C1-C6)алкіл, (С2-C6)алкеніл, (С2-C6)алкініл, феніл(С1-C6)алкіл або група, яка відповідає поданому нижче визначенню для Rс, за винятком водню, або Ra і Rb разом з атомом вуглецю, до якого вони приєднані, утворюють циклоалкіл або гетероцикл, a Rc є водень, -ОН, -SH, галоген, -CN, -СO2Н, (C1-С4)перфторалкіл, -СН2OН, -СO2(C1-C6)алкіл, -O(C1-C6)алкіл, -O(С2-C6)алкеніл, -S(С1-C6)алкіл, -SO(С1-C6)алкіл, -SO2(С1-C6)алкіл, -S(С2-C6)алкеніл, -SO(С2-C6)алкеніл, -SO2(С2-C6)алкеніл або група -Q-W, де Q є зв'язок або -О-, -S-, -SO- або -SO2-, і W є феніл, фенілалкіл, (С3-С8)циклоалкіл, (С3-С8)циклоалкілалкіл, (С4-С8)циклоалкеніл, (С4-С8)циклоалкенілалкіл, гетероарил або гетероарилалкіл, причому група W може бути факультативно заміщена одним або декількома замісниками, незалежно вибраними з групи, до якої входять гідроксил, галоген, -CN, -СO2H, -СO2(С1-C6)алкіл, -CONH2, -СОNH(С1-C6)алкіл, -СОNН(С1-C6алкіл)2, -СНО, -СН2OН, (С1-С4)перфторалкіл, -O(С1-C6)алкіл, -S(С1-C6)алкіл, -SO(C1-C6)алкіл, -SO2(C1-C6)алкіл, -NO2, -NH2, NН(C1-C6)алкіл, -N((C1-C6)алкіл)2, -NHCO(C1-C6)алкіл, (C1-C6)алкіл, (С2-C6)алкеніл, (С2-C6)алкініл, (С3-С8)циклоалкіл, (С4-С1)циклоалкеніл, феніл або бензил.
14. Сполука за будь-яким із пп. 1-12, яка відрізняється тим, що R3 є бензил, феніл, циклогексилметил, піридин-3-ілметил, трет-бутоксиметил, ізо-пропіл, ізо-бутил, втор-бутил, трет-бутил, 1-бензилтіо-1-метилетил, 1-метилтіо-1-метилетил або 1-меркапто-1-метилетил.
15. Сполука за будь-яким із пп. 1-12, яка відрізняється тим, що R3 є (C1-С4)алкіл або арил-(C1-С4)алкіл.
16. Сполука за будь-яким із пп. 1-12, яка відрізняється тим, що R3 є бензил, трет-бутоксиметил, ізо-пропіл, трет-бутил або ізо-бутил.
17. Сполука за будь-яким з попередніх пунктів, яка відрізняється тим, що R4 є факультативно заміщений (C1-C6)алкіл; (С3-С8)циклоалкіл; феніл; моноциклічний гетероцикл або моноциклічний гетероарил.
18. Сполука за будь-яким із пп. 1-16, яка відрізняється тим, що R4 є C1-С4-алкіл, арил, гетероарил, 3-8-членний циклоалкіл, що факультативно містить у згаданому циклі 1-3 гетероатоми, вибрані з групи, до якої входять N, О і S, арил-(C1-С4)алкіл або гетероарил-(C1-С4)алкіл.
19. Сполука за будь-яким із пп. 1-16, яка відрізняється тим, що R4 є факультативно заміщений метил, етил, н- або ізопропіл, проп-2-іл, трет-бутил, циклопропіл, циклопентил; феніл; морфоліногрупа; тієніл або фураніл.
20. Сполука за п. 2, яка відрізняється тим, що R1 є -ОН; W є -C(=O)NHOH, Х є -О- і R3 є трет-бутил.
21. Сполука за п. 2, яка відрізняється тим, що R1 є -ОН; W є -C(=O)NHOH, Х є -О-, R3 є трет-бутил, a R2 є С1-С12-алкіл або феніл(C1-C12-алкіл)-, чи гетероарил(C1-C6-алкіл)-, факультативно заміщений при згаданому фенільному або гетероарильному циклі.
22. Сполука за п. 2, яка відрізняється тим, що R1 є -ОН; W є -C(=O)NHOH, Х є -О-, R3 є трет-бутил, а R2 є фенілпропіл- або етоксифенілпропіл.
23. Сполука за п. 2, яка відрізняється тим, що R1 є -ОН; W є -C(=O)NHOH, Х є -О-, R3 є трет-бутил, а R4 є розгалужений С1-С6-алкіл, циклоалкіл, феніл, гетероарил, феніл(C1-C6-алкіл)- або гетероарил(C1-C6-алкіл)-.
24. Сполука за п. 2, яка відрізняється тим, що R1 є -ОН; W є -C(=O)NHOH, Х є -О-, R3 є трет-бутил, R2 є етоксифенілпропіл, а R4 є феніл або гетероарил.
25. Сполука за п. 3, яка відрізняється тим, що W є -C(=O)NHOH і Х є -O-.
26. Сполука за п. 3, яка відрізняється тим, що W є -C(=O)NHOH, Х є -О-, а R3 є трет-бутил.
27. Сполука за п. 3, яка відрізняється тим, що W є -C(=O)NHOH, Х є -О-, а R1 є -ОН, (C1-C6)алкоксигрупа або (С2-C6)алкеніл.
28. Сполука за п. 3, яка відрізняється тим, що W є -C(=O)NHOH, Х є -О-, R1 є -ОН, (C1-C6)алкоксигрупа або (С2-C6)алкеніл, R3 є трет-бутил або бензил і R4 є ізопропіл.
29. Сполука формули (ІА) за п. 1, де
Х є -O-;
W є HONH(C=O)-;
R1 є -ОН;
R2 є ізобутил;
R3 є трет-бутил;
R4 є 2-тієніл.
30. Сполука, вибрана з групи, до якої входять:
3R-[2,2-диметил-1S-(5-феніл-[1,2,4]оксадіазол-3-іл)-пропілкарбамоїл]-2S-гідрокси-5-метилгексангідроксамова кислота,
3R-[2,2-диметил-1S-(5-феніл-[1,2,4]оксадіазол-3-іл)-пропілкарбамоїл]-2R-гідрокси-5-метилгексангідроксамова кислота,
3R-[2,2-диметил-1S-(3-феніл-[1,2,4]оксадіазол-5-іл)-пропілкарбамоїл]-2S-гідрокси-5-метилгексангідроксамова кислота,
2R-[3-(4-етоксифеніл)-пропіл]-N1-[1S-(5-тіофен-2-іл-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропіл]-3S,N4-дигідроксисукцинамід,
2S-гідрокси-3R-[1S-(5-ізопропіл-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл]-5-метилгексангідроксамова кислота,
2S-гідрокси-3R-[1S-(5-фуран-2-іл-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл]-5-метилгексангідроксамова кислота,
2S-гідрокси-3R-[1S-(5-циклопентилметил-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл]-5-метилгексангідроксамова кислота,
2S-гідрокси-3R-[1S-(5-тіофен-2-ілметил-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл] -5-метилгексангідроксамова кислота,
2S-гідрокси-3R-[1S-(5-етил-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл]-5-метилгексангідроксамова кислота,
2S-гідрокси-3R-[1S-(5-циклопентил-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл]-5-метилгексангідроксамова кислота,
2S-гідрокси-3R-[1S-(5-бензил-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл]-5-метилгексангідроксамова кислота,
2S-гідрокси-3R-[1S-(5-ізобутил-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл]-5-метилгексангідроксамова кислота,
2S-гідрокси-3R-[1S-(5-трет-бутил-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл]-5-метилгексангідроксамова кислота,
3R-[1S-(5-тіофен-2-іл-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл]-5-метилгексангідроксамова кислота,
2S-гідрокси-3R-[1S-(5-(2,2-диметилпропіл)-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл]-5-метилгексангідроксамова кислота,
2S-гідрокси-3R-[1S-(5-n-толіл-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл]-5-метилгексангідроксамова кислота,
2S-гідрокси-3R-[1S-(5-циклопропіл-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл]-5-метилгексангідроксамова кислота,
2S-гідрокси-3R-[1S-(5-метил-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл]-5-метилгексангідроксамова кислота,
2S-гідрокси-3R-[15-(3-ізопропіл-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл]-5-метилгексангідроксамова кислота,
2S,N1-дигідрокси-3R-ізобутил-N4-[2-метил-15-(3-феніл-[1,2,4]оксадіазол-5-іл)-пропіл]-сукцинамід,
2S-аліл-5-метил-3R-[2-феніл-1S-(3-феніл-[1,2,4]оксадіазол-5-іл)-етилкарбамоїл]-гексангідроксамова кислота,
2S-аліл-5-метил-3R-[2-феніл-1S-(3-ізопропіл-[1,2,4]оксадіазол-5-іл)-етилкарбамоїл]-гексангідроксамова кислота,
2S-аліл-3R-[2,2-диметил-1S-(3-метил-[1,2,4]оксадіазол-5-іл)-пропілкарбамоїл]-5-метилгексангідроксамова кислота,
3R-[2,2-диметил-1S-(3-феніл-[1,2,4]оксадіазол-5-іл)-пропілкарбамоїл]-5-метилгексангідроксамова кислота,
2S-метокси-5-метил-3R-[1S-(3-метил-[1,2,4]оксадіазол-5-іл)-2-фенілетилкарбамоїл]-гексангідроксамова кислота,
3R-[2,2-диметил-1S-(3-феніл-[1,2,4]оксадіазол-5-іл)-пропілкарбамоїл]-гептадеканова кислота,
3R-[2,2-диметил-1S-(3-феніл-[1,2,4]оксадіазол-5-іл)-пропілкарбамоїл]-нонадеканова кислота,
6-(4-хлорфеніл)-3R-[2,2-диметил-1S-(5-феніл-[1,2,4]оксадіазол-3-іл)-пропілкарбамоїл]-гексанова кислота,
6-(4-хлорфеніл)-3R-[2,2-диметил-1R-(5-феніл-[1,2,4]оксадіазол-3-іл)-пропілкарбамоїл]-гексанова кислота,
3R-[2,2-диметил-1S-(5-тіофен-2-іл-[1,2,4]оксадіазол-3-іл)-пропілкарбамоїл]-2S-гідрокси-5-метилгексанова кислота,
3R-[1S-(5-фуран-2-іл-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл]-2S-гідрокси-5-метилгексанова кислота
2R-циклопентилметил-3S,N4-дигідрокси-N1-[1S-(3-ізопропіл-[1,2,4]оксадіазол-5-іл)-2,2-диметилпропіл]-сукцинамід,
2R-[3-(3,5-біс-трифторметилфеніл)-пропіл]-N1-[2,2-диметил-1S-(5-тіофен-2-іл-[1,2,4]оксадіазол-3-іл)-пропіл]-3S,N4-дигідроксисукцинамід,
2R-[3-(3,5-біс-трифторметилфеніл)-пропіл]-N1-[1S-(5-фуран-2-іл-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропіл]-3S,N4-дигідроксисукцинамід,
2R-[3-(4-етоксифеніл)-пропіл]-N1-[1S-(5-фуран-2-іл-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропіл]-3S,N4-дигідроксисукцинамід,
3-циклопентил-N-[2,2-диметил-1S-(3-феніл-[1,2,4]оксадіазол-5-іл)-пропіл]-2R-[(формілгідроксіаміно)-метил]-пропіонамід,
3-циклопентил-R-[2,2-диметил-1S-(5-феніл-[1,2,4]оксадіазол-3-іл)-пропіл]-2R-[(форміл-гідроксіаміно)-метил]-пропіонамід,
та фармацевтично прийнятні солі, гідрати або сольвати цих сполук.
31. 2S-гідрокси-3R-[1S-(5-тіофен-2-іл-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропілкарбамоїл]-5-метилгексангідроксамова кислота та фармацевтично прийнятні солі, гідрати або сольвати цієї сполуки.
32. Фармацевтична або ветеринарна композиція, що містить сполуку за будь-яким попереднім пунктом.
33. Сполука за будь-яким із пп. 1-31 для застосування в медицині або ветеринарії.
34. Застосування сполуки за будь-яким із пп. 1-31 для виготовлення лікарського засобу для лікування або профілактики захворювань, опосередкованих ММР.
35. Застосування за п. 34, яке відрізняється тим, що згаданим захворюванням є резорбція кісток, ріст пухлини або її інвазія внаслідок вторинних метастазів; ревматоїдний артрит, септичний артрит, остеоартрит, періодонтит, гінгівіт, укривання виразками рогівки, нейрозапальні захворювання, наприклад, розсіяний склероз; рестеноз; емфізематоз; фіброзні захворювання, наприклад, фіброз печінки і муковісцидоз; хронічне обструктивне легеневе захворювання; бронхіт; астма; автоімунне захворювання; відторгнення трансплантата (наприклад, стан "трансплантат проти хазяїна"); муковісцидоз; псоріаз; псоріатичний артрит; дегенеративне ураження хрящів; запальні стани у шлунку, наприклад, хвороба Крона, запальне кишкове захворювання і виразковий коліт; атопічний дерматит, бульозний епідермоліз; укривання виразками епідерми; невропатія або нефропатія, наприклад, інтерстиційний нефрит, гломерулонефрит і ниркова недостатність; очне запалення; цироз печінки, синдром Шегрена або запальний стан нервової системи.
36. Застосування за п. 34, яке відрізняється тим, що згаданим захворюванням є розсіяний склероз, емфізема, фіброз печінки, муковісцидоз, хронічне обструктивне легеневе захворювання, хвороба Крона, запальне кишкове захворювання або склероз печінки.
37. Застосування за п. 34, яке відрізняється тим, що згаданим захворюванням є гепатит.
38. Спосіб одержання сполуки за п. 1, де W є група гідроксамової кислоти HONH(C=O)-, який відрізняється тим, що включає проведення реакції кислоти загальної формули (ІІА) або (ІІВ)
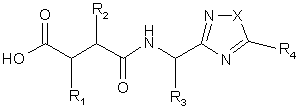 , (IIA)
, (IIA)
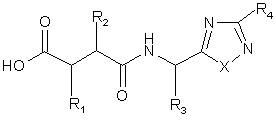 (IIB)
(IIB)
або її активованої похідної з гідроксиламіном, O-захищеним гідроксиламіном або N,O-дизахищеним гідроксиламіном, або їхніми солями, причому X, R1, R2, R3 і R4 відповідають визначенням за п. 1, за винятком того, що будь-який замісник при R1, R2, R3 і R4, який потенціально здатний вступати в реакцію з гідроксиламіном, O-захищеним гідроксиламіном, згаданим N,O-дизахищеним гідроксиламіном або їхніми солями, факультативно сам є захищеним від такої реакції, з подальшим відщепленням будь-яких захисних груп від одержаної групи гідроксамової кислоти і від будь-яких захищених замісників при R1, R2, R3 і R4.
39. Спосіб одержання сполуки за п. 1, де W є N-формілгідроксиламіногрупа H(C=O)NH(OH)-, який відрізняється тим, що включає N-формілування відповідної сполуки, в якій W є -NH(OP), де P є група захисту О, з подальшим відщепленням згаданої групи P захисту О.
40. Спосіб одержання сполуки за п. 1, де W є група карбонової кислоти -СООН, який відрізняється тим, що включає: взаємодію кислоти формули (III) або її активованої похідної 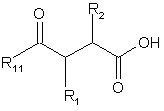 (III)
(III)
з аміном формули (IVA) або (IVB)
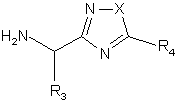 , (IVA)
, (IVA)
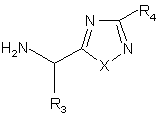 , (IVB)
, (IVB)
де X, R1 R2, R3 і R4 відповідають визначенням за п. 1, за винятком того, що будь-який замісник при R1, R2, R3 і R4, який потенціально здатний вступати в реакцію сполучення, може сам бути захищеним від такої реакції, а R11 є група захисту гідроксилу, і подальше відщеплення захисної групи R11 і будь-яких захисних груп при R1 R2, R3 і R4.
Текст
1. Сполука формули (ІА) або (IВ) R2 N X H W N R4 N UA (21) 20040806941 (22) 20.02.2003 (24) 15.03.2007 (86) PCT/GB03/00741, 20.02.2003 (31) 0204159.8 (32) 22.02.2002 (33) GB (46) 15.03.2007, Бюл. № 3, 2007 р. (72) Аскоу Ендру Пол, GB, Дейвіс Стівен Джон, GB, Пен Жіль , GB, Жійон Жан-Ів , FR (73) ВЕРНЕЙЛІС (ОКСФОРД) ЛТД, GB, ЛАБОРАТУАР СЕРОНО С.А., CH (56) CHEN J J ET AL: "Design, synthesis, activity, and structure of a novel class of matrix metalloproteinase inhibitors containing a heterocyclic P2'-P3' amide bond isostere" BIOORGANIC & MEDICIN AL CHEMISTR Y LETTERS, vol. 6, no. 13, 9 July 1996 (1996-07-09), pages 1601-1606. 2 N X R3 (IB), (19) 1 78275 (54) ОКСА- І ТІАДІАЗОЛИ ТА ЇХ ЗАСТОСУВАННЯ ЯК ІНГІБІТОРІВ МЕТАЛОПРОТЕЇНАЗ 3 78275 4 де (C1-С3)перфторалкіл, W є НО(С=O)-, HONH(C=O)- або H(C=O)N(OH)-; циклоалкіл, X є -О- або -S-; циклоалкіл(С 1-C6-алкіл) -, R1 є циклоалкеніл, водень; циклоалкеніл(C1-C6-алкіл)-, -ОН або -SH; феніл, фтор або хлор; феніл(С 1-C6-алкіл)-, -СF3; нафтил, (С1-С6)алкіл; неароматичний гетероцикліл, (С1-С6)алкоксигрупа; неароматичний гетероцикліл(C1-C6-алкіл)-, (С2-С6)алкеніл; гетероарил або феніл або заміщений феніл; гетероарил(C1-C6-алкіл)-; феніл-(С1-С6)алкіл або заміщений феніл-(С1або її фармацевтично прийнятна сіль, гідрат або С6)алкіл; сольват. феніл-(С2-С6)алкеніл або заміщений феніл-(С22. Сполука за п. 1, яка відрізняється тим, що має С6)алкеніл; формулу (ІА). гетероцикліл або заміщений гетероцикліл; 3. Сполука за п. 1, яка відрізняється тим, що має гетероцикліл-(C1-C6)алкіл або заміщений гетероформулу (ІВ). цикліл-(С1-C6)алкіл; 4. Сполука за будь-яким попереднім пунктом, яка група BSOn A-, де n є 0, 1 або 2, В є водень або (C1відрізняє ться тим, що W є HONH(C=O)-. C6)алкіл, феніл, заміщений феніл, гетероцикліл, 5. Сполука за будь-яким попереднім пунктом, яка заміщений гетероцикліл, (C1-C6)ацил, фенацил відрізняє ться тим, що Х є -O-. або заміщений фенацил і А є (C1-C6)алкілен; 6. Сполука за будь-яким попереднім пунктом, яка -NH2, (C1-C6)алкіламіно або ді(C1відрізняє ться тим, що R1 є C6)алкіламіногрупа; водень, гідроксил, фтор, хлор, метил, метоксигруаміно-(C1-C6)алкіл, (C1-C6)алкіламіно-(C1-C6)алкіл, па, трифторметил, етил, н-пропіл, аліл, фенілпроді(C1-C6)алкіламіно-(C1-C6)алкіл, гідроксі-(C1піл, циклопропілметил, фенілпроп-2-еніл, тієнілсуC6)алкіл, меркапто-(C1-C6)алкіл або карбоксі-(C1льфанілметил, тієнілсульфінілметил або C6) алкіл, де згадані аміно-, гідрокси-, меркаптогтієнілсульфонілметил; або рупа або карбоксил факультативно захищені або (C1-С4)алкіл, наприклад, метил, етил, н-пропіл або згаданий карбоксил амідований; або н-бутил, заміщений замісником, вибраним із групи, циклоалкіл, циклоалкеніл або неароматичний гедо якої входять фталімідогрупа, 1,2-диметил-3,5тероцикл, що містить до 3 гетероатомів, кожен з діоксо-1,2,4-триазолідин-4-іл, 3-метил-2,5-діоксо-1яких може бути (і) заміщений одним або декількоімідазолідиніл, 3,4,4-триметил-2,5-діоксо-1ма замісниками, вибраними з групи, до якої вхоімідазолідиніл, 2-метил-3,5-діоксо-1,2,4дять (C1-C6)алкіл, (С2-C6)алкеніл, галоген, ціаногоксадіазол-4-іл, 3-метил-2,4,5-триоксо-1рупа (-CN), імідазолідиніл, 2,5-діоксо-3-феніл-1-імідазолідиніл, -CO2H, -CO2R, -CONH2, -CONHR, -CON(R)2, -ОН, 2-оксо-1-піролідиніл, 2,5-діоксо-1-піролідиніл або OR, оксогрупа, -SH, -SR, -NHCOR та -NHCO2R, де 2,6-діоксопіперидиніл, 5,5-диметил-2,4-діоксо-3R є (C1-C6)алкіл або бензил, та/або (іі) конденсооксазолідиніл, гексагідро-1,3-діоксопіразолований з циклоалкілом або гетероциклом; [1,2,а][1,2,4]-триазол-2-іл, нафталімідогрупа (тобто R2 є гр упа R10-(X) n-(ALK)m-, де 1,3-дигідро-1,3-діоксо-2Н-бенз[f]ізоіндол-2-іл), 1,3R10 є водень або (C1-C6)алкіл, (С2-C6)алкеніл, (С2дигідро-1-оксо-2Н-бенз[f]ізоіндол-2-іл, 1,3-дигідроC6)алкініл, циклоалкіл, арил або гетероцикліл, ко1,3-діоксо-2Н-піроло[3,4-b]хінолін-2-іл та 2,3жен з яких може бути незаміщений або заміщений дигідро-1,3-діоксо-1Н-бенз[d,е]ізохінолін-2-іл; або замісником, вибраним із групи, до якої входять (C1циклогексил, циклооктил, циклогептил, циклопенC12)алкіл, (C1-C12)алкокси-, гідрокси-, меркапто-, тил, циклобутил, циклопропіл, тетрагідропіраніл (С1-C12)алкілтіо-, аміногрупа, галоген (в тому числі або морфолініл. фтор, хлор, бром і йод), трифторметил, ціано-, 7. Сполука за будь-яким із пп. 1-5, яка відрізнянітро-, оксогрупа, -СООН, -CONH 2, -COOR A, – ється тим, що R1 є водень, гідроксил, (С2NHCORA, –CONHRA, –NHRA, -NRARB та –CONRARB С4)алкеніл або (C1-С4)алкоксигрупа. де RA і RB незалежно один від одного є (C18. Сполука за будь-яким із пп. 1-5, яка відрізняС12)алкіл, і ється тим, що R1 є водень, гідроксил, фтор, метоALK є лінійний або розгалужений двовалентний ксигрупа, циклопентил, н-пропіл або аліл. радикал, вибраний з групи, до якої входять (C19. Сполука за будь-яким із пп. 1-8, яка відрізняC6)алкілен, (С2-C6)алкенілен та (С2-C6)алкінілен, і ється тим, що R2 є (C1-С12)алкіл, (С3-C6)алкеніл може бути перерваний одним або декількома неабо (С3-C6)алкініл; суміжними містками -NH-, -О- або -S-, Х є -NH-, -Оциклоалкіл(C1-C6-алкіл)-; або -S-, -NRC або –NCORC, де RC є (C1-C12)алкіл, і феніл(С 1-C6-алкіл)-, феніл(С 3-C6-алкеніл)- або феm і n незалежно один від одного є 0 або 1; ніл(С3-C6-алкініл)-, факультативно заміщений при згаданому фенільному циклі; R3 є бічний ланцюг природної або синтетичної a гетероарил(C1-C6-алкіл)-, гетероарил(С 3-C6амінокислоти; алкеніл)- або гетероарил(С3-C6-алкініл)-, факульR4 є факультативно заміщений тативно заміщений при згаданому гетероарильно(C1-C6)алкіл, му циклі; (С2-C6)алкеніл, 4-фенілфеніл(С 1-C6-алкіл)-, 4-фенілфеніл(С 3-C6(С2-C6)алкініл, 5 78275 6 алкеніл)-, 4-фенілфеніл(С 3-C6-алкініл)-, 4рупа, (C1-C6)алканоїл, трифторметил(C1-C6)алкіл, гетероарилфеніл(C1-C6-алкіл)-, 4гідроксил, форміл, аміно-, (C1-C6)алкіламіно-, дігетероарилфеніл(С3-C6-алкеніл)-, 4(C1-C6)алкіламіно-, меркапто-, (C 1-C6)алкілтіогрупа, гетероарилфеніл(С3-C6-алкініл)-, факультативно гідроксі(C1-C6)алкіл, меркапто(C1-C6)алкіл або (C1заміщений при кінцевому фенільному або гетероC6)алкілфенілметил; або арильному циклі; або група –CRaRbRc, в якій: феноксі(C1-C6-алкіл)- або гетероарилоксі(C1-C6кожний з Ra, Rb і Rc незалежно від інших є водень, алкіл)-, факультативно заміщений при згаданому (C1-C6)алкіл, (С2-C6)алкеніл, (С2-C6)алкініл, фефенільному або гетероарильному циклі. ніл(C1-C6)алкіл, (С3-С8)циклоалкіл; 10. Сполука за будь-яким із пп. 1-8, яка відрізняабо ється тим, що R2 є метил, етил, н- або ізопропіл, Rc є водень і Ra і Rb незалежно один від одного є н-, ізо- або трет-бутил, н-пентил, н-гексил, нфеніл або гетероарил, наприклад піридил; або гептил, н-ноніл, н-децил, проп-2-ін-1-іл, циклогекRc є водень, (C1-C6)алкіл, (С2-C6)алкеніл, (С2силетил, циклопентилметил, 3-фенілпроп-2-ін-1-іл, C6)алкініл, феніл(C1-C6)алкіл або (С33-(2-хлорфеніл)проп-2-ін-1-іл, бензилфенілпропіл, С8)циклоалкіл, і Ra і Rb разом з атомом вуглецю, 4-хлорфенілпропіл, 4-метилфенілпропіл, 4до якого вони приєднані, утворюють 3-8-членний метоксифенілпропіл, феноксибутил, 3-(4циклоалкіл або 5-6-членний гетероцикл; або піридилфеніл)пропіл-, 3-(4-(4-піридил)феніл)пропRa, Rb і Rc разом з атомом вуглецю, до якого вони 2-ін-1-іл, 3-((4-феніл)феніл)пропіл-, 3-((4приєднані, утворюють трициклічну груп у (наприфеніл)феніл)проп-2-ін-1-іл та 3-[(4-хлорфеніл)клад адамантил); або феніл]пропіл-. кожний з Ra і Rb незалежно від іншого є (C111. Сполука за будь-яким із пп. 1-8, яка відрізняC6)алкіл, (С2-C6)алкеніл, (С2-C6)алкініл, феніл(С 1ється тим, що R2 є (C1-С4)алкіл, 3-8-членний цикC6)алкіл або група, яка відповідає поданому нижче лоалкіл-(С1-С4)алкіл-, який факультативно містить визначенню для Rс, за винятком водню, або Ra і Rb у згаданому циклі 1-3 гетероатоми, вибрані із груразом з атомом вуглецю, до якого вони приєднані, пи, до якої входять N, О і S або арил-(C 1-С4)алкіл. утворюють циклоалкіл або гетероцикл, a Rc є во12. Сполука за будь-яким із пп. 1-8, яка відрізнядень, -ОН, -SH, галоген, -CN, -СO2Н, (C1ється тим, що R2 є бензил, н-бутил, ізобутил, нС4)перфторалкіл, -СН2OН, -СO2(C1-C6)алкіл, -O(C1гексил, циклопентилметил, 4-етоксифенілпропіл C6)алкіл, -O(С2-C6)алкеніл, -S(С1-C6)алкіл, -SO(С1або фенілпропіл. C6)алкіл, -SO2(С1-C6)алкіл, -S(С2-C6)алкеніл, 13. Сполука за будь-яким з попередніх пунктів, яка SO(С2-C6)алкеніл, -SO2(С2-C6)алкеніл або група відрізняє ться тим, що R3 є (C1-C6)алкіл, феніл, 2-, Q-W, де Q є зв'язок або -О-, -S-, -SO- або -SO2-, і 3- або 4-піридил, 2- або 3-тієніл, 2-, 3- або 4W є феніл, фенілалкіл, (С3-С8)циклоалкіл, (С3гідроксифеніл, 2-, 3- або 4-метоксифеніл, 2-, 3- або С8)циклоалкілалкіл, (С4-С8)циклоалкеніл, (С44-піридилметил, бензил, 2-, 3або 4С8)циклоалкенілалкіл, гетероарил або гетероаригідроксибензил, 2-, 3- або 4-бензилоксибензил, 2-, лалкіл, причому група W може бути факультатив3- або 4-C1-C6-алкоксибензил або бензилоксі(C1но заміщена одним або декількома замісниками, C6алкіл)-; або незалежно вибраними з групи, до якої входять гідроксил, галоген, -CN, -СO2H, -СO 2(С1-C6)алкіл, характеристична група природної a -амінокислоти, CONH2, -СОNH(С1-C6)алкіл, -СОNН(С1-C6алкіл)2, в якій будь-яка функціональна група може бути СНО, -СН2OН, (С1-С4)перфторалкіл, -O(С1захищеною, будь-яка аміногрупа може бути ациC6)алкіл, -S(С1-C6)алкіл, -SO(C1-C6)алкіл, -SO2(C1лованою і будь-яка карбоксильна група може бути C6)алкіл, -NO2, -NH2, NН(C1-C6)алкіл, -N((C1амідованою; або C6)алкіл)2, -NHCO(C1-C6)алкіл, (C1-C6)алкіл, (С2група -[Аlk]nR6 , де Alk є (C1-C6)алкіл або (С2C6)алкеніл, (С2-C6)алкініл, (С3-С8)циклоалкіл, (С4C6)алкеніл, факультативно перерваний одним або С1)циклоалкеніл, феніл або бензил. декількома атомами -О- чи -S- або групами -N(R7)14. Сполука за будь-яким із пп. 1-12, яка відрізня[де R7 є атом водню або (C1-C6)алкіл], n є 0 або 1, і ється тим, що R3 є бензил, феніл, циклогексилмеR6 є факультативно заміщена циклоалкільна або тил, піридин-3-ілметил, трет-бутоксиметил, ізоциклоалкенільна група; або пропіл, ізо-бутил, втор-бутил, трет-бутил, 1бензильна група, заміщена при фенільному циклі бензилтіо-1-метилетил, 1-метилтіо-1-метилетил групою формули -OCH2COR8, де R8 є гідроксил, або 1-меркапто-1-метилетил. аміно-, (С1-C6)алкокси-, феніл-(C1-C6)алкокси-, (C115. Сполука за будь-яким із пп. 1-12, яка відрізняC6)алкіламіно-, ді((C1-C6)алкіл)аміно-, феніл-(C1ється тим, що R3 є (C1-С4)алкіл або арил-(C1C6)алкіламіногрупа, залишок амінокислоти або С4)алкіл. галогенангідриду амінокислоти, її складного ефіру 16. Сполука за будь-яким із пп. 1-12, яка відрізняабо аміду, причому згаданий залишок приєднаний ється тим, що R3 є бензил, трет-бутоксиметил, ізочерез амідний зв'язок, згадана амінокислота вибпропіл, трет-бутил або ізо-бутил. рана з групи, до якої входять гліцин, a - або b 17. Сполука за будь-яким з попередніх пунктів, яка аланін, валін, лейцин, ізолейцин, фенілаланін, відрізняє ться тим, що R4 є факультативно замітирозин, триптофан, серин, треонін, цистеїн, метіщений (C1-C6)алкіл; (С3-С8)циклоалкіл; феніл; моонін, аспарагін, глутамін, лізин, гістидин, аргінін, ноциклічний гетероцикл або моноциклічний гетеглутамінова кислота та аспарагінова кислота; або роарил. гетероцикл-(C1-C6)алкіл, незаміщений або заміще18. Сполука за будь-яким із пп. 1-16, яка відрізняний при згаданому гетероциклі одним або двома ється тим, що R4 є C1-С4-алкіл, арил, гетероарил, замісниками, вибраними з групи, до якої входять 3-8-членний циклоалкіл, що факультативно місгалоген, нітро-, карбокси-, (C1-C6)алкокси-, ціаног 7 78275 8 тить у згаданому циклі 1-3 гетероатоми, вибрані з [1,2,4]оксадіазол-3-іл)-2,2групи, до якої входять N, О і S, арил-(C1-С4)алкіл диметилпропілкарбамоїл]-5або гетероарил-(C1-С4)алкіл. метилгексангідроксамова кислота, 19. Сполука за будь-яким із пп. 1-16, яка відрізня2S-гідрокси-3R-[1S-(5-тіофен-2-ілметилється тим, що R4 є факультативно заміщений ме[1,2,4]оксадіазол-3-іл)-2,2тил, етил, н- або ізопропіл, проп-2-іл, трет-бутил, диметилпропілкарбамоїл] -5циклопропіл, циклопентил; феніл; морфоліногруметилгексангідроксамова кислота, па; тієніл або фураніл. 2S-гідрокси-3R-[1S-(5-етил-[1,2,4]оксадіазол-3-іл)20. Сполука за п. 2, яка відрізняється тим, що R1 2,2-диметилпропілкарбамоїл]-5є -ОН; W є -C(=O)NHOH, Х є -О- і R3 є трет-бутил. метилгексангідроксамова кислота, 21. Сполука за п. 2, яка відрізняється тим, що R1 2S-гідрокси-3R-[1S-(5-циклопентилє -ОН; W є -C(=O)NHOH, Х є -О-, R3 є трет-бутил, a [1,2,4]оксадіазол-3-іл)-2,2R2 є С1-С12-алкіл або феніл(C1-C12-алкіл)-, чи гетедиметилпропілкарбамоїл]-5роарил(C1-C6-алкіл)-, факультативно заміщений метилгексангідроксамова кислота, при згаданому фенільному або гетероарильному 2S-гідрокси-3R-[1S-(5-бензил-[1,2,4]оксадіазол-3циклі. іл)-2,2-диметилпропілкарбамоїл]-522. Сполука за п. 2, яка відрізняється тим, що R1 метилгексангідроксамова кислота, є -ОН; W є -C(=O)NHOH, Х є -О-, R3 є трет-бутил, а 2S-гідрокси-3R-[1S-(5-ізобутил-[1,2,4]оксадіазол-3R2 є фенілпропіл- або етоксифенілпропіл. іл)-2,2-диметилпропілкарбамоїл]-523. Сполука за п. 2, яка відрізняється тим, що R1 метилгексангідроксамова кислота, є -ОН; W є -C(=O)NHOH, Х є -О-, R3 є трет-бутил, а 2S-гідрокси-3R-[1S-(5-трет-бутил-[1,2,4]оксадіазолR4 є розгалужений С 1-С6-алкіл, циклоалкіл, феніл, 3-іл)-2,2-диметилпропілкарбамоїл]-5гетероарил, феніл(C1-C6-алкіл)- або гетерометилгексангідроксамова кислота, арил(C1-C6-алкіл)-. 3R-[1S-(5-тіофен-2-іл-[1,2,4]оксадіазол-3-іл)-2,224. Сполука за п. 2, яка відрізняється тим, що R1 диметилпропілкарбамоїл]-5є -ОН; W є -C(=O)NHOH, Х є -О-, R3 є трет-бутил, метилгексангідроксамова кислота, R2 є етоксифенілпропіл, а R4 є феніл або гетеро2S-гідрокси-3R-[1S-(5-(2,2-диметилпропіл)арил. [1,2,4]оксадіазол-3-іл)-2,225. Сполука за п. 3, яка відрізняється тим, що W диметилпропілкарбамоїл]-5є -C(=O)NHOH і Х є -O-. метилгексангідроксамова кислота, 26. Сполука за п. 3, яка відрізняється тим, що W 2S-гідрокси-3R-[1S-(5-n-толіл-[1,2,4]оксадіазол-3є -C(=O)NHOH, Х є -О-, а R3 є трет-бутил. іл)-2,2-диметилпропілкарбамоїл]-527. Сполука за п. 3, яка відрізняється тим, що W метилгексангідроксамова кислота, є -C(=O)NHOH, Х є -О-, а R1 є -ОН, (C12S-гідрокси-3R-[1S-(5-циклопропілC6)алкоксигрупа або (С2-C6)алкеніл. [1,2,4]оксадіазол-3-іл)-2,228. Сполука за п. 3, яка відрізняється тим, що W диметилпропілкарбамоїл]-5є -C(=O)NHOH, Х є -О-, R1 є -ОН, (C1метилгексангідроксамова кислота, C6)алкоксигрупа або (С2-C6)алкеніл, R3 є трет2S-гідрокси-3R-[1S-(5-метил-[1,2,4]оксадіазол-3бутил або бензил і R4 є ізопропіл. іл)-2,2-диметилпропілкарбамоїл]-529. Сполука формули (ІА) за п. 1, де метилгексангідроксамова кислота, Х є -O-; 2S-гідрокси-3R-[15-(3-ізопропіл-[1,2,4]оксадіазол-3W є HONH(C=O)-; іл)-2,2-диметилпропілкарбамоїл]-5R1 є -ОН; метилгексангідроксамова кислота, R2 є ізобутил; 2S,N 1-дигідрокси-3R-ізобутил-N4-[2-метил-15-(3R3 є трет-бутил; феніл-[1,2,4]оксадіазол-5-іл)-пропіл]-сукцинамід, R4 є 2-тієніл. 2S-аліл-5-метил-3R-[2-феніл-1S-(3-феніл30. Сполука, вибрана з групи, до якої входять: [1,2,4]оксадіазол-5-іл)-етилкарбамоїл]3R-[2,2-диметил-1S-(5-феніл-[1,2,4]оксадіазол-3гексангідроксамова кислота, іл)-пропілкарбамоїл]-2S-гідрокси-52S-аліл-5-метил-3R-[2-феніл-1S-(3-ізопропілметилгексангідроксамова кислота, [1,2,4]оксадіазол-5-іл)-етилкарбамоїл]3R-[2,2-диметил-1S-(5-феніл-[1,2,4]оксадіазол-3гексангідроксамова кислота, іл)-пропілкарбамоїл]-2R-гідрокси-52S-аліл-3R-[2,2-диметил-1S-(3-метилметилгексангідроксамова кислота, [1,2,4]оксадіазол-5-іл)-пропілкарбамоїл]-53R-[2,2-диметил-1S-(3-феніл-[1,2,4]оксадіазол-5метилгексангідроксамова кислота, іл)-пропілкарбамоїл]-2S-гідрокси-53R-[2,2-диметил-1S-(3-феніл-[1,2,4]оксадіазол-5метилгексангідроксамова кислота, іл)-пропілкарбамоїл]-5-метилгексангідроксамова 2R-[3-(4-етоксифеніл)-пропіл]-N1-[1S-(5-тіофен-2кислота, іл-[1,2,4]оксадіазол-3-іл)-2,2-диметилпропіл]-3S,N42S-метокси-5-метил-3R-[1S-(3-метилдигідроксисукцинамід, [1,2,4]оксадіазол-5-іл)-2-фенілетилкарбамоїл]2S-гідрокси-3R-[1S-(5-ізопропіл-[1,2,4]оксадіазол-3гексангідроксамова кислота, іл)-2,2-диметилпропілкарбамоїл]-53R-[2,2-диметил-1S-(3-феніл-[1,2,4]оксадіазол-5метилгексангідроксамова кислота, іл)-пропілкарбамоїл]-гептадеканова кислота, 2S-гідрокси-3R-[1S-(5-фуран-2-іл-[1,2,4]оксадіазол3R-[2,2-диметил-1S-(3-феніл-[1,2,4]оксадіазол-53-іл)-2,2-диметилпропілкарбамоїл]-5іл)-пропілкарбамоїл]-нонадеканова кислота, метилгексангідроксамова кислота, 6-(4-хлорфеніл)-3R-[2,2-диметил-1S-(5-феніл2S-гідрокси-3R-[1S-(5-циклопентилметил[1,2,4]оксадіазол-3-іл)-пропілкарбамоїл]-гексанова 9 78275 10 кислота, стан нервової системи. 6-(4-хлорфеніл)-3R-[2,2-диметил-1R-(5-феніл36. Застосування за п. 34, яке відрізняється тим, [1,2,4]оксадіазол-3-іл)-пропілкарбамоїл]-гексанова що згаданим захворюванням є розсіяний склероз, кислота, емфізема, фіброз печінки, муковісцидоз, хронічне 3R-[2,2-диметил-1S-(5-тіофен-2-ілобструктивне легеневе захворювання, хвороба [1,2,4]оксадіазол-3-іл)-пропілкарбамоїл]-2SКрона, запальне кишкове захворювання або склегідрокси-5-метилгексанова кислота, роз печінки. 3R-[1S-(5-фуран-2-іл-[1,2,4]оксадіазол-3-іл)-2,237. Застосування за п. 34, яке відрізняється тим, диметилпропілкарбамоїл]-2S-гідрокси-5що згаданим захворюванням є гепатит. метилгексанова кислота 38. Спосіб одержання сполуки за п. 1, де W є гр упа 2R-циклопентилметил-3S,N4-дигідрокси-N1-[1S-(3гідроксамової кислоти HONH(C=O)-, який відрізізопропіл-[1,2,4]оксадіазол-5-іл)-2,2няється тим, що включає проведення реакції кисдиметилпропіл]-сукцинамід, лоти загальної формули (ІІА) або (ІІВ) 2R-[3-(3,5-біс-трифторметилфеніл)-пропіл]-N1-[2,2R2 O N X диметил-1S-(5-тіофен-2-іл-[1,2,4]оксадіазол-3-іл)H пропіл]-3S,N4-дигідроксисукцинамід, N R4 HO N 2R-[3-(3,5-біс-трифторметилфеніл)-пропіл]-N1-[1S(5-фуран-2-іл-[1,2,4]оксадіазол-3-іл)-2,2O диметилпропіл]-3S,N4-дигідроксисукцинамід, R1 R3 , (IIA) 2R-[3-(4-етоксифеніл)-пропіл]-N1-[1S-(5-фуран-2-ілR4 [1,2,4]оксадіазол-3-іл)-2,2-диметилпропіл]-3S,N4R2 O N дигідроксисукцинамід, H 3-циклопентил-N-[2,2-диметил-1S-(3-фенілN N [1,2,4]оксадіазол-5-іл)-пропіл]-2RHO X [(формілгідроксіаміно)-метил]-пропіонамід, O 3-циклопентил-R-[2,2-диметил-1S-(5-фенілR1 R3 (IIB) [1,2,4]оксадіазол-3-іл)-пропіл]-2R-[(формілабо її активованої похідної з гідроксиламіном, Oгідроксіаміно)-метил]-пропіонамід, захищеним гідроксиламіном або N,O-дизахищеним та фармацевтично прийнятні солі, гідрати або согідроксиламіном, або їхніми солями, причому X, львати цих сполук. R1, R2, R3 і R4 відповідають визначенням за п. 1, за 31. 2S-гідрокси-3R-[1S-(5-тіофен-2-ілвинятком того, що будь-який замісник при R1, R2, [1,2,4]оксадіазол-3-іл)-2,2R3 і R4, який потенціально здатний вступати в реадиметилпропілкарбамоїл]-5кцію з гідроксиламіном, O-захищеним гідроксиламетилгексангідроксамова кислота та фармацевтиміном, згаданим N,O-дизахищеним гідроксиламічно прийнятні солі, гідрати або сольвати цієї споном або їхніми солями, факультативно сам є луки. захищеним від такої реакції, з подальшим відщеп32. Фармацевтична або ветеринарна композиція, ленням будь-яких захисних груп від одержаної що містить сполуку за будь-яким попереднім пункгрупи гідроксамової кислоти і від будь-яких захитом. щених замісників при R1, R2, R3 і R4. 33. Сполука за будь-яким із пп. 1-31 для застосу39. Спосіб одержання сполуки за п. 1, де W є Nвання в медицині або ветеринарії. формілгідроксиламіногрупа H(C=O)NH(OH)-, який 34. Застосування сполуки за будь-яким із пп. 1-31 відрізняє ться тим, що включає N-формілування для виготовлення лікарського засобу для лікуванвідповідної сполуки, в якій W є -NH(OP), де P є ня або профілактики захворювань, опосередковагрупа захисту О, з подальшим відщепленням зганих ММР. даної групи P захисту О. 35. Застосування за п. 34, яке відрізняється тим, 40. Спосіб одержання сполуки за п. 1, де W є гр упа що згаданим захворюванням є резорбція кісток, карбонової кислоти -СООН, який відрізняється ріст пухлини або її інвазія внаслідок вторинних тим, що включає: взаємодію кислоти формули (III) метастазів; ревматоїдний артрит, септичний артR2 рит, остеоартрит, періодонтит, гінгівіт, укривання O виразками рогівки, нейрозапальні захворювання, OH наприклад, розсіяний склероз; рестеноз; емфізематоз; фіброзні захворювання, наприклад, фіброз R 11 печінки і муковісцидоз; хронічне обструктивне леO R1 геневе захворювання; бронхіт; астма; автоімунне або її активованої похідної захворювання; відторгнення трансплантата (на(III) приклад, стан "трансплантат проти хазяїна"); муз аміном формули (IVA) або (IVB) ковісцидоз; псоріаз; псоріатичний артрит; дегенеN X ративне ураження хрящів; запальні стани у шлунку, наприклад, хвороба Крона, запальне кишH 2N R4 кове захворювання і виразковий коліт; атопічний N дерматит, бульозний епідермоліз; укривання виразками епідерми; невропатія або нефропатія, наR3 , (IVA) приклад, інтерстиційний нефрит, гломерулонефрит і ниркова недостатність; очне запалення; цироз печінки, синдром Шегрена або запальний 11 R4 N H2N 78275 12 де X, R1 R2, R3 і R4 відповідають визначенням за п. 1, за винятком того, що будь-який замісник при R 1, R2, R3 і R4, який потенціально здатний вступати в реакцію сполучення, може сам бути захи щеним від такої реакції, а R11 є група захисту гідроксилу, і подальше відщеплення захисної групи R11 і будьяких захисних груп при R1 R2, R3 і R4. N X R3 , (IVB) Цей винахід стосується терапевтично активних похідних гідроксамових та карбонових кислот, способів їх одержання, фармацевтичних композицій, що їх містять, та застосування таких сполук в медицині. Зокрема, ці сполуки є інгібіторами матричних металопротеаз. Передумови створення винаходу Матричні металопротеази (ММР) є сімейством цинквмісних ендопептидаз, здатних розщеплювати великі біомолекули, наприклад, колагени, протеоглікани та желатини. Дисбаланс між активними ММР та ендогенними інгібіторами призводить до надмірного розкладу тканин. Трьома головними групами ММР є колагенази, желатинази та стромелізини. До колагеназ належать фібробластова колагеназа (ММР-1), нейтрофільна колагеназа (ММР-S) та колагеназа-3 (ММР-13). До желатиназ належать желатиназа з молекулярною масою 72кДа (желатиназа А; ММР-2) та желатиназа з молекулярною масою 92кДа (желатиназа В; ММР9). До стромелізинів належать стромелізин-1 (ММР-3), стромелізин-2 (ММР-10) та матрилізин (ММР-7). Однак відомі ММР, які не можна точно віднести до перелічених вище груп, наприклад, металоеластаза (ММР-12), ММР мембранного типу (МТ-ММР або ММР-14) та стромелізин-3 (ММР-11). Надмірне продукування та активування ММР пов'язано з широким спектром захворювань, до яких належать, наприклад, рак; ревматоїдний артрит; остеоартрит; хронічні запальні захворювання, наприклад, астма, бронхіт та емфізема; серцевосудинні захворювання, наприклад, атеросклероз; укривання виразками рогівки; стоматологічні захворювання, наприклад, гінгівіт та періодонтит; неврологічні захворювання, наприклад, розсіяний склероз і рестеноз. Наприклад, ММР-12 є необхідною для розвитку індукованої сигаретним димом де W є НО(С = О H(C=O)N(OH)-; )-, HONH(C=O) або емфіземи в мишей [Science, 277, 2002 (1997)]. Інгібування ММР є, таким чином, стратегією лікування таких хворобливих станів. Однак є очевидним, що неселективне інгібування активності матричних металопротеаз може зашкоджувати звичайним фізіологічним процесам, що призводить до виникнення побічних ефектів, які обмежують припустиму дозу інгібіторів. Селективне інгібування ММР-12 та/або ММР-9, як вважають, стосується, зокрема, стратегії впливу на запальні стани. ММР можуть гідролізувати зв'язаний з мембранами попередник запального цитокіну - aфактора некрозу пухлин (TNF-a). Це відщеплення призводить до утворення зрілого розчинного TNFa, а інгібітори ММР здатні блокувати продукування TNF-a як in vitro, так і in vivo. Цей фармакологічний ефект є можливою складовою протизапальної дії цього класу сполук. Сучасний стан проблеми інгібування ММР, відображений у патентній літературі, охарактеризовано в огляді Догерті та ін. [Doherty et al., Therapeutic Developments in Matrix Metalloproteinase Inhibition; Expert Opinions on Therapeutic Patents, 2002, 12, 665-707]. Цей винахід пропонує клас сполук, які є інгібіторами ММР. Цей клас охоплює сполуки, які є селективними інгібіторами ММР-12 у порівнянні до колагеназаз та стромелізинів. Крім того, сполуки за цим винаходом можуть виявляти селективну активність відносно ММР-9. Сполуки за цим винаходом, таким чином, призначені для лікування захворювань, опосередкованих, головним чином, ММР-9 та/або ММР-12, особливо запальних станів, наприклад, розсіяного склерозу і фіброзу. Згідно з цим винаходом, запропонована сполука формули (ІА) або (IB) X є -О- або -S-; R1 є водень; -ОН або -SH; 13 78275 14 фтор або хлор; 1; -CF3; R3 є бічний ланцюг природної або синтетичної (С1-С6)алкіл; a-амінокислоти; (С1-С6)алкоксигрупа; R4 є факультативно заміщений (С2-С6)алкеніл; (С1-С6)алкіл, феніл або заміщений феніл; (С2-С6)алкеніл, феніл-(С1-С6)алкіл або заміщений феніл-(С1(С2-С6)алкініл, С6)алкіл; (С1-С3)перфторалкіл, феніл-(С2-С6)алкеніл або заміщений фенілциклоалкіл, (С2-С6)алкеніл; циклоалкіл (С1-С6-алкіл)-, гетероцикліл або заміщений гетероцикліл; циклоалкеніл, гетероцикліл-(С1-С6)алкіл або заміщений гетециклоалкеніл(С 1-С6-алкіл)-, роцикліл-(С1-С6)алкіл; феніл, група BSOn A-, де n є 0, 1 або 2 і В є водень феніл(С 1-С6-алкіл)-, або (С1-С6)-алкіл, феніл, заміщений феніл, гетеронафтил, цикліл, заміщений гетероцикліл, (С1-С2)ацил, фенеароматичний гетероцикліл, нацил або заміщений фенацил, і А є (С1неароматичний гетероцикліл(С1-С6-алкіл)-, С6)алкілен; гетероарил; -NH2, (С1-С6)алкіламіноабо ди(С 1або гетероарил (С1-С6-алкіл) -; С6)алкіламіногрупа; та фармацевтично прийнятні гідрати і сольвааміно-(С1-С6)алкіл, (С1-С6)алкіламіно-(С1ти її солей. С6)алкіл, ди(С1-С6)алкіламіно-(С1-С6)алкіл, гідроУ значенні, вживаному в цьому описі, термін кси-(С1-С6)алкіл, меркапто-(С1-С6)алкіл або карбо"(С1-С6)алкіл" означає лінійну або розгалужену кси-(С1-С6)алкіл, де згадані аміно-, гідрокси-, мералкільну гр упу, що містить від 1 атому до 6 атомів каптогрупа або карбоксил факультативно вуглецю, в тому числі, наприклад, метил, етил, нзахищені або згаданий карбоксил амідований; або пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, циклоалкіл, циклоалкеніл або неароматичний гетрет-бутил, н-пентил і н-гексил. тероцикл, що містить до 3 гетероатомів, кожен з У значенні, вживаному в цьому описі, термін яких може бути (і) заміщений одним або декілько"двовалентний (С1-С6)алкілен(овий радикал)" ма замісниками, вибраними з групи, до якої вхоозначає насичений вуглеводневий ланцюг, що дять (С1-С6)алкіл, (С2-С6)алкеніл, галоген, ціаногмістить від 1 до 6 атомів вуглецю і має дві вільних рупа (-CN), -СО2Н, -CO2R, -CONH2 , -CONHR, валентності. CON(R)2, -OH, -OR, оксогрупа, -SH, -SR, -NHCOR У значенні, вживаному в цьому описі, термін та -NHCO2R, де R є (С1-С6)алкіл або бензил, "(С2-С6)алкеніл" означає лінійну або розгалужену та/або (іі) конденсований з циклоалкілом або гетеалкенільну групу, що містить від 2 атомів до 6 роциклом; атомів вуглецю, має щонайменше один подвійний R2 є гр упа R10-(X) n-(ALK)m-, де зв'язок і знаходиться в стереохімічній конфігурації циклоалкіл, циклоалкеніл або неароматичний Е або Z в разі, якщо таке поняття може бути загетероцикл, що містить до 3 гетероатомів, кожен з стосовано. Термін охоплює, наприклад, вініл, аліл, яких може бути (і) заміщений одним або декілько1- і 2-бутеніл і 2-метил-2-пропеніл. ма замісниками, вибраними з групи, до якої вхоУ значенні, вживаному в цьому описі, термін дять (С1-С6)алкіл, (С2-С6)алкеніл, галоген, ціаног"двовалентний (С2-С6)алкенілен(овий радикал)" рупа (-CN), -СО2Н, -CO2R, -CONH2 , -CONHR, означає вуглеводневий ланцюг, що містить від 2 CON(R)2, -OH, -OR, оксогрупа, -SH, -SR, -NHCOR атомів до 6 атомів вуглецю, щонайменше один та -NHCO2R, де R є (С1-С6)алкіл або бензил, подвійний зв'язок і має дві вільних валентності. та/або (іі) конденсований з циклоалкілом або гетеУ значенні, вживаному в цьому описі, термін роцикл ом; "(С2-С6)алкініл" означає лінійну або розгалужену R2 є гр упа R1o-(X) n-(ALK)m-, де вуглеводневу груп у, що містить від 2 атомів до 6 R10 є водень або (С1-С6)алкіл, (С2-С6)алкеніл, атомів вуглецю і, крім того, має один потрійний (С2-С6)алкініл, циклоалкіл, арил або гетероцикліл, зв'язок. Цей термін охоплює, наприклад, етиніл, 1кожен з яких може бути незаміщений або заміщепропініл, 1- і 2-бутиніл, 2-метил-2-пропініл, 2ний замісником, вибраним із групи, до якої входять пентиніл, 3-пентиніл, 4-пентиніл, 2-гексиніл, 3(С1-С12)алкіл, (С1-С12)алкокси-, гідрокси-, меркаптогексиніл, 4-гексиніл і 5-гексиніл. , (С1-С12)алкілтіо-, аміногрупа, галоген (в тому чисУ значенні, вживаному в цьому описі, термін лі фтор, хлор, бром і йод), трифторметил, ціано-, "двовалентний (С2-С6)алкінілен(овий радикал)" нітро-, оксогрупа, -СООН, -CONH 2, -COOR A означає вуглеводневий ланцюг, що містить від 2 NHCORA, -CONHRA, -NHRA, -NRARB та -CONRARB, атомів до 6 атомів вуглецю, щонайменше один де RA і RB незалежно один від одного є (С1потрійний зв'язок і має дві вільних валентності. С6)алкіл і У значенні, вживаному в цьому описі, термін ALK є лінійний або розгалужений двовалент"циклоалкіл" означає насичену аліциклічну групу, ний радикал, вибраний з групи, до якої входять що містить від 3 атомів до 8 атомів вуглецю, і охо(С1-С6)алкілен, (С2-С6)-алкенілен та (С2плює, наприклад, циклопропіл, циклобутил, циклоС6)алкінілен, і може бути перерваний одним або пентил, циклогексил, циклогептил і циклооктил. декількома несуміжними містками -NH-, -О- або -SУ значенні, вживаному в цьому описі, термін , X є -NH-, -О-, -S-, -NRC або -NCORC, де RC є (С1"циклоалкеніл" означає ненасичену аліциклічну С12)алкіл і m і з незалежно один від одного є 0 або груп у, що містить від 3 атомів до 8 атомів вуглецю, 15 78275 16 і охоплює, наприклад, циклопропеніл, циклобутенокислоті формули NH2-CH(Rx)-СООН. ніл, циклопентеніл, циклогексеніл, циклогептеніл і До прикладів бічних ланцюгів природних aциклооктеніл. У випадку, якщо циклоалкенільний амінокислот належать бічні ланцюги аланіну, аргіцикл складається з 5-S атомів вуглецю, згаданий ніну, аспарагіну, аспарагінової кислоти, цистеїну, цикл може мати більше ніж один подвійний зв'язок. цистину, глутамінової кислоти, гістидину, 5У значенні, вживаному в цьому описі, термін гідроксилізину, 4-гідроксипроліну, ізолейцину, лей"арил" означає моно-, ди-або трициклічну карбоцину, лізину, метіоніну, фенілаланіну, проліну, сециклічну ароматичну групу, а також групи, що рину, треоніну, триптофану, тирозину, валіну, aскладаються з двох ковалентно зв'язаних моноциаміноадипінової кислоти, a-аміно-н-масляної кисклічних карбоциклічних ароматичних груп. Прилоти, 3,4-дигідроксифенілаланіну, гомосерину, aкладами таких груп є феніл, біфеніл і нафтил. метилсерину, орнітину, піпеколінової кислоти і У значенні, вживаному в цьому описі, не уточтироксину. нений додатково термін "гетероцикліл" або "гетеВ бічних ланцюгах природних a-амінокислот роциклічний" охоплює "гетероарил", визначений (таких як, наприклад, аргінін, лізин, глутамінова нижче, і, зокрема, означає 5-S-членний ароматичкислота, аспарагінова кислота, триптофан, гістиний або неароматичний гетероцикл, що містить дин, серин, треонін, тирозин і цистеїн), які містять один або декілька гетероатомів, вибраних із групи, функціональні замісники, наприклад, аміногрупу, до якої входять S, N і О, і факультативно конденкарбоксил, гідроксил, меркаптогрупу, гуанідил, сований з бензольним циклом або другим гетероімідазоліл або індоліл, такі функціональні заміснициклом; цей термін охоплює, наприклад, піроліл, ки факультативно можуть бути захи щені. фурил, тієніл, піперидиніл, імідазоліл, оксазоліл, Подібним чином, в бічних ланцюгах синтетичтіазоліл, тіадіазоліл, тіазепініл, піразоліл, піридиних a-амінокислот, які містять функціональні замініл, піролідиніл, піримідиніл, морфолініл, піперасники, наприклад, аміногрупу, карбоксил, гідрозиніл, індоліл та бензимідазоліл. ксил, меркаптогрупу, гуанідил, імідазоліл або У значенні, вживаному в цьому описі, термін індоліл, такі функціональні замісники факультати"гетероарил" означає 5- або 6-членний ароматичвно можуть бути за хищені. ний цикл, що містить один або декілька гетероТермін "захищений", застосований до функціатомів і факультативно конденсований з бензольонального замісника в бічному ланцюгу природної ним або піридиновим циклом; групи, що або синтетичної a-амінокислоти, означає похідну складаються з двох ковалентно зв'язаних 5- або 6такого замісника, яка є практично не функціональчленних ароматичних циклів, кожен з яких містить ною. Огляд проблеми захисту можна знайти в шиодин або декілька гетероатомів; і групи, що склароко відомій монографії Гріні та Вутса [T.W. даються з моноциклічної карбоциклічної ароматиGreene and P.G. Wuts "Protective Groups in Organic чної групи, ковалентно зв'язаної з 5- або 6Synthesis", Second Edition, Wiley, New York, 1991]. членними ароматичними циклами, що містять Наприклад, карбоксильні групи можуть бути захиодин або декілька гетероатомів. Прикладами таких щені шляхом утворення складного ефіру (напригруп є тієніл, фурил, піроліл, імідазоліл, бензиміклад, (С1-С6-алкіл)ового складного ефіру), амінодазоліл, тіазоліл, піразоліл, ізоксазоліл, ізотіазогрупи можуть бути перетворені в аміди ліл, триазоліл, тіадіазоліл, оксадіазоліл, піридиніл, (наприклад, NHCO(C1-C6-aлкiл)aмiд) або карбамапіридазиніл, піримідиніл, піразиніл, триазиніл, 4ти (наприклад, NHC(=O)O(C1-C6)алкіл або ([1,2,3]-тіадіазол-4-іл)феніл і 5-ізоксазол-3-ілтієніл. NHC(=O)OCH2Ph-карбамат), гідроксильні групи У значенні, вживаному в цьому описі, не уточможуть бути перетворені в прості ефіри (напринений додатково термін "карбоцикліл" або "карбоклад О(С 1-С6-алкіл)овий або О(С 1-С6циклічний" означає 5-S-членний цикл, всі атоми алкіл)феніловий простий ефір) або складні ефіри циклу якого є вуглецем. (наприклад ОС(=О)(С1-С6-алкіл)овий складний Термін "заміщений", застосований до будьефір), а тіольні групи можуть бути перетворені в якої групи у цьому описі, якщо в контексті, в якому прості тіоефіри (наприклад, трет-бутиловий або він уживається, не зазначено інше, означає замібензиловий простий тіоефір) або складні тіоефіри щений замісниками в кількості до чотирьох, кож(наприклад, SС(=О)(С1-С6-алкіл)овий складний ний з яких незалежно від інших може бути вибратіоефір). ний з групи, до якої входять (С1-С6)алкіл, феніл, У сполуках за цим винаходом присутні щонайбензил, (С1-С6)алкокси-, феноксигрупа, гідроксил, менше два реальних або потенціальних хіральних меркапто-, (С1-С6)алкілтіо-, аміногрупа, галоген (в центри внаслідок присутності в них асиметричних тому числі фтор, хлор, бром і йод), трифторметил, атомів вуглецю. Присутність кількох асиметричних A ціано-, нітро-, оксогрупа, -СООН, -CONH 2 -COR , атомів вуглецю призводить до утворення кількох A A A A A B COOR , -NHCOR , -CONHR , -NHR , -NR R або діастереоізомерів зі стереохімічною конфігурацією A B A B CONR R , де кожний R і R незалежно один від R або S при кожному хіральному центрі. Цей винаіншого є (С1-С6)алкіл. У випадку, якщо "заміщений" хід охоплює усі такі діастереізомери та їхні суміші. означає заміщений бензилом, фенільний цикл На цей час перевага віддається стереоізомерам, в бензилу може сам бути заміщений будь-яким із яких атом вуглецю, до якого приєднана група R2, вищезгаданих замісників, за винятком фенілу або має стереохімічну конфігурацію R; атом вуглецю, бензилу. до якого приєднана група R1 (якщо він є асиметриУ значенні, вживаному в цьому описі, терміни чним), має конфігурацію R; і атом вуглецю, до яко"бічний ланцюг природної a-амінокислоти" і "бічго приєднана група R3 (якщо він є асиметричним), ний ланцюг синтетичної a-амінокислоти" означає має конфігурацію S. груп у Rx відповідно в природній і синтетичній аміГрупа R1 17 78275 18 R1 може бути, наприклад, вибрана з групи, до ніл] пропіл-. якої входять: До груп R2, яким на даний час віддається певодень, гідроксил, метил, метоксигрупа, триревага, належать бензил, н-бутил, ізо-бутил, нфторметил, етил, н-пропіл, алілфенілпропіл, цикгексил, етоксифенілпропіл, за варіантом, якому лопропілметил, фенілпроп-2-еніл, тієнілсульфанівіддається перевага, 4-етоксифенілпропіл і циклолметил, тієнілсульфінілметил та пентилметил. З них на даний час більша перевага тієнілсульфонілметил; або віддається ізобутилу і етоксифенілпропілу, особ(С1-С4)алкіл, наприклад, метил, етил, н-пропіл ливо 4-етоксифенілпропілу. або н-бутил, заміщений замісником, вибраним із Група R3 групи, до якої входять фталімідогрупа, 1,2R3 може бути, наприклад, вибрана з групи, до диметил-3,5-діоксо-1,2,4-триазолідин-4-іл, 3якої входять (С1-С6)алкіл, феніл, 2-, 3- або 4метил-2,5-діоксо- 1-імідазолідиніл, 3,4,4-триметилпіридил, 2- або 3-тієніл, 2-, 3- або 4-гідроксифеніл, 2,5-діоксо-1-імідазолідиніл, 2-метил-3,5-діоксо2-, 3- або 4-метоксифеніл, 2-, 3- або 41,2,4-оксадіазол-4-іл, 3-метил-2,4,5-триоксо-1піридилметил, бензил, 2-, 3- або 4-гідроксибензил, імідазолідиніл, 2,5-діоксо-3-феніл-1-імідазолідиніл, 2-, 3- або 4-бензилоксибензил, 2-, 3- або 4-(С1-С62-оксо-1-піролідиніл, 2,5-діоксо-1-піролідиніл, 2,6алкокси)бензил та бензилокси(С 1-С6-алкіл)-; або діоксопіперидиніл, 5,5-диметил-2,4-діоксо-3характеристична група природної aоксазолідиніл, гексагідро-1,3-діоксопіразоло-[1,2,а] амінокислоти, в якій будь-яка функціональна група [1,2,4]-триазол-2-іл, нафталімідогрупа (тобто 1,3може бути захищеною, будь-яка аміногрупа може дигідро-1,3-діоксо-2Н-бенз[f]ізоіндол-2-іл), 1,3бути ацилованою і будь-яка карбоксильна група дигідро-1-оксо-2Н-бенз[f|ізоіндол-2-іл, 1,3-дигідроможе бути амідованою; або 1,3-діоксо-2Н-піроло[3,4-b]хінолін-2-іл та 2,3група -[Alk]nR6, де Alk є (С1-С6)алкіл або (С2дигідро-1,3-діоксо- 1Н-бенз[(d,е]ізохінолін-2-іл; або С6)алкеніл, факультативно перерваний одним або циклогексил, циклооктил, циклогептил, циклодекількома атомами -О- чи -S- або групами -N(R7)пентил, циклобутил, циклопропіл, тетрагідропіра[де R7 є атом водню або (С1-С6)алкіл], з є 0 або 1, ніл або морфолініл. а R6 є факультативно заміщена циклоалкільна або До груп R1, яким на даний час віддається пециклоалкенільна група; або ревага, належать водень, гідроксил, метоксигрупа, бензильна група, заміщена при фенільному циклопентил, н-пропіл і аліл. З них на даний час циклі групою формули -OCH2COR8, де R8 є гідробільша перевага віддається водню, гідроксилу, ксил, аміно-, (С1-С6)алкокси-, феніл-(С1метоксигрупі і алілу. С6)алкокси-, (С1-С6)алкіламіно-, ди((С1Група R2 С6)алкіл)аміно-, феніл(С 1-С6)алкіламіногрупа, заR2 може бути, наприклад, вибрана з групи, до лишок амінокислоти або галогенангідриду аміноякої входять кислоти, її складного ефіру або аміду, причому (С1-С12)алкіл, (С3-С6)алкеніл або (С3-С6)алкініл; згаданий залишок приєднаний через амідний зв'яциклоалкіл(С 1-С6-алкіл)-; зок, згадана амінокислота вибрана з групи, до якої феніл(С 1-С6-алкіл)-, феніл(С 3-С6-алкеніл)- або входять гліцин, a- або b-аланін, валін, лейцин, феніл(С 3-С6-алкініл)-, факультативно заміщений ізолейцин, фенілаланін, тирозин, триптофан, сепри згаданому фенільному циклі; рин, треонін, цистеїн, метіонін, аспарагін, глутамін, гетероарил(С1-С6-алкіл)-, гетероарил(С 3-С6лізин, гістидин, аргінін, глутамінова кислота та асалкеніл)- або парагінова кислота; або гетероарил(С3-С6-алкініл)-, факультативно загетероцикл(С1-С6)алкіл, незаміщений або заміщений при згаданому гетероарильному циклі; міщений при згаданому гетероциклі одним або 4-фенілфеніл(С 1-С6-алкіл)-, 4-фенілфеніл(С 3двома замісниками, вибраними з групи, до якої С6-алкеніл)-, входять галоген, нітро-, карбокси-, (С1-С6)алкокси-, 4-фенілфеніл(С 3-С6-алкініл)-, 4ціаногрупа, (С1-С6)алканоїл, трифторметил(С1гетероарилфеніл(С1-С6-алкіл)-, С6)алкіл, гідроксил, форміл, аміно-, (С14-гетероарилфеніл(С3-С6-алкеніл)-, 4С6)алкіламіно-, ди-(С1-С6)алкіламіно-, меркапто-, гетероарилфеніл(С3-С6-алкініл)-, факультативно (С1-С6)алкілтіогрупа, гідрокси(С 1-С6)алкіл, меркапзаміщений при кінцевому фенільному або гетерото(С1-С6)алкіл або (С1-С6)алкілфенілметил; або арильному циклі; група -CRaRbRc, в якій: фенокси(С1-С6-алкіл)- або гетероарилокси(С 1кожний з Ra, Rb і Rс незалежно від інших є воС6-алкіл)-, день, (С1-С6)алкіл, (С2-С6)алкеніл, (С2-С6)алкініл, факультативно заміщені при згаданому феніфеніл(С 1-С6)алкіл, (С3-С8)циклоалкіл; або льному або гетероарильному циклі. Rс є водень, a Ra і Rb незалежно один від іншоДо конкретних прикладів таких гр уп належать го є феніл або гетероарил, наприклад, піридил; метил, етил, н- або ізо-пропіл, н-, ізо- або третабо бутил, н-пентил, н-гексил, н-гептил, н-ноніл, нRс є водень, (С1-С6)алкіл, (С2-С6)алкеніл, (С2децил, проп-2-ін-1-іл, циклогексилетил, циклопенС6)алкініл, феніл(С 1-С6)алкіл або (С3тилметил, 3-фенілпроп-2-ін-1-іл, 3-(2С8)циклоалкіл, a Ra і Rb, разом з атомом вуглецю, хлорфеніл)проп-2-ін-1-іл, бензил фенілпропіл, 4до якого вони приєднані, утворюють 3-S-членний хлорфенілпропіл, 4-метилфенілпропіл, 4циклоалкіл або 5-6-членний гетероцикл; або метоксифенілпропіл, феноксибутил, 3-(4Ra, Rb і Rс разом з атомом вуглецю, до якого піридилфеніл)-пропіл-, 3-(4-(4-піридил)феніл)пропвони приєднані, утворюють трициклічну групу (на2-ін-1-іл, 3-(4-феніл)феніл)пропіл-, 3-(4приклад, адамантил); або феніл)феніл)проп-2-ін-1-іл і 3-[(4-хлорфеніл) фекожний з Ra і Rb незалежно від іншого є (С1 19 78275 20 С6)алкіл, (С2-С6)алкеніл, (С2-С6)алкініл, феніл(С 1(ііі) застосування сполуки, що є членом групи, С6)алкіл або група, яка відповідає поданому нижче визначеної вище, при виготовленні лікарського визначенню для Rc за винятком водню, або Ra і Rb засобу для терапії (під якою розуміється лікування разом з атомом вуглецю, до якого вони приєднані, або профілактика) захворювань або хворобливих утворюють циклоалкіл або гетероцикл, a Rс є востанів, опосередкованих ММР. день, -ОН, -SH, галоген, -CN, -СО2Н, (С1До захворювань або хворобливих станів, опоС4)перфторалкіл, -СН2ОН, -СО2(С1-С6)алкіл, -О(С1середкованих ММР, належать ті з них, які виклиС6)алкіл, -О(С2-С6)алкеніл, -S(С1-С6)алкіл, -SО(С1кають руйнування тканин, наприклад, резорбція С6)алкіл, -SО2(С1-С6)алкіл, -S(С2-С6)алкеніл, кісток, запальні захворювання, дерматологічні паSО(С2-С6)алкеніл, -SО2(С2-С6)алкеніл або група тологічні стани і ріст пухлини або її інвазія внасліQ-W, де Q є зв'язок або -О-, -S-, -SO- або -SO2- і W док вторинних метастазів; зокрема, ревматоїдний є феніл, фенілалкіл, (С3-С8)циклоалкіл, (С3артрит, остеоартрит, періодонтит, гінгівіт, укриванС8)циклоалкілалкіл, (С4-С8)циклоалкеніл, (С4ня виразками рогівки, нейрозапальні захворюванС8)циклоалкенілалкіл, гетероарил або гетероариня, в тому числі такі, що викликають руйнування лалкіл, причому група W може бути факультативмієлінових волокон, наприклад, розсіяний склероз; но заміщена одним або декількома замісниками, рестеноз, емфізематоз, бронхіт та астма. незалежно один від одного вибраними з групи, до За подальшим аспектом цього винаходу, проякої входять гідроксил, галоген, -CN, -СО2Н, понується фармацевтична композиція для застоСО2(С1-С6)алкіл, -CONH2, -CONH(C1-C6-алкіл), сування в медицині або ветеринарії, яка містить CONH(C1-C6-алкіл)2, -СНО, -СН2ОН, (С1сполуку, що є членом групи, визначеної вище, раС4)перфторалкіл, -О(С1-С6)алкіл, -S(С1-С6)алкіл, зом з фармацевтично або ветеринарно прийнятSО(С1-С6)алкіл, -SО2(С1-С6)алкіл, -NO2, -NH2, ним наповнювачем або носієм. NН(С1-С6)алкіл, -N((C1-C6)aлкiл)2, -NНСО(С1Мається на увазі, що конкретний рівень дозуС6)алкіл, (С1-С6)алкіл, (С2-С6)алкеніл, (С2вання для будь-якого окремого пацієнта залежить С6)алкініл, (С3-С8)циклоалкіл, (С4-С8)циклоалкеніл, від різноманітних чинників, в тому числі від активфеніл або бензил. ності конкретної застосовуваної сполуки, віку, маДо конкретних прикладів груп R3 належать беси тіла, загального стану здоров'я, статі, харчунзил, феніл, циклогексилметил, піридин-3-ілметил, вання, часу введення в організм, способу трет-бутоксиметил, ізо-пропіл, ізо-бутил, вторвведення, швидкості виведення, суп утньої терапії бутил, трет-бутил, 1-бензилтіо-1-метилетил, 1та тяжкості конкретного захворювання, що підляметилтіо-1-метилетил і 1-меркапто-1-метилетил. гає терапії. Оптимальні рівні дозування та частоту До груп R3, яким на даний час віддається пезастосування визначають шляхом клінічних проб. ревага, належать феніл, бензил, третСполуки, яких стосується цей винахід, можуть бутоксиметил, ізо-пропіл, трет-бутил, і ізо-бутил. З бути приготовані для введення в організм будьних на даний час більша перевага віддається третяким шляхом, сумісним з їхніми фармакокінетичбутил і бензилу. ними властивостями. Композиції для пероральноГрупа R4 го застосування можуть мати форму таблеток, R4 може бути, наприклад, вибрана з групи, до капсул, порошків, гранул, пастилок, рідин або геякої входять (С1-С6)алкіл, наприклад, метил, етил, лів, наприклад, розчинів або суспензій для перон- або ізо-пропіл, проп-2-іл, і трет-бутил; (С3рального, місцевого або стерильного парентераС8)циклоалкіл, наприклад, циклопропіл або циклольного введення. Таблетки та капсули для пентил; феніл; феніл(С 1-С6алкіл)-, наприклад, бенперорального застосування можуть мати форму зил; гетероарил(С1-С6алкіл)-, наприклад, тієнілмедозованих одиниць і містити звичайні допоміжні тил; моноциклічний гетероцикл, наприклад, речовини, наприклад, в'яжучі речовини, наприморфоліногрупа; або моноциклічний гетероарил, клад, сироп, акацієву камедь, желатин, сорбіт, наприклад, тієніл або фураніл. Будь-який зі згадатрагант або полівінілпіролідон; наповнювачі, наних ви ще замісників може бути факультативно приклад, лактозу, цукор, кукурудзяний крохмаль, заміщений, наприклад замісником, вибраним із фосфа т кальцію, сорбіт або гліцин; змащувальний групи до якої входять метил, трифторметил, гідрозасіб для таблетування, наприклад, стеарат магксил, меркапто-, аміногрупа або карбоксил. нію, тальк, поліетиленгліколь або діоксид кремнію; Як вказано вище, сполуки за цим винаходом є дезінтегратори, наприклад, картопляний крохмаль, корисними в медицині або ветеринарії, оскільки або прийнятні змочувачі, наприклад, лаурилсульвони діють як інгібітори ММР. Відповідно, в іншому фат натрію. Таблетки можуть мати покриття, нааспекті цей винахід стосується: несене способами, добре відомими у фармацев(і) способу терапії (під якою розуміється лікутичній практиці. Рідкі лікарські форми для вання або профілактика) захворювань або хвороперорального застосування можуть мати форму, бливих станів, опосередкованих ММР, у ссавців, наприклад, суспензій, розчинів, емульсій, сиропів зокрема, у людей, який включає введення в оргаабо еліксирів на водній або масляній основі, або нізм згаданого ссавця ефективної кількості сполуможуть бути виготовлені у формі сухих продуктів ки, що є членом групи, визначеної вище, або фардля відновлення за допомогою води або іншого мацевтично прийнятної солі такої сполуки; і придатного носія перед застосуванням. Такі рідкі (іі) сполуки, що є членом групи, визначеної лікарські форми можуть містити відомі домішки, вище, для застосування в медицині або ветеринанаприклад, суспендувальні речовини, наприклад, рії, зокрема, в терапії (під якою розуміється лікусорбіт, сироп, метилцелюлозу, сироп глюкози, жевання або профілактика) захворювань або хворолатин, гідровані їстівні жири; емульгатори, наприбливих станів, опосередкованих ММР; і клад, лецитин, сорбітанмоноолеат або акацієву 21 78275 22 камедь; неводні носії (до яких можуть належати наприклад, метабісульфіт натрію або динатрієву їстівні олії), наприклад, мигдальну олію, фракціосіль етилендіамінтетраоцтової кислоти; консервановану кокосову олію, маслоподібні складні ефіри, нти, в тому числі бактерициди та фунгіциди, нанаприклад, гліцерин, пропіленгліколь, або етилоприклад, ацетат або нітрат фенілртуті, бензалковий спирт; консерванти, наприклад, метил- або нійхлорид або хлоргексидин, і загусники, пропіл-n-гідроксибензоат або сорбінову кислоту, і, наприклад, гідроксипропілметилцелюлозу. за бажанням, звичайні смакоароматичні домішки Активний інгредієнт можна вводити в організм або барвники. також парентерально у стерильному середовищі. Для місцевого нанесення на шкіру лікарська Залежно від застосовуваного носія та концентраречовина може бути введена до складу крему, ції, лікарська речовина може бути розчинена або лосьйону або мазі. Креми або мазі, які можуть бусуспендована в носії. Доцільно,щоб у носії були ти застосовані для використання вищезгаданих розчинені також допоміжні речовини, наприклад, лікарських речовин, є відомими в галузі звичайнимісцеві анестетики, консерванти та буферні сполуми лікарськими формами, описаними, наприклад, ки. у стандартних підручниках та довідниках із фармаСполуки за цим винаходом, в яких W є група кології, наприклад, у Британській Фармакопеї гідроксамової кислоти HONH(C=O)-, можуть бути (British Pharmacopeia). одержані з відповідних сполук за цим винаходом, в Для місцевого внесення в око лікарська речояких W є карбоксильна група -СООН, або з відповина може бути введена до складу розчину або відних похідних захищених гідроксамових кислот. суспензії у відповідному стерильному водному або Спосіб, який становить інший аспект цього винаневодному носії. Така лікарська форма може місходу, включає проведення реакції кислоти загальтити також домішки, наприклад, буферні сполуки, ної формули (ІІА) або (ИВ) або її активованої похідної з гідроксил аміном, О-захищеним (тобто захищеним при атомі О) гідроксиламіном або N,O-дизахищеним гідроксиламіном, або їхніми солями, причому X, R1, R2, R3 і R4 відповідають визначенням для загальної формули (ІА) або (IB), за винятком того, що будь-який замісник при R1, R2, R3 і R4 , який потенціально здатний вступати в реакцію з гідроксиламіном, Озахищеним гідроксиламіном, N,O-дизахищеним гідроксиламіном або їхніми солями, може сам бути захищеним від такої реакції, з подальшим відщепленням будь-яких захисних груп від одержаної групи гідроксамової кислоти та від будь-яких захи щених замісників при R1, R2, R3 і R4 . Перетворення сполуки формули (IIА) або (IIВ) в активовану похідну, наприклад, у згадані пентафтор феніловий, гідроксисукциніловий або гідроксибензотриазоліловий складний ефір, може бути здійснено шляхом проведення реакції з придатним спиртом у присутності дегідрувального реагенту, наприклад, дициклогексилдикарбодііміду (DCC), N,N-диметил-амінопропіл-N-етилкарбодііміду (EDC) або 2-етокси-1-етоксикарбоніл-1,2дигідрохіноліну (EEDQ). Захисні групи, наприклад, вказані вище, самі по собі добре відомі, наприклад, у галузі хімії пептидів. Аміногрупи часто можна захистити бензилоксикарбонілом, трет-бутоксикарбонілом або ацетилом, або шляхом утворення фталімідогрупи. Гідроксильні групи часто можна захистити шляхом утворення легко розщеплюваних простих ефірів, наприклад, трет -бутилового або бензилового простого ефіру, або шляхом утворення легко розщеп люваних складних ефірів, наприклад, ацетату. Карбоксильні групи часто можна захистити шляхом утворення легко розщеплюваних складних ефірів, наприклад, трет-бутилового або бензилового складного ефіру. До прикладів О-захищених гідроксиламінів, придатних для застосування у вищезгаданому способі (а), належать О-бензилгідроксиламін, О-4метоксибензилгідроксиламін, Отриметилсилілгідроксиламін і О-третбутоксикарбонілгідроксиламін. До прикладів O,N-дизахищених гідроксиламінів, придатних для застосування у вищезгаданому способі (а), належать N,О-біс(бензил)гідроксиламін, N,О-біс(4метоксибензил)гідроксиламін, N-трет-бутоксикарбоніл-О-трет -бутилдиметилсилілгідроксиламін, N-трет-бутоксикарбоніл-Отетрагідропіранілгідроксиламін і N,O-бic(третбутоксикарбоніл)-гідроксиламін. Сполуки за цим винаходом, в яких W є Nформілгідроксиламіногрупа H(C=O)NH(OH)-, можуть бути одержані шляхом N-формілування відповідних О-захищених сполук, в яких W є -NH(OH), з подальшим відщепленням згаданої групи захисту О. Сполуки за цим винаходом, в яких W є карбоксильна група -СООН, тобто сполуки вищезгаданої формули (ІІА) або (ІІВ), можуть бути одержані за допомогою способу, який включає: сполучення кислоти формули (III) або її активованої похідної 23 78275 де X, R1 R 2, R 3 і R4 відповідають визначенням для загальної формули (ІА) і (IB), за винятком того, що будь-який замісник при R1, R2, R3 і R4, який є потенціально здатним до згаданої реакції сполучення, може сам бути захищений від такої реакції, і R11 є група захисту гідроксилу, з подальшим відщепленням захисної групи R11 і будь-яких захисних гр уп від R1 R 2, R3 та R4 . До активних похідних кислот (III) належать активовані складні ефіри, наприклад, пентафторфеніловий складний ефір, ангідриди кислот та галогенангідриди кислот, наприклад, хлорангідриди. Придатні групи захисту гідроксилу можна вибрати з груп, відомих у галузі. Сполуки формули (IVА) і (IVB) можна одержати способами, аналогічними загальним способам формування оксадіазольного циклу, ілюстрованими у Схемі 1 і Схемі 2, поданими нижче у Прикладі 1 і Прикладі 2. У поданих нижче препаративних Прикладах описано одержання сполук, які можна застосовувати згідно з цим винаходом. У Прикладах застосовані такі абревіатури: DCM - ди хлорметан 24 з аміном формули (IVA) або (ІVB) DMF - N,N-диметилформамід НОВТ - 1-гідроксибензотриазол Pfp - Пентафторфенол WSCDI N-(3-димeтилaмiнoпpoпiл)-N'eтилкapбoдiiмiдy гідрохлорид НСl - хлористоводнева кислота THF - тетрагідрофуран TFA - трифтороцтова кислота Р(O-Тоl)3 - три-О-толілфосфін AcOEt - е тилацетат CH3CN - ацетонітрил Приклад 1 3R-[2,2-димeтил-1S-(5-фeнiл-[1,2,4]oкcaдiaзoл3-iл)-пpoпiлкapбaмoїл]-2S-гідрокси-5-метилгексангідроксамова кислота 25 78275 Реагенти та умови: Стадія A: HOBt, WSC, NH3, DMF. Стадія В: РОСl3, піридин. Стадія С: водний NH2OH, етанол, 70°С. Стадія D: RCOCl, DMAP, піридин, DMF, 100°С. Стадія Е: НВr/оцтова кислота. Стадія F: хіральний сукцинат, DMF. С тадія G: водний NH 2OH, метанол. Стадія Н: Pfp, WSC, DMF. Стадія І: 1 М НСl, THF. Сполуку за Прикладом 1 одержали, як зображено на Схемі 1, із застосуванням методики, описаної нижче. Стадія А. Бензиловий складний ефір (1Sкарбамоїл-2,2-диметилпропіл)-карбамінової кислоти N-бензилоксикарбоніл-d-трет-бутилгліцин (50г, 189 ммоль) розчиняли у DMF (500мл) і охолоджували на водо-льодяній бані, після чого додавали НОВТ (28,05г, 208 ммоль) і WSCDI (39,8г, 208 ммоль). Реакційну суміш перемішували при 0°С протягом 1 год, а потім додавали 0,880 розчину 26 аміаку (21мл, 377 ммоль). Реакційну суміш витримували для нагрівання до кімнатної температури і перемішували протягом 18 год. DMF видаляли під зниженим тиском, і одержаний залишок розподіляли між етилацетатом і 1М НСl. Одержаний органічний шар відділяли і промивали 1М НСl, насиченим водним розчином бікарбонату натрію і розсолом, сушили над сульфатом магнію, фільтрували і концентрували під зниженим тиском. Одержали бензиловий складний ефір (1Sкарбамоїл-2,2-диметилпропіл)-карбамінової кислоти у вигляді білої твердої речовини (44,1г, 89%). 1 Н-ЯМР; d (CDCl3), 7,32 (5Н, m), 6,05 (1Н, bs), 5,71 (1H, bs), 5,60 (1H, d, J=6,5Гц), 5,08 (2H, s), 4,01 (1H, d, J=6,5Гц) і 1,00 (9H, s). Mac-спектроскопія низького розділення (LRMS); позитивний іон 265 (М+Н), 287 (M+Na). Стадія В. Бензиловий складний ефір (1S-ціан2,2-диметилпропіл)-карбамінової кислоти 27 78275 28 Бензиловий складний ефір (1S-карбамоїл-2,2Стадія Е. 2,2-диметил-1S-(5-фенілдиметилпропіл)-карбамінової кислоти (44,1г, 167 [1,2,4]оксадіазол-3-іл)-пропіламін ммоль) розчиняли в безводному піридині (203мл, Бензиловий складний ефір [2,2-диметил-1S-(52,5 моль) в інертній атмосфері і охолоджували на феніл-[1,2,4]оксадіазол-3-іл)-пропіл]-карбамінової водо-льодяній бані. Протягом приблизно 15хв покислоти (0,2г, 0,5 ммоль) обробляли 48% розчивільно додавали оксихлорид фосфору (21,8мл, ном бромоводню в оцтовій кислоті (10мл). Реак234 ммоль), і одержану реакційну суміш витримуційну суміш перемішували при кімнатній темперавали при перемішуванні на водо-льодяній бані турі протягом 3 год. Реакційну суміш протягом 2 год, потім нагрівали до кімнатної темконцентрували під зниженим тиском і розподіляли ператури і перемішували протягом 12 год. Одерміж етилацетатом і 1М Na2CO3. Органічний шар жану реакційну суміш обробляли сумішшю льоду з додатково промивали 1М Na2CO3 і розсолом, суводою (400мл) і екстрагували етилацетатом шили над сульфатом магнію, фільтрували і конце(2x300мл). Органічний шар відділяли і промивали нтрували під зниженим тиском. Продукт виділяли у 1М НСl, насиченим водним розчином бікарбонату вигляді жовтого масла (0,13г, 98%). натрію і розсолом, сушили над сульфатом магнію, LRMS; позитивний іон 232 (М+Н). фільтрували і концентрували під зниженим тиском. Стадія F. [2,2-диметил-1S-(5-фенілХроматографією на колонці із силікагелем із за[1,2,4]оксадіазол-3-іл)-пропіл]-амід 2R-(2,2стосуванням суміші етилацетату з гексаном як димeтил-5-oкco-[1,3]дioкcoлaн-4S-iл)-4-мeтилелюенту виділяли потрібний продукт у вигляді пeнтaнoвoї кислоти оранжевого масла (36,72г, 89%). 2,2-диметил-1S-(5-феніл-[1,2,4]оксадіазол-31 іл)-пропіламін (0,13 г, 0,6 ммоль) розчиняли у DMF Н-ЯМР; d (CDCl3), 7,42 (5Н, m), 5,28 (2Н, m), (5 мл) і охолоджували на водо-льодяній бані, після 4,55 (2Н, d, J=6,5 Гц) і 1,11 (9Н, s). LRMS; позитивний іон 269 (M+Na), 247,2 чого додавали пентафторфеніловий складний ефір 2R-(2,2-диметил-5S-оксо-[1,3]діоксолан-4-іл)(М+Н). 4-метил-пентанової кислоти (0,22 г, 0,6 ммоль). Стадія С. Бензиловий складний ефір [1S-(NРеакційну суміш ви тримували для нагрівання до гідрокси-карбамімідоїл)-2,2-диметилпропіл]кімнатної температури і перемішували протягом 15 карбамінової кислоти Бензиловий складний ефір (1S-ціан-2,2год. DMF видаляли під зниженим тиском, і реакційну суміш розбавляли етилацетатом і промивали диметилпропіл)-карбамінової кислоти (37,60г, 153 1М НСl, насиченим водним розчином бікарбонату ммоль) розчиняли в етанолі (300мл) і додавали натрію і розсолом, сушили над сульфатом магнію, краплями 50% водний розчин гідроксил аміну фільтрували і концентрували під зниженим тиском. (51мл, 764 ммоль). Реакційну суміш нагрівали зі зворотним холодильником і перемішували протяХроматографією на колонці із силікагелем із застосуванням суміші етилацетату і гексану (1:1) гом 3 год. Потім реакційну суміш о холоджували і виділяли потрібний продукт у вигляді білої твердої концентрували під зниженим тиском, одержуючи речовини (0,16 г, 64%). потрібний продукт у вигляді білої піни/смоли (41,5г, 97%). 1Н-ЯМР; d (CDCl3), 8,12 (2Н, m), 7,55 (3Н, m), 1 6,65 (1Н, d, J=6,4 Гц), 5,25 (1Н, d, J=6,5 Гц), 4,55 Н-ЯМР; d (CDCl3), 7,32 (5Н, m), 6,21 (1Н, bs), (1H, d, J=5,9 Гц), 2,75 (1H, m), 1,64 (3H, s), 1,55 5,95 (1H, bs), 5,81 (1H, d, J=6,4Гц), 5,08 (2H, m), (3H, s), 1,04 (9H, s) і 0,88 (6H, m). 4,79 (1H, bs), 4,05 (1H, d, J=6,5 Гц) і 0,95 (9H, s). LRMS; позитивний іон 444 (М+Н). LRMS; позитивний іон 279,8 (М+Н). Стадія G. 3R-[2,2-димeтил-1S-(5-фeнiлСтадія D. Бензиловий складний ефір [2,2[1,2,4]oкcaдiaзoл-3-iл)-пpoпiл-карбамоїл]-2Sдиметил-1S-(5-феніл-[1,2,4]оксадіазол-3-іл)гідрокси-5-метил-гексангідроксамова кислота пропіл]-карбамінової кислоти [2,2-диметил-1S-(5-феніл-[1,2,4]оксадіазол-3Бензиловий складний ефір [1S-(Nіл)-пропіл]-амід 2R-(2,2-диметил-5S-оксогідроксикарбамімідоїл)-2,2-диметилпропіл][1,3]діоксолан-4-іл)-4-метил-пентанової кислоти карбамінової кислоти (0,21г, 0,75 ммоль) розчиня(0,05 г, 0,11 ммоль) розчиняли у метанолі (2 мл) і ли у DMF (5мл), і додавали піридин (0,1мл, 1,28 обробляли 50% водним розчином гідроксиламіну ммоль), бензоїлхлорид (0,13мл, 1,1 ммоль) і DMAP (0,04 мл, 0,5 ммоль). Реакційну суміш перемішу(каталітичну кількість). Реакційну суміш перемішували при кімнатній температурі протягом 2 год, вали при кімнатній температурі протягом 4 год, після чого випаровували під зниженим тиском. потім нагрівали до 100°С і перемішували протягом Продукт реакції відділяли препаративною хрома16 год. Реакційну суміш знову о холоджували до тографією з оберненою фазою, одержуючи потрікімнатної температури і концентрували під знижебний продукт у вигляді білої твердої речовини ним тиском. Одержану реакційну суміш розбавля(0,02 г, 44%). ли етилацетатом і промивали 1М НСl, насиченим 1 водним розчином бікарбонату натрію і розсолом, Н-ЯМР; d (CH3OD), 8,13 (2Н, m), 7,65 (1Н, m), сушили над сульфатом магнію, фільтрували і кон7,58 (2H, m), 5,14 (1H, s), 4,01 (1H, d, J=7,1 Гц), центрували під зниженим тиском. Потрібний про2,94 (1H, m), 1,60 (1H, m), 1,45 (1H, m), 1,16 (1H, дукт виділяли у вигляді оранжевого масла (0,22г, m), 1,07 (9H, s), 0,89 (3H, d, J=6,5 Гц) і 0,86 (3H, d, 78%). J=6,6 Гц). 1 13 Н-ЯМР; d (CDCl3), 8,12 (2Н, m), 7,55 (3Н, m), С-ЯМР; d (CH3OD), 177,1, 176,3, 172,0, 171,6, 7,32 (5Н, m), 5,55 (1Н, d, J=6,4 Гц), 5,12 (2H, m), 134,6, 130,8, 129,4, 125,7, 73,7, 55,8, 49,6, 39,7, 4,95 (1H, d, J=6,5 Гц) і 1,10 (9H, s). 36,2, 27,4, 27,2, 24,2 і 22,5. LRMS; позитивний іон 366,2 (М+Н), 388,2 LRMS; позитивний іон 419 (М+Н); негативний (M+Na). іон 417 (М-Н). 29 78275 30 Стадія Н. Пентафторфеніловий складний ефір нижче. 2R-(2,2-диметил-5-oкco-[1,3]діоксолан-4S-іл)-4Стадія І. 3R-[1S-(5-фypaн-2-iлметил-пентанової кислоти [1,2,4]oкcaдiaзoл-3-iл)-2,2-димeтилпpoпiл2R-(2,2-димeтил-5-oкco-[1,3]дioкcoлaн-4S-iл)-4карбамоїл]-2S-гідрокси-5-метил-гексанова кислота мeтил-пeнтaнoвy кислоту (одержану відповідно до [2,2-диметил-1S-(5-фуран-2-ілWO 94/02447, (30 г, 130 ммоль) розчиняли в ети[1,2,4]оксадіазол-3-іл)-пропіл]-амід 2R-(2,2лацетаті (300 мл) і обробляли пентафторфенолом диметил-5S-оксо-[1,3]діоксолан-4-іл)-4-метил(28,8 г, 156 ммоль) і WSCDI (30 г, 156 ммоль). Реапентанової кислоти (0,05 г, 0,12ммоль) розчиняли кційну суміш нагрівали зі зворотним холодильниу те трагідрофурані (5 мл) і охолоджували до 4°С, ком протягом 2 год і потім витримували при передодаючи одночасно 1 М хлористоводневу кислоту мішуванні при кімнатній температурі протягом 12 (5 мл). Одержаний розчин витримували для нагрігод. Одержану реакційну суміш промивали 1М вання до кімнатної температури і потім перемішуNa2CO3 і розсолом, сушили над сульфатом магнію, вали протягом 18 год. Більшу частину розчинника фільтрували і концентрували під зниженим тиском. видаляли під зниженим тиском, сушили залишок Продукт перекристалізовували із суміші етилацепід високим вакуумом, одержуючи білу піну (0,045 тату з гексаном, одержуючи потрібний продукт у г, ви хід майже кількісний). 1 формі індивідуального діастереомеру (21,2 г, Н-ЯМР; d (CH3OD), 7,88 (1Н, s), 7,45 (1H, d, 42%). J=3,6 Гц), 6,74 (1H, m), 5,15 (1H, s), 4,18 (2H, d, 1 Н-ЯМР; d (CDCl3), 4,55 (1Н, d, J=6,7 Гц), 3,31 J=6,4 Гц), 2,91 (1H, m), 1,65 (1H, m), 1,50 (1H, m), (1H, m), 1,85 (3H, bm), 1,65 (3H, s), 1,58 (3H, s), 1,31 (1H, m), 1,06 (9H, s), 0,88 (3H, d, J=6,4 Гц) і 1,05 (3H, d, J=6,5 Гц) і 0,99 (3H, d, J=6,5 Гц). 0,82 (3H, d, J=6,5 Гц). Одержали також діастереомерну 3R-[2,2LRMS; негативний іон 392,2 (M-H). диметил-1S-(5-феніл-[1,2,4] оксадіазол-3-іл)Приклад 2 пропілкарбамоїл]-2R-гідрокси-5-метил3R-[2,2-димeтил-1S-(3-фeнiл-[1,2,4]oкcaдiaзoлгексангідроксамову кислоту. 5-iл)-пpoпiлкapбaмoїл]-2S-гідрокси-5-метилгексангідроксамова кислота М+Н=420,0, M+Na=441,5, M-H=417,5. Відповідну карбонову кислоту одержали, як зображено на Схемі 1, і за методикою, описаною 31 78275 Реагенти та умови: Стадія А: НОВТ, WSCDI, DMF. Стадія В: толуол, 100°С. Стадія С: водний NH2OH, етанол, 70°С. Стадія D: TFA, DCM. Стадія Е: НОВТ, WSCDI, DMF. Стадія F: водний NH2OH, метанол. Сполуку за Прикладом 2 одержали, як зображено на Схемі 2, із застосуванням методики, описаної нижче. Стадія А. Бензотриазол-1-іловий складний ефір 2S-трет-бутокси-карбоніламіно-3,3диметилмасляної кислоти Розчин N-трет-бyтoкcикapбoнiл-L-третбyтилглiцинy (5 г, 21,6 ммоль) в етилацетаті (80 мл) охолоджували на водо-льодяній бані. Додавали НОВТ (3,22 г, 23,8 ммоль) і WSCDI (4,56 г, 23,8 ммоль), і одержану реакційну суміш витримували при перемішуванні при кімнатній температурі протягом 12 год. Одержану реакційну суміш промивали 1 М Na2CO3 і розсолом, сушили над сульфатом 32 магнію, фільтрували і концентрували, одержуючи білу піну (5,74 г, 76%). 1 Н-ЯМР; d (CDCl3), 8,05 (1Н, m), 7,65 (2H, m), 7,41 (1H, m), 5,10 (1H, d, J=6,7 Гц), 4,45 (1H, d, J=6,5 Гц), 1,55 (9H, s) і 1,21 (9H, s). LRMS; позитивний іон 349 (M+H). Стадія В. Трет-бутиловий складний ефір [2,2диметил-1S-(3-феніл-[1,2,4]оксадіазол-5-іл)пропіл]-карбамінової кислоти Бензотриазол-1-іловий складний ефір 28-третбутоксикарбоніламіно-3,3-диметил-масляної кислоти (3,71 г, 10,7 ммоль) розчиняли у толуолі (80 мл) і додавали N-гідроксибензамідин (2,9 г, 21,3 ммоль). Реакційну суміш перемішували при 110°С протягом 18 год. Одержаний розчин концентрували під зниженим тиском і розподіляли між етилацетатом і 1 М Na2CO3. Органічний шар додатково промивали 1 М Na2CO3 і розсолом, сушили над 33 78275 34 сульфатом магнію, фільтрували і концентрували фатом магнію, фільтрували і концентрували під під зниженим тиском. Хроматографією на колонці зниженим тиском. Хроматографією на колонці із із силікагелем із застосуванням суміші етилацетасилікагелем із застосуванням суміші етилацетату і ту з гексаном (1:4) виділяли потрібний продукт гексану (1:4) виділяли потрібний продукт (0,26 г, (2,58 г, 73%). 46%). 1 1 Н-ЯМР; d (CDCl3), 8,10 (2Н, m), 7,50 (3Н, m), Н-ЯМР; d (CDCl3), 8,10 (2Н, m), 7,50 (3Н, m), 5,30 (1Н, bd), 4,95 (1Н, d, J=6,5 Гц), 1,44 (9H, s) і 6,80 (1Н, d, J=9,3 Гц), 5,24 (1H, d, J=9,3 Гц), 4,55 1,03 (9H, s). (1H, d, J=5,1 Гц), 2,81 (1H, m), 1,63 (3H, s), 1,55 LRMS; позитивний іон 354.2 (M+Na). (3H, s), 0,92 (3H, d, J=6,1 Гц) і 0,89 (3Н, d, J=6,2 Стадія С. N-гідрокси-бензамідин Гц). Бензонітрил (5 г, 48 ммоль) розчиняли в етаLRMS; позитивний іон 444 (М+Н). нолі (100 мл) і обробляли 50% водним розчином Стадія F. 3R-[2,2-димeтил-1S-(3-фeнiлгідроксил аміну (16 мл, 242 ммоль). Реакційну су[1,2,4]oкcaдiaзoл-5-iл)-пpoпiл-карбамоїл]-2Sміш нагрівали зі зворотним холодильником протягідрокси-5-метил-гексангідроксамова кислота гом 3 год, концентрували під зниженим тиском, [2,2-диметил-1S-(3-феніл-[1,2,4]оксадіазол-5одержуючи світлу піну (4,5 г, 68%). іл)-пропіл]-амід 2R-(2,2-диметил-5-оксоLRMS; позитивний іон 137 (М+Н). [1,3]діоксолан-4S-іл)-4-метил-пентанової кислоти Стадія D. 2,2-диметил-1S-(3-феніл(0,26 г, 0,6 ммоль) розчиняли у метанолі (5 мл), і [1,2,4]оксадіазол-5-іл)-пропіламін додавали 50% водний розчин гідроксиламіну (0,2 Трет-бутиловий складний ефір [2,2-диметилмл, 2,95 ммоль). Реакційну суміш перемішували 15-(3-феніл-[1,2,4]оксадіазол-5-іл)-пропіл]при кімнатній температурі протягом 3 год, після карбамінової кислоти (1 г, 3,0 ммоль) розчиняли у чого концентрували під зниженим тиском. ПотрібDCM (5 мл) і додавали TFA (5 мл). Реакційну суний продукт перекристалізовували із суміші етиміш перемішували при кімнатній температурі пролацетату з гексаном, одержуючи потрібний протягом 3 год. Реакційну суміш концентрували під дукт (0,11 г, 41%). 1 зниженим тиском і розподіляли між етилацетатом і Н-ЯМР; d (CH3OD), 8,06 (2Н, m), 7,53 (3Н, m), 1 М Na2CO3. Ор ганічний шар додатково промива5,21 (1Н, s), 4,01 (1H, d, J=7,5 Гц), 2,99 (1H, m), ли 1 М Na2CO3 і розсолом, сушили над сульфатом 1,60 (1H, m), 1,50 (1H, m), 1,15 (1H, m), 1,10 (9H, s), магнію, фільтрували і концентрували під зниженим 0,92 (3H, d, J=6,6 Гц) і 0,81 (3Н, d, J=6,5 Гц). 13 тиском, одержуючи потрібний продукт (0,65 г, С-ЯМР; d (CH3OD), 180,3, 176,7, 172,0, 169,7, 93%). 132,9, 130,5, 128,8, 128,4, 73,7, 57,1, 49,5, 39,5, 1 Н-ЯМР; d (CH3OD), 8,10 (2Н, m), 7,55 (3Н, m), 36,5, 27,3, 24,3 і 22,5. 4,81 (1Н, s) і 1,19 (9H, s). LRMS; позитивний іон 419 (М+Н); негативний LRMS; позитивний іон 232 (М+Н). іон 417 (М-1). Стадія Е. [2,2-диметил-1S-(3-фенілПриклад 3 [1,2,4]оксадіазол-5-іл)-пропіл]-амід 2R-(2,22R-[3-(4-eтoкcи-фeнiл)-пpoпiл]-N1-[1S-(5димeтил-5-oкco-[1,3]дioкcoлaн-4S-iл)-4-мeтилтioфeн-2-iл)-[1,2,4]oкcaдiaзoл-3-іл)-2,2пeнтaнoвoї кислоти диметилпропіл]-3S,N4-дигідрокси-сукцинамід 2R-(2,2-димeтил-5-oкco-[1,3]дioкcoлaн-4S-iл)-4мeтил-пeнтaнoвy кислоту (0,27 г, 1,17 ммоль) розчиняли у DMF (5 мл) і охолоджували на водольодяній бані, після чого додавали НОВТ (0,17 г, 1,29 ммоль) і WSCDI (0,25 г, 1,29 ммоль). Реакційну суміш перемішували при 0°С протягом 1 год, потім додавали 2,2-диметил-1S-(3-феніл[1,2,4]оксадіазол-5-іл)-пропіламін (0,3 г, 1,29 ммоль). Реакційну суміш витримували для нагрівання до кімнатної температури і перемішували протягом 18 год. DMF видаляли під зниженим тиском, і одержаний залишок розподіляли між етилацетатом і 1 М НСl. Органічний шар відділяли, промивали 1 М НСl, насиченим водним розчином бікарбонату натрію ірозсолом, сушили над суль 35 78275 Реагенти та умови: Стадія A: LiHMDS, AlIBr, THF, від -78°С до кімнатної температури; Стадія В: 4-ОЕt-фенілбромід, три-о-толілфосфат, Pd(OAc)2, триетиламін, CH3CN; Стадія С: 10% Pd/C, H2, МеОН; Стадія D: LiOH, МеОН, Н2О; Стадія Е: СuСl2, диметоксіацетон, ацетон; Стадія F: пентафторфенол, WSC, HOAt, CH2Cl2; Стадія G: амін (детально зображений на Схемі 1, Стадія Е), DMF; Стадія Н: водний NH 2OH, iPrOH Сполуку за Прикладом 3 одержали, як зображено на Схемі 3, із застосуванням методики, описаної нижче. Стадія А: Діізопропіловий складний ефір 2Raлiл-3S-гiдpoкcи-бурштинової кислоти До холодного (-78С) розчину діізопропілового складного ефіру 2S-гідрокси-бурштинової кислоти (19,70 мл, 95 ммоль) у THF (35 мл) додавали краплями LiHMDS (200 мл, 0,2 моль, 2,1 екв.). Реакційну суміш перемішували при -78°С протягом 2 год і потім при -30°С протягом 30 хв. Потім реакційну суміш охолоджували до -78°С, і додавали краплями алілбромід (12,36 мл, 0,14 моль, 1,5 екв.). Реакційну суміш витримували для нагрівання до кімнатної температури протягом ночі. її виливали у суміш насиченого розчину NH4C1 із льодом (200 мл). Після екстрагування AcOEt (3 x200 мл) із подальшим промиванням водою (50 мл) і розсолом (50 мл) і видалення розчинника під вакуумом одержали жовте масло. Після очищення флешхроматографією одержали діізопропіловий складний ефір 2R-aлiл-3S-гiдpoкcи-бypштинoвoї кислоти у вигляді безбарвного масла (7,76 г, діастереомерний надлишок 80%, вихід 40%). 1 Н-ЯМР; d (CDCl3), 5,77-5,88 (1Н, m), 4,98-5,21 (4H, m), 4,22 (1H, brs), 3,18 (1H, bs), 2,87-2,94 (1H, m), 2,56-2,65 (1H, m), 2,40-2,48 (1H, m), 1,29 (6H, d, J=6,3 Гц) і 1,22 (6H, d, J=6,3 Гц). LRMS: позитивний іон 281 (M+Na). 36 Стадія В: Діізопропіловий складний ефір 2R-[3(4-eтoкcи-фeнiл)-aлiл]-3S-гідроксибурштинової кислоти До розчину діізопропілового складного ефіру 2R-aлiл-3S-гiдpoкcи-бурштинової кислоти (4,79 г, 18,5 ммоль), 4-бромфенетолу (3,19 мл, 22,2 ммоль, 1,2 екв.) і NEt3 (6,22 мл, 44,6 ммоль, 2,4 екв.) у CH3CN (40 мл), додавали дисперговану за допомогою ультразвуку (протягом 2 хв) суспензію Р(О-Тоl)3 (0,57 г, 2,22 ммоль, 0,1 екв.) і Pd(OAc)2 (209 мг, 5%) у CH3CN (5 мл). Реакційну суміш нагрівали зі зворотним холодильником протягом 2 год. CH3CN видаляли під вакуумом. Неочищений продукт екстрагували AcOEt (3x200 мл), промивали водою (50 мл) і розсолом (50 мл). Після очищення флеш-хроматографією одержали потрібний діізопропіловий складний ефір 2R-[3-(4-eтoкcифeнiл)-aлiл]-3S-гiдpoкcи-бypштинoвoї кислоти (5,92 г, ви хід 84%). 1 Н-ЯМР; d (CDCl3), 7,28 (2Н, d, J=8,8 Гц), 6,83 (2Н, d, J=8,8 Гц), 6,46 (1Н, d, J=15,7 Гц), 6,02-6,12 (1H, m), 4,98-5,13 (2H, m), 4,26 (1H, dd, J=7,1 Гц, 3,0 Гц), 4,02 (2H, q, J=7,0 Гц), 3,23 (1Н, d, J=7,1 Гц), 2,92-2,97 (1Н, m), 2,68-2,79 (1H, m), 2,49-2,62 (1H, m), 1,41 (3H, t, J=7,0 Гц) і 1,19-1,30 (12H, m). LRMS: позитивний іон 400 (M+Na). Стадія С: Діізопропіловий складний ефір 2R[3-(4-етокси-феніл)-пропіл]-3S-гідроксибурштинової кислоти До розчину діізопропілового складного ефіру 2R-[3-(4-етокси-феніл)-аліл]-3S-гідроксибурштинової кислоти (129 мг, 0,34 ммоль) у МеОН (10 мл) в інертній атмосфері додавали 10% Pd/C (13 мг). Через одержану суспензію барботували Н 2 протягом 30 хв. Реакційну суміш потім перемішували в атмосфері Н 2 під тиском 1 атм протягом 16 год. Pd/C відфільтровували, і розчинник видаляли під зниженим тиском, одержуючи діізопропіловий складний ефір 2R-[3-(4-eтoкcи-фeнiл)-пpoпiл]-3S 37 78275 38 гiдpoкcи-бypштинoвoї кислоти (115 мг, вихід 88%). торфеніловий складний ефір 2R-(2,2-диметил-51 oкco-[1,3]діоксолан-4S-іл)-5-(4-етокси-феніл)Н-ЯМР; d (CDCl3), 7,08 (2Н, d, J=8,6 Гц), 6,81 (2Н, d, J=8,6 Гц), 4,97-5,14 (2Н, m), 4,20 (1Н, dd, пентанової кислоти (3,94 г, 65% вихід). 1 J=7,3, 3,5 Гц), 4,01 (2H, q, J=7,0 Гц), 3,18 (1H, d, Н-ЯМР; d (CDCl3), 7,09 (2Н, d, J=8,4 Гц), 6,83 J=7,3 Гц), 2,77-2,83 (1H, m), 2,55-2,62 (2H, m), 1,45(2Н, d, J=8,4 Гц), 4,56 (1Н, d, J=6,0Гц), 4,01 (2H, q, 1,94 (4H, m), 1,40 (3H, t, J=7,0 Гц) і 1,12-1,30 (12H, J=7,0 Гц), 3,20-3,28 (1H, m), 2,64 (2H, t, J=7,6 Гц), m). 1,98-2,08 (2H, m), 1,70-1,86 (2H, m), 1,62 (3H, s), LRMS: позитивний іон 402.0 (M+Na). 1,57 (3H, s) і 1,40 (3H, t, J=7,0 Гц). Стадія D: 2R-[3-(4-eтoкcи-фeнiл)-пpoпiл]-3SСтадія G. 2R-[3-(4-eтoкcи-фeнiл)-пpoпiл]-N1гiдpoкcи-бypштинoвa кислота [1S-(5-тioфeн-2-iл)-[1,2,4]оксадіазол-3-іл)-2,2До розчину діізопропілового складного ефіру диметилпропіл]-[1,3]діоксолан-4S-он 2R-[3-(4-етокси-феніл)-пропіл]-3S-гідроксиДо розчину пентафторфенілового складного бурштинової кислоти (4,78 г, 12,6 ммоль) у суміші ефіру 2R-(2,2-димeтил-5-оксо-[1,3]діоксолан-4STHF із водою (3:1, 120 мл) додавали NaOH (1,66 г, іл)-5-(4-етокси-феніл)-пентанової кислоти (150 мг, 41,5 ммоль, 5,5 екв.). Реакційну суміш потім пере0,30 ммоль) у СН 2Сl2 (10 мл) додавали 2,2мішували протягом 16 год при кімнатній темперадиметил-1S-(5-тіофен-2-іл)-[1,2,4]оксадіазол-3-іл)турі. Суміш концентрували під зниженим тиском і пропіламін (100 мг, 0,42 ммоль, 1,4 екв.). Реакційпідкислювали до рН=3 доданням 1-н. НСl. Одерну суміш перемішували протягом 16 год, і розчинжану діоксикислоту екстрагували AcOEt. Органічник видаляли під вакуумом. Неочищений продукт ний шар сушили над MgSO4, і розчинник видаляли розчиняли в AcOEt (70 мл) і промивали водою (10 під зниженим тиском, одержуючи потрібну 2R-[3мл), потім Na2CO3 (10 мл) і, нарешті, розсолом (10 (4-eтoкcи-фeнiл)-пpoпiл]-3S-гiдpoкcи-бyρштинoвy мл). Розчинник сушили над MgSO4 і видаляли під кислоту (3,66 г, вихід 85%). зниженим тиском, одержуючи потрібний 2R-[3-(41 eтoкcи-фeнiл)-пpoпiл]-N1-[1S-(5-тioфeн-2-iл)Н-ЯМР; d (CH3OD), 7,07 (2Н, d, J=8,6 Гц), 6,79 [1,2,4]oкcaдiaзoл-3-iл)-2,2-диметилпропіл](2Н, d, J=8,6 Гц), 4,23 (1Н, d, J=5,8 Гц), 3,98 (2H, q, [1,3]діоксолан-4S-он (82 мг, вихід неочищеного J=7,0 Гц), 2,76-2,81 (1H, m), 2,53-2,59 (2H, m), 1,55продукту 33%). 1,72 (4H, m), 1,35 (3H, t, J=7,0 Гц). 1 LRMS: позитивний іон 319 (M+Na); негативний Н-ЯМР; d (CDCl3), 7,88 (1Н, m), 7,62 (1H, m), іон 295 (M-H). 7,20 (1H, m), 6,95 (2H, d, J=8,4 Гц), 6,71 (2H, d, Стадія Е: 2R-(2,2-димeтил-5-oкcoJ=8,4 Гц), 6,55 (1H, d, J=9,7 Гц), 5,19 (1H, d, J=9,7 [1,3]дioкcoлaн-4S-iл)-5-(4-eтoкcи-феніл)-пентанова Гц), 4,56 (1H, d, J=6,4 Гц), 3,95 (2H, q, J=7,0 Гц), кислота 2,64 (3H, bm), 1,84 (2H, m), 1,70 (2H, m), 1,62 (3H, До розчину 2R-[3-(4-eтoкcи-фeнiл)-пpoпiл]-3Ss), 1,54 (3H, s), 1,38 (3H, t, J=6,9 Гц) і 1,02 (9H, s). гiдpoкcи-бypштинoвoї кислоти (3,66 г, 12,3 ммоль) LRMS: позитивний іон 556,0 (M+H). в ацетоні (50 мл) додавали в інертній атмосфері Стадія H. 2R-[3-(4-eтoкcи-фeнiл)-пpoпiл]-N1диметоксипропан (2,58 мл, 21 ммоль, 1,7 екв.) і [1S-(5-тioфeн-2-iл)-[1,2,4]оксадіазол-3-іл)-2,2дихлорид міді (165 мг, 1,2 ммоль, 0,1 екв.). Реакдиметилпропіл]-3S,N4-дигідрокси-сукцинамід ційну суміш перемішували при кімнатній темпераДо розчину 2R-[3-(4-eтoкcи-фeнiл)-пpoпiл]-N1турі протягом 16 год. Розчинник потім видаляли [1S-(5-тioфeн-2-iл)-[1,2,4]оксадіазол-3-іл)-2,2під вакуумом, одержуючи 2R-(2,2-диметил-5-оксодиметилпропіл]-[1,3]діоксолан-4S-ону (82 мг, 0,15 [1,3]діоксолан-4S-іл)-5-(4-етокси-феніл)-пентанову ммоль) в i-РrOН (5 мл) додавали водний розчин кислоту (4,03 г, вихід 97%). гідроксиламіну (50%, 48 мл, 0,7 ммоль, 5 екв.). 1 Реакційну суміш перемішували при кімнатній темН-ЯМР; d (CDCl3), 7,08 (2H, d, J=8,5 Гц), 6,82 пературі протягом 16 год. Розчинник видаляли під (2H, d, J=8,5 Гц), 4,48 (1H, d, J=4,8 Гц), 4,01 (2H, q, зниженим тиском і одержали масло, яке очищали J=7,0 Гц), 2,91-2,98 (1H, m), 2,54-2,64 (3H, m), 1,23препаративною хроматографією з оберненою фа2,20 (4H, m), 1,58 (3H, s), 1,53 (3H, s) і 1,40 (3H, t, J=7,0 Гц). зою, одержуючи потрібний продукт (25,3 мг, 32%). 1 LRMS: позитивний іон 359 (M+Na); негативний Н-ЯМР; d (CH3OD), 7,86 (2Н, m), 7,25 (1Н, dd, іон 335 (M-H). J=3,8 Гц), 6,83 (2H, d, J=8,6 Гц), 6,54 (2H, d, J=8,6 Стадія F. Пентафторфеніловий складний ефір Гц), 5,14 (1H, s), 4,03 (1H, d, J=7,6 Гц), 3,87 (2H, q, 2R-(2,2-диметил-5-оксо-[1,3]діоксолан-4S-іл)-5-(4J=6,96), 2,88 (1H, m), 2,45 (2H, bm), 1,53 (4H, bm), етокси-феніл)-пентанової кислоти 1,33 (3H, t, J=7,0 Гц) і 1,06 (9H, s). До холодного (0°С) розчину 2R-(2,2-димeтилLRMS: позитивний іон 553,2 (M+Na); негатив5-oкco-[1,3]дioкcoлaн-4S-іл)-5-(4-етокси-феніл)ний іон 529,2 (М-Н). пентанової кислоти (4,03 г, 12 ммоль) і пентафтоСполуки за Прикладами 4-17 одержали за мерфенолу (2,43 г, 13,2 ммоль, 1,1 екв.) у СН 2Сl2 (50 тодикою Прикладу 1 шляхом паралельного синтемл) додавали WSC (2,54 г, 13,2 ммоль, 1,1 екв.). зу, застосовуючи на Стадії D відповідні хлорангідРеакційну суміш ви тримували для нагрівання до риди кислот. Продукти очищали препаративною кімнатної температури протягом ночі. СН2Сl2 виHPLC: даляли під вакуумом, і одержану неочищену реакПриклад 4 ційну суміш розчиняли в AcOEt (200 мл). Органіч2S-гiдpoкcи-3R-[1S-(5-iзoпpoпiлний шар промивали водою (50 мл), насиченим [1,2,4]oкcaдiaзoл-3-iл)-2,2розчином NaHCO3 (20 мл) і, нарешті, розсолом (20 диметилпропілкарбамоїл]-5мл). Розчинник видаляли під зниженим тиском, і метилгексангідроксамова кислота одержали масло, яке очищали флешхроматографією, одержуючи очікуваний пентаф 39 LRMS; позитивний іон 407 (M+Na); негативний іон 383 (М-Н) Приклад 5 2S-гiдpoкcи-3R-[1S-(5-фypaн-2-iл[1,2,4]oкcaдiaзoл-3-iл)-2,2диметилпропілкарбамоїл]-5метилгексангідроксамова кислота LRMS; позитивний іон 431 (M+Na), негативний іон 407 (М-Н). Приклад 6 2S-гiдpoкcи-3R-[1S-(5-циклoпeнтилмeтил[1,2,4]oкcaдiaзoл-3-iл)-2,2диметилпропілкарбамоїл]-5метилгексангідроксамова кислота LRMS; позитивний іон 425 (М+Н), негативний іон 423 (М-Н). Приклад 7 2S-гiдpoкcи-3R-[1S-(5-тioфeн-2-iлмeтил[1,2,4]oкcaдiaзoл-3-iл)-2,2диметилпропілкарбамоїл] -5метилгексангідроксамова кислота LRMS; позитивний іон 461 (M+Na), негативний іон 437 (М-Н). Приклад 8 2S-гiдpoкcи-3R-[1S-(5-eтил-[1,2,4]oкcaдiaзoл-3iл)-2,2-диметилпропілкарбамоїл] -5метилгексангідроксамова кислота 78275 40 LRMS; позитивний іон 393 (M+Na), негативний іон 369 (М-Н). Приклад 9 2S-гiдpoкcи-3R-[1S-(5-циклoпeнтил[1,2,4]oкcaдiaзoл-3-iл)-2,2диметилпропілкарбамоїл]-5метилгексангідроксамова кислота LRMS; позитивний іон 411 (М+Н), негативний іон 409 (М-Н). Приклад 10 2S-гiдpoкcи-3R-[1S-(5-бeнзил[1,2,4]oкcaдiaзoл-3-iл)-2,2диметилпропілкарбамоїл]-5метилгексангідроксамова кислота LRMS; позитивний іон 433 (М+Н), негативний іон 431 (М-Н). Приклад 11 2S-гiдpoкcи-3R-[1S-(5-iзoбyтил[1,2,4]oкcaдiaзoл-3-iл)-2,2диметилпропілкарбамоїл]-5метилгексангідроксамова кислота 41 78275 LRMS; позитивний іон 421 (M+Na), негативний іон 397 (М-Н). Приклад 12 2S-гiдpoкcи-3R-[1S-(5-трет-бyтил[1,2,4]oкcaдiaзoл-3-iл)-2,2диметилпропілкарбамоїл]-5метилгексангідроксамова кислота LRMS; позитивний іон 421 (M+Na), негативний іон 397 (М-Н). Приклад 13 2S-riдpoкcи-3R-[1S-(5-тioфeн-2-iл[1,2,4]oкcaдiaзoл-3-iл)-2,2диметилпропілкарбамоїл]-5метилгексангідроксамова кислота LRMS; позитивний іон 425 (М+Н), негативний іон 423 (М-Н). Одержали також діастереомер, 2R-гiдpoкcи3R-[1S-(5-тioфeн-2-iл-[1,2,4]оксадіазол-3-іл)-2,2диметилпропілкарбамоїл]-5метилгексангідроксамову кислоту. M+H=425,1, M+Na=447,1, M-H=423,0. 42 LRMS; позитивний іон 435 (M+Na), негативний іон 411 (М-Н). Приклад 15 2S-гiдpoкcи-3R-[1S-(5-n-тoлiл[1,2,4]oкcaдiaзoл-3-iл)-2,2диметилпропілкарбамоїл]-5метилгексангідроксамова кислота LRMS; позитивний іон 433 (М+Н), негативний іон 431 (М-Н). Приклад 16 2S-гiдpoкcи-3R-[1S-(5-циклoпpoпiл[1,2,4]oкcaдiaзoл-3-iл)-2,2диметилпропілкарбамоїл]-5метилгексангідроксамова кислота LRMS; позитивний іон 405 (M+Na), негативний іон 381 (М-Н). Приклад 17 2S-гiдpoкcи-3R-[1S-(5-мeтил-[1,2,4]oкcaдiaзoл3-iл)-2,2-диметилпропілкарбамоїл]-5метилгексангідроксамова кислота Приклад 14 2S-гiдpoкcи-3R-[1S-(5-(2,2-димeтилпpoпiл)[1,2,4]oкcaдiaзoл-3-iл)-2,2диметилпропілкарбамоїл]-5метилгексангідроксамова кислота 43 78275 44 (1H, m), 2,36 (1H, m), 1,63 (1H, m), 1,54 (1H, m), 1,16 (1H,m), 1,09 (3H, d, J=6,8 Гц), 1,00 (3Н, d, J=6,8 Гц), 0,95 (3Н, d, J=6,3 Гц), 0,84 (3Н, d, J=6,3 Гц). 13 С-ЯМР; d (CH3OD), 181,0, 176,8, 172,0, 169,9, 132,9, 130,5, 128,7, 128,4, 73,7, 54,3, 49,6, 39,5, 33,3, 27,2, 24,4, 22,5, 19,8 і 19,4. LRMS; позитивний іон 427 (M+Na), негативний іон 403 (М-Н). Сполуки за Прикладами 20-23 одержали за методикою Прикладу 2, застосовуючи відповідний нітрил на Стадії С та/або відповідний амінокислот1 ний залишок на Стадії А. Синтез відповідного хіН-ЯМР; d (CH3OD), 8,26 (1Н, d, J=9,4 Гц), 5,02 рального сукцинату на Стадії Е детально описано (1H, d, J=9,5 Гц), 4,02 (1H, d, J=6,4 Гц), 2,89 (1H, у WO 94/21625. m), 2,57 (3H, s), 1,61 (1H, m), 1,44 (1H, m), 1,22 (1H, Приклад_20 m), 1,00 (9H, s). 13 2S-алiл-5-мeтил-3R-[2-фeнiл-1S-(3-фeнiлС-ЯМР; d (CH3OD), 178,6, 176,1, 171,9, 170,7, [1,2,4]oкcaдiaзoл-5-iл)-етилкарбамоїл]73,5, 55,6, 49,5, 39,9, 36,2, 27,6, 26,6, 24,2, 22,7 і гексангідроксамова кислота 12,4. LRMS; позитивний іон 379 (M+Na), негативний іон 355 (М-Н). Сполуки за Прикладами 18-19 одержали за методикою Прикладу 2, застосовуючи відповідний нітрил на Стадії С та/або відповідний амінокислотний залишок на Стадії А: Приклад18 2S-гiдpoкcи-3R-[1S-(3-iзoпpoпiл[1,2,4]oкcaдiaзoл-3-iл)-2,2диметилпропілкарбамоїл]-5метилгексангідроксамова кислота 1 Н-ЯМР; d (CH3OD), 5,12 (1Н, s), 3,98 (1H, d, J=7,5 Гц), 3,06 (1H, m), 2,92 (1H, m), 1,61 (1H, m), 1,43 (1H, m), 1,31 (6H, d, J=6,9 Гц), 1,14 (1H, m), 1,03 (9H, s), 0,89 (3H, d, J=6,7 Гц), 0,81 (3Н, d, J=6,8 Гц). 13 С-ЯМР; d (CH3OD), 179,7, 176,6, 176,5, 172,0, 73,7, 56,9, 49,2, 39,5, 36,5, 28,3, 27,3, 24,5, 22,3, 21,2 і 21,1. LRMS; позитивний іон 385 (М+Н), негативний іон 383 (М-Н). Приклад 19 2S,N1-дигідрокси-3R-ізобутил-N4-[2-метил-1S(3-феніл-[1,2,4]оксадіазол-5-іл)-пропіл]-сукцинамід 1 Н-ЯМР; d (CH3OD), 8,05 (2Н, m), 7,52 (3Н, m), 5,14 (1Н, d, J=7,2 Гц), 4,00 (1H, d, J=7,7 Гц), 2,91 1 Н-ЯМР; d (CH3OD), 9,13 (1Н, d, J=8,26 Гц), 8,05 (2H, m), 7,55 (3H, m), 7,25 (5H, m), 5,66 (1H, m), 5,45 (1H, m), 4,90 (2H, m), 4,50 (1H, s) 3,51 (1H, dd, J=13,92, 4,84 Гц), 3,17 (1H, dd, J=13,92, 10,90 Гц), 2,50 (1H, m), 2,0 (2H, m), 1,50 (3H, m), 1,0 (3H, d, J=6,5 Гц), 0,96 (3H, d, J=6,6 Гц). 13 С-ЯМР; d (CH3OD), 181,0, 177,0, 172,7, 138,0, 136,5, 133,0, 130,8, 130,6, 130,5, 130,1, 128,7, 128,7, 117,7, 48,4, 48,3, 42,1, 39,5, 36,2, 27,1, 24,9 і 22,0. Приклад 21 2S-алiл-5-мeтил-3R-[2-фeнiл-1S-(3-iзoпpoпiл[1,2,4]oкcaдiaзoл-5-iл)-етилкарбамоїл]гексангідроксамова кислота 1 Н-ЯМР; d (D MSO), 10,28 (1Н, s), 8,64 (1Н, d, J=6,2 Гц), 8,64 (1Н, br s), 7,25 (5H, m), 5,45 (2H, m), 4,51 (1H, m), 4,30 (2H, m), 3,15 (1H, m), 2,85 (2H, m), 2,20 (1H, dt, J=10,6, 3,12 Гц), 1,70 (2H, m), 1,25 (6H, d, J=6,91 Гц), 0,70 (1H, m), 0,52 (3H, d, J=6,4 Гц), 0,48(3Н, d, J=6,4 Гц). 13 С-ЯМР; d (MEOD), 179,0, 175,6, 175,5, 171,3, 136,6, 135,0, 129,2, 128,6, 127,3, 116,4, 48,7, 46,9, 40,6, 38,1, 34,8, 26,9, 25,6, 23,5, 20,7 і 19,9. Приклад 22 45 2S-aлiл-5-мeтил-3R-[2-фeнiл-1S-(3-мeтил[1,2,4]oкcaдiaзoл-5-iл)-етилкарбамоїл]гексангідроксамова кислота 78275 46 ного сукцинату на Стадії Е детально описано в WO 97/02239. Приклад 25 2S-мeтoкcи-5-мeтил-3R-[1S-(3-мeтил[1,2,4]oкcaдiaзoл-5-iл)-2-фeнiл-етилкарбамоїл] гексангідроксамова кислота 1 Н-ЯМР; d (CH3OD), 8,98 (1Н, d, J=8,41 Гц), 7,27 (5H, m), 5,51 (2H, m), 4,85 (2H, m), 3,41 (1H, dd, J=14,0, 5,0 Гц), 3,14 (1H, dd, J=14,0, 10,97 Гц), 2,47 (1H, dt, J=11,0, 3,25 Гц), 2,16 (3H, s), 2,00 (1H, dt, J=11,40, 3,30 Гц), 1,80 (1H, m), 1,15 (1H, m), 0,98 (3H, d, J=6,6 Гц), 0,92 (3H, d, J=6,6 Гц). 13 С-ЯМР; d (CH3OD), 172,62, 168,27, 133,59, 132,07, 126,34, 125,66, 124,28, 113,36, 45,19, 44,04, 43,95, 37,61, 35,15, 31,75, 22,72, 20,44, 17,59 і 7,36. Приклад 23 2S-алiл-3R-[2,2-димeтил-1S-(3-мeтил[1,2,4]oкcaдiaзoл-5-iл)-пропілкарбамоїл]-5-метилгексангідроксамова кислота 1 Н-ЯМР; d (CH3OD), 8,81 (1Н, d, J=8,59 Гц), 7,65 (1H, m), 5,70 (1H, m), 5,15 (1H, d, J=8,62 Гц), 4,95 (2H, m), 2,60 (1H, dt, J=11,10, 3,16 Гц), 2,39 (3H, s), 1,38 (1H, dt, J=13,10, 3,33 Гц), 1,31 (1H, m), 0,98 (1H, m), 0,98 (9H,s), 0,86(3H, d, J=6,6 Гц), 0,84(3Н, d, J=6,6 Гц). Сполуку за Прикладом 24 одержали за методикою Прикладу 2. Синтез відповідного хірального сукцинату на Стадії Е детально описано в WO 95/19956. Приклад 24 3R-[2,2-димeтил-1S-(3-фeнiл-[1,2,4]oкcaдiaзoл5-iл)-пpoпiлкapбaмoїл]-5-метил-гексангідроксамова кислота LRMS; позитивний іон 403,5 (М+Н), негативний іон 401,3 (М-Н). Сполуку за Прикладом 25 одержали за методикою Прикладу 2, застосовуючи відповідний нітрил на Стадії С та/або відповідний амінокислотний залишок на Стадії А. Синтез відповідного хіраль 1Н-ЯМР; d (CH3OD), 7,14 (5Н, m), 5,34 (1Н, m), 3,38 (1H, d, J=9,68 Гц), 3,20 (2H, m), 3,02 (3H, s), 2,65 (1H, m), 2,22 (3H, s), 1,35 (2H, m), 0,90 (1H, m), 0,73 (3H, d, J=6,55 Гц), і 0,70 (3H, d, J=6,57 Гц). Сполуки за Прикладами 26 і 27 одержали за методикою Прикладу 2. Синтез відповідного хірального сукцинату на Стадії Е детально описано в WO 92/13831 із застосуванням методик, аналогічних розкритим в WO 95/32944. Приклад 26 3R-[2,2-димeтил-1S-(3-фeнiл-[1,2,4]oкcaдiaзoл5-iл)-пpoпiлкapбaмoїл]-гептадеканова кислота 1 Н-ЯМР; d (CH3OD), 8,05 (2Н, m), 7,49 (3Н, m), 5,22 (1Н, s), 2,93 (1H, m), 2,65 (1H, dd, J=9,8,16,7 Гц), 2,38 (1H, dd, J=4,6,16,6 Гц), 1,52 (1H, m), 1,43 (1H, m), 1,26 (24H, m), 1,10 (9H, s) і 0,89 (3Н, m). LRMS; позитивний іон 528,4 (M+H). Приклад 27 3R-[2,2-димeтил-1S-(3-фeнiл-[1,2,4]oкcaдiaзoл5-iл)-пpoпiлкapбaмoїл]-нонадеканова кислота LRMS; позитивний іон 556.2 (М+Н). Сполуку за Прикладом 28 одержали за методикою Прикладу 1. Синтез відповідного хірального сукцинату на Стадії 3 детально описано в WO 92/13831 із застосуванням методик, аналогічних розкритим в WO 95/32944. Приклад 28 6-(4-xлopфeнiл)-3R-[2,2-димeтил-1S-(5-фeнiл[1,2,4]oкcaдiaзoл-3-iл)-пропілкарбамоїл]-гексанова кислота 47 78275 1 Н-ЯМР; d (CH3OD), 8,07 (2H, m), 7,61 (3H, m), 6,93 (4H, m), 5,15 (1Н, s), 2,94 (1H, m), 2,5 (4H, m), 1,5 (4H, m) і 1,07 (9H, s). 13 С-ЯМР; d (CH3OD), 178,0, 177,1, 142,6, 134,6, 132,7, 131,0, 130,8, 129,5, 129,4, 125,7, 55,7, 43,8, 39,0, 36,3, 36,1, 34,1, 30,3 і 27,4. LRMS; позитивний іон 506,2 (M+Na), негативний іон 482,4 (М-Н). Одержали також діастереомерну 6-(4-xлopфeнiл)-3R-[2,2-димeтил-1R-(5-феніл[1,2,4]оксадіазол-3-іл)-пропілкарбамоїл]-гексанову кислоту М+Н=485, M+Na=507,2, M-H=482,6. Сполуки за Прикладами 29 і 30 одержали за методикою Прикладу 1. Приклад 29 3R-[2,2-димeтил-1S-(5-тioфeн-2-iл[1,2,4]oкcaдiaзoл-3-iл)-пропілкарбамоїл]-2Sгідрокси-5-метил-гексанова кислота 1 Н-ЯМР; d (CH3OD), 7,95 (1Н, m), 7,87 (1Н, d, J=5,0 Гц), 7,28 (1H, m), 5,15 (1H, s), 4,18 (2H, d, J=6,4 Гц), 2,94 (1H, m), 1,68 (1H, m), 1,48 (1H, m), 1,31 (1H, m), 1,06 (9H, s), 0,88 (3H, d, J=6,4 Гц) і 0,82 (3H, d, J=6,5 Гц). LRMS; негативний іон 408,2 (М-Н). Приклад 30 3R-[1S-(5-фypaн-2-iл-[1,2,4]oкcaдiaзoл-3-iл)2,2-димeтилпpoпiлкapбaмoїл]-2S-гідрокси-5-метилгексанова кислота 1 Н-ЯМР; d (CH3OD), 7,88 (1H, s), 7,45 (1H, d, J=3,6 Гц), 6,74 (1H, m), 5,15 (1H, s), 4,18 (2H, d, J=6,4 Гц), 2,91 (1H, m), 1,65 (1H, m), 1,50 (1H, m), 1,31 (1H, m), 1,06 (9H, s), 0,88 (3H, d, J=6,4 Гц) і 0,82 (3H, d, J=6,5 Гц). LRMS; негативний іон 392.2 (M-H). 48 Сполуки за Прикладами 31 і 32 одержали за методикою Прикладу 2. Синтез відповідного хірального сукцинату на Стадії Е детально описано в WO 94/02446 із застосуванням відповідно циннамілброміду або циклопентилметилйодиду замість металілйодиду, як описано у ви щезгаданому документі. Приклад 31 N4-[2,2-диметил-1S-(3-феніл-[1,2,4]оксадіазол5-іл)-пропіл]-2S,N1-дигiдpoкcи-3R-(3-фeнiл-aлiл)cyкцинaмiд 1 Н-ЯМР; d (CH3OD), 7,95 (2Н, d, J=7,2 Гц), 7,53 (1Н, m), 7,48 (2H, m), 7,09 (2H, d, J=6,4 Гц), 6,91 (3H, m), 6,31 (1Н, d, J=15,8 Гц), 6,04 (1Н, m), 5,26 (1H, s), 4,14 (1H, d, J=7,6 Гц), 3,02 (1H, m), 2,46 (1H, m), 2,37 (1H, m) і 1,07 (9H, s). 13 С-ЯМР; d (CH3OD), 179,8, 175,9, 172,0, 169,6, 138,8, 134,0, 132,8, 130,4, 129,7, 128,9, 128,4, 128,4, 127,3, 73,2, 56,5, 51,3, 36,8 і 34,0. LRMS; позитивний іон 501,2 (M+Na), негативний іон 477,4 (M-H). Приклад 32 2R-циклoпeнтилмeтил-3S,N4-дигiдpoкcи-N1[1S-(3-iзoпpoпiл-[1,2,4]оксадіазол-5-іл)-2,2диметилпропіл]-сукцинамід 1 Н-ЯМР; d (CH3OD), 5,13 (1З, s), 3,99 (1H, d, J=7,7 Гц), 3,06 (1H, m), 2,87 (1H, m), 1,83 (1H, m), 1,72 (1H, m), 1,63-1,39 (6H, bm), 1,31 (6H, d, J=6,9 Гц), 1,27 (1H, m), 1,03 (9H, s) і 1,02 (2H, m). 13 С-ЯМР; d (CH3OD), 179,6, 176,6, 176,5, 172,0, 73,6, 56,8, 50,8, 39,6, 36,7, 36,5, 34,7, 33,6, 28,3, 27,2, 26,5 і 21,2. LRMS; позитивний іон 411,2 (M+H), негативний іон 409,6 (М-Н). Сполуки за Прикладами 33-35 одержали за методикою Прикладу 3 застосовуючи відповідний арилбромід на Стадії В. Приклад 33 2R-[3-(3,5-бic-тpифтopмeтилфeнiл)-пpoпiл]-N1[2,2-димeтил-1S-(5-тioфeн-2-іл-[1,2,4]оксадіазол-3іл)-пропіл]-3S,N4-дигідрокси-сукцинамід 49 78275 50 1 Н-ЯМР; d (CH3OD), 8,38 (1Н, d, J=9,4 Гц), 7,86 (1H, s), 7,75 (3H, bs), 7,4 (1H, d, J=3,5 Гц), 6,7 (1H, m), 5,12 (1H, d, J=9,4 Гц), 4,26 (1H, d, J=4,0 Гц), 2,8 (3H, bm), 1,8 (4H, bm) і 1,0 (9H, s). LRMS; позитивний іон 623.2 (M+H), негативний іон 621,0 (М-Н). Приклад 34 2R-[3-(3,5-бic-тpифтopмeтил-фeнiл)-пpoпiл]N1-[1S-(5-фypaн-2-iл-[1,2,4]оксадіазол-3-іл)-2,2диметилпропіл] -3S,N4-дигідрокси-сукцинамід 1 Н-ЯМР; d (CH3OD), 8,38 (1Н, d, J=9,4 Гц), 7,86 (1Н, s), 7,75 (3H, bs), 7,4 (1H, d, J=3,5 Гц), 6,7 (1H, m), 5,12 (1H, d, J=9,4 Гц), 4,26 (1H, d, J=4,0 Гц), 2,8 (3H, bm), 1,8 (4H, bm) і 1,0 (9H, s). LRMS; позитивний іон 629,4 (M+Na), негативний іон 605,4 (М-Н). Приклад 35 2R-[3-(4-eтoкcифeнiл)-пpoпiл]-N1-[1S-(5-фypaн2-iл-[1,2,4]oкcaдiaзoл-3-іл)-2,2-диметилпропіл]3S,N4-дигідрокси-сукцинамід 1 Н-ЯМР; d (CH3OD), 7,86 (2Н, m), 7,25 (1Н, dd, J=3,8 Гц), 6,83 (2H, d, J=8,6 Гц), 6,54 (2H, d, J=8,6 Гц), 5,14 (1H, s), 4,03 (1H, d, J=7,6 Гц), 3,87 (2H, q, J=6,96,14,0 Гц), 2,88 (1H, m), 2,45 (2H, bm), 1,53 (4H, bm), 1,33 (3H, t, J=7,0 Гц) і 1,06 (9H, s). LRMS; позитивний іон 515.2 (M+H), негативний іон 513,2 (М-Н). Сполуку за Прикладом 36 одержали за методикою Прикладу 2. Синтез відповідного хірального сукцинату на Стадії Е детально описано в WO 01/10834. Приклад 36 3-циклопентил-N-[2,2-диметил-1S-(3-феніл[1,2,4]оксадіазол-5-іл)-пропіл]-2R[(формілгідроксіаміно)-метил]-пропіонамід 1 Н-ЯМР; d (CH3OD), 8,26 (03 Н, s), 8,05 (2H, d, J=6,9 Гц), 7,84 (0,7H, s), 7,52 (3H, m), 5,20 (1H, m), 3,75 (1H, m), 3,63 (0,3H, dd, J=13,9, 5,5 Гц), 3,43 (0,7H, dd, J=14,2, 4,6 Гц), 3,18 (0,7H, m), 3,00 (0,3H, m), 1,92 (1H, m), 1,47 (8H, m), 1,10 (3H, s), 1,08 (6H, s) і 0,98 (2H, m). 13 С-ЯМР; d (CH3OD), 179,9, 176,9, 176,6, 169,3, 163,8, 159,2, 132,5, 130,0, 129,6, 128,9, 128,3, 127,9, 56,8, 56,7, 53,9, 50,3, 44,8, 44,6, 39,1, 38,9, 37,9, 37,7, 35,9, 35,8, 34,1, 33,4, 33,3, 26,9, 26,1 і 25,9. LRMS; позитивний іон 451 (M+Na), негативний іон 427 (М-Н). Сполуку за Прикладом 37 одержали за методикою Прикладу 1. Синтез відповідного хірального сукцинату на Стадії Е детально описано в WO 01/10834. Приклад 37 3-циклoпeнтил-N-[2,2-димeтил-1S-(5-фeнiл[1,2,4]oкcaдiaзoл-3-iл)-пропіл]-2R-[(формілгідрокси-аміно)-метил] -пропіонамід 1 Н-ЯМР; d (CH3OD), 8,49 (0,6Н, d, J=8,7 Гц), 8,37 (0,4Н, d, J=8,l Гц), 8,28 (0,4H, s), 8,14 (2H, m), 7,85 (0,6H, s), 7,65 (1H, m), 7,59 (2H, m), 4,81 (1H, s), 3,79 (1H, m), 3,63 (0,4H, m), 3,43 (0,6H, m), 3,13 (0,6H, m), 2,97 (0,4H, m), 1,55 (9H, m), 1,08 (3H, s), 1,07 (6H, s) і 1,04 (2H, m). 13 С-ЯМР; d (CH3OD), 176,6, 171,6, 164,2, 159,7, 134,6, 132,8, 130,8, 130,3, 129,4, 125,7, 69,5, 56,0, 54,3, 50,8, 45,4, 45,3, 40,6, 39,5, 38,3, 38,2, 35,9, 34,5, 33,8, 33,7, 32,0, 27,5, 26,4 і 26,3. LRMS; позитивний іон 429 (M+H). Результати біологічних випробувань А. Випробування інгібування ферментів Сполуки за цим винаходом випробовували з метою визначення їхньої активності як інгібіторів ММР9 та ММР12. Методика випробування інгібування ММР9 Сполуки випробовували на інгібувальну активність відносно желатинази з молекулярною масою 92 кДа (ММР9) у пробах із застосуванням пептидного субстрату, міченого кумарином (7метоксикумарин-4-іл)ацетил-Pro-Leu-Gly-Leu-(3[2,4-динiтpoфeнiл]-L-2,3-дiaмiнoпpoпioнiл)-Ala-ArgNH2 (McaPLGLDpaAR) [Knight et al., FEBS Lett. 1992; 263-266]. Вихідні розчини готували, як описано нижче: 51 78275 52 Випробувальний буфер: 100мм Трис-НСІ рН паралельних проб для кожної з 10 концентрацій 7,6, що містить 100мм NaCl, 10мм СаСl2 і 0,05% інгібітора. Значення ІС50 (концентрація сполуки, Brij 35; потрібна для забезпечення зниження активності Субстрат: ви хідний розчин 0,4мм ферменту на 50%) одержували шляхом наблиMcaPLGLDpaAR (від фірми Bachem) (0,437 мг/ мл) ження даних до рівняння Y=a+((b-a)/(l+(c/X)d)) (де у 100% DMSO (зберігання при -20°С). Розведення Х - інгібування, досягнуте при певній дозі; X - згадо 8 мкМ у випробувальному буфері. дана доза в наномолях; а - мінімальний відрізок на Фермент: Рекомбінантна желатиназа 92 кДа осі у або 0% інгібування; b - максимальний відрізок людини (ММР-9; в разі необхідності активована на осі у або 100% інгібування; с - значення ІС50; d АРМА (ацетатом 4-амінофенілртуті)), відповідним нахил кривої). Результат округлювали до однієї чином розведена у випробувальному буфері. значущої ци фри. Випробовувані сполуки готували спочатку у Методика випробування інгібування ММР12 вигляді вихідних 10мм розчинів сполук у 100% Сполуки випробовували на інгібувальну активDMSO, розводили до 1мм 100% DMSO, а потім ність відносно металоеластази (ММР12) у пробах послідовно тричі розводили 100% DMSO у колоніз застосуванням пептидного субстрату, міченого ках 1-10 96-лункового мікротитрувального планкумарином (7-мeтoкcикyмaρин-4-iл)aцeтил-Proшета. Діапазон випробовуваних концентрацій від Leu-Gly-Leu-(3-[2,4-динiтpoфeнiл]-L-2,3100 мкМ (колонка 1) до 5,1 нМ (колонка 10). дiaмiнoпpoпioнiл)-Ala-Arg-NH 2 (McaPLGLDpaAR) Випробування виконували у загальному об'ємі [Knight et al., FEBS Lett. 1992; 263-266]. Випробу100 мкл на одну лунку 96-лункового мікротитрувавання виконували, як описано вище для випробульного планшета. У лунку вносили активований вання інгібування ММР9. фермент (20 мкл), а потім 20 мкл випробувального Методика випробування інгібування ММР1 буфера. Потім додавали випробовувані сполуки у Сполуки випробовували на інгібувальну активвідповідних концентраціях, розчинені в 10 мкл ність відносно колагенази (ММР1) у пробах із заDMSO, а потім 50 мкл McaPLGLDpaAR (8 мкМ, стосуванням пептидного субстрату, міченого куприготований розведенням вихідного розчину вимарином (7-мeтoкcикyмapин-4-iл)aцeтил-Pгo-Leuпробувальним буфером). У кожному експерименті Gly-Leu-(3-[2,4-динiтpoфeнiл]-L-2,3застосовували 10 концентрацій випробовуваної діамінопропіоніл)-Ala-Arg-NH 2 (McaPLGLDpaAR) сполуки, виконуючи по 2 паралельні проби для (Knight et al., FEBS Lett. 1992; 263-266]. Випробукожної. У контрольні лунки не вносили або фервання виконували, як описано вище для випробумент, або випробовувану сполуку. Реакційні суміші вання інгібування ММР9. інкубували при 37°С протягом 2 год. Потім, не Результати: припиняючи реакцію, одразу ж вимірювали флуоРозшифровка позначень біологічних характересценцію на довжині хвилі 405 нм за допомогою ристик флуориметра SLT Fluostar [виробник SLT Діапазон А 10000 нМ кривої доза-реакція, побудованої за даними двох Сполука за Прикладом 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 ММР9 ІС50 (н М) В В А В В С С В С С С В В С В В С В В А А Не випробувана ММР12 ІС50 (н М) А А А А А А В А А А А А А А А А А А А А А Не випробувана ММР1 ІС50 (н М) В В D В В В С В В С С В В С В В В В В В В А 53 Сполука за Прикладом 23 24 25 26 27 28 29 30 31 32 33 34 35 78275 ММР9 ІС50 (нМ) А С В D D Не випробувана С D D А D D А Ці результати свідчать, що випробовані сполуки, як правило, є інгібіторами ММР12, а деякі з них виявляють селективну інгібувальну активність відносно як ММР9, так і ММР12 у порівнянні до ММР1. В. Модель фіброзу печінки, індукованого ССl4 Чотирихлористий вуглець (ССl4) при внутрішньоочеревинному введенні викликає фіброз печінки [Bulbena О., Culat J., Bra vo M.L., Inflammation 1997 Oct; 21(5):475-88]. Сполуки за цим винаходом можна оцінити за їхньою здатністю до запобігання утворенню фіброзної тканини, індукованому ССl4. Піддослідні тварини Самці пацюків лінії Sprague-Dawley, вік 7 тижнів, маса тіла приблизно 300 г (одержані від фірми Charles River/Iffa-Credo, St-Germain/l'Arbresle, Франція). Перед початком дослідження пацюків витримували для акліматизації протягом 5 днів у приміщенні з кондиціонованим повітрям, по 2 тварини у клітці. Температура: 22±2°С. Відносна вологість: 55±10%. Світловий режим: 12-годинний цикл (7.0019.00). Тип кліток: клітки Makrolon® 42,5x26,6x15, обладнані годівницями з кришками з нержавіючої сталі. Для дослідження застосовували перелічені нижче групи по 8 тварин у кожній. Група 1: Негативний контроль: тварини одержували носій ССl4 (внутрішньоочеревинно) та один раз на день носій випробовуваної сполуки (підшкірно) Група 2: Позитивний контроль: тварини одержували ССl4 (внутрішньоочеревинно) та один раз на день носій випробовуваної сполуки (підшкірно). Група 3: Експериментальна група: тварини одержували ССl4 (внутрішньоочеревинно) та один раз на день 2 мг/кг сполуки за Прикладом 13 (підшкірно). Група 4: Експериментальна група: тварини одержували ССl4 (внутрішньоочеревинно) та один раз на день 10 мг/кг сполуки за Прикладом 13 (підшкірно). Група 5: Експериментальна група: тварини одержували ССl4 (внутрішньоочеревинно) та один раз на день 20 мг/кг сполуки за Прикладом 13 (підшкірно). Пацюків позначали ярликами, прикріпленими до хвостів. Ярлики перевіряли та в разі потреби замінювали після кожної ін'єкції ССl4. 54 ММР12 ІС50 (нМ) А А А D D D В С В А В D А ММР1 ІС50 (нМ) В С В Не випробувана Не випробувана Не випробувана С D D А D D D Процедура експериментів ССl4 (Prolabo) в оливковій олії вводили піддослідним тваринам через кожні 3 дні протягом 3 тижнів шляхом внутрішньоочеревинної ін'єкції (0,25 мл ССl4/кг маси тіла, розведеного в олії в об'ємному співвідношенні 1:1 до загального об'єму 0,5 мл/кг). Тварин зважували щоденно. Якщо маса тіла зменшувалася більше ніж на 10% від початкової, тварину виключали з дослідження. Носії та сполуку застосовували, як вказано нижче: - ССl4 вводили в оливковій олії (prolabo) у розведенні 1:1; - Сполуку за Прикладом 13 суспендували в розчині 0,25% Твін-80 і 0,25% карбоксиметилцелюлози в стерильному 0,9% NaCl. Одержаний розчин на протязі експерименту зберігали при 4°С і щоденно використовували для приготування суспензії. Сполуку за Прикладом 13 вводили щоденно шляхом підшкірної ін'єкції в об'ємі 5 мл/кг. Тваринам групи 1 і групи 2 підшкірно вводили 5 мл/кг носія. Кожного дня експерименту використовували свіжоприготовані розчини. Ін'єкції виконували щодня в один і той самий час. Оброблення кожної тварини груп, залучених до експерименту, починали в момент першого введення ССl4 і продовжували протягом 21 послідовних днів. Останнє введення випробовуваних речовин або носіїв виконували за 1 день до умертвіння тварин. Результати Зареєстровано смерть 16 тварин. Дата та гадана причина смерті вказані в Таблиці. Рівні ферменту в сироватці крові Тварин умертвляли через 21 день після першого введення ССl4 шляхом інгаляції ізофурану. Індивідуальні проби крові відбирали в момент умертвіння, тобто через один день після останнього введення випробовуваної речовини або носія. Кров центрифугували при 4°С. Обережно збирали плазму, і відбирали три аліквотні частки. Для оцінки ступеня некрозу печінки вимірювали вміст аспартатамінотрансферази (ASAT) та аланінамінотрансферази (ALAT) у плазмі. Підвищені рівні ASAT і ALAT у сироватці пов'язані з пошкодженням печінки. Середні рівні ASAT і AL AT для контрольних тварин та тварин, оброблених сполукою за Прикладом 13 у трьох різних дозах, показано на Фіг.1 55 78275 56 (по осі Х відкладено активність ферменту в одиникров'яні тільця у очеревині шляхом трьохразового цях на літр крові, IU/L). Підшкірне введення сполупослідовного промивання очеревинної порожнини ки за Прикладом 13 явно спричиняє зниження рів5 мл сольового розчину з фосфатним буфером нів ASAT і ALAT у порівнянні з тваринами, які (PBS) та 1мм EDTA (+4°С). Одержану суспензію одержували носій. Цей факт свідчить, що сполука центрифугували (1700g x 10 хв при +4°С). Одерза Прикладом 13 виявляє ефект захисту печінки. жаний осад суспендували в 1 мл розчину PBS Гістологічна оцінка фіброзу печінки 1мM EDTA. Фіброз печінки оцінювали шляхом вимірюванЛімфоцити ідентифікували і рахували, застоня величини ураженої фіброзом ділянки в печінці совуючи лічильник Beckman/Coulter. із застосуванням мікротомії. Результати виражали Схема експерименту як частку ураженої фіброзом ділянки в процентах. Тварин розділяли на 5 груп (по 6 мишей у кожПечінку видаляли, три частки печінки розсіканій групі): ли, і відбирали проби, які або фіксували в 10% Група 1: (негативний контроль) одержувала формальдегіді, або заморожували при -80°С. розчин 0,5% СМС/0,25% Твін-20 (носій сполуки за Проби заливали у парафінові блоки.Виконувинаходом) і сольовий розчин (носій IL2); вали зрізання і забарвлення Сіріусом червоним. Група 2: (контроль IL2) одержувала розчин Кількісне визначення фіброзу в печінці виконували 0,5% СМС/0,25% Твін-20 та ін'єкцію IL2; щонайменше на трьох зрізах, взятих із різних діляГрупа 3: експериментальна група (сполука за нок печінки. Кількісний аналіз виконували із застовинаходом, доза 1) одержувала сполуку за цим суванням аналізатора зображення (Imstar) та провинаходом та ін'єкцію IL2; грами Morphostar. Група 4: експериментальна група (сполука за Розраховували середні значення величини винаходом, доза 2) одержувала сполуку за цим ураженої фіброзом ділянки у печінках тварин різвинаходом та ін'єкцію IL2; них гр уп. Одержані результати показано на Фіг.2. Група 5: експериментальна група (сполука за В. Надходження лімфоцитів у очеревину, індувинаходом, доза 3) одержувала сполуку за цим коване IL2 винаходом та ін'єкцію IL2; Внутрішньоочеревинне введення інтерлейкінуГрупа 6: група порівняння одержувала сполуку 2 (IL2) спричиняє міграцію лімфоцитів у очеревинпорівняння (дексаметазон) та ін'єкцію IL2. ну порожнину. Це явище є моделлю міграції кліРозрахунки тин, яка відбувається під час запалення. Інгібування надходження лімфоцитів розрахоСполуки за цим винаходом пригнічують індувували за формулою: коване IL2 надходження лімфоцитів. 1- (LyX - Ly1) % інгібування = x100% Процедура експериментів (Ly2 - Ly1) Мишам лінії C3H/HEN (одержаним від Elevage де Ly1 - кількість лімфоцитів у тварин групи 1 Janvier, Франція) вводили внутрішньоочеревинно (Е3/мкл); Ly2 - кількість лімфоцитів у тварин групи IL2 (одержаний від Serono Pharmaceutical 2 (Е3/мкл), LyX - кількість лімфоцитів у тварин груResearch Institute, 20 мкг/кг, у сольовому розчині). пи X (3-5) (Е3/мкл). Сполуки за цим винаходом суспендували в Дозу сполуки за цим винаходом, необхідну для розчині 0,5% карбоксиметилцелюлози (CMC) та інгібування надходження лімфоцитів на 50% (ID50), 0,25% Твін-20 і вводили підшкірно або перорально розраховували за звичайною методикою апрокси(10 мл/кг) за 15 хв до введення IL2. мації до кривої. Результати подано в Таблиці 1. Через 24 год після введення IL2 збирали білі Таблиця ID50 для інгібування індукованого IL2 надходження лімфоцитів у очеревину сполуками за цим винаходом Приклад Дексаметазон Приклад 13 Приклад 13 Приклад 5 Діапазон доз або дози (мг/кг) 0,1-1 0,03; 0,3; 3; 30 0,3; 3; 30 0,3; 1; 3; 10; 30 Спосіб введення Підшкірно Підшкірно Перорально Підшкірно ID50 (мг/кг) 0,05 0,1 1 1 57 Комп’ютерна в ерстка А. Крулевський 78275 Підписне 58 Тираж 26 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюOxa- and thiadiasols and their use as inhibitors of matrix metalloproteinases
Назва патенту російськоюОкса- и тиадиазолы и их применение в качестве ингибиторов металлопротеиназ
МПК / Мітки
МПК: A61P 11/00, A61P 29/00, A61P 13/12, A61P 17/06, A61K 31/4245, A61P 1/04, A61P 27/02, A61P 11/06, C07D 271/06, C07D 285/08, A61P 1/02, A61P 17/00, C07D 413/04, A61P 19/02, A61P 37/06, A61P 1/16, A61P 43/00, A61P 9/10, A61P 1/00, A61P 11/08, A61P 37/02, A61P 19/08, A61P 35/04, A61P 25/02, A61P 25/00, C07D 413/06, A61P 35/00, A61P 17/02, A61P 31/04
Мітки: застосування, тіадіазоли, окса, металопротеїназ, інгібіторів
Код посилання
<a href="https://ua.patents.su/29-78275-oksa-i-tiadiazoli-ta-kh-zastosuvannya-yak-ingibitoriv-metaloprotenaz.html" target="_blank" rel="follow" title="База патентів України">Окса- і тіадіазоли та їх застосування як інгібіторів металопротеїназ</a>
Попередній патент: Спосіб одержання таблеток антибактеріального лікарського засобу на основі пефлоксацину
Наступний патент: Заклепувальний інструмент із засобом контролю операцій заклепування
Випадковий патент: Пристрій для вимірювання кутів та розмірів анатомічних структур












