Спосіб одержання 6-азацитидину-2бета-d-рибофуранозиду 5-аміно-1,2,4-триазин-3(2н)-ону
Номер патенту: 32901
Опубліковано: 15.02.2001
Автори: Алексєєва Інна Володимирівна, Пальчиківська Лариса Гнатівна
Формула / Реферат
Спосіб одержання 2-![]() -D-рибофуранозиду-5-аміно-1,2,4-триазин-3(2Н)-ону (6-азацитидину) формули:
-D-рибофуранозиду-5-аміно-1,2,4-триазин-3(2Н)-ону (6-азацитидину) формули:
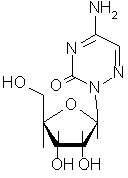
шляхом каталітичного глікозидування триазинової основи ацильованим цукром в присутності силілувальних агентів і тетрахлориду олова та подальшим деацилюванням проміжної сполуки, який відрізняється тим, що як основу використовують 5-метилмеркапто-1,2,4-триазин-3(2Н)-он, як ацильну похідну цукру - тетраацетилрибофуранозу, а наступну реакцію деацилювання здійснюють одночасно з амінолізом метилмеркаптогрупи у водному середовищі аміаком при кімнатній температурі.
Текст
Спосіб одержання 6-азацитидипу - 2b-Dрибофуранозиду 5-аміно-1,2,4-триазин-3 (2H)-oну формули: 32901 УФ-спектр у воді: l max 263 нм (e 8000), lmin 228 нм (e 3000). ПМР- спектр (DMSO- d6) d, м. д. : 8,01, 7,89 s (2Н, NН2); 7,52 d (1H,C5H); 6,01 d (1H,Сl H); 5,15 d, 4,89 d, 4,60 m (протони гидроксилів вуглеводневого кільця). Приклад 2. Синтез 6-азацитидину виконується аналогічно прикладу 1, але в конденсацію вводять 2,33 мл (20 ммоль) тетрахлориду олова. Після виконання всіх операцій одержують 1,64 г (67%) 6-азацитидину. Приклад 3. Висушен у суміш 14,3 г (0,1 моль) основи та 31,8 г (0,1 моль) цукру закладають в реактор та суспендують у 0,6 л сухого розчинника. При перемішуванні до суміші додають 16,8 мл гексаметилдісілазана, 20,5 мл триметилхлорсилана та 23,4 мл (0,2 моль) тетрахлорида олова; суміш залишають при кімнатній температурі ~ на 6 годин (моніторінг ТШХ у системі МеОН: хлороформ, 1:14). Розчинник видаляють у вакуумі, залишок розчиняють у хлороформі, промивають Н2О, роз-чинами NaHCO3 NaCI до нейтральної реакції про-мивних вод, сушать над Na2SО4 та упарюють до отримання густого олієподібного залишка три-ацетата 5метилмеркапто-нуклеозида. Ацил нук-леозид заливають 350 мл 25% водного аміака та витримують при кімнатній температурі впродовж 20 год., розчин упарюють в вакуумі, залишок кристалізують з води. Одержують 18,3 5 г (75%) 6азацитидину. Запропонований спосіб одержання 6-азацитидину не потребує спеціального обладнання, зменшує матеріальні та енергетичні витрати на стадії амонолізу внаслідок об'єднання двох процесів (деацилювання та амінування) в один та використанню дешевого і доступного водного розчину аміаку. Завдяки вдалому підбору вихідних компонентів синтезу, а саме: 5-метилмеркапто-1,2,4триазин-3(2н)-ону та тетраацетилрібози спрощується також виділення та очистка цільового продукту, що забезпечує його високий вихід. До суттєви х недоліків наведеного вище спо-собу, взятого нами як прототип, потрібно віднести слідуюче: -вибір бензольних груп, блокуючих гідроксили в цукровому компоненті, примушують процес деацилювання проводить як окрему стадію, використовуючи однонормальний розчин алкоголяту натрію у безводному спирті, як деацилюючий агент. Приготування такого виду розчину у виробничих масштабах представляє собою особливо складну та небезпечну задачу, пов'язану з додатковими витратами па зневоднювання спирту та підвищенні вимоги до безпеки виробництва. Виділення та очистка цільового нуклеозиду від похідних бензойної кислоти, які по масі значно перевищують вихід 6-азацитидину і їх утилізація, суттєво знижують ефективність способу вцілому, так як пов'язані з додатковими витратами енергії та те хнологічними незручностями. Задачею винаходу є спрощення способу одержання 6-азацитидину та підвищення його технологічності. Це досягається завдяки вдалому підбору співвідношення каталізатора та цукрового компоненту при каталітичному глікозилюванні гетероциклічної основи 1-ацилокси похідним цукру в середовищі ацетонітрила в присутності силілюючих агентів. За основу беруть -5-метилмеркапто-1,2,4-триазніі-3(2Н)-он, а цукровим компонентом тетраацетилрібофуранозу. Реакція конденсації протікає в присутності тетра хлориду олова при співвідношенні цукор/каталізатор рівному 1,6:2.0. Амоноліз продукту конденсації проводять у водному розчині аміаку при кімнатній температурі. В цих умовах реакція амінування і деацилювання проводяться в одну технологічну стадію, без виділення проміжних інтермедіатів. Новим, в способі який заявляється, є проведення обох процесів у водному середовищі аміаку при кімнатній температурі. Цей технологічний прийом вдалося втілити завдяки тому, що ви хідні основа та цукор мають функціональні замісники, які збігаються за спроможністю заміщення(амонолізу) під дією гідроксиду амонію. Спосіб одержання 6-азацитидину ілюструється слідуючими прикладами: Приклад 1. Одержання 6-азацитидину У реакційну суміш яка містить 1,43 г (10 ммоль) триазину та 3,18 г (10 ммоль) тетраацетату рібофуранози у 60 мл сухого ацетонітрилу, вносять 1,68 мл (8 ммоль) гексамстилдісилазану, 2,05 мл (16 ммоль) триметилхлорсилану та 1,87 мл (16 ммоль) тетрахлориду олова у 10 мл діхлоретану і перемішують протягом 4 годин (ТШХ-контроль). Розводять 100 мл хлороформу та 50 мл води. Органічну фазу відокремлюють, промивають розчином бікарбонату нагрію (50 мл), водою (3*50 мл), сушать над сульфатом натрія та випорюють до сухого залишку. Останній суспендують у 50 мл розчину водного аміаку та витримують протягом 20 годин при кімнатній температурі. Після випаровування розчинника залишок кристалізують з води. Одержують 1,46 г (60%) цільового продукту, т.топл. 223 - 225° С (за літературними даними 222 - 224° С). Джерела інформації 1. Cherneckij V., Chladek S.. Sorm F. Et al. 6Azacytidine and some its N4-derivatives // Coll. Czechoslov. Chem. Comm. - 1962- v.27, № 1.- P. 87-92. 2. Zemlicka J., Sorm F. Nucleic acids components and their analogues. LXI. A new synthesis of 6-azacytidine // Coll. Czechoslov. Chem. Comm.1965. - v.30. - P. 2052-2067. 3. A.c. CPCP № 175483, MKB C 07 H 12/10. "Изобретения" 1965, № 20. 4. Пат. ФРН № 2122991 MKB C 07 H 19/06, 19/12. Публ. 9.07.1982 (Auszuge aus den Patentschriftcn, № 23). 5. Пат. СРР № 91798, MKB C 07 Д 253/06. Публ. 30.05.1981. 6. А.с. CPCP № 1625881, MKB C 07 H 19/12. "Изобретения", 1991, № 5. 7. Пат. України № 17209 MKB C 07 H 19/12. "Промислова власність", 1997, № 5 (прототип). 2 32901 __________________________________________ ДП "Український інститут промислової власності" (Укрпатент) Україна, 01133, Київ-133, бульв. Лесі Українки, 26 (044) 295-81-42, 295-61-97 __________________________________________________________ Підписано до друку ________ 2001 р. Формат 60х84 1/8. Обсяг ______ обл.-вид. арк. Тираж 50 прим. Зам._______ ____________________________________________________________ УкрІНТЕІ, 03680, Київ-39 МСП, вул. Горького, 180. (044) 268-25-22 ___________________________________________________________ 3
ДивитисяДодаткова інформація
Назва патенту англійськоюA method for preparation of 6-azacytidine -2b-d-ribofuranoside 5-amino-1,2,4-triazine-3(2н)-on
Автори англійськоюAleksieieva Inna Volodymyrivna, Alekseeva Inna Volodymyrivna
Назва патенту російськоюСпособ получения 6-азацитидина-2b-d-рибофуранозида 5-амино-1,2,4-триазин-3(2н)-она
Автори російськоюАлексеева Инна Владимировна
МПК / Мітки
МПК: C07H 19/12
Мітки: 6-азацитидину-2бета-d-рибофуранозиду, 5-аміно-1,2,4-триазин-3(2н)-ону, спосіб, одержання
Код посилання
<a href="https://ua.patents.su/3-32901-sposib-oderzhannya-6-azacitidinu-2beta-d-ribofuranozidu-5-amino-124-triazin-32n-onu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 6-азацитидину-2бета-d-рибофуранозиду 5-аміно-1,2,4-триазин-3(2н)-ону</a>
Попередній патент: Засіб для лікування хвороб, спричинених герпетичною інфекцією
Наступний патент: Спосіб визначення оріентації фібрил колагенових волокон остеонів кістки
Випадковий патент: Спосіб гастроєюнопластики







