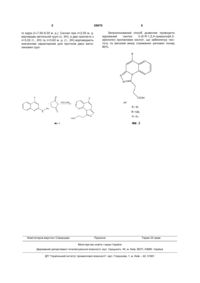
Спосіб отримання 3-(5-r-1,2,4-триазоло[4,3-а]хінолін)пропанових кислот
Номер патенту: 59970
Опубліковано: 10.06.2011
Автори: Бражко Олександр Анатолійович, Коваленко Данило Сергійович, Омельянчик Людмила Олександрівна, Завгородній Михайло Петрович
Формула / Реферат
Спосіб отримання 3-(5-R-1,2,4-триазоло[4,3-а]хінолін)пропанових кислот, що включає розчинення відповідних гідразинопохідних гетероциклів у органічному розчиннику, циклізацію сполуки кип'ятінням реакційної суміші, фільтрування осаду, переосадження отриманої сполуки, який відрізняється тим, що розчинення еквівалентних кількостей відповідного 2-гідразинохіноліну та ангідриду бурштинової кислоти проводять в оцтовій кислоті, кип'ятіння здійснюють протягом 2±0,1 годин, а переосадження сполуки виконують з водного розчину соди із подальшим підкисленням розчином 30 %-ї хлоридної кислоти до рН=4 з одержанням сполуки загальної формули:
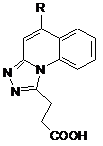 ,
,
де:
R=H;
R=Alk;
R=Ar.
Текст
Спосіб отримання 3-(5-R-1,2,4-триазоло[4,3а]хінолін)пропанових кислот, що включає розчинення відповідних гідразинопохідних гетероциклів у органічному розчиннику, циклізацію сполуки кип'ятінням реакційної суміші, фільтрування осаду, переосадження отриманої сполуки, який відрізняється тим, що розчинення еквівалентних кількостей відповідного 2-гідразинохіноліну та ангідриду бурштинової кислоти проводять в оцтовій кислоті, кип'ятіння здійснюють протягом 2±0,1 годин, а пе реосадження сполуки виконують з водного розчину соди із подальшим підкисленням розчином 30 %-ї хлоридної кислоти до рН=4 з одержанням сполуки загальної формули: R Корисна модель належить до синтезу хімічних речовин, а саме до синтезу похідних гетероциклів та карбонових кислот. Відомий спосіб отримання (гетерил)карбонових кислот, (Journal; Reynolds; Van Allan; JOCEAH; Journal of Organic Chemistry; 24; 1959; 1478,1481; DOI: 10.1021/jo01092a023; ISSN: 0022-3263.), який включає проведення реакції синтезу відповідних хінолін-2-ілгідразонів шляхом розчинення відповідного 2-гідразонохіноліну і відповідної оксосполуки в органічних розчинниках та їх змішування, фільтрування осаду з подальшою його циклізацією в присутності окислювача - мурашиної кислоти, кип'ятіння розчину протягом кількох годин, фільтрування осаду, переосадження отриманої сполуки з органічного розчинника. Недоліками цього способу є: - утворення продукту в 2 стадії: перша стадія одержання відповідних 2-гідразинохінолінів; друга - їх циклізація в присутності окислювача; - використання мурашиної кислоти високої якості, для забезпечення протікання реакції. Спільними ознаками, з рішенням що заявляється, є: • розчинення гідразинопохідних відповідних гетеро циклів у органічному розчиннику; • кип'ятіння реакційної суміші; • циклізація сполуки; • фільтрування осаду; • переосадження отриманої сполуки з органічного розчинника. Відомий спосіб синтезу похідних 1,2,4триазоло[4,3-а]хіноліну (Journal; L. Savini, L. Chiasserini, W. Filippelli, С Pellerano, G. Falcone, Synthesis and pharmacological activity of 1,2,4triazolo[4,3-a]quinolines, 2001 II Farmaco, Vol.56, 939-945), який включає проведення реакції синтезу відповідних хінолін-2-ілгідразонів та їх циклізацію в 98 %-й мурашиній кислоті під час кип'ятіння із зворотним холодильником протягом 6-8 годин, і подальшим переосадженням отриманої сполуки з органічного розчинника. Недоліками цього способу є: N N N COOH , (19) UA (11) 59970 (13) U де: R=H; R=Alk; R=Ar. 3 59970 - фільтрування осаду відповідного хінолін-2ілгідразону; - використання мурашиної кислоти високої якості. Спільними з прототипами ознаками є: • розчинення гідразинопохідних відповідних гетероциклів в органічному розчиннику; • кип'ятіння реакційної суміші; • циклізація сполуки кип'ятінням реакційної суміші; • фільтрування осаду; • переосадження отриманої сполуки. В основу корисної моделі поставлено задачу розробити спосіб отримання 3-(5-R-1,2,4триазоло[4,3-а]хінолін)пропанових кислот, де R= H; R=Alk; R=Ar, який шляхом розчинення відповідного 2-гідразинохіноліну в оцтовій кислоті з одночасним додаванням ангідриду бурштинової кислоти з подальшим кип'ятінням, яке призводить до циклізації утвореного гідразиду, що дозволяє отримати новий ряд потенційно біологічно активних сполук, які можуть проявляти анальгезуючу, протизапальну, транквілізуючу, мембраностабілізуючу, антиоксидантну активність, виступати як антагоністи рецепторів гама-аміномасляної кислоти та тирозин фосфотази, з високим виходом продукту, з використанням доступних реактивів. Суттєвими ознаками способу є: - розчинення еквівалентних кількостей відповідного 2-гідразинохіноліну та ангідриду бурштинової кислоти в оцтовій кислоті; - кип'ятіння реакційної суміші протягом 2±0,1 годин; - фільтрування утвореного осаду; - переосадження отриманої сполуки з водного розчину соди із подальшим підкисленням розчином 30 %-ї хлоридної кислоти до рН=4. Відмінними від прототипу ознаками є: - розчинення еквівалентних кількостей відповідного 2-гідразинохіноліну та ангідриду бурштинової кислоти в оцтовій кислоті; - кип'ятіння реакційної суміші протягом 2±0,1 годин; - переосадження отриманої сполуки з водного розчину соди із подальшим підкисленням розчином 30%-ї хлоридної кислоти до рН=4. 4 На фіг. 1 зображено схему отримання 3-(5-R1,2,4-триазоло[4,3-а]хінолін)пропанових кислот, де: R= H; R=Alk; R=Ar. На фіг. 2 зображено загальну структурну формулу синтезованих сполук ряду 3-(5-R-1,2,4триазоло[4,3-а]хінолін)пропанових кислот. Спосіб здійснюють таким чином: • еквівалентні кількості відповідного 2гідразинохіноліну та ангідриду бурштинової кислоти розчиняють в оцтовій кислоті; • одержану реакційну суміш кип'ятять протягом 2±0,1 годин; • фільтрують утворений осад; • переосаджують отриману сполуку з водного розчину соди із подальшим підкисленням розчином 30 %-ї хлоридної кислоти до рН=4. Приклад одержання сполуки 3-(5-метил-1,2,4триазоло[4,3-а]хінолін)-пропанової кислоти: - еквівалентні кількості (0,01 моль) 4-метил-2гідразинохіноліну (1,73 г) та ангідриду бурштинової кислоти (1 г) розчиняли в 20 мл оцтової кислоти; - отриману реакційну суміш кип'ятили на піщаному нагрівнику протягом 2 годин; - утворений осад фільтрували та промивали на фільтрі водою; - переосаджували отриману сполуку з водного розчину соди підкисливши розчином 30 %-ї хлоридної кислоти до рН=4. Вихід 3-(5-метил-1,2,4-триазоло[4,3а]хінолін)пропанової кислоти складає 2,1 г (82,4 %). Тпл=225-227 °С. Знайдено: С, 69,40; Н, 6,40; N, 24,21. Вирахувано: С, 69,34; Н, 6,40; N, 24,26. Індивідуальність сполуки контролювали і підтвердили методом тонкошарової хроматографії на пластинках "Silufol" у системі розчинників: оцтова кислота-вода (1:1). Значення Rf =0,78. Хімічну структуру сполуки було доведено за допомогою спектроскопії парамагнітного резонансу (ПМР) та ІЧ-спектроскопією. Синтезована 3-(5-метил-1,2,4-триазоло [4,3а]хінолін)пропанова кислота є жовтою кристалічною речовиною, розчинна в диметилформаміді, розчинах гідроксидів лужних металів, мало розчинна у воді. Таблиця 1 ІЧ-спектри 3-(5-метил 1,2,4-триазоло[4,3-а]хінолін)пропанової кислоти Сполука ІЧ-спектри, , см C=N, asC=O C=C 3-(5-метил 1,2,4триазоло[4,3-а]хінолін) 1570, 1620 пропанова кислота -1 1690 В ІЧ-спектрах сполук присутні інтенсивні смуги коливань, які характерні для валентних симетричних та асиметричних коливань карбонільної групи -1 в ділянки 1690 см . Малоінтенсивні смуги коли-1 вань знаходяться в ділянки 3550 см , що свідчить про асоціацію молекул кислоти за рахунок карбоксильної групи. Широкі смуги інтенсивності харак sCOOH Інші групи 1720 3200(N-H), 2250(CH3), 1410(CH2), 640(CH2-CH2) -1 терні в ділянки 2500-3000 см , що свідчить про існування кислот у формі біполярного іону. Смуги коливань зв'язків C=N та C=C проявляються в -1 ділянки 1620-1570 см (табл. 1). У ПМР спектрах спостерігається складний мультиплет протонів ароматичного кільця хіноліново 5 59970 го ядра (=7,50-8,30 м. д.). Сигнал при =2,55 м. д. відповідає метильній групі (с, 3Н), а два триплети з =3,02 (т., 2Н) та =3,62 м. д. (т., 2Н) відповідають значенням характерним для протонів двох метиленових груп. Комп’ютерна верстка І.Скворцова 6 Запропонований спосіб дозволяє проводити керований синтез 3-(5-R-1,2,4-триазоло[4,3а]хінолін) пропанових кислот, що забезпечує чистоту та високий вихід отриманих речовин понад 80%. Підписне Тираж 24 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 3-(5-r-1,2,4-triazolo[4,3-a]quinoline)propanoic acids
Автори англійськоюKovalenko Danylo Serhiiovych, Brazhko Oleksandr Anatoliiovych, Omelianchyk Liudmyla Oleksandrivna, Zavhorodnii Mykhailo Petrovych
Назва патенту російськоюСпособ получения 3-(5-r-1,2, 4-триазоло[4, 3-а]хинолин)пропановых кислот
Автори російськоюКоваленко Данила Сергеевич, Бражко Александр Анатолиевич, Омельянчик Людмила Александровна, Завгородний Михаил Петрович
МПК / Мітки
МПК: C07D 413/00, C07D 403/14
Мітки: 3-(5-r-1,2,4-триазоло[4,3-а]хінолін)пропанових, спосіб, отримання, кислот
Код посилання
<a href="https://ua.patents.su/3-59970-sposib-otrimannya-3-5-r-124-triazolo43-akhinolinpropanovikh-kislot.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання 3-(5-r-1,2,4-триазоло[4,3-а]хінолін)пропанових кислот</a>
Попередній патент: Спосіб прогнозування перебігу захворювання у хворих на рак шлунка
Наступний патент: Спосіб отримання 3-(5-r-1,2,4-триазоло[4,3-a]хінолін)пропенових кислот
Випадковий патент: Спосіб керування зварювальним струмом при електродуговому зварюванні