Алілвмісні бісфеноли з перфторованими ядрами як мономери для поліарилових етерів
Номер патенту: 63449
Опубліковано: 10.10.2011
Автори: Ткаченко Ігор Михайлович, Шевченко Валерій Васильович, Москаленко Олег Вадимович, Шекера Олег Васильович
Формула / Реферат
Алілвмісні бісфеноли (АБФ)з перфторованими ядрами загальної формули
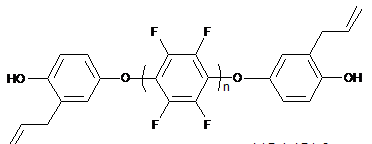 ,
,
де при n = 1 АЕБФ-1, АБФ-1, при n = 2 АЕБФ-2, АБФ-2 як мономери для поліарилових етерів.
Текст
Алілвмісні бісфеноли (АБФ) з перфторованими ядрами загальної формули 3 63449 Поставлена задача вирішується синтезом алілвмісних бісфенолів, які містять перфторовані моно- або біфеніленові ядра за представленою схемою: F HO F O n F O OH F Br F O F O n F O O F АEФБ-1, АEБФ-2 F HO F O n F O OH F АФБ-1, АБФ-2 де при n = 1 АЕБФ-1, АБФ-1, при n = 2 АЕБФ-2, АБФ-2 як мономери для поліарилових етерів. Вказані алілвмісні бісфеноли з перфторароматичними ядрами, їх властивості та спосіб отримання в літературі не описані. Сутність запропонованої корисної моделі пояснюється наступними прикладами. Приклад 1 Синтез алілвмісного перфторароматичного бісфенолу АБФ-1 здійснювали у дві стадії. На першій стадії отримували діаліловий етер 1,4-біс(4гідроксифенокси)тетрафторбензолу (АЕБФ-1). На другій - перегрупуванням Кляйзена АЕБФ-1 отримували кінцевий бісфенол АБФ-1. І-а стадія. Синтез 1,4-біс(4алілоксифенокси)тетрафторбензолу (АЕБФ-1). До розчину 3 г (0,00819 моль) 1,4-біс(4гідроксифенокси)тетрафторбензолу в 37 мл ацетону вносили 2,83 г (0,02048 моль) K2СО3 і до отриманої суміші при перемішуванні додавали 2,18 г (0,01802 моль) алілброміду, кип'ятили протягом 20 год. Після охолодження реакційну масу виливали у воду з льодом. Отриманий осад відфільтровували, промивали 10 %-ним розчином NaOH, водою та перекристалізовували з ізопропілового спирту. Будова синтезованого перфторароматичного діалілового етеру АЕБФ-1 доведена даними еле1 ментного аналізу, ІЧ- та Н ЯМР спектроскопії. Брутто формула: C24H18F4O4. Вихід (%) - 80. Тпл. = 107-108 °С. Обчислено (%): С - 64;57; F - 17,02. Знайдено (%): С - 64,12; F - 17,43. -1 ІЧ-спектр: (см ): 927 (СН2=СН), 988 (C-F), 1240 (Аr-О-Аr), 1504 (С=Саром.), 2800-3100 (СН). 1 Н ЯМР (500 МГц, CDCI3), , м. д.: 4,52 (д, 4Н, J=5,4 Гц, -СН2-), 5,32 (д.д.д., 2Н, Jцис=10,8; 1,5; 0,98 4 а Гц, =СН2 ), 5,44 (д.д.д., 2Н, Jтранс=17,6; 1,5; 0,98 Гц, б =СН2 ), 6,03-6,10 (м, 2Н, =СН-), 6,90 (д, 4Н, J=9,3 Гц, Ph), 6,96 (д, 4Н, J=9,3 Гц, Ph). ІІ-а стадія. Синтез 2,2-діаліл-1,4-біс(4гідроксифенокси)тетрафтор-бензолу (АБФ-1). 2 г (0,00448 моль) АЕБФ-1 витримували при температурі 210 °С протягом 15 хв в атмосфері аргону. Отриманий в такий спосіб алілвмісний перфторований бісфенол АБФ-1 перекристалізовували із гептану. Будова синтезованого АБФ-1 доведена дани1 ми елементного аналізу, 14-та Н ЯМР спектроскопії. Брутто формула: C24H18F4O4. Вихід (%) - 75. Тпл. = 124-127 °С. Обчислено (%): С - 64,57; F - 17,02. Знайдено (%): С - 64,21; F - 17,78. -1 ІЧ-спектр: (см ): 914 (СН2=СН), 993 (C-F), 1250 (Аr-О-Аr), 1499 (С=Саром.), 2800-3000 (СН), 31003600 (ОН). 1 Н ЯМР (500 МГц, CDCI3), , м. д.: 3,29 (д, 4Н, J=6,2 Гц, -СН2-), 5,00-5,06 (м, 4Н, =СН2), 5,90-6,00 (м, 2Н, =СН-), 6,75-6,88 (м, 6Н, Ph), 9,32 (с, 2Н, ОН). Приклад 2 Синтез алілвмісного перфторароматичного бісфенолу АБФ-2 проводили аналогічно синтезу АБФ-1. 1,4-біс(4-алілоксифенокси)октафторбензол (АЕБФ-2). Брутто формула: C30H18F804. Вихід (%) - 75. Тпл. = 93-94 °С. Обчислено (%): С - 60;61; F - 25,57. Знайдено (%):С - 61,08; F - 25,88. -1 ІЧ-спектр: (см ): 924 (СН2=СН), 980 (C-F), 1244 (Ar-O-Ar), 1497 (С=Саром.), 2800-3100 (СН). 1 Н ЯМР (500 МГц, CDCI3), , м. д.: 4,55 (д, 4Н, J=4,89 Гц, -СН2-), 5,33 (д.д.д., 2Н, Jцис=10,3; 0,97; а 0,97 Гц, =СН2 ), 5,44 (д.д.д., 2Н, Jтранс=17,6; 1,5; б 0,98 Гц, =СН2 ), 6,03-6,11 (м, 2Н, =СН-), 6,93 (д, 4Н, J=8,8 Гц, Ph), 7,02 (д, 4Н, J=9,3 Гц, Ph). 2,2-діаліл-1,4-біс(4гідроксифенокси)октафторбензол (АБФ-2). Даний бісфенол перекристалізовували з декану. Брутто формула: C30H18F8O4. Вихід (%) - 70. Тпл. = 108-111 °С. Обчислено (%): С - 60,61; F - 25,57. Знайдено (%): С - 61,54; F - 25,93. -1 ІЧ-спектр: (см ): 926 (СН2=СН), 974 (C-F), 1242 (Аr-О-Аr), 1489 (С=Саром.), 2850-3000 (СН), 3500 (ОН). 1 Н ЯМР (500 MHz, CDCI3), , м. д.: 3,42 (д, 4Н, J=5,9 Гц, -СН2-), 4,87 (с, 2Н, ОН), 5,19-5,23 (м, 4Н, =СН2), 5,99-6,07 (м, 2Н, =СН-), 6,91 (д, 2Н, J=7,8 Гц, Ph), 6,84 (д, 2Н, J=7,8 Гц, Ph), 6,83 (с, 2Н, Ph). Фторований поліариловий етер (ФПАЕ) синтезований на основі 2,2-діаліл-1,4-біс(4гідроксифенокси)тетрафторбензолу та декафторбіфенілу. Будова отриманого ФПАЕ, який містить алільні групи вздовж полімерного ланцюга, дове1 дена даними ІЧ- та Н ЯМР спектроскопії: 1 ІЧ-спектр (см- ): 918 (СН2=СН), 980 (C-F), 1270 (Аr-О-Аr), 1477 (С=Саром), 2800-3000 (СН). 1 Н ЯМР (500 МГц, CDCI3), , м. д.: 3,54 (д, 4Н, J=6,1 Гц, -СН2-), 5,10-5,16 (м, 4Н, =СН2), 5,92-6,08 5 (м, 2Н, = СН-), 6,70-6,80 (м, 4Н, Ph), 6,96 (с, 2Н, Ph). Джерела інформації: 1. Шевченко В.В., Ткаченко И.М., Шекера О.В. Фторированные в ядро ароматические полиэфиры // Высокомолекулярные соединения, сер. Б. 2010. - 52, №7. - С. 1208-1231. 2. Synthesis and characterization of partly fluorinated poly(phthalazinone ether)s crosslinked by allyl group for passive optical waveguides / G. Li, J. Wang, G. Yu et al. // Polymer. - 2010. - 51, No 6. - P. 1524-1529. 3. Synthesis and characterization of poly(aryl ether ketone) ionomers with sulfonic acid groups on pendant aliphatic chains for proton-exchange membrane fuel cells / Z.P. Guan, M. Xiao, S.J. Wang et al. // European Polymer Journal. - 2010. - 46, Nol. P. 81-91. 4. Lee K.-S., Kim J.-P., Lee J.-S. Synthesis and characterization of low-birefringent crosslinkable Комп’ютерна верстка М. Ломалова 63449 6 fluorinated poly(arylene ether sulfide)s containing pendant phenyl moiety // Polymer. - 2010. - 51, No 3. - P. 632-638. 5. Optimizing fluorinated poly(arylene ether)s for optical waveguide applications / J. Jiang, C.L. Callender, C. Blanchetiere et al. // Optical Materials. 2006. - 28, No 3. - P. 189-194. 6. Synthesis and characterizations of highly fluorinated poly(arylene ether)s for quadratic nonlinear optics / K. Aljoumaa, Y. Qi, J. Ding // Macromolecules. - 2009. - 42, No 23. - P. 9275-9288. 7. Fluorinated poly(arylene ether sulfide) for polymeric optical waveguide devices / J.-P. Kim, W.Y. Lee, J.-W. Kang et al. // Macromolecules. - 2001. 34, No 22. - P. 7817-7821. 8. Bis allyl benzoxazine: synthesis, polymerisation and polymer properties / K.S. Santhosh Kumar, C.P. Reghunadhan Nair, T.S. Radhakrishnan et al. // European Polymer Journal. 2007. - 43, No 6. - P. 2504-2514. Підписне Тираж 23 прим. Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюAllyl-containing bisphenols with perfluorinated rings as monomers for polyaryl ethers
Автори англійськоюShevchenko Valerii Vasyliovych, Tkachenko Ihor Mykhailovych, Moskalenko Oleh Vadymovych, Shekera Oleh Vasylovych
Назва патенту російськоюАллилсодержащие бисфенолы с перфторироваными ядрами как мономеры для полиариловых этеров
Автори російськоюШевченко Валерий Васильевич, Ткаченко Игорь Михайлович, Москаленко Олег Вадимович, Шекера Олег Васильевич
МПК / Мітки
МПК: C07C 39/00, C07C 25/00
Мітки: мономери, бісфеноли, поліарилових, перфторованими, етерів, ядрами, алілвмісні
Код посилання
<a href="https://ua.patents.su/3-63449-alilvmisni-bisfenoli-z-perftorovanimi-yadrami-yak-monomeri-dlya-poliarilovikh-eteriv.html" target="_blank" rel="follow" title="База патентів України">Алілвмісні бісфеноли з перфторованими ядрами як мономери для поліарилових етерів</a>
Попередній патент: Спосіб приготування модифікованої полістирольної піни
Наступний патент: Спосіб формування фібробетонних виробів
Випадковий патент: Машина безперервного лиття







