Похідні 2-арилімідазолу як інгібітори ферменту pde10a
Номер патенту: 107817
Опубліковано: 25.02.2015
Автори: Кехлер Ян, Кілберн Джон Пол, Ланґґор Мортен, Маріґо Мауро, Пюшл Аск, Нільсен Якоб
Формула / Реферат
1. Сполуки, що мають структуру І
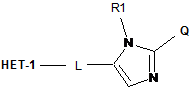 , І
, І
де НЕТ1 являє собою гетероароматичну групу формули II, що містить від 2 до 4 атомів азоту:
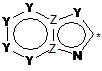 , II
, II
де Y може бути N або СН, Z може бути N або С, і де НЕТ1 необов'язково може бути заміщений за допомогою аж до трьох замісників R2-R4, індивідуально вибраних з водню, С1-С6алкілу; галогену; ціано, галоген(С1-С6)алкілу; арилу, алкокси і С1-С6гідроксіалкілу, і де символ * позначає місце приєднання;
Q являє собою феніл, необов'язково заміщений 1-5 замісниками, або моноциклічну 5-членну або 6-членну гетероароматичну групу, що містить 1 або 2 гетероатоми;
-L- являє собою сполучну ланку, вибрану з -S-CH2-, -CH2-S-, -CH2-CH2-, -СН=СН- і -С≡С-;
R1 вибраний з Н, С1-С6алкілу; С1-С6алкіл(С3-С8)циклоалкілу; С1-С6гідроксіалкілу, CH2CN, CH2C(O)NH2, С1-С6арилалкілу і C1-С6алкілгетероциклоалкілу,
та їх таутомери і фармацевтично прийнятні солі,
за умови, що сполука не являє собою 2-(5-феніл-1Н-імідазол-2-ілметилсульфаніл)-1Н-бензімідазол або 2-(5-феніл-1Н-імідазол-2-ілсульфанілметил)-1Н-бензімідазол.
2. Сполука за п. 1, де НЕТ1 являє собою імідазо[1,2-а]піримідиновий фрагмент.
3. Сполука за п. 1, де НЕТ1 являє собою [1,2,4]триазоло[1,5-а]піридиновий фрагмент.
4. Сполука за п. 1, де НЕТ1 являє собою імідазо[1,2-а]піридиновий фрагмент.
5. Сполука за п. 1, де НЕТ1 являє собою імідазо[4,5-b]піримідиновий фрагмент.
6. Сполука за п. 1, де НЕТ1 являє собою піразоло[1,5-а]піридиновий фрагмент.
7. Сполука за п. 1, де НЕТ1 являє собою [1,2,4]триазоло[1,5-а]піримідиновий фрагмент.
8. Сполука за п. 1, де НЕТ1 являє собою [1,2,4]триазоло[1,5-а]піразиновий фрагмент.
9. Сполука за п. 1, де НЕТ1 являє собою [1,2,4]триазоло[1,5-с]піримідиновий фрагмент.
10. Сполука за п. 1, де Q вибраний з групи, що складається з фенілу, тіофену, фурану, тіазолу, піразолу, піридину, піримідину і піразину.
11. Сполука за будь-яким з пп. 1-10, де R2, R3 і R4 - всі являють собою водень.
12. Сполука за будь-яким з пп. 1-10, де щонайменше один з R2, R3 і R4 являє собою С1-С6алкіл, такий як метил.
13. Сполука за будь-яким з пп. 1-10, де щонайменше один з R2, R3 і R4 являє собою галоген, такий як хлор або бром.
14. Сполука за п. 1, де сполука вибрана з групи, що складається з:
5,8-диметил-2-[2-(2-феніл-1Н-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-а]піразину;
5,8-диметил-2-[2-(1-метил-2-феніл-1Н-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-а]піразину;
8-етил-5-метил-2-[2-(1-метил-2-феніл-1Н-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-а]піридину;
5,8-диметил-2-[2-(1-метил-2-тіофен-2-іл-1Н-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-а]піразину;
5,8-диметил-2-[2-(1-метил-2-тіазол-2-іл-1Н-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-а]піразину;
8-метокси-5-метил-2-[2-(2-феніл-1Н-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-а]піридину;
8-метокси-5-метил-2-[2-(1-метил-2-тіофен-2-іл-1Н-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-а]піридину і
8-метокси-5-метил-2-[2-(1-метил-2-феніл-1Н-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-а]піридину,
та їх фармацевтично прийнятних солей.
15. Сполука за будь-яким з пп. 1-14 для використання як лікарського засобу.
16. Сполука за будь-яким з пп. 1-14 для використання при лікуванні нейродегенеративного або психічного розладу самої по собі або в комбінації з одним або декількома нейролептичними лікарськими засобами, такими як сертиндол, оланзапін, рисперидон, кветіапін, арипіпразол, галоперидол, клозапін, зипрасидон і осанетант, де нейродегенеративний розлад вибраний з групи, що складається з хвороби Альцгеймера, мультиінфарктної деменції, алкогольної деменції або деменції, пов'язаної з іншими наркотичними засобами, деменції, пов'язаної з внутрішньочерепними пухлинами або травмою мозку, деменції, пов'язаної з хворобою Хантінгтона або хворобою Паркінсона, або деменції, пов'язаної зі СНІДом; делірію; амнестичного розладу; посттравматичного стресового розладу; вродженого недоумства; розладу навчання, наприклад розладу навчання читанню, розладу навчання математиці або розладу навчання письмовому виразу думок; синдрому дефіциту уваги/гіперактивності та вікового зниження когнітивних функцій; а психічний розлад вибраний з групи, що складається з шизофренії, наприклад, параноїдного, дезорганізованого, кататонічного, недиференційованого або резидуального типу; шизофреніформного розладу; шизоафективного розладу, наприклад, маревного типу або депресивного типу; маревного розладу; психотичного розладу, викликаного речовиною, наприклад психозу, викликаного алкоголем, амфетаміном, марихуаною, кокаїном, галюциногенами, леткими сполуками, опіоїдами або фенциклідином; розладу особистості параноїдного типу і розладу особистості шизоїдного типу.
17. Сполука за будь-яким з пп. 1-14 для використання при лікуванні наркотичної залежності у ссавця, включаючи людину, такої як хронічний алкоголізм, амфетамінова наркоманія, кокаїнова наркоманія або опіатна наркоманія.
18. Сполука за будь-яким з пп. 1-14 для приготування лікарського засобу для використання при лікуванні наркотичної залежності у ссавця, включаючи людину, такої як хронічний алкоголізм, амфетамінова наркоманія, кокаїнова наркоманія або опіатна наркоманія.
19. Сполука за будь-яким з пп. 1-14 для приготування лікарського засобу для використання при лікуванні нейродегенеративного або психічного розладу, де нейродегенеративний розлад вибраний з групи, що складається з хвороби Альцгеймера, мультиінфарктної деменції, алкогольної деменції або деменції, пов'язаної з іншими наркотичними засобами, деменції, пов'язаної з внутрішньочерепними пухлинами або травмою мозку, деменції, пов'язаної з хворобою Хантінгтона або хворобою Паркінсона, або деменції, пов'язаної зі СНІДом; делірію; амнестичного розладу; посттравматичного стресового розладу; вродженого недоумства; розладу навчання, наприклад розладу навчання читанню, розладу навчання математиці або розладу навчання письмовому виразу думок; синдрому дефіциту уваги/гіперактивності та вікового зниження когнітивних функцій; а психічний розлад вибраний з групи, що складається з шизофренії, наприклад, параноїдного, дезорганізованого, кататонічного, недиференційованого або резидуального типу; шизофреніформного розладу; шизоафективного розладу, наприклад, маревного типу або депресивного типу; маревного розладу; психотичного розладу, викликаного речовиною, наприклад психозу, викликаного алкоголем, амфетаміном, марихуаною, кокаїном, галюциногенами, леткими сполуками, опіоїдами або фенциклідином; розладу особистості параноїдного типу і розладу особистості шизоїдного типу.
20. Сполука для приготування лікарського засобу для використання при лікуванні за п. 15, де лікування психічних розладів включає сумісне введення нейролептичного засобу, такого як сертиндол, оланзапін, рисперидон, кветіапін, арипіпразол, галоперидол, клозапін, зипрасидон і осанетант.
21. Спосіб лікування суб'єкта, страждаючого нейродегенеративним або психічним розладом, де нейродегенеративний розлад вибраний з групи, що складається з хвороби Альцгеймера, мультиінфарктної деменції, алкогольної деменції або деменції, пов'язаної з іншими наркотичними засобами, деменції, пов'язаної з внутрішньочерепними пухлинами або травмою мозку, деменції, пов'язаної з хворобою Хантінгтона або хворобою Паркінсона, або деменції, пов'язаної зі СНІДом; делірію; амнестичного розладу; посттравматичного стресового розладу; вродженого недоумства; розладу навчання, наприклад розладу навчання читанню, розладу навчання математиці або розладу навчання письмовому виразу думок; синдрому дефіциту уваги/гіперактивності та вікового зниження когнітивних функцій; а психічний розлад вибраний з групи, що складається з шизофренії, наприклад, параноїдного, дезорганізованого, кататонічного, недиференційованого або резидуального типу; шизофреніформного розладу; шизоафективного розладу, наприклад, маревного типу або депресивного типу; маревного розладу; психотичного розладу, викликаного речовиною, наприклад психозу, викликаного алкоголем, амфетаміном, марихуаною, кокаїном, галюциногенами, леткими сполуками, опіоїдами або фенциклідином; розладу особистості параноїдного типу і розладу особистості шизоїдного типу; де вказаний спосіб включає введення ефективної кількості сполуки за будь-яким з пп. 1-14 самої по собі або в комбінації з одним або декількома нейролептичними засобами, такими як сертиндол, оланзапін, рисперидон, кветіапін, арипіпразол, галоперидол, клозапін, зипрасидон і осанетант.
22. Спосіб лікування суб'єкта-ссавця, включаючи людину, що страждає наркотичною залежністю, наприклад хронічним алкоголізмом, амфетаміновою, кокаїновою або опіатною залежністю, який включає введення вказаному суб'єктові сполуки формули І в кількості, ефективній при лікуванні наркотичної залежності.
23. Спосіб лікування суб'єкта-ссавця, включаючи людину, що страждає наркотичною залежністю, наприклад хронічним алкоголізмом, амфетаміновою, кокаїновою або опіатною залежністю, який включає введення вказаному суб'єктові сполуки формули І в кількості, ефективній для інгібування PDE10A.
24. Фармацевтична композиція, яка містить терапевтично ефективну кількість сполуки за будь-яким з пп. 1-14 і один або декілька фармацевтично прийнятних носіїв, розріджувачів і ексципієнтів.
Текст
Реферат: Цей винахід стосується сполук, які є інгібіторами ферменту PDE10A. Винахід також стосується фармацевтичної композиції, яка містить терапевтично ефективну кількість сполуки цього винаходу і фармацевтично прийнятний носій. Цим винаходом також пропонуються способи отримання сполук формули (І). Крім того, цей винахід стосується способу лікування суб'єкта, страждаючого нейродегенеративним розладом, який включає введення суб'єктові терапевтично ефективної кількості сполуки формули (І). Цей винахід також стосується способу лікування суб'єкта, страждаючого наркотичною залежністю, який включає введення суб'єктові терапевтично ефективної кількості сполуки формули (І). Цей винахід також стосується способу лікування суб'єкта, страждаючого психічним розладом, який включає введення суб'єктові терапевтично ефективної кількості сполуки формули (І). UA 107817 C2 (12) UA 107817 C2 UA 107817 C2 5 10 15 20 25 30 35 40 45 50 55 60 Галузь техніки, до якої відноситься винахід Цим винаходом пропонуються гетероароматичні сполуки, які є інгібіторами ферменту PDE10A, і як такі корисні при лікуванні нейродегенеративних і психічних розладів. Зокрема, цим винаходом пропонуються сполуки, які є високоселективними відносно підтипу PDE10 в порівнянні з іншими підтипами PDE. Цим винаходом пропонуються також фармацевтичні композиції, які містять сполуки цього винаходу, і способи лікування розладів з використанням сполук цього винаходу. Попередній рівень техніки У даному описі надаються посилання на різні публікації у їх повному обсязі. Таким чином, зміст цих публікацій включений в даний опис за допомогою посилання для повнішого опису рівня галузі техніки, до якої відноситься цей винахід. Циклічні нуклеотиди циклічний аденозинмонофосфат (сAMP) і циклічний гуанозинмонофосфат (cGMP) - функціонують як вторинні внутріклітинні месенджери, що регулюють широкий спектр процесів в нейронах. Внутріклітинні сAMP і cGMP генеруються аденіл- і гуанілциклазами і розкладаються циклонуклеотид-фосфодіестеразами (PDE). Внутріклітинні рівні сAMP і cGMP регулюються внутріклітинною передачею сигналу, і стимуляція/репресія аденіл- і гуаніл-циклаз у відповідь на активацію GPCR є конкретно описаним шляхом регуляції концентрацій циклічних нуклеотидів (Antoni, F.A. Front. Neuroendocrinol. 2000, 21, 103-132). Рівні сAMP і cGMP, у свою чергу, регулюють активність сAMP- і cGMP-залежних кіназ, а також інших білків з елементами циклічних нуклеотидних відповідей, які через подальше фосфорилування білків і інші процеси регулюють ключові нейронні функції, такі як синаптична передача, нейронна диференціація і виживаність. Існує 21 ген фосфодіестерази, які можна підрозділити на 11 генних сімейств. Існує десять сімейств аденіліл-циклаз, два гуаніліл-циклаз і одинадцять фосфодіестераз. PDE являє собою клас внутріклітинних ферментів, які регулюють рівні сAMP і cGMP за допомогою гідролізу циклічних нуклеотидів у відповідні нуклеотидмонофосфати. Деякі PDE розкладають сAMP, деякі розкладають cGMP, а деякі розкладають як ті, так і інші. Більшість PDE широко експресовані і вони функціонують в багатьох тканинах, тоді як деякі є більш тканина-специфічними. Фосфодіестераза 10А (PDE10A) є фосфодіестеразою подвійної специфічності, яка може перетворювати як сAMP в АМР, так і cGMP в GMP (Loughney, K. et al. Gene 1999, 234, 109-117; Fujishige, K. et al. Eur. J. Biochem. 1999, 266, 1118-1127; та Soderling, S. et al. Proc. Natl. Acad. Sci. 1999, 96, 7071-7076). PDE10A експресована, головним чином, в нейронах в смугастому тілі, прилеглому ядрі і в нюховому горбику (Kotera, J. et al. Biochem. Biophys. Res. Comm. 1999, 261, 551-557; та Seeger, T.F. et al. Brain Research, 2003, 985, 113-126). Мишача PDE10А є першим ідентифікованим представником сімейства фосфодіестераз PDE10 (Fujishige, K. et al. J. Biol. Chem. 1999, 274, 18438-18445; та Loughney, K. et al. Gene 1999, 234, 109-117), і були ідентифіковані сплайсовані на N-кінці варіанти генів щура і людини (Kotera, J. et al. Biochem. Biophys. Res. Comm. 1999, 261, 551-557; та Fujishige, K. et al. Eur. J. Biochem. 1999, 266, 1118-1127). Існує високий ступінь гомології між видами. Але на відміну від інших PDE сімейств, PDE10A локалізована тільки у ссавців. мРНК для PDE10 високо експресована в чоловічій статевій залозі і в мозку (Fujishige, K. et al. Eur J. Biochem. 1999, 266, 1118-1127; Soderling, S. et al. Proc. Natl. Acad. Sci. 1999, 96, 7071-7076; та Loughney, K. et al. Gene 1999, 234, 109-117). Вказані дослідження показують, що експресія PDE10 в мозку є найвищою в смугастому тілі (хвіст і шкаралупа сочевицеподібного ядра), прилеглому ядрі і нюховому горбику. Пізніше був проведений аналіз конфігурації експресії мРНК PDE10A (Seeger, T.F. et al. Abst. Soc. Neurosci. 2000, 26, 345.10) і білка PDE10A (Menniti, F.S. et al. William Harvey Research Conference 'Phosphodiesterase in Health and Disease', Porto, Portugal, Dec. 5-7, 2001) в мозку гризунів. PDE10A експресується з високими рівнями середніми колючковими нейронами (medium spiny neurons-MSN) хвостових ядер, прилеглих ядер і відповідними нейронами нюхового горбика. Вони утворюють ядро базальної системи нервових вузлів. MSN грають ключову роль в кортико-базальній гангліально-таламо-кортикальній петлі, інтегруючи конвергентний кортикально/таламний вхід і посилаючи цю інтегровану інформацію назад в кортикальний шар. MSN експресує два функціональні класи нейронів: клас D1, експресуючий D1-дофамінові рецептори, і клас D2, експресуючий D2-дофамінові рецептори. Клас D1 нейронів є частиною "прямого" стріарного метаболічного шляху виходу, який вільно функціонує для посилення поведінкових відповідей. Клас D2 нейронів є частиною "непрямого" стріарного шляху виходу, який функціонує для пригнічення поведінкових відповідей, що конкурують з відповідями, яким сприяє "прямий" шлях. Ці конкуруючі провідні шляхи діють подібно до гальма і акселератора в автомобілі. У найпростішому уявленні обмежений рух при хворобі Паркінсона є результатом 1 UA 107817 C2 5 10 15 20 25 30 35 40 45 50 55 60 надактивності "непрямого" шляху, тоді як надмірний рух при таких розладах, як хвороба Хантінгтона, відображає підвищену активність прямого шляху метаболізму. PDE10A-регуляція проведення сигналів сАМР і/або cGMP в дендритному компартменті цих нейронів може бути залучена у фільтрацію кортико/таламного входу в MSN. Крім того, PDE10A може бути залучена в регуляцію вивільнення GABA в чорній речовині (substantia nigra) і середній частині сочевицеподібного ядра (globus pallidus) (Seeger, T.F. et al. Brain Research, 2003, 985, 113-126). Антагонізм дофамінового D2-рецептора чітко встановлений при лікуванні шизофренії. Починаючи з 1950-х років антагонізм дофамінового D2-рецептора був головною основою лікування психозу, і всі ефективні антипсихотичні лікарські засоби протидіють D2-рецепторам. Дія D2, ймовірно, проводиться, головним чином, через нейрони в смугастому тілі, прилеглому ядрі і нюховому горбику, оскільки ці ділянки сприймають найбільш щільні дофамінергічні проекції і мають найбільш сильну експресію D2-рецепторів (Konradi, C. and Heckers, S. Society of Biological Psychiatry, 2001, 50, 729-742). Агонізм дофамінових D2-рецепторів призводить до зниження рівнів сАМР в клітинах, де він експресується через аденілат-циклазне інгібування, і це є компонентом процесу проведення D2-сигналу (Stoof, J.C.; Kebabian J.W. Nature 1981, 294, 366368; та Neve, K.A. et al. Journal of Receptors and Signal Transduction 2004, 24, 165-205). І навпаки, антагонізм D2-рецептора ефективно підвищує рівні сАМР, і цей результат міг би бути імітований інгібуванням сАМР розкладаючих фосфодіестераз. Більшість з 21 фосфодіестеразного гена широко експресована; отже, інгібування, ймовірно, має побічні ефекти. Оскільки PDE10A в даному контексті має бажаний профіль експресії з високою і відповідною специфічною експресією в нейронах в смугастому тілі, прилеглому ядрі і нюховому горбику, то інгібування PDE10A, ймовірно, має ефекти, аналогічні антагонізму D2рецептора, і, отже, має антипсихотичну дію. Хоча інгібування PDE10А, як очікується, частково імітує антагонізм D2-рецептора, можна чекати, що воно має інший профіль. D2-рецептор має, окрім сАМР, і інші компоненти проведення сигналу (Neve, K.A. et al. Journal of Receptors and Signal Transduction 2004, 24, 165205), а тому інтерференція з сАМР через інгібування PDE10A може негативно модулювати, а не безпосередньо пригнічувати проведення дофамінового сигналу через D2-рецептори. Це може знижувати ризик екстрапірамідальних побічних ефектів, які спостерігалися при сильному антагонізмі D2. І навпроти, інгібування PDE10A може мати деякі ефекти, які не спостерігаються при антагонізмі D2-рецептора. PDE10A також експресована в стріарних нейронах, експресуючих D1-рецептор (Seeger, T.F. et al. Brain Research, 2003, 985, 113-126). Оскільки агонізм D1рецептора приводить до стимулювання аденілат-циклази і, як результат, до підвищення рівнів сАМР, то інгібування PDE10A, ймовірно, також має ефекти, які імітують агонізм D1-рецептора. І нарешті, інгібування PDE10A не тільки підвищуватиме рівні сАМР в клітинах, але, як може очікуватися, також підвищуватиме рівні cGMP, оскільки PDE10A є фосфодіестеразою з подвійною специфічністю. сGMP активує ряд цільових білків в клітинах, подібних сАМР, а також взаємодіє з шляхами проведення сАМР сигналу. Висновок: інгібування PDE10A, ймовірно, частково імітує антагонізм D2-рецептора і, отже, має антипсихотичну дію, але його профіль може відрізнятися від профілю, який спостерігається у класичних антагоністів D2-рецептора. Було показано, що папаверин, інгібітор PDE10A, є активним на деяких антипсихотичних моделях. Папаверин підсилював каталептичну дію антагоніста D2-рецептора галоперидолу у щурів, але сам по собі не викликав каталепсії (WO 03/093499). Папаверин знижував підвищену активність щурів, викликану РСР, тоді як зниження амфетамін-індукованої гіперактивності було незначним (WO 03/093499). Ці моделі показують, що інгібування PDE10A має класичний антипсихотичний потенціал, який є очікуваним з теоретичних міркувань. У WO 03/093499 додатково описано застосування селективних інгібіторів PDE10 для лікування асоційованих неврологічних і психічних розладів. Крім того, інгібування PDE10A повертає назад підгострі PCP-індуковані дефіцити уваги в зсувах нервових відповідей у щурів (Rodefer et al. Eur. J. Neurosci. 2005, 4, 1070-1076). Дана модель підтверджує, що інгібування PDE10A може послаблювати когнітивні розлади, пов'язані з шизофренією. Розподіл PDE10A в тканинах показує, що інгібітори PDE10A можуть застосовуватися для підвищення рівнів сАМР і/або cGMP усередині клітин, які експресують фермент PDE10, зокрема нейронів, які включають базальні ганглії, і, отже, інгібітори PDE10A цього винаходу можуть застосовуватися при лікуванні різних асоційованих нейропсихіатричних станів, в яких задіяні базальні ганглії, таких як неврологічні і психічні розлади, шизофренія, біполярний розлад, обсесивно-компульсивний розлад і тому подібне, і можуть мати перевагу завдяки відсутності небажаних побічних ефектів, які асоціюються з терапевтичними лікарськими засобами, що існують на ринку в даний час. Крім того, дані останніх публікацій (WO 2005/120514, WO 2005012485, Cantin et al., 2 UA 107817 C2 5 10 15 20 25 30 35 40 Bioorganic & Medicinal Chemistry Letters 17 (2007) 2869-2873) свідчать про те, що інгібітори PDE10A можуть бути корисними при лікуванні ожиріння та інсулін-незалежного цукрового діабету. Що стосується інгібіторів PDE10A, то в ЕР 1250923 описано застосування селективних інгібіторів PDE10 в цілому і, зокрема, папаверину для лікування деяких неврологічних і психічних розладів. У WO 05/113517 описані стереоспецифічні бензодіазепінові сполуки як інгібітори фосфодіестерази, зокрема 2 і 4 типів, і попередження і лікування патологій, в які залучені розлади центральної та/або периферичної нервової системи. У WO 02/88096 описані похідні бензодіазепіну і їх застосування як інгібіторів фосфодіестерази, зокрема 4 типу, в галузі терапії. У WO 04/41258 описані похідні бензодіазепінону і їх застосування як інгібіторів фосфодіестерази, зокрема 2 типу, в галузі терапії. Піролодигідроізохіноліни і їх похідні описані як інгібітори PDE10 у WO 05/03129 і WO 05/02579. Піперидиніл-заміщені хіназоліни та ізохіноліни, які служать як інгібітори PDE10, описані в WO 05/82883. У WO 06/11040 описані заміщені похідні хіназоліну і ізохіноліну, які служать як інгібітори PDE10. У US 20050182079 описані заміщені тетрагідроізохінолінільні похідні хіназоліну і ізохіноліну, які служать як ефективні інгібітори фосфодіестерази (PDE). Зокрема, в US 20050182079 описані вказані сполуки, які є селективними інгібіторами PDE10. Аналогічно, в US 20060019975 описані піперидинові похідні хіназоліну і ізохіноліну, які служать як ефективні інгібітори фосфодіестерази (PDE). US 20060019975 також стосується сполук, які є селективними інгібіторами PDE10. У WO 06/028957 описані похідні цинноліну як інгібітори фосфодіестерази типу 10 для лікування психічних і неврологічних синдромів. Проте, в наведених вище публікаціях не описані сполуки цього винаходу, які за своєю структурою не відносяться до жодного з відомих інгібіторів PDE10 (Kehler, J. et al. Expert Opin. Ther. Patents 2007, 17, 147-158) та Kehler, J. et al. Expert Opin. Ther. Patents 2009, 19, 1715-1725) і які, як було виявлено авторами цього винаходу, є високоактивними і селективними інгібіторами ферменту PDE10A. Сполуки цього винаходу можуть стати альтернативними сполуками лікарським засобам, що продаються в даний час для лікування нейродегенеративних і/або психічних розладів, які неоднаково ефективні для всіх пацієнтів. Тому все ще існує потреба в альтернативних способах лікування. Суть винаходу Завданням цього винаходу є надання сполук, які є селективними інгібіторами ферменту PDE10A. Додатковим завданням цього винаходу є надання сполук, які мають таку активність і які мають підвищену розчинність, метаболічну стабільність і/або біологічну доступність в порівнянні із сполуками попереднього рівня техніки. Ще одним завданням цього винаходу є надання ефективного лікування, зокрема тривалого лікування, пацієнту, яким є людина, без побічних ефектів, зазвичай пов'язаних з вживаними в даний час терапевтичними засобами для лікування неврологічних і психічних розладів. Інші завдання цього винаходу стануть зрозумілими із цього опису. Відповідно, в одному аспекті цей винахід відноситься до сполук формули I: 45 де HET1 являє собою гетероароматичну групу формули II, що містить від 2 до 4 атомів азоту: 3 UA 107817 C2 5 10 15 20 25 30 35 40 де Y може бути N або CH, Z може бути N або C, і де HET1 може бути необов'язково заміщений за допомогою аж до трьох замісників R7, R8 і R9, індивідуально вибираних з H; С1-C6 алкілу, такого як Me; галогену, такого як хлор і бром; ціано; галоген(С1-C6)алкілу, такого як трифторметил; арилу, такого як феніл; алкокси, такого як метокси, диметокси, етокси, метоксіетокси і етоксиметокси; і С1-C6 гідроксіалкілу, такого як CH2CH2OH, і де * позначає точку приєднання. -L- являє собою сполучну ланку, вибрану з -S-CH2-, -CH2-S-, -CH2-CH2-, -CH=CH- і -С≡С-; R1 вибраний з H; С1-C6 алкілу, такого як метил, етил, 1-пропіл, 2-пропіл, ізобутил; С1-C6 алкіл(C3-C8)циклоалкілу, такого як циклопропілметил; С1-C6 гідроксіалкілу, такого як гідроксіетил; CH2CN; CH2C(О)NH2; С1-C6 арилалкілу, такого як бензил і 4-хлорбензил; і С1-C6 алкілгетероциклоалкілу, такого як тетрагідропіран-4-ілметил і 2-морфолін-4-ілетил; де Q являє собою феніл, необов'язково заміщений 1, 2 або трьома замісниками, або Q являє собою моноциклічну 5-членну або 6-членну гетероароматичну групу, що містить 1 або 2 гетероатоми, переважно Q вибраний із структур нижченаведених формул, де символ "*" позначає місце приєднання: де R2-R6 кожен незалежно вибраний з H; С1-C6 алкокси, такого як метокси; і галогену, такого як хлор або фтор; і їх таутомерів, і фармацевтично прийнятних солей, і їх поліморфних форм. У окремих варіантах здійснення цього винаходу сполука формули I вибрана з конкретних сполук, розкритих в експериментальній частині даного опису. Винахід також відноситься до сполуки формули I або її фармацевтично прийнятних кислотно-адитивних солей для використання як лікарського засобу. У ще одному аспекті цей винахід відноситься до фармацевтичної композиції, яка містить терапевтично ефективну кількість сполуки формули I і фармацевтично прийнятний носій, розріджувач або ексципієнт. Винахід також відноситься до застосування сполуки формули I або її фармацевтично прийнятної кислотно-адитивної солі для приготування лікарського засобу для лікування нейродегенеративного або психічного розладу. Крім того, в ще одному аспекті цей винахід відноситься до способу лікування суб'єкта, страждаючого нейродегенеративним розладом, який включає введення суб'єктові терапевтично ефективної кількості сполуки формули I. У ще одному аспекті цей винахід відноситься до способу лікування суб'єкта, страждаючого психічним розладом, який включає введення суб'єктові терапевтично ефективної кількості сполуки формули I. У ще одному варіанті здійснення цей винахід відноситься до способу лікування суб'єкта, страждаючого наркотичною залежністю, такою як хронічний алкоголізм, амфетамінова, кокаїнова або опіатна наркоманія. Докладний опис винаходу 4 UA 107817 C2 5 10 15 20 25 30 35 40 Визначення замісників Терміни "гало" і "галоген", коли використовуються в контексті цього винаходу, є взаємозамінними і відносяться до атома фтору, хлору, брому або йоду. Термін "C1-C6 алкіл" відноситься до насиченого вуглеводню з прямим або розгалуженим ланцюгом, що містить від одного до шести атомів вуглецю, включно. Приклади таких груп включають, але не обмежуються тільки ними, метил, етил, 1-пропіл, 2-пропіл, 1-бутил, 2-бутил, 2-метил-2-пропіл, 2-метил-1-бутил і н-гексил. Вираз "C1-C6 гідроксіалкіл" відноситься до C1-C6 алкільної групи, яку визначено вище, яка заміщена однією гідроксильною групою. Термін "галоген(C1-C6)алкіл" відноситься до C1-C6 алкільної групи, яку визначено вище, яка заміщена, аж до трьох, атомами галогену, наприклад, до трифторметилу. Вираз "C1-C6 алкокси" відноситься до насиченої алкоксигрупи з прямим або розгалуженим ланцюгом, що містить від одного до шести атомів вуглецю, включно, з відкритою валентністю на кисні. Приклади таких груп включають, але не обмежуються тільки ними, метокси, етокси, нбутокси, 2-метилпентокси і н-гексилокси. Термін "С3-С8 циклоалкіл" зазвичай відноситься до циклопропілу, циклобутилу, циклопентилу, циклогексилу, циклогептилу або циклооктилу. Вираз "C 1-C6 алкіл(С3С8)циклоалкіл" відноситься до С3-С8 циклоалкілу, який визначено вище, який заміщений C 1-C6 алкілом з прямим або розгалуженим ланцюгом. Приклади таких груп включають, але не обмежуються тільки ним, циклопропілметил. Термін "гетероциклоалкіл" відноситься до чотири - восьмичленного кільця, що містить атоми вуглецю і, аж до трьох, атоми N, O або S, за умови, що чотири - восьмичленне кільце не містить суміжних атомів O або суміжних атомів S. Відкрита валентність знаходиться на гетероатомі або на атомі вуглецю. Приклади таких груп включають, але не обмежуються тільки ними, азетидиніл, оксетаніл, піперазиніл, морфолініл, тіоморфолініл і [1,4]діазепаніл. Термін "гідроксигетероциклоалкіл" відноситься до гетероциклоалкілу, який визначено вище, який заміщений однією гідроксильною групою. Термін "C1-C6 алкілгетероциклоалкіл" відноситься до гетероциклоалкільної групи, яку визначено вище, яка заміщена C1-C6 алкільною групою. Приклади таких груп включають, але не обмежуються тільки ними, тетрагідропіран-4-ілметил і 2-морфолін-4-ілетил. Термін "арил" відноситься до фенільного кільця, необов'язково заміщеного галогеном, C 1-C6 алкілом, C1-C6 алкокси або галоген(C1-C6)алкілом, які визначено вище. Приклади таких груп включають, але не обмежуються тільки ними, феніл і 4-хлорфеніл. Термін "C1-C6арилалкіл" відноситься до арилу, який визначено вище, який заміщений C 1-C6 алкілом з прямим або розгалуженим ланцюгом. Приклади таких груп включають, але не обмежуються тільки ними, бензил і 4-хлорбензил. Додатково, цей винахід також відноситься до певних варіантів здійснення цього винаходу, які описані нижче. У одному варіанті здійснення винаходу група HET1 являє собою гетероароматичну групу формули II, що містить 2 атоми азоту. У іншому варіанті здійснення винаходу HET1 являє собою гетероароматичну групу формули II, що містить 3 атоми азоту. У ще одному варіанті здійснення винаходу HET1 являє собою гетероароматичну групу формули II, що містить 4 атоми азоту. Група HET1 переважно вибрана з представлених нижче гетероароматичних груп, де "*" означає точку приєднання: 45 5 UA 107817 C2 5 10 У додатковому варіанті здійснення винаходу один або декілька з атомів водню сполуки формули I заміщені дейтерієм. Зокрема, водень заміщений дейтерієм, коли R7-R9 є метилом або метокси. У окремих варіантах здійснення винаходу сполука формули I вибрана з перелічених нижче сполук у формі вільної основи, одного або декількох таутомерів або фармацевтично прийнятної солі. У таблиці 1 наведений перелік сполук цього винаходу і відповідні значення IC 50, визначені згідно з методиками, описаними в розділі "Дослідження інгібування PDE10A". Кожна з вказаних сполук складає окремий варіант здійснення цього винаходу. Слід розуміти, що різні аспекти, варіанти здійснення, реалізації і відмітні ознаки винаходу, наведені в даному описі, можуть бути заявлені окремо або в будь-якій комбінації, як показано в наведених нижче прикладах, які не обмежують обсяг цього винаходу. Таблиця 1 Сполуки цього винаходу і значення IC50 Сполука 8-Метокси-5-метил-2-[2-(2-феніл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5a]піридин 8-Метокси-5-метил-2-[2-(1-метил-2-феніл-1H-імідазол-4-іл)етил][1,2,4]триазоло[1,5-a]піридин 8-Етил-5-метил-2-[2-(1-метил-2-феніл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5a]піридин 5,8-Диметил-2-[2-(2-феніл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піразин 5,8-Диметил-2-[2-(1-метил-2-феніл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5a]піразин 8-Метокси-5-метил-2-[2-(1-метил-2-тіофен-2-іл-1H-імідазол-4-іл)етил][1,2,4]триазоло[1,5-a]піридин 5,8-Диметил-2-[2-(1-метил-2-тіофен-2-іл-1H-імідазол-4-іл)етил][1,2,4]триазоло[1,5-a]піразин 5,8-Диметил-2-[2-(1-метил-2-тіазол-2-іл-1H-імідазол-4-іл)етил][1,2,4]триазоло[1,5-a]піразин 5,8-Диметил-2-[2-(2-тіазол-5-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5a]піразин 5,8-Диметил-2-[2-(2-тіазол-5-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5a]піридин 5,8-Диметил-2-[2-(1-метил-2-тіазол-5-іл-1H-імідазол-4-іл)етил][1,2,4]триазоло[1,5-a]піразин 2-[2-(2-Фуран-2-іл-1-метил-1H-імідазол-4-іл)етил]-5,8-диметил[1,2,4]триазоло[1,5-a]піразин 5,8-Диметил-2-[2-(2-тіазол-4-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5a]піразин 5,8-Диметил-2-[2-(2-тіазол-4-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5a]піридин 2-[2-(2-Фуран-2-іл-1-метил-1H-імідазол-4-іл)етил]-5,8-диметил[1,2,4]триазоло[1,5-a]піридин 5,8-Диметил-2-[2-(2-тіофен-2-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5a]піридин 5,8-Диметил-2-[2-(2-тіазол-2-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5a]піридин 2-[2-(2-Фуран-2-іл-1H-імідазол-4-іл)етил]-5,8-диметил-[1,2,4]триазоло[1,5a]піридин 2-[2-(2-Фуран-3-іл-1H-імідазол-4-іл)етил]-5,8-диметил-[1,2,4]триазоло[1,5a]піридин 5,8-Диметил-2-[2-(2-тіофен-2-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5a]піразин 5,8-Диметил-2-[2-(2-тіазол-2-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5a]піразин 6 IC50 (нМ) 5,9 79 23 4,2 45 9,0 1,0 7,7 6,5 3,1 22 1,1 3,5 3,5 0,75 0,34 1,6 0,62 0,65 0,4 0,63 UA 107817 C2 Сполука 2-[2-(2-Фуран-3-іл-1H-імідазол-4-іл)етил]-5,8-диметил-[1,2,4]триазоло[1,5a]піразин 2-[2-(2-Фуран-2-іл-1H-імідазол-4-іл)етил]-5,8-диметил-[1,2,4]триазоло[1,5a]піразин 5,8-Диметил-2-{2-[1-метил-2-(5-метилфуран-2-іл)-1H-імідазол-4-іл]етил}[1,2,4]триазоло[1,5-a]піразин 5,8-Диметил-2-[2-(1-метил-2-тіазол-4-іл-1H-імідазол-4-іл)етил][1,2,4]триазоло[1,5-a]піразин 2-{2-[2-(4-Фторфеніл)-1H-імідазол-4-іл]етил}-5,8-диметил-[1,2,4]триазоло[1,5a]піразин 5 10 15 20 25 30 35 40 45 IC50 (нМ) 0,27 0,97 3,5 11 12 У особливому варіанті здійснення цього винаходу значення IC50 сполук цього винаходу становить менше 50 нМ, наприклад, знаходиться в інтервалі0,2-20 нМ, конкретно в інтервалі 0,2-10 нМ, наприклад, в інтервалі 0,2-5 нМ або в інтервалі 0,2-1 нМ. Фармацевтично прийнятні солі Цей винахід включає також солі сполук, як правило, фармацевтично прийнятні солі. Такі солі включають фармацевтично прийнятні кислотно-адитивні солі. Кислотно-адитивні солі включають солі неорганічних кислот, а також солі органічних кислот. Конкретні приклади відповідних неорганічних кислот включають хлористоводневу, бромистоводневу, йодистоводневу, фосфорну, сірчану, сульфамінову, азотну і тому подібні кислоти. Конкретні приклади відповідних органічних кислот включають мурашину, оцтову, трихлороцтову, трифтороцтову, пропіонову, бензойну, коричну, лимонну, фумарову, гліколеву, ітаконову, молочну, метансульфонову, малеїнову, яблучну, малонову, мигдалеву, щавлеву, пікринову, піровиноградну, саліцилову, бурштинову, метансульфонову, етансульфонову, винну, аскорбінову, памову, біс-метиленсаліцилову, етандисульфонову, глюконову, цитраконову, аспаргінову, стеаринову, пальмітинову, EDTA, гліколеву, п-амінобензойну, глютамінову, бензолсульфонову, п-толуолсульфонову кислоти, теофіліноцтові кислоти, а також 8галогентеофіліни, наприклад, 8-бромтеофілін, і тому подібне. Додаткові приклади фармацевтично прийнятних неорганічних або органічних кислотно-адитивних солей включають фармацевтично прийнятні солі, перелічені в публікації Berge, S. M. et al., J. Pharm. Sci. 1977, 66, 2, зміст якої включений в даний опис за допомогою посилання. Крім того, сполуки цього винаходу можуть існувати в несольватованих, а також в сольватованих формах з фармацевтично прийнятними розчинниками, такими як вода, етанол і тому подібне. Зазвичай сольватовані форми розглядаються як еквівалент несольватованим формам для цілей цього винаходу. Фармацевтичні композиції Цей винахід додатково відноситься до фармацевтичної композиції, яка містить терапевтично ефективну кількість сполуки формули I і фармацевтично прийнятний носій або розріджувач. Цей винахід також відноситься до фармацевтичної композиції, яка містить терапевтично ефективну кількість однієї з конкретних сполук, розкритих в експериментальній частині даного опису, і фармацевтично прийнятний носій або розріджувач. Сполуки цього винаходу можуть вводитися самі по собі або у поєднанні з фармацевтично прийнятними носіями, розріджувачами або ексципієнтами в разовій або множинних дозах. Фармацевтичні композиції цього винаходу можуть бути виготовлені змішуванням з фармацевтично прийнятними носіями або розріджувачами, а також з будь-якими іншими відомими ад'ювантами і ексципієнтами відповідно до стандартних методик, таких як ті, що th описані, наприклад, в Remington: The Science and Practice of Pharmacy, 19 Edition, Gennaro, Ed., Mack Publishing Co., Easton, PA, 1995. Фармацевтичні композиції можуть бути специфічно розробленими для введення будь-яким відповідним способом введення, таким як пероральний, ректальний, назальний, легеневий, місцевий (включаючи трансбукальний і під'язиковий), трансдермальний, інтрацистернальний, інтраперитонеальний, вагінальний і парентеральний (включаючи підшкірний, внутрішньом'язовий, інтратекальний, внутрівенний і внутрішньошкірний) способи введення. Очевидно, що спосіб введення залежатиме від загального стану і віку суб'єкта, що підлягає лікуванню, природи стану, що підлягає лікуванню, і активного інгредієнта. Фармацевтичні композиції для перорального введення включають тверді лікарські форми, такі як капсули, пігулки, драже, пілюлі, пастили, порошки і гранули. Коли це прийнятно, тоді композиції можуть бути виготовлені з покриттями, такими як ентеросолюбільні покриття, або вони можуть бути виготовлені так, щоб забезпечити контрольоване вивільнення активного 7 UA 107817 C2 5 10 15 20 25 30 35 40 45 50 55 60 інгредієнта, такого як поступове або тривале вивільнення, відповідно до способів, відомих в даній галузі техніки. Рідкі дозовані форми для перорального введення включають розчини, емульсії, суспензії, сиропи і еліксири. Фармацевтичні композиції для парентерального введення включають стерильні водні і неводні розчини, дисперсії, суспензії або емульсії для ін'єкцій, а також стерильні порошки, призначені для отримання стерильних розчинів або дисперсій для ін'єкції перед застосуванням. Інші відповідні форми для введення включають, але не обмежуються тільки ними, супозиторії, спреї, мазі, креми, гелі, лікарські форми для інгаляції, дермальні пластири і імпланти. Типові дозування для перорального введення знаходяться в інтервалі від приблизно 0,001 до приблизно 100 мг/кг маси тіла на день. Типові дозування для перорального введення також знаходяться в інтервалі від приблизно 0,01 до приблизно 50 мг/кг маси тіла на день. Типові дозування для перорального введення також знаходяться в інтервалі від приблизно 0,05 до приблизно 10 мг/кг маси тіла на день. Дозування для перорального введення зазвичай вводяться в одній або декількох дозах, зазвичай від однієї до трьох доз на день. Конкретна доза залежатиме від частоти і способу введення, статі, віку, маси тіла і загального стану суб'єкта, що підлягає лікуванню, природи і тяжкості стану, що підлягає лікуванню, і будь-яких супутніх захворювань, що підлягають лікуванню, а також інших чинників, очевидних для фахівця даної галузі техніки. Препарати також можуть бути представлені в стандартній лікарській формі за методами, відомими фахівцеві даної галузі техніки. Для ілюстрації: типова стандартна лікарська форма для перорального введення може містити від приблизно 0,01 до приблизно 1000 мг, від приблизно 0,05 до приблизно 500 мг або від приблизно 0,5 мг до приблизно 200 мг. Для парентеральних способів введення, таких як внутрівенне, інтратекальне, внутрішньом'язове і аналогічні способи введення, типова доза складає близько половини дози, вживаної для перорального введення. Цей винахід також відноситься до способу приготування фармацевтичної композиції, який включає змішування терапевтично ефективної кількості сполуки формули I і щонайменше одного фармацевтично прийнятного носія або розріджувача. У варіанті здійснення цього винаходу сполукою, використовуваною у вказаному вище способі, є одна з конкретних сполук, розкритих в експериментальній частині даного опису. Сполуки цього винаходу зазвичай використовуються у вигляді вільної основи або у вигляді її фармацевтично прийнятної солі. Одним з таких прикладів є кислотно-адитивна сіль сполуки, що має корисні властивості вільної основи. Коли сполука формули I містить вільну основу, тоді такі солі отримують за стандартним способом шляхом обробки розчину або суспензії вільної основи формули I молярним еквівалентом фармацевтично прийнятної кислоти. Конкретні приклади відповідних органічних і неорганічних кислот визначені вище. Для парентерального введення можуть використовуватися розчини сполук формули I в стерильному водному розчині, водному пропіленгліколі, водному вітаміні Е або кунжутній або арахісовій олії. Такі водні розчини мають бути відповідним чином забуферені, якщо це необхідно, і рідкому розріджувачу спочатку надається ізотонічність за допомогою достатньої кількості сольового розчину або глюкози. Водні розчини особливо підходять для внутрівенного, внутрішньом'язового, підшкірного і інтраперитонеального введення. Сполуки формули I можуть бути легко введені у відоме стерильне водне середовище з використанням стандартних методик, відомих фахівцеві даної галузі. Відповідні фармацевтичні носії включають тверді інертні розріджувачі або наповнювачі, стерильні водні розчини і різні органічні розчинники. Приклади твердих носіїв включають лактозу, каолін, сахарозу, циклодекстрин, тальк, желатин, агар, пектин, гуміарабік, стеарат магнію, стеаринову кислоту і нижчі алкілові етери целюлози. Приклади рідких носіїв включають, але не обмежуються тільки ними, сироп, арахісову олію, оливкову олію, фосфоліпіди, жирні кислоти, аміни жирних кислот, поліоксіетилен і воду. Аналогічно, носій або розріджувач може включати будь-який матеріал для сповільненого вивільнення, відомий в даній галузі, такий як гліцерилмоностеарат або гліцерилдистеарат, сам по собі або в суміші з воском. Фармацевтичні композиції, отримані об'єднанням сполук формули I і фармацевтично прийнятного носія, потім легко вводяться в різні лікарські форми, відповідні для вказаних способів введення. Препарати можуть бути легко отримані в стандартній лікарській формі за способами, відомими в галузі фармації. Препарати цього винаходу, відповідні для перорального введення, можуть бути представлені у вигляді дискретних одиниць, таких як капсули або пігулки, кожна з яких містить обумовлену кількість активного інгредієнта і, необов'язково, відповідний ексципієнт. Крім того, перорально доступні препарати можуть бути представлені у формі порошку або гранул, розчину 8 UA 107817 C2 5 10 15 20 25 30 35 40 45 50 55 60 або суспензії у водній або неводній рідині або емульсії типу "масло-у-воді" або "вода-в-маслі". Якщо для перорального введення використовується твердий носій, тоді препарат може бути представлений у вигляді пігулки, поміщеного в тверду желатинову капсулу порошку або гранул, або він може бути представлений у формі коржика або пастилки. Кількість твердого носія змінюватиметься в широких межах, але знаходитиметься в інтервалі від приблизно 25 мг до приблизно 1 г на одиницю дози. Якщо використовується рідкий носій, то препарат може бути представлений у формі сиропу, емульсії, м'якої желатинової капсули або стерильної рідини для ін'єкції, такої як водна або неводна рідка суспензія або розчин. Фармацевтичні композиції цього винаходу можуть бути отримані за способами, традиційними для даної галузі техніки. Наприклад, пігулки можуть бути отримані змішуванням активного інгредієнта із звичайними ад'ювантами і/або розріджувачами і подальшим пресуванням суміші в стандартній таблетувальній машині, з отриманням пігулок. Приклади ад'ювантів або розріджувачів включають кукурудзяний крохмаль, картопляний крохмаль, тальк, стеарат магнію, желатин, лактозу, смоли і тому подібне. Можуть використовуватися будь-які інші ад'юванти або добавки, зазвичай використовувані для таких цілей, такі як барвники, смакові добавки, консерванти і так далі, за умови, що вони сумісні з активними інгредієнтами. Терапевтично ефективна кількість Як застосовується в цьому описі, термін "терапевтично ефективна кількість" сполуки означає кількість, достатню для лікування, пом'якшення або часткового пригнічення клінічних проявів даного захворювання і його ускладнень при терапевтичній дії, що включає введення вказаної сполуки. Кількість, достатню для забезпечення цього, визначають як "терапевтично ефективна кількість". Ефективні кількості для кожної мети залежать від тяжкості захворювання або пошкодження, а також від маси тіла і загального стану пацієнта. Зрозуміло, що визначення відповідної дози можна проводити із застосуванням рутинних досліджень, шляхом створення матриці значень і перевірки різних точок цієї матриці, що усе входить в звичайні навики навченого лікаря. Як застосовується в цьому описі, терміни "лікування" і "лікувати" означають ведення пацієнта і догляд за ним з метою боротьби із станом, таким як захворювання або порушення. Термін повинен включати повний спектр способів лікування для даного стану, від якого страждає пацієнт, таких як введення активної сполуки для пом'якшення симптомів або ускладнень, для затримки розвитку захворювання, порушення або стану, для пом'якшення або полегшення симптомів і ускладнень і/або для лікування або усунення захворювання, розладу або стану, а також для профілактики стану, де "профілактика" має на увазі ведення пацієнта і догляд за ним з метою боротьби із захворюванням, патологічним станом або розладом, і де вказана профілактика включає введення активної сполуки, для запобігання появі симптомів або ускладнень. При цьому профілактичний (превентивний) і терапевтичний (лікувальний) підходи в лікуванні є двома окремими аспектами цього винаходу. Пацієнт, що підлягає лікуванню, є переважно ссавцем, зокрема людиною. Лікування розладів Як вказано вище, сполуки формули I є інгібіторами ферменту PDE10A і як такі можуть застосовуватися для лікування пов'язаних з ним неврологічних і психічних розладів. Таким чином, цей винахід відноситься до сполуки формули I або її фармацевтично прийнятної кислотно-адитивної солі, а також до фармацевтичної композиції, яка містить таку сполуку, для використання при лікуванні нейродегенеративного розладу, психічного розладу або наркоманії у ссавців, включаючи людей; де нейродегенеративний розлад вибраний з групи, що складається з хвороби Альцгеймера, мультиінфарктної деменції, алкогольної деменції або деменції, пов'язаної з іншими наркотичними засобами, деменції, пов'язаної з внутрічерепними пухлинами або травмою мозку, деменції, пов'язаної з хворобою Хантінгтона або хворобою Паркінсона, або деменції, пов'язаної зі СНІДом; делірію; амнестичного розладу; посттравматичного стресового розладу; вродженого недоумства; розладу навчання, наприклад, розладу навчання читанню, розладу навчання математиці або розладу навчання письмовому виразу думок; синдрому дефіциту уваги/гіперактивності та вікового зниження когнітивних функцій; а психічний розлад вибраний з групи, що складається з шизофренії, наприклад, параноїдного, дезорганізованого, кататонічного, недиференційованого або резидуального типу; шизофреніформного розладу; шизоафективного розладу, наприклад, маревного типу або депресивного типу; маревного розладу; психотичного розладу, викликаного речовиною, наприклад психозу, викликаного алкоголем, амфетаміном, марихуаною, кокаїном, галюциногенами, леткими сполуками, опіоїдами або фенциклідином; розладу особистості параноїдного типу і розладу особистості шизоїдного типу; і де наркотична залежність являє собою хронічний алкоголізм, амфетамінову, кокаїнову або опіатну залежність. 9 UA 107817 C2 5 10 15 20 25 30 35 40 45 50 55 60 Сполуки формули I або їх фармацевтично прийнятні солі можуть використовуватися в комбінації з одним або декількома іншими лікарськими засобами для лікування захворювань або станів, для яких можуть бути корисні сполуки цього винаходу, де комбінації лікарських засобів є безпечнішими або ефективнішими, ніж будь-який один лікарський засіб. Додатково, сполуки цього винаходу можуть використовуватися в комбінації з одним або декількома іншими лікарськими засобами, які лікують, попереджають, контролюють, полегшують або знижують ризик побічних ефектів або токсичність сполук цього винаходу. Отже, такі інші лікарські засоби можуть вводитися традиційним способом і в традиційно використовуваній кількості, одночасно або послідовно із сполуками цього винаходу. Відповідно, фармацевтичні композиції цього винаходу включають фармацевтичні композиції, які містять окрім сполук цього винаходу один або декілька інших активних інгредієнтів. Вказані комбінації можуть вводитися як частина стандартної лікарської форми комбінованого продукту або у вигляді набору або відповідно до схеми лікування, коли один або декілька додаткових лікарських засобів вводиться(яться) в окремих лікарських формах як частина схеми лікування. Цим винаходом пропонується спосіб лікування ссавця, включаючи людину, страждаючу нейродегенеративним розладом, вибраним з розладу пізнавальної здатності або розладу рухової здатності, де спосіб включає введення суб'єктові терапевтично ефективної кількості сполуки формули I. Цим винаходом пропонується також спосіб лікування нейродегенеративного розладу або стану у ссавця, включаючи людину, який включає введення вказаному ссавцеві кількості сполуки формули I, ефективної для інгібування PDE10. Цим винаходом пропонується також спосіб лікування суб'єкта, страждаючого психічним розладом, який включає введення суб'єктові терапевтично ефективної кількості сполуки формули I. Приклади психічних розладів, які можуть лікуватися відповідно до цього винаходу, включають, але не обмежуються тільки ними, шизофренію, наприклад, параноїдного, дезорганізованого, кататонічного, недиференційованого або резидуального типу; шизофреніформний розлад; шизоафективний розлад, наприклад маревного типу або депресивного типу; маревний розлад; психотичний розлад, викликаний речовиною, наприклад психоз, викликаний алкоголем, амфетаміном, марихуаною, кокаїном, галюциногенами, леткими сполуками, опіоїдами або фенциклідином; розлад особистості параноїдного типу; розлад особистості шизоїдного типу; і тривожний розлад вибраний з панічного розладу; агорафобії; специфічної фобії; соціальної фобії; обсесивно-компульсивного розладу; посттравматичного стресового розладу; гострого стресового розладу і генералізованого тривожного розладу. Було виявлено, що сполуки формули I або їх фармацевтично прийнятні солі можуть переважно вводитися в комбінації щонайменше з одним нейролептичним засобом (який може бути типовим або атиповим антипсихотичним засобом) для забезпечення покращеного лікування психічних розладів, таких як шизофренія. Комбінації, застосування і способи лікування цього винаходу можуть також забезпечувати переваги в лікуванні тих пацієнтів, які не відповідають адекватно на інші відомі способи лікування або є резистентними до них. Таким чином, цей винахід відноситься до способу лікування ссавця, страждаючого психічним розладом, таким як шизофренія, який включає введення ссавцеві терапевтично ефективної кількості сполуки формули I, самої по собі або у вигляді комбінованої терапії разом щонайменше з одним нейролептичним засобом. Термін "нейролептичний засіб", коли використовується в даному описі, відноситься до лікарських засобів, що мають вплив на пізнавальну і поведінкову дію антипсихотичних лікарських засобів, які знижують сплутаність свідомості, марення, галюцинації, психомоторне збудження у пацієнтів з психозами. Нейролептичні засоби, відомі як основні транквілізатори і антипсихотичні лікарські засоби, включають також, але не обмежуються тільки ними, типові антипсихотичні лікарські засоби, такі як фентіазини, які у свою чергу підрозділяються на аліфатичні похідні, піперидини і піперазини, тіоксантени (наприклад, цисординол), бутирофенони (наприклад, галоперидол), дибензоксазепіни (наприклад, локсапін), дигідроіндолони (наприклад, моліндон), дифенілбутилпіперидини (наприклад, пімозид), і нетипові антипсихотичні лікарські засоби, такі як бензізоксазоли (наприклад, рисперидон), сертиндол, оланзапін, кветіапін, осанетант і зипрасидон. Особливо переважними нейролептичними засобами для використання в цьому винаході є сертиндол, оланзапін, рисперидон, кветіапін, арипіпразол, галоперидол, клозапін, зипрасидон і осанетант. Цим винаходом забезпечується також спосіб лікування суб'єкта, страждаючого розладом пізнавальної здатності, вказаний спосіб включає введення суб'єктові терапевтично ефективної кількості сполуки формули I. Приклади розладів пізнавальної здатності, які можуть лікуватися за 10 UA 107817 C2 5 10 15 20 25 30 35 40 45 50 55 60 цим винаходом, включають, але не обмежуються тільки ними, хворобу Альцгеймера, мультиінфарктну деменцію, алкогольну деменцію або деменцію, пов'язану з іншими наркотичними речовинами, деменцію, пов'язану з внутрічерепними пухлинами або травмою мозку, деменцію, пов'язану з хворобою Хантінгтона або хворобою Паркінсона, або деменцію, пов'язану зі СНІДом; делірій; амнестичний розлад; посттравматичний стресовий розлад; вроджене недоумство; розлад навчання, наприклад, розлад навчання читанню, розлад навчання математиці або розлад навчання письмовому виразу думок; синдром дефіциту уваги/гіперактивності і вікове зниження когнітивних функцій. Цим винаходом забезпечується також спосіб лікування розладу рухової функції, який включає введення пацієнтові терапевтично ефективної кількості сполуки формули I. Приклади розладів рухової функції, які можуть лікуватися за цим винаходом, включають, але не обмежуються тільки ними, хворобу Хатінгтона і дискінезію, пов'язану з терапевтичним лікуванням агоністами дофаміну. Цим винаходом забезпечується також спосіб лікування розладу рухової функції, вибраного з хвороби Паркінсона і синдрому втомлених ніг, який включає введення суб'єктові терапевтично ефективної кількості сполуки формули I. Цим винаходом забезпечується також спосіб лікування розладу настрою, який включає введення суб'єктові терапевтично ефективної кількості сполуки формули I. Приклади розладів настрою і епізодів аномального настрою, які можуть лікуватися за цим винаходом, включають, але не обмежуються тільки ними, головний депресивний епізод слабкого, середнього і важкого типу, епізод маніакального або змішаного настрою, епізод гіпоманіакального настрою; депресивний епізод з типовими відмітними ознаками; депресивний епізод з меланхолійними відмітними ознаками; депресивний епізод з кататонічними відмітними ознаками; епізод післяродового розладу настрою; постінсультну депресію; глибокий депресивний розлад; дистимічний розлад; незначний депресивний розлад; передменструальний дисфоричний розлад; постпсихотичний депресивний розлад при шизофренії; глибокий депресивний розлад, накладений на психотичний розлад, такий як маревний розлад або шизофренія; біполярний розлад, наприклад, біполярний розлад I типу, біполярний розлад II типу і циклотимічний розлад. Слід розуміти, що розлад настрою є психічним розладом. Цей винахід відноситься також до способу лікування наркотичної залежності, наприклад, хронічного алкоголізму, амфетамінової, кокаїнової або опіатної наркоманії, у ссавця, включаючи людину, де вказаний спосіб включає введення вказаному ссавцеві кількості сполуки формули I, ефективної в лікуванні наркотичної залежності. Цей винахід відноситься також до способу лікування наркотичної залежності, наприклад, хронічного алкоголізму, амфетамінової, кокаїнової або опіатної наркоманії, у ссавця, включаючи людину, де вказаний спосіб включає введення вказаному ссавцеві кількості сполуки формули I, ефективної в інгібуванні PDE10. Термін "наркотична залежність", коли використовується в даному описі, означає патологічну потребу в наркотичному засобі і зазвичай характеризується мотиваційними порушеннями психічної рівноваги, такими як компульсивні спонуки приймати бажаний наркотичний засіб, і епізодами пристрасного бажання споживати наркотичний засіб. Наркотична залежність є достатньо патологічним станом, що широко вивчається. Розлад залежності включає прогрес розладу від гострого вживання наркотичних засобів до розвитку поведінки пошуку наркотичних засобів, сприйнятливості до рецидиву їх прийому і пониженої сповільненої здатності реагувати на природно-корисні стимули. Наприклад, в монографії Diagnostic and Statistical Manual of Mental Disorders, Fourth Edition (DSM-IV) визначено три стадії залежності: захоплення/антиципація, пияцтво/інтоксикація і абстиненція/негативна емоційна реакція. Ці стадії характеризуються, відповідно, повсюдною постійною сильною потребою вживання і заклопотаністю в отриманні речовини; використанням більшої кількості речовини, ніж це необхідно для відчуття ефектів інтоксикації; і відчуття симптомів толерантності і абстиненції, а також зниження мотивації до нормальної життєдіяльності. Цим винаходом додатково забезпечується спосіб лікування розладу, який включає симптом дефіциту уваги і/або пізнавальної здатності, у ссавця, включаючи людину, де вказаний спосіб включає введення вказаному ссавцеві кількості сполуки формули I, ефективної в лікуванні вказаного розладу. Іншими розладами, які можуть бути піддані лікуванню за цим винаходом, є обсесивнокомпульсивні розлади, синдром Тауретта та інші тикові розлади. Термін "нейродегенеративний розлад або стан", коли використовується в даному описі і якщо не вказане інше, відноситься до розладу або стану, який викликаний дисфункцією і/або загибеллю нейронів центральної нервової системи. Лікуванню вказаних розладів і станів може сприяти введення засобу, який попереджає дисфункцію або загибель нейронів при ризику таких 11 UA 107817 C2 5 10 15 20 25 30 35 40 45 50 55 60 розладів або станів і/або підвищує функцію пошкоджених або здорових нейронів таким чином, що компенсує втрату функції, викликану дисфункцією або загибеллю нейронів підвищеного ризику. Термін "нейротрофічний засіб", як використовується в даному описі, відноситься до речовини або засобу, який має деякі з вказаних властивостей або всі вказані властивості. Приклади нейродегенеративних розладів і станів, які можуть лікуватися за цим винаходом, включають, але не обмежуються тільки ними, хворобу Паркінсона, хворобу Хантінгтона; деменцію, наприклад, деменцію при хворобі Альцгеймера, мультиінфарктну деменцію, деменцію, пов'язану зі СНІДом, лобно-скроневу деменцію; нейродегенерацію, пов'язану з травмою мозку; нейродегенерацію, пов'язану з інсультом; нейродегенерацію, пов'язану з церебральним інфарктом; нейродегенерацію, викликану гіпоглікемією; нейродегенерацію, пов'язану з епілептичним нападом; нейродегенерацію, пов'язану з отруєнням нейротоксинами; і мультисистемну атрофію. У одному варіанті здійснення цього винаходу в нейродегенеративний розлад або стан залучена нейродегенерація стріарних середніх колючкових нейронів у ссавців, включаючи людину. У додатковому варіанті здійснення цього винаходу нейродегенеративний розлад або стан являє собою хворобу Хантінгтона. У ще одному варіанті здійснення винахід відноситься до способу лікування суб'єкта для зниження вмісту жиру в організмі, для зниження маси тіла або лікування інсулін-незалежного цукрового діабету (NIDDM), метаболічного синдрому або нетолерантності до глюкози, який включає введення суб'єктові, що потребує такого лікування, терапевтично ефективної кількості сполуки формули I. У переважних варіантах здійснення винаходу суб'єктом є людина, яка має надмірну масу або страждає ожирінням, і антагоніст вводиться перорально. У іншому переважному варіанті здійснення винаходу спосіб додатково включає введення суб'єктові другого терапевтичного засобу, переважно лікарського засобу для лікування ожиріння, наприклад, римонабанту, орлістату, сибутраміну, бромокриптину, ефедрину, лептину, псевдоефедрину, пептиду YY3-36 або їх аналогів. Термін "метаболічний синдром", коли використовується в даному описі, відноситься до констеляції станів, які приводять до високого ризику виникнення у людей захворювання коронарної артерії. Такі стани включають діабет 2 типу, ожиріння, високий кров'яний тиск і поганий ліпідний профіль з підвищеним вмістом LDL ("поганого") холестерину, низьким вмістом HDL ("хорошого") холестерину і підвищеним вмістом тригліцеридів. Всі такі стани пов'язані з високими рівнями вмісту інсуліну в крові. Основним порушенням при метаболічному синдромі є інсулінорезистентність в жировій тканині і м'язі. Всі посилання, включаючи публікації, патентні заявки і патенти, що цитуються в даному описі, включені в даний опис за допомогою посилання у повному їх обсязі і в тому ж ступені, неначебто кожна публікація була окремо вказана як введена в опис за допомогою посилання і внесена до опису у повному її обсязі (у максимальному ступені, дозволеному законом). Заголовки і підзаголовки використовуються в даному описі тільки для зручності і не повинні розглядатися як такі, що обмежують цей винахід будь-яким чином. Застосування будь-якого прикладу або всіх прикладів або виразів, що вказують на приклади (включаючи "наприклад" і "такий як"), в цьому описі призначено тільки для повнішого освітлення цього винаходу і не обмежує обсяг винаходу, якщо не вказане інше. Цитування і введення патентних документів виконане тільки для зручності, і не відображує будь-якої оцінки обґрунтованості, патентоспроможності і/або наявності позовної сили вказаних патентних документів. Цей винахід включає всі модифікації і еквіваленти об'єктів, вказаних у формулі винаходу, що додається, наскільки це дозволено законом. Цей винахід, описаний тут, далі проілюстрований наступними необмежувальними прикладами. Експериментальна частина Загальні способи Дані аналізу LC-MS (РХ-МС) отримують з використанням одного з наступних способів. Спосіб А Використовують апарат PE Sciex API 150EX, забезпечений фотоіонізацією при атмосферному тиску, і РХ-систему Shimadzu LC-8A/SLC-10A. Колонка: 4,6 × 30 мм Waters Symmetry C18 з розміром частинок 3,5 мкм; температура колонки: 60 °C; система розчинників: A = вода/трифтороцтова кислота (100:0,05), B = вода/ацетонітрил/трифтороцтова кислота (5:95:0,035); елюювання з лінійним градієнтом: A:B = від 90:10 до 0:100 протягом 2,4 хвилини при витраті потоку 3,3 мл/хв. 12 UA 107817 C2 5 10 15 20 25 30 35 40 Спосіб B Використовують апарат PE Sciex API 300, забезпечений фотоіонізацією при атмосферному тиску, і систему Waters UPLC. Колонка: Acquity UPLC BEH C18 1,7 мкм, 2,1 × 50 мм (Waters); температура колонки: 60 °C; система розчинників: A = вода/трифтороцтова кислота (100:0,05) і B = вода/ацетонітрил/трифтороцтова кислота (5:95:0,035); елюювання з лінійним градієнтом: A:B = від 90:10 до 0:100 протягом 1,0 хвилини при витраті потоку 1,2 мл/хв. Спосіб С Використовують апарат PE Sciex API 150EX, забезпечений фотоіонізацією при атмосферному тиску, і РХ систему Shimadzu LC-8A/SLC-10A. Колонка: 4,6 × 30 мм Waters Symmetry C18 з розміром частинок 3,5 мкм; температура колонки: 60 °C; система розчинників: A = вода/трифтороцтова кислота (99,95:0,05) і B = метанол/трифтороцтова кислота (99,965:0,035); елюювання з лінійним градієнтом: A:B = від 83:17 до 0:100 протягом 2,4 хвилини при витраті потоку 3,0 мл/хв. Очищення з використанням препаративної РХ-МС проводять на апараті PE Sciex API 150EX з хімічною іонізацією при атмосферному тиску. Колонка: 50 × 20 мм YMC ODS-A з розміром частинок 5 мкм; елюювання з лінійним градієнтом: A:B = від 80:20 до 0:100 протягом 7 хвилин при витраті потоку 22,7 мл/хв. Збір фракцій проводять за допомогою МС детектора розділеного потоку. 1 Спектри Н ЯМР записують при 500,13 МГц на апараті Bruker Avance AV500 або при 250,13 МГц на апараті Bruker Avance DPX250. Як внутрішній стандарт використовують ТМС. Значення хімічного зсуву виражають в м.д. (ppm). Для позначення мультиплетності ЯМР-сигналів використовують наступні абревіатури: c означає синглет, д означає дуплет, т означає триплет, кв означає квартет, квін означає квінтет, г означає гептет, дд означає дуплет дуплетів, дт означає дуплетний триплет, дкв означає квартет дуплетів, тт означає триплет триплетів, м означає мультиплет, уш.с означає розширений синглет, уш. означає розширений сигнал. Абревіатури відповідають ACS Styl Guide: "The ACS Styleguide-A manual for authors and editors" Janet S. Dodd, Ed. 1997, ISBN: 0841234620. Основні сполуки: п-Толуолсульфонілгідразид (98 %) був отриманий від фірми Avocado. 2Феніл-1H-імідазол-4-карбальдегід був отриманий від фірми ASDI. Отримання сполук за винаходом Сполуки загальної формули I за винаходом можуть бути отримані так, як показано на нижченаведених схемах реакції. Якщо не вказане інше, в схемах реакції і в наступному обговоренні HET1, R1-R9, -L-, Z і Y є такими ж, як визначено вище. Сполуки формули I, де -L- являє собою -S-CH2-, можуть бути отримані приєднанням нуклеофіла формули V або Va до електрофіла формули VI, де X являє собою групу, що видаляється, наприклад, Cl, Br, I, метансульфоніл, 4-толуолсульфоніл, як показано на схемі 1. При реакції між Va і VI алкілування атома сірки сполуки Va за допомогою сполуки VI і замикання кільця з утворенням сконденсованого біциклічного триазольного кільця відбуваються в однакових реакційних умовах, в процесі, що протікає в одній посудині. 13 UA 107817 C2 5 10 15 20 25 30 35 Схема 1 Цю реакцію зазвичай здійснюють в розчиннику, такому як 1-пропанол, толуол, диметилформамід (DMF (ДМФА)) або ацетонітрил, необов'язково у присутності карбонатної основи, такої як карбонат калію, або основи, що походить від третинного аміну, наприклад, триетиламін або діізопропілетиламін (DIPEA), при температурі в інтервалі від приблизно 0 °C до приблизно 200 °C, необов'язково під тиском в закритій посудині. Інші придатні розчинники включають бензол, хлороформ, діоксан, етилацетат, 2-пропанол і ксилол. Альтернативно, можна використовувати суміші розчинників, таких як суміш толуолу/2-пропанолу. Сполуки формули V є або комерційно доступними, або можуть бути отримані так, як описано в літературі, див., наприклад, публікації: Brown et al. Aust. J Chem. 1978, 31, 397-404; Yutilov et al. Khim. Geter. Soedin. 1988, 799-804; Wilde et al. Bioorg. Med. Chem. Lett. 1995, 5, 167-172; Kidwai et al. J. Korean Chem. Soc. 2005, 49, 288-291. Сполуки формули Va можуть бути отримані так, як описано в міжнародній публікації WO 96/01826 з відповідних 1,2-діамінопіридинів за реакцією з тіокарбонілдіімідазолом у відповідному розчиннику, такому як хлороформ, при відповідній температурі, такій як кімнатна температура або +40 °C. Потрібні 1,2-діамінопіридини легко отримують з відповідних комерційно доступних 2-амінопіридинів шляхом взаємодії з відповідним реагентом N-амінування, таким як О-(мезитилсульфоніл)гідроксиламін, в придатному розчиннику, такому як хлороформ, при відповідній температурі, такій як 0 °C або кімнатна температура, див. міжнародну публікацію WO 96/01826. 2-Галогенметил-4-(арил)-1H-триазоли формули VI можуть бути отримані галогенуванням відповідних (2-арил-1H-імідазол-4-іл)метанолів або (2-гетероарил-1H-імідазол-4-іл)метанолів, використовуючи придатний реагент, наприклад, тіонілхлорид, трихлорид фосфору або трибромід фосфору, необов'язково з використанням відповідного розчинника, такого як дихлорметан, з використанням способів, загальновідомих для хіміків-фахівців в даній галузі. Необхідні (2-арил-1H-імідазол-4-іл)метаноли можуть бути отримані за способами, відомими в даній галузі техніки (див., наприклад, Journal of Medicinal Chemistry 1986, 29(2), 261-267; WO2005014588A1). Необхідні (2-арил-1H-імідазол-4-іл)метаноли або (2-гетероарил-1H-імідазол-4іл)метаноли також легко отримати відновленням альдегідів XV (див. схему 4, наведену нижче) за способами, відомими хімікам-фахівцям в даній галузі техніки, наприклад, взаємодією альдегідів формули XV з придатним відновником, таким як борогідрид натрію, в придатному розчиннику, такому як ТГФ (THF) або метанол. Сполуки формули I, де -L- являє собою -СН2-S-, можуть бути отримані за реакцією приєднання нуклеофіла формули XII до електрофіла формули VIII, як показано на схемі 2. 14 UA 107817 C2 5 10 15 20 25 30 35 40 Схема 2 Цю реакцію зазвичай проводять в розчиннику, такому як 1-пропанол, толуол, диметилформамід (DMF (ДМФА)) або ацетонітрил, необов'язково у присутності карбонатної основи, такої як карбонат калію, або основи, що походить від третинного аміну, наприклад, триетиламін або діізопропілетиламін (DIPEA), при температурі, що знаходиться в діапазоні від приблизно 0 °C до приблизно 200 °C, необов'язково під тиском в закритій посудині. Інші відповідні розчинники включають бензол, хлороформ, діоксан, етилацетат, 2-пропанол і ксилол. Альтернативно, можуть бути використані суміші розчинників, такі як суміш толуолу/2-пропанолу. Деякі електрофільні сполуки формули VIII є комерційно доступними, а багато інших відомо в даній галузі, див., наприклад, JP 59176277. Електрофільна сполука VIII, де Х являє собою групу, що видаляється, наприклад, Cl, Br, I, метансульфоніл, 4-толуолсульфоніл, також може бути отримана перетворенням первинного спирту сполук формули VII в згадану групу, що видаляється, за способами, відомими хімікам-фахівцям в даній галузі. Згадані способи можуть бути вибрані, наприклад, з реакційної взаємодії сполук формули VII з тіонілхлоридом, трихлоридом фосфору, трибромідом фосфору, метансульфонілхлоридом або 4толуолсульфонілхлоридом, необов'язково у присутності відповідного розчинника, такого як дихлорметан або 1,2-дихлоретан, і необов'язково у присутності основи, такої як триетиламін, діізопропілетиламін або піридин. Альтернативно, електрофільні сполуки формули VIII можуть бути отримані реакційною взаємодією комерційно доступних ароматичних амінів формули IX з 1,3-дигалогенацетонами формули XI, наприклад, з 1,3-дихлорацетоном, у відповідному розчиннику, такому як 1,2-диметоксіетан або етанол, при відповідній температурі, такій як кімнатна температура або температура дефлегмації. Деякі електрофіли формули VII є комерційно доступними, а багато інших відомі в даній галузі, див., наприклад, публікації: Tsuchiya, T.; Sashida, H. J. Chem. Soc., Chem. Commun. 1980, 1109-1110; Tsuchiya, T.; Sashida, H; Konoshita, A. Chem. Pharm. Bull. 1983, 31, 4568-4572. Альтернативно, спирти формули VII можуть бути отримані реакційною взаємодією комерційно доступних ароматичних амінів формули IX з відповідним реагентом N-амінування, таким як О(мезитилсульфоніл)гідроксиламін, у відповідному розчиннику, такому як хлороформ, при відповідній температурі, такій як 0 °C або кімнатна температура, див. міжнародну публікацію WO 96/01826, що дає сполуки формули X. Згадані сполуки формули X можуть бути перетворені на сполуки формули VII за реакцією з метилгліколятом з подальшим відновленням метилового естеру до необхідного спирту з використанням відповідного відновлювального агента, такого як алюмогідрид літію, у відповідному розчиннику, такому як діетиловий етер або тетрагідрофуран, з використанням способів, відомих хімікам-фахівцям в даній галузі. Сполуки формули XII можуть бути отримані, як описано в літературі, див., наприклад, Zoete, Vincent et. al. Journal of the Chemical Society, Perkin transactions 1: Organic and Bio-Organic Chemistry 1997, (20), 2983-2988. Сполуки формули I, де R1 не є воднем, можуть бути отримані алкілуванням сполук формули I, де R1 є воднем, за допомогою алкілгалогеніду формули XIII, як показано на схемі 3. 15 UA 107817 C2 5 10 15 20 25 Схема 3 Цю реакцію зазвичай проводять в придатному розчиннику, такому як диметилформамід, диметилaцетамід або ацетонітрил, у присутності придатної основи, такої як карбонатна основа, наприклад, карбонат калію, або основи, що походить від третинного аміну, наприклад, триетиламін або діізопропілетиламін (DIPEA), при температурі, що знаходиться в діапазоні від приблизно 0 °C до приблизно 100 °C. Сполуки формули I, де -L- являє собою -СН=СН- або -СН2-СН2-, можуть бути отримані за допомогою послідовності реакцій, показаної на схемі 4. Схема 4 Детально, сполуки формули I, де -L- являє собою -СН2-СН2-, можуть бути отримані відновленням алкена формули I, де -L- являє собою -СН=СН-, гідрогенізацією з використанням каталізатора на основі перехідного металу, такого як металевий паладій, разом з джерелом водню, таким як газоподібний водень, гідрокарбонат амонію або циклогексадієн. Згадані алкени формули I, де -L- являє собою -СН=СН-, можуть бути отримані за реакцією Віттіга між фосфонієвою сіллю формули XIV і альдегідом формули XV у відповідному розчиннику, такому як тетрагідрофуран, у присутності відповідної основи, такої як 1,8-діазабіцикло[5.4.0]ундец-7-ен. Фосфонієву сіль формули XIV легко отримують реакційною взаємодією сполук формули VIII (див. схему 2 вище) з трифенілфосфіном за способами, відомими хімікам-фахівцям в даній галузі. Альдегіди формули XV легко отримують окисненням спиртів формули VII (див. схему 2 вище) за способами, відомими хімікам-фахівцям в даній галузі, наприклад, реакційною взаємодією спиртів формули VII з відповідним окиснювальним агентом, таким як періодинан Десса-Мартіна, у відповідному розчиннику, такому як дихлорметан або 1,2-дихлоретан. Або альдегіди формули XV легко отримують за способами, описаними в літературі, див., наприклад, Dhainaut, A. et. al. Journal of Medicinal Chemistry, 2000, 43, 2165-2175. Цей винахід, описаний тут, далі проілюстрований наступними необмежувальними 16 UA 107817 C2 прикладами. Отримання проміжних сполук Приклад 1 2-Тіофен-2-іл-1H-імідазол-4-карбальдегід 5 10 15 20 25 30 35 40 При кімнатній температурі (rt) додавали 1,3-дигідрокси-2-пропанон (11,08 г, 123,0 ммоль) до перемішуваного розчину 2-тіофенкарбоксамідину гідрохлориду в 12,4 М розчині аміаку у воді (200 мл). Розчин нагрівали протягом 1 години при температурі дефлегмації. Розчин охолоджували до кімнатної температури і екстрагували за допомогою EtOAc (2 × 300 мл) і ТГФ (300 мл). Об'єднані органічні фази промивали насиченим сольовим розчином (150 мл), сушили (Na2SO4) і упарювали у вакуумі, щоб отримати 6,4 г неочищеного спирту, який очищали хроматографією на силікагелі (елюент: 10 % MeOH в EtOAc). Вихід: 2,00 г спирту, (2-тіофен-2-іл1H-імідазол-4-іл)метанолу. ТШХ (TLC): Rf приблизно 0,1 в EtOAc. Періодинан Десс-Мартіна (4,71 г, 11,1 ммоль) додавали до перемішуваної суспензії (2тіофен-2-іл-1H-імідазол-4-іл)метанолу (2,00 г, 11,1 ммоль), розчиненого в метиленхлориді (111 мл), при кімнатній температурі в атмосфері Ar. Суміш темніла, і її перемішували при кімнатній температурі протягом ночі. Додавали ще дихлорметан (DCM (ДХМ)) (100 мл) і насичений розчин NaHCO3 (100 мл) і фази розділяли після фільтрування для видалення деяких твердих частинок. Органічний шар наносили на силікагель і очищали хроматографією на силікагелі (елюент: 0-100 % EtOAc в н-гептані). Вихід: 0,57 г сполуки, вказаної в заголовку, у вигляді + червоної твердої речовини. РХ/МС: m/z=178,6 (MH ), tR=0,31 хв., спосіб C. Приклад 2 1-Метил-2-тіазол-2-іл-1H-імідазол-4-карбальдегід Використовували модифікацію способу, описаного в публікації Baldwin et al. J. Med. Chem. 1975, 895 (стадію алкілування здійснювали перед відновленням за допомогою DIBAL-H). При кімнатній температурі додавали 1,1-дибромтрифторацетон (26,24 г, 97,22 ммоль) до перемішуваного розчину ацетату натрію (16,0 г, 194 ммоль) у воді (90 мл). Розчин кип'ятили із зворотним холодильником протягом 30 хвилин і потім охолоджували до кімнатної температури. Охолоджений розчин додавали до перемішуваного розчину 2-формілтіазолу (10,00 г, 88,39 ммоль) в метанолі (400 мл) і 12,4 М розчину аміаку у воді (100 мл). Розчин перемішували, підтримуючи кімнатну температуру. Розчин упарювали, використовуючи роторний випарник, до 190 мл і додавали воду (100 мл). Розчин витримували при 4 °C протягом 30 хвилин і одержану оранжеву тверду речовину відфільтровували. Оранжеву тверду речовину акуратно нагрівали у воді (приблизно 100 мл) протягом 5 хвилин (не доводячи до повного розчинення). Колір мінявся до світло-коричневого. Тверду речовину відфільтровували і сушили у вакуумі, отримуючи 6,50 г 1 проміжного 2-(4-трифторметил-1H-імідазол-2-іл)тіазолу. H-ЯМР (ДМСО-d6) аналогічний опублікованому спектру ЯМР (J. Med Chem (2000) 2165). 2-(4-Трифторметил-1H-імідазол-2-іл)тіазол (6,25 г, 28,5 ммоль) розчиняли в метанолі (300 мл) і додавали 12,4 М розчин аміаку у воді (40 мл) і воду (180 мл). Розчин нагрівали при 60 °C 17 UA 107817 C2 5 10 15 20 25 протягом ночі. Додавали ще 12 М розчин аміаку у воді (40 мл) і розчин нагрівали при 70 °C протягом 5 годин. Реакційну суміш упарювали в роторному випарнику до меншого об'єму. Випадав жовтий твердий осад. Зберігали при 4 °C протягом 2 годин. Жовтий порошок відфільтровували і сушили у вакуумі. Вихід 2-тіазол-2-іл-1H-імідазол-4-карбонітрилу складав 5,54 г неочищеної речовини. Метилйодид (4,06 г, 28,6 ммоль), розчинений в ДМФА (DMF) (8 мл), по краплях додавали до перемішуваного розчину 2-тіазол-2-іл-1H-імідазол-4-карбонітрилу (5,31 г, 30,1 ммоль) і карбонату калію (4,58 г, 33,1 ммоль), розчинених в N, N-диметилформаміді (50 мл). Суміш перемішували при 60 °C протягом 1 години в атмосфері Ar. Більшу частину DMF (ДМФА) видаляли у вакуумі і залишок розподіляли між EtOAc (150 мл) і насиченим сольовим розчином (50 мл). Органічну фазу промивали додатковою кількістю насиченого сольового розчину і сушили (МgSO4). Розчин упарювали, використовуючи роторний випарник, і неочищений продукт очищали хроматографією на силікагелі (елюент: 20-50 % EtOAc в н-гептані). Вихід: 0,982 г жовтої твердої речовини, 1-метил-2-тіазол-2-іл-1H-імідазол-4-карбонітрилу. H-ЯМР: (ДМСО-d6) δ 8,35 (с, 1H), 8,03 (д, 1H), 7,92 (д, 1H), 4,10 (с, 3H). Додавали 1,00 М розчин діізобутилалюмінійгідриду в толуолі (7,73 мл) до перемішуваного розчину 1-метил-2-тіазол-2-іл-1H-імідазол-4-карбонітрилу (0,980 г, 5,15 ммоль), розчиненого в сухому тетрагідрофурані (10 мл), при -78 °C в атмосфері Ar. Температуру повільно (протягом приблизно 1 години) піднімали до -40 °C. Охолоджувальну баню видаляли і суміш гасили, додаючи MeOH (2,6 мл). Суміш упарювали на роторному випарнику і неочищений продукт хроматографували, використовуючи силікагель (елюент: 0-30 % MeOH в EtOAc), щоб отримати 0,321 г забрудненої домішками речовини. Речовину повторно очищали хроматографією на силікагелі (використовуючи EtOAc як елюент). Вихід: 140 мг сполуки, вказаної в заголовку, у вигляді жовтої твердої речовини. H-ЯМР (ДМСО-d6): δ 9,76 (с, 1H), 8,28 (с, 1H) 8,04 (д, 1H), 7,90 + (д, 1H), 4,12 (с, 3H). РХ/МС: m/z=193,8 (MH ), tR=0,36 хв., спосіб C. Приклад 3 2-Тіазол-5-іл-1H-імідазол-4-карбальдегід 30 Використовували спосіб, описаний в Baldwin et al. J. Med. Chem. 1975, 895. Аналогічно отримують нижченаведені проміжні сполуки: 2-фуран-2-іл-1H-імідазол-4-карбальдегід: ; 35 2-ізотіазол-5-іл-1H-імідазол-4-карбальдегід: ; 40 2-оксазол-2-іл-1H-імідазол-4-карбальдегід: 18 UA 107817 C2 ; 2-ізоксазол-5-іл-1H-імідазол-4-карбальдегід: ; 5 2-оксазол-5-іл-1H-імідазол-4-карбальдегід: ; 10 2-тіазол-4-іл-1H-імідазол-4-карбальдегід: ; 15 2-оксазол-4-іл-1H-імідазол-4-карбальдегід: ; 2-ізоксазол-3-іл-1H-імідазол-4-карбальдегід: 20 ; 2-ізотіазол-3-іл-1H-імідазол-4-карбальдегід: ; 25 2-фуран-3-іл-1H-імідазол-4-карбальдегід: 19 UA 107817 C2 . Приклад 4 1-Метил-2-тіофен-2-іл-1H-імідазол-4-карбальдегід 5 10 15 20 25 30 При кімнатній температурі метилйодид (477 мг, 3,36 ммоль), розчинений в ДМФА (0,5 мл), по краплях додавали до перемішуваного розчину 2-тіофен-2-іл-1H-імідазол-4-карбальдегіду (0,57 г, 3,2 ммоль) і карбонату калію (0,486 г, 3,52 ммоль) в сухому N, N-диметилформаміді (6 мл). Розчин перемішували при 70 °C протягом 3 годин. Більшу частину ДМФА випаровували, а залишок розподіляли між EtOAc (50 мл) і насиченим сольовим розчином (25 мл). Фази розділяли, і органічну фазу сушили (Na2SО4), і розчинник випаровували. Неочищений продукт очищали хроматографією на силікагелі (елюент: 50-100 % EtOAc в н-гептані). Вихід: 211 мг сполуки, вказаної в заголовку, у вигляді оливи. H-ЯМР (ДМСО-d6): δ 9,71 (с, 1H), 7,80 (с, 1H) + 7,54 (м, 2H), 7,17 (м, 1H), 4,14 (с, 3H). РХ/МС: m/z=192,9 (MH ), tR=0,34 хв., спосіб C. (211 мг ізомеру (3-метил-2-тіофен-2-іл-3H-імідазол-4-карбальдегіду), що швидко вимивається, відокремлювали і відкидали). Приклад 5 2-Хлорметил-5,7-диметил-[1,2,4]триазоло[1,5-a]піримідин До розчину 4,6-диметилпіримідин-2-іламіну (25 г, 200 ммоль) в 400 мл CH2Cl2 при 0 °C по краплях додавали розчин гідроксиламін-2,4,6-триметилбензолсульфонату (105 г, 488 ммоль) в 300 мл CH2Cl2 і суміш перемішували при 0 °C протягом 1 години і фільтрували. Зібрану тверду речовину промивали CH2Cl2 (100 мл), щоб отримати 1-аміно-4,6-диметил-1H-піримідин-2іліденамонію 2,4,6-триметилбензолсульфонат (40 г, вихід 62 %). Суміш 1-аміно-4,6-диметил-1H-піримідин-2-іліденамонію 2,4,6-триметилбензолсульфонату (40 г, 0,1 моль) і NaOH (10 г, 0,2 моль) в 500 мл EtOH перемішували при 50-60 °C протягом 1 20 UA 107817 C2 5 10 15 20 25 30 35 години. Після додавання метилового естеру хлороцтової кислоти (16,6 г, 0,15 моль) отриману суміш перемішували при температурі дефлегмації протягом 4 годин. Після концентрації при зниженому тиску залишок розбавляли водою (1000 мл) і екстрагували за допомогою CH 2Cl2 (300 мл х 3). Об'єднані органічні шари промивали насиченим сольовим розчином (200 мл), сушили над Na2SO4, фільтрували і концентрували у вакуумі. Залишок очищали колоночною хроматографією на силікагелі (сумішшю петролейний ефір/EtOAc=2/1), отримуючи 2 г 21 хлорметил-5,7-диметил-[1,2,4]триазоло[1,5-a]піримідину з виходом 9 %. H-ЯМР (300 MГц, + ДМСО-d6): δ 8,55 (с, 1H), 6,25 (с, 2H), 4,05 (с, 3H), 3,95 (с, 3H). РХ/МС (MH ): m/z=196,9, tR=0,52 хв., спосіб A. Нижченаведені проміжні сполуки одержують аналогічним чином. 7-Хлор-2-хлорметил-5,8-диметил-[1,2,4]триазоло[1,5-c]піримідин одержують з 6-хлор-2,5диметилпіримідин-4-іламіну, отриманого, як описано в Henze et al. J. Org. Chem 1952, 17, 1320+ 1327. Вихід 3,2 %; РХ/МС: m/z=231,5 (MH ), tR=1,13 хв., спосіб С. 2-Хлорметил-5,8-диметил-[1,2,4]триазоло[1,5-a]піразин одержують з 2-аміно-3,61 диметилпіразину. Вихід 60 %, H-ЯМР (500 MГц, CDCl3): δ 7,91 (с, 1H), 4,87 (с, 2H), 2,91 (с, 3H), + 2,74 (с, 3H). РХ/МС: m/z=196,9 (MH ), tR=0,64 хв., спосіб A. 2-Хлорметил-5,8-диметил-[1,2,4]триазоло[1,5-a]піридин одержують з 6-хлор-5-етил-2+ метилпіримідин-4-іламіну. Вихід 21 %, РХ/МС: m/z=245,0 (MH ), tR=0,72 хв., спосіб A. 2-Хлорметил-8-метокси-5-метил-[1,2,4]триазоло[1,5-a]піридин одержують з 3-метокси-61 метилпіридин-2-іламіну. Вихід 64 %, H-ЯМР (500 MГц, ДМСО-d6): δ 7,11-7,08 (д, 1H), 7,01-6,98 (д, 1H), 4,93 (с, 2H), 3,98 (с, 3H), 2,61 (с, 3H). 2-Хлорметил-8-метокси-5-метил-[1,2,4]триазоло[1,5-a]піридин одержують з 2-аміно-6+ метилпіридину; РХ/МС: m/z=181,8 (MH ), tR=0,64 хв., спосіб A. 2-Хлорметил-8-метил-[1,2,4]триазоло[1,5-a]піридин одержують з 2-аміно-3-метилпіридину. 2-Хлорметил-8-метокси-[1,2,4]триазоло[1,5-a]піридин одержують з 2-аміно-3+ метоксипіридину; РХ/МС: m/z=197,8 (MH ), tR=0,40 хв., спосіб B. 2-Хлорметил-8-етил-5-метил-[1,2,4]триазоло[1,5-a]піридин одержують з 2-аміно-3-етил-6+ метилпіридину; РХ/МС: m/z=209,8 (MH ), tR=0,60 хв., спосіб B. Нижченаведені сполуки є відомими в даній галузі техніки: 2-хлорметил-1-феніл-1H-бензімідазол (JP 59176277); 1-метил-1,3-дигідробензімідазол-2-тіон (Wilde et al. Bioorg. Med. Chem. Lett. 1995, 5, 167172); 1-феніл-1,3-дигідробензімідазол-2-тіон (Kidwai et al. J. Korean Chem. Soc. 2005, 49, 288-291); [1,2,4]триазоло[1,5-a]піримідин-2-тіон (Brown et al. Aust. J. Chem. 1978, 31, 397-404); 1,3-дигідроімідазо[4,5-b]піридин-2-тіон (Yutilov et al. Khim. Geter. Soedin. 1988, 799-804); піразоло[1,5-a]піридин-2-ілметанол (Tsuchiya, Т.; Sashida, H. J. Chem. Soc, Chem. Commun. 1980, 1109-1110; Tsuchiya, Т.; Sashida, H; Konoshita, A. Chem. Pharm. Bull. 1983, 31, 4568-4572). Приклад 6 (5,8-Диметил-[1,2,4]триазоло[1,5-a]піразин-2-ілметил)трифенілфосфонійхлорид 40 45 Розчин 2-хлорметил-5,8-диметил-[1,2,4]триазоло[1,5-a]піразину (1,351 г, 6,87 ммоль) і трифенілфосфіну (1,80 г, 6,87 ммоль) в ацетонітрилі (150 мл) нагрівали протягом 12 годин при температурі дефлегмації. Розчинники видаляли у вакуумі і залишок суспендували в етері, фільтрували і сушили, отримуючи (5,8-диметил-[1,2,4]триазоло[1,5-a]піразин-2ілметил)трифенілфосфонійхлорид у вигляді не зовсім білої твердої речовини (2,412 г, 74,9 %). + РХ/МС: m/z=423,2 ([M-Cl] ), tR=0,86 хв., спосіб A. Нижченаведені проміжні сполуки одержують аналогічним чином. 50 21 UA 107817 C2 5 10 15 (5,8-Диметил-[1,2,4]триазоло[1,5-a]піридин-2-ілметил)трифенілфосфонійхлорид одержують + з 2-хлорметил-5,8-диметил-[1,2,4]триазоло[1,5-a]піридину; РХ/МС: m/z=422,2 (MH ), tR=1,02 хв., спосіб A; (8-Метокси-5-метил-[1,2,4]триазоло[1,5-a]піридин-2-ілметил)трифенілфосфонійхлорид одержують з 2-хлорметил-8-метокси-5-метил-[1,2,4]триазоло[1,5-a]піридину; РХ/МС: m/z=438,4 + (MH ), tR=0,96 хв., спосіб A; (5-Метил-[1,2,4]триазоло[1,5-a]піридин-2-ілметил)трифенілфосфонійхлорид одержують з 2+ хлорметил-5-метил-[1,2,4]триазоло[1,5-a]піридину; РХ/МС: m/z=408,4 (MH ), tR=0,88 хв., спосіб A; 20 (8-Метил-[1,2,4]триазоло[1,5-a]піридин-2-ілметил)трифенілфосфонійхлорид одержують з 2+ хлорметил-8-метил-[1,2,4]триазоло[1,5-a]піридину; РХ/МС: m/z=408,2 (MH ), tR=0,59 хв., спосіб B; 25 (5,7-Диметил-[1,2,4]триазоло[1,5-a]піримідин-2-ілметил)трифенілфосфонійхлорид одержують з 2-хлорметил-5,7-диметил-[1,2,4]триазоло[1,5-a]піримідину; РХ/МС: m/z=423,3 + (MH ), tR=0,85 хв., спосіб A; 30 22 UA 107817 C2 5 10 (8-Метокси-[1,2,4]триазоло[1,5-a]піридин-2-ілметил)трифенілфосфонійхлорид одержують з + 2-хлорметил-8-метокси-[1,2,4]триазоло[1,5-a]піридину, РХ/МС: m/z=423,9 (MH ), tR=0,55 хв., спосіб В; (8-Етил-5-метил-[1,2,4]триазоло[1,5-a]піридин-2-ілметил)трифенілфосфонійхлорид одержують з 2-хлорметил-8-етил-5-метил-[1,2,4]триазоло[1,5-a]піридину; РХ/МС: m/z=423,9 + (MH ), tR=0,55 хв., спосіб B. Отримання сполук за винаходом Приклад 7 5,8-Диметил-2-[2-(2-феніл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піразин 15 20 25 30 35 40 До перемішуваної суспензії (5,8-диметил-[1,2,4]триазоло[1,5-a]піразин-2-ілметил)трифенілфосфонійхлориду (0,27 г, 0,58 ммоль) і 2-феніл-1H-імідазол-4-карбальдегіду (0,100 г, 0,581 ммоль) в сухому ТГФ (8 мл) додавали 1,8-діазабіцикло[5.4.0]ундец-7-ен (0,087 мл, 0,58 ммоль) і цю суміш перемішували при кімнатній температурі в атмосфері аргону протягом ночі. Деяку кількість твердої речовини відфільтровували і розчинник видаляли у вакуумі. Залишки розчиняли в ДХМ і очищали хроматографією на силікагелі (елюент: 0-100 % EtOAc в н-гептані). Вихід: 97 мг проміжної сполуки у вигляді оливи, що є сумішшю цис/транс-ізомерів (53 %). Цю речовину (0,090 г, 0,28 ммоль) розчиняли в ДМФА (8 мл) і додавали птолуолсульфонілгідразид (0,16 г, 0,85 ммоль). Реакційну суміш перемішували при 120 °C протягом 8 годин в атмосфері Ar. Розчин залишали для досягнення кімнатної температури і перемішували протягом ночі. Додавали ще п-толуолсульфонілгідразид (0,08 г), і протягом 6 годин реакційна суміш знаходилася при 120 °C у атмосфері Ar. ДМФА випарювали, а залишок розчиняли в EtOAc (20 мл) і екстрагували насиченим розчином NaHCO 3 (2 × 20 мл). Органічну фазу промивали насиченим сольовим розчином, сушили (MgSO 4) і упарювали, використовуючи роторний випарник. Неочищений продукт очищали хроматографією на силікагелі (елюент: 0100 % EtOAc в н-гептані). Вихід: 40 мг (40 %) продукту у вигляді не зовсім білої твердої + 1 речовини. РХ/МС: m/z=319,2 (MH ), tR=0,63 хв., спосіб E. H-ЯМР (600 MГц, CDCl3): δ 7,90 (м, 3H), 7,43 (м, 2H), 7,35 (м, 1H), 6,96 (с, 1H), 3,40 (м, 2H), 3,22 (м, 2H) 2,98 (с, 3H), 2,75 (с, 3H). Нижченаведені сполуки отримували аналогічним чином: 5,8-диметил-2-[2-(1-метил-2-феніл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піразин (2), + РХ/МС: m/z=333,3 (MH ), tR=0,56 хв., спосіб E; 8-етил-5-метил-2-[2-(1-метил-2-феніл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піридин + (3), РХ/МС: m/z=345,9 (MH ), tR=0,49 хв., спосіб C; 5,8-диметил-2-[2-(1-метил-2-тіофен-2-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піразин 23 UA 107817 C2 + (4), РХ/МС: m/z=338,8 (MH ), tR=0,35 хв., спосіб C. Приклад 8 5,8-Диметил-2-[2-(1-метил-2-тіазол-2-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піразин 5 10 15 20 25 30 35 40 45 50 До перемішуваної суспензії (5,8-диметил-[1,2,4]триазоло[1,5-a]піразин-2-ілметил)трифенілфосфонійхлориду (332 мг, 0,72 ммоль) і 1-метил-2-тіазол-2-іл-1H-імідазол-4карбальдегіду (140 мг, 0,72 ммоль) в сухому ТГФ (18 мл) додавали 1,8-діазабіцикло[5.4.0]ундец7-ен (0,109 мл, 0,72 ммоль) і цю суміш перемішували при кімнатній температурі в атмосфері аргону протягом 2 годин. Розчинник видаляли у вакуумі. Залишки розчиняли в ДХМ і очищали хроматографією на силікагелі (елюент: 0-10 % MeOH в EtOAc). Вихід: 102 мг (42 %) суміші цис/транс проміжних сполук у вигляді білої твердої речовини. Цю речовину (102 мг, 0,30 ммоль) розчиняли в ДХМ (5 мл) і MeOH (5 мл), і додавали 10 % Pd/C (35 мг), і здійснювали реакцію гідрування в шейкері Парра протягом ночі при тиску 1,8 бар. Каталізатор відфільтровували і розчинник видаляли у вакуумі. Неочищений продукт очищали хроматографією на силікагелі (елюент: 0-10 % MeOH в EtOAc). Вихід: 80 мг (78 %) продукту, + вказаного в заголовку, у вигляді не зовсім білої твердої речовини. РХ/МС: m/z=339,9 (MH ), 1 tR=0,35 хв., спосіб C. H-ЯМР (600 MГц, ДМСО-d6): δ 7,95 (с, 1H), 7,91 (д, 1H), 7,73 (д, 1H), 7,15 (с, 1H), 3,97 (с, 3H), 3,21 (м, 2H), 3,04 (м, 2H), 2,75 (с, 3H), 2,65 (с, 3H). Нижченаведені сполуки отримували аналогічним чином: 8-метокси-5-метил-2-[2-(2-феніл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піридин; РХ/МС: + m/z=334,5 (MH ), tR=0,78 хв., спосіб E; 8-метокси-5-метил-2-[2-(1-метил-2-тіофен-2-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5+ a]піридин (7); РХ/МС: m/z=354,4 (MH ), tR=0,41 хв., спосіб C; 8-метокси-5-метил-2-[2-(2-феніл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піридин; РХ/МС: + m/z=334,159 (MH ), tR=0,78 хв., спосіб C; 8-метокси-5-метил-2-[2-(1-метил-2-феніл-1H-імідазол-4-іл) етил-[1,2,4]триазоло[1,5+ a]піридин; РХ/МС: m/z=348,1746 (MH ), tR=0,7 хв., спосіб C; 8-етил-5-метил-2-[2-(1-метил-2-феніл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-а]піридин; + РХ/МС: m/z=346,1953 (MH ), tR=0,49 хв., спосіб C; 5,8-диметил-2-[2-(2-феніл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піразин; РХ/МС: + m/z=319,1593 (MH ), tR=0,63 хв., спосіб C; 5,8-диметил-2-[2-(1-метил-2-феніл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піразин; + РХ/МС: m/z=333,1749 (MH ), tR=0,56 хв., спосіб C; 8-метокси-5-метил-2-[2-(1-метил-2-тіофен-2-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5+ a]піридин; РХ/МС: m/z=354,131 (MH ), tR=0,41 хв., спосіб C; 8-метокси-5-метил-2-[2-(3-метил-2-тіофен-2-іл-3H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5+ a]піридин; РХ/МС: m/z=354,2 (MH ), tR=0,4 хв., спосіб C; 5,8-диметил-2-[2-(1-метил-2-тіофен-2-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піразин; + РХ/МС: m/z=338,8 (MH ), tR=0,35 хв., спосіб C; 5,8-диметил-2-[2-(1-метил-2-тіазол-2-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піразин; + РХ/МС: m/z=339,9 (MH ), tR=0,35 хв., спосіб C; 5,8-диметил-2-[2-(2-тіазол-5-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піразин; РХ/МС: + m/z=326,111 (MH ), tR=0,43 хв., спосіб C; 5,8-диметил-2-[2-(2-тіазол-5-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піридин; РХ/МС: + m/z=325,1157 (MH ), tR=0,76 хв., спосіб C; 5,8-диметил-2-[2-(1-метил-2-тіазол-5-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піразин; + РХ/МС: m/z=340,1266 (MH ), tR=0,45 хв., спосіб C; 2-[2-(2-фуран-2-іл-1-метил-1H-імідазол-4-іл)етил]-5,8-диметил-[1,2,4]триазоло[1,5-a]піразин; + РХ/МС: m/z=323,1542 (MH ), tR=0,36 хв., спосіб C; 5,8-диметил-2-[2-(2-тіазол-4-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піразин; РХ/МС: + m/z=326,111 (MH ), tR=0,33 хв., спосіб C; 5,8-диметил-2-[2-(2-тіазол-4-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піридин; РХ/МС: 24 UA 107817 C2 + 5 10 15 20 25 30 35 40 45 50 m/z=325,1157 (MH ), tR=0,39 хв., спосіб C; 2-[2-(2-фуран-2-іл-1-метил-1H-імідазол-4-іл)етил]-5,8-диметил-[1,2,4]триазоло[1,5-a]піридин; + РХ/МС: m/z=322 (MH ), tR=0,43 хв., спосіб C; 5,8-диметил-2-[2-(2-тіофен-2-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піридин; РХ/МС: + m/z=323,9 (MH ), tR=0,43 хв., спосіб C; 5,8-диметил-2-[2-(2-тіазол-2-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піридин; РХ/МС: + m/z=324,8 (MH ), tR=0,4 хв., спосіб C; 2-[2-(2-фуран-2-іл-1H-імідазол-4-іл)етил]-5,8-диметил-[1,2,4]триазоло[1,5-a]піридин; РХ/МС: + m/z=308,2 (MH ), tR=0,41 хв., спосіб C; 2-[2-(2-фуран-3-іл-1H-імідазол-4-іл)етил]-5,8-диметил-[1,2,4]триазоло[1,5-a]піридин; РХ/МС: + m/z=308,2 (MH ), tR=0,41 хв., спосіб C; 5,8-диметил-2-[2-(2-тіофен-2-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піразин; РХ/МС: + m/z=325,1157 (MH ), tR=0,4 хв., спосіб C; 5,8-диметил-2-[2-(2-тіазол-2-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піразин; РХ/МС: + m/z=326,111 (MH ), tR=0,37 хв., спосіб C; 2-[2-(2-фуран-3-іл-1H-імідазол-4-іл)етил]-5,8-диметил-[1,2,4]триазоло[1,5-a]піразин; РХ/МС: + m/z=309,1386 (MH ), tR=0,38 хв., спосіб C; 2-[2-(2-фуран-2-іл-1H-імідазол-4-іл)етил]-5,8-диметил-[1,2,4]триазоло[1,5-a]піразин; РХ/МС: + m/z=309,1386 (MH ), tR=0,32 хв., спосіб C; 2-[2-(1H-імідазол-4-іл)етил]-5,8-диметил-[1,2,4]триазоло[1,5-a]піразин; РХ/МС: m/z=243,3 + (MH ), tR=0,24 хв., спосіб C; 5,8-диметил-2-{2-[1-метил-2-(5-метилфуран-2-іл)-1H-імідазол-4-іл]етил}-[1,2,4]триазоло[1,5+ a]піразин; РХ/МС: m/z=337,1 (MH ), tR=0,37 хв., спосіб C; 5,8-диметил-2-[2-(1-метил-2-тіазол-4-іл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піразин; + РХ/МС: m/z=340,1266 (MH ), tR=0,61 хв., спосіб C; 2-{2-[2-(4-фторфеніл)-1H-імідазол-4-іл]етил}-5,8-диметил-[1,2,4]триазоло[1,5-a]піразин; + РХ/МС: m/z=337,1 (MH ), tR=0,36 хв., спосіб C. Приклад 9 8-Метокси-5-метил-2-[2-(1-метил-2-феніл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5a]піридин Метилйодид (0,035 мл, 0,57 ммоль) додавали до перемішуваної суспензії 8-метокси-5метил-2-[2-(2-феніл-1H-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-a]піридину (145 мг, 0,435 ммоль) і Cs2CO3 (360 мг, 1,1 ммоль) в 2-бутаноні (10 мл). Суміш нагрівали при 50 °C протягом 7 годин в атмосфері аргону. Суміш охолоджували до кімнатної температури і розчинник випаровували. Неочищений продукт розчиняли в ДХМ і очищали хроматографією на силікагелі (елюент: 0100 % EtOAc в н-гептані, потім замінений на 0-5 % MeOH в EtOAc). Вихід: 31 мг (20 %) сполуки, + вказаної в заголовку, у вигляді не зовсім білої твердої речовини. РХ/МС: m/z=348,2 (MH ), tR=0,70 хв., спосіб E. Фармакологічне тестування Фермент PDE10A Активний фермент PDE10A отримують за декількома способами для використання в біологічних випробуваннях PDE (Loughney, K. et al. Gene 1999, 234, 109-117; Fujishige, K. et al. Eur J Biochem. 1999, 266, 1118-1127; та Soderling, S. et al. Proc. Natl. Acad. Sci. 1999, 96, 70717076). PDE10A може експресуватися у вигляді первинних продуктів трансляції або у вигляді процесованих білків доти, доки вони експресують каталітичний домен. PDE10A може бути отриманий в клітинах різних типів, наприклад в клітинах комах або E. coli. Прикладом способу отримання каталітично активного PDE10A є наступний спосіб: каталітичний домен PDE10A людини (амінокислоти 440-779 з послідовності з номером доступу NP 006652) ампліфікують із загальної РНК мозку людини за допомогою стандартної RT-PCR і клонують в сайти BamH1 і Xho1 вектора pET28a (Novagen). Експресію в E. coli виконують відповідно до стандартних методик. Стисло: плазміди експресії трансформують в штам E. coli BL21 (DE3) і 50 мл культур, 25 UA 107817 C2 5 10 15 20 25 30 35 40 інокульованих клітинами, дають зростати до оптичної щільності OD600, рівній 0,4-0,6 перед експресією білка, яку індукують за допомогою 0,5 мМ IPTG (ізопропіл-тіогалактозид). Після індукції клітини інкубують протягом ночі при кімнатній температурі та потім збирають центрифугуванням. Клітини, що експресують PDE10A, знову суспендують в 12 мл (50 мМ TRISHCl, pH 8,0, 1 мМ MgCl2 та інгібітори протеази). Клітини піддають лізису обробкою ультразвуком і після лізування всіх клітин згідно з методиками Novagen додають TritonX100. PDE10A частково очищають на сефарозі Q і більшу частину активних фракцій об'єднують. Дослідження інгібування PDE10A Дослідження інгібування PDE10A можна проводити відповідно до наступної методики. Дослідження проводять в зразках об'ємом 60 мкл, що містять фіксовану кількість відповідного ферменту PDE (достатню для перетворення 20-25 % циклонуклеотидного субстрату), буфер (50 3 мМ HEPES 7,6; 10 мМ MgCl2; 0,02 % Tween 20), 0,1 мг/мл BSA, 225 пКi H-міченого циклонуклеотидного субстрату, міченого тритієм сАМР до кінцевої концентрації 5 нM та змінні кількості інгібіторів. Реакції ініціюють додаванням циклонуклеотидного субстрату і реакції дають можливість протікати протягом однієї години при кімнатній температурі до припинення шляхом змішування з гранулами SPA (15 мкл, 8 мг/мл) силікату ітрію (Amersham). Гранулам дають осідати протягом однієї години в темряві перед прочитуванням планшетів за допомогою лічильника Wallac 1450 Microbeta. Величину виміряного сигналу перетворюють в активність щодо неінгібованого контролю (100 %), а значення IC50 можуть бути обчислені з використанням Xlfit-розширення в EXCEL. Гіперактивність, індукована фенциклідином (РСР) У дослідженні використовують самців мишей (NMRI, Charles River) з масою тіла 20-25 г. Кожна група мишей, що одержує випробовувану сполуку (5 мг/кг) плюс PCP (2,3 мг/кг), а також паралельні контрольні групи, що одержують ін'єкцією або наповнювач для випробовуваної сполуки плюс РСР, або тільки наповнювач, включає вісім мишей. Об'єм ін'єкції становить 10 мл/кг. Тест проводять в умовах нормального освітлення в кімнаті зі спокійними умовами. Випробовувану сполуку вводять перорально за 60 хвилин до ін'єкції PCP, яку роблять підшкірно. Одразу після ін'єкції РСР мишей поокремо поміщають в спеціально розроблену дослідницьку клітку (20 см х 32 см). Активність кількісно визначають за допомогою 5 × 8 джерел інфрачервоного світла і фотоелементів, розташованих на відстані 4 см. Промені світла проходять крізь клітку на 1,8 см вище за дно клітки. Для реєстрації одиничного пересування необхідний перетин суміжних світлових променів, що запобігає реєстрації руху мишей без пересування. Пересування записують з інтервалами у 5 хвилин протягом періоду в 1 годину. Дію лікарського засобу розраховують за загальною кількістю пересувань, зареєстрованих протягом періоду оцінки поведінки, рівному 1 годині, відповідно до наступної методики. Як початкове значення використовують середню кількість пересувань, викликаних наповнювачем у відсутності PCP. 100-відсотковий ефект PCP, відповідно, обчислюється як загальна кількість мимовільних пересувань за винятком початкового значення. Таким чином, реакцію в групах, що приймають випробовувану сполуку, визначають як обчислену кількість загальних пересувань за винятком початкового значення і виражають у відсотках від аналогічного результату, зафіксованого в паралельній контрольній групі тварин, що одержують РСР. Відсоток реакцій перетворюють у відсоток інгібування. 45 ФОРМУЛА ВИНАХОДУ 1. Сполуки, що мають структуру І R1 Q N HET-1 50 L N ,І де НЕТ1 являє собою гетероароматичну групу формули II, що містить від 2 до 4 атомів азоту: Y Y Y Y Z Z Y * N , II 26 UA 107817 C2 5 10 15 20 25 30 35 40 45 50 55 60 де Y може бути N або СН, Z може бути N або С, і де НЕТ1 необов'язково може бути заміщений за допомогою аж до трьох замісників R2-R4, індивідуально вибраних з водню, С1-С6алкілу; галогену; ціано, галоген(С1-С6)алкілу; арилу, алкокси і С1-С6гідроксіалкілу, і де символ * позначає місце приєднання; Q являє собою феніл, необов'язково заміщений 1-5 замісниками, або моноциклічну 5-членну або 6-членну гетероароматичну групу, що містить 1 або 2 гетероатоми; -L- являє собою сполучну ланку, вибрану з -S-CH2-, -CH2-S-, -CH2-CH2-, -СН=СН- і -С≡С-; R1 вибраний з Н, С1-С6алкілу; С1-С6алкіл(С3-С8)циклоалкілу; С1-С6гідроксіалкілу, CH2CN, CH2C(O)NH2, С1-С6арилалкілу і C1-С6алкілгетероциклоалкілу, та їх таутомери і фармацевтично прийнятні солі, за умови, що сполука не являє собою 2-(5-феніл-1Н-імідазол-2-ілметилсульфаніл)-1Нбензімідазол або 2-(5-феніл-1Н-імідазол-2-ілсульфанілметил)-1Н-бензімідазол. 2. Сполука за п. 1, де НЕТ1 являє собою імідазо[1,2-а]піримідиновий фрагмент. 3. Сполука за п. 1, де НЕТ1 являє собою [1,2,4]триазоло[1,5-а]піридиновий фрагмент. 4. Сполука за п. 1, де НЕТ1 являє собою імідазо[1,2-а]піридиновий фрагмент. 5. Сполука за п. 1, де НЕТ1 являє собою імідазо[4,5-b]піримідиновий фрагмент. 6. Сполука за п. 1, де НЕТ1 являє собою піразоло[1,5-а]піридиновий фрагмент. 7. Сполука за п. 1, де НЕТ1 являє собою [1,2,4]триазоло[1,5-а]піримідиновий фрагмент. 8. Сполука за п. 1, де НЕТ1 являє собою [1,2,4]триазоло[1,5-а]піразиновий фрагмент. 9. Сполука за п. 1, де НЕТ1 являє собою [1,2,4]триазоло[1,5-с]піримідиновий фрагмент. 10. Сполука за п. 1, де Q вибраний з групи, що складається з фенілу, тіофену, фурану, тіазолу, піразолу, піридину, піримідину і піразину. 11. Сполука за будь-яким з пп. 1-10, де R2, R3 і R4 - всі являють собою водень. 12. Сполука за будь-яким з пп. 1-10, де щонайменше один з R2, R3 і R4 являє собою С1-С6алкіл, такий як метил. 13. Сполука за будь-яким з пп. 1-10, де щонайменше один з R2, R3 і R4 являє собою галоген, такий як хлор або бром. 14. Сполука за п. 1, де сполука вибрана з групи, що складається з: 5,8-диметил-2-[2-(2-феніл-1Н-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-а]піразину; 5,8-диметил-2-[2-(1-метил-2-феніл-1Н-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-а]піразину; 8-етил-5-метил-2-[2-(1-метил-2-феніл-1Н-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-а]піридину; 5,8-диметил-2-[2-(1-метил-2-тіофен-2-іл-1Н-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-а]піразину; 5,8-диметил-2-[2-(1-метил-2-тіазол-2-іл-1Н-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-а]піразину; 8-метокси-5-метил-2-[2-(2-феніл-1Н-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-а]піридину; 8-метокси-5-метил-2-[2-(1-метил-2-тіофен-2-іл-1Н-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5а]піридину і 8-метокси-5-метил-2-[2-(1-метил-2-феніл-1Н-імідазол-4-іл)етил]-[1,2,4]триазоло[1,5-а]піридину, та їх фармацевтично прийнятних солей. 15. Сполука за будь-яким з пп. 1-14 для використання як лікарського засобу. 16. Сполука за будь-яким з пп. 1-14 для використання при лікуванні нейродегенеративного або психічного розладу самої по собі або в комбінації з одним або декількома нейролептичними лікарськими засобами, такими як сертиндол, оланзапін, рисперидон, кветіапін, арипіпразол, галоперидол, клозапін, зипрасидон і осанетант, де нейродегенеративний розлад вибраний з групи, що складається з хвороби Альцгеймера, мультиінфарктної деменції, алкогольної деменції або деменції, пов'язаної з іншими наркотичними засобами, деменції, пов'язаної з внутрішньочерепними пухлинами або травмою мозку, деменції, пов'язаної з хворобою Хантінгтона або хворобою Паркінсона, або деменції, пов'язаної зі СНІДом; делірію; амнестичного розладу; посттравматичного стресового розладу; вродженого недоумства; розладу навчання, наприклад розладу навчання читанню, розладу навчання математиці або розладу навчання письмовому виразу думок; синдрому дефіциту уваги/гіперактивності та вікового зниження когнітивних функцій; а психічний розлад вибраний з групи, що складається з шизофренії, наприклад, параноїдного, дезорганізованого, кататонічного, недиференційованого або резидуального типу; шизофреніформного розладу; шизоафективного розладу, наприклад, маревного типу або депресивного типу; маревного розладу; психотичного розладу, викликаного речовиною, наприклад психозу, викликаного алкоголем, амфетаміном, марихуаною, кокаїном, галюциногенами, леткими сполуками, опіоїдами або фенциклідином; розладу особистості параноїдного типу і розладу особистості шизоїдного типу. 17. Сполука за будь-яким з пп. 1-14 для використання при лікуванні наркотичної залежності у ссавця, включаючи людину, такої як хронічний алкоголізм, амфетамінова наркоманія, кокаїнова наркоманія або опіатна наркоманія. 27 UA 107817 C2 5 10 15 20 25 30 35 40 45 50 18. Сполука за будь-яким з пп. 1-14 для приготування лікарського засобу для використання при лікуванні наркотичної залежності у ссавця, включаючи людину, такої як хронічний алкоголізм, амфетамінова наркоманія, кокаїнова наркоманія або опіатна наркоманія. 19. Сполука за будь-яким з пп. 1-14 для приготування лікарського засобу для використання при лікуванні нейродегенеративного або психічного розладу, де нейродегенеративний розлад вибраний з групи, що складається з хвороби Альцгеймера, мультиінфарктної деменції, алкогольної деменції або деменції, пов'язаної з іншими наркотичними засобами, деменції, пов'язаної з внутрішньочерепними пухлинами або травмою мозку, деменції, пов'язаної з хворобою Хантінгтона або хворобою Паркінсона, або деменції, пов'язаної зі СНІДом; делірію; амнестичного розладу; посттравматичного стресового розладу; вродженого недоумства; розладу навчання, наприклад розладу навчання читанню, розладу навчання математиці або розладу навчання письмовому виразу думок; синдрому дефіциту уваги/гіперактивності та вікового зниження когнітивних функцій; а психічний розлад вибраний з групи, що складається з шизофренії, наприклад, параноїдного, дезорганізованого, кататонічного, недиференційованого або резидуального типу; шизофреніформного розладу; шизоафективного розладу, наприклад, маревного типу або депресивного типу; маревного розладу; психотичного розладу, викликаного речовиною, наприклад психозу, викликаного алкоголем, амфетаміном, марихуаною, кокаїном, галюциногенами, леткими сполуками, опіоїдами або фенциклідином; розладу особистості параноїдного типу і розладу особистості шизоїдного типу. 20. Сполука для приготування лікарського засобу для використання при лікуванні за п. 15, де лікування психічних розладів включає сумісне введення нейролептичного засобу, такого як сертиндол, оланзапін, рисперидон, кветіапін, арипіпразол, галоперидол, клозапін, зипрасидон і осанетант. 21. Спосіб лікування суб'єкта, страждаючого нейродегенеративним або психічним розладом, де нейродегенеративний розлад вибраний з групи, що складається з хвороби Альцгеймера, мультиінфарктної деменції, алкогольної деменції або деменції, пов'язаної з іншими наркотичними засобами, деменції, пов'язаної з внутрішньочерепними пухлинами або травмою мозку, деменції, пов'язаної з хворобою Хантінгтона або хворобою Паркінсона, або деменції, пов'язаної зі СНІДом; делірію; амнестичного розладу; посттравматичного стресового розладу; вродженого недоумства; розладу навчання, наприклад розладу навчання читанню, розладу навчання математиці або розладу навчання письмовому виразу думок; синдрому дефіциту уваги/гіперактивності та вікового зниження когнітивних функцій; а психічний розлад вибраний з групи, що складається з шизофренії, наприклад, параноїдного, дезорганізованого, кататонічного, недиференційованого або резидуального типу; шизофреніформного розладу; шизоафективного розладу, наприклад, маревного типу або депресивного типу; маревного розладу; психотичного розладу, викликаного речовиною, наприклад психозу, викликаного алкоголем, амфетаміном, марихуаною, кокаїном, галюциногенами, леткими сполуками, опіоїдами або фенциклідином; розладу особистості параноїдного типу і розладу особистості шизоїдного типу; де вказаний спосіб включає введення ефективної кількості сполуки за будьяким з пп. 1-14 самої по собі або в комбінації з одним або декількома нейролептичними засобами, такими як сертиндол, оланзапін, рисперидон, кветіапін, арипіпразол, галоперидол, клозапін, зипрасидон і осанетант. 22. Спосіб лікування суб'єкта-ссавця, включаючи людину, що страждає наркотичною залежністю, наприклад хронічним алкоголізмом, амфетаміновою, кокаїновою або опіатною залежністю, який включає введення вказаному суб'єктові сполуки формули І в кількості, ефективній при лікуванні наркотичної залежності. 23. Спосіб лікування суб'єкта-ссавця, включаючи людину, що страждає наркотичною залежністю, наприклад хронічним алкоголізмом, амфетаміновою, кокаїновою або опіатною залежністю, який включає введення вказаному суб'єктові сполуки формули І в кількості, ефективній для інгібування PDE10A. 24. Фармацевтична композиція, яка містить терапевтично ефективну кількість сполуки за будьяким з пп. 1-14 і один або декілька фармацевтично прийнятних носіїв, розріджувачів і ексципієнтів. Комп’ютерна верстка М. Мацело Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 28
ДивитисяДодаткова інформація
Назва патенту англійською2-arylimidazole derivatives as pde10a enzyme inhibitors
Автори англійськоюPuschl, Ask, Nielsen, Jacob, Kehler, Jan, Kilburn, John, Paul, Marigo, Mauro, Langgard, Morten
Автори російськоюПюшл Аск, Нильсен Якоб, Кехлер Ян, Килберн Джон Пол, Мариго Мауро, Ланггор Мортен
МПК / Мітки
МПК: A61P 25/00, C07D 471/04, A61K 31/519, C07D 487/04
Мітки: 2-арилімідазолу, pde10a, похідні, ферменту, інгібітори
Код посилання
<a href="https://ua.patents.su/30-107817-pokhidni-2-arilimidazolu-yak-ingibitori-fermentu-pde10a.html" target="_blank" rel="follow" title="База патентів України">Похідні 2-арилімідазолу як інгібітори ферменту pde10a</a>
Попередній патент: Спосіб хонінгування та інструмент для його реалізації
Наступний патент: Похідні аміноалкілпіримідину як антагоністи н4-гістамінових рецепторів
Випадковий патент: Пристрій для очистки трубопроводу












