5-[(3,3,3-трифторо-2-гідроксі-1-арилпропіл)-аміно]-1н-хінолін-2-они, спосіб їх одержання і їх застосування як протизапальних засобів
Номер патенту: 100251
Опубліковано: 10.12.2012
Автори: Хассфельд Йорма, Ревінкель Хартмут, Май Еккехард, Цолльнер Томас, Бергер Маркус, Шьокке Хайке
Формула / Реферат
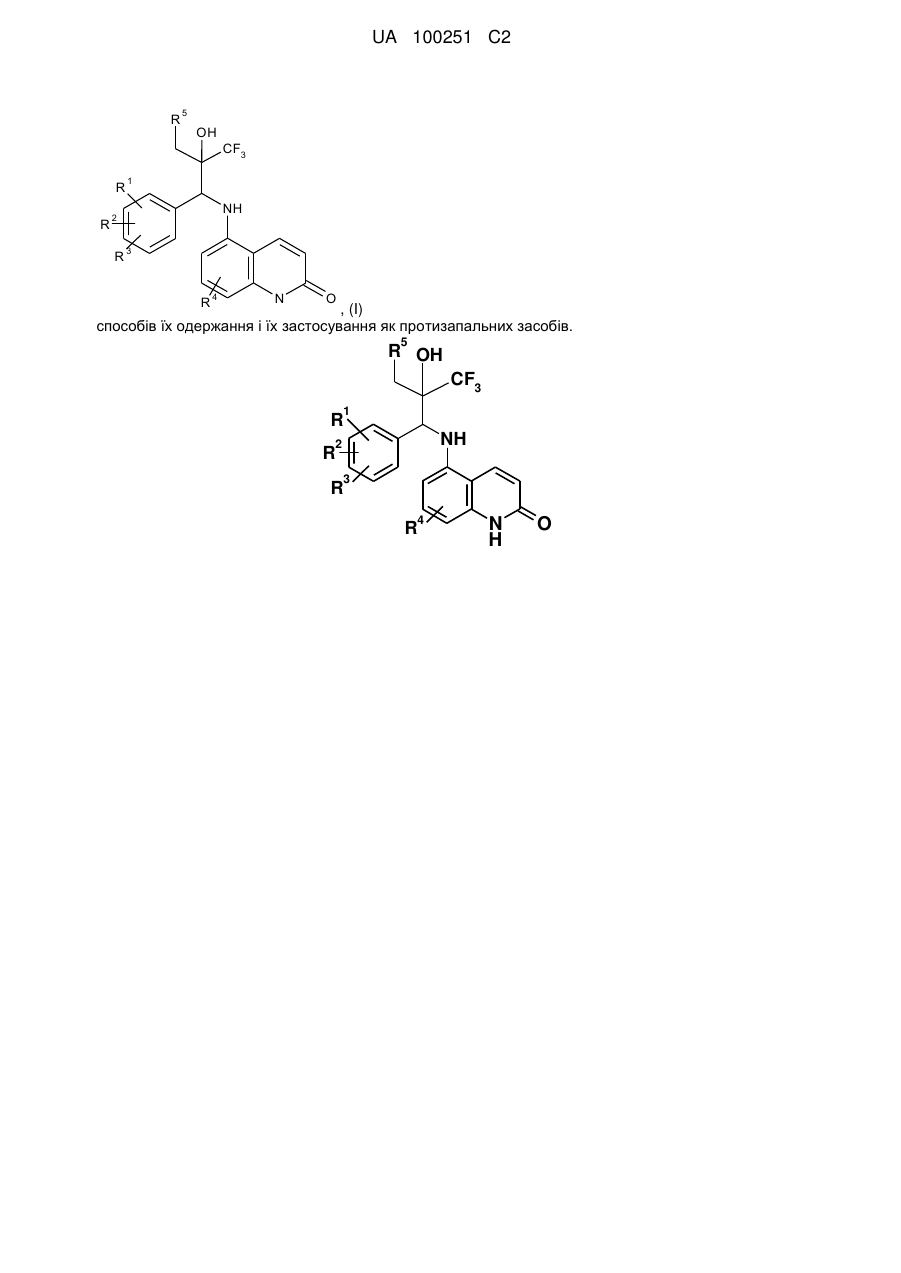
1. Сполуки загальної формули 1
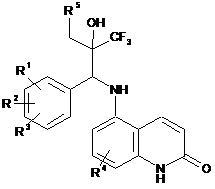 , (I)
, (I)
де R1 і R2 незалежно один від одного. означають атом водню, гідроксигрупу, атом галогену, необов'язково заміщену (С1-С10)-алкільну групу, необов'язково заміщену (С1-С10)-алкоксильну групу, (С1-С10)-алкілтіогрупу, (С1-С5)-перфтороалкільну групу, ціаногрупу, нітрогрупу, або R1 і R2
разом означають групу. вибрану з груп -О-(СH2)p-О-, -O-(CH2)p-CH2-, -О-СH=СH-. -(СН2)р+2-, -NH-(CH2)p+1, -N(С1-С3-алкіл)-(СН2)р+1, і -NH-N=CH-,
при ньому р = 1 або 2, і термінальні атоми кисню і/або атоми вуглецю і/або атоми азоту зв'язані з безпосередньо суміжними кільцевими атомами вуглецю, або NR6R7,
при цьому R6 і R7, незалежно один від одного, означають водень, С1-С5-алкіл або (СO)-(С1-С5)-алкіл,
R3 означає атом водню, гідроксигрупу. атом галогену, ціаногрупу, необов'язково заміщену (С1-С10)-алкільну групу, (С1-С10)-алкоксильну групу, (С1-С10)-алкілтіогрупу, або (С1-С5)-перфтороалкільну групу,
R4 означає водень, галоген, гідроксигрупу, (С1-С5)-алкіл, (С1-С5)-алкокси групу, (С1-С5)-алкілтіогрупу, (С1-С5)-перфтороалкіл, ціаногрупу, нітрогрупу, NR6R7, COOR9, (CO)NR6R7 або (C1-C5-алкілен)-О-(СО)-(С1-С5)-алкільну групу,
R5 означає групу, вибрану з
-(С1-С10)-алкілу, який може бути необов'язково частково або повністю галогенованим,
-(С2-С10)-алкенілу,
-(С2-С10)-алкінілу,
(С3-С7)-циклоалкіл-(С1-С8)-алкілу.
(С3-С7)-циклоалкіл-(С1-С8)-алкенілу.
(С3-С7)-циклоалкіл-(С2-С8)-алкінілу,
гетероцикліл-(С1-С8)-алкілу,
гегероцикліл-(С1-С8)-алкенілу,
гетероцикліл-(С2-С8)-алкінілу,
-R8,
R8-(С1-С8)-алкілу,
R8-(C2-C8)-алкенілу,
R8-(C2-Cs)-алкенілу,
-S-(С1-С10)-алкілу,
-SO2-(С1-С10)- алкілу
-S-R8,
-SO2-R8,
-CN
-Hal,
-О-(С1-С10,)-алкілу,
-NR6R7 де R6, R7 мають визначені вище значення,
-O-R8,
-OH,
за винятком -СН(СН3)2, або -С(СH3) = СH2,
R8 означає арильну групу, яка може необов'язково бути заміщеною 1-3 гідроксигрупами, галогенами, С1-С5-алкілами, С1-С5-алкоксигрупами, ціаногрупами, СF3, нітрогрупами, СOO(С1-С5-алкільними) або С(O)OСН2-фенільними або гетероарильними групами, при цьому гетероарильна група може містити 1-3 гетероатоми, яка може необов'язково бути заміщеною 1-3 алкільними групами, гідроксигрупами, галогенами, ціаногрупами або С1-С5-алкоксильпими групами і їх солі, сольвати або солі сольватів.
2. Сполуки загальної формули І згідно з пунктом 1, де
R1 і R2 незалежно один від одного. означають атом водню, гідроксигрупу, атом галогену, необов'язково заміщену (С1-С10)-алкільну групу, необов'язково заміщену (С1-С10)-алкоксильну групу, (С1-С5)-перфтороалкільну групу, ціаногрупу, або NR6R7 при цьому R6 і R7, незалежно один від одного, означають водень, С1-С5-алкіл або (СО)-(С1-С5)-алкіл,
R3 означає атом водню, гідроксигрупу, атом галогену, ціаногрупу, необов'язково заміщену (С1-С10)-алкільну групу, (С1-С10)-алкоксильну групу, або (С1-С5)-перфтороалкільну групу,
R4 означає водень, С1-С3-алкіл, С1-С3-алкоксигрупу, гідроксигрупу, галоген,
R5 означає групу, вибрану з
-(С1-С10)-алкілу, який може бути необов'язково частково або повністю галогенованим,
-(С2-С10)-алкенілу,
-(С2-С10)-алкінілу,
-(С3-С7)-циклоалкіл-(С1-С8)-алкілу,
-(С3-С7)-циклоалкіл -(С1-С8)-алкенілу,
-S-(С1-С10)-алкілу,
-SO2-(С1-С10)-алкілу,
-CN
-Hal.
-О-(С1-С10)-алкілу,
-NR6R7, де R6, R7 мають визначені нище значення.
-ОН.
за винятком -СH(СH3)2, або -С(СН3)=СН2,
і їх солі, сольвати або солі сольватів.
3. Сполуки загальної формули І згідно з пунктом 1. де
R1, R2 і R3 незалежно один від одного означають водень, фтор, хлор, бром, ціаногрупу, метоксигрупу, етоксигрупу, гідроксигрупу,
R4 означає водень. С1-С3-алкіл, галоген.
R5 означає гідроксигрупу. хлор. -S-СН3, -S-CH2-CH3, -S-CH2-СН2-СH3, -О-СH3 або -О-СН2-СH3, -О-СН2-СH2-СН3, і їх солі, сольвати або солі сольватів.
4. Сполуки згідно з принаймні одним з пунктів 1-3 в енантіомерно чистій формі і їх солі, сольвати або солі сольватів.
5. Сполуки згідно з пунктом 1, вибрані зі списку, що включає 5-{[1-(2-Фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфоніл]-метил)-пропіл]-аміно}-1H-хінолін-2-он
5-{[2-([Етилсульфаніл]-метил)-1-(2-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідроксипропіл]-аміно}-1H-хінолін-2-он
5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфоніл]-метил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(2-Хлоро-3-фторо-4-метоксифееіл)-2-([етилсульфаніл]-метил)-3,3,3-трифторо-2-гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(метоксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-(етоксиметил)-3,3,3-трифторо-2-гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(5-Хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(5-Хлоро-3-фторо-2-метоксифеніл)-2-(хлорометил)-3,3,3-трифторо-2-гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[3,3,3-трифторо-2-гідрокси-2-([метоксиметил)-1-фенілпропіл]-аміно}-1H-хінолін-]-1-он
5-{[1-(2-Хлоро-3-фторо-4-метоксифсніл)-2-(діамінометил)-3,3,3-трифторо-2-гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(4-Хлоро-3-(фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(метоксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(4-Хлоро-3-фторо-2-метоксифеніл)-2-(етоксиметил)-3,3,3-трифторо-2-гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(2-Хлоро-3-фторо-4-гідроксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
і їх солі, сольвати або солі сольватів.
6. Енантіомерно чисті сполуки мідно з пунктом 1, вибрані зі списку, що включає
5-{(1S,2R)[1-(2-Фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфоніл]-метил)-пропіл]-аміно}-1H-хінолін-2-он
5-{(1S,2R)[2-([Етилсульфаніл]-метил)-1-(2-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідроксипропіл]-аміно}-1H-хінолін-2-он
5-{(1S,2R)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфоніл]-метил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{(1S,2R)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-([етилсульфаніл]-метил)-3,3,3-трифторо-2-гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{(1S,2S)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3.3,3-трифторо-2-гідрокси-2-(метоксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{(1S,2S)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-(етоксиметил)-3,3,3-трифторо-2-гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{(1S,2S)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{(1S,2S)[1-(5-Хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{(1S,2R)[1-(5-Хлоро-3-фторо-2-метоксифеніл)-2-(хлорометил)-3,3,3-трифторо-2-гідроксипроніл]-аміно}-7-фторо-1H-хінолін-2-он
5-{(1S,2S)[3,3,3-трифторо-2-гідрокси-2-([метоксиметил)-1-фенілпропіл]-аміно}-1H-хінолін-1-он
5-{(1S,2R)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-(діамінометил)-3,3,3-трифторо-2-гідроксипроніл]-аміно}-7-фторо-1H-хінолін -2-он
5-{(1S,2S)[1-(2-Хлоро-3-фторо-4-гідроксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
і їх солі, сольвати або солі сольватів.
7. Сполуки загальної формули I згідно з пунктом 1, де
R1, R2 і R.3 незалежно один від одного вибирають з хлору, фтору та метоксигрупи,
R4 означає замісник 7-фтор,
R5 вибирають з -S-CH2-CH3, -O-CH2-CH3, -S-CH3 -О-СН3, -ОН та -Сl,
і їх солі, сольвати або солі сольватів.
8. Сполуки загальної формули I згідно і пунктом 7, вибрані зі списку, що включає
5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфоніл]-метил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-([етилсульфаніл]-метил)-3,3,3-трифторо-2-гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(метоксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(2-Хлоро-3-фторо-4-метоксифсніл)-2-(етоксиметил)-3,3,3-трифторо-2-гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(5-Хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(5-Хлоро-3-фторо-2-метоксифеніл)-2-(хлорометил)-3,3,3-трифторо-2-гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(4-Хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(метоксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(4-Хлоро-3-фторо-2-метоксифеніл)-2-(етоксиметил)-3,3,3-трифторо-2-гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он
5-{[1-(2-Хлоро-3-фторо-4-гідроксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он
і їх солі, сольвати або солі сольватів.
9. Застосування сполук згідно формули І принаймні одного з пунктів 1-8 для одержання фармацевтичних агентів.
10. Застосування сполук згідно формули І принаймні одного з пунктів 1-8 для одержання фармацевтичних агентів для лікування запальних захворювань.
11. Фармацевтична композиція, що містить сполуку формули (І) або її фармацевтично прийнятну сіль як визначено в пунктах 1-8, і фармацевтично прийнятний ад'ювант, розчинник або носій.
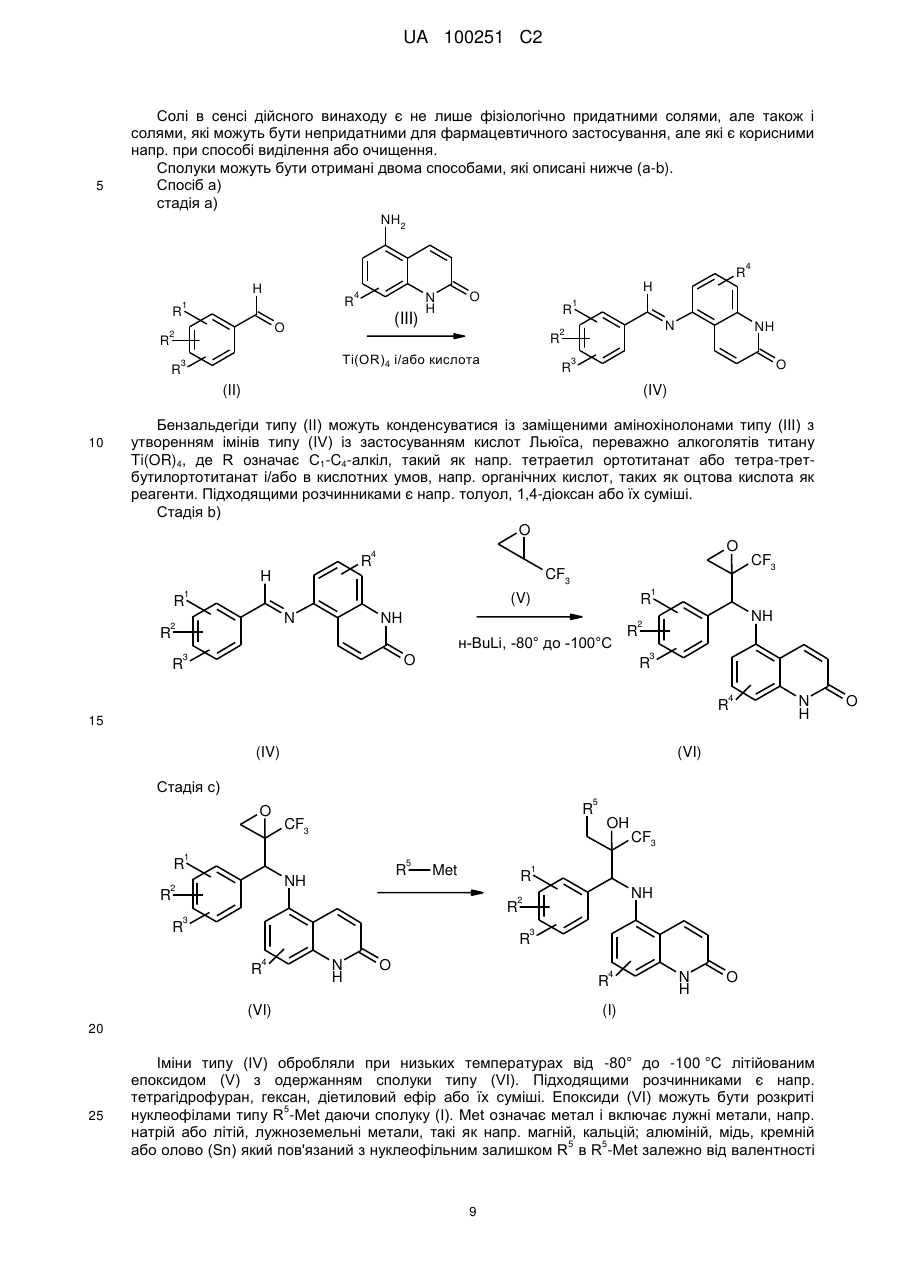
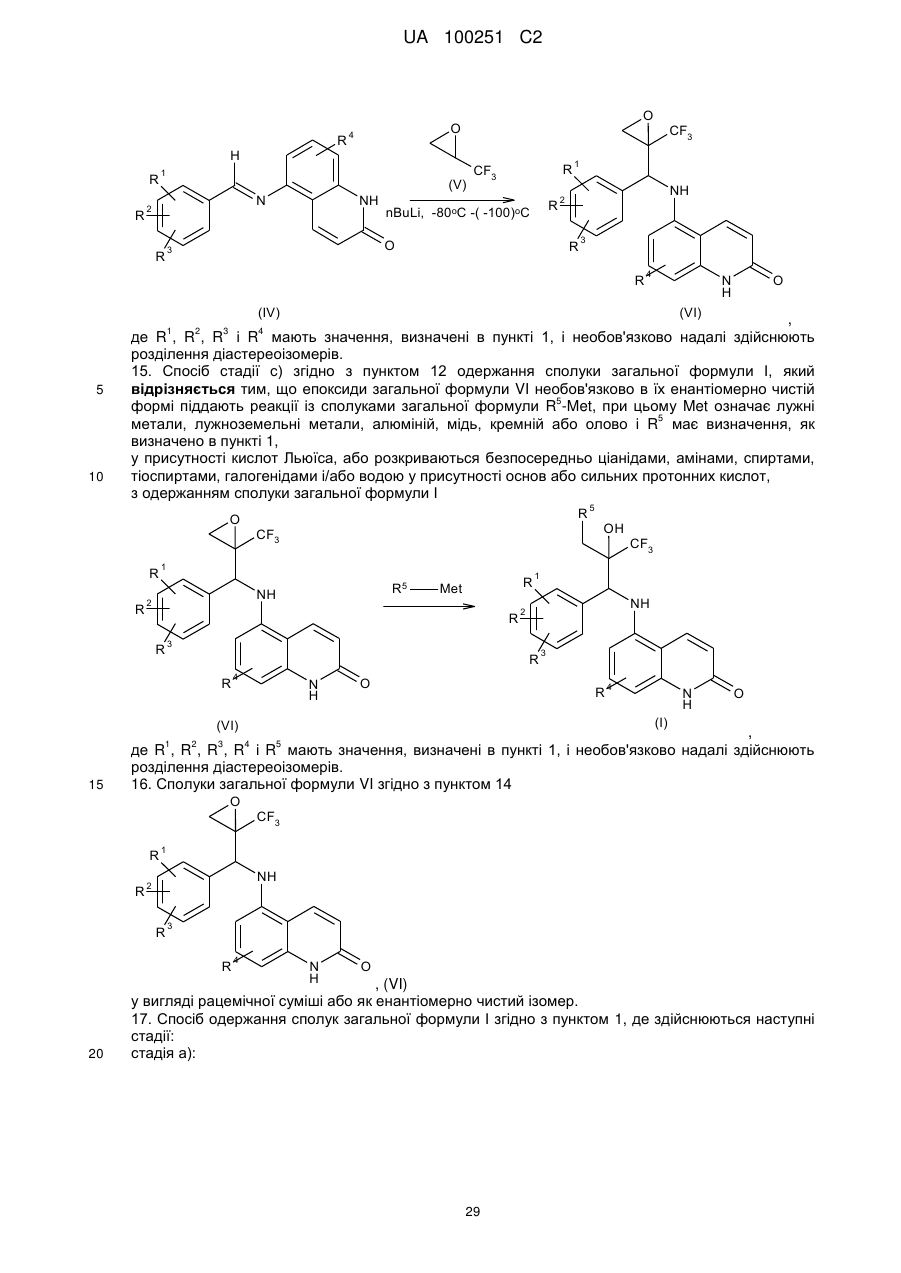
12 Спосіб одержання сполук загальної формули І згідно з пунктом 1, в якому здійснюють наступні стадії:
стадія а):
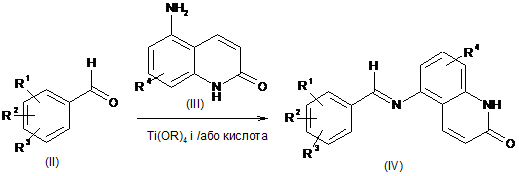 ,
,
стадія b):
 ,
,
стадія с):
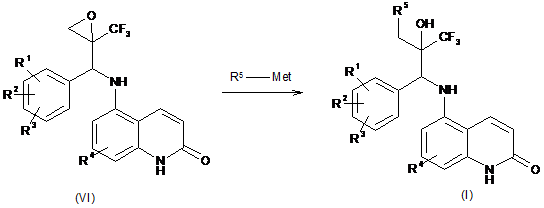 ,
,
де всі залишки мають визначення, дані в пункті 1, і R означає С1-С4-алкіл і Met означає лужні метали, лужноземельні метали, алюміній, мідь, кремній або олово.
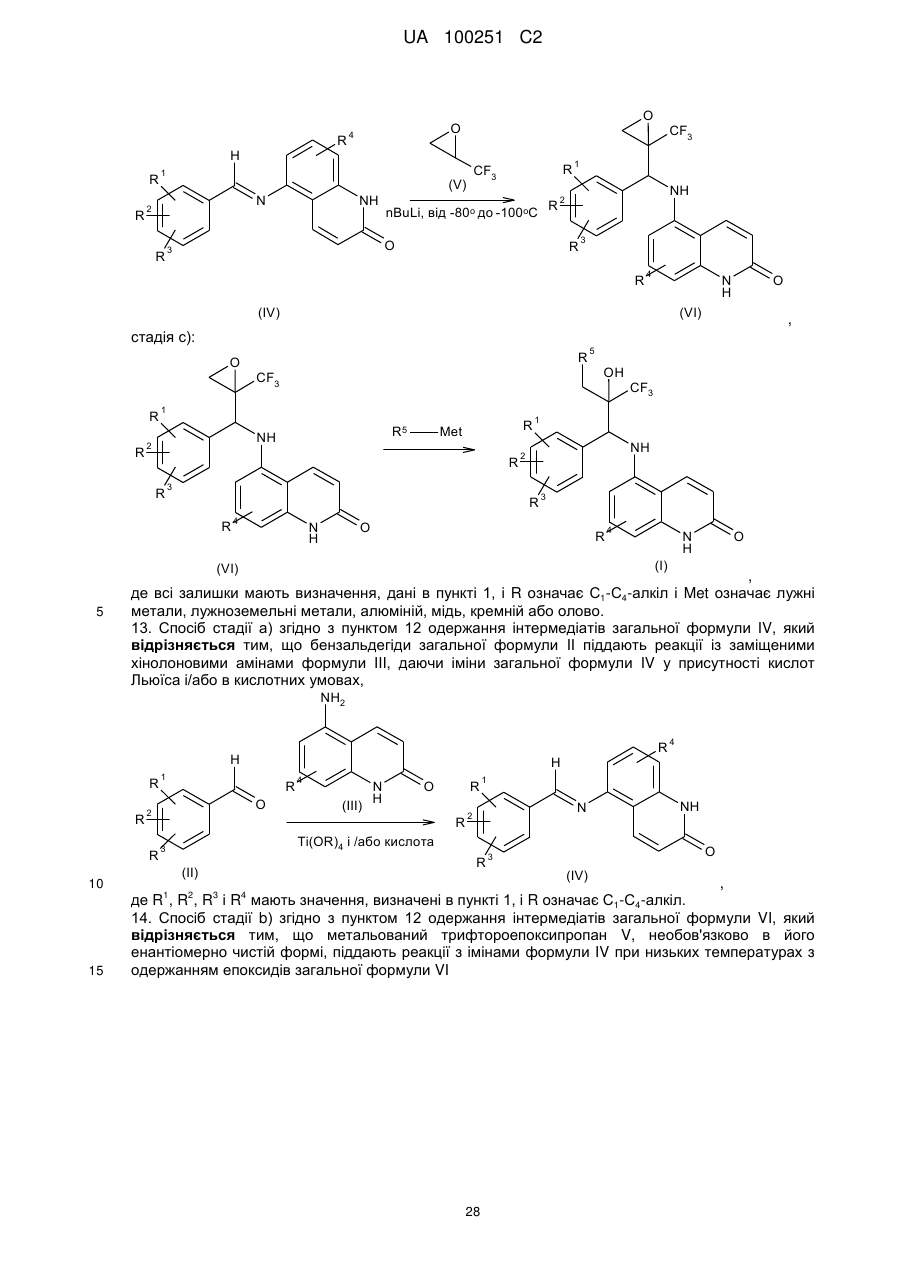
13. Спосіб стадії а) згідно з пунктом 12 одержання інтермедіатів загальної формули IV. який відрізняється тим, що бензальдегіди загальної формули II піддають реакції із заміщеними хінолоновими амінами формули III, даючи іміни загальної формули IV у присутності кислот Льюїса і/або в кислотних умовах,

де R1, R2, R3 і R4 мають значення, визначені в пункті 1, і R означає С1-С4-алкіл.
14. Спосіб стадії b) згідно ч пунктом 12 одержання інтермедіатів загальної формули VI, який відрізняється тим, що метальований трифтороепоксипропан V, необов'язково в його енантіомерно чистій формі, піддають реакції з імінами формули IV при низьких температурах з одержанням еноксидів загальної формули VI

де R1, R2, R3 і R4 мають значення, визначені в пункті 1, і необов'язково надалі здійснюють розділення діастереоізомерів.
15. Спосіб стадії с) згідно з пунктом 12 одержання сполуки загальної формули І, який відрізняється тим, що епоксиди загальної формули VI необов'язково в їх енантіомерно чистій формі піддають реакції із сполуками загальної формули R5-Met при цьому Met означає лужні метали, лужноземельні метали, алюміній, мідь, кремній або олово і R5 має визначення як визначено в пункті 1,
у присутності кислот Льюїса, або розкриваються безпосередньо ціанідами, амінами, спиртами, тіоспиртами, галогенідами і/або водою у присутності основ або сильних протонних кислот.
з одержанням сполуки загальної формули І
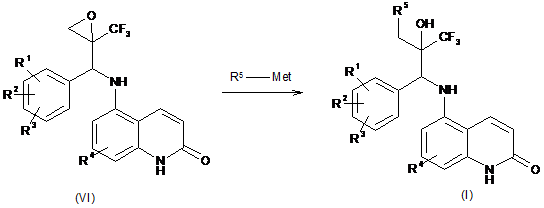
де R1, R2, R3, R4 і R5 мають значення, визначені в пункті 1, і необов'язково падалі здійснюють розділення діастереоізомерів.
16. Сполуки загальної формули VI згідно з пунктом 14,
 , (VI)
, (VI)
у вигляді рацемічної суміші або як енантіомерно чистий ізомер.
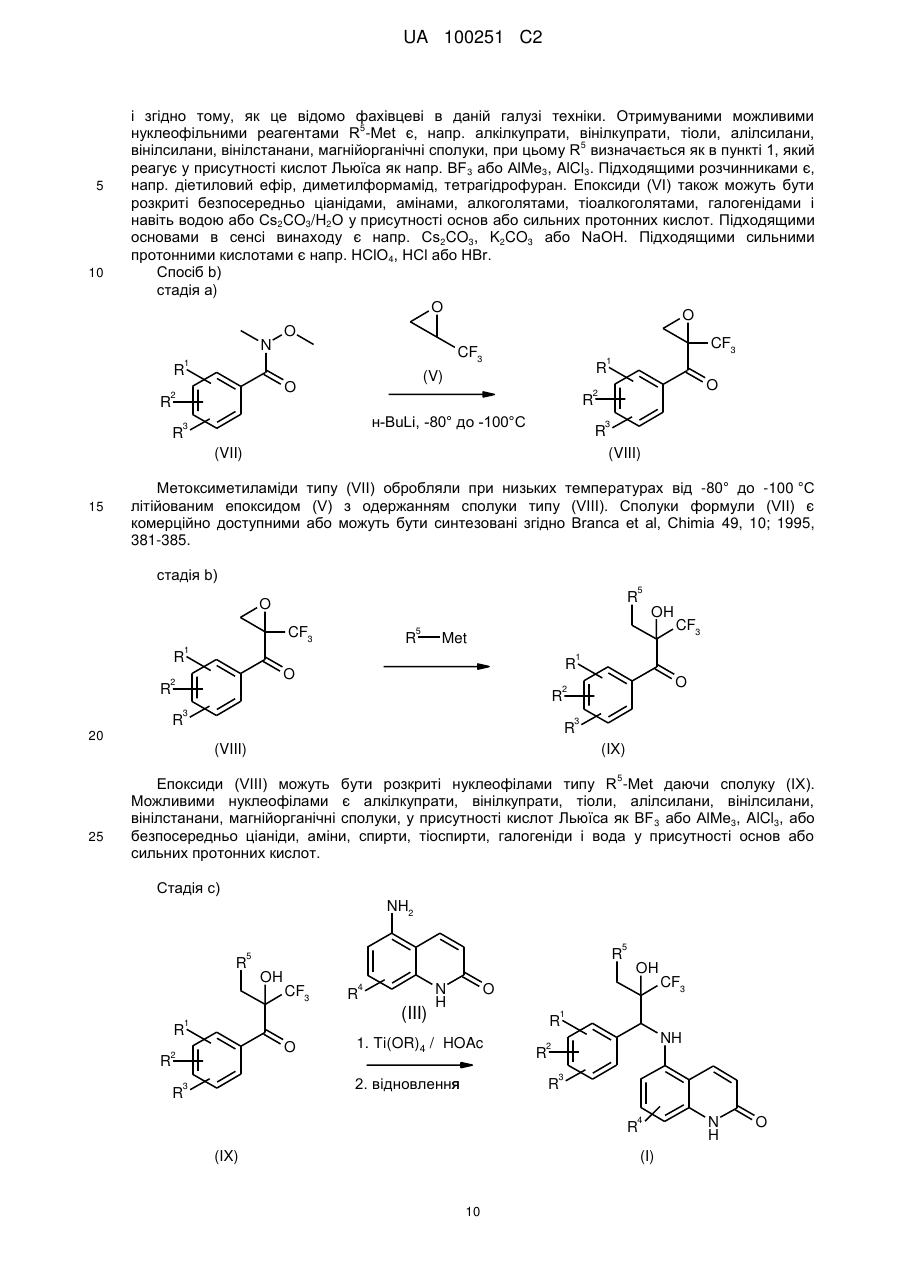
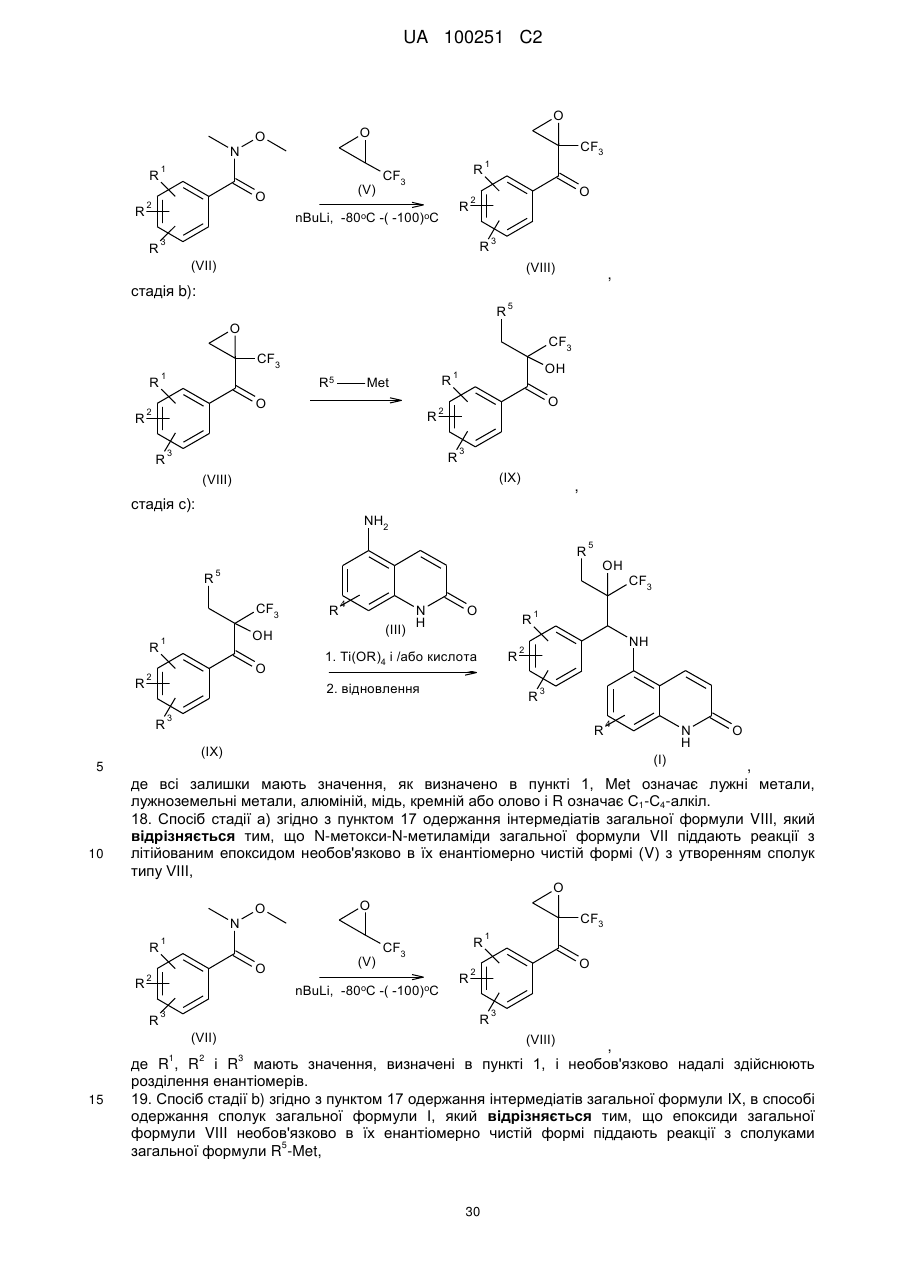
17. Спосіб одержання сполук загальної формули 1 згідно з пунктом 1, де здійснюються наступні стадії:
стадія а):
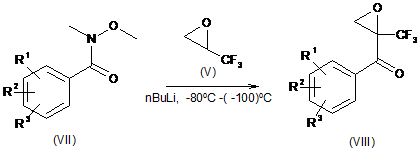 ,
,
стадія b):
 ,
,
стадія с):
 ,
,
де всі залишки мають значення як визначено в пункті 1, Met означає лужні метали, лужноземельні метали, алюміній, мідь, кремній або олово і R означає С1-С4-алкіл.
18. Спосіб стадії а) згідно з пунктом 17 одержання інтермедіатів загальної формули VIII, який відрізняється тим, що N-метокси-N-метиламіди загальної формули VII піддають реакції з літійованим епоксидом необов'язково в їх енантіомерно чистій формі (V) з утворенням
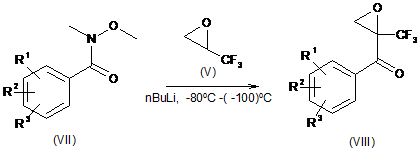
сполук типу VIII, де R1, R2 і R3 мають значення, визначені в пункті 1, і необов'язково надалі здійснюють розділення енантіомерів.
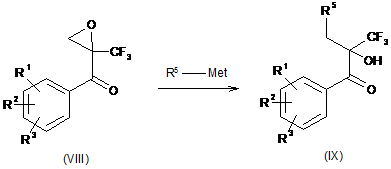
19. Спосіб стадії b) згідно з пунктом 17 одержання інтермедіатів загальної формули IX, в способі одержання сполук загальної формули І, який відрізняється тим, що епоксиди загальної формули VIII необов'язково в їх енантіомерно чистій формі піддають реакції з
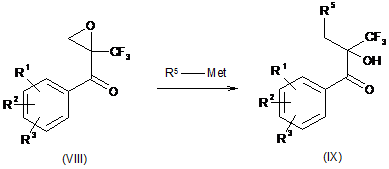
сполуками загальної формули R5-Met, де R1, R2, R3 і R5 мають значення, визначені в пункті 1, і Met має значення як визначено в пункті 13 і необов'язково надалі здійснюють розділення енантіомерів.
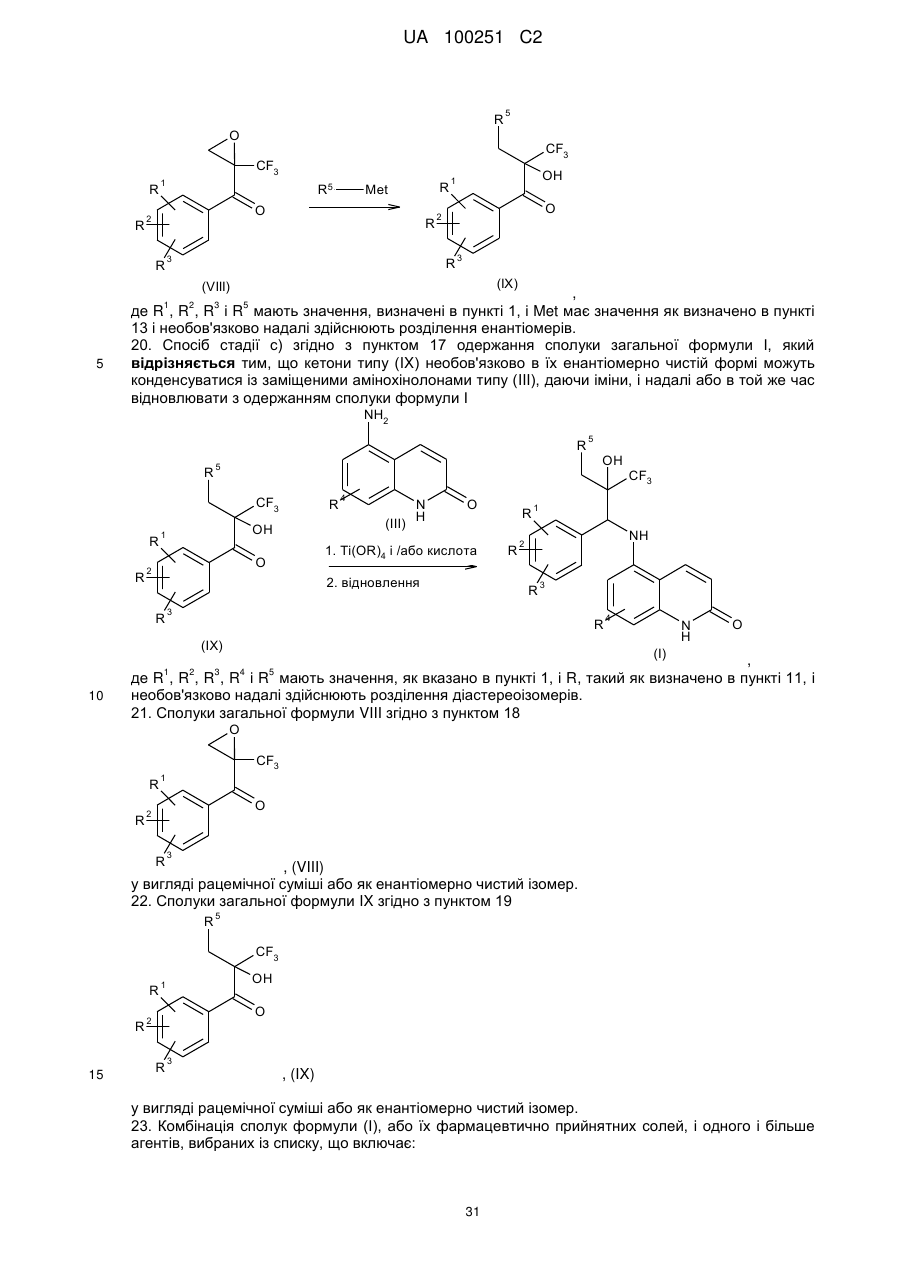
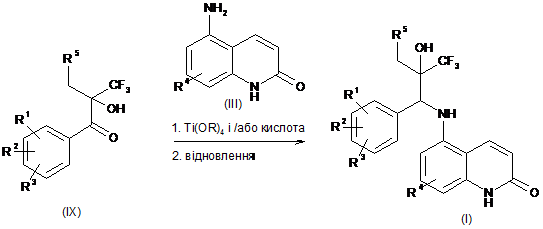
20. Спосіб стадії с) згідно з пунктом 17 одержання сполуки загальної формули І, який відрізняється тим, що кетони типу (IX) необов'язково в їх енантіомерно чистій формі можуть конденсуватися із заміщеними амінохінолонами типу (III), даючи іміни, і надалі або в той же час відновлювати з одержанням сполуки формули І

де R1, R2, R3, R4 і R5 мають значення як вказано в пункті 1 і R як визначено в пункті 11 і необов'язково надалі здійснюють розділення діастереоізомерів.
21. Сполуки загальної формули VIII згідно з пунктом 18
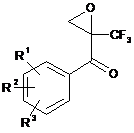 , (VIII)
, (VIII)
у вигляді рацемічної суміші або як енантіомерно чистий ізомер.
22. Сполуки загальної формули IX згідно з пунктом 19
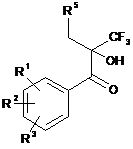 , (IX)
, (IX)
у вигляді рацемічної суміші або як енантіомерно чистий ізомер.
23. Комбінація сполук формули (І), або їх фармацевтично прийнятних солей, і одного і більше агентів, вибраних із списку, що включає:
- інгібітор PDE4, включаючи інгібітор ізоформи PDE4D;
- селективний β.sub2. адреноміметик, такий як метапротеренол, ізопротеренол, ізопреналін, альбутерол, сальбугамол, формотерол, салметерол, тербуталін, орципреналін, бітолтерол, мезилат, пірбутерол або індакатерол;
- антагоніст мускаринового рецептора (наприклад, M1, M2 або М3 антагоніст, такий як селективний М3 антагоніст), такий як іпратропію бромід, тіотропію бромід, окситропію бромід, пірензепін або телензепін;
- модулятор функції хемокінового рецептора (такий як антагоніст рецептора CCR1); або
- інгібітор функції кінази р38.
Текст
Реферат: Даний винахід стосується сполук формули І СПОСІБ ЇХ UA 100251 C2 (12) UA 100251 C2 R 5 OH CF3 R R 1 NH 2 R 3 R 4 N O , (I) способів їх одержання і їх застосування як протизапальних засобів. 5 R OH CF3 1 R NH 2 R 3 R 4 R N H O UA 100251 C2 5 10 15 20 Дійсний винахід належить до сполук формули I, способу їх одержання і їх застосуванню як протизапальні засоби. Найбільш поширеними протизапальними засобами все ще є глюкокортикоїди (GC), які є маленькими молекулами, що мають стероїдну будову, які взаємодіють з глюкокортикоїдним рецептором (GR), або ендогенним, як кортизол, або синтетичним, як дексаметазон та інші. Проте, застосування високо ефективних GC, особливо протягом тривалого періоду обробки, приводить до прояви небажаних ефектів. Деякі їх цих ефектів, є важкими і інколи незворотними, такі як напр. діабет, остеопороз, шкіряна і мускульна атрофії, глаукома (Schäcke et al., 2002 Pharmacol. & Therapeutics (2002) 96(1):23-43., Miner et al., 2005 Expert Opin. Investig. Drugs (2005) 14(12):1527-1545.) GC істотно інгібують прозапальні цитокіни і хемокіни в місці застосування, при цьому вони виявляють лише обмежену системну дію (O'Connell, 2003 Clin. Ther. (2003) 25(Suppl. C):C42-60; Welker et al. Int. Arch. Allergy Immunol. (1996) 109(2):110-115, 1996, Günther et al, 1998. Skin Pharmacol. Appl. Skin Physiol. (1998) 11(1):35-42). Хоча локально активні GCи очевидно є ідеальними протизапальними лікарськими засобами, їх застосування обмежене унаслідок локальних побічних ефектів і унаслідок недостатньої ефективності при важких станах захворювання. Внаслідок цього, існує значна медична потреба в нових сполуках, які мають протизапальну/імуномодулюючу активність подібно до ринкових GC, і менш ймовірно викликають небажані ефекти. З попереднього рівня техніки DE 100 38 639 і WO 02/10143, відомі протизапальні засоби наступної загальної формули 2 1 R R HO R3 B A 25 H N Ar де Ar радикал включає фталіди, тіофталіди, бензоксазинони або фталазинони. Під час експерименту, ці сполуки показують відокремлення дії між протизапальними і небажаними метаболічними діями і перевершують раніше описані нестероїдні глюкокортикоїди або показують принаймні таку ж хорошу дію. Сполуки, структурно родинні описаним в дійсній патентній заявці, розкриті в WO 2005/035518. a b OH 3 R c 1 R NH 2 R 30 Унаслідок способу виробництва ці сполуки завжди містять групу a b c 35 40 де зв'язок між а і b або між b і с може бути ненасиченим, і яка таким чином повинна містити групу, вибрану з -CH2-CH(CH3)2, -CH=C(CH3)2 або -CH2-C(CH3)=CH2). Сполуки такого складу особливо відкидаються в дійсній заявці. Не дивлячись на всі спроби, селективність сполук відомого рівня техніки по відношенню до глюкокортикоїдного рецептора (GR) в порівнянні з іншими стероїдними рецепторами так само як їх ефективності або ефективність все ще вимагають поліпшення. Внаслідок цього завдання дійсного винаходу створити сполуки, здатні показати ознаки поліпшення принаймні в одному вищезазначеному аспекті. Це завдання було досягнуте за допомогою сполук згідно пунктам формули винаходу. Дійсний винахід таким чином належить до сполук загальної формули I 1 UA 100251 C2 5 R OH CF3 1 R NH 2 R 3 R 4 R 5 10 15 20 25 30 35 40 45 N H O (I) де 1 2 R і R незалежно один від одного, означають атом водню, гідроксигрупу, атом галогену, необов'язково заміщену (C1-C10)-алкільну групу, необов'язково заміщену (C1-C10)-алкоксильну групу, (C1-C10)-алкілтіогрупу, (C1-C5)-перфтороалкільну групу, ціаногрупу, нітрогрупу, 1 2 або R і R разом означають групу, вибрану з груп -O-(CH2)p-O-, -O-(CH2)p-CH2-, -O-CH=CH-, -(CH2)p+2-, -NH-(CH2)p+1, -N(C1-C3-алкіл)-(CH2)p+1, і -NH-N=CH-, при цьому p=1 або 2, і термінальні атоми кисню і/або атоми вуглецю і/або атоми азоту зв'язані з безпосередньо суміжними кільцевими атомами вуглецю, 6 7 6 7 або NR R , при цьому R і R , незалежно один від одного, означають водень, C1-C5-алкіл або (CO)-(C1-C5)-алкіл, 3 R означає атом водню, гідроксигрупу, атом галогену, ціаногрупу, необов'язково заміщену (C1-C10)-алкільну групу, (C1-C10)-алкоксильну групу, (C1-C10)-алкілтіогрупу, або (C1-C5)перфтороалкільну групу, 4 R означає водень, галоген, гідроксигрупу, (C1-C5)-алкіл, (C1-C5)-алкоксигрупу, (C1-C5)6 7 9 6 7 алкілтіогрупу, (C1-C5)-перфтороалкіл, ціаногрупу, нітрогрупу, NR R , COOR , (CO)NR R або (C1-C5-алкілен)-O-(CO)-(C1-C5)-алкільну групу 5 R означає групу, вибрану з, -(C1-C10)-алкілу, який може бути необов'язково частково або повністю галогенованим, (C2-C10)-алкенілу, (C2-C10)-алкінілу, (C3-C7)-циклоалкіл-(C1-C8)-алкілу, (C3-C7)циклоалкіл-(C1-C8)-алкієнілу, (C3-C7)-циклоалкіл-(C2-C8)-алкінілу, гетероцикліл-(C1-C8)-алкілу, 8 8 8 гетероцикліл-(C1-C8)-алкенілу, гетероцикліл-(C2-C8)-алкінілу, R , R -(C1-C8)-алкілу, R -(C2-C8)8 алкенілу, R -(C2-C8)-алкінілу, -S-(C1-C10)-алкілу, -SO2-(C1-C10)-алкілу 8 8 _ 6 7 6 7 -S-R , -SO2-R , -CN, -Hal, -O-(C1 C10)-алкілу, -NR R , де R , R мають визначені вище 8 значення, -O-R , -OH, за винятком -CH(CH3)2, або -C(CH3)=CH2, 8 R означає арильну групу, яка може необов'язково бути заміщеною 1-3 гідроксигрупами, галогенами, C1-C5-алкілами, C1-C5-алкоксигрупами, ціаногрупами, CF3, нітрогрупами, COO(C1-C5-алкілами) або C(O) OCH2-фенілами або гетероарильною групою, при цьому гетероарильна група може містити 1-3 гетероатоми, яка може необов'язково бути заміщеною 13 алкільними групами, гідроксигрупами, галогенами, ціаногрупами або C 1-C5-алкоксильними групами і їх солі, сольвати або солі сольватів. Один аспект винаходу належить до сполук формули I, де 1 2 R і R незалежно один від одного, означають атом водню, гідроксигрупу, атом галогену, необов'язково заміщену (C1-C10)-алкільну групу, необов'язково заміщену (C1-C10)-алкоксильну 1 2 групу, (C1-C10)-алкілтіогрупу, (C1-C5)-перфтороалкільну групу, ціаногрупу, нітрогрупу, або R і R разом означають групу, вибрану з груп -O-(CH2)p-O-, -O-(CH2)p-CH2-, -O-CH=CH-, -(CH2)p+2-, -NH(CH2)p+1, -N(C1-C3-алкіл)-(CH2)p+1, і -NH-N=CH-, термінальні атоми кисню і/або атоми вуглецю і/або атоми азоту зв'язані з безпосередньо 6 7 суміжними кільцевими атомами вуглецю, або NR R 6 7 при цьому R і R незалежно один від одного означають водень, C 1-C5-алкіл або (CO)(C1-C5)-алкіл, 3 R означає атом водню, гідроксигрупу, атом галогену, ціаногрупу, необов'язково заміщену (C1-C10)-алкільну групу, (C1-C10)-алкоксильну групу, (C1-C10)-алкілтіогрупу, або (C1-C5)перфтороалкільну групу, 4 R означає атом водню, гідроксигрупу, атом галогену, 5 R означає групу, вибрану з -(C1-C10)-алкілу який може бути необов'язково частково або повністю галогенованим 2 UA 100251 C2 5 10 15 20 25 30 35 40 45 50 55 -(C2-C10)-алкенілу, (C2-C10)-алкінілу, (C3-C7)-циклоалкіл-(C1-C8)-алкілу, (C3-C7)циклоалкіл-(C2-C8-)-алкенілу, (C3-C7)-циклоалкіл-(C2-C8-)-алкінілу, гетероцикліл-(C1-C8)-алкілу, 8 8 8 гетероцикліл-(C2-C8)-алкенілу, гетероцикліл-(C2-C8)-алкінілу, R , R -(C1-C8)-алкілу, R -(C2-C8)8 8 8 алкенілу, R -(C2-C8)-алкінілу -S-(C1-C10)-алкілу, -S-R , -SO2-R , -SO2-(C1-C10)-алкілу, -CN, -Hal, 6 7 6 7 8 -O-(C1-C10)-алкілу, -NR R де R , R мають визначені вище значення, -O-R , -OH, за винятком -CH(CH3)2, або -C(CH3)=CH2, 8 R означає арил, який може необов'язково бути заміщеним 1-3 алкілами, гідроксигрупами, галогенами, ціаногрупами або C1-C5-алкоксигрупами або гетероарильну групу, де гетероарильна група може містити 1-3 гетероатоми, яка може необов'язково бути заміщеною 13 алкілами, гідроксигрупами, галогенами, ціаногрупами або C1-C5-алкоксигрупами, n означає ціле число, вибране з 1, 2, 3, 4, 5 і їх солі, сольвати або солі сольватів. 1 2 Іншим аспектом винаходу є сполуки загальної формули I згідно пункту 1, де R і R незалежно один від одного, означають атом водню, гідроксигрупу, атом галогену, необов'язково заміщену (C1-C10)-алкільну групу, необов'язково заміщену (C1-C10)-алкоксильну групу, (C1-C5)6 7 6 7 перфтороалкільну групу, ціаногрупу, або NR R , при цьому R і R , незалежно один від одного, 3 означають водень, C1-C5-алкіл або (CO)-(C1-C5)-алкіл, R означає атом водню, гідроксигрупу, атом галогену, ціаногрупу, необов'язково заміщену (C1-C10)-алкільну групу, (C1-C10)-алкоксильну 4 групу, або (C1-C5)-перфтороалкільну групу, R означає водень, C1-C3-алкіл, C1-C3-алкоксигрупу, 5 гідроксигрупу, галоген, R означає групу, вибрану з, -(C1-C10)-алкілу, який може бути необов'язково частково або повністю галогенованим, -(C2-C10)-алкенілу, -(C2-C10)-алкінілу, -(C3-C7)-циклоалкіл-(C1-C8)-алкілу, -(C3-C7)-циклоалкіл-(C2-C8)-алкенілу, -S-(C1-C10)-алкілу, 6 7 6 7 SO2-(C1-C10)-алкілу, -CN, -Hal, -O-(C1-C10)-алкілу, -NR R , де R , R мають визначені вище значення, -OH, за винятком -CH(CH3)2, або -C(CH3)=CH2, і їх солі, сольвати або солі сольватів. 1 2 3 Додатковим аспектом винаходу є сполуки загальної формули I згідно пункту 1, де R , R і R незалежно один від одного означають водень, фтор, хлор, бром, ціаногрупу, метоксигрупу, 4 5 етоксигрупу, гідроксигрупу, R означає водень, C1-C3-алкіл, галоген, R означає гідроксигрупу, хлор, –S-CH3, -S-CH2-CH3, -S-CH2-CH2-CH3, -O-CH3 або -O-CH2-CH3, -O-CH2-CH2-CH3, -N-(CH3)2, N-(CH2-CH3)2 і їх солі, сольвати або солі сольватів. Додатковим аспектом винаходу є сполуки 1 2 3 загальної формули I згідно пункту 1, де R , R і R незалежно один від одного означають водень, 4 фтор, хлор, бром, ціаногрупу, метоксигрупу, етоксигрупу, гідроксигрупу, R означає водень, 5 C1-C3-алкіл, галоген, R означає гідроксигрупу, хлор, –S-CH3, -S-CH2-CH3, -S-CH2-CH2-CH3, O-CH3, -O-CH2-CH3, -O-CH2-CH2-CH3 або N(CH3)2 і їх солі, сольвати або солі сольватів. 1 2 3 Ще іншим аспектом винаходу є сполуки загальної формули I згідно пункту 1, де R , R і R незалежно один від одного означають водень, фтор, хлор, бром, ціаногрупу, метоксигрупу, 4 5 етоксигрупу, гідроксигрупу R означає водень C1-C3-алкіл, галоген, R означає гідроксигрупу, хлор, –S-CH3, -S-CH2-CH3, -S-CH2-CH2-CH3, -O-CH3 або -O-CH2-CH3, -O-CH2-CH2-CH3 і їх солі, сольвати або солі сольватів. 1 2 Одним аспектом винаходу є сполуки загальної формули I згідно пункту 1, де R і R 3 незалежно один від одного означають водень, фтор, хлор, метоксигрупу, гідроксигрупу, R 4 5 означає водень, фтор, хлор або метоксигрупу, R означає водень або фтор, R означає гідроксигрупу, атом хлору, –S-CH3, -S-CH2-CH3, -O-CH3, -O-CH2-CH3 або N(CH3)2 і їх солі, сольвати або солі сольватів. Додатковим аспектом винаходу є сполуки загальної формули I 1 2 згідно пункту 1, де R і R незалежно один від одного означають водень, фтор, хлор, 3 4 5 метоксигрупу, R означає водень, фтор, хлор або метоксигрупу, R означає водень або фтор, R означає гідроксигрупу, атом хлору, –S-CH3,-S-CH2-CH3, -O-CH3, або -O-CH2-CH3 і їх солі, сольвати або солі сольватів. Іншим аспектом винаходу є сполуки згідно принаймні одному з пунктів 1-4 в енантіомерно чистій формі і їх солі, сольвати або солі сольватів. Іншим аспектом винаходу є сполуки згідно пункту 1, вибрані зі списку, що включає 5-{[1-(2-Фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфаніл]-метил)пропіл]-аміно}-1H-хінолін-2-он 5-{[2-([Етилсульфаніл]-метил)-1-(2-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідроксипропіл]аміно}-1H-хінолін-2-он 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфаніл]метил)-пропіл]-аміно}-1H-хінолін-2-он 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-([етилсульфаніл]-метил)-3,3,3-трифторо-2гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(метоксиметил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он 3 UA 100251 C2 5 10 15 20 25 30 35 40 45 50 55 60 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-(етоксиметил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{[1-(5-Хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{[1-(5-Хлоро-3-фторо-2-метоксифеніл)-2-(хлорометил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он 5-{[3,3,3-Трифторо-2-гідрокси-2-([метоксиметил)-1-фенілпропіл]-аміно}-1H-хінолін-1-он 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-(діамінометил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он 5-{[1-(4-Хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(метоксиметил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-(етоксиметил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он 5-{[1-(2-Хлоро-3-фторо-4-гідроксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он і їх солі, сольвати або солі сольватів. Ще іншим аспектом винаходу є енантіомерно чисті сполуки згідно пункту 1, вибрані зі списку, що включає 5-{[1-(2-Фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфаніл]-метил)пропіл]-аміно}-1H-хінолін-2-он 5-{[2-([Етилсульфаніл]-метил)-1-(2-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідроксипропіл]аміно}-1H-хінолін-2-он 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфаніл]метил)-пропіл]-аміно}-1H-хінолін-2-он 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-([етилсульфаніл]-метил)-3,3,3-трифторо-2гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(метоксиметил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-(етоксиметил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{[1-(5-Хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{[1-(5-Хлоро-3-фторо-2-метоксифеніл)-2-(хлорометил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он 5-{[3,3,3-Трифторо-2-гідрокси-2-([метоксиметил)-1-фенілпропіл]-аміно}-1H-хінолін-1-он і їх солі, сольвати або солі сольватів. Іншим аспектом винаходу є енантіомерно чисті сполуки згідно пункту 1, вибрані зі списку, що включає 5-{(1S, 2R)[1-(2-Фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфаніл]метил)-пропіл]-аміно}-1H-хінолін-2-он 5-{(1S, 2R)[2-([Етилсульфаніл]-метил)-1-(2-фторо-4-метоксифеніл)-3,3,3-трифторо-2гідроксипропіл]-аміно}-1H-хінолін-2-он 5-{(1S, 2R)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2([метилсульфаніл]-метил)-пропіл]-аміно}-1H-хінолін-2-он 5-{(1S, 2R)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-([етилсульфаніл]-метил)-3,3,3-трифторо2-гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{(1S, 2S)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2(метоксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{(1S, 2S)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-(етоксиметил)-3,3,3-трифторо-2гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{(1S, 2S)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2(гідроксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{(1S, 2S)[1-(5-Хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2(гідроксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{(1S, 2R)[1-(5-Хлоро-3-фторо-2-метоксифеніл)-2-(хлорометил)-3,3,3-трифторо-2гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он 4 UA 100251 C2 5-{(1S, 2S)[3,3,3-трифторо-2-гідрокси-2-([метоксиметил)-1-фенілпропіл]-аміно}-1H-хінолін-1он 5 10 15 20 25 30 35 40 45 50 55 60 5-{[(1S, 2R)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-(діамінометил)-3,3,3-трифторо-2гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{(1S, 2S)[1-(2-Хлоро-3-фторо-4-гідроксифеніл)-3,3,3-трифторо-2-гідрокси-2(гідроксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он і їх солі, сольвати або солі сольватів. Додатковим аспектом винаходу є енантіомерно чисті сполуки згідно пункту 1, вибрані зі списку, що включає 5-{(1S, 2R)[1-(2-Фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфаніл]метил)-пропіл]-аміно}-1H-хінолін-2-он 5-{(1S, 2R)[2-([Етилсульфаніл]-метил)-1-(2-фторо-4-метоксифеніл)-3,3,3-трифторо-2гідроксипропіл]-аміно}-1H-хінолін-2-он 5-{(1S, 2R)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2([метилсульфаніл]-метил)-пропіл]-аміно}-1H-хінолін-2-он 5-{(1S, 2R)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-([етилсульфаніл]-метил)-3,3,3-трифторо2-гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{(1S, 2S)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2(метоксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{(1S, 2S)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-(етоксиметил)-3,3,3-трифторо-2гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{(1S, 2S)[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2(гідроксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{(1S, 2S)[1-(5-Хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2(гідроксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{(1S, 2R)[1-(5-Хлоро-3-фторо-2-метоксифеніл)-2-(хлорометил)-3,3,3-трифторо-2гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-{(1S, 2S)[3,3,3-Трифторо-2-гідрокси-2-([метоксиметил)-1-фенілпропіл]-аміно}-1H-хінолін-1он і їх солі, сольвати або солі сольватів. 1 2 3 Сполуки загальної формули I, де принаймні один з R , R або R є відмінним від водню, є одним переважним варіантом втілення винаходу. 1 2 3 Сполуки загальної формули I згідно пунктам 1-7, де принаймні один з R , R або R є відмінним від водню, є одним переважним варіантом втілення винаходу. 1 2 3 У іншому варіанті втілення два з R , R або R згідно пункту 1 або пунктам 1-7 є відмінними від водню. 1 2 3 У ще додатковому варіанті втілення всі три R , R або R згідно пункту 1 або пунктам 1-7 є відмінними від водню. У одному аспекті винаходу алкільні групи сполук формули (I) мають 1-5 атомів вуглецю. У іншому аспекті алкільні групи сполук формули (I) мають 1-3 атоми вуглецю. 4 Хінолонове кільце формули I може бути заміщеним радикалом R , вибраним з групи, що містить галоген, гідроксигрупу, (C1-C5)-алкіл, (C1-C5)-алкоксигрупу, (C1-C5)-алкілтіогрупу, (C1-C5)7 8 9 7 8 перфтороалкіл, ціаногрупу, нітрогрупу, NR R COOR (CO)NR R або (C1-C5-алкілен)-O-(CO)-(C14 C5)-алкільну групу, переважно R вибраний з групи C1-C3-алкіл, C1-C3-алкоксигрупа, 4 гідроксигрупа, галоген. У іншому аспекті винаходу R вибраний з групи водень, C1-C3-алкіл, галоген, гідроксигрупа, переважно з водню або галогену, переважніше з водню, хлору або фтору. 4 Іншим об'єктом винаходу є сполуки згідно формули 1, де R означає водень або фтор. 4 Ще іншим об'єктом винаходу є сполуки згідно формули 1, де R означає фтор. 4 Особливіші сполуки згідно формули I, де R означає 7-фторо-замісник або водень і 1 2 3 5 принаймні один з R , R і R вибраний з хлору, фтору, метоксигрупи, гідроксигрупи, R вибраний з S-CH2-CH3, -O-CH2-CH3, -S-CH3, -O-CH3 -, N(CH3)2, -OH і –Cl. 4 Іншим аспектом винаходу є сполуки згідно формули I, де R означає 7-фторо-замісник або 1 2 3 5 водень і принаймні один з R , R і R вибраний з хлору, фтору, метоксигрупи, R вибраний з S-CH2-CH3, -O-CH2-CH3, -S-CH3, -O-CH3 -, -OH і –Cl. Переважним аспектом винаходу є субкомбінації зі всіх груп, як розкрито в прикладах. Одним аспектом винаходу є сполуки загальної формули I, де фенільна група заміщена 1-3 1 2 3 1 2 однаковими або різними замісниками R , R і R . R і R незалежно один від одного, означають атом водню, гідроксигрупу, атом галогену, необов'язково заміщену (C 1-C10)-алкільну групу, необов'язково заміщену (C1-C10)-алкоксильну групу, (C1-C10)-алкілтіогрупу, (C1-C5) 5 UA 100251 C2 1 5 10 15 20 25 30 35 40 45 50 55 2 перфтороалкільну групу, ціаногрупу, нітрогрупу, або R і R разом означають групу, вибрану з груп -O-(CH2)p-O-, –O-(CH2)p-CH2-, -O-CH=CH-, -(CH2)p+2-, -NH-(CH2)p+1, -N(C1-C3-алкіл)-(CH2)p+1, і -NH-N=CH-, при цьому p=1 або 2, і термінальні атоми кисню і/або атоми вуглецю і/або атоми 1 2 азоту зв'язані з безпосередньо суміжними кільцевими атомами вуглецю, або R і R означають 6 7 6 7 NR R , при цьому R і R , незалежно один від одного, означають водень, C1-C5-алкіл або (CO)(C1-C5)-алкіл. 3 Третій замісник R означає атом водню, гідроксигрупу, атом галогену, ціаногрупу, необов'язково заміщену (C1-C10)-алкільну групу, (C1-C10)-алкоксильну групу, (C1-C10)алкілтіогрупу, або (C1-C5)-перфтороалкільну групу. У іншому аспекті будь-яка інша фенільна група може бути заміщеною групою, вибраною з C1-C3-алкоксигрупи, гідроксигрупи, і галогену, особливо метоксигрупи, гідроксигрупи, фтору, хлору, або брому. 5 У іншому аспекті винаходу R сполук пунктів 1-6, вибрані з -(C1-C10)-алкілу, який може бути необов'язково частково або повністю галогенованим, -(C2-C10)-алкенілу, -(C2-C10)-алкінілу, (C3-C7)-циклоалкіл-(C1-C8)-алкілу, (C3-C7)-циклоалкіл-(C2-C8)-алкенілу, (C3-C7)циклоалкіл-(C1-C8)-алкінілу, гетероцикліл-(C1-C8)-алкілу, гетероцикліл-(C2-C8)-алкенілу, 8 8 8 8 гетероцикліл-(C2-C8)-алкінілу, -R , R -(C1-C8)-алкілу, R -(C2-C8)-алкенілу, R -(C2-C8)-алкінілу, 8 8 6 7 6 -S-(C1-C10)-алкілу, -SO2-(C1-C10)-алкіл-S-R , -SO2-R , -CN, -Hal, -O-(C1-C10)-алкілу, -NR R (де R , 7 8 R мають визначені вище значення), -O-R і -OH за винятком -CH(CH3)2, або -C(CH3)=CH2. У ще 5 іншому аспекті R вибраний з групи, що складається з -(C1-C10)-алкілу, який може бути необов'язково частково або повністю галогенованим, -(C2-C10)-алкенілу, -(C2-C10)-алкінілу, -(C3-C7)-циклоалкіл-(C1-C8)-алкілу, -(C3-C7)-циклоалкіл-(C2-C8)-алкенілу, -S-(C1-C10)-алкілу, 6 7 6 7 -SO2-(C1-C10)-алкілу, -CN, -Hal, -O-(C1-C10)-алкілу, -NR R (де R , R мають визначені вище 5 значення), -OH за винятком -CH(CH3)2, або -C(CH3)=CH2, переважно R означає –OH, Cl, -S-CH3, -S-CH2-CH3, -S-CH2-CH2-CH3, -O-CH3, -O-CH2-CH3, -O-CH2-CH2-CH3, N(CH3)2, NHCH3 за винятком 5 -CH(CH3)2, або -C(CH3)=CH2, R переважніше означає -OH, –S-CH3, -S-CH2-CH3, -O-CH3, -O-CH2-CH3 або N(CH3)2. 5 У іншому аспекті винаходу R сполук пунктів 1-6 вибраний з (C3-C7)-циклоалкіл-(C1-C8)алкілу, (C3-C7)-циклоалкіл-(C2-C8)-алкенілу, (C3-C7)-циклоалкіл-(C1-C8)-алкінілу, 8 гетероцикліл-(C1-C8)-алкілу, гетероцикліл-(C2-C8)-алкенілу, гетероцикліл-(C2-C8)-алкінілу, -R , 8 8 8 R -(C1-C8)-алкілу, R -(C2-C8)-алкенілу, R -(C2-C8)-алкінілу, -S-(C1-C10)-алкілу, -SO2-(C1-C10)-алкіл8 8 6 7 6 7 S-R , -SO2-R , -CN, -Hal, -O-(C1-C10)-алкілу, -NR R (де R , R мають визначені вище значення), 8 O-R і -OH. 5 У ще іншому аспекті R сполук пунктів 1-6 вибраний з групи, що складається з -(C3-C7)циклоалкіл-(C1-C8)-алкілу, -(C3-C7)-циклоалкіл-(C2-C8)-алкенілу, -S-(C1-C10)-алкілу, 6 7 6 7 SO2-(C1-C10)-алкілу, -CN, -Hal, -O-(C1-C10)-алкілу, -NR R (де R , R мають визначені вище 5 значення), -OH; переважно R означає –OH, Cl, -S-CH3, -S-CH2-CH3, -S-CH2-CH2-CH3, -O-CH3, 5 -O-CH2-CH3, -O-CH2-CH2-CH3, N(CH3)2, NHCH3, R переважніше означає –OH, –S-CH3, S-CH2-CH3, -O-CH3, -O-CH2-CH3 або N(CH3)2. 5 8 Інший аспект винаходу належить до сполук згідно пунктам 1-6, де R вибраний з -R , 8 8 6 7 6 S-(C1-C10)-алкілу, -SO2-(C1-C10)-алкілу, -S-R , -SO2-R , -CN, -Hal, -O-(C1-C10)-алкілу, -NR R , де R , 7 8 R має значення, визначені в пункті 1, -O-R або -OH. 5 Інший аспект винаходу належить до сполук згідно пунктам 1-6, де R вибраний з 6 7 6 7 S-(C1-C10)-алкілу, -SO2-(C1-C10)-алкілу, -CN, -Hal, -O-(C1-C10)-алкілу, -NR R , де R , R має значення, визначені в пункті 1, або -OH. 5 Інший аспект винаходу належить до сполук згідно пунктам 1-6, де R вибраний з -S-(C1-C10)6 7 6 7 алкілу, -O-(C1-C10)-алкілу, -NR R , де R , R має значення, визначені в пункті 1, або -OH. 5 Одним аспектом винаходу є сполуки згідно пунктам 1-7, де R не означає -(C1-C10)-алкіл або -(C2-C10)-алкеніл. Інший аспект дійсного винаходу означає сполуки загальної формули I згідно пунктам 1-7, де 5 1 2 3 R не означає -(C1-C10)-алкіл або -(C2-C10)-алкеніл і з R /R /R принаймні два є відмінними від 1 2 3 4 водню або R /R /R всі є відмінними від водню і R означає галоген. До того ж, винахід належить до застосування сполук загальної формули I для виготовлення фармацевтичних агентів, так само як до їх застосування для виготовлення фармацевтичних агентів для лікування запальних захворювань. Визначення Якщо не заявлено інакше термін "алкіл" відноситися до нерозгалуженого або розгалуженого, заміщеного або незаміщеного ланцюга. Наприклад, термін пропіл включає н-пропіл і ізо-пропіл, термін бутил включає н-бутил, ізо-бутил і трет-бутил. 6 UA 100251 C2 5 10 15 20 25 30 35 40 45 50 55 Алкільні групи можуть бути нерозгалуженими або розгалуженими і означають напр. метил, етил, н-пропіл, ізо-пропіл, н-бутил, ізо-бутил, трет-бутил або н-пентильну групу, або 2,2диметилпропіл, 2-метилбутил або 3-метилбутильну групу. Метильна або етильна група є переважними. Вони можуть необов'язково бути заміщеними 1-3 гідроксигрупами, ціаногрупами, галогенами, 1-3 C1-C5-алкоксильними групами, і/або 1-3 COO(C1-C10-алкільной або бензильною) групами. Переважними є гідроксигрупи. Загальне число замісників залежить від числа атомів вуглецю ланцюга. Як правило, число замісників не перевищує числа атомів вуглецю за винятком галогену, що приводить до максимального числа замісників, напр. перфторовані алкільні групи. Для частково або повністю фторованої C1-C3-алкільної групи, розглядаються наступні частково або повністю фторовані групи: фторометил, дифторометил, трифторометил, фтороетил, 1,1-дифтороетил, 1,2-дифтороетил, 1,1,1-трифтороетил, тетрафтороетил, і пентафтороетил. З останніх, трифторометильна група або пентафтороетильна група є переважними. 1 2 3 5 C1-C5-алкоксильні групи в R , R , R і R можуть бути нерозгалуженими або розгалуженими і означають метоксигрупу, етоксигрупу, н-пропоксигрупу, ізо-пропоксигрупу, н-бутоксигрупу, ізобутоксигрупу, трет-бутоксигрупу або н-пентоксигрупу, 2,2-диметилпропоксигрупу, 2метилбутоксигрупу або 3-метилбутоксигрупу. Метоксигрупа або етоксигрупа є переважними. Вони можуть необов'язково бути заміщеними C 1-C5-алкільними групами, ціаногрупами або галогеном. C1-C5-алкілтіогрупи можуть бути нерозгалуженими або розгалуженими і означають метилтіогрупу, етилтіогрупу, н-пропілтіогрупу, ізо-пропілтіогрупу, н-бутилтіогрупу, ізобутилтіогрупу, трет-бутилтіогрупу або н-пентилтіогрупу, 2,2-диметилпропілтіогрупу, 2метилбутилтіогрупу або 3-метилбутилтіогрупу. Метилтіогрупа або етилтіогрупа є переважними. Термін атом галогену, Hal або галоген означає атом фтору, хлору, брому або йоду. Переважним є атом фтору, хлору або брому. 6 7 NR R група включає, наприклад, NH2, N(H)CH3, N(CH3)2, N(H)(CO)CH3, N(CH3)(CO)CH3, N[(CO)CH3]2, N(H)CO2CH3, N(CH3)CO2CH3, або N(CO2CH3)2. Термін C2-C8-алкеніл означає нерозгалужений або розгалужений, заміщений або незаміщений ланцюг, включаючи ізомери, що мають E- або Z-конфігурований подвійний зв'язок, такі як напр. вініл, пропен-1-іл, пропен-2-іл (Аліл), бут-1-ен-1-іл, бут-1-ен-2-іл, бут-2-ен-1-іл, бут2-ен-2-іл, 2-метил-проп-2-ен-1-іл, 2-метил-проп-1-ен-1-іл, бут-1-ен-3-іл, бут-3-ен-1-іл. Якщо алкенільний залишок знаходиться між двома іншими фрагментами, термін алкеніл означає алкенілен, такий як напр. вінілен, пропен-1-ілен, пропен-2-ілен (Алілен), бут-1-ен-1-ілен, бут-1ен-2-ілен, бут-2-ен-1-ілен, бут-2-ен-2-ілен, 2-метил-проп-2-ен-1-ілен, 2-метил-проп-1-ен-1-ілен, бут-1-ен-3-ілен, бут-3-ен-1-ілен. Термін C2-C8-алкініл означає нерозгалужений або розгалужений ланцюг напр. -CCH, -CH2-CCH, -CC-CH3, -CH(CH3)-CCH, -CC-CH2(CH3), -C(CH3)2-CCH, -CC-CH(CH3)2, -CH(CH3)-CC-CH3, -CH2-CC-CH2(CH3) або, якщо алкінільний залишок знаходиться між двома іншими фрагментами, термін алкініл означає алкінілен, такий як напр. -CC-, -CH2-CC-, -CC-CH2-, -CH(CH3)-CC-, -CC-CH(CH3)-, -C(CH3)2-CC-, -CC-C-(CH3)2-, -CH(CH3)-CC-CH2-, -CH2-CC-CH(CH3)-. Термін C3-C7-циклоалкіл означає заміщену або незаміщену групу, вибрану з циклопропілу, циклобутилу, циклопентилу, циклогексилу, циклогептилу. Можливі замісники можуть бути 4 5 вибрані з гідроксигрупи, галогену, (C1-C5)-алкілу, (C1-C5)-алкоксигрупи, NR R , COO(C1-C5)алкілу, CHO, ціаногрупи. Термін C3-C7-циклоалкіл-(C1-C10)-алкіл- означає напр. –(CH2)-циклоалкіл, -(C2H4)-циклоалкіл, -(C3H6)-циклоалкіл, -(C4H8)-циклоалкіл, -(C5H10)-циклоалкіл, при цьому циклоалкіл означає напр. циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил. Термін C3-C7-циклоалкіл-(C2-C8)-алкеніл означає напр. –(CH=CH)-циклоалкіл, -[C(CH3)=CH]циклоалкіл, -[CH=C(CH3)]-циклоалкіл, -(CH=CH-CH2)-циклоалкіл, -(CH2-CH=CH)-циклоалкіл, -(CH=CH-CH2-CH2)-циклоалкіл, -(CH2-CH=CH-CH2)-циклоалкіл, -(CH2-CH2-CH=CH)-циклоалкіл, -(C(CH3)=CH-CH2)-циклоалкіл, -(CH=C(CH3)-CH2)-циклоалкіл, при цьому термін циклоалкіл визначений вище. Термін гетероцикліл означає напр. піперидиніл-, морфолініл-, тіоморфолініл-, піперазиніл-, тетрагідрофураніл-, тетрагідротієніл-, імідазолідинілабо піролідиніл-, при цьому гетероциклільна група може бути зв'язана через будь-який можливий кільцевий атом. Гетероциклільна група може бути заміщена C1-C5-алкілом (необов'язково заміщеним), гідрокси-, 4 5 8 C1-C5-алкокси-, NR R -, галогеном, ціано-, COOR -, CHO-. Якщо можливо ці замісники можуть 7 UA 100251 C2 5 10 15 20 25 30 35 40 45 50 55 бути пов'язані з одним з вільних атомів азоту, якщо вони є. N-оксиди також включені в це визначення. Термін гетероцикліл-(C1-C10)-алкеніл- означає алкіленову групу як визначено вище, яка пов'язана з гетероциклільною групою, яка також раніше визначена вище. Термін гетероцикліл-(C2-C8)-алкеніл- означає алкіленіленову групу як визначено вище, яка пов'язана з гетероциклільною групою, яка також раніше визначена вище. Термін арил в сенсі винаходу означає ароматичне або частково ароматичне карбоциклічне кільце, що має від 6 до 14 атомів вуглецю, напр. феніл, і яке також може мати друге або третє сконденсоване кільце, таке як напр. нафтил або антраніл. Додатковими прикладами є феніл, нафтил, тетралініл, антраніл, бензоксазинон, дигідроіндолон, інданіл, і інденіл. Арильні групи можуть бути заміщені в будь-якій позиції, що приводить до стабільної молекули, одним або декількома замісниками, напр. 1-3 замісниками, такими як напр. гідроксигрупа, галоген, C1-C5-алкіл, C1-C5-алкоксигрупа, ціаногрупа, CF3, нітрогрупа, COO(C1-C5алкіл або бензил) або гетероарильна група, переважно 1-3 C1-C5-алкільними групами, гідроксилами, галогенами, ціаногрупами або C1-C5-алкоксигрупами. Необов'язково заміщена фенільна група є одним аспектом винаходу. Ще одним аспектом є 8 сполуки формули I, при цьому R не означає феніл. Термін гетероарил означає ароматичну кільцеву систему, що має 1-3 гетероатоми, вибраних з азоту, кисню або сірки, для пятичленних кілець максимальне число гетероатомів дорівнює трьом, при цьому допускаються лише два атоми кисню або сірки за умови, що вони не зв'язані безпосередньо один з одним. Можливими гетероарильними кільцями є напр. тієніл, фураніл, піроліл, оксазоліл, тіазоліл, імідазоліл, піразоліл, ізоксазоліл, ізотіазоліл, оксадіазоліл, триазоліл, тіадіазоліл, бензофураніл, бензотієніл, бензотіазол, бензоксазоліл, бензімідазоліл, індазоліл, індоліл, ізоіндоліл, піридил, піридазиніл, піримідиніл, піразиніл, триазиніл, азаіндолізиніл, бензопіридил, бензопіридазиніл, бензопіримідиніл, бензопіразиніл, бензотриазиніл, хіноліл, ізохіноліл, фталідил-, тіофталідил, індолоніл-, дигідроіндолоніл-, ізоіндолоніл, дигідроізоіндолоніл-, бензофураніл- або бензімідазоліл. Сполуки дійсного винаходу можуть існувати в стереоізомерних формах, таких як енантіомери діастереоізомерів залежно від їх структури і замісників як визначено у формулі I. У одному аспекті винаходу тому охоплені всі ці енантіомери, діастереоізомери або їх суміші. Виділення енантіомерно або діастереомерно чистих ізомерів може бути здійснене способами існуючого рівня техніки, напр. застосуванням колонкової хроматографії з хіральною нерухомою фазою. Якщо можливо, що сполуки винаходу також існують в таутомерних формах, вони також є аспектом дійсного винаходу. У одному аспекті винаходу охоплені всі сполуки, визначені у формулі I, так само як їх солі, сольвати і сольвати солей, особливо солі, сольвати і солі сольватів сполук, розкритих в прикладах, є одним аспектом винаходу, за умови, що розкриті сполуки самі вже не є солями, сольватами або сольватами солей. Солі в сенсі дійсного винаходу означають не лише фізіологічно придатні солі, але також солі, які можуть бути непридатними для фармацевтичного застосування, але які є корисними напр. при способі виділення або очищення. Термін фізіологічно придатні солі включає солі приєднання мінеральних кислот, карбонових кислот, сульфонових кислот, напр. солі хлористоводневої кислоти, бромистоводневої кислоти, сірчаної кислоти, азотної кислоти, фосфорної кислоти, метансульфонової кислота, етансульфонової кислоти, толуолсульфонової кислоти, бензолсульфонової кислоти, нафталінсульфонової кислоти, оцтової кислоти, трифторооцтової кислоти, пропіонової кислоти, молочної кислоти, винної кислоти, яблучної кислоти, лимонної кислоти, фумарової кислоти, півалевої кислоти, малеїнової кислоти, янтарної кислоти і бензойної кислоти. Крім того термін фізіологічно придатні солі включає солі звичайних підходящих основ, напр. солі лужних металів (напр. солі натрію і калію), лужноземельні солі (напр. солі кальцію і магнію) і амонієві солі, отримані з NH3 або органічних амінів з від 1 до 16 атомами вуглецю, напр. етиламін, діетиламін, триетиламін, етилдіізопропіламін, моноетаноламін, діетаноламін, триетаноламін, дициклогексиламін, диметиламіноетанол, прокаїн, дибензиламін, Nметилморфолін, аргінін, лізин, етилендіамін і N-метилпіперидин. Сольвати в сенсі винаходу означають такі форми сполук дійсних комбінацій, які створюють комплекси координацією з молекулами розчинника в рідкій або твердій фазі. Гідрати є особливими формами сольватів, в яких координовані молекули води. 8 UA 100251 C2 5 Солі в сенсі дійсного винаходу є не лише фізіологічно придатними солями, але також і солями, які можуть бути непридатними для фармацевтичного застосування, але які є корисними напр. при способі виділення або очищення. Сполуки можуть бути отримані двома способами, які описані нижче (а-b). Спосіб а) стадія а) NH2 4 R H 4 R 1 R (III) O 2 N H H O 1 R Ti(OR)4 і/або кислота 3 3 O R (II) 10 NH R R R N 2 (IV) Бензальдегіди типу (II) можуть конденсуватися із заміщеними амінохінолонами типу (III) з утворенням імінів типу (IV) із застосуванням кислот Льюїса, переважно алкоголятів титану Ti(OR)4, де R означає C1-C4-алкіл, такий як напр. тетраетил ортотитанат або тетра-третбутилортотитанат і/або в кислотних умов, напр. органічних кислот, таких як оцтова кислота як реагенти. Підходящими розчинниками є напр. толуол, 1,4-діоксан або їх суміші. Стадія b) O O 4 CF3 R CF3 H 1 1 (V) R R NH N NH 2 2 R R н-BuLi, -80° до -100°C 3 3 O R R 4 R 15 (IV) N H (VI) Стадія c) O 5 R OH CF3 1 R 5 R NH 2 CF3 1 Met R R NH 2 R 3 R 3 R 4 R N H O 4 R (VI) N H O (I) 20 25 Іміни типу (IV) обробляли при низьких температурах від -80° до -100 °C літійованим епоксидом (V) з одержанням сполуки типу (VI). Підходящими розчинниками є напр. тетрагідрофуран, гексан, діетиловий ефір або їх суміші. Епоксиди (VI) можуть бути розкриті 5 нуклеофілами типу R -Met даючи сполуку (I). Met означає метал і включає лужні метали, напр. натрій або літій, лужноземельні метали, такі як напр. магній, кальцій; алюміній, мідь, кремній 5 5 або олово (Sn) який пов'язаний з нуклеофільним залишком R в R -Met залежно від валентності 9 O UA 100251 C2 5 10 15 і згідно тому, як це відомо фахівцеві в даній галузі техніки. Отримуваними можливими 5 нуклеофільними реагентами R -Met є, напр. алкілкупрати, вінілкупрати, тіоли, алілсилани, 5 вінілсилани, вінілстанани, магнійорганічні сполуки, при цьому R визначається як в пункті 1, який реагує у присутності кислот Льюїса як напр. BF3 або AlMe3, AlCl3. Підходящими розчинниками є, напр. діетиловий ефір, диметилформамід, тетрагідрофуран. Епоксиди (VI) також можуть бути розкриті безпосередньо ціанідами, амінами, алкоголятами, тіоалкоголятами, галогенідами і навіть водою або Cs2CO3/H2O у присутності основ або сильних протонних кислот. Підходящими основами в сенсі винаходу є напр. Cs2CO3, K2CO3 або NaOH. Підходящими сильними протонними кислотами є напр. HClO4, HCl або HBr. Спосіб b) стадія а) O O O CF3 N CF3 1 1 R R (V) O O 2 2 R R н-BuLi, -80° до -100°C 3 3 R R (VII) (VIII) Метоксиметиламіди типу (VII) обробляли при низьких температурах від -80° до -100 °C літійованим епоксидом (V) з одержанням сполуки типу (VIII). Сполуки формули (VII) є комерційно доступними або можуть бути синтезовані згідно Branca et al, Chimia 49, 10; 1995, 381-385. стадія b) 5 R O OH CF3 5 R Met 1 R CF3 1 R O 2 R O 2 R 3 R 3 R 20 (VIII) (IX) 5 25 Епоксиди (VIII) можуть бути розкриті нуклеофілами типу R -Met даючи сполуку (IX). Можливими нуклеофілами є алкілкупрати, вінілкупрати, тіоли, алілсилани, вінілсилани, вінілстанани, магнійорганічні сполуки, у присутності кислот Льюїса як BF 3 або AlMe3, AlCl3, або безпосередньо ціаніди, аміни, спирти, тіоспирти, галогеніди і вода у присутності основ або сильних протонних кислот. Стадія с) NH2 5 R 5 R OH OH CF3 4 R (III) 1 R O 2 O N H 1 R 1. Ti(OR)4 / HOAc R NH 2 R 3 2. відновлення я 3 R CF3 R 4 R (IX) (I) 10 N H O UA 100251 C2 5 10 15 20 25 30 35 40 45 50 55 Кетон типу (IX) може конденсуватися із заміщеними амінохінолонами типу (III) даючи іміни і надалі або в той же час відновлюватися до аміноспиртів I за допомогою відновного амінування використовуючи комплексні гідриди як напр. NaBH4 або LiAlH4 (Katritzky et al. J.Org.Chem. 1995, 60, 7631-7640) або водень у присутності каталітичних кількостей паладію або платини або застосовуючи асиметричне органокаталізоване гідрування (List et al. Angew. Chem. 2005, 117, 7590-7593). Ці описані вище способи можуть бути здійснені енантіоселективно шляхом застосування енантіомерно чистого епоксиду формули (V) з одержанням енантіомерно чистих сполук формули (VI), (VIII), (IX) і (I). Остання стадія відновлення b) може бути здійснена діастереоселективним способом з одержанням енантіомерно чистої сполуки I коли як початковий матеріал використовують енантіомерно чисту сполуку IX. Альтернативно під час способу одержання сполук формули I на різних стадіях може бути здійснене очищення для одержання енантіомерно або діастереомерно чистих інтермедіатів, напр. інтермедіати формул VI, VIII, IX можуть бути очищені на стадії, коли вони виходять або можуть бути очищені сполуки формули I з одержанням енантіомерно або діастереомерно чистих кінцевих продуктів після завершення каскаду реакцій. Приклади способів для одержання енантіомерно чистої (енантіомерно чистих) сполуки описані нижче. Розділення оптичних ізомерів може бути здійснене розділенням одного або більше інтермедіатів і/або розділенням кінцевих продуктів. Як правило розділення інтермедіатів і розділення кінцевих продуктів є альтернативними варіантами, оскільки під час способу одержання не відбувається рацемізації. Якщо сполуки згідно винаходу знаходяться у вигляді рацемічної суміші, вони можуть бути розділені в чисті, оптично активні форми згідно способам розділення рацематів, які відомі фахівцеві в даній галузі техніки. Наприклад, рацемічні суміші можуть бути розділені за допомогою хроматографії на навіть оптично активному носієві (CHIRALPAK AD ) до чистих ізомерів. Також можливе застосування хіральних допоміжних агентів як оптично чисті кислоти. Для цих цілей вільну гідроксигрупу естерифікують з одержанням рацемічної сполуки загальної формули I за допомогою оптично активної кислоти, щоб розділити діастереоізомерні ефіри, які отримують фракційною кристалізацією або за допомогою хроматографії, і омилити розділені ефіри в кожному випадку до оптично чистих ізомерів. Як оптично активна кислота може використовуватися, наприклад, мигдалева кислота, камфорсульфонова кислота або винна кислоти. Таким чином одним аспектом винаходу є спосіб одержання сполуки формули I в діастереомерно чистій формі, необов'язково використовуючи хроматографію з колонками, що містять хіральний матеріал або використовуючи хіральні допоміжні агенти. Кожен з інтермедіатів синтезу сполук формули I є одним аспектом дійсного винаходу так само як особливо їх застосування для синтезу сполук формули I. Особливим аспектом винаходу є конкретні інтермедіати як використані для синтезу сполуки прикладів, або як рацемічна суміш або в їх енантіомерно (має один хіральний центр) або діастереомерно (має два хіральні центри) чистих формах. Зв'язування речовин з глюкокортикоїдним рецептором (GR) і іншими гормональними стероїдними рецепторами (мінеральний кортикоїдний рецептор (MR), рецептор прогестерону (PR) і рецептор андрогена (AR)) досліджене за допомогою рекомбінантно продукованих рецепторів. Цитозольні препарати клітин Sf9, які були заражені рекомбінантними бациловірусами, які кодуються GR, використовувалися для обов'язкових досліджень. В 3 порівнянні з еталонною речовиною [ H]-дексаметазоном, речовини показують від високої до дуже високої афіність до GR. Таким чином було виміряно IC 50 (GR) = 6.8 нМ, IC50 (GR) = 5.7 нМ і IC50 (GR) = 3.1 нМ і IC50 (GR) = 7.1 нМ для сполуки з Прикладів 1, 4, 5 і 7 відповідно. Як істотний, розглядався молекулярний механізм для протизапальної дії глюкокортикоїдів, GR-опосередковане інгібування транскрипції цитокінів, адгезивних молекул, ферментів і інших прозапальних чинників. Це інгібування продуковане взаємодією GR з іншими факторами транскрипції, наприклад, AP-1 і NF-каппа-B (для перевірки див. Cato, A. C. B., and Wade, E., BioEssays 18, 371-378, 1996). Сполуки загальної формули I відповідно винаходу інгібують секрецію цитокіна IL-8 в людській клітинній моноцитарній лінії THP-1, який ініційований ліпополісахаридом (LPS). Концентрація цитокінів була визначена в супернатанті за допомогою комерційно доступних комплектів ELISA. Сполука з Прикладів 4, 5, 7 і 8 показала інгібування IC 50 (IL8) = 0.61 нмоль, IC50 (IL8) = 0.19 нмоль, IC50 (IL8) = 0.44 нмоль і IC50 (IL8) = 3.1 нмоль з ефективністю 97 %, 98 %, 98 % і 80 % відповідно в порівнянні з дексаметазоном як еталоном. 11 UA 100251 C2 5 10 15 20 25 30 35 40 45 50 55 60 Антизапальна дія сполук загальної формули I була перевірена в експерименті з тваринними тестами із запаленням викликаним кротоновим маслом у щурів і мишей (J. Exp. Med. 1995, 182, 99-108). З цією метою було застосовано кротонове масло в етанольном розчині місцево на вухах тварин. Тестовані речовини були також застосовані місцево або систематично в той же час або за дві години до кротонового масла. Після 16-24 годин вага вуха була виміряна як критерій для запального набряку, активність пероксидази як критерій для інвазії гранулоцитів, і активність еластази як критерій для інвазії нейтрофільних гранулоцитів. У цьому тесті сполуки загальної формули І інгібують три вищезазначені параметри запалення і після місцевого введення, і після загального введення. Однією з найчастіших небажаних дій глюкокортикоїдної терапії є так званий "стероїдний діабет" [див, Hatz, H. J., Glucocorticoide: Immunologische Grundlagen, Pharmakologie und Therapierichtlinien [Glucocorticoids: Immunological Bases, Pharmacology and Therapy Guidelines], Wissenschaftliche Verlagsgesellschaft mbH, Stuttgart, 1998]. Причиною для нього є стимуляція глюконеогенезу в печінці індукцією ферментів, відповідальних в цьому відношенні і вільними амінокислотами, які генеруються з розщеплювання білків (катаболічна дія глюкокортикоїдів). Ключовим ферментом катаболічного метаболізму в печінці є тирозинаміно трансфераза (ТАТ). Активність цього ферменту може бути визначена з печінкових гомогенатів фотометрією і представляє гарну оцінку небажаних метаболічних дій глюкокортикоїдів. Щоб виміряти індукцію ТАТ, тварин вбивали через 8 годин після того, як ввели тестовані речовини, печінку видаляли, і активність ТАТ вимірювали в гомогенаті. У цьому тесті, при дозах, в яких вони мали антизапальну активність, сполуки загальної формули І індукують незначну кількість або не індукують тирозинаміно трансферазу. Внаслідок своєї протизапальної і, крім того, антиалергічної, імунодепресивної і антипроліферативної дії, сполуки загальної формули I відповідно винаходу можуть використовуватися як лікарські засоби для лікування або профілактики наступних патологічних станів у ссавців і людей: В цьому випадку, термін "захворювання" визначається наступними ознаками: (i) Легеневі захворювання, які супроводжуються запальними, алергічними і/або проліферативними процесами: - Хронічні обструктивні легеневі захворювання будь-якого походження, переважно бронхіальна астма - Бронхіти різного походження - Синдром розладу дихання у дорослих (СРДД), синдром гострої дихальної недостатності - Бронхоектазія - Всі форми рестриктивних легеневих захворювань - Всі форми легеневого набряку, переважно токсичний легеневий набряк, напр. радіогенний пневмоніт - Саркоїдози і гранулематози, особливо захворювання Бека (ii) Ревматичні/ аутоіммунні захворювання/захворювання суглобів, які супроводжуються запальними, алергічними і/або проліферативними процесами: - Всі форми ревматизмів, особливо ревматоїдний артрит, ревматична атака, ревматична поліміалгія, захворювання Бехчета - Реактивний артрит - Запальні захворювання м'якої тканини інших походжень - Симптоми артриту в разі дегенеративних захворювань суглоба (артроз) - Травматичні артрити - Вітиліго - Колагенози будь-якого походження, напр. системні червоні вовчаки, склеродермія, поліміозит, дерматоміозит, синдром Шегрена, синдром Стілла, синдром Фелті - Саркоїдози і грануломатози - Ревматизм м'якої тканини (iii) Алергії або псевдоалергічні захворювання, які супроводжуються запальними, алергічними і/або проліферативними процесами: - Всі форми алергічних реакцій, напр. набряк Квінке, сінна лихоманка, укуси комахи, алергічні реакції на фармацевтичні препарати, похідні крові, контрастне середовище, тощо, анафілактичний шок, уртикарія, алергічний і подразнюючий контактний дерматит, алергічні судинні захворювання - Алергічний васкуліт (iv) Васкулярні запалення (васкуліти) - Панартеріїт нодозний, темпоральний артеріїт, нодозна еритема 12 UA 100251 C2 5 10 15 20 25 30 35 40 45 50 55 - Поліартеріїт нодозний - Гранулематоз Вегенера - Гігантоклітинний артеріїт (v) Дерматологічні захворювання, які супроводжуються запальними, алергічними і/або проліферативними процесами: - Атопічні дерматити (переважно у дітей) - Всі форми екземи, такі як, напр. атопічна екзема (переважно у дітей) - Висипання будь-якого походження або дерматози - Групи псоріазу і парапсоріазу - Червоний волосистий пітиріаз - Еритематозний захворювання, викликані різними згубними для здоров'я чинниками, напр. радіація, хімікати, опіки, тощо - Булезні дерматози, такі як, напр. аутоіммунна звичайна пухирчатка, булезний пемфігоїд - Захворювання ліхеноїдної групи - Пруріт (напр. алергічного походження) - Себорейна екзема - Група розацеа - Еритема багатоформова ексудативна - Баланіт - Вульвіт - Прояв васкулярних захворювань - Облисіння таке як гніздова алопеція - Шкірна лімфома (vi) Ниркові захворювання, які супроводжуються запальними, алергічними і/або проліферативними процесами: - Нефротичний синдром - Всі нефрити, напр., гломерулонефрит (vii) Печінкові захворювання, які супроводжуються запальними, алергічними і/або проліферативними процесами: - Гостре розкладання печінкових клітин - Гострий гепатит різних походжень, напр., вірусного, токсичного, викликаного фармацевтичним препаратом - Хронічний агресивний гепатит і/або хронічний інтермітуючий гепатит (viii) Шлунково-кишкові захворювання, які супроводжуються запальними, алергічними і/або проліферативними процесами: - Регіонарний ентерит (захворювання Крону) - Виразковий коліт - Гастрит - Рефлюксний езофагіт - Виразковий коліт іншого походження, напр. природні виразкові афти (ix) Проктологічні захворювання, які супроводжуються запальними, алергічними і/або проліферативними процесами: - Анальна екзема - Тріщини - Геморрої - Ідіопатичний проктит (x) Очні захворювання, які супроводжуються запальними, алергічними і/або проліферативними процесами: - Алергічний кератит, увеїт, ірит - Кон'юнктивіт - Блефарит - Неврит зорового нерва - Хоріоїдит - Симпатична офтальмія (xi) Захворювання вуха-горла-носа, які супроводжуються запальними, алергічними і/або проліферативними процесами: - Алергічний риніт, сінна лихоманка - Отит зовнішнього вуха, напр., викликаний контактним дерматитом, інфекцією, тощо - отит середнього вуха 13 UA 100251 C2 5 10 15 20 25 30 35 40 45 50 55 (xii) Неврологічні захворювання, які супроводжуються запальними, алергічними і/або проліферативними процесами: - Набряк мозку, переважно набряк мозку викликаний пухлиною - Множинний склероз - Гострий енцефаломієліт - Менінгіт - Різні форми конвульсій, напр. дитячі кивальні судоми - Гостре пошкодження спинного мозку - Апоплексичний удар (xiii) Захворювання крові, які супроводжуються запальними, алергічними і/або проліферативними процесами, такі як, напр.: М. Ходжкинськая або неходжкинськая лімфома, тромбоцитемія, еритроцитози - Придбана гемолітична анемія - Ідіопатична тромбоцитопенія (xiv) Пухлинні захворювання, які супроводжуються запальними, алергічними і/або проліферативними процесами, такі як, напр.: карцинома або саркома - Гострий лімфолейкоз - Злоякісна лімфома - Лімфогранулематози - Лімфосаркома - Обширні метастази, головним чином при раках грудей, бронхів і простати (xv) Ендокринологічні захворювання, які супроводжуються запальними, алергічними і/або проліферативними процесами, такі як, напр: - Ендокринна орбітопатія - Тиреотоксичний криз - Тиреоїдит де Кервена - Тиреоїдит Хашимото - Базедова хвороба - Гранулематозний зоб - Хронічний лімфоматозний тиреоїдит (xvi) Пересадки органів і тканин, реакція "трансплантант проти господаря" (xvii) Важкі шокові стани, напр., анафілактичний шок, синдром системної запальної реакції (ССЗР) (xviii) Терапія заміни при таких захворюваннях: - Природжена переважно надниркова недостатність, напр. природжений адреногенітальний синдром - Придбана переважно надниркова недостатність, напр. захворювання Аддісона, аутоіммунний адреналіт, постінфекційні пухлини, метастази, тощо - Природжена вторинна надниркова недостатність, напр. природжений гіпопітуїтаризм - Придбана вторинна надниркова недостатність, напр., постінфекційні пухлини, тощо (xix) Нудота, яка поєднується із запальними, алергічними і/або проліферативними процесами: - напр., в комбінації з антагоністом 5-HT3 при цитостатик-індукованій блювоті (xx) Болі запального походження, напр. люмбаго (xxi) Інші різні стадії захворювання, включаючи діабет І типу (інсулінзалежний діабет), остеоартрит, синдром Гійєна-Баре, рестенози після черезшкірної транслюмінальної ангіопластики, захворювання Альцгеймера, гострий і хронічний біль, артеріосклероз, реперфузійне пошкодження, застійна серцева недостатність, інфаркт міокарду, термічне пошкодження, множинне ураження органів на фоні травми, гострий гнійний менінгіт, некротичний ентероколіт і синдроми пов'язані з гемодіалізом, лейкаферезом, і гранулоцитарною трансфузією. Крім того, сполуки загальної формули I відповідні винаходу можуть використовуватися для лікування і профілактики додаткових патологічних станів, які не згадані вище, для яких тепер використовуються синтетичні глюкокортикоїди (див. в цьому відношенні Hatz, H. J., Glucocorticoide: Immunologische Grundlagen, Pharmakologie und Therapierichtlinien, Wissenschaftliche Verlagsgesellschaft mbH, Stuttgart, 1998). Всі раніше згадані ознаки (i) - (xx) описані детальніше в Hatz, H. J., Glucocorticoide: Immunologische Grundlagen, Pharmakologie und Therapierichtlinien, Wissenschaftliche Verlagsgesellschaft mbH, Stuttgart, 1998. 14 UA 100251 C2 5 10 15 20 25 30 35 40 45 50 55 Всі згадані вище захворювання дійсно мають загальним те, що вони, як передбачається, виникають в результаті запальних, алергічних, імунодепресивних або антипроліферативних процесів. Таким чином, винахід також відносяться до способів лікування запальних, алергічних, імунодепресивних або антипроліферативних захворювань і застосування сполук формули I або їх фармацевтично прийнятної солі для виготовлення лікарського засобу для їх лікування. Одним спеціальним об'єктом є лікування запальних захворювань. Глюкокортікоїдний рецептор, як відомо, включений в процес запалення. Таким чином, іншим об'єктом винаходу є спосіб лікування хворобливого стану опосередкованого глюкокортикоїдним рецептором у ссавця, який включає введення ссавцеві, що потребує такого лікування, ефективної дози сполуки формули (I), або її фармацевтично прийнятної солі і застосування сполуки формули (I), або її фармацевтично прийнятної солі, за пунктом 1-6, для виготовлення лікарського засобу для застосування в лікуванні хворобливого стану, опосередкованого глюкокортикоїдним рецептором. Іншим об'єктом винаходу є сполуки формули (I), або їх фармацевтично прийнятна сіль, за пунктом 1-6 для застосування в терапії. Для терапевтичних дій при вищезазначених патологічних станах підходяща доза змінюється і залежить від, наприклад, активності сполуки загальної формули I, господаря, типу введення, і типу і серйозності станів, які потрібно лікувати, так само як від застосування і як профілактичний агент або як терапевтичний агент. На додаток, винахід забезпечує: (i) Застосування одної з сполук формули I відповідно винаходу або їх суміші для виробництва лікарського засобу для лікування ЗАХВОРЮВАННЯ; (ii) Спосіб лікування ЗАХВОРЮВАННЯ, вказаний спосіб включає введення кількості сполуки відповідно винаходу, де кількість пригнічує хворобу, і де кількість сполуки дається пацієнтові, який потребує такого лікарського засобу; (iii) Фармацевтичну композицію для лікування ЗАХВОРЮВАННЯ, вказане лікування включає одну із сполук відповідно винаходу або його суміш і принаймні один фармацевтичний ад'ювант і/або середовище. Взагалі, задовільні результати можуть очікуватися у тварин, коли щоденні дози включають діапазон 1 мкг – 100,000 мкг сполуки відповідно винаходу на кг маси тіла. В разі великих ссавців, наприклад людини, щоденна доза, що рекомендується, знаходиться в діапазоні 1 мкг – 100,000 мкг на кг маси тіла. Переважна доза 10-30,000 мкг на кг маси тіла, і переважніша доза 10-10,000 мкг на кг маси тіла. Наприклад, цю дозу відповідно вводять кілька разів щодня. Для лікування гострого шоку (наприклад, анафілактичного шоку), можуть бути дані окремі дози, які значно вище згаданих доз. Складання рецептур фармацевтичних препаратів, заснованих на нових сполуках, здійснюється шляхом, який відомий в галузі техніки, за допомогою активного компонента, що обробляється середовищами, які зазвичай використовуються в галенових препаратах, наповнювачами, речовинами, які впливають на розкладання, зв'язуючими агентами, зволожуючими речовинами, мастилами, абсорбентами, розчинниками, ароматичними коригентами, барвниками, тощо, і перетвореного в бажану форму введення. В цьому випадку, зроблено посилання на Remington's Pharmaceutical Science, 15th Edition, Mack Publishing Company, East Pennsylvania (1980). Для перорального введення придатні, особливо таблетки, таблетки з покриттям, капсули, пілюлі, порошки, гранули, таблетки для розсмоктування, суспензії, емульсії або розчини. Для парентерального введення можливі ін'єкційні і інфузійні препарати. Для внутрішньосуставної ін'єкції, можуть бути використані приготовані відповідним чином кристалічні суспензії. Для внутрішньом'язової ін'єкції можуть бути використані водні і масляні ін'єкційні розчини або суспензії і відповідні накопичувальні препарати. Для ректального введення, нові сполуки можуть бути використані у формі супозиторіїв, капсул, розчинів (напр. у формі клізми) і мазей, і те й інше для системного і для місцевого лікування. Для пульмонального введення нових сполук, останні можуть використовуватися у формі аерозолів і інгаляторів. Для місцевого застосування до очей, зовнішнього вуха, середнього вуха, носових западин, і параносових пазух, нові сполуки можуть використовуватися як краплі, мазі і настойки у відповідних фармацевтичних препаратах. 15 UA 100251 C2 5 10 15 20 25 30 35 40 Для зовнішнього застосування, є можливими препарати в гелях, мазях, жирних мазях, кремах, пастах, порошках, молочку і настойках. Дозування сполук загальної формули I в цих препаратах може бути 0.01 %-20 %, щоб досягти достатньої фармакологічної дії. Винахід також включає сполуки загальної формули I відповідно винаходу як терапевтичні активні компоненти. Крім того, сполуки загальної формули I відповідно винаходу є частиною винаходу як терапевтичні активні компоненти разом з фармацевтично сумісними і прийнятними ад'ювантами і середовищами. Винахід також включає фармацевтичну композицію, яка містить одну з фармацевтично активних сполук відповідно винаходу або їх суміш або їх фармацевтично сумісні солі і фармацевтично сумісні солі або фармацевтично сумісні ад'юванти і середовища. Сполуки загальної формули (I) відповідно винаходу можуть довільно також бути включені в склади і/або вводитися в комбінації з іншими активними компонентами. Винахід тому також належить до комбінованого лікування або комбінованих композицій, в яких сполука загальної формули (I) або її фармацевтично прийнятна сіль, або фармацевтична композиція, яка містить сполуку загальної формули (I) або її фармацевтично прийнятну сіль, вводяться або одночасно (необов'язково в тій же самій композиції) або по черзі разом з одним або більш фармацевтичними засобами для лікування одного з вищезазначених патологічних станів. Наприклад, для лікування ревматичного артриту, остеоартриту, ХОЗЛ (хронічне обструктивне захворювання легень), астми або алергічного риніту, сполука загальної формули (I) цього винаходу може бути скомбінована з одним або більш фармацевтичними засобами для лікування такого стану. Коли така комбінація вводиться інгаляцією, фармацевтичний засіб, з яким об'єднують, може бути вибраний з наступного списку: - Інгібітор PDE4, включаючи інгібітор ізоформи PDE4D - Селективний β.sub2. адреноміметик, такий як, наприклад, метапротеренол, ізопротеренол, ізопреналін, альбутерол, сальбутамол, формотерол, салметерол, тербуталін, орципреналін, бітолтерол, мезилат, пірбутерол або індакатерол; - Антагоніст мускаринового рецептора (наприклад, M1, M2 або M3 антагоніст, такий як, наприклад, більш селективний антагоніст M3), такий як, наприклад, іпратропію бромід, тіотропію бромід, окситропію бромід, пірензепін або телензепін; - Модулятор функції хемокінового рецептора (такий як, наприклад, антагоніст CCR1 рецептора); або - Інгібітор функції p38 кінази. Для іншого об'єкту цього винаходу така комбінація із сполукою загальної формули (I) або її фармацевтично прийнятною сіллю використовується для лікування ХОЗЛ, астми або алергічного риніту і може вводитися інгаляцією або перорально в комбінації з ксантином (таким як, наприклад, амінофілін або теофілін), який також може вводитися інгаляцією або перорально. Експериментальна частина: Різні аспекти винаходу, описані в дійсній заявці, ілюструються наступними прикладами, які в будь-якому разі не мають на увазі обмеження винаходу. Приклад 1 S F OH F F F NH O N H 45 50 55 O 5-{[1-(2-Фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфаніл]-метил)пропіл]-аміно}-1H-хінолін-2-он 5-{[(2-Фторо-4-метоксифеніл)(2-трифторометил-оксираніл)-метил]-аміно}-1H-хінолін-2-он До 600 мг (3.9 ммоль) 5-аміно-7-фторо-1H-хінолін-2-ону і 624 мг (3.9 ммоль) 2-фторо-4метоксибензальдегіду в 12 мл толуолу додавали 18 мкл оцтової кислоти і 2 г молекулярних сит. Суміш нагрівали протягом 25 год. при кипінні і після охолоджування фільтрували через подушку целіту. Розчинник випаровували і залишок двічі азеотропно випаровували з невеликими порціями толуолу з одержанням 5-{[1-(2-фторо-4-метоксифеніл)-метиліден]-аміно}-1H-хінолін-2ону кількісно. 0.81 мл (11.6 ммоль) 1,1,1-трифтороепоксипропану в 12 мл THF і 3.5 мл гексану охолоджували до -100 °C і додавали протягом 10 хв. 3.75 мл 2.5 M розчину н-бутиллітію (9.4 ммоль) в гексані, тоді як температура не перевищувала -95 °C. Через 10 хв. після закінчення додавання протягом 15 хв. додавали 1.11 г (12 ммоль) 5-{[1-(2-фторо-4метоксифеніл)-метиліден]-аміно}-1H-хінолін-2-ону у 10 мл THF, тоді як температура не 16 UA 100251 C2 5 10 15 перевищувала -95 °C. Через 3 год. при -100 °C додавали 3.75 мл діетилового ефіру і реакційну суміш нагрівали до -10 °C протягом однієї години. Реакцію гасили додаванням насиченого розчину хлориду амонію. Фази розділяли і водний шар двічі екстрагували етилацетатом, об'єднані органічні фази промивали розсолом, сушили над сульфатом натрію і потім випаровували. Флеш хроматографія на силікагелі (ацетон в гексані від 0 до 80 %) дає 410 мг 5{[(2-фторо-4-метоксифеніл)(2-трифторометил-оксираніл)-метил]-аміно}-1H-хінолін-2-ону. 1 H-ЯМР (CDCl3); = 2.59 (dq, 1H), 3.15 (d, 1H), 3.78 (s, 3H), 4.93 (d, 1H), 5.53 (d, 1H), 6.21 (d, 1H), 6.67 (m, 3H), 6.77 (d, 1H), 7.13 (t, 1H), 7.22 (t, 1H), 7.96 (d, 1H). До 50 мг (0.12 ммоль) 5-{[(2-фторо-4-метоксифеніл)(2-трифторометил-оксираніл)-метил]аміно}-1H-хінолін-2-ону і 80 мг Cs2CO3 в 0.5 мл DMF додавали 0.18 мл 1M розчину метилмеркаптану в DMF. Суміш інтенсивно перемішували протягом 4 год. і додавали воду. Водний шар екстрагували етилацетатом, органічні фази промивали розсолом і сушили над сульфатом натрію. Після видалення розчинника тонкошарова хроматографія на силікагелі (ацетон в гексані 50 %) дає 27 мг названої сполуки. 1 H-ЯМР (CDCl3); = 2.09 (s, 3H), 2.87 (d, 1H), 3.06 (d, 1H), 3.81 (s, 3H), 5.24 (d, 1H), 5.88 (d, 1H), 6.22 (d, 1H), 6.68 (m, 4H), 7.23 (t, 1H), 7.38 (t, 1H), 7.97 (d, 1H). Приклад 2 S F OH F F F NH O 39 N H 20 25 O 5-{[2-([Етилсульфаніл]-метил)-1-(2-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідроксипропіл]аміно}-1H-хінолін-2-он До 50 мг (0.12 ммоль) 5-{[(2-фторо-4-метоксифеніл)(2-трифторометил-оксираніл)-метил]аміно}-1H-хінолін-2-ону і 80 мг Cs2CO3 в 0.5 мл DMF додавали 14 мкл (0.18 ммоль) етилмеркаптану в DMF. Суміш інтенсивно перемішували протягом 4 год. і додавали воду. Водний шар екстрагували етилацетатом, органічні фази промивали розсолом і сушили над сульфатом натрію. Після видалення розчинника тонкошарова хроматографія на силікагелі (ацетон в гексані 50 %) дає 20 мг названої сполуки. 1 H-ЯМР (CDCl3); = 1.18 (t, 3H), 2.45 (dq, 2H), 2.85 (d, 1H), 3.09 (d, 1H), 3.81 (s, 3H), 5.19 (d, 1H), 5.82 (d, 1H), 6.21 (d, 1H), 6.68 (m, 4H), 7.23 (t, 1H), 7.38 (t, 1H), 7.98 (d, 1H). Приклад 3 S F OH F F Cl F NH O 30 35 40 45 F N H O 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфаніл]метил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он 2-Хлоро-3-фторо-4-метоксибензальдегід 1 г (6.2 ммоль) 3-хлоро-2-фтороанізолу в 20 мл THF охолоджували до -70 °C і додавали 2.7 мл 2.5 M розчину н-бутиллітію в гексані. Через одну годину при -70° додавали при -70 °C 3.93 мл DMF в 7 мл THF і суміш перемішували ще одну годину при -70 °C. Додавали 15 мл 1 M водного HCl і реакцію нагрівали до кімнатної температури протягом 18 год. Реакційну суміш розділяли між діетиловим ефіром і водою. Водну фазу екстрагували діетиловим ефіром, об'єднані органічні фази промивали розсолом, сушили над сульфатом натрію і випаровували. Сирий продукт очищали за допомогою хроматографії на силікагелі з одержанням 0.25 г 2-хлоро3-фторо-4-метоксибензальдегіду. 1 H-ЯМР (CDCl3); = 3.98 (s, 3H), 6.98 (dd, 1H), 7.75 (dd, 1H), 10.30 (s, 1H). 5-Аміно-7-фторо-1H-хінолін-2-он До розчину 2-бромо-3-фтороаніліну (6.5 г, 34.17 ммоль) і піридину (2.7 г, 34.17 ммоль) в 20 мл CH2Cl2, по краплях додавали цинамоїл хлорид (5.95 г, 35.88 моль) в 10 мл CH2Cl2 і суміш кип'ятили протягом 30 хв. Реакційну суміш розводили CH2Cl2, органічний шар промивали розведеною HCl, насиченим розчином Na2CO3, водою, і сушили (Na2SO4). Розчинник видаляли у вакуумі з одержанням 10.5 г N-(2-бромо-3-фторофеніл)-3-фенілакриламіду. До розчину N-(2 17 UA 100251 C2 5 10 15 20 25 30 35 40 45 50 55 60 бромо-3-фторофеніл)-3-фенілакриламіду (10.5 г, 32.8 ммоль) у 70 мл хлоробензолу при 130 °C частинами додавали AlCl3 (21.9 г, 0.164 моль), суміш перемішували при цій температурі 2 год. і виливали в льодяну воду. Осад відфільтровували і сушили. Вихід 6.05 г (76 %). 6 г (24.8 ммоль) 8-бромо-7-фторо-1H-хінолін-2-ону кип'ятили в 30 мл POCl3 протягом 2 год., потім виливали на лід, екстрагували бензолом. Бензольний екстракт сушили (Na 2SO4) з одержанням 6.1 г 8-бромо2-хлоро-7-фторохіноліну після видалення розчинника. До суміші 10 мл 10 %-олеуму і 1.4 г (22.2 ммоль) димлячої HNO3 частинами додавали 8-бромо-2-хлоро-7-фторохінолін (4.8 г 18.5 ммоль). Суміш нагрівали при 100 °C протягом 2 год. додатково додавали HNO3 (0.17 г) і перемішували додатково протягом 1 год. Реакційну суміш виливали в льодяну воду, екстрагували EtOAc, фільтрували через силікагель, і кристалізували з суміші гептан-толуол з одержанням 2.3 г (50 %) 8-бромо-2-хлоро-7-фторо-5-нітрохіноліну. 2.3 г (7.54 ммоль) 8-бромо-2хлоро-7-фторо-5-нітрохіноліну нагрівали при 100 °C протягом 5 год. у розчині, що містить 16 мл CH3COOH, 3.2 мл H2O і 5 мл конц. HCl. Суміш виливали у воду, отриманий осад відфільтровували, перемішували в EtOAc і фільтрували з одержанням 1.71 г 8-бромо-7-фторо5-нітро-1H-хінолін-2-ону. До суспензії 1.7 г (5.92 ммоль) 8-бромо-7-фторо-5-нітро-1H-хінолін-2ону і 2.3 г (35.5 ммоль) HCOONH4 в 10 мл етанолу додавали 0.1 г 10 % Pd-C, і перемішували протягом 2 год. при 60 °C. Осад зникає і потім формується знову. Осад відфільтровували, розчиняли в 3 мл DMSO і фільтрували через силікагель. До елюату додавали 15 мл води, осад відфільтровували і сушили з одержанням 0.5 г (47 %) 5-аміно-7-фторо-1H-хінолін-2-ону. 1 H-ЯМР (DMSO-d6); = 6.14 (dd, 1H), 6.20 (dd, 1H), 6.23 (d, 1H), 6.27 (br, 2H), 8.06 (d, 1H), 11.50 (br, 1H). 5-{[(2-Хлоро-3-фторо-4-метоксифеніл)(2-трифторометил-оксираніл)-метил]-аміно}-7-фторо1H-хінолін-2-он До 1.6 г (9 ммоль) 5-аміно-7-фторо-1H-хінолін-2-ону і 1.69 г (9 ммоль) 2-хлоро-3-фторо-4метоксибензальдегіду в 27 мл толуолу і 8 мл 1,4-діоксану додавали 1.96 мл оцтової кислоти і 7 мл тетрабутилортотитанату. Суміш нагрівали протягом 20 год. до 110 °C, охолоджували до кімнатної температури і виливали у водний розчин фториду амонію. Додавали етилацетат і суміш інтенсивно перемішували протягом 1 год. Фази розділяли і додавання етилацетату повторювали двічі з перемішуванням при кипінні і фази розділяли, поки вони ще гарячі. Об'єднані органічні фази концентрували і залишок очищали флеш хроматографією на силікагелі (етилацетат, потім метанол в дихлорометані від 15 % до 20 %) з одержанням 2.17 г 5-[1-(2хлоро-3-фторо-4-метоксифеніл)-метиліден]-аміно}-7-фторо-1H-хінолін-2-ону. 465 мг NaH (55 % у маслі, 9.7 ммоль) промивали сухим THF і суспендували разом з 2.6 г (7.5 ммоль) 5-{[1-(2-хлоро3-фторо-4-метоксифеніл)-метиліден]-аміно}-7-фторо-1H-хінолін-2-оном у 90 мл THF. Додавали трет-бутилдиметилсилілхлорид в твердому вигляді і суміш перемішували протягом 3.5 год. до утворення прозорого розчину. Паралельно 0.96 мл 1,1,1-трифторо-2,3-епоксипропану в 24 мл THF і 7 мл гексану охолоджували до -100 °C і додавали протягом 10 хв. 4.5 мл 2.5 M розчину н-бутиллітію в гексані, тоді як температура не перевищувала -95 °C. Через 10 хв. після закінчення додавання заздалегідь приготований розчин 1-{трет-бутилдиметилсиліл}-5-{[1-(2хлоро-3-фторо-4-метоксифеніл)-метиліден]-аміно}-7-фторохінолін-2-ону у THF додавали протягом 30 хв., тоді як температура не перевищувала -95 °C. Через 3 год. при -100 °C додавали 7.5 мл діетилового ефіру і реакційну суміш нагрівали до кімнатної температури протягом однієї години. Реакцію гасили додаванням насиченого розчину хлориду амонію. Після перемішування протягом 30 хв. фази розділяли і водний шар екстрагували дихлорометаном, об'єднані органічні фази промивали розсолом, сушили над сульфатом натрію і потім випаровували. Флеш хроматографія на силікагелі (етилацетат в гексані від 50 до 100 %) дає 2.14 г 5-{[(2-хлоро-3-фторо-4-метоксифеніл)(2-трифторометилоксираніл)-метил]-аміно}-7-фторо1H-хінолін-2-ону, який використовували в декількох наступних прикладах для розкриття оксиранового кільця різними нуклеофілами. 1 H-ЯМР (DMSO-d6); = 2.62 (m, 1H), 3.29 (d, 1H), 3.87 (s, 3H), 5.49 (d, 1H), 5.83 (d, 1H), 6.34 (d, 1H), 6.37 (d, 1H), 7.04 (d, 1H), 7.22 (dd, 1H), 7.44 (d, 1H), 8.31 (d, 1H), 11.63 (s, 1H). До 65 мг (0.14 ммоль) 5-{[(2-хлоро-3-фторо-4-метоксифеніл)(2-трифторометил-оксираніл)метил]-аміно}-7-фторо-1H-хінолін-2-ону і 92 мг (0.28 ммоль) Cs2CO3 в 0.5 мл DMF додавали 0.21 мл 1M розчину метилмеркаптану в DMF. Суміш інтенсивно перемішували протягом 20 год. і додавали воду. Водний шар екстрагували етилацетатом, органічні фази промивали розсолом і сушили над сульфатом натрію. Після видалення розчинника тонкошарова хроматографія на силікагелі (етилацетат) дає 22 мг названої сполуки. 1 H-ЯМР (CDCl3); = 1.91 (s, 3H), 2.68 (d, 1H), 3.04 (d, 1H), 3.87 (s, 3H), 5.21 (d, 1H), 5.80 (dd, 1H), 5.94 (d, 1H), 6.38 (dd, 1H), 6.57 (d, 1H), 6.87 (dd, 1H), 7.24 (dd, 1H), 7.84 (d, 1H). Приклад 4 18 UA 100251 C2 S F OH Cl F F F NH O F 5 10 N H O 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-([етилсульфаніл]-метил)-3,3,3-трифторо-2гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он До 66 мг (0.14 ммоль) 5-{[(2-хлоро-3-фторо-4-метоксифеніл)(2-трифторометил-оксираніл)метил]-аміно}-7-фторо-1H-хінолін-2-ону, отриманого в прикладі 3, і 93 мг (0.29 ммоль) Cs2CO3 в 0.6 мл DMF додавали 16 мкл (0.22 ммоль) етилмеркаптану в DMF. Суміш інтенсивно перемішували протягом 20 год. і додавали воду. Водний шар екстрагували етилацетатом, органічні фази промивали розсолом і сушили над сульфатом натрію. Після видалення розчинника тонкошарова хроматографія на силікагелі (етилацетат) дає 14 мг названої сполуки. 1 H-ЯМР (CDCl3); = 1.07 (t, 3H), 2.27 (dq, 2H), 2.69 (d, 1H), 3.06 (d, 1H), 3.88 (s, 3H), 5.20 (d, 1H), 5.79 (dd, 1H), 5.92 (d, 1H), 6.37 (dd, 1H), 6.57 (d, 1H), 6.87 (dd, 1H), 7.24 (dd, 1H), 7.84 (d, 1H). Приклад 5 O F OH Cl F F F NH O F 15 20 N H O 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(метоксиметил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он 2.14 г (4.64 ммоль) 5-{[(2-хлоро-3-фторо-4-метоксифеніл)(2-трифторометил-оксираніл)метил]-аміно}-7-фторо-1H-хінолін-2-ону, отриманого в прикладі 3, перемішували з 2.57 г (7.9 ммоль) карбонату кальцію в 37 мл метанолу. Через 3 дні додавали воду і водну фазу екстрагували етилацетатом. Об'єднані органічні фази промивали розсолом і сушили над сульфатом натрію. Після видалення розчинника флеш хроматографія на силікагелі (метанол в дихлорометані від 0 до 5 %) дає 0.98 г названої сполуки. 1 H-ЯМР (CD3OD); = 3.07 (d, 1H), 3.23 (s, 3H), 3.50 (d, 1H), 3.84 (s, 3H), 5.33 (s, 1H), 6.02 (dd, 1H), 6.29 (dd, 1H), 6.43 (d, 1H), 7.05 (dd, 1H), 7.47 (dd, 1H), 8.04 (d, 1H). Приклад 6 O F OH Cl F F F NH O 25 30 35 F N H O 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-(етоксиметил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он 70 мг (0.15 ммоль) 5-{[(2-хлоро-3-фторо-4-метоксифеніл)(2-трифторометил-оксираніл)метил]-аміно}-7-фторо-1H-хінолін-2-ону, отриманого в прикладі 3, перемішували з 84 мг (0.26 ммоль) карбонату кальцію в 0.67 мл етанолу. Через 40 год. додавали воду і водну фазу екстрагували етилацетатом. Об'єднані органічні фази промивали розсолом і сушили над сульфатом натрію. Після видалення розчинника препаративна тонкошарова хроматографія на силікагелі (етилацетат) дає 22 мг названої сполуки. 1 H-ЯМР (CDCl3); = 1.15 (t, 3H), 3.39 (dq, 1H), 3.42 (d, 1H), 3.51 (dq, 1H), 3.69 (d, 1H), 3.87 (s, 3H), 5.26 (d, 1H), 5.86 (dd, 1H), 6.18 (d, 1H), 6.33 (dd, 1H), 6.54 (d, 1H), 6.87 (dd, 1H), 7.25 (dd, 1H), 7.80 (d, 1H). Приклад 7 19 UA 100251 C2 OH F OH Cl F F F NH O F 5 10 N H 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он 250 мг (0.54 ммоль) 5-{[(2-хлоро-3-фторо-4-метоксифеніл)(2-трифторометил-оксираніл)метил]-аміно}-7-фторо-1H-хінолін-2-ону перемішували з 353 мг (1.1 ммоль) карбонату кальцію в 3 мл DMF, 1.9 мл води і 0.5 мл DMSO. Додавали воду і водну фазу екстрагували етилацетатом. Об'єднані органічні фази промивали розсолом і сушили над сульфатом натрію. Після видалення розчинника флеш хроматографія на силікагелі (метанол в дихлорометані від 0 до 5 %) дає 0.98 г названої сполуки. 1 H-ЯМР (CD3OD); = 3.60 (d, 1H), 3.71 (d, 1H), 3.85 (s, 3H), 5.34 (s, 1H), 5.96 (dd, 1H), 6.29 (dd, 1H), 6.45 (d, 1H), 7.06 (dd, 1H), 7.51 (dd, 1H), 8.04 (d, 1H). Приклад 8 OH F OH O NH Cl 20 25 30 35 40 45 50 F F F 15 O F N H O 5-{[1-(5-Хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он 5-Хлоро-3-фторо-2-метоксибензальдегід До 5 г (34 ммоль) 4-хлоро-2-фторофенолу і 416 мг (3.41 ммоль) 4-диметиламінопіридину в 18 мл THF додавали 3.7 мл (37.5 ммоль) ізопропілізоціанату і суміш нагрівали протягом 20 год. при 60 °C. Після охолоджування до кімнатної температури додавали 2 M HCl і водну фазу екстрагували діетиловим ефіром. Об'єднані органічні фази промивали розсолом, сушили над сульфатом натрію і випаровували з одержанням 7.2 г 4-хлоро-2-фторофенілового ефіру ізопропілкарбамінової кислоти як сирий продукт. До 7.2 г (31 ммоль) 4-хлоро-2фторофенілового ефіру ізопропілкарбамінової кислоти і 5.1 мл тетраметилендіаміну в 300 мл діетилового ефіру додавали 5.9 мл (32.5 ммоль) (триметилсиліл)(трифторометан)сульфонату при кімнатній температурі. Через 30 хв. суміш охолоджували до -70 °C, послідовно додавали 10.2 мл тетраметилендіаміну і 27 мл 2.5 M розчину н-BuLi. Через одну годину при -70° додавали 24 мл DMF при -70 °C і суміш перемішували ще одну годину при -70 °C. Додавали 130 мл етанолу і 36 мл 2 M водного NaOH і реакцію нагрівали до кімнатної температури протягом 18 год. Реакційну суміш підкисляли додаванням 100 мл 2 M водною HCl і розділяли між діетиловим ефіром і водою. Водну фазу екстрагували діетиловим ефіром, об'єднані органічні фази промивали розсолом, сушили над сульфатом натрію і випаровували. Сирий продукт очищали за допомогою хроматографії на силікагелі з одержанням 1.1 г 5-хлоро-3-фторо-2гідроксибензальдегіду. 1.1 г (6.1 ммоль) 5-хлоро-3-фторо-2-гідроксибензальдегіду і 1.56 г (11.3 ммоль) карбонату калію інтенсивно перемішували в 11 мл DMF і в той же час додавали 0.7 мл метилйодиду. Перемішування продовжували протягом 18 год. і додавали воду. Водну фазу екстрагували діетиловим ефіром, об'єднані органічні фази сушили над сульфатом натрію і випаровували. Сирий продукт очищали за допомогою хроматографії на силікагелі (етилацетат в гексані від 0 до 10 %) з одержанням 570 мг 5-хлоро-3-фторо-2-метоксибензальдегіду. 1 H-ЯМР (CDCl3); = 4.10 (d, 3H), 7.35 (dd, 1H), 7.59 (m, 1H), 10.35 (s, 1H). 5-{[(5-Хлоро-3-фторо-2-метоксифеніл)(2-трифторометил-оксираніл)-метил]-аміно}-7-фторо1H-хінолін-2-он До 0.54 г (3 ммоль) 5-аміно-7-фторо-1H-хінолін-2-ону і 0.57 г (3 ммоль) 5-хлоро-3-фторо-2метоксибензальдегіду в 9 мл толуолу і 2.6 мл 1,4-діоксану додавали 0.65 мл оцтової кислоти і 2.4 мл тетрабутилортотитанату. Суміш нагрівали протягом 17 год. до 110 °C, охолоджували до кімнатної температури і виливали у водний розчин фториду амонію. Додавали етилацетат і суміш інтенсивно перемішували протягом 1 год. Фази розділяли і додавання етилацетату повторювали двічі з перемішуванням при кипінні і фази розділяли, поки вони ще гарячі. Об'єднані органічні фази концентрували і залишок очищали флеш хроматографією на силікагелі (етилацетат, потім метанол в дихлорометані від 10 % до 20 %) з одержанням 0.63 г 5-{[1(5хлоро-3-фторо-2-метоксифеніл)-метиліден]-аміно}-7-фторо-1H-хінолін-2-ону. 57 мг NaH (55 % 20 UA 100251 C2 5 10 15 20 25 у маслі, 1.4 ммоль) промивали сухим THF і суспендували разом з 0.63 г (1.8 ммоль) 5-{[1-(5хлоро-3-фторо-2-метоксифеніл)-метиліден]-аміно}-7-фторо-1H-хінолін-2-ону у 22 мл THF. третБутилдиметилсилілхлорид додавали в твердому вигляді і суміш перемішували протягом 2.5 год. до утворення прозорого розчину. Паралельно 0.24 мл 1,1,1-трифторо-2,3-епоксипропану в 6 мл THF і 2 мл гексану охолоджували до -100 °C і протягом 10 хв. додавали 1.1 мл 2.5 M розчину нбутиллітію в гексані, тоді як температура не перевищувала -95 °C. Через 10 хв. після закінчення додавання протягом 20 хв. додавали заздалегідь приготований розчин 1-{третбутилдиметилсиліл}-5-{[1-(5-хлоро-3-фторо-2-метоксифеніл)-метиліден]-аміно}-7-фторохінолін2-ону у THF, тоді як температура не перевищувала -95 °C. Через 3.5 год. при -100 °C додавали 2 мл діетилового ефіру і реакційну суміш нагрівали до кімнатної температури протягом однієї години. Реакцію гасили додаванням насиченого розчину хлориду амонію. Після перемішування протягом 30 хв. фази розділяли і водний шар екстрагували дихлорометаном, об'єднані органічні фази промивали розсолом, сушили над сульфатом натрію і потім випаровували. Флеш хроматографія на силікагелі (етилацетат в гексані від 0 до 100 %) дає 152 мг 5-{[(5-хлоро-3фторо-2-метоксифеніл)(2-трифторометилоксираніл)-метил]-аміно}-7-фторо-1H-хінолін-2-ону 1 H-ЯМР (CDCl3); = 2.48 (m, 1H), 3.18 (d, 1H), 4.11 (s, 3H), 5.13 (d, 1H), 5.54 (d, 1H), 5.86 (dd, 1H), 6.53 (dd, 1H), 6.64 (d, 1H), 6.94 (m, 1H), 7.14 (d, 1H), 7.88 (d, 1H) і 87 мг 5-{[1-(5-хлоро-3фторо-2-метоксифеніл)-2-(хлорометил)-3,3,3-трифторо-2-гідроксипропіл]-аміно}-7-фторо-1Hхінолін-2-ону 50 мг (0.11 ммоль) 5-{[(5-хлоро-3-фторо-2-метоксифеніл)(2-трифторометил-оксираніл)метил]-аміно}-7-фторо-1H-хінолін-2-ону перемішували з 67 мкл перхлорної кислоти (70 %) в 0.55 мл DMF протягом 24 год. при 40 °C. Додатково додавали 67 мкл перхлорної кислоти (70 %) і суміш перемішували додатково протягом 48 год. при 40 °C. Додавали насичений водний розчин NH4Cl і водну фазу екстрагували етилацетатом. Об'єднані органічні фази промивали розсолом і сушили над сульфатом натрію. Після видалення розчинника тонкошарова хроматографія на силікагелі (етилацетат) дає 39 мг названої сполуки. 1 H-ЯМР (CD3OD); = 3.49 (d, 1H), 3.78 (d, 1H), 4.14 (d, 3H), 5.48 (s, 1H), 6.12 (dd, 1H), 6.34 (d, 1H), 6.47 (d, 1H), 7.20 (dd, 1H), 7.52 (m, 1H), 8.10 (d, 1H). Приклад 9 Cl F OH O F F NH Cl 30 35 F F N H O 5-{[1-(5-Хлоро-3-фторо-2-метоксифеніл)-2-(хлорометил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он Може бути виділений як продукт в синтезі епоксиду прикладу 8 після обробки водним розчином хлориду амонію. 1 H-ЯМР (DMSO-d6); = 3.88 (d, 1H), 4.00 (d, 3H), 4.19 (d, 1H), 5.49 (d, 1H), 6.12 (d, 1H), 6.37 (d, 2H), 6.51 (d, 1H), 7.42 (d, 1H), 7.66 (s, 1H), 8.24 (d, 1H). Приклад 10 O F OH F F NH N H 40 45 O 5-{[3,3,3-Трифторо-2-гідроксі-2-([метоксиметил)-1-фенілпропіл]-аміно}-1H-хінолін-1-он 3,3,3-Трифторо-2-гідрокси-2-метоксиметилпропан-1-он 2.3 мл (26 ммоль) 1,1,1-трифторо-2,3-епоксипропану в 30 мл THF і 8 мл гексану охолоджували до -100 °C і додавали 6.3 мл 2.5 M розчину н-бутиллітію (16 ммоль) в гексані протягом 15 хв., тоді як температура не перевищувала -95 °C. Через 10 хв. після закінчення додавання протягом 15 хв. додавали 2.0 (12 ммоль) г N-метокси-N-метилбензаміду в 38 мл THF, тоді як температура не перевищувала -95 °C. Через 5 год. при -100 °C додавали12 мл діетилового ефіру і реакційну суміш нагрівали до кімнатної температури протягом 14 год. Реакцію гасили додаванням насиченого розчину хлориду амонію. Фази розділяли і водний шар двічі екстрагували етилацетатом, об'єднані органічні фази промивали розсолом, сушили над 21 UA 100251 C2 5 10 15 20 25 сульфатом натрію і потім випаровували з одержанням 2.59 г феніл-[2-(трифторометил)оксираніл]-метанону. 1 H-ЯМР (CDCl3); = 3.07 (dq, 1H), 3.38 (d, 1H), 7.50 (t, 2H), 7.65 (tt, 1H), 8.07 (d, 2H). 2.59 г (12 ммоль) феніл-[2-(трифторометил)-оксираніл]-метанону перемішували з 8.8 г (27 ммоль) карбонату кальцію в 94 мл метанолу. Реакцію гасили додаванням води через 3 дні. Водний шар екстрагували етилацетатом, об'єднані органічні фази промивали розсолом, сушили над сульфатом натрію і потім випаровували з одержанням 2.87 г 3,3,3-трифторо-2-гідрокси-2метоксиметилпропан-1-ону. 1 H-ЯМР (CDCl3); = 3.42 (s, 3H), 3.89 (d, 1H), 4.23 (d, 1H), 4.55 (s, 1H), 7.47 (t, 2H), 7.60 (t, 1H), 8.01 (d, 2H). До 194 мг (1.2 ммоль) 5-аміно-1H-хінолін-2-ону і 300 мг (1.2 ммоль) 3,3,3-трифторо-2гідрокси-2-метоксиметилпропан-1-ону в 4 мл толуолу і 1 мл 1,4-діоксану додавали 0.26 мл оцтової кислоти і 1 мл тетрабутилортотитанату. Суміш нагрівали протягом 20 год. до 110 °C, охолоджували до кімнатної температури і виливали у водний розчин фториду амонію. Додавали етилацетат і суміш інтенсивно перемішували протягом 30 хв. Фази розділяли і двічі екстрагували етилацетатом. Об'єднані органічні фази концентрували з одержанням кількісно 5[(3,3,3-трифторо-2-гідрокси-2-метоксиметил-1-фенілпропіліден)-аміно]-1H-хінолін-2-ону. 396 мг (1 ммоль) іміну в 22 мл метанолу охолоджували до 5 °C і додавали 700 мг борогідриду натрію в декілька порцій протягом періоду 24 год. Реакцію гасили додаванням насиченого розчину хлориду амонію і розводили водою і етилацетатом. Фази розділяли, водний шар екстрагували етилацетатом, об'єднані органічні фази промивали розсолом і сушили над сульфатом натрію. Після видалення розчинника флеш хроматографія на силікагелі (етилацетат в гексані від 0 до 80 %) дає 53 мг названої сполуки. 1 H-ЯМР (CD3OD); = 3.45 (s, 3H), 3.47 (d, 1H), 3.64 (d, 1H), 4.97 (s, 1H), 6.19 (d, 1H), 6.58 (t, 2H), 7.16 (t, 1H), 7.30 (m, 3H), 7.50 (d, 2H), 8.05 (d, 1H). Приклад 11 N F OH Cl F F F NH O F 30 35 N H O 5-{[1-(2-Хлоро-3-фторо-4-метоксифеніл)-2-(діамінометил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он 150 мг (0.33 ммоль) 5-{[(2-хлоро-3-фторо-4-метоксифеніл)(2-трифторометил-оксираніл)метил]-аміно}-7-фторо-1H-хінолін-2-ону, отриманого в прикладі 3, перемішували з 69 мг перхлорату літію і молекулярними ситами в 3.25 мл (6.5 ммоль) 2 M розчину диметиламіну в THF в автоклаві при 60 °C. Через 20 год. реакційну суміш фільтрували від осаду, який промивали етилацетатом. Після видалення розчинника флеш хроматографія на силікагелі (етилацетат в гексані від 0 до 100 %) дає 129 мг названої сполуки. 1 H-ЯМР (CDCl3); = 1.68 (br, 3H), 2.30 (d, 1H), 2.36 (br, 3H), 2.77 (br, 1H), 3.87 (s, 3H), 5.09 (d, 1H), 5.81 (d, 1H), 5.98 (d, 1H), 6.35 (d, 1H), 6.56 (d, 1H), 6.88 (dd, 1H), 7.32 (d, 1H), 7.85 (d, 1H). Приклад 12 O F OH O F F F NH Cl F 40 45 N H O 5-{[1-(4-Хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(метоксиметил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он (4-Хлоро-3-фторо-2-метоксифеніл)[2-(трифторометил)-оксираніл]-метанон. 1 г (6.2 ммоль) 3-хлоро-2-фтороанізолу в 10 мл THF охолоджували до -70 °C і додавали 2.7 мл 2.5 M розчину н-бутиллітію в гексані. Через 1.5 год. при -70° додавали 1 г (6.9 ммоль) N, N'-диметокси-N, N'-диметилсечовини в 6 мл THF при -70 °C і суміш перемішували ще одну годину при -70 °C. додавали 7.5 мл 2 M водною HCl і реакцію нагрівали до кімнатної температури протягом 18 год. Реакційну суміш розділяли між діетиловим ефіром і водою. Водну фазу екстрагували діетиловим ефіром, об'єднані органічні фази промивали розсолом, сушили над сульфатом натрію і випаровували. Сирий продукт очищали за допомогою хроматографії на 22 UA 100251 C2 5 10 15 20 25 30 35 силікагелі (етилацетат в гексані від 0 до 30 %) з одержанням 0.59 г 4-хлоро-3-фторо-2,Nдиметокси-N-метилбензаміду. 1 H-ЯМР (CDCl3); = 3.35 (br, 3H), 3.49 (br, 3H), 3.98 (s, 3H), 6.99 (dd, 1H), 7.13 (dd, 1H). 0.44 мл (5.1 ммоль) 1,1,1-трифторо-2,3-епоксипропану в 7.5 мл THF і 2.2 мл гексану охолоджували до -100 °C і протягом 15 хв. додавали 2.03 мл 2.5 M розчину н-бутиллітію (5.1 ммоль) в гексані, тоді як температура не перевищувала -95 °C. Через 10 хв. після закінчення додавання протягом 15 хв. додавали 0.57 г (2.3 ммоль) 4-хлоро-3-фторо-2,Nдиметокси-N-метилбензаміду в 10 мл THF, тоді як температура не перевищувала -95 °C. Через 3 год. при -100 °C додавали 2.3 мл діетилового ефіру і реакційну суміш нагрівали до кімнатної температури протягом 14 год. Реакцію гасили додаванням насиченого розчину хлориду амонію. Фази розділяли і водний шар двічі екстрагували діетиловим ефіром, об'єднані органічні фази промивали розсолом, сушили над сульфатом натрію і потім випаровували з одержанням 570 мг (4-хлоро-3-фторо-2-метоксифеніл)[2-(трифторометил)-оксираніл]-метанону. 1 H-ЯМР (CDCl3); = 2.99 (dq, 1H), 3.37 (d, 1H), 4.14 (d, 3H), 7.18 (m, 1H), 7.19 (m, 1H). 285 мг (0.95 ммоль) (4-хлоро-3-фторо-2-метоксифеніл)[2-(трифторометил)-оксираніл]метанону перемішували з 622 мг (1.9 ммоль) карбонату кальцію в 6.7 мл метанолу. Реакцію гасили додаванням через один день води. Водний шар екстрагували етилацетатом, об'єднані органічні фази промивали розсолом, сушили над сульфатом натрію і потім випаровували з одержанням 262 мг 1-(4-хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2метоксиметилпропан-1-ону. До 27 мг (0.15 ммоль) 5-аміно-7-фторо-1H-хінолін-2-ону і 50 мг (0.15 ммоль) 1-(4-хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2метоксиметилпропан-1-ону у 0.45 мл толуолу і 0.13 мл 1,4-діоксану додавали 33 мкл оцтової кислоти і 0.12 мл тетрабутилортотитанату. Суміш нагрівали протягом 20 год. при 110 °C, охолоджували до кімнатної температури і виливали у водний розчин фториду амонію. Додавали етилацетат і суміш інтенсивно перемішували протягом 30 хв. Фази розділяли і двічі екстрагували етилацетатом. Об'єднані органічні фази концентрували з одержанням кількісно 5{[1-(4-хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-метоксиметилпропіліден]аміно}-7-фторо-1H-хінолін-2-ону. Сирий імін в 4.2 мл метанолу охолоджували до 5 °C і додавали 120 мг борогідриду натрію в декілька порцій протягом періоду 72 год. Реакцію гасили додаванням насиченого розчину хлориду амонію і розводили водою і етилацетатом. Фази розділяли, водний шар екстрагували етилацетатом, об'єднані органічні фази промивали розсолом і сушили над сульфатом натрію. Після видалення розчинника препаративна тонкошарова хроматографія на силікагелі (ацетон в хлористому метилені, 30 %) дає 9.5 мг названої сполуки. 1 H-ЯМР (CD3OD); = 3.44 (s, 3H), 3.65 (m, 1H), 3.69 (d, 1H), 4.05 (d, 3H), 5.44 (s, 1H), 6.03 (dd, 1H), 6.30 (dd, 1H), 6.45 (d, 1H), 7.12 (dd, 1H), 7.35 (dd, 1H), 7.94 (d, 1H). Приклад 13 O F OH O F F F NH Cl F 40 45 50 N H O 5-{[1-(4-Хлоро-3-фторо-2-метоксифеніл)-2-(етоксиметил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он 1-(4-Хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-етоксиметил-2-гідроксипропан-1-он 285 мг (0.95 ммоль) (4-хлоро-3-фторо-2-метоксифеніл)[2-(трифторометил)-оксираніл]метанону, отриманого в прикладі 12, перемішували з 622 мг (1.9 ммоль) карбонату кальцію в 8 мл етанолу. Реакцію гасили додаванням через 1 день води. Водний шар екстрагували етилацетатом, об'єднані органічні фази промивали розсолом, сушили над сульфатом натрію і потім випаровували з одержанням 173 мг 1-(4-хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо2-етоксиметил-2-гідроксипропан-1-ону. 1 H-ЯМР (CDCl3); = 1.20 (t, 3H), 3.60 (dq, 1H), 3.62 (dq, 1H), 3.79 (d, 1H), 3.97 (d, 3H), 4.09(d, 1H), 4.72 (s, 1H), 7.11 (dd, 1H), 7.18 (dd, 1H). До 26 мг (0.15 ммоль) 5-аміно-7-фторо-1H-хінолін-2-ону і 50 мг (0.15 ммоль) 1-(4-хлоро-3фторо-2-метоксифеніл)-3,3,3-трифторо-2-етоксиметил-2-гідроксипропан-1-ону у 0.44 мл толуолу і 0.13 мл 1,4-діоксану додавали 30 мкл оцтової кислоти і 0.11 мл тетрабутилортотитанату. Суміш нагрівали протягом 20 год. до 110 °C, охолоджували до кімнатної температури і виливали у водний розчин фториду амонію. Додавали етилацетат і 23 UA 100251 C2 5 10 суміш інтенсивно перемішували протягом 30 хв. Фази розділяли і двічі екстрагували етилацетатом. Об'єднані органічні фази концентрували з одержанням кількісно 5-{[1-(4-хлоро-3фторо-2-метоксифеніл)-3,3,3-трифторо-2-етоксиметил-2-гідроксипропіліден]-аміно}-7-фторо-1Hхінолін-2-ону. Сирий імін в 4.7 мл метанолу охолоджували до 5 °C і додавали 180 мг борогідриду натрію в декілька порцій протягом періоду 72 год. Реакцію гасили додаванням насиченого розчину хлориду амонію і розводили водою і етилацетатом. Фази розділяли, водний шар екстрагували етилацетатом, об'єднані органічні фази промивали розсолом і сушили над сульфатом натрію. Після видалення розчинника препаративна тонкошарова хроматографія на силікагелі (ацетон в хлористому метилені 30 %) дає 3.2 мг названої сполуки. 1 H-ЯМР (CD3OD); = 1.25 (t, 3H), 3.58 (dq, 1H), 3.59 (dq, 1H), 3.68 (dq, 1H), 3.74 (d, 1H), 4.05 (d, 3H), 5.47 (s, 1H), 6.02 (dd, 1H), 6.30 (dd, 1H), 6.43 (d, 1H), 7.13 (dd, 1H), 7.34 (dd, 1H), 7.93 (d, 1H). Приклад 14 OH F OH Cl F F F NH HO F 15 20 25 N H O 5-{[1-(2-хлоро-3-фторо-4-гідроксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)-пропіл]аміно}-7-фторо-1H-хінолін-2-он До 100 мг (0.20 ммоль) 5-{[1-(2-хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2(метоксиметил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-ону прикладу 5 в 8.6 мл дихлорометану при -30 °C під аргоном додавали 1.6 мл 1 M розчину трьохбромистого бору в дихлорометані. Реакційну суміш перемішували протягом 16 год. у температурному інтервалі між 0 °C і 25 °C. Реакційну суміш змішували при 0 °C з насиченим розчином бікарбонату натрію. Після розведення етилацетатом завантаженню дали нагрітися до кімнатної температури, перемішували протягом 10 хв. і фази розділяли. Водну фазу підкисляли 4 M HCl і екстрагували 10 % метанолу в дихлорометані. Після видалення розчинника препаративна тонкошарова хроматографія на силікагелі (етилацетат/метанол 4:1) дає 16 мг названої сполуки. 1 H-ЯМР (CD3OD); = 3.62 (d, 1H), 3.71 (d, 1H), 5.32 (s, 1H), 5.99 (dd, 1H), 6.30 (dd, 1H), 6.45 (d, 1H), 6.87 (dd, 1H), 7.38 (dd, 1H), 8.05 (d, 1H). ФОРМУЛА ВИНАХОДУ 30 1. Сполуки загальної формули I R 5 OH CF3 R R 1 NH 2 R 3 R 35 40 4 N H O , (I) 1 2 де R і R , незалежно один від одного, означають атом водню, гідроксигрупу, атом галогену, необов'язково заміщену (С1-С10)-алкільну групу, необов'язково заміщену (С1-С10)-алкоксильну 1 2 групу, (С1-С10)-алкілтіогрупу, (С1-С5)-перфтороалкільну групу, ціаногрупу, нітрогрупу, або R і R разом означають групу, вибрану з груп -О-(СH2)p-О-, -O-(CH2)p-CH2-, -О-СH=СH-, -(СН2)р+2-, -NH(CH2)p+1, -N(С1-С3-алкіл)-(СН2)р+1, і -NH-N=CH-, при цьому р=1 або 2, і термінальні атоми кисню і/або атоми вуглецю, і/або атоми азоту зв'язані з 6 7 безпосередньо суміжними кільцевими атомами вуглецю, або NR R , 6 7 при цьому R і R , незалежно один від одного, означають водень, С1-С5-алкіл або (СO)-(С1-С5)алкіл, 24 UA 100251 C2 3 5 10 15 20 25 30 35 40 45 50 55 60 R означає атом водню, гідроксигрупу, атом галогену, ціаногрупу, необов'язково заміщену (С1С10)-алкільну групу, (С1-С10)-алкоксильну групу, (С1-С10)-алкілтіогрупу або (С1-С5)перфтороалкільну групу, 4 R означає водень, галоген, гідроксигрупу, (С1-С5)-алкіл, (С1-С5)-алкоксигрупу, (С1-С5)6 7 9 6 7 алкілтіогрупу, (С1-С5)-перфтороалкіл, ціаногрупу, нітрогрупу, NR R , COOR , (CO)NR R або (C1C5-алкілен)-О-(СО)-(С1-С5)-алкільну групу, 5 R означає групу, вибрану з -(С1-С10)-алкілу, який може бути необов'язково частково або повністю галогенованим, -(С2-С10)-алкенілу, -(С2-С10)-алкінілу, (С3-С7)-циклоалкіл-(С1-С8)-алкілу, (С3-С7)-циклоалкіл-(С1-С8)-алкенілу, (С3-С7)-циклоалкіл-(С2-С8)-алкінілу, гетероцикліл-(С1-С8)-алкілу, гегероцикліл-(С1-С8)-алкенілу, гетероцикліл-(С2-С8)-алкінілу, 8 -R , 8 R -(С1-С8)-алкілу, 8 R -(C2-C8)-алкенілу, 8 R -(C2-Cs)-алкенілу, -S-(С1-С10)-алкілу, -SO2-(С1-С10)- алкілу, 8 -S-R , 8 -SO2-R , -CN, -Hal, -О-(С1-С10,)-алкілу, 6 7 6 7 -NR R , де R , R мають визначені вище значення, 8 -O-R , -OH, за винятком -СН(СН3)2 або -С(СH3)=СH2, 8 R означає арильну групу, яка може необов'язково бути заміщеною 1-3 гідроксигрупами, галогенами, С1-С5-алкілами, С1-С5-алкоксигрупами, ціаногрупами, СF3, нітрогрупами, СOO(С1С5-алкільними) або С(O)OСН2-фенільними, або гетероарильними групами, при цьому гетероарильна група може містити 1-3 гетероатоми, яка може необов'язково бути заміщеною 13 алкільними групами, гідроксигрупами, галогенами, ціаногрупами або С1-С5-алкоксильними групами, і їх солі, сольвати або солі сольватів. 2. Сполуки загальної формули І згідно з пунктом 1, де 1 2 R і R , незалежно один від одного, означають атом водню, гідроксигрупу, атом галогену, необов'язково заміщену (С1-С10)-алкільну групу, необов'язково заміщену (С1-С10)-алкоксильну 6 7 6 7 групу, (С1-С5)-перфтороалкільну групу, ціаногрупу або NR R , при цьому R і R , незалежно один від одного, означають водень, С1-С5-алкіл або (СО)-(С1-С5)-алкіл, 3 R означає атом водню, гідроксигрупу, атом галогену, ціаногрупу, необов'язково заміщену (С1С10)-алкільну групу, (С1-С10)-алкоксильну групу або (С1-С5)-перфтороалкільну групу, 4 R означає водень, С1-С3-алкіл, С1-С3-алкоксигрупу, гідроксигрупу, галоген, 5 R означає групу, вибрану з -(С1-С10)-алкілу, який може бути необов'язково частково або повністю галогенованим, -(С2-С10)-алкенілу, -(С2-С10)-алкінілу, -(С3-С7)-циклоалкіл-(С1-С8)-алкілу, -(С3-С7)-циклоалкіл -(С1-С8)-алкенілу, -S-(С1-С10)-алкілу, -SO2-(С1-С10)-алкілу, -CN, -Hal, -О-(С1-С10)-алкілу, 6 7 6 7 -NR R , де R , R мають визначені нижче значення, -ОН, за винятком -СH(СH3)2 або -С(СН3)=СН2, і їх солі, сольвати або солі сольватів. 25 UA 100251 C2 5 10 15 20 25 30 35 40 45 50 55 60 3. Сполуки загальної формули І згідно з пунктом 1, де 1 2 3 R , R і R , незалежно один від одного, означають водень, фтор, хлор, бром, ціаногрупу, метоксигрупу, етоксигрупу, гідроксигрупу, 4 R означає водень, С1-С3-алкіл, галоген, 5 R означає гідроксигрупу, хлор, -S-СН3, -S-CH2-CH3, -S-CH2-СН2-СH3, -О-СH3 або -О-СН2-СH3, О-СН2-СH2-СН3, і їх солі, сольвати або солі сольватів. 4. Сполуки згідно з принаймні одним з пунктів 1-3 в енантіомерно чистій формі і їх солі, сольвати або солі сольватів. 5. Сполуки згідно з пунктом 1, вибрані зі списку, що включає 5-{[1-(2-фторо-4-метоксифеніл)3,3,3-трифторо-2-гідрокси-2-([метилсульфоніл]-метил)-пропіл]-аміно}-1H-хінолін-2-он, 5-{[2-([етилсульфаніл]-метил)-1-(2-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідроксипропіл]аміно}-1H-хінолін-2-он, 5-{[1-(2-хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфоніл]-метил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(2-хлоро-3-фторо-4-метоксифеніл)-2-([етилсульфаніл]-метил)-3,3,3-трифторо-2гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(2-хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(метоксиметил)-пропіл]аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(2-хлоро-3-фторо-4-метоксифеніл)-2-(етоксиметил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(2-хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)-пропіл]аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(5-хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)-пропіл]аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(5-хлоро-3-фторо-2-метоксифеніл)-2-(хлорометил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он, 5-{[3,3,3-трифторо-2-гідрокси-2-([метоксиметил)-1-фенілпропіл]-аміно}-1H-хінолін-]-1-он, 5-{[1-(2-хлоро-3-фторо-4-метоксифеніл)-2-(діамінометил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(4-хлоро-3-(фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(метоксиметил)-пропіл]аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(4-хлоро-3-фторо-2-метоксифеніл)-2-(етоксиметил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(2-хлоро-3-фторо-4-гідроксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)-пропіл]аміно}-7-фторо-1H-хінолін-2-он, і їх солі, сольвати або солі сольватів. 6. Енантіомерно чисті сполуки згідно з пунктом 1, вибрані зі списку, що включає 5-{(1S,2R)[1-(2-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфоніл]-метил)пропіл]-аміно}-1H-хінолін-2-он, 5-{(1S,2R)[2-([етилсульфаніл]-метил)-1-(2-фторо-4-метоксифеніл)-3,3,3-трифторо-2гідроксипропіл]-аміно}-1H-хінолін-2-он, 5-{(1S,2R)[1-(2-хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфоніл]метил)-пропіл]-аміно}-7-фторо-1H-хінолін-2-он, 5-{(1S,2R)[1-(2-хлоро-3-фторо-4-метоксифеніл)-2-([етилсульфаніл]-метил)-3,3,3-трифторо-2гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он, 5-{(1S,2S)[1-(2-хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(метоксиметил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он, 5-{(1S,2S)[1-(2-хлоро-3-фторо-4-метоксифеніл)-2-(етоксиметил)-3,3,3-трифторо-2гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он, 5-{(1S,2S)[1-(2-хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он, 5-{(1S,2S)[1-(5-хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он, 5-{(1S,2R)[1-(5-хлоро-3-фторо-2-метоксифеніл)-2-(хлорометил)-3,3,3-трифторо-2гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он, 5-{(1S,2S)[3,3,3-трифторо-2-гідрокси-2-([метоксиметил)-1-фенілпропіл]-аміно}-1H-хінолін-1-он, 5-{(1S,2R)[1-(2-хлоро-3-фторо-4-метоксифеніл)-2-(діамінометил)-3,3,3-трифторо-2гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он, 5-{(1S,2S)[1-(2-хлоро-3-фторо-4-гідроксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он, 26 UA 100251 C2 5 10 15 20 25 30 35 і їх солі, сольвати або солі сольватів. 7. Сполуки загальної формули I згідно з пунктом 1, де 1 2 3 R , R і R , незалежно один від одного, вибирають з хлору, фтору та метоксигрупи, 4 R означає замісник 7-фтор, 5 R вибирають з -S-CH2-CH3, -O-CH2-CH3, -S-CH3, -О-СН3, -ОН та -Сl, і їх солі, сольвати або солі сольватів. 8. Сполуки загальної формули I згідно з пунктом 7, вибрані зі списку, що включає 5-{[1-(2-хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-([метилсульфоніл]-метил)пропіл]-аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(2-хлоро-3-фторо-4-метоксифеніл)-2-([етилсульфаніл]-метил)-3,3,3-трифторо-2гідроксипропіл]-аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(2-хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(метоксиметил)-пропіл]аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(2-хлоро-3-фторо-4-метоксифеніл)-2-(етоксиметил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(2-хлоро-3-фторо-4-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)-пропіл]аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(5-хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)-пропіл]аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(5-хлоро-3-фторо-2-метоксифеніл)-2-(хлорометил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(4-хлоро-3-фторо-2-метоксифеніл)-3,3,3-трифторо-2-гідрокси-2-(метоксиметил)-пропіл]аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(4-хлоро-3-фторо-2-метоксифеніл)-2-(етоксиметил)-3,3,3-трифторо-2-гідроксипропіл]аміно}-7-фторо-1H-хінолін-2-он, 5-{[1-(2-хлоро-3-фторо-4-гідроксифеніл)-3,3,3-трифторо-2-гідрокси-2-(гідроксиметил)-пропіл]аміно}-7-фторо-1H-хінолін-2-он, і їх солі, сольвати або солі сольватів. 9. Застосування сполук згідно з формулою І принаймні одного з пунктів 1-8 для одержання фармацевтичних агентів. 10. Застосування сполук згідно з формулою І принаймні одного з пунктів 1-8 для одержання фармацевтичних агентів для лікування запальних захворювань. 11. Фармацевтична композиція, що містить сполуку формули (І) або її фармацевтично прийнятну сіль, як визначено в пунктах 1-8, і фармацевтично прийнятний ад'ювант, розчинник або носій. 12 Спосіб одержання сполук загальної формули І згідно з пунктом 1, в якому здійснюють наступні стадії: стадія а): NH2 H R R 1 R O 2 R (III) N H R O N 2 R стадія b): 27 4 1 Ti(OR)4 і/або кислота (II) 40 4 R 3 R H NH O 3 (IV) , UA 100251 C2 R H R R 1 2 nBuLi, від R CF3 (V) NH N R O O 4 R -80о до -100оС 1 NH 2 O 3 CF3 R 3 R 4 O N H (IV) (VI) , стадія с): R O R R CF3 1 R5 NH 2 R Met R R 3 O N H R 4 O N H (I) (VI) 5 CF3 NH 2 R 4 OH 1 3 R 5 , де всі залишки мають визначення, дані в пункті 1, і R означає С1-С4-алкіл і Met означає лужні метали, лужноземельні метали, алюміній, мідь, кремній або олово. 13. Спосіб стадії а) згідно з пунктом 12 одержання інтермедіатів загальної формули IV, який відрізняється тим, що бензальдегіди загальної формули II піддають реакції із заміщеними хінолоновими амінами формули III, даючи іміни загальної формули IV у присутності кислот Льюїса і/або в кислотних умовах, NH2 H R R 10 15 1 R O 2 R R H 4 (III) N H R O R 1 N 2 Ti(OR)4 і /або кислота 3 R (II) 4 NH O 3 (IV) , де R , R , R і R мають значення, визначені в пункті 1, і R означає С1-С4-алкіл. 14. Спосіб стадії b) згідно з пунктом 12 одержання інтермедіатів загальної формули VI, який відрізняється тим, що метальований трифтороепоксипропан V, необов'язково в його енантіомерно чистій формі, піддають реакції з імінами формули IV при низьких температурах з одержанням епоксидів загальної формули VI 1 2 3 4 28
ДивитисяДодаткова інформація
Назва патенту англійською5-[(3,3,3-trifluoro-2-hydroxy-1-arylpropyl)amino]-1h-quinolin-2-ones, a process for their production and their use as anti-inflammatory agents
Автори англійськоюBerger, Markus, Schmees Norbert, Zollner, Thomas, May, Ekkehard, Hassfeld, Jorma, Schaecke Heike
Назва патенту російською5-[(3,3,3-трифторо-2-гидрокси-1-арилпропил)-амино]-1н-хинолин-2-оны, способ их получения и их применение в качестве противовоспалительных средств
Автори російськоюБергер Маркус, Ревинкель Хартмут, Цолльнер Томас, Май Эккехард, Хассфельд Йорма, Шьокке Хайке
МПК / Мітки
МПК: C07D 215/38, A61K 31/4704, A61P 29/00, C07D 303/02, C07C 49/233, C07D 405/12
Мітки: одержання, протизапальних, застосування, засобів, 5-[(3,3,3-трифторо-2-гідроксі-1-арилпропіл)-аміно]-1н-хінолін-2-они, спосіб
Код посилання
<a href="https://ua.patents.su/34-100251-5-333-triftoro-2-gidroksi-1-arilpropil-amino-1n-khinolin-2-oni-sposib-kh-oderzhannya-i-kh-zastosuvannya-yak-protizapalnikh-zasobiv.html" target="_blank" rel="follow" title="База патентів України">5-[(3,3,3-трифторо-2-гідроксі-1-арилпропіл)-аміно]-1н-хінолін-2-они, спосіб їх одержання і їх застосування як протизапальних засобів</a>
Попередній патент: Інгібітори реплікації вірусу імунодефіциту людини
Наступний патент: Композиція будівельного матеріалу та її застосування
Випадковий патент: Спосіб визначення стану карієсрезистентності емалі зуба в експерименті