3,7-діазадицикло[3.3.0]октани та їх застосування при лікуванні серцевих аритмій
Номер патенту: 75382
Опубліковано: 17.04.2006
Автори: Вільстерманн Міхаель, Бйорсне Маґнус, Страндлунд Герт, Свенссон Педер, Понтен Фрітьйоф
Формула / Реферат
1. Сполука формули І
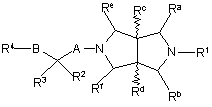 , І
, І
де хвилясті лінії представляють, як варіант, відносну цис- або трансстереобудову;
R1 представляє С1-12алкіл (як варіант, заміщений та/або закінчений одним або більше замісниками, вибраними з групи: атом галогену, ціаногрупа, нітрогрупа, арил, Het1, -C(O)R5a, -OR5b, -N(R6)R5c, -C(O)XR7, -C(O)N(R8)R5d та -S(O)2R9), Het2, -C(O)R5a, -C(O)XR7, -C(O)N(R8)R5d або -S(O)2R9;
R5a - R5d незалежно представляють, у кожному випадку своєї наявності, Н, С1-6алкіл (як варіант, заміщений та/або закінчений одним або більше замісниками, вибраними з групи: ОН, С1-6алкоксил, атом галогену, ціаногрупа, нітрогрупа, арил, Het3 та -NHC(O)R10), арил або Het4, або R5d разом з R8 представляє С3-6алкілен (цю алкіленову групу, як варіант, перервано атомом О та/або, як варіант, заміщено одною або більше С1-3алкілгрупами);
R10 представляє Н, С1-4алкіл (як варіант, заміщений та/або закінчений одним або більше замісниками, вибраними з групи: атом галогену, ціаногрупа, арил та -NHC(O)R11) або арил;
R11 представляє Н, С1-4алкіл або арил;
R6 представляє Н, С1-6алкіл (як варіант, заміщений та/або закінчений одним або більше замісниками, вибраними з групи: -ОН, атом галогену, ціаногрупа, нітрогрупа та арил), арил, -C(O)R12a, -С(O)ОR12d або -C(O)N(H)R12c;
R12a, R12d та R12c представляють С1-6алкіл (як варіант, заміщений та/або закінчений одним або більше замісниками, вибраними з групи: -ОН, атом галогену, ціаногрупа, нітрогрупа та арил) або арил, або R12a та R12c представляють Н;
Х представляє О або S;
R7 представляє, у кожному випадку своєї наявності, арил або С1-12алкіл (ця алкілгрупа, як варіант, заміщена та/або закінчена одним або більш замісниками, вибраними з групи: -ОН, атом галогену, ціаногрупа, нітрогрупа, арил, С1-6алкоксил, -SO2R13a, -C(O)R13b та Het5);
R13a та R13b незалежно представляють С1-6алкіл або арил;
R8 представляє, у кожному випадку своєї наявності, Н, С1-12алкіл, С1-6алкоксил (ці останні дві групи, як варіант, заміщені та/або закінчені одним або більше замісниками, вибраними з групи: -ОН, атом галогену, ціаногрупа, нітрогрупа, С1-4алкіл та С1-4алкоксил), -D-арил, -D-арилокси, -D-Het6, -D-N(H)C(O)R14a, -D-S(O)2R15a, -D- C(O)R14b, -D-C(O)OR15b, -D-C(O)N(R14c)RI4d, або R8 разом з R5d представляє С3-6алкілен (цю алкіленову групу, як варіант, перервано атомом О та/або, як варіант, заміщено одною або більше С1-3алкілгрупами);
R14а – R14d незалежно представляють Н, С1-6алкіл (як варіант, заміщений та/або закінчений одним або більше замісниками, вибраними з групи: -ОН, атом галогену, ціаногрупа, нітрогрупа та арил), арил, або R14c тa R14d разом представляють С3-6алкілен;
R15a та R15b незалежно представляють С1-6алкіл (як варіант, заміщений та/або закінчений одним або більше замісниками, вибраними з групи: -ОН, атом галогену, ціаногрупа, нітрогрупа та арил) або арил;
D представляє безпосередній зв'язок або С1-6алкілен;
R9 представляє, у кожному випадку своєї наявності, С1-6алкіл (як варіант, заміщений та/або закінчений одним або більше замісниками, вибраними з групи: -ОН, атом галогену, ціаногрупа, нітрогрупа та арил), арил або Het7;
R2 представляє Н, атом галогену, С1-6алкіл, -E-OR16, -E-N(R17)R18 або, разом з R3, представляє =O;
R3 представляє Н, С1-6алкіл або, разом з R2, представляє =O;
R16 представляє Н, С1-6алкіл, -Е-арил, -E-Het8, -C(O)R19a, -C(O)OR19b або –C(O)N(R20a)R20b;
R17 представляє Н, С1-6алкіл, -Е-арил, -E-Het8, -С(O)R19a, -С(O)ОR19b, -S(O)2R19c, -[C(O)]pN(R20a)R20b або -C(NH)NH2;
R18 представляє Н, С1-6алкіл, -Е-арил або –C(O)R19d;
R19a – R19d незалежно представляють, у кожному випадку своєї наявності, С1-6алкіл (як варіант, заміщений та/або закінчений одним або більше замісниками, вибраними з групи: атом галогену, арил та Het9), арил, Het10, або R19a та R19d незалежно представляють Н;
R20a та R20b незалежно представляють, у кожному випадку своєї наявності, Н або С1-6алкіл (як варіант, заміщений та/або закінчений одним або більше замісниками, вибраними з групи: атом галогену, арил та Het11), арил, Het12, або разом представляють С3-6алкілен, як варіант, перерваний атомом О;
Е представляє, у кожному випадку своєї наявності, безпосередній зв'язок або С1-4алкілен;
р дорівнює 1 або 2;
А представляє -G-, -J-N(R21)- або -J-O-(в останніх двох групах N(R21)- або O приєднано до атома карбону, що з'єднаний з R2 та R3);
В представляє -Z-, -Z-N(R22), -N(R22)-Z-, -Z-S(O)n-, -Z-O-(в останніх двох групах Z приєднано до атома карбону, що з'єднаний з R2 та R3);
G представляє безпосередній зв'язок або С1-6алкілен;
J представляє С2-6алкілен;
Z представляє безпосередній зв'язок або С1-4алкілен;
R21 та R22 незалежно представляють Н або С1-6алкіл;
R4 представляє арил або Het13, обидві ці групи, як варіант, заміщені одним або більше замісниками, вибраними з групи: -ОН, ціаногрупа, атом галогену, нітрогрупа, С1-6алкіл (як варіант, закінчений групою –N(H)C(O)OR23a), С1-6алкоксил, Het1, арил, -N(R24a)R24b, -C(O)R24c, -С(O)ОR24d, -C(O)N(R24e)R24f, -N(R24g)C(O)R24h, -N(R24i)C(O)N(R24j)R24k, -N(R24m)S(O)2R23b, -S(O)nR23c, -OS(O)2R23d, -S(O)2N(R24n)R24p та (тільки у випадку Het13) оксогрупа;
Het13 представляє чотири-дванадцятичленну гетероциклічну групу, що містить один або більше гетероатомів, вибраних з оксигену, нітрогену та/або сульфуру;
Het1 - Het12 незалежно представляють, у кожному випадку своєї наявності, чотири-дванадцятичленну гетероциклічну групу, що містить один або більше гетероатомів, вибраних з оксигену, нітрогену та/або сульфуру, ці гетероциклічні групи, як варіант, заміщені одним або більше замісниками включаючи =O, -ОН, ціаногрупу, атом галогену, нітрогрупу, С1-6алкіл (як варіант, закінчений групою -N(H)C(O)OR23a), С1-6алкоксил, Het1, арил, -N(R24a)R24b, -C(O)R24c, -С(O)ОR24d, -C(O)N(R24e)R24f, -N(R24g)C(O)R24h, -N(R24i)C(O)N(R24j)R24k, -N(R24m)S(O)2R23b, -S(O)nR23c, -OS(O)2R23d та –S(O)2N(R24n)R24p;
R23a - R23d незалежно представляють, у кожному випадку своєї наявності, С1-6алкіл;
R24a - R24p незалежно представляють, у кожному випадку своєї наявності, Н або С1-6алкіл;
n дорівнює, у кожному випадку, 0, 1 або 2, а
Ra - Rf незалежно представляють Н або С1-4алкіл;
де кожний арил та кожну арилоксигрупу, якщо не визначено інше, як варіант, заміщено;
або її фармацевтично прийнятне похідне;
за умови, що:
(a) коли R3 представляє Н або С1-4алкіл; а
А представляє -J-N(R21)- або -J-O-;
то В не представляє -N(R22)-, -S(O)n-, -О- або –N(R22)-Z- (в останньому групу -N(R22) приєднано до атома карбону, що з'єднаний з R2 тa R3);
(b) коли R2 представляє -E-OR15 або -E-N(R17)R18, в яких Е представляє безпосередній зв'язок, то:
(і) А не представляє безпосереднього зв'язку, -J-N(R21)- або -J-O-, а
(іі) В не представляє -N(R22)-, -S(O)n-, -О- або -N(R22)-Z- (в останньому групу -N(R22) приєднано до атома карбону, що з'єднаний з R2 тa R3);
(c) Het1 та Het13 не представляють 9-членних гетероциклів, що містять конденсоване бензольне або піридинове кільце; та
(d) сполука не представляє:
3,7-біс(1-фенілетил)-3,7-діазадицикло[3.3.0]октан;
2-{4-(7-бензил-3,7-діазадицикло[3.3.0]октан-3-іл)бутил}-1,2-бензізотіазол-3-он-1,1-діоксид;
3-метил-7-бензил-3,7-діазадицикло[3.3.0]октан;
3-циклогексил-7-бензил-3,7-діазадицикло[3.3.0]октан;
3-(тіазол-2-іл)-7-бензил-3,7-діазадицикло[3.3.0]октан;
3-(2-піримідил)-7-бензил-3,7-діазадицикло[3.3.0]октан або
3-(5,5-диметокси)пентил-7-бензил-3,7-діазадицикло[3.3.0]октан;
2. Сполука за п. 1, де у сполуці формули І один або більше необов'язкових замісників на арил- та арилоксигрупах вибрані з групи: -ОН, ціаногрупа, атом галогену, нітрогрупа, С1-6алкіл (як варіант, закінчений групою -N(H)C(O)OR23a), С1-6алкоксил, Het1, арил (ця арилгрупа може не бути заміщеною будь-якими іншими арил-групами), -N(R24a)R24b, -C(O)R24c, -С(O)ОR24d, -C(O)N(R24e)R24f, -N(R24g)C(O)R24h, -N(R24i)C(O)N(R24j)R24k, -N(R24m)S(O)2R23b, -S(O)nR23c, -ОS(О)2R23d та -S(O)2N(R24n)R24p, де Het1, R23a – R23d, R24a - R24p та n визначені у п. 1.
3. Сполука за п. 1 або п. 2, де хвилясті лінії представляють відносну цис-стереобудову.
4. Сполука за будь-яким одним з пп. 1 - 3, де R1 представляє С1-8алкіл (як варіант, заміщений та/або закінчений одним або більше замісниками, вибраними з групи: атом галогену, як варіант, заміщений феніл, Het1, -C(O)R5a, -OR5b, -C(O)OR7, -C(O)N(H)R8 та -S(O)2-C1-6алкіл), Het2, -C(O)OR7, -С(O)N(Н)Rs або -S(O)2R9.
5. Сполука за будь-яким одним з пп. 1 - 4, де R5a та R5b незалежно представляють у кожному випадку Н, С1-6алкіл (як варіант, заміщений та/або закінчений одним або більше замісниками, вибраними з групи: -ОН, С1-4алкоксил та атом галогену), як варіант, заміщений феніл або Het4.
6. Сполука за будь-яким одним з пп. 1 - 5, де R7 представляє, у кожному випадку, С1-8алкіл (цю групу, як варіант, заміщено та/або закінчено одним або більше замісниками, вибраними з групи: -ОН, атом галогену, ціаногрупа, як варіант, заміщений феніл, С1-4алкоксил, -SO2R13a, -C(O)R13b тa Het5).
7. Сполука за п. 6, де R13a та R13b незалежно представляють С1-6алкіл.
8. Сполука за будь-яким одним з пп. 1 - 7, де R8 представляє, у кожному випадку, С1-8алкіл (цю групу, як варіант, заміщено та/або закінчено одним або більше замісниками, вибраними з групи: -ОН, атом галогену, ціаногрупа та С1-4алкоксил), -D-(як варіант, заміщений феніл), -D-Het6, -D-S(O)2R15a, -D-С(O)-С1-6алкіл або -D-C(O)OR15b.
9. Сполука за п. 8, де R15a та R15b незалежно представляють С1-6алкіл (як варіант, заміщений та/або закінчений одним або більше замісниками, вибраними з групи: атом галогену, ціаногрупа та, як варіант, заміщений феніл) або, як варіант, заміщений феніл.
10. Сполука за будь-яким одним з пп. 1 - 9, де D представляє безпосередній зв'язок або С1-3алкілен.
11. Сполука за будь-яким одним з пп. 1 - 10, де R9 представляє, у кожному випадку, С1-5алкіл (як варіант, заміщений та/або закінчений одним або більше замісниками, вибраними з групи: атом галогену, ціаногрупа та, якваріант, заміщений феніл) або, як варіант, заміщений феніл.
12. Сполука за будь-яким одним з пп. 1 - 11, де R2 представляє Н, С1-2алкіл, -OR16, -N(H)R17 або, разом з R3, представляє =O.
13. Сполука за будь-яким одним з пп. 1 - 12, де R3 представляє Н, С1-2алкіл або, разом з R2, представляє =O.
14. Сполука за будь-яким одним з пп. 1 - 13, де R16 представляє Н, С1-4алкіл, -Е-(як варіант, заміщений феніл), -C(O)R19a –C(O)N(H)R20a.
15. Сполука за будь-яким одним з пп. 1 - 13, де R17 представляє Н, С1-4алкіл, -Е-(як варіант, заміщений феніл), -C(O)R19a або –C(O)OR19b.
16. Сполука за будь-яким одним з пп. 1 - 15, де R19a та R19b незалежно представляють у кожному випадку С1-6алкіл, як варіант, заміщений феніл або Het10.
17. Сполука за будь-яким одним з пп. 1 - 14, де R20a представляє Н або С1-4алкіл.
18. Сполука за будь-яким одним з пп. 1 - 17, де Е представляє, у кожному випадку, безпосередній зв'язок або С1-2алкілен.
19. Сполука за будь-яким одним з пп. 1 - 18, де А представляє -G-.
20. Сполука за будь-яким одним з пп. 1 - 19, де В представляє -Z-, -Z-N(H)-, -Z-S(O)n-, -Z-O- (у останніх трьох групах Z приєднано до атома карбону, що з'єднаний з R2 та R3).
21. Сполука за п. 19, де G представляє безпосередній зв'язок або С1-5алкілен.
22. Сполука за будь-яким одним з пп. 1 - 21, де Z представляє безпосередній зв'язок або С1-3алкілен.
23. Сполука за будь-яким одним з пп. 1 - 22, де R4 представляє феніл або Het13, де обидві ці групи, як варіант, заміщені одним або більше замісниками, вибраними з групи: ціаногрупа, атом галогену, нітрогрупа, С1-4лкіл (як варіант, закінчений групою –N(H)C(O)OR23a), С1-4алкоксил, як варіант, заміщений феніл, -C(O)N(H)R24e, -N(Н)С(O)R24h, -N(Н)С(O)N(Н)R24j, -N(H)S(O)2R23b, -S(O)2R23с та –S(O)2N(R24n)R24p.
24. Сполука за п. 23, де Het13 представляє п'яти-десятичленну гетероциклічну групу, що містить один або більше гетероатомів, вибраних з оксигену, нітрогену та/або сульфуру.
25. Сполука за будь-яким одним з пп. 1 - 24, де Het1 - Het12 незалежно представляють, у кожному випадку своєї наявності, п'яти-десятичленні гетероциклічні групи, що містять один або більше гетероатомів, вибраних з оксигену, нітрогену та/або сульфуру, ці гетероциклічні групи, як варіант, заміщені одним або більше замісниками, включаючи =O, -ОН, ціаногрупу, атом галогену, нітрогрупу, С1-4алкіл, С1-4алкоксил, як варіант, заміщений феніл, -NH2, -C(O)R24c, -C(O)OR24d, -C(O)N(H)R24e, -N(Н)С(O)R24h та –S(O)nR23c.
26. Сполука за будь-яким одним з пп. 1 - 25, де Ra – Rf незалежно представляють Н або С1-2алкіл.
27. Сполука за будь-яким одним з пп. 1 - 26, де необов'язкові замісники на фенольних групах вибрані з групи: -ОН, ціаногрупа, атом галогену, нітрогрупа, С1-4алкіл (як варіант, закінчений групою –N(H)C(O)OR23a), С1-4алкоксил, -NН2, -C(O)R24c, -С(O)ОR24d, -C(O)N(H)R24e, -N(H)C(O)R24h, -N(H)C(O)N(H)R24j, -N(H)S(O)2R23b, -S(O)nR23c тa –S(O)2N(R24n)R24p.
28. Сполука за п. 27, де R23a - R23c, R24c, R24d, R24e, R24h, R24j, R24n та R24p незалежно представляють С1-4алкіл.
29. Сполука за будь-яким одним з пп. 1 - 28, де n дорівнює 0 або 2.
30. Сполука за будь-яким одним з пп. 1 - 29, де алкільні групи та алкоксигрупи можуть бути, якщо не визначено інше:
(і) лінійними або розгалуженими, циклічними або частково циклічними/ациклічними;
(іі) насиченими або ненасиченими;
(ііі) перерваними одним або більше атомами оксигену та/або
(iv) заміщеними одним або більше атомами флуору або хлору.
31. Сполука, яку визначено у будь-якому одному з пп. 1-30, для застосування як фармацевтичного засобу.
32. Сполука, яку визначено у будь-якому одному з пп. 1 - 30, але за винятком умов (с) та (d), для застосування у профілактиці або лікуванні аритмій.
33. Фармацевтична композиція, що містить сполуку, яку визначено у будь-якому одному з пп. 1 – 30, у суміші з фармацевтично прийнятним ад'ювантом, розріджувачем або носієм.
34. Фармацевтична композиція для застосування у профілактиці або лікуванні аритмій, що містить сполуку, яку визначено у будь-якому одному з пп. 1 до 30.
35. Застосування сполуки, яку визначено у будь-якому одному з пп. 1 до 30, але за винятком умов (с) та (d), як активного інгредієнта для виробництва медикаменту для застосування у профілактиці або лікуванні аритмій.
36. Застосування за п. 35, де аритмія є атріальною або вентрикулярною аритмією.
37. Спосіб профілактики або лікування аритмій, у якому застосовують терапевтично ефективну кількість сполуки, яку визначено у будь-якому одному з пп. 1 -30, але за винятком умов (с) та (d), до особи, що потерпає від такого стану або схильна до нього.
38. Спосіб отримання сполуки формули І, яку визначено у п. 1, у якому:
(а) проводять реакцію сполуки формули II
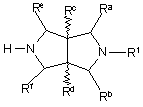 , ІІ
, ІІ
де R1 та Ra - Rf визначені у п. 1, зі сполукою формули ІІІ
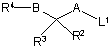 , ІІІ
, ІІІ
де L1 представляє групу, що відщеплюється а R2, R3, R4, A та В визначені у п. 1;
(b) для сполук формули І, в яких А представляє С2алкілен, а R2 та R3 разом представляють =O, проводять реакцію відповідної сполуки формули II, яку визначено вище, зі сполукою формули IV
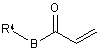 , IV
, IV
де R4 та В визначені у п. 1;
(с) для сполук формули І, в яких А представляє СН2, а R2 представляє -ОН або -N(H)R17, проводять реакцію відповідної сполуки формули II, яку визначено вище, зі сполукою формули V
![]() , V
, V
де Y представляє О або N(R17), а R3, R4, R17 та В визначені у п. 1;
(d) для сполук формули І, в яких А представляє С1-6алкілен, В представляє С1-4алкілен, а R2 та R3 представляють Н, відновлюють відповідну сполуку формули І, в якій R2 та R3 разом представляють =O;
(e) для сполук формули І, в яких R2 та R3 представляють Н, а (1) А представляє одиничний зв'язок або -J-N(R21), та В представляє С1-4алкілен, або (2) А представляє С1-6алкілен, а В представляє N(R22) або –N(R22)-Z- (у останній групі -N(R22) приєднано до атома карбону, що з'єднаний з R2 та R3), відновлюють відповідну сполуку формули І, в якій R2 та R3 разом представляють =O;
(f) для сполук формули І, в яких А представляє С1-4алкілен, В представляє безпосередній зв'язок, С1-4алкілен, -Z-N(R22)-, -Z-S(O)n- або –Z-O- (в останніх трьох групах Z представляє С1-4алкілен), R2 представляє ОН, а R3 представляє Н, відновлюють відповідну сполуку формули І, в якій R2 та R3 разом представляють =O;
(g) для сполук формули І, в яких R2 представляє -E-N(R18)C(O)N(H)R20a, проводять реакцію відповідної сполуки формули І, в якій R2 представляє -E-N(R18)H, зі сполукою формули XII
R20aN=C=О , XII
де R20a визначено у п. 1;
(h) для сполук формули І, в яких R2 представляє -E-N(H)[C(O)]2NH2, проводять реакцію відповідної сполуки формули І, в якій R2 представляє -Е-NН2, з діамідом щавлевої кислоти;
(і) для сполук формули І, в яких R2 представляє -E-N(R17)R18, де R17 та R18 визначені вище, за умови, що R17 не представляє H, проводять реакцію відповідної сполуки формули І, в якій R2 представляє -D-N(H)R18 зі сполукою формули XIII
R17a–L3 , XIII
де R17a представляє R17, що визначено у п. 1, за винятком того, що він не представляє Н, a L3 представляє групу, що відщеплюється;
(j) для сполук формули І, в яких R2 представляє -E-OR16, де R16 представляє С1-6алкіл, -Е-арил або -E-Het8, проводять реакцію відповідної сполуки формули І, в якій R2 представляє -Е-ОН, зі сполукою формули XIV
R16aOH , XIV
де R16a представляє С1-6алкіл, -Е-арил або -E-Het8, де Het8 визначено у п. 1;
(k) для сполук формули І, в яких R2 представляє E-OR16 (де R16 визначено у п. 1, за умови, що він не представляє Н, проводять реакцію відповідної сполуки формули І, в якій R2 представляє -Е-ОН, зі сполукою формули XVI
R16b–L4 , XVI
де R16b представляє R16, що визначено у п.1, за винятком того, що він не представляє Н, а L4 представляє групу, що відщеплюється;
(l) для сполук формули І, в яких R2 представляє атом галогену, заміщують відповідну сполуку формули І, в якій R2 представляє -ОН, використовуючи засіб галогенування;
(аа) знімають захист з захищеного похідного сполуки формули І, яку визначено у п. 1.
39. Спосіб отримання сполуки формули І, яку визначено у п.1, у якому:
(а) для сполук формули І, в яких В представляє -Z-О-, проводять реакцію сполуки формули VI
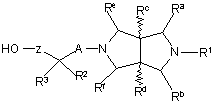 , VI
, VI
де R1, R2, R3, Ra – Rf, А та Z визначені у п. 1, зі сполукою формули VII
R4 ОН , VII
в якій R4 визначено у п. 1;
(b) для сполук формули І, в яких В представляє -Z-O-, проводять реакцію сполуки формули VI, яку визначено вище, зі сполукою формули VIII
R4–L2 , VIII
де L2 представляє групу, що відщеплюється, а R4 визначено у п. 1.
40. Спосіб отримання сполуки формули І, яку визначено у п.1, у якому:
(a) проводять реакцію відповідної сполуки формули XVII
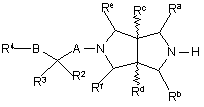 , XVII
, XVII
де R2, R3, R4, Ra – Rf, А та В визначені у п. 1, зі сполукою формули XVIII,
R1–L5 , XVIII
де L5 представляє групу, що відщеплюється, а R1 визначено у п. 1;
(b) для сполук формули І, в яких R1 представляє -C(O)N(H)R8, проводять реакцію відповідної сполуки формули XVII, що визначено вище, зі сполукою формули XXI,
R8-N=C=O , XXI
де R8 визначено у п. 1;
(c) для сполук формули І, в яких R1 представляє С1-12алкіл, причому алкільна група є заміщеною при С-2-атомі карбону (стосовно біспідинового атома нітрогену) групою ОН або N(H)R6, а інакше, як варіант, заміщеною одним або більше подальшими замісниками, які визначено у п. 1 для R1, проводять реакцію відповідної сполуки формули XVII, що визначено вище, зі сполукою формули XXII
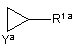 , XXII
, XXII
де Yа представляє О або N(R6), R1a представляє С1-10алкіл, як варіант, заміщений одним або більше замісниками, які визначено у п. 1 для R1, a R6 визначено у п. 1.
41. Спосіб отримання сполуки формули І, яку визначено у п.1, у якому
для сполук формули І, в яких А представляє С1-6алкілен, а В представляє –N(R22)-Z- (де групу -N(R22)- приєднано до атома карбону, що з'єднаний з R2 та R3), проводять реакцію сполуки формули IX
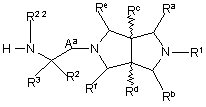 , IX
, IX
де Аa представляє С1-6алкілен, а R1, R2, R3, R22 та Ra – Rf визначені у п. 1, зі сполукою формули X
R4-Z-L2, X
де L2 визначено вище, а R4 та Z визначені у п. 1.
42. Спосіб отримання сполуки формули І, яку визначено у п.1, у якому
для сполук формули І, в яких R2 представляє -E-NH2, відновлюють відповідну сполуку формули XI
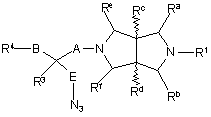 , XI
, XI
де R1, R3, R4, Ra – Rf, А, В та Е визначені у п. 1.
43. Спосіб отримання сполуки формули І, яку визначено у п.1, у якому
для сполук формули І, в яких R2 представляє -E-OR16 (де R16 представляє С1-6алкіл, -Е-арил або -E-Het8), проводять реакцію відповідної сполуки формули XV
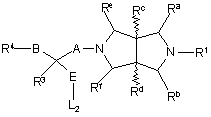 , XV
, XV
де L2 визначено вище, a R1, R3, R4, Ra - Rf, А, В та Е визначено у п. 1, зі сполукою формули XIV, яку визначено вище.
44. Спосіб отримання сполуки формули І, яку визначено у п.1, у якому
для сполук формули І, в яких R1 представляє -C(O)XR7 або –C(O)N(R8)R5d, проводять реакцію сполуки формули XIX
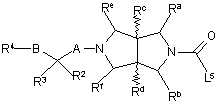 , XIX
, XIX
де R2, R3, R4, Ra – Rf, А, В визначені у п. 1, a L5 визначено вище, зі сполукою формули XX
R26-H , XX
де R26 представляє -XR7 або -N(R8)R5d, a R5d, R7, R8 та Х визначені у п. 1.
45. Спосіб отримання сполуки формули І, яку визначено у п.1, у якому
для сполук формули І, в яких R1 представляє -C(O)OR7, а Ra та/або Rb представляють С1-4алкіл, проводять реакцію відповідної сполуки формули І, в якій R1 представляє -C(O)OR7, a Ra та Rb представляють Н, з одним або більше еквівалентами сполуки формули XXIII
R27-L2 , XXIII
де R27 представляє С1-4алкіл, а L2 визначено вище, у присутності прийнятної сильної основи, здатної депротонувати 3,7-діазадицикло[3.3.0]октанове кільце у позиції ![]() -стосовно атома нітрогену, що з'єднаний з групою -C(O)OR7.
-стосовно атома нітрогену, що з'єднаний з групою -C(O)OR7.
46. Спосіб отримання сполуки формули І, яку визначено у п.1, у якому
для сполук формули І, які є N-оксидними похідними 3,7-діазадицикло[3.3.0]октанового атому нітрогену, здійснюють окиснення відповідного 3,7-діазадицикло[3.3.0]октанового атома нітрогену відповідної сполуки формули І.
47. Спосіб отримання сполуки формули І, яку визначено у п.1, у якому
для сполук формули 1, які є похідними солі четвертинного С1-4алкіламонію, в яких алкілгрупу приєднано до 3,7-діазадицикло[3.3.0]октанового атома нітрогену, проводять реакцію на 3,7-діазадицикло[3.3.0]октановому атомі нітрогену відповідної сполуки формули І зі сполукою формули XXIII, яку визначено вище.
48. Сполука формули II, яку визначено у п. 38, або її захищене похідне, за умови, що коли усі Rа – Rf представляють Н, то R1 не представляє:
(і) С1-12алкіл, як варіант, заміщений арилом або Het1;
(іі) -С(O)-(як варіант, заміщений арил); або
(ііі) трет-бутилоксикарбоніл.
49. Сполука формули VI, яку визначено у п. 39, або її захищене похідне.
50. Сполука формули IX, яку визначено у п. 41, або її захищене похідне.
51. Сполука формули XI, яку визначено у п. 42, або її захищене похідне.
52. Сполука формули XV, яку визначено у п. 43, або її захищене похідне.
53. Сполука формули XVII, яку визначено у п. 40, або її захищене похідне, за умови, що коли В представляє Z, то R2 представляє -Е-О-(як варіант, заміщений арил).
54. Сполука формули XIX, яку визначено у п. 44, або її захищене похідне.
Текст
1. Сполука формули І Re Ra Rc C2 2 (19) 1 3 75382 4 більше замісниками, вибраними з групи: -ОН, атом дванадцятичленну гетероциклічну групу, що місгалогену, ціаногрупа, нітрогрупа та арил) або арил; тить один або більше гетероатомів, вибраних з D представляє безпосередній зв'язок або С1оксигену, нітрогену та/або сульфуру, ці гетероциклічні групи, як варіант, заміщені одним або більше 6алкілен; R9 представляє, у кожному випадку своєї наявносзамісниками включаючи =O, -ОН, ціаногрупу, атом ті, С1-6алкіл (як варіант, заміщений та/або закінчегалогену, нітрогрупу, С1-6алкіл (як варіант, закінчений одним або більше замісниками, вибраними з ний групою -N(H)C(O)OR23a), С1-6алкоксил, Het1, групи: -ОН, атом галогену, ціаногрупа, нітрогрупа арил, -N(R24a)R24b, -C(O)R24c, -С(O)ОR24d, 7 та арил), арил або Het ; C(O)N(R24e)R24f, -N(R24g)C(O)R24h, 2 24i 24j 24k R представляє Н, атом галогену, С1-6алкіл, -EN(R )C(O)N(R )R , -N(R24m)S(O)2R23b, OR16, -E-N(R17)R18 або, разом з R3, представляє S(O)nR23c, -OS(O)2R23d та –S(O)2N(R24n)R24p; =O; R23a - R23d незалежно представляють, у кожному R3 представляє Н, С1-6алкіл або, разом з R2, предвипадку своєї наявності, С1-6алкіл; ставляє =O; R24a - R24p незалежно представляють, у кожному 16 8 R представляє Н, С1-6алкіл, -Е-арил, -E-Het , випадку своєї наявності, Н або С1-6алкіл; C(O)R19a, -C(O)OR19b або –C(O)N(R20a)R20b; n дорівнює, у кожному випадку, 0, 1 або 2, а R17 представляє Н, С1-6алкіл, -Е-арил, -E-Het8, Ra - Rf незалежно представляють Н або С1-4алкіл; С(O)R19a, -С(O)ОR19b, -S(O)2R19c, -[C(O)]pN(R20a)R20b де кожний арил та кожну арилоксигрупу, якщо не або -C(NH)NH2; визначено інше, як варіант, заміщено; R18 представляє Н, С1-6алкіл, -Е-арил або – або її фармацевтично прийнятне похідне; C(O)R19d; за умови, що: R19a – R19d незалежно представляють, у кожному (a) коли R3 представляє Н або С1-4алкіл; а випадку своєї наявності, С1-6алкіл (як варіант, заА представляє -J-N(R21)- або -J-O-; міщений та/або закінчений одним або більше заміто В не представляє -N(R22)-, -S(O)n-, -О- або – сниками, вибраними з групи: атом галогену, арил N(R22)-Z- (в останньому групу -N(R22) приєднано до 9 10 19a 19d та Het ), арил, Het , або R та R незалежно атома карбону, що з'єднаний з R2 тa R3); представляють Н; (b) коли R2 представляє -E-OR15 або -E-N(R17)R18, R20a та R20b незалежно представляють, у кожному в яких Е представляє безпосередній зв'язок, то: випадку своєї наявності, Н або С1-6алкіл (як варі(і) А не представляє безпосереднього зв'язку, -Jант, заміщений та/або закінчений одним або більN(R21)- або -J-O-, а ше замісниками, вибраними з групи: атом галоге(іі) В не представляє -N(R22)-, -S(O)n-, -О- або 11 12 ну, арил та Het ), арил, Het , або разом N(R22)-Z- (в останньому групу -N(R22) приєднано до 2 3 представляють С3-6алкілен, як варіант, перерваний атома карбону, що з'єднаний з R тa R ); 1 13 атомом О; (c) Het та Het не представляють 9-членних гетеЕ представляє, у кожному випадку своєї наявності, роциклів, що містять конденсоване бензольне або безпосередній зв'язок або С1-4алкілен; піридинове кільце; та р дорівнює 1 або 2; (d) сполука не представляє: А представляє -G-, -J-N(R21)- або -J-O-(в останніх 3,7-біс(1-фенілетил)-3,7-діазадицикло[3.3.0]октан; двох групах N(R21)- або O приєднано до атома 2-{4-(7-бензил-3,7-діазадицикло[3.3.0]октан-3карбону, що з'єднаний з R2 та R3); іл)бутил}-1,2-бензізотіазол-3-он-1,1-діоксид; В представляє -Z-, -Z-N(R22), -N(R22)-Z-, -Z-S(O)n-, 3-метил-7-бензил-3,7-діазадицикло[3.3.0]октан; Z-O-(в останніх двох групах Z приєднано до атома 3-циклогексил-7-бензил-3,7карбону, що з'єднаний з R2 та R3); діазадицикло[3.3.0]октан; G представляє безпосередній зв'язок або С13-(тіазол-2-іл)-7-бензил-3,7діазадицикло[3.3.0]октан; 6алкілен; J представляє С2-6алкілен; 3-(2-піримідил)-7-бензил-3,7Z представляє безпосередній зв'язок або С1діазадицикло[3.3.0]октан або 3-(5,5-диметокси)пентил-7-бензил-3,74алкілен; R21 та R22 незалежно представляють Н або С1діазадицикло[3.3.0]октан; 2. Сполука за п. 1, де у сполуці формули І один 6алкіл; R4 представляє арил або Het13, обидві ці групи, як або більше необов'язкових замісників на арил- та варіант, заміщені одним або більше замісниками, арилоксигрупах вибрані з групи: -ОН, ціаногрупа, вибраними з групи: -ОН, ціаногрупа, атом галогеатом галогену, нітрогрупа, С1-6алкіл (як варіант, ну, нітрогрупа, С1-6алкіл (як варіант, закінчений закінчений групою -N(H)C(O)OR23a), С1-6алкоксил, 23a 1 групою –N(H)C(O)OR ), С1-6алкоксил, Het , арил, Het1, арил (ця арилгрупа може не бути заміщеною 24a 24b 24c 24d -N(R )R , -C(O)R , -С(O)ОR , будь-якими іншими арил-групами), -N(R24a)R24b, C(O)N(R24e)R24f, -N(R24g)C(O)R24h, C(O)R24c, -С(O)ОR24d, -C(O)N(R24e)R24f, 24i 24j 24k 24m 23b 24g 24h 24i N(R )C(O)N(R )R , -N(R )S(O)2R , N(R )C(O)R , -N(R )C(O)N(R24j)R24k, S(O)nR23c, -OS(O)2R23d, -S(O)2N(R24n)R24p та (тільки N(R24m)S(O)2R23b, -S(O)nR23c, -ОS(О)2R23d та 13 24n 24p 1 23a 23d 24a 24p у випадку Het ) оксогрупа; S(O)2N(R )R , де Het , R – R , R - R та 13 Het представляє чотири-дванадцятичленну гетеn визначені у п. 1. роциклічну групу, що містить один або більше ге3. Сполука за п. 1 або п. 2, де хвилясті лінії предтероатомів, вибраних з оксигену, нітрогену та/або ставляють відносну цис-стереобудову. сульфуру; 4. Сполука за будь-яким одним з пп. 1 - 3, де R1 1 12 Het - Het незалежно представляють, у кожному представляє С1-8алкіл (як варіант, заміщений випадку своєї наявності, чотирита/або закінчений одним або більше замісниками, 5 75382 6 вибраними з групи: атом галогену, як варіант, заніх трьох групах Z приєднано до атома карбону, міщений феніл, Het1, -C(O)R5a, -OR5b, -C(O)OR7, що з'єднаний з R2 та R3). 8 2 7 C(O)N(H)R та -S(O)2-C1-6алкіл), Het , -C(O)OR , 21. Сполука за п. 19, де G представляє безпосеС(O)N(Н)Rs або -S(O)2R9. редній зв'язок або С1-5алкілен. 5. Сполука за будь-яким одним з пп. 1 - 4, де R5a та 22. Сполука за будь-яким одним з пп. 1 - 21, де Z 5b R незалежно представляють у кожному випадку представляє безпосередній зв'язок або С1Н, С1-6алкіл (як варіант, заміщений та/або закінче3алкілен. ний одним або більше замісниками, вибраними з 23. Сполука за будь-яким одним з пп. 1 - 22, де R4 групи: -ОН, С1-4алкоксил та атом галогену), як вапредставляє феніл або Het13, де обидві ці групи, як 4 ріант, заміщений феніл або Het . варіант, заміщені одним або більше замісниками, 6. Сполука за будь-яким одним з пп. 1 - 5, де R7 вибраними з групи: ціаногрупа, атом галогену, нітпредставляє, у кожному випадку, С1-8алкіл (цю рогрупа, С1-4лкіл (як варіант, закінчений групою – групу, як варіант, заміщено та/або закінчено одним N(H)C(O)OR23a), С1-4алкоксил, як варіант, заміщеабо більше замісниками, вибраними з групи: -ОН, ний феніл, -C(O)N(H)R24e, -N(Н)С(O)R24h, атом галогену, ціаногрупа, як варіант, заміщений N(Н)С(O)N(Н)R24j, -N(H)S(O)2R23b, -S(O)2R23с та – 13a 13b 5 феніл, С1-4алкоксил, -SO2R , -C(O)R тa Het ). S(O)2N(R24n)R24p. 13a 13b 7. Сполука за п. 6, де R та R незалежно пред24. Сполука за п. 23, де Het13 представляє п'ятиставляють С1-6алкіл. десятичленну гетероциклічну групу, що містить 8. Сполука за будь-яким одним з пп. 1 - 7, де R8 один або більше гетероатомів, вибраних з оксигепредставляє, у кожному випадку, С1-8алкіл (цю ну, нітрогену та/або сульфуру. групу, як варіант, заміщено та/або закінчено одним 25. Сполука за будь-яким одним з пп. 1 - 24, де або більше замісниками, вибраними з групи: -ОН, Het1 - Het12 незалежно представляють, у кожному атом галогену, ціаногрупа та С1-4алкоксил), -D-(як випадку своєї наявності, п'яти-десятичленні гетеваріант, заміщений феніл), -D-Het6, -D-S(O)2R15a, роциклічні групи, що містять один або більше геD-С(O)-С1-6алкіл або -D-C(O)OR15b. тероатомів, вибраних з оксигену, нітрогену та/або 9. Сполука за п. 8, де R15a та R15b незалежно предсульфуру, ці гетероциклічні групи, як варіант, заставляють С1-6алкіл (як варіант, заміщений та/або міщені одним або більше замісниками, включаючи закінчений одним або більше замісниками, вибра=O, -ОН, ціаногрупу, атом галогену, нітрогрупу, С1ними з групи: атом галогену, ціаногрупа та, як ва4алкіл, С1-4алкоксил, як варіант, заміщений феніл, ріант, заміщений феніл) або, як варіант, заміщеNH2, -C(O)R24c, -C(O)OR24d, -C(O)N(H)R24e, ний феніл. N(Н)С(O)R24h та –S(O)nR23c. 10. Сполука за будь-яким одним з пп. 1 - 9, де D 26. Сполука за будь-яким одним з пп. 1 - 25, де Ra f представляє безпосередній зв'язок або С1– R незалежно представляють Н або С1-2алкіл. 27. Сполука за будь-яким одним з пп. 1 - 26, де 3алкілен. 11. Сполука за будь-яким одним з пп. 1 - 10, де R9 необов'язкові замісники на фенольних групах вибпредставляє, у кожному випадку, С1-5алкіл (як варані з групи: -ОН, ціаногрупа, атом галогену, нітроріант, заміщений та/або закінчений одним або бігрупа, С1-4алкіл (як варіант, закінчений групою – льше замісниками, вибраними з групи: атом галоN(H)C(O)OR23a), С1-4алкоксил, -NН2, -C(O)R24c, гену, ціаногрупа та, як варіант, заміщений феніл) С(O)ОR24d, -C(O)N(H)R24e, -N(H)C(O)R24h, або, як варіант, заміщений феніл. N(H)C(O)N(H)R24j, -N(H)S(O)2R23b, -S(O)nR23c тa – 12. Сполука за будь-яким одним з пп. 1 - 11, де R2 S(O)2N(R24n)R24p. представляє Н, С1-2алкіл, -OR16, -N(H)R17 або, ра28. Сполука за п. 27, де R23a - R23c, R24c, R24d, R24e, 3 зом з R , представляє =O. R24h, R24j, R24n та R24p незалежно представляють 3 13. Сполука за будь-яким одним з пп. 1 - 12, де R С1-4алкіл. представляє Н, С1-2алкіл або, разом з R2, предста29. Сполука за будь-яким одним з пп. 1 - 28, де n вляє =O. дорівнює 0 або 2. 14. Сполука за будь-яким одним з пп. 1 - 13, де R16 30. Сполука за будь-яким одним з пп. 1 - 29, де представляє Н, С1-4алкіл, -Е-(як варіант, заміщеалкільні групи та алкоксигрупи можуть бути, якщо ний феніл), -C(O)R19a –C(O)N(H)R20a. не визначено інше: 15. Сполука за будь-яким одним з пп. 1 - 13, де R17 (і) лінійними або розгалуженими, циклічними або представляє Н, С1-4алкіл, -Е-(як варіант, заміщечастково циклічними/ациклічними; ний феніл), -C(O)R19a або –C(O)OR19b. (іі) насиченими або ненасиченими; 16. Сполука за будь-яким одним з пп. 1 - 15, де (ііі) перерваними одним або більше атомами оксиR19a та R19b незалежно представляють у кожному гену та/або випадку С1-6алкіл, як варіант, заміщений феніл або (iv) заміщеними одним або більше атомами флуоHet10. ру або хлору. 17. Сполука за будь-яким одним з пп. 1 - 14, де 31. Сполука, яку визначено у будь-якому одному з R20a представляє Н або С1-4алкіл. пп. 1-30, для застосування як фармацевтичного 18. Сполука за будь-яким одним з пп. 1 - 17, де Е засобу. представляє, у кожному випадку, безпосередній 32. Сполука, яку визначено у будь-якому одному з зв'язок або С1-2алкілен. пп. 1 - 30, але за винятком умов (с) та (d), для за19. Сполука за будь-яким одним з пп. 1 - 18, де А стосування у профілактиці або лікуванні аритмій. представляє -G-. 33. Фармацевтична композиція, що містить сполу20. Сполука за будь-яким одним з пп. 1 - 19, де В ку, яку визначено у будь-якому одному з пп. 1 – 30, представляє -Z-, -Z-N(H)-, -Z-S(O)n-, -Z-O- (у остану суміші з фармацевтично прийнятним ад'ювантом, розріджувачем або носієм. 7 75382 8 34. Фармацевтична композиція для застосування у влюють відповідну сполуку формули І, в якій R2 та профілактиці або лікуванні аритмій, що містить R3 разом представляють =O; сполуку, яку визначено у будь-якому одному з пп. (f) для сполук формули І, в яких А представляє С11 до 30. 4алкілен, В представляє безпосередній зв'язок, С122 35. Застосування сполуки, яку визначено у будь4алкілен, -Z-N(R )-, -Z-S(O)n- або –Z-O- (в останніх 2 якому одному з пп. 1 до 30, але за винятком умов трьох групах Z представляє С1-4алкілен), R пред3 (с) та (d), як активного інгредієнта для виробництставляє ОН, а R представляє Н, відновлюють ва медикаменту для застосування у профілактиці відповідну сполуку формули І, в якій R2 та R3 раабо лікуванні аритмій. зом представляють =O; 36. Застосування за п. 35, де аритмія є атріальною (g) для сполук формули І, в яких R2 представляє або вентрикулярною аритмією. E-N(R18)C(O)N(H)R20a, проводять реакцію відповід37. Спосіб профілактики або лікування аритмій, у ної сполуки формули І, в якій R2 представляє -Eякому застосовують терапевтично ефективну кільN(R18)H, зі сполукою формули XII кість сполуки, яку визначено у будь-якому одному R20aN=C=О , XII з пп. 1 -30, але за винятком умов (с) та (d), до осоде R20a визначено у п. 1; би, що потерпає від такого стану або схильна до (h) для сполук формули І, в яких R2 представляє нього. E-N(H)[C(O)]2NH2, проводять реакцію відповідної 38. Спосіб отримання сполуки формули І, яку висполуки формули І, в якій R2 представляє -Е-NН2, з значено у п. 1, у якому: діамідом щавлевої кислоти; (а) проводять реакцію сполуки формули II (і) для сполук формули І, в яких R2 представляє E-N(R17)R18, де R17 та R18 визначені вище, за умоRe Ra Rc ви, що R17 не представляє H, проводять реакцію відповідної сполуки формули І, в якій R2 представляє -D-N(H)R18 зі сполукою формули XIII H N N R1 R17a–L3 , XIII де R17a представляє R17, що визначено у п. 1, за d Rf винятком того, що він не представляє Н, a L3 R Rb , ІІ представляє групу, що відщеплюється; де R1 та Ra - Rf визначені у п. 1, зі сполукою фор(j) для сполук формули І, в яких R2 представляє мули ІІІ E-OR16, де R16 представляє С1-6алкіл, -Е-арил або 4 R B -E-Het8, проводять реакцію відповідної сполуки A 1 L формули І, в якій R2 представляє -Е-ОН, зі сполукою формули XIV R2 R3 , ІІІ R16aOH , XIV де L1 представляє групу, що відщеплюється а R2, де R16a представляє С1-6алкіл, -Е-арил або -E-Het8, 3 4 R , R , A та В визначені у п. 1; де Het8 визначено у п. 1; (b) для сполук формули І, в яких А представляє (k) для сполук формули І, в яких R2 представляє E2 3 С2алкілен, а R та R разом представляють =O, OR16 (де R16 визначено у п. 1, за умови, що він не проводять реакцію відповідної сполуки формули II, представляє Н, проводять реакцію відповідної яку визначено вище, зі сполукою формули IV сполуки формули І, в якій R2 представляє -Е-ОН, зі O сполукою формули XVI R16b–L4 , XVI 4 R де R16b представляє R16, що визначено у п.1, за B , IV винятком того, що він не представляє Н, а L4 де R4 та В визначені у п. 1; представляє групу, що відщеплюється; (с) для сполук формули І, в яких А представляє (l) для сполук формули І, в яких R2 представляє СН2, а R2 представляє -ОН або -N(H)R17, провоатом галогену, заміщують відповідну сполуку фодять реакцію відповідної сполуки формули II, яку рмули І, в якій R2 представляє -ОН, використовуювизначено вище, зі сполукою формули V чи засіб галогенування; (аа) знімають захист з захищеного похідного споB R4 луки формули І, яку визначено у п. 1. Y 39. Спосіб отримання сполуки формули І, яку виR3 ,V значено у п.1, у якому: 17 3 4 17 де Y представляє О або N(R ), а R , R , R та В (а) для сполук формули І, в яких В представляє -Zвизначені у п. 1; О-, проводять реакцію сполуки формули VI (d) для сполук формули І, в яких А представляє С1Re Ra 2 3 Rc 6алкілен, В представляє С1-4алкілен, а R та R представляють Н, відновлюють відповідну сполуку формули І, в якій R2 та R3 разом представляють HO z A N N R1 =O; 2 3 (e) для сполук формули І, в яких R та R предстаR2 R3 вляють Н, а (1) А представляє одиничний зв'язок Rf Rd Rb або -J-N(R21), та В представляє С1-4алкілен, або (2) , VI 22 1 2 3 a f А представляє С1-6алкілен, а В представляє N(R ) де R , R , R , R – R , А та Z визначені у п. 1, зі або –N(R22)-Z- (у останній групі -N(R22) приєднано сполукою формули VII до атома карбону, що з'єднаний з R2 та R3), відноR4 ОН , VII 9 75382 10 в якій R4 визначено у п. 1; 42. Спосіб отримання сполуки формули І, яку ви(b) для сполук формули І, в яких В представляє -Zзначено у п.1, у якому O-, проводять реакцію сполуки формули VI, яку для сполук формули І, в яких R2 представляє -Eвизначено вище, зі сполукою формули VIII NH2, відновлюють відповідну сполуку формули XI R4–L2 , VIII Re Ra Rc 2 4 де L представляє групу, що відщеплюється, а R визначено у п. 1. R4 B 40. Спосіб отримання сполуки формули І, яку виA N N R1 значено у п.1, у якому: (a) проводять реакцію відповідної сполуки формуE R3 Rf ли XVII Rd Rb e c N3 R Ra R , XI R4 B A N R2 R3 N Rf Rd H Rb , XVII де R , R , R , R – R , А та В визначені у п. 1, зі сполукою формули XVIII, R1–L5 , XVIII де L5 представляє групу, що відщеплюється, а R1 визначено у п. 1; (b) для сполук формули І, в яких R1 представляє C(O)N(H)R8, проводять реакцію відповідної сполуки формули XVII, що визначено вище, зі сполукою формули XXI, R8-N=C=O , XXI де R8 визначено у п. 1; (c) для сполук формули І, в яких R1 представляє С1-12алкіл, причому алкільна група є заміщеною при С-2-атомі карбону (стосовно біспідинового атома нітрогену) групою ОН або N(H)R6, а інакше, як варіант, заміщеною одним або більше подальшими замісниками, які визначено у п. 1 для R1, проводять реакцію відповідної сполуки формули XVII, що визначено вище, зі сполукою формули XXII 2 3 4 a f де R1, R3, R4, Ra – Rf, А, В та Е визначені у п. 1. 43. Спосіб отримання сполуки формули І, яку визначено у п.1, у якому для сполук формули І, в яких R2 представляє -EOR16 (де R16 представляє С1-6алкіл, -Е-арил або E-Het8), проводять реакцію відповідної сполуки формули XV Re Ra Rc R4 B N Aa R3 R2 N Rf N Rd Rb R1 , IX де А представляє С1-6алкілен, а R1, R2, R3, R22 та Ra – Rf визначені у п. 1, зі сполукою формули X R4-Z-L2, X де L2 визначено вище, а R4 та Z визначені у п. 1. a N Rf Rd R1 Rb , XV де L2 визначено вище, a R1, R3, R4, Ra - Rf, А, В та Е визначено у п. 1, зі сполукою формули XIV, яку визначено вище. 44. Спосіб отримання сполуки формули І, яку визначено у п.1, у якому для сполук формули І, в яких R1 представляє C(O)XR7 або –C(O)N(R8)R5d, проводять реакцію сполуки формули XIX Re Ra Rc B A R2 R3 а H N L2 Ya , XXII де Y представляє О або N(R6), R1a представляє С1-10алкіл, як варіант, заміщений одним або більше замісниками, які визначено у п. 1 для R1, a R6 визначено у п. 1. 41. Спосіб отримання сполуки формули І, яку визначено у п.1, у якому для сполук формули І, в яких А представляє С122 6алкілен, а В представляє –N(R )-Z- (де групу 22 N(R )- приєднано до атома карбону, що з'єднаний з R2 та R3), проводять реакцію сполуки формули IX Re Ra Rc R2 2 E R3 R4 R1 a A O N N L5 Rf Rd Rb , XIX де R , R , R , R – R , А, В визначені у п. 1, a L5 визначено вище, зі сполукою формули XX R26-H , XX де R26 представляє -XR7 або -N(R8)R5d, a R5d, R7, R8 та Х визначені у п. 1. 45. Спосіб отримання сполуки формули І, яку визначено у п.1, у якому для сполук формули І, в яких R1 представляє C(O)OR7, а Ra та/або Rb представляють С1-4алкіл, проводять реакцію відповідної сполуки формули І, в якій R1 представляє -C(O)OR7, a Ra та Rb представляють Н, з одним або більше еквівалентами сполуки формули XXIII R27-L2 , XXIII де R27 представляє С1-4алкіл, а L2 визначено вище, у присутності прийнятної сильної основи, здатної депротонувати 3,7-діазадицикло[3.3.0]октанове кільце у позиції -стосовно атома нітрогену, що з'єднаний з групою -C(O)OR7. 46. Спосіб отримання сполуки формули І, яку визначено у п.1, у якому 2 3 4 a f 11 75382 12 для сполук формули І, які є N-оксидними похідни(і) С1-12алкіл, як варіант, заміщений арилом або ми 3,7-діазадицикло[3.3.0]октанового атому нітроHet1; гену, здійснюють окиснення відповідного 3,7(іі) -С(O)-(як варіант, заміщений арил); або діазадицикло[3.3.0]октанового атома нітрогену (ііі) трет-бутилоксикарбоніл. відповідної сполуки формули І. 49. Сполука формули VI, яку визначено у п. 39, 47. Спосіб отримання сполуки формули І, яку виабо її захищене похідне. значено у п.1, у якому 50. Сполука формули IX, яку визначено у п. 41, для сполук формули 1, які є похідними солі четвеабо її захищене похідне. ртинного С1-4алкіламонію, в яких алкілгрупу приєд51. Сполука формули XI, яку визначено у п. 42, нано до 3,7-діазадицикло[3.3.0]октанового атома або її захищене похідне. нітрогену, проводять реакцію на 3,752. Сполука формули XV, яку визначено у п. 43, діазадицикло[3.3.0]октановому атомі нітрогену або її захищене похідне. відповідної сполуки формули І зі сполукою форму53. Сполука формули XVII, яку визначено у п. 40, ли XXIII, яку визначено вище. або її захищене похідне, за умови, що коли В 48. Сполука формули II, яку визначено у п. 38, або представляє Z, то R2 представляє -Е-О-(як варіа f її захищене похідне, за умови, що коли усі R – R ант, заміщений арил). представляють Н, то R1 не представляє: 54. Сполука формули XIX, яку визначено у п. 44, або її захищене похідне. Цей винахід стосується нових фармацевтично корисних сполук, зокрема сполук, які корисні при лікуванні серцевих аритмій. Серцеві аритмії можна визначити як аномалії частоти, регулярності або місця походження серцевого імпульсу, або як порушення провідності, що викликає аномальну послідовність активації. Аритмії можна класифікувати клінічно за припустимою ділянкою походження (тобто як суправентрикулярні, включаючи атріальні та атріовентрикулярні аритмії та вентрикулярні аритмії) та/або за частотою (тобто брадіаритмії (повільні) та тахіаритмії (швидкі)). При лікуванні серцевих аритмій негативний результат клінічних досліджень [дивися, наприклад, результат дослідження супресії серцевих аритмій (CAST), наведений у New England Journal of Medicine, 321, 406 (1989)], "традиційними" антіаритмічними ліками, які первісно діють уповільненням швидкості провідності (клас І антіаритмічних ліків), підказав розробку ліків стосовно сполук, які селективно затримують серцеву реполяризацію, подовжуючи цим інтервал QT. Клас III антіаритмічних ліків можна визначити як ліки, які подовжують тривалість трансмембранної дії потенціалу (що може бути викликаним блокуванням спрямованих назовні струмів К+ або збільшенням спрямованих усередину іонних струмів) та несприйнятливість, без впливу на серцеву провідність. Одним з ключових недоліків досі відомих ліків, які діють затримкою реполяризації (клас III або іншим способом) є те, що усі вони, як відомо, викликають унікальну форму проаритмії, відому як тріпотіння-мерехтіння (torsades de pointes), яке може іноді бути фатальним. З точки зору безпеки мінімізація цього феномену (який також спостерігали як результат застосування несерцевих ліків, як-то фенотіазинів, трициклічних антидепресантів, антигістамінів, та антибіотиків) є ключовою проблемою для вирішення проблеми створення ефективних антіаритмічних ліків. Антіаритмічні ліки на основі біспідинів (3,7діазадицикло[3,3,1]нонанів), відомі серед іншого з [міжнародних патентних заявок WO 91/07405, WO 99/31100, WO 00/76997, WO 00/76998, WO 00/76999 та WO 00/77000, Європейських патентних заявок 306 871, 308 843 та 655 228 та патентів США 3,962,449, 4,556,662, 4,550,112, 4,459,301 та 5,468,858, а також публікацій в журналах, включаючи серед іншого: J. Med. Chem. 39, 2559 (1996); Pharmacol. Res. 24, 149 (1991); Circulation, 90, 2032 (1994); Anal. Sci. 9, 429, (1993)]. Сполуки на основі 3,7-діазадицикло[3.3.0]октану не розкриті і не запропоновані у будь-якому з цих документів. Сполуки на основі 3,7діазадицикло[3.3.0]октану відомі як використовувані у багатьох з медичних застосувань, включаючи, серед іншого: засоби проти мігрені [як описано у WO 98/06725 та WO 97/11945]; антибіотики [як описано у WO 97/10223 та WO 96/35691]; нейролептики [як описано у WO 95/15327 та WO 95/13279]; інгібітори вторинного поглинання серотоніну [як описано у WO 96/07656]; інгібітори тромбіну [як описано у Helvetica Chim. Ada 83, 855 (2000), Chem. & Biol. 4, 287 (1997) та Angew. Chem. Int. Ed. Eng. 34, 1739 (1995)]; та анксіолітичні засоби [як описано у J. Med. Chem. 32, 1024 (1989)], далі, сполуки на основі 3,7діазадицикло[3.3.0]октану використовувані у лікуванні, серед іншого, шлунково-кишкових розладів [як описано у DE 3930266 А1] та хвороб, викликаних несправним функціонуванням глутамінергічної системи [як описано у WO 01/04107]. Інші 3,7-діазадицикло[3.3.0]октанові сполуки відомі як хімічна дивина серед іншого з [J. Heterocyclic. Chem. 20, 321 (1983), Chem. Веr. 101, 3010 (1968), J. Chem. Soc, Perkin Транс. Θ 1475 (1983), Tetrahedron, Suppl. 8 Частина I, 279 (1966) та J. Org. Chem. 61, 8897 (1996)], далі, 3,7-біс(1фенілетил)-3,7-діазадицикло[3.3.0]октан, як відомо, є корисним у контролюванні енантіоселективності реакцій між реагентами Гриньяра та альдегідами [як описано у Tetrahedron 5, 569 (1994)]. Жодний згаданий вище документ з попереднього рівня техніки, що стосується 3,7-діазадицикло[3.3.0]октанів не розкриває і не запропоно 13 75382 14 вує будь-яких свідоцтв, що розкриті тут сполуки або більше замісниками, вибраними з групи: -ОН, можуть бути корисними у лікуванні серцевих аритатом галогену, ціаногрупа, нітрогрупа, С1-4алкіл та мій. С1-4алкоксил), -D-арил, -D-арилоксил, -D-Het6, -DМи несподівано виявили, що нова група споN(H)C(O)R14a, -D-S(O)2R15a, -D-C(O)R14b, -D15b 14c 14d лук на основі 3,7-діазадицикло[3.3.0)-октанів виявC(O)OR , -D-C(O)N(R )R , або R8, разом з R5d, ляє електрофізіологічну активність, переважно представляє С3-6алкілен (цю алкіленову групу, як електрофізіологічну активність класу III, а тому варіант, перервано атомом О та/або, як варіант, можна чекати, є корисними у лікуванні серцевих заміщено одною або більше С1-3алкіл-групами); аритмій. R14a - R14b незалежно представляють Н, С1Згідно з винаходом запропоновано сполуки 6алкіл (як варіант, заміщений та/або закінчений формули І, одним або більше замісниками, вибраними з групи: -ОН, атом галогену, ціаногрупа, нітрогрупа та арил), арил., або R14cTa R14d разом представляють С3-6алкілен; R15a та R15b незалежно представляють С16алкіл (як варіант, заміщений та/або закінчений одним або більше замісниками, вибраними з групи: -ОН, атом галогену, ціаногрупа, нітрогрупа та арил) або арил; D представляє безпосередній зв'язок або С1де 6алкілен; хвилясті лінії представляють, як варіант, цисR9 представляє, у кожному випадку своєї наяабо транс- стереобудову; вності, С1-6алкіл (як варіант, заміщений та/або заR1 представляє С1-12апкіл (як варіант, заміщекінчений одним або більше замісниками, вибраниний та/або закінчений одним або більше замісними з групи: -ОН, атом галогену, ціаногрупа, ками, вибраними з групи: атом галогену, ціаногрунітрогрупа та арил), арил або Het7; па, нітрогрупа, арил, Het1, -C(O)R5a, -OR5b, R2 представляє Н, атом галогену, С1-6алкіл, -EN(R6)R5c, -C(O)XR7, -C(O)N(R8)R5d та -S(O)2R9), OR16, -E-N(R17)R18 або, разом з R3, представляє Het2, -C(O)R5a, -C(O)XR7, -C(О)N(R8)R5d або =О; S(O)2R9; R3 представляє Н, С1-6алкіл або, разом з R2, 5a 5d R - R незалежнo представляють, у кожному представляє =О; випадку своєї наявності, Н, С1-6алкіл (як варіант, R16 представляє Н, С1-6алкіл, -Е-арил, -E-Het8, 19a 19b 20a 20b заміщений та/або закінчений одним або більше -C(O)R , -C(O)OR або -C(O)N(R )R ; 17 замісниками, вибраними з групи: ОН, С1-6лкоксил, R представляє Η, С1-6алкіл, -Е-арил, -E-Het8, атом галогену, ціаногрупа, нітрогрупа, арил, Het3 -C(O)R19a, -C(O)OR19b, -S(O)2R19c, 10 4 5d 8 20a 20b та -NHC(O)R ), арил або Het , або R разом з R , [C(O)]pN(R )R або -C(NH)NH2; представляє С3-6алкілен (цю алкіленову групу, як R18 представляє Η, С1-6алкіл, -Е-арил або варіант, перервано атомом О та/або, як варіант, C(O)R19d; заміщено одною або більше С1-3алкіл-групами); R19a - R19d незалежно представляють, у кожR10 представляє Н, С1-4алкіл (як варіант, заміному випадку своєї наявності, С1-6алкіл (як варіант, щений та/або закінчений одним або більше замісзаміщений та/або закінчений одним або більше никами, вибраними з групи: атом галогену, ціаногзамісниками, вибраними з групи: атом галогену, рупа, арил та -NHC(O)R11) або арил; арил та Het9), арил, Het10, або R19a та R19d незалеR11 представляє Н, С1-4алкіл або арил; жно представляють Н; R6 представляє Н, С1-6алкіл (як варіант, заміR20a та R20b незалежно представляють, у кожщений та/або закінчений одним або більше замісному випадку своєї наявності, Η або С1-6алкіл (як никами, вибраними з групи: -ОН, атом галогену, варіант, заміщений та/або закінчений одним або ціаногрупа, нітрогрупа та арил), арил, -C(O)R12a, більше замісниками, вибраними з групи: атом гаC(O)OR12b або -C(O)N(H)R12c; логену, арил та Het11), арил, Het12, або разом 12a 12b 12c R , R та R представляють С1-6алкіл (як представляють С3-6алкілен, як варіант, перерваний варіант, заміщений та/або закінчений одним або атомом О; більше замісниками, вибраними з групи: -ОН, атом Ε представляє, у кожному випадку своєї наявгалогену, ціаногрупа, нітрогрупа та арил) або арил, ності, безпосередній зв'язок або С1-4алкілен;. або R12a та R12c представляють Н; p дорівнює 1 або 2; X представляє О або S; А представляє -G-, -J-N(R21)- або -J-O-(b 7 R представляє, у кожному випадку своєї наяостанніх двох групах N(R21)- або О-приєднано до вності, арил або С1-12алкіл (ця алкіл-група, як варіатому карбону, що з'єднаний з R2 та R3); ант, заміщена та/або закінчена одним або більш В представляє -Z-, -Z-N(R22), -N(R22)-Z-, -Zзамісниками, вибраними з групи: -ОН, атом галоS(O)n-, -Z-O-(b останніх двох групах Ζ приєднано 2 3 гену, ціаногрупа, нітрогрупа, арил, С1-6алкоксил, до атому карбону, що з'єднаний з R та R ); SO2R13a, -C(O)R13b тa Het5); G представляє безпосередній зв'язок або С1R13a та R13b незалежно представляють С16алкілен; 6алкіл або арил; J представляє С2-еалкілен; R8 представляє, у кожному випадку своєї наяΖ представляє безпосередній зв'язок або С1вності, Н, С1-12алкіл, С1-6алкоксил (ці останні дві 4алкілен; групи, як варіант, заміщені та/або закінчені одним R21 та R22 незалежно представляють Η або С1 15 75382 16 алкіл; діазадицикло[3.3.0]октан; або 6 R4 представляє арил або Het13, обидві ці гру3-(5,5-диметокси)пентил-7-бензил-3,7пи, як варіант, заміщені одним або більше замісдіазадицикло[3.3.0]октан; никами, вибраними з групи: -ОН, ціаногрупа, атом вищенаведені сполуки позначають далі як галогену, нітрогрупа, С1-6алкіл (як варіант, закінче"сполуки винаходу". Якщо не визначено інше, ал23a 1 ний групою -N(H)C(O)OR ), С1-6алкоксил, Het , кіл-групи та алкоксигрупи, які визначені тут, мо24a 24b 24c 24d арил, -N(R )R , -C(O)R , -C(O)OR , жуть мати лінійний ланцюг або, коли існує достатC(O)N(R24e)R24f, -N(R24g)C(O)R24h, нє число (тобто мінімум три) атомів карбону, мати N(R24i)C(O)N(R24j)R24k, -N(R24m)S(O)2R23b, розгалужений та/або циклічний ланцюг. Далі, коли S(O)nR23c, -OS(O)2R23d,-S(O)2N(R24n)R24p та (тільки існує достатнє число (тобто мінімум чотири) атомів у випадку Het13) оксогрупа; Het13 представляє чокарбону, такі алкільні та алкоксигрупи можуть татири-дванадцяти-членну гетероциклічну групу, що кож мати циклічні/ациклічні частини. Такі алкільні містить один або більше гетероатомів, вибраних з та алкоксигрупи можуть також бути насиченими оксигену, нітрогену та/або сульфуру; або, коли існує достатнє число (тобто мінімум два) Het1 - Het12 незалежно представляють, у кожатомів карбону, бути ненасиченими та/або перерному випадку своєї наявності, чотири-дванадцятиваними одним або більше атомами оксигену членну гетероциклічну групу, що містить один або та/або сульфур. Якщо не визначено інше, алкільні більше гетероатомів, вибраних з оксигену, нітрота алкоксигрупи можуть також бути заміщеними гену та/або сульфуру, ці гетероциклічні групи, як одним або більше атомами галогену, а особливо варіант, заміщені одним або більше замісниками флуору. включаючи =O, -ОН, ціаногрупу, атом галогену, Якщо не визначено інше, алкіленові групи, які нітрогрупу, С1-6алкіл (як варіант, закінчений групою визначені тут, можуть мати лінійний , ланцюг або, -N(H)C(O)OR23a), С1-6алкоксил, Het1, арил, коли існує достатнє число (тобто мінімум два) N(R24a)R24b, -C(O)R24c, -C(O)OR24d, атомів карбону, мати розгалужений ланцюг. Такі -C(O)N(R24e)R24f, -N(R24g)C(O)R24h, алкіленові ланцюги можуть також бути насиченими N(R24i)C(O)N(R24j)R24k, -N(R24m)S(O)2R23b, або, коли існує достатнє число (тобто мінімум два) S(O)nR23c, -OS(O)2R23d та -S(O)2N(R24n)R24p; атомів карбону, бути ненасиченими та/або перерR23a - R23d незалежно представляють, у кожваними одним або більше атомами оксигену ному випадку своєї наявності, С1-6алкіл;. та/або сульфуру. Якщо не визначено інше, алкілеR24a - R24p незалежно представляють, у кожнові групи можуть також бути заміщеними одним ному випадку своєї наявності, Η або С1-6алкіл; або більше атомами галогену. n дорівнює, у кожному випадку, 0, 1 або 2; а Термін "арил", при використанні тут, включає a f R - R незалежно представляють Η або С1С6-10арил-групи, як-то феніл, нафтил тощо. Термін "арилоксил", при використанні тут, включає Сб4алкіл; де кожний арил та кожну арилоксигрупу, якщо юарилоксигрупи, як-то феноксил, нафтоксил тощо. не визначено інше, як варіант, заміщено; Для запобігання невизначеності, арилоксигрупи, або її фармацевтично прийнятне похідне; визначені тут, приєднані до залишкової частини за умови, що: молекули через атом О оксигрупи. Якщо не визна(a) коли R3 представляє Η або С1-4алкіл; а А чено інше, арильні та арилоксигрупи можуть бути представляє -J-N(R21)- або -J-O-; заміщеними одним або більше замісниками вклюто В не представляє -N(R22)-, -S(O)n-, -О- або чаючи -ОН, ціаногрупу, атом галогену, нітрогрупу, N(R22)-Z- (у останній групі -N(R22) С1-6алкіл (як варіант, закінчений групою приєднано до атому карбону, що з'єднаний з N(H)C(O)OR23a), С1-6алкоксил, Het1, арил (ця арил2 3 R тa R ); група може не бути заміщеною жодною з наступ(b) коли R2 представляє -E-OR15 або -Eних арил-груп), -N(R24a)R24b, -C(O)R24c, -C(O)OR24d, 17 18 N(R )R , в яких Ε представляє безпосередній -C(O)N(R24e)R24f, -N(R24g)C(O)R24h, зв'язок, то: N(R24i)C(O)N(R24j)R24k, -N(R24m)S(O)2R23b, (і) А не представляє безпосереднього зв'язку, S(O)nR23c, -OS(O)2R223d та -S(O)2N(R24n)R24p (де J-N(R21)- або -J-O-; а Het1, R23a - R23d, R24a - R24p та n визначені вище). 22 (іі) В не представляє -N(R )-, -S(O)n-, -О- або Коли вони заміщені, арил та арилоксигрупи є пеN(R22)-Z- (у останній групі -N(R22) приєднано до реважно заміщеними замісниками числом від одатому карбону, що з'єднаний з R2 тa R3); ного до трьох. (c) Het1 та Het13 не представляють 9-членних Термін "галоген", при використанні тут, вклюгетероциклів, що містять конденсоване бензольне чає флуор, хлор, бром та йод. або піридинове кільце; та Групи Het (Het1 - Het13), що можна згадати, (d) сполука не представляє: 3,7-біс(1включають групи, що містять 1-4 гетероатоми (вифенілетил)-3,7-діазадицикло[3.3.0]октан; брані з оксигену, нітрогену та/або сульфуру), в 2-{4-(7-бензил-3,7-діазадицикло[3.3.0]октан-3яких загальне число атомів у кільцевій системі, іл)бутил}-1,2-бензізотіазол-3-он-1,1-діоксид; знаходиться між п'ятьма та дванадцятьма. Групи 1 13 3-метил-7-бензил-3,7Het (Het - Het ) можуть бути повністю насиченидіазадицикло[3.3.0]октан; ми, цілком ароматичними, частково ароматичними 3-циклогексил-7-бензил-3,7та/або дициклічними за характером. Гетероциклічдіазадицикло[3.3.0]октан; ні групи що можна згадати, включають бензодіок3-(тіазол-2-іл)-7-бензил-3,7саніл, бензодіоксепаніл, бензодіоксоліл, бензофудіазадицикло[3.3.0]октан; раніл, бензофуразаніл, бензімідазоліл, 3-(2-піримідил)-7-бензил-3,7бензоморфолініл, бензотіофеніл, хроманіл, цино 17 75382 18 лініл, діоксаніл, фураніл, гідантоїніл, імідазоліл, Скорочення наведені у кінці цього опису. імідазо[1,2-а]піридиніл,індоліл, ізохінолініл, ізоксаСполуки формули І, що можна згадати, вклюзоліл, малеїнімідо, морфолініл, оксазоліл, фталачають сполуки, в яких: зиніл, піперазиніл, піперидиніл, пуриніл, піраніл, R1 представляє С1-12алкіл (як варіант, заміщепіразиніл, піразоліл, піридиніл, піримідиніл, піроліний та/або закінчений одним або більше заміснидиноніл, піролідиніл, піролініл, піроліл, хіназолініл, ками, вибраними з групи: атом галогену, ціаногрухінолініл, 3-сульфоленіл, тетрагідропіраніл, тетрапа, нітрогрупа, арил, Het1, -C(O)R5a, -OR5b, гідрофураніл, тіазоліл, тієніл, тіохроманіл, триазоN(R6)R5C, -C(O)XR7, -C(O)N(R8)R5d та -S(O)2R9), 1 ліл тощо. Значення Het , що можна згадати, вклюC(O)XR7, -C(O)N(Rs)R5d або -S(O)2R9; 2 чають піперазиніл та тіазоліл. Значення Het , що R5a - R5d незалежно представляють, у кожному можна згадати, включають тіазоліл. Значення Het4 випадку своєї наявності, Н, С1-6алкіл (як варіант, що можна згадати, включають ізоксазоліл та тетзакінчений одним або більше замісниками, вибрарагідропіраніл. Значення Het5, що можна згадати, ними з групи -ОН, С1-6алкоксил, атом галогену, включають морфолініл, піперазиніл та піридиніл. ціаногрупа, нітрогрупа, арил, та Het3), арил або 6 Значення Het , що можна згадати, включають ізокHet4, або R5d, разом з R8, представляє С3-6алкілен сазоліл та тетрагідропіраніл. (цю алкіленову групу, як варіант, перервано атоКоли група Het (Het1 - Het13) є заміщеною одмом О та/або, як варіант, заміщено одною або ним або більше арилами та/або групами Het1, ці більше С1-3алкіл-групами); вказані арильні та/або Het1-замісники можуть самі R7 представляє, у кожному випадку своєї наябути заміщеними будь-яким арилом та/або групою вності, С1-12алкіл (цю алкіл-групу, як варіант, заміHet1. Замісники на групах Het (Het1 - Het13) можуть, щено та/або закінчено одним або більше замісниде можливо, бути локалізованими на будь-якому ками, вибраними з групи: -ОН, атом галогену, атомі у кільцевій системі, включаючи гетероатом. ціаногрупа, нітрогрупа, арил, С1-6алкоксил, Місце приєднання групи Het (Het1 - Het13) може SO2R13a, -C(O)R13b тa Het5); бути на будь-якому атомі у кільцевій системі, R9 представляє, у кожному випадку своєї наявключаючи (де можливо) гетероатом, або атом на вності, С1-6алкіл (як варіант, заміщений та/або забудь-якому конденсованому карбоциклічному кікінчений одним або більше замісниками, вибранильці, що може бути представленим як частина ми з групи: -ОН, атом галогену, ціаногрупа, кільцевої системи. Групи Het (Het1 - Het13) можуть нітрогрупа та арил) або арил; також бути у Ν- або S-окисненій формі. R2 представляє Н, атом галогену, С1-6алкіл, 16 Фармацевтично прийнятні похідні включають OR , -E-N(R17)R18 чи разом з R3 представляє =O; солі та сольвати. Солі, які можна згадати, включаR4 представляє арил або піридил, ці групи, як ють кислотно-адитивні солі. Фармацевтично приваріант, заміщені одним або більше замісниками, йнятні похідні також включають солі четвертинного вибраними з групи: -ОН, ціаногрупа, атом галогеС1-4алкіламонію на 3,8-діазадицикло[3,2,1]октані ну, нітрогрупа, С1-6алкіл (як варіант, закінчений або (коли ' , група Het (Het1 - Het13) містить третингрупою -N(H)C(O)OR23a), С1-6алкоксил, -N(R24a)R24b, ний атом нітрогену) третинному гетероциклічному -C(O)R24c, -C(O)OR24d, -C(O)N(R24e)R24f, 24g 24h 24i атомі нітрогену, та N-оксиди, за умови, що коли N(R )C(O)R , -N(R )C(O)N(R24j)R24k, представлено N-оксид: N(R24m)S(O)2R23b, -S(O)nR23c та -OS(O)2R23d. (a) жодна група Het (Het1 - Het13) не містить Подальші сполуки, що можна згадати, вклюнеокиснений S-атом; та/або чають сполуки, в яких: Het1 та Het13 незалежно (b) n не представляє 0, коли В представляє -Zпредставляють 4-8-членні гетероциклічні групи, що S(O)n-. містять один або більше гетероатомів, вибраних з Сполуки формули І можуть виявляти таутомеоксигену, нітрогену та/або сульфуру, ці групи, як рію. Усі таутомерні форми та їх суміші включені у варіант, заміщені як описано вище. рамки винаходу. Наступні сполуки, що можна згадати, включаСполуки формули І можуть також мати один ють сполуки, в яких:. або більше асиметричних атомів карбону та моR1 представляє С1-12алкіл (як варіант, заміщежуть тому виявляти оптичну та/або діастереоізоний та/або закінчений одним або більше заміснимерію. ками, вибраними з групи: атом галогену, ціаногруДіастереоізомери можна розділяти викориспа, нітрогрупа, арил, Het1, -OR, -N(R6)R5c, танням звичайних способів, наприклад, хроматогC(O)XR7, -C(O)N(R8)R5d та -S(O)2R9), Het2, рафією або фракційною кристалізацією. РізномаC(O)R5a, -C(O)XR7, -C(O)N(R6)R5d, -S(O)2R9, -СН2нітні стереоізомери можна виділяти розділенням С(О)-(незаміщений С1-6алкіл) або -СН2-С(О)-(арил) рацемічної або іншої суміші сполук використанням (арильну частину останньої групи, як варіант, зазвичайних способів, наприклад, фракційної крисміщено одним або більше замісниками, вибраними талізації або ВЕРХ. Альтернативно потрібні оптичз групи: -ОН, ціаногрупа, атом галогену, нітрогруні ізомери можна отримувати реакцією прийнятнопа, С1-6алкіл (як варіант, закінчений групою го оптично активного вихідного матеріалу в N(H)C(O)OR23a), С1-6алкоксил, Het1, арил (ця арилумовах, які не викликатимуть рацемізації або епігрупа може не бути заміщеною будь-якими настумеризації, або дериватизацією, наприклад, гомохіпними арил-групами), -N(С1-6алкіл)R24b, -C(O)R24c, ральною кислотою, а потім розділенням, діастереC(O)OR24d, -C(O)N(R24e)R24f, -N(R24g)C(O)R24h, омерних естерів звичайними засобами N(R24i)C(O)N(R24j)R24k, -N(R24m)S(O)2R23b, -S(O)nR23c (наприклад, ВЕРХ, хроматографією через оксид та -S(O)2N(R24n)R24p); силіцію). Усі стереоізомери включені у рамки виR2 та R3 разом не представляють =O; находу. G не представляє безпосереднього зв'язку; 19 75382 20 та/або ному випадку своєї наявності, С1-6алкіл, як варіант, Het3 та Het4 незалежно представляють 4-8заміщений феніл або Het10; членні гетероциклічні групи, що містять один або R20a представляє Η або С1-4алкіл; більше гетероатомів, вибраних з оксигену, нітроΕ представляє, у кожному випадку своєї наявгену та/або сульфуру, ці групи, як варіант, заміщеності, безпосередній зв'язок або С1-2алкілен; ні як описано вище. А представляє -G-; Переважні сполуки винаходу включають споВ представляє -Ζ-, -Z-N(H)-, -Z-S(O)n-, -Z-O- (у луки, в яких: останніх трьох групах Ζ приєднано до атому кархвилясті лінії представляють відносну цисбону, що з'єднаний з R2 та R3); стереобудову; G представляє безпосередній зв'язок або С1R1 представляє С1-8алкіл (як варіант, заміще5алкілен; ний та/або закінчений одною або більше групами, Ζ представляє безпосередній зв'язок або С1вибраними з групи: атом галогену, як варіант, за3алкілен; міщений феніл, Het1, -C(O)R5a, -0R5b, -C(O)OR7, R4 представляє феніл або Het13, обидві ці гру8 2 7 C(O)N(H)R та S(О)2-С1-6алкіл), Het , -C(O)OR , пи, як варіант, заміщені одним або більше замісC(O)N(H)R8 або -S(O)2R9; никами, вибраними з групи: ціаногрупа, атом галоR5a та R5b незалежно представляють, у кожногену, нітрогрупа, С1-4алкіл (як варіант, закінчений му випадку своєї наявності, Н, С1-6алкіл (як варігрупою -N(H)C(O)OR23a), С1-4алкоксил, як варіант, ант, заміщений та/або закінчений одним або більзаміщений феніл, -C(O)N(H)R24e, -N(H)C(O)R24h, ше замісниками, вибраними з групи: -ОН, С1N(H)C(O)N(H)R24j, -N(H)S(O)2R23b, -S(O)2R23c та S(O)2N(R24n)R24p; 4алкоксил та галоген), як варіант, заміщений феніл 4 або Het ; Het13 представляє п'яти-десяти-членну гетеR7 представляє, у кожному випадку своєї наяроциклічну групу, що містить один або більше гевності, С1-8алкіл (цю групу, як варіант, заміщено тероатомів, вибраних з оксигену, нітрогену та/або та/або закінчено одним або більше замісниками, сульфуру; вибраними з групи: -ОН, атом галогену, ціаногруHet1 - Het12 незалежно представляють, у кожпа, як варіант, заміщений феніл, С1-4алкоксил, ному випадку своєї наявності п'яти-десяти-членні SO2R13a, -C(O)R13b та Het5); гетероциклічні групи, що містять один або більше R13a та R13b незалежно представляють С1гетероатомів, вибраних з оксигену, нітрогену та/або сульфуру, ці гетероциклічні групи, як варі6алкіл; R8 представляє, у кожному випадку своєї наяант, заміщені одним або більше замісниками вності, С1-8алкіл (цю групу, як варіант, заміщено включаючи =O, -ОН, ціаногрупу, атом галогену, та/або закінчено одним або більше замісниками, нітрогрупу, С1-4алкіл, С1-4алкоксил, як варіант, завибраними з групи: -ОН, атом галогену, ціаногрупа міщений феніл, -NH2, -C(O)R24c, -C(O)OR24d, та С1-4алкоксил), -D-(як варіант, заміщений феніл), C(O)N(H)R24e, -N(H)C(O)R24h та -S(O)nR23c; 6 15a -D-Het , -D-S(O)2R , -D-C(O)-С1-4алкіл aбo-DRa - Rf незалежно представляють Η або С115b C(O)OR ; 2алкіл; R8 представляє, у кожному випадку своєї наяНеобов'язкові замісники на феніл-групах предвності, С1-8алкіл (цю групу, як варіант, заміщено ставляють одну або більше груп, вибраних з групи: та/або закінчено одним або більше замісниками, -ОН, ціаногрупа, атом галогену, нітрогрупа, С1вибраними з групи: -ОН, атом галогену, ціаногрупа (як варіант, закінчений групою 4алкіл та С1-4алкоксил), -D-(як варіант, заміщений феніл), N(H)C(O)OR23a), С1-4алкоксил, -NH2, -C(O)R24c, -D-Het6, -D-S(O)2R15a, -О-С(О)-С1-4алкіл a6o-DC(O)OR24d, -C(O)N(H)R24e, -N(H)C(O)R24h, 15b 24j 23b C(O)OR ; N(H)C(O)N(H)R , -N(H)S(O)2R , -S(O)nR23c та R15a та R15b незалежно представляють С1S(O)2N(R24n)R24p; R23a- R23c, R24c, R24d, R24e, R24h, R24i, R24n та R24p 6алкіл (як варіант, заміщений та/або закінчений одним або більше замісниками, вибраними з грунезалежно представляють, у кожному випадку С1пи: атом галогену, ціаногрупа та, як варіант, замі4алкіл; щений феніл) або, як варіант, заміщений феніл; n дорівнює 0 або 2; D представляє безпосередній зв'язок або С1алкіл-групи та алкоксигрупи можуть бути, якщо не визначено інше: 3алкілен; R9 представляє, у кожному випадку своєї ная(і) лінійними чи розгалуженими, або циклічнивності, С1-5алкіл (як варіант, заміщений та/або зами чи мати циклічні/ациклічні частини; кінчений одним або більше замісниками, вибрани(іі) насиченими або ненасиченими; ми з групи: атом галогену, ціаногрупа та, як (ііі) перерваними одним або більше атомами варіант, заміщений феніл) або, як варіант, заміщеоксигену; та/або ний феніл; (iv) заміщеними одним або більше атомами R2 представляє Н, С1-2алкіл, -OR16, -N(H)R17 флуору або хлору. або, разом з R3 представляє =O; Більш переважні сполуки винаходу включають 3 2 R представляє Н, С1-2алкіл або, разом з R сполуки, в яких: представляє =O; R1 представляє С1-6алкіл (як варіант, заміщеR16 представляє Н, С1-4алкіл, -Е-(як варіант, ний та/або закінчений одним або більше заміснизаміщений феніл), -C(O)R19a або -C(O)N(H)R20a; ками, вибраними з групи: атом галогену, феніл (як R17 представляє Н, С1-4алкіл, -Е-(як варіант, варіант, заміщений одним або більше замісниказаміщений феніл), -C(O)R19a або -C(O)OR19b; ми, вибраними з групи: атом галогену, ціаногрупа R19a та R19b незалежно представляють, у кожта С1-2алкоксил), Het1, -C(O)R5a, -0R5b, -С(О)N(Н) 21 75382 22 С1-4алкіл та -S(О)2-С1-4алкіл), Het2, -C(O)OR7, R4 представляє феніл, як груп, як варіант, заC(O)N(H)R8 або -S(О)2-С1-5алкіл; міщено одним або більше замісниками, вибраними Het2 представляє 5-членну гетероциклічну з групи: ціаногрупа, атом галогену, нітрогрупа, С1групу, що містить один-чотири гетероатоми, виб4алкіл та С1-4алкоксил; рані з оксигену, нітрогену та/або сульфуру, цю Ra - Rf усі представляють Н; гетероциклічну групу, як варіант, заміщено одним алкіл-групи та алкоксигрупи можуть бути, якщо або більше замісниками, вибраними з групи: ціаноне визначено інше: група, атом галогену, нітрогрупа, С1-4алкіл та СмС1(і) лінійними чи розгалуженими, або циклічними чи мати циклічні/ациклічні частини; 4алкоксил; R5a та R5b незалежно представляють, у кожно(іі) насиченими або ненасиченими; му випадку своєї наявності, Н, С1-5алкіл (як варі(ііі) перерваними одним або більше атомами ант, заміщений та/або закінчений одним або більоксигену; та/або ше замісниками, вибраними з групи: С1-2алкоксил (iv) заміщеними одним або більше атомами та атом галогену) або феніл (як варіант, заміщефлуору або хлору. ний одним або більше замісниками, вибраними з Особливо переважні сполуки винаходу вклюгрупи: атом галогену, ціаногрупа та С1-2алкоксил); чають сполуки, в яких: R7 представляє С1-6алкіл (цю групу, як варіант, R1 представляє С1-5алкіл (ця алкіл-група є, як заміщено та/або закінчено одним або більше заміваріант, частково циклічною/ациклічною, перервасниками, вибраними з групи: -ОН, атом галогену, ною атомом оксигену та/або заміщеною або закінціаногрупа, С1-2алкоксил, -SО2-С1-4алкіл, -С(О)-С1ченою одним замісником, вибраним з групи: феніл 5 (як варіант, заміщений одним або більше замісни5алкіл та Het ); Het1 та Het5 незалежно представляють 5-7ками, вибраними з групи: флуор та метоксил), членні гетероциклічні групи, ці групи містять одинHet1, -C(O)R5a, -OR5b, -С(О)N(Н)-С1-3алкіл -S(О)2-С12 7 8 чотири гетероатоми, вибрані з атомів оксигену, 3алкіл), Het , -C(O)OR , -C(O)N(H)R або -S(О)2-С1нітрогену та/або сульфуру, і ці гетероциклічні груалкіл; 5 пи, як варіант, заміщені одним або більше замісHet2 представляє 5-членну гетероциклічну никами, вибраними з групи: ціаногрупа, атом галогрупу, що містить один або два гетероатоми, вибгену, нітрогрупа, С1-4алкіл, С1-4алкоксил та -С(О)рані з оксигену, нітрогену та/або сульфуру, цю С1-4алкіл; гетероциклічну групу, як варіант, заміщено одним R8 представляє, у кожному випадку своєї наяабо більше замісниками, вибраними з групи: атом вності, С1-6алкіл (цю групу, як варіант, заміщено галогену, С1-2алкіл та С1-2алкоксил; та/або закінчено одним або більше замісниками, R5a та R5b незалежно представляють, у кожновибраними з групи: атом галогену та С1-3алкоксил), му випадку своєї наявності, Н, С1-4алкіл (як варіфеніл (цю групу, як варіант, заміщено одним або ант, заміщений або закінчений метоксилом) або більше замісниками, вибраними з групи: -ОН, ціафеніл (як варіант, заміщений одним або більше ногрупа, атом галогену, нітрогрупа, С1-4алкіл, С1замісниками, вибраними з групи: флуор та меток6 15a ; сил); 4алкоксил, та -S-(С1-4алкіл)), Het або-S(O)2R Het6 представляє 5-7-членну гетероциклічну R7 представляє С1-5алкіл (ця група, як варіант, групу, що містить один-чотири гетероатоми, вибє ненасиченою та/або її заміщено одним заміснирані з оксигену, нітрогену та/або сульфуру, цю ком, вибраним з групи: -ОН, ціаногрупа, метоксил, гетероциклічну групу, як варіант, заміщено одним -SO2-С1-2алкіл, -С(О)-С1-4алкіл та Het5); або більше замісниками, вибраними з групи: ціаноHet1 та Het5 незалежно представляють 5-7група, атом галогену, нітрогрупа, С1-4алкіл та С1членні гетероциклічні групи, як групи містять одинтри гетероатоми, вибрані з атомів оксигену, нітро4алкоксил; R15a представляє С1-4алкіл або феніл (цю гругену та/або сульфуру, та, ці гетероциклічні групи, пу, як варіант, заміщено одним або більше замісяк варіант, заміщені одним або більше замісниканиками, вибраними з групи: -ОН, ціаногрупа, атом ми, вибраними з групи: С1-2алкіл, С1-2алкоксил та галогену, нітрогрупа, С1-4алкіл та С1-4алкоксил); С(О)-С1-2алкіл; R2 представляє Н, -OR16 або -N(H)R17; R8 представляє, у кожному випадку своєї ная3 R представляє Η або метил; вності, С1-5алкіл (ця група є, як варіант, ненасичеR16 представляє Н, С1-2алкіл або феніл (цю ною, частково циклічною/ациклічною, перерваною групу, як варіант, заміщено одним або більше заатомом оксигену та/або заміщеною або закінченою місниками, вибраними з групи: -ОН, ціаногрупа, метоксилом), феніл (цю групу, як варіант, заміщеатом галогену, нітрогрупа, С1-4алкіл та С1но одним або більше замісниками, вибраними з групи: флуор, С1-2алкіл, С1-2алкоксил, та -S-(С14алкоксил); R17 представляє Н, С1-2алкіл, -(СН2)0-1-феніл 2алкіл) (алкільну частину останньої групи, як варі(цю групу, як варіант, заміщено одним або більше ант, заміщено одним або більше атомами флуозамісниками, вибраними з групи: ОН, ціаногрупа, ру)), Het або -S(O)2R15a; атом галогену, нітрогрупа, С1-4алкіл та С1Het6 представляє 5-7-членну гетероциклічну групу, ця група містить один-три гетероатоми, ви4алкоксил), або -С(О)О-(С1-4алкіл); А представляє С1-4алкілен; брані з оксигену, нітрогену та/або сульфуру, і цю В представляє -Ζ-, -Z-N(H)-, -Z-S(O)2-, -Z-O- (у гетероциклічну групу, як варіант, заміщено одним останніх трьох групах Ζ приєднано до атому карабо більше замісниками, вибраними з групи: С1бону, що з'єднаний з R1 та R2); 2алкіл та С1-2алкоксил; Ζ представляє безпосередній зв'язок або С1R15a представляє феніл (цю групу, як варіант, заміщено одним або більше замісниками, вибра2алкілен; 23 75382 24 ними з групи: С1-2алкіл та С1-2алкоксил); N(R24m)S(О)2R23b, -S(O)nR23c, -OS(O)2R23d та R2 представляє Н, -OR16 або -NH2; S(O)2N(R24n)R24p) або Het4a; 3 R представляє Н; R5a2 представляє Н, С1-6алкіл (як варіант, за16 R представляє Η або феніл (цю групу, як ваміщений та/або закінчений одним або більше заміріант, заміщено одним або більше замісниками, сниками, вибраними з групи: -ОН, С1-6алкоксил, 3a вибраними з групи: ціаногрупа або С1атом галогену, ціаногрупа, нітрогрупа, арил, Het 10 4a тa -NHC(O)R ), арил або Het ; 2алкоксигрупа); А представляє С1-3алкілен; R5b - R5d незалежно представляють, у кожному В представляє -Ζ-, -Z-N(H)-, -Z-S(O)2-, -Z-O- (у випадку своєї наявності, Н, С1-6алкіл (як варіант, останніх трьох групах Ζ приєднано до атому карзаміщений та/або закінчений одним або більше бону, що з'єднаний з R2 та R3); замісниками, вибраними з групи: -ОН, С1Ζ представляє безпосередній зв'язок або СН2; 6алкоксил, атом галогену, ціаногрупа, нітрогрупа, R4 представляє феніл, цю групу заміщено щоарил, Het3 та -NHC(O)R10), арил або Het4, або R5d, найменше одною ціаногрупою і цю групу, як варіразом з R8, представляє С3-6алкілен (цю алкіленоант, заміщено одним або двома наступними замісву групу, як варіант, перервано атомом О та/або, никами, вибраними з групи: ціаногрупа, атом як варіант, заміщено одною або більше С1-3алкілгалогену та нітрогрупа; групами); алкіл-групи та алкоксигрупи можуть мати, якR10 представляє Н, С1-4алкіл (як варіант, заміщо не визначено інше, лінійний або розгалужений щений та/або закінчений одним або більше замісланцюг. никами, вибраними з групи: атом галогену, ціаногОсобливо переважні сполуки винаходу вклюрупа, арил та -NHC(O)R11) або арил; чають сполуки, в яких: R11 представляє Н, С1-4алкіл або арил; R16 представляє Η або феніл (цю групу заміR6 представляє Н, С1-6алкіл (як варіант, заміщено одною-трьома метоксигрупами); щений та/або закінчений одним або більше замісА представляє С1-3алкілен; никами, вибраними з групи: -ОН, атом галогену, В представляє -Ζ-, -Z-N(H)-, -Z-S(O)2-, -Z-O- (у ціаногрупа, нітрогрупа та арил), арил, -C(O)R12a, останніх трьох групах Ζ приєднано до атому карC(O)OR12b або -C(O)N(H)R12c; бону, що з'єднаний з R2 та R3); R12a, R12b та R12c представляють С1-6алкіл (як Ζ представляє безпосередній зв'язок або, коли варіант, заміщений та/або закінчений одним або R2 представляє ОН або ΝΗ2, Ζ представляє СН2; більше замісниками, вибраними з групи: -ОН, атом R4 представляє феніл, заміщений у 4-позиції галогену, ціаногрупа, нітрогрупа та арил) або арил, (стосовно групи В) ціаногрупою, та, як варіант, або R12a та R12c представляють Н; заміщений у 2-позиції (стосовно групи В) наступX представляє О або S; ною ціаногрупою. R7 представляє, у кожному випадку своєї наяЗгідно з наступним аспектом винаходу запровності, арил або С1-12алкіл (ця алкіл-група, як варіпоновано сполуки формули І, які є сполуками фоант, заміщена та/або закінчена одним або більш рмули Іа, замісниками, вибраними з групи: -ОН, атом галогену, ціаногрупа, нітрогрупа, арил, С1-6алкоксил, SO2R13a, -C(O)R13b та Het5); R13a та R13b незалежно представляють С16алкіл або арил; R8 представляє, у кожному випадку своєї наявності, Н, С1-12алкіл, С1-6алкоксил (ці останні дві групи, як варіант, заміщені та/або закінчені одним або більше замісниками, вибраними з групи: -ОН, атом галогену, ціаногрупа, нітрогрупа, С1-4алкіл та С1-4алкоксил), -D-арил, -D-арилокси, -D-Het6, -DN(H)C(O)R14a, -D-S(O)2R15a, -D-C(O)R14b, -Dде 15b 14c 14d C(O)OR , -D-C(O)N(R )R , або R8, разом з R5d, хвилясті лінії представляють, як варіант, відпредставляє С3-6алкілен. (цю алкіленову групу, як носну цис- або транс-стереобудову; варіант, перервано атомом О та/або, як варіант, R1 представляє С1-12алкіл (як варіант, заміщезаміщено одною або більше С1-3алкіл-групами); ний та/або закінчений одним або більше замісниR14a - R14d незалежно представляють Н, С1ками, вибраними з групи: атом галогену, ціаногру1a 5a1 5b 6алкіл (як варіант, заміщений та/або закінчений па, нітрогрупа, арил, Het , -C(O)R , -OR , одним або більше замісниками, вибраними з груN(R6)R5c, -C(O)XR7, -C(O)N(R8)R5d та -S(O)2R9), пи: -ОН, атом галогену, ціаногрупа, нітрогрупа та Het2, -C(O)R5a2, -(O)XR7, -(O)N(R8)R5d, S(O)2R9 або арил), арил, або R14c та R14d разом представляють СН2С(О)-(незаміщений С1-6алкіл); 5a1 С3-6алкілен; R представляє арил (останню групу, як ваR15a та R15b незалежно представляють С1ріант, заміщено одним або більше замісниками, 6алкіл (як варіант, заміщений та/або закінчений вибраними з групи: -ОН, ціаногрупа, атом галогеодним або більше замісниками, вибраними з груну, нітрогрупа, С1-6алкіл (як варіант, закінчений пи: -ОН, атом галогену, . ціаногрупа, нітрогрупа та групою -N(H)C(O)OR23a), С1-6алкоксил, Неt1, арил арил) або арил; (ця арил-група може не бути заміщеною будьD представляє безпосередній зв'язок або С1якими наступними арил-групами), -N(С124b 24c 24d 24e 24f 6алкілен; , -C(O)R , -C(O)OR , -C(O)N(R )R , 6алкіл)R R9 представляє, у кожному випадку своєї ная-N(R24g)C(O)R224h, -N(R24i)C(O)N(R24j)R24k, 25 75382 26 вності, С1-6алкіл (як варіант, заміщений та/або за-N(R24g)C(O)R24h, -N(R24i)C(O)N(R24j)R24k, кінчений одним або більше замісниками, вибраниN(R24m)S(O)2R23b, S(O)nR23c, -OS(O)2R23d та ми з групи: -ОН, атом галогену, ціаногрупа, нітрогS(O)2N(R24n)R24p; 7 рупа та арил), арил або Het ; Het1a, Het3a та Het4a незалежно представляють, 2 R представляє Н, атом галогену, С1-6алил, -Eу кожному випадку своєї наявності, чотири-восьми16 17 18 OR або -E-N(R )R ; членні гетероциклічні групи, що містять один або R3 представляє Η або С1-6алкіл; більше гетероатомів, вибраних з оксигену, нітроR16 представляє Н, С1-6алкіл, -Е-арил, -E-Het8, гену та/або сульфуру, ці гетероциклічні групи, як -C(O)R19a, -C(O)OR19b або -C(O)N(R20a)R20b; варіант, заміщені одним або більше замісниками R17 представляє Η, С1-6алкіл, -Е-арил, -E-Het8, включаючи =O, -ОН, ціаногрупу, атом галогену, -C(O)R19a, -C(O)OR19b, -S(O)2R19c, нітрогрупу, С1-6алкіл (як варіант, закінчений групою [C(O)]pN(R20a)R20b або -C(NH)NH2; -N(H)C(O)OR23a), С1-6алкоксил, Het1, арил, R18 представляє Η, С1-6алкіл, -Е-арил або N(R24a)R24b, -C(O)R24C, -С(О)ОR21d, -C(O)N(R24e)R24f, 19d C(O)R ; -N(R24g)C(O)R24h, -N(R24i)C(O)N(R24j)R24k, 19a 19d 24m 23b R - R незалежно представляють, у кожN(R )S(O)2R , -S(O)nR23c, OS(O)2R24d та ному випадку своєї наявності, С1-6алкіл (як варіант, S(O)2N(R24n)R24p; заміщений та/або закінчений одним або більше R23a - R23d незалежно представляють, у кожзамісниками, вибраними з групи: атом галогену, ному випадку своєї наявності, С1-6алкіл; арил та Het9), арил, Het10, або R19a та R19d незалеR124a - R24p незалежно представляють, у кожжно представляють Н; ному випадку своєї наявності, Η або С1-6алкіл; R20a та R20b незалежно представляють, у кожn дорівнює, у кожному випадку, 0, 1 або 2; а ному випадку своєї наявності, Η або С1-6алкіл (як Ra - Rf незалежно представляють Η або С1варіант, заміщений та/або закінчений одним або алкіл; 4 більше замісниками, вибраними з групи: атом гаде кожний арил та кожну арилоксигрупу, якщо 11 12 логену, арил та Het ), арил, Het , або разом не визначено інше, як варіант, заміщено; представляють С3-6алкілен, як варіант, перерваний або її фармацевтично прийнятне похідне; атомом О; за умови, що: Ε представляє, у кожному випадку його вико(a) коли R3 представляє Η або С1-4алкіл; а А ристання, безпосередній зв'язок або С1-4алкілен; представляє -J-N(R21)- або -J-O-; то В не предстаp дорівнює 1 або 2; вляє -N(R22)-, -S(O)n-, -О- або -N(R22)-Z- (у останній 21 А представляє -G-, -J-N(R )- або -J-O- (в групі -N(R22) приєднано до атому карбону, що з'єд21 останніх двох групах N(R )- або О-приєднано до наний з R2 тa R3); та 2 3 2 16 атому карбону, що з'єднаний з R та R ); (b) коли R представляє -E-OR або -E22 22 17 18 В представляє -Z-, -Z-N(R )-, -N(R )-Z-, -ZN(R )R , де Ε представляє безпосередній зв'язок, S(O)n-, -Z-O-(в останніх двох групах Ζ приєднано то: до атому карбону, що з'єднаний з R2 та R3); (і) А не представляє -J-N(R21)- або -J-O-; та G представляє С1-6алкілен; (іі) В не представляє -N(R22)-, -S(O)n-; -О- або 22 J представляє С2-6алкілен; N(R )-Z-(в останній групі -N(R22) приєднано до Ζ представляє безпосередній зв'язок або С1атому карбону, що з'єднаний з R2 та R3); алкілен; Ці сполуки також визначені далі як "сполуки 4 R21 та R22 незалежно представляють Η або С1винаходу". Переважні сполуки формули Іа включають (за 6алкіл; R4 представляє арил або Het13, обидві ці груприйнятністю) переважні сполуки формули І, які пи, як варіант, заміщені одним або більше замісописані вище. никами, вибраними з групи: -ОН, ціаногрупа, атом Переважні сполуки формули Іа також включагалогену, нітрогрупа, С1-6алкіл (як варіант, закінчеють сполуки, в яких: ний групою -N(H)C(O)OR23a), С1-6алкоксил, Het1, R1 представляє С1-2алкіл (заміщений або за24a 24b 24C 24d арил, -N(R )R , -C(O)R , -C(O)OR , кінчений групою Het1a або -C(O)R5a1) -C(O)R5a2, або 24e 24f 24g 24h C(O)N(R )R , -N(R )C(O)R , -СН2С(О)-(незаміщений С1-4 алкіл); N(R24i)C(O)N(R24i)R24k, -N(R24m)S(O)2R23b, R5a1 представляє феніл (останню групу замі23c 23d 24n 24p S(O)nR , -OS(O)2R , -S(O)2N(R )R та (у вищено одним або два замісниками, вибраними з падку тільки Het13) оксогрупа; групи: атом галогену та С1-2алкоксил) Het13 представляє чотири-восьми-членну гетеR5a2 представляє Н, С1-6алкіл (як варіант, зароциклічну групу, що містить один або більше геміщений та/або закінчений одним або більше замітероатомів, вибраних з оксигену, нітрогену та/або сниками, вибраними з групи: С1-3алкоксил та атом сульфуру; галогену) або Het4a; Het1 - Het12 незалежно представляють, у кожG представляє С1-4алкілен; ному випадку своєї наявності, чотири-дванадцятиHet13 представляє п'яти- або шести-членну гечленні гетероциклічні групи, що містять один або тероциклічну групу, що містить один або більше більше гетероатомів, вибраних з оксигену, нітрогетероатомів, вибраних з оксигену, нітрогену гену та/або сульфуру, ці гетероциклічні групи, як та/або сульфуру; варіант, · заміщені одним або більше замісниками Het1a, Het3a та Het4a незалежно представляють, включаючи. =O, -ОН,- ціаногрупу, атом галогену, у кожному випадку своєї наявності, п'яти- або шеснітрогрупу, Сьеалкіл (як варіант, закінчений групою ти-членні гетероциклічні групи, що містять один -N(H)C(O)OR23a), С1-6алкоксил, Het1, арил, або більше гетероатомів, вибраних з оксигену, N(R24a)R24b, -C(O)R24c, -C(O)OR24d, -C(O)N(R24e)R24f, нітрогену та/або сульфуру, ці гетероциклічні групи, 27 75382 28 як варіант, заміщені одним до три замісниками, R3представляють Н, відновлення відповідної сповибраними з групи: =O, ціаногрупа, атом галогену, луки формули І, в якій R2 та R3 разом представля24a нітрогрупа, С1-4алкіл, С1-4алкоксил, арил, -N(H)R , ють =O, у присутності придатного відновнику та у -C(O)R24c, -C(O)OR24d, -C(O)N(H)R24e, прийнятних умовах реакції, наприклад, активацією N(R24g)C(O)R24h та -S(O)nR23c. релевантної групи С—О, використовуючи прийняПереважні сполуки винаходу включають спотний засіб (як-то тозилгідразин) у присутності прилуки з розкритих далі прикладів. датного відновнику (наприклад, борогідриду наОтримання трію або ціаноборогідриду натрію) та прийнятного Згідно з винаходом також запропоновано споорганічного розчиннику (наприклад, нижчого алкісіб отримання сполук формули І, спосіб включає: лового спирту (наприклад, С1-6алкілового спирту); (a) реакцію сполуки формули II. (е) для сполуки формули І, в якій R2 та R3 представляють Н, а (1) А представляє одиничний зв'язок або -J-N(R21), а В представляє С1-4алкілен, або (2) А представляє С1-6алкілен, а В представляє N(R22) або -N(R22)-Z- (у останній групі -N(R22) приєднано до атому карбону, що з'єднаний з R2 та R3), відновлення відповідної сполуки формули І, в якій R2 та R3 разом представляють =Щ, у присутності придатного відновнику (наприклад, LіАІН4) та прийнятного розчиннику (наприклад, ТГФ); де R1 та Ra - Rf визначені вище, зі сполукою (f) для сполуки формули І, в якій А представформули III, ляє С1-6алкілен, В представляє безпосередній зв'язок, С1-4алкілен, -Z-N(R22)-, -Z-S(O)n- або -ZrO(в останніх трьох групах Ζ представляє С12 3 4алкілен), R представляє ОН, a R представляє Н, відновлення відповідної сполуки формули І, в якій R2 та R3 разом представляють =O, у присутності придатного відновнику (наприклад, NaBH4) та придеL1 представляє відщеплювану групу (наприйнятного органічного розчиннику (наприклад, ТГФ); клад, мезилат, тозилат або галоген) a R2, R3, R4 та (д) для сполуки формули І, в якій В представВ визначені вище, наприклад, при температурі між ляє -Z-O-, реакцію сполуки формули VI, -10°С та температурою кипіння під зворотним холодильником у присутності придатної основи (наприклад: триетиламіну або К2СО3) та прийнятного органічного розчиннику (наприклад, дихлорметан, ацетонітрил або ДМСО); (b) для сполуки формули І, в якій А представляє С2алкілен, a R2 та R3 разом представляють =O, реакцію відповідної сполуки формули II, яку описано вище, зі сполукою формули IV, де R4 та В визначені вище, наприклад, при кімнатній температурі у присутності придатного органічного розчиннику (наприклад, етанолу); (c) для сполуки формули І, в якій А представляє СН2, a R2 представляє -ОН або -N(H)R17, реакцію відповідної сполуки формули II, яку описано вище, зі сполукою формули V, де Υ представляє О або N(R17), a R3, R4, R17 та В визначені вище, наприклад, при підвищеній температурі (наприклад, від 60°С до кипіння під зворотним холодильником) у присутності придатного розчиннику (наприклад, нижчого алкілового спирту (наприклад, ІПС), ацетонітрилу, або суміші нижчого алкілового спирту та води); (d) для сполуки формули І, в якій А представляє С1-6алкілен, В представляє С1-4алкілен, a R2 та де R1, R2, R3, Ra - Rf, та Ζ визначені вище, зі сполукою формули VII, R4OH VII в якій R4 описано вище, наприклад, в умовах типу Міцунобу наприклад, при температурі між зовнішньою (наприклад, 25°С) та температурою кипіння під зворотним холодильником у присутності третинного фосфіну (наприклад, трибутилфосфіну або трифенілфосфіну), азодикарбоксилатного похідного (наприклад, діетилазодикарбоксилату або 11'-(азодикарбоніл)дипіперидину) та прийнятного органічного розчиннику (наприклад, дихлорметану або толуолу); (h) для сполуки формули І, в якій В представляє -Z-O-, реакцію сполуки формули VI, яку описано вище, зі сполукою формули. VIII, R4-L2 VIII де L2 представляє відщеплювану групу, як-то галоген, алкансульфонат, перфлуоралкансульфонат або аренсульфонат, a R4 описано вище, наприклад, в умовах, відомих фахівцям (наприклад, коли R4 представляє 2- або 4-піридил, реакцію при температурі між 10°С та температурою кипіння під зворотним холодильником у присутності придатної основи (як-то гідрид натрію) та прийнятного розчиннику (як-то Ν,Ν-диметилформамід)); 29 75382 30 (і) для сполуки формули І, в якій А представOC(O)OR19b, або -OS(O)2R19c, де R19a - R19c визналяє С1-6алкілен, а В представляє -N(R22)-Z-(де гручені вище, наприклад, в умовах, що добре відомі пу -N(R22)- приєднано до атому карбону, що з'єдфахівцям; наний з R2 та R3), реакцію сполуки формули IX, (n) для сполук формули І, в яких R2 представляє -E-OR16, де R16 представляє С1-6алкіл, -Е-арил 3 або -E-Het , реакцію відповідної сполуки формули 2 І, в якій R представляє -Е-ОН, зі сполукою формули XIV, R16aOH XIV де R16a представляє С1-6алкіл, -Е-арил або -EHet8, де Het8 описано вище, наприклад, при температурі між зовнішньою (наприклад, 25°С) та температурою кипіння під зворотним холодильниа 1 2 3 22 де А представляє С1-6алкілен, a R , R , R , R ком, в умовах типу Міцунобу (тобто у присутності, a f та R - R визначені вище, зі сполукою формули X, наприклад, похідного трифенілфосфіну,. азодика4 2 R -Z-L ' X рбоксилату (наприклад, 1,1'2 4 де L , R та Ζ визначені вище, наприклад, при (азодикарбоніл)дипіперидину) та придатного орга40°С у присутності придатного органічного розчиннічного розчиннику (наприклад, дихлорметану)); нику (наприклад, ацетонітрилу); (о) для сполук формули І, в яких R2 представ2 (j) для сполуки формули І, в якій R представляє -E-OR16 (де R16 представляє С1-6алкіл, -Е-арил ляє -E-NH2, відновлення відповідної сполуки форабо -E-Het8), реакцію відповідної сполуки формули мули XI XV, де R1, R3, R4, Ra - Rf, А, В та Ε визначені вище, наприклад, гідруванням при придатному тиску у присутності придатного каталізатору (наприклад, паладію на вугіллі) та прийнятного розчиннику (наприклад, суміші вода-етанол); (k) для сполуки формули І, в якій R2 представляє -E-N(R18)C(O)N(H)R20a, реакцію . відповідної сполуки формули І, в якій R2 представляє -EN(R18)H, зі сполукою формули XII, R20aN=C=O XII де R20a описано вище, наприклад, при зовнішній температурі, (наприклад, 25°С) у присутності придатного розчиннику (наприклад, бензолу); (І) для. сполук формули І, в яких R2 представляє -E-N(H)[C(O)]2NH2, реакцію відповідної сполуки формули І, в якій R2 представляє -E-NH2 з діамідом щавлевої кислоти, наприклад, при температурі між -10 та 25°С у присутності придатного засобу сполучення (наприклад, 1-(3-диметиламінопропіл)3-етилкарбодііміду), прийнятного активуючого засобу (наприклад, 1-гідроксибензотриазолу), придатної основи (наприклад, триетиламіну) та реакційно-інертного органічного розчиннику (наприклад, ДМФ); (m) для сполук формули І, в яких R2 представляє -E-N(R17)R18, де R17 та R18 визначені вище, за умови, що R17 не представляє Н, реакцію відповідної сполуки формули І, в якій R2 представляє -DN(H)R18 зі сполукою формули XIII, R17a-L3 XIII де R17a представляє R17, що описано вище за винятком того, що він не представляє Н, a L3 представляє відщеплювану групу, як-то галоген (наприклад, хлор або бром), п-нітрофенолат, С1С1-4алкілтіолат, -OC(O)R19a, 4алкоксид, де L2, R1, R3,R4, Ra - Rf, А, В та Е визначені вище, зі сполукою формули XIV, яку описано вище, наприклад, при температурі між зовнішньою (наприклад, 25°С) та температурою кипіння під зворотним холодильником, в умовах типу Уільямсона (тобто у присутності прийнятної основи(наприклад, КОН або NaH) та придатного органічного розчиннику (наприклад, диметилсульфоксид або ДМФ)); (р) для сполук формули І, в яких R2 представляє E-OR16 (де R16 описано вище, за умови, що він не представляє Н, реакцію відповідної сполуки формули І, в якій R2 представляє -Е-ОН, зі сполукою формули XVI, R16b-L4 XVI де R16b представляє R16, що описано вище, за винятком того, що він не представляє Н, та L4 представляє відщеплювану групу, як-то ОН, галоген, алкансульфонат, аренсульфонат або OC(O)R19a, де R19a описано вище, наприклад, при температурі між кімнатною та температурою кипіння під зворотним холодильником, як варіант, у присутності реакційно-інертного органічного розчиннику (наприклад, ТГФ або хлороформу, придатної основи (наприклад, триетиламіну або К2СО3) та/або прийнятного засобу сполучення (наприклад, 1,3-дициклогексилкарбодііміду або 1-(3диметиламінопропіл)-3-етилкарбодііміду, як варіант, у поєднанні з придатним каталізатором, як-то 4-диметиламінопіридин) (наприклад, коли R16b представляє -C(O)R19a, a L4 представляє ОН, цю реакцію можна проводити при зовнішній температурі (наприклад, 25°С) у присутності засобу сполучення, як-то 1-(3-диметиламінопропіл)-3етилкарбодіімід, прийнятного каталізатору, як-то 4 31 75382 32 (диметил-аміно)піридин та розчиннику, як-то ТГФ); хівцям; (q) для сполук формули І, в яких R2 представ(u) для сполук формули І, в яких R1 представляє атом галогену, заміщення відповідної сполуки ляє С1-12алкіл, причому алкіл-група є заміщеною формули І, в якій R2 представляє -ОН, використопри С-2-атомі карбону (стосовно біспідинового вуючи прийнятний засіб галогенування (наприатому нітрогену) групою ОН або N(H)R6, а інакше, 2 клад, для сполуки, в яких R представляє флуор, як варіант, заміщеною одним або більше подальреакцію з трифлуоридом (діетиламіно)сульфуру); шими замісниками, які визначено вище для R1, (r) реакцію відповідної сполуки формули XVII, реакцію відповідної сполуки формули XVII, що описано вище, зі сполукою формули XXII, де R2, R3, R4, Ra - Rf, А та В визначені вище, зі сполукою формули VIII, R1-L5 XVIII де L5 представляє відщеплювану групу, як-то галоген, ОН, алкансульфонат, перфлуоралкансульфонат, аренсульфонат, імідазол, R25O- (де R25 представляє, наприклад, С1-10алкіл або арил, ці групи, як варіант, заміщені одним або більше замісниками, вибраними з групи: атом галогену, або нітрогрупа) -OC(O)R5a, -OC(O)OR або -OS(O)2R9, a R1, R5a, R7 та R9 визначені вище, наприклад, при температурі між -10°С та температурою кипіння під зворотним холодильником, як варіант, у присутності придатного розчиннику (наприклад, СНСІ3, CH3CN, 2-пропанолу, діетилового етеру, СН2СІ2, ДМСО, ДМФ, ТГФ, толуолу, або їх сумішей) та/або прийнятної основи (наприклад, К2СО3, піридину або триетиламіну); (s) для сполук формули І, в яких R1 представляє -C(O)XR7 або -C(O)N(R8)R5d, реакцію сполуки формули XIX, де R2, R3, R4, Ra - Rf, А, В та L5 визначені вище, зі сполукою формули XX, R26-H XX де R26 представляє -XR7 або -N(R8), a R5d, R7, 8 R та X визначені вище, наприклад, в умовах, описаних вище (етап (r) способу); (t) для сполук формули і, в яких R1 представляє -C(O)N(H)R8, реакцію відповідної сполуки формули XVII, що описано вище, зі сполукою формули XXI, R8-N=C=O XXI де R8 описано вище, наприклад, при температурі між 0°С та температурою кипіння під зворотним холодильником у присутності прийнятного органічного розчиннику (наприклад, дихлорметан), або тверофазним синтезом в умовах, відомих фа де Ya представляє О або N(R6), R1a представляє С1-10алкіл, як варіант, заміщений одним або більше замісниками, які описано вище для R1, a R6 описано вище, наприклад, як описано вище для отримання сполук формули І (етап (с) способу); (ν) для сполуки формули І, в якій R1 представляє -C(O)OR7, a Ra та/або Rb представляють С14алкіл, реакцію відповідної сполуки формули І, в якій R1 представляє -C(O)OR7, a Ra та Rb представляють Н, одним або більше еквівалентами сполуки формули XXIII, R27-L2 XXIII де R27 представляє С1-4алкіл, a L2 описано вище, у присутності прийнятної сильної основи, (тобто основи, здатної депротонувати 3,7діазадицикло[3.3.0]октанове кільце у позиції стосовно атому нітрогену, що з'єднаний з групою C(O)OR7 (наприклад, бутиллітію)), наприклад, при температурі між -80°С та кімнатною температурою у присутності придатного розчиннику (наприклад, Ν,Ν,Ν',Ν'-тетраметилетилендіаміну, ТГФ або їх сумішей); (w) для сполук формули І, які є N-оксидними похідними 3,7-діазадицикло[3.3.0]октану, окиснення відповідного 3,7-діаза-дицикло[3.3.0]октанового атому нітрогену відповідної сполуки формули І у присутності придатного окиснику (наприклад, мХПБК), наприклад, при 0°С 5 у присутності придатного органічного розчиннику (наприклад, ДХМ); (х) для сполук формули І, які є похідними солі четвертинного С1-4алкіламонію, в яких алкіл-групу приєднано до 3,7-діазадицикло-[3.3.0]октанового атому нітрогену, реакцію на 3,7діазадицикло[3.3.0]октановому атомі нітрогену відповідної сполуки формули І зі сполукою формули XXIII, яку описано вище, наприклад, при кімнатній температурі у присутності прийнятного органічного розчиннику (наприклад, ДМФ), а потім очисткою (використанням, наприклад, ВЕРХ) у присутності придатного поглиначу проти-іону (наприклад, NH4OAc); (у) перетворення одного заміснику на R4 на інший використанням способів, добре відомих фахівцям; (z) перетворення одної групи R1 іншу використанням способів, добре відомих фахівцям. Сполуки формули II можна отримувати реакцією відповідної сполуки формули XXIV, 33 75382 34 присутності прийнятного розчиннику (наприклад, діетилового етеру, ТГФ, або їх суміші), а потім окисненням утвореного боранового адукту придатним окисником (наприклад, перборатом натрію), а далі перетворенням утвореної групи ОН у групу L1 в умовах, відомих фахівцям. Сполуки формули III, в яких А представляє С122 6алкілен та В представляє -Z-N(R )- (у останньому a f де R - R визначені вище, зі сполукою формувипадку Ζ приєднано до атому карбону, що з'єднали XVIII, що описано вище, наприклад, описано ний з R2 та R3) можна отримувати сполученням вище для синтезу сполук формули І (етап (r) спосполук формули VIII, що описано вище, зі сполусобу). кою формули XXX, Сполуки формули III можна отримувати станHN(R22)-Z-C(R2)(R3)-AaOH XXX дартними способами. Наприклад, сполуки формуде Aa, Ζ, R2, R3 та R22 визначені вище, наприли III, в яких: клад, при температурі між кімнатною та темпера(1) В представляє -Z-Ο-, можна отримувати турою кипіння під зворотним холодильником, як сполученням сполук формули VII, що описано виваріант, у присутності придатного розчиннику ще, зі сполуками формули XXV, та/або прийнятної основи, а потім перетворенням L'-Z-C(R2)(R3)-A-L1 XXV групи ОН у групу L1 в умовах, відомих фахівцям. де R2, R3, Α, Ζ та L1 визначені вище, та дві груСполуки формули III, в яких В представляє -Zпи L1 можуть бути однаковими або відмінними; або S(O)- або -Z-S(O)2-, можна отримувати окисненням 22 22 (2) В представляє -N(R )-Z- (де N(R ) приєдвідповідних сполук формули III, в яких В представнано до атому карбону, що приєднаний до R2 та ляє -Z-S-, де Ζ описано вище, у присутності при3 2 3 R ), a R та R разом представляють =O, можна йнятної кількості придатного окиснику (наприклад, отримувати сполученням сполук формули XXVI мХПБК) та прийнятного органічного розчиннику. R4-Z-N(H)R22 XXVI Сполуки формули V можна отримувати згідно де R4, R22 та Ζ визначені вище, зі сполуками з зі способами, що відомі фахівцям. Наприклад, формули XXVII, сполуки формули V, в яких: L6-C(O)-A-L1 XXVII (1) В представляє -СН2О-, a Y представляє О, де L6 представляє придатну відщеплювану можна отримувати реакцією сполуки формули VII, групу (наприклад, -ОН або галоген), а А та L1 вищо описано вище, зі сполукою формули XXXI значено вище; в обох випадках в умовах, які добре відомі фахівцям. Сполуки формули III, в яких А представляє С2алкілен, a R2 представляє -OR16, де R16 представляє d-балкіл, -Е-арил або -E-Het8, можна альде R3 та L2 визначені вище, наприклад, при пітернативно отримувати реакцією сполуки формудвищеній температурі (наприклад, між 60°С та ли XIV, що описано вище, зі сполукою формули температурою кипіння під зворотним холодильниXXVIII, ком) у присутності придатної основи (наприклад, карбонату калію або NaOH) та прийнятного органічного розчиннику (наприклад, ацетонітрилу або суміші толуол/вода), або інакше як описано у попередньому рівні техніки; 3 4 27 (2) R3 представляє Н, В представляє безпоседе R , R , R та В визначені вище, наприклад, редній зв'язок, С1-4алкілен, -Z-N(R22)-, -Z-S(O)n- або при температурі між зовнішньою температурою -Z-O- (в яких у кожному випадку група Ζ представ(наприклад, 25°С) та температурою кипіння під ляє С1-4алкілен, приєднаний до атому карбону, що зворотним холодильником у присутності придатної з'єднаний з R3), a Y представляє О, можна отриоснови (наприклад, карбонату калію) та прийнятмувати відновленням сполук формули ХХХІІА чи ного органічного розчиннику (наприклад, ацетонітХХХІІВ, рилу), а потім перетворенням естерної функціональної групи у групу -СН2-L1 (в якій L1 описано вище), в умовах, що добре відомі фахівцям. Сполуки формули III, в яких А представляє С26алкілен, можна отримувати відновленням відповідної сполуки формули XXIX, а де Аb представляє безпосередній зв'язок або С1-4алкілен, a R2, R3, R4 та В визначені вище, з придатним бораном або комплексом боран-основа Льюїса (наприклад, боран-диметил сульфід) у a 22 a де В представляє -Z -N(R ), -Z -S(O)n- або Za-O- (в яких у кожному випадку, група Za представляє безпосередній зв'язок або С1-3алкілен, приєднаний до атому карбону, що з'єднаний з R3), Вb представляє безпосередній зв'язок або С14 22 та n визначені вище, наприклад, 4алкілен, a R , R при температурі між -15°С та кімнатною темпера 35 75382 36 турою у присутності придатного відновнику (ната придатної основи (наприклад, гідрокарбонату приклад, NaBH4) та прийнятного органічного рознатрію). чиннику (наприклад, ТГФ), а потім реакцією внутСполуки формули XI можна також отримувати рішньомолекулярного перегрупування в реакцією сполуки формули II, що описано вище, зі утвореному інтермедіаті, наприклад, при кімнатній сполукою формули XXXVI температурі у присутності придатної основи (наприклад, карбонату калію) та прийнятного органічного розчиннику (наприклад, ацетонітрилу); (3) В представляє безпосередній зв'язок, С122 4алкілен, -Z-N(R )-, -Z-S(O)2- або -Z-O-(в яких у кожному випадку, група Ζ представляє С1-4алкілен, приєднаний до атому карбону, що з'єднаний з R3), a Y представляє О, можна отримувати окисненням сполук формули XXXIНА або ХХХІІІВ, де R3, R4, А, В, Ε та L2 визначені вище, наприклад, в умовах, аналогічним описаним вище для синтезу сполук формули І (етап (а) способу). Сполуки формули XV можна альтернативно отримувати заміщенням групи -ОН відповідної сполуки формули І, в якій R2 представляє -Е-ОН групою L2 групою в умовах, що відомі фахівцям. Сполуки формули XVII можна отримувати реакцією відповідної сполуки ι формули XXIV, що опиде R3, R4 та Вb визначені вище, а Ва описано сано вище, зі сполукою формули III, що описано вище, за винятком того, що n дорівнює 2, у присувище, наприклад, в умовах, аналогічним описаним тності придатного окиснику (наприклад, мХПБК), вище для синтезу сполук формули І (етап (а) спонаприклад, кип'ятінням під зворотним холодильнисобу). ком у присутності придатного органічного розчинСполуки формули XVII, в яких А представляє нику (наприклад, дихлорметану); або С2алкілен, a R2 та R3 разом представляють =О (4) В представляє -Ζ-Ο-, в якому група Ζ предможна отримувати реакцією відповідної сполуки ставляє С1-4алкілен, приєднаний до атому карбоформули XXIV, що описано вище, зі сполукою фону, що з'єднаний з R3, a Y представляє -N(R17), де рмули IV, що описано вище, наприклад, як описаR17 представляє -C(O)OR19b або -S(O)2R19c, можна но вище для синтезу сполук формули І (етап (b) отримувати циклізацією сполуки формули XXXIV, способу). Сполуки формули XVII, в яких А представляє , a R2 представляє -ОН або -N(H)R17, можна отримувати реакцією відповідних сполук формули XXIV, що описано вище, зі сполукою формули V, що описано вище, наприклад, як описано вище де R17b представляє -C(O)OR19b або -S(O)2R19c, для синтезу сполук формули І (етап (с) способу). Ζb представляє С1-4алкілен, a R3; R4, R19b, R19c та L2 Сполуки формули XIX можна отримувати реавизначені вище, наприклад, при температурі між кцією відповідної сполуки формули II, що описано 0°С та температурою кипіння під зворотним холовище, зі сполукою формули XXXVII, дильником у присутності придатної основи (наприL5-C(O)-L5 XXXVII клад, гідроксиду натрію), прийнятного розчиннику де L5 описано вище, та, в яких дві групи L5 мо(наприклад, дихлорметану, води, або їх суміші) та, жуть бути однаковими або відмінними, ι наприза необхідністю, каталізатору фазопереносу (як-то клад, при температурі між 0°С та температурою гідросульфату тетрабутиламонію). кипіння під зворотним холодильником у присутноСполуки формули VI, IX, XI та XV можна отристі придатної основи (наприклад, триетиламіну або мувати подібно сполукам формули І (дивися, накарбонату калію) та прийнятного органічного розприклад, етапи (а) - (с) способу). чиннику (наприклад, толуолу або дихлорметану). Сполуки формули XI можна альтернативно Сполуки формули XXIV, в яких Ra та Rb предотримувати реакцією відповідної сполуки формули ставляють Н, можна отримувати відновленням І, в якій R2 представляє -Е-ОН, зі сполукою форвідповідних сполук формули XXXVIII, мули XXXV, R28S(O)2CI XXXV де R28 представляє С1-4алкіл або арил (ці дві групи, як варіант, заміщені одним або більше замісниками, вибраними з групи: С1-4алкіл, атом галогену та нітрогрупа), наприклад, при температурі між -10 та 25°С у присутності придатного розчиннику (наприклад, дихлорметану), а потім реакцією з придатним джерелом іону азиду (наприклад, або їх N-захищених похідних, де Rc - Rf визнаазидом натрію), наприклад, при температурі між чені вище, наприклад, при температурі між кімнатзовнішньою та температурою кипіння під зворотною температурою та температурою кипіння під ним холодильником у присутності прийнятного зворотним холодильником у присутності придатнорозчиннику (наприклад, Ν,Ν-диметилформаміду) 37 75382 38 го відновнику (наприклад, LіАІН4) та прийнятного 20, 321 (1983)], розкриття цього документу тут органічного розчиннику (наприклад, ТГФ). уведено як посилання (наприклад, гідруванням Сполуки формули XXIV, в яких Ra та Rb предпри підвищеному тиску (наприклад, 25-35кПа) у ставляють Η можна альтернативно отримувати присутності придатного каталізатору (наприклад, реакцією відповідних сполук формули XXXIX, паладію на вугіллі) та придатного розчиннику (наприклад, льодяної оцтової кислоти)). Сполуки формули XXXVIII можна альтернативно отримувати сполученням сполук формули XLIIA або XLIIB, або їх N-захищених похідних, де Rc - Rf та L2 визначені вище, з аміаком або його захищеними похідними (наприклад, бензиламіном), наприклад, в умовах, що описано у міжнародній патентній заявці WO 96/07656, розкриття цього документу тут уведено як посилання, (наприклад, при температурі між кімнатною температурою та температурою кипіння під зворотним холодильником у присутності придатного розчиннику (наприклад, нижчого алкілового спирту (як-то метанол) або ДМФ)). Сполуки формули XXIV, в яких Rc та Rd представляють метил, a Ra, Rb, Re та Rf усі представляють Η можна альтернативно отримувати згідно зі способом, описаним у [J. Оrg. Chem. 61, 8897 (1996)], розкриття цього документу тут уведено як посилання. Сполуки формули XXIX, в як В представляє С1-4алкілен, можна отримувати сполученням сполук формули XL, де Вс представляє С1-4алкілен, Hal представляє хлор, бром або йод, та Ab, R2 та R3 визначені вище, зі сполукою формули VIII, що описано вище, наприклад, при температурі між -25°С та кімнатною температурою у присутності придатної солі цинку(ІІ) (наприклад, безводного ZnBr2), прийнятного каталізатору (наприклад, Pd(PPh3)4 або Ni(PPh3)4) та реакційно-інертного органічного розчиннику (наприклад, ТГФ, толуолу або діетилового етеру). Сполуки формули XXXVI можна отримувати аналогічно сполукам формули XI (тобто з відповідного спирту). Сполуки формули XXXVIII, в як Rc та Rd представляють Н, можна отримувати відновленням відповідних сполук формули XLI, або їх N-захищених чи Ν,Ν-захищених похідних, наприклад, як описано у [J. Heterocyclic Chem. або їх N-захищених похідних, де L7 представляє відщеплювану групу (як-то галоген або -ОН), a Ra - Rf визначені вище, з аміаком або його захищеними похідними (наприклад, бензиламіном), наприклад, в умовах, що добре відомі фахівцям (наприклад, де реагент є сполукою формули XLIIB, реакцію можна проводити при температурі між кімнатною температурою та температурою кипіння під зворотним холодильником у присутності придатного розчиннику (як-то ТГФ)), а потім циклізацією утвореного амідного інтермедіату в умовах, що добре відомі фахівцям (наприклад, реакцією з дегідратувальним засобом, як-то SOCI2). Сполуки формули XXXVIII можна також отримувати реакцією сполуки формули XLIII, або її N-захищеного (наприклад, Nбензильного) похідного, де Ls представляє придатну відщеплювану групу (як-то нижчий алкоксил (наприклад, метоксил) або ціаногрупу), R29a - R29c незалежно представляють С1-6алкіл або феніл, Rx представляє Re або Rf, Ry представляє Rf або Re (за прийнятністю), a Re та Rf визначені вище, зі сполукою формули XLIV, або її N-захищеного (наприклад, Nбензильного) похідного, де Rc та Rd визначені вище, наприклад, в умовах, ідентичних або аналогічних умовам, описаним у міжнародній патентній заявці WO 97/11945 та Tempahedron 41(17), 3529 (1985), розкриття цих документів тут уведено як посилання (наприклад, при температурі між кімна 39 75382 40 тною температурою та температурою кипіння під вище, наприклад, в умовах, що описано вище з зворотним холодильником у присутності придатноогляду на отримання сполук формули XXXIX, а го розчиннику (наприклад, дихлорметану) та припотім перетворенням двох груп -C(O)OR27 в утвойнятного каталізатору (наприклад, кислоти, як-то реному інтермедіаті у групи -C(O)L7 в умовах, добтрифлуороцтової кислоти або джерела флуоридре відомих фахівцям. іону, як-то флуорид тетрабутиламонію або флуоСполуки формули XLIIB можна отримувати рид аргентуму)). реакцією відповідних сполук формули XLIX, Сполуки формули XXXDC можна отримувати реакцією діестеру малеїнової кислоти, як-то сполуки формули XLV, де R27, Rc та Rd визначені вище, зі сполукою формули XLVI, Н2N-CН(Rx)-C(O)ОН XLVI де Rx описано вище, у присутності сполуки формули XLVIІ, RyCHO XLVII де Ry описано вище, наприклад, в умовах, ідентичних або аналогічних умовам, описаним у міжнародних патентних заявках WO 96/07656 та WO 95/15327, розкриття цих документів тут уведено як посилання, а потім перетворенням двох груп C(O)OR27 в утвореному інтермедіаті у групи -CH2L2 в умовах, що добре відомі фахівцям. Сполуки формули XLI можна отримувати сполученням сполук формули XLVIIIА чи XLVIIIB, або її N-захищених (наприклад, N-бензильних) похідних, де Re, Rf та L7 визначені вище, з аміаком або його захищеними похідними (наприклад, бензиламіном), наприклад, в умовах, що описано тут з огляду на отримання сполук формули XXXVIII, а потім циклізацією утвореного амідного інтермедіату в умовах, відомих фахівцям. Сполуки формули XLIIA можна отримувати реакцією відповідних сполук формули XLV зі: (1) сполукою формули XLIII, що описано вище, або її N-захищеним (наприклад, N-бензильним) похідним, наприклад, в умовах, що описано вище з огляду на отримання сполук формули XXXVIII, а потім перетворенням двох груп -C(O)OR27 в утвореному інтермедіаті у групи -С(О)L7 в умовах, добре відомих фахівцям (наприклад, для сполук формули XLIIA, в яких L7 представляє ОН, гідролізом у присутності основи лужного металу (як-то КОН) та придатного розчиннику (наприклад, етанолу, води або їх сумішей)); або (2) сполукою формули XLVI, що описано вище, у присутності сполуки формули XLVII, що описано де Rc та Rd визначені вище, зі: (1) сполукою формули XLIII, що описано вище, або її N-захищеним (наприклад, N-бензильним) похідним, наприклад, в умовах, що описано вище з огляду на отримання сполук формули XXXVIII; або (2) сполукою формули XLVI, що описано вище, у присутності сполуки формули XLVII, що описано вище, наприклад, в умовах, що описано вище з огляду на отримання сполук формули XXXIX. Сполуки формули XLIIB можна альтернативно отримувати циклізацією відповідних сполук формули XLIIA, в яких L представляє ОН, наприклад, в умовах, що добре відомі фахівцям (наприклад, реакцією з дегідратувальним засобом (як-то Ν,Ν'дициклогексилкарбодіімід) у присутності придатного розчиннику (як-то ТГФ)). Сполуки формули XLIII можна отримувати реакцією відповіднюї сполуки формули L або її N-захищеного (наприклад, Nбензильного) похідного, де Rx та R29a - R29c визначені вище, зі сполукою формули XLVII, яку визначено вище, у присутності нижчого алкілового спирту, як-то метанол (для отримання сполук формули XLIII, в яких Ls представляє нижчий алкоксил; наприклад, в умовах, ідентичних або аналогічних умовам, описаним у міжнародній патентній заявці WO 97/11945 (наприклад, при температурі між 0°С та кімнатною температурою у присутності води)) або джерела ціанід-іону, як-то ціаніду калію (для отримання сполук формули XLIII, в як L8 представляє ціаногрупу, наприклад, в умовах, ідентичних або аналогічних умовам, описаним у Tempahedron 41(17), 3529 (1985)). Сполуки формул XLVIIIA та XLVIIIIB можна отримувати відомими способами, наприклад, згідно зі способами, описаними у [J. Heterocyclic Chem. 20, 321 (1983)]. Сполуки формули L можна отримувати відомими способами, наприклад, згідно зі способами, описаними у міжнародній патентній заявці WO 97/11945. Сполуки формул IV, VII, VIII, X, XII, ХIIІ, XIV, XVI, XVIII, XX, XXI, XXII, ХХIII, XXV, XXVI, XXVII, XXVIII, XXX, XXXI, ХХХІІА, ХХХІІВ, ХХХІІІА, ХХХІІІВ, XXXIV, XXXV, XXXVII, XL, XLIV, XLV, XLVI, 41 75382 42 XLVII, XLIX та їх похідні є комерційно доступними, більш зручним способом, індивідуальні етапи згавідомі з літератури, або їх можна отримувати анаданого тут способу можна проводити у відмінному логічно способам, описаним тут, або звичайними порядку, та/або індивідуальні реакції можна проспособами синтезу, згідно зі стандартними спосоводити на відмінних етапах загального шляху бами, з легко доступних вихідних матеріалів, вико(тобто замісники можна додавати до відмінних ристовуючи прийнятні реагенти та умови реакції. інтермедіатів та/або проводити хімічні перетвоНаприклад, перетворення для отримання сполук рення на відмінних інтермедіатах, у порівнянні з формули І (наприклад, етапи (d), (e), (f), (j), (k), (I), асоційованими вище з певною реакцією). Це за(m), (n), (ο), (p), (q), (v), (у) та (z) способу) можна, лежатиме серед іншого від таких факторів, як приде прийнятно, проводити на інтермедіатних сполурода інших функціональних груп, представлених в ках, розкритих тут (наприклад, сполуках формул II, певних субстратах, наявності ключових інтермедіVI, IX, XI, XV, XVII та XIX) для отримання інших атів та стратегії захисних груп (якщо це має місце), інтермедіатів, що є корисними у синтезі сполук що треба пристосувати. Ясно, що тип залученої формули І. хімії впливатиме на вибір реагенту що використоЗамісники на арильних (наприклад, фенілі), та вують у вказаних етапах синтезу, потребу у захис(за прийнятністю) гетероциклічних, групах у сполуних групах, що застосовують, та їх тип, та послідоках, описаних тут, можна перетворити в інші заяввність завершення синтезу. лені замісники використаннямспособів, що добре Фахівцям треба також розуміти що, хоча деякі відомі фахівцям. Наприклад, гідроксигрупу можна захищені похідні сполук формули І, які можна перетворити в алкоксил, феніл можна галогенуваотримувати до кінцевого етапу зняття захисту, ти для отримання галогенфенілу, нітрогрупу можможуть не виявляти фармакологічну активність як на відновити для отримання аміногрупи, галоген такі, їх можна застосовувати парентерально або можна щамінити ціаногрупою, тощо. перорально та після цього вони метаболізують у Фахівцю також слід розуміти що різноманітні тілі з утворенням сполуки винаходу, яка є фармастандартні перегрупування та перетворення замікологічно активною. Такі похідні можуть тому бути сників або функціональних груп у деяких сполуках описаними як "проліки". Більш того, деякі сполуки формули І даватимуть інші сполуки формули І. формули І можуть діяти як проліки інших сполук Наприклад, карбоніл можна відновити до гідроксиформули І. лу або алкілену, а гідроксигрупу можна перетвориУсі проліки сполук формули І включені у рамки ти у атом галогену. винаходу. Сполуки винаходу можна виділяти з їх реакФахівцям також слід розуміти що деякі сполуки ційних сумішей використанням звичайних спософормули І можуть бути корисними як інтермедіати бів. у синтезі деяких інших сполук формули І. Фахівцям треба розуміти що у описаному виДеякі вищенаведені інтермедіати є новими. ще способі функціональн групи інтермедіатної Згідно з наступним аспектом винаходу запропоносполуки можуть бути захисними групами або мовано тому: (а) сполуку формули II, що описано жуть потребувати захисту ними. вище (за умови, що коли Ra - Rf усі представляють Функціональн групи, які бажано захищати, Н, то R1 не представляє (і) С1-12алкілу, як варіант, включають гідроксил, аміногрупи та карбонові кисзаміщеного арилом або Het1, (ii) -С(О)-(як варіант, лоти. Придатні захисні групи для гідроксигрупи заміщеного арилу), або (ііі) третвключають триапкілсиліл та діарилалкілсиліл (набутилоксикарбонілу), або її захищене похідне; (b) приклад, трет-бутилдиметилсиліл, третсполуку формули VI, що описано вище, або її забутилдифенілсиліл або триметилсиліл), тетрагідхищене похідне; (с) сполуку формули IX, що опиропіраніл та алкілкарбоніл (наприклад, метил- та сано вище, або її захищене похідне; (d) сполуку етил карбоніл). Придатні захисні групи для аміногформули XI, що описано вище, або її захищене рупи включають бензил, сульфонамідогрупу (напохідне; (c) сполуку формули XV, що описано виприклад, бензолсульфонамідогрупу), третще, або її захищене похідне; (f) сполуку формули бутилоксикарбоніл, 9-флуоренілметоксикарбоніл XVIII, що описано вище (за умови, що коли В або бензилоксикарбоніл. Придатні захисні групи представляє Z, то R2 представляє -Е-О-(як варідля амідиногрупи та гуанідиногрупи включають ант, заміщений арил)), або її захищене похідне; та бензилоксикарбоніл. Придатні захисні групи для (g) сполуку формули XIX, що описано вище, або її карбонових кислот включають С1-6алкільні або захищене похідне. бензилові естери. Сполуки формули II, що можна згадати, вклюЗахист та зняття захисту з функціональн групи чають сполуки, в яких: можуть мати місце перед або після будь-яких опи(а) коли R1 представляє -C(O)XR7, то: саних вище етапів реакції. R7 не представляє незаміщений С1-12алкіл; Захисні групи можна видалити згідно з зі споR7 представляє арил; собами, якц добре відомі фахівцям та описано X представляє S; далі: (b) коли Ra - Rf усі представляють Η, тο R1 не Застосування захисних груп повністю описано представляє: у ["Protective Groups in Organic Chemistry", видавн. (і) -C(O)XR7; J.W.F. McOmie, Plenum Press (1973), та "Protective (іі) незаміщений, лінійний або розгалужений Groups in Organic Synthesis", 3rd вид., T.W. Greene С1-4алкіл & P.G.M. Wutz, Wiley-lnterscience (1999)]. (ііі) незаміщений, лінійний або розгалужений Фахівцям зрозуміло, що для отримання сполук С1-6алкіл винаходу альтернативним, а, у деяких випадках (iv) лінійний або розгалужений С1-4алкіл, замі 43 75382 44 щений фенілом (ця остання група є моно- або динафтил (останню групу, як варіант, заміщено заміщеною одним замісником, вибраним з групи: одним або більше замісниками, вибраними з груфлуор, хлор, бром, метил або метоксил); пи: -ОН, ціаногрупа, атом галогену, нітрогрупа, С1(ν) лінійний або розгалужений С1-4алкіл, замі(як варіант, закінчений групою 6алкіл щений одним замісником, вибраним з групи: флуN(H)C(O)OR23a), С1-6алкоксил, Het1, арил (ця арилор, хлор, бром, метил або феніл (ця остання група група може не бути заміщеною будь-якими настує заміщеною одною або двома , метоксигрупами); пними арил-групами), -N(R24a)R24b, -C(O)R24c, (νі) лінійний або розгалужений С1-4алкіл, заміC(O)OR24d, -C(O)N(R24e)f -N(R24j)C(O)R224h, 24i 24j 24k щений одним замісником, вибраним з групи: флуN(R )C(O)N(R )R , -N(R24m)S(O)2R23b, ор, хлор, бром, метил або феніл; S(O)nR23c, -OS(O)2R23d та -S(O)2N(R24n)R24p) (vii) лінійний або розгалужений С1-4алкіл, заHet1, міщений замісником, вибраним з групи: атом гало-C(O)R5a, гену, метил, метоксил або арил; -OR5b, 1 (c) R представляє: -N(R6)R5c, 2 5a 7 8 5d (і) Het , -C(O)R , -C(O)XR , -C(O)N(R )R , -C(O)XR7, 9 S(O)2R , незаміщений, циклічний або частково -C(O)N(R8)R5d та циклічний/ациклічний С4-12алкіл, або С1-4алкіл за-S(O)2R9; міщений або закінчений, або С5-12алкіл, як варіант, (iii) Het2, -C(O)R5a, -C(O)XR7, -C(O)N(R8)R5d, заміщений та/або закінчений, одним або більше S(O)2R9, незаміщений, циклічний або частково замісниками, вибраними з групи: циклічний/ациклічний С4-12алкіл, або С1-4алкіл заатом галогену, міщений або закінчений, або С5-12алкіл, як варіант, ціаногрупа, заміщений та/або закінчений, одним або більше нітрогрупа, замісниками, вибраними з групи: атом галогену, феніл (останню групу, як варіант, заміщено ціаногрупа, нітрогрупа, Het1, -C(O)R5a, -OR5b, групою -ОН, ціаногрупою, нітрогрупою, С2-6алкілом N(R6)R5c, -C(O)XR7,-C(O)N(R8)R5d та -S(O)2R9; 23a (як варіант, закінченим групою -N(H)C(O)OR ), С2(iv) Het2, -C(O)R5a, -C(O)XR7, -C(O)N(R8)R5d, 1 S(O)2R9, незаміщений, циклічний або частково 6алкоксилом, Het , арилом (ця арил-група може не бути заміщеною будь-якими наступними арилциклічний/ациклічний С4-12алкіл, або С1-5алкіл загрупами), -N(R24a)R24b, -C(O)R24c, -C(O)OR24d, міщений або закінчений, або С6-12алкіл, як варіант, C(O)N(R24e)R24f, -N(R24d)C(O)R24h, заміщений та/або закінчений, одним або більше N(R24i)C(O)N(R24j)R24k, -N(R24ra)S(O)2R23b, замісниками, вибраними з групи: ціаногрупа, нітроS(O)nR23c, -OS(O)2R23d та -S(O)2N(R24n)R24p), група, Het1, -C(O)R5a, -N(R6)R5c, -C(O)XR7, 8 5d 9 5b 5b нафтил (останню групу, як варіант, заміщено O(Ο)Ν(R )R , -S(O)2R та -OR (де R представодним або більше замісниками, вибраними з груляє Η, С2-6алкіл (як варіант, заміщений та/або запи: -ОН, ціаногрупа, атом галогену, нітрогрупа, С1кінчений одним або більше замісниками, вибрани(як варіант, закінчений групою ми з групи: -ОН, С1-6алкоксил, атом галогену, 6алкіл N(H)C(O)OR23a), С1-6алкоксил, Het1, арил (ця арилціаногрупа, нітрогрупа, арил, Het3 та -NHC(O)R10), група може не бути заміщеною будь-якими настуарил або Het4). 24a 24b 24c пними арил-групами), -N(R )R , -C(O)R , Сполуки формули XVII, що можна згадати, C(O)OR24d, -C(O)N(R248)R24f, -N(R24g)C(O)R24h, включають сполуки, в яких: N(R24i)C(O)N(R24i)R24k, -N(R24m)S(O)2R23b, (a) коли Ra - Rf усі представляють Н, а група S(O)nR23c, -OS(O)2R23d та -S(O)2N(R24n)R24p) A-C(R2)(R3)-B- представляє С1-4алкілен, то R4 не Het1, представляє феніл, що є моно- або ди-заміщеним -C(O)R5a, одним замісником, вибраним з групи: флуор, хлор, -OR5b, бром, метил або метоксил; -N(R6)R5c, (b) коли Ra - Rf усі представляють Н, а група -C(O)XR7, A-C(R2) (R3)-B- представляє С1-5алкілен, С14 -C(O)N(R8)R5d та не 4алкілен, заміщений атомом галогену, то R 9 -S(O)2R ; представляє феніл, що є моно- або ди-заміщеним (ii) Het2, -C(O)R5a, -C(O)XR7, -C(O)N(R8)R5d, метоксилом; S(O)2R9, незаміщений, циклічний або частково (c) R4 представляє нафтил або Het13, обидві ці циклічний/ациклічний С4-12алкіл, або С1-5алкіл загрупи, як варіант, заміщені одним або більше заміміщений або закінчений, або С6-12алкіл, як варіант, сниками, вибраними з групи: -ОН, ціаногрупа, газаміщений та/або закінчений, одним або більше логен, нітрогрупа, С1-6алкіл (як варіант, закінчений замісниками, вибраними з групи: групою -N(H)C(O)OR23a), С1-6алкоксил, Het1, арил, ціаногрупа, N(R24a)R24b, -C(O)R24c, -C(O)OR24d, -C(O)N(R24e)R24f, нітрогрупа, -N(R24g)C(O)R24h, -N(R24i)C(O)N(R24i)R24k, 24ra 23b феніл (останню групу, як варіант, заміщено N(R )S(O)2R , -S(O)nR23c, -OS(O)2R23d, групою -ОН, атомом галогену, ціаногрупою, нітрогS(O)2N(R24n)R24p та (у випадку тільки Het13) оксог4 рупою, С1-6алкілом (як варіант, закінченим групою рупа, або R представляє феніл заміщений [] або 23a 1 N(H)C(O)OR ), С2-6алкоксилом, Het , арилом (ця більше замісниками, вибраними з групи: -ОН, ціаарил-група може не бути заміщеною будь-якими ногрупа, нітрогрупа, С2-6алкіл (як варіант, закінченаступними арил-групами), -N(R24a)R24b, -C(O)R24c, ний . групою -N(H)C(O)OR23a), C2-6алкоксил, Het1, -C(O)OR24d, -C(O)N(R24e)R24f, -N(R24f)C(O)R24h, арил, -N(R24a)R24b, -C(O)R24c, -C(O)OR24d, 24i 24j 24k 24ra 23b N(R )C(O)N(R )R , -N(R )S(O)2R , C(O)N(R24e)R24f, -N(R24g)C(O)R24h, 23c 23d 24n 24p 24i 24j 24k S(O)nR , -OS(O)2R та -S(O)2N(R )R ), N(R )C(O)N(R )R , -N(R24ra)S(O)2R23b, 45 75382 46 S(O)nR23c, -OS(O)2R23d, -S(O)2N(R24n)R24p). Сполуки винаходу також мати перевагу в тому, Медичне та фармацевтичне застосування що можуть бути більш ефективними, менш токсиСполуки винаходу є корисними, оскільки вони чними, мати ширші межі активності (включаючи виявляють фармакологічну активність. Вони тому виявлення будь-якої комбінації активності класу І, показані як фармацевтичні засоби. класу II, класу III та/або класу IV (особливо активОтже, згідно з наступним аспектом винаходу ності класу І та/або класу IV на додаток до активзапропоновано сполуки винаходу для застосуванності класу III)), бути більш потужними, бути більш ня як фармацевтичні засоби. довгодіючими, продукувати меншу побічну дію Зокрема, сполуки винаходу виявляють міокар(включаючи нижчий випадок проаритмії, як-то трідіальну електрофізіологічну активність, як продепотіння-мерехтіння), більш легко поглинатися, або монстровано, наприклад, у описаних нижче тестах. мати інші корисні фармакологічні властивості, ніж Сполуки винаходу, можна тому чекати, будуть сполуки, відомі у попередньому рівні техніки. корисними при профілактиці та лікуванні аритмій, Біологічні Тести а зокрема атріальних та вентрикулярних аритмій. Тест А Сполуки винаходу отже, показані при профілаПервісна електрофізіологічна дія на анестезоктиці або лікуванні серцевих хвороб, або при виваних морських свинках значенні пов'язаних з серцем хвороб, в яких аритВикористовували морських свинок масою між мії, можна вважати, грають головну роль, 660 та 1100г. Тварин розміщали щонайменше за включаючи ішемічну хворобу серця, несподіваний один тиждень перед початком експерименту з вісерцевий напад, інфаркт міокарду, серцеву нестальним доступом до їжі та води протягом цього печу, серцеву хірургію та тромбоемболічні випадки. ріоду. При лікуванні аритмій, сполуки винаходу, як Анестезію здійснювали інтраперитонеально виявлено, селективно затримують серцеву репоін'єкцією пентобарбіталу (40-50мг/кг) та уводили ляризацію, подовжуючи тим інтервал QT, а зокрекатетери в одну сонну артерію (для реєстрування ма, виявляють активність класу III. Хоча сполуки тиску крові та відбору зразків крові) та в одну яревинаходу, як виявлено, виявляють активність кламну вену (для вливання ліків). Голчасті електроди су III, зокрема при лікуванні аритмій, різновиди їх розміщали на кінцівках для реєстрування ЕКГ (ввід активності необов'язково обмежені цим класом. II). Термометр розміщали у ректальному отворі та Згідно з наступним аспектом винаходу, запророзміщали тварин на нагрівальній підкладці, підтпоновано спосіб лікування аритмії, спосіб включає римуючи ректальну температуру в межах між 37,5 застосування терапевтично ефективної кількості та 38,5°С. сполуки винаходу до особи, що потерпає від такоПроводили трахеотомію та тварин штучно вего стану або схильна до нього. нтилювали кімнатним повітрям з використанням Фармацевтичні препарати невеликого вентилятору для тварин, підтримуючи Сполуки винаходу звичайно застосовують пеу крові рівень газів в нормальних для виду межах. рорально, підшкірно, внутрішньовенно, інтраартеДля зменшення автономних впливів обидва блуріально, трансдермально, інтраназально, інгаляцікаючих нерви були розрізані на шиї та внутрішньоєю, або будь-яким іншим парентеральним шляхом, венно уводили 0,5мг/кг пропанололу за 15 хвилин у формі фармацевтичних препаратів, що містять перед початком експерименту. активний інгредієнт як вільну основу, фармацевтиЛівий вентрикулярний епікардій відкривали лічно прийнятний іонообміннник або нетоксичну орвосторонньою трахеотомією та звичайний електганічну або неорганічну кислотно-адитивну сіль, у род-присоску для реєстрування монофазного діюфармацевтично прийнятній дозованій формі. Зачого потенціалу (МАР) кріпили до лівої лежно від розладу та пацієнта, якого лікують, а вентрикулярної вільної стінки. Електрод тримали у також шляху застосування композиції можна запозиці так довго, як можна було б реєструвати стосовувати в різних дозах. прийнятний сигнал, в іншому випадку його переноСполуки винаходу можна також поєднувати з сили у нову позицію. Біполярний електрод для будь-якими іншими ліками, корисними у лікуванні кардіостимуляції кріпили до лівого шлуночка. Караритмій та/або інших серцево-судинних розладів. діостимуляцію (тривалість 2мс, двічі діастолічний Згідно з наступним аспектом винаходу запропоріг) проводили виконаним на замовлення стипоновано тому фармацевтичну композицію, що мулятором постійного струму. Серце електростивключає сполуку винаходу у суміші з фармацевтимулювали з частотою дещо вище нормальної сично прийнятним ад'ювантом, розріджувачем або нусної частоти протягом 1 хвилини кожні п'ять носієм. хвилин протягом усього дослідження. Придатні добові дози сполуки при терапевтичКров'яний тиск, сигнал МАР та ввід II ЕКГ реному лікуванні людини складають приблизно єстрували самописом Mingograph ink-jet (Siemens0,005-25,0мг/кг маси тіла при пероральному застоElema, Sweden). Усі сигнали збирали (частота висуванні та приблизно 0,005-10,0мг/кг маси тіла при бірки 1000Гц) на персональному комп'ютері протяпарентеральному застосуванні. Переважні межі гом останніх 10с кожної кардіостимуляційної посдобових доз сполук винаходу при терапевтичному лідовності та останніх 10с наступної хвилини лікуванні людини складають приблизно 0,005синусного ритму. Сигнали обробляли, використо10,0мг/кг маси тіла при пероральному застосуванні вуючи спеціальну програму, розроблену для отрита приблизно 0,005-5,0мг/кг маси тіла при паренмання та аналізу фізіологічних сигналів, виміряних теральному застосуванні. у експериментальних тварин [дивися Axenborg та Сполуки винаходу мають перевагу в тому, що Hirsch, Comput. Methods Programs Biomed. 41, 55 є ефективними проти серцевих аритмій. (1993)]. 47 75382 48 Тест-процедура складалася з отримання двох Фібробласти мишей Itk (1-клітини) отримували базових контрольних реєструвань, 5 хвилин порізз Американської колекції типових культур (АТСС, но, протягом кардіостимуляційного та синусного Manass'a, VA) та культивували у модифікованому ритмів. Після другого контрольного реєстрування, Дубекко середовищі Ігла, доповненому сироватпершу дозу тест-речовини уводили у об'ємі 0,2мл кою зародка теляти (5% за об'ємом), пеніциліном у катетер яремної вени протягом 30с. Через 3 хви(500од./мл), стрептоміцином (500од./мл) та Lлини починали кардіостимуляцію і робили нове аланін-L-глутаміном (0,862мг/мл). Клітини пересіреєстрування. Через 5 хвилин після попередньої вали кожні 3-4 доби, використовуючи трипсин дози застосовували наступну дозу тест-речовини. (0,5мг/мл у позбавленому кальцію буферованому Протягом кожного експерименту давали 6-10 посфосфатом фізіологічному розчині, Gibco BRL). За лідовних доз. три доби перед експерименти, суспензію клітин Аналіз результатів переносили піпеткою у чорні пластмасові, 96З ряду змінних, виміряних у цьому аналізі, три коміркові планшети з прозорим дном, (Costar) при вибирали як найважливіші для порівняння та ви25000клітин/комірку. бору активних сполук. Трьома вибраними змінниФлуоресцентний зонд DіВас4(3) (DiBac ми були тривалість МАР при 75 процентній репоMolecular probes) використовували для виміру ляризації протягом кардіостимуляції, час атріомембранного потенціалу. DiBac4(3) максимально вентрикулярної (AV) провідності (визначений як поглинає при 488нМ та випромінює при 513нМ. інтервал між атріальним кроком серцевого ритму DiBac4(3) є бізоксонолом, а отже є негативно зарята початком вентрикулярного МАР) протягом кардженим при рН 7. Внаслідок свого негативного діостимуляції, та серцеву частоту (визначену як заряду розподіл DiBac4(3) на мембрані є залежним інтервал RR протягом синусного ритму). Систолічвід трансмембранного потенціалу: якщо клітина ний та діастолічний тиск крові вимірювали, для деполяризована (тобто внутрішня частина клітини судження про гемодинамічний статус анестезовастає менш . негативною відносно зовнішньої часних тварин. Далі, ЕКГ досліджували стосовно аритини клітини), концентрація DiBac4(3) у внутрішній тмії та/або морфологічних змін. частині клітини збільшується внаслідок електросСередні значення двох контрольних реєструтатичних сил. Входячи у внутрішню частину клітивань приймали за нуль та реєстровані ефекти пісни, молекули DiBac4(3) можуть приєднуватися до ля послідовних доз тест-речовини виражали як ліпідів та білків, що викликає збільшення флуорепроцент змін від цієї величини. Побудовою графіку сцентного випромінювання. Отже, деполяризація цього проценту величини проти застосованої дози призводитиме до збільшення флуоресценції у перед кожним реєструванням створювали криві DіВас4(3). Зміну флуоресценції DіВас4(3) визначали доза-реакція. Таким чином, кожний експеримент за допомогою FLIPR. давав три криві доза-реакція, одну для тривалості Перед кожним експериментом клітини промиМАР, одну для часу AV-провідності та одну для вали 4 рази у буферованому фосфатом фізіологісинусної частоти (інтервал RR). Середню криву чному розчині (PBS) для видалення усього культидля усіх експериментів, проведених з тестваційного середовища. Клітини , обробляли 5мкМ речовиною, розраховували та величини потужносDіВас4(3) (у 180мкл PBS) при 35°С. При досягненні ті виводили з середньої кривої. Усі криві дозастабільної флуоресценції (звичайно через 10 хвиреакція у цих експериментах будували за лінійним лин) додавали 20мкл тест-речовини, використозв'язком отриманих результатів визначення. Кумувуючи FLIPR's внутрішню 96-коміркову систему лятивну дозу, що подовжувала тривалість МАР на переносу піпеткою. Флуоресценційні виміри далі 10% від базових даних, використовували як індекс робили кожні 20 с протягом ще 10 хвилин. Усі ексдля оцінки електрофізіологічної потужності класу перименти проводили при 35°С, внаслідок високої III засобу при дослідженні (D10). температурної чутливості провідності затриманого Тест В ректифікованого калієвого каналу та флуоресценОброблені глюкокортикоїдом фібробласти ції DiBac4(3). Тест-речовини готували у другому 96мишей як модель для визначення блокераторів комірковому планшеті у PBS з вмістом 5мкМ затриманого ректифікованого К-струму DіВас4(3). Концентрація речовин була у 10 разів ІК50 для блокади калієвого каналу визначали, більшою від потрібної концентрації у експерименті, використовуючи мікротитрувальний планшет, на оскільки здійснювали додаткове розбавлення 1:10 базі способу скринування на основі змін мембранпри додаванні речовини протягом експерименту. ного потенціалу оброблених глюкокортикоїдом Дофетилід (10мкМ) використовували як позитивфібробластів мишей. Мембранний потенціал обний контроль, тобто для визначення максимальнороблених глюкокортикоїдом фібробластів мишей го збільшення флуоресценції. вимірювали, використовуючи флуоресценцію бізоПідгонку кривих, використовувану для визнаксонольного барвнику DіВас4(3), який можна легко чення величин ІК50, проводили за допомогою провизначати, використовуючи флуоресцентний лаграми Graphpad Prism (Graphpad Software Inc, San зерний зчитувач відтворення відображення з Diego, CA). планшету (FLIPR). Експресію затриманого ректиТест С фікованого калієвого каналу викликали у фібробМетаболічна стабільність тест-сполук ластах мишей 24-годинною експозицією глюкокорСкринінг in vitro проводили для визначення тикоїдом дексамехазоном (5мкМ). Блокада цього метаболічної стабільності сполуки А винаходу. калієвого каналу деполяризувала фібробласти, Використовували печінкову фракцію S-9 від призводячи до збільшеної флуоресценції собак, людини, кролів та щурів з NADPH як кофакDіВас4(3). тором. Дослідження проводили в таких умовах: S 49 75382 50 9 (3мг/мл), NADPH (0,83мМ), буфер Трис-НСІ 341ммоль; з етапу (а) вище) у СН3ОН в атмосфері (50мМ) при рН 7,4 та 10мкМ тест-сполуки. азоту. До утвореного розчину додавали 10% Pd/C Реакцію починали додаванням тест-сполуки та (за масою; 5г). Атмосферу азоту заміняли на Н2 закінчували через 0,1, 5, 15 та 30 хвилин підви(1атм. тиску) та реакційну суміш перемішували щенням величини рН у зразку вище 10 (NaOH; протягом 12 годин. Реакційну суміш розбавляли 1мМ). Після екстракції розчиннику концентрацію водою (160мл), фільтрували через шар целюлози тест-сполуки вимірювали проти внутрішнього стадля видалення каталізатору та фільтрат концентндарту за допомогою рідинної хроматографії (дерували у вакуумі, отримуючи твердий продукт. тектування флуоресценція/УФ). Розтирання з абсолютним ЕtOН дало 74,6г (82%) Процент тест-сполуки, що залишився через 30 потрібної сполуки як білуватого твердого продукту хвилин (а тим t1/2) розраховували та використовупісля сушки у вакуумній шафі при 50°С/66,5Па вали як вимір метаболічної стабільності. (0,5мм Hg). 1Н ЯМР (300МГц, CDCI3) 5 7,4-7,2 (m, Винахід ілюстровано наступними прикладами. 5H), 4,6 (s, 2H), 3,5 (d, 2H, J=12,5Гц), 3,25 (d, 2H, Приклади J=7,5Гц), 3,0 (dd, 2H, J=7,5, 12,5). Загальні експериментальні способи (с) 3-бензил-цис-3,7-діазадицикло[3.3.0]октан Мас-спектри реєстрували на одному з наступГідрохлорид 3-бензил-3,7них приладів: спектрометр Perkin-Elmer SciX API діазадицикло[3.3.0]октан-2,4-діону (73,8г, 150ex; VG Quattro II; одиничний квадрупольний 275ммоль; з етапу (b) вище) додавали порціями до мас-спектрометр VG Platform II; або одиничний суспензії LiAH4, (83,5г, 2,26моль) у ТГФ при 0°С. квадрупольний мас-спектрометр MiKpomass Реакційну суміш повільно гріли до кипіння під звоPlatform LCZ (останні три прилади опоряджені ротним холодильником. Після кип'ятіння під зворопневматичним напівавтоматичним інтерфейсом тним холодильником протягом 16 годин реакційну електророзпилення (ПІ-МС)). Виміри 1Н ЯМР та суміш охолоджували до 0°С. До холодної реакцій13 С ЯМР проводили на спектрометрах BRUKER ної суміші додавали краплями послідовно Н2О АСР 300 та Varian 300, 400 та 500, що працюють (84мл), 3Μ NaOH (84мл) та воду (250мл). Реакційпри частотах 1Н 300, 400 та 500МГц відповідно та ну суміш далі перемішували протягом додаткових при частотах 13С 75,5, 100,6 та 125,7МГц відповід15 хвилин та фільтрували через шар броунмілерино. Альтернативно, виміри 13С ЯМР проводили на ту (Celite ) для видалення неорганічної солі. Фільспектрометрі BRUKER АСЕ 200 при частоті трат концентрували у вакуумі, отримуючи сирий 50,3МГц. продукт. Перегонка Кугельрохра (95-115°С/66,5Па Ротамери можуть бути позначеними у спект(0,5мм Hg)) дала 46,8г (84%) потрібної сполуки як рах залежно від легкості інтерпретації спектрів. безбарвне масло. 1 Якщо не визначене інше, хімічні зсуви наведені у Н ЯМР (300МГц, CDCI3) 7,3-7,2 (m, 5H), млн.-1 з розчинником як внутрішнім стандартом. 3,51 (s, 2H), 2,9 (dd, 2H, J=6,6, 12Гц), 2,75 (d, Синтез інтермедіатів 12Гц), 2,7-2,5 (m, 4H), 2,3 (d, 2H, J=7,5Гц),2,0 (bs, Наступні інтермедіати не були комерційно до2H). ступними та були тому отримані описаними нижче (d) Гідрохлорид 3-бензил-7-(третспособами. бутоксикарбоніл)-цис-37-діазадицикло[3.3.0]октану Отримання А Розчин ди-трет-бутил-дикарбонату (65,3г, Трет-бутилгексагідропіроло[3,4-е]пірол-2(1Н)299ммоль) у ТГФ (100мл) додавали краплями до карбоксилат перемішуваного розчину 3-бензил-3,7(a) 3,7-Дибензил-цис-3,7діазадицикло[3.3.0]октану (55г, 272ммоль; з етапу діазадицикло[3.3.01октан-2,4-діон (с) вище) у ТГФ (650мл) при 0°С. Після завершенТрифлуороцтову кислоту (1-3мл) додавали ня додавання реакційну суміш перемішували прокраплями до розчину N-(метоксиметил)-Nтягом 12 годин при кімнатній температурі. Реактриметилсилілметил)бензиламіну (137,0г, ційну суміш розбавляли етилацетатом (300мл) та 580ммоль) та N-бензилмалеїніміду (95,0г, розсолом (300мл). Органічний шар відділяли та 500ммоль) у СН2СІ2 (1л), доки відбувалася енервідставляли убік, водний шар екстрагували етилагійна екзотермічна реакція. Після закінчення екзоцетатом (5 200мл). Поєднані органічні фази сушитермічної реакції (приблизно 10 хвилин) суміш ли Na2SO4, фільтрували та концентрували у вакугріли при кипінні під зворотним холодильником умі, отримуючи безбарвне масло. Масло протягом 3 годин. Реакційну суміш охолоджували, розчиняли у ЕtOАс (750мл), охолоджували до 0°С а далі гасили 1Η NaOH (200мл). Органічний шар та повільно додавали 1Μ розчин НСІ у Et2O відділяли, промивали розсолом, сушили Na2SO4, (275мл). Осаджену сіль НСІ збирали та сушили у фільтрували та концентрували у вакуумі, отримувакуумній шафі, отримуючи 91,1г (99%) потрібної ючи 170,0г сирого продукту. Кристалізація з ізопсполуки як білуватого твердого продукту. 1Н ЯМР ропілового етеру дала 109,0г (67%) потрібної спо(300МГц, CD3OD) 7,6-7,4 (m, 5H), 4,4 (s, 2H), 3,8луки. 3,6 (bs, 2H), 3,5-3,3 (bs, 4H), 3,3-3,0 (bs, 2H), 1,45 1 Н ЯМР (300 МГц, CDCI3) 7,4-7,0 (m, 10Н), (s, 9H). 4,65 (s, 2H), 3,55 (s, 2H), 3,30 (d, 2H, J=12Гц), 3,15 (e) Гідрохлорид трет-бутил гексагідропіро(d, 2H, J=6Гц), 2,35 (m, 2H). ло[3,4-с]пірол-2(1Н)-карбоксилату (b) Гідрохлорид 3-бензил-цис-3,7До розчину гідрохлориду 3-бензил-7-(третдіазадицикло[3.3.0]октан-2,4-діону бутоксикарбоніл)-3,7-діазадицикло[3.3.0]-октану Концентровану гідрохлоридну кислоту (28,4мл, (91,1г, 269ммоль; з етапу (d) вище) у метанолі 341ммоль) додавали до суспензії 3,7-дибензил(250мл) в атмосфері азоту додавали 10% Pd/C (за 3,7-діазадицикло[3.3.0]октан-2,4-діону (109,0г, масою; 9,8г). Атмосферу азоту заміняли на Н2 51 75382 52 (1атм. тиску) та реакційну суміш перемішували рі. Реакційну суміш перемішували протягом 2 гопротягом 18 годин. Реакційну суміш фільтрували дин при кімнатній температурі перед додаванням через шар целюлози для видалення каталізатору. води та ДХМ. Органічний шар відділяли, промиваФільтрат концентрували у вакуумі, отримуючи біли водою, сушили сульфатом магнію та концентлуватий твердий продукт. Твердий продукт сурували у вакуумі з отриманням 68,1г (100%) потріспендували у ЕtOАс та збирали. Після сушки у бної сполуки. вакуумній шафі протягом 18 годин при (e) Трет-бутилу 2-[(4-ціанофенокси)метил]-160°С/66,5Па (0,5мм Hg) отримували 58,0г (87%) азиридинкарбоксилат потрібної сполуки як білуватого твердого продукту. Охолоджений (0°С) розчин 2-[(третТемп. плавл.: 175-178°С. Rf=0,45 (50:40:9:1, бутоксикарбоніл)аміно]-1-[(4-ціаноСН2СІ2:СНСІ3:МеОН:конц. NH4OH). фенокси)метил]етилметансульфонату (з етапу (d) MC (XI): m/z=213(M+H). вище; 30,6г, 82,6ммоль) та гідросульфат тетрабу1 тиламонію (3г, 8,8ммоль) у ДХМ (100мл) обробляН ЯМР (300МГц, CD3OD) 3,6 (m, 4H), 3,35 ли 50мас.% водним NaOH (60мл) в інертній атмо(dd, 2H), 3,14 (m, 4H), 1,48(s,9H). 13 сфері. Утворену суміш перемішували та давали С ЯМР (75МГц, CD3OD) 156, 81,5, 50,5, повільно досягти кімнатної температури протягом 51,2, 43,0, 28,5. 4 годин, а далі екстрагували ефіром. Органічний Відповідну вільну основу отримували так: гідшар промивали водою та концентрували у вакуумі рохлорид розчиняли у CH3CN. Чотири еквіваленти для отримання залишку, який очищали хроматогК2СО3 додавали разом з невеликою кількістю ворафією на колонці(дихлорметан елюент). Кристади. Суміш перемішували протягом 2 годин, а далі лізація з суміші діетиловий етер:ди-ізопропіловий фільтрування та випарювання дали основу з кільетер дала потрібну сполук з кількісним виходом. кісним виходом. (f) трет-бутил (2S)-2-[(4-ціанофенокси)метил]Отримання В 1-азиридинкарбоксилат Трет-бутилу (1S)-2-(4-ціаноФенокси)-1Потрібну сполуку отримували згідно зі спосо(гексагідропіроло[3,4-с]пірол-2(1Н)бами, описаними на етапах (а)-(e) вище для синілметил)етилкарбамат тезу трет-бутилу 2-[(4-ціанофенокси)-метил]-1(а) 4-(2-оксиранілметокси)бензонітрил азиридинкарбоксилату, але з використанням (S)Потрібну сполуку отримували з 75% виходом (+)-епіхлоргідрину замість епіхлоргідрину на етапі згідно зі способом, описаним у міжнародній патен(а). тній заявці WO 99/31100 (тобто реакцією між п(g) Бензилу трет-бутилу тетрагідропіроло[3,4ціанофенолом та епіхлоргідрином). с]пірол-2,5(1Н,3Н)-дикарбоксилат (b) 4-[(3-Аміно-2Гідрохлорид трет-бутилу гексагідропіроло[3,4гідроксипропіл)окси]бензонітрил с]пірол-2(1Н)-карбоксилату (10г, 0,04моль; дивися 4-(2-оксиранілметокси)бензонітрил (100г, отримання вище) та триетиламін (14мл, 0,1моль) 0,57моль; дивися етап (а) вище) додавали у суміш змішували у СНСІ3 (100мл). N-бензилоксиконцентрованого водного розчину гідроксиду амокарбонілоксисукцинімід (11г, 0,044моль), розчиненію (500мл) та ізо-пропанол (300мл). Утворену ний у CDCI3 (100мл), додавали при 0-5°С. Суміші кашку перемішували при кімнатній температурі давали повільно досягти кімнатної температури та протягом 3 діб. Реакційну суміш фільтрували для перемішували при кімнатній температурі протягом видалення нерозчинного побічного продукту, а 5 годин. Реакційну суміш промивали водою, сушифільтрат концентрували у вакуумі для отримання ли сульфатом натрію та випарювали, отримуючи сирого продукту, який кристалізували з ацетонітпотрібну сполуку з кількісним виходом рилу з отриманням 50г (46%) потрібної сполуки. 13 С ЯМР (CD3CI3) 155,01, 155,64, 136,99, (с) трет-бутил 3-(4-ціанофенокси)-2128,71, 128,22, 128,13, 79,80, 67,12, 50,30, 49,88, гідроксипропілкарбамат 41,76, 28,71. Охолоджений (0°С) розчин 4-[(3-аміно-2(h) Бензилу гексагідропіроло[3,4-с]пірол-2(1Н)гідроксипропіл)окси]бензонітрилу (з етапу (b) викарбоксилат ще; 44,6г, 0,23моль) у суміші ТГФ:Н2О (1,5л 1:1) Бензилу трет-бутилу тетрагідропіроло[3,4обробляли ди-трет-бутил-дикарбонатом (53г, с]пірол-2,5(1Н,3Н)-дикарбоксилат (40ммоль; з ета0,24моль). Суміш перемішували при кімнатній тепу (а) вище) розчиняли у етилацетаті. Етилацетат, мпературі протягом ночі, після чого додавали NaCI насичений НСІ (г) (500мл) додавали при 0°С та та утворен органічний шар відділяли. Водний шар перемішували, даючи досягти кімнатної темпераекстрагували ефіром та поєднані органічні фази тури. Розчинник випарювали та продукт розчиняли сушили та концентрували у вакуумі. Утворене мау CH3CN. К2СО3 (4eq.) та воду (2мл) додавали. сло (70г) фільтрували через шар оксиду силіцію, а Суміш перемішували протягом 2 годин, перед фідалі кристалізували з суміші діетиловий етер:дильтруванням та випарюванням з отриманням 8г ізопропіловий етер з отриманням 50г потрібної (82%) потрібної сполуки, яку використовували без сполуки. наступної очистки у наступному етапі. (d) 2-[(трет-бутоксикарбоніл)аміно]-1-[(4(i) Бензилу 5-[(2S)-2-[(третціанофенокси)метил]етилметансульфонат бутоксикарбоніл)аміно]-3-(4-ціанофенокси)Метансульфонілхлорид (22,3г 0,195моль) допропіл]гексагідропіроло[3,4-с]пірол-2(1Н)давали протягом 1,5 годин до охолодженого (0°С) карбоксилат розчину трет-бутил 3-(4-ціанофенокси)-2Трет-бутилу (2S)-2-[(4гідроксипропілкарбамату (з етапу (с) вище; 51,2г, ціанофенокси)метил]азиридин-1-карбоксилат (2,5г, 0,177моль) та 4-(диметиламіно)піридину (1,3г, 9,1ммоль; дивися етап (f) вище) та бензилу гекса10,6ммоль) у піридині (250мл) в інертній атмосфе 53 75382 54 гідропіроло[3,4-с]пірол-2(1Н)-карбоксилат (2,24г, вакуумі. Утворений залишок очищали хроматог9,1ммоль; дивися етап (h) вище) розчиняли в ізопрафією на силікагелі, елюючи сумішшю ропанолі (30iriL) та перемішували при 56°С протяІПС:етилацетат:гептан (5:25:70) з отриманням гом 24 годин. Розчинник далі випарювали. Продукт 14,5г (77%) потрібної сполуки. очищали хроматографією на оксиді силіцію (ети(с) 4-(4-Ціанофеніл)-4-(3,4лацетат, 0-5% МеОН елюент), отримуючи 3,8г диметоксифенокси)бутилметансульфонат (80%) потрібної сполуки. МС (ЕР): m/z=521 (М+Н)+. Розчин метансульфонілхлориду (3,4мл, 5,0г, (i) Трет-бутилу (1S)-2-(4-ціанофенокси)-144ммоль) у ДХМ (15мл) повільно додавали до (гексагідропіроло[3,4-с]пірол-2(1Н)охолодженої (-5°С) суміші 4-[1-(3,4ілметил)етилкарбамат диметоксифенокси)-4-гідроксибутил]бензонітрилу Бензилу 5-[(2S)-2-[(трет(з етапу (b) вище; 11г, 34ммоль) та триетиламіну бутоксикарбоніл)аміно]-3-(4-ціанофенокси)(7мл, 5,2г, 50,6ммоль) у ДХМ (50мл), протягом пропіл]гексагідропіроло[3,4-с]пірол-2(1Н)додавання температура не зростала вище 2°С. карбоксилат (3,6г, 6,9ммоль; з етапу (і) вище) розПеремішування продовжували при температурі чиняли в етанолі (300мл 95%) та гідрували над 5% між 0 та 5°С протягом ще 2 годин перед додаванPd/C (за масою). Реакцю зупиняли, коли було погням води. Утворений органічний шар відділяли та линуто теоретичну кількість водню (173мл). Суміш промивали водою, відділяли знов, а далі сушили отримуючи потрібну сполуку зі100% виходом. фільтрували (через броунмілерит (Celite )), а далі (d) Трет-бутилу 5-[4-(4-ціанофеніл)-4-(3.4випарювали. Очистка хроматографією на оксиді диметоксифенокси)бутил]-гексагідропіроло[3,4силіцію (ДХМ, 5% МеОН елюент) дала 1,7г (63,6%) с]пірол-2(1Н)-карбоксилат потрібної сполуки. 13С ЯМР (CD3CI3) 161,86, 4-(4-Ціанофеніл)-4-(3,4155,48, 154,42, 136,81, 133,91, 128,36, 127,84, диметоксифенокси)бутилметансульфонат (1,12г, 127,73, 118,99, 115,21, 104,22, 79,69, 68,14, 66,64, 2,8ммоль; дивися етап (с) вище), трет-бутил гекса60,28, 55,20, 51,72, 48,72, 42,04, 41,06, 28,41. MC гідропіроло[3,4-с]-пірол-2(1Н)-карбоксилат (0,59г, (EP): m/z=387(М+Н)+. 2,8ммоль; дивися отримання вище) та Cs2CO3 Отримання С змішували у CH3CN (30мл) та перемішували при 4-[1-(3,4-Диметоксифенокси)-4кімнатній температурі протягом 3 діб. Суміш далі гексагідропіроло[3,4-с]пірол-2(1Н)фільтрували та випарювали. Очистка на оксиді ілбутил]бензонітрил силіцію (етилацетат: МеОН (9:1) елюент) дала 0,9г (a) 4-[1-(3,4-Диметоксифенокси)-3(60%) потрібної сполуки. МС (ЕР): m/z=522 (М+Н)+ бутеніл]бензонітрил (e) 4-[1-(3,4-Диметоксифенокси)-4Охолоджену (0°С) суміш 4-(1-гідрокси-3гексагідропіроло[3,4-с]пірол-2(1Н)бутеніл)бензонітрил (14,6г, 84,3ммоль) та 3,4ілбутил]бензонітрил диметоксифенол (19,5г, 125,4ммоль) у толуолі Трет-бутилу 5-[4-(4-ціанофеніл)-4-(3,4(500мл) обробляли трибутилфосфіном (32,14мл диметоксифенокси)бутил]гексагідропіроло[3,4чистота 97%, 25,6г, 126,4ммоль), а потім 1,1'с]пірол-2(1Н)-карбоксилат (0,9г, 1,7ммоль; з етапу (азодикарбоніл)дипіперидином (31,8г, (d) вище) розчиняли в етилацетаті (25мл). Розчин 126,4ммоль). Після завершення додавання реакохолоджували до 0°С. Етилацетат (25мл), насичеційна суміш густіла та температура збільшувалася ний газуватим НСІ, додавали та суміш перемішудо 15°С. Додатковий толуол додавали (500мл) та вали при кімнатній температурі протягом 4 годин. суміш перемішували при кімнатній температурі Суміш - випарювали, а далі розчиняли у CH3CN. протягом ночі. Осад трибутилфосфіноксиду далі К2CO3 (1г) та воду (0,05мл) додавали та суміш видаляли фільтруванням та фільтрат концентруперемішували протягом 2 годин. Солі відфільтровали у вакуумі для отримання 65,8г сирого продуквували та розчинник випарювали, отримуючи 0,71г ту, який очищали хроматографією на силікагелі, (100%) потрібної сполуки. МС (ЕР): m/z=421 елюючи сумішшю толуол:метанол (98:2), з отри(М+Н)+. манням 17,9г потрібної сполуки. Отримання D (b) 4-[1-(3,4-Диметоксифенокси)-44-{[(2S)-3-Гексагідропіроло[3,4-с]пірол-2(1Н)гідроксибутил]бензонітрил іл-2-гідроксипропіл]-окси)бензонітрил Боран-метил-сульфідний комплекс (2Μ у ефі(а) трет-бутилу 5-[(2S)-3-(4-ціанофенокси)-2рі, 11мл, 22ммоль) додавали краплями до охологідроксипропіл]гексагідропіроло[3,4-с]пірол-2(1Н)дженого (-5°С) розчину 4-[1-(3,4-диметоксикарбоксилат фенокси)-3-бутеніл]бензонітрилу (з етапу (а) вище; 4-[(2,S)-оксиранілметокси]бензонітрил (4,36г, 17,6г, 56,8ммоль) у сухому ТГФ (15мл) протягом 0,025моль; отриманий, як описано у міжнародній періоду 15 хвилин (при цьому температура реакпатентній заявці WO 99/31100) та трет-бутил гекційної суміші зростала до 0°С). Утворену суміш сагідропіроло[3,4-с]пірол-2(1Н)-карбоксилат (6,2г, перемішували при температурі між 0 та 10°С про0,025моль; дивися отримання вище) змішували в тягом 1,5 годин, перед тим, як давали нагрітися до ізопропанолі та перемішували при 60°С протягом кімнатної температури. Перемішування продовжуночі. Розчинник випарювали та продукт очищали вали протягом ще 3,5 годин при цій температурі флеш-хроматографією на оксиді силіцію, елюючи перед додаванням води (22мл) та тетрагідрату етилацетатом з 10% МеОН. Це дало 1,2г (88%) перборату натрію (11г, 66ммоль). Двофазну суміш потрібної сполуки. перемішували протягом 2 годин при кімнатній тем(b) 4-([(2S)-3-Гексагідропіроло[3,4-с]піролпературі перед відділенням водного шару та екст2(1Н)-іл-2-гідроксипропіл]-окси)бензонітрил рагуванням ефіром. Поєднані органічні шари проПотрібну сполуку отримували у 90% виходом мивали розсолом, сушили та концентрували у 55 75382 56 згідно зі способами, описаними в отриманні С, 3,0моль) у MeCN (450 л) перемішували при кипінні етап (e) вище, використанням трет-бутилу 5-[(2S)під зворотним холодильником протягом ночі. Су3-(4-ціанофенокси)-2міш фільтрували та випарювали для отримання гідроксипропіл]гексагідропіроло[3,4-с]пірол-2(1Н)30,2г (45%) потрібної сполуки, яку використовувакарбоксилату (0,9г, 2,3ммоль; дивися етап (а) вили без подальшої очистки. ще) замість трет-бутилу 5-[4-(4-ціанофеніл)-4-(3,4(b) трет-бутилу 5-[2-(4диметоксифенокси)бутил]гексагідропіроло[3,4-с]ціанофенокси)етил]гексагідропіроло[3,4-с]піролпірол-2(1Н)карбоксилату. 2(1Н)-карбоксилат Отримання Е Потрібну сполуку отримували з 91% виходом 4-[(3-Гексагідропіроло[3,4-с]пірол-2(1Н)згідно зі способом, описаним в отриманні Е, етап ілпропіл)аміно]бензонітрил (с) вище, використанням 4-(2-брометокси)(а) 4-[(3-Пдроксипропіл)аміно]бензонітрил бензонітрилу (дивися етап (а) вище) замість 3-(4Суміш 4-флуорбензонітрилу (12,0г, 99,1ммоль) ціаноаніліно)пропіл 4-метилбензолсульфонату. та 3-аміно-1-пропанолу (59,6г,793ммоль) перемі(с) 4-(2-Гексагідропіроло[3,4-с]пірол-1-2(1Н)шували при 80°С в інертній атмосфері протягом 3 ілетокси)бензонітрил годин перед тим, як додавали воду (150мл). СуміПотрібну сполуку отримували з 100% виходом ші давали охолонути до кімнатної температури, а згідно зі способом, описаним в отриманні С, етап далі екстрагували діетиловим етером. Органічний (e) вище, використанням трет-бутилу 5-[2-(4-ціаношар відділяли, сушили сульфатом натрію, фільтфенокси)етил]гексагідропіроло[3,4-с]пірол-2(1Н)рували та концентрували у вакуумі з отриманням карбоксилату (дивися етап (b) вище) замість трет17г (97%) потрібної сполуки як масла, що кристалібутилу 5-[4-(4-ціанофеніл)-4-(3,4-диметоксизувалося при стоянні. фенокси)бутил]гексагідропіроло[3,4-с]пірол-2(1Н)(b) 3-(4-Ціаноаніліно)пропіл 4карбоксилату. метилбензолсульфонат Отримання G Охолоджений (0°С) розчин 4-[(34-[(3-Гексагідропіроло[3,4-с]пірол-2(1Н)гідроксипропіл)аміно]бензонітрилу (з етапу (а) виілпропіл)сульфоніл]бензонітрил ще; 17г, 96,5ммоль) у сух MeCN (195мл) обробля(а) 4-[(3-бромпропіл)сульфаніл]бензонітрил ли з триетиламін (9,8г, 96,5ммоль), а далі рСуміш 4-ціанотіофенолу (20,8г, 154ммоль), толуолсульфонілхлорид (20,2г, 106ммоль). Суміш 1,3-дибромпропану (155г, 0,77моль) та К2СО3 перемішували при 0°С протягом 90 хвилин перед (21,3г, 154ммоль) у MeCN (300мл) кип'ятили під концентруванням у вакуумі. Воду (200мл) додавазворотним холодильником протягом ночі. Фільтрули до залишку, та водний розчин екстрагували вання та випарювання розчиннику дало коричневе ДХМ. Органічну фазу сушили сульфатом натрію, масло, що кристалізувалося, коли його обробляли фільтрували та концентрували у вакуумі. УтвореЕtOН. Кристали були виділені фільтруванням для ний залишок очищали кристалізацією з ізоотримання потрібної сполуки (24,5г, 62%). пропанолу з отриманням 24,6г (77%) потрібної (b) 4-[(3-бромпропіл)сульфоніл]бензонітрил сполуки. 3-Хлорпероксибензойну кислоту (44,9г 70%, (c) трет-бутил у 5-{3-[(4182ммоль) повільно додавали до охолодженого ціанофеніл)аміно]пропіл)гексагідропіроло[3,4(0°С) розчину 4-[(3с]пірол-2-(1Н)-карбоксилат бромпропіл)сульфаніл]бензонітрилу (з етапу (а) 3-(4-Ціаноаніліно)пропіл 4вище; 23,4г, 91ммоль) у ДХМ (250мл). Суміш далі метилбензолсульфонат (1,98г, 6 ммоль; дивися перемішували при кімнатній температурі протягом етап (b) вище), та трет-бутилу гексагідропіроночі та утворений осад відфільтровували. Фільтло[3,4-с]пірол-2(1Н)-карбоксилату (1,49г, 6ммоль; рат концентрували у вакуумі для отримання залидивися отримання вище) змішували з К2СО3 (1,93г, шку, який показав (за ЯМР-аналізом) вміст 25% 14ммоль) та CH3CN (100мл), а далі перемішували сульфоксиду на додаток до потрібного продукту. при 50°С протягом ночі. Розчинник випарювали та Залишок знов розчиняли у ДХМ (250мл), додаткопродукт очищали хроматографією на оксиді силіву 3-хлорпероксибензойну кислоту (5,6г 70%, цію (ДХМ:МеОН (20:1)) для отримання 1,83г (82%) 23ммоль) додавали, та суміш перемішували пропотрібної сполуки. тягом 30 хвилин. Диметилсульфоксид (20ммоль) (d) 4-[(3-Гексагідропіроло[3,4-с]пірол-2(1Н)додавали для руйнування надлишку rnСРВА пеілпропіл)аміно]бензонітрил ред тим, як розчин ДХМ промивали водним розчиПотрібну сполуку отримували з кількісним вином NaHCO3, відділяли, сушили та концентрували ходом способом, описаним в отриманні С, етап (e) у вакуумі. Це дало сполуку з 76% виходом. вище, використанням трет-бутилу 5-{3-[(4(с) трет-бутилу 5-{3-[(4ціанофеніл)аміно]пропіл}гексагідропіроло[3,4ціанофеніл)сульфоніл]пропіл)гексагідропіроло[3,4с]пірол-2(1Н)-карбоксилату (дивися етап (с) вище) с]пірол-2(1Н)-карбоксилат замість трет-бутилу 5-[4-(4-ціанофеніл)-4-(3,4Потрібну сполуку отримували з 75% виходом диметоксифенокси)бутил]-гексагідропіроло[3,4згідно зі способом, описаним в отриманні Е, етап с]пірол-2(1Н)-карбоксилату. (с) вище, використанням 4-[(3Отримання F бромпропіл)сульфоніл]бензонітрилу (дивися етап 4-(2-Гексагідропіроло[3,4-с]пірол-2(1Н)(b) вище) замість 3-(4-ціаноаніліно)пропіл 4ілетокси)бензонітрил метилбензолсульфонату. (а) 4-(2-брометокси)бензонітрил (d) 4-[(3-Гексагідропіроло[3,4-с]пірол-2(1Н)Суміш 4-ціанофенолу (35,7г, 0,3моль), К2СО3 ілпропіл)сульфонал]бензонітрил (41,4г, 0,3моль) та 1,2-диброметану (561г, Потрібну сполуку отримували з 100% виходом 57 75382 58 згідно зі способом, описаним в отриманні С, етап суміш промивали водою. Водний шар далі екстра(e) вище, використанням трет-бутилу 5-{3-[(4гували ДХМ. Поєднані органічні шари сушили ціанофеніл)сульфоніл]пропіл}гексагідропіроло[3,4Na2SO4 та випарювали для отримання 6,0г (70%) с]пірол-2(1Н)-карбоксилату (дивися етап (с) вище) потрібної сполуки. замість трет-бутилу 5-[4-(4-ціанофеніл)-4-(3,4Отримання L диметоксифенокси)бутил]гексагідропіроло[3,42-(4-Піридиніл)етилу 1Н-імідазол-1с]пірол-2(1Н)-карбоксилату. карбоксилат Отримання Η Потрібну сполуку отримували зі 100% виходом 4-(2-Гексагідропіроло[3,4-с]пірол-2(1Н)згідно зі способом, описаним в отриманні К вище, ілетокси)ізофталонітрил використанням 2-(4-піридиніл)-1-етанолу замість (а) 4-(2-брометокси)ізофталонітрил 2-(4-морфолініл)-1-етанолу. Потрібну сполуку отримували з 64% виходом Отримання Μ згідно зі способом, описаним в отриманні F, етап N-[2-(2-Метоксіетокси)етил]-1Н-імідазол-1(а) вище, використанням 4карбоксамід гідроксиізофталонітрилу замість 4-ціанофенолу. Потрібну сполуку отримували з 40% виходом (b) трет-бутилу 5-[2-(2,4згідно зі способом, описаним в отриманні К вище, диціанофенокси)етил]гексагідропіроло[3,4-с]використанням 2-(2-метоксіетокси)етиламіну запірол-2(1Н)-карбоксилат мість 2-(4-морфолініл)-1-етанолу. Потрібну сполуку отримували з 75% виходом Отримання N згідно зі способом, описаним в отриманні Е, етап 2-(4-Ацетил-1-піперазиніл)етилу 1Н-імідазол(с) вище, використанням 4-(2-брометокси)1-карбоксилат ізофталонітрилу (дивися етап (а) вище) замість 3(і) 1-[4-(2-Гідроксіетил)-1-піперазиніл]-1-етанон (4-ціаноаніліно)пропіл 4-метилбензолсульфонату. Розчин 2-(1-піперазиніл)-1-етанолу (6,5г, (с) 4-(2-Гексагiдропіроло[3,4-с]пірол-]-2(1Н)0,05моль) у ДХМ (5мл) обробляли краплями оцтоілетокси)ізофталонітрил вим ангідридом (5,1г, 0,05моль). Протягом додаПотрібну сполуку отримували з 80% виходом вання температура реакційної суміші зростала від згідно зі способом, описаним в отриманні С, етап 22 до 60°С. Реакційну суміш випарювали кілька (e) вище, використанням трет-бутилу 5-[2-(2,4разів з толуолом з отриманням 5,6г (65%) потрібдиціанофенокси)етил]гексагідропіроло[3,4-с]піролної сполуки. 2(1Н)-карбоксилату; (дивися етап (b) вище) замість (іі) 2-(4-Ацетил-1-піперазиніл)етилу 1Нтрет-бутилу 5-[4-(4-ціанофеніл)-4-(3,4-диімідазол-1-карбоксилат метоксифенокси)бутил]-гексагідропіроло[3,4Розчин 1,1'-карбонілдіімідазолу (5г, 31ммоль) с]пірол-2(1Н)-карбоксилату. у ДХМ (200мл) обробляли розчином 1-[4-(2Отримання І гідроксіетил)-1-піперазиніл]-1-етанону (дивися 2-(Ацетилокси)-1,1-диметилетилу 1Н-імідазолетап (і) вище; 5г, 29ramol) у ДХМ (50мл). Реакційну 1-карбоксилат суміш перемішували при кімнатній температурі Суміш 2-гідрокси-2-метилпропілацетату (3,35г, протягом ночі перед тим, як додавали воду. Шари 25,3ммоль) та 1,1'-карбонілдіімідазолу (4,11г, розділяли, та органічний шар промивали водою, 25,3ммоль) у ДХМ перемішували протягом 8 годин сушили та концентрували у вакуумі з отриманням при кімнатній температурі. Суміш далі переносили 7,4г (96%) потрібної сполуки. у закриту посудину та гріли до 100°С протягом Отримання О ночі. Суміш концентрували у вакуумі перед тим, як 1-[4-(3-бромпропіл)-1-піперазиніл]-1-етанон додавали етер та воду. Органічну фазу відділяли, Суміш 1-(1-піперазиніл)-1-етанону (6,7г, сушили та концентрували у вакуумі. Утворений 0,052моль), дибромпропану (330мл, надлишок) та залишок очищали хроматографією на силікагелі, К2СО3 (10,2г, 0,079моль) перемішували при кімнаелюючи сумішшю ТГФ:гептан (1:1), для отримання тній температурі протягом 4 годин. Суміш промипотрібної сполуки з 20% виходом. вали 4 100мл води, та органічну фазу (розбавлеОтримання J ну ДХМ) підкислювали водною гідробромідною 1-Ціано-1-метилетил 1Н-імідазол-1кислотою (7мл 62% НВr розчиненo у 150 л води). карбоксилат Органічний шар відділяли та промивали водою Суміш 1,1'-карбонілдіімідазолу (5г, 31ммоль) (2 50мл). Поєднані водні шари екстрагували ефіта 2-гідрокси-2-метилпропаннітрилу (2,6г, ром, нейтралізували (до рН 7) з 13мл 10Μ NaOH, а 31ммоль) у ДХМ перемішували при кімнатній темдалі екстрагували ДХМ. Поєднані органічні шари пературі протягом ночі. сушили та концентрували у вакуумі для отримання Воду додавали та органічний шар відділяли, 4,1г (32%) потрібної сполуки. сушили сульфатом натрію та концентрували у Отримання Ρ вакуумі. Утворений залишок очищали хроматог3-(Етилсульфоніл)пропілу 4рафією на силікагелі, елюючи етилацетатом, для метилбензолсульфонат отримання 2,7г (50%) потрібної сполуки. (і) 3-(ЕтилсульФоніл)-1-пропанол Отримання К Розчин 3-(етилтіо)-1-пропанолу (13г, 0,11моль) 2-(4-Морфолініл)етилу 1Н-імідазол-1у оцтовій кислоті (40мл) обробляли краплями Н2О2 карбоксилат (30% у воді, 12,2г, 0,11моль). Суміш перемішували Суміш 1,1’-карбонілдіімідазол (6,5г, 40ммоль) протягом 2 годин при кімнатній температурі, перед та 2-(4-морфолініл)-1-етанолу (5,0г, 38,1ммоль) у концентруванням у вакуумі. ЯМР-аналіз показав, ДХМ (200мл) перемішували протягом 22 годин при що утворений залишок складався з 40% потрібнокімнатній температурі. Етер (400мл) додавали та го продукту та 60% відповідного О-ацетату. ι Аце 59 75382 60 тат гідролізували розчиненням реакційної суміші у 5-[(2S)-3-(4-ціанофенокси)-2-гідроксипропіл]-N200мл метанолу та додаванням 3г NaOH (розчиетилгексагідропіроло[3,4-с]пірол-2(1Н)неного у невеликій кількості води). Цю суміш пекарбоксамід (m/z=359); ремішували протягом ночі при кімнатній темпера4-({(2R)-3-[5-[2-(3,4турі, далі концентрували у вакуумі. Утворений диметоксифеніл)етил]гексагідропіроло[3,4-с]сирий продукт розчиняли у ДХМ, та нерозчинний пірол-2(1Н)-іл]-2-гідроксипропіл}окси)бензонітрил матеріал відфільтровували. ДХМ видаляли випа(m/z=452); рюванням для отримання 13,4г (88%) потрібної 4-({3-[5-(бутилсульфоніл)гексагідропіроло[3,4сполуки. с]пірол-2(1Н)-іл]пропіл}-аміно)бензонітрил (іі) 3-(Етилсульфоніл)пропіл 4(m/z=391); метилбензолсульфонат 4-({3-[5-(3,3-диметил-2Суміш 3-(етилсульфоніл)-1-пропанолу (дивися оксобутил)гексагідропіроло[3,4-с]пірол-2(1Н)етап (і) вище; 13,4г, 88ммоль) та піл]пропіл}аміно)-бензонітрил (m/z=369); толуолсульфонілхлориду (16,8г, 88ммоль) у ДХМ 4-({3-[5-[2-(3,4(150мл) обробляли краплями TEA (13,4г, диметоксифеніл)етил]гексагідропіроло[3,4-с]пірол132ммоль). Утворену суміш перемішували при 2(1Н)-іл]пропіл) аміно)бензонітрил (m/z=435); кімнатній температурі протягом 3 годин перед тим, 5-[2-(4-цiанофенокси)етил]-Nяк промивали водним розчином хлориду амонію. етилгексагідропiроло[3,4-с]пiрол-2(1Н)Органічний шар далі відділяли, сушили та конценкарбоксамід (m/z=329); трували у вакуумі. Продукт кристалізували з ефіру, 5-[4-(4-ціанофеніл)-4-(3,4що містить невелику кількостість ДХМ, з отримандиметоксифенокси)бутил]-Nням 17,9г (66%) потрібної сполуки. етилгексагідропіроло[3,4-с]пірол-2(1Н)Синтез сполук формули І карбоксамід (m/z=493); Приклад 1 4-{2-[5-(бутилсульфоніл)гексагідропіроло[3,4Загальний опис отримання сполук у прикладі 2 с]пірол-2(1Н)-іл]етокси}-бензонітрил (m/z=378); нижче: 4-[4-[5-(бутилсульфоніл)гексагідропіроло[3,4Один з продуктів з отримань від В до Η с]пірол-2(1Н)-іл]-1-(3,4-диметоксифенокси)(0,25ммоль) розчиняли у СНСІ3 (0,5мл). Прийнятбутил]бензонітрил (m/z 542); ний електрофіл (0,25ммоль), розчинений у CH3CN 4-{2-[5-(3,3-диметил-2(2мл), додавали, а потім К2СО3 або триетиламін оксобутил)гексагідропіроло[3,4-с]пірол-2(1Н)(0,375ммоль) (такі основи не потрібні, коли електіл]етокси}бензонітрил (m/z=356); рофілом є ізоціанат). 4-{1-(3,4-диметоксифенокси)-4-[5-(3,3Реакційну суміші перемішували при темперадиметил-2-оксобутил)гексагідропіроло[3,4-с]піролтурі між кімнатною температурою та 50°С протя2(1Н)-іл]бутил}бензонітрил (m/z=520); гом 2-5 діб. Реакції контролювали за допомогою 4-{2-[5-[2-(3,4ЕІ-МС. Коли реакції було завершено, реакційну диметоксифеніл)етил]гексагідропіроло[3,4-с]піролсуміші фільтрували, розчинники випарювали, а 2(1Н)-іл]етокси}бензонітрил (m/z=422); далі залишки розчиняли у MeCN або СН2СІ2 (2мл). 4-{1-(3,4-диметоксифенокси)-4-[5-[2-(3,4Утворений розчин додавали до іонообмінного тведиметоксифеніл)етил]гексагідропіроло[3,4-с]піролрдо-фазного екстракційного шару (2г СВА), який 2(1Н)-іл]бутил}бензонітрил (m/z=586); далі елювали сумішшю ДXM:MeCN (4:1, фракція 4-({(21S)-3-[5(бутилсульфоніл)гексагідропіроло[3,4-с]пірол1), а потім ДХМ:МеОН:ТЕА (8,1:1, 4 2мл). Фракції 2(1Н)-іл]-2-гідроксипропіл)окси)бензонітрил; випарювали. ВЕРХ та МС-аналіз далі дали мож4-({(2S)-3-[5-(3,3-диметил-2ливість ідентифікації фракцій, в яких був продукт. оксобутил)гексагідропіроло[3,4-с]пірол-2(1Н)-іли-2Приклад 2 гідроксипропіл}окси)бензонітрил (m/z=386); Наступні сполуки отримували з прийнятних ін5-{3-[(4-ціанофеніл)аміно]пропіл}-Nтермедіатів (які описано вище) згідно зі способами етилгексагідропіроло[3,4-с]-пірол-2(1Н)чи аналогічно способам, описаним тут (наприклад, карбоксамід (m/z=342); способом, описаним вище) та/або стандартними трет-бутилу 5-[4-(4-ціанофеніл)-4-(3,4способами хімії розчинних фаз (мас-спектри сподиметоксифенокси)бутил]гекса-гідропіроло[3,4лук, де їх визначено, є у дужках): с]пірол-2(1Н)-карбоксилат (m/z=522); трет-бутилу 5-[3-(4-ціанофенокси)-2трет-бутилу 5-{3-[(4гідроксипропіл]гексагідропіроло[3,4-с]пірол-2(1Н)ціанофеніл)сульфоніл]пропіл}гексагідропіроло[3,4карбоксилат (m/z=388); с]-пірол-2(1Н)-карбоксилат (m/z=420); трет-бутилу 5-[2-(45-[(2S)-3-(4-ціанофенокси)-2-гідроксипропіл]-Nціанофеніл)етил]гексагідропіроло[3,4-с]пірол(3,5-диметилізохазол-4-іл)-гексагідропіроло[3,42(1Н)-карбоксилат (m/z=342); с]пірол-2(1Н)-карбоксамід; трет-бутилу 5-[(2S)-3-(4-ціанофенокси)-2N-{[5-[(2S)-3-(4-суамофенокси)-2гідроксипропіл]гексагідропіроло[3,4-с]пірол-2(1Н)гідроксипропіл]гексагідропіроло[3,4-с]пірол-2(1Н)карбоксилат (m/z=388); іл]карбоніл}-4-метилбензолсульфонамід; трет-бутилу 5-{3-[(45-[(2S)-3-(4-ціанофенокси)-2-гідроксипропіл]-Nціанофеніл)аміно]пропіл}гексагідропіроло[3,4-с](4-метоксифеніл)-гексагідропіроло[3,4-с]піролпірол-2(1Н)-карбоксилат (m/z=371); 2(1Н)-карбоксамід; трет-бутилу 5-[2-(45-[(2S)-3-(4-ціанофенокси)-2-гідроксипропіл]-Nціанофенокси)етил]гексагідропіроло[3,4-с]пірол{4-[(трифлуорметил)-тіо]феніл}2(1Н)-карбоксилат (m/z=358);
ДивитисяДодаткова інформація
Назва патенту англійською3,7-diazodicyclo[3.3.0]octanes and use thereof in the treatment of cardiac arrhythmias
Автори англійськоюStrandlund Gert, Svensson, Peder
Назва патенту російською3,7-диазадицикло[3.3.0]октаны и их применение при лечении сердечных аритмий
Автори російськоюСтрандлунд Герт
МПК / Мітки
МПК: C07D 487/04, A61P 9/06, A61K 31/407
Мітки: аритмій, 3,7-діазадицикло[3.3.0]октани, лікуванні, серцевих, застосування
Код посилання
<a href="https://ua.patents.su/34-75382-37-diazadiciklo330oktani-ta-kh-zastosuvannya-pri-likuvanni-sercevikh-aritmijj.html" target="_blank" rel="follow" title="База патентів України">3,7-діазадицикло[3.3.0]октани та їх застосування при лікуванні серцевих аритмій</a>
Попередній патент: Жатка
Наступний патент: Парашут десантника
Випадковий патент: Унітарний бойовий патрон малого калібру












