Сполуки 4-заміщеного 3-фенілсульфанілметилбіцикло[3.1.0]гексану як антагоністи mglur 2/3
Номер патенту: 110039
Опубліковано: 10.11.2015
Автори: Лі Женьхуа, Ветман Татіана Наталі, Мітч Чарлз Говард, Сміт Стефон Корнелл
Формула / Реферат
1. Сполука формули
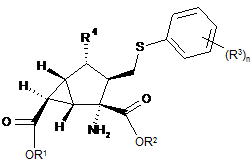 ,
,
де R1 і R2, кожен незалежно один від одного, є водень, С1-С3алкоксикарбонілоксиметил, С1-С5алкілкарбонілоксиметил або С3-C6циклоалкілкарбонілоксиметил;
R3 незалежно один від інших R3 у кожному випадку є метил, фтор або хлор;
R4 є гідроксил, аміногрупа, метилкарбоніламіногрупа або 1,2,4-триазолілтіогрупа; і
n дорівнює 1 або 2;
або її фармацевтично прийнятна сіль.
2. Сполука за п. 1, де кожен з R1 і R2 є водень, або її фармацевтично прийнятна сіль.
3. Сполука за п. 1, де і R1, і R2 обидва не є водень, або її фармацевтично прийнятна сіль.
4. Сполука за п. 1, де R1 і R2 є однакові і не є водень, або її фармацевтично прийнятна сіль.
5. Сполука за п. 4, де кожен з R1 і R2 є ізопропілоксикарбонілоксиметил.
6. Сполука за будь-яким з пп. 1-5, де n = 2, і групи R3 знаходяться у 3- і 4- положеннях фенільного кільця.
7. Сполука за будь-яким з пп. 1-6, де R3 незалежно один від інших R3 у кожному випадку є хлор або фтор.
8. Сполука за п. 1, що являє собою (1S,2R,3S,4S,5R,6R)-2-аміно-3-{[(3,4-дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбонову кислоту або її фармацевтично прийнятну сіль.
9. Сполука за п. 1, що являє собою біс({[(1-метилетокси)карбоніл]окси}метил)(1S,2R,3S,4S,5R,6R)-2-аміно-3-{[(3,4-дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат або його фармацевтично прийнятну сіль.
10. Сполука за п. 1, що являє собою (1S,2R,3S,4S,5R,6R)-2-аміно-3-{[(3-хлор-4-фторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбонову кислоту або її фармацевтично прийнятну сіль.
11. Сполука за п. 1, що являє собою біс({[(1-метилетокси)карбоніл]окси}метил)(1S,2R,3S,4S,5R,6R)-2-аміно-3-{[(3-хлор-4-фторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат або його фармацевтично прийнятну сіль.
12. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-11 або її фармацевтично прийнятну сіль у комбінації із щонайменше одним(ією) фармацевтично прийнятним носієм, допоміжною речовиною або розріджувачем.
13. Сполука за будь-яким з пп. 1-11 або її фармацевтично прийнятна сіль для застосування у терапії.
14. Сполука за будь-яким з пп. 1-11 або її фармацевтично прийнятна сіль для застосування при лікуванні депресивних розладів.
15. Сполука за будь-яким з пп. 1-11 або її фармацевтично прийнятна сіль для застосування при лікуванні розладів, що супроводжуються надмірною сонливістю.
16. Сполука для застосування за п. 14 або п. 15 щодо людини.
17. Сполука за будь-яким з пп. 1-11 або її фармацевтично прийнятна сіль для застосування у одночасній, роздільній або послідовній комбінації з інгібітором повторного поглинання серотоніну при лікуванні депресивних розладів.
18. Сполука для застосування за п. 17, де інгібітором повторного поглинання серотоніну є флуоксетин або циталопрам.
19. Сполука для застосування за п. 17 або п. 18 щодо людини.
20. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-11 або її фармацевтично прийнятну сіль та інгібітор повторного поглинання серотоніну у комбінації із щонайменше одним(ією) фармацевтично прийнятним носієм, допоміжною речовиною або розріджувачем.
21. Фармацевтична композиція за п. 20, яка відрізняється тим, що інгібітором повторного поглинання серотоніну є флуоксетин або циталопрам.
Текст
Реферат: Описаний антагоніст рецепторів mGlu2/3 формули (І), варіанти його застосування і способи його одержання. 4 R S H H O O 1 OR H NH2 OR2 3 (R )n UA 110039 C2 (12) UA 110039 C2 UA 110039 C2 5 10 15 20 25 30 35 40 Глутамат являє собою основний збуджувальний нейротрансміттер у головному мозку і є залученим до найрізноманітніших фізіологічних процесів, які опосередковуються не менше ніж 11 різними рецепторами, кожен зі своїми фармакологічними характеристиками. Метаботропні рецептори глутамату підтипів 2 і 3 (відомі як mGlu2 і mGlu3) часто об'єднують як рецептори mGlu групи II на основі гомології їх послідовностей, подібного зв'язування вторинних месенджерів і аналогічних фармакологічних характеристик. Антагоністи рецепторів mGlu2/3 продемонстрували значні фармакологічні впливи на тваринних моделях стосовно депресивних розладів і розладів, що супроводжуються надмірною сонливістю. Як такі, антагоністи mGlu2/3 вважаються придатними для лікування депресивних розладів, таких як тяжкий депресивний розлад (MDD), уніполярна депресія, дистимія та/або циклотимія, і/або придатними для лікування розладів, що супроводжуються надмірною сонливістю, таких як надмірна денна сонливість (EDS), гіперсомнія, пов'язана з обструктивним апное сну або нарколепсією, порушення циркадних ритмів (у тому числі, але без обмеження ними, розлад, пов'язаний із змінним трудовим графіком, розлад, пов'язаний з пересіканням часових поясів, синдром затримки фази сну, синдром передчасної фази сну і синдром не 24-годинного циклу сну і неспання), ідіопатична гіперсомнія та/або надмірна сонливість, пов'язана з невідновлювальним сном (NRS). У US 5,916,920 описані деякі сполуки 3-монозаміщеного-біцикло[3.1.0]гексану як модулятори метаботропних рецепторів глутамату, придатні для лікування різноманітних розладів, у тому числі як антидепресантні агенти. У US 7,157,594 описані різні сполуки 3-монозаміщеногобіцикло[3.1.0]гексану як антагоністи рецепторів mGlu групи II для застосування при лікуванні різних розладів, у тому числі депресивних симптомів. У US 2007/0021394 А1 описані різні сполуки 3-монозаміщеного-біцикло[3.1.0]гексану як антагоністи рецепторів mGlu групи II та їх проліки для застосування при лікуванні різних розладів, у тому числі депресії. Даний винахід пропонує сімейство сполук 4-заміщеного-3-фенілсульфанілметилбіцикло[3.1.0]гексану з високою антагоністичною активністю відносно рецепторів mGlu2 і mGlu3. Сполуки за цим винаходом є також селективними щодо рецепторів mGlu2 і mGlu3, особливо у зіставленні з іншими рецепторами mGlu. Деякі сполуки також продемонстрували на тваринних моделях, що сполуки за цим винаходом можуть бути придатними для лікування депресивних розладів (які можуть включати тяжкий депресивний розлад (MDD), уніполярну депресію, дистимію та/або циклотимію) і розладів, що супроводжуються надмірною сонливістю (які можуть включати надмірну денну сонливість (EDS), гіперсомнію, пов'язану з обструктивним апное сну або нарколепсією, порушення циркадних ритмів (у тому числі, але без обмеження ними, розлад, пов'язаний із змінним трудовим графіком, розлад, пов'язаний з пересіканням часових поясів, синдром затримки фази сну, синдром передчасної фази сну і синдром не 24-годинного циклу сну і неспання), ідіопатичну гіперсомнію та/або надмірну сонливість, пов'язану з невідновлювальним сном (NRS)). Вплив за цим механізмом дії, що є подібним до впливу антидепресанта, а також вплив, що стимулює неспання, дозволяють прогнозувати також вплив на симптоми депресивних розладів, такі як втома, які в іншому випадку важко піддаються лікуванню за допомогою існуючих антидепресантів. Даний винахід пропонує сполуки формули I: 4 R S 3 (R )n H H O O 1 OR 50 NH2 OR2 ; де R і R , кожен незалежно один від одного, є водень, С1-С3 алкоксикарбонілоксиметил, С1С5 алкілкарбонілоксиметил або C3-6 циклоалкілкарбонілоксиметил; 3 3 R незалежно один від інших R у кожному випадку є метил, фтор або хлор; 4 R є гідроксил, аміногрупа, метилкарбоніламіногрупа або 1,2,4-триазолілтіогрупа, і n дорівнює 1 або 2; або її фармацевтично прийнятну сіль. 1 2 Особливість цього винаходу полягає у тому, що сполуки формули I, де і R , і R обидва є водень (двокислотні сполуки), є терапевтично активними сполуками in vivo, у той час як 1 2 сполуки, в яких R , або R , або обидва не є водень, являють собою проліки їх терапевтично 1 45 H 2 1 UA 110039 C2 1 5 10 15 20 25 30 35 40 45 50 55 60 2 активних двокислотних аналогів. Сполуки, в яких R , або R , або обидва не є водень, гідролізуються in vivo з утворенням терапевтично активного двокислотного аналогу. Сполуки, що являють собою проліки, зокрема проліки зі складних діефірів, при пероральному введенні забезпечують поліпшену біодоступність двокислотного метаболіту в порівнянні з пероральним 1 2 введенням згаданих двокислотних сполук (і R , і R обидва є водень), але двокислотні сполуки забезпечують кращу активність при внутрішньовенному, внутрішньом'язовому або підшкірному введенні. За іншим аспектом цього винаходу запропонована фармацевтична композиція, що містить сполуку формули I або її фармацевтично прийнятну сіль у комбінації із щонайменше одним(ією) фармацевтично прийнятним носієм, розріджувачем або допоміжною речовиною. Крім того, за цим аспектом винаходу запропонована фармацевтична композиція, яка містить сполуку формули I або її фармацевтично прийнятну сіль в поєднанні з одним або декількома фармацевтично прийнятними допоміжними речовинами, носіями або розріджувачами, призначену для лікування депресивних розладів, наприклад, тяжкого депресивного розладу, уніполярної депресії, дистимії і/або циклотимії. За іншим варіантом цього аспекту винаходу запропонована фармацевтична композиція, що містить сполуку формули I або її фармацевтично прийнятну сіль, у комбінації із щонайменше одним(-ією) фармацевтично прийнятним носієм, допоміжною речовиною або розріджувачами і факультативно іншими терапевтичними інгредієнтами. За ще одним варіантом цього аспекту винаходу фармацевтична композиція також містить другий терапевтичний агент, яким є лікарський засіб, придатний для лікуванні депресивних розладів, як, наприклад, інгібітор повторного поглинання серотоніну, такий як, наприклад, флуоксетин і/або циталопрам. За ще одним варіантом цього аспекту винаходу запропонована фармацевтична композиція, яка містить сполуку формули I або її фармацевтично прийнятну сіль в поєднанні з одним(-єю) або декількома фармацевтично прийнятними допоміжними речовинами, носіями або розріджувачами, призначена для лікування розладів, що супроводжуються надмірною сонливістю, наприклад, надмірної денної сонливості (EDS), гіперсомнії, пов'язаної з обструктивним апное сну або нарколепсією, порушення циркадних ритмів (у тому числі, але без обмеження ними, розладу, пов'язаного із змінним трудовим графіком, розладу, пов'язаного з пересіканням часових поясів, синдрому затримки фази сну, синдрому передчасної фази сну і синдрому не 24-годинного циклу сну і неспання), ідіопатичної гіперсомнії та/або надмірної сонливості, пов'язаної з невідновлювальним сном (NRS). За цим винаходом також запропонований спосіб лікування депресивних розладів, як, наприклад, класичний тяжкий депресивний розлад (MDD), уніполярна депресія, дистимія та/або циклотимія, у ссавця, що включає введення ссавцю, який потребує такого лікування, ефективної кількості сполуки формули I або її фармацевтично прийнятної солі. За іншим варіантом цього аспекту винаходу згаданий спосіб також включає введення в одночасній, роздільній або послідовній комбінації другого терапевтичного агента, яким є лікарський засіб, придатний для лікуванні депресивних розладів, як, наприклад, інгібітор повторного поглинання серотоніну, такий як, наприклад, флуоксетин і/або циталопрам. За іншими варіантами здійснення винаходу запропоновані способи лікування розладів, що супроводжуються надмірною сонливістю, що включають введення ссавцю, який потребує такого лікування, ефективної кількості сполуки формули I або її фармацевтично прийнятної солі. За іншими варіантами цього аспекту винаходу надмірна сонливість обумовлена будь-яким одним або декількома з таких факторів: надмірною денною сонливістю (EDS), гіперсомнією, пов'язаною з обструктивним апное сну або нарколепсією, порушенням циркадних ритмів (у тому числі, але без обмеження ними, розладом, пов'язаним із змінним трудовим графіком, розладом, пов'язаним з пересіканням часових поясів, синдромом затримки фази сну, синдромом передчасної фази сну і синдромом не 24-годинного циклу сну і неспання), ідіопатичною гіперсомнією та/або надмірною сонливістю, пов'язаною з невідновлювальним сном (NRS). За одним з конкретних варіантів здійснення цих способів лікування згаданий ссавець являє собою людину. За цим винаходом сполука формули I або її фармацевтично прийнятна сіль також запропоновані для застосування в терапії. За цим аспектом винаходу сполука формули I або її фармацевтично прийнятна сіль запропоновані для застосування при лікуванні депресивних розладів. За іншими варіантами здійснення винаходу згаданим депресивним розладом є будьякий розлад з-посеред тяжкого депресивного розладу (MDD), уніполярної депресії, дистимії та/або циклотимії. За іншим варіантом цього аспекту винаходу сполука формули I або її фармацевтично прийнятна сіль запропоновані для застосування в одночасній, роздільній або послідовній комбінації з інгібітором повторного поглинання серотоніну, таким як, наприклад, 2 UA 110039 C2 5 10 15 20 25 30 35 40 45 50 55 60 флуоксетин і/або циталопрам, для лікування депресивних розладів. Крім того, за цим аспектом винаходу сполука формули I або її фармацевтично прийнятна сіль запропоновані для застосування при лікуванні розладів, що супроводжуються надмірною сонливістю. За конкретними варіантами цього аспекту винаходу надмірна сонливість обумовлена будь-яким одним або декількома з таких факторів: надмірною денною сонливістю (EDS), гіперсомнією, пов'язаною з обструктивним апное сну або нарколепсією, порушенням циркадних ритмів (у тому числі, але без обмеження ними, розладом, пов'язаним із змінним трудовим графіком, розладом, пов'язаним з пересіканням часових поясів, синдромом затримки фази сну, синдромом передчасної фази сну і синдромом не 24-годинного циклу сну і неспання), ідіопатичною гіперсомнією та/або надмірною сонливістю, пов'язаною з невідновлювальним сном (NRS). За одним з конкретних варіантів цього аспекту винаходу згадані варіанти застосування призначені для ссавців, зокрема людей. За іншим аспектом цього винаходу запропоноване застосування сполуки формули I або її фармацевтично прийнятної солі для виробництва лікарського засобу для лікування депресивних розладів, таких як, наприклад, тяжкий депресивний розлад (MDD), уніполярна депресія, дистимія та/або циклотимія. За іншим варіантом цього аспекту винаходу для виготовлення лікарського засобу для лікування депресивних розладів запропоноване застосування сполуки формули I або її фармацевтично прийнятної солі і другого терапевтичного агенту, придатного для лікування депресивних розладів, як, наприклад, інгібітор повторного поглинання серотоніну, наприклад флуоксетин і/або циталопрам. За іншим варіантом здійснення цього винаходу запропоноване застосування сполуки формули I або її фармацевтично прийнятної солі для виготовлення лікарського засобу для лікування розладів, що супроводжуються надмірною сонливістю. За конкретними прикладами цього аспекту винаходу згаданий лікарський засіб призначений для лікування будь-якого одного або декількох з наведених розладів: надмірної денної сонливості (EDS), гіперсомнії, пов'язаної з обструктивним апное сну або нарколепсією, порушення циркадних ритмів (у тому числі, але без обмеження ними, розладу, пов'язаного із змінним трудовим графіком, розладу, пов'язаного з пересіканням часових поясів, синдрому затримки фази сну, синдрому передчасної фази сну і синдрому не 24-годинного циклу сну і неспання), ідіопатичної гіперсомнії та/або надмірної сонливості, пов'язаної з невідновлювальним сном (NRS). Сполуки за цим винаходом мають основні і кислотні складові, і, відповідно, реагують з рядом органічних і неорганічних кислот і основ з одержанням фармацевтично прийнятних солей. Фармацевтично прийнятні солі кожної зі сполук за цим винаходом входять до обсягу даної заявки. Термін "фармацевтично прийнятна сіль" у значенні, вживаному у цьому описі, означає будь-яку сіль сполуки за цим винаходом, що є по суті нетоксичною для живих організмів. Такі солі охоплюють солі, перераховані в Journal of Pharmaceutical Science, 66, 2-19 (1977), які є відомими фахівцям. Класами сполук за цим винаходом, яким віддають перевагу, є сполуки, де: 1 2 1) і R , і R обидва є водень; 1 2 2) R або R чи обидва не є водень; 1 2 3) і R , і R обидва не є водень; 1 2 4) R і R є однакові і не є водень; 1 2 5) Кожен з R і R є ізопропоксикарбонілоксиметил; 6) n=2; 3 3 7) R незалежно один від інших R у кожному випадку є фтор або хлор; 3 8) n=2 і групи R знаходяться у 3- і 4-положеннях фенільного кільця; 3 9) n=2 і кожна з груп R , незалежно одна від одної, є фтор або хлор, і знаходиться у 3- і 4положеннях фенільного кільця; 3 10) n=2, обидві групи R є фтор, і групи фтору знаходяться у 3- і 4-положеннях фенільного кільця; 3 11) n=2, групи R , разом з фенільною складовою, до якої вони приєднані, утворюють 3-хлор4-фторфеніл; 4 12) R є гідроксил. Слід мати на увазі, що іншими сполуками, яким віддають перевагу, є такі сполуки, що поєднують згадані вище переважні варіанти вибору для даних замісників з переважними варіантами вибору інших замісників. Приклади таких комбінацій включають, але ними не обмежуються, такі переважні класи сполук: 1 2 13) переважні сполуки за будь-яким з пунктів 1-5 (переважні варіанти вибору для R і R ), де 3 n дорівнює 2, обидві групи R єфтор, і групи фтору знаходяться у 3- і 4-положеннях фенільного 3 UA 110039 C2 5 10 15 20 25 30 35 40 45 50 55 60 кільця (пункт 10); 1 2 14) переважні сполуки за будь-яким з пунктів 1-5 (переважні варіанти вибору для R і R ), де 3 n дорівнює 2, і групи R разом з фенільною складовою, до якої вони приєднані, утворюють 3хлор-4-фторфеніл (пункт 11); 1 2 15) переважні сполуки за будь-яким з пунктів 1-5 (переважні варіанти вибору для R і R ), де 4 R є гідроксил (пункт 12); 4 16) переважні сполуки за будь-яким з пунктів 13-14, де R є гідроксил (пункт 12); Конкретними сполуками, яким віддають перевагу, є сполуки, описані в Прикладах, у тому числі їх вільні основи і фармацевтично прийнятні солі. Конкретними сполуками, яким віддають перевагу, є: (1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3,4-дифторфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6-дикарбонова кислота або її фармацевтично прийнятна сіль; (1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3-хлор-4-фторфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6-дикарбонова кислота або її фармацевтично прийнятна сіль; біс({[(1-метилетокси)карбоніл]окси}метил)(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3,4дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат або його фармацевтично прийнятна сіль; та біс({[(1-метилетокси)карбоніл]окси}метил)(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3-хлор-4фторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат або його фармацевтично прийнятна сіль (тобто сполуки Прикладів 1, 2, 12, 22 та 32 і альтернативно їх фармацевтично прийнятні солі). Скорочення, вжиті у цьому описі, визначаються так: "BSA" означає бичачий сироватковий альбумін. "DCG IV" означає (2S, 2'R, 3'R)-2-(2',3'-дикарбоксициклопропіл)гліцин. "DMEM" означає модифіковане за способом Дульбекко середовище Ігла. "DMSO" означає диметилсульфоксид. "DPBS" означає забуферений фосфатом фізіологічний розчин Дульбекко. "EDTA" означає етилендіамінтетраоцтову кислоту. "GTP" означає трифосфат гуанозина. "HBSS" означає збалансований сольовий розчин Хенкса. "HEPES" означає 4-(2-гідроксиетил)-1-піперазинетансульфонову кислоту. "HPLC" означає високоефективну рідинну хроматографію. "IBMX" означає 3-ізобутил-1-метилксантин. "IC50" означає концентрацію, при якій досягається 50 % максимального пригнічення. "i.v." означає внутрішньовенний або внутрішньовенно. "i.p." означає інтраперитонеальний. "L-AP-4" означає L-(+)-2-аміно-4-фосфономасляну кислоту. "LC/MS" означає рідинну хроматографію з мас-спектроскопією. "mFST" означає тест примусового плавання мишей; тваринна модель антидепресантної активності. "MS" означає мас-спектроскопію. "MS(ES+)" означає мас-спектроскопію з іонізацією електророзпиленням. "ЯМР" означає ядерний магнітний резонанс. "p.o." означає per os, через рот. "tBu" означає трет-бутильну складову. Загальна хімія Сполуки за цим винаходом можна одержати відповідно до наведених нижче схем синтезу методами, добре відомими і визнаними в цій галузі. Відповідні умови проведення реакцій для етапів за цими схемами є добре відомими у цій галузі, і відповідні заміни розчинників і сумісно застосовуваних реагентів знаходяться у межах фахових можливостей спеціаліста. Більше того, фахівцям в цій галузі буде зрозуміло, що проміжні синтетичні продукти можуть бути виділені і/або очищені різними добре відомими способами, за необхідністю або потребою, і що часто буде можливим використання різних проміжних хімічних сполук безпосередньо на наступному етапі синтезу при незначному очищенні або взагалі без нього. Крім того, фахівцю в цій галузі буде зрозуміло, що в деяких випадках порядок введення складових не є критичним. Конкретний порядок етапів, необхідних для одержання сполук за цим винаходом, залежить від конкретної сполуки, що синтезується, вихідної сполуки і відносної обов'язковості замісних складових, що є добре зрозумілим досвідченому хіміку. Всі замісники, якщо не вказано інше, відповідають попередньо наведеному визначенню і всі реагенти є добре відомими і визнаними в цій галузі. 4 UA 110039 C2 1 2 3 Сполуку 1, що являє собою проліки, можна одержати як показано на Схемі I, де R , R , R , 1 2 R і n є такими, як визначено вище, а і R , і R обидва не є водень. Схема I 4 2 1 3 4 5 10 15 20 25 30 35 Сполука 4 реагує з амінозахисним реагентом, таким як ди-трет-бутилдикарбонат, за умов, 1 2 добре відомих фахівцю у цій галузі, з одержанням сполуки 3. Коли групи R і R у сполуці 2 є ідентичними, сполука 3 реагує з достатньою кількістю відповідного хлорметилалкілкарбонату і відповідними реагентами, такими як йодид натрію і карбонат цезію, у відповідному розчиннику, такому як диметилформамід, з одержанням бажаної сполуки 2, що являє собою складний 1 2 1 2 диефір, з однаковими групами R і R . Коли R і R у сполуці 2 є різними, карбонову кислоту на п'ятичленному кільці, шляхом регулювання кількості першого хлорметилалкілкарбонату на рівні 2 приблизно одного еквіваленту, можна спочатку перетворити на складний R вмісний моноефір. 2 Згаданий складний R вмісний моноефір може реагувати ще з одним еквівалентом іншого хлорметилалкілкарбонату. Вільна карбоксильна група на тричленному кільці може у 1 подальшому бути перетвореною на складний R вмісний ефір для одержання бажаного 1 2 2 складого діефіру з різними R і R . Для одержання R вмісного складного моноефіру на п'ятичленному кільці сполуки 2, сполуку 3 вводять в реакцію з приблизно одним еквівалентом відповідного хлорметилалкілкарбонату і відповідними реагентами, такими як йодид натрію і карбонат цезію, у відповідному розчиннику, такому як диметилформамід, з одержанням бажаної 2 1 1 сполуки 2, що являє собою бажаний R вмісний моноефір, де R є водень. Для одержання R вмісного складного моноефіру на тричленному кільці спочатку треба захистити карбоксильну групу на п'ятичленному кільці, оскільки вона є більш реакційноздатною за лужних умов. Більш конкретно, карбоксильна група на п'ятичленному кільці сполуки 3 може бути введена в реакцію з альфа-хлор-4-метокситолуолом, йодидом натрію і бікарбонатом натрію у відповідному розчиннику, такому як диметилформамід, з одержанням 4-метоксилбензилового складного моноефіру. Вільну карбоксильну групу на тричленному кільці захищеного 4метоксилбензилового складного моноефіру потім вводять в реакцію з відповідним 1 хлорметилалкілкарбонатом з одержанням бажаного R вмісного складного ефіру на тричленному кільці. Цей складний діефір обробляють відповідною кислотою, такою як трифтороцтова кислота, для відщеплення 4-метоксилбензильної групи захисту і N-трет1 бутоксикарбонільної групи захисту з одержанням бажаної сполуки 1, що являє собою R вмісний 2 складний моноефір, де R є водень. Для одержання бажаної сполуки 1 або її фармацевтично 2 прийнятної солі згадану сполуку 2, у тому числі R вмісний складний моноефір і складний діефір 1 2 з однаковими або різними R і R , у подальшому позбавляють захисних груп за допомогою відповідної кислоти, такої як розчин хлористоводневої кислоти у діоксані. Схема II 5 UA 110039 C2 4 5 10 15 Активну вихідну сполуку 4, де R не є гідроксильна група, можна одержати як показано на схемі II. Сполуку 7 вводять в реакцію з метансульфонілхлоридом і відповідною основою, такою як піридин, з одержанням сполуки 6, що являє собою мезилат. Сполука 6 може бути введена в реакцію з гетероциклічною тіольною сполукою, такою як 1Н-1,2,4-триазол-3-тіол, і відповідною основою, такою як карбонат цезію, у розчиннику, такому як диметилформамід, з одержанням 4 бажаної сполуки 5, де R є бажаний тіосполучений гетероцикл. Сполука 6 може також бути введена в реакцію з азидом натрію з одержанням азидної проміжної сполуки, яку потім відновлюють відновлювальним реагентом, таким як 1,3-пропандитіол, у відповідному 4 розчиннику, такому як метанол, з одержанням сполуки 5, де R є аміногрупа. Одержаний амін може крім того утворювати амід за способами, добре відомими досвідченим фахівцям у цій 4 галузі, з одержанням сполуки 5, де R є бажаний амід. Надалі від сполуки 5 за допомогою відповідної кислоти, такої як хлористоводнева кислота або оцтова кислота, відщеплюють захисні групи з одержанням сполуки 4. Схема III 6 UA 110039 C2 4 5 10 15 20 25 4 Активну вихідну сполуку 8, де R є гідроксильна група, і ключову проміжну сполуку 7, де R є група, відмінна від гідроксильної групи, можна одержати як показано на схемі III. Сполуку 12 (подробиці синтезу дивись у WO03/104217/A2) вводять в реакцію з третбутоксибіс(диметиламіно)метаном у толуолі з одержанням сполуки 11. Сполуку 11 у прийнятному розчиннику, такому як тетрагідрофуран, обробляють відповідною основою, такою як триетиламін, і відповідним відновлювальним реагентом, таким як гідрид диізобутилалюмінію, при зниженій температурі з одержанням сполуки 10. Після цього сполуку 10 вводять в реакцію з триетиламіном і відповідним заміщеним бензолтіолом, таким як 3,4-дифторбензолтіол, у відповідному розчиннику, такому як толуол, з одержанням сполуки 9. Кетогрупа сполуки 9 може бути селективно відновлена до бажаної (S)-гідроксильної або (R)-гідроксильної сполуки за допомогою (R)-метилоксазаборолідину або (S)-метилоксазаборолідину, відповідно. За допомогою відповідної кислоти, такої як хлористоводнева кислота, у розчиннику, такому як діоксан, від (S)-гідроксильної проміжної сполуки відщеплюють захисні групи з одержанням 4 бажаної активної вихідної сполуки 8, де R являє собою (S)-гідроксильну групу. (R)-гідроксильна проміжна сполука 7 може бути перетворена на бажаний продукт за способом, показаним на схемі II. Препаративна методика 1: Ди-трет-бутил(1S, 2R, 5R, 6R)-2-(трет-бутоксикарбоніламіно)-3(диметиламінометилен)-4-оксо-біцикло[3.1.0]гексан-2,6-дикарбоксилат До розчину ди-трет-бутил(1S, 2S, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-4оксобіцикло[3.1.0]гексан-2,6-дикарбоксилату (15,15 г, 36,82 ммоль, подробиці синтезу дивись у WO03/104217/A2) у толуолі (90,90 мл) додають трет-бутоксибіс(диметиламіно)метан (12,83 г, 73,63 ммоль). Потім цю суміш нагрівають до температури 80С протягом 1 год., і після цього залишають охолоджуватися до температури навколишнього середовища. Об'єм розчинника зменшують до приблизно 35 мл. Суміш перемішують з одночасним доданням діетилового ефіру 7 UA 110039 C2 5 10 15 20 25 30 35 40 і гексану, що спричинює утворення осаду. Тверді речовини відфільтровують, промивають гексаном, і піддають повітряному сушінню з одержанням вказаної в заголовку сполуки (16,7 г, 35,79 ммоль, 97,2 % вихід). MS (m/z): 467,2 (М+Н). Препаративна методика 2: Ди-трет-бутил(1S, 2R, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-3метиліден-4-оксобіцикло[3.1.0]гексан-2,6-дикарбоксилат До розчину ди-трет-бутил(1S, 2R, 5R, 6R)-2-(трет-бутоксикарбоніламіно)-3(диметиламінометилен)-4-оксо-біцикло[3.1.0]гексан-2,6-дикарбоксилату (15,7 г, 33,8 ммоль) у тетрагідрофурані (340 мл) додають триетиламін (6,6 мл, 47,32 ммоль). Суміш охолоджують до температури -78С. Протягом однієї години додають розчин гідриду диізобутилалюмінію (1н в толуолі, 50 мл, 50 ммоль). Суміш перемішують протягом іще двох годин. Потім додають 30 мл насиченого водного розчину хлориду амонію. Суміш витримують для нагрівання до кімнатної температури. Суміш переносять до ділильної лійки, і промивають розсолом. Органічний шар сушать MgSO4, фільтрують, і концентрують при зниженому тиску до одержання залишку. Залишок очищають за допомогою флеш-хроматографії (від 0 % до 50 % етилацетат/гексани) з одержанням вказаної в заголовку сполуки (12 г, 33,34 ммоль, 83,8 % вихід). MS (m/z): 422 (М-Н). Препаративна методика 3: Ди-трет-бутил(1S, 2R, 3S, 4S, 5R, 6R)-2-[(третбутоксикарбоніл)аміно]-3-{[(3,4-дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан2,6-дикарбоксилат Розчин ди-трет-бутил(1S, 2R, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-3-метиліден-4оксобіцикло[3.1.0]гексан-2,6-дикарбоксилату (1,03 г, 2,43 ммоль) у діетиловому ефірі (100 мл) барботують газоподібним азотом протягом 10 хв. Додають 3,4-дифторбензолтіол (0,36 г, 2,43 ммоль) і триетиламін (0,01 мл, 0,05 мкмоль). Суміш нагрівають до температури 40C, і перемішують протягом 15 хв. Потім суміш витримують з охолодженням до температури навколишнього середовища, переносять до ділильної лійки, розбавляють гексаном (40 мл), промивають 2н водним розчином КОН (130 мл), сушать сульфатом магнію, фільтрують, і концентрують при зниженому тиску з одержанням ди-трет-бутил(1S, 2R, 3S, 5R, 6R)-2-[(третбутоксикарбоніл)аміно]-3-{[(3,4-дифторфеніл)сульфаніл]метил}-4-оксобіцикло[3.1.0]гексан-2,6дикарбоксилату (1,35 г, 2,37 ммоль): MS (m/z): 567,8 (М-Н). Цей матеріал розчиняють у 120 мл діетилового ефіру, і повільно протягом 2 год. при температурі -10С додають до 200 мл ефірного розчину, який містить R-(+)-2-метил-CBS-оксазаборолідин (981,72 мг, 3,54 ммоль) і розчин боран-метилсульфидного комплексу (2 М у тетрагідрофурані, 5,02 мл, 10,04 ммоль). Суміш перемішують протягом іще однієї години після закінчення додавання ди-трет-бутил(1S, 2R, 3S, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-3-{[(3,4-дифторфеніл)сульфаніл]метил}-4оксобіцикло[3.1.0]гексан-2,6-дикарбоксилату. Протягом 30 хв додають силікагель (30 г), і поступово нагрівають реакційну суміш до температури навколишнього середовища. Суспензію відфільтровують, і промивають 300 мл діетилового ефіру. Розчинник концентрують при зниженому тиску до одержання залишку. Залишок очищають за допомогою флешхроматографії, елююючи сумішшю (від 0 % до 15 % етилацетат/гексани) з одержанням вказаної в заголовку сполуки (0,844 г, 1,48 ммоль, 60,7 % вихід): MS (m/z): 569,8 (M-H). 8 UA 110039 C2 Наведені нижче сполуки одержують по суті за препаративною методикою 3: Вихід (%) Фізичні дані MS(m/z) 4 Ди-трет-бутил(1S, 2R, 3S, 4S, 5R, 6R)-2[(трет-бутоксикарбоніл)аміно]-3-{[(3-хлор4-фтор-феніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилат 84,0 (M+H): 585,8 5 Ди-трет-бутил(1S, 2R, 3S, 4S, 5R, 6R)-2(трет-бутоксикарбоніламіно)-3-[(4-фтор-3метил-феніл)сульфанілметил]-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат 73,5 (M+Na): 590,0 6 Ди-трет-бутил(1S, 2R, 3S, 4S, 5R, 6R)-2(трет-бутоксикарбоніламіно)-3-[(3,4дихлорфеніл)сульфанілметил]-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат 75,2 (M+Na): 625,8 7 Ди-трет-бутил(1S, 2R, 3S, 4S, 5R, 6R)-2(трет-бутоксикарбоніламіно)-3-[(3хлорфеніл)сульфанілметил]-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат 82,6 (M-H): 567,8 8 Ди-трет-бутил(1S, 2R, 3S, 4S, 5R, 6R)-2(трет-бутоксикарбоніламіно)-3-[(4фторфеніл)сульфанілметил]-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат 50,3 (M+Na): 576,0 9 Ди-трет-бутил(1S, 2R, 3S, 4S, 5R, 6R)-2(трет-бутоксикарбоніламіно)-4-гідрокси-3(птолілсульфанілметил)біцикло[3.1.0]гексан2,6-дикарбоксилат 77,0 (M+Na): 572,2 Препаративна мето-дика № 5 10 Хімічна назва Структура Препаративна методика 10: Ди-трет-бутил(1S, 2R, 3S, 4R, бутоксикарбоніл)аміно]-3-{[(4-фтор-3-метилфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат 5R, 6R)-2-[(трет Розчин ди-трет-бутил(1S, 2R, 5R, 6R)-2-(трет-бутоксикарбоніламіно)-3-метилен-4оксобіцикло[3.1.0]гексан-2,6-дикарбоксилату (8 г, 18,9 ммоль) у діетиловому ефірі (80 мл) барботують газоподібним азотом протягом 10 хв. Додають 4-фтор-3-метил-бензолтіол (2,7 г, 18,9 ммоль) і триетиламін (0,26 мл, 1,89 ммоль). Суміш нагрівають до температури 40C, і 9 UA 110039 C2 5 10 15 20 25 30 35 перемішують протягом 15 хв. Потім суміш витримують з охолодженням до температури навколишнього середовища, переносять до краплинної лійки, і повільно протягом 2 год. при температурі -10С додають до 200 мл ефірного розчину, який містить розчин S-(-)-2-метил-CBSоксазаборолідину (1 М у тетрагідрофурані) (5,67 мл, 5,67 ммоль) і розчин боранметилсульфідного комплексу (2 М у тетрагідрофурані, 8,5 мл, 17 ммоль). Після завершення додавання суміш перемішують протягом іще однієї години. Потім протягом 30 хв додають силікагель (40 г), і поступово нагрівають реакційну суміш до температури навколишнього середовища. Суспензію відфільтровують, і промивають 300 мл діетилового ефіру. Розчинник концентрують при зниженому тиску до одержання залишку. Залишок очищають за допомогою флеш-хроматографії, елююючи сумішшю (від 0 % до 15 % етилацетат/гексани) з одержанням вказаної в заголовку сполуки (9,8 г, 17,3 ммоль, 91,5 % вихід): MS (m/z): 565,8 (M-H). Препаративна методика 11: Ди-трет-бутил(1S, 2R, 3S, 4R, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(4-фтор-3-метилфеніл)сульфанілметил]-4-метилсульфонілоксибіцикло[3.1.0]гексан-2,6-дикарбоксилат Розчин ди-трет-бутил(1S, 2R, 3S, 4R, 5R, 6R)-2-(трет-бутоксикарбоніламіно)-3-[(4-фтор-3метилфеніл)сульфанілметил]-4-гідрокси-біцикло[3.1.0]гексан-2,6-дикарбоксилату (4,6 г, 8,10 ммоль) у піридині (60 мл) охолоджують до температури 0С. До цієї суміші додають метансульфонілхлорид (1,88 мл, 24,31 ммоль). Суміш нагрівають до температури 40C, перемішують протягом 1 год., охолоджують до температури навколишнього середовища, і перемішують протягом 18 год. Суміш концентрують при зниженому тиску до одержання залишку. Залишок розподіляють між етилацетатом і 1н водним розчином HCl (250 мл). Органічний шар відокремлюють, висушують сульфатом магнію, фільтрують, і концентрують при зниженому тиску до одержання вказаної в заголовку сполуки (5,2 г, 8,05 ммоль, 99,4 % вихід): MS (m/z): 643,6 (M-H). Препаративна методика 12: Ди-трет-бутил(1R, 2R, 3R, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(4-фтор-3-метилфеніл)сульфанілметил]-4-(1H-1,2,4-триазол-3ілсульфаніл)біцикло[3.1.0]гексан-2,6-дикарбоксилат Ди-трет-бутил(1S, 2R, 3S, 4R, 5R, 6R)-2-(трет-бутоксикарбоніламіно)-3-[(4-фтор-3метилфеніл)сульфанілметил]-4-метилсульфонілокси-біцикло[3.1.0]гексан-2,6-дикарбоксилат (5,3 г, 8,21 ммоль) розчиняють у диметилформаміді (100 мл). До цієї суміші додають карбонат цезію (5,40 г, 16,41 ммоль), 1H-1,2,4-триазол-3-тіол (3,42 г, 32,83 ммоль) і триацетоксиборогідрид натрію (906 мг, 4,10 ммоль). Суміш перемішують при температурі 40С протягом 72 год. Реакційну суміш охолоджують і гасять водою і водним розчином NH 4Cl. Суміш переносять до ділильної лійки і екстрагують діетиловим ефіром, сушать сульфатом магнію, фільтрують, і концентрують при зниженому тиску до одержання залишку. Залишок очищають за допомогою флеш-хроматографії (від 0 % до 50 % етилацетат/гексани) з одержанням вказаної в 10 UA 110039 C2 заголовку сполуки (0,88 г, 1,35 ммоль, 16,5 % вихід). MS (m/z): 651 (M+H). Препаративна методика 13: Ди-трет-бутил(1S, 2R, 3R, 4S, 5R, 6S)-4-азидо-2-(третбутоксикарбоніламіно)-3-[(4-фтор-3-метилфеніл)сульфанілметил]біцикло[3.1.0]гексан-2,6дикарбоксилат 5 10 15 20 25 30 Ди-трет-бутил(1S, 2R, 3S, 4R, 5R, 6R)-2-(трет-бутоксикарбоніламіно)-3-[(4-фтор-3метилфеніл)сульфанілметил]-4-метилсульфонілокси-біцикло[3.1.0]гексан-2,6-дикарбоксилат (5,9 г, 9,14 ммоль) розчиняють у диметилсульфоксиді (30 мл). До цієї суміші додають азид натрію (2,5 г, 38,37 ммоль). Суміш перемішують при температурі 100С протягом 18 год. Розчинник видаляють при зниженому тиску до одержання залишку. Залишок суспендують у діетиловому ефірі (100 мл), і відфільтровують. Органічний шар переносять до ділильної лійки, промивають водою і розсолом, сушать сульфатом магнію, фільтрують, і концентрують при зниженому тиску до одержання залишку. Залишок очищають за допомогою флешхроматографії (від 0 % до 15 % етилацетат/гексани) з одержанням вказаної в заголовку сполуки (3,14 г, 5,30 ммоль, 58 % вихід). MS (m/z): 591 (М-Н). Препаративна методика 14: Ди-трет-бутил(1S, 2R, 3R, 4S, 5R, 6S)-4-аміно-2-(третбутоксикарбоніламіно)-3-[(4-фтор-3-метилфеніл)сульфанілметил]біцикло[3.1.0]гексан-2,6дикарбоксилат Ди-трет-бутил(1S, 2R, 3R, 4S, 5R, 6S)-4-азидо-2-(трет-бутоксикарбоніламіно)-3-[(4-фтор-3метилфеніл)сульфанілметил]біцикло[3.1.0]гексан-2,6-дикарбоксилат (1,88 г, 3,17 ммоль) розчиняють у метанолі (15,86 мл). До цієї суміші додають триетиламін (1,77 мл, 12,7 ммоль) і 1,3-пропандитіол (1,28 мл, 12,69 ммоль). Суміш перемішують при температурі навколишнього середовища протягом 18 год. Суміш виливають у воду, і екстрагують етилацетатом, сушать над сульфатом натрію, фільтрують, і концентрують при зниженому тиску до одержання залишку. Залишок очищають за допомогою флеш-хроматографії (від 50 % до 100 % етилацетат/гексани) з одержанням вказаної в заголовку сполуки (1,2 г, 2,12 моль, 66,76 % вихід). MS (m/z): 567,2 (М+1). Препаративна методика 15: Ди-трет-бутил(1S, 2R, 3R, 4S, 5R, 6S)-4-ацетамідо-2-(третбутоксикарбоніламіно)-3-[(4-фтор-3-метилфеніл)сульфанілметил]біцикло[3.1.0]гексан-2,6дикарбоксилат 11 UA 110039 C2 5 10 15 20 25 30 35 Ди-трет-бутил(1S, 2R, 3R, 4S, 5R, 6S)-4-аміно-2-(трет-бутоксикарбоніламіно)-3-[(4-фтор-3метилфеніл)сульфанілметил]біцикло[3.1.0]гексан-2,6-дикарбоксилат (0,15 г, 264,67 мкмоль) розчиняють у дихлорметані (10 мл). До цієї суміші додають триетиламін (55,34 мкл, 397,01 мкмоль) і ацетилхлорид (28,25 мкл, 397,01 мкмоль). Суміш перемішують при температурі навколишнього середовища протягом 10 хв. Розчинник видаляють при зниженому тиску до одержання залишку. Залишок очищають за допомогою флеш-хроматографії (від 10 % до 100 % етилацетат/гексани) з одержанням вказаної в заголовку сполуки (100 мг, 164,27 мкмоль, 1 62,06 % вихід). H ßÌÐ (CD3Cl) δ 1,44 (t, 27H), 1,95 (s, 3H), 2,16 (m, 1H), 2,22 (s, 3H), 2,60 (dd, 1H), 2,78 (bs, 1H), 3,10 (dd, 1H), 4,59 (m, 1H), 5,50 (d, 1H), 6,92 (t, 1H), 7,06 (m, 1H), 7,11 (d, 1H). Препаративна методика 16: (1S, 2R, 3S, 4S, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-3-{[(3,4дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбонова кислота Ди-трет-бутил(1S, 2R, 3S, 4S, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-3-{[(3,4дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат (4,11 г, 7,19 ммоль) відважують в однолітрову колбу з круглим дном, у яку вміщений якір магнітної мішалки. Додають розчин хлористого водню (4н у діоксані, 120 мл, 480,0 ммоль). Суміш нагрівають до температури 70С протягом 2 год., і потім витримують з охолодженням до температури навколишнього середовища. Розчинник видаляють при зниженому тиску до одержання залишку. Залишок розчиняють у дихлорметані (200 мл), і видаляють розчинник при зниженому тиску до одержання залишку. Це повторюють ще два рази до одержання гідрохлориду (1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-[(3,4-дифторфеніл)сульфанілметил]-4-гідрокси-біцикло[3.1.0]гексан2,6-дикарбонової кислоти. Цей матеріал розчиняють у тетрагідрофурані (100 мл) з одержанням суспензії. До цієї суспензії додають триетиламін (40,08 мл, 287,57 ммоль). Суспензію перемішують протягом 10 хв, після чого додають метанол (50 мл). До реакційної суміші додають ди-трет-бутилдикарбонат (4,71 г, 21,57 ммоль), і нагрівають суміш до температури 80С протягом 2 год. Суміш витримують з охолодженням до температури навколишнього середовища, і видаляють розчинник при зниженому тиску до одержання залишку. Залишок розчиняють в ацетонітрилі (50 мл), переносять до ділильної лійки і промивають гексанами. Шар ацетонітрилу відокремлюють, і видаляють при зниженому тиску до одержання залишку. Залишок суспендують у діетиловом ефірі, переносять до ділильної лійки, промивають 1н водним розчином НСl, сушать сульфатом магнію, фільтрують, і концентрують при зниженому тиску до одержання вказаної в заголовку сполуки (3 г, 6,53 ммоль, 90,82 % вихід). MS (m/z): 457,8 (М-Н). Наведені нижче сполуки одержують по суті за препаративною методикою 16: 12 UA 110039 C2 17 (M+H): 476,0 (1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(4-фтор-3метилфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбонова кислота 94,6 (M-H): 453,8 (1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(3,4диметилфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбонова кислота 92,3 (M+H): 450,2 20 15 76,2 19 10 (1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(3-хлор-4фторфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбонова кислота 18 5 Хімічна назва Ди-трет-бутил(1S, 2R, 3S, 4S, 5R, 6R)-2-(трет-бутоксикарбоніламіно)3-[(3-хлорфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 95,6 (M-H): 440,0 Структура Вихід (%) Фізичні дані MS(m/z) Препаративна мето-дика № Препаративна методика 21: Біс(хлорметил)(1S, 2R, 3S, 4S, 5R, бутоксикарбоніламіно)-3-[(4-фтор-3-метилфеніл)сульфанілметил]-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат 6R)-2-(трет До перемішуваної суміші (1S, 2R, 3S, 4S, 5R, 6R)-2-(трет-бутоксикарбоніламіно)-3-[(4-фтор3-метилфеніл)сульфанілметил]-4-гідрокси-біцикло[3.1.0]гексан-2,6-дикарбонової кислоти (2,4 г, 5,27 ммоль), бісульфату тетра(н-бутил)амонія (178,90 мг, 526,89 мкмоль) та бікарбонату натрія (3,54 г, 42,15 ммоль) у дихлорметані (13,2 мл) і воді (13,2 мл) додають хлорметилхлорсульфат (1,20 мл, 11,59 ммоль). Суміш перемішують при температурі навколишнього середовища протягом 18 год. Потім реакційну суміш виливають у воду, і екстрагують дихлорметаном. Об'єднані органічні шари сушать сульфатом магнію, фільтрують, і концентрують до одержання залишку. Залишок очищають за допомогою флеш-хроматографії (20-35 % етилацетат/гексани) до одержання вказаної в заголовку сполуки (1,37 г, 2,48 ммоль, 47 % вихід). MS (m/z): 574,0 (M+Na). Наведені нижче сполуки одержують по суті за препаративною методикою 21: 13 UA 110039 C2 Препаративна методика № Хімічна назва 22 (Біс(хлорметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(3хлор-4фторфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан2,6-дикарбоксилат Структура Фізичні дані Вихід MS (m/z) або (%) ЯМР 31,2 (M+Na): 593,97 1 23 Хлорметил-2-метилпропаноат 95,8 H ßÌÐ (CD3Cl) δ 1,17 (d, 6H), 2,58 (m, 1H), 2,48 (d, 1H), 5,67 (s, 2H) Препаративна методика 24: Біс({[(1-метилетокси)карбоніл]окси}метил)(1S, 2R, 3S, 4S, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-3-{[(3,4-дифторфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат 5 10 15 Карбонат калію (668,43 мг, 4,79 ммоль), йодид натрію (75,03 мг, 500,58 мкмоль) додають до розчину (1S, 2R, 3S, 4S, 5R, 6R)-2-(трет-бутоксикарбоніламіно)-3-[(3,4дифторфеніл)сульфанілметил]-4-гідрокси-біцикло[3.1.0]гексан-2,6-дикарбонової кислоти (1 г, 2,18 ммоль) у диметилформаміді (13,06 мл). Суміш перемішують протягом 10 хв при температурі навколишнього середовища. Додають хлорметилізопропілкарбонат (1 г, 6,53 ммоль). Суміш перемішують при температурі навколишнього середовища протягом 18 год. Додають оцтову кислоту (4 мл), і перемішують суміш протягом 10 хв. Об'єм розчиннику упарюють приблизно до 10 мл при зниженому тиску з одержанням в'язкого залишку. Залишок розбавляють діетиловим ефіром, і перемішують протягом 10 хв. Розчин пропускають через фільтр, і видаляють розчинник при зниженому тиску до одержання залишку. Залишок залишається під високим вакуумом протягом 1 год. Згаданий залишок очищають за допомогою флеш-хроматографії, елююють (від 0 % до 35 % тетрагидрофуран/гексани) з одержанням вказаної в заголовку сполуки (0,88 г, 1,27 ммоль, 58,5 % вихід). MS (m/z): 714,2 (M+Na). Наведені нижче сполуки одержують по суті за препаративною методикою 24: 20 14 UA 110039 C2 Препаратив-на методика № Хімічна назва 25 (Біс(ізопропоксикарбонілоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(3-хлор-4фторфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 52,9 (M+Na): 730,2 26 Біс(ізопропоксикарбонілоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(4-фтор-3метилфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 35,8 (M+Na): 709,8 27 Біс(етоксикарбонілоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(3,4дифторфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 62,7 (M+Na): 686,2 28 Біс(етоксикарбонілоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(3-хлор-4фторфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 44,9 (M+Na): 702,2 29 Біс(етоксикарбонілоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(4-фтор-3метилфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 39,7 (M+Na): 682,0 30 Біс(етоксикарбонілоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(3,4диметилфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 31,4 (M+Na): 677,8 Структура 15 Вихід (%) Фізичні дані MS (m/z) UA 110039 C2 Препаратив-на методика № Хімічна назва 31 Біс(етоксикарбонілоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(4фторфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 62,4 (M+Na): 668,2 32 Біс(ацетоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(трет-бутоксикарбоніламіно)-3[(4-фтор-3метилфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 60,3 (M+Na): 622,00 33 Біс(ацетоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(трет-бутоксикарбоніламіно)-3[(3-хлор-4фторфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 51,2 (M+Na): 642,00 34 Біс(2-метилпропаноїлоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(3,4дифторфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 29,5 (M+Na): 682,00 Структура Вихід (%) Фізичні дані MS (m/z) Препаративна методика 35: Bis{[(2-метилпропаноїл)окси]метил}(1S, 2R, 3S, 4S, 5R, 6R)-2[(трет-бутоксикарбоніл)аміно]-3-{[(4-фтор-3-метилфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат 5 10 Ізомасляну кислоту (0,21 г, 2,42 ммоль) розчиняють у диметилформаміді (10 мл). До цього розчину додають карбонат калію (0,54 г, 3,87 ммоль). Суміш перемішують при температурі 50C протягом 3 год., після чого охолоджують до кімнатної температури. До суміші додають біс(хлорметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(трет-бутоксикарбоніламіно)-3-[(4-фтор-3метилфеніл)сульфанілметил]-4-гідрокси-біцикло[3.1.0]гексан-2,6-дикарбоксилат (535 мг, 0,97 ммоль). Суміш перемішують при температурі навколишнього середовища протягом 18 год. Суміш розбавляють етилацетатом, переносять до ділильної лійки, промивають розсолом, 16 UA 110039 C2 сушать сульфатом магнію, і концентрують при зниженому тиску до одержання залишку. Залишок очищають за допомогою флеш-хроматографії (10-40 % етилацетат/гексани) з одержання вказаної в заголовку сполуки (230 мг, 0,36 ммоль, 37 %). MS (m/z): 678,2 (M+Na). Наведені нижче сполуки одержують по суті за препаративною методикою 35: 5 Препа ративна методика № Хімічна назва 36 (Біс(2-метилпропаноїлоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(3-хлор-4фторфеніл)сульфанілметил]-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат 37,0 (M+Na): 698,0 37 Біс[[(2S)-2метилбутаноїл]оксиметил](1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(4-фтор-3метилфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 52,0 (M+Na): 706,2 38 Біс(2-етилбутаноїлоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(4-фтор-3метилфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 30,2 (M+Na): 733,8 39 Біс(3-метилбутаноїлоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(4-фтор-3метилфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 29,1 (M+Na): 706,2 40 Біс(циклопропанкарбонілоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(4-фтор-3метилфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 40,6 (M+Na): 674,0 41 Біс(циклопентанкарбонілоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(третбутоксикарбоніламіно)-3-[(4-фтор-3метилфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 51,8 (M+Na): 730,2 Структура 17 Вихід (%) Фізичні дані MS (m/z) UA 110039 C2 Препа ративна методика № Хімічна назва 42 Біс(пропаноїлоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(трет-бутоксикарбоніламіно)3-[(4-фтор-3метилфеніл)сульфанілметил]-4гідрокси-біцикло[3.1.0]гексан-2,6дикарбоксилат 19,8 (M+Na): 650,0 43 Біс(пропаноїлоксиметил)(1S, 2R, 3S, 4S, 5R, 6R)-2-(трет-бутоксикарбоніламіно)3-[(3-хлор-4фторфеніл)сульфанілметил]-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат 28,0 (M+Na): 670,0 Структура Вихід (%) Фізичні дані MS (m/z) Приклад 1: (1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3,4-дифторфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0] гексан-2,6-дикарбонової кислоти гідрохлорид 5 10 Ди-трет-бутил(1S, 2R, 3S, 4S, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-3-{[(3,4дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат (0,58 г, 7,19 ммоль) відважують у 100 мл колбу з круглим дном, у яку вміщений якір магнітної мішалки. Додають розчин хлористого водню (4н у діоксані, 33 мл, 132,0 ммоль). Суміш нагрівають до температури 70С протягом 2 год., і потім витримують з охолодженням до температури навколишнього середовища. Розчинник видаляють при зниженому тиску до одержання залишку. Залишок розчиняють у дихлорметані (50 мл), і видаляють розчинник при зниженому тиску до одержання залишку. Це повторюють ще три рази з одержанням вказаної в заголовку сполуки (567 мг, 1,43 ммоль, 97 % вихід). MS (m/z): 360,0 (М+1). Наведені нижче сполуки одержують по суті за способом Прикладу 1: 15 Фізичні Вихід (%) дані MS (m/z) Приклад № Хімічна назва 2 (1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3{[(3-хлор-4фторфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбонової кислоти гідрохлорид 57,1 (M+H): 376,0 3 (1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3{[(4-фтор-3метилфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбонової кислоти гідрохлорид 93,4 (M+H): 356,0 Структура 18 UA 110039 C2 Фізичні Вихід (%) дані MS (m/z) Приклад № Хімічна назва 4 (1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3{[(3,4дихлорфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбонової кислоти гідрохлорид 101,4 (M+H): 392,0 5 (1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3{[(3-хлорфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбонової кислоти гідрохлорид 82,6 (M+H): 358,0 6 (1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3{[(4-фторфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбонової кислоти гідрохлорид 110,4 (M+H): 341,8 7 (1R, 2R, 3R, 4S, 5R, 6R)-2-аміно-3{[(4-фтор-3метилфеніл)сульфаніл]метил}-4(1H-1,2,4-триазол-3ілсульфаніл)біцикло[3.1.0]гексан2,6-дикарбонової кислоти гідрохлорид 93,0 (M+H): 438,8 Структура Приклад 8: (1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-4-гідрокси-3-{[(4метилфеніл)сульфаніл]метил}біцикло[3.1.0]гексан-2,6-дикарбонова кислота 5 10 Ди-трет-бутил (1S, 2R, 3S, 4S, 5R, 6R)-2-(трет-бутоксикарбоніламіно)-4-гідрокси-3-(птолілсульфанілметил)біцикло[3.1.0]гексан-2,6-дикарбоксилат (300 мг, 545,73 мкмоль) вміщують у пробірку для мікрохвильової печі. У пробірку додають воду (2 мл, 110 ммоль) і оцтову кислоту (2 мл, 34,9 ммоль). Одержану суміш нагрівають у мікрохвильовій печі до температури 140C протягом 20 хв. Розчинник видаляють при зниженому тиску з одержанням вказаної в заголовку сполуки (165 мг, 489,04 мкмоль, 89,6 %). MS (m/z): 338,0 (М+Н). Наведені нижче сполуки одержують по суті за способом Прикладу 8: Приклад № Хімічна назва 9 (1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3,4диметилфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6-дикарбонова кислота Структура 19 Фізичні Вихід дані (%) MS (m/z) 96,3 (M+H): 352,0 UA 110039 C2 Фізичні Вихід дані (%) MS (m/z) Приклад № Хімічна назва 10 (1S, 2R, 3R, 4S, 5R, 6S)-4-(ацетиламіно)-2-аміно-3{[(4-фтор-3метилфеніл)сульфаніл]метил}біцикло[3.1.0]гексан2,6-дикарбонова кислота 93,2 (M+H): 397,0 11 (1S, 2R, 3R, 4S, 5R, 6S)-2,4-діаміно-3-{[(4-фтор-3метилфеніл)сульфаніл]метил}біцикло[3.1.0]гексан2,6-дикарбонова кислота 84,6 (M+H): 355,2 Структура Приклад 12: Біс({[(1-метилетокси)карбоніл]окси}метил)(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3{[(3,4-дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилату гідрохлорид 5 10 Біс({[(1-метилетокси)карбоніл]окси}метил)(1S, 2R, 3S, 4S, 5R, 6R)-2-[(третбутоксикарбоніл)аміно]-3-{[(3,4-дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан2,6-дикарбоксилат (0,88 г, 1,27 ммоль) розчиняють у хлористому водні (4н у діоксані, 30 мл, 120,00 ммоль), і перемішують при температурі навколишнього середовища протягом 1,5 год. Розчинник видаляють при зниженому тиску до одержання залишку. Залишок розчиняють у дихлорметані, і видаляють розчинник при зниженому тиску. Цей процес повторюють 8 разів. Залишок залишається під високим вакуумом протягом ночі з одержанням вказаної в заголовку сполуки (0,692 г, 1,10 ммоль, 86,61 % вихід). MS (m/z): 591,8 (М+Н). Наведені нижче сполуки одержують по суті за способом Прикладу 12: 15 Фізичні Вихід дані MS (%) (m/z) Приклад № Хімічна назва 13 Біс{[(2-метилпропаноїл)окси]метил}(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(4-фтор-3метилфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 90,8 (M+H): 555,8 14 Біс{[(2-метилпропаноїл)окси]метил}(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3-хлор-4фторфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 95,5 (M+H): 575,8 Структура 20 UA 110039 C2 Фізичні Вихід дані MS (%) (m/z) Приклад № Хімічна назва 15 Біс[(пропаноїлокси)метил](1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(4-фтор-3метилфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 93,3 (M+H): 528,0 16 Біс[(пропаноїлокси)метил](1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3-хлор-4фторфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 55,5 (M+H): 548,0 17 6-({[(2S)-2-метилбутаноїл]окси}метил)-2({[(2S)-2-метилбутаноїл]окси}метил)(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(4-фтор-3метилфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 68,2 (M+H): 584,0 18 Біс{[(циклопентилкарбоніл)окси]метил}(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(4-фтор-3метилфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 71 (M+H): 608,2 19 Біс{[(етоксикарбоніл)окси]метил}(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3,4диметилфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 79,4 (M+H): 556,2 20 Біс{[(2-метилпропаноїл)окси]метил}(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3,4дифторфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 89,7 (M+H): 560,2 21 Біс{[(етоксикарбоніл)окси]метил}(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(4фторфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 89,5 (M+H): 546,2 Структура 21 UA 110039 C2 Фізичні Вихід дані MS (%) (m/z) Приклад № Хімічна назва 22 Біс({[(1метилетокси)карбоніл]окси}метил)(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3-хлор-4фторфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 100 (M+H): 607,8 23 Біс({[(1метилетокси)карбоніл]окси}метил)(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(4-фтор-3метилфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 101,5 (M+H): 587,8 24 Біс{[(2-етилбутаноїл)окси]метил}(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(4-фтор-3метилфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 36,5 (M+H): 612,0 25 Біс{[(3-метилбутаноїл)окси]метил}(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(4-фтор-3метилфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 36,1 (M+H): 584,2 26 Біс[(ацетилокси)метил](1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(4-фтор-3метилфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 84,6 (M+H): 500,0 27 Біс[(ацетилокси)метил](1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3-хлор-4фторфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 94,7 (M+H): 520,0 28 Біс{[(циклопропілкарбоніл)окси]метил}(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(4-фтор-3метилфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 79,2 (M+H): 552,2 Структура 22 UA 110039 C2 Фізичні Вихід дані MS (%) (m/z) Приклад № Хімічна назва 29 Біс{[(етоксикарбоніл)окси]метил}(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3,4дифторфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 96,2 (M+H): 564,2 30 Біс{[(етоксикарбоніл)окси]метил}(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(4-фтор-3метилфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 96,2 (M+H): 560,2 31 Біс{[(етоксикарбоніл)окси]метил}(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3-хлор-4фторфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6дикарбоксилату гідрохлорид 95,1 (M+H): 580,0 Структура Приклад 32: Біс({[(1-метилетокси)карбоніл]окси}метил)(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3{[(3,4-дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилату гідрохлорид 5 10 Стадія 1: Ди-трет-бутил(1S, 2R, 5R, 6R)-2-(трет-бутоксикарбоніламіно)-3(диметиламінометилен)-4-оксо-біцикло[3.1.0]гексан-2,6-дикарбоксилат Трет-бутоксибіс(диметиламіно)метан (481,1 мл, 2,33 моль) додають до суспензії ди-третбутил(1S, 2S, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-4-оксобіцикло[3.1.0]гексан-2,6дикарбоксилату (600 г, 1,46 моль) у безводному толуолі (3,6 л) при кімнатній температурі в атмосфері азоту. Суміш нагрівають при температурі 80C протягом 3 год. і 45 хв, потім 23 UA 110039 C2 5 10 15 20 25 30 35 охолоджують до кімнатної температури, і перемішують протягом ночі. Об'єм реакційної суміші зменшують in vacuo, розбавляють метил-трет-бутиловим ефіром (1,8 л) і гексаном (1,8 л), і перемішують протягом 3 год. при температурі 15С. Через 3 год. одержану тверду речовину збирають шляхом фільтрування, промивають холодним гексаном (21,8 л), і сушать у вакуумі з одержанням вказаної в заголовку сполуки (620,4 г, вихід 91 %). HPLC-MS: 98 %. Стадія 2: Ди-трет-бутил(1S, 2R, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-3-метиліден-4оксобіцикло[3.1.0]гексан-2,6-дикарбоксилат До розчину ди-трет-бутил(1S, 2R, 5R, 6R)-2-(трет-бутоксикарбоніламіно)-3(диметиламінометилен)-4-оксо-біцикло[3.1.0]гексан-2,6-дикарбоксилату (620,4 г, 1,33 моль) у безводному тетрагідрофурані (12 л) при кімнатній температурі в атмосфері азоту додають триетиламін (277,3 мл, 1,99 моль). Суміш охолоджують до температури -47C, і краплями впродовж 2 год. додають розчин гідриду диізобутилалюмінію (1 М в гексані, 2,06 л, 2,06 моль). Одержану суміш перемішують при температурі -47C. Через 1 год. 15 хв краплями при температурі -47C додають оцтову кислоту (118 мл, 2,06 моль), суміш нагрівають до кімнатної температури, і потім перемішують протягом ночі. Додають 20 % розчин H3PO4 у воді до рН=2. Органічну фазу відокремлюють, і екстрагують водну фазу етилацетатом (21,7 л). Об'єднані органічні фази послідовно промивають 10 % водним розчином HCl (1,5 л), водою (1,5 л) і розсолом (1,5 л), сушать безводним сульфатом натрію, фільтрують, і концентрують з одержанням твердої речовини. Одержану тверду речовину розтирають з водою (3,2 л), збирають шляхом фільтрування, після чого сушать з одержанням вказаної в заголовку сполуки (558,2 г, вихід 99 %). HPLC-MS: 97,4 %. Стадія 3: Ди-трет-бутил(1S, 2R, 3S, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-3-{[(3,4дифторфеніл)сульфаніл]метил}-4-оксобіцикло[3.1.0]гексан-2,6-дикарбоксилат Суспензію ди-трет-бутил(1S, 2R, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-3-метиліден-4оксобіцикло[3.1.0]гексан-2,6-дикарбоксилату (350,00 г, 826,43 ммоль) у толуолі (2,95 л) обробляють 3,4-дифторбензолтіолом (172,49 г, 1,18 моль) і триетиламіном (205,61 мл, 149,28 г, 1,48 моль) при температурі 25С. Суміш перемішують при температурі 80C. Через дванадцять годин реакційну суміш охолоджують до кімнатної температури, послідовно промивають 2н водним розчином NaOH (рН=10) і 1н водним розчином HCl (рН=4), сушать MgSO4, і концентрують in vacuo до одержання залишку. Залишок розтирають з гексаном (1 л), і видаляють розчинник до одержання вказаної в заголовку сполуки (664 г, 100 % вихід). Стадія 4: Ди-трет-бутил(1S, 2R, 3S, 4S, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-3-{[(3,4дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилат 24 UA 110039 C2 5 10 15 20 25 1н розчин (R)-метилоксазаборолідину у толуолі (228,21 мл) і боран-метилсульфідного комплексу (86,68 г, 101,98 мл, 1,14 моль) у безводному метил-трет-бутиловому ефірі (4,56 л) охолоджують до температури -40C. До цього розчину через краплинну лійку впродовж 2 год. додають розчин ди-трет-бутил(1S, 2R, 3S, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-3-{[(3,4дифторфеніл)сульфаніл]метил}-4-оксобіцикло[3.1.0]гексан-2,6-дикарбоксилату (650,00 г, 1,14 моль) у метил-трет-бутиловому ефірі (3,42 л), після чого вказану реакційну суміш нагрівають до температури 0C. Через 1 год. додають метанол (461,80 мл, 11,41 моль), і підтримують внутрішню температуру нижче 15С. Реакційну суміш промивають 2н водним розчином NaOH (2 л), сушать MgSO4, і концентрують in vacuo до одержання залишку. Залишок очищають за допомогою хроматографії на силікагелі (від 8:1 до 1:1 гексан/етилацетат) з одержанням вказаної в заголовку сполуки (580 г, 89 % вихід). Стадія 5: (1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3,4-дифторфеніл)сульфаніл]метил}-4гідроксибіцикло[3.1.0]гексан-2,6-дикарбонова кислота Воду (1,10 л) і 12,18 M розчин хлористого водню у воді (789,88 мл, 9,62 моль) додають до розчину ди-трет-бутил(1S, 2R, 3S, 4S, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-3-{[(3,4дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилату (550,00 г, 962,07 ммоль) у 1,4-діоксані (192,41 мл). Одержану суспензію перемішують при температурі 100C. Через 12 год. реакційну суміш охолоджують до температури 25С, перемішують протягом 12 год., а потім підлужують розчином NaOH (50 % (мас.)) до рН=2,65. Одержану суміш перемішують при температурі 10C протягом 30 хв, після чого осад збирають шляхом фільтрування, промивають водою (1 л) і метил-трет-бутиловим ефіром (1 л), і сушать протягом 2 год. при температурі 25С, і потім при температурі 60C в печі до постійної маси з одержанням вказаної в заголовку сполуки (300 г, 87 % вихід). MS (m/z): 360 (М+1). Стадія 6: (1S, 2R, 3S, 4S, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-3-{[(3,4дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбонова кислота 25 UA 110039 C2 5 10 15 20 25 Триетиламін (407,27 мл, 2,92 моль) і [2-(трет-бутоксикарбонілоксііміно)-2-фенілацетонітрил] (308,39 г, 1,25 моль) додають до суспензії (1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3,4дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбонової кислоти (300,00 г, 834,84 ммоль) у 1,4-діоксані (500,9 мл) і воді (500,9 мл) при температурі 25С. Цю суміш нагрівають до температури 50С. Через 12 год. реакційну суміш охолоджують до температури 25С, розбавляють водою (2,5 л), і промивають метил-трет-бутиловим ефіром (61 л). 1н водним розчином HCl доводять основність водної фази до рН=2, і екстрагують етилацетатом (32 л). Об'єднані етилацетатні екстракти промивають розсолом, сушать MgSO 4, і концентрують in vacuo з одержанням вказаної в заголовку сполуки (250 г, 65 % вихід). MS (m/z): 360 (М+-Вос). Стадія 7: Біс({[(1-метилетокси)карбоніл]окси}метил)(1S, 2R, 3S, 4S, 5R, 6R)-2-[(третбутоксикарбоніл)аміно]-3-{[(3,4-дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан2,6-дикарбоксилат Розчин (1S, 2R, 3S, 4S, 5R, 6R)-2-[(трет-бутоксикарбоніл)аміно]-3-{[(3,4дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбонової кислоти (150,00 г, 326,46 ммоль) у диметилформаміді (3,38 л) послідовно обробляють карбонатом калію (180,48 г, 1,31 моль), хлорметилізопропілкарбонатом (149,43 г, 979,39 ммоль) і йодидом натрію (9,79 г, 65,29 ммоль), і перемішують суміш у атмосфері азоту при температурі 25С. Через 12 год. до згаданої суміші додають воду (1,5 л), тверді речовини відфільтровують, і екстрагують фільтрат метил-трет-бутиловим ефіром (31,5 л). Об'єднані органічні шари послідовно промивають водою, розсолом, сушать MgSO4, і концентрують in vacuo. Одержаний залишок очищають за допомогою хроматографії на силікагелі (від 2:1 до 1:1 гексан/етилацетат) з одержанням вказаної в заголовку сполуки (225 г, 70 % вихід). MS (m/z): 592 (М+-Вос). Стадія 8: Біс({[(1-метилетокси)карбоніл]окси}метил)(1S, 2R, 3S, 4S, 5R, 6R)-2-аміно-3-{[(3,4дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан-2,6-дикарбоксилату гідрохлорид 26 UA 110039 C2 5 10 15 20 25 30 35 40 45 Біс({[(1-метилетокси)карбоніл]окси}метил)(1S, 2R, 3S, 4S, 5R, 6R)-2-[(третбутоксикарбоніл)аміно]-3-{[(3,4-дифторфеніл)сульфаніл]метил}-4-гідроксибіцикло[3.1.0]гексан2,6-дикарбоксилат (124,9 г, 180,57 ммоль) обробляють 4н розчином хлористого водню у 1,4діоксані (1,12 л, 4,50 моль) при температурі 25С. Через 90 хв розчинник видаляють in vacuo, і суспендують залишок у метил-трет-бутиловому ефірі (1 л) протягом 30 хв. Одержаний осад збирають шляхом фільтрування, промивають метил-трет-бутиловим ефіром (500 мл), і сушать в сушильній шафі при температурі 45С протягом 16 год. Одержану сіль розчиняють у дихлорметані і воді, потім нейтралізують триетиламіном. Органічну фазу відокремлюють, сушать MgSO4, і концентрують in vacuo з одержанням залишку. Цей залишок очищають за допомогою хроматографії на силікагелі (від 3:1 до 1:1 гексан/етилацетат) з одержанням вільної основи, яку обробляють 4н розчином HCl у 1,4-діоксані (950 мл) при температурі 25С. Через 15 хв розчинник випарюють in vacuo, і залишок суспендують у метил-трет-бутиловому ефірі (1 л) і гексанах (250 мл). Одержану тверду речовину фільтрують, промивають метил-трет-бутиловим ефіром (500 мл), і сушать in vacuo при температурі 45C до постійної маси з одержанням вказаної в заголовку сполуки (98,5 г, 87 % вихід). MS (m/z): 592 (М+1). Літературні дані (Witkin, Jeffrey M., and Eiler, William J.A. (2006), Antagonism of Metabotropic Glutamate Group II Receptors in the Potential Treatment of Neurological and Neuropsychiatric Disorders. Drug Development Research vol 67, pg. 757-769; and Yasuhara, Akito and Chaki, Shigeyuki, (2010) Metabotropic Glutamate Receptors: Potential Drug Targets for Psychiatric Disorders, The Open Medicinal Chemistry Journal, vol. 4, pg. 20-36.) і дані, які були одержані під час проведення доклінічних досліджень на тваринах, підтверджують роль антагоністів mGlu2/3 у лікуванні депресивних розладів та розладів, що супроводжуються надмірною сонливістю. Зокрема встановлено, що антагоністи рецепторів mGlu 2/3 є ефективними у разі моделей депресивних розладів і стимулювання неспання на гризунах із застосуванням моніторингу ЕЕГ гризунів без непропорційної або клінічно значущої гіперактивності або надмірної компенсаторної гіперсомнії. Підвищена настороженість проявляється підвищенням уваги, поліпшенням когнітивних функцій та ймовірністю зниження стомлюваності. Оскільки попередньо описані розлади представляють собою звичайні супутні хворобливі клінічні стани, антагоніст рецепторів mGlu2/3 може бути особливо ефективним для специфічних груп пацієнтів, наприклад, пацієнтів з тяжким депресивним розладом, депресією, що не піддається лікуванню, уніполярною депресією, дистимією та/або циклотимією чи будь-якими розладами, що супроводжуються надмірною сонливістю. Розлади, що супроводжуються надмірною сонливістю, можуть включати, але без обмеження ними, надмірну денну сонливість (EDS), гіперсомнію, пов'язану з обструктивним апное сну або нарколепсією, порушення циркадних ритмів (у тому числі, але без обмеження ними, розлад, пов'язаний із змінним трудовим графіком, розлад, пов'язаний з пересіканням часових поясів, синдром затримки фази сну, синдром передчасної фази сну і синдром не 24-годинного циклу сну і неспання), ідіопатичну гіперсомнію та/або надмірну сонливість, пов'язану з невідновлювальним сном (NRS). Для подальшої демонстрації характеристик сполук за цим винаходом, репрезентативні сполуки можуть бути застосовані при проведенні наведених нижче аналізів in vitro та in vivo: Аналізи ефекту антагоністів рецепторів mGlu2 і mGlu3 на продукування цАМФ Антагоністичну активність аналізують на рекомбінантних клітинах AV12, що стабільно експресують людські рецептори mGlu2 або mGlu3 і пацючий транспортер глутамату EAAT1 (транспортер збуджувальної амінокислоти 1). Клітинні лінії підтримували шляхом культивування в середовищі DMEM (модифіковане за способом Дульбекко середовище Ігла) з високим вмістом глюкози і гідрохлориду піридоксину, доповненому 5 % діалізованої сироватки плода крупної рогатої худоби (FBS), 1 мМ розчином пірувату натрію, 1 мМ розчином HEPES і 1 мМ розчином L-глутаміну; генетицин і гігроміцин В застосовуються як селективні антибіотики. Зливні культури 27 UA 110039 C2 5 10 15 20 25 30 35 40 45 50 55 60 вирощують при температурі 37С в атмосфері, що містить 6,5 % СО2, з пересіванням двічі на тиждень. Клітини збирають із застосуванням 0,25 % трипсину, суспендують у живильному 7 середовищі для заморожування (FBS з 10 % DMSO) з густиною 10 клітин/мл, і аліквоти зберігають у рідкому азоті. За двадцять чотири години до проведення аналізу клітини висівають з густиною 8000-10000 клітин на лунку на 96-лункові напівчорні планшети (Costar 3875), оброблені культурою клітин тканини у 50 мкл середовища DMEM з високим вмістом глюкози і гідрохлориду піридоксину, доповненого 5 % діалізованої FBS, 1 мМ розчином пірувату натрію, 1 мМ розчином HEPES, 100 мкг/мл ампіциліну і 250 мкМ (mGlu2) або 125 мкМ (mGlu3) розчину Lглутаміну. Інверсію пригнічення форсколін-стимульованого продукування цАМФ досліджуваними сполуками визначають з використанням методу гомогенної флуоресценції з часовим розділенням (HTRF; компанія Cisbio, № за каталогом: 62AM4PEB). Середовище видаляють, і клітини інкубують з 100 мкл цАМФ-стимулювального буферу (STIM) протягом 30 хв при температурі 37С. (Буфер STIM містить 500 мл HBSS, 1000 мл DPBS, 0,034 % BSA, 1,67 мМ HEPES і 500 мкМ IBMX (компанія Sigma, № за каталогом: I5879)) Сполуки випробують за 10точковою кривою залежності "концентрація-ефект", використовуючи 3 послідовне розведення з подальшим 40-кратним розведенням у буфері STIM. DCG IV (компанія Tocris, № за каталогом: 0975) відіграє роль еталонного агоніста. Кінцева реакційна суміш містить 1 мкМ (для mGlu2) або 3 мкМ (для mGlu3) форсколіна (компанія Sigma, № за каталогом: F6886), DCG IV у кількості, що становить EC90, і до 25 мкМ досліджуваної сполуки. Клітини інкубують при температурі 37С протягом 20 хв. Для визначення рівнів цАМФ, кон'югат цАМФ-d2 і кон'югат анти-цАМФ-кріптат у лізисному буфері інкубують з обробленими клітинами при кімнатній температурі протягом 1 год. (mGlu2) або 1,5 год. (mGlu3). Сигнал HTRF виявляють за допомогою планшет-рідеру EnVision (компанія Perkin-Elmer) для обчислення відношення флуоресценції 665 нМ/620 нМ. Необроблені дані перетворюють на кількість цАМФ (пмоль/лунку) з використанням стандартної кривої цАМФ, яку одержують для кожного експерименту. Відносні значення IC 50 розраховують у межах повного (від максимального до мінімального значень) діапазону кривої залежності "концентрація-ефект", із застосуванням програми (ActivityBase v5.3.1.22) для підгонки до чотирипараметрової логістичної кривої. Аналізи з використанням FLIPR і цАМФ для визначення селективності рецепторів mGlu Відносна антагоністична активність сполук за цим винаходом стосовно інших людських рецепторів mGlu може оцінюватись за допомогою аналізу цАМФ або флуорометричного аналізу реакції на кальцій (дивись, наприклад, Fell et al., JPET (у публікації)). Стисло, для проведення цих досліджень використовують індивідуальні клітинні лінії AV12, що містять пацючий транспортер глутамату EAAT1, і які стабільно експресують людські рецептори mGlu1, mGlu 2, mGlu 3, mGlu 4, mGlu 5, mGlu 6 та mGlu 8. Рецептори mGlu1 і mGlu 5 є сполученими з Gqбілком, тому вони природним чином передають сигнал через фосфоліпазу С, викликаючи реакцію, яка полягає у надлишковому виділенні кальцію і яка може бути використаною для визначення активації рецептора за допомогою планшет-рідера для роботи з флуорометричним аналізатором (FLIPR, компанія Molecular Devices). Клітинні лінії, що експресують рецептори mGlu2, mGlu 3, mGlu 4 і mGlu 8, конструюють таким чином, щоб вони експресували субодиницю Gα15, завдяки чому ці Gi-сполучені рецептори будуть спричинювати реакцію надлишкового виділення кальцію, подібно до клітинних ліній, що експресують рецептори mGlu1 та mGlu 5. Рецептор MGlu6 випробовують у форматі цАМФ з використанням способів, аналогічних вказаним вище, які були розроблені для mGlu2 і mGlu3. Ці клітинні лінії підтримують, як описано вище, за винятком того, що кількість L-глутаміну і селективних агентів (генетицин, гігроміцин В, зеоцин і бластицидин) може змінюватись в залежності від клітинної лінії. Зливні культури пересівають двічі на тиждень. Внутрішньоклітинні рівні кальцію контролюють за допомогою FLIPR до і після додання досліджуваних сполук і барвника Fluo-3 AM (компанія Invitrogen) або Calcium 4 (компанія Molecular Devices), залежно від клітинної лінії. Клітини висівають за 24 год. до аналізу зі змінною концентрацією глутаміну і змінною густиною клітин на лунку, залежно від клітинної лінії. Середовище видаляють, і клітини інкубують з 8 мкМ розчином барвника (50 мкл на лунку) протягом 90 хв або 120 хв (залежно від клітинної лінії) при температурі 25С. Щоб підтвердити відповідну чутливість клітин, перед кожним експериментом проводять аналіз із застосуванням FLIPR з одноразовим додаванням, що надає можливість одержання 11-точкової кривої залежності "концентрація-ефект" для агоніста глутамата. Результати аналізують за допомогою програми GraphPad Prism v4.03 для розрахунку концентрацій глутамату, необхідних для індукування EC90 (аналіз антагоністів) і EC10 (аналіз потенціювальних засобів) реакцій. Сполуки випробують на кожному рецепторі mGlu у аналізі із застосуванням FLIPR з 28
ДивитисяДодаткова інформація
Назва патенту англійськоюNormal;heading 1;heading 2;heading 3;4-substituted-3-phenylsulfanylmethyl-bicyclo[3.1.0]hexane compounds as mglur 2/3 antagonists
Автори англійськоюSmith, Stephon Cornell, Li, Renhua, Mitch, Charles Howard, Vetman, Tatiana Natali
Назва патенту російськоюСоединения 4-замещенного 3-фенилсульфанилметилбицикло[3.1.0]гексана как антагонисты mglur 2/3
Автори російськоюСмит Стефон Корнелл, Ли Женьхуа, Митч Чарлз Говард, Ветман Татиана Натали
МПК / Мітки
МПК: C07C 323/58, A61K 31/10
Мітки: mglur, сполуки, антагоністи, 3-фенілсульфанілметилбіцикло[3.1.0]гексану, 4-(заміщеного
Код посилання
<a href="https://ua.patents.su/37-110039-spoluki-4-zamishhenogo-3-fenilsulfanilmetilbiciklo310geksanu-yak-antagonisti-mglur-2-3.html" target="_blank" rel="follow" title="База патентів України">Сполуки 4-заміщеного 3-фенілсульфанілметилбіцикло[3.1.0]гексану як антагоністи mglur 2/3</a>
Попередній патент: Керуючий клапан для автоматичних пневматичних гальм
Наступний патент: Вентильований курильний виріб, спосіб формування курильного виробу та установка для виготовлення курильних виробів
Випадковий патент: Система цифрового кодування-декодування, кодер, декодер, носій запису та спосіб передавання широкосмугового цифрового звукового сигналу